Purificazione di purificazione e studio di proteine
|
|
|
- Fiora Vitale
- 7 anni fa
- Visualizzazioni
Transcript
1 Purificazione di purificazione e studio di proteine Lo studio delle proteine richiede spesso di avere a disposizione una popolazione di molecole (proteine) omogenea, pura
2 Estratto di E. coli (circa 1000 proteine)
3 Le proteine di E. coli sono macromolecole che hanno: Un determinato grado di solubilità Un peso molecolare Una carica totale negativa o positiva (anche un pi) Caratteristiche proprietà biologiche Devo poterla riconoscere tra le migliaia saggio di attività
4 Sviluppo di un metodo di saggio adeguato per il riconoscimento della proteina da purificare. Esempio: isolamento della lattico deidrogenasi da fegato. + 2e- + 2H + NAD + + 2e- + 2H + NADH+H +
5
6 IL SAGGIO 1. Deve essere eseguibile rapidamente su molti campioni; 2. Deve indicare in modo affidabile la quantità della proteina desiderata presente ai vari stadi di purificazione (specificità, sensibilità, riproducibilità);
7 Purificazione delle proteine: Il PRINCIPIO - ROMPERE L ORGANIZZAZIONE CELLULARE - REINTRODURRE UN NUOVO ORDINE SULLA BASE DELLE SEGUENTI PROPRIETÀ: 1) Solubilità (in soluzioni saline; in solventi organici; ph della soluzione; temperatura, ecc.); 2) Proprietà acido-basiche (cromatografia a scambio ionico; elettroforesi; focalizzazione isoelettrica; ); 3) Grandezza molecolare (setaccio molecolare/gel-filtrazione; ultracentrifugazione;..); 4) Proprietà idrofobiche (cromatografia ad interazione idrofobica; cromatografia a fase inversa); 5) Proprietà biologiche (cromatografia di affinità)
8 Attività preliminari
9 Controllo di Temperatura e ph Soluzione tampone : soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi. Si tratta generalmente di soluzioni di un acido debole e il suo sale con una base forte (per esempio il sistema acido acetico - acetato di sodio) o, viceversa, di una base debole e il suo sale con un acido forte (per esempio il sistema ammoniaca - cloruro d'ammonio) o ancora di un sale, di una base debole e di un acido debole di acidi e basi forti concentrate. SISTEMI TAMPONE DI USO COMUNE pk Acido acetico - acetato di sodio 4,75 Carbonato d'ammonio 6,10 e 10,22 Na fosfato di sodio mono e bibasico 1,93, 6,70 e 12,30 Tricina (N-tris(idrossimetil)metil-glicina) 10,0 HEPES (acido N-2-idrossietilpiperazina-N -2-etansulfonico) 7,50 Tris-Cl (2 ammino-2-idrossimetil propano 1,3-diolo) 8,14
10 Soluzioni fisiologiche Le soluzioni fisiologiche comprendono soluzioni tampone impiegate per incubazioni di breve durata emediumdicrescitaa lungo termine di colture cellulari, piante o tessuti animali. Le proprietà chimico fisiche delle soluzioni sono pensate per minimizzare gli artefatti e la loro composizione tende a mimare quella dei fluidi corporei. Fattori cruciali delle soluzioni fisiologiche sono la isotonicità del medium rispetto alle cellule e la capacità tamponante ad un ph fisiologico. Una soluzione fisiologica di riferimento è una soluzione contenente 0,9% Peso/Volume di NaCl (cioè circa 9 g/l). Quanto Molare (M)????? 9 g sono 9/58,45 che da 0,154 moli che per litro (0,154 M)
11 Omogenati di organi, tessuti e cellule L omogeneizzazione distrugge il tessuto e rilascia i componenti intracellulari in sospensione. L omogeneizzazione viene anche usata come fase preliminare per la purificazione parziale di organuli cellulari per gli studi sulla compartimentazione metabolica. Per il successo della omogeneizzazione sono molto importanti: i) la scelta del tessuto, ii) le proprietà fisiche e chimiche della soluzione fisiologica usata e, iii) il metodo impiegato per la distruzione delle cellule. Il materiale biologico deve essere ricco di organuli specifici e molto attivo nei processi metabolici di interesse (es. fegato per mitocondri, timo per nuclei). La soluzione impiegata è fondamentale per preservare gli organuli, l integrità metabolica e, se necessario, prevenire alcune attività enzimatiche. Essa deve mantenere le condizioni isoosmotiche, un adatto ph e gli livelli ottimali di ioni inorganici. Di seguito sono elencati alcuni componenti delle soluzioni e la loro funzione.
12 Saccarosio Componente Funzione Impiego Agente osmotico Prevenire il rigonfiamento e l esplosione degli organuli 2-mercaptoetanolo DTT cisteina Agenti riducenti Riduzione dei ponti disolfurici degli enzimi Citrato Etilendiamminotetracetato (EDTA) o Etilenglicoltetracetato (EGTA) Mg ++ Disattivante della desossiribonucleasi neutra Agenti chelanti (rimozione di cationi) Catione bivalente Preservare i nuclei Inattivazione delle proteasi di membrana Preservare l integrità del nucleo e dei ribosomi
13 Distruzione delle cellule Le procedure di omogeneizzazione (così come quelle di purificazione delle proteine!) implicano necessariamente una fase di distruzione cellulare. La scelta del metodo dipende dalla natura della parete/membrana cellulare da distruggere. Cellule di mammifero. 10 m. Membrana plasmatica Cellule vegetali. 100 m. Parete rigida (complessi di carboidrati, lignina o cera) Cellule batteriche. 1-4 m. Parete estremamente rigida (peptidoglicani) Cellule di funghi e lieviti. vario. Parete estremamente rigida (polisaccaridi)
14 Omogeneizzatori. Waring-Blender ed il Polytron. Metodi di distruzione delle cellule Meccanici, chimici ed enzimatici. Mortaio con pestello di ceramica Altri metodi meccanici La French Press èilsistemapiù impiegato per cellule con parete estremamente rigida (microbi). Gli omogeneizzatori Dounce e Potter-Elvehjem distruggono le cellule forzandone il passaggio (mediante pressione esercitata manualmente o automaticamente) attraverso il ristretto spazio tra pestello e parete. Sonicatori. Bagni o sonde ad immersione capaci di generare onde sonore ad alta frequenza (ultrasuoni). La distruzione delle cellule avviene per il fenomeno denominato cavitazione.
15 Metodi enzimatici. Le pareti cellulari possono essere degradate utilizzando enzimi specifici. Il lisozima ad esempio taglia i peptidoglicani e può essere quindi utilizzato per i batteri mentre zimolasi e liticasi esercitano la medesima funzione sulle pareti dei lieviti. La chitinasi viene invece impiegata per i funghi filamentosi. Shock osmotico. L utilizzo di una soluzione ipotonica determina l esplosione delle membrane cellulari a causa della penetrazione del solvente nelle cellule. Il metodo può essere impiegato per le cellule non dotate di parete oppure congiuntamente ad altri metodi. Congelamento/Scongelamento. L integrità delle cellule può essere anche danneggiata da rapidi cicli di congelamento/scongelamento. L acqua presente all interno della cellula, formando cristalli di ghiaccio, aumenta di volume e rompe le membrane. Anche in questo caso il trattamento è adatto alle cellule prive di parete. Detergenti e solventi organici. Rottura delle membrane SDS, Triton X 100, Tween 20, Nonidet P40
16 Effettuata la omogenizzazione, come procedere? Quantità? Preparativa o analitica? Grado di purezza? Forma? Nativa o denaturata? Fattori che influenzano la scelta Costo Tempo
17 Esempi Produzione di anticorpi. Produzione di enzimi. Studi di cristallografia o strutturali. Quantità: elevate; Purezza: non elevata; Quantità: elevata; Purezza: non eccessiva; Per utilizzo biotecnologico Quantità: non elevata; Purezza: elevata;
18 Strategia di purificazione Sviluppo di un metodo di saggio adeguato; Selezione del materiale di partenza migliore; Estrazione (solubilizzazione) della proteina; Sviluppo della serie di passaggi di frazionamento, concentrazione e conservazione. Quantizzazione della proteina e calcolo della resa durante la purificazione. Indispensabile: Procedere velocemente, a freddo (se possibile!) ed inattivare le proteasi
19 Selezione del materiale di partenza migliore Se sono disponibili materiali di partenza diversi, scegliere la migliore combinazione dei seguenti parametri: Maggiore quantità di proteina Costi meno elevati Estrazione più agevole
20 Estrazione (solubilizzazione) della proteina Per estrarre una proteina occorre solubilizzarla per i successivi passaggi di purificazione. proteine proteine proteine extracellulari intracellulari di membrana separazione dalle cellule disintegrazione disintegrazione cellulare cellulare separazione da materiale insolubile (chiarificazione dell estratto) isolamento della isolamento frazione cellulare della frazione di membrana, solubilizzazione tecniche cromatografiche (logica nella sequenza)
21 Centrifugazione, tecnica di routine Una particella sottoposta ad un campo centrifugo tende a sedimentare
22
23
24 Il rapporto tra la velocità di sedimentazione di un corpo ideale e della particella in studio soggetto a campo campo centrifugo è detto coefficiente di sedimentazione (è adimensionale).
25 Centrifugazione in gradiente di densità Nella centrifugazione zonale o a banda si fa pre-formare un gradiente di densità in una provetta mediante il mescolamento in proporzioni diverse di una soluzione a bassa densità con una ad alta densità. Si stratifica il campione da centrifugare sopra la miscela e durante la centrifugazione le proteine si muoveranno attraverso il gradiente e si separeranno secondo i loro coefficienti di sedimentazione. DNA in gradiente CsCl-Etidio bromuro
26
27 Disintegrazione cellulare
28 Ultraturrax Potter
29 Pistone French Press Camera di compressione Valvola a spillo
30 Waring Blendor Sonicatore
31 Chiarificazione dell estratto (1) Allontanamento del particolato: filtrazione (garza o carta) centrifugazioni; Allontanamento degli acidi nucleici: protammina solfato o streptomicina al 2% (p/v); Allontanamento delle proteine con caratteristiche differenti: salting in, salting-out; precipitazione isoelettrica; precipitazione con acetone o alcool; denaturazione al calore.
32 Chiarificazione dell estratto (2) La proteina desiderata ha caratteristiche differenti dalla maggior parte delle proteine presenti nell estratto! E molto acida o molto basica? PRECIPITAZIONE ISOELETTRICA Precipita ad una particolare concentrazione di sali? SALTING-IN, SALTING-OUT Protein solubility Precipita selettivamente in presenza di solventi organici? PRECIPITAZIONE CON ACETONE O ALCOOL. Resiste a temperature elevate? DENATURAZIONE AL CALORE. Protein denaturation C
33 Isolamento della frazione cellulare Centrifugazione frazionata
34 Solubilizzazione delle proteine di membrana
35 Purificazione - tecniche cromatografiche (Logica nella sequenza) 1. Passaggio iniziale ad alta capacità ed alta purificazione (cromatografia affinità); 2. Sequenza di passaggi disposta in modo da utilizzare direttamente il materiale ottenuto da un passaggio per quello successivo, senza troppe manipolazioni (scambio ionico, prima di RP, o gel filtrazione quando c è anche bisogno di un cambio di tampone); 3. Non impiegare mai più passaggi che sfruttano le medesime proprietà della proteina.
36 Cromatografia Tswett 1906 Colonna di vetro riempita con particelle di argilla e lavando successivamente il campione. Fece poi colare, attraverso la colonna, dell'etere di petrolio. Fase mobile e fase stazionaria K r = [A mobile ] [A stazionaria ] devono essere immiscibili tra di loro!, ovviamente
37 Il profilo cromatografico Volume di eluizione
38
39 Scambio ionico gel-filtrazione
40 Setaccio molecolare Ve= V0 + kvi Gel-filtrazione o setaccio molecolare Volume di eluizione (ml)
41
42 Cromatografia a scambio ionico Eluisco poi variando il ph e la forza ionica (concentrazione di Sali) pi e ph di esercizio + - Carica netta della proteuina pi ph
43
44 Le resine: una matrice (supporto con uno scambiatore legato covalentemente
45 Impossibile visualizzare l'immagine. Resine diverse differente capacità di separazione
46 Cromatografia di Affinità
47 Cromatografia di Affinità
48 Cromatografia di Affinità
49 Le cromatografia d affinità quindi possono usare anche gli anticorpi, glicoproteine
50
51 Profilo cromatografico e saggio d attività
52 La risoluzione delle colonne cromatografiche aumenta all aumentare dei piatti teorici Eluente Eluente
53 La risoluzione delle colonne cromatografiche aumenta all aumentare dei piatti teorici La zona più piccola lungo la resina in colonna sufficiente all analita per istaurare un equilibrio completo tra le due fasi è chiamata: PIATTO TEORICO. (Ogni colonna ha N-piatti teorici)
54 HPLC (Cromatografia liquida ad alta prestazioni). Per aumentare la risoluzione della cromatografie si è aumentata la possibilità di equilibri lungo la colonna (i piatti teorici) per unità di lunghezza. Sono diminuiti i diametri delle sfere della matrice, per aumentare le superfici di interazione. Meno spazi tra le sfere e maggiori difficoltà di passaggio dell eluente, per ovviare l eluente si applica sotto pressione. L HPLC è tra i metodi più usati nei LAB per separare qualsiasi cosa -> analita e/o proteine.
55
56 1000 piatti teorici piatti teorici litri di campione
57 Quali principi di separazione? tutti, ma in particolare la cromatografia a fase inversa
58 Il saggio può essere quantitativo e quindi posso definire delle Unità di Misura L'unità enzimatica (U, nota anche come Unità internazionale di attività enzimatica) è un'unità di misura della quantità di un particolare enzima.
59 Come seguire l andamento della purificazione di proteina? Ad ogni passaggio determinare: 1- Attività specifica= Unità enzimatiche mg di proteine totali 2-Resa = U di proteina di interesse nella frazione U di proteina di interesse nella preparazione originale X Grado di purificazione= attività specifica della frazione attività specifica iniziale
60
61 Elettroforesi: movimento di molecole o macromolecole in un campo elettrico In condizioni native o in presenza di SDS (nota come SDS-PAGE) + pi - Carica netta della proteuina ph perché in un picco ci possono stare più proteine
62
63 Eletttroforesi SDS-PAGE
64
65
66
67 SDS-PAGE metodica analitica per verificare la purezza di una proteina
68 Proteina omogenea a quantità crescenti
69 Anfoline, formano un gradiente di ph
70 Focalizzazione isoelettrica
71 Elettroforesi bidimensionale
72 2D-PAGE
73 Sviluppo dei passaggi per il cambiamento di tampone e la concentrazione del campione - Precipitazione (entrambi) - Filtrazione (entrambi) TECNICHE AUSILIARIE - Cromatografia per gel filtrazione (cambio tampone) - Dialisi (cambio tampone) Ultrafiltrazione Dialisi Provetta di recupero Camera di caricamento Campione concentrato Membrana Supporto inerte Guarnizione Ultrafiltrato Campo centrifugo
74 Ultrafiltrazione TECNICHE AUSILIARIE Celle Amicon
75 Sulla proteine pura si potranno determinare: - Spettro di assorbimento - Composizione amminoacidica - Sequenza amminoacidica (struttura primaria) vediamo. - Peso molecolare - Punto isoelettrico; - Struttura secondaria, terziaria e quaternaria - Proprietà biologiche Struttura e Funzione!!!!!
76
77 La determinazione della struttura primaria prevede di lavorare con un singolo polipeptide/proteina, quindi se lo struttura quaternaria dei separare i differenti polipeptidi e se sono legati da ponti disolfuro ridurli.
78
79
80 Determinazione della sequenza di una proteina struttura primaria: degradazione di Edman La degradazione di Edman permette di staccare chimicamente un amminoacido alla volta dall N-terminale. La reazione tra amminoacidi e fenilisotiocianato permette anche di rendere gli amminoacidi staccati più facilmente monitorabili, aggiungendo un gruppo fenilico. L ambiente iniziale è basico poiché.
81 Ambiente acido senza acqua derivato fenilidantoil
82 La reazione non ha una resa del 100%, quindi non si può ottenere la struttura primaria completa di una proteina
83 PTH amminoacidi
84
85
86
87 Enzimi per proteolisi specifici: Tripsina, taglia a K ed R
88 Frammentazione chimica con CNBr: frammenta a Met
89
90 Rappresentazione schematica della determinazione della sequenza di una proteina: il procedimento della sovrapposizione.
91
92 Spettrometria di Massa
93
94 Citocromo C (100aa, E. Smith - E. Margoliash analisi della sequenza di 80 specie, particolarmente conservate regioni che sono in contatto con eme e Gly, Cyt ossidasi umana reagisce con Cyt c di germe di grano)
95
96
97 Nanometri, distanza tra gli atomi
98
99 Per ottenere cristalli ci voglio sistemi ordinati
100
101 Diffrazione ai raggi X Struttura terziaria
102
103
104
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
Strategie di purificazione di proteine
 Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea
 la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea Analisi delle sue proprietà fisiche e biologiche Come viene modulata la sua espressione
la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea Analisi delle sue proprietà fisiche e biologiche Come viene modulata la sua espressione
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008. Eloise Mastrangelo
 Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
GENERALITA SULLA CROMATOGRAFIA
 GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
TIPI di CROMATOGRAFIA
 Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Metodi di studio delle proteine (o altre macromolecole)
 Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
cromatografia Elettroforesi
 Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria contesto fisiologico livelli superiori funzione Elettrofores i
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria contesto fisiologico livelli superiori funzione Elettrofores i
ESTRAZIONE CON SOLVENTE
 ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
TECNOLOGIE BIOMOLECOLARI
 TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
Estrazione con solventi. Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti
 Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
2. LA PURIFICAZIONE DI PROTEINE:
 2. LA PURIFICAZIONE DI PROTEINE: LA CROMATOGRAFIA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU-16 ore) Marco Scocchi ( BIO/10-11) LA PURIFICAZIONE DI PROTEINE Purificare
2. LA PURIFICAZIONE DI PROTEINE: LA CROMATOGRAFIA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU-16 ore) Marco Scocchi ( BIO/10-11) LA PURIFICAZIONE DI PROTEINE Purificare
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 12
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 12 Purificazione delle proteine Concetti chiave: Le condizioni ambientali, come il ph e la temperatura, influenzano la stabilitàdi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 12 Purificazione delle proteine Concetti chiave: Le condizioni ambientali, come il ph e la temperatura, influenzano la stabilitàdi
BENZILPENICILLINA BENZATINICA PREPARAZIONE INIETTABILI. Benzilpenicillina Benzatinica polvere sterile per preparazioni iniettabili
 1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
TIPI DI CROMATOGRAFIE
 Corso di Chimica Analitica TIPI DI CROMATOGRAFIE Prof. Paola Gramatica Fasi in successione: 2) Separazione dei componenti la miscela Dopo l isolamento della miscela da analizzare, se ne devono separare
Corso di Chimica Analitica TIPI DI CROMATOGRAFIE Prof. Paola Gramatica Fasi in successione: 2) Separazione dei componenti la miscela Dopo l isolamento della miscela da analizzare, se ne devono separare
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia. Corso di Analisi Chimico-Tossicologica.
 Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI
 METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione.
 Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Soluzioni unità 3, modulo D del libro
 Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 13 Cromatografia ed elettroforesi Concetti chiave: Il comportamento cromatografico di una proteina è influenzato da alcune
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 13 Cromatografia ed elettroforesi Concetti chiave: Il comportamento cromatografico di una proteina è influenzato da alcune
La struttura covalente delle proteine (la sequenza amminoacidica)
 La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
Elemento fondamentale
 Acqua Elemento fondamentale Usata x 90% Produzione Malteria Caldaie frigoriferi Lavaggio e sterilizzazione Ruoli dell acqua Permette il trasporto e la distribuzione nelle cellule delle sostanze Garantisce
Acqua Elemento fondamentale Usata x 90% Produzione Malteria Caldaie frigoriferi Lavaggio e sterilizzazione Ruoli dell acqua Permette il trasporto e la distribuzione nelle cellule delle sostanze Garantisce
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Proprietà delle Soluzioni
 Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
Amministrazione, finanza e marketing - Turismo Ministero dell Istruzione, dell Università e della Ricerca PROGRAMMAZIONE DISCIPLINARE PER U. di A.
 MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
IL PROBLEMA ANALITICO
 IL PROBLEMA ANALITICO COSA CERCARE? COME TROVARLO? 1. TRATTAMENTO CAMPIONE 2. ESTRAZIONE 3. PURIFICAZIONE 4. DETERMINAZIONE QUALI-QUANTITATIVA STORIA Cromatografia = colore + grafia 1906 Michael Tswett,
IL PROBLEMA ANALITICO COSA CERCARE? COME TROVARLO? 1. TRATTAMENTO CAMPIONE 2. ESTRAZIONE 3. PURIFICAZIONE 4. DETERMINAZIONE QUALI-QUANTITATIVA STORIA Cromatografia = colore + grafia 1906 Michael Tswett,
Never impure protein PURIFICAZIONE DI PROTEINE
 Never waste pure thoughts on an impure protein PURIFICAZIONE DI PROTEINE PURIFICARE Purificare significa ottenere solamente la nostra molecola di interesse. Purificare una proteina per: Determinarne la
Never waste pure thoughts on an impure protein PURIFICAZIONE DI PROTEINE PURIFICARE Purificare significa ottenere solamente la nostra molecola di interesse. Purificare una proteina per: Determinarne la
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
MINISTERO DELLA PUBBLICA ISTRUZIONE DIREZIONE GENERALE ISTRUZIONE TECNICA
 MINISTERO DELLA PUBBLICA ISTRUZIONE DIREZIONE GENERALE ISTRUZIONE TECNICA ISTITUTO TECNICO COMMERCIALE LORGNA-PINDEMONTE VERONA INDIRIZZO AMMINISTRAZIONE, FINANZA E MARKETING/TURISMO PROGRAMMA ANALITICO
MINISTERO DELLA PUBBLICA ISTRUZIONE DIREZIONE GENERALE ISTRUZIONE TECNICA ISTITUTO TECNICO COMMERCIALE LORGNA-PINDEMONTE VERONA INDIRIZZO AMMINISTRAZIONE, FINANZA E MARKETING/TURISMO PROGRAMMA ANALITICO
OGRAMMA DI CHIMICA 2016
 ISTITUT TO DI ISTRUZIONE SUPERIORE M MARIANO IV D ARBOREA Sede distaccata IPSIA di GHILARZA PRO OGRAMMA DI CHIMICA A.S. 2015-2016 2016 Classe: I sez. A Docenti: Federica Piras, Carmelo Floris PARTE TEORICA
ISTITUT TO DI ISTRUZIONE SUPERIORE M MARIANO IV D ARBOREA Sede distaccata IPSIA di GHILARZA PRO OGRAMMA DI CHIMICA A.S. 2015-2016 2016 Classe: I sez. A Docenti: Federica Piras, Carmelo Floris PARTE TEORICA
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Elettroforesi di Tamara Benincasa
 Elettroforesi di Tamara Benincasa L elettroforesi è una metodologia utilizzata in laboratorio attraverso la quale molecole biologiche (ammino acidi, peptidi, proteine, nucleotidi ed acidi nucleici), dotate
Elettroforesi di Tamara Benincasa L elettroforesi è una metodologia utilizzata in laboratorio attraverso la quale molecole biologiche (ammino acidi, peptidi, proteine, nucleotidi ed acidi nucleici), dotate
Chimica e laboratorio
 ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
Il potenziale di membrana a riposo
 Il potenziale di membrana a riposo Per poter comprendere il potenziale di membrana a riposo dobbiamo considerare: i fluidi ricchi di sali presenti su entambe le facce della membrana; la membrana stessa;
Il potenziale di membrana a riposo Per poter comprendere il potenziale di membrana a riposo dobbiamo considerare: i fluidi ricchi di sali presenti su entambe le facce della membrana; la membrana stessa;
Estrazione con solvente 18/01/2010. Laboratorio di chimica. Prof. Aurelio Trevisi
 Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
ESTRAZIONE PURIFICAZIONE. Modificazione chimica ANALISI STRUMENTALE
 Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
L'attività di queste proteine, a sua volta è modulata dalla composizione dei fosfolipidi della membrana
 La funzione di ogni membrana biologica è determinata principalmente dall insieme di proteine integrali incorporate e dalle proteine periferiche collegate alla superficie della membrana L'attività di queste
La funzione di ogni membrana biologica è determinata principalmente dall insieme di proteine integrali incorporate e dalle proteine periferiche collegate alla superficie della membrana L'attività di queste
FONDAMENTI ANATOMO-FISIOLOGICI DELL ATTIVITA PSICHICA
 FONDAMENTI ANATOMO-FISIOLOGICI DELL ATTIVITA PSICHICA Il potenziale di membrana a riposo Per poter comprendere il potenziale di membrana a riposo dobbiamo considerare: i fluidi ricchi di sali presenti
FONDAMENTI ANATOMO-FISIOLOGICI DELL ATTIVITA PSICHICA Il potenziale di membrana a riposo Per poter comprendere il potenziale di membrana a riposo dobbiamo considerare: i fluidi ricchi di sali presenti
LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI
 LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI 1 Che cosa sono le proteine? Indispensabili per il corretto funzionamento 2 Dove si trovano le proteine? Le proteine sono macromolecole ubiquitarie,
LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI 1 Che cosa sono le proteine? Indispensabili per il corretto funzionamento 2 Dove si trovano le proteine? Le proteine sono macromolecole ubiquitarie,
METODI GRAVIMETRICI DI ANALISI
 METODI GRAVIMETRICI DI ANALISI I metodi gravimetrici si basano sulla misura della massa e sono sostanzialmente di due tipi: - nei metodi di precipitazione l analita viene trasformato in un precipitato
METODI GRAVIMETRICI DI ANALISI I metodi gravimetrici si basano sulla misura della massa e sono sostanzialmente di due tipi: - nei metodi di precipitazione l analita viene trasformato in un precipitato
SOLUZIONI TAMPONE SOLUZIONI TAMPONE
 SOLUZIONI TAMPONE Le soluzioni tampone (o tamponi) sono costituite da: un acido debole e un suo sale (tampone acido) oppure una base debole e un suo sale (tampone basico) Una soluzione di un acido debole
SOLUZIONI TAMPONE Le soluzioni tampone (o tamponi) sono costituite da: un acido debole e un suo sale (tampone acido) oppure una base debole e un suo sale (tampone basico) Una soluzione di un acido debole
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
2. La chimica della vita Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA
 Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
EQUILIBRI DI SOLUBILITA
 EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
Sostanza pura. Il termine sostanza indica il tipo di materia di cui è fatto un corpo.
 Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
Genomica e Proteomica
 Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
UNITA DIDATTICA P A1.01
 Titolo: Grandezze fisiche fondamentali e derivate, unità di misura. Conversioni di unità di misura e notazione scientifica. Codice: A1-P-Tec-Gra Campo di indagine della chimica. Il Sistema Internazionale
Titolo: Grandezze fisiche fondamentali e derivate, unità di misura. Conversioni di unità di misura e notazione scientifica. Codice: A1-P-Tec-Gra Campo di indagine della chimica. Il Sistema Internazionale
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
2. SISTEMA DI PURIFICAZIONE CROMATOGRAFICA A MEDIA PRESSIONE (Biotage).
 1. APPARECCHIO PER REAZIONI A MICROONDE (Cem). Apparecchio per reazioni a microonde con sistema di sfiato automatico delle sovrappressioni, che consente di condurre reazioni che superano i 300 psi (20
1. APPARECCHIO PER REAZIONI A MICROONDE (Cem). Apparecchio per reazioni a microonde con sistema di sfiato automatico delle sovrappressioni, che consente di condurre reazioni che superano i 300 psi (20
I RECETTORI: Caratterizzazione e isolamento
 I RECETTORI: Caratterizzazione e isolamento Andrea Ferrigno Funzione dei recettori di membrana Secrezione dell ormone nel sangue L ormone è trasportato attraverso il circolo sanguigno L ormone raggiunge
I RECETTORI: Caratterizzazione e isolamento Andrea Ferrigno Funzione dei recettori di membrana Secrezione dell ormone nel sangue L ormone è trasportato attraverso il circolo sanguigno L ormone raggiunge
Polymerase chain reaction - PCR. Biotecnologie applicate all ispezione degli alimenti di origine animale
 Prof.ssa Tiziana Pepe Polymerase chain reaction - PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali tiziana.pepe@unina.it Metodologia
Prof.ssa Tiziana Pepe Polymerase chain reaction - PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali tiziana.pepe@unina.it Metodologia
PRECIPITAZIONE FRAZIONATA DI PROTEINE Obiettivo: separare proteine sfruttando differenze di solubilità
 PRECIPITAZIONE FRAZIONATA DI PROTEINE Obiettivo: separare proteine sfruttando differenze di solubilità SOLUBILITA DELLE PROTEINE ph FORZA IONICA SOLVENTI POLIMERI ORGANICI TEMPERATURA Effetto del ph Precipitazione
PRECIPITAZIONE FRAZIONATA DI PROTEINE Obiettivo: separare proteine sfruttando differenze di solubilità SOLUBILITA DELLE PROTEINE ph FORZA IONICA SOLVENTI POLIMERI ORGANICI TEMPERATURA Effetto del ph Precipitazione
AMPICILLINA SODICA PREPARAZIONE INIETTABILE. Ampicillina sodica polvere sterile per preparazioni iniettabili
 1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
KIT Le forme invisibili La cristallizzazione del lisozima
 KIT Le forme invisibili La cristallizzazione del lisozima MATERIALE NEL KIT - 3 provette da 1,5 ml contenenti la proteina del lisozima purificata (da conservare in freezer) - 6 piastre multiwell - una
KIT Le forme invisibili La cristallizzazione del lisozima MATERIALE NEL KIT - 3 provette da 1,5 ml contenenti la proteina del lisozima purificata (da conservare in freezer) - 6 piastre multiwell - una
Cromatografia ionica (IC)
 Cromatografia ionica (IC) Il principio di base della cromatografia ionica è lo scambio ionico su resine scambiatrici forti, che costituiscono la fase stazionaria con cui sono impaccate le colonne, in parziale
Cromatografia ionica (IC) Il principio di base della cromatografia ionica è lo scambio ionico su resine scambiatrici forti, che costituiscono la fase stazionaria con cui sono impaccate le colonne, in parziale
CORSO DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA LEZIONE SECONDA PARTE. Dott.ssa A. Fiarè
 CORSO DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA LEZIONE SECONDA PARTE Dott.ssa A. Fiarè CELLULA VEGETALE FASE PRELIMINARE: ETICHETTARE IL MATERIALE I FASE: PREPARAZIONE DELLA SOLUZIONE DI ESTRAZIONE
CORSO DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA LEZIONE SECONDA PARTE Dott.ssa A. Fiarè CELLULA VEGETALE FASE PRELIMINARE: ETICHETTARE IL MATERIALE I FASE: PREPARAZIONE DELLA SOLUZIONE DI ESTRAZIONE
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Tecniche Centrifugative
 Tecniche Centrifugative Metodologie Biochimiche 29 Novembre 2015 Il materiale contenuto in queste diapositive è ad esclusivo uso didattico per l università di Teramo Centrifugazione Permette la separazione
Tecniche Centrifugative Metodologie Biochimiche 29 Novembre 2015 Il materiale contenuto in queste diapositive è ad esclusivo uso didattico per l università di Teramo Centrifugazione Permette la separazione
PROGRAMMA DEL CORSO DI CHIMICA ANALITICA 1 CON LABORATORIO a.a
 PROGRAMMA DEL CORSO DI CHIMICA ANALITICA 1 CON LABORATORIO a.a. 2009-2010 Testo consigliato: Daniel C. Harris, Chimica Analitica Quantitativa, Seconda Edizione Italiana, Ed. Zanichelli, 2005 Alcune parti
PROGRAMMA DEL CORSO DI CHIMICA ANALITICA 1 CON LABORATORIO a.a. 2009-2010 Testo consigliato: Daniel C. Harris, Chimica Analitica Quantitativa, Seconda Edizione Italiana, Ed. Zanichelli, 2005 Alcune parti
Primo Levi Il sistema periodico
 Primo Levi Il sistema periodico L anidride carbonica [...] questo gas che costituisce la materia prima della vita, la scorta permanente a cui tutto ciò che cresce attinge, e il destino ultimo di ogni carne,
Primo Levi Il sistema periodico L anidride carbonica [...] questo gas che costituisce la materia prima della vita, la scorta permanente a cui tutto ciò che cresce attinge, e il destino ultimo di ogni carne,
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
da Erriu, Nitti, Verniglio Element i di Fisica ed. Mondurri
 7.17. SEDIMENTAZIONE da Erriu, Nitti, Verniglio Element i di Fisica ed. Mondurri Se si vogliono studiare le proprietà fisiche e chimiche dei componenti subcellulari (membrane, nuclei, mitocondri, ecc.)
7.17. SEDIMENTAZIONE da Erriu, Nitti, Verniglio Element i di Fisica ed. Mondurri Se si vogliono studiare le proprietà fisiche e chimiche dei componenti subcellulari (membrane, nuclei, mitocondri, ecc.)
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa
 Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 22 Acidi e basi si scambiano protoni 3 Sommario 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. La forza
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 22 Acidi e basi si scambiano protoni 3 Sommario 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. La forza
Strategie per la purificazione delle proteine
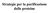 Strategie per la purificazione delle proteine Attenzione! E opportuno distinguere tra metodi di separazione per specifici scopi analitici (basati su tecniche ad alta risoluzione, quali, ad esempio, IEF,,g
Strategie per la purificazione delle proteine Attenzione! E opportuno distinguere tra metodi di separazione per specifici scopi analitici (basati su tecniche ad alta risoluzione, quali, ad esempio, IEF,,g
20/03/2014 ANALISI VOLUMETRICA ACIDO-BASE PRECIPITAZIONE COMPLESSOMETRICA OSSIDO-RIDUZIONE REQUISITI PER UNA TITOLAZIONE
 ANALISI VOLUMETRICA ACIDO-BASE PRECIPITAZIONE COMPLESSOMETRICA OSSIDO-RIDUZIONE In una titolazione l analita reagisce con un reagente addizionato sotto forma di una soluzione di concentrazione nota (soluzione
ANALISI VOLUMETRICA ACIDO-BASE PRECIPITAZIONE COMPLESSOMETRICA OSSIDO-RIDUZIONE In una titolazione l analita reagisce con un reagente addizionato sotto forma di una soluzione di concentrazione nota (soluzione
PURIFICAZIONE DI DNA
 PURIFICAZIONE DI DNA Esistono diverse metodiche per la purificazione di DNA da cellule microbiche, più o meno complesse secondo il grado di purezza e d integrità che si desidera ottenere. In tutti i casi
PURIFICAZIONE DI DNA Esistono diverse metodiche per la purificazione di DNA da cellule microbiche, più o meno complesse secondo il grado di purezza e d integrità che si desidera ottenere. In tutti i casi
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE
 Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
Le proprietà colligative delle soluzioni
 1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
INDICE PARTE I CHIMICA. Autori Introduzione
 INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
Esercitazioni di Elementi di Chimica. Modulo 3 Trasformazioni della Materia
 Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Programma svolto nell a.s
 ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Parti svolte dal libro di testo Chimica Analitica Quantitativa
 PROGRAMMA DEL CORSO DI CHIMICA ANALITICA 1 CON LABORATORIO a.a. 2007-2008 E stato seguito il testo: Daniel C. Harris, Chimica Analitica Quantitativa, Seconda Edizione Italiana, Ed. Zanichelli, 2005 mentre
PROGRAMMA DEL CORSO DI CHIMICA ANALITICA 1 CON LABORATORIO a.a. 2007-2008 E stato seguito il testo: Daniel C. Harris, Chimica Analitica Quantitativa, Seconda Edizione Italiana, Ed. Zanichelli, 2005 mentre
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Osmometria ed Emolisi
 Osmometria ed Emolisi 1 ADE: MISURA DELLA RESISTENZA OSMOTICA DEI GLOBULI ROSSI (2/12/08). Il globulo rosso è una piccola cellula del sangue deputata al trasporto dell'ossigeno e priva di nucleo e di organelli.
Osmometria ed Emolisi 1 ADE: MISURA DELLA RESISTENZA OSMOTICA DEI GLOBULI ROSSI (2/12/08). Il globulo rosso è una piccola cellula del sangue deputata al trasporto dell'ossigeno e priva di nucleo e di organelli.
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 17 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 17 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 5 Maggio 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma
 Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma Apparato strumentale Sodio e potassio vengono determinati in campioni
Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma Apparato strumentale Sodio e potassio vengono determinati in campioni
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
