1 - COMPOSIZIONE CHIMICA DELLA TERRA Di che cosa è fatta la Terra
|
|
|
- Adelaide Pini
- 8 anni fa
- Visualizzazioni
Transcript
1 1 - COMPOSIZIONE CHIMICA DELLA TERRA Di che cosa è fatta la Terra La Terra (fig. 1.1) può essere suddivisa nel seguente modo: biosfera, insieme di tutti gli organismi viventi sulla Terra; atmosfera, involucro gassoso della Terra; idrosfera, insieme delle acque superficiali (mari, fiumi, laghi, nubi,...) e sotterranee (falde acquifere, umidità del suolo, acque ipogee,...); litosfera, involucro rigido della Terra (crosta e porzione superficiale del mantello superiore); astenosfera, costituisce gran parte del mantello superiore (fino ad un massimo di 250 km di profondità); mantello inferiore e nucleo, le parti più profonde della Terra, quelle meno conosciute. Fig Schema semplificato dei domini della Terra. Il raggio del nucleo (~ km) è la metà del raggio terrestre). La crosta è spessa da pochi chilometri ad alcune decine. L atmosfera é quasi tutta concentrata nei primi 10 km di altezza. Usando una terminologia cara ai naturalisti di un tempo, astenosfera, litosfera, idrosfera a atmosfera costituiscono il dominio minerale, mentre la biosfera è il dominio vivente; più modernamente ambiente fisico e ambiente biologico rispettivamente. È un modello a sfere concentriche, in cui si succedono una serie di strati fra loro interdipendenti, ispirato da certe visioni medioevali del mondo, protese a raffigurare una grande struttura unitaria, una sorta di architettura dell Universo. Conosciamo abbastanza bene la biosfera, l atmosfera, l idrosfera e la parte più superficiale della litosfera (poco delle sue porzioni profonde). Sappiamo nulla direttamente della astenosfera, ma è possibile formulare ipotesi attendibili. Le supposizioni sulla composizione delle porzioni più profonde della Terra vanno considerate con molta cautela. Ciò che conosciamo e che possiamo conoscere del nostro pianeta è sempre più approssimativo e difficile dalla superficie verso il centro. Qual è lo stato attuale delle conoscen-ze? Per rispondere a tale domanda è necessario conoscere un po di chimica (scheda 1.1) Elementi della biosfera, dell atmosfera e dell idrosfera Le sostanze elementari (specie atomiche) più diffuse nei viventi, animali e vegetali, di qualunque dimensione, acquatici o terrestri, sono rappresentati nella tab Esse partecipano alla formazione della materia vivente per il 97 % in massa circa. Quali costituenti fondamentali del corpo degli organismi, sono detti elementi primari plastici; essi hanno numero atomico minore di 10, tanto che l atomo più pesante, l ossigeno (M ~ 16) è uno dei più leggeri tra quelli elencati in tab Il restante 3 % è costituito da più di venti elementi, i più importanti dei quali con numero atomico compreso fra 10 e 20 (scheda 1.2). Gli elementi pesanti nella materia vivente sono scarsi. elemento simbolo numero atomico (Z) massa atomica relativa (M) ossigeno O 8 15,99 carbonio C 6 12,01 idrogeno H 1 1,01 azoto N 7 14,01 Tab Elementi primari plastici. L atmosfera, escludendo l acqua in essa contenuta (umidità, nebbia, nuvole, pioggia, grandine, neve) ed eventuali sostanze inquinanti, è costituita dagli elementi riportati in tab. 1.2; i valori tengono conto anche degli elementi che compongono l anidride carbonica (CO 2 ; ~ 0,03 %) ed il metano (CH 4 ; ~ 0,0002 %). È difficile stabilire i limiti dell atmosfera; il suo strato più basso (troposfera) compenetra parte delle altre sfere (litosfera, idrosfera e biosfera). L aria si mescola con le acque superficiali, si insinua nelle minuscole discontinuità del suolo, entra nella materia vivente a tutti i livelli della sua organizzazione. 1
2 elemento simbolo Perosino G.C., Scienze della Terra (cap. 1 - modulo II). CREST (To). numero atomico (Z) massa atomica relativa (M) % in volume azoto N 7 14,01 78,08 ossigeno O 8 15,99 20,97 argon Ar 18 39,95 0,93 carbonio C 6 12,01 0,017 neon Ne 10 20,18 0,002 elio He 2 4,00 0,0005 idrogeno H 1 1,01 0,0002 kripton Kr 36 83,80 0,0001 xenon Xe ,30 0, Tab Gli elementi dell atmosfera. La troposfera, parte dell atmosfera che si innalza a non più di una decina di chilometri di altezza, contiene il % della massa totale dell aria; in essa avvengono la circolazione dell aria (fondamentale per il tempo atmosferico in tutto il globo) e una parte importante dei processi legati ai viventi. Ha un spessore sottile, meno della cinquecentesima parte del raggio terrestre, come una pellicola inferiore al millimetro che avvolge una sfera di un metro di diametro. All aumentare della altitudine la pressione dell aria diminuisce (fig. 1.2); l aria si fa più rarefatta, fino a diventare quasi inesistente, senza che sia possibile stabilire un confine. Le molecole dei diversi gas che compongono l atmosfera, in funzione della loro massa, tendono a stratificarsi; le più pesanti (azoto e ossigeno) sono in prossimità della superficie, quelle più leggere (idrogeno), al di sopra (tab. 1.3). La situazione è più evidente dall osservazione della fig. 1.3, dove viene illustrata l abbondanza dei gas più comuni in funzione dell altezza e dove si osserva che il più leggero costituisce quasi interamente l atmosfera oltre i 130 km di altezza. Le molecole più pesanti sono quelle dell anidride carbonica e dell acqua, ma in quantità così ridotte (0,03 % e 0,2 % rispettivamente) che non sono rappresentate nel diagramma. Salendo di quota l argo diventa molto rarefatto, fino a diventare assente fra i 60 e 80 km di altezza, mentre compare l elio che diventa il gas più importante Fig Andamento della pressione atmosferica [hpa] e della temperatura dell aria [ C] in funzione dell altitudine [m s.l.m.]. con l idrogeno. In linea di massima il comportamento fisico dell atmosfera obbedisce alle classiche leggi della termodinamica (scheda 1.3). Altezza (km) pressione mm Hg A [%] N 2 [%] H 2 O [%] O 2 [%] CO 2 [%] H 2 [%] He [%] 140 0,0040-0, ,63 0, ,0052-0, ,35 0, ,0067-2,97 0,05 0,11-96,31 0, , ,39 0,17 1,86-65,11 0, ,0935 0,03 81,33 0,15 7,70-10,69 0, ,94 0,22 86,43 0,06 12,61-0,67 0, ,99 0,59 81,24 0,02 18,10 0,01 0, ,66 0,77 79,52 0,01 19,66 0,02 0, ,00 0,94 78,02 0,01 20,99 0,03 0, ,00 0,94 77,89 0,18 20,95 0,03 0,01 - suolo 760,00 0,93 78,08 0,20 20,75 0,03 0,01 - Tab Composizione dell atmosfera alle varie altitudini. Sono espresse le percentuali in volume (rispetto al totale) relative ai diversi gas. L acqua pura è costituita dall 89 % in peso di ossigeno e dell 11 % in peso di idrogeno, ma in essa sono presenti altre sostanze, comunque in percentuali quasi sempre molto piccole. La maggior parte della superficie della Terra (3/4) è coperta dall acqua (fig. 1.4). La temperatura dell aria, a livello del suolo, è tale da consentire l esistenza dell acqua contemporaneamente nei tre stati: solido (il ghiaccio e la neve sulle montagne e sui poli), liquido (mari, 2
3 laghi e fiumi) e gassoso (l umidità contenuta nell atmosfera). Questa speciale condizione, rispetto agli altri pianeti del Sistema Solare (e forse rispetto ad altri satelliti di altri sistemi stellari dell Universo), è la ragione della vita. Il diverso irraggiamento solare, maggiore all equatore e minore ai poli, determina squilibri termici tali da provocare grandi spostamenti di masse d aria che sono all origine della successione degli eventi meteorologici nel tempo e nello spazio. In questi processi è ancora protagonista l acqua, coinvolta in un grande ciclo che ne permette la distribuzione sulle terre emerse, consentendo l alimentazione dei ghiacciai, dei fiumi, dei laghi. L acqua costituisce la frazione principale degli organismi (tab. 1.4) e costituisce il mezzo fondamentale dei liquidi di trasporto in natura (sangue, linfa delle piante, soluzioni nutritive presenti nel suolo a disposizione delle radici). L acqua è il solvente per eccellenza (col tempo quasi tutte le sostanze presenti in natura si sciolgono in essa). Fig Composizione dell atmosfera alle varie altezze. % (rispetto al totale) in volume relative ai gas più importanti: azoto (N 2 ), ossigeno (O 2 ) e idrogeno (H 2 ). Tutti gli altri citati nelle tabb. 1.2 e 1.3 sono in quantità trascurabili per essere rappresentati Elementi della litosfera e della Terra profonda Le analisi chimiche, effettuate da diversi decenni su un elevato numero di campioni di materiali della litosfera provenienti un po da tutto il globo (raccogliendo frammenti della superficie o di pozzi e di miniere molto profonde o di materiali espulsi dai vulcani,... e, più recentemente, anche dai fondali oceanici, abissi compresi) hanno permesso, con buona approssimazione, di determinare gli elementi più abbondanti della litosfera (tab. 1.5), quasi tutti mediamente più pesanti rispetto a quelli delle altre sfere. volume [km 3 ] % oceani e mari ,3 ghiacciai ,3 acque sotterranee laghi e fiumi , ,03 atmosfera ,001 totale ,0 Fig I valori riportati nella tabella a lato sono raffigurati con cubi di volumi proporzionali. Il cubo dell acqua marina compare solo per 1/8 del suo volume; quello dell acqua atmosferica è leggermente ingrandito rispetto alle dimensioni reali. Questa immagine è anche un esempio di rappresentazione del ciclo dell acqua. L ossigeno e il silicio rappresentano insieme i 3/4 del peso totale e quasi il 95 % del volume. Gli altri elementi sono distinti in tre gruppi fondamentali: alluminio/ferro (sempre presenti ed abbondanti), calcio/sodio/potassio/magnesio (quasi sempre presenti e, salvo qualche caso, quasi mai abbondanti) e quello di tutti gli altri elementi (molto rari, talvolta presenti in tracce, eccezionalmente in quantità apprezzabili). Considerando maggiori profondità della Terra, le conoscenze diminuiscono. Ciò che sappiamo sui materiali profondi, sotto la crosta, non è il risultato di indagini dirette, ma basato su prove indirette e su modelli compatibili con esse. Fenomeni di origine profonda possono infatti essere registrati in superficie. 3
4 Vegetali Animali Uomo seme di girasole 5 ratto 65 corpo umano 65 chicco di 70 aringa 67 ossa 22 frutto di ananas 87 gallina 74 cervello 74 pomodoro 95 rana 78 muscolo 77 aragosta 79 rene 81 lombrico 80 sangue 84 medusa 96 Tab Percentuali dell acqua rispetto al peso di alcuni organismi o di parti di essi. Non vi sono valide ragioni per negare che tutto il mantello sia costituito dagli stessi elementi della litosfera, ma non è ancora possibile indicare le percentuali in peso o in volume delle singole specie atomiche, come sopra visto per le altre sfere. Possiamo ipotizzare percentuali minori dell insieme silicio/ossigeno e una maggiore presenza degli elementi più pesanti; il ferro, per esempio, dovrebbe essere in percentuale crescente con la profondità. D altra parte sappiamo che in una miscela di materiali, i più leggeri tendono a galleggiare sugli altri che migrano, per gravità, verso il basso. L ipotesi che i materiali del mantello siano costituiti da elementi più pesanti in funzione della profondità è coerente con le caratteristiche fisico-meccaniche che tali materiali debbono avere per rendere ragione delle modalità con le quali si propagano le onde sismiche. Si ipotizza che le composizioni chimiche qualitative dei materiali della crosta e del mantello siano simili; con la profondità cambia la composizione quantitativa a vantaggio degli elementi più pesanti. Al di sotto dei km, nel nucleo, tutto cambia repentinamente tanto che la densità dei materiali quasi raddoppia (oltre 10 kg/dm 3 ), fino a più di 13 kg/dm 3 nel nucleo interno. Si pensa ad una composizione in elementi in grado di rendere ragione di simili densità, pur con tutte le cautele del caso, dato che il centro della Terra è in condizioni di pressione e temperatura poco note e molto diverse da quelle che conosciamo, sulle quali fondiamo le nostre conoscenze di fisica e di chimica. È possibile che il nucleo terrestre sia composto di ferro con piccole quantità di altri minerali. Il ferro è un elemento comune nel Sistema Solare, è il più abbondante nella Terra dopo l ossigeno, il silicio e l alluminio e ha una densità vicina al valore desunto dallo studio della propagazione delle onde sismiche. Le meteoriti metalliche sono composte di ferro con un po di nichel e anche nel Sole si trova del ferro. Esso è stato sottoposto in laboratorio a pressioni molto grandi e i risultati di questi esperimenti non danno motivo per escludere che, insieme al nichel, possa essere il principale elemento costituente il nucleo. Secondo un altra ipotesi, meno elemento simbolo numero massa atomica % in % in atomico (Z) relativa (M) peso volume ossigeno O 8 15,99 46,6 93,8 silicio Si 14 55,85 27,7 0,9 alluminio Al 13 26,98 8,1 0,5 ferro Fe 26 55,85 5,0 0,4 calcio Ca ,6 1,0 sodio Na 11 22,99 2,8 1,3 potassio k 19 39,10 2,6 1,8 magnesio Mg 26 24,31 2,1 0,3 tutti gli altri ,5 0,9 totali Tab Gli elementi della litosfera. accettata, il nucleo non sarebbe chimicamente molto diverso dal mantello, ma il materiale, sottoposto a straordinarie pressioni, vi raggiungerebbe un alta densità e si comporterebbe come un metallo Una breve sintesi Riassumendo quanto sopra sulla composizione in elementi delle diverse sfere della Terra, si possono trarre le seguenti conclusioni: l ossigeno, considerando l insieme di tutte le sfere e ad eccezione del nucleo, è l elemento più abbondante ed è sempre accompagnato da uno o più elementi caratteristici; il nucleo sembra costituito da ferro e da una minore quantità di nichel; questa sfera può essere indicata con il termine nife (dai simboli chimici Ni e Fe); il mantello profondo sembra costituito dagli elementi più pesanti fra quelli presenti nella crosta; l ossigeno è forse ancora l elemento più abbondante, accompagnato dal silicio; il ferro sembra in maggiore percentuale rispetto alla crosta e crescente con la profondità; altro elemento più abbondante rispetto alla crosta è il magnesio; questa sfera è indicata con il termine sima (dal simbolo chimico Si e dalle iniziali del magnesio); la litosfera (comprensiva della crosta e del mantello superiore) è dominata dalla prevalenza dell ossigeno e dal silicio; il silicio è l elemento caratterizzante il dominio minerale; il ferro, pur essendo il quarto elemento, è meno importante; diminuisce il magnesio ed aumenta l alluminio; questa sfera è indicata con il termine sial (dai simboli chimici Si ed Al); 4
5 l idrosfera è anch essa dominata dall ossigeno, ma questa volta l elemento caratteristico è l idrogeno, raro sulla Terra, ma il più abbondante nell Universo; nell atmosfera l ossigeno, pur essendo l elemento più importante per i processi fisici, chimici e biologici di cui è responsabile, perde il primato dell abbondanza a favore dell azoto, importante nel regno vivente e decisamente meno rilevante in quello minerale; anche nella biosfera l ossigeno è abbondante, insieme all idrogeno e all azoto; ma l elemento più caratteristico è il carbonio che, per contrasto, è fra i più rari e meno disponibili nel dominio minerale. La denominazione delle sfere del dominio minerale in nife, sima e sial tiene conto della composizione chimica dei materiali che le costituiscono e ricalcano il modello di costituzione della Terra proposto da SUESS nel Successivamente furono proposte altre teorie, basate su nuove conoscenze; tuttavia si è descritto il modello di Suess perché più semplice ed in grado di associare meglio l abbondanza degli elementi fondamentali in funzione della profondità. È necessario sottolineare che gli elementi che caratterizzano le varie sfere del nostro pianeta non costituiscono quasi mai sostanze pure, ma combinazioni di atomi diversi a formare composti e miscugli (scheda 1.4) e con continue trasformazioni chimiche che sono alla base dei cicli degli elementi stessi Sostanze organiche ed inorganiche: il ciclo del carbonio Non si conoscono validi motivi per pensare che la composizione chimica della litosfera di oltre tre miliardi di anni fa fosse diversa dalla attuale (tab. 1.5). Allora, secondo le teorie più accreditate, ebbe origine la vita. I primi semplici organismi avevano a disposizione, come oggi, tanta acqua (ossigeno e idrogeno), moltissimo silicio, molto alluminio e ferro e una discreta abbondanza di calcio, sodio, potassio e magnesio. Si potrebbe quindi supporre che la composizione chimica dei viventi (biosfera) preveda gli elementi appena citati. In realtà, come abbiamo appena visto, il 97 % in peso degli organismi viventi è composto da quattro elementi: ossigeno, idrogeno, carbonio e azoto (tab. 1.1). Che i primi due siano abbondanti non ci stupisce in quanto l acqua costituisce una percentuale variabile dal 60 al 90 % del peso degli organismi (tab. 1.4). Ma i quattro succitati elementi e soprattutto l azoto ed il carbonio rimangono predominanti in un vivente anche quando ad esso è sottratta tutta l acqua. Eppure carbonio e azoto sono elementi rari sulla crosta tanto che, insieme ad una novantina di altri (tab. 1.5), costituiscono appena l 1,5 % in peso della litosfera. Sembrerebbe che, sull insieme dei complessi e non ancora ben chiariti processi di formazione della vita, il carbonio, per le sue caratteristiche speciali (leggerezza e possibilità di formazione di un elevatissimo numero di composti con altri elementi), sia stato scelto come l elemento cardine di tutta l evoluzione successiva, a dispetto del silicio che, sebbene così abbondante nell ambiente, compare soltanto come accidentale negli organismi. Fig Con la fotosintesi i vegetali, utilizzando la luce, costruiscono sostanza organica, consumando CO 2 e H 2 O. Con la respirazione vegetali, animali ed altri organismi consumano sostanza organica liberando nell ambiente le sostanze di partenza (CO 2 e H 2 O) per produrre l energia necessaria a tutte le attività. La chimica organica è la scienza che studia le sostanze composte contenenti carbonio. Tutte le sostanze che ci circondano possono essere suddivise in due grandi categorie: composti organici (contenenti carbonio, escluse poche eccezioni come CO 2 e CH 4 ) e composti inorganici (che non lo contengono). I primi sono legati ai viventi (biosfera) e quasi sempre combustibili; i secondi appartengono al dominio minerale (l ambiente fisico), quasi mai combustibili. Gran parte dei materiali che ci circondano sono costituiti da sostanze organiche come tutti i manufatti in legno, i tessuti, il cuoio, le pelli, le materie plastiche e i prodotti combustibili (il petrolio e il carbone hanno ancestrali origini organogene), i cibi,... La ringhiera metallica, i mattoni e le mattonelle, i piatti di ceramica, il vetro dei bicchieri,... sono invece esempi di sostanze inorganiche. Quali sono i processi naturali che rendono interdipendenti il regno organico e quello inorganico, il regno vivente (l ambiente biologico) e quello minerale (l ambiente fisico)? A questo quesito, semplificando molto, si può rispondere citando due processi biologici fondamentali: la fotosintesi e la respirazione. Un organismo vegetale è in grado di svolgere un processo chimico formidabile, difficilmente attuabile dall uomo nei più attrezzati dei laboratori; è in grado di costrui- 5
6 re complesse sostanze organiche (zuccheri, grassi, proteine,...) utilizzando, come materie prime, semplici composti inorganici come l anidride carbonica (CO 2, presente come gas nell aria e nelle acque), acqua (H 2 O, nel terreno, fiumi, laghi, mari,...) e sali minerali (sciolti nell acqua e contenenti azoto e minori quantità di fosforo, calcio, sodio,...). Per far ciò un vegetale ha bisogno di energia ed utilizza, grazie alla clorofilla, quella più disponibile: la luce solare. Questo processo, che come prodotto di scarto produce ossigeno che va ad arricchire l ambiente circostante, è la fotosintesi (fig. 1.5). In tal modo i vegetali crescono e si riproducono; attraverso la fotosintesi si costruiscono la materia di cui essi stessi sono costituiti. I vegetali sono detti autotrofi (dal greco trophe = nutrizione; autosufficienti) oppure produttori. La fotosintesi consente alla materia di passare dallo stato inorganico a quello organico (organicazione). Fino ai primi decenni del secolo scorso si pensava che le sostanze organiche potessero essere costruite solo dagli organismi e non potessero essere sintetizzabili artificialmente o formarsi spontaneamente dal regno inorganico, ma un interessante esperimento dimostrò il contrario, aprendo nuove prospettive nella ricerca sull origine della vita (scheda 1.5). Un organismo animale deve utilizzare, come fonte di accrescimento, sostanza organica già costruita. È un consumatore: deve cibarsi direttamente di vegetali se erbivoro, di animali se carnivoro; oppure è un decompositore (vermi, insetti, funghi, batteri,...), cioè un consumatore che utilizza, come fonte di cibo, detriti o rifiuti organici, spoglie di altri organismi o loro residui. I consumatori sono anche detti eterotrofi, non in grado di autoprodursi sostanza organica. In questo caso gran parte del materiale organico utilizzato come cibo viene distrutto, con consumo di ossigeno e produzione di scarti come acqua e anidride carbonica, secondo un processo contrario a quello della fotosintesi (fig. 1.5) e denominato respirazione, esclusivo negli eterotrofi e presente anche negli autotrofi e utilizzato allo scopo di ottenere energia per tutte le attività metaboliche. La respirazione è il processo che permette alla materia di passare dallo stato organico a quello inorganico (mineralizzazione). Se con la fotosintesi avviene la trasformazione da sostanze inorganiche semplici a sostanze organiche complesse (con consumo di energia e produzione di ossigeno), con la respirazione avviene l opposto e si viene così a chiudere il ciclo regno organico - regno minerale. La fig. 1.6 illustra un esempio caratteristico di un ambiente acquatico. Fig Con il processo di fotosintesi gli autotrofi (produttori, in massima parte vegetali) utilizzano il carbonio presente nell anidride carbonica (CO 2 ) insieme all acqua e i sali minerali in essa disciolti (assunta per mezzo delle radici se piante terrestri o semplicemente dall ambiente che le circonda se piante acquatiche; es. le alghe). Grazie alla luce tali sostanze vengono coinvolte in complessi processi chimici che portano alla formazione di sostanza organica. Una parte di questa è utilizzata per essere demolita dagli stessi vegetali, che ricavano così l energia necessaria per tutte le funzioni vitali, un altra parte viene utilizzata dagli eterotrofi (erbivori, come lo zooplancton a loro volta utilizzati dai carnivori e dai decompositori) attraverso il processo di respirazione, che consente il ritorno di CO 2 e H 2 O all ambiente circostante. Il ciclo del carbonio è molto importante per lo studio degli ambienti naturali; prendiamo come esempio un piccolo lago (o uno stagno). Le acque sono popolate da tanti organismi fra i quali numerosissimi e piccolissimi esseri, la maggior parte dei quali visibili solo al microscopio; sono incapaci di compiere veri e propri spostamenti e rimangono più o meno sospesi nel mezzo acqueo circostante. L insieme di quei piccolissimi esseri costituisce il plancton. Una parte di quegli organismi (fitoplancton) è costituita da autotrofi; essi si accrescono e si riproducono utilizzando l acqua del lago e l anidride carbonica e i sali in essa disciolti, sfruttando l energia della luce solare che riesce a penetrare per qualche metro di profondità. Il fitoplancton costituisce un vero e proprio pascolo a disposizione dello zooplancton (plancton animale) che ottiene quindi materia ed energia per mezzo unicamente della respirazione. Il plancton costituisce cibo per altri organismi di maggiori dimensioni come i piccoli pesci. Questi, a loro volta, sono prede di pesci più grandi e così via fino agli uccelli acquatici ed altri predatori, uomo compreso (fig. 1.6). Abbiamo appena descritto una catena alimentare, dove il primo anello (o livello trofico) comprende gli autotrofi (i produttori come il fitoplancton), il secondo anello comprende gli erbivori (i consumatori primari come lo zooplancton), il terzo i carnivori (i consumatori secondari come i piccoli pesci), e così via... Un luccio, un martin pescatore, una lontra, l uomo, per esempio, si trovano agli ultimi livelli trofici. Mentre i produttori trasformano sostanza inorganica in organica (ma consumandone una parte), i consumatori demoliscono quest ultima esclusivamente consumandola e producendo scorie costituite da composti inorganici 6
7 (acqua, anidride carbonica,...) e da residui organici (come gli escrementi) che vengono dispersi nell ambiente circostante a costituire cibo per microrganismi (per lo più batteri e funghi decompositori) che completano la demolizione (con la respirazione) fino a riottenere semplici composti inorganici, cioè nuovamente quei sali minerali a disposizione dei produttori. I processi biologici appena esaminati sono comuni anche ad altri ambienti acquatici come i mari e i fiumi ed analoghi a quelli degli ambienti terrestri (come per esempio un bosco); essi sono materia di studio dell ecologia; tale termine deriva dal greco oikos, che significa casa o posto per vivere. Letteralmente l ecologia è lo studio degli organismi nella loro casa o meglio la disciplina che studia le interazioni reciproche tra l ambiente e gli organismi. Le considerazioni sopra espresse hanno carattere molto generale. In realtà il ciclo del carbonio è molto più complesso e caratterizzato da diversi sottocicli che coinvolgono gli ambienti terrestri e quelli acquatici, andando ad interessare la litosfera, la biosfera, l idrosfera e l atmosfera. Parte del carbono entra a far parte delle rocce sedimentarie carbonatiche nei sedimenti dei laghi e dei mari oppure va a costituire la materia organica coinvolta nei processi di carbonizzazione e di trasformazione in petrolio e derivati (fig. 1.7). Una parte della massa organica, dopo la morte degli organismi, può precipitare sul fondale oceanico, venire sepolta e qui trasformarsi (in assenza di ossigeno) in combustibili fossili. Questi restano nella litosfera per molto tempo e rappresentano una frazione di carbonio sottratta al ciclo biologico ed immessa nel ciclo geologico. Sono rocce caratterizzate da abbondanza di materia organica, derivata dall accumulo di resti di organismi viventi in condizioni di scarsa ossigenazione. In queste condizioni, la materia organica non viene ossidata e può essere seppellita con il graduale accumulo dei sedimenti, dando origine ad una massa amorfa definita kerogene. Con l'aumentare della profondità di seppellimento, l aumento della temperatura (oltre 100 C) provoca la progressiva rottura (cracking) dei legami molecolari del kerogene, che si trasforma in composti più semplici: gli idrocarburi che si originano secondo la successione solidi (bitume), liquidi (petrolio), gassosi (con molecole sempre più semplici, fino al metano). Fig Complessità del ciclo del carbonio. L atmosfera può essere arricchita di CO 2 con le emissioni vulcaniche e con quelle di origine antropica che, consumando combustibili fossili (petrolio, carbone, gas) rimettono in ciclo del carbonio che era stato, in tempi geologici, inglobato nel sottosuolo, andando così ad alterare il bilancio complessivo del ciclo stesso. Si possono effettuare alcuni calcoli, sebbene in termini generale ed approssimativi. Sommando le emissioni dovute alla respirazione dalle comunità viventi terrestri, acquatiche e vulcaniche (rispettivamente frecce verso l alto verdi, azzurre e rosse in fig. 1.8) si ottiene un valore molto vicino a quello della somma delle quantità di CO 2 immagazzinate come materia organica attraverso la fotosintesi (frecce rivolte verso il basso nella succitata fig. 1.8). Ciò dimostra un equilibrio nel ciclo del carbonio. A questo punto occorre considerare anche le emissioni dovute alle attività antropiche (freccia nera rivolta verso l alto) dovute prevalentemente al consumo dei combustibili fossili. Il 40 % circa delle emissioni umane di CO 2 vengono assorbite prevalentemente da vegetazione ed oceani. Ciò che resta rimane in atmosfera. La conseguenza è che la CO 2 atmosferica è attualmente al livello più alto mai raggiunto negli ultimi milioni di anni. L incremento dovuto alle attività umane negli ultimi 120 anni è paragonabile a quelli che, in natura, avvengono nell arco di migliaia ed anche decine di migliaia di anni. Tale situazione sembra all origine dei recenti mutamenti climatici ormai riconosciuti da quasi tutta la comunità scientifica. 7
8 Fig Rappresentazione, molto schematica, delle quantità di CO 2 in gioco nel ciclo del carbonio. Valori espressi in gigatonnellate (10 9 tonnellate) per anno [Gt/anno]. Le frecce rivolte verso il basso rappresentano le quantità fissate prevalentemente sotto forma di materia organica tramite la fotosintesi, sia dai vegetali terrestri (frecce verdi), sia da quelli aquatici (frecce azzurre). Con le frecce dello stesso colore sono rappresentate le quantità che ritornano all atmosfera prevalentemente con i processi di respirazione dei viventi. La quantità di CO 2 liberata con le eruzioni vulcaniche è poco rilevante, ma influenza il ciclo del carbonio su scala dei tempi geologici. Attualmente e nel prossimo futuro, molto più importanti sono le emissioni dovute alle attività umane Il carbonio inorganico A rigore il termine organico non definisce più con esattezza un confine della materia, essendo una eredità dei tempi in cui, fino al 1850, si credeva che i composti organici potessero essere sintetizzati esclusivamente dagli organismi. Oggi è invece possibile ottenere numerosi composti del carbonio per via sintetica, in laboratorio, senza l intervento di organismi. Tuttavia la distinzione tra natura organica ed inorganica appare ancora molto utile e comoda per la classificazione dei fenomeni naturali. Fig Il reticolo cristallino del diamante è costituito unicamente da atomi di carbonio (C) distribuiti in una struttura che si ripete all infinito. Ogni atomo è legato a quelli vicini con forti legami uguali in tutte le direzioni. Questa distribuzione spiega la notevole durezza di tale materiale. La cella cubica interna al reticolo rappresenta la simmetria base con la quale gli atomi sono disposti nello spazio. Nella figura appaiono quasi 100 atomi; ne occorrerebbero quasi per un diamante del peso di un grammo. Fig La grafite, come il diamante, è costituita unicamente da carbonio, ma la simmetria della disposizione degli atomi (C) nello spazio è diversa. Nella grafite sono legati con forza solo su piani di forma esagonale; all interno di essi la grafite è più dura del diamante, ma fra essi la distanza è maggiore e le forze più deboli. La grafite infatti si può facilmente sfaldare lungo piani paralleli. Se il carbonio fosse un elemento esclusivamente legato al vivente non potrebbe esistere in un mondo privo di vita. Invece questo elemento, seppure relativamente raro, era presente sulla Terra in tempi precedenti l origine della vita, affinché questa potesse averlo disponibile per la sintesi organica. Sembra una sorta di circolo vizioso; tuttavia la presenza di carbonio inorganico (CO 2 e CH 4 soprattutto), presente del resto nell atmosfera di alcuni pianeti del Sistema Solare privi di vita, è ammessa in un atmosfera terrestre primordiale priva di ossigeno. La 8
Acqua azzurra, acqua chiara. Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao
 Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
INDIRIZZO TECNOLOGICO CLASSE A033 n. 2
 INDIRIZZO TECNOLOGICO CLASSE A033 n. 2 1) La tensione di rete domestica è in Italia di 230 V. In una stanza è accesa una lampada di 100W, in un altra stanza una lampada di 200W. L intensità di corrente
INDIRIZZO TECNOLOGICO CLASSE A033 n. 2 1) La tensione di rete domestica è in Italia di 230 V. In una stanza è accesa una lampada di 100W, in un altra stanza una lampada di 200W. L intensità di corrente
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
LA MATERIA Suggerimenti didattici e schede
 LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
La radioattività e la datazione al radio-carbonio
 1 Espansione 2.2 La radioattività e la datazione al radio-carbonio Henry Becquerel. I coniugi Pierre e Marie Curie. La radioattività La radioattività è un fenomeno naturale provocato dai nuclei atomici
1 Espansione 2.2 La radioattività e la datazione al radio-carbonio Henry Becquerel. I coniugi Pierre e Marie Curie. La radioattività La radioattività è un fenomeno naturale provocato dai nuclei atomici
Capitolo 03 LA PRESSIONE ATMOSFERICA. 3.1 Esperienza del Torricelli 3.2 Unità di misura delle pressioni
 Capitolo 03 LA PRESSIONE ATMOSFERICA 3.1 Esperienza del Torricelli 3.2 Unità di misura delle pressioni 12 3.1 Peso dell aria I corpi solidi hanno un loro peso, ma anche i corpi gassosi e quindi l aria,
Capitolo 03 LA PRESSIONE ATMOSFERICA 3.1 Esperienza del Torricelli 3.2 Unità di misura delle pressioni 12 3.1 Peso dell aria I corpi solidi hanno un loro peso, ma anche i corpi gassosi e quindi l aria,
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
Quando si parla di inquinamento dell'acqua, si intende sia l'inquinamento dell'acqua superficiale (fiumi, laghi, mare) sia dell'acqua presente sotto
 L'acqua inquinata Quando si parla di inquinamento dell'acqua, si intende sia l'inquinamento dell'acqua superficiale (fiumi, laghi, mare) sia dell'acqua presente sotto il suolo (falde acquifere). Va tenuto
L'acqua inquinata Quando si parla di inquinamento dell'acqua, si intende sia l'inquinamento dell'acqua superficiale (fiumi, laghi, mare) sia dell'acqua presente sotto il suolo (falde acquifere). Va tenuto
GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce)
 GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce) I MINERALI I minerali sono sostanze solide omogenee, inorganiche, esprimibili mediante
GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce) I MINERALI I minerali sono sostanze solide omogenee, inorganiche, esprimibili mediante
La scuola integra culture. Scheda3c
 Scheda3c Gli ELEMENTI DEL CLIMA che caratterizzano le condizioni meteorologiche di una regione sono: la temperatura, la pressione atmosferica, i venti, l umidità e le precipitazioni. La temperatura è data
Scheda3c Gli ELEMENTI DEL CLIMA che caratterizzano le condizioni meteorologiche di una regione sono: la temperatura, la pressione atmosferica, i venti, l umidità e le precipitazioni. La temperatura è data
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Determinazione della composizione elementare dello ione molecolare. Metodo dell abbondanza isotopica. Misure di massa esatta
 Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
METALLI FERROSI GHISA ACCIAIO
 METALLI FERROSI I metalli ferrosi sono i metalli e le leghe metalliche che contengono ferro. Le leghe ferrose più importanti sono l acciaio e la ghisa. ACCIAIO: lega metallica costituita da ferro e carbonio,
METALLI FERROSI I metalli ferrosi sono i metalli e le leghe metalliche che contengono ferro. Le leghe ferrose più importanti sono l acciaio e la ghisa. ACCIAIO: lega metallica costituita da ferro e carbonio,
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
COME SI SONO PRODOTTE? Tutte le fonti di energia rinnovabili ed esauribili, oggi a nostra disposizione si sono generate dal sole.
 LE FONTI DI ENERGIA COSA SONO? Le fonti di energia sono sostanze in cui all origine è immagazzinata l energia che gli uomini utilizzano. Le fonti di energia più importanti sono quelle che sono in grado
LE FONTI DI ENERGIA COSA SONO? Le fonti di energia sono sostanze in cui all origine è immagazzinata l energia che gli uomini utilizzano. Le fonti di energia più importanti sono quelle che sono in grado
Classificazione della materia: Sostanze pure e miscugli
 Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
OSSIGENO DISCIOLTO ED EUTROFIZZAZIONE
 OSSIGENO DISCIOLTO ED EUTROFIZZAZIONE Un esempio di misure di ossigeno e ph in acque contenenti piante acquatiche (alla luce e al buio) Misura (con un ossimetro) dell ossigeno disciolto all inizio di un
OSSIGENO DISCIOLTO ED EUTROFIZZAZIONE Un esempio di misure di ossigeno e ph in acque contenenti piante acquatiche (alla luce e al buio) Misura (con un ossimetro) dell ossigeno disciolto all inizio di un
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
Total P Total S Ammonio NH 4
 2- - - LIMS Code Conductivity Calcio Magnesio Mg Sodio Na Potassio K Ione cloruro Cl- Solfati SO 4 Nitrati NO 3 Cation Total Anion Total Bromo Br Nitriti NO 2 µs cm -1 mg l -1 mg l -1 mg l -1 mg l -1 mg
2- - - LIMS Code Conductivity Calcio Magnesio Mg Sodio Na Potassio K Ione cloruro Cl- Solfati SO 4 Nitrati NO 3 Cation Total Anion Total Bromo Br Nitriti NO 2 µs cm -1 mg l -1 mg l -1 mg l -1 mg l -1 mg
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
LO STATO GASSOSO. Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi
 LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
La candela accesa. Descrizione generale. Obiettivi. Sequenza didattica e metodo di lavoro. Esperimenti sulla crescita delle piante
 Esperimenti sulla crescita delle piante unità didattica 1 La candela accesa Durata 60 minuti Materiali per ciascun gruppo - 1 candela - 1 vaso di vetro - 1 cronometro - 1 cannuccia - fiammiferi - 1 pezzo
Esperimenti sulla crescita delle piante unità didattica 1 La candela accesa Durata 60 minuti Materiali per ciascun gruppo - 1 candela - 1 vaso di vetro - 1 cronometro - 1 cannuccia - fiammiferi - 1 pezzo
SCUOLA PRIMARIA CURRICOLO DI SCIENZE CLASSE PRIMA. INDICATORI COMPETENZE ABILITA CONOSCENZE 1. Esplorare e descrivere oggetti e materiali
 SCUOLA PRIMARIA CURRICOLO DI SCIENZE CLASSE PRIMA INDICATORI 1. Esplorare e descrivere oggetti e materiali 2. Osservare e sperimentare sul campo Sviluppa atteggiamenti di curiosità verso il mondo circostante
SCUOLA PRIMARIA CURRICOLO DI SCIENZE CLASSE PRIMA INDICATORI 1. Esplorare e descrivere oggetti e materiali 2. Osservare e sperimentare sul campo Sviluppa atteggiamenti di curiosità verso il mondo circostante
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
CURRICOLO SCUOLA PRIMARIA SCIENZE COMPETENZE
 CURRICOLO SCUOLA PRIMARIA SCIENZE COMPETENZE - L alunno sviluppa atteggiamenti di curiosità e modi di guardare il mondo che lo stimolano a cercare spiegazioni di quello che vede succedere. - Esplora i
CURRICOLO SCUOLA PRIMARIA SCIENZE COMPETENZE - L alunno sviluppa atteggiamenti di curiosità e modi di guardare il mondo che lo stimolano a cercare spiegazioni di quello che vede succedere. - Esplora i
LEGGE DI STEVINO. La pressione non dipende dalla superficie della base del recipiente
 LA PRESSIONE NEI LIQUIDI DOVUTA ALLA FORZA PESO In condizioni di equilibrio la superficie libera di un liquido pesante deve essere piana ed orizzontale. Liquido di densitàρ Ogni strato orizzontale di liquido
LA PRESSIONE NEI LIQUIDI DOVUTA ALLA FORZA PESO In condizioni di equilibrio la superficie libera di un liquido pesante deve essere piana ed orizzontale. Liquido di densitàρ Ogni strato orizzontale di liquido
SCALA DEI PESI ATOMICI RELATIVI E MEDI
 SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Elettronica II Legame covalente e bande di energia nei solidi p. 2
 Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
LA MATERIA MATERIA. COMPOSIZIONE (struttura) Atomi che la compongono
 LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
Ciao, il mio nome è Sheppy e aiuterò il professore nella sua lezione! Salve, io sono il prof KinderCovi e oggi vi accompagnerò nel mondo dellʼacqua
 L acqua è la sostanza che rende possibile la vita degli uomini, degli animali e delle piante sulla terra. Non a caso le prime forme di vita si sono sviluppate nell acqua. Anche se la terra è ricoperta
L acqua è la sostanza che rende possibile la vita degli uomini, degli animali e delle piante sulla terra. Non a caso le prime forme di vita si sono sviluppate nell acqua. Anche se la terra è ricoperta
Lunghezza Massa Peso Volume Capacità Densità Peso specifico Superficie Pressione Forza Lavoro Potenza
 Misurare una grandezza La Grandezza 1. La grandezza è una caratteristica misurabile. Lunghezza Massa Peso Volume Capacità Densità Peso specifico Superficie Pressione Forza Lavoro Potenza 2. Misurare una
Misurare una grandezza La Grandezza 1. La grandezza è una caratteristica misurabile. Lunghezza Massa Peso Volume Capacità Densità Peso specifico Superficie Pressione Forza Lavoro Potenza 2. Misurare una
L acqua. Quando tantissime molecole di acqua si fondono insieme possiamo vedere l'acqua e berla o usarla.
 L acqua L'acqua è una sostanza molto importante, poiché forma la maggior parte dell'organismo umano. E' fatta di particelle molto piccole, gli ATOMI. Uno di questi atomi è chiamato IDROGENO (H) e l'altro
L acqua L'acqua è una sostanza molto importante, poiché forma la maggior parte dell'organismo umano. E' fatta di particelle molto piccole, gli ATOMI. Uno di questi atomi è chiamato IDROGENO (H) e l'altro
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 5. Il degli elementi SEGUI LA MAPPA B C N O F e Ne Na K Mg Ca Sc Ti V Cr Mn Fe Co
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 5. Il degli elementi SEGUI LA MAPPA B C N O F e Ne Na K Mg Ca Sc Ti V Cr Mn Fe Co
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Pressione. www.easymaths.altervista.org. 01 - Pressione.
 Pressione 01 - Pressione La forza è una grandezza fisica caratterizzata dal fatto di essere in grado di modificare lo stato di moto di un corpo o di modificarne la struttura interna Supponiamo che una
Pressione 01 - Pressione La forza è una grandezza fisica caratterizzata dal fatto di essere in grado di modificare lo stato di moto di un corpo o di modificarne la struttura interna Supponiamo che una
L ambiente è costituito da: una componente abiotica - (aria, acqua, terra, rocce, ecc.)
 L ambiente è costituito da: una componente abiotica - (aria, acqua, terra, rocce, ecc.) una componente biotica (esseri viventi) - (batteri, funghi, piante, animali, ecc.) ECOLOGIA (Häckel 1866) Scienza
L ambiente è costituito da: una componente abiotica - (aria, acqua, terra, rocce, ecc.) una componente biotica (esseri viventi) - (batteri, funghi, piante, animali, ecc.) ECOLOGIA (Häckel 1866) Scienza
Simulazione test di ingresso Ingegneria Industriale Viterbo. Quesiti di Logica, Chimica e Fisica. Logica
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
La materia. La materia è ogni cosa che occupa uno spazio (e possiamo percepire con i nostri sensi).
 La materia La materia è ogni cosa che occupa uno spazio (e possiamo percepire con i nostri sensi). Essa è costituita da sostanze, ciascuna delle quali è formata da un determinato tipo di particelle piccolissime,
La materia La materia è ogni cosa che occupa uno spazio (e possiamo percepire con i nostri sensi). Essa è costituita da sostanze, ciascuna delle quali è formata da un determinato tipo di particelle piccolissime,
CURRICOLO DISCIPLINARE DI SCIENZE
 A.S. 2014/2015 MINISTERO DELL ISTRUZIONE DELL UNIVERSITÀ E DELLA RICERCA Istituto Comprensivo Palena-Torricella Peligna Scuola dell Infanzia, Primaria e Secondaria di 1 grado Palena (CH) SCUOLA PRIMARIA
A.S. 2014/2015 MINISTERO DELL ISTRUZIONE DELL UNIVERSITÀ E DELLA RICERCA Istituto Comprensivo Palena-Torricella Peligna Scuola dell Infanzia, Primaria e Secondaria di 1 grado Palena (CH) SCUOLA PRIMARIA
Pressione. Esempio. Definizione di pressione. Legge di Stevino. Pressione nei fluidi EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI
 Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria
 Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
TEORIA CINETICA DEI GAS
 TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
RADIAZIONI RADIAZIONI IONIZZANTI RADIAZIONI IONIZZANTI
 RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
RADIAZIONI Le radiazioni ionizzanti sono quelle onde elettromagnetiche in grado di produrre coppie di ioni al loro passaggio nella materia (raggi X, raggi gamma, raggi corpuscolari). Le radiazioni non
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Gli organismi viventi
 Gli organismi viventi Gli organismi viventi Quali caratteristiche contraddistinguono i viventi? È facile distinguere un organismo vivente da un oggetto non vivente? Gli organismi viventi Tutti gli organismi
Gli organismi viventi Gli organismi viventi Quali caratteristiche contraddistinguono i viventi? È facile distinguere un organismo vivente da un oggetto non vivente? Gli organismi viventi Tutti gli organismi
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti.
 Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Esperto prof. C. Formica
 Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
Analisi delle acque dell isola di Favignana
 Analisi delle acque dell isola di Favignana Durante le attività svolte al campo scuola nell ambito del progetto Un mare di.. risorse, il nostro gruppo si è occupato di analizzare le acque del mare in diversi
Analisi delle acque dell isola di Favignana Durante le attività svolte al campo scuola nell ambito del progetto Un mare di.. risorse, il nostro gruppo si è occupato di analizzare le acque del mare in diversi
Proprieta meccaniche dei fluidi
 Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
Base di lavoro. Idea principale
 Base di lavoro Idea principale «Gli esseri viventi vivono in relazione tra loro e con l ambiente che li ospita, all interno di particolari ecosistemi dotati di un equilibrio ben preciso. Tutti gli organismi
Base di lavoro Idea principale «Gli esseri viventi vivono in relazione tra loro e con l ambiente che li ospita, all interno di particolari ecosistemi dotati di un equilibrio ben preciso. Tutti gli organismi
Il sistema periodico degli elementi
 Il sistema periodico degli elementi Gli elementi mostrano una variazione progressiva delle proprietà chimiche; dopo un definito numero di elementi, le medesime proprietà si ripetono con deboli variazioni
Il sistema periodico degli elementi Gli elementi mostrano una variazione progressiva delle proprietà chimiche; dopo un definito numero di elementi, le medesime proprietà si ripetono con deboli variazioni
CORSO DI GEOPEDOLOGIA A.S. 2012 2013 prof. Luca Falchini LA STRUTTURA INTERNA DELLA TERRA
 CORSO DI GEOPEDOLOGIA A.S. 2012 2013 prof. Luca Falchini LA STRUTTURA INTERNA DELLA TERRA Indagini dirette Scavi per ricerche minerarie, energetiche e idriche; carotaggi Non si giunge oltre i 12 km di
CORSO DI GEOPEDOLOGIA A.S. 2012 2013 prof. Luca Falchini LA STRUTTURA INTERNA DELLA TERRA Indagini dirette Scavi per ricerche minerarie, energetiche e idriche; carotaggi Non si giunge oltre i 12 km di
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Gli elementi di transizione
 Gli elementi di transizione A partire dal quarto periodo del Sistema Periodico, nella costruzione della configurazione elettronica degli elementi, dopo il riempimento degli orbitali s del guscio di valenza
Gli elementi di transizione A partire dal quarto periodo del Sistema Periodico, nella costruzione della configurazione elettronica degli elementi, dopo il riempimento degli orbitali s del guscio di valenza
Il concetto di valore medio in generale
 Il concetto di valore medio in generale Nella statistica descrittiva si distinguono solitamente due tipi di medie: - le medie analitiche, che soddisfano ad una condizione di invarianza e si calcolano tenendo
Il concetto di valore medio in generale Nella statistica descrittiva si distinguono solitamente due tipi di medie: - le medie analitiche, che soddisfano ad una condizione di invarianza e si calcolano tenendo
L ENERGIA. Suona la sveglia. Accendi la luce. Ti alzi e vai in bagno. Fai colazione. A piedi, in bicicletta o in autobus, vai a scuola.
 L ENERGIA Suona la sveglia. Accendi la luce. Ti alzi e vai in bagno. Fai colazione. A piedi, in bicicletta o in autobus, vai a scuola. La giornata è appena iniziata e hai già usato tantissima ENERGIA:
L ENERGIA Suona la sveglia. Accendi la luce. Ti alzi e vai in bagno. Fai colazione. A piedi, in bicicletta o in autobus, vai a scuola. La giornata è appena iniziata e hai già usato tantissima ENERGIA:
LA LEGGE DI GRAVITAZIONE UNIVERSALE
 GRAVIMETRIA LA LEGGE DI GRAVITAZIONE UNIVERSALE r La legge di gravitazione universale, formulata da Isaac Newton nel 1666 e pubblicata nel 1684, afferma che l'attrazione gravitazionale tra due corpi è
GRAVIMETRIA LA LEGGE DI GRAVITAZIONE UNIVERSALE r La legge di gravitazione universale, formulata da Isaac Newton nel 1666 e pubblicata nel 1684, afferma che l'attrazione gravitazionale tra due corpi è
-assicurare il fabbisogno plastico necessario alla riparazione protezione e ricambio dei tessuti.
 Il principali compiti derivanti dall assunzione periodica di cibo sono: -assicurare il giusto fabbisogno energetico necessario alla vita ed all attività muscolare (tenendo conto che entrate ed uscite devono
Il principali compiti derivanti dall assunzione periodica di cibo sono: -assicurare il giusto fabbisogno energetico necessario alla vita ed all attività muscolare (tenendo conto che entrate ed uscite devono
Capitolo II. La forma del valore. 7. La duplice forma in cui si presenta la merce: naturale e di valore.
 Capitolo II La forma del valore 7. La duplice forma in cui si presenta la merce: naturale e di valore. I beni nascono come valori d uso: nel loro divenire merci acquisiscono anche un valore (di scambio).
Capitolo II La forma del valore 7. La duplice forma in cui si presenta la merce: naturale e di valore. I beni nascono come valori d uso: nel loro divenire merci acquisiscono anche un valore (di scambio).
I SISTEMI DI UNITA DI MISURA
 Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
CICLO DELL ACQUA. Marco Carozzi
 CICLO DELL ACQUA Marco Carozzi Sommario Ciclo biogeochimico La molecola d acqua: breve introduzione Ciclo dell acqua ed elementi del ciclo evaporazione, evapotraspirazione, condensazione, precipitazioni,
CICLO DELL ACQUA Marco Carozzi Sommario Ciclo biogeochimico La molecola d acqua: breve introduzione Ciclo dell acqua ed elementi del ciclo evaporazione, evapotraspirazione, condensazione, precipitazioni,
SCIENZE SCUOLA PRIMARIA
 SCIENZE SCUOLA PRIMARIA CLASSE PRIMA 1 I CINQUE SENSI 1. Osservare il funzionamento del proprio corpo per riconoscerlo come organismo complesso 2. Osservare e riconoscere alcune caratteristiche dei corpi
SCIENZE SCUOLA PRIMARIA CLASSE PRIMA 1 I CINQUE SENSI 1. Osservare il funzionamento del proprio corpo per riconoscerlo come organismo complesso 2. Osservare e riconoscere alcune caratteristiche dei corpi
STUDIO GEOCHIMICO DEL PARTICOLATO ATMOSFERICO
 UNIVERSITA CA FOSCARI VENEZIA DIPARTIMENTO DI SCIENZE AMBIENTALI STUDIO GEOCHIMICO DEL PARTICOLATO ATMOSFERICO Prof. Rampazzo Giancarlo CHE COS E LA GEOCHIMICA 1.La geochimica studia la composizione chimica
UNIVERSITA CA FOSCARI VENEZIA DIPARTIMENTO DI SCIENZE AMBIENTALI STUDIO GEOCHIMICO DEL PARTICOLATO ATMOSFERICO Prof. Rampazzo Giancarlo CHE COS E LA GEOCHIMICA 1.La geochimica studia la composizione chimica
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
Istituto Comprensivo Casalgrande (R.E.) PROGETTAZIONE DI ISTITUTO. "SCIENZE" - Scuola primaria. Obiettivi formativi di Istituto
 Istituto Comprensivo Casalgrande (R.E.) PROGETTAZIONE DI ISTITUTO "SCIENZE" - Scuola primaria Obiettivi formativi di Istituto CLASSE PRIMA SCIENZE - ED. ALLA SALUTE - ED. AMBIENTALE Esplorare ii mondo
Istituto Comprensivo Casalgrande (R.E.) PROGETTAZIONE DI ISTITUTO "SCIENZE" - Scuola primaria Obiettivi formativi di Istituto CLASSE PRIMA SCIENZE - ED. ALLA SALUTE - ED. AMBIENTALE Esplorare ii mondo
 Il Sole Variazioni dell energia solare entrante: Obliquità orbitale Attualmente l asse di rotazione terrestre è inclinato di 23.4 rispetto alla perpendicolare sul piano orbitale terrestre. Ogni 41 000
Il Sole Variazioni dell energia solare entrante: Obliquità orbitale Attualmente l asse di rotazione terrestre è inclinato di 23.4 rispetto alla perpendicolare sul piano orbitale terrestre. Ogni 41 000
9. Urti e conservazione della quantità di moto.
 9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
OBIETTIVI DI APPRENDIMENTO (AL TERMINE DELLA CLASSE PRIMA DELLA SCUOLA PRIMARIA) TRAGUARDI PER LO SVILUPPO DELLE COMPETENZE SCIENZE
 (AL TERMINE DELLA SCUOLA DELL INFANZIA) /ESPERIENZE LA CONOSCENZA DEL MONDO L alunno osserva con curiosità lo svolgersi dei più comuni fenomeni, ne immagina e ne verifica le cause, rendendosi sempre più
(AL TERMINE DELLA SCUOLA DELL INFANZIA) /ESPERIENZE LA CONOSCENZA DEL MONDO L alunno osserva con curiosità lo svolgersi dei più comuni fenomeni, ne immagina e ne verifica le cause, rendendosi sempre più
MODELLI ATOMICI. Modello Atomico di Dalton
 MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
MODELLI ATOMICI Gli atomi sono i piccoli mattoni che compongono la materia. Circa 2500 anni fa, il filosofo DEMOCRITO credeva che tutta la materia fosse costituita da piccole particelle che chiamò atomi.
Nascita e morte delle stelle
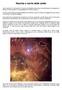 Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
La catena alimentare. Sommario
 La catena alimentare classe Istituto Comprensivo anno scolastico 2009/10 Sommario Che cos è la catena alimentare Il ciclo alimentare I produttori I consumatori primari I consumatori secondari I consumatori
La catena alimentare classe Istituto Comprensivo anno scolastico 2009/10 Sommario Che cos è la catena alimentare Il ciclo alimentare I produttori I consumatori primari I consumatori secondari I consumatori
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
MODULO D LE VENTI REGIONI ITALIANE VOLUME 1 CAPITOLO 2 ... ... ... ... ... ...
 VOLUME 1 CAPITOLO 2 MODULO D LE VENTI REGIONI ITALIANE ACQUE INTERNE 1. Parole per capire A. Conosci già queste parole? Scrivi il loro significato o fai un disegno: valle... ghiacciaio... vulcano... cratere...
VOLUME 1 CAPITOLO 2 MODULO D LE VENTI REGIONI ITALIANE ACQUE INTERNE 1. Parole per capire A. Conosci già queste parole? Scrivi il loro significato o fai un disegno: valle... ghiacciaio... vulcano... cratere...
Scuola Media Piancavallo 2
 LA CELLULA Una caratteristica di quasi tutti gli esseri viventi è quella di possedere una struttura più o meno complessa in cui parti diverse, gli organi, sono adatte a svolgere funzioni specifiche. Il
LA CELLULA Una caratteristica di quasi tutti gli esseri viventi è quella di possedere una struttura più o meno complessa in cui parti diverse, gli organi, sono adatte a svolgere funzioni specifiche. Il
I MATERIALI SCELTA DEL MATERIALE SCELTA DEL MATERIALE FUNZIONALITÀ
 SCELTA DEL MATERIALE I MATERIALI LA SCELTA DEL MATERIALE PER LA COSTRUZIONE DI UN PARTICOLARE MECCANICO RICHIEDE: LA CONOSCENZA DELLA FORMA E DELLE DIMEN- SIONI DELL OGGETTO LA CONOSCENZA DEL CICLO DI
SCELTA DEL MATERIALE I MATERIALI LA SCELTA DEL MATERIALE PER LA COSTRUZIONE DI UN PARTICOLARE MECCANICO RICHIEDE: LA CONOSCENZA DELLA FORMA E DELLE DIMEN- SIONI DELL OGGETTO LA CONOSCENZA DEL CICLO DI
10) Se ad una soluzione aumentiamo la temperatura cosa succede? Dire quale delle seguenti affermazioni è corretta.
 Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
CORRENTE E TENSIONE ELETTRICA LA CORRENTE ELETTRICA
 CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
L APPARATO CIRCOLATORIO
 L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
LABORATORI SULL ARIA E SULLA PRESSIONE ATMOSFERICA (ALL.
 L'ARIA L'aria è una cosa leggera che ricopre tutta la terra come copre la buccia la pera ma nessuno la vede o l'afferra E' una specie di fumo lucente e anche se non si vede con gli occhi, la respira col
L'ARIA L'aria è una cosa leggera che ricopre tutta la terra come copre la buccia la pera ma nessuno la vede o l'afferra E' una specie di fumo lucente e anche se non si vede con gli occhi, la respira col
1. LE GRANDEZZE FISICHE
 1. LE GRANDEZZE FISICHE La fisica (dal greco physis, natura ) è una scienza che ha come scopo guardare, descrivere e tentare di comprendere il mondo che ci circonda. La fisica si propone di descrivere
1. LE GRANDEZZE FISICHE La fisica (dal greco physis, natura ) è una scienza che ha come scopo guardare, descrivere e tentare di comprendere il mondo che ci circonda. La fisica si propone di descrivere
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Ripasso pre-requisiti di scienze per gli studenti che si iscrivono alle classi prime
 Ripasso pre-requisiti di scienze per gli studenti che si iscrivono alle classi prime Per seguire proficuamente i corsi di scienze della scuola superiore devi conoscere alcune definizioni e concetti di
Ripasso pre-requisiti di scienze per gli studenti che si iscrivono alle classi prime Per seguire proficuamente i corsi di scienze della scuola superiore devi conoscere alcune definizioni e concetti di
Un po di statistica. Christian Ferrari. Laboratorio di Matematica
 Un po di statistica Christian Ferrari Laboratorio di Matematica 1 Introduzione La statistica è una parte della matematica applicata che si occupa della raccolta, dell analisi e dell interpretazione di
Un po di statistica Christian Ferrari Laboratorio di Matematica 1 Introduzione La statistica è una parte della matematica applicata che si occupa della raccolta, dell analisi e dell interpretazione di
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI
 Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail danidvd@hotmail.it daniela.devita@uniroma1.it
Corso di Chimica e Stechiometria per il corso di laurea in SCIENZE AMBIENTALI Dott.ssa DANIELA DE VITA Orario ricevimento (previo appuntamento):lunedì 17.30-18.30 E-mail danidvd@hotmail.it daniela.devita@uniroma1.it
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Glossario dei termini utilizzati nella tabella dei dati di rilevamento:
 Glossario dei termini utilizzati nella tabella dei dati di rilevamento: CONCENTRAZIONE DEGLI IONI IDROGENO (PH) E' la misura della quantità di ioni idrogeno presenti nell'acqua, e ne fornisce di conseguenza
Glossario dei termini utilizzati nella tabella dei dati di rilevamento: CONCENTRAZIONE DEGLI IONI IDROGENO (PH) E' la misura della quantità di ioni idrogeno presenti nell'acqua, e ne fornisce di conseguenza
Quiz di scienze l acqua
 Quiz di scienze l acqua 1. Da cos e composta l acqua? Idrogeno e ossigeno Tanti piccoli animaletti trasparenti chiamati pesci acquiferi E uno dei misteri dell umanita, gli scienziati non sono ancora riusciti
Quiz di scienze l acqua 1. Da cos e composta l acqua? Idrogeno e ossigeno Tanti piccoli animaletti trasparenti chiamati pesci acquiferi E uno dei misteri dell umanita, gli scienziati non sono ancora riusciti
Intorno alla Terra è presente un atmosfera diversa da quella degli altri pianeti rende possibile la vita fornendo ossigeno e diossido di carbonio
 L Atmosfera Intorno alla Terra è presente un atmosfera diversa da quella degli altri pianeti rende possibile la vita fornendo ossigeno e diossido di carbonio Protegge la superficie terrestre da temperature
L Atmosfera Intorno alla Terra è presente un atmosfera diversa da quella degli altri pianeti rende possibile la vita fornendo ossigeno e diossido di carbonio Protegge la superficie terrestre da temperature
Lavoro di. Istituto Comprensivo Statale Console Marcello MILANO
 Lavoro di Istituto Comprensivo Statale Console Marcello MILANO Anno Scolastico 2009/2010 INDICE Presentazione Prima parte : -Gli elementi del computer (presentazione degli elementi del computer al fine
Lavoro di Istituto Comprensivo Statale Console Marcello MILANO Anno Scolastico 2009/2010 INDICE Presentazione Prima parte : -Gli elementi del computer (presentazione degli elementi del computer al fine
MASSA VOLUMICA o DENSITA
 MASSA VOLUMICA o DENSITA Massa volumica di una sostanza: è la massa di sostanza, espressa in kg, che occupa un volume pari a 1 m 3 1 m 3 di aria ha la massa di 1,2 kg 1 m 3 di acqua ha la massa di 1000
MASSA VOLUMICA o DENSITA Massa volumica di una sostanza: è la massa di sostanza, espressa in kg, che occupa un volume pari a 1 m 3 1 m 3 di aria ha la massa di 1,2 kg 1 m 3 di acqua ha la massa di 1000
Gas e gas perfetti. Marina Cobal - Dipt.di Fisica - Universita' di Udine 1
 Gas e gas perfetti 1 Densita Densita - massa per unita di volume Si misura in g/cm 3 ρ = M V Bassa densita Alta densita Definizione di Pressione Pressione = Forza / Area P = F/A unita SI : 1 Nt/m 2 = 1
Gas e gas perfetti 1 Densita Densita - massa per unita di volume Si misura in g/cm 3 ρ = M V Bassa densita Alta densita Definizione di Pressione Pressione = Forza / Area P = F/A unita SI : 1 Nt/m 2 = 1
Lunedì 20 dicembre 2010. Docente del corso: prof. V. Maiorino
 Lunedì 20 dicembre 2010 Docente del corso: prof. V. Maiorino Se la Terra si spostasse all improvviso su un orbita dieci volte più lontana dal Sole rispetto all attuale, di quanto dovrebbe variare la massa
Lunedì 20 dicembre 2010 Docente del corso: prof. V. Maiorino Se la Terra si spostasse all improvviso su un orbita dieci volte più lontana dal Sole rispetto all attuale, di quanto dovrebbe variare la massa
