L OSSIGENO, L INCENDIO, GLI EFFETTI SULL UOMO.
|
|
|
- Gilda Scotti
- 6 anni fa
- Visualizzazioni
Transcript
1 in collaborazione con Consulta Regionale Ordini Ingegneri Lombardia L OSSIGENO, L INCENDIO, GLI EFFETTI SULL UOMO. Bortolo Balduzzi Mantova, 26 maggio 2017
2 L OSSIGENO molecolabiatomica O 2 ; numeroatomico8 1s 2 2s 2 2p 4 n quantico principale 1 n quantico principale 2 massaatomica15,9994gmol -1 massamolecolare32gmol -1 percentuale in volume nell aria ambiente20,9%;
3 CONSIDERAZIONI SUL VOLUME DEI GAS COINVOLTI NELL INCENDIO nell incendio, contrariamente a quanto avvieneperaltreconsiderazionisuiprocessi di combustione, non si tiene mai conto dell eccessod aria; tale considerazione deriva dal fatto che si presuppone che il materiale bruci fino al suototaleesaurimentoecheilquantitativo d aria necessario sia, nell ipotesi più cautelativa,quellostechiometrico;
4 CONSIDERAZIONI SUL VOLUME DEI GAS COINVOLTI NELL INCENDIO In realtà la massa combustibile interessata da incendio difficilmente partecipa nella sua totalità al processo di combustioneper: materiale combustibile entro contenitori incombustibili; distribuzionespazialesfavorevole; ammassamentosfavorevole; abbassamentodella%dio 2 nelcompart. umiditàdellamassacombustibile.
5 CONSIDERAZIONI SUL VOLUME DEI GAS COINVOLTI NELL INCENDIO di questa circostanza si tiene conto, per i materiali principalmente cellulosici, con il fattoredipartecipazioneallacombustione m i = 0,80 80 e con il fattore di limitazione alla combustione ψ i = 0,85 combustibili. 85 per contenitori non (UNI EN , D.M , D.M cap. S.2-Co.p.i.).
6 CONSIDERAZIONI SUL VOLUME DEI GAS COINVOLTI NELL INCENDIO Il rapporto tra la massa mo 2 di O 2, necessaria per ossidare una massa m c di combustibile è denominata oxigenfuel mass ratio ed è frequently indicatainletteraturaconr O m O r = 2 o m c
7 CONSIDERAZIONI SUL VOLUME DEI GAS COINVOLTI NELL INCENDIO Il rapporto tra la massa m aria di aria, necessaria per ossidare una massa m c di combustibile è indicata in letteratura conr aria r = aria m aria m c
8 CONSIDERAZIONI SUL VOLUME DEI GAS COINVOLTI NELL INCENDIO Considerando che una mole di aria ha massamolareparia28,8g,cheunadi O 2 ha massa molare di 32 g e che la percentuale,involume, dio 2 inariaè del21%siottiene: r aria r O = m m c aria m c mo 2 = 1 0,21 28,8 32 = 4,29 equindi: r = 4,29 r aria O
9 tab. 1 r O e r aria PER ALCUNI COMBUSTIBILI COMBUSTIBILE r o (g O2 /g combust. ) r aria (g aria /g combust. ) COMBUSTIBILE r o (g O2 /g combust. ) r aria (g aria /g combust. ) ACETILENE 3,10 13,30 FORMALDEIDE 1,07 4,59 ACETONE 2,20 9,40 IDROGENO 8,00 34,30 BENZENE 3,10 13,30 CARBONE 2,70 11,60 ETANOLO 2,10 9,00 ACIDO CIANIDRICO CARBON MONOXIDE POLICLORURO DI VINILE 1,48 6,53 0,57 2,44 1,40 6,00 METANO 4,00 17,20 POLISTIRENE 3,10 13,20 LEGNO 1,30 5,70 POLIURETANO 1,70 7,30 PROPANO 3,60 15,60 NYLON 2,30 9,90 POLIETILENE 3,40 14,60 CELLULOSA 1,20 5,10 POLIPROPILEN E 3,80 16,30 POLICARBONATO 2,30 9,80 STIRENE 3,07 13,30 TOLUENE 3,10 13,30
10 Con i valori di tab. 1 è rapido ed immediato eseguire i calcoli del fabbisogno di O 2. esercizio: per bruciare 664,48 g di CH 4 (1 m 3 a 20 C ed a p atmosferica) servono, con il dato di tab. 1, per il metano: 664,48 r aria CH4 = 664,48 x 17,20 = ,05 g di aria che, a 20 C, corrispondono ad un volume: R T ,05 8, ,15 V = n = = p 28,8 101,226E3 9,51 m 3 Per bruciare 1m 3 di metano, a pressione atmosferica, servono, notoriamente, ~ 10 m 3 di aria.
11 ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DI MASSA DI COMBURENTE ARIA (MJ/kg aria ) Se si divide il valore del p.c.i. (MJ) di un qualsiasi combustibile per la massa di comburente necessaria per la combustione completa si ottiene che tale rapporto vale: P = 3, 00 c aria ΜJ kg aria
12 ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DI MASSA DICOMBURENTE O 2 (MJ/kg O2 ) Se si divide il valore del p.c.i. (MJ) di un qualsiasi combustibile per la massa di comburente, necessaria per la combustione completa si ottiene che tale rapporto vale: MJ P c O 2 = 13, 10 kg O 2
13 esempio :il legno standard ha p.c.i. pari a x 427 x 9,8 E-6 = 17,57 MJ/kg e necessita di 5,7 kg di aria (o di 1,3 kg di O 2 ) (tab.1). Si ottiene pertanto: 17,57 P = = 3, 08 c aria, legno 5,7 MJ kg aria P c 17,57 = = 13, 51 O2, legno 1,3 MJ kg O 2
14 Tali rapporti sono fondamentali perché rappresentano l energia rilasciata dall incendio per unità di massa comburente entrante nel compartimento. E ciò indipendentemente dal combustibile ivi contenuto.
15 tab. 2 - ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DIMASSADICOMBURENTE (MJ/kg O2,aria ) COMBUSTIBILE MJ/kg O2 MJ/kg aria METANO 12,54 2,91 PROPANO 12,80 2,97 ETANOLO 12,88 2,99 ACETONE 14,00 3,25 CELLULOSA 13,59 3,15 LEGNO 13,85 3,23 POLIETILENE 12,65 2,93 POLIPROPILENE 12,66 2,94 CLORURO DI VINILE 12,84 2,98 POLISTIRENE 12,97 3,01 NYLON 12,67 2,94 POLIURETANO 15,27 3,56 POLICARBONATO 13,12 3,04
16 Tali rapporti permettono facilmente, tra l altro,di: determinare la massima energia rilasciabiledall incendionotalaquantitàdi comburente in ingresso o presente nel compartimento; determinare la massa di combustibile che può bruciare a fronte di una determinata quantità di comburente disponibile nel compartimento.
17 determinare il volume di aria totale necessariaperlacombustione. Sinotiche: è possibile limitare lo sviluppo di energia da combustione limitando l apporto di aria (dio 2 )alcompartimento;
18 ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DI MASSA DI COMBURENTE esempio: dato un compartimento avente dimensioni di 30,00 x 100,00 x 7,00 m, determinare la massima energia rilasciabile nel compartimento senza apporto di aria esterna; -volume di aria del compartimento: 30,00x100,00x7,00= m 3 30,00 m 7,00 m
19 ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DI MASSA DI COMBURENTE -corrispondenteadunnumerodimolidio 2 n = p V R T = , 56 (0, ) 8, , 15 = ,23 moli di O 2 -massadio 2 presentenelcompartimento: ,23 E3 32 = 5.861,06 kg di O 2
20 ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DI MASSA DI COMBURENTE -energia massima rilasciabile nel compartimento 5.861,06 P O 2 c = 1.172,21 13,1 = , 93 MJ corrispondente ad un carico specifico d incendio: q f ,93 MJ 25,60 kg = = 25,60 2 = = 1, m 17,5 m di l.s.
21 ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DI MASSA DI COMBURENTE -nel compartimento quindi il carico di incendio di riferimento non può essere superioreatalevalore. -dividendo l energia massima rilasciabile, MJ, per il p.c.i. del materiale combustibile si ottiene la massa bruciabile. Nelcasodilegnocon p.c.i. = 18,41 MJ/kg m = = 834, 11 c 18, 41 kg
22 ENERGIA RILASCIATA DA UN COMBUSTIBILE PER UNITA DI MASSA DI COMBURENTE N.B. In realtà tale quantità di combustibile non potrà bruciare completamente; risultati sperimentali indicano infatti che quando la % di O 2 in ambiente scende al di sotto del % (~ ½ della concentrazione atmosferica) il processo di combustione non è più in grado diautosostenersi.
23 La piròlisi
24 La piròlisi
25 La piròlisi del legno n FASE t ( C) ESSICAZIONE EvaporazioneH 2 O GASSIFICAZIONE Scomposizione termica piròlisi, liberazione gas combustibili (CO, C n H m )ecarbonesolido(c) OSSIDAZIONE Combustione dei gas di piròlisi e del carbone(c) 100 < t < < t < < t < 1.300
26 Lapiròlisièpiùveloceinmasseconbassainerziatermica con: b ρ densità del materiale (kg/m 3 ); ( kj / m 2 s 0,5 K) c p calore specifico del materiale (kj/kg K); p = ρ λ conduttività termica del materiale (kw/m K); Esempio: -Poliuretano,inerziatermicab=41kJ/m 2 s 0,5 K -Legnodipino,inerziatermicab=500kJ/m 2 s 0,5 K c p λ IL POLIURETANO BRUCIA PIU FACILMENTE DEL LEGNO DI PINO
27 Temperatura T ( C) LA CURVA T-t Temperatura tempo (1) t = 0 INCENDIO PIENAMENTE SVILUPPATO (post Flashover) MISURE PASSIVE VELOCITA DI COMBUSTIONE ṁ c = COSTANTE Requisiti all.to A D. M R, E, EI, M, W, S.. 2 d T 2 dt = 0 tempo t (min)
28 LA CURVA T-t Temperatura tempo (2)
29 LA CURVA T-t Temperatura-tempo(3) la curva Temperatura - tempo non fornisce tutte le indicazioni utili per essere considerata un modello esaustivo dell incendio. fino al punto di flashover ha valore puramente convenzionale e non descrive fisicamente alcun fenomeno; il flashover è sempre possibile e non è noto il tempo a cui si verifica; parimenti non si hanno informazioni sulla durata dell incendio.
30 LA CURVA T-t Temperatura-tempo(3) non si hanno indicazioni sull energia messa in gioco (potenza liberata nel compartimento) nell evoluzione temporale dell incendio; non vengono forniti valori di concentrazione dei gas di combustione nel compartimento; gli effetti delle eventuali azioni di spegnimento sono di difficile valutazione;
31 VELOCITA MASSIMA DI COMBUSTIONE - INCENDIO PIENAMENTE SVILUPPATO E CONTROLLATO DALLA VENTILAZIONE (post FLASHOVER) (Kawagoe& Sekine) mc, max = 0,092 A v h ṁ c, max Velocità massima di combustione (kg/s) A v Area superfici ventilanti (m 2 ) i i i h Dato dall espressione: (m) A i Area di ventilazione i-esima (m 2 ) h = Σ Ah Σ A i i h i Altezza della i-esima superficie ventilante A i (m)
32 OPENING FACTOR O A v h eq (rappresenta la normalizzazione di rispetto ad A t ) O = A v h eq A t O Opening factor (m 0,5 ) rappresenta la normalizzazione del compartimento, rispetto ad A t, sotto il profilo dell apporto di aria comburente. h = h eq Dato dall espressione: (m) A t Area superficie totale del compartimento (pareti, soffitto, pavimento) (m 2 ) A v Area superfici ventilanti (m 2 ) eq Σi Avi h Σ A i vi A v = Σ bh i i i i
33 OPENING FACTOR O ) 0,5 t eq v (m h O A A = ) (m 2 A 2 t L L L L L L = ) (m bh Σ A i i i v 2 = (m) A A h Σ h v i vi i eq =
34 VENTILATION FACTOR O (dal manuale CFAST)
35 Es.4: determinare il fattore di ventilazione O di un compartimento avente dimensioni larghezza 19,00 m, lunghezza 23 m, altezza 4,00 m; sulle pareti laterali sono presenti: -n 2porte 2,00x2,20m -n 4finestre 2,00x1,50m -n 5finestre 2,50x1,50m 1.0-DIMENSIONI DEL COMPARTIMENTO (m) L1 L2 L3 4,00 19,00 23, DIMENSIONE APERTURE progr. n b h n b h n b h 2 DI VENTILAZIONE (m) 1 2 2,00 2,20 8,80 19, ,00 1,50 12,00 18, ,50 1,50 18,75 28, ,00 0,00 0,00 0, ,00 0,00 0,00 0, ,00 0,00 0,00 0, ,00 0,00 0,00 0, A t = 1.210,00 m h eq = 1,66 m 4.0- A v = 39,55 m O = 0,042 m 0,5
36 Burning rate ṁ c in funzione di q f e di O INCENDIO PIENAMENTE SVILUPPATO (curve sperimentali di Thomas-Heselden) ṁ c ventilation controlled fuel bed controlled key q f (MJ/m 2 ) x mc, max = 6 A v h ( Heselden) mc, max = 5, 5 A v h ( Kawagoe) A v A At h v h eq Da O. Vassart: Background & Applications Structural Fire Design
37 INCENDIO CONTROLLATO DALLA VENTILAZIONE E INCENDIO CONTROLLATO DAL COMBUSTIBILE(1) Incendio controllato dalla ventilazione: la velocità di combustione ṁ c dipende solo dall apporto di comburente valutato tramite il fattore di ventilazione O, (Kawagoe & Sekine, Heselden, Law.); Incendio controllato dal combustibile: la velocità di combustione è fortemente influenzata da quantità (q f ), forma, porosità, pezzatura, orientamento del combustibile e non dall apporto di comburente; ad es. le bobine di carta bruciano molto più facilmente se immagazzinate con l asse verticale anziché orizzontale.;
38 Lavelocitàdicombustioneṁ c èall incircaproporzionalealvaloredi q f ; INCENDIO CONTROLLATO DALLA VENTILAZIONE E INCENDIO CONTROLLATO DAL COMBUSTIBILE(2) Il valore di O che separa i due regimi è all incirca di 0,06 0,07m 0,5 (inletteraturavienespessoindicatoancheilvalore 0,08m 0,5 ). Generalmente l incendio, nelle prime fasi, ignizione e crescita, è controllato dal combustibile e, successivamente, in particolare dopo il flashover, diventa controllato dalla ventilazione;
39 VELOCITA MASSIMA DI COMBUSTIONE - INCENDIO PIENAMENTE SVILUPPATO E CONTROLLATO DALLA VENTILAZIONE (post FLASHOVER) - INFLUENZADI WeD(Law-1983) eq c, max = 0,18 Av e m h D W ( 0,036 Ω 1 ) ṁc, max Velocità massima di combustione (kg/s) A v Area superfici ventilanti (m 2 ) h = h eq Dato dall espressione: (m) A i Area di ventilazione i-esima (m 2 ) eq Σi Avi h Σ A i vi i h i Altezza della i-esima superficie ventilante A i (m)
40 VELOCITA MASSIMA DI COMBUSTIONE - INCENDIO PIENAMENTE SVILUPPATO E CONTROLLATO DALLA VENTILAZIONE (post FLASHOVER) - INFLUENZADI WeD(Law-1983) W D Larghezza del compartimento (m) Lunghezza del compartimento (m) Ω Dato dall espressione: (m -0,5 ) Ω Quando W=D(compartimento a pianta quadrata) ed O = = 0,05 = m 0,5 (W = 20) la formula di Law e quella di Kawagoe & Sekine forniscono gli stessi risultati. A A t v A h v eq A A v h eq t
41 Composizione dell aria atmosferica secca COMPONENTE FORMULA PROPORZIONE O FRAZIONE MOLARE AZOTO N 2 78,08% (in volume) OSSIGENO O 2 20,95% (in volume) ARGON Ar 0,934% (in volume) ANIDRIDECARBONICA CO 2 404,16 ppm NEON Ne 18,18 ppm ELIO He 5,24 ppm MONOSSIDO DI AZOTO NO 5 ppm KRIPTON Kr 1,14 ppm METANO CH ppm HIDROGENO H 2 0,5 ppm OSSIDO DIAZOTO N 2 O 0,5 ppm XENO Xe 0,087 ppm DIOSSIDO DIAZOTO NO 2 0,02 ppm OZONO O 3 da 0 a 0,01 ppm RADON Rn ppm
42 Standard atmosphere 1976 ALTITUDINE (geometrica, m) TEMPERATURA ASSOLUTA (K) PRESSIONE (hpa) DENSITÀ (kg/m³) VISCOSITÀ DINAMICA (Pa s) VELOCITÀ DEL SUONO (m/s)
43 O 2 (%lein vol.) effetti e sintomi 22,50 Massima concentrazione di sicurezza. 21 Concentrazione media in aria Non ci sono sintomi riconoscibili da parte della persona esposta. Si deve effettuare valutazione del rischio per appurarelasicurezza* ) Riduzione delle prestazioni fisiche e intellettuali senza che la personaespostanesiacosciente.* esposta ne sia ) Possibilità di svenimento entro pochi minuti, senza preavviso. Rischiodimorteper%lediO 2 <11%* ) Esposizione di 6 minuti: 50% di probabilità di morte; Esposizione di 8 minuti: 100% di probabilità di morte; Svenimento immediato, coma in 40 secondi, convulsioni, blocco respirazione, morte, danni cerebrali anche se la vittima èsoccorsa.* ) * ) Da documento
44 Legge di DALTON o delle proporzioni multiple In una miscuglio di gas, volume V e temperatura T, la pressione totale è pari alla somma della pressione che ciascun gas ha nel medesimo volume alla stessa temperatura. N 2 = 0,79 V V ptot p 2 p N 2 = V + O O 2 N 2 V O 2 = 0,21 V p tot = po2 + pn 2
45 p tot V Legge di DALTON o delle proporzioni multiple = ( no 2 + nn 2 ) R T (1) applicata a tutto il volume V p O 2 V = no 2R T (2) applicata a tutto il volume V al solo O 2 p tot 0,21V = no 2R T (3) applicata a 0,21 V al solo O 2 dividendo membro a m. la (2) con la (1) e tenendo conto della (3): p p O2 tot = n no 2 +n O2 tot = p 0, 21 V R T ptot V R T tot = 0, 21 Alla pressione di 760 mm Hg la tensione parziale di ossigeno vale: p O2 = 0, = 159,60mm Hg (0, ,225 E3 = 21,258 kpa)
46 pressione parziale O 2 kpa quota m. s.l.m. pressione atmosferica kpa
47 La saturazione dell emoglobina Gli eritrociti (globuli rossi) sono cellule anucleate presenti nel sangue, responsabili, tra l'altro, del suo colore rosso. La loro funzione di trasporto dell'ossigeno dai polmoni ai tessuti è resa possibile da una proteina in essi presente, l'emoglobina, capace di legarsi stabilmente alla molecoladio 2.
48 La saturazione dell emoglobina La loro forma biconcava si deve interpretare come un adattamento biologico che ne rende massima la superficie di scambio rapportata al volume(s/v max).
49 La saturazione dell emoglobina eritrociti cellule anucleate emoglobina Hb (proteina) gruppo EME Fe ++ catene α, catene β
50 La saturazione dell emoglobina
51 La saturazione dell emoglobina quota s.l.m. pressione parziale O 2 in aria (mm Hg) saturazione di O 2 (%ledi emoglobina saturata) 0, % % % 78% limite di sicurezza per la saturazione dell emoglobina Saturazione dell emoglobina in funzione della pressione parzialedio 2 inaria.
LA STIMA DELLA CURVA RHR
 in collaborazione con CORSO DI AGGIORNAMENTO ANTINCENDIO LA STIMA DELLA CURVA RHR MANTOVA, 20 NOVEMBRE 2015 BORTOLO BALDUZZI EQUAZIONE DI STATO DEI GAS (ideali) (1) p V = n R T con: p pressione assoluta
in collaborazione con CORSO DI AGGIORNAMENTO ANTINCENDIO LA STIMA DELLA CURVA RHR MANTOVA, 20 NOVEMBRE 2015 BORTOLO BALDUZZI EQUAZIONE DI STATO DEI GAS (ideali) (1) p V = n R T con: p pressione assoluta
LA STIMA DELLA CURVA RHR
 in collaborazione con CORSO DI AGGIORNAMENTO ANTINCENDIO LA STIMA DELLA CURVA RHR MANTOVA, 11 marzo 2016 BORTOLO BALDUZZI bbalduzzi@comune.bg.it Tutto iniziò da una candela. Nel 1860, Michael Faraday tenne
in collaborazione con CORSO DI AGGIORNAMENTO ANTINCENDIO LA STIMA DELLA CURVA RHR MANTOVA, 11 marzo 2016 BORTOLO BALDUZZI bbalduzzi@comune.bg.it Tutto iniziò da una candela. Nel 1860, Michael Faraday tenne
I gas e loro proprietà Cap , 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96
 2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
Analisi qualitativa degli incendi per un approccio corretto alla FSE Ing. Pierpaolo Gentile, PhD Direttore del Corpo Nazionale dei Vigili Del Fuoco
 Ordine degli Ingegneri Provincia di Latina DIPARIMENTO DEI VIGLI DEL FUOCO DEL SOCCORSO PUBBLICO E DELLA DIFESA CIVULE Analisi qualitativa degli incendi per un approccio corretto alla FSE Ing. Pierpaolo
Ordine degli Ingegneri Provincia di Latina DIPARIMENTO DEI VIGLI DEL FUOCO DEL SOCCORSO PUBBLICO E DELLA DIFESA CIVULE Analisi qualitativa degli incendi per un approccio corretto alla FSE Ing. Pierpaolo
12/03/2013. Aria umida. Proprietà e trasformazioni
 Aria umida Proprietà e trasformazioni 1 Costituente Concentrazione volumetrica (%) Massa molecolare [kg/ kmol] Azoto (N 2 ) 78,084 28,0134 Ossigeno (O 2 ) 20,9476 31,9988 Argon (Ar) 0,934 39,948 Anidride
Aria umida Proprietà e trasformazioni 1 Costituente Concentrazione volumetrica (%) Massa molecolare [kg/ kmol] Azoto (N 2 ) 78,084 28,0134 Ossigeno (O 2 ) 20,9476 31,9988 Argon (Ar) 0,934 39,948 Anidride
Esercizi sui Gas. Insegnamento di Chimica Generale CCS CHI e MAT. A.A. 2015/2016 (I Semestre)
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio 1 Un campione
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Gas Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio 1 Un campione
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Argomento. Dipartimento di Ingegneria civile e Industriale GLI INCENDI. Docente: ing. Mauro Marchini.
 Dipartimento di Ingegneria civile e Industriale «Scienza e Tecnica della Prevenzione Incendi» Argomento GLI INCENDI Docente: ing. Mauro Marchini mgm@mauromarchini.com Gli eventi: gli incendi L incendio
Dipartimento di Ingegneria civile e Industriale «Scienza e Tecnica della Prevenzione Incendi» Argomento GLI INCENDI Docente: ing. Mauro Marchini mgm@mauromarchini.com Gli eventi: gli incendi L incendio
Dimensionamento di canna fumaria singola
 Dimensionamento di canna fumaria singola Progettazione e verifica secondo UNI EN 13384-1 EDIFICIO INDIRIZZO DESCRIZIONE COMMITTENTE Scuola Calvino Via Santa Maria a Cintoia Nuova Canna Fumaria Comune di
Dimensionamento di canna fumaria singola Progettazione e verifica secondo UNI EN 13384-1 EDIFICIO INDIRIZZO DESCRIZIONE COMMITTENTE Scuola Calvino Via Santa Maria a Cintoia Nuova Canna Fumaria Comune di
Il 'triangolo' del fuoco
 Il 'triangolo' del fuoco Schematizzazione del fenomeno della combustione In corrispondenza, dei vertici del triangolo del fuoco sono indicati tre parametri essenziali del fenomeno della combustione: -
Il 'triangolo' del fuoco Schematizzazione del fenomeno della combustione In corrispondenza, dei vertici del triangolo del fuoco sono indicati tre parametri essenziali del fenomeno della combustione: -
Esercitazione di Meccanica dei fluidi con Fondamenti di Ingegneria Chimica. Scambio di materia (II)
 Esercitazione di Meccanica dei fluidi con Fondamenti di Ingegneria himica Esercitazione 6 (FI) - 1 Gennaio 016 Scambio di materia (II) Esercizio 1 Evaporazione di acqua da una piscina Stimare la perdita
Esercitazione di Meccanica dei fluidi con Fondamenti di Ingegneria himica Esercitazione 6 (FI) - 1 Gennaio 016 Scambio di materia (II) Esercizio 1 Evaporazione di acqua da una piscina Stimare la perdita
Fisica dell Atmosfera: composizione e struttura
 : composizione e struttura giuliano.vitali@unibo.it Indice 1 Indice 1 dell Atmosfera Cos è l Atmosfera Terrestre Involucro gassoso che avvolge la Terra, sede dei fenomeni meteorologici di varia natura
: composizione e struttura giuliano.vitali@unibo.it Indice 1 Indice 1 dell Atmosfera Cos è l Atmosfera Terrestre Involucro gassoso che avvolge la Terra, sede dei fenomeni meteorologici di varia natura
Dinamica dei fluidi viscosi
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Dinamica dei fluidi viscosi 14/3/2006 Ripartizione del sangue portata totale NQ diametro iniziale D diametro d dei rami secondari
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Dinamica dei fluidi viscosi 14/3/2006 Ripartizione del sangue portata totale NQ diametro iniziale D diametro d dei rami secondari
Inquinamento ARIA. Inquinamento ARIA. Inquinamento ARIA. Inquinamento ARIA
 COMBUSTIONE: principi Processo di ossidazione di sostanze contenenti C ed H condotto per ottenere energia termica (calore) C,H + O 2 calore + gas comb. COMBUSTIBILE + COMBURENTE CALORE + RESIDUI [ARIA]
COMBUSTIONE: principi Processo di ossidazione di sostanze contenenti C ed H condotto per ottenere energia termica (calore) C,H + O 2 calore + gas comb. COMBUSTIBILE + COMBURENTE CALORE + RESIDUI [ARIA]
Nell evoluzione dell incendio si possono individuare quattro fasi caratteristiche (http://www.vvfmontelanico.it) 50 :
 2.3.1.3 Dinamica dell incendio Nell evoluzione dell incendio si possono individuare quattro fasi caratteristiche (http://www.vvfmontelanico.it) 50 : Fase di agnizione; Fase di propagazione; Incendio generalizzato
2.3.1.3 Dinamica dell incendio Nell evoluzione dell incendio si possono individuare quattro fasi caratteristiche (http://www.vvfmontelanico.it) 50 : Fase di agnizione; Fase di propagazione; Incendio generalizzato
Esercitazione di Fisica Tecnica
 Anno Accademico 2016-2017 Prof. Ing. L. Maffei 1 Anno Accademico 2016-2017 - PARTE 1 Grandezze e unità di misura Consumi energetici 2 Grandezze e unità di misura 3 Convertire le seguenti misure usando
Anno Accademico 2016-2017 Prof. Ing. L. Maffei 1 Anno Accademico 2016-2017 - PARTE 1 Grandezze e unità di misura Consumi energetici 2 Grandezze e unità di misura 3 Convertire le seguenti misure usando
Soluzioni. capitolo La massa assoluta di una molecola si calcola moltiplicando M r per u.
 Soluzioni capitolo 8 VERIFICA LE TUE CONOSCENZE LA MASSA ATOMICA ASSOLUTA E RELATIVA 1 La massa atomica assoluta è la massa di un atomo espressa in kg; il suo simbolo è m a. 2 Affermazione falsa: B Corrisponde
Soluzioni capitolo 8 VERIFICA LE TUE CONOSCENZE LA MASSA ATOMICA ASSOLUTA E RELATIVA 1 La massa atomica assoluta è la massa di un atomo espressa in kg; il suo simbolo è m a. 2 Affermazione falsa: B Corrisponde
Corso di Termofluidodinamica
 Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1
 I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
Applicazioni della Termochimica: Combustioni
 CHIMICA APPLICATA Applicazioni della Termochimica: Combustioni Combustioni Il comburente più comune è l ossigeno dell aria Aria secca:! 78% N 2 21% O 2 1% gas rari Combustioni Parametri importanti:! 1.Potere
CHIMICA APPLICATA Applicazioni della Termochimica: Combustioni Combustioni Il comburente più comune è l ossigeno dell aria Aria secca:! 78% N 2 21% O 2 1% gas rari Combustioni Parametri importanti:! 1.Potere
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Lezione 2. Leggi ponderali
 Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Comburente Solitamente l ossigeno contenuto nell aria o nelle molecole (esplosivi)
 termini Combustione Reazione chimica una sostanza combustibile con l ossigeno accompagnatada da sviluppo calore, fiamma, gas, fumo e luce. Inceno Combustione rapida e non controllata senza limitazioni
termini Combustione Reazione chimica una sostanza combustibile con l ossigeno accompagnatada da sviluppo calore, fiamma, gas, fumo e luce. Inceno Combustione rapida e non controllata senza limitazioni
Il prodotto della pressione per il volume di una determinata massa gassosa è direttamente proporzionale alla temperatura assoluta: PV = KT
 ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
5. Calcolo termodinamico e fluidodinamico di progetto di un riscaldatore d aria con fluidi in controcorrente.
 5. Calcolo termodinamico e fluidodinamico di progetto di un riscaldatore d aria con fluidi in controcorrente. Si vuole effettuare il dimensionamento di un riscaldatore d aria con fluidi in controcorrente
5. Calcolo termodinamico e fluidodinamico di progetto di un riscaldatore d aria con fluidi in controcorrente. Si vuole effettuare il dimensionamento di un riscaldatore d aria con fluidi in controcorrente
A DIPARTIMENTO DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA Primo parziale 29 Aprile 2015 COGNOME NOME
 A DIPARTIMENTO DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA Primo parziale 29 Aprile 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
A DIPARTIMENTO DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA Primo parziale 29 Aprile 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
ADDESTRAMENTO APVR. Maschera pieno facciale EN 136
 ADDESTRAMENTO APVR Maschera pieno facciale EN 136 MASCHERE ANTIGAS L'uso di maschere antigas a filtro è necessario per evitare l'inalazione di vapori, polveri e gas irritanti o nocivi durante gli incendi.
ADDESTRAMENTO APVR Maschera pieno facciale EN 136 MASCHERE ANTIGAS L'uso di maschere antigas a filtro è necessario per evitare l'inalazione di vapori, polveri e gas irritanti o nocivi durante gli incendi.
Problemi di Fisica per l ammissione alla Scuola Galileiana Problema 1
 Problemi di Fisica per l ammissione alla Scuola Galileiana 2015-2016 Problema 1 Un secchio cilindrico di raggio R contiene un fluido di densità uniforme ρ, entrambi ruotanti intorno al loro comune asse
Problemi di Fisica per l ammissione alla Scuola Galileiana 2015-2016 Problema 1 Un secchio cilindrico di raggio R contiene un fluido di densità uniforme ρ, entrambi ruotanti intorno al loro comune asse
U.M.A. e le masse ATOMICHE
 U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
BARRIERE ARCHITETTONICHE E SICUREZZA ANTINCENDIO NEGLI EDIFICI
 Bergamo, 4 maggio 2007 PROGETTARE L ACCESSIBILITA 5 INCONTRI DI APPROFONDIMENTO TECNICO BARRIERE ARCHITETTONICHE E SICUREZZA ANTINCENDIO NEGLI EDIFICI by Bortolo Balduzzi bortolobalduzzi@alice.it LA DIRETTIVA
Bergamo, 4 maggio 2007 PROGETTARE L ACCESSIBILITA 5 INCONTRI DI APPROFONDIMENTO TECNICO BARRIERE ARCHITETTONICHE E SICUREZZA ANTINCENDIO NEGLI EDIFICI by Bortolo Balduzzi bortolobalduzzi@alice.it LA DIRETTIVA
Relazione di Sistemi Energetici: Calcolo semplificato del rendimento di una caldaia con e senza "air-heater" rigenerativo.
 Relazione di Sistemi Energetici: Calcolo semplificato del rendimento di una caldaia con e senza "air-heater" rigenerativo. Palagiano, Riccardo matricola 792668 Ostojic, Roberto matricola 811142 Perucchini,
Relazione di Sistemi Energetici: Calcolo semplificato del rendimento di una caldaia con e senza "air-heater" rigenerativo. Palagiano, Riccardo matricola 792668 Ostojic, Roberto matricola 811142 Perucchini,
CICLONE SEPARATORE Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m)
 ALLEGATO n. CICLONE SEPARATORE Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m) Portata massima di progetto (m 3 s -1) Sezione del camino (m2) Percentuale di materiale
ALLEGATO n. CICLONE SEPARATORE Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m) Portata massima di progetto (m 3 s -1) Sezione del camino (m2) Percentuale di materiale
MISCELE DI GAS PERFETTI
 Lezione IX 2/04/2014 ora 09.30 12.30 Miscele di gas perfetti Originale di Chiari Giulio, Mannelli Andrea MISCELE DI GAS PERFETTI In questo corso prenderemo in considerazione due miscele di gas perfetti.
Lezione IX 2/04/2014 ora 09.30 12.30 Miscele di gas perfetti Originale di Chiari Giulio, Mannelli Andrea MISCELE DI GAS PERFETTI In questo corso prenderemo in considerazione due miscele di gas perfetti.
PSICROMETRIA PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI
 PSICROMETRIA PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI Un modello di comportamento interessante per la termodinamica è quello cosiddetto di gas perfetto. Il gas perfetto è naturalmente un astrazione, tuttavia
PSICROMETRIA PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI Un modello di comportamento interessante per la termodinamica è quello cosiddetto di gas perfetto. Il gas perfetto è naturalmente un astrazione, tuttavia
LA COMBUSTIONE. La combustione è una reazione di ossidazione in cui il combustibile rappresenta la sostanza ossidabile e il. ossidante.
 LA COMBUSTIONE La combustione è una reazione chimica i molto rapida che si manifesta con elevato sviluppo di calore, emissione di luce, fumo, vapori e gas di combustione. Essa avviene tra una sostanza
LA COMBUSTIONE La combustione è una reazione chimica i molto rapida che si manifesta con elevato sviluppo di calore, emissione di luce, fumo, vapori e gas di combustione. Essa avviene tra una sostanza
1 Determinazione del carico di incendio specifico di progetto
 1. Definizioni 1/7 ALLEGATO Ai fini della presente norma si fa riferimento ad un incendio convenzionale di progetto definito attraverso una curva di incendio che rappresenta l andamento, in funzione del
1. Definizioni 1/7 ALLEGATO Ai fini della presente norma si fa riferimento ad un incendio convenzionale di progetto definito attraverso una curva di incendio che rappresenta l andamento, in funzione del
STATICA DEI FLUIDI G. ROBERTI
 STATICA DEI FLUIDI G. ROBERTI FLUIDI G. Roberti Definizione:sostanze che assumono la forma dei recipienti che le contengono oppure Definizione: sostanze che si deformano senza che si compia lavoro ΔV /
STATICA DEI FLUIDI G. ROBERTI FLUIDI G. Roberti Definizione:sostanze che assumono la forma dei recipienti che le contengono oppure Definizione: sostanze che si deformano senza che si compia lavoro ΔV /
Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore
 Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore Legge di Stevino La pressione in un liquido a densità costante cresce linearmente con la profondità Il principio di
Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore Legge di Stevino La pressione in un liquido a densità costante cresce linearmente con la profondità Il principio di
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C)
 COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
Formule empiriche e formule molecolari
 COMPLEMENTI A Formule empiriche e formule molecolari Nella prima metà del diciannovesimo secolo J.J. Berzelius, J.B. A. Dumas, Justus Liebig e Stanislao Cannizzaro misero a punto i metodi per la determinazione
COMPLEMENTI A Formule empiriche e formule molecolari Nella prima metà del diciannovesimo secolo J.J. Berzelius, J.B. A. Dumas, Justus Liebig e Stanislao Cannizzaro misero a punto i metodi per la determinazione
IMPIANTI DELL INDUSTRIA DI PROCESSO ESERCITAZIONE N. 2. Bilanci di energia
 1 IMPIANTI DELL INDUSTRIA DI PROCESSO ESERCITAZIONE N. 2 Bilanci di energia 1. Calcolare la quantità di calore ceduta da 1 m 3 di aria a TPS nel raffreddamento da 500 C a 0 C, alla pressione costante di
1 IMPIANTI DELL INDUSTRIA DI PROCESSO ESERCITAZIONE N. 2 Bilanci di energia 1. Calcolare la quantità di calore ceduta da 1 m 3 di aria a TPS nel raffreddamento da 500 C a 0 C, alla pressione costante di
è completamente immerso in acqua. La sua
 In un tubo scorre in regime stazionario un liquido ideale con densità 1.00 10 3 kg/m 3 ; in un punto A il tubo ha raggio R A = 2.00 cm, la velocità di scorrimento è v A = 5.00 m/se la pressione è P A =
In un tubo scorre in regime stazionario un liquido ideale con densità 1.00 10 3 kg/m 3 ; in un punto A il tubo ha raggio R A = 2.00 cm, la velocità di scorrimento è v A = 5.00 m/se la pressione è P A =
Università degli studi di Cassino e del Lazio Meridionale Facoltà di Ingegneria. Esempio di calcolo sulle trasmittanze termiche
 Università degli studi di Cassino e del Lazio Meridionale Facoltà di Ingegneria Esempio di calcolo sulle trasmittanze termiche } Trasmittanza termica di un componente opaco; } Trasmittanza termica di un
Università degli studi di Cassino e del Lazio Meridionale Facoltà di Ingegneria Esempio di calcolo sulle trasmittanze termiche } Trasmittanza termica di un componente opaco; } Trasmittanza termica di un
Lecture 18. Text: Motori Aeronautici Mar. 26, Mauro Valorani Università La Sapienza. Analisi dimensionale delle turbomacchine
 Lecture 18 Analisi Text: Motori Aeronautici Mar. 26, 2015 Analisi Mauro Valorani Università La Sapienza 18.331 Agenda Analisi 1 Numero di giri e 18.332 Analisi L analisi e il confronto tra le turbomacchine
Lecture 18 Analisi Text: Motori Aeronautici Mar. 26, 2015 Analisi Mauro Valorani Università La Sapienza 18.331 Agenda Analisi 1 Numero di giri e 18.332 Analisi L analisi e il confronto tra le turbomacchine
CORSO DI CHIMICA. Esercitazione del 7 Giugno 2016
 CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI)
 1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
PER ESERCITARSI Parte 2. Esercizi su Corpo rigido, variabili angolari, momenti, fluidi, termodinamica
 PER ESERCITARSI Parte 2 Esercizi su Corpo rigido, variabili angolari, momenti, fluidi, termodinamica ESERCIZIO n.1 Due forze uguali ed opposte sono applicate ad un oggetto lungo rette di azione tra loro
PER ESERCITARSI Parte 2 Esercizi su Corpo rigido, variabili angolari, momenti, fluidi, termodinamica ESERCIZIO n.1 Due forze uguali ed opposte sono applicate ad un oggetto lungo rette di azione tra loro
POLITECNICO DI MILANO Scuola di Ingegneria Industriale Fondamenti di Fisica Sperimentale, a.a I Appello, 10 luglio 2013
 POLITECNICO DI MILNO Scuola di Ingegneria Industriale Fondamenti di Fisica Sperimentale, a.a. 0-3 I ppello, 0 luglio 03 Giustificare le risposte e scrivere in modo chiaro e leggibile. Sostituire i valori
POLITECNICO DI MILNO Scuola di Ingegneria Industriale Fondamenti di Fisica Sperimentale, a.a. 0-3 I ppello, 0 luglio 03 Giustificare le risposte e scrivere in modo chiaro e leggibile. Sostituire i valori
QUALITA DELL ARIA E INQUINAMENTO ATMOSFERICO
 QUALITA DELL ARIA E INQUINAMENTO ATMOSFERICO Gruppo di Ricerca di Chimica dell Atmosfera Dipartimento di Scienze dell Ambiente e del Territorio e Scienze della Terra (DISAT), Università degli Studi di
QUALITA DELL ARIA E INQUINAMENTO ATMOSFERICO Gruppo di Ricerca di Chimica dell Atmosfera Dipartimento di Scienze dell Ambiente e del Territorio e Scienze della Terra (DISAT), Università degli Studi di
Foto funzioni apparato respiratorio
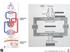 RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
CdL Professioni Sanitarie A.A. 2012/2013. Unità 9: Gas e processi di diffusione
 L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
Caratterizzazione delle onde: lunghezza d onda, velocità, frequenza, periodo
 Esercizi di acustica Caratterizzazione delle onde: lunghezza d onda, velocità, frequenza, periodo Esercizio 1 La velocità del suono nell aria dipende dalla sua temperatura. Calcolare la velocità di propagazione
Esercizi di acustica Caratterizzazione delle onde: lunghezza d onda, velocità, frequenza, periodo Esercizio 1 La velocità del suono nell aria dipende dalla sua temperatura. Calcolare la velocità di propagazione
Fondamenti di Acustica
 Fondamenti di Acustica Fisica Tecnica Corso di Laurea in Ingegneria dei trasporti Definizione di suono Per suono in un punto si intende una rapida variazione di pressione, intorno alla pressione atmosferica,
Fondamenti di Acustica Fisica Tecnica Corso di Laurea in Ingegneria dei trasporti Definizione di suono Per suono in un punto si intende una rapida variazione di pressione, intorno alla pressione atmosferica,
Innalzamento capillare = E+01 cm. Pressione = E+06 Pa
 --------------- 1 -------------- Innalzamento capillare = 0.1565E+01 cm Pressione = 0.8588E+06 Pa Valor medio della tensione superficiale = 0.2001E-01 N/m --------------- 2 -------------- Calore specifico
--------------- 1 -------------- Innalzamento capillare = 0.1565E+01 cm Pressione = 0.8588E+06 Pa Valor medio della tensione superficiale = 0.2001E-01 N/m --------------- 2 -------------- Calore specifico
Gas X Y Gas X Y 7,7 8,9 8,0 9,8 8,4 11,0 10,5 10,6 8,5 8,9 9,2 8,9 9,5 8,0 11,0 9,2 9,2 9,0 8,9 10,9 9,1 8,6 8,5 9,2 8,5 8,9 9,5 7,3
 Viscosità dei Gas A) Alcuni valori di Viscosità di Gas Viscosità di alcuni Gas (µ G = centipoise) La viscosità può essere ricavata con il nomogramma di Figura 1 Acetico Acido Acetone Acqua Acetilene Ammoniaca
Viscosità dei Gas A) Alcuni valori di Viscosità di Gas Viscosità di alcuni Gas (µ G = centipoise) La viscosità può essere ricavata con il nomogramma di Figura 1 Acetico Acido Acetone Acqua Acetilene Ammoniaca
Quantita` di calore = E+03 cal. `` `` `` = E+10 erg. Calore prodotto = E+06 joule = 0.
 --------------- 1 -------------- Quantita` di calore = 0.2311E+03 cal. `` `` `` = 0.9672E+10 erg Calore prodotto = 0.1187E+06 joule = 0.2840E+05 cal Ampiezza del moto = 0.9511E-02 m --------------- 2 --------------
--------------- 1 -------------- Quantita` di calore = 0.2311E+03 cal. `` `` `` = 0.9672E+10 erg Calore prodotto = 0.1187E+06 joule = 0.2840E+05 cal Ampiezza del moto = 0.9511E-02 m --------------- 2 --------------
La misura della portata massica
 Products Solutions Services La misura della portata massica Facoltà di Ingegneria, Università degli Studi di Bologna DIEM - Dipartimento di Ingegneria delle Costruzioni Meccaniche, Nucleari, Aeronautiche
Products Solutions Services La misura della portata massica Facoltà di Ingegneria, Università degli Studi di Bologna DIEM - Dipartimento di Ingegneria delle Costruzioni Meccaniche, Nucleari, Aeronautiche
Flamma fumo est proxima. Paolo Cardillo. pcardillo@alice.it. Dove c è fumo c è fiamma
 Flamma fumo est proxima Dove c è fumo c è fiamma Paolo Cardillo pcardillo@alice.it Incendio? Un incendio è una reazione chimica che coinvolge la rapida ossidazione, cioè la combustione, di un combustibile
Flamma fumo est proxima Dove c è fumo c è fiamma Paolo Cardillo pcardillo@alice.it Incendio? Un incendio è una reazione chimica che coinvolge la rapida ossidazione, cioè la combustione, di un combustibile
EMISSIONI IN ATMOSFERA
 EMISSIONI IN ATMOSFERA RAPPORTO DI PROVA Rif. AMB-2015/22 Insediamento: SIME ENERGIA SRL - VIALE DELLO SPORT, 103 - ZOLA PREDOSA - BO Committente: SIME ENERGIA SRL EMISSIONE - sigla: E2 - origine: Caldaia
EMISSIONI IN ATMOSFERA RAPPORTO DI PROVA Rif. AMB-2015/22 Insediamento: SIME ENERGIA SRL - VIALE DELLO SPORT, 103 - ZOLA PREDOSA - BO Committente: SIME ENERGIA SRL EMISSIONE - sigla: E2 - origine: Caldaia
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
L importanza della valutazione del rischio nella progettazione di Impianti Antincendio. C. Claudi COLLEGIO DEGLI INGEGNERI E ARCHITETTI DI MILANO
 L importanza della valutazione del rischio nella progettazione di Impianti Antincendio C. Claudi 30 Giugno 2008 Rischio Frequenza Numero di Eventi Attesi / Numero totale di eventi Conseguenze Effetti dovuti
L importanza della valutazione del rischio nella progettazione di Impianti Antincendio C. Claudi 30 Giugno 2008 Rischio Frequenza Numero di Eventi Attesi / Numero totale di eventi Conseguenze Effetti dovuti
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Bilanci macroscopici. Esercizi dal libro Fenomeni di Trsporto, Bird, Stewart, Lightfoot
 Bilanci macroscopici Esercizi dal libro Fenomeni di Trsporto, Bird, Stewart, Lightfoot 7A 7B 7C 7D 7E 7F Esercizio 1 Due recipienti, le cui basi si trovano su uno stesso piano, sono messi in comunicazione
Bilanci macroscopici Esercizi dal libro Fenomeni di Trsporto, Bird, Stewart, Lightfoot 7A 7B 7C 7D 7E 7F Esercizio 1 Due recipienti, le cui basi si trovano su uno stesso piano, sono messi in comunicazione
FASCICOLO degli ALLEGATI. fascicolo degli allegati. Sala polifunzionale Il Portico Prog. VVF.149v1. Committente:
 STUDIO TERMOTECNICO TASCHETTI PROGETTISTI ASSOCIATI Sala polifunzionale Il Portico Prog. VVF.149v1 Committente: Ubicazione intervento: Progettista: Parrocchia SS. Martiri Gervaso e Protaso P. zza Nazionale,
STUDIO TERMOTECNICO TASCHETTI PROGETTISTI ASSOCIATI Sala polifunzionale Il Portico Prog. VVF.149v1 Committente: Ubicazione intervento: Progettista: Parrocchia SS. Martiri Gervaso e Protaso P. zza Nazionale,
DINAMICA DEGLI INQUINANTI A.A PROPRIETA DELL ATMOSFERA PROF. RENATO BACIOCCHI
 DINAMICA DEGLI INQUINANTI A.A. 2012 2013 PROPRIETA DELL ATMOSFERA PROF. RENATO BACIOCCHI ARGOMENTI TRATTATI: 1. ATMOSFERA Estensione e struttura dell atmosfera Composizione dell aria Principali parametri
DINAMICA DEGLI INQUINANTI A.A. 2012 2013 PROPRIETA DELL ATMOSFERA PROF. RENATO BACIOCCHI ARGOMENTI TRATTATI: 1. ATMOSFERA Estensione e struttura dell atmosfera Composizione dell aria Principali parametri
La legge dei gas perfetti
 La legge dei gas perfetti In condizioni normali l aria ambiente secca contiene approssimativamente 78,08% di azoto (N2), 20,94% di ossigeno (O2), 0,93% di argon (Ar), 0,04% di biossido di carbonio (CO2)
La legge dei gas perfetti In condizioni normali l aria ambiente secca contiene approssimativamente 78,08% di azoto (N2), 20,94% di ossigeno (O2), 0,93% di argon (Ar), 0,04% di biossido di carbonio (CO2)
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare
 Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Combustione. Energia chimica. Energia termica Calore. Combustibili fossili
 Combustione La combustione è un processo di ossidazione rapido con produzione di luce e calore, con trasformazione di energia chimica in energia termica Energia chimica Combustibili fossili Energia termica
Combustione La combustione è un processo di ossidazione rapido con produzione di luce e calore, con trasformazione di energia chimica in energia termica Energia chimica Combustibili fossili Energia termica
APPLICAZIONE DEL MODELLATORE DI INCENDI CFAST CON UNA CURVA TEORICA DEL TASSO DI RILASCIO TERMICO
 APPLICAZIONE DEL MODELLATORE DI INCENDI CFAST CON UNA CURVA TEORICA DEL TASSO DI RILASCIO TERMICO SOMMARIO Prof. Piero Masini (1), Prof. Ubaldo Ayr (1), Ing. Maria Romano (1), Ing. Fedele Decandia (2)
APPLICAZIONE DEL MODELLATORE DI INCENDI CFAST CON UNA CURVA TEORICA DEL TASSO DI RILASCIO TERMICO SOMMARIO Prof. Piero Masini (1), Prof. Ubaldo Ayr (1), Ing. Maria Romano (1), Ing. Fedele Decandia (2)
Mezzi di protezione delle vie respiratorie: Autoprotettori
 Mezzi di protezione delle vie respiratorie: Autoprotettori 1. cenni sulla respirazione umana aria che noi respiriamo è una miscela gassosa di ossigeno (20,9%) e di azoto (78,1% in volume), con quantità
Mezzi di protezione delle vie respiratorie: Autoprotettori 1. cenni sulla respirazione umana aria che noi respiriamo è una miscela gassosa di ossigeno (20,9%) e di azoto (78,1% in volume), con quantità
Analisi inquinanti. Università di Roma La Sapienza Sistemi Energetici II
 Analisi inquinanti Combustione diretta Reazione di ossidazione esotermica tra il combustibile e il comburente (ossigeno presente nell aria) In una reazione esotermica l energia chimica contenuta nel combustibile
Analisi inquinanti Combustione diretta Reazione di ossidazione esotermica tra il combustibile e il comburente (ossigeno presente nell aria) In una reazione esotermica l energia chimica contenuta nel combustibile
La combustione ed i combustibili
 La combustione ed i combustibili Concetti di base Potere calorifico Aria teorica di combustione Fumi: volume e composizione Temperatura teorica di combustione Perdita al camino Combustibili Gassosi Solidi
La combustione ed i combustibili Concetti di base Potere calorifico Aria teorica di combustione Fumi: volume e composizione Temperatura teorica di combustione Perdita al camino Combustibili Gassosi Solidi
Reazione al fuoco dei materiali. Le prove
 Reazione al fuoco dei materiali Le prove prove di reazione al fuoco - Italia UNI ISO 1182 Prova di non combustibilità UNI 8456 Materiali combustibili suscettibili di essere investiti dalla fiamma su entrambe
Reazione al fuoco dei materiali Le prove prove di reazione al fuoco - Italia UNI ISO 1182 Prova di non combustibilità UNI 8456 Materiali combustibili suscettibili di essere investiti dalla fiamma su entrambe
PROGETTO ANTINCENDI DETERMINAZIONE DI PRESTAZIONE E CLASSIFICAZIONE DI RESISTENZA AL FUOCO DELLE STRUTTURE
 Esempio di Calcolo Carico Incendio con il software AntiFuocus di ACCA software PROGETTO ANTINCENDI AL COMANDO PROVINCIALE dei VV.F. di MILANO - Lombardia DETERMINAZIONE DI PRESTAZIONE E CLASSIFICAZIONE
Esempio di Calcolo Carico Incendio con il software AntiFuocus di ACCA software PROGETTO ANTINCENDI AL COMANDO PROVINCIALE dei VV.F. di MILANO - Lombardia DETERMINAZIONE DI PRESTAZIONE E CLASSIFICAZIONE
CATALOGO 2016/Rev.1 BOMBOLE MONOUSO
 CATALOGO 2016/Rev.1 BOMBOLE MONOUSO Miscele di gas e gas puri per taratura, rilevazione gas, uso di laboratorio. Dispositivi di prelievo. Risam Gas srl Via Padova, 221-20127 Milano Uff.Comm./Operativo:
CATALOGO 2016/Rev.1 BOMBOLE MONOUSO Miscele di gas e gas puri per taratura, rilevazione gas, uso di laboratorio. Dispositivi di prelievo. Risam Gas srl Via Padova, 221-20127 Milano Uff.Comm./Operativo:
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici
 La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
applicati ad un caso reale
 9:40 Pagina 58 senti rilevatori di fumo, il tempo di rivelazione è molto variabile. Si passa dall attivazione praticamente istantanea del rilevatore 1; per arrivare ai 70 s dell ultimo rilevatore, il numero
9:40 Pagina 58 senti rilevatori di fumo, il tempo di rivelazione è molto variabile. Si passa dall attivazione praticamente istantanea del rilevatore 1; per arrivare ai 70 s dell ultimo rilevatore, il numero
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della
 Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
Ponti termici Edifici esistenti maggiorazione lordo
 Ponti termici Edifici esistenti Il ponte termico si calcola mediante maggiorazione della trasmittanza della parete sulla quale sono presenti. L area si calcola al lordo, comprendendo tamponamento e ponte
Ponti termici Edifici esistenti Il ponte termico si calcola mediante maggiorazione della trasmittanza della parete sulla quale sono presenti. L area si calcola al lordo, comprendendo tamponamento e ponte
Camini Collettivi per App. stagni tipo C - UNI EN EX_A1
 Camini Collettivi per App. stagni tipo C - UNI EN 13384-2 - EX_A1 DATI Si consideri una canna fumaria COLLETTIVA SEMPLICE CIRCOLARE (senza condotto aria) in acciaio al servizio di 3 Generatori di Calore.
Camini Collettivi per App. stagni tipo C - UNI EN 13384-2 - EX_A1 DATI Si consideri una canna fumaria COLLETTIVA SEMPLICE CIRCOLARE (senza condotto aria) in acciaio al servizio di 3 Generatori di Calore.
Motori Alternativi a Combustione Interna Generalità
 Motori Alternativi a Combustione Interna Generalità Storicamente nascono dopo le macchine alternative a vapore (seconda metà del XIX secolo) ma hanno avuto larghissimo sviluppo e conseguente diffusione
Motori Alternativi a Combustione Interna Generalità Storicamente nascono dopo le macchine alternative a vapore (seconda metà del XIX secolo) ma hanno avuto larghissimo sviluppo e conseguente diffusione
CAMPIONAMENTI ALLE EMISSIONI
 CAMPIONAMENTI ALLE EMISSIONI PORTATA Metodica di riferimento: UNI 10169 del 31/12/2001 Strumentazione: Punti di misurazione: Area della sezione di Tubo di Pitot di cui si conosca la costante Micromanometro
CAMPIONAMENTI ALLE EMISSIONI PORTATA Metodica di riferimento: UNI 10169 del 31/12/2001 Strumentazione: Punti di misurazione: Area della sezione di Tubo di Pitot di cui si conosca la costante Micromanometro
+ + Corso di Chimica e Propedeutica Biochimica Le equazioni chimiche e la stechiometria. CH 4 (g)+ 2 O 2 (g) CO 2 (g) + 2 H 2 O(l) 1
 Corso di Chimica e Propedeutica Biochimica Le equazioni chimiche e la stechiometria + + 1 molecola di metano (CH 4 ) 2 molecole di ossigeno (O 2 ) 1 molecola di biossido di carbonio (CO 2 ) 2 molecole
Corso di Chimica e Propedeutica Biochimica Le equazioni chimiche e la stechiometria + + 1 molecola di metano (CH 4 ) 2 molecole di ossigeno (O 2 ) 1 molecola di biossido di carbonio (CO 2 ) 2 molecole
UNITA DI VENTILAZIONE MECCANICA CONTROLLATA CON RECUPERO DI CALORE PER EDIFICI RESIDENZIALI (η= min. 75% max. >90%)
 (η= min. 75% max. >9%) REVERSUS file temporaneo: Dic. 22 (η= min. 75% max >9%) REVERSUS Unità di Ventilazione Meccanica Controllata con recupero di calore ad alta efficienza (>9%) Installazione verticale
(η= min. 75% max. >9%) REVERSUS file temporaneo: Dic. 22 (η= min. 75% max >9%) REVERSUS Unità di Ventilazione Meccanica Controllata con recupero di calore ad alta efficienza (>9%) Installazione verticale
Scenari di incendio di progetto. VIGILI DEL FUOCO Direzione Piemonte
 By F.D. By Scenari di incendio di progetto Sicurezza antincendio REGOLA TECNICA ORIZZONTALE RTO PRIMA FASE: Analisi preliminare Scenario incendio di progetto 1 Inizio incendio Zona lavorazione Deposito
By F.D. By Scenari di incendio di progetto Sicurezza antincendio REGOLA TECNICA ORIZZONTALE RTO PRIMA FASE: Analisi preliminare Scenario incendio di progetto 1 Inizio incendio Zona lavorazione Deposito
DIAGRAMMA DI MOLLIER TABELLE DEL VAPOR D'ACQUA
 DIAGRAMMA DI MOLLIER TABELLE DEL VAPOR D'ACQUA 1 DIAGRAMMA DI MOLLIER DEL VAPORE D'ACQUA RAPPRESENTA I VALORI DELLE VARIABILI TERMODINAMICHE DEL VAPOR D'ACQUA IN UN PIANO h (ASSE Y) / s (ASSE X) h = ENTALPIA
DIAGRAMMA DI MOLLIER TABELLE DEL VAPOR D'ACQUA 1 DIAGRAMMA DI MOLLIER DEL VAPORE D'ACQUA RAPPRESENTA I VALORI DELLE VARIABILI TERMODINAMICHE DEL VAPOR D'ACQUA IN UN PIANO h (ASSE Y) / s (ASSE X) h = ENTALPIA
WORKSHOP PVC CABLES 2014
 Laboratorio Prevenzioni Incendi SpA WORKSHOP PVC CABLES 2014 BOLOGNA 20/11/2014 www.laboratoriolapi.it lapi@laboratoriolapi.it LAPI SpA è un Organismo Notificato e Laboratorio di prove che opera dal 1983
Laboratorio Prevenzioni Incendi SpA WORKSHOP PVC CABLES 2014 BOLOGNA 20/11/2014 www.laboratoriolapi.it lapi@laboratoriolapi.it LAPI SpA è un Organismo Notificato e Laboratorio di prove che opera dal 1983
SOLUZIONI COMPITO A DI CHIMICA DEL
 SOLUZIONI COMPITO A DI CHIMICA DEL 26-11-10 1A) Il permanganato di potassio reagisce con il perossido di idrogeno in presenza di acido solforico dando luogo alla formazione di ossigeno, diossido di manganese
SOLUZIONI COMPITO A DI CHIMICA DEL 26-11-10 1A) Il permanganato di potassio reagisce con il perossido di idrogeno in presenza di acido solforico dando luogo alla formazione di ossigeno, diossido di manganese
Soluzioni degli esercizi
 Soluzioni degli esercizi Compito 1. Formula risolutiva: Q = (Q 1 +Q 2 +Q 3 +Q 4 +Q 5 )/5 Valor medio della quantità di calore = 0.556E+02 J Formula risolutiva: C = Q/ΔT con ΔT = variazione temperatura
Soluzioni degli esercizi Compito 1. Formula risolutiva: Q = (Q 1 +Q 2 +Q 3 +Q 4 +Q 5 )/5 Valor medio della quantità di calore = 0.556E+02 J Formula risolutiva: C = Q/ΔT con ΔT = variazione temperatura
Metabolismo: trasformazione dell energia chimica in energia termica e lavoro
 Metabolismo: trasformazione dell energia chimica in energia termica e lavoro Uomo: stufetta da 100W Al giorno: Uomo 2500 kcal; Donna 1800 kcal 1 Metabolismo - (lavoro+evaporazione+respirazione+radiazione+convezione)
Metabolismo: trasformazione dell energia chimica in energia termica e lavoro Uomo: stufetta da 100W Al giorno: Uomo 2500 kcal; Donna 1800 kcal 1 Metabolismo - (lavoro+evaporazione+respirazione+radiazione+convezione)
Fondamenti di combustione [1-32]
![Fondamenti di combustione [1-32] Fondamenti di combustione [1-32]](/thumbs/70/63741257.jpg) Politecnico di Milano Facoltà di Ingegneria Industriale Corso di Laurea in Ingegneria Aerospaziale Insegnamento di Propulsione Aerospaziale Anno accademico 2011/12 Capitolo 3 sezione d Fondamenti di combustione
Politecnico di Milano Facoltà di Ingegneria Industriale Corso di Laurea in Ingegneria Aerospaziale Insegnamento di Propulsione Aerospaziale Anno accademico 2011/12 Capitolo 3 sezione d Fondamenti di combustione
LEGGI DI FISICA PER LA SUBACQUEA PRINCIPIO DI ARCHIMEDE
 LEGGI DI FISICA PER LA SUBACQUEA PRINCIPIO DI ARCHIMEDE Un corpo immerso in un fluido riceve una spinta dal basso verso l'alto pari al peso del volume del fluido che sposta. Il GAV è una applicazione pratica
LEGGI DI FISICA PER LA SUBACQUEA PRINCIPIO DI ARCHIMEDE Un corpo immerso in un fluido riceve una spinta dal basso verso l'alto pari al peso del volume del fluido che sposta. Il GAV è una applicazione pratica
Esercizi di. Stechiometria dei composti. mercoledì 9 dicembre 2015
 Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
SGE Bollitore a condensazione a gas / solare
 Bollitore a condensazione a gas / solare SGE - 40/60 Controllo solare Scalda acqua a gas/solare, ad alta efficienza, a condensazione e completamente ermetico, con scambiatore di calore solare integrato
Bollitore a condensazione a gas / solare SGE - 40/60 Controllo solare Scalda acqua a gas/solare, ad alta efficienza, a condensazione e completamente ermetico, con scambiatore di calore solare integrato
Lezione di Combustione
 Lezione di Combustione Introduzione Da un punto di vista chimico-fisico la combustione è un processo reattivo fortemente esotermico Generalmente le temperature in gioco sono particolarmente elevate e dipendono
Lezione di Combustione Introduzione Da un punto di vista chimico-fisico la combustione è un processo reattivo fortemente esotermico Generalmente le temperature in gioco sono particolarmente elevate e dipendono
temperatura ambientale massa totale d aria contenuta nella stanza temperatura raggiunta nella stanza dalla massa d aria pressione atmosferica
 Esercizio n.21 di pagina 26. L 1 = 6 m L 2 = 8 m L 3 = 10 m t 0F = 20 F M = 28.8 kg/kmol = 28.8 g/mol m =? t 1F = 75 F p a = 1.013 10 5 Pa temperatura ambientale massa molecolare media dell aria massa
Esercizio n.21 di pagina 26. L 1 = 6 m L 2 = 8 m L 3 = 10 m t 0F = 20 F M = 28.8 kg/kmol = 28.8 g/mol m =? t 1F = 75 F p a = 1.013 10 5 Pa temperatura ambientale massa molecolare media dell aria massa
Sonda di misura Modello A2G-FM
 Speciale Modello A2G-FM Scheda tecnica WIKA SP 69.10 Applicazioni Misura della portata aria in tubi di ventilazione circolari Misura della portata aria in condotti di ventilazione rettangolari Caratteristiche
Speciale Modello A2G-FM Scheda tecnica WIKA SP 69.10 Applicazioni Misura della portata aria in tubi di ventilazione circolari Misura della portata aria in condotti di ventilazione rettangolari Caratteristiche
Sistemi Gassosi. GAS = specie che occupa tutto lo spazio disponibile. VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 )
 Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO
 2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO E' noto che la combustione di un combustibile fossile produce anidride carbonica (CO 2 ), rinvenibile dunque nei prodotti della combustione. Nella
2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO E' noto che la combustione di un combustibile fossile produce anidride carbonica (CO 2 ), rinvenibile dunque nei prodotti della combustione. Nella
