Per le lezioni del prof. P.P. Battaglini Schemi di. v 3.2. ph = pka + log10 [!$]
|
|
|
- Pasquale Rubino
- 5 anni fa
- Visualizzazioni
Transcript
1 Per le lezioni del prof. P.P. Battaglini Schemi di v 3.2 ph = pka + log10! " [!$]
2 Dichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei. Queste immagini vengono utilizzate per l elevato contenuto didattico e per promuovere la conoscenza delle opere da cui sono tratte, la cui consultazione è consigliata e certamente utile allo studio degli argomenti qui trattati Il materiale presentato non è sufficiente a superare adeguatamente l esame di Fisiologia. E necessario, quindi, completare lo studio su testi reperibili in commercio, fra cui: Guyton e Hall: Fisiologia Medica. EdiSES Autori vari (a cura di F. Conti); Fisiologia medica. EdiErmes W. F. Ganong; Fisiologia Medica. Piccin Silverthorn; Fisiologia umana: un approccio integrato. Pearson Nessun diritto di copyright è invocato per il materiale originale presente in questo file. Chi desideri utilizzarlo è solo invitato a citarne la fonte
3 Principali funzioni renali Eliminazione di scorie (urea, creatinina, acido urico, ammoniaca) Regolazione della PA (diuresi, RAAS) Omeostasi minerale (Vit D) Bilancio idrico ed elettrolitico (H2O, Na+, K+, Mg++, PO4- - ) Regolazione dell emopoiesi (EPO) Equilibrio acido/base
4 Equilibrio acido base E l insieme dei processi fisiologici utili a mantenere il ph a valori compatibili con lo svolgimento delle principali funzioni metaboliche ph arterioso 7,35 7,45 Il mantenimento di un ph entro limiti fisiologici è fondamentale perché gli ioni H+ sono dei composti particolarmente reattivi, in particolare con le proteine. [H + ] Al variare della [H + ] le proteine acquistano o perdono protoni con conseguenti Alterazioni strutturali Alterazioni funzionali!
5 Acido, base, ph Acido Sostanza in grado di cedere ioni H + Base Sostanza in grado di accettare ioni H + Per semplicità matematica, la [H + ] viene espressa in scala logaritmica ph = -log [H + ]
6 2 tipi di acidità 1. Acidità volatile (CO 2 ) CO 2 + H 2 O H 2 CO 3 H + + HCO 3 - Deriva dal metabolismo cellulare dei carboidrati e dei lipidi. Viene eliminata dai polmoni. In condizioni fisiologiche non costituisce guadagno di H + perché, nell unità di tempo, la quota di CO 2 prodotta è uguale alla quantità eliminata con la respirazione. 2. Acidità fissa Deriva dal metabolismo proteico. Viene eliminata dai reni. H 2 SO 4 (cisteina, metionina) HCl (lisina, arginina, istidina) H 2 PO 4- (assunto con la dieta) Acidi organici (lattato, chetoacidi, tossici, farmaci) ph
7 Sistemi di regolazione del ph 1. Risposta immediata I sistemi tampone si combinano istantaneamente con gli acidi o le basi in eccesso per impedire variazioni consistenti di ph 2. Risposta rapida Il centro respiratorio regola in pochi minuti la ventilazione e quindi l eliminazione di CO 2 3. Risposta lenta Il rene elimina dal corpo gli acidi e le basi in eccesso (giorni)
8 Tamponi dell organismo Un sistema tampone è una soluzione che, grazie alla capacità di legare o rilasciare ioni H +, ha l abilità di OPPORSI alle variazioni di ph quando alla soluzione stessa vengono aggiunti degli acidi o delle basi. Il sistema tampone NON elimina il carico acido/basico E composto da un acido debole e dalla sua base coniugata HA A - + H + ph = -log 10 [H + ] K A =!" [$ & ] [!$] K A (costante acida): concentrazione di H + alla quale la forma acida e basica sono presenti in uguale concentrazione ph = pk A + log 10! " [!$] Equazione di Handerson- Hasselbach : logaritmo negativo della costante acida
9 Nell organismo esistono numerosi sistemi tampone e ciascuno di essi ha un equilibrio descritto dalla sua equazione di H-H. Extracellulari (HCO 3 -/H 2 CO 3, ) Intracellulari (Hb, Proteine citoplasmatiche,...) Urinari (Fosfato, Ammonio) Tessuto osseo Però, poiché tutti sono in equilibrio tra di loro, è sufficiente studiarne uno solo per conoscere l equilibrio acido-base di un soggetto.
10 Il sistema tampone bicarbonato/acido carbonico CO 2 + H 2 O H 2 CO 3 HCO H + ph= pk + log [$'( ) " ] ['( * ] È il tampone quantitativamente più importante nell extracellulare È un sistema aperto: le due componenti (CO 2 e HCO 3- ) sono facilmente misurabili e direttamente influenzate dai due sistemi principalmente coinvolti nella regolazione dell equilibrio acido-base: rene e polmone
11 Regolazione respiratoria dell equilibrio acido base CO 2 + H 2 O H 2 CO 3 HCO H + ph= pk + log [$'( ) " ] ['( * ] Aumento di pco 2 significa diminuzione del ph, diminuzione di pco 2 aumento del ph. Regolando la pco 2 attraverso variazioni della ventilazione, i polmoni possono regolare il ph: Se il ph diminuisce, la ventilazione è stimolata e la conseguente riduzione di pco 2 riporta il ph vicino ai valori normali Se il ph aumenta il centro respiratorio viene depresso, la ventilazione si riduce e il conseguente aumento di pco 2 riporta il ph vicino ai valori normali
12 Regolazione renale dell equilibrio acido base (1) CO 2 + H 2 O H 2 CO 3 HCO H + ph= pk + log [$'( ) " ] ['( * ] Ogni giorno vengono prodotti circa 70 meq di H + Tale quota acida viene subito neutralizzata (non eliminata) dai sistemi tampone La CO 2 formata in eccesso viene rapidamente eliminata con la ventilazione Questo meccanismo, però, consuma bicarbonati
13 Regolazione renale dell equilibrio acido base (2) I reni devono Riassorbire tutto il bicarbonato filtrato (principalmente nel tubulo contorto prossimale) Eliminare una quantità di ioni idrogeno equivalente a quella prodotta e tramite questo processo rigenerare l HCO 3- consumato dai processi metabolici Entrambi questi processi avvengono grazie alla secrezione di ioni H + nel tubulo
14 Riassorbimento del bicarbonato nel tubulo contorto prossimale
15 Eliminazione degli H + e rigenerazione del bicarbonato Il ph delle urine non può scendere sotto 4,5 Se tutti i 70mEq di H + prodotti giornalmente dovessero essere escreti in forma libera servirebbero più di 2000 l di urina Per eliminare i carichi acidi il rene utilizza dei tamponi urinari (sistema del fosfato e sistema dell ammonio) Ogni volta che uno ione H + secreto nel lume si combina con un tampone diverso da HCO 3- (Fosfato, Ammoniaca), un nuovo bicarbonato viene immesso in circolo
16 Tampone Fosfato Tubulo distale (H 3 PO 4 + 2NaHCO 3 Na 2 HPO 2 + 2H 2 CO 3 ) Gli H + secreti vengono tamponati da parte di HPO 4 2- filtrato. Per ogni ione H + secreto che si combina con un tampone diverso dal bicarbonato un nuovo ione HCO 3- ritorna ai capillari peritubulari.
17 Formazione di ammonio urinario (NH 4+ ) Tubulo distale Tubulo prossimale Tubulo prossimale: la glutammina intracellulare è metabolizzata in 2 NH 4+ e α-chetoglutarato. Il metabolismo di quest ultimo forma HCO 3-. NH 4+ viene scambiato con Na +. Segmento spesso dell ansa di Henle: L ammonio viene riassorbito. Nell interstizio della midollare si trova in equilibrio con NH 3 Tubulo distale: l ammoniaca liposolubile diffonde nel lume dove reagisce con H + secreto per formare NH 4+, che viene eliminato con le urine.
18 Dis-equilibrio acido-base: definizioni Acidemia ph arterioso < 7,35 Alcalemia ph arterioso > 7,45 Acidosi Alcalosi Processo fisiopatologico che tende ad aumentare [H + ] e a ridurre il ph Processo fisiopatologico che tende a ridurre [ H + ] e ad aumentare il ph Acidosi metabolica Acidosi causata da riduzione primitiva di HCO - 3 Alcalosi metabolica Alcalosi causata da aumento primitivo di HCO - 3 Acidosi respiratoria Acidosi causata da aumento primitiva della pco 2 Alcalosi respiratoria Alcalosi causata da riduzione primitiva della pco 2 Disordine misto Compenso Condizione nella quale è presente più di un disturbo acido-base primitivo Risposta fisiologica all acidosi o all alcalosi che determina un parziale ritorno del ph verso i livelli normali
19 Compensi Squilibrio primitivo respiratorio à compenso metabolico Squilibrio primitivo metabolico à compenso respiratorio acidosi metabolica alcalosi metabolica acidosi respiratoria alcalosi respiratoria riduzione PaCO 2 (polmone) aumento PaCO 2 (polmone) aumento bicarbonati (rene) riduzione bicarbonati (rene)
20 da Carrol, Fisiologia, ElsevierMasson
Rene ed equilibrio acido base. La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica. Principali funzioni renali
 Rene ed equilibrio acido base La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica Savi Umberto Scuola di Specializzazione in Nefrologia S.C. di Nefrologia e Dialisi Cattinara
Rene ed equilibrio acido base La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica Savi Umberto Scuola di Specializzazione in Nefrologia S.C. di Nefrologia e Dialisi Cattinara
Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca
 Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
ph = log 1/[H + ] = log [H + ]
![ph = log 1/[H + ] = log [H + ] ph = log 1/[H + ] = log [H + ]](/thumbs/49/24977942.jpg) ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
Le reazioni metaboliche sono estremamente sensibili alla concentrazione degli ioni H + nel liquido in cui avvengono, perché gli ioni H + influenzano
 EQUILIBRIO ACIDOBASE Le reazioni metaboliche sono estremamente sensibili alla concentrazione degli ioni H + nel liquido in cui avvengono, perché gli ioni H + influenzano il funzionamento degli enzimi.
EQUILIBRIO ACIDOBASE Le reazioni metaboliche sono estremamente sensibili alla concentrazione degli ioni H + nel liquido in cui avvengono, perché gli ioni H + influenzano il funzionamento degli enzimi.
Equilibrio acido-base
 Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
Rene ed equilibrio acido-base
 Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia Obiettivi Produzione e bilancio degli idrogenioni Regolazione respiratoria e renale del ph Riassorbimento del bicarbonato e secrezione
Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia Obiettivi Produzione e bilancio degli idrogenioni Regolazione respiratoria e renale del ph Riassorbimento del bicarbonato e secrezione
Equilibrio acido-base
 Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
Equilibrio acido base
 Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio
 Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
a.a. 2017/18 Prof.ssa Pia Lucidi Laboratorio di Cognizione e Benessere Animale RICEVIMENTO: Lunedì 17:30-18:30
 a.a. 2017/18 Prof.ssa Pia Lucidi Laboratorio di Cognizione e Benessere Animale RICEVIMENTO: Lunedì 17:3018:30 Omeostasi acidobasica Gli enzimi operano ad un ph ottimale in un range molto ristretto (7.4
a.a. 2017/18 Prof.ssa Pia Lucidi Laboratorio di Cognizione e Benessere Animale RICEVIMENTO: Lunedì 17:3018:30 Omeostasi acidobasica Gli enzimi operano ad un ph ottimale in un range molto ristretto (7.4
I tre sistemi per la regolazione del ph
 I tre sistemi per la regolazione del ph Se vuoi finalmente capire quali sono e come funzionano i sistemi per la regolazione del ph questo breve articolo fa proprio al caso tuo. In questo articolo parleremo
I tre sistemi per la regolazione del ph Se vuoi finalmente capire quali sono e come funzionano i sistemi per la regolazione del ph questo breve articolo fa proprio al caso tuo. In questo articolo parleremo
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI
 EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
2.Controllo dell equilibrio acido-base - II. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
Principali funzioni renali
 FISIOLOGIA RENALE per le lezioni del prof. P. Paolo Battaglini v 3.5 Principali fonti delle figure: Conti et al., FISIOLOGIA MEDICA, Edi Ermes Guyton e Hall, FISIOLOGIA MEDICA, Elsevier Silverthorn, Fisiologia
FISIOLOGIA RENALE per le lezioni del prof. P. Paolo Battaglini v 3.5 Principali fonti delle figure: Conti et al., FISIOLOGIA MEDICA, Edi Ermes Guyton e Hall, FISIOLOGIA MEDICA, Elsevier Silverthorn, Fisiologia
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra ). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Sistema urinario: la funzione renale
 Sistema urinario: la funzione renale FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici, i reni ne regolano la concentrazione plasmatica
Sistema urinario: la funzione renale FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici, i reni ne regolano la concentrazione plasmatica
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante di dissociazione
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante di dissociazione
Dichiarazione. Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei.
 Per le lezioni del prof. P.P. Battaglini Schemi di Dichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei. Queste immagini vengono utilizzate per l
Per le lezioni del prof. P.P. Battaglini Schemi di Dichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei. Queste immagini vengono utilizzate per l
Tamponi Biologici. AO/Febbraio 2016
 Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Emogasanalisi in t.i.
 Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
DISORDINI DELL EQUILIBRIO ACIDO - BASE
 DISORDINI DELL EQUILIBRIO ACIDO - BASE Equilibrio acido-base e potassio Nel tubulo distale e dotto collettore il riassorbimento del bicarbonato è legato a quello del potassio Il riassorbimento del bicarbonato
DISORDINI DELL EQUILIBRIO ACIDO - BASE Equilibrio acido-base e potassio Nel tubulo distale e dotto collettore il riassorbimento del bicarbonato è legato a quello del potassio Il riassorbimento del bicarbonato
Il Rene Regola la Concentrazione di Idrogenioni nel LEC attraverso Tre Meccanismi Fondamentali:
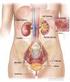 Il Rene Regola la Concentrazione di Idrogenioni nel LEC attraverso Tre Meccanismi Fondamentali: 1) Secerne Idrogenioni; 1a) Riassorbe il Bicarbonato Filtrato; 1b) Produce Nuovo Bicarbonato. 4320 meq/die
Il Rene Regola la Concentrazione di Idrogenioni nel LEC attraverso Tre Meccanismi Fondamentali: 1) Secerne Idrogenioni; 1a) Riassorbe il Bicarbonato Filtrato; 1b) Produce Nuovo Bicarbonato. 4320 meq/die
Equilibrio acido-base: il ph è importante
 Equilibrio acido-base: il ph è importante il ph è strettamente controllato il ph influenza l attività enzimatica il ph è diverso nei vari compartimenti: Esempio: stomaco- acido duodeno alcalino Il ph varia
Equilibrio acido-base: il ph è importante il ph è strettamente controllato il ph influenza l attività enzimatica il ph è diverso nei vari compartimenti: Esempio: stomaco- acido duodeno alcalino Il ph varia
LA RISPOSTA POLMONARE
 IL CONTROLLO INTEGRATO DELL EQUILIBRIO ACIDO-BASE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE --------------------------------------------------------------------------------------------------------------
IL CONTROLLO INTEGRATO DELL EQUILIBRIO ACIDO-BASE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE --------------------------------------------------------------------------------------------------------------
45. Fisiologia dell'equilibrio acido-base
 Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione ebook Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione ebook Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
45. Fisiologia dell'equilibrio acido-base
 Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione print edition Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione print edition Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO BASE Le reazioni metaboliche sono molto sensibili a cambiamenti del ph: il ph dei liquidi dell organismo è mantenuto entro un range di valori molto stretto. ph intracellulare è generalmente
EQUILIBRIO ACIDO BASE Le reazioni metaboliche sono molto sensibili a cambiamenti del ph: il ph dei liquidi dell organismo è mantenuto entro un range di valori molto stretto. ph intracellulare è generalmente
17/05/2010. Equilibrio idrico. Variazioni del volume ematico indicono risposte omeostatiche
 Equilibrio idrico Variazioni del volume ematico indicono risposte omeostatiche 1 Ruolo del rene nel bilancio idrico Variazioni dell osmolarità attraverso la midollare 2 Scambio per controcorrente nella
Equilibrio idrico Variazioni del volume ematico indicono risposte omeostatiche 1 Ruolo del rene nel bilancio idrico Variazioni dell osmolarità attraverso la midollare 2 Scambio per controcorrente nella
LEZIONE 29: REGOLAZIONE NEUROORMONALE MECCANISMI NEUROORMONALI DI REGOLAZIONE DEL RENE
 LEZIONE 29: REGOLAZIONE NEUROORMONALE MECCANISMI NEUROORMONALI DI REGOLAZIONE DEL RENE 1 ALDOSTERONE Ormone steroideo rilasciato dalla corticale surrenale l aldosterone stimola: riassorbimento di Na +
LEZIONE 29: REGOLAZIONE NEUROORMONALE MECCANISMI NEUROORMONALI DI REGOLAZIONE DEL RENE 1 ALDOSTERONE Ormone steroideo rilasciato dalla corticale surrenale l aldosterone stimola: riassorbimento di Na +
Equilibri acido-base, ph e sistemi tampone
 Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
PSEUDOIPERKALEMIA o IPERPOTASSIEMIA SPURIA. Il paziente non ha problemi cardiaci ma iperpotassiemia
 PSEUDOIPERKALEMIA o IPERPOTASSIEMIA SPURIA Il paziente non ha problemi cardiaci ma iperpotassiemia Cause: Prolungato utilizzo del laccio emostatico Rottura delle cellule, durante il prelievo di sangue
PSEUDOIPERKALEMIA o IPERPOTASSIEMIA SPURIA Il paziente non ha problemi cardiaci ma iperpotassiemia Cause: Prolungato utilizzo del laccio emostatico Rottura delle cellule, durante il prelievo di sangue
Sistema urinario: la funzione renale
 Sistema urinario: la funzione renale La principale funzione dei reni è il bilancio idrosalino FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici,
Sistema urinario: la funzione renale La principale funzione dei reni è il bilancio idrosalino FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici,
Funzioni. Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto
 La Funzione Renale Funzioni Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto Il Nefrone Distinguiamo un tubulo renale (trasporto) ed un corpuscolo renale
La Funzione Renale Funzioni Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto Il Nefrone Distinguiamo un tubulo renale (trasporto) ed un corpuscolo renale
PRINCIPALI SISTEMI TAMPONE
 SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
Alterazione della capacità tampone nell'organismo. Alterazione capacità tampone rev. 0 - data: 5 luglio
 Alterazione della capacità tampone nell'organismo Alterazione capacità tampone rev. 0 - data: 5 luglio 2008 1 Il ph fisiologico dell'organismo è compreso tra 7.38 e 7.44 Nel liquido extracellulare sono
Alterazione della capacità tampone nell'organismo Alterazione capacità tampone rev. 0 - data: 5 luglio 2008 1 Il ph fisiologico dell'organismo è compreso tra 7.38 e 7.44 Nel liquido extracellulare sono
Trasporto dei gas respiratori nel sangue
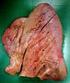 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
L'EQUILIBRIO ACIDO-BASE
 L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
1. Controllo dell equilibrio acido-base. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO - BASE da appunti del dott. Claudio Italiano, internista ospedaliero Che significa? Vuol dire che l organismo ha un suo equilibrio, detto omeòstasi, cioè il sangue deve necessariamente
EQUILIBRIO ACIDO - BASE da appunti del dott. Claudio Italiano, internista ospedaliero Che significa? Vuol dire che l organismo ha un suo equilibrio, detto omeòstasi, cioè il sangue deve necessariamente
SOLUZIONE TAMPONE. Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti
 SOLUZIONE TAMPONE Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti Una soluzione tampone è costituita da Acido debole in presenza della propria base coniugata
SOLUZIONE TAMPONE Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti Una soluzione tampone è costituita da Acido debole in presenza della propria base coniugata
FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua
 FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie Università degli Studi Verona Obiettivi Funzioni
FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie Università degli Studi Verona Obiettivi Funzioni
Teorie Acido-Base. Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH -
 Teorie Acido-Base Arrhenius: Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH - Broensted-Lowry: Gli acidi rilasciano H + Le basi accettano H + Lewis gli
Teorie Acido-Base Arrhenius: Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH - Broensted-Lowry: Gli acidi rilasciano H + Le basi accettano H + Lewis gli
Equilibrio Acido-Base: interpretazione dati emogasanalitici
 Equilibrio Acido-Base: interpretazione dati emogasanalitici Dott.ssa M. Martino Corso di medicina generale Anno 2010 L EMOGASANALISI è stata definita dall OMS come l esame in assoluto con il miglior rapporto
Equilibrio Acido-Base: interpretazione dati emogasanalitici Dott.ssa M. Martino Corso di medicina generale Anno 2010 L EMOGASANALISI è stata definita dall OMS come l esame in assoluto con il miglior rapporto
Raffaele Alvisi 14 gennaio 1916
 Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
diminuito aumentato I disordini acido-base primari metabolici si riconoscono attraverso la valutazione della concentrazione di HCO3-
 diminuito aumentato I disordini acido-base primari metabolici si riconoscono attraverso la valutazione della concentrazione di HCO3- Risposta compensatoria all acidosi metabolica Compensazione polmonare
diminuito aumentato I disordini acido-base primari metabolici si riconoscono attraverso la valutazione della concentrazione di HCO3- Risposta compensatoria all acidosi metabolica Compensazione polmonare
In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + +
 Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
L anatomia dell apparato urinario
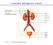 L anatomia dell apparato urinario Le funzioni del rene Secrezione (escrezione) Equilibrio idrico (controllo della pressione arteriosa) Equilibrio salino (controllo della composizione elettrolitica) Endocrina
L anatomia dell apparato urinario Le funzioni del rene Secrezione (escrezione) Equilibrio idrico (controllo della pressione arteriosa) Equilibrio salino (controllo della composizione elettrolitica) Endocrina
CHIRURGIA III ED EMERGENZE MEDICO - CHIRURGICHE. Sezione di Anestesia e Rianimazione Dir. Prof. Carlo Alberto Volta
 CHIRURGIA III ED EMERGENZE MEDICO - CHIRURGICHE Sezione di Anestesia e Rianimazione Dir. Prof. Carlo Alberto Volta Equilibrio acido-base Ph normale: 7.35-7.45 Acidemia per ph < 7.35 Alcalemia per ph >
CHIRURGIA III ED EMERGENZE MEDICO - CHIRURGICHE Sezione di Anestesia e Rianimazione Dir. Prof. Carlo Alberto Volta Equilibrio acido-base Ph normale: 7.35-7.45 Acidemia per ph < 7.35 Alcalemia per ph >
La eliminazione dei protoni nelle urine permette il ripristino di bicarbonato nel circolo sistemico.
 ESCREZIONE URINARIA DI ACIDI : 1-1,5 meq/l Es. produzione endogena di ac. solforico o cloridrico, formazione di sodio solfato o cloruro, eliminazione urinaria di ammonio legato ai sali. La eliminazione
ESCREZIONE URINARIA DI ACIDI : 1-1,5 meq/l Es. produzione endogena di ac. solforico o cloridrico, formazione di sodio solfato o cloruro, eliminazione urinaria di ammonio legato ai sali. La eliminazione
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
Trasporto epiteliale
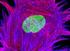 Trasporto epiteliale Rivestono le cavità e le superfici corporee: interfaccia tra gli spazi interni dell organismo e l ambiente Semplice rivestimento o funzione di regolazione (es:osmoregolazione) Trasporto
Trasporto epiteliale Rivestono le cavità e le superfici corporee: interfaccia tra gli spazi interni dell organismo e l ambiente Semplice rivestimento o funzione di regolazione (es:osmoregolazione) Trasporto
SOLUZIONI derivate da: Acido debole/ sale (CH 3 COOH/CH 3 COONa) Base debole/ suo sale (NH 4 OH/NH 4 Cl)
 Soluzioni Tampone Si definiscono soluzioni tampone quelle soluzioni in grado di mantenere pressoché costante il proprio ph per aggiunta di una ragionevole quantità di acido o di base forte o per moderata
Soluzioni Tampone Si definiscono soluzioni tampone quelle soluzioni in grado di mantenere pressoché costante il proprio ph per aggiunta di una ragionevole quantità di acido o di base forte o per moderata
Per le lezioni del prof. P.P. Battaglini. Per il corso di: Medicina e Chirurgia Dell Università di Trieste. Dichiarazione
 Schemi di Per le lezioni del prof. P.P. Battaglini Per il corso di: Medicina e Chirurgia Dell Università di Trieste Dichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate
Schemi di Per le lezioni del prof. P.P. Battaglini Per il corso di: Medicina e Chirurgia Dell Università di Trieste Dichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate
Il rene regola l escrezione dei diversi soluti indipendentemente l uno dall altro, controllandone la velocità di riassorbimento.
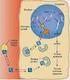 Il rene regola l escrezione dei diversi soluti indipendentemente l uno dall altro, controllandone la velocità di riassorbimento. Lungo i tubuli renali viene riassorbita la maggior parte dei soluti e il
Il rene regola l escrezione dei diversi soluti indipendentemente l uno dall altro, controllandone la velocità di riassorbimento. Lungo i tubuli renali viene riassorbita la maggior parte dei soluti e il
SCOPI DELL EMOGASANALISI
 EMOGASANALISI SCOPI DELL EMOGASANALISI La funzione principale della respirazione è quella di assicurare ossigeno all organismo e di eliminare l eccesso di anidride carbonica. L emogasanalisi arteriosa
EMOGASANALISI SCOPI DELL EMOGASANALISI La funzione principale della respirazione è quella di assicurare ossigeno all organismo e di eliminare l eccesso di anidride carbonica. L emogasanalisi arteriosa
Sodio. L introduzione giornaliera con la dieta di sodio (200 meq/l) è maggiore del nostro fabbisogno (20 meq/l): è necessaria l escrezione urinaria
 Sodio L introduzione giornaliera con la dieta di sodio (200 meq/l) è maggiore del nostro fabbisogno (20 meq/l): è necessaria l escrezione urinaria E elemento principale per il controllo dell osmolalità
Sodio L introduzione giornaliera con la dieta di sodio (200 meq/l) è maggiore del nostro fabbisogno (20 meq/l): è necessaria l escrezione urinaria E elemento principale per il controllo dell osmolalità
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE
 EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
Anatomia funzionale del rene
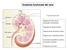 Anatomia funzionale del rene Funzione dei reni: Regolazione del volume del liquido extracellulare Regolazione dell osmolarità Mantenimento del bilancio idrico Regolazione omeostatica del ph Escrezione
Anatomia funzionale del rene Funzione dei reni: Regolazione del volume del liquido extracellulare Regolazione dell osmolarità Mantenimento del bilancio idrico Regolazione omeostatica del ph Escrezione
Gli scambi gassosi LA MISURA DELLA FUNZIONE RESPIRATORIA. OLTRE LA SPIROMETRIA Torino, 5 ottobre 2013
 LA MISURA DELLA FUNZIONE RESPIRATORIA OLTRE LA SPIROMETRIA Torino, 5 ottobre 2013 Gli scambi gassosi Claudio Norbiato AO Ordine Mauriziano SC Medicina Interna Emogasanalisi L emogasanalisi e l analisi
LA MISURA DELLA FUNZIONE RESPIRATORIA OLTRE LA SPIROMETRIA Torino, 5 ottobre 2013 Gli scambi gassosi Claudio Norbiato AO Ordine Mauriziano SC Medicina Interna Emogasanalisi L emogasanalisi e l analisi
acqua, CO 2, O 2, sali e ioni H +
 Legge dell Equilibrio di Massa Se la quantità di una sostanza nell organismo deve rimanere costante, ad ogni sua acquisizione deve corrispondere una perdita di eguale entità acqua, CO 2, O 2, sali e ioni
Legge dell Equilibrio di Massa Se la quantità di una sostanza nell organismo deve rimanere costante, ad ogni sua acquisizione deve corrispondere una perdita di eguale entità acqua, CO 2, O 2, sali e ioni
[H + ] X [A - ] [ HA ]
![[H + ] X [A - ] [ HA ] [H + ] X [A - ] [ HA ]](/thumbs/81/84332766.jpg) Equazione di Handerson-HasselbalchHasselbalch [H + ] X [A - ] [ HA ] = K [H + ]X[HCO3 - ] [H2C03] = K 1 Composizione aria O 2 = 20.93% CO 2 = 0.03% N 2 + gas nobili = 79.04% Pressione esercitata dai gas
Equazione di Handerson-HasselbalchHasselbalch [H + ] X [A - ] [ HA ] = K [H + ]X[HCO3 - ] [H2C03] = K 1 Composizione aria O 2 = 20.93% CO 2 = 0.03% N 2 + gas nobili = 79.04% Pressione esercitata dai gas
ESCREZIONE DEI FARMACI
 ESCREZIONE DEI FARMACI RENALE (urine) GASTROINTESTINALE ED EPATICA (feci) POLMONARE (aria espirata) CUTANEA (sudore) MAMMARIA (latte) ALTRE (saliva, lacrime) 1 La quantità e la velocità di escrezione renale
ESCREZIONE DEI FARMACI RENALE (urine) GASTROINTESTINALE ED EPATICA (feci) POLMONARE (aria espirata) CUTANEA (sudore) MAMMARIA (latte) ALTRE (saliva, lacrime) 1 La quantità e la velocità di escrezione renale
Acidi e basi di Lewis
 Gli acidi e le basi Acidi e basi di Lewis Acidi di Lewis= specie che possono accettare in compartecipazione una coppia di elettroni da un altra specie. Base di Lewis = specie che può cedere in compartecipazione
Gli acidi e le basi Acidi e basi di Lewis Acidi di Lewis= specie che possono accettare in compartecipazione una coppia di elettroni da un altra specie. Base di Lewis = specie che può cedere in compartecipazione
CONTROLLO DELL OSMOLALITA DEI LIQUIDI CORPOREI
 CONTROLLO DELL OSMOLALITA DEI LIQUIDI CORPOREI Il rene è responsabile del controllo dell escrezione di acqua. Altre vie che consentono l eliminazione di acqua dall organismo includono sudorazione, feci
CONTROLLO DELL OSMOLALITA DEI LIQUIDI CORPOREI Il rene è responsabile del controllo dell escrezione di acqua. Altre vie che consentono l eliminazione di acqua dall organismo includono sudorazione, feci
Escrezione renale di Na + e sua regolazione
 Escrezione renale di e sua regolazione L escrezione di dipende dal carico filtrato (e quindi dalla VFG) e dal carico riassorbito Il riassorbimento di avviene in tutti i segmenti del nefrone e nel nefrone
Escrezione renale di e sua regolazione L escrezione di dipende dal carico filtrato (e quindi dalla VFG) e dal carico riassorbito Il riassorbimento di avviene in tutti i segmenti del nefrone e nel nefrone
IL RUOLO DELL EMOGASANALISI NELL INSUFFIENZA RESPIRATORIA
 I CONGRESSO REGIONALE SIMEU BASILICATA 13 E 14 GIUGNO 2014 IL RUOLO DELL EMOGASANALISI NELL INSUFFIENZA RESPIRATORIA DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA NOCERAPAGANI SEGRETARIO NAZIONALE FIMEUC PRESISDENTE
I CONGRESSO REGIONALE SIMEU BASILICATA 13 E 14 GIUGNO 2014 IL RUOLO DELL EMOGASANALISI NELL INSUFFIENZA RESPIRATORIA DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA NOCERAPAGANI SEGRETARIO NAZIONALE FIMEUC PRESISDENTE
ALTERAZIONI IDROELETTROLITICHE. ACIDO-BASE (2 parte) scaricato da EQUILIBRIO ACIDO-BASE (EAB) NECESSITA : EQUILIBRIO ACIDO-BASE
 (EAB) ALTERAZIONI IDROELETTROLITICHE ED ACIDOBASE (2 parte) NECESSITA : Mantenere costante il ph dei liquidi dell organismo su valori di 7,407,41 a fronte della produzione continua di acidi fissi ( 1mEq/kg
(EAB) ALTERAZIONI IDROELETTROLITICHE ED ACIDOBASE (2 parte) NECESSITA : Mantenere costante il ph dei liquidi dell organismo su valori di 7,407,41 a fronte della produzione continua di acidi fissi ( 1mEq/kg
La costanza di questi volumi dipende dall equilibrio tra assunzione ed eliminazione di acqua. Plasma 3 litri. Sistema linfatico. extracellulare (LEC)
 Equilibrio idrico-salino Liquidi corporei Plasma 3 litri Sistema linfatico Liquido extracellulare (LEC) 14 litri Endotelio capillare Liquido interstiziale 11 litri Nell adulto, in condizioni normali, i
Equilibrio idrico-salino Liquidi corporei Plasma 3 litri Sistema linfatico Liquido extracellulare (LEC) 14 litri Endotelio capillare Liquido interstiziale 11 litri Nell adulto, in condizioni normali, i
Eliminare dall organismo prodotti di rifiuto e sostanze tossiche idrosolubili(soprattutto prodotti azotati e creatinina);
 Funzioni del rene Eliminare dall organismo prodotti di rifiuto e sostanze tossiche idrosolubili(soprattutto prodotti azotati e creatinina); Regolare il volume e la composizione del liquido extracellulare;
Funzioni del rene Eliminare dall organismo prodotti di rifiuto e sostanze tossiche idrosolubili(soprattutto prodotti azotati e creatinina); Regolare il volume e la composizione del liquido extracellulare;
Omeostasi idro-elettrolitica
 Omeostasi idro-elettrolitica Riassorbimento idrico isoosmotico o obbligatorio Riassorbimento idrico non-isoosmotico o facoltativo Il bilancio idrico richiede l azione integrata di molteplici sistemi 1
Omeostasi idro-elettrolitica Riassorbimento idrico isoosmotico o obbligatorio Riassorbimento idrico non-isoosmotico o facoltativo Il bilancio idrico richiede l azione integrata di molteplici sistemi 1
Per le lezioni del prof. P.P. Battaglini. Dichiarazione
 Schemi di Per le lezioni del prof. P.P. Battaglini ichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei. Queste immagini vengono utilizzate per l
Schemi di Per le lezioni del prof. P.P. Battaglini ichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei. Queste immagini vengono utilizzate per l
OSMOREGOLAZIONE DEI LIQUIDI CORPOREI
 OSMOREGOLAZIONE DEI LIQUIDI CORPOREI Lezione 25 1 Distribuzione dei liquidi corporei L H 2 O contenuta nel corpo è circa il 60% del peso totale ed è così ripartita: 67% 33% EXTRACELLULARE 33% INTRACELLULARE
OSMOREGOLAZIONE DEI LIQUIDI CORPOREI Lezione 25 1 Distribuzione dei liquidi corporei L H 2 O contenuta nel corpo è circa il 60% del peso totale ed è così ripartita: 67% 33% EXTRACELLULARE 33% INTRACELLULARE
ELIMINAZIONE DEI FARMACI. L eliminazione di un farmaco avviene per escrezione e/o per biotrasformazione.
 ELIMINAZIONE DEI FARMACI L eliminazione di un farmaco avviene per escrezione e/o per biotrasformazione. Possono essere escreti: il farmaco immodificato i suoi metaboliti Le principali vie di escrezione
ELIMINAZIONE DEI FARMACI L eliminazione di un farmaco avviene per escrezione e/o per biotrasformazione. Possono essere escreti: il farmaco immodificato i suoi metaboliti Le principali vie di escrezione
L EMOGASANALISI. P. Scavalli, M. Vitto, S. Mosillo
 L EMOGASANALISI P. Scavalli, M. Vitto, S. Mosillo EMOGASANALISI Consente la misurazione immediata dei due gas più importanti del sangue e di un terzo parametro fondamentale per la valutazione dell omeostasi
L EMOGASANALISI P. Scavalli, M. Vitto, S. Mosillo EMOGASANALISI Consente la misurazione immediata dei due gas più importanti del sangue e di un terzo parametro fondamentale per la valutazione dell omeostasi
INTRODUZIONE ALLA FARMACOCINETICA
 Diapositiva 1 INTRODUZIONE ALLA FARMACOCINETICA FARMACOCINETICA FARMACODINAMICA Farmaco a livello del sito di somministrazione Farmaco nel plasma Assorbimento Meccanismo d azione Metabolizzazione Distribuzione
Diapositiva 1 INTRODUZIONE ALLA FARMACOCINETICA FARMACOCINETICA FARMACODINAMICA Farmaco a livello del sito di somministrazione Farmaco nel plasma Assorbimento Meccanismo d azione Metabolizzazione Distribuzione
Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori:
 Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori: 1) Dalla differenza netta di pressione tra il lume del capillare ed il lume della capsula di Bowman; 2) dalla
Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori: 1) Dalla differenza netta di pressione tra il lume del capillare ed il lume della capsula di Bowman; 2) dalla
Riassorbimento dell acqua lungo il nefrone
 Riassorbimento dell acqua lungo il nefrone La quota escreta di acqua varia fra 0.25% (0.5 L/giorno, massima antidiuresi) ed il 13% (24 L/giorno, massima diuresi), attestandosi in condizioni normali intorno
Riassorbimento dell acqua lungo il nefrone La quota escreta di acqua varia fra 0.25% (0.5 L/giorno, massima antidiuresi) ed il 13% (24 L/giorno, massima diuresi), attestandosi in condizioni normali intorno
Milano, 9 giugno acido-base? Ernesto Cristiano Lauritano
 ACQUA E SALE Milano, 9 giugno 2012 Quale approccio ai disordini acido-base? Ernesto Cristiano Lauritano Dipartimento di Emergenza e Accettazione Azienda Ospedaliera Nazionale SS. Antonio e Biagio e Cesare
ACQUA E SALE Milano, 9 giugno 2012 Quale approccio ai disordini acido-base? Ernesto Cristiano Lauritano Dipartimento di Emergenza e Accettazione Azienda Ospedaliera Nazionale SS. Antonio e Biagio e Cesare
Dott.ssa Marta Tavecchia. COS E IL ph?
 Dott.ssa Marta Tavecchia COS E IL ph? IL RENE: COSA FA? Regola il bilancio idrico Regola il bilancio elettrolitico Regola l equilibrio acido base Elimina le scorie del metabolismo azotato Svolge un ruolo
Dott.ssa Marta Tavecchia COS E IL ph? IL RENE: COSA FA? Regola il bilancio idrico Regola il bilancio elettrolitico Regola l equilibrio acido base Elimina le scorie del metabolismo azotato Svolge un ruolo
Indice INTRODUZIONE
 EQUILIBRIO ACIDO-BASE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 OMEOSTASI DEL PH --------------------------------------------------------------------------------------------------------
EQUILIBRIO ACIDO-BASE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 OMEOSTASI DEL PH --------------------------------------------------------------------------------------------------------
L INSUFFICIENZA RESPIRATORIA ACUTA DAL TERRITORIO ALLA MEDICINA D URGENZA
 L INSUFFICIENZA RESPIRATORIA ACUTA DAL TERRITORIO ALLA MEDICINA D URGENZA 28 SETTEMBRE 2010 NOLA MONITORAGGIO DEGLI SCAMBI GASSOSI ED ALTERAZIONI EMOGASANALITICHE DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA
L INSUFFICIENZA RESPIRATORIA ACUTA DAL TERRITORIO ALLA MEDICINA D URGENZA 28 SETTEMBRE 2010 NOLA MONITORAGGIO DEGLI SCAMBI GASSOSI ED ALTERAZIONI EMOGASANALITICHE DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA
I RENI I reni sono organi pari parenchimatosi escretori (nello specifico, emuntori) dei vertebrati. Insieme alle vie urinarie costituiscono l'apparato
 FISIOLOGIA RENALE I RENI I reni sono organi pari parenchimatosi escretori (nello specifico, emuntori) dei vertebrati. Insieme alle vie urinarie costituiscono l'apparato urinario, che filtra dal sangue
FISIOLOGIA RENALE I RENI I reni sono organi pari parenchimatosi escretori (nello specifico, emuntori) dei vertebrati. Insieme alle vie urinarie costituiscono l'apparato urinario, che filtra dal sangue
Fisiologia Renale 5. Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale 5. Equilibrio acidobase: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Produzione e bilancio
Fisiologia Renale 5. Equilibrio acidobase: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Produzione e bilancio
Le Quattro Funzioni principali di eliminazione nel rene: I -Ultrafiltrazione (capsula di Bowman) II -Diffusione (riassorbimento) III -Secrezione per:
 Escrezione I Farmaci previa o meno biotrasformazione (metabolismo) possono essere escreti dal rene (urine), dal fegato e intestino (bile e feci), dal polmone (aria espirata), ma anche col latte materno,
Escrezione I Farmaci previa o meno biotrasformazione (metabolismo) possono essere escreti dal rene (urine), dal fegato e intestino (bile e feci), dal polmone (aria espirata), ma anche col latte materno,
FORZA DI ACIDI E BASI HA + :B HB + + A
 FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
Biochimica clinica. Corso di Laurea Triennale in Biotecnologie per la salute
 Corso di Laurea Triennale in Biotecnologie per la salute Biochimica clinica Argomenti della lezione:» Aspetti generali dell'equilibrio acidobase» Regolazione renale e polmonare» Emogasanalisi Gli elettroliti
Corso di Laurea Triennale in Biotecnologie per la salute Biochimica clinica Argomenti della lezione:» Aspetti generali dell'equilibrio acidobase» Regolazione renale e polmonare» Emogasanalisi Gli elettroliti
LEZIONE 28: RIASSORBIMENTO E SECREZIONE TUBULARE
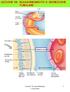 LEZIONE 28: RIASSORBIMENTO E SECREZIONE TUBULARE 1 2 capillare peritubulare 80% >19% : riassorbito 20% Frazione di filtrazione riassorbimento = movimento di soluti filtrati e di acqua dal lume tubulare
LEZIONE 28: RIASSORBIMENTO E SECREZIONE TUBULARE 1 2 capillare peritubulare 80% >19% : riassorbito 20% Frazione di filtrazione riassorbimento = movimento di soluti filtrati e di acqua dal lume tubulare
Soluzioni tampone. Se ad un litro di acqua pura (ph=7) vengono aggiunte 0,01 moli di HCl il ph varia da 7 a 2 (ph=-log(0,01) =2,0), ovvero di 5 unità.
 Soluzioni tampone Se ad un litro di acqua pura (ph=7) vengono aggiunte 0,01 moli di HCl il ph varia da 7 a 2 (ph=-log(0,01) =2,0), ovvero di 5 unità. Un tampone è una soluzione che varia in maniera trascurabile
Soluzioni tampone Se ad un litro di acqua pura (ph=7) vengono aggiunte 0,01 moli di HCl il ph varia da 7 a 2 (ph=-log(0,01) =2,0), ovvero di 5 unità. Un tampone è una soluzione che varia in maniera trascurabile
In base all equazione di Henderson-Hasselbalch
 Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
 Trigliceridi Colesterolo Esteri del Colesterolo Fosfolipidi Trasporti attraverso le membrane Diffusione facilitata: Scambio dei cloruri o Scambio Cl - /HCO - 3 Cl - HCO3
Trigliceridi Colesterolo Esteri del Colesterolo Fosfolipidi Trasporti attraverso le membrane Diffusione facilitata: Scambio dei cloruri o Scambio Cl - /HCO - 3 Cl - HCO3
Riassorbimento tubulare
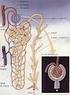 Riassorbimento tubulare Riassorbimento Secrezione Qtr = Qf- Qe Qts = Qe Qf Qtr = VFG*P UV Qts = UV VFG*P Le urine si formano mediante tre processi: Filtrazione glomerulare Riassorbimento di acqua e soluti
Riassorbimento tubulare Riassorbimento Secrezione Qtr = Qf- Qe Qts = Qe Qf Qtr = VFG*P UV Qts = UV VFG*P Le urine si formano mediante tre processi: Filtrazione glomerulare Riassorbimento di acqua e soluti
Corso di Laboratorio Integrato di Chimica Generale BIOTEC-2011 Esercizi Svolti su Equilibri acido-base
 Corso di Laboratorio Integrato di Chimica Generale BIOTEC2011 Esercizi Svolti su Equilibri acidobase 1. Quanto vale il ph di una soluzione 0.1 M di CO 2 se si ritiene che essa non esiste più come tale
Corso di Laboratorio Integrato di Chimica Generale BIOTEC2011 Esercizi Svolti su Equilibri acidobase 1. Quanto vale il ph di una soluzione 0.1 M di CO 2 se si ritiene che essa non esiste più come tale
equilibrio acido base
 Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Presentazione della collana (Ivo Casagranda)... Prefazione... Hanno collaborato...
 pag. Presentazione della collana (Ivo Casagranda).................. Prefazione............................................ Hanno collaborato....................................... XVII XIX XXI Capitolo
pag. Presentazione della collana (Ivo Casagranda).................. Prefazione............................................ Hanno collaborato....................................... XVII XIX XXI Capitolo
Teoria di Lewis. Un acido di Lewis è una specie chimica che può formare un legame covalente accettando una coppia di elettroni da un altra specie.
 Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
