Gas ideali o perfetti
|
|
|
- Geronimo Santini
- 5 anni fa
- Visualizzazioni
Transcript
1 Gas deal o perfett le partcelle del gas soo amate da moto peree ed occupao omogeeamete tutto lo spazo a dsposzoe; l movmeto delle partcelle è regolato dalle legg del caso le partcelle hao u volume propro trascurable rspetto al volume a dsposzoe del gas (partcelle putform) fra le partcelle o esstoo terazo gl urt soo completamete elastc Codzo d lquefazoe alta pressoe bassa temperatura Stato stadard p atm cost (5 C)
2 La legge d Boyle (soterma) Le legg de gas A temperatura costate l volume occupato da ua determata massa d gas è versamete proporzoale alla pressoe: ( ) cost ra due stat dvers del gas:
3 Gas real Fattore d comprmbltà Z gas reale gas deale R gas reale emperatura d versoe: al d sotto d essa compare u mmo el dagramma Z vs. ( temperatura crtca)
4 a b ( ) cost Legge d Boyle per gas real calcolo del covolume b: Rr r r 4 4 π R π (r) 8 π r 4 er ua partcella: 8 v 4 v b 4 v N A
5 Gas a (ltr atm mol - ) b (ltr mol - ) Elo.4.7 Neo.7.79 Argo.45.9 Krpto Xeo Idrogeo Ossgeo.6.8 Azoto.9.9 Cloro Cloruro d drogeo Moossdo d carboo Adrde carboca Ammoaca Metao.5.478
6 La legge d olta-gay Lussac (socora) Quado ua determata massa d gas vee rscaldata a volume costate, per og aumeto d temperatura d C la pressoe aumeta d 7 rspetto al valore che essa aveva a C: ( t) ( ) α t ( t ) t 7 7 t 7 cost k ra due stat dvers del gas:
7 Rappresetazoe della legge dell socora: -7 t ( C) (K)
8 La legge d Charles (sobara) Quado ua determata massa d gas vee rscaldata a pressoe costate, per og aumeto d temperatura d C l volume aumeta d 7 rspetto al valore che essa aveva a C: ( t) ( ) α t ( t ) 7 t t 7 7 cost k ra due stat dvers del gas:
9 Rappresetazoe della legge dell sobara: -7 t ( C) (K)
10 La temperatura ropretà della matera a cu è dovuta la possbltà de corp d trasferre calore dall uo all altro, medate coduzoe (cotatto dretto) e/o per rraggameto; msura la tedeza del calore a sfuggre da u corpo re prcpal scale termometrche: scala assoluta o termodamca scala Celsus o cetgrada scala Fahrehet ermometr: a) a mercuro: tra e 6 C b) ad alcool, toluee, petao: tra e C c) a gas (He): msurao poch grad assolut d temperatura
11 La legge d Avogadro (8) olum ugual dello stesso gas o d gas dvers, elle stesse codzo d temperatura e d pressoe, cotegoo u ugual umero d partcelle (atom o molecole) permette la msura de pes molecolar delle sostaze allo stato gassoso
12 M N M M N M M M N M N M M M M M Codzo ormal (c..) p atm 7 K ( C) mole d gas deale c.. occupa u volume par a.44 ltr (olume molare stadard)
13 Gas olume molare stadard [cm ] Idrogeo 4 Azoto 4 Ossgeo 9 Metao 9 Ammoaca 9 Adrde carboca 6
14 L equazoe d stato de gas deal t C mole d gas deale Rscaldameto a costate (t) ( αt) t C t Aumeto della pressoe a t costate t t C t α 7 7 t 7 ( t) t
15 Legge d Avogadro k k R R Equazoe d stato de gas deal
16 La costate uversale de gas R Forza Lughezza Lughezza Forza Lughezza Lavoro ( Eerga) mol emperatura mol emperatura mol emperatura valor umerc: a) sfruttado la defzoe d volume molare stadard: atm.44ltr ltr atmosfere R. 8 mol 7.5 K mol K b) el Sstema Iterazoale, base all espereza d orrcell: vuoto h d g R mol 7.5 K h76 cm Hg.76 m 595 kg m 9.86 m s mol 7.5 K.44 Joule 8.4 mol K dove d destà del mercuro (a C) h altezza della coloa d Hg g accelerazoe d gravtà m
17 c) sfruttado la defzoe d calora termochmca: 8.4 cal calora 4.84 J R mol K
18 Gas real: equazoe d va der Waals a b ( ) R a : pressoe tera o d coesoe b : covolume o volume propro delle molecole
19 La legge d Dalto I ua mscela d gas deal la pressoe ale è par alla somma delle presso parzal. er pressoe parzale s tede la pressoe che cascu compoete l mscuglo gassoso esercterebbe se occupasse da solo l tero volume dspoble
20 I geerale, per compoet gassos: pressoe parzale del compoete -esmo della mscela gassosa R R R R ( )... R R... X R... X R X R X R
21 I geerale: X X frazoe molare del compoete -esmo (rapporto tra le mol del compoete e le mol al) X mol d mol al
22 Legge d Amagat Il volume occupato da ua mscela gassosa costtuta da compoet è uguale alla somma de volum che cascu gas occuperebbe elle stesse codzo d pressoe e temperatura: dove X
23 d g La destà assoluta d u gas essedo f(, ) d f(, ) g R R M d g M R
24 La destà relatva d u gas rspetto ad u altro gas d destà relatva del gas rspetto al gas d destà relatva del gas rspetto al gas d d g g d g d d g g g d d g g M R M R d d d M R M R M M
25 M d u mscuglo gassoso M M M M M X M X M...X M X M % volume frazoe molare Esempo: calcolo M medo dell ara N 78% O % CO.% Ar.97% X(N ).78 X(O ). X(CO ). X(Ar).97 M ara
26 I I H O H ½ O Cl 5 Cl Cl La dssocazoe termca de gas α grado d dssocazoe (rapporto tra l umero d molecole che s soo dssocate e l umero d molecole che erao preset prma della dssocazoe) < α < N umero d molecole preset prma della dssocazoe Z umero d partcelle che s formao dalla dssocazoe d molecola d gas αn umero d molecole che s soo dssocate N-αN umero d molecole o dssocate ZαN umero d partcelle (o molecole) prodotte dalla dssocazoe Numero ale d molecole preset a dssocazoe avveuta: N-αN ZαN N [ α (Z-)] α (Z-) bomo d dssocazoe
27 La dssocazoe termca agsce: sul peso molecolare del gas: M a M α (Z -) M a peso molecolare apparete sulla pressoe eserctata dal gas: e [ (Z -)] t α e pressoe effettva sulla destà del gas: dt de α (Z-) d e destà effettva
28 Dstrbuzoe delle veloctà molecolar legge della dstrbuzoe delle veloctà molecolar d Maxwell: dn 4πN m k π e mv k v dv
29 Legge d Graham La veloctà d efflusso d u gas attraverso u foro sottle o ua parete porosa è versamete proporzoale alla radce quadrata del suo peso molecolare. v costate M Cosderado due gas dvers, e, mateut elle stesse codzo d e, s può scrvere che v v t t d d M M
= cost a p costante V 1 /T 1 =V 2 /T 2 LEGGE DI GAY-LUSSAC: Un sistema allo stato gassoso è definito da 4. mmhg (torr), bar.
 GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
GAS IDEALI Un sistema allo stato gassoso è definito da 4 parametri: OLUME () l, m 3 PRESSIONE (p) Pa, atm, mmhg (torr), bar QUANTITA DI SOSTANZA (n) mol TEMPERATURA (T) K Sperimentalmente sono state determinate
Lo stato gassoso gas. Caratteristiche dello stato gassoso. liquido. solido. assenza di volume proprio forma fluida
 Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Lo stato gassoso. L atmosfera terrestre è il sistema gassoso in cui siamo immersi
 Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
Comportamento dei gas da un punto di vista macroscopico
 GAS Può essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
GAS Può essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
Istogrammi e confronto con la distribuzione normale
 Istogramm e cofroto co la dstrbuzoe ormale Suppoamo d effettuare per volte la msurazoe della stessa gradezza elle stesse codzo (es. la massa d u oggetto, la tesoe d ua pla, la lughezza d u oggetto, ecc.):
Istogramm e cofroto co la dstrbuzoe ormale Suppoamo d effettuare per volte la msurazoe della stessa gradezza elle stesse codzo (es. la massa d u oggetto, la tesoe d ua pla, la lughezza d u oggetto, ecc.):
Teoria cinetica dei gas
 Teora cnetca de gas Fsca de gas n Termodnamca Grandezze macroscopche P, V, T tutte conseguenza del moto delle partcelle Pressone: Urt contro paret Volume: Assenza d legam tra le partcelle Temperatura:
Teora cnetca de gas Fsca de gas n Termodnamca Grandezze macroscopche P, V, T tutte conseguenza del moto delle partcelle Pressone: Urt contro paret Volume: Assenza d legam tra le partcelle Temperatura:
Lo stato gassoso. Particelle con volume proprio trascurabile puntiformi
 Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Calcolo della composizione e della temperatura di uscita da un reattore adiabatico di ossidazione parziale di CH 4.
 Dpartmeto d Eerga oltecco d Mlao azza Leoardo da Vc - MILANO Eserctazo del corso FONDAMENTI DI ROCESSI IMICI rof. Gapero Gropp ESERCITAZIONE 6 Calcolo della composzoe e della temperatura d uscta da u reattore
Dpartmeto d Eerga oltecco d Mlao azza Leoardo da Vc - MILANO Eserctazo del corso FONDAMENTI DI ROCESSI IMICI rof. Gapero Gropp ESERCITAZIONE 6 Calcolo della composzoe e della temperatura d uscta da u reattore
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Il prodotto della pressione per il volume di una determinata massa gassosa è direttamente proporzionale alla temperatura assoluta: PV = KT
 ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
GAS IDEALI (o gas perfetti )
 GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STTI DI GGREGZIONE DELL MTERI Lo stato gassoso Classificazioe della materia MTERI Composizioe Struttura roprietà Trasformazioi 3 STTI DI GGREGZIONE SOLIDO (volume e forma propri) LIQUIDO (volume defiito
GLI STTI DI GGREGZIONE DELL MTERI Lo stato gassoso Classificazioe della materia MTERI Composizioe Struttura roprietà Trasformazioi 3 STTI DI GGREGZIONE SOLIDO (volume e forma propri) LIQUIDO (volume defiito
Definizioni. Unità strutturale. Massa dell unità strutturale (M 0.) = 100 a.m.u. Macromolecola o Catena polimerica
 Defzo Utà strutturale (massa o moomero) assa dell utà strutturale (.) a.m.u acromolecola o Catea polmerca grado d polmerzzazoe (DP) massa molecolare x.p. Luda ateral polmerc 6 Defzo Grado d polmerzzazoe
Defzo Utà strutturale (massa o moomero) assa dell utà strutturale (.) a.m.u acromolecola o Catea polmerca grado d polmerzzazoe (DP) massa molecolare x.p. Luda ateral polmerc 6 Defzo Grado d polmerzzazoe
Lo stato gassoso e le sue proprietà
 Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
ATOMI E MOLECOLE. ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche.
 1 ATOMI E MOLECOLE ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche. SIMBOLO ATOMICO= 1 o 2 lettere che identificano elemento A= numero di massa (protoni+neutroni) Z=
1 ATOMI E MOLECOLE ATOMO= unità più piccola di un elemento che ne mantiene le caratteristiche chimiche. SIMBOLO ATOMICO= 1 o 2 lettere che identificano elemento A= numero di massa (protoni+neutroni) Z=
I gas e loro proprietà Cap , 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96
 2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
2016 2017 CCS - Biologia CCS Scienze Geologiche 1 I gas e loro proprietà Cap 11. 1-7, 9-12, 15-24, 27-28, 31-33, 37-40, 52, 93-96 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito.
I gas. Pressione: tendenza del gas ad espandersi. 1 atm = 760 torr (o anche mmhg) = Pa = bar
 I gas eperatura: è la sura della tendenza del calore ad abbandonare un corpo (ovvero è la sura del contenuto calorco d un corpo S hanno tre scale teroetrche: ressone: tendenza del gas ad espanders densonalente
I gas eperatura: è la sura della tendenza del calore ad abbandonare un corpo (ovvero è la sura del contenuto calorco d un corpo S hanno tre scale teroetrche: ressone: tendenza del gas ad espanders densonalente
Un modello per il gas ideale
 Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
P i Pf. = P=P f -P i =0,2 atm. tot = =
 Stato gassoso 1) La camera d aria di uo peumatico viee riempita fio alla pressioe di,5 atmosfere alla temperatura di 5 C; i movimeto, la temperatura ella camera d aria sale fio a 65 C ed il volume aumeta
Stato gassoso 1) La camera d aria di uo peumatico viee riempita fio alla pressioe di,5 atmosfere alla temperatura di 5 C; i movimeto, la temperatura ella camera d aria sale fio a 65 C ed il volume aumeta
Queste proprietà derivano dalla grande distanza che separa le molecole che compongono un gas.
 Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Approfondimenti Lezione 3. Mara Bruzzi
 Approfodmet Lezoe 3 Mara Bruzz APPROFONDIMENTO 1 : I BOSONI Partcelle come le a, foto, meso hao vece fuzo d oda smmetrche y S. Esse o obbedscoo al prcpo d esclusoe d Paul. Tal partcelle soo dette BOSONI.
Approfodmet Lezoe 3 Mara Bruzz APPROFONDIMENTO 1 : I BOSONI Partcelle come le a, foto, meso hao vece fuzo d oda smmetrche y S. Esse o obbedscoo al prcpo d esclusoe d Paul. Tal partcelle soo dette BOSONI.
Comportamento dei gas da un punto di vista macroscopico
 GAS uò essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
GAS uò essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
-GAS IDEALI- Le particelle che costituiscono un gas ideale:
 -GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
-GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
Stati di aggregazione della materia
 Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Il Gas Ideale. Il gas ideale é un'astrazione
 Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
LE MEDIE. Quadratica. Italo Nofroni. Statistica medica. Medie. Le medie vengono classificate in due gruppi
 Le mede Italo Nofro LE MEDIE Statstca medca Le mede (o valor med) soo dc d tedeza cetrale e costtuscoo u modo semplce ed mmedato per stetzzare u solo valore dat eterogee raccolt el collettvo oggetto d
Le mede Italo Nofro LE MEDIE Statstca medca Le mede (o valor med) soo dc d tedeza cetrale e costtuscoo u modo semplce ed mmedato per stetzzare u solo valore dat eterogee raccolt el collettvo oggetto d
STATO GASSOSO. parte I a. - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio
 STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
STATO GASSOSO parte I a - GAS PERFETTI - GAS REALI Lucidi del Prof. D. Scannicchio GAS PERFETTI molecole puntiformi (volume proprio nullo) urti elastici (stesse particelle prima e dopo l'urto) parametri
Variabilità = Informazione
 Varabltà e formazoe Lo studo d u feomeo ha seso solo se esso s preseta co modaltà/testà varabl da u soggetto all altro. Ad esempo, se dobbamo studare l reddto ua certa regoe è ecessaro osservare utà statstche
Varabltà e formazoe Lo studo d u feomeo ha seso solo se esso s preseta co modaltà/testà varabl da u soggetto all altro. Ad esempo, se dobbamo studare l reddto ua certa regoe è ecessaro osservare utà statstche
approfondimento Fasi e cambiamenti di fase
 approfondimento Fasi e cambiamenti di fase Gas ideali e gas reali Teoria cinetica dei gas e conseguenze Cambiamenti di fase e conservazione della energia Gas ideali e gas reali In un gas ideale: l interazione
approfondimento Fasi e cambiamenti di fase Gas ideali e gas reali Teoria cinetica dei gas e conseguenze Cambiamenti di fase e conservazione della energia Gas ideali e gas reali In un gas ideale: l interazione
LE MEDIE. Le Medie. Medie razionali. Medie di posizione
 LE MEDIE RAZIONALI LE MEDIE Msure stetche trodotte per valutare aspett compless e global d ua dstrbuzoe d u feomeo X medate u solo umero reale costruto modo da dsperdere al mmo le formazo su dat orgar.
LE MEDIE RAZIONALI LE MEDIE Msure stetche trodotte per valutare aspett compless e global d ua dstrbuzoe d u feomeo X medate u solo umero reale costruto modo da dsperdere al mmo le formazo su dat orgar.
Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1
 I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
I gas Capitolo 5 Elementi che esistono come gas a 25 0 C and 1 atmosfera 5.1 Tabella 5.1 Alcune sostanze che si trovano allo stato gassoso a 1 atm e 25 C Elementi H 2 (idrogeno molecolare) N 2 (azoto molecolare)
Come descrivere fisicamente con facilità questi eventi?
 Come descrvere scamete co acltà quest evet? Quattà d moto Osservazoe: Tato maggore è la massa d u corpo, tato pù è dcle ermarlo ( a partà d veloctà) Data ua partcella d massa m e veloctà v s desce quattà
Come descrvere scamete co acltà quest evet? Quattà d moto Osservazoe: Tato maggore è la massa d u corpo, tato pù è dcle ermarlo ( a partà d veloctà) Data ua partcella d massa m e veloctà v s desce quattà
Stati di aggregazione della materia. dal microscopico al macroscopico: struttura. interazioni GASSOSO. proprietà SOLIDO LIQUIDO
 Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
Stati di aggregazione della materia GASSOSO dal microscopico al macroscopico: struttura interazioni proprietà SOLIDO LIQUIDO Lo stato gassoso È uno dei tre stati di aggregazione della materia, caratterizzato
TERMODINAMICA stato gassoso. TERMODINAMICA stato gassoso. Elio GIROLETTI - Università degli Studi di Pavia, Dip. Fisica nucleare e teorica
 UNIERSITÀ DEGLI STUDI DI PAIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 038298.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti TERMODINAMICA stato gassoso FISICA
UNIERSITÀ DEGLI STUDI DI PAIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 038298.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti TERMODINAMICA stato gassoso FISICA
Teoria dei Fenomeni Aleatori AA 2012/13
 La Legge de Grad Numer Cosderata ua sere d prove rpetute co p par alla probabltà d successo ua sgola prova, l rapporto tra l umero d success K ed l umero d prove tede a p quado tede ad fto: K P p ε per
La Legge de Grad Numer Cosderata ua sere d prove rpetute co p par alla probabltà d successo ua sgola prova, l rapporto tra l umero d success K ed l umero d prove tede a p quado tede ad fto: K P p ε per
1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5.
 Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Lezione 4. Metodi statistici per il miglioramento della Qualità
 Tecologe Iormatche per la Qualtà Lezoe 4 Metod statstc per l mglorameto della Qualtà Msure d Tedeza Cetrale Ultmo aggorameto: 30 Settembre 2003 Il materale ddattco potrebbe coteere error: la segalazoe
Tecologe Iormatche per la Qualtà Lezoe 4 Metod statstc per l mglorameto della Qualtà Msure d Tedeza Cetrale Ultmo aggorameto: 30 Settembre 2003 Il materale ddattco potrebbe coteere error: la segalazoe
Gli indici sintetici Forma. Un caso studio. Gli indici sintetici. Qualche considerazione. Qualche considerazione. Tendenza centrale Forma
 Uverstà d Macerata Dpartmeto d Sceze Poltche, della Comucazoe e delle Relaz. Iterazoal Gl dc d varabltà Crsta Davo Gl dc stetc Qualche cosderazoe Tedeza cetrale Varabltà La scelta dell dce d tedeza cetrale/poszoe
Uverstà d Macerata Dpartmeto d Sceze Poltche, della Comucazoe e delle Relaz. Iterazoal Gl dc d varabltà Crsta Davo Gl dc stetc Qualche cosderazoe Tedeza cetrale Varabltà La scelta dell dce d tedeza cetrale/poszoe
1atm = 760 torr (o anche mmhg) = 101325 Pa = 1.01325 bar
 ressone: tendenza del gas ad espanders densonalente è Forza superce ewton L'untà d sura usata n pratca è l'atosera (at) a (ascal) at 760 torr (o anche Hg) 05 a.05 bar olue: sura d una porzone d spazo densonalente
ressone: tendenza del gas ad espanders densonalente è Forza superce ewton L'untà d sura usata n pratca è l'atosera (at) a (ascal) at 760 torr (o anche Hg) 05 a.05 bar olue: sura d una porzone d spazo densonalente
Prova parziale di Fisica Generale L-B e di Elementi di Fisica L-B. Corsidilaureainingegneriacivileedenergetica. Prof. D. Galli. 25 maggio 2002 (1)
 Prova parzale d Fsca Generale L-B e d Element d Fsca L-B Corsdlaureanngegneracvleedenergetca Prof. D. Gall 5 maggo 00 (). Traccare nel dagramma d Clapeyron l soterma d un gas perfetto. Traccare nel dagramma
Prova parzale d Fsca Generale L-B e d Element d Fsca L-B Corsdlaureanngegneracvleedenergetca Prof. D. Gall 5 maggo 00 (). Traccare nel dagramma d Clapeyron l soterma d un gas perfetto. Traccare nel dagramma
L equilibrio dei gas
 L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
Leggi dei gas Equazione di stato dei gas perfetti
 Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
dei quali si conoscono solo la media x e la deviazione standard σ e dato un valore reale positivo K, possiamo affermare che:
 Eserctazoe VI: Il teorema d Chebyshev Eserczo La statura meda d u gruppo d dvdu è par a 73,78cm e la devazoe stadard a 3,6. Qual è la frequeza relatva delle persoe che hao ua statura superore o ferore
Eserctazoe VI: Il teorema d Chebyshev Eserczo La statura meda d u gruppo d dvdu è par a 73,78cm e la devazoe stadard a 3,6. Qual è la frequeza relatva delle persoe che hao ua statura superore o ferore
Leggi ricavate da osservazioni sperimentali : mantenendo costante due dei 4 parametri, come variano gli altri due?
 Le leggi dei gas Lo stato gassoso è caratterizzato da mancanza di forma e volume propri, e dalla tendenza a occupare tutto il volume disponibile. Lo stato di un gas dipende da 4 parametri: Volume (V) Pressione
Le leggi dei gas Lo stato gassoso è caratterizzato da mancanza di forma e volume propri, e dalla tendenza a occupare tutto il volume disponibile. Lo stato di un gas dipende da 4 parametri: Volume (V) Pressione
Dilatazione termica di solidi e liquidi:
 Dlatazone termca d sold e lqud: temperatura aumenta corp s dlatano; es.: bnaro de tren Dlatazone lneare: sbarra spazo tra d loro L L 0 α pù e lunga, pù s dlata coeffcente d dlatazone lneare es: α Fe 12
Dlatazone termca d sold e lqud: temperatura aumenta corp s dlatano; es.: bnaro de tren Dlatazone lneare: sbarra spazo tra d loro L L 0 α pù e lunga, pù s dlata coeffcente d dlatazone lneare es: α Fe 12
0 00 moli NaCl 0 50 moli NaCl 0 00 M NaCl 250 moli NaCl moli NaCl ml 625 ml
 ESERCIAZIONI Si ha bisogo di 0.50 moli di NaCl e tutto quello di cui si dispoe è di ua soluzioe «0.400 M di NaCl». Quale volume (i ml) di questa soluzioe si dovrà usare? M M 0.400M NaCl 0.400moli NaCl.00l
ESERCIAZIONI Si ha bisogo di 0.50 moli di NaCl e tutto quello di cui si dispoe è di ua soluzioe «0.400 M di NaCl». Quale volume (i ml) di questa soluzioe si dovrà usare? M M 0.400M NaCl 0.400moli NaCl.00l
SISTEMA TERMODINAMICO STATO TERMODINAMICO
 SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
Università Politecnica delle Marche, Facoltà di Agraria. C.d.L. Scienze Forestali e Ambientali, A.A. 2010/2011, Fisica. Diagramma di fase:
 Dagramma d fase: Cambament d stato dell acqua: Spazo tra bnar de tren - per far s che la la dlatazone ndotta dalle temperature estve possa avvenre lungo l'asse del bnaro stesso Dlatazone termca d sold
Dagramma d fase: Cambament d stato dell acqua: Spazo tra bnar de tren - per far s che la la dlatazone ndotta dalle temperature estve possa avvenre lungo l'asse del bnaro stesso Dlatazone termca d sold
CAPITOLO 2: PRIMO PRINCIPIO
 Introduzone alla ermodnamca Esercz svolt CAIOLO : RIMO RINCIIO Eserczo n 7 Una certa quanttà d Hg a = atm e alla temperatura = 0 C è mantenuta a = costante Quale dventa la se s porta la temperatura a =
Introduzone alla ermodnamca Esercz svolt CAIOLO : RIMO RINCIIO Eserczo n 7 Una certa quanttà d Hg a = atm e alla temperatura = 0 C è mantenuta a = costante Quale dventa la se s porta la temperatura a =
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDI NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
LE LEGGI DEI GAS. Prof. Michele Barcellona
 LE LEGGI DEI GAS Prof. Michele Barcellona STATO DI UN GAS Lo stato di un gas dipende dalle seguenti grandezze: Massa (in moli) Volume V Pressione P Temperatura T LE TRASFORMAZIONI DI UN GAS La modifica
LE LEGGI DEI GAS Prof. Michele Barcellona STATO DI UN GAS Lo stato di un gas dipende dalle seguenti grandezze: Massa (in moli) Volume V Pressione P Temperatura T LE TRASFORMAZIONI DI UN GAS La modifica
UNITA DI MISURA. Le unità di misura sono molto importanti
 Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
Modulo di Fisica Tecnica. Differenze finite per problemi di conduzione in regime instazionario
 Dpartmeto d Meccaca, Strutture, Ambete e Terrtoro UNIVERSITÀ DEGLI STUDI DI CASSINO Laurea Specalstca Igegera Meccaca: Modulo d Fsca Tecca Lezoe d: Dffereze fte per problem d coduzoe regme stazoaro /20
Dpartmeto d Meccaca, Strutture, Ambete e Terrtoro UNIVERSITÀ DEGLI STUDI DI CASSINO Laurea Specalstca Igegera Meccaca: Modulo d Fsca Tecca Lezoe d: Dffereze fte per problem d coduzoe regme stazoaro /20
P T. 273 x. x
 Ua certa quatità di idrogeo viee posta i ua camera di platio a volume costate. Quado la camera viee immersa i u bago di ghiaccio che sta fodedo, la pressioe assoluta del gas è di 000 mm di mercurio. (a)
Ua certa quatità di idrogeo viee posta i ua camera di platio a volume costate. Quado la camera viee immersa i u bago di ghiaccio che sta fodedo, la pressioe assoluta del gas è di 000 mm di mercurio. (a)
FISICA per SCIENZE BIOLOGICHE, A.A. 2005/2006 Prova scritta del 21 Giugno 2006
 FISICA per SCIENZE BIOLOGICHE, A.A. 5/6 Prova scrtta del Gugno 6 ) Un corpo d massa m = 5 g scvola lungo un pano nclnato lsco d altezza h = m e nclnazone θ=3 rspetto all orzzontale. Il corpo parte da ermo
FISICA per SCIENZE BIOLOGICHE, A.A. 5/6 Prova scrtta del Gugno 6 ) Un corpo d massa m = 5 g scvola lungo un pano nclnato lsco d altezza h = m e nclnazone θ=3 rspetto all orzzontale. Il corpo parte da ermo
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
Diagramma di stato di H 2 O
 Lezione 13 1. Pressione e temperatura 2. Leggi dei gas 3. Teoria cinetica ei gas 4. Gas ideali e gas reali 5. Miscele gassose: legge di Dalton 6. Frazioni molari Diagramma di stato di H 2 O Diagrammi di
Lezione 13 1. Pressione e temperatura 2. Leggi dei gas 3. Teoria cinetica ei gas 4. Gas ideali e gas reali 5. Miscele gassose: legge di Dalton 6. Frazioni molari Diagramma di stato di H 2 O Diagrammi di
CORSO DI STATISTICA I (Prof.ssa S. Terzi)
 CORSO DI STATISTICA I (Prof.ssa S. Terz) 1 STUDIO DELLE DISTRIBUZIONI SEMPLICI Eserctazoe 2 2.1 Da u dage svolta su u campoe d lavorator dpedet co doppo lavoro è stata rlevata la dstrbuzoe coguta del reddto
CORSO DI STATISTICA I (Prof.ssa S. Terz) 1 STUDIO DELLE DISTRIBUZIONI SEMPLICI Eserctazoe 2 2.1 Da u dage svolta su u campoe d lavorator dpedet co doppo lavoro è stata rlevata la dstrbuzoe coguta del reddto
Legge di stato dei gas ideali
 Legge di stato dei gas ideali Le leggi di Boyle e Charles/Gay Lussac possono essere riunite, insieme al principio di Avogadro, in un'unica equazione che correla fra loro P, V, T e numero di moli di un
Legge di stato dei gas ideali Le leggi di Boyle e Charles/Gay Lussac possono essere riunite, insieme al principio di Avogadro, in un'unica equazione che correla fra loro P, V, T e numero di moli di un
Facoltà di Economia - STATISTICA - Corso di Recupero a.a Prof.ssa G. Balsamo CONCETTI di BASE Carattere X [o A ] i = 1
![Facoltà di Economia - STATISTICA - Corso di Recupero a.a Prof.ssa G. Balsamo CONCETTI di BASE Carattere X [o A ] i = 1 Facoltà di Economia - STATISTICA - Corso di Recupero a.a Prof.ssa G. Balsamo CONCETTI di BASE Carattere X [o A ] i = 1](/thumbs/74/71433944.jpg) Facoltà d Ecooma - STATISTICA - Corso d Recupero a.a. 2012-13 Prof.ssa G. Balsamo CONCETTI d BASE Carattere X [o A ] caratterstca quattatva [o qualtatva] rappresetatva d u feomeo sottoposto ad dage Popolazoe
Facoltà d Ecooma - STATISTICA - Corso d Recupero a.a. 2012-13 Prof.ssa G. Balsamo CONCETTI d BASE Carattere X [o A ] caratterstca quattatva [o qualtatva] rappresetatva d u feomeo sottoposto ad dage Popolazoe
Gli indici sintetici Forma. Gli indici sintetici. Gli indici sintetici. Qualche considerazione. Qualche considerazione. Tendenza centrale Forma
 Uverstà d Macerata Facoltà d Sceze Poltche - Ao accademco 01-013013 Gl dc d varabltà Crsta Davo Gl dc stetc Qualche cosderazoe Tedeza cetrale Varabltà La scelta dell dce d tedeza cetrale/poszoe dpede dal
Uverstà d Macerata Facoltà d Sceze Poltche - Ao accademco 01-013013 Gl dc d varabltà Crsta Davo Gl dc stetc Qualche cosderazoe Tedeza cetrale Varabltà La scelta dell dce d tedeza cetrale/poszoe dpede dal
Statistica descrittiva per l Estimo
 Statstca descrttva per l Estmo Paolo Rosato Dpartmeto d Igegera Cvle e Archtettura Pazzale Europa 1-34127 Treste. Itala Tel: +39-040-5583569. Fax: +39-040-55835 80 E-mal: paolo.rosato@da.uts.t 1 A cosa
Statstca descrttva per l Estmo Paolo Rosato Dpartmeto d Igegera Cvle e Archtettura Pazzale Europa 1-34127 Treste. Itala Tel: +39-040-5583569. Fax: +39-040-55835 80 E-mal: paolo.rosato@da.uts.t 1 A cosa
Teoria dei Fenomeni Aleatori AA 2012/13
 La Legge de Grad Numer Cosderata ua sere d prove rpetute co p par alla probabltà d successo ua sgola prova, l rapporto tra l umero d success K ed l umero d prove tede a p quado tede ad fto: K P p per co
La Legge de Grad Numer Cosderata ua sere d prove rpetute co p par alla probabltà d successo ua sgola prova, l rapporto tra l umero d success K ed l umero d prove tede a p quado tede ad fto: K P p per co
( ) 2 i 1 X. n(n + 1) a) si determini se sono corretti; b) per quelli non corretti, si calcoli la distorsione d;
 ESERCIZIO 5. Sa (X, X,, X ) u campoe casuale geerato da ua v.c. X f(x; θ) per la quale è oto che E(X) θ e Var(X). S cosdero 3 stmator d θ: X ; X ; ( ) X 3 a) s determ se soo corrett; b) per quell o corrett,
ESERCIZIO 5. Sa (X, X,, X ) u campoe casuale geerato da ua v.c. X f(x; θ) per la quale è oto che E(X) θ e Var(X). S cosdero 3 stmator d θ: X ; X ; ( ) X 3 a) s determ se soo corrett; b) per quell o corrett,
LE MEDIE. Quadratica. Italo Nofroni. Statistica medica. Medie. Le medie vengono classificate in
 Le mede Italo Nofro LE MEDIE Le mede (o valor med) soo dc d tedeza cetrale e costtuscoo u modo semplce ed mmedato per stetzzare u solo valore dat eterogee raccolt u collettvo Statstca medca Le mede Le
Le mede Italo Nofro LE MEDIE Le mede (o valor med) soo dc d tedeza cetrale e costtuscoo u modo semplce ed mmedato per stetzzare u solo valore dat eterogee raccolt u collettvo Statstca medca Le mede Le
Gas. Vapore. Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente. microscopico MACROSCOPICO
 Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Stati di aggregazione della materia
 SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
SOLIDO: Forma e volume propri. Stati di aggregazione della materia LIQUIDO: Forma del recipiente in cui è contenuto, ma volume proprio. GASSOSO: Forma e volume del recipiente in cui è contenuto. Parametri
Esercitazione 6 del corso di Statistica (parte 1)
 Eserctazoe del corso d Statstca parte Dott.ssa aola Costat 8 Marzo 0 Eserczo S ha motvo d rteere che u uovo farmaco A abba la propretà d abbassare l lvello d glcema el sague. I cascuo de pazet dabetc osservat,
Eserctazoe del corso d Statstca parte Dott.ssa aola Costat 8 Marzo 0 Eserczo S ha motvo d rteere che u uovo farmaco A abba la propretà d abbassare l lvello d glcema el sague. I cascuo de pazet dabetc osservat,
Gas ideale (perfetto):
 C.d.L. Scenze e ecnologe grare,.. 2015/2016, Fsca Gas deale (perfetto): non esste n realtà drogeno e elo assomglano d pù a un gas deale - le molecole sono puntform; - nteragscono tra loro e con le paret
C.d.L. Scenze e ecnologe grare,.. 2015/2016, Fsca Gas deale (perfetto): non esste n realtà drogeno e elo assomglano d pù a un gas deale - le molecole sono puntform; - nteragscono tra loro e con le paret
Lezione 4. La Variabilità. Lezione 4 1
 Lezoe 4 La Varabltà Lezoe 4 1 Defzoe U valore medo, comuque calcolato, o è suffcete a rappresetare l seme delle osservazo effettuate (o l seme de valor assut dalla varable statstca); è ecessaro qud affacare
Lezoe 4 La Varabltà Lezoe 4 1 Defzoe U valore medo, comuque calcolato, o è suffcete a rappresetare l seme delle osservazo effettuate (o l seme de valor assut dalla varable statstca); è ecessaro qud affacare
La media aritmetica. Le medie. Esempio. Esempio. Media aritmetica Mediana. Medie analitiche Medie di posizione. x 1
 Le mede Mede: permettoo d stetzzare ua dstrbuzoe sulla base d u solo valore. Possoo essere classcate : Mede aaltche: calcolate tramte operazo algebrche su valor del carattere solo per caratter quattatv
Le mede Mede: permettoo d stetzzare ua dstrbuzoe sulla base d u solo valore. Possoo essere classcate : Mede aaltche: calcolate tramte operazo algebrche su valor del carattere solo per caratter quattatv
STATI DI AGGREGAZIONE
 STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
STATI DI AGGREGAZIONE SOLIDO HA FORMA E VOLUME PROPRIO LIQUIDO NON HA FORMA PROPRIA HA VOLUME PROPRIO GAS NON HA NE FORMA NE VOLUME PROPRI FORZE INTERMOLECOLARI Solidi > liquidi >> gas 0 Gas reali> gas
Gas Ideale: Legge di Charles. V t =V 0 (1+αT)
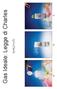 Gas Ideale: Legge di Charles V t =V 0 (1+αT) Gas Ideale: Legge di Charles Repeating the experiment with different gases or different starting V, we can observe different linear curves, but the intercept
Gas Ideale: Legge di Charles V t =V 0 (1+αT) Gas Ideale: Legge di Charles Repeating the experiment with different gases or different starting V, we can observe different linear curves, but the intercept
LEZIONI DI STATISTICA MEDICA
 LEZIONI DI STATISTICA MEDICA A.A. 00/0 - Idc d dspersoe Sezoe d Epdemologa & Statstca Medca Uverstà degl Stud d Veroa La dspersoe o varabltà è la secoda mportate caratterstca d ua dstrbuzoe d dat. Essa
LEZIONI DI STATISTICA MEDICA A.A. 00/0 - Idc d dspersoe Sezoe d Epdemologa & Statstca Medca Uverstà degl Stud d Veroa La dspersoe o varabltà è la secoda mportate caratterstca d ua dstrbuzoe d dat. Essa
CORSO DI LAUREA IN SCIENZE BIOLOGICHE Appello di FISICA, 22 febbraio 2011
 CORSO DI LAUREA IN SCIENZE BIOLOGICHE Appello d FISICA, febbrao 11 1) Un autocarro con massa a peno carco par a M = 1.1 1 4 kg percorre con veloctà costante v = 7 km/h, un tratto stradale rettlneo. A causa
CORSO DI LAUREA IN SCIENZE BIOLOGICHE Appello d FISICA, febbrao 11 1) Un autocarro con massa a peno carco par a M = 1.1 1 4 kg percorre con veloctà costante v = 7 km/h, un tratto stradale rettlneo. A causa
Stati di aggregazione della materia. GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti
 9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
Controlli Automatici A
 Cotroll Automatc A Cors d laurea treal Igegera Elettroca, Iformatca, Telecomucazo a.a. 200/2002 Docete: Prof. Aurelo Pazz Emal: aurelo@ce.upr.t http://www.ce.upr.t/people/pazz/ Cotroll Automatc A Prof.
Cotroll Automatc A Cors d laurea treal Igegera Elettroca, Iformatca, Telecomucazo a.a. 200/2002 Docete: Prof. Aurelo Pazz Emal: aurelo@ce.upr.t http://www.ce.upr.t/people/pazz/ Cotroll Automatc A Prof.
Sistemi Gassosi. GAS = specie che occupa tutto lo spazio disponibile. VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 )
 Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
Sistemi Gassosi GAS = specie che occupa tutto lo spazio disponibile VOLUME = spazio occupato si misura in: m 3, L (1L = 1dm 3 ) PRESSIONE = forza per unità di superficie Unità di misura: Forza Newton (N)
Mole e Numero di Avogadro
 Mole e Numero di Avogadro La mole È ua uatità i grammi di ua sostaza che cotiee u umero preciso e be determiato di particelle (atomi o molecole) Numero di Avogadro Ua mole di ua sostaza cotiee u umero
Mole e Numero di Avogadro La mole È ua uatità i grammi di ua sostaza che cotiee u umero preciso e be determiato di particelle (atomi o molecole) Numero di Avogadro Ua mole di ua sostaza cotiee u umero
Quale retta? La retta migliore è quella che più si avvicina all insieme dei 115
 Quale retta? Quale retta? Questa? Oppure questa? Questa certamete o! 0 1 0 1 La retta mglore è quella che pù s avvca all seme de 115 put corrspodet alle coppe d valor (x, y ). Per la stma de parametr s
Quale retta? Quale retta? Questa? Oppure questa? Questa certamete o! 0 1 0 1 La retta mglore è quella che pù s avvca all seme de 115 put corrspodet alle coppe d valor (x, y ). Per la stma de parametr s
TEORIA CINETICA DEI GAS IDEALI
 TEORIA CINETICA DEI GAS IDEALI T R AT TO DA: I P ro b l e m i D e l l a F i s i c a - C u t n e l l, J o h n s o n, Yo u n g, S t a d l e r Z a n i c h e l l i e d i t o r e La F i s i c a di A m a l d
TEORIA CINETICA DEI GAS IDEALI T R AT TO DA: I P ro b l e m i D e l l a F i s i c a - C u t n e l l, J o h n s o n, Yo u n g, S t a d l e r Z a n i c h e l l i e d i t o r e La F i s i c a di A m a l d
Il lavoro in termodinamica
 Il lavoro n termodnamca Il lavoro esterno: W est =-F e Dl (-: orza e spos. dscord) Il lavoro atto dal sstema sarà: W=-W est = F e Dl La orza eserctata dall ambente può essere dervata dalla pressone esterna:
Il lavoro n termodnamca Il lavoro esterno: W est =-F e Dl (-: orza e spos. dscord) Il lavoro atto dal sstema sarà: W=-W est = F e Dl La orza eserctata dall ambente può essere dervata dalla pressone esterna:
Aritmetica 2016/2017 Esercizi svolti in classe Quarta lezione
 Artmetca 06/07 Esercz svolt classe Quarta lezoe Rcorreze o lear Sa a c a cq ua rcorreza dove {c }, c C e c 0. Sa P C[λ] l polomo caratterstco della rcorreza. Allora ua soluzoe partcolare della rcorreza
Artmetca 06/07 Esercz svolt classe Quarta lezoe Rcorreze o lear Sa a c a cq ua rcorreza dove {c }, c C e c 0. Sa P C[λ] l polomo caratterstco della rcorreza. Allora ua soluzoe partcolare della rcorreza
Funzioni di più variabili Massimi e Minimi una funzione definita in un insieme E. Un punto ( x0, y0)
 Massm e Mm Fuzo d pù varabl Massm e Mm Dezoe: Sa z = (, ) ua uzoe deta u seme E U puto (, E s dce puto d massmo (rsp mmo) relatvo per (, ) se esste δ > tale che ((, ) B((, ), δ ) E (, ) (, ) (rsp (, )
Massm e Mm Fuzo d pù varabl Massm e Mm Dezoe: Sa z = (, ) ua uzoe deta u seme E U puto (, E s dce puto d massmo (rsp mmo) relatvo per (, ) se esste δ > tale che ((, ) B((, ), δ ) E (, ) (, ) (rsp (, )
La media aritmetica. La sua individuazione si basa sulla logica della trasferibilità di un carattere. Se la funzione f( ) corrisponde alla somma:
 La meda artmetca La sua dvduazoe s basa sulla logca della trasferbltà d u carattere. ( ) = ( µ µ ) f,, f,, volte Se la fuzoe f( ) corrspode alla somma: + + + = µ + µ + + µ volte + + + = µ µ X= = La meda
La meda artmetca La sua dvduazoe s basa sulla logca della trasferbltà d u carattere. ( ) = ( µ µ ) f,, f,, volte Se la fuzoe f( ) corrspode alla somma: + + + = µ + µ + + µ volte + + + = µ µ X= = La meda
Esercizi sull incertezza di misura
 Esercz sull certezza d sura Eserczo 1 S vuole deterare l certezza tpo da attrbure al rsultato d ua surazoe d ressteza effettuata co etodo e struetazoe d certezza trascurable rspetto a quella legata alle
Esercz sull certezza d sura Eserczo 1 S vuole deterare l certezza tpo da attrbure al rsultato d ua surazoe d ressteza effettuata co etodo e struetazoe d certezza trascurable rspetto a quella legata alle
Energia e Lavoro. In pratica, si determina la dipendenza dallo spazio invece che dal tempo
 Energa e Lavoro Fnora abbamo descrtto l moto de corp (puntform) usando le legg d Newton, tramte le forze; abbamo scrtto l equazone del moto, determnato spostamento e veloctà n funzone del tempo. E possble
Energa e Lavoro Fnora abbamo descrtto l moto de corp (puntform) usando le legg d Newton, tramte le forze; abbamo scrtto l equazone del moto, determnato spostamento e veloctà n funzone del tempo. E possble
8) Soluzioni diluite
 8) Soluzo dlute Per solut sesso s usao le cocetrazo olar (olartà) c [ ]: (utà d sura: ol/ltro) V soluzoe Però le olartà o soo costat e sste chus a ressoe ssata: V soluzoe dede dalla teeratura! Per ovvare
8) Soluzo dlute Per solut sesso s usao le cocetrazo olar (olartà) c [ ]: (utà d sura: ol/ltro) V soluzoe Però le olartà o soo costat e sste chus a ressoe ssata: V soluzoe dede dalla teeratura! Per ovvare
Capitolo 2 Errori di misura: definizioni e trattamento
 Captolo Error d msura: )Geeraltà defzo e trattameto I cocett d meda, varaza e devazoe stadard s utlzzao ormalmete per otteere formazo sulla botà d ua msura. I geerale, s assume come msura m della gradezza
Captolo Error d msura: )Geeraltà defzo e trattameto I cocett d meda, varaza e devazoe stadard s utlzzao ormalmete per otteere formazo sulla botà d ua msura. I geerale, s assume come msura m della gradezza
LA MATERIA ED I SUOI STATI
 LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
La teoria cinetica dei gas
 La teora cnetca de gas Gas: un numero grandssmo gandssmodmolecole n moto caotco. Interazone tra molecole solo n caso d urto. Calcolando la pressone come dovuta all urto d tutte le molecole con le paret
La teora cnetca de gas Gas: un numero grandssmo gandssmodmolecole n moto caotco. Interazone tra molecole solo n caso d urto. Calcolando la pressone come dovuta all urto d tutte le molecole con le paret
Indipendenza in distribuzione
 Marlea Pllat - Semar d Statstca (SVIC) "Lo studo delle relazo tra due caratter" Aals delle relazo tra due caratter Dpedeza dstrbuzoe s basa sul cofroto delle dstrbuzo codzoate Dpedeza meda s basa sul cofroto
Marlea Pllat - Semar d Statstca (SVIC) "Lo studo delle relazo tra due caratter" Aals delle relazo tra due caratter Dpedeza dstrbuzoe s basa sul cofroto delle dstrbuzo codzoate Dpedeza meda s basa sul cofroto
