Besponsa: descrizione e gestione di specifiche reazioni avverse
|
|
|
- Benedetto Tommasi
- 5 anni fa
- Visualizzazioni
Transcript
1 Besponsa: descrizione e gestione di specifiche reazioni avverse
2 Premesse/1 Inotuzumab Ozogamicin (InO) nella Leucemia Linfoblastica Acuta (LLA) Recidivata/Refrattaria (R/R) InO è un anticorpo monoclonale anti-cd22 coniugato con la calicheamicina, un potente antibiotico citotossico. I risultati dello studio randomizzato di fase 3 INO-VATE hanno dimostrato la tollerabilità complessiva e l efficacia superiore di InO in confronto alla chemioterapia standard come 1 o 2 trattamento di salvataggio nei pazienti adulti con LLA a cellule B Philadelphia (Ph)-positiva o Ph-negativa recidivata o refrattaria: Nei pazienti con LLA recidivata/refrattaria, l obiettivo primario è quello di indurre una remissione completa per permettere al paziente di accedere ad un trattamento potenzialmente curativo, quale il trapianto allogenico (SCT). Il trattamento con InO in monoterapia nei pazienti adulti con B-LLA recidivata/refrattaria ha indotto tassi di remissione completa significativamente più alti di quelli osservati nel gruppo chemioterapia standard (80,7% vs. 29,4%). Nello studio INO-VATE, il 41% dei pazienti trattati con InO è stato in grado di procedere direttamente a un SCT, rispetto all 11% di quelli riceventi chemioterapia standard, con un tasso di sopravvivenza globale a 2 anni del 23% verso il 10%, rispettivamente. Tuttavia InO è gravato da alcuni eventi avversi Kebriaei P et al. Bone Marrow Transplant 2018;53: Kantarjian HM et al. N Engl J Med 2016;375:740 53
3 Premesse/2 Sicurezza di Inotuzumab Ozogamicin (InO) Nello studio INO-VATE, i più frequenti eventi avversi (AE) associati al trattamento con InO erano rappresentati da citopenie, seguite da nausea, cefalea e piressia. InO (n=139) SC (n=120) All Grade Grade 3 All Grade Grade 3 Ogni AE, n (%) 136 (98) 126 (91) 119 (99) 114 (95) Trombocitopenia 62 (45) 51 (37) 73 (61) 71 (59) Neutropenia 67 (48) 64 (46) 53 (44) 50 (42) Anemia 42 (30) 26 (19) 64 (53) 48 (40) Nausea 44 (32) 3 (2) 56 (47) 0 Piressia 37 (27) 5 (4) 51 (43) 6 (5) Leucopenia 38 (27) 35 (25) 47 (39) 47 (39) Neutropenia febbrile 37 (27) 33 (24) 62 (52) 59 (49) Cefalea 39 (28) 2 (1) 33 (28) 0 á AST 28 (20) 7 (5) 12 (10) 4 (3) á GGT 24 (17) 12 (9) 9 (8) 5 (4) á Bilirubina totale 21 (15) 5 (4) 12 (10) 4 (3) á lipasi 14 (10) 6 (4) 0 0 VOD 15 (11) 13 (9) 1 (1) 1 (1) Fra gli AE seri, la malattia veno-occlusiva (VOD) o sindrome da ostruzione sinusoidale, è risultata più frequente nei pazienti riceventi InO rispetto alla terapia standard (incidenza: 11% verso 1%), in particolare nei pazienti che procedono verso un SCT (10/48 pazienti, 21% dei casi). Kantarjian HM et al. N Engl J Med 2016;375:
4 VOD Overview La VOD è una complicazione epatica del SCT grave e potenzialmente fatale, il cui tasso di mortalità nei casi gravi raggiunge l 84%. La patogenesi della VOD è legata al danno sull endotelio sinusoidale e sugli epatociti causato dai metaboliti tossici generati dai regimi di condizionamento con chemioterapia alchilante ad alte dosi. In aggiunta, è stato postulato un effetto diretto della calicheamicina sulle cellule endoteliali sinusoidali. Criteri EBMT per la diagnosi di VOD VOD Classica Nei primi 21 giorni dopo SCT Bilirubina 2 mg/dl e 2 dei seguenti criteri: epatomegalia dolorosa aumento di peso >5% ascite VOD a esordio tardivo Più di 21 giorni dopo SCT VOD classica oltre il g21 o VOD provata istologicamente o 2 dei seguenti criteri: bilirubina 2 mg/dl epatomegalia dolorosa aumento di peso >5% ascite e evidenza di VOD emodinamica e/o ecografica L aumento di peso da ritenzione renale di acqua e sodio è uno dei primi segni di VOD. Kebriaei P et al. Bone Marrow Transplant 2018;53: Mohty M et al. Bone Marrow Transplant 2016;51:
5 VOD Overview La severità della VOD viene determinata, secondo i criteri dell European Society for Blood and Marrow Transplantation, sulla base del livello di bilirubina e della sua velocità di aumento, della funzionalità epatica, dell aumento di peso e della funzione renale, così come della cinetica di comparsa della VOD stessa. Valutazione della gravità della VOD secondo EBMT Criteri MOD: Disfunzione multi-organo; MOF: Insufficienza multi-organo. Grado della VOD Lieve Moderata Severa Molto severa Tempo dai primi sintomi clinici alla diagnosi di VOD >7 giorni 5-7 giorni 4 giorni Ogni tempo Bilirubina, mg/dl 2 e <3 3 e <5 5 e <8 8 Bilirubina, mmol/l 34 e <51 51 e <85 85 e < Bilirubina, cinetica Raddoppio entro 48 ore Transaminasi 2 x normale >2 e 5 x normale >5 e 8 x normale >8 x normale Aumento di peso <5% 5% e <10% 5% e <10% 10% Funzionalità renale <1,2 x basale 1,2 e <1,5 x basale 1,5 e <2 x basale al trapianto al trapianto al trapianto 2 x basale al trapianto o altri segni di MOD/MOF I pazienti vengono assegnati alla categoria di gravità dove soddisfano almeno 2 criteri. Se un paziente soddisfa 2 criteri in 2 differenti categorie, deve essere classificato nella categoria più grave. Kebriaei P et al. Bone Marrow Transplant 2018;53: Mohty M et al. Bone Marrow Transplant 2016;51:
6 VOD Incidenza di VOD e associazione tra tempo al trapianto e insorgenza di VOD Nell analisi aggiornata dello studio INO-VATE, l incidenza di VOD di ogni grado e 3 è stata maggiore nel gruppo InO (11% e 9%, rispettivamente) rispetto al gruppo terapia standard (entrambe <1%). Dopo un successivo SCT, una VOD è stata riportata: - nell 8% dei pazienti che avevano ricevuto 1 ciclo di InO, - nel 19% dei riceventi 2 cicli di InO, - nel 29% dei casi riceventi >2 cicli di InO. Il tempo medio alla comparsa di VOD era pari a: - 30 giorni (range: ) dopo la 1 dose di InO - a 15 giorni post-sct nei pazienti sottoposti a trapianto. Kebriaei P et al. Bone Marrow Transplant 2018;53: Kantarjian HM et al. Lancet Haematol. 2017;4:e387-e398. Kantarjian HM et al. N Engl J Med 2016;375:740 53
7 VOD Fattori di rischio correlati all utilizzo di Ino Nei seguenti sottogruppi, la frequenza riportata di VOD/SOS post-hsct era 50%: Pazienti che hanno ricevuto un regime di condizionamento HSCT contenente 2 agenti alchilanti; Pazienti di età 65 anni; e Pazienti con bilirubina sierica ULN prima dell HSCT. Deve essere evitato l uso di regimi di condizionamento HSCT contenenti 2 agenti alchilanti. Il rapporto rischio/beneficio deve essere valutato attentamente prima di somministrare BESPONSA a pazienti in cui è probabilmente inevitabile l uso futuro di regimi di condizionamento HSCT contenenti 2 agenti alchilanti. Altri fattori dei pazienti che sembrano essere associati a un aumento del rischio di VOD/SOS dopo il HSCT comprendono: HSCT precedente, età 55 anni, storia di malattia epatica e/o epatite prima del trattamento, terapie di salvataggio in fase avanzata, maggior numero di cicli di trattamento. RCP Besponsa
8 VOD Raccomandazioni per la prevenzione e il monitoraggio della VOD nei pazienti riceventi InO Prevenzione della VOD Evitare i regimi di condizionamento al trapianto SCT con doppio alchilante, tiotepa o entrambi. Usare agenti profilattici (ad es. ursodiolo). Quando possibile, evitare agenti epatotossici (ad es. azoli) in combinazione con la somministrazione di terapia di condizionamento con alchilante ad alte dosi. In pazienti con bilirubina sierica ULN prima del SCT, il SCT dopo il trattamento con Ino può essere effettuato solo dopo attenta considerazione del rapporto rischio/beneficio. Se si procede con il SCT, la presenza di eventuali segni e sintomi di VOD/SOS deve essere monitorata attentamente Nei pazienti che procedono al SCT, limitare il trattamento con InO a 2 cicli; un terzo ciclo potrebbe essere considerato per i pazienti che non raggiungono una CR o una CRi e una negatività della MRD dopo 2 cicli Monitoraggio per la VOD Monitorare giornalmente il peso del paziente per la presenza di ritenzione di liquidi. Prima e dopo ogni dose di InO, monitorare i livelli di ALT, AST, bilirubina totale e fosfatasi alcalina e aggiustare la dose di InO come raccomandato. Monitorare più frequentemente i test di funzionalità epatica (LFT) e cercare segni e sintomi di epatotossicità nei pazienti che sviluppano LFT anormali. Nei pazienti che procedono verso il SCT, monitorare strettamente i LFT durante il primo mese post-sct, poi meno frequentemente sulla base della pratica standard. I pazienti che iniziano un trattamento con InO dovrebbero essere subito valutati per una procedura trapiantologica; se questa viene presa in considerazione, vanno attuate tutte le misure per la prevenzione della VOD. Tutti i pazienti trattati con InO devono essere considerati ad alto rischio di VOD e quindi sottoposti a un monitoraggio attento che permetta una diagnosi e un trattamento precoci. Devono essere monitorati attentamente i segni e sintomi di VOD/SOS in tutti i pazienti, in particolare post-hsct. Kebriaei P et al. Bone Marrow Transplant 2018;53:
9 VOD Raccomandazioni per la gestione della VOD nei pazienti riceventi InO Gestione della VOD La terapia di supporto per il trattamento dei sintomi di VOD è il primo passo nella gestione di questa complicanza. Una particolare attenzione al bilancio idrico è raccomandata in tutti i pazienti, indipendentemente dalla severità della VOD. Può essere usato il trattamento sintomatico con diuretici, ossigeno e emodialisi/emofiltrazione. La paracentesi è raccomandata se l ascite compromette la respirazione. Uno shunt portosistemico intraepatico transgiugulare può essere considerato nei casi severi. I pazienti dovrebbero continuare a ricevere ursodiolo in profilassi. Accanto al trattamento sintomatico, defibrotide è l unico agente approvato per la terapia della VOD con compromissione renale o polmonare (6,25 mg/kg ogni 6 ore per un minimo di 21 giorni e fino a risoluzione dei segni e sintomi di VOD, fino a un massimo di 60 giorni). Devono essere seguite le raccomandazioni per la modifica del dosaggio di InO per le tossicità extra-ematologiche. La gestione della VOD nei pazienti sottoposti a trattamento con InO, così come la diagnosi e il monitoraggio, dovrebbero essere basati sulle raccomandazioni fornite dal documento di posizionamento dell EBMT. Kebriaei P et al. Bone Marrow Transplant 2018;53: Mohty M et al. Bone Marrow Transplant 2016;51:906-12
10 Modifiche del dosaggio di InO Tossicità extra-ematologiche Tossicità VOD/SOS o altra tossicità epatica severa Bilirubina totale >1,5 x ULN e AST/ALT >2,5 ULN Reazione legata all infusione Tossicità extra-ematologiche di grado 2 a (correlata a InO) Modifiche del dosaggio Interrompere definitivamente il trattamento Sospendere la somministrazione fino a recupero della bilirubina totale a valori 1,5 x ULN e AST/ALT fino a 2,5 x ULN prima di ogni dose (tranne che se dovute a sindrome di Gilbert o emolisi). Interrompere definitivamente il trattamento se la bilirubina totale non si riduce fino a valori 1,5 x ULN e AST/ALT fino a 2,5 x ULN. Sospendere l infusione e istituire un appropriato trattamento medico. Sulla base della gravità della reazione associata all infusione, prendere in considerazione l interruzione dell infusione o la somministrazione di steroidi e antistaminici. Per reazioni all infusione gravi o pericolose per la vita, interrompere definitivamente il trattamento. Interrompere il trattamento fino al recupero ad un Grado 1 o ai livelli di Grado pretrattamento prima di ogni dose. La comparsa di VOD o di altra tossicità epatica severa è ragione per l interruzione definitiva del trattamento con InO. Abbreviazioni: ALT = alanina aminotransferasi; AST = aspartato aminotransferasi; ULN = limite superiore della norma; VOD/SOS = malattia veno-occlusiva/sindrome da ostruzione sinusoidale. ( a ) Grado di gravità in base ai National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE) versione 3.0. Kebriaei P et al. Bone Marrow Transplant 2018;53: Besponsa RCP.
11 Modifiche del dosaggio di InO Tossicità ematologiche Criteri Se prima del trattamento con InO i PMN erano 1 x 10 9 /L Se prima del trattamento con InO la conta piastrinica era 50 x 10 9 /L Se prima del trattamento con InO i PMN erano <1 x 10 9 /L e/o la conta piastrinica era <50 x 10 9 /L a Modifiche del dosaggio Se i PMN si riducono, sospendere il prossimo ciclo di trattamento fino a recupero dei PMN 1 x 10 9 /L. Se le Plts si riducono, sospendere il prossimo ciclo di trattamento fino a recupero delle Plts 50 x 10 9 /L. Se i valori di PMN o Plts si riducono, sospendere il prossimo ciclo di trarttamento, fino a che si verifichi almeno 1 delle seguenti condizioni: PMN e Plts recuperano fino a un livello almeno pari a quello basale del ciclo precedente, o PMN recuperano fino a 1 x 10 9 /L e Plts fino a 50 x 10 9 /L, o Malattia stabile o in miglioramento (sulla base della più recente valutazione midollare) e la riduzione di PMN e Plts viene considerata dovuta alla malattia sottostante (non è considerata essere una tossicità correlata a InO). PMN: Polimorfonucleati neutrofili; Plts: Piastrine. ( a ) La conta piastrinica utilizzata per la somministrazione deve essere indipendente dalla trasfusione di sangue La gestione di alcune reazioni avverse associate alla somministrazione di InO può richiedere una sospensione della somministrazione e/o la riduzione della dose oppure l interruzione definitiva del trattamento, secondo quanto indicato nella Scheda Tecnica del farmaco. Kebriaei P et al. Bone Marrow Transplant 2018;53: Besponsa RCP.
12 Modifiche della dosaggio di InO In base alla durata della sospensione della somministrazione per tossicità Durata della sospensione della somministrazione a causa della tossicità Modifica/modifiche della dose < 7 giorni (all interno di un ciclo) Sospendere la dose successiva (far trascorrere almeno 6 giorni tra una dose e l altra). 7 giorni 14 giorni Omettere la dose successiva all interno del ciclo. Una volta raggiunto un recupero adeguato, ridurre la dose totale del 25% per il ciclo successivo. Se è necessaria un ulteriore modifica della dose, ridurre il numero di dosi a 2 per ciclo per i cicli successivi. Se una diminuzione del 25% della dose totale seguita da una diminuzione a 2 dosi per ciclo non è tollerata, interrompere definitivamente il trattamento. > 28 giorni Prendere in considerazione l interruzione permanente di Ino
13 Conclusioni L incidenza di eventi avversi associati con il trattamento con InO è nel complesso simile o più basso delle terapie convenzionali. La maggiore preoccupazione è legata alla più alta frequenza di VOD, come riportato nello studio INO-VATE. I pazienti riceventi InO che vengono successivamente sottoposti a SCT sono ad alto rischio di sviluppare una VOD e dovrebbero quindi essere appropriatamente monitorati e trattati. Complessivamente, il rischio di questi AE clinicamente rilevanti associati a InO può essere ridotto con misure preventive e una diagnosi e un trattamento tempestivi. Kebriaei P et al. Bone Marrow Transplant 2018;53:
14
ACTA BIOMEDICA QUADERNI
 Acta Biomed. - Vol. 89 - Quad. 5 - Novembre 2018 ISSN 0392-4203 ACTA BIOMEDICA QUADERNI Atenei parmensis founded 1887 Official Journal of the Society of Medicine and Natural Sciences of Parma and Centre
Acta Biomed. - Vol. 89 - Quad. 5 - Novembre 2018 ISSN 0392-4203 ACTA BIOMEDICA QUADERNI Atenei parmensis founded 1887 Official Journal of the Society of Medicine and Natural Sciences of Parma and Centre
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
Linee guida per il dosaggio e l infusione Informazioni sulla preparazione e somministrazione di Elaprase
 Linee guida per il dosaggio e l infusione Informazioni sulla preparazione e somministrazione di Elaprase ELAPRASE (idursulfasi) Terapia enzimatica sostitutiva per il trattamento a lungo termine dei pazienti
Linee guida per il dosaggio e l infusione Informazioni sulla preparazione e somministrazione di Elaprase ELAPRASE (idursulfasi) Terapia enzimatica sostitutiva per il trattamento a lungo termine dei pazienti
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI
 ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Da quando è stata concessa l autorizzazione all immissione in commercio di Esmya sono stati riportati quattro casi di gravi lesioni epatiche
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Da quando è stata concessa l autorizzazione all immissione in commercio di Esmya sono stati riportati quattro casi di gravi lesioni epatiche
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 57 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso con esito mortale di insufficienza epatica fulminante in un paziente
Allegato IV Conclusioni scientifiche 57 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso con esito mortale di insufficienza epatica fulminante in un paziente
MIGLIORAMENTO DELLA QUALITA DELL ASSISTENZA E RIDUZIONE DEGLI EFFETTI COLLATERALI: RUOLO DELL INFERMIERE
 MIGLIORAMENTO DELLA QUALITA DELL ASSISTENZA E RIDUZIONE DEGLI EFFETTI COLLATERALI: RUOLO DELL INFERMIERE Inf. Tania Buttiron Webber E.O. Ospedali Galliera, DH Oncologia Medica Genova, 6 aprile 2019 IMMUNOTERAPIA
MIGLIORAMENTO DELLA QUALITA DELL ASSISTENZA E RIDUZIONE DEGLI EFFETTI COLLATERALI: RUOLO DELL INFERMIERE Inf. Tania Buttiron Webber E.O. Ospedali Galliera, DH Oncologia Medica Genova, 6 aprile 2019 IMMUNOTERAPIA
REAZIONI AVVERSE EMATOLOGICHE
 REAZIONI AVVERSE EMATOLOGICHE DISTRIBUZIONE DELLE ADR PER SYSTEM ORGAN CLASSES (SOCs) NEL 2016 OsservatOriO NaziONale sull impiego dei medicinali L uso dei Farmaci in Italia - Rapporto Nazionale 2016
REAZIONI AVVERSE EMATOLOGICHE DISTRIBUZIONE DELLE ADR PER SYSTEM ORGAN CLASSES (SOCs) NEL 2016 OsservatOriO NaziONale sull impiego dei medicinali L uso dei Farmaci in Italia - Rapporto Nazionale 2016
Tossicità Polmonare da Immunoterapia A. Stagno
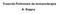 Tossicità Polmonare da Immunoterapia A. Stagno Epidemiologia L incidenza della tossicità polmonare da farmaci anti CTLA4, anti PD-L1 e anti PD-1 si attesta tra il 2,5-3,5% L incidenza è più alta fra i
Tossicità Polmonare da Immunoterapia A. Stagno Epidemiologia L incidenza della tossicità polmonare da farmaci anti CTLA4, anti PD-L1 e anti PD-1 si attesta tra il 2,5-3,5% L incidenza è più alta fra i
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 59 Conclusioni scientifiche Informazioni di base Ponatinib è un inibitore delle tirosin-chinasi (Tyrosine Kinase Inhibitor, TKI), concepito per inibire l attività tirosin-chinasica
Allegato IV Conclusioni scientifiche 59 Conclusioni scientifiche Informazioni di base Ponatinib è un inibitore delle tirosin-chinasi (Tyrosine Kinase Inhibitor, TKI), concepito per inibire l attività tirosin-chinasica
Allegato III. Modifiche ai paragrafi rilevanti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Modifiche ai paragrafi rilevanti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Le sezioni relative delle Caratteristiche del Prodotto e Foglio Illustrativo
Allegato III Modifiche ai paragrafi rilevanti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Le sezioni relative delle Caratteristiche del Prodotto e Foglio Illustrativo
Linfomi di Hodgkin e Linfomi anaplastici sistemici ricaduti e refrattari
 Linfomi di Hodgkin e Linfomi anaplastici sistemici ricaduti e refrattari Meldola 24 Settembre 2016 Sabati Ematologici della Romagna Letizia Gandolfi Istututo di Ematologia e Oncologia L. & A. Seràgnoli
Linfomi di Hodgkin e Linfomi anaplastici sistemici ricaduti e refrattari Meldola 24 Settembre 2016 Sabati Ematologici della Romagna Letizia Gandolfi Istututo di Ematologia e Oncologia L. & A. Seràgnoli
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
Uso di etanolo nell'embolizzazione trans-arteriosa (TAELE) in miscela 1:1 con lipiodol VS TACE nell HCC: Studio di tossicità e sopravvivenza
 S.C. RADIOLOGIA INTERVENTISTICA DIRETTORE PROF. FRANCESCO FIORE Uso di etanolo nell'embolizzazione trans-arteriosa (TAELE) in miscela 1:1 con lipiodol VS TACE nell HCC: Studio di tossicità e sopravvivenza
S.C. RADIOLOGIA INTERVENTISTICA DIRETTORE PROF. FRANCESCO FIORE Uso di etanolo nell'embolizzazione trans-arteriosa (TAELE) in miscela 1:1 con lipiodol VS TACE nell HCC: Studio di tossicità e sopravvivenza
Tossicita nei trattamenti dell Apparato Gastroenterico
 Tossicita nei trattamenti dell Apparato Gastroenterico NAUSEA, VOMITO e TOSSICITA EPATOLOGICA Cenni di patogenesi e strumenti di valutazione F. Cellini Gemelli ART Fondazione Policlinico A. Gemelli Università
Tossicita nei trattamenti dell Apparato Gastroenterico NAUSEA, VOMITO e TOSSICITA EPATOLOGICA Cenni di patogenesi e strumenti di valutazione F. Cellini Gemelli ART Fondazione Policlinico A. Gemelli Università
Oncologia. Moderatore: Gloria Taliani. Tutor: B. Daniele, M. Fasano
 Oncologia Moderatore: Gloria Taliani Tutor: B. Daniele, M. Fasano Marzo 2008 Comparsa di una voluminosa adenopatia in regione ascellare dx in donna ucraina di 52 anni. Anamnesi positiva per exeresi di
Oncologia Moderatore: Gloria Taliani Tutor: B. Daniele, M. Fasano Marzo 2008 Comparsa di una voluminosa adenopatia in regione ascellare dx in donna ucraina di 52 anni. Anamnesi positiva per exeresi di
Allegato II. Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio 6 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio 6 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Le leucemie acute mieloidi La diagnosi
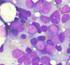 LEUCEMIE MIELOIDI Le leucemie acute mieloidi sono una patologia dell adulto più frequente nell anziano con un età media >60 anni; entrambi i sessi sono colpiti, con una lieve predominanza per quello maschile.
LEUCEMIE MIELOIDI Le leucemie acute mieloidi sono una patologia dell adulto più frequente nell anziano con un età media >60 anni; entrambi i sessi sono colpiti, con una lieve predominanza per quello maschile.
CIRROSI HBV/HCV Perché trattare? Chi trattare?
 Associazione Medici Rhodensi e U.O. Gastroenterologia - Ospedale G. Salvini - Rho ANNUAL MEETING 2008 Gestione del paziente con Epatite HBV e HCV correlata e Steatoepatite non Alcolica CIRROSI HBV/HCV
Associazione Medici Rhodensi e U.O. Gastroenterologia - Ospedale G. Salvini - Rho ANNUAL MEETING 2008 Gestione del paziente con Epatite HBV e HCV correlata e Steatoepatite non Alcolica CIRROSI HBV/HCV
LEUCEMIE MIELOIDI CRONICHE
 LEUCEMIE MIELOIDI CRONICHE La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica relativamente rara (1-2 casi/100.000 abitanti/anno) prevalente nell adulto-anziano. Le cellule leucemiche sono caratterizzate
LEUCEMIE MIELOIDI CRONICHE La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica relativamente rara (1-2 casi/100.000 abitanti/anno) prevalente nell adulto-anziano. Le cellule leucemiche sono caratterizzate
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
Dott.ssa Federica Ferrari. Prof. Domenico Alvaro
 Dott.ssa Federica Ferrari Prof. Domenico Alvaro 1. COLANGITE SCLEROSANTE AUTOIMMUNE 2. VALUTAZIONE DELLA FIBROSI EPATICA COLANGITE SCLEROSANTE AUTOIMMUNE Descrizione dello studio Studio di coorte condotto
Dott.ssa Federica Ferrari Prof. Domenico Alvaro 1. COLANGITE SCLEROSANTE AUTOIMMUNE 2. VALUTAZIONE DELLA FIBROSI EPATICA COLANGITE SCLEROSANTE AUTOIMMUNE Descrizione dello studio Studio di coorte condotto
SINOSSI DEL PROTOCOLLO
 Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
SINTESI DEL PROTOCOLLO
 SINTESI DEL PROTOCOLLO Titolo dello studio Studio di Fase 2, randomizzato, multicentrico, in aperto per valutare l efficacia e la sicurezza di Azacitidina sottocutanea somministrata in combinazione con
SINTESI DEL PROTOCOLLO Titolo dello studio Studio di Fase 2, randomizzato, multicentrico, in aperto per valutare l efficacia e la sicurezza di Azacitidina sottocutanea somministrata in combinazione con
RASSEGNA STAMPA. 07 aprile Sommario: Rassegna Associativa. Rassegna Sangue e Emoderivati
 RASSEGNA STAMPA 07 aprile 2014 Sommario: Rassegna Associativa 2 Rassegna Sangue e Emoderivati 5 Rassegna Medico-scientifica, politica sanitaria e terzo settore 8 Prime Pagine 15 Rassegna associativa FIDAS
RASSEGNA STAMPA 07 aprile 2014 Sommario: Rassegna Associativa 2 Rassegna Sangue e Emoderivati 5 Rassegna Medico-scientifica, politica sanitaria e terzo settore 8 Prime Pagine 15 Rassegna associativa FIDAS
RoActemra (tocilizumab) Brochure per gli operatori sanitari per le seguenti indicazioni:
 RoActemra (tocilizumab) Brochure per gli operatori sanitari per le seguenti indicazioni: Artrite reumatoide [endovena o sottocute] Arterite a cellule giganti [sottocute] Poliartrite idiopatica giovanile
RoActemra (tocilizumab) Brochure per gli operatori sanitari per le seguenti indicazioni: Artrite reumatoide [endovena o sottocute] Arterite a cellule giganti [sottocute] Poliartrite idiopatica giovanile
Leucemie acute e sindromi mielodisplastiche
 Leucemie acute e sindromi mielodisplastiche Gli strumenti di governo clinico e la vigilanza da parte della Farmacia 23/02/2012 Paola Fiacchi Strumenti di governo Individuare per ogni molecola ad alto costo
Leucemie acute e sindromi mielodisplastiche Gli strumenti di governo clinico e la vigilanza da parte della Farmacia 23/02/2012 Paola Fiacchi Strumenti di governo Individuare per ogni molecola ad alto costo
OPDIVO. (nivolumab) Concentrato per soluzione per infusione. Guida alla gestione delle reazioni avverse immunocorrelate
 OPDIVO (nivolumab) Concentrato per soluzione per infusione Guida alla gestione delle reazioni avverse immunocorrelate Indicazioni terapeutiche Melanoma 1 OPDIVO in monoterapia o in combinazione con ipilimumab
OPDIVO (nivolumab) Concentrato per soluzione per infusione Guida alla gestione delle reazioni avverse immunocorrelate Indicazioni terapeutiche Melanoma 1 OPDIVO in monoterapia o in combinazione con ipilimumab
NUOVE FRONTIERE DI CURA: LA TERAPIA GENICA CAR-T
 NUOVE FRONTIERE DI CURA: LA TERAPIA GENICA CAR-T Franca Fagioli Presidente AIEOP Direttore S.C. Oncologia Pediatrica, Presidio Infantile Regina Margherita Città della Salute e della Scienza di Torino ASSOCIAZIONE
NUOVE FRONTIERE DI CURA: LA TERAPIA GENICA CAR-T Franca Fagioli Presidente AIEOP Direttore S.C. Oncologia Pediatrica, Presidio Infantile Regina Margherita Città della Salute e della Scienza di Torino ASSOCIAZIONE
Parte I - LINEE GUIDA. (Centro Nazionale Trapianti - 1 marzo 2005) PRINCIPI GENERALI. Razionale
 Parte I - LINEE GUIDA PROTOCOLLO PER L UTILIZZO DI DONATORI POSITIVI PER GLI ANTICORPI DIRETTI CONTRO L ANTIGENE CORE (HBCA-IGG) DEL VIRUS B DELL EPATITE (HBV) NEL TRAPIANTO DI FEGATO (Centro Nazionale
Parte I - LINEE GUIDA PROTOCOLLO PER L UTILIZZO DI DONATORI POSITIVI PER GLI ANTICORPI DIRETTI CONTRO L ANTIGENE CORE (HBCA-IGG) DEL VIRUS B DELL EPATITE (HBV) NEL TRAPIANTO DI FEGATO (Centro Nazionale
Ruxolitinib nella mielofibrosi. Francesca Palandri Istituto di Ematologia L.e A. Seràgnoli Università di Bologna
 Ruxolitinib nella mielofibrosi Francesca Palandri Istituto di Ematologia L.e A. Seràgnoli Università di Bologna 1 212: Ruxolitinib è stato approvato in EU 214: Ruxolitinib è disponibile in Italia Ruxolitinib
Ruxolitinib nella mielofibrosi Francesca Palandri Istituto di Ematologia L.e A. Seràgnoli Università di Bologna 1 212: Ruxolitinib è stato approvato in EU 214: Ruxolitinib è disponibile in Italia Ruxolitinib
Abseamed (epoetina alfa)
 EMA/552931/2018 EMEA/H/C/000727 Sintesi di Abseamed e perché è autorizzato nell Unione europea (UE) Cos è Abseamed e per cosa si usa? Abseamed è un medicinale usato nei seguenti casi: per trattare l anemia
EMA/552931/2018 EMEA/H/C/000727 Sintesi di Abseamed e perché è autorizzato nell Unione europea (UE) Cos è Abseamed e per cosa si usa? Abseamed è un medicinale usato nei seguenti casi: per trattare l anemia
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO
 EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 10 marzo 2016, il comitato indipendente per il monitoraggio dei dati sulla sicurezza ha informato la Commissione europea di un aumento
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 10 marzo 2016, il comitato indipendente per il monitoraggio dei dati sulla sicurezza ha informato la Commissione europea di un aumento
AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri)
 AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
MONOGRAFIA. ZYDELIG (idelalisib) Leucemia linfatica cronica
 MONOGRAFIA ZYDELIG (idelalisib) Leucemia linfatica cronica 1 SINTESI DELLA VALUTAZIONE - LEUCEMIA LINFATICA CRONICA 1.1 SINTESI DELLE EVIDENZE Sintesi delle prove di efficacia e di sicurezza CLL recidivata/refrattaria
MONOGRAFIA ZYDELIG (idelalisib) Leucemia linfatica cronica 1 SINTESI DELLA VALUTAZIONE - LEUCEMIA LINFATICA CRONICA 1.1 SINTESI DELLE EVIDENZE Sintesi delle prove di efficacia e di sicurezza CLL recidivata/refrattaria
MONOGRAFIA SINTESI. IBRANCE (palbociclib) Carcinoma Mammario. A cura della Commissione Terapeutica Oncologica
 MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
SCHEDA FARMACO. Principio attivo (nome commerciale) Ponatinib. (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Ponatinib SCHEDA FARMACO (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg Posologia: La dose
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Ponatinib SCHEDA FARMACO (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg Posologia: La dose
Tecentriq (atezolizumab)
 Tecentriq (atezolizumab) Importanti informazioni sulla sicurezza per ridurre al minimo il rischio di reazioni avverse immuno-correlate Per gli operatori sanitari Approvato da AIFA in data 15/04/2019 v.
Tecentriq (atezolizumab) Importanti informazioni sulla sicurezza per ridurre al minimo il rischio di reazioni avverse immuno-correlate Per gli operatori sanitari Approvato da AIFA in data 15/04/2019 v.
AULA ROSSA Policitemia Vera Le Novità Terapeutiche. Alessandro M. Vannucchi
 AULA ROSSA Policitemia Vera Le Novità Terapeutiche Alessandro M. Vannucchi CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi Farmaci in Sperimentazione Clinica Interferone
AULA ROSSA Policitemia Vera Le Novità Terapeutiche Alessandro M. Vannucchi CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi Farmaci in Sperimentazione Clinica Interferone
Il CHMP ha adottato un opinione finale a seguito delle raccomandazioni del PRAC sulla procedura di revisione di Esmya
 Il CHMP ha adottato un opinione finale a seguito delle raccomandazioni del PRAC sulla procedura di revisione di Esmya Budapest, Ungheria 1 giugno 2018 Gedeon Richter Plc. ha annunciato oggi che a seguito
Il CHMP ha adottato un opinione finale a seguito delle raccomandazioni del PRAC sulla procedura di revisione di Esmya Budapest, Ungheria 1 giugno 2018 Gedeon Richter Plc. ha annunciato oggi che a seguito
Approccio Terapeutico all iperglicemia a digiuno e postprandiale. Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013
 Approccio Terapeutico all iperglicemia a digiuno e postprandiale Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013 La triade glicemica nella gestione del diabete Glicemia
Approccio Terapeutico all iperglicemia a digiuno e postprandiale Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013 La triade glicemica nella gestione del diabete Glicemia
DALLA FARMACOVIGILANZA AGLI INTERVENTI REGOLATORI
 Farmacovigilanza, FAD e farmacisti: i risultati del Progetto della Regione Toscana DALLA FARMACOVIGILANZA AGLI INTERVENTI REGOLATORI Loredano Giorni Monteriggioni, Il Piccolo Castello Hotel, 9 Maggio 2009
Farmacovigilanza, FAD e farmacisti: i risultati del Progetto della Regione Toscana DALLA FARMACOVIGILANZA AGLI INTERVENTI REGOLATORI Loredano Giorni Monteriggioni, Il Piccolo Castello Hotel, 9 Maggio 2009
Le novità terapeutiche
 VIII Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 28 aprile 2018 Le novità terapeutiche Guido Finazzi CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative
VIII Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 28 aprile 2018 Le novità terapeutiche Guido Finazzi CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Tra l autorizzazione all immissione in commercio di Esmya (ulipristal acetato) e il novembre 2017 sono stati segnalati 3 casi di lesione
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Tra l autorizzazione all immissione in commercio di Esmya (ulipristal acetato) e il novembre 2017 sono stati segnalati 3 casi di lesione
SCLC - terapia di ii linea 53 II LINEA - RISULTATI E LIMITII
 SCLC - terapia di ii linea TRATTAMENTO STANDARD IN 53 II LINEA - RISULTATI E LIMITII SCLC - terapia di ii linea trattamento standard in ii linea - risultati e limiti Quasi la totalità dei pazienti affetti
SCLC - terapia di ii linea TRATTAMENTO STANDARD IN 53 II LINEA - RISULTATI E LIMITII SCLC - terapia di ii linea trattamento standard in ii linea - risultati e limiti Quasi la totalità dei pazienti affetti
Anticorpo. Chimerico. Murino mab. Umanizzato. ..tinib 18/05/09. Totalmente umano
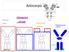 Anticorpo Murino mab Chimerico ximab Umanizzato zumab Totalmente umano mumab..tinib Anticorpi monoclonali anti EGFR Vengono somministrati per via endovenosa ogni settimana o ogni 2 Sono specifiche per
Anticorpo Murino mab Chimerico ximab Umanizzato zumab Totalmente umano mumab..tinib Anticorpi monoclonali anti EGFR Vengono somministrati per via endovenosa ogni settimana o ogni 2 Sono specifiche per
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
LEUCEMIA ACUTA LINFOBLASTICA RUOLO DEL TRAPIANTO
 LEUCEMIA ACUTA LINFOBLASTICA RUOLO DEL TRAPIANTO Renato FANIN Anna CANDONI CLINICA EMATOLOGICA CENTRO TRAPIANTI e TERAPIE CELLULARI AZIENDA OSPEDALIERO-UNIVERSITARIA UDINE ACUTE LEUKAEMIA REGISTRY
LEUCEMIA ACUTA LINFOBLASTICA RUOLO DEL TRAPIANTO Renato FANIN Anna CANDONI CLINICA EMATOLOGICA CENTRO TRAPIANTI e TERAPIE CELLULARI AZIENDA OSPEDALIERO-UNIVERSITARIA UDINE ACUTE LEUKAEMIA REGISTRY
Commissione Regionale Farmaco (D.G.R. 1209/2002)
 Commissione Regionale Farmaco (D.G.R. 1209/2002) Documento relativo a: BUDESONIDE + FORMOTEROLO SALMETEROLO XINAFOATO + FLUTICASONE PROPIONATO usi appropriati delle associazioni di farmaci steroidei e
Commissione Regionale Farmaco (D.G.R. 1209/2002) Documento relativo a: BUDESONIDE + FORMOTEROLO SALMETEROLO XINAFOATO + FLUTICASONE PROPIONATO usi appropriati delle associazioni di farmaci steroidei e
1. SINOSSI DEL PROTOCOLLO
 Versione finale 1.0, 23LUGLIO2014 1. SINOSSI DEL PROTOCOLLO Titolo dello studio Codice dello Sponsor Pseudonimo/Acronimo Primo studio nell uomo con MEN1112, un anticorpo monoclonale mirato al CD157 nella
Versione finale 1.0, 23LUGLIO2014 1. SINOSSI DEL PROTOCOLLO Titolo dello studio Codice dello Sponsor Pseudonimo/Acronimo Primo studio nell uomo con MEN1112, un anticorpo monoclonale mirato al CD157 nella
De-prescribing e strumenti
 De-prescribing e strumenti SIMI Winter School 2016 Milano, Dicembre 2016 Luca Pasina Istituto di Ricerche Farmacologiche Mario Negri, Milano Ottimizzazione delle (poli-)terapie intervento orientato al
De-prescribing e strumenti SIMI Winter School 2016 Milano, Dicembre 2016 Luca Pasina Istituto di Ricerche Farmacologiche Mario Negri, Milano Ottimizzazione delle (poli-)terapie intervento orientato al
Written by Tuesday, 12 August :26 - Last Updated Sunday, 21 November :45
 Anemia Aplastica acquisita Rara malattia ematologia, non oncologica Sua caratteristica è una netta riduzione di globuli bianchi, rossi e piastrine nel sangue (pancitopenia periferica) a volte gravissima
Anemia Aplastica acquisita Rara malattia ematologia, non oncologica Sua caratteristica è una netta riduzione di globuli bianchi, rossi e piastrine nel sangue (pancitopenia periferica) a volte gravissima
LA LEUCEMIA MIELOIDE CRONICA
 LA LEUCEMIA MIELOIDE CRONICA Opuscolo informativo Anno 2014 1 Leucemia Mieloide Cronica (LMC) La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica che colpisce le cellule staminali emopoietica,
LA LEUCEMIA MIELOIDE CRONICA Opuscolo informativo Anno 2014 1 Leucemia Mieloide Cronica (LMC) La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica che colpisce le cellule staminali emopoietica,
Effetti collaterali delle nuove terapie oncologiche. Stefania Vecchio Oncologia Medica 2 Genova, 22/06/2018
 Effetti collaterali delle nuove terapie oncologiche Stefania Vecchio Oncologia Medica 2 Genova, 22/06/2018 La chemioterapia Correlazione lineare fra intensità di dose ed effetto tumoricida Affinità fra
Effetti collaterali delle nuove terapie oncologiche Stefania Vecchio Oncologia Medica 2 Genova, 22/06/2018 La chemioterapia Correlazione lineare fra intensità di dose ed effetto tumoricida Affinità fra
La qualità della vita nelle terapie ematologiche
 La qualità della vita nelle terapie ematologiche Macroglobulinemia di Waldenstrom: vivere con una patologia rara I medici incontrano i pazienti 21 Aprile 2018 Anna Maria Frustaci ASST Grande Ospedale Metropolitano
La qualità della vita nelle terapie ematologiche Macroglobulinemia di Waldenstrom: vivere con una patologia rara I medici incontrano i pazienti 21 Aprile 2018 Anna Maria Frustaci ASST Grande Ospedale Metropolitano
AMPHOTERICIN B (AMBISOME
 SYNOPSIS Titolo dello Studio LIPOSOMAL AMPHOTERICIN B (AMBISOME ) 10 mg/kg once a week for 10 weeks as maintenance antifungal therapy for Proven/Probable Invasive Fungal Infection in hematologic patients
SYNOPSIS Titolo dello Studio LIPOSOMAL AMPHOTERICIN B (AMBISOME ) 10 mg/kg once a week for 10 weeks as maintenance antifungal therapy for Proven/Probable Invasive Fungal Infection in hematologic patients
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Novembre 2015 TECFIDERA (DIMETILFUMARATO): NUOVE MISURE PER MINIMIZZARE IL RISCHIO DI
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Novembre 2015 TECFIDERA (DIMETILFUMARATO): NUOVE MISURE PER MINIMIZZARE IL RISCHIO DI
SINDROME DA ANTICORPI ANTI-FOSFOLIPIDI
 SINDROME DA ANTICORPI ANTI-FOSFOLIPIDI Malattia caratterizzata da trombosi arteriose e/o venose ricorrenti, aborti ripetuti, trombocitopenia,, in associazione a titoli medio-alti di anticorpi anti-fosfolipidi
SINDROME DA ANTICORPI ANTI-FOSFOLIPIDI Malattia caratterizzata da trombosi arteriose e/o venose ricorrenti, aborti ripetuti, trombocitopenia,, in associazione a titoli medio-alti di anticorpi anti-fosfolipidi
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR DASATINIB
 RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE06 (SPRYCEL ) Presentata da COMMISSIONE PRONTUARIO TERAPEUTICO PROVINCIA SASSARI In data gennaio 2008 Per le seguenti motivazioni (sintesi): Dasatinib è un inibitore
RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE06 (SPRYCEL ) Presentata da COMMISSIONE PRONTUARIO TERAPEUTICO PROVINCIA SASSARI In data gennaio 2008 Per le seguenti motivazioni (sintesi): Dasatinib è un inibitore
2017: le novità nella mastocitosi e nella ipereosinofilia
 Settima Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 13 Maggio 2017 CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi 2017:
Settima Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 13 Maggio 2017 CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi 2017:
Area Strategia ed Economia del Farmaco Settore HTA ed economia del farmaco
 Area Strategia ed Economia del Farmaco Settore HTA ed economia del farmaco Elenco dei farmaci innovativi ai sensi dell articolo 10, comma 2, Legge 8 novembre 2012, n. 189, come definito dall'art.1 comma
Area Strategia ed Economia del Farmaco Settore HTA ed economia del farmaco Elenco dei farmaci innovativi ai sensi dell articolo 10, comma 2, Legge 8 novembre 2012, n. 189, come definito dall'art.1 comma
GIMEMA LLC1215. Clinical Trial Number NCT Numero EudraCT: Data 05/06/2015 Versione finale #1.1
 Studio di fase II sulla combinazione di Ofatumumab e Ibrutinib seguita da trapianto allogenico di midollo osseo o mantenimento per pazienti pretrattati ad alto rischio con leucemia linfoide cronica. GIMEMA
Studio di fase II sulla combinazione di Ofatumumab e Ibrutinib seguita da trapianto allogenico di midollo osseo o mantenimento per pazienti pretrattati ad alto rischio con leucemia linfoide cronica. GIMEMA
Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una
 1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
Vittorio Sargentini- SIPMeL, Società Italiana di Patologia Clinica e Medicina di Laboratorio
 Vittorio Sargentini- SIPMeL, Società Italiana di Patologia Clinica e Medicina di Laboratorio Ricerca di nuovi strumenti diagnostici Biomarcatore ideale 1. Operare uno screening al momento della comparsa
Vittorio Sargentini- SIPMeL, Società Italiana di Patologia Clinica e Medicina di Laboratorio Ricerca di nuovi strumenti diagnostici Biomarcatore ideale 1. Operare uno screening al momento della comparsa
Gammopatia monoclonale e Mieloma Multiplo. Dott.ssa Ciccone U.O. Ematologia
 Gammopatia monoclonale e Mieloma Multiplo Dott.ssa Ciccone U.O. Ematologia 1 Mieloma Multiplo: Epidemiologia 1% di tutti i tumori ed il 10% dei tumori ematologici In Europa l incidenza e di 4.5 6.0/100
Gammopatia monoclonale e Mieloma Multiplo Dott.ssa Ciccone U.O. Ematologia 1 Mieloma Multiplo: Epidemiologia 1% di tutti i tumori ed il 10% dei tumori ematologici In Europa l incidenza e di 4.5 6.0/100
Tossicità da Immunoterapia
 28/05/2018 La gestione medico-infermieristica delle urgenze da trattamenti antitumorali Tossicità da Immunoterapia Raffaella Casolino U.O.C. Oncologia Medica Ospedale Sacro Cuore-Don Calabria Negrar- VR
28/05/2018 La gestione medico-infermieristica delle urgenze da trattamenti antitumorali Tossicità da Immunoterapia Raffaella Casolino U.O.C. Oncologia Medica Ospedale Sacro Cuore-Don Calabria Negrar- VR
Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica
 Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica Clinical Practice Guidelines for Chronic Kidney Disease Chronic kidney disease: NICE guideline LINEA GUIDA
Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica Clinical Practice Guidelines for Chronic Kidney Disease Chronic kidney disease: NICE guideline LINEA GUIDA
Casi di IFI in pazienti sottoposti a HSCT allogenico con GVHD
 Casi di IFI in pazienti sottoposti a HSCT allogenico con GVHD Sindrome polmonare Sindrome sino-facciale Terapia pre-emptive Sepsi Sindrome al CNS Sindrome cutanea 58 CASO #1 Sepsi nel HSCT allogenico:
Casi di IFI in pazienti sottoposti a HSCT allogenico con GVHD Sindrome polmonare Sindrome sino-facciale Terapia pre-emptive Sepsi Sindrome al CNS Sindrome cutanea 58 CASO #1 Sepsi nel HSCT allogenico:
Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali. Meccanismo di azione e interazioni farmacologiche
 A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
DIAGNOSI PRECOCE E TERAPIA DELLA CARDIOTOSSICITA DA FARMACI ANTITUMORALI
 DIAGNOSI PRECOCE E TERAPIA DELLA CARDIOTOSSICITA DA FARMACI ANTITUMORALI Dr. Carlo M Cipolla Divisione di Cardiologia Istituto Europeo di Oncologia - Milano ROMA, 25 GENNAIO 2013 1 Dimensioni del fenomeno
DIAGNOSI PRECOCE E TERAPIA DELLA CARDIOTOSSICITA DA FARMACI ANTITUMORALI Dr. Carlo M Cipolla Divisione di Cardiologia Istituto Europeo di Oncologia - Milano ROMA, 25 GENNAIO 2013 1 Dimensioni del fenomeno
DAI DATI SCIENTIFICI ALLE PROSPETTIVE DI CURA
 DAI DATI SCIENTIFICI ALLE PROSPETTIVE DI CURA Franca Fagioli Direttore SC Oncoematologia Pediatrica e Centro Trapianti Presidio Ospedaliero Infantile Regina Margherita AOU Città della Salute e della Scienza
DAI DATI SCIENTIFICI ALLE PROSPETTIVE DI CURA Franca Fagioli Direttore SC Oncoematologia Pediatrica e Centro Trapianti Presidio Ospedaliero Infantile Regina Margherita AOU Città della Salute e della Scienza
STUDI CLINICI IN CORSO nella MIELOFIBROSI
 Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
INTOSSICAZIONI FUNGINE MAGGIORI INTOSSICAZIONI FUNGINE MAGGIORI INTOSSICAZIONI FUNGINE MAGGIORI INTOSSICAZIONI FUNGINE SINDROME FALLOIDEA
 INTOSSICAZIONI FUNGINE MAGGIORI INTOSSICAZIONI FUNGINE MAGGIORI PRINCIPALI CARATTERISTICHE DISTINTIVE Lunga latenza Interessamento parenchimale Elevata mortalità INTOSSICAZIONI FUNGINE MAGGIORI Sindrome
INTOSSICAZIONI FUNGINE MAGGIORI INTOSSICAZIONI FUNGINE MAGGIORI PRINCIPALI CARATTERISTICHE DISTINTIVE Lunga latenza Interessamento parenchimale Elevata mortalità INTOSSICAZIONI FUNGINE MAGGIORI Sindrome
Approccio clinico al paziente oncologico con diabete: sfide e indicazioni
 Approccio clinico al paziente oncologico con diabete: sfide e indicazioni Gabriele Riccardi Dipartimento di Medicina Clinica e Chirurgia Università Federico II, Napoli ? Il diabete ha un impatto sulla
Approccio clinico al paziente oncologico con diabete: sfide e indicazioni Gabriele Riccardi Dipartimento di Medicina Clinica e Chirurgia Università Federico II, Napoli ? Il diabete ha un impatto sulla
Gli antinfiammatori in Pediatria I FANS. Dott.ssa Alessia Nucci Università degli Studi di Firenze AOU Meyer
 Gli antinfiammatori in Pediatria I FANS Dott.ssa Alessia Nucci Università degli Studi di Firenze AOU Meyer Cosa sono i FANS? I FANS sono un gruppo di composti di classi chimiche diverse con proprietà analgesiche,
Gli antinfiammatori in Pediatria I FANS Dott.ssa Alessia Nucci Università degli Studi di Firenze AOU Meyer Cosa sono i FANS? I FANS sono un gruppo di composti di classi chimiche diverse con proprietà analgesiche,
Allegato III. Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali
 Allegato II Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali Il Riassunto delle Caratteristiche del Prodotto e il foglio
Allegato II Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali Il Riassunto delle Caratteristiche del Prodotto e il foglio
 www.fisiokinesiterapia.biz LA TERAPIA DELL ARTRITE REUMATOIDE Concetti introduttivi e nuove terapie farmacologiche MODELLO EVOLUTIVO AR A- Popolazione generale + Fattori di rischio B- Poliartrite infiammatoria
www.fisiokinesiterapia.biz LA TERAPIA DELL ARTRITE REUMATOIDE Concetti introduttivi e nuove terapie farmacologiche MODELLO EVOLUTIVO AR A- Popolazione generale + Fattori di rischio B- Poliartrite infiammatoria
GLOSSARIO GOOD CLINICAL PRACTICE (GCP)
 GLOSSARIO GOOD CLINICAL PRACTICE (GCP) Standard internazionale di etica e qualità scientifica per progettare, condurre, registrare e relazionare gli studi clinici che coinvolgono soggetti umani. L adesione
GLOSSARIO GOOD CLINICAL PRACTICE (GCP) Standard internazionale di etica e qualità scientifica per progettare, condurre, registrare e relazionare gli studi clinici che coinvolgono soggetti umani. L adesione
MONOGRAFIA Sintesi. GAZYVARO (obinutuzumab) Linfoma follicolare II linea o successive
 MONOGRAFIA Sintesi GAZYVARO (obinutuzumab) Linfoma follicolare II linea o successive 1 A cura della Commissione Terapeutica Oncologica 2 1 SINTESI DELLA VALUTAZIONE «Gazyvaro» in associazione a bendamustina,
MONOGRAFIA Sintesi GAZYVARO (obinutuzumab) Linfoma follicolare II linea o successive 1 A cura della Commissione Terapeutica Oncologica 2 1 SINTESI DELLA VALUTAZIONE «Gazyvaro» in associazione a bendamustina,
Caso clinico. Benedetta Puccini AOU Careggi Ematologia
 Caso clinico Benedetta Puccini AOU Careggi Ematologia Introduzione Uomo di 63 anni, 1 fratello di 55 anni A.Fisiologica:, non ha figli, non fuma. Da dicembre 2012 comparsa di dolore addominale e febbre
Caso clinico Benedetta Puccini AOU Careggi Ematologia Introduzione Uomo di 63 anni, 1 fratello di 55 anni A.Fisiologica:, non ha figli, non fuma. Da dicembre 2012 comparsa di dolore addominale e febbre
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO
 ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
RIASSUNTO DEL PROTOCOLLO DI SPERIMENTAZIONE CLINICA per la richiesta di parere al Comitato Etico dell Istituto Scientifico H.
 pag 1 di 6 Valutazione della tossicità e dell efficacia del treosulfano in combinazione con citarabina e fludarabina come condizionamento pre-autotrapianto di cellule staminali ematopoietiche, nei pazienti
pag 1 di 6 Valutazione della tossicità e dell efficacia del treosulfano in combinazione con citarabina e fludarabina come condizionamento pre-autotrapianto di cellule staminali ematopoietiche, nei pazienti
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori sanitari è
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori sanitari è
INSUFFICIENZA RENALE ACUTA
 INSUFFICIENZA RENALE ACUTA Sindrome clinico-metabolica caratterizzata da una rapida (ore, giorni) riduzione del filtrato glomerulare (VFG) con conseguente ritenzione dei prodotti del catabolismo azotato
INSUFFICIENZA RENALE ACUTA Sindrome clinico-metabolica caratterizzata da una rapida (ore, giorni) riduzione del filtrato glomerulare (VFG) con conseguente ritenzione dei prodotti del catabolismo azotato
STUDI CLINICI IN CORSO
 Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO Rajmonda Fjerza Laboratorio Congiunto MMPC, AOU Careggi Università degli
Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO Rajmonda Fjerza Laboratorio Congiunto MMPC, AOU Careggi Università degli
Nel caso del mieoloma multiplo, un tumore che colpisce un tipo di globuli bianchi detti cellule plasmatiche, Revlimid è usato:
 EMA/112959/2016 EMA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/112959/2016 EMA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE RoActemra 20 mg/ml concentrato per soluzione per infusione. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascun
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE RoActemra 20 mg/ml concentrato per soluzione per infusione. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascun
IL POST-ACUTO: LA RIABILITAZIONE RESPIRATORIA
 Dott. Michele Maiellari Specialista in Malattie dell Apparato Respiratorio Universita di Bari U.O. di Medicina e Chirurgia d Urgenza e Pronto Soccorso Resp.Dott.F. Serafino Ospedale San Giacomo Monopoli
Dott. Michele Maiellari Specialista in Malattie dell Apparato Respiratorio Universita di Bari U.O. di Medicina e Chirurgia d Urgenza e Pronto Soccorso Resp.Dott.F. Serafino Ospedale San Giacomo Monopoli
1 step: 30 pazienti se EFS 40% e TRM 5%
 PROSPETTICO DI FASE II DI TERAPIA MIELOABLATIVA AD ALTE DOSI, CON SUPPORTO DI CELLULE STAMINALI PERIFERICHE, IN PAZIENTI ANZIANI (65 E 75 ANNI) AFFETTI DA LINFOMA NON HODGKIN AGGRESSIVO RECIDIVATO O RESISTENTE
PROSPETTICO DI FASE II DI TERAPIA MIELOABLATIVA AD ALTE DOSI, CON SUPPORTO DI CELLULE STAMINALI PERIFERICHE, IN PAZIENTI ANZIANI (65 E 75 ANNI) AFFETTI DA LINFOMA NON HODGKIN AGGRESSIVO RECIDIVATO O RESISTENTE
STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI
 STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI Dott. Marino Clavio Ospedale Policlinico S Martino-IST
STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI Dott. Marino Clavio Ospedale Policlinico S Martino-IST
Relatrice: Elisa Malnis
 ASSISTENZA AL PAZIENTE CON NEOPLASIA DEL COLON Relatrice: Elisa Malnis 1 CRO Avian o SEDI DELLA MALATTIA Neoplasia del piccolo intestino Neoplasia del colon-retto Neoplasia dell ano 2 INCIDENZA CARCINOMA
ASSISTENZA AL PAZIENTE CON NEOPLASIA DEL COLON Relatrice: Elisa Malnis 1 CRO Avian o SEDI DELLA MALATTIA Neoplasia del piccolo intestino Neoplasia del colon-retto Neoplasia dell ano 2 INCIDENZA CARCINOMA
