CHIMICA E LUCE: GIOCHIAMO CON I COLORI DELLA NATURA
|
|
|
- Fiora Poggi
- 7 anni fa
- Visualizzazioni
Transcript
1 CHIMICA E LUCE: GIOCHIAMO CON I COLORI DELLA NATURA
2 Cos è la CHIMICA? è la disciplina che si interessa di capire come è fatto il mondo e come funziona (compreso l uomo) Usa un suo linguaggio che è quello degli atomi e molecole
3 Cos è la LUCE? Cosa sono i quanti di luce? Cinquant anni di intensa meditazione i non mi hanno permesso di rispondere a questa domanda. Naturalmente oggi tante persone superficiali pensano di saperlo, ma sbagliano. A. Einstein, Lettera a N. Besso, 12 dicembre 1951
4 Cosa fa la LUCE?
5
6 I chimici sanno molto bene cosa fa la luce e sanno sfruttarla per svariati i scopi
7 La luce ci permette di vedere L Chi i i i il ll b La Chimica ci spiega il processo alla base della visione
8 Alla luce si deve il colore delle cose La Chimica ci spiega come si origina il colore
9 Come si origina il colore Dobbiamo considerare che la luce che ci appare bianca è in realtà formata dall insieme di radiazioni di vario colore Luce bianca rosso arancio giallo verde violetto azzurro indaco
10
11 Come si origina il colore La luce interagisce con le molecole che formano la materia Le molecole sono in grado di assorbire solo le radiazioni che corrispondono a certi colori
12 Il colore che assume un oggetto, colpito da luce bianca, è dato dal mescolamento dei colori delle radiazioni i i che NON vengono assorbite
13 Secondo i filosofi greci la luce bianca era luce pulita mentre il colore era un impurezza che contaminava la luce bianca quando essa veniva a contatto con gli oggetti
14 Il colore, quindi, non è una caratteristica intrinseca di un oggetto, ma dipende da quello della sorgente che lo illumina
15 Se un tempo l unica sorgente di luce era il Sole, oggi disponiamo di svariate sorgenti artificiali di luce create con il contributo dei chimici: lampadine di tutti i tipi i
16 Il laser una sorgente molto intensa e focalizzata di radiazioni i i di un solo colore
17 Lampadine chimiche: la luce può accompagnare la formazioni dei prodotti di una reazione A + B C + D + Reazioni chemiluminescenti
18 I colori della natura La maggior parte dei colori dei fiori e delle piante, nonché i loro cambiamenti, derivano dalla produzione, interazione, decomposizione di queste 3 classi di sostanze: porfirine carotenoidi flavonoidi
19 O H 3 C COOH H 3 CH 2 C N C 2 H 5 CO 2 C 20 H 39 N Mg N H 3 C N CH 3 H 2 CHC CH 3 Clorofilla ll a
20 ß-carotene
21 O OH E E E E E E E HO E E O xantofilla
22 PAGE 1-A Me Me2C E E E E E E E E Me Me Me Me Me PAGE 1-B E E E CMe 2 Licopene
23 I flavonoidi e i flavonoli li si trovano nelle foglie di alcune piante. Tuttavia il loro maggiore contributo è nei petali dei fiori. i Le antocianine sono responsabili per la maggioranza dei colori rossi, blu e porpora delle piante. In alcuni casi c è cè anche dipendenza dalla quantità di luce utilizzabile. Per es., la parte di una fragola esposta al sole diventa rossa più velocemente della parte all ombra.
24 O Ph O Ph OH O flavone O flavonolo Antocianine OMe HO O+ HO O + OH OH OH OH OH OH OH cianidina peonidina
25 Acero rosso
26 I colori della natura Una caratteristica interessante della maggior parte di queste sostanze colorate che si trovano nelle piante e nei fiori è che il loro colore cambia a contatto di acidi e basi
27 ACIDI e BASI Non serve aver studiato t la chimica per riconoscere all aceto, al succo di limone e anche alle bibite tipo cola i caratteri tipici i degli acidi : sono ruvidi al tatto e hanno sapore aspro I caratteri tipici delle basi : scivolosi al tatto a di sapore amaro Si riconoscono nel bicarbonato e in alcuni prodotti casalinghi
28 Misura dell acidità e della basicità I chimici usano il ph 0 < ph < 14 ph < 7 sostanze acide ph = 7 sostanze neutre ph > 7 sostanze basiche
29 Gamma di colori che si ottiene con l indicatore universale al variare del ph della soluzione
30
31 OH OH HO O+ O CIANIDINA-3-GLUCOSIDE OH HO R S O HO S S R OH OH FORMA ROSSA FORMA VIOLETTA FORMA BLU ph<3 ph 7-8 ph>11 acido neutro basico
32 Papavero Fiordaliso Viola odorata
33 Cavolo rosso
34 Il succo del cavolo rosso è capace di assumere svariate colorazioni a seconda del ph del liquido a cui viene aggiunto p ph= acido neutro basico
35 I coloranti naturali possono anche essere p usati per tingere tessuti, lana, seta
36 Lana tinta con la robbia
37 Camomilla m dei Tintori Anthemis tintoria
38 Dactylopius coccus cacti
39 Alfabeto con le ali Kjiell Sandved, fotografo dello statunitense Smithsonian Institute, una delle più importanti istituzioni di scienze naturali del mondo, notò per la prima volta sulle ali di una farfalla di una collezione privata una lettera P, inequivocabile. Da allora ha cercato in Nuova Guinea, Malesia e Brasile, raggiungendo un risultato veramente straordinario
40
Radiazioni elettromagnetiche
 LUCE E E COLORE Onde meccaniche Radiazioni elettromagnetiche Le radiazioni sono onde associate al movimento di cariche elettriche e vengono chiamate elettromagnetiche perché possono essere scomposte in
LUCE E E COLORE Onde meccaniche Radiazioni elettromagnetiche Le radiazioni sono onde associate al movimento di cariche elettriche e vengono chiamate elettromagnetiche perché possono essere scomposte in
I Colori sono gli Atti della Luce. (Goethe)
 I Colori sono gli Atti della Luce (Goethe) tutto cominciò con JSAC NEWTON 1600 e rotti DISTINZIONE TRA: MONDO FISICO dove tutto è oggettivo e misurabile MONDO DELLA PERCEZIONE dove tutto è soggettivo
I Colori sono gli Atti della Luce (Goethe) tutto cominciò con JSAC NEWTON 1600 e rotti DISTINZIONE TRA: MONDO FISICO dove tutto è oggettivo e misurabile MONDO DELLA PERCEZIONE dove tutto è soggettivo
ESPERIENZE IN LABORATORIO 4^B. 13 Marzo 2019
 ESPERIENZE IN LABORATORIO 4^B 13 Marzo 2019 ESPERIMENTO 1: ESTRAZIONE DEI PIGMENTI DELLE FOGLIE 13 Marzo 2019 INTRODUZIONE Vi abbiamo portato alcuni tipi di verdure A FOGLIA: - Spinaci (con foglie verdi)
ESPERIENZE IN LABORATORIO 4^B 13 Marzo 2019 ESPERIMENTO 1: ESTRAZIONE DEI PIGMENTI DELLE FOGLIE 13 Marzo 2019 INTRODUZIONE Vi abbiamo portato alcuni tipi di verdure A FOGLIA: - Spinaci (con foglie verdi)
Estrazione di pigmenti vegetali da sostanze naturali
 Estrazione di pigmenti vegetali da sostanze naturali Il cavolo rosso deve il suo colore agli antociani o antocianine, che sono una classe di pigmenti idrosolubili appartenente alla famiglia dei flavonoidi.
Estrazione di pigmenti vegetali da sostanze naturali Il cavolo rosso deve il suo colore agli antociani o antocianine, che sono una classe di pigmenti idrosolubili appartenente alla famiglia dei flavonoidi.
Iniziativa realizzata con il contributo della Regione Toscana nell ambito del progetto. Rete Scuole LSS. a.s. 2016/2017
 Iniziativa realizzata con il contributo della Regione Toscana nell ambito del progetto Rete Scuole LSS a.s. 2016/2017 ph CHIMICA Classi IV A-B Liceo Linguistico Orbetello a.s. 2016 17 Docente: Carmelina
Iniziativa realizzata con il contributo della Regione Toscana nell ambito del progetto Rete Scuole LSS a.s. 2016/2017 ph CHIMICA Classi IV A-B Liceo Linguistico Orbetello a.s. 2016 17 Docente: Carmelina
Esperimenti con ACIDI e BASI
 Esperimenti con ACIDI e BASI PRESENTAZIONE Questa volta faremo alcuni semplici esperimenti di chimica per iniziare a conoscere gli acidi e le basi. Vedremo come si misura l'acidità delle sostanze, faremo
Esperimenti con ACIDI e BASI PRESENTAZIONE Questa volta faremo alcuni semplici esperimenti di chimica per iniziare a conoscere gli acidi e le basi. Vedremo come si misura l'acidità delle sostanze, faremo
Le sostanze che ci circondano possono essere classificate in tre grandi gruppi: 1) SOSTANZE ACIDE. - Corrosive ed irritanti
 Le sostanze che ci circondano possono essere classificate in tre grandi gruppi: 1) SOSTANZE ACIDE - Corrosive ed irritanti Gli acidi corrodono i metalli ...ed i materiali carbonatici I succhi gastrici
Le sostanze che ci circondano possono essere classificate in tre grandi gruppi: 1) SOSTANZE ACIDE - Corrosive ed irritanti Gli acidi corrodono i metalli ...ed i materiali carbonatici I succhi gastrici
Esperienza n 3: Determinazione del grado di acidità dell aceto commerciale
 Esperienza n : Determinazione del grado di acidità dell aceto commerciale Obiettivo: determinare il grado di acidità di un aceto commerciale tramite titolazione con una soluzione di NaOH a titolo noto
Esperienza n : Determinazione del grado di acidità dell aceto commerciale Obiettivo: determinare il grado di acidità di un aceto commerciale tramite titolazione con una soluzione di NaOH a titolo noto
Punto finale di un analisi volumetrica. Cambiamento di colore del reagente (analita) Uso di indicatore Variazione del potenziale elettrico
 Punto finale di un analisi volumetrica Cambiamento di colore del reagente (analita) Uso di indicatore Variazione del potenziale elettrico Punto finale di una titolazione con il calcolo del P. equivalente
Punto finale di un analisi volumetrica Cambiamento di colore del reagente (analita) Uso di indicatore Variazione del potenziale elettrico Punto finale di una titolazione con il calcolo del P. equivalente
REAZIONI CHIMICHE IN SOLUZIONE ACQUOSA
 REAZIONI CHIMICHE IN SOLUZIONE ACQUOSA A) studio delle REAZIONI IN SOLUZIONE (acquosa): suggerimento di un esempio sperimentale. B) indicazione del range di ph di una soluzione acquosa: suggerimento di
REAZIONI CHIMICHE IN SOLUZIONE ACQUOSA A) studio delle REAZIONI IN SOLUZIONE (acquosa): suggerimento di un esempio sperimentale. B) indicazione del range di ph di una soluzione acquosa: suggerimento di
MISURAZIONE DEL DIVERSO PH DI ALCUNE SOSTANZE
 MISURAZIONE DEL DIVERSO PH DI ALCUNE SOSTANZE Relazione di Edoardo Prosperi e Luisa Beorchia. Immagini di Matilde Cescutti. L esperimento è stato effettuato dall intera classe 4^B coadiuvata dalla Prof.ssa
MISURAZIONE DEL DIVERSO PH DI ALCUNE SOSTANZE Relazione di Edoardo Prosperi e Luisa Beorchia. Immagini di Matilde Cescutti. L esperimento è stato effettuato dall intera classe 4^B coadiuvata dalla Prof.ssa
GLI ACIDI E LE BASI nel quotidiano L acido acetico: è presente nell aceto; L acido formico: a questo composto si deve il bruciore che si avverte dopo
 GLI ACIDI E LE BASI nel quotidiano L acido acetico: è presente nell aceto; L acido formico: a questo composto si deve il bruciore che si avverte dopo il morso di una formica; L acido citrico: è contenuto
GLI ACIDI E LE BASI nel quotidiano L acido acetico: è presente nell aceto; L acido formico: a questo composto si deve il bruciore che si avverte dopo il morso di una formica; L acido citrico: è contenuto
Le definizioni di acido e di base Un percorso storico
 Le definizioni di acido e di base Un percorso storico Corpaci Ivana Teoria degli acidi e delle basi w Cos è un acido?! Una sostanza corrosiva, chimicamente molto attiva, che colora di rosso la cartina
Le definizioni di acido e di base Un percorso storico Corpaci Ivana Teoria degli acidi e delle basi w Cos è un acido?! Una sostanza corrosiva, chimicamente molto attiva, che colora di rosso la cartina
UNITA' DIDATTICA SU ACIDI E BASI
 UNIVERSITA' ALGI STUDI DI TORINO CORS DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA ANNO ACCADEMICO 2016-2017 FONDAMENTI E DIDATTICA DELLA CHIMICA PROF. GIUSEPPINA CERRATO STUDENTE: GAMBA IRENE MATRICOLA:
UNIVERSITA' ALGI STUDI DI TORINO CORS DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA ANNO ACCADEMICO 2016-2017 FONDAMENTI E DIDATTICA DELLA CHIMICA PROF. GIUSEPPINA CERRATO STUDENTE: GAMBA IRENE MATRICOLA:
Modulo di Chimica VII lezione. Acidi e basi Il ph
 Modulo di Chimica VII lezione Acidi e basi Il ph Un po di etimologia Acido: dal latino acidus (ac, essere pungente) Base: dal greco βασιξ (sostenere) Alcali: dall arabo al-qalì (potassa, dalle ceneri di
Modulo di Chimica VII lezione Acidi e basi Il ph Un po di etimologia Acido: dal latino acidus (ac, essere pungente) Base: dal greco βασιξ (sostenere) Alcali: dall arabo al-qalì (potassa, dalle ceneri di
GLI ACIDI E LE BASI nel quotidiano L acido acetico: è presente nell aceto; L acido formico: a questo composto si deve il bruciore che si avverte dopo
 GLI ACIDI E LE BASI nel quotidiano L acido acetico: è presente nell aceto; L acido formico: a questo composto si deve il bruciore che si avverte dopo il morso di una formica; L acido citrico: è contenuto
GLI ACIDI E LE BASI nel quotidiano L acido acetico: è presente nell aceto; L acido formico: a questo composto si deve il bruciore che si avverte dopo il morso di una formica; L acido citrico: è contenuto
Teoria di Lewis. Un acido di Lewis è una specie chimica che può formare un legame covalente accettando una coppia di elettroni da un altra specie.
 Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
"Scienziati in azione
 Scuola Secondaria di 1 Grado Statale Gaetano Santomauro - Bari Programma Operativo Nazionale Scuola 2008 FONDO SOCIALE EUROPEO Competenze per lo sviluppo PON- C-1-FSE 2008-694 "Scienziati in azione Alunni
Scuola Secondaria di 1 Grado Statale Gaetano Santomauro - Bari Programma Operativo Nazionale Scuola 2008 FONDO SOCIALE EUROPEO Competenze per lo sviluppo PON- C-1-FSE 2008-694 "Scienziati in azione Alunni
*Gli atomi sono tutti uguali tra loro?
 *Gli atomi sono tutti uguali tra loro? *Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni sono più piccoli, altri più grandi. La piccolezza o la grandezza
*Gli atomi sono tutti uguali tra loro? *Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni sono più piccoli, altri più grandi. La piccolezza o la grandezza
Misure di ph e titolazione acidobase con metodo potenziometrico
 - Laboratorio di Chimica 1 Misure di ph e titolazione acidobase con metodo potenziometrico PAS A.A. 2013-14 Obiettivi 2 Uso di un ph-metro per la misura del ph Titolazione acido-base: costruzione della
- Laboratorio di Chimica 1 Misure di ph e titolazione acidobase con metodo potenziometrico PAS A.A. 2013-14 Obiettivi 2 Uso di un ph-metro per la misura del ph Titolazione acido-base: costruzione della
Le Reazioni Chimiche
 Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI
 IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
Olimpiadi di Chimica
 Olimpiadi di Chimica Acqua Oro Zucchero Acidi e basi Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza
Olimpiadi di Chimica Acqua Oro Zucchero Acidi e basi Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza
a.s. 2009/10 VELIA GIANGIORDANO
 a.s. 2009/10 VELIA GIANGIORDANO Era un sabato mattina e tutti i colori uscirono per andare al mercato. "Buon giorno signor Arancione!" - disse il signor Blu. "Buon giorno a Lei Signor Arancione ha visto
a.s. 2009/10 VELIA GIANGIORDANO Era un sabato mattina e tutti i colori uscirono per andare al mercato. "Buon giorno signor Arancione!" - disse il signor Blu. "Buon giorno a Lei Signor Arancione ha visto
Sommario della lezione 22. Idrolisi Indicatori di ph Soluzioni tampone - Titolazioni
 Sommario della lezione 22 Idrolisi Indicatori di ph Soluzioni tampone - Titolazioni Determinazione del ph Il ph di una soluzione può essere determinato in modo approssimato mediante l uso di un indicatore.
Sommario della lezione 22 Idrolisi Indicatori di ph Soluzioni tampone - Titolazioni Determinazione del ph Il ph di una soluzione può essere determinato in modo approssimato mediante l uso di un indicatore.
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 22 Acidi e basi si scambiano protoni 3 Sommario 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. La forza
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 22 Acidi e basi si scambiano protoni 3 Sommario 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. La forza
PRECIPITAZIONI. Esperimento 1: rilevazione dello ione piombo (Pb 2+ ) in acqua
 COSA C È DIETRO? L obiettivo di questa mostra è stato imparare a utilizzare alcuni nuovi strumenti di laboratorio di recente acquisto. Durante i giorni di preparazione ci siamo accorti di un filo rosso
COSA C È DIETRO? L obiettivo di questa mostra è stato imparare a utilizzare alcuni nuovi strumenti di laboratorio di recente acquisto. Durante i giorni di preparazione ci siamo accorti di un filo rosso
Progetto Lauree Scientifiche Anno Scolastico 2008/09. Responsabili progetto: Dr. L. Maiuolo Dr. B. Russo
 Progetto Lauree Scientifiche Anno Scolastico 2008/09 ACIDI e BASI Responsabili progetto: Prof O Bortolini Prof. O. Bortolini Dr. L. Maiuolo Dr. B. Russo In chimica, le definizioni di acido e base hanno
Progetto Lauree Scientifiche Anno Scolastico 2008/09 ACIDI e BASI Responsabili progetto: Prof O Bortolini Prof. O. Bortolini Dr. L. Maiuolo Dr. B. Russo In chimica, le definizioni di acido e base hanno
Equilibri Acido Base e ph
 Equilibri Acido Base e ph Definizioni di Acido e Base Secondo la teoria di Arrhenius, un acido è una sostanza che dissociandosi in acqua libera ioni H +, una base è invece una sostanza che dissociandosi
Equilibri Acido Base e ph Definizioni di Acido e Base Secondo la teoria di Arrhenius, un acido è una sostanza che dissociandosi in acqua libera ioni H +, una base è invece una sostanza che dissociandosi
DOMANDA O IPOTESI DESTINATARI MATERIALE OCCORRENTE
 DOMANDA O IPOTESI DESTINATARI MATERIALE OCCORRENTE DESCRIZIONE DELLA PROVA ASPETTI POSITIVI E NEGATIVI DIFFICOLTÀ INCONTRATE GRADIMENTO DEGLI ALUNNI VALUTAZIONE DEGLI APPRENDIMENTI Che cosa succede se
DOMANDA O IPOTESI DESTINATARI MATERIALE OCCORRENTE DESCRIZIONE DELLA PROVA ASPETTI POSITIVI E NEGATIVI DIFFICOLTÀ INCONTRATE GRADIMENTO DEGLI ALUNNI VALUTAZIONE DEGLI APPRENDIMENTI Che cosa succede se
GAIALAB:INCONTRIAMO L AMBIENTE IN LABORATORIO
 LABORATORIO DI SCIENZE NATURALI Raggi di sole e molecole di zucchero: i cloroplasti come laboratori chimici Tradescantia pallida Tradescantiafluminensis 1 Trasformazione energetica luce energia chimica
LABORATORIO DI SCIENZE NATURALI Raggi di sole e molecole di zucchero: i cloroplasti come laboratori chimici Tradescantia pallida Tradescantiafluminensis 1 Trasformazione energetica luce energia chimica
Circuiti in Serie / Parallelo
 Circuiti in Serie / Parallelo Utilizzatori in serie Più utilizzatori sono collegati in serie quando sono montati uno dopo l altro in modo che la stessa corrente li attraversi in successione. In tal modo
Circuiti in Serie / Parallelo Utilizzatori in serie Più utilizzatori sono collegati in serie quando sono montati uno dopo l altro in modo che la stessa corrente li attraversi in successione. In tal modo
Le Reazioni Chimiche
 I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
L idrolisi salina. Vi sono sali che sciolti in acqua, impartiscono alla soluzione una reazione acida o basica.
 L idrolisi salina Abbiamo imparato che i sali sono solidi ionici che si comportano in soluzione come elettroliti forti. Sappiamo anche che i sali possono venire considerati come sostanze neutre che si
L idrolisi salina Abbiamo imparato che i sali sono solidi ionici che si comportano in soluzione come elettroliti forti. Sappiamo anche che i sali possono venire considerati come sostanze neutre che si
Esperimenti sul ph. Nel mondo esistono milioni di sostanze chimiche. Alcune di esse hanno proprietà acide ed altre basiche.
 Introduzione al ph Esperimenti sul ph Nel mondo esistono milioni di sostanze chimiche. Alcune di esse hanno proprietà acide ed altre basiche. Gli acidi sono sostanze che poste in acqua liberano ioni idrogeno
Introduzione al ph Esperimenti sul ph Nel mondo esistono milioni di sostanze chimiche. Alcune di esse hanno proprietà acide ed altre basiche. Gli acidi sono sostanze che poste in acqua liberano ioni idrogeno
SECONDO CIRCOLO DIDATTICO DI SELARGIUS. Progetto d arricchimento dell Offerta Formativa Percorsi scientifici e di laboratorio A.S.
 SECONDO CIRCOLO DIDATTICO DI SELARGIUS Progetto d arricchimento dell Offerta Formativa Percorsi scientifici e di laboratorio A.S. 2015-16 Reazioni, legami, soluzioni, miscugli piccoli chimici scoprono
SECONDO CIRCOLO DIDATTICO DI SELARGIUS Progetto d arricchimento dell Offerta Formativa Percorsi scientifici e di laboratorio A.S. 2015-16 Reazioni, legami, soluzioni, miscugli piccoli chimici scoprono
DIARIO DELLO STUDENTE E REPORT DELLE ATTIVITA
 PROGETTO DIOR -PROGRESS Progetto di Didattica Orientativa in ambito scientifico -Summer Chemistry Lab-DIOR 2017 Laboratorio teorico pratico di CHIMICA Laboratorio didattico di Chimica del Dipartimento
PROGETTO DIOR -PROGRESS Progetto di Didattica Orientativa in ambito scientifico -Summer Chemistry Lab-DIOR 2017 Laboratorio teorico pratico di CHIMICA Laboratorio didattico di Chimica del Dipartimento
Composti di coordinazione
 Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
le reazioni chimiche
 le reazioni chimiche Una reazione (o equazione) chimica e una trasformazione di sostanze dette reagenti in altre sostanze dette prodotti. reagenti prodotti ESEMPI DI REAZIONI CHIMICHE: - ACETO + BICARBONATO
le reazioni chimiche Una reazione (o equazione) chimica e una trasformazione di sostanze dette reagenti in altre sostanze dette prodotti. reagenti prodotti ESEMPI DI REAZIONI CHIMICHE: - ACETO + BICARBONATO
La vita dipende dall acqua
 La vita dipende dall acqua La vita sulla Terra dipende dalle proprietà dell acqua. L acqua è il composto più abbondante negli esseri viventi. Le proprietà dell acqua derivano dalla sua particolare struttura
La vita dipende dall acqua La vita sulla Terra dipende dalle proprietà dell acqua. L acqua è il composto più abbondante negli esseri viventi. Le proprietà dell acqua derivano dalla sua particolare struttura
21/03/2017 EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA
 EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA 1 Concentrazione Molarità : numero di moli di soluto per litro di soluzione. Molalità : numero di moli di soluto
EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA 1 Concentrazione Molarità : numero di moli di soluto per litro di soluzione. Molalità : numero di moli di soluto
Progetto Lauree Scientifiche Dipartimento di Chimica Università degli Studi di Sassari
 Progetto Lauree Scientifiche Dipartimento di Chimica Università degli Studi di Sassari Estrazione ed impiego di indicatori acido-base vegetali ACIDI E BASI NELLA VITA QUTIDIANA Acidi Sono di sapore aspro
Progetto Lauree Scientifiche Dipartimento di Chimica Università degli Studi di Sassari Estrazione ed impiego di indicatori acido-base vegetali ACIDI E BASI NELLA VITA QUTIDIANA Acidi Sono di sapore aspro
ASSORBIMENTO UV-VIS. Atomo
 ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
H n A+ H 2 O H n-1 A - + H 3 O + 1) H n-1 A - + H 2 O H n-2 A 2- + H 3 O + 2) H n-2 A 2- + H 2 O H n-3 A 3- + H 3 O + 3)
 Acidi poliprotici Consideriamo un generico acido H n A e scriviamo gli equilibri: H n A H O H n1 A H O 1) H n1 A H O H n A H O ) H n A H O H n A H O ) HA (n1) H O A n H O n) [Hn 1A [HO 1 [HnA [HnA [HO
Acidi poliprotici Consideriamo un generico acido H n A e scriviamo gli equilibri: H n A H O H n1 A H O 1) H n1 A H O H n A H O ) H n A H O H n A H O ) HA (n1) H O A n H O n) [Hn 1A [HO 1 [HnA [HnA [HO
Idrolisi salina. HCl + NaOH NaCl + H 2 O. In acqua i sali si dissociano nei loro ioni i quali si circondano di molecole
 Idrolisi salina I sali sono solidi ionici che si comportano in soluzione come elettroliti forti. Sappiamo anche che i sali possono venire considerati come sostanze neutre che si ottengono dalla reazione
Idrolisi salina I sali sono solidi ionici che si comportano in soluzione come elettroliti forti. Sappiamo anche che i sali possono venire considerati come sostanze neutre che si ottengono dalla reazione
Il giardino della scuola: fucina di trasformazioni e scambi. IISS IPSIA Ettore Majorana Bari Classe I settore Fotografico Classe I settore Ottico
 Formazione attiva: UN LUOGO PER VIVERE scuola secondaria di 2 grado Percorso Il giardino della scuola: fucina di trasformazioni e scambi IISS IPSIA Ettore Majorana Bari Classe I settore Fotografico Classe
Formazione attiva: UN LUOGO PER VIVERE scuola secondaria di 2 grado Percorso Il giardino della scuola: fucina di trasformazioni e scambi IISS IPSIA Ettore Majorana Bari Classe I settore Fotografico Classe
Anno Scolastico 2015 / 2016 Prof. Paolo Beretti. i Colori
 Anno Scolastico 2015 / 2016 Prof. Paolo Beretti i Colori 1. L ARCOBALENO Nella seconda metà del XVII secolo (1665-1676) lo scienziato inglese Isaac Newton proiettò un raggio di luce bianca attraverso un
Anno Scolastico 2015 / 2016 Prof. Paolo Beretti i Colori 1. L ARCOBALENO Nella seconda metà del XVII secolo (1665-1676) lo scienziato inglese Isaac Newton proiettò un raggio di luce bianca attraverso un
La Spettrofotometria
 La Spettrofotometria Brevi cenni Un corpo, che non emetta luce propria, appare di un colore che dipende dalla luce con cui è investito. Esso tratterrà alcune lunghezze d onda e rifletterà quelle che non
La Spettrofotometria Brevi cenni Un corpo, che non emetta luce propria, appare di un colore che dipende dalla luce con cui è investito. Esso tratterrà alcune lunghezze d onda e rifletterà quelle che non
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 17 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 17 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione
legge dell azione di massa: all equilibrio K c = [C] c [D] d / [A] a [B] b = k 1 /k -1
![legge dell azione di massa: all equilibrio K c = [C] c [D] d / [A] a [B] b = k 1 /k -1 legge dell azione di massa: all equilibrio K c = [C] c [D] d / [A] a [B] b = k 1 /k -1](/thumbs/71/65830231.jpg) EQUILIBRIO CHIMICO 1 Consideriamo la reazione chimica seguente: CH 3 COOH + C 2 H 5 OH CH 3 COOC 2 H 5 + H 2 O K c = [estere] [acqua] / [acido] [alcol] K c = costante di equilibrio legge dell azione di
EQUILIBRIO CHIMICO 1 Consideriamo la reazione chimica seguente: CH 3 COOH + C 2 H 5 OH CH 3 COOC 2 H 5 + H 2 O K c = [estere] [acqua] / [acido] [alcol] K c = costante di equilibrio legge dell azione di
ph e indicatori acido-base
 ph e indicatori acido-base La dissociazione ionica dell acqua H 2 O + H 2 O OH - + H 3 O + acido base base acido coniugata coniugato 2 H 2 O (l) OH - (aq) + H 3 O + (aq) Il numero di molecole di acqua
ph e indicatori acido-base La dissociazione ionica dell acqua H 2 O + H 2 O OH - + H 3 O + acido base base acido coniugata coniugato 2 H 2 O (l) OH - (aq) + H 3 O + (aq) Il numero di molecole di acqua
ACIDI E BASI ORGANICI: pka e ph
 Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Oggi: disponiamo di tecniche di analisi strumentale, molte delle quali utilizzano radiazione elettromagnetica
 Come si riconosce un composto chimico? In passato: in base al punto di ebollizione o fusione, alla solubilità in un dato solvente, a parametri organolettici, alla reattività con altri composti Oggi: disponiamo
Come si riconosce un composto chimico? In passato: in base al punto di ebollizione o fusione, alla solubilità in un dato solvente, a parametri organolettici, alla reattività con altri composti Oggi: disponiamo
La Magia della Chimica
 La Magia della Chimica Coloriamo l acidità: il colore del cavolo rosso e le antocianine Dal punto di vista dell acidità la sostanza di riferimento è l acqua. L acqua pura contiene piccole quantità di ioni
La Magia della Chimica Coloriamo l acidità: il colore del cavolo rosso e le antocianine Dal punto di vista dell acidità la sostanza di riferimento è l acqua. L acqua pura contiene piccole quantità di ioni
Corso di Chimica e Propedeutica Biochimica La chimica degli acidi e delle basi
 Corso di Chimica e Propedeutica Biochimica La chimica degli acidi e delle basi Svante Arrhenius (1859 1927) Johannes Nicolaus Brønsted (1879 1947) Thomas Martin Lowry (1874-1936) Gilbert Newton Lewis (1875-1946)
Corso di Chimica e Propedeutica Biochimica La chimica degli acidi e delle basi Svante Arrhenius (1859 1927) Johannes Nicolaus Brønsted (1879 1947) Thomas Martin Lowry (1874-1936) Gilbert Newton Lewis (1875-1946)
Esperimento: Erosione Foglio di lavoro
 Esperimento 1: Erosione Informazioni per il docente 1/5 Compito Obiettivo Gli studenti sono "amanti" di varie bevande dolci. Sempre più spesso la mattina capita di vedere ragazzi che vanno a scuola con
Esperimento 1: Erosione Informazioni per il docente 1/5 Compito Obiettivo Gli studenti sono "amanti" di varie bevande dolci. Sempre più spesso la mattina capita di vedere ragazzi che vanno a scuola con
Arrhenius. HCl H + + Cl - NaOH Na + + OH -
 Arrhenius Un acido è una sostanza che contiene H ed è in grado di cedere ioni H + e base è una sostanza che ha tendenza a cedere ioni OH - in acqua H 2 O HCl H + + Cl - H 2 O NaOH Na + + OH - Reazione
Arrhenius Un acido è una sostanza che contiene H ed è in grado di cedere ioni H + e base è una sostanza che ha tendenza a cedere ioni OH - in acqua H 2 O HCl H + + Cl - H 2 O NaOH Na + + OH - Reazione
LABORATORIO DI CHIMICA
 LABORATORIO DI CHIMICA Presentazione 3 a ESPERIENZA Titolazione Acido-Base ANALISI VOLUMETRICA Tipi di titolazioni Esistono diversi tipi di titolazione, classificati in funzione della reazione su cui si
LABORATORIO DI CHIMICA Presentazione 3 a ESPERIENZA Titolazione Acido-Base ANALISI VOLUMETRICA Tipi di titolazioni Esistono diversi tipi di titolazione, classificati in funzione della reazione su cui si
Nanoparticelle - Presentazione. Presentazione. Nanoparticelle metalliche. NanoLab - Le nanoscienze a scuola -
 Presentazione Nanoparticelle metalliche Colore e visione Ossidoriduzioni - Elettroliti Principi di spettroscopia Interazione luce - materia Sensori colorimetrici Diffusione di particelle in un solido Nanoscienze,
Presentazione Nanoparticelle metalliche Colore e visione Ossidoriduzioni - Elettroliti Principi di spettroscopia Interazione luce - materia Sensori colorimetrici Diffusione di particelle in un solido Nanoscienze,
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
1.2.5 Titolazioni acido-base
 1.2.5 Titolazioni acidobase Queste titolazioni si basano su reazioni di neutralizzazione in cui un acido cede un protone ad una base capace di accettarlo. Nel caso più semplice di un acido forte (es. HCl)
1.2.5 Titolazioni acidobase Queste titolazioni si basano su reazioni di neutralizzazione in cui un acido cede un protone ad una base capace di accettarlo. Nel caso più semplice di un acido forte (es. HCl)
Abbiamo scoperto che la luce viaggia IN LINEA RETTA
 Abbiamo scoperto che la luce viaggia IN LINEA RETTA Scuola primaria «Calvino» - Moncalieri - Laboratorio "LUCE E VISIONE" con Rosanna Petiti e Angela Cane 1 Abbiamo provato a far passare la luce di una
Abbiamo scoperto che la luce viaggia IN LINEA RETTA Scuola primaria «Calvino» - Moncalieri - Laboratorio "LUCE E VISIONE" con Rosanna Petiti e Angela Cane 1 Abbiamo provato a far passare la luce di una
LE STELLE. LE DISTANZE ASTRONOMICHE Unità astronomica = distanza media Terra-Sole ( km)
 LE STELLE LE DISTANZE ASTRONOMICHE Unità astronomica = distanza media Terra-Sole (149 600 000 km) Anno luce = distanza percorsa in un anno dalla luce, che viaggia ad una velocità di 300 000 km/sec. (9
LE STELLE LE DISTANZE ASTRONOMICHE Unità astronomica = distanza media Terra-Sole (149 600 000 km) Anno luce = distanza percorsa in un anno dalla luce, che viaggia ad una velocità di 300 000 km/sec. (9
Farmacopea Europea (European Pharmacopeia)
 LA FARMACOPEA Le Farmacopea Ufficiale della Repubblica Italiana (XII edizione) era un codice farmaceutico, cioè un insieme di disposizioni tecniche ed amministrative rivolte a permettere il controllo della
LA FARMACOPEA Le Farmacopea Ufficiale della Repubblica Italiana (XII edizione) era un codice farmaceutico, cioè un insieme di disposizioni tecniche ed amministrative rivolte a permettere il controllo della
1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di
 Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
A Cosa serve l'ottica?
 A Cosa serve l'ottica? Chiara Vitelli Master Class di Ottica 6 Marzo 2012 Che cos'è l'ottica? Dal mouse wireless al lettore blue ray, gran parte della tecnologia che condiziona la nostra vita si basa sull'ottica.
A Cosa serve l'ottica? Chiara Vitelli Master Class di Ottica 6 Marzo 2012 Che cos'è l'ottica? Dal mouse wireless al lettore blue ray, gran parte della tecnologia che condiziona la nostra vita si basa sull'ottica.
Distribuito da: Lambré Srl Via Isonzo, Altavilla Vicentina (VI) Tel:
 Distribuito da: Lambré Srl Via Isonzo, 26 36077 Altavilla Vicentina (VI) Tel: +39 0444 276258 e-mail: info@lambrenature.com I COLORI, LA NOSTRA PASSIONE Una Selezione dalla Natura Rendere un prodotto alimentare
Distribuito da: Lambré Srl Via Isonzo, 26 36077 Altavilla Vicentina (VI) Tel: +39 0444 276258 e-mail: info@lambrenature.com I COLORI, LA NOSTRA PASSIONE Una Selezione dalla Natura Rendere un prodotto alimentare
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
Spettroscopia. 05/06/14 SPET.doc 0
 Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Verifica della fermentazione alcolica
 ALUNNO: Stefano Vicino CLASSE: 2 G DATA: 11/11/2011 ESPERIMENTO N : 1 TITOLO: Verifica della fermentazione alcolica SCOPO: > Verificare lo svolgimento della fermentazione alcolica da parte del Saccharomyces
ALUNNO: Stefano Vicino CLASSE: 2 G DATA: 11/11/2011 ESPERIMENTO N : 1 TITOLO: Verifica della fermentazione alcolica SCOPO: > Verificare lo svolgimento della fermentazione alcolica da parte del Saccharomyces
COLORANTI ALIMENTARI IDROSOLUBILI (Conformi al regolamento CE n 1333/2008)
 COLORANTI ALIMENTARI IDROSOLUBILI F.33.2599.0000 E100 CURCUMINA E100 F.22.2156.0000 CURCUMA Estratti vegetali F.33.3343.0000 GIALLO UOVO LIQUIDO NATURALE UNV/1 E160a, estratti vegetali F.33.7790.0000 GIALLO
COLORANTI ALIMENTARI IDROSOLUBILI F.33.2599.0000 E100 CURCUMINA E100 F.22.2156.0000 CURCUMA Estratti vegetali F.33.3343.0000 GIALLO UOVO LIQUIDO NATURALE UNV/1 E160a, estratti vegetali F.33.7790.0000 GIALLO
Assorbimento UV-visibile di sostanze coloranti per uso alimentare
 Universit egli tudi di Parma cienze e Tecnologie Chimiche 1 ntroduzione Assorbimento UVvisibile di sostanze coloranti per uso alimentare La luce bianca contiene tutti i colori. n altre parole, contiene
Universit egli tudi di Parma cienze e Tecnologie Chimiche 1 ntroduzione Assorbimento UVvisibile di sostanze coloranti per uso alimentare La luce bianca contiene tutti i colori. n altre parole, contiene
Formazione di complessi
 Formazione di complessi Struttura degli ioni complessi Gli ioni complessi sono formati da un catione metallico legato ad anioni come OH -, Cl -, CN -, SCN -, o a molecole neutre come H 2 O, NH 3., detti
Formazione di complessi Struttura degli ioni complessi Gli ioni complessi sono formati da un catione metallico legato ad anioni come OH -, Cl -, CN -, SCN -, o a molecole neutre come H 2 O, NH 3., detti
L acqua e il legame idrogeno
 Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Diapositive n. 3, 4 Ma quali sono le proprietà degli acidi e delle basi?
 it Acidi e basi. Diapositiva n. 2 La parola acido viene dal latino acidum che significa aspro, pungente. La parola alcali (le parole alcali e basi sono sinonimi) viene dall arabo al-qalì che sta ad indicare
it Acidi e basi. Diapositiva n. 2 La parola acido viene dal latino acidum che significa aspro, pungente. La parola alcali (le parole alcali e basi sono sinonimi) viene dall arabo al-qalì che sta ad indicare
Esperienze di laboratorio sulla variazione del colore delle foglie
 Esperienze di laboratorio sulla variazione del colore delle foglie In primavera il colore più comune nel mondo della natura è il verde. La sua dominanza è dovuta soprattutto alle foglie delle piante. Esperienza
Esperienze di laboratorio sulla variazione del colore delle foglie In primavera il colore più comune nel mondo della natura è il verde. La sua dominanza è dovuta soprattutto alle foglie delle piante. Esperienza
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
Capitolo 2 La chimica della vita
 Capitolo 2 La chimica della vita Atomi e molecole 2.1 Le proprietà caratteristiche dei viventi si possono osservare a ogni livello della loro struttura gerarchica Le strutture biologiche hanno un organizzazione
Capitolo 2 La chimica della vita Atomi e molecole 2.1 Le proprietà caratteristiche dei viventi si possono osservare a ogni livello della loro struttura gerarchica Le strutture biologiche hanno un organizzazione
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
-DEFINIZIONE DI ACIDI E BASI-
 -DEFINIZIONE DI ACIDI E BASI- DEFINIZIONE DI ARRHENIUS ACIDO: rilascia ioni H + HCl H + + Cl - BASE: rilascia ioni OH - NaOH Na + + OH - DEFINIZIONE DI BRÖNSTED ACIDO: rilascia ioni H + BASE: lega ioni
-DEFINIZIONE DI ACIDI E BASI- DEFINIZIONE DI ARRHENIUS ACIDO: rilascia ioni H + HCl H + + Cl - BASE: rilascia ioni OH - NaOH Na + + OH - DEFINIZIONE DI BRÖNSTED ACIDO: rilascia ioni H + BASE: lega ioni
Orticoltura e Floricoltura
 Corso di laurea in Scienze e Tecnologie Agrarie Anno accademico 2017/2018 Orticoltura e Floricoltura In questa lezione Misurare il colore degli ortaggi COSA SI INTEDE PER COLORE? Aspetto cromatico che
Corso di laurea in Scienze e Tecnologie Agrarie Anno accademico 2017/2018 Orticoltura e Floricoltura In questa lezione Misurare il colore degli ortaggi COSA SI INTEDE PER COLORE? Aspetto cromatico che
Progetto Il tessile per me a.s. 2018/2019 ISIS VALDARNO
 Progetto Il tessile per me a.s. 2018/2019 ISIS VALDARNO Tinte intorno a noi: nell orto, in giardino, in cucina. Nel giardino della nostra scuola ci sono molti alberi ornamentali, dei susini dalle foglie
Progetto Il tessile per me a.s. 2018/2019 ISIS VALDARNO Tinte intorno a noi: nell orto, in giardino, in cucina. Nel giardino della nostra scuola ci sono molti alberi ornamentali, dei susini dalle foglie
Soluzioni Acido Base Definizione di Brønsted
 acido + base sale + acqua Soluzioni Acido Base Definizione di Brønsted acido: sostanza capace di donare protoni* HCl + H 2 O Cl + H 3 O + * In soluzione, il protone esiste in forma idratata (H 3 O + )
acido + base sale + acqua Soluzioni Acido Base Definizione di Brønsted acido: sostanza capace di donare protoni* HCl + H 2 O Cl + H 3 O + * In soluzione, il protone esiste in forma idratata (H 3 O + )
Le membrane dei tilacoidi sono la sede delle reazioni alla luce della fotosintesi
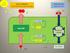 Grazie infatti all energia della luce solare, alcuni elettroni vengono pompati su lungo due forti dislivelli energetici (prima nel fotosistema II e poi nel fotosistema I) e, nel ridiscendere, liberano
Grazie infatti all energia della luce solare, alcuni elettroni vengono pompati su lungo due forti dislivelli energetici (prima nel fotosistema II e poi nel fotosistema I) e, nel ridiscendere, liberano
Light Amplification by Stimulated Emission of Radiation
 Laser? Light Amplification by Stimulated Emission of Radiation Produce un fascio coerente di radiazione ottica da una stimolazione elettronica, ionica, o transizione molecolare a più alti livelli energetici
Laser? Light Amplification by Stimulated Emission of Radiation Produce un fascio coerente di radiazione ottica da una stimolazione elettronica, ionica, o transizione molecolare a più alti livelli energetici
INCHIOSTRI SPECIALI PER TIMBRI
 INCHIOSTRI SPECIALI PER TIMBRI 4010 inchiostro per timbri in gomma e polimero per timbrare su carta disponibile nei colori nero, blu, viola, rosso, verde fornito in flaconi da 28 ml confezionati in scatole
INCHIOSTRI SPECIALI PER TIMBRI 4010 inchiostro per timbri in gomma e polimero per timbrare su carta disponibile nei colori nero, blu, viola, rosso, verde fornito in flaconi da 28 ml confezionati in scatole
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Reazione chimica In una reazione chimica le sostanze di partenza sono dette reagenti; le sostanze che si ottengono sono dette prodotti della reazione.
 Reazioni chimiche Reazione chimica Tutte le volte che una o più sostanze si trasformano in altre si verifica una reazione chimica. Una reazione chimica è il processo che porta alla rottura di alcuni legami
Reazioni chimiche Reazione chimica Tutte le volte che una o più sostanze si trasformano in altre si verifica una reazione chimica. Una reazione chimica è il processo che porta alla rottura di alcuni legami
Anno Scolastico 2015 / 2016 Prof. Paolo Beretti. i Colori
 Anno Scolastico 2015 / 2016 Prof. Paolo Beretti i Colori 1. L ARCOBALENO Nella seconda metà del XVII secolo (1665-1676) lo scienziato inglese Isaac Newton proiettò un raggio di luce bianca attraverso un
Anno Scolastico 2015 / 2016 Prof. Paolo Beretti i Colori 1. L ARCOBALENO Nella seconda metà del XVII secolo (1665-1676) lo scienziato inglese Isaac Newton proiettò un raggio di luce bianca attraverso un
ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione
![ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione](/thumbs/57/40353116.jpg) ESERCIZI 1) Il prodotto ionico dell acqua (K w ) vale 10-14 : a. a qualunque temperatura b. solo per una soluzione acida c. solo per una soluzione basica d. solo a T = 25 C 2) Per l acqua pura risulta
ESERCIZI 1) Il prodotto ionico dell acqua (K w ) vale 10-14 : a. a qualunque temperatura b. solo per una soluzione acida c. solo per una soluzione basica d. solo a T = 25 C 2) Per l acqua pura risulta
LUCE E OSSERVAZIONE DEL COSMO
 LUCE E OSSERVAZIONE DEL COSMO ALUNNI CLASSI QUINTE SAN BERARDO Ins. DE REMIGIS OSVALDO Ins.SANTONE M. RITA CHE COS E LA LUCE? Perché vediamo gli oggetti? Che cos è la luce? La propagazione della luce
LUCE E OSSERVAZIONE DEL COSMO ALUNNI CLASSI QUINTE SAN BERARDO Ins. DE REMIGIS OSVALDO Ins.SANTONE M. RITA CHE COS E LA LUCE? Perché vediamo gli oggetti? Che cos è la luce? La propagazione della luce
REAZIONE ACIDO PERIODICO-reattivo di SCHIFF (PAS) PRINCIPI SU CUI SI BASA LA REAZIONE
 Metodo del PAS REAZIONE ACIDO PERIODICO-reattivo di SCHIFF (PAS) PRINCIPI SU CUI SI BASA LA REAZIONE Questa reazione fu introdotta in istochimica da Mc Manus successivamente elaborata da altri Autori (Lillie,
Metodo del PAS REAZIONE ACIDO PERIODICO-reattivo di SCHIFF (PAS) PRINCIPI SU CUI SI BASA LA REAZIONE Questa reazione fu introdotta in istochimica da Mc Manus successivamente elaborata da altri Autori (Lillie,
Amministrazione, finanza e marketing - Turismo Ministero dell Istruzione, dell Università e della Ricerca PROGRAMMAZIONE DISCIPLINARE PER U. di A.
 MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
Chimica SM 032. Informazioni sul corso
 Chimica SM 032 Informazioni sul corso Chimica (6 CFU) Docente : Jan Kašpar e-mail: kaspar@units.it tel. 040 5583960 Ed. C11 V piano - stanza 504 home page corso: www.dsch.units.it e seguire link phone
Chimica SM 032 Informazioni sul corso Chimica (6 CFU) Docente : Jan Kašpar e-mail: kaspar@units.it tel. 040 5583960 Ed. C11 V piano - stanza 504 home page corso: www.dsch.units.it e seguire link phone
CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq) + H 2 O (l)
 2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero Le soluzioni La diluizione è il procedimento per preparare una soluzione meno concentrata da una soluzione più concentrata. Diluizione Aggiungi Solvente
La Vita è una Reazione Chimica Acqua Oro Zucchero Le soluzioni La diluizione è il procedimento per preparare una soluzione meno concentrata da una soluzione più concentrata. Diluizione Aggiungi Solvente
MA NON è UNA PAROLACCIA!!!
 MA NON è UNA PAROLACCIA!!! Abbiamo incontrato il professor Roberto Saettone che ci ha raccontato un sacco di cose interessanti sulla chimica. Abbiamo scoperto che la CHIMICA è dappertutto! Tutto è fatto
MA NON è UNA PAROLACCIA!!! Abbiamo incontrato il professor Roberto Saettone che ci ha raccontato un sacco di cose interessanti sulla chimica. Abbiamo scoperto che la CHIMICA è dappertutto! Tutto è fatto
