Calore Latente di Fusione
|
|
|
- Gilda Giuliani
- 7 anni fa
- Visualizzazioni
Transcript
1 Calore Latente di Fusione Obiettivo Con questa attività ci si propone di studiare il processo di trasferimento di calore all interno di un sistema termodinamico mentre avviene la fusione di un pezzo di ghiaccio immerso in acqua. L'esperimento consiste nell'osservare il grafico della temperatura dell acqua durante il passaggio di stato di una determinata massa di ghiaccio. I dati raccolti con una calcolatrice grafica vengono analizzati usando la curva esponenziale della legge del raffreddamento ed il modello per il trasferimento di calore durante i passaggi di stato. Viene anche stimato il valore del calore latente di fusione dell'acqua. Contenuti Aspetti Teorici Apparato Sperimentale Acquisizione Dati (TI83) Analisi Dati (TI83) Analisi Dati (Excel) Aspetti Teorici Passaggi di stato dovuti al trasferimento di energia termica Il trasferimento di energia termica può causare variazioni molto significative nella struttura interna di un materiale e può portare al passaggio ad un differente stato di aggregazione della materia. Il passaggio da una fase all'altra è detto transizione di fase. Esempi di transizione di fase sono i passaggi di stato liquido-gassoso, liquido-solido, solido-gas. Per una data sostanza ogni passaggio di stato (ad una data pressione) avviene ad una ben definita temperatura, in cui si ha la coesistenza delle due fasi differenti. Lo scambio di calore non provoca variazioni di temperatura finchè la transizione di fase non è conclusa. La quantità di energia termica necessaria per la transizione di fase solido-liquido per unità di massa di una data sostanza è detta calore latente di fusione di quella sostanza e si indica con L[J/kg]. Il calore di fusione di un materiale dipende anche dalla pressione. La quantità di energia termica (calore) Q m necessaria per fondere una massa m di una data sostanza è data dall'equazione 1: (1) 1
2 La figura 1 mostra l'andamento della temperatura e lo stato fisico di una sostanza quando viene fornita in modo continuo dell'energia termica. Si parte dallo stato solido: la temperatura aumenta sino ad arrivare ad una temperatura ben definita, detta "temperatura di fusione"; a questo punto l'energia assorbita non provoca un ulteriore aumento di temperatura, ma un passaggio di fase da solido-liquido. Quando tutta la massa è passata allo stato liquido la temperatura riprende ad aumentare. Quindi il liquido aumenta di temperatura sino ad arrivare ad un'altra temperatura caratteristica (punto di ebollizione) alla quale inizia la transizione di fase liquido-gas. Di nuovo si osserva che un trasferimento continuo di energia termica non provoca ulteriori aumenti di temperatura ma un passaggio di fase. Fig.1. Variazioni di temperatura di un campione d'acqua sottoposto a riscaldamento. Quando oggetti di temperatura diversa sono posti in contatto (per esempio mischiati) scambiano energia termica. Il corpo caldo cede calore a quello freddo. Il processo continua sino al raggiungimento dell'equilibrio termico (puoi vedere anche il modulo Equilibrio termico tra due corpi). Se il sistema è isolato termicamente e non scambia calore con l'ambiente circostante la quantità di calore persa dal corpo caldo Q i eguaglia quella acquisita dal corpo freddo Q g. Questa è una situazione ideale molto difficile da realizzare nella pratica. Anche usando appositi strumenti da laboratorio (calorimetri) si verifica comunque una piccolo scambio di calore con l'ambiente. La temperatura del contenuto del calorimetro tende comunque a raggiungere la temperatura ambiente. Se inizialmente è più alta tende a diminuire seguendo un andamento esponenziale (puoi vedere anche il modulo sulla Legge del Raffreddamento di Newton)). Se si vuol fare una misura calorimetrica accurata occorre tener conto di questi scambi di calore. Metodi calorimetrici per la determinazione del Calore Latente di Fusione Il calore latente di fusione dell'acqua (o meglio del ghiaccio)l può essere misurato immergendo alcuni pezzi di ghiaccio (che si trovano esattamente alla temperatura di fusione, 0 C)all'interno di un calorimetro che contiene una quantità nota di acqua alla temperatura iniziale T 1. Il calore fluisce dall'acqua al ghiaccio ed il ghiaccio inizia a sciogliersi. Al termine del processo la miscela raggiunge la temperatura finale T 2. Tutte le parti del calorimetro prendono parte a questo processo di trasferimento di calore. Perciò dobbiamo includere la quantità di calore perso Q C nel bilancio energetico. 2
3 L'energia totale ceduta Q l può essere espressa come la somma di due parti: il calore perso dall'acqua Q W, la cui quantità è data dall'equazione 2: (2) dove: m W è la massa dell'acqua contenuta inizialmente nel calorimetro c W è il calore specifico dell'acqua T 1 è la temperatura iniziale del calorimetro con dentro l'acqua T 2 è la temperatura finale all'interno del calorimetro il calore perduto dal calorimetro Q C, che è dato da: (3) dove: m C è la massa del contenitore e del supporto isolante del calorimetro c C è il calore specifico del materiale del quale è fatto il calorimetro T 1 è la temperatura iniziale del calorimetro con l'acqua T 2 è la temperatura finale all'interno del calorimetro L'energia termica totale assorbita Q g consiste di: il calore assorbito dal ghiaccio ed utilizzato per la transizione di fase Q m, che è dato dall'equazione 5: (5) dove: m i è la massa del ghiaccio L è il calore latente di fusione il calore assorbito dall'acqua generata dalla fusione del ghiaccio Q i, che è dato dall'equazione 6: (6) dove: m i è la massa di ghiaccio c w è il calore latente di fusione dell'acqua T 0 è la temperatura del punto di fusione dell'acqua T 2 è la temperatura finale del contenuto del calorimetro Perciò l'energia totale assorbita è data dall'equazione 7: 3
4 Assumendo che il contenuto del calorimetro si trovi termicamente isolato, l'energia termica ceduta Q l eguaglia l'energia termica assorbita Q g : (7) e: (8) Il Calore Latente di Fusione L può essere ricavato dall'equazione 9 come: (9) Quindi misurando la temperatura del contenuto di un calorimetro di massa nota riempito con una quantità nota di acqua, conoscendo la quantità di ghiaccio che viene immessa, si può calcolare il calore latente di fusione del ghiaccio. La figura 2 mostra l'andamento teorico previsto. Il ghiaccio viene immerso nell'acqua all'istante t 0. Prima del momento t 0 la temperatura è costante. Quando si immerge il ghiaccio dell'energia termica viene impiegata per sciogliere il ghiaccio e l'acqua viene raffreddata dal ghiaccio fuso. Così la temperatura della miscela diminuisce. Lo scambio di calore cessa quando la temperatura assume un valore ben definito. (10) Fig.2. Variazioni di temperatura durante la fusione. Caso ideale senza raffreddamento. 4
5 In pratica però non si ottiene mai questo andamento perché il calorimetro partecipa agli scambi di calore; il grafico della temperatura è diverso da quello ideale. Prima dell'immersione del ghiaccio la temperatura comunque diminuisce seguendo la legge esponenziale del raffreddamento. Dell'energia termica viene trasferita all'ambiente in modo continuo sia durante la fusione del ghiaccio che successivamente. Il grafico che si ottiene è mostrato in figura 3. L'equazione 10 richiede due valori della temperatura: quella iniziale T 1 e quella finale T 2 dopo che il ghiaccio è fuso e l'intero contenuto del calorimetro è ad una temperatura uniforme. Questi valori possono essere stimati con una costruzione geometrica. Si possono estrapolare le due parti e si può tracciare una linea verticale in modo da bilanciare le due aree definite dal grafico. I punti di intersezione con le linee estrapolate ci danno i valori della temperatura ricercati per l'equazione precedente. Fig.3. Variazione della temperatura durante la fusione. Caso reale con raffreddamento. 5
6 Apparato Sperimentale L apparato sperimentale è mostrato nella foto della prima pagina. I valori della temperatura sono stati acquisiti facendo uso di un apparato sperimentale molto semplice che consiste di un calorimetro di alluminio ed di un agitatore elettromagnetico, come mostrato in figura 4. La sonda che abbiamo usato è un semplice sensore a semiconduttore che immerso nel contenitore del calorimetro, misura i valori della temperatura. Il calorimetro minimizza gli scambi di calore con l'esterno, mentre l'agitatore serve per rendere uniforme la temperatura del contenuto del calorimetro. La bilancia da laboratorio serve per determinare la massa del calorimetro, dell'acqua e del ghiaccio. I materiali e gli strumenti necessari sono: Fig.4. Calorimeter. un calorimetro di alluminio con un alloggiamento per la sonda, vedi foto. un agitatore elettromagnetico, vedi foto bilancia di laboratorio (portata 200 gr), vedi foto acqua calda (100 gr) alcuni pezzi di giaccio (circa 20 gr) una interfaccia CBL o CBL2, vedi foto una sonda di temperatura (sonda standard in dotazione col CBL)), vedi foto. una calcolatrice grafica TI83 Plus, TI83 Plus SE, TI89, TI92, TI92 Plus, TI Voyage 200 un cavo di collegamento standard, vedi foto. il programma LHEATF disponibile qui: LHEATF un cavo TI-GRAPH LINK TM (opzionale) e il programma un PC con il programma TI Connect TM software (opzionale) - description: download: Note pratiche sulla predisposizione dell'apparato La sonda di temperatura deve essere collegata al canale CH1 del CBL. La temperatura iniziale dell'acqua deve essere di circa gradi superiore alla temperatura ambiente. Il ghiaccio deve essere tenuto per un po' di tempo fuori dal freezer per raggiungere la temperatura di fusione. La sonda di temperatura deve stare sempre immersa nell'acqua contenuta nel calorimetro. E' bene che il coperchio del calorimetro sia isolato termicamente. L'agitatore elettromagnetico deve stare sempre in azione per tutto l'esperimento per avere una temperatura uniforme della miscela contenuta nel calorimetro. 6
7 Acquisizione Dati (TI 83) L'esperimento consiste nella misura della temperatura in funzione del tempo dell'acqua contenuta in un calorimetro. Le variazioni di temperatura sono dovute sia alla perdita di calore nell'ambiente circostante che, sopratutto, all'assorbimento di calore da parte del ghiaccio che assorbe energia termica durante il passaggio di stato. E' necessario inoltre misurare la masse del contenitore del calorimetro, dell'acqua e del ghiaccio. L'acquisizione dati è controllata dal programma LHEATF che deve essere trasferito sulla calcolatrice prima di iniziare l'esperimento. Se hai bisogno di informazioni per compiere questa operazione, trovi sul CD o sul sito una finestra di aiuto. Operazioni preliminari: Pesa, utilizzando una bilancia da laboratorio, il contenitore del calorimetro con la barretta dell'agitatore. Annota il valore della massa m C. Accerta di che materiale è fatto il contenitore del calorimetro. Riempi il contenitore del calorimetro per circa metà del suo volume con dell'acqua, possibilmente distillata. Pesa nuovamente il contenitore, con dentro l'acqua e la barretta dell'agitatore. Calcola la massa d'acqua - m w. Scalda il contenitore con l'acqua sino a raggiungere una temperatura tra 40 e 50 o C. Puoi usare un riscaldatore elettrico oppure riempire direttamente il contenitore con acqua calda. Inserisci il contenitore nel calorimetro e coprilo con l'apposito coperchio. Inserisci la sonda di temperatura, facendo attenzione che sia immersa nell'acqua. Connetti la sonda al CBL e il CBL alla calcolatrice. Con questo video puoi vedere i dettagli della fase di preparazione. Raccolta Dati Avvia il programma LHEATF selezionandolo dal menù PRGM. Scegli l'opzione 1: COLLECT DATA dal menù principale. Imposta i valori della temperatura minima e massima per il grafico della temperatura. Questi valori non influiscono sull'acquisizione dei dati ma solo sulla visualizzazione durante la misura. Imposta la durata dell'esperimento espressa in secondi. Occorre considerare un tempo di 5-15 minuti prima e dopo la transizione di fase. Imposta l'intervallo di campionamento in secondi quando il programma lo richiede. Poiché la temperatura dell'acqua varia rapidamente durante la transizione di fase, suggeriamo di campionare ogni 5 secondi. Introduci la velocità di riferimento della variazione di temperatura R, quando il programma lo richiede. Il valore di riferimento non deve essere superiore a R è definito dall'equazione 11. Il valore R è usato dal programma LHEATF per registrare o escludere i punti sperimentali. Verranno registrati solo quei punti per i quali R è superiore al valore di riferimento, ossia quelli per i quali c'è un una significativa variazione della temperatura. Questa procedura è utile per occupare meno memoria sulla calcolatrice, ma non è indispensabile. Sistema il calorimetro sull'agitatore elettromagnetico ed accendilo. L'agitatore serve perchè il liquido all'interno del contenitore abbia una temperatura uniforme. Controlla la posizione della sonda di temperatura ed inizia la raccolta dati premendo [ENTER]. Osserva il grafico sullo schermo della calcolatrice per qualche minuto. Il grafico viene aggiornato man mano che la temperatura diminuisce a causa degli scambi termici con l'esterno (Fig.). Prepara alcuni pezzi di ghiaccio di grandezza opportuna per le dimensioni del calorimetro. Lasciali fuori dal freezer. (11) 7
8 Dopo qualche minuto (da 3 a 5) immergi il ghiaccio nel calorimetro. Osserverai una rapida variazione di temperatura. (Fig.). Prosegui con la raccolta dati sino al termine del tempo stabilito per l'osservazione, al termine del quale il grafico finale verrà visualizzato sullo schermo. Temperature vs time Quindi scegli Quit dal menù principale per uscire dal programma. Pesa nuovamente il contenitore. Calcola la massa del ghiaccio m i. Sul CD o sul sito puoi trovare un video che mostra le varie fasi dell'esperimento. I dati sono registrati nella memoria della calcolatrice. 8
9 Dati Campione (TI 83) Parametri per la Raccolta e l'elaborazione Dati: Dati Campione - massa del calorimetro m C = kg - massa d'acqua m W = 0,08965kg - massa del ghiaccio m i = kg - calore latente per l'acqua c W = 4190 J/kgK - calore latente per l'alluminio c C = 910 J/kgK - durata totale della misura: 800 sec - intervallo di campionamento:5 sec - velocità di riferimento per la variazione di temperatura R= temperatura massima attesa: T max =50 o C - temperatura minima attesa: T min =20 o C - Istanti di tempo t, in secondi - Lista L 1 - Valori della Temperatura T in [ o C] - Lista L 2 IL programma LHEATF crea delle copie delle liste e le registra in due coppie liste ausiliarie: - I : istanti di tempo in secondi - Lista L 3 ; valori della temperatura T in [ o C] - Lista L 4 - II pair: istanti di tempo in secondi - Lista L 5 ; valori della temperatura T in [ o C] - Lista L 6 Queste liste possono essere usate per graficare ed analizzare i dati lasciando inalterate le liste dati originali L 1 e L 2. I dati sperimentali sono disponibili sul CD o sul sito anche in formato Excel 9
10 Analisi Dati (TI 83) I dati sono registrati nelle liste della calcolatrice: - Istanti di tempo t, in secondi - Lista L 1 - Valori della Temperatura T in [ o C] - Lista L 2 Il programma LHEATF crea delle coppie di liste ausiliarie: - I: Istanti di tempo t, in secondi L 3 ; Valori della Temperatura T in [ o C] - List L 4 - II: Istanti di tempo t, in secondi - List L 5 ; Valori della Temperatura T in [ o C] - List L 6 Queste liste possono essere usate per l'analisi grafica senza modificare i dati originali contenuti nelle liste L1 e L2. Un set di dati campione è disponibile sul CD e sul sito. Come trovare il valore delle temperature. Per calcolare il valore del calore latente di fusione con l'equazione 10 abbiamo bisogno dei valori della temperatura dell'acqua prima e dopo la transizione di fase, rispettivamente T 1 e T 2. A causa del continuo processo di scambio di calore con l'esterno il grafico reale differisce da quello teorico Le temperature T 1 e T 2 possono essere determinate dal grafico sperimentale col metodo della interpolazione geometrica. Il grafico può essere diviso in tre parti: prima, durante e dopo il cambiamento di fase nella transizione ghiaccio-acqua. Nella calcolatrice TI83 tale divisone può essere fatta selezionando i dati a partire dal grafico. Per far ciò conviene usare le liste ausiliarie L 3, L 4, L 5, L 6. Sul sito o sul CD puoi trovare altre figure che mostrano le schermate della calcolatrice nei vari passaggi. Per separare la parte iniziale della curva di raffreddamento. Definisci il Plot2 graficando L 3 in funzione di L 4 (Fig.). Usa la funzione Select dal [2nd] [LIST] menù (Fig.) e digita il nome delle liste (Fig.). Evidenzia il primo e l'ultimo punto del grafico (Fig.) Con questa operazione i dati nelle liste saranno sostituiti con i soli dati selezionati sul grafico. (10) 10
11 Estrapolazione della parte iniziale. Assumendo che il raffreddamento abbia un andamento esponenziale, effettuiamo una regressione esponenziale scegliendola dal menù [STAT] [CALC]. Dobbiamo digitare i nomi delle liste come argomenti della funzione ExpReg, insieme al nome della variabile nella quale vogliamo registrare l'equazione della regressione Y 1,. Sullo schermo vengono mostrati i valori dei parametri della funzione di regressione. Si possono sovrapporre ai dati sperimentali. In modo simile si possono isolare ed estrapolare i valori della parte finale usando le liste L 5 ed L 6. La seconda funzione di regressione viene registrata nella variabile Y 2 e graficata sul Plot3. Adesso si possono vedere insieme i dati originali e le funzioni di regressione (activate all plots ). Interpolazione delle temperature Le temperature T 1 e T 2 possono essere determinate dal grafico tracciando una linea verticale tale da bilanciare le due aree definite dalle curve di interpolazione. Seleziona la parte centrale del grafico con l'opzione ZBox del menù ZOOM (Fig.). Seleziona parte del grafico (Fig.). Usa l'opzione Vertical dal menù [DRAW] per tracciare la linea verticale (Fig.). Aggiusta la posizione della linea sino ad ottenere il bilanciamento delle aree (Fig.). Muovi il cursore sulla linea verticale per trovare il punto di intersezione con la prima parte della curva di raffreddamento, che potrai leggere sulla parte inferiore dello schermo. Registra il valore della temperatura T 1 come mostrato in figura. 11
12 Muovi il cursore sulla linea verticale per trovare il punto di intersezione con la parte finale della curva di raffreddamento. Annota il valore della temperatura T 2. Temperatura Iniziale T 1 Temperatura Finale T 2 Calcolo del Calore Latente di Fusione. Il valore del Calore di Fusione si può calcolare con l'equazione 10. Cerca il valore del calore specifico dell'acqua c w ( 4190 [J/kgK] e del materiale di cui è fatto il calorimetro c C (alluminio: 910 [J/kgK] ) sulle tavole. Usa i valori delle masse m w, m c, m i e dei calori specifici c w e c C nell'equazione 10. Il valore del calore latente di fusione ottenuto con i nostri dati sperimentali è pari a L =321 x 10 3 [J/kg]. Questo valore è vicino al valore tabulato: 334x10 3 [J/kg]. 12
13 Analisi Dati (Excel) Il documento MS Excel con i dati campione è disponibile sul CD o sul sito. Trasferimento dei dati sperimentali al computer I dati possono essere trasferiti dalla calcolatrice al PC usando il cavo TI GRAPH LINK ed il programma TI Connect TM che permette di visualizzare il contenuto della calcolatrice (TI DEVICE EXPLORER) e di editare i dati (TI DATA EDITOR). I dati sperimentali sono registrati sulla calcolatrice: - il tempo t in secondi è nella lista L 1 - la temperatura T nella [ o C] - lista L 2 I dettagli della procedura di trasferimento sono disponibili sul CD o sul sito. All'interno del programma TI Connect program - all'interno del menù TI DEVICE EXPLORER - si possono salvare le liste sul PC ed aprirle con TI DATA EDITOR. Analisi del grafico Crea un foglio di calcolo ed importa le liste. Costruisci il grafico a dispersione T (t), se hai bisogno è disponibile una finestra di aiuto qui. Temperatura in funzione del tempo: dati sperimentali. Determinazione delle temperature. Per calcolare il valore del calore latente di fusione con l'equazione 10 abbiamo bisogno dei valori della temperatura dell'acqua prima e dopo la transizione di fase, rispettivamente T 1 e T 2 (10) 13
14 A causa del continuo processo di scambio di calore con l'esterno il grafico reale differisce da quello teorico (Fig.). Le temperature T 1 e T 2 possono essere determinate dal grafico sperimentale col metodo della interpolazione geometrica come mostrato in figura (Fig.). Il grafico può essere diviso in tre parti: prima, durante e dopo il cambiamento di fase nella transizione ghiaccio-acqua. Nel foglio di calcolo MS Excel tale separazione si fa semplicemente selezionando parte di dati. Estrapolazione della parte iniziale e finale della curva di raffreddamento. Imposta un nuovo grafico a dispersione con i dati iniziali della curva. I punti possono essere interpolati con una curva esponenziale; applichiamo quindi un modello di regressione esponenziale aggiungendo ai dati sperimentali una linea di tendenza esponenziale. Sul grafico può essere mostrata la linea di tendenze e l'equazione. In modo simile possiamo agire sull'ultima parte dei dati. La parte centrale dei dati verrà usata per definire la terza parte del grafico. Interpolazione della temperatura Interpolazione delle temperature. Le temperature T 1 e T 2 possono essere detrminate tracciando una linea verticale in modo da bilanciare le due aree, come mostrato in figura Stima dal grafico la coordinata x per tracciare correttamente la linea verticale e annota questo valore in una celle del foglio di calcolo. Definisci una linea verticale T(t) con una coppia di coordinate. Definisci una colonna che rappresenta i valori del tempo copiando il contenuto della cella di riferimento. Aggiungi al grafico una quarta serie di dati, in modo da visualizzare la linea verticale - in rosso nel nostro grafico. Aggiusta la posizione della linea verticale sino ad ottenere il bilanciamento delle aree. In questo modo, utilizzando la funzione esponenziale si individuano le due temperature T 1 e T 2. 14
15 Calcolo del calore latente di fusione. Il calore latente di fusione si ottiene alla equazione eq.10. Cerca il valore del calore specifico dell'acqua c w ( 4190 [J/kgK] e del materiale di cui è costituito il calorimetro c C (nel nostro caso allumnio 910 [J/kgK] ) su un manuale. Sostituisci i valori della massa m w, m c, m i e del calore specifico c w c C nell'equazione10. Risultati del calcolo Il valore del calore latente di fusione dell'acqua così come risulta dai dati sperimentali risulta quindi: L =333 x 10 3 [J/kg]. Questo valore è molto vicino a quello riportato in letteratura pari a : 334x10 3 [J/kg]. Note: L'analisi numerica completa è disponibile all'interno del foglio Excel. 15
Onde Stazionarie
 Onde Stazionarie www.lepla.eu Obiettivo L'obiettivo di questo esperimento è analizzare l'impulso sonoro che si genera battendo, per esempio con un dito, un tubo di cartone. Cosa accade? quali sono le sue
Onde Stazionarie www.lepla.eu Obiettivo L'obiettivo di questo esperimento è analizzare l'impulso sonoro che si genera battendo, per esempio con un dito, un tubo di cartone. Cosa accade? quali sono le sue
MISURE DI CALORIMETRIA
 MISURE DI CALORIMETRIA L esperienza comprende tre parti: Determinazione del calore specifico di alcuni materiali Verifica del valore della costante di Joule J. Misura del calore latente di fusione del
MISURE DI CALORIMETRIA L esperienza comprende tre parti: Determinazione del calore specifico di alcuni materiali Verifica del valore della costante di Joule J. Misura del calore latente di fusione del
LA TRASMISSIONE DEL CALORE NEI LIQUIDI: LE CORRENTI CONVETTIVE E IL COMPORTAMENTO ANOMALO DELL ACQUA
 LA TRASMISSIONE DEL CALORE NEI LIQUIDI: LE CORRENTI CONVETTIVE E IL COMPORTAMENTO ANOMALO DELL ACQUA PERSONAGGIO STORICO: Evangelista Torriccelli (1608-1647), discepolo di Galileo, è noto soprattutto per
LA TRASMISSIONE DEL CALORE NEI LIQUIDI: LE CORRENTI CONVETTIVE E IL COMPORTAMENTO ANOMALO DELL ACQUA PERSONAGGIO STORICO: Evangelista Torriccelli (1608-1647), discepolo di Galileo, è noto soprattutto per
CALDO O FREDDO? TEMPERATURA, CALORE, SENSAZIONI TERMICHE
 CALDO O FREDDO? TEMPERATURA, CALORE, SENSAZIONI TERMICHE PERSONAGGIO STORICO: JOHN LOCKE Ludwig Eduard Boltzmann (Vienna, 20 febbraio 1844 - Duino, Trieste, 5 settembre 1906)) è stato uno dei più grandi
CALDO O FREDDO? TEMPERATURA, CALORE, SENSAZIONI TERMICHE PERSONAGGIO STORICO: JOHN LOCKE Ludwig Eduard Boltzmann (Vienna, 20 febbraio 1844 - Duino, Trieste, 5 settembre 1906)) è stato uno dei più grandi
CALORIMETRO DELLE mescolanze
 CALORIMETRO DELLE mescolanze Scopo dell esperienza è la misurazione del calore specifico di un corpo solido. Il funzionamento del calorimetro si basa sugli scambi di energia, sotto forma di calore, che
CALORIMETRO DELLE mescolanze Scopo dell esperienza è la misurazione del calore specifico di un corpo solido. Il funzionamento del calorimetro si basa sugli scambi di energia, sotto forma di calore, che
ELEMENTI DI DIDATTICA DELLA FISICA ESPERIENZA DI LABORATORIO SU CALORE E TEMPERATURA DI EQUILIBRIO A.A.
 ELEMENTI DI DIDATTICA DELLA FISICA ESPERIENZA DI LABORATORIO SU CALORE E TEMPERATURA DI EQUILIBRIO A.A. 2015-2016 Prof. Augusto Garuccio Tutor di Laboratorio: Dott.ssa Angela Laurora MISURE DI TEMPERATURE:
ELEMENTI DI DIDATTICA DELLA FISICA ESPERIENZA DI LABORATORIO SU CALORE E TEMPERATURA DI EQUILIBRIO A.A. 2015-2016 Prof. Augusto Garuccio Tutor di Laboratorio: Dott.ssa Angela Laurora MISURE DI TEMPERATURE:
Equilibrio Termico tra Due Corpi
 Equilibrio Termico tra Due Corpi www.lepla.eu OBIETTIVO L attività ha l obiettivo di fare acquisire allo sperimentatore la consapevolezza che: 1 il raggiungimento dell'equilibrio termico non è istantaneo
Equilibrio Termico tra Due Corpi www.lepla.eu OBIETTIVO L attività ha l obiettivo di fare acquisire allo sperimentatore la consapevolezza che: 1 il raggiungimento dell'equilibrio termico non è istantaneo
DETERMINAZIONE DELLA TEMPERATURA ED ENTALPIA DI FUSIONE DELLO STAGNO MEDIANTE CALORIMETRIA A SCANSIONE DIFFERENZIALE
 DETERMINAZIONE DELLA TEMPERATURA ED ENTALPIA DI FUSIONE DELLO STAGNO MEDIANTE CALORIMETRIA A SCANSIONE DIFFERENZIALE La tecnica della calorimetria a scansione differenziale (DSC) permette di effettuare
DETERMINAZIONE DELLA TEMPERATURA ED ENTALPIA DI FUSIONE DELLO STAGNO MEDIANTE CALORIMETRIA A SCANSIONE DIFFERENZIALE La tecnica della calorimetria a scansione differenziale (DSC) permette di effettuare
Attività A: masse d acqua uguali
 Interazioni termiche tra masse d'acqua e temperatura di equilibrio Negli esperimenti proposti in questa scheda un recipiente contenente acqua a temperatura maggiore viene posto in acqua a temperatura minore.
Interazioni termiche tra masse d'acqua e temperatura di equilibrio Negli esperimenti proposti in questa scheda un recipiente contenente acqua a temperatura maggiore viene posto in acqua a temperatura minore.
Legge del Raffreddamento di Newton
 Legge del Raffreddamento di Newton www.lepla.eu Obiettivo L'obiettivo di questo esperimento è studiare l'andamento temporale della temperatura di un oggetto che si raffredda e trovare un modello matematico
Legge del Raffreddamento di Newton www.lepla.eu Obiettivo L'obiettivo di questo esperimento è studiare l'andamento temporale della temperatura di un oggetto che si raffredda e trovare un modello matematico
CAPACITÀ TERMICA del CALORIMETRO e CALORE SPECIFICO di un COMPOSTO SOLIDO
 CAPACITÀ TERMICA del CALORIMETRO e CALORE SPECIFICO di un COMPOSTO SOLIDO Attività svolta con le classi 2^B/2^D nell anno scolastico 2007-08 Scopo dell esperienza L obiettivo dell esperimento é duplice
CAPACITÀ TERMICA del CALORIMETRO e CALORE SPECIFICO di un COMPOSTO SOLIDO Attività svolta con le classi 2^B/2^D nell anno scolastico 2007-08 Scopo dell esperienza L obiettivo dell esperimento é duplice
Determinazione del calore specifico dell alluminio con il calorimetro di Regnault
 Gruppo A2 XXX XXX XXX XXX Cesa Joshua 77685 Udine, 17/11/2006 Determinazione del calore specifico dell alluminio con il calorimetro di Regnault Oggetto della prova L oggetto della prova è di misurare la
Gruppo A2 XXX XXX XXX XXX Cesa Joshua 77685 Udine, 17/11/2006 Determinazione del calore specifico dell alluminio con il calorimetro di Regnault Oggetto della prova L oggetto della prova è di misurare la
In questo esperimento impariamo a calibrare un calorimetro e ad utilizzarlo per trovare il calore specifico di un solido metallico.
 1. Misura di calore specifico In questo esperimento impariamo a calibrare un calorimetro e ad utilizzarlo per trovare il calore specifico di un solido metallico. Materiali - un calorimetro con un volume
1. Misura di calore specifico In questo esperimento impariamo a calibrare un calorimetro e ad utilizzarlo per trovare il calore specifico di un solido metallico. Materiali - un calorimetro con un volume
Appunti di Excel per risolvere alcuni problemi di matematica (I parte) a.a
 Appunti di Excel per risolvere alcuni problemi di matematica (I parte) a.a. 2001-2002 Daniela Favaretto* favaret@unive.it Stefania Funari* funari@unive.it *Dipartimento di Matematica Applicata Università
Appunti di Excel per risolvere alcuni problemi di matematica (I parte) a.a. 2001-2002 Daniela Favaretto* favaret@unive.it Stefania Funari* funari@unive.it *Dipartimento di Matematica Applicata Università
temperatura ambientale massa totale d aria contenuta nella stanza temperatura raggiunta nella stanza dalla massa d aria pressione atmosferica
 Esercizio n.21 di pagina 26. L 1 = 6 m L 2 = 8 m L 3 = 10 m t 0F = 20 F M = 28.8 kg/kmol = 28.8 g/mol m =? t 1F = 75 F p a = 1.013 10 5 Pa temperatura ambientale massa molecolare media dell aria massa
Esercizio n.21 di pagina 26. L 1 = 6 m L 2 = 8 m L 3 = 10 m t 0F = 20 F M = 28.8 kg/kmol = 28.8 g/mol m =? t 1F = 75 F p a = 1.013 10 5 Pa temperatura ambientale massa molecolare media dell aria massa
[E] l energia occorrente per innalzare di 1 K la temperatura di 1 Mol di sostanza.
![[E] l energia occorrente per innalzare di 1 K la temperatura di 1 Mol di sostanza. [E] l energia occorrente per innalzare di 1 K la temperatura di 1 Mol di sostanza.](/thumbs/54/33206954.jpg) 1. Il calore specifico di una sostanza è: [A] La quantità di calore contenuta nella massa di una determinata sostanza; [B] la massima temperatura che la sostanza può raggiungere; [C] l energia occorrente
1. Il calore specifico di una sostanza è: [A] La quantità di calore contenuta nella massa di una determinata sostanza; [B] la massima temperatura che la sostanza può raggiungere; [C] l energia occorrente
DETERMINAZIONE DEL CALORE SPECIFICO
 DETERMINAZIONE DEL CALORE SPECIFICO Il calorimetro delle mescolanze è lo strumento usato per determinare i calori specifici e i calori latenti delle sostanze. Si tratta di un thermos con le pareti rivestire
DETERMINAZIONE DEL CALORE SPECIFICO Il calorimetro delle mescolanze è lo strumento usato per determinare i calori specifici e i calori latenti delle sostanze. Si tratta di un thermos con le pareti rivestire
Lezione 13: Calore e sua propagazione. Elementi di Fisica AA 2011/2012 Doc Claudia R. Calidonna
 Lezione 13: Calore e sua propagazione 1 Energia Interna L'energia interna di un sistema è la somma totale di tutta l'energia delle molecole presenti nel sistema. Include: Energia cinetica traslazionale
Lezione 13: Calore e sua propagazione 1 Energia Interna L'energia interna di un sistema è la somma totale di tutta l'energia delle molecole presenti nel sistema. Include: Energia cinetica traslazionale
La temperatura e il calore. Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 2/3
 La temperatura e il calore Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 2/3 Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti
La temperatura e il calore Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 2/3 Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti
 isidoro.sciarratta@alice.it vedere filmato eseguire esperimento isidoro.sciarratta@alice.it 2 isidoro.sciarratta@alice.it 3 isidoro.sciarratta@alice.it 4 isidoro.sciarratta@alice.it 5 isidoro.sciarratta@alice.it
isidoro.sciarratta@alice.it vedere filmato eseguire esperimento isidoro.sciarratta@alice.it 2 isidoro.sciarratta@alice.it 3 isidoro.sciarratta@alice.it 4 isidoro.sciarratta@alice.it 5 isidoro.sciarratta@alice.it
IL LAGO GHIACCIATO PERSONAGGIO STORICO
 IL LAGO GHIACCIATO Cosa succede ai pesci che stanno in un lago quando fuori fa molto freddo ed il lago congela? Per cercare di rispondere a questa domanda abbiamo costruito e studiato un modello che riproduce
IL LAGO GHIACCIATO Cosa succede ai pesci che stanno in un lago quando fuori fa molto freddo ed il lago congela? Per cercare di rispondere a questa domanda abbiamo costruito e studiato un modello che riproduce
Titolo: Fisica in cucina
 Titolo: Fisica in cucina Argomenti: Misure di temperatura, efficienza Tempo: 90 Minuti Età: 13-16 Differenziazione: Linee guida, supporti ICT, etc.: Se possibile, usare una termocamera - le immagini e
Titolo: Fisica in cucina Argomenti: Misure di temperatura, efficienza Tempo: 90 Minuti Età: 13-16 Differenziazione: Linee guida, supporti ICT, etc.: Se possibile, usare una termocamera - le immagini e
TERMODINAMICA. Studia le trasformazioni dei sistemi in relazione agli scambi di calore e lavoro. GENERALITÀ SUI SISTEMI TERMODINAMICI
 TERMODINAMICA Termodinamica: scienza che studia le proprietà e il comportamento dei sistemi, la loro evoluzione e interazione con l'ambiente esterno che li circonda. Studia le trasformazioni dei sistemi
TERMODINAMICA Termodinamica: scienza che studia le proprietà e il comportamento dei sistemi, la loro evoluzione e interazione con l'ambiente esterno che li circonda. Studia le trasformazioni dei sistemi
Determinazione del calore di combustione specifico di un pellet vegetale
 Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
La misura della temperatura
 Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Studio del movimento Spazio di frenata
 Studio del movimento Spazio di frenata www.lepla.eu Scopo di questo esperimento è mettere in relazione velocità e spazio di frenata. Anche se la maggior parte delle linee guida dei curriculi europei non
Studio del movimento Spazio di frenata www.lepla.eu Scopo di questo esperimento è mettere in relazione velocità e spazio di frenata. Anche se la maggior parte delle linee guida dei curriculi europei non
L ENERGIA CINETICA DELLE MOLECOLE DI UN GAS E LA TEMPERATURA Ogni molecola ha in media un'energia cinetica
 Primo principio- 1 - TERMODINAMICA ENERGIA INTERNA DI UN SISTEMA Ad ogni sistema fisico possiamo associare varie forme di energia, l energia cinetica delle molecole di cui è formato, energia potenziale,
Primo principio- 1 - TERMODINAMICA ENERGIA INTERNA DI UN SISTEMA Ad ogni sistema fisico possiamo associare varie forme di energia, l energia cinetica delle molecole di cui è formato, energia potenziale,
Esercitazione n 2. Costruzione di grafici
 Esercitazione n 2 Costruzione di grafici I grafici I grafici sono rappresentazione di dati numerici e/o di funzioni. Devono facilitare all utente la visualizzazione e la comprensione dei numeri e del fenomeno
Esercitazione n 2 Costruzione di grafici I grafici I grafici sono rappresentazione di dati numerici e/o di funzioni. Devono facilitare all utente la visualizzazione e la comprensione dei numeri e del fenomeno
Temperatura. Temperatura
 TERMOMETRIA E CALORE Che cos è la? Grandezza che misura l energia accumulata da un corpo come energia 2 La regola molti processi chimico fisici, quali ad esempio la formazione delle calotte polari, le
TERMOMETRIA E CALORE Che cos è la? Grandezza che misura l energia accumulata da un corpo come energia 2 La regola molti processi chimico fisici, quali ad esempio la formazione delle calotte polari, le
Calcolo del calore di fusione del ghiaccio
 Battistella Francesco 18/11/2011 Laboratorio di Fisica del Liceo Scientifico L. da Vinci Calcolo del calore di fusione del ghiaccio Materiale utilizzato: Calorimetro, termometro a mercurio, acqua, ghiaccio,
Battistella Francesco 18/11/2011 Laboratorio di Fisica del Liceo Scientifico L. da Vinci Calcolo del calore di fusione del ghiaccio Materiale utilizzato: Calorimetro, termometro a mercurio, acqua, ghiaccio,
Esercizi di termologia
 Esercizi di termologia L. Paolucci 4 dicembre 2009 Sommario Termologia: esercizi e problemi con soluzioni. Per la classe seconda. Anno Scolastico 2009/0. Versione: v Si ricordi che cal 4,86. Quindi il
Esercizi di termologia L. Paolucci 4 dicembre 2009 Sommario Termologia: esercizi e problemi con soluzioni. Per la classe seconda. Anno Scolastico 2009/0. Versione: v Si ricordi che cal 4,86. Quindi il
Studio del moto di una pallina che rimbalza!
 Corso di Fisica a Scienze Biologiche, AA 2014-15 Studio del moto di una pallina che rimbalza Con questo esperimento avrai modo di utilizzare il sistema di acquisizione dati costituito dalla calcolatrice
Corso di Fisica a Scienze Biologiche, AA 2014-15 Studio del moto di una pallina che rimbalza Con questo esperimento avrai modo di utilizzare il sistema di acquisizione dati costituito dalla calcolatrice
Calcolo dell errore sui coefficienti in una regressione lineare. Giacomo Torzo e Michele Impedovo
 Calcolo dell errore sui coefficienti in una regressione lineare. Giacomo Torzo e Michele Impedovo Se due grandezze x e y sono legate teoricamente da una formula, y = f(x, a i ), con M parametri a i che
Calcolo dell errore sui coefficienti in una regressione lineare. Giacomo Torzo e Michele Impedovo Se due grandezze x e y sono legate teoricamente da una formula, y = f(x, a i ), con M parametri a i che
Esperimentazioni di Fisica 1 Tracce delle lezioni di TERMOLOGIA
 Esperimentazioni di Fisica 1 Tracce delle lezioni di TERMOLOGIA AA 2015-2016 Temperatura Temperatura misura oggettiva della sensazione di caldo e freddo Grandezza intensiva Misura la direzione del trasferimento
Esperimentazioni di Fisica 1 Tracce delle lezioni di TERMOLOGIA AA 2015-2016 Temperatura Temperatura misura oggettiva della sensazione di caldo e freddo Grandezza intensiva Misura la direzione del trasferimento
SCHEDA PER LO STUDENTE LA LEGGE DI BOYLE AL LABORATORIO RTL
 SCHEDA PER LO STUDENTE LA LEGGE DI BOYLE AL LABORATORIO RTL I Titolo dell esperienza LA LEGGE DI BOYLE AL LABORATORIO RTL Autori Paola Cattaneo, Savina Ieni, Lorella Liberatori e Marco Litterio Docenti
SCHEDA PER LO STUDENTE LA LEGGE DI BOYLE AL LABORATORIO RTL I Titolo dell esperienza LA LEGGE DI BOYLE AL LABORATORIO RTL Autori Paola Cattaneo, Savina Ieni, Lorella Liberatori e Marco Litterio Docenti
INDICAZIONI TECNICHE TERMOCOPPIE
 INDICAZIONI TECNICHE TERMOCOPPIE 1. Principio di funzionamento 2. Metodi di misura con le termocoppie 3. Costruzione delle Termocoppie 4. Termocoppie ad isolamento tradizionale 5. Termocoppie ad isolamento
INDICAZIONI TECNICHE TERMOCOPPIE 1. Principio di funzionamento 2. Metodi di misura con le termocoppie 3. Costruzione delle Termocoppie 4. Termocoppie ad isolamento tradizionale 5. Termocoppie ad isolamento
Termodinamica e trasmissione del calore 3/ed Yunus A. Çengel Copyright 2009 The McGraw-Hill Companies srl
 RISOLUZIONI cap.11 11.1 Si devono determinare le masse dell'aria secca e del vapore acqueo contenuti in una stanza in condizioni specificate e a un'umidità relativa specificata. Ipotesi L'aria e il vapore
RISOLUZIONI cap.11 11.1 Si devono determinare le masse dell'aria secca e del vapore acqueo contenuti in una stanza in condizioni specificate e a un'umidità relativa specificata. Ipotesi L'aria e il vapore
Progetto lauree scientifiche Scheda 2 Studente:. Scuola e classe: Data:.. Programma DataStudio Sensore di moto PASPORT Interfaccia PASPORT-USB Link
 Progetto lauree scientifiche Scheda 2 Studente:. Scuola e classe: Data:.. Laboratorio Materiali Introduzione Programma DataStudio Sensore di moto PASPORT Interfaccia PASPORT-USB Link Userai un sensore
Progetto lauree scientifiche Scheda 2 Studente:. Scuola e classe: Data:.. Laboratorio Materiali Introduzione Programma DataStudio Sensore di moto PASPORT Interfaccia PASPORT-USB Link Userai un sensore
Cavo Carbonio. Sergio Rubio Carles Paul Albert Monte
 Cavo o Sergio Rubio Carles Paul Albert Monte o, Rame e Manganina PROPRIETÀ FISICHE PROPRIETÀ DEL CARBONIO Proprietà fisiche del o o Coefficiente di Temperatura α o -0,0005 ºC -1 o Densità D o 2260 kg/m
Cavo o Sergio Rubio Carles Paul Albert Monte o, Rame e Manganina PROPRIETÀ FISICHE PROPRIETÀ DEL CARBONIO Proprietà fisiche del o o Coefficiente di Temperatura α o -0,0005 ºC -1 o Densità D o 2260 kg/m
Problemi di Fisica La termologia
 MODELLO ATOMIO E AMBIAMENTI DI STATO Problemi di Fisica La termologia. MODELLO ATOMIO E AMBIAMENTI DI STATO Una massa di 2 kg di un solido non noto assorbe una quantità di calore pari a 18, 10. Sapendo
MODELLO ATOMIO E AMBIAMENTI DI STATO Problemi di Fisica La termologia. MODELLO ATOMIO E AMBIAMENTI DI STATO Una massa di 2 kg di un solido non noto assorbe una quantità di calore pari a 18, 10. Sapendo
COMPITO A. 4) Primo principio della termodinamica per sistemi chiusi ed aperti. 5)Teoremi di Carnot: enunciati ed esempi
 COMPITO A 1)In un vaso di alluminio, di massa m1, è contenuta la massa m2 di acqua di cui non si conosce la temperatura. Nell acqua si immerge un pezzo di rame di massa m3, riscaldato a t1 C e con ciò
COMPITO A 1)In un vaso di alluminio, di massa m1, è contenuta la massa m2 di acqua di cui non si conosce la temperatura. Nell acqua si immerge un pezzo di rame di massa m3, riscaldato a t1 C e con ciò
TERMODINAMICA Per lo studio scientifico di un problema occorre separare idealmente una regione di spazio limitata ( sistema ) da tutto ciò che la
 ERMODINAMICA Per lo studio scientifico di un problema occorre separare idealmente una regione di spazio limitata ( sistema ) da tutto ciò che la circonda e può influenzarne il comportamento ( ambiente
ERMODINAMICA Per lo studio scientifico di un problema occorre separare idealmente una regione di spazio limitata ( sistema ) da tutto ciò che la circonda e può influenzarne il comportamento ( ambiente
Il primo principio della termodinamica
 La termodinamica In molte reazioni viene prodotto o assorbito del calore. Altre reazioni possono essere usate per produrre del lavoro: il motore a scoppio produce energia meccanica sfruttando la reazioni
La termodinamica In molte reazioni viene prodotto o assorbito del calore. Altre reazioni possono essere usate per produrre del lavoro: il motore a scoppio produce energia meccanica sfruttando la reazioni
Bilancio di energia: il Primo Principio della Termodinamica. Termodinamica dell Ingegneria Chimica
 Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
Grafici. 1 Generazione di grafici a partire da un foglio elettronico
 Grafici In questa parte analizzeremo le funzionalità relative ai grafici. In particolare: 1. Generazione di grafici a partire da un foglio elettronico 2. Modifica di un grafico 1 Generazione di grafici
Grafici In questa parte analizzeremo le funzionalità relative ai grafici. In particolare: 1. Generazione di grafici a partire da un foglio elettronico 2. Modifica di un grafico 1 Generazione di grafici
Misura del rapporto Q/V durante la fase di carica di un Condensatore.
 Misura del rapporto Q/V durante la fase di carica di un Condensatore. Torino, Gennaio 27. Liceo Scientifico G. Bruno Testato grazie alla collaborazione della classe 5E Lorenzo Galante (lorenzo_galante@yahoo.it)
Misura del rapporto Q/V durante la fase di carica di un Condensatore. Torino, Gennaio 27. Liceo Scientifico G. Bruno Testato grazie alla collaborazione della classe 5E Lorenzo Galante (lorenzo_galante@yahoo.it)
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN CORPO SOLIDO
 SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN CORPO SOLIDO I Titolo dell esperienza N 2 DETERMINAZIONE DEL VOLUME E DELLA DENSITÀ DI UN CORPO SOLIDO IRREGOLARE Autori Prof.sse Fabbri Fiamma,
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN CORPO SOLIDO I Titolo dell esperienza N 2 DETERMINAZIONE DEL VOLUME E DELLA DENSITÀ DI UN CORPO SOLIDO IRREGOLARE Autori Prof.sse Fabbri Fiamma,
1. Studia la funzione che rappresenta la superficie del parallelepipedo in funzione del lato b della base quadrata e rappresentala graficamente;
 PROBLEMA 2: Il ghiaccio Il tuo liceo, nell'ambito dell'alternanza scuola lavoro, ha organizzato per gli studenti del quinto anno un attività presso lo stabilimento ICE ON DEMAND sito nella tua regione.
PROBLEMA 2: Il ghiaccio Il tuo liceo, nell'ambito dell'alternanza scuola lavoro, ha organizzato per gli studenti del quinto anno un attività presso lo stabilimento ICE ON DEMAND sito nella tua regione.
TERMOLOGIA & TERMODINAMICA I
 TERMOLOGIA & TERMODINAMICA I 1 Meccanica: studia il moto dei corpi e le cause che lo genera Grandezze meccaniche: massa, velocità, accelerazione, forza, energia Struttura atomica dei gas: particelle tutte
TERMOLOGIA & TERMODINAMICA I 1 Meccanica: studia il moto dei corpi e le cause che lo genera Grandezze meccaniche: massa, velocità, accelerazione, forza, energia Struttura atomica dei gas: particelle tutte
Proprietà volumetriche delle sostanze pure. Principi di Ingegneria Chimica Ambientale
 Proprietà volumetriche delle sostanze pure Principi di Ingegneria Chimica Ambientale le fasi di una specie pura Una sostanza la cui composizione chimica non varia in tutta la massa presa in considerazione
Proprietà volumetriche delle sostanze pure Principi di Ingegneria Chimica Ambientale le fasi di una specie pura Una sostanza la cui composizione chimica non varia in tutta la massa presa in considerazione
DEFINIZIONI SMART E RELATIVE ESERCITAZIONI
 DEFINIZIONI SMART E RELATIVE ESERCITAZIONI A B C D E 1 2 3 4 5 6 7 8 9 MODULO 3 Creazione e gestione di fogli di calcolo MODULO 3 CREAZIONE E GESTIONE DI FOGLI DI CALCOLO Gli elementi fondamentali del
DEFINIZIONI SMART E RELATIVE ESERCITAZIONI A B C D E 1 2 3 4 5 6 7 8 9 MODULO 3 Creazione e gestione di fogli di calcolo MODULO 3 CREAZIONE E GESTIONE DI FOGLI DI CALCOLO Gli elementi fondamentali del
ESERCITAZIONI 1 e 2: calcoli
 ESERCITAZIONI 1 e 2: calcoli L uso del foglio elettronico nel laboratorio di ispezione degli alimenti. Funzioni utilizzate negli esercizi e traduzione in inglese americano per l utilizzo su computer con
ESERCITAZIONI 1 e 2: calcoli L uso del foglio elettronico nel laboratorio di ispezione degli alimenti. Funzioni utilizzate negli esercizi e traduzione in inglese americano per l utilizzo su computer con
Transizioni liquido-solido: Aspetti cinetici
 Transizioni liquido-solido: Aspetti cinetici Prof.G.Marletta Chimica Fisica dei Materiali II e Laboratorio Laurea Magistrale in Chimica dei Materiali Università di Catania A.A. 2011/2012 1- Caratteri generali
Transizioni liquido-solido: Aspetti cinetici Prof.G.Marletta Chimica Fisica dei Materiali II e Laboratorio Laurea Magistrale in Chimica dei Materiali Università di Catania A.A. 2011/2012 1- Caratteri generali
Unità 1. La temperatura
 Unità 1 La temperatura 1. Il termometro La sensazione di caldo e di freddo è soggettiva: per renderla misurabile si usa il termoscopio. È un recipiente di vetro con tappo forato e tubicino, contenente
Unità 1 La temperatura 1. Il termometro La sensazione di caldo e di freddo è soggettiva: per renderla misurabile si usa il termoscopio. È un recipiente di vetro con tappo forato e tubicino, contenente
Capitolo 4: Tabelle. y(x) = x 3 ì 2x. Capitolo 4: Tabelle 67. Nota: le tabelle non sono disponibili nel modo di rappresentazione grafica 3D.
 Capitolo 4: Tabelle 4 Definizione di tabelle...68 Panoramica della procedura per generare una tabella...69 Impostazione dei parametri di tabella...70 Visualizzazione di una tabella in modo automatico...72
Capitolo 4: Tabelle 4 Definizione di tabelle...68 Panoramica della procedura per generare una tabella...69 Impostazione dei parametri di tabella...70 Visualizzazione di una tabella in modo automatico...72
Pannelli solari a HEAT PIPE
 Pannelli solari a HEAT PIPE Gli heat pipe applicati ai sistemi di condizionamento estivo Negli ultimi anni, la domanda di elettricità nel periodo estivo ha raggiunto picchi estremi per l uso eccessivo
Pannelli solari a HEAT PIPE Gli heat pipe applicati ai sistemi di condizionamento estivo Negli ultimi anni, la domanda di elettricità nel periodo estivo ha raggiunto picchi estremi per l uso eccessivo
IL CALORE. Il calore. Esperimento di Joule. Il calore
 l calore l calore Q è energia che sta transitando da un sistema all altro, e compare ogni volta che c è un dislivello di temperatura. L CALORE l corpo più caldo cede parte della sua energia interna al
l calore l calore Q è energia che sta transitando da un sistema all altro, e compare ogni volta che c è un dislivello di temperatura. L CALORE l corpo più caldo cede parte della sua energia interna al
GALLERY. Album immagini
 GALLERY In questo menù del pannello di amministrazione si trovano tutte le funzioni utili alla gestione delle foto, dei video e degli album da inserire all'interno delle pagine con funzione ALBUM IMMAGINI
GALLERY In questo menù del pannello di amministrazione si trovano tutte le funzioni utili alla gestione delle foto, dei video e degli album da inserire all'interno delle pagine con funzione ALBUM IMMAGINI
Fisica per scienze ed ingegneria
 Serway, Jewett Fisica per scienze ed ingegneria Capitolo 20 Fino a circa il 1850 su riteneva che la meccanica e la termodinamica fossero due scienze completamente distinte. La legge di conservazione dell
Serway, Jewett Fisica per scienze ed ingegneria Capitolo 20 Fino a circa il 1850 su riteneva che la meccanica e la termodinamica fossero due scienze completamente distinte. La legge di conservazione dell
Misure di termometria e calorimetria
 Misure di termometria e calorimetria Strumentazione a disposizione: sonde di temperatura interfacciate con il sistema di acquisizione Lab- Pro; termometri al mercurio; calorimetro o termos (:po vaso Dewar);
Misure di termometria e calorimetria Strumentazione a disposizione: sonde di temperatura interfacciate con il sistema di acquisizione Lab- Pro; termometri al mercurio; calorimetro o termos (:po vaso Dewar);
Termodinamica e termochimica
 Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
Lezione 9. Statica dei fluidi
 Lezione 9 Statica dei fluidi Meccanica dei fluidi Un fluido e un corpo che non ha una forma definita, ma che, se e contenuto da un contenitore solido, tende a occupare (riempire) una parte o tutto il volume
Lezione 9 Statica dei fluidi Meccanica dei fluidi Un fluido e un corpo che non ha una forma definita, ma che, se e contenuto da un contenitore solido, tende a occupare (riempire) una parte o tutto il volume
Stati della materia. Esempio. Fusione e solidificazione. Esempio. Stati di aggregazione della materia
 Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
il ciclo di Ericsson (1853) caratterizzato da due isoterme e due isobare; il ciclo di Reitlinger (1873) con due isoterme e due politropiche.
 16 Il ciclo di Stirling Il coefficiente di effetto utile per il ciclo frigorifero di Carnot è, in base alla (2.9): T min ɛ =. (2.31) T max T min Il ciclo di Carnot è il ciclo termodinamico che dà il maggior
16 Il ciclo di Stirling Il coefficiente di effetto utile per il ciclo frigorifero di Carnot è, in base alla (2.9): T min ɛ =. (2.31) T max T min Il ciclo di Carnot è il ciclo termodinamico che dà il maggior
MISURE DI VISCOSITA CON IL METODO DI STOKES
 MISURE DI VISCOSITA CON IL METODO DI STOKES INTRODUZIONE La viscosità di un fluido rappresenta l attrito dinamico nel fluido. Nel caso di moto in regime laminare, la forza di attrito è direttamente proporzionale
MISURE DI VISCOSITA CON IL METODO DI STOKES INTRODUZIONE La viscosità di un fluido rappresenta l attrito dinamico nel fluido. Nel caso di moto in regime laminare, la forza di attrito è direttamente proporzionale
Attività sperimentale da laboratorio sul ciclo CaO-CaCO3 per la cattura della CO2 ad alta temperatura
 COPERTINA DEF2009-26.RdS:Layout 1 19-06-2009 12:25 Pagina 1 Attività sperimentale da laboratorio sul ciclo CaO-CaCO3 per la cattura della CO2 ad alta temperatura A. Calabrò, S. Stendardo Report RSE/2009/26
COPERTINA DEF2009-26.RdS:Layout 1 19-06-2009 12:25 Pagina 1 Attività sperimentale da laboratorio sul ciclo CaO-CaCO3 per la cattura della CO2 ad alta temperatura A. Calabrò, S. Stendardo Report RSE/2009/26
DIAGRAMMI DI STATO. Una singola fase ha in ogni sua parte un identico comportamento se sottoposta a sollecitazioni fisiche o chimiche
 DIAGRAMMI DI STATO Sono grafici che descrivono il numero delle fasi presenti in un sistema all equilibrio, la loro composizione chimica e la quantita relativa di ciascuna di esse, in funzione di alcuni
DIAGRAMMI DI STATO Sono grafici che descrivono il numero delle fasi presenti in un sistema all equilibrio, la loro composizione chimica e la quantita relativa di ciascuna di esse, in funzione di alcuni
Lab. 2 - Excel. Prof. De Michele e Farina
 Lab. 2 - Excel Prof. De Michele e Farina 1 Utilizzo avanzato di un foglio elettronico: - Utilizzo di funzioni Regressioni lineari Istogrammi 2 La funzione somma restituisce la somma dei valori dei propri
Lab. 2 - Excel Prof. De Michele e Farina 1 Utilizzo avanzato di un foglio elettronico: - Utilizzo di funzioni Regressioni lineari Istogrammi 2 La funzione somma restituisce la somma dei valori dei propri
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici
 La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
10. LA MISURA DELLA TEMPERATURA
 1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore
 Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore Legge di Stevino La pressione in un liquido a densità costante cresce linearmente con la profondità Il principio di
Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore Legge di Stevino La pressione in un liquido a densità costante cresce linearmente con la profondità Il principio di
2 Legge di Newton del raffreddamento
 1 Il calorimetro delle mescolanze Un ambiente isolato termicamente dall esterno nel quale è possibile far avvenire processi termodinamici controllando le variazioni della temperatura interna viene indicato
1 Il calorimetro delle mescolanze Un ambiente isolato termicamente dall esterno nel quale è possibile far avvenire processi termodinamici controllando le variazioni della temperatura interna viene indicato
Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA
 Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
8 Quale delle seguenti affermazioni è vera? A Il potere calorifico di una sostanza è direttamente proporzionale alla sua capacità termica. B Il calore
 Test 1 Quale delle seguenti affermazioni è corretta? A Si ha un passaggio di temperatura quando c è un dislivello di calore. B Si ha passaggio di calore quando c è un dislivello di energia interna. C Si
Test 1 Quale delle seguenti affermazioni è corretta? A Si ha un passaggio di temperatura quando c è un dislivello di calore. B Si ha passaggio di calore quando c è un dislivello di energia interna. C Si
LABORATORIO DI FISICA Studio della lunghezza di corde perpendicolari
 Studio della lunghezza di corde perpendicolari Eseguire con il righello una serie di misure della lunghezza di corde perpendicolari ottenute posizionando più volte la squadretta sul goniometro (dal lato
Studio della lunghezza di corde perpendicolari Eseguire con il righello una serie di misure della lunghezza di corde perpendicolari ottenute posizionando più volte la squadretta sul goniometro (dal lato
Calcolare con il computer: Excel. Saro Alioto 1
 Calcolare con il computer: Excel Saro Alioto 1 Excel è un programma che trasforma il vostro computer in un foglio a quadretti. In altri termini con Excel potrete fare calcoli, tabelle, grafici, ecc...
Calcolare con il computer: Excel Saro Alioto 1 Excel è un programma che trasforma il vostro computer in un foglio a quadretti. In altri termini con Excel potrete fare calcoli, tabelle, grafici, ecc...
2) Primo principio della Termodinamica
 2) Primo principio della Termodinamica Antefatto: conservazione dell energia dalla descrizione molecolare (secondo la meccanica classica/quantistica) del sistema materiale Energia() = energia cinetica
2) Primo principio della Termodinamica Antefatto: conservazione dell energia dalla descrizione molecolare (secondo la meccanica classica/quantistica) del sistema materiale Energia() = energia cinetica
Dati sperimentali Nella serie di 10 misurazioni di tempo effettuate, si sono ottenuti i seguenti valori espressi in secondi:
 ESPERIMENTO DI LABORATORIO DI FISICA MISURE DI TEMPO Obiettivo L obiettivo dell esperimento, oltre che familiarizzare con le misure di tempo, è quello di rivelare gli errori casuali, elaborare statisticamente
ESPERIMENTO DI LABORATORIO DI FISICA MISURE DI TEMPO Obiettivo L obiettivo dell esperimento, oltre che familiarizzare con le misure di tempo, è quello di rivelare gli errori casuali, elaborare statisticamente
3. Le coordinate geografiche: latitudine e longitudine
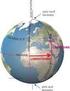 Introduzione 3. Le coordinate geografiche: latitudine e longitudine Ogni volta che vogliamo individuare un punto sulla superficie terrestre gli associamo due numeri, le coordinate geografiche: la latitudine
Introduzione 3. Le coordinate geografiche: latitudine e longitudine Ogni volta che vogliamo individuare un punto sulla superficie terrestre gli associamo due numeri, le coordinate geografiche: la latitudine
Impulso e quantità di moto www.lepla.eu
 Impulso e quantità di moto www.lepla.eu Obiettivo In questo esperimento si vuole confrontare l'impulso su un carrello con la variazione della sua quantità di moto. Il moto del carrello viene studiato con
Impulso e quantità di moto www.lepla.eu Obiettivo In questo esperimento si vuole confrontare l'impulso su un carrello con la variazione della sua quantità di moto. Il moto del carrello viene studiato con
Eventuale post-riscaldamento se la necessitàdi deumidificazione ha comportato una diminuzione eccessiva di temperatura
 La scelta delle condizioni termoigrometriche di immissione in Ideve essere fatta in modo tale da compensare le qt e gli apporti di mv. Si utilizza ti pari a 30-35 C. Cmq in modo da avere nell embinete
La scelta delle condizioni termoigrometriche di immissione in Ideve essere fatta in modo tale da compensare le qt e gli apporti di mv. Si utilizza ti pari a 30-35 C. Cmq in modo da avere nell embinete
Motore di Stirling. Scopo dell esperienza
 Motore di Stirling Scopo dell esperienza Lo scopo dell esperienza è duplice: calcolare il rendimento del motore in seguito alla realizzazione di un ciclo termico determinare il potere refrigerante e calorifico
Motore di Stirling Scopo dell esperienza Lo scopo dell esperienza è duplice: calcolare il rendimento del motore in seguito alla realizzazione di un ciclo termico determinare il potere refrigerante e calorifico
Microsoft Excel II parte Import di dati & Funzioni predefinite
 Laboratorio di Informatica 2004/ 2005 Corso di laurea in biotecnologie - Novara Viviana Patti patti@di.unito.it Microsoft Excel II parte Import di dati & Funzioni predefinite 1 Sommario Import di dati
Laboratorio di Informatica 2004/ 2005 Corso di laurea in biotecnologie - Novara Viviana Patti patti@di.unito.it Microsoft Excel II parte Import di dati & Funzioni predefinite 1 Sommario Import di dati
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE
 SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE I Titolo dell esperienza N 4 DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO CON IL PRINCIPIO DI ARCHIMEDE
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE I Titolo dell esperienza N 4 DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO CON IL PRINCIPIO DI ARCHIMEDE
 La costante (p 0 0 /273) la si riesprime come n R dove R è una costante universale il cui valore dipende solo dalle unità di misura usate: R8.31 Joule/(K mole) e n è il numero di moli L equazione di stato
La costante (p 0 0 /273) la si riesprime come n R dove R è una costante universale il cui valore dipende solo dalle unità di misura usate: R8.31 Joule/(K mole) e n è il numero di moli L equazione di stato
La palla che rimbalza
 La palla che rimbalza www.lepla.eu Obiettivo In questo modulo ci proponiamo di studiare il moto di una palla che rimbalza. Useremo un sonar per misurare la distanza tra il sensore e la palla. I dati acquisiti
La palla che rimbalza www.lepla.eu Obiettivo In questo modulo ci proponiamo di studiare il moto di una palla che rimbalza. Useremo un sonar per misurare la distanza tra il sensore e la palla. I dati acquisiti
Variazioni di Pressione: 'Sonic Boom'
 Variazioni di Pressione: 'Sonic Boom' www.lepla.eu Obiettivo Con questo esperimento ci si propone di osservare le variazioni di pressione all interno di una siringa quando il pistone viene tirato fuori
Variazioni di Pressione: 'Sonic Boom' www.lepla.eu Obiettivo Con questo esperimento ci si propone di osservare le variazioni di pressione all interno di una siringa quando il pistone viene tirato fuori
ANALISI DI SEGNALI TEMPO VARIANTI
 ANALISI DI SEGNALI TEMPO VARIANTI Nel corso di questa esercitazione verrà illustrato come utilizzare Excel per eseguire la FFT di un segnale. Algebra complessa Excel consente di eseguire calcoli anche
ANALISI DI SEGNALI TEMPO VARIANTI Nel corso di questa esercitazione verrà illustrato come utilizzare Excel per eseguire la FFT di un segnale. Algebra complessa Excel consente di eseguire calcoli anche
Misuratore di umidità XA1000 misuratore portatile per rilevare temperatura e umidità relativa con alta precisione / sensore di pressione integrato /
 Misuratore di umidità XA1000 misuratore portatile per rilevare temperatura e umidità relativa con alta precisione / sensore di pressione integrato / registrazione dei dati online e offline / display touch
Misuratore di umidità XA1000 misuratore portatile per rilevare temperatura e umidità relativa con alta precisione / sensore di pressione integrato / registrazione dei dati online e offline / display touch
Laboratorio di Didattica di elaborazione dati 5 STIMA PUNTUALE DEI PARAMETRI. x i. SE = n.
 5 STIMA PUNTUALE DEI PARAMETRI [Adattato dal libro Excel per la statistica di Enzo Belluco] Sia θ un parametro incognito della distribuzione di un carattere in una determinata popolazione. Il problema
5 STIMA PUNTUALE DEI PARAMETRI [Adattato dal libro Excel per la statistica di Enzo Belluco] Sia θ un parametro incognito della distribuzione di un carattere in una determinata popolazione. Il problema
Grandezze e Misure 1
 Grandezze e Misure 1 Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Misure dirette e indirette Strumenti di misura Errori nelle
Grandezze e Misure 1 Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Misure dirette e indirette Strumenti di misura Errori nelle
INTRODUZIONE ALLA TERMODINAMICA. Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta
 INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
PRIMI ELEMENTI DI TERMODINAMICA. La termodinamica studia le leggi con cui i sistemi scambiano (cedono e ricevono) energia con l ambiente.
 PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
Termodinamica: introduzione
 Termodinamica: introduzione La Termodinamica studia i fenomeni che avvengono nei sistemi in seguito a scambi di calore (energia termica) ed energia meccanica, a livello macroscopico. Qualche concetto rilevante
Termodinamica: introduzione La Termodinamica studia i fenomeni che avvengono nei sistemi in seguito a scambi di calore (energia termica) ed energia meccanica, a livello macroscopico. Qualche concetto rilevante
Excel 3. Master Universitario di II livello in MANAGER NELLE AMMINISTRAZIONI PUBBLICHE A.A Prof.ssa Bice Cavallo
 Excel 3 Master Universitario di II livello in MANAGER NELLE AMMINISTRAZIONI PUBBLICHE A.A. 2013-2014 Prof.ssa Bice Cavallo Ordinamento dei dati: ordinamento di un elenco l Excel è in grado di ordinare
Excel 3 Master Universitario di II livello in MANAGER NELLE AMMINISTRAZIONI PUBBLICHE A.A. 2013-2014 Prof.ssa Bice Cavallo Ordinamento dei dati: ordinamento di un elenco l Excel è in grado di ordinare
PASSAGGI DI STATO. sublimazione fusione ebollizione. solidificazione. condensazione. brinamento. Calore processi fisici endotermici ( H>0).
 PASSAGGI DI STATO Calore processi fisici endotermici (H>0). sublimazione fusione ebollizione S solidificazione L condensazione V brinamento Scrittura in formule: - H 2 O (s) H 2 O (l) fusione - H 2 O (l)
PASSAGGI DI STATO Calore processi fisici endotermici (H>0). sublimazione fusione ebollizione S solidificazione L condensazione V brinamento Scrittura in formule: - H 2 O (s) H 2 O (l) fusione - H 2 O (l)
MISURA dell EFFETTO JOULE
 MISURA dell EFFETTO JOULE attività svolta con la classe 3^D - a.s. 2010/11 Scopo dell esperienza Le finalità dell esperimento sono: 1) Verificare che il moto degli elettroni di conduzione genera calore,
MISURA dell EFFETTO JOULE attività svolta con la classe 3^D - a.s. 2010/11 Scopo dell esperienza Le finalità dell esperimento sono: 1) Verificare che il moto degli elettroni di conduzione genera calore,
Calore specifico e legge fondamentale della calorimetria
 Calore specifico e legge fondamentale della calorimetria L aumento della temperatura di un corpo è sempre causato dal passaggio di calore dall esterno all interno del corpo, la diminuzione di temperatura
Calore specifico e legge fondamentale della calorimetria L aumento della temperatura di un corpo è sempre causato dal passaggio di calore dall esterno all interno del corpo, la diminuzione di temperatura
ELABORAZIONE TRAMITE PC DEI DATI RACCOLTI. / /
 ELABORAZIONE TRAMITE PC DEI DATI RACCOLTI BILANCIA LAMBERT-BEER Alla Lavagna / 103/ hep.fi.infn.it/fisichetta1/lab_bio/ Schermata iniziale del PC Alla Lavagna / 104/ hep.fi.infn.it/fisichetta1/lab_bio/
ELABORAZIONE TRAMITE PC DEI DATI RACCOLTI BILANCIA LAMBERT-BEER Alla Lavagna / 103/ hep.fi.infn.it/fisichetta1/lab_bio/ Schermata iniziale del PC Alla Lavagna / 104/ hep.fi.infn.it/fisichetta1/lab_bio/
