Dott. Giovanni Aste 1
|
|
|
- Franco Rota
- 7 anni fa
- Visualizzazioni
Transcript
1 1 Dott. Giovanni Aste
2 Introduzione Metabolismo Produzione di meq di H+ proteine e fosfolipidi di mmol di CO2 carboidrati e lipidi 2
3 concetti Acidità (Bronsted and Lowry) HA = A- + H+ H+ + H2O = H3O+ (soluzione acquosa) Osmolalità/temperatura ph ( equazione di Sǿrensen) ph = -log 10 [H+] = log 10 1/ [H+] 3 [H] in ECF 40 neq/l ph = 7.398
4 concetti Legge di Azione di massa (Henderson-Hassolbah) ph= pka + log [sale/ A- ]/[acido/ HA] Valori di Ka elevati/ bassi pka (HCl, H2SO4) Valori di Ka bassi/ elevati pka (NH4) 4 Principio «isoidrico»
5 5
6 Sostanza Tampone Composto che dona/accetta protoni (H+) e minimizza i cambiamenti del ph) Sistema Bicarbonato- Acido carbonico [CO2 diss ]= α (PCO2) α (PCO2)= 0,0301 [CO2 diss ] + H2O H2CO3 pka = 2,72 [CO2 diss ] + H2O H2CO3 H+ HCO3 H+ = 40nmol/L (ph = 7.40) HCO3 = 6800 ioni 340 Co2 dissolte 6
7 Sostanze tampone corporee HCO3 predominante in Non-bicarbonati (proteine, fosfati organiciinorganici) predominanti in Tessuto Fonte principale di tamponi. Calcio carbonato, calcio fosfato in corso di acidosi metabolica cronica Contribuisce per 40% durante Acidosi acuta da carico La somministrazione di NaHCO3 deposizione di 7 carbonato
8 ECF HCO3 elevata concentrazione (24mEq/L 2 meq dei fosfati) + + SISTEMA APERTO, CO2 eliminata attraverso la ventilazione alveolare 8
9 Proteine-tampone Ruolo limitato in ECF Predominante in ICF Gruppi dissociabili; Hb anello imidazolico dei residui di istidina Aminoacidi terminali Hb 80% dei tamponi non-bicarbonati Proteine Plasmatiche 20% (ALBUMINA >> globuline) 16mEq/L contributo delle proteine plasmatiche 9
10 10 Proteine-tampone
11 Tampone FOSFATO Tampone ICF (40 meq cellule muscolari/ 2mEq in ECF) Fosfati organici (ATP, ADP, 2,3difosfoglicerato) Inorganici (H2PO4-) pka = 6.8 H2PO4- pka fosfati organici Importanza nelle urine, ph 6 7 dei tubuli (acidità titolata) 11
12 terminologia Processo patologico che comporta un accumulo di acidi o alcali nell organismo Acidemia, alcalemia si riferiscono al valore di ph in ECF 12
13 Difesa fisiologica alle modifiche del ph HCO3 ECF (minuti ora) Ventilazione alveolare CO2 normalità del rapporto HCO3- CO2 RENI rigenerano HCO3 aumento del ph, PCO2 ritorna normale La risposta renale inizia a distanza di ore e raggiunge la sua massima efficienza in 2-5 giorni CO2 non è tamponato da HCO3 H+ (dalla dissociazione di H2CO3) tamponi intracellulari (Hb, fosfati, proteine) Adattamento renale: aumento riassorbimento HCO3, escrezione acida netta 13
14 Alterazione Acido-base primarie Acidosi Metabolica, (perdita HCO3, acidi non-volatili) Alcalosi Metabolica (perdita di Cl, ipoalbuminemia, accumulo di H alcali in caso di deplezione del ECFV/disfunzione renale) Acidosi Respiratoria, (aumento PCO2, ipercapnia) Alcalosi Respiratoria, (diminuzione PCO2 ipocapnia) 14
15 Alterazione Acido-base miste o semplici SEMPLICE, (limitata a un disordine primario cui si associa una risposta attesa secondaria) MISTA, (caratterizzato dalla presenza di almeno due disordini concomitanti) 15
16 Alterazioni acido-base primarie Acidosi respiratoria Alcalosi respiratoria Acidosi metabolica Alcalosi metabolica ph [H+] Alterazione primaria Compenso PCO2 [HCO3] PCO2 [HCO3] [HCO3] PCO2 [HCO3] PCO2 16
17 Valutazione della risposta compensatoria (alterazione primaria semplice), cane e gatto cane gatto Acidosi metab. -1mmEq/l HCO3-1 mmhg PCO2 -- Alcalosi metab. +1mmEq/l HCO mmhg PCO mmhg PCO2 Acidosi Resp. Acuta +1mmHg PCO mEq/L HCO mEq/L HCO3 Cronica +1mmHg PCO mEq/L HCO3 NC Long Stand +1mmHg PCO mEq/L HCO3 NC Alcalosi Resp. Acuta -1mmHg PCO2-0.35mEq/L HCO3-0.25mEq/L HCO3 Cronica -1mmHg PCO2-0.55mEq/L HCO3 Simile 17
18 18
19 19
20 20
21 21
22 ph PCO2 HCO3 Determinazione emogas-analitica Base eccesso (quantità di acido/base forte per titolare 1 ml di sangue a 7.4, 40mmHg CO2, 37 c) TCO2 (CO2 + HCO3), > 1-2 meq/l HCO3 HCO3 Standard (plasma ossigenato, 40mmHgCO2, 37 C) Wh.blood buffer base (40-50 meq/l) Whole body buffer base 22
23 Modalità di prelievo Prelievo arterioso Prelievo venoso 23
24 Modalità di prelievo 24
25 VALORI DI NORMALITÀ Valori emogas-analitici arteriosi cane e gatto (aria respirata) cane gatto ph 7.41 ( ) 7.39 ( ) PaCO2 (mmhg) 37 (31-43) 31 (25-37) HCO3 (Meq/L) 22 (19-26) 18 (14-22) PO2 (mmhg) 91 (81-103) 107 (95-118) 25
26 Valori emogas arterioso,misto e venoso cane-gatto (aria-respirata) arterioso misto v. giugulare v.cefalica ph ± ± ± ± PCO ± ± ± ± 3.2 PO ± ± ± ± 8.8 HCO ± ± ± ± 1.4 TCO ± ± ± ± 1.4 BE -1.8 ± ± ± ± 1.1 SHCO ± ± ± ±
27 Interpretazione emogasanalisi 1. Determinare se il ph è normale 2. Valutare PCO2 (componente respiratoria) 3. Valutare HCO3 (componente non-respiratoria) 4. Quale è il problema primario? 5. Quale è la risposta secondaria di adattamento attesa? 6. 27
28 Normale concentrazione cationi/anioni (meq/l) cationi cane gatto anioni cane gatto sodio cloro Potassio 4 4 bicarbonat calcio 5 5 Fosfato 2 2 magnesio 2 2 Solfato 2 2 tracce 1 1 lattato 2 2 Ac organici 4 6 proteine tot
29 ANION GAP (NA + K )- (Cl HCO3) meq/l cane, 13-27mEq/L gatto Na + K + UC = Cl + HCO3 + UA UC-UA = (Na +K) (CL + HCO3) 29
30 ANION GAP Aumento AG ES. ACIDOSI da ac. organici (lattato, chetoacidosi diabetica),, Emoconcentrazione Diminuzione AG mieloma multiplo (IgG), ipoalbuminemia (per ogni 1g/dl meq/l AG) Utilità nell identificazione dei disordini misti negativa : perdita di protoni dalle proteine e aumento della carica Aumento della produzione di acido lattico per stimolazione della fosfofruttochinasi. 30
31 Approccio non-tradizionale ph PCO2 respiratorio HCO3 matabolico (Reni) PCO2 = variabile indipendente Na, K, Cl? - Equazione di Stewart 1. mantenimento della elettroneutralità 2. soddisfacimento degli equilibri per soluti noncompletamente dissociabili 3. conservazione di massa 31
32 Approccio non-tradizionale Indipendenti: sono variabili che posso essere alterate da «fuori» del sistema Dipendenti: interne al sistema, variano in risposta al comportamento delle indipendenti Le variabili indipendenti individuate dalla Eq. Di Stewart sono: SID (Strong Ions difference) Concentrazione totale degli Acidi deboli PCO2 32
33 Differenza delle variazioni tra la somma dei cationi «forti» e la somma degli anioni «forti» Forti: quasi completamente dissociati al ph dei fluidi corporei Cationi: Na, K, Mg, Ca Anioni: Cl + Unmeasured Strong Anions (lattato, solfato, acetoacetato, BetaHbutirrato) ANIONI DEBOLI HCO3,proteine plasmatiche, fosfati Proteine plasmatiche, fosfati indipendenti HCO3 dipendente 33 SID
34 Bilanciamento esterno idrogenioni H+ Produzione da processi metabolici, dieta Escrezione Renale 34 Metabolismo: H+ dai processi che convertono i composti cationici in neutri Quelli che convertono i composti anionici in neutri consumano H+ Fonti di acidi: ossidazione di aminoacidi contenenti gr. Solfuro (cisteina, metionina), aa cationici (lisina, arginina), idrolisi dei diesteri dei fosfati organici (fosfolipidi, ac nucleici) Fonte di basi: ossidazione di AA anionici (glutammato,aspartato), uso ai fini glucogenetici di altri anioni organici (lattato, citrato)
35 Regolazione whole-body Fegato Metabolismo delle proteine (glucosio,trigliceridi) con produzione di NH4 e CO2, formazione di UREA e produzione di H+ con titolazione di HCO3. Produce la maggior parte degli acidi non-volatili escreti dal rene Reni Polmoni 35
36 Fegato Reni Regolazione whole-body Mantiene [HCO3] in ECF riassorbimento COMPLETO, la rigenerazione del HCO3 titolata Il riassorbimento di HCO3 ECFV (Na) Escrezione di NH4 GFR Glutammina alfaketoglutarato + NH4 Alfaketoglut + 2H CO2 + H2o (ossidazione) Alfaketoglut + CO2 Urea + 2H (ciclo dell urea) Acidità Titolabile (fosfati creatinina, urati), escrezione acida netta: NH4 + Acidità titolabili HCO3 36
37 37
38 ACIDOSI RESPIRATORIA Ipercapnia primaria ipo-ventilazione, ipossiemia Dimunuzione del ph ematico Aumento della PCO2 Risposta compensatoria: HCO3 38
39 ACIDOSI RESPIRATORIA Attivazione sistema simpatico Aumento out-put cardiaco (tachiaritmia) Aumento della pressione intracranica Aumento del flusso cerebrale Disorientamento, narcosi e COMA per valori di PCO2 superiori a mmhg 39
40 ACIDOSI RESPIRATORIA CAUSE Depressione del centro del respiro Farmaci (anestetici inalatori, oppioidi, barbiturici Neuropatie (tronco encefalico, lesioni spinali cervivali «alte») Ostruzione vie aeree Aspirazione (vomito, corpo estraneo) Neoplasia- massa Collasso tracheale Malattie polmonari croniche ostruttive Asma Ostruzione del tubo endotracheale Laringospasmo-paralisi 40 Sindrome-brachiocefalica
41 ACIDOSI RESPIRATORIA CAUSE Aumento CO2 con deficit della ventilazione alveolare Arresto cardio-polmonare Colpo di calore Ipertermia (grave- maligna) Malattie polmonari estrinseche restrittive Ernia diaframmatica Malattie dello spazio pleurico Trauma costale-parietale 41
42 ACIDOSI RESPIRATORIA CAUSE Malattie polmonari intrinseche, malattie delle vie aeree inferiori ARDS M. polmonari croniche Asma Edema polmonare (grave) Polmoniti (gravi) Fibrosi polmonari Metastasi diffuse Inalazione da fumo Ventilazione meccanica inefficace 42
43 Malattie Neuromuscolari Miastenia grave Tetano Botulismo Poliradicoloneurite Malattie da zecche ACIDOSI RESPIRATORIA CAUSE Alterazioni elettrolitiche (ipokalemia) Farmacoindotta (organofosfati, curariformi, aminoglicosidi + anestetici) 43 Sindrome di Pickwick (eccessiva obesità)
44 ACIDOSI metabolica Dimunuzione del ph ematico Diminuzione di HCO3 Diminuzione di BE Risposta compensatoria: diminuzione della PCO2 44
45 ACIDOSI metabolica Grave ph < 7.1 o HCO3 < 8 meq/l Depressione del sensorio tachipnea 45
46 ACIDOSI metabolica CAUSE Aumento AG (normocloremica) Tossicità (salicilati, gl. Etilenico, metanolo, paraldeide) Chetoacidosi Acidosi uremica Acidosi lattica 46 AG normale (ipercloremica) Diarrea Inibitori della anidrasi carbonica (acetazolamide) Cloruro di Ammonio Amino acidi cationici ( lisina, arginina, istidina) Acidosi postipocapnoica Acidosi da diluizione ( overidration) ipoadrenocorticismo
47 SID ACIDOSI Acidosi da ac organici ACIDOSI metabolica CAUSE Tossicità (salicilati, gl. Etilenico ) Acidosi lattica Acidosi uremica Chetoacidosi diabetica Acidosi da diluizione (iponatremia, aumento dell acqua libera) Infusione di fluidi ipotonici (ipervolemia) Insuff. Cardiaca Congestizia Insuff. Epatica (grave) 47
48 ACIDOSI metabolica CAUSE-SID Guadagno di acqua corporea (normovolemia) Infusione di fluidi ipotonici Polidipsia psicogena Perdite IPERTONICHE (IPOVOLEMIA) Amministrazione di diuretici Ipoadrenocorticismo 48
49 ACIDOSI metabolica CAUSE - SID Acidosi IPERCLOREMICA Insuff Renale Total Parenteral nutrition Terapia fluida (NaCl 7,2%, KCL supplementato) Ipoadrenocorticismo Diarrea 49
50 ACIDOSI metabolica CAUSE Acidosi ioni tampone non-volatili Acidosi iperfosfatemica Insuff Renale Ostruzione uretrale Uroaddome Supplementazione con fosfati Uso di fosfati (enemas) 50
51 ALCALOSI RESPIRATORIA IPOcapnia primaria IPER-ventilazione Aumento del ph ematico DIMINUZIONE della PCO2 DIMINUZIONE di HCO3 Risposta compensatoria 51
52 ALCALOSI RESPIRATORIA PCO2 diminuizione spuria Eccesso di anticoaguloante nella siringa (diluizione) Presenza di micro-macro bolle d aria Anormalità nella preparazione e manualità del campione 52
53 ALCALOSI RESPIRATORIA Vasocostrizione arteriolare PCO2 < 25 mmhg ph > 7.6 DiMINUZIONE del flusso CEREBRALE e MIOCARDICO Tachipnea, disorientamento, crisi convulsive, aritmie cardiache 53
54 ALCALOSI RESPIRATORIA CAUSE Paura, eccitazione, ansietà o DOLORE Iperventilazione (paziente, ventilazione meccanica) Diminuzione di PO2 inspirata Malattie Polmonari (edema polm, polmoniti, fibrosi, tromboembolismo) Insufficienza Cardiaca congestizia Anemia Grave Grave Ipotensiane Neuropatie Centrali 54
55 ALCALOSI RESPIRATORIA CAUSE Paura, eccitazione, ansietà o DOLORE Iperventilazione (paziente, ventilazione meccanica) Diminuzione di PO2 inspirata Malattie Polmonari (edema polm, polmoniti, fibrosi, tromboembolismo) Insufficienza Cardiaca congestizia Anemia Grave Grave Ipotensiane Neuropatie Centrali 55
56 ALCALOSI RESPIRATORIA CAUSE Stimolazione dei tensiocettori o nocicettori polmonari Farmaci: xantine, glucocorticoidi Malattie epatiche Iperadrenocorticismo Sepsi Coplo di calore Esercizio prolungato Esito di una acidosi metabolica 56
57 ALCALOSI metabolica AUMENTO del ph ematico AUMENTO di HCO3 AUMENTO di BE Risposta compensatoria: AUMENTO della PCO2 57
58 ALCALOSI metabolica Grave ph >
59 SID ALCALOSI ALCALOSI metabolica CAUSE Acidosi IPOCLOREMICA Vomito (contenuto gastrico) Somministrazione di diuretici dell ansa (furosemide), tiazidi o sodio bicarbonato ALCALOSI CLORO -RESISTENTE Iperaldosteronismo Iperadrenocorticismo ALCALOSI da concentrazione (perdita di acqua pura, ipernatriemia) Deprivazione di acqua Vomito e diarrea 59
60 ALCALOSI metabolica CAUSE Alcalosi da ioni-tampone non-volatili IPOALBUMINEMIA Nefropatia proteinurica Enteropatia proteino-disperdente Insufficienza epatica 60
61 61 Caso 1
62 62
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI
 EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
Rene ed equilibrio acido base. La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica. Principali funzioni renali
 Rene ed equilibrio acido base La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica Savi Umberto Scuola di Specializzazione in Nefrologia S.C. di Nefrologia e Dialisi Cattinara
Rene ed equilibrio acido base La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica Savi Umberto Scuola di Specializzazione in Nefrologia S.C. di Nefrologia e Dialisi Cattinara
Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca
 Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acido base
 Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
Milano, 9 giugno acido-base? Ernesto Cristiano Lauritano
 ACQUA E SALE Milano, 9 giugno 2012 Quale approccio ai disordini acido-base? Ernesto Cristiano Lauritano Dipartimento di Emergenza e Accettazione Azienda Ospedaliera Nazionale SS. Antonio e Biagio e Cesare
ACQUA E SALE Milano, 9 giugno 2012 Quale approccio ai disordini acido-base? Ernesto Cristiano Lauritano Dipartimento di Emergenza e Accettazione Azienda Ospedaliera Nazionale SS. Antonio e Biagio e Cesare
Emogasanalisi in t.i.
 Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
In base all equazione di Henderson-Hasselbalch
 Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
ph = log 1/[H + ] = log [H + ]
![ph = log 1/[H + ] = log [H + ] ph = log 1/[H + ] = log [H + ]](/thumbs/49/24977942.jpg) ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
equilibrio acido base
 Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Trasporto dei gas respiratori nel sangue
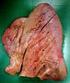 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
EMOGASANALISI ARTERIOSA
 EMOGASANALISI ARTERIOSA L EGA rappresenta l esame principe dell urgenza, poiché è un ottima finestra su: VENTILAZIONE ALVEOLARE SCAMBIO GASSOSO PH ed EQUILIBRIO ACIDO-BASE In particolare l equilibrio acido-base
EMOGASANALISI ARTERIOSA L EGA rappresenta l esame principe dell urgenza, poiché è un ottima finestra su: VENTILAZIONE ALVEOLARE SCAMBIO GASSOSO PH ed EQUILIBRIO ACIDO-BASE In particolare l equilibrio acido-base
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
EMOGASANALISI ARTERIOSA INTERPRETAZIONE
 EMOGASANALISI ARTERIOSA INTERPRETAZIONE A cosa serve? Esame rapido Valutare la ventilazione Valutare il metabolismo Valutare parametri quali: Emoglobina Glicemia Elettroliti Interpretazione emogasanalisi
EMOGASANALISI ARTERIOSA INTERPRETAZIONE A cosa serve? Esame rapido Valutare la ventilazione Valutare il metabolismo Valutare parametri quali: Emoglobina Glicemia Elettroliti Interpretazione emogasanalisi
Raffaele Alvisi 14 gennaio 1916
 Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
Emogasanalisi arteriosa: Valutaz. dell ossiemia Trasporto della PaCO2 Disturbi dell EAB. ph potere tampone compenso renale
 Emogasanalisi arteriosa: Valutaz. dell ossiemia Trasporto della PaCO2 Disturbi dell EAB ph potere tampone compenso renale EMOGASANALISI ARTERIOSA Misura l efficienza della funzione respiratoria e della
Emogasanalisi arteriosa: Valutaz. dell ossiemia Trasporto della PaCO2 Disturbi dell EAB ph potere tampone compenso renale EMOGASANALISI ARTERIOSA Misura l efficienza della funzione respiratoria e della
Equilibrio acido-base
 Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
L'EQUILIBRIO ACIDO-BASE
 L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia Obiettivi Produzione e bilancio degli idrogenioni Regolazione respiratoria e renale del ph Riassorbimento del bicarbonato e secrezione
Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia Obiettivi Produzione e bilancio degli idrogenioni Regolazione respiratoria e renale del ph Riassorbimento del bicarbonato e secrezione
Interpretazione dell emogasanalisi
 Interpretazione dell emogasanalisi Guglielmo IMBRIACO Gaetano TAMMARO Rianimazione Terapia Intensiva Ospedale MAGGIORE - Bologna A cosa serve l emogasanalisi? Esame rapido Valutare la ventilazione Valutare
Interpretazione dell emogasanalisi Guglielmo IMBRIACO Gaetano TAMMARO Rianimazione Terapia Intensiva Ospedale MAGGIORE - Bologna A cosa serve l emogasanalisi? Esame rapido Valutare la ventilazione Valutare
2.Controllo dell equilibrio acido-base - II. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
Rene ed equilibrio acido-base
 Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Emogasanalisi Arteriosa
 Emogasanalisi Arteriosa Dr. Francesco Ponzetta UO Anestesia Rianimazione NOCSAE Modena L'EGA è un analisi dei gas ematici su sangue arterioso, può essre effettuata in laboratorio ma anche, in maniera decentralizzata,
Emogasanalisi Arteriosa Dr. Francesco Ponzetta UO Anestesia Rianimazione NOCSAE Modena L'EGA è un analisi dei gas ematici su sangue arterioso, può essre effettuata in laboratorio ma anche, in maniera decentralizzata,
INTERPRETAZIONE DELL EMOGASANALISI ACQUA ELETTROLITI ED EQUILIBRIO ACIDI-BASE
 INTERPRETAZIONE DELL EMOGASANALISI ACQUA ELETTROLITI ED EQUILIBRIO ACIDI-BASE Il prelievo arterioso può essere eseguito a livello di arteria femorale e arteria radiale (più doloroso) Il prelievo venoso
INTERPRETAZIONE DELL EMOGASANALISI ACQUA ELETTROLITI ED EQUILIBRIO ACIDI-BASE Il prelievo arterioso può essere eseguito a livello di arteria femorale e arteria radiale (più doloroso) Il prelievo venoso
La eliminazione dei protoni nelle urine permette il ripristino di bicarbonato nel circolo sistemico.
 ESCREZIONE URINARIA DI ACIDI : 1-1,5 meq/l Es. produzione endogena di ac. solforico o cloridrico, formazione di sodio solfato o cloruro, eliminazione urinaria di ammonio legato ai sali. La eliminazione
ESCREZIONE URINARIA DI ACIDI : 1-1,5 meq/l Es. produzione endogena di ac. solforico o cloridrico, formazione di sodio solfato o cloruro, eliminazione urinaria di ammonio legato ai sali. La eliminazione
Tamponi Biologici. AO/Febbraio 2016
 Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Equilibrio acido base
 Equilibrio acido base Le Acidosi e Alcalosi Respiratorie INTRODUZIONE ACIDOSI RESPIRATORIA - Cause - Sintomi - Terapia ALCALOSI RESPIRATORIA - Cause - Sintomi - Terapia INTRODUZIONE I prodotti terminali
Equilibrio acido base Le Acidosi e Alcalosi Respiratorie INTRODUZIONE ACIDOSI RESPIRATORIA - Cause - Sintomi - Terapia ALCALOSI RESPIRATORIA - Cause - Sintomi - Terapia INTRODUZIONE I prodotti terminali
Biochimica clinica. Corso di Laurea Triennale in Biotecnologie per la salute
 Corso di Laurea Triennale in Biotecnologie per la salute Biochimica clinica Argomenti della lezione:» Aspetti generali dell'equilibrio acidobase» Regolazione renale e polmonare» Emogasanalisi Gli elettroliti
Corso di Laurea Triennale in Biotecnologie per la salute Biochimica clinica Argomenti della lezione:» Aspetti generali dell'equilibrio acidobase» Regolazione renale e polmonare» Emogasanalisi Gli elettroliti
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO BASE Le reazioni metaboliche sono molto sensibili a cambiamenti del ph: il ph dei liquidi dell organismo è mantenuto entro un range di valori molto stretto. ph intracellulare è generalmente
EQUILIBRIO ACIDO BASE Le reazioni metaboliche sono molto sensibili a cambiamenti del ph: il ph dei liquidi dell organismo è mantenuto entro un range di valori molto stretto. ph intracellulare è generalmente
SCOPI DELL EMOGASANALISI
 EMOGASANALISI SCOPI DELL EMOGASANALISI La funzione principale della respirazione è quella di assicurare ossigeno all organismo e di eliminare l eccesso di anidride carbonica. L emogasanalisi arteriosa
EMOGASANALISI SCOPI DELL EMOGASANALISI La funzione principale della respirazione è quella di assicurare ossigeno all organismo e di eliminare l eccesso di anidride carbonica. L emogasanalisi arteriosa
Presentazione della collana (Ivo Casagranda)... Prefazione... Hanno collaborato...
 pag. Presentazione della collana (Ivo Casagranda).................. Prefazione............................................ Hanno collaborato....................................... XVII XIX XXI Capitolo
pag. Presentazione della collana (Ivo Casagranda).................. Prefazione............................................ Hanno collaborato....................................... XVII XIX XXI Capitolo
Gli scambi gassosi LA MISURA DELLA FUNZIONE RESPIRATORIA. OLTRE LA SPIROMETRIA Torino, 5 ottobre 2013
 LA MISURA DELLA FUNZIONE RESPIRATORIA OLTRE LA SPIROMETRIA Torino, 5 ottobre 2013 Gli scambi gassosi Claudio Norbiato AO Ordine Mauriziano SC Medicina Interna Emogasanalisi L emogasanalisi e l analisi
LA MISURA DELLA FUNZIONE RESPIRATORIA OLTRE LA SPIROMETRIA Torino, 5 ottobre 2013 Gli scambi gassosi Claudio Norbiato AO Ordine Mauriziano SC Medicina Interna Emogasanalisi L emogasanalisi e l analisi
Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio
 Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
L INSUFFICIENZA RESPIRATORIA ACUTA DAL TERRITORIO ALLA MEDICINA D URGENZA
 L INSUFFICIENZA RESPIRATORIA ACUTA DAL TERRITORIO ALLA MEDICINA D URGENZA 28 SETTEMBRE 2010 NOLA MONITORAGGIO DEGLI SCAMBI GASSOSI ED ALTERAZIONI EMOGASANALITICHE DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA
L INSUFFICIENZA RESPIRATORIA ACUTA DAL TERRITORIO ALLA MEDICINA D URGENZA 28 SETTEMBRE 2010 NOLA MONITORAGGIO DEGLI SCAMBI GASSOSI ED ALTERAZIONI EMOGASANALITICHE DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA
EMOGASANALISI. Dr. Federico Olliveri Medicina d Urgenza H G. Bosco.
 EMOGASANALISI Dr. Federico Olliveri Medicina d Urgenza H G. Bosco Email: fed.olliveri@tin.it Gerarchia degli equilibri nell organismo: 1) equilibrio fra cariche elettriche 2) equilibrio osmolare 3) equilibrio
EMOGASANALISI Dr. Federico Olliveri Medicina d Urgenza H G. Bosco Email: fed.olliveri@tin.it Gerarchia degli equilibri nell organismo: 1) equilibrio fra cariche elettriche 2) equilibrio osmolare 3) equilibrio
Alterazione della capacità tampone nell'organismo. Alterazione capacità tampone rev. 0 - data: 5 luglio
 Alterazione della capacità tampone nell'organismo Alterazione capacità tampone rev. 0 - data: 5 luglio 2008 1 Il ph fisiologico dell'organismo è compreso tra 7.38 e 7.44 Nel liquido extracellulare sono
Alterazione della capacità tampone nell'organismo Alterazione capacità tampone rev. 0 - data: 5 luglio 2008 1 Il ph fisiologico dell'organismo è compreso tra 7.38 e 7.44 Nel liquido extracellulare sono
L EMOGASANALISI. P. Scavalli, M. Vitto, S. Mosillo
 L EMOGASANALISI P. Scavalli, M. Vitto, S. Mosillo EMOGASANALISI Consente la misurazione immediata dei due gas più importanti del sangue e di un terzo parametro fondamentale per la valutazione dell omeostasi
L EMOGASANALISI P. Scavalli, M. Vitto, S. Mosillo EMOGASANALISI Consente la misurazione immediata dei due gas più importanti del sangue e di un terzo parametro fondamentale per la valutazione dell omeostasi
aggiustamenti respiratori durante l esercizio fisico
 aggiustamenti respiratori durante l esercizio fisico 1 generalita durante l esercizio fisico aumento consumo O 2 e produzione CO 2 e calore e necessario portare piu O 2 ai tessuti e rimuovere piu CO 2
aggiustamenti respiratori durante l esercizio fisico 1 generalita durante l esercizio fisico aumento consumo O 2 e produzione CO 2 e calore e necessario portare piu O 2 ai tessuti e rimuovere piu CO 2
DEFINIZIONE ANALISI DELLE PRESSIONI PARZIALI DEI GAS E DEL EQUILIBRIO ACIDO- BASE NEL SANGUE ARTERIOSO
 DEFINIZIONE ANALISI DELLE PRESSIONI PARZIALI DEI GAS E DEL EQUILIBRIO ACIDO- BASE NEL SANGUE ARTERIOSO INDICAZIONI ALL EGA Dispnea (cardiaca, respiratoria, metabolica) Dolore toracico (embolie polmonari
DEFINIZIONE ANALISI DELLE PRESSIONI PARZIALI DEI GAS E DEL EQUILIBRIO ACIDO- BASE NEL SANGUE ARTERIOSO INDICAZIONI ALL EGA Dispnea (cardiaca, respiratoria, metabolica) Dolore toracico (embolie polmonari
domande iniziali Obiettivi della fluido terapia aspetti fisiologici solidi interstizio 14% LIC plasma transcellulare LEC = 20 %
 domande iniziali quando si deve praticare? quale tipo di soluz. impiegare? quanto liquido somministrare? con quale velocità di infusione? quale via di somministrazione? Obiettivi della fluido terapia Risoluzione
domande iniziali quando si deve praticare? quale tipo di soluz. impiegare? quanto liquido somministrare? con quale velocità di infusione? quale via di somministrazione? Obiettivi della fluido terapia Risoluzione
Controllo nervoso del respiro
 Controllo nervoso del respiro La respirazione è una funzione involontaria controllata da 3 gruppi di neuroni (centri) localizzati nel tronco encefalico: Controllo nervoso del respiro Centro respiratorio
Controllo nervoso del respiro La respirazione è una funzione involontaria controllata da 3 gruppi di neuroni (centri) localizzati nel tronco encefalico: Controllo nervoso del respiro Centro respiratorio
IL RUOLO DELL EMOGASANALISI NELL INSUFFIENZA RESPIRATORIA
 I CONGRESSO REGIONALE SIMEU BASILICATA 13 E 14 GIUGNO 2014 IL RUOLO DELL EMOGASANALISI NELL INSUFFIENZA RESPIRATORIA DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA NOCERAPAGANI SEGRETARIO NAZIONALE FIMEUC PRESISDENTE
I CONGRESSO REGIONALE SIMEU BASILICATA 13 E 14 GIUGNO 2014 IL RUOLO DELL EMOGASANALISI NELL INSUFFIENZA RESPIRATORIA DOTT.SSA GIOVANNA ESPOSITO PS e MU DEA NOCERAPAGANI SEGRETARIO NAZIONALE FIMEUC PRESISDENTE
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra ). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Equilibrio idroelettrolitico
 Equilibrio idroelettrolitico Sodio Potassio Sodio e volume extracellulare Bilancio e distribuzione dell acqua corporea Regolazione del bilancio dell acqua Aumento dell osmolarità o Riduzione del volume
Equilibrio idroelettrolitico Sodio Potassio Sodio e volume extracellulare Bilancio e distribuzione dell acqua corporea Regolazione del bilancio dell acqua Aumento dell osmolarità o Riduzione del volume
Teorie Acido-Base. Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH -
 Teorie Acido-Base Arrhenius: Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH - Broensted-Lowry: Gli acidi rilasciano H + Le basi accettano H + Lewis gli
Teorie Acido-Base Arrhenius: Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH - Broensted-Lowry: Gli acidi rilasciano H + Le basi accettano H + Lewis gli
PRINCIPALI SISTEMI TAMPONE
 SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
Equilibri acido-base, ph e sistemi tampone
 Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
Alterazioni equilibrio acidobase
 Alterazioni equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Acidosi: rapporto HCO 3 /CO 2 ph. Se diminuzione dipende da: HCO 3 acidosi metabolica (nonrespiratoria)
Alterazioni equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Acidosi: rapporto HCO 3 /CO 2 ph. Se diminuzione dipende da: HCO 3 acidosi metabolica (nonrespiratoria)
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Funzioni. Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto
 La Funzione Renale Funzioni Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto Il Nefrone Distinguiamo un tubulo renale (trasporto) ed un corpuscolo renale
La Funzione Renale Funzioni Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto Il Nefrone Distinguiamo un tubulo renale (trasporto) ed un corpuscolo renale
DEBOLE MEDIA FORTE FARMACI DIURETICI AD INTENSITÀ D AZIONE
 FARMACI DIURETICI AD INTENSITÀ D AZIONE a) osmotici mannitolo (Isotol), glicerina b) inibitori dell anidrasi carbonica acetazolamide (Diamox) c) risparmiatori di spironolattone (Aldactone, Spirolang),
FARMACI DIURETICI AD INTENSITÀ D AZIONE a) osmotici mannitolo (Isotol), glicerina b) inibitori dell anidrasi carbonica acetazolamide (Diamox) c) risparmiatori di spironolattone (Aldactone, Spirolang),
UNIVERSITÀ DI PISA ANALISI COMPARATIVA DI TRE APPROCCI DI VALUTAZIONE DELL EMOGAS VENOSO IN CANI SOTTOPOSTI A EMODIALISI
 UNIVERSITÀ DI PISA Dipartimento Di Scienze Veterinarie Corso di Laurea Magistrale in Medicina Veterinaria Tesi di Laurea ANALISI COMPARATIVA DI TRE APPROCCI DI VALUTAZIONE DELL EMOGAS VENOSO IN CANI SOTTOPOSTI
UNIVERSITÀ DI PISA Dipartimento Di Scienze Veterinarie Corso di Laurea Magistrale in Medicina Veterinaria Tesi di Laurea ANALISI COMPARATIVA DI TRE APPROCCI DI VALUTAZIONE DELL EMOGAS VENOSO IN CANI SOTTOPOSTI
1. Controllo dell equilibrio acido-base. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO - BASE da appunti del dott. Claudio Italiano, internista ospedaliero Che significa? Vuol dire che l organismo ha un suo equilibrio, detto omeòstasi, cioè il sangue deve necessariamente
EQUILIBRIO ACIDO - BASE da appunti del dott. Claudio Italiano, internista ospedaliero Che significa? Vuol dire che l organismo ha un suo equilibrio, detto omeòstasi, cioè il sangue deve necessariamente
EQUILIBRIO IDRO-ELETTROLITICO ED ACIDO-BASE EQUILIBRIO IDRO-ELETTROLITICO IL SODIO CONTENUTO CORPOREO DI ACQUA IL SODIO
 EQUILIBRIO IDROELETTROLITICO ED ACIDOBASE EQUILIBRIO IDROELETTROLITICO CONTENUTO CORPOREO DI ACQUA PLASMA = 4 L INTERSTIZIO = 18 L INTRACELLULARE = 28 L IL SODIO E CONTENUTO SOPRATTUTTO NELLO SPAZIO EXTRACELLULARE
EQUILIBRIO IDROELETTROLITICO ED ACIDOBASE EQUILIBRIO IDROELETTROLITICO CONTENUTO CORPOREO DI ACQUA PLASMA = 4 L INTERSTIZIO = 18 L INTRACELLULARE = 28 L IL SODIO E CONTENUTO SOPRATTUTTO NELLO SPAZIO EXTRACELLULARE
I VOLUMI DEI PRINCIPALI COMPARTIMENTI IDRICI DELL ORGANISMO CALCOLATI PER UN INDIVIDUO DI 70 Kg
 LEZIONE RENE 6 I VOLUMI DEI PRINCIPALI COMPARTIMENTI IDRICI DELL ORGANISMO CALCOLATI PER UN INDIVIDUO DI 70 Kg BL 4.2mM 150mM BILANCIO DEL POTASSIO 4 moli di K nei compartimenti liquidi Liquido intracellulare
LEZIONE RENE 6 I VOLUMI DEI PRINCIPALI COMPARTIMENTI IDRICI DELL ORGANISMO CALCOLATI PER UN INDIVIDUO DI 70 Kg BL 4.2mM 150mM BILANCIO DEL POTASSIO 4 moli di K nei compartimenti liquidi Liquido intracellulare
ALTERAZIONI IDROELETTROLITICHE
 ALTERAZIONI IDROELETTROLITICHE EQUILIBRIO IDROELETTROLITICO RUOLO DEL RENE: Il rene è l organo deputato al mantenimento dell equilibrio idrico ed elettrolitico dell organismo EQUILIBRIO IDROELETTROLITICO
ALTERAZIONI IDROELETTROLITICHE EQUILIBRIO IDROELETTROLITICO RUOLO DEL RENE: Il rene è l organo deputato al mantenimento dell equilibrio idrico ed elettrolitico dell organismo EQUILIBRIO IDROELETTROLITICO
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE
 FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
4ª UNITA DIDATTICA Modello Nutrizionale metabolico
 4ª UNITA DIDATTICA Modello Nutrizionale metabolico Contenuti Modello Nutrizionale metabolico Sezione del modello: Equilibrio idro-elettrolitico e acido-base Assistenza alla persona con problemi relativi
4ª UNITA DIDATTICA Modello Nutrizionale metabolico Contenuti Modello Nutrizionale metabolico Sezione del modello: Equilibrio idro-elettrolitico e acido-base Assistenza alla persona con problemi relativi
I compartimenti liquidi corporei
 Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Sistema urinario: la funzione renale
 Sistema urinario: la funzione renale FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici, i reni ne regolano la concentrazione plasmatica
Sistema urinario: la funzione renale FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici, i reni ne regolano la concentrazione plasmatica
ALTERAZIONI IDROELETTROLITICHE ED ACIDO-BASE
 ALTERAZIONI IDROELETTROLITICHE ED ACIDO-BASE EQUILIBRIO IDROELETTROLITICO RUOLO DEL RENE: Il rene è l organo deputato al mantenimento dell equilibrio idrico ed elettrolitico dell organismo EQUILIBRIO IDROELETTROLITICO
ALTERAZIONI IDROELETTROLITICHE ED ACIDO-BASE EQUILIBRIO IDROELETTROLITICO RUOLO DEL RENE: Il rene è l organo deputato al mantenimento dell equilibrio idrico ed elettrolitico dell organismo EQUILIBRIO IDROELETTROLITICO
45. Fisiologia dell'equilibrio acido-base
 Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione ebook Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione ebook Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
Quadri emogasanalitici complessi in terapia intensiva. Dott.ssa Valentina Alvisi U.O. Anestesia e Rianimazione Universitaria
 Quadri emogasanalitici complessi in terapia intensiva. Dott.ssa Valentina Alvisi U.O. Anestesia e Rianimazione Universitaria Normali valori dell EGA ph 7.35 7.45 PCO 2 PO 2 HCO 3 35 45 mmhg 80 100 mmhg
Quadri emogasanalitici complessi in terapia intensiva. Dott.ssa Valentina Alvisi U.O. Anestesia e Rianimazione Universitaria Normali valori dell EGA ph 7.35 7.45 PCO 2 PO 2 HCO 3 35 45 mmhg 80 100 mmhg
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE
 Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
La spirometria. La spirometria
 La spirometria La spirometria studia a fondo la funzione polmonare. Con questo semplice esame infatti è possibile determinare numerosi parametri che guidano il medico nella diagnosi delle malattie polmonari.
La spirometria La spirometria studia a fondo la funzione polmonare. Con questo semplice esame infatti è possibile determinare numerosi parametri che guidano il medico nella diagnosi delle malattie polmonari.
I compartimenti liquidi corporei
 Bilancio idrico I compartimenti liquidi corporei Mantenere costanti volume ed osmolarità dei liquidi corporei è essenziale per l omeostasi. Questo è possibile solo se assunzione ed eliminazione di H 2
Bilancio idrico I compartimenti liquidi corporei Mantenere costanti volume ed osmolarità dei liquidi corporei è essenziale per l omeostasi. Questo è possibile solo se assunzione ed eliminazione di H 2
Proprietà delle Soluzioni
 Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Prof. Antonio Galzerano, Azienda ospedaliero-universitaria SMM di Perugia. Peter Stewart1981
 Prof. Antonio Galzerano, Azienda ospedaliero-universitaria SMM di Perugia Peter Stewart1981 www.acidbase.org - Uno stretto controllo della concentrazione degli idrogenioni è indispensabile per l attività
Prof. Antonio Galzerano, Azienda ospedaliero-universitaria SMM di Perugia Peter Stewart1981 www.acidbase.org - Uno stretto controllo della concentrazione degli idrogenioni è indispensabile per l attività
Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori:
 Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori: 1) Dalla differenza netta di pressione tra il lume del capillare ed il lume della capsula di Bowman; 2) dalla
Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori: 1) Dalla differenza netta di pressione tra il lume del capillare ed il lume della capsula di Bowman; 2) dalla
Chetoacidosi diabetica Sindrome iperosmolare
 Chetoacidosi diabetica Sindrome iperosmolare DKA Cheto-acidosi Diabetica Insufficienza Insulinica (relativa!) corpi chetonici Acidosi metabolica Disidratazione (grave) shock Metabolismo epatico Corpi chetonici
Chetoacidosi diabetica Sindrome iperosmolare DKA Cheto-acidosi Diabetica Insufficienza Insulinica (relativa!) corpi chetonici Acidosi metabolica Disidratazione (grave) shock Metabolismo epatico Corpi chetonici
Ad esempio un acido, come HCl, si dissocia in acqua per fornire idrogenioni nel seguente modo:
 Fisiologia, fisiopatologia e terapia dei disturbi dell equilibrio acido-base. C. Terzano L obiettivo di questo capitolo è duplice: 1) fornire le basi necessarie per comprendere l equilibrio acidobase,
Fisiologia, fisiopatologia e terapia dei disturbi dell equilibrio acido-base. C. Terzano L obiettivo di questo capitolo è duplice: 1) fornire le basi necessarie per comprendere l equilibrio acidobase,
DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE
 VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
L emogas analisi (EGA) Arterial Blood Gases (ABG) analysis. Marianna Maranghi
 L emogas analisi (EGA) Arterial Blood Gases (ABG) analysis Marianna Maranghi Leggere l EGA in 6 punti 1. Il ph è normale? 2. La CO2 è normale? 3. L HCO3 è normale? 4. Accoppia la CO2 o l HCO3 con il ph
L emogas analisi (EGA) Arterial Blood Gases (ABG) analysis Marianna Maranghi Leggere l EGA in 6 punti 1. Il ph è normale? 2. La CO2 è normale? 3. L HCO3 è normale? 4. Accoppia la CO2 o l HCO3 con il ph
tra fisiopatologia e clinica AOU S. Maria della Misericordia Udine
 Acidosi metabolica tra fisiopatologia e clinica RG CRAVERO AOU S. Maria della Misericordia Udine Casi clinici Ragazza di 31 anni, sintomatica per astenia da diversi giorni, nei giorni precedenti sintomi
Acidosi metabolica tra fisiopatologia e clinica RG CRAVERO AOU S. Maria della Misericordia Udine Casi clinici Ragazza di 31 anni, sintomatica per astenia da diversi giorni, nei giorni precedenti sintomi
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Gli equilibri omeodinamici: dalla fisiopatologia alla clinica pratica
 CONVEGNO SIMI Gli equilibri omeodinamici: dalla fisiopatologia alla clinica pratica Dr. Francesco Sgambato U. O. Complessa di Medicina Interna Ospedale Fatebenefratelli - Benevento sgambatof@gmail.com
CONVEGNO SIMI Gli equilibri omeodinamici: dalla fisiopatologia alla clinica pratica Dr. Francesco Sgambato U. O. Complessa di Medicina Interna Ospedale Fatebenefratelli - Benevento sgambatof@gmail.com
Interpretazione rapida dell emogasanalisi
 Interpretazione rapida dell emogasanalisi ph (7,35-7,45) PaCO2 (35-45 mmhg) Bicarbonato Standard (22-26 meq/l) Anion Gap [ Na (HCO3 + Cl) = 12 +- 2] PaO2 (60aa-80; 70-70; 80aa-60) PaO2/FiO2 (> 350; < 300
Interpretazione rapida dell emogasanalisi ph (7,35-7,45) PaCO2 (35-45 mmhg) Bicarbonato Standard (22-26 meq/l) Anion Gap [ Na (HCO3 + Cl) = 12 +- 2] PaO2 (60aa-80; 70-70; 80aa-60) PaO2/FiO2 (> 350; < 300
Fisiologia Renale 8. Bilancio idro-elettrolitico III. Carlo Capelli, Fisiologia Generale e dell Esercizio Facoltà di Scienze Motorie di Verona
 Fisiologia Renale 8. Bilancio idro-elettrolitico III Carlo Capelli, Fisiologia Generale e dell Esercizio Facoltà di Scienze Motorie di Verona Obiettivi Bilancio del sodio e regolazione del volume extracellulare
Fisiologia Renale 8. Bilancio idro-elettrolitico III Carlo Capelli, Fisiologia Generale e dell Esercizio Facoltà di Scienze Motorie di Verona Obiettivi Bilancio del sodio e regolazione del volume extracellulare
scaricato da sunhope.it Edema
 Edema rigonfiamento cutaneo evidente all esame obiettivo, quindi visibile e/o palpabile, da aumento liquido interstiziale sede consistenza evidenza localizzato, se alterazione non sistemica generalizzato,
Edema rigonfiamento cutaneo evidente all esame obiettivo, quindi visibile e/o palpabile, da aumento liquido interstiziale sede consistenza evidenza localizzato, se alterazione non sistemica generalizzato,
Fisiologia Renale 6. Bilancio idro-elettrolitico I. Carlo Capelli Fisiologia Corso di Laurea in Scienze Motorie Università di Verona
 Fisiologia Renale 6. Bilancio idro-elettrolitico I Carlo Capelli Fisiologia Corso di Laurea in Scienze Motorie Università di Verona Obiettivi Acqua corporea totale: volume e distribuzione Distretti intra
Fisiologia Renale 6. Bilancio idro-elettrolitico I Carlo Capelli Fisiologia Corso di Laurea in Scienze Motorie Università di Verona Obiettivi Acqua corporea totale: volume e distribuzione Distretti intra
L acidosi metabolica Giuseppe Regolisti
 L acidosi metabolica Giuseppe Regolisti Terapia Intensiva Dipartimento di Emergenza-Urgenza e Area Medica Generale e Specialistica Azienda Ospedaliero-Universitaria e Università degli Studi di Parma Prevalenza
L acidosi metabolica Giuseppe Regolisti Terapia Intensiva Dipartimento di Emergenza-Urgenza e Area Medica Generale e Specialistica Azienda Ospedaliero-Universitaria e Università degli Studi di Parma Prevalenza
17/05/2010. Equilibrio idrico. Variazioni del volume ematico indicono risposte omeostatiche
 Equilibrio idrico Variazioni del volume ematico indicono risposte omeostatiche 1 Ruolo del rene nel bilancio idrico Variazioni dell osmolarità attraverso la midollare 2 Scambio per controcorrente nella
Equilibrio idrico Variazioni del volume ematico indicono risposte omeostatiche 1 Ruolo del rene nel bilancio idrico Variazioni dell osmolarità attraverso la midollare 2 Scambio per controcorrente nella
PROGRAMMA DEL CORSO. ipossica. ipossico-ipercapnica. Lo scambio dei gas. L Insufficienza respiratoria
 PROGRAMMA DEL CORSO Lo scambio dei gas L Insufficienza respiratoria ipossica ipossico-ipercapnica L equilibrio acido base e l emogasanalisi normale EGA:tecnica di esecuzione EGA:principi teorici e interpretazione
PROGRAMMA DEL CORSO Lo scambio dei gas L Insufficienza respiratoria ipossica ipossico-ipercapnica L equilibrio acido base e l emogasanalisi normale EGA:tecnica di esecuzione EGA:principi teorici e interpretazione
Acqua: nutriente essenziale
 Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
Classificazione dei principali Diuretici
 Classificazione dei principali Diuretici 1. Diuretici Osmotici 2. Inibitori dell Anidrasi Carbonica 3. Tiazidici 4. Diuretici dell ansa 5. Risparmiatori di potassio Tiazidi Agenti risparmiatori di potassio
Classificazione dei principali Diuretici 1. Diuretici Osmotici 2. Inibitori dell Anidrasi Carbonica 3. Tiazidici 4. Diuretici dell ansa 5. Risparmiatori di potassio Tiazidi Agenti risparmiatori di potassio
Il Sangue e il Plasma 1. Caratteristiche fisico-chimiche del sangue. Carlo Capelli Fisiologia Università di Verona
 Il Sangue e il Plasma 1. Caratteristiche fisico-chimiche del sangue Carlo Capelli Fisiologia Università di Verona Obiettivi 1. Funzioni e composizione del sangue 2. Sedimentazione e concentrazione: VES
Il Sangue e il Plasma 1. Caratteristiche fisico-chimiche del sangue Carlo Capelli Fisiologia Università di Verona Obiettivi 1. Funzioni e composizione del sangue 2. Sedimentazione e concentrazione: VES
Controllo nervoso del respiro
 Controllo nervoso del respiro La respirazione è una funzione involontaria controllata da 3 gruppi di neuroni (centri) localizzati nel tronco encefalico: Controllo nervoso del respiro Centro respiratorio
Controllo nervoso del respiro La respirazione è una funzione involontaria controllata da 3 gruppi di neuroni (centri) localizzati nel tronco encefalico: Controllo nervoso del respiro Centro respiratorio
Siti. d azione dei diuretici
 Siti d azione dei diuretici I diuretici aumentano la velocità del flusso urinario e la natriuresi (maggiore velocità di escrezione di Na + ). Modificano anche l escrezione di vari ioni: K +, H +,Cl - e
Siti d azione dei diuretici I diuretici aumentano la velocità del flusso urinario e la natriuresi (maggiore velocità di escrezione di Na + ). Modificano anche l escrezione di vari ioni: K +, H +,Cl - e
Fisiologia Renale 5. Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale 5. Equilibrio acidobase: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Produzione e bilancio
Fisiologia Renale 5. Equilibrio acidobase: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Produzione e bilancio
FOGLIO ILLUSTRATIVO. Sodio bicarbonato S.A.L.F. 1,4% soluzione per infusione Sodio bicarbonato S.A.L.F. 8,4% soluzione per infusione
 FOGLIO ILLUSTRATIVO Sodio bicarbonato S.A.L.F. 1,4% soluzione per infusione Sodio bicarbonato S.A.L.F. 8,4% soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Elettroliti. INDICAZIONI TERAPEUTICHE Trattamento
FOGLIO ILLUSTRATIVO Sodio bicarbonato S.A.L.F. 1,4% soluzione per infusione Sodio bicarbonato S.A.L.F. 8,4% soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Elettroliti. INDICAZIONI TERAPEUTICHE Trattamento
Contiene informazioni su: diagnosi differenziale degli stati confusionali acuti, gestione clinica dell alcalosi metabolica
 Capitolo 9 Alterazione acuta dello stato di coscienza e della vigilanza, associata a respiro superficiale, in persona affetta da linfoma non Hodgkin alto grado, stadio III B, sottoposta di recente a trattamento
Capitolo 9 Alterazione acuta dello stato di coscienza e della vigilanza, associata a respiro superficiale, in persona affetta da linfoma non Hodgkin alto grado, stadio III B, sottoposta di recente a trattamento
EMOGASANALISI ARTERIOSA
 EMOGASANALISI ARTERIOSA U.O.S PNEUMOLOGIA Ospedale «PISPICO» POGGIARDO Dott.ssa L.FERRAMOSCA EMOGASANALISI ARTERIOSA E FACILE DA ESEGUIRE E RAPIDA E SOLO LIMITATAMENTE INVASIVA COMPLICANZE INFREQUENTI
EMOGASANALISI ARTERIOSA U.O.S PNEUMOLOGIA Ospedale «PISPICO» POGGIARDO Dott.ssa L.FERRAMOSCA EMOGASANALISI ARTERIOSA E FACILE DA ESEGUIRE E RAPIDA E SOLO LIMITATAMENTE INVASIVA COMPLICANZE INFREQUENTI
In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + +
 Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
ph = log 1/[H+] = - log [H+]
![ph = log 1/[H+] = - log [H+] ph = log 1/[H+] = - log [H+]](/thumbs/34/16948015.jpg) ph = log 1/[H+] = log [H+] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = inizio 7,36 max 6.8) ph superiori = alcalosi (limite ph inizio 7,44 max 7.8) ph intracellulare
ph = log 1/[H+] = log [H+] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = inizio 7,36 max 6.8) ph superiori = alcalosi (limite ph inizio 7,44 max 7.8) ph intracellulare
SOLUZIONI ELETTROLITICHE. Classificazione dello Shock Ipovolemico Traumatico Cardiogeno Settico (Hyperdynamic/Hypodynamic) Neurogeno Hypoadrenal
 SOLUZIONI ELETTROLITICHE Classificazione dello Shock Ipovolemico Traumatico Cardiogeno Settico (Hyperdynamic/Hypodynamic) Neurogeno Hypoadrenal 1 La terapia infusionale Lo scopo della terapia infusionale
SOLUZIONI ELETTROLITICHE Classificazione dello Shock Ipovolemico Traumatico Cardiogeno Settico (Hyperdynamic/Hypodynamic) Neurogeno Hypoadrenal 1 La terapia infusionale Lo scopo della terapia infusionale
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Dott.ssa Marta Tavecchia. COS E IL ph?
 Dott.ssa Marta Tavecchia COS E IL ph? IL RENE: COSA FA? Regola il bilancio idrico Regola il bilancio elettrolitico Regola l equilibrio acido base Elimina le scorie del metabolismo azotato Svolge un ruolo
Dott.ssa Marta Tavecchia COS E IL ph? IL RENE: COSA FA? Regola il bilancio idrico Regola il bilancio elettrolitico Regola l equilibrio acido base Elimina le scorie del metabolismo azotato Svolge un ruolo
