Tecniche elettroforetiche
|
|
|
- Gabriela Giorgi
- 8 anni fa
- Просмотров:
Транскрипт
1 Tecniche elettroforetiche Biochimica e biotecnologie degli alimenti Lezione 4
2 Elettroforesi L elettroforesi è la migrazione di ioni in un campo elettrico. L elettroforesi di proteine utilizza di norma supporti costituiti da gel di poliacrilammide (PAGE) che separano le proteine in base alle dimensioni ed alla carica delle molecole. È un supporto molto usato perchéha una porositàomogenea e riproducibile.
3 Elettroforesi Il gel di poliacrilammide è un copolimero cross-linked della acrilammide. Il gel si prepara per polimerizzazione di una soluzione di un monomero monofunzionale, l'acrilammide (CH 2 =CH-CO-NH 2 ), e uno bifunzionale, la N,N'-metilen-bis-acrilammide(CH 2 =CH-CO-NH-CH 2 -NH-CO-CH=CH 2 ). La polimerizzazione avviene per mezzo di una reazione a catena dovuta all'aggiunta di ammonio persolfato e della base N,N,N',N'-tetrametiletilendiammina (TEMED). Il TEMED catalizza la decomposizione dello ione persolfato con la produzione del corrispondente radicale libero. In questo modo si formano catene di acrilammide tenute insieme da legami crociati di bis-acrilammide.
4 SDS-PAGE Nell elettroforesi in presenza di SDS, le proteine sono denaturate mediante l aggiunta del detergente sodio dodecil solfato (SDS) che denatura le proteine conferendo a tutte una carica netta negativa. [CH 3 -(CH 2 ) 10 -CH 2 -OSO 3- ]Na Interagisce con le proteine in un rapporto costante di circa 1.4 g SDS ogni g di proteina. Le cariche negative dell SDS mascherano la carica intrinseca della proteina conferendo a tutte un rapporto carica/massa simile. La separazione avviene quindi mediante filtrazione su gel in base alla massa delle proteine.
5 Colorazione Per visualizzare le proteine si ricorre a colorazioni specifiche O S C H 2 5 CH N C N CH CH C H SO H C 5 2 N C H 2 5 Nitrato d argento (1-2 ng) Ponceau S (100 1,000 ng) Coomassie Blue( ng)
6 SDS-PAGE Mediante SDS-PAGE è possibile determinare la massa molecolare delle proteine. La mobilità relativa (migrazione) è in questo caso direttamente proporzionale al logaritmo della sua massa molecolare. E possibile costruire rette di calibrazione utilizzando proteine con peso molecolare noto.
7 SDS-PAGE Mediante SDS-PAGE è possibile determinare la composizione in subunità di una proteina multimerica. In presenza di un agente riducente (DTT o Mecaptoetanolo) si ha la rottura dei ponti disolfurici e la separazione su gel delle subunità. Proteina dimericacon due subunità A B Proteina con una subunità C SDS e Mercaptoetanolo Elettroforesi su gel di poliacrilammide Gel di poliacrilammide
8 SDS-PAGE Mediante SDS-PAGE è possibile monitorare l andamento della purificazione e verificare il livello di purezza della proteina di interesse.
9 Focalizzazione isoelettrica Per isoelettrofocalizzazione (IEF) o focalizzazione isoelettrica si intende un processo per il quale le proteine si separano su un supporto solido, molto spesso un gel, in base al loro punto isoelettrico. Questa tecnica elettroforetica viene quindi utilizzata sia per la separazione di proteine che per determinarne il loro punto isoelettrico. Sul gel viene creato un gradiente di ph grazie a miscele di anfoliti che, una volta applicato un campo elettrico, si dispongono tra anodo e catodo conferendo in quel punto un ph uguale al loro pi.
10 2D-PAGE Nell'elettroforesi bidimensionale, tecnica elettroforetica utilizzata nel campo della proteomica per separare miscele proteiche complesse, le proteine sono separate in due dimensioni sfruttando principi fisici differenti. Nel caso dell'elettroforesi bidimensionale, i principi più utilizzati sono il punto isoelettrico e il peso molecolare.
11 Dal genoma al proteoma Lo studio della chimica delle proteine può essere basato su approcci differenti e complementari che includono l approccio biochimico tradizionale e il più recente approccio proteomico.
12 Dal genoma al proteoma PROTEOMA: PROTEine espresse dal genoma Il termine PROTEOMA è stato coniato nel 1994 da Marc Wilkins (Macquarie University, Sydney) TOTALITÀDELLE PROTEINE ESPRESSE DAL GENOMA IN UNA DATA CELLULA IN UN CERTO ISTANTE, INCLUSE LE ISOFORME E LE PROTEINE MODIFICATE POST- TRADUZIONALMENTE (Wilkins, 1994)
13 Dal genoma al proteoma
14 Dal genoma al proteoma Nell era post-genomica, lo studio del proteoma mediante approcci innovativi è estremamente promettente per fornire risposte concrete a problematiche in campo biomedico ed agroalimentare.
15 Approccio proteomico Pre-frazionamento 2D-PAGE 1D-LC o 2D-LC MALDI-ToF F MS Tandem MS (MS/MS) Ricerca in banca dati
16 2D-PAGE
17 I Dimensione: focalizzazione isoelettrica Supporto per IEF Alto ph Basso ph
18 I Dimensione: focalizzazione isoelettrica Alto ph Basso ph 8 Ore
19 I Dimensione: focalizzazione isoelettrica Le proteinemigrerannonelcampo elettricofinoa quandopi = ph dove la lorocaricanettasaràugualea zero Alto ph Basso ph 16 Ore
20 II Dimensione: : SDS-PAGE Gel di poliacrilammide
21 II Dimensione: : SDS-PAGE Setacciomolecolare Gel di poliacrilammide
22 II Dimensione: : SDS-PAGE Gel di poliacrilammide + ve + ve
23 Metodi di lisi
24 Metodi di lisi
25 Solubilizzazione, denaturazione e riduzione UREA DETERGENTI L urea è l agente denaturante più utilizzato, in casi specifici con problemi di solubilizzazione si può utilizzare la tiourea. Normalmente si utilizza urea 8M, ma anche miscele di tiourea 2M e urea 5-8M. I detergenti vengono aggiunti per rompere interazioni idrofobiche e incrementare la solubilità proteica. I detergenti devono essere non ionici o zwitterionici. Di solito viene utilizzato il CHAPS AGENTI RIDUCENTI Necessari per rompere i ponti disolfurici e mantenere in forma ridotta le proteina. Generalmente si utilizza o ditiotreitolo(dtt) o tributil-fosfina(tbp). ANFOLITI Per ogni range di ph una miscela di anfoliti carrier che aumentano la solubilità del campione e generano una conduttività uniforme attraverso il gradiente di ph durante l IEF
26 Solubilizzazione dei campioni biologici Tipo di campione Cellule eucariotiche Tampone di solubilizzazione urea 7M, tiourea 2M, CHAPS 2%, TX-100 2%, DTT 1%, Anfoline 1.6%, TRIS 15mM, PMSF 3mM Membrane cellulari, membrane globulo rosso urea 7M, tiourea 2M, CHAPS 2%, TX-100 2%, DTT 1%, Anfoline 1.6%, TRIS 15mM Tessuto muscolare tal quale urea 9.5M, CHAPS 2%, DTT 1%, Anfoline 2%, PMSF 3mM Tessuti già estratti ad esempio con guanidinio cloruro (es. muscolo, fegato, rene, ghiandola mammaria, cervello) Urea 8M, CHAPS 4%, DTT 1%, Anfoline 1.6%, TRIS 15mM Urine Urea 8M, CHAPS 4%, DTT 1%, Anfoline 1.6% Estratto da microrganismi Urea 8M, CHAPS 4%, DTT 1%, Anfoline 1.6%, TRIS 10mM Siero, plasma, liquido sinoviale Latte Urea 8M, CHAPS 4%, DTT 1%, Anfoline 1.6%, TRIS 15mM urea 7M, tiourea 2M, CHAPS 4%, DTT 1%, Anfoline 1.6%, TRIS 15mM
27 Gradienti di ph generati da anfoliti Miscele complesse di acidi poliammino-policarbossilici sintetici altamente solubili molecole anfoteriche(presenza contemporanea di gruppi basici e acidici => hanno un pi determinato da questi gruppi) alto poteretamponanteal loropi Quando èapplicato una voltaggio alla miscela di anfoliti, questi si muoveranno in base al loro pi allineandosi tra i due poli, creando un gradiente continuo di ph SVANTAGGI Il gradientenon èstabile neltempo (spostamento) e la forma del gradienteè influenzabile dalle molecole che vengono analizzate
28 Gradienti di ph immobilizzati Il gradiente di ph viene creato con setdi tamponi derivati dall acrilammide, copolimerizzazandoli entro le fibre della matrice CH 2 CH C N R R= -COOH oppure N(CH 3 ) 2 O H IMMOBILINE La copolimerizzazione di questi monomeri con diverso pkain diversa concentrazione permette di creare dei gradienti preformati di ph all'interno del gel. Una volta integrate nel gel, le immobiline conferiscono una capacità tamponante controllata e una bassa conduttività all'interno del gradiente
29 Gradienti di ph immobilizzati Sottili strisce di gel di poliacrilamideal 5% T polimerizzato su un supporto di plastica Utilizzano gradienti di ph immobilizzati Acquistate in commercio oppure prodotte direttamente in laboratorio Disponibili in differenti lunghezze e rangedi ph (7, 11, 13, e 18 e 24 cm) Disidratate Devono essere reidratate prima dell IEF
30 Vantaggi dei gradienti di ph immobilizzati Possibilità di reperire in commercio gel preformati minimizzando variazioni dovute alla preparazione dei gel I gel vengono preparati su una pellicola di plastica che ne facilita l utilizzo I gradienti di ph sono stabili nel tempo e non subiscono alterazioni dovute alla presenza del campione stesso Il gradiente pre-esiste al passaggio della corrente, essendo creato al momento della polimerizzazione I gradientisonopraticamentecontinuie possonoesserecostruitisecondodiverse esigenze: lineari/non lineari; ampi(ad esempio ph 3-10)/molto ristretti(ph 4-5)
31 Parametri per la reidratazione Nota:occorre rispettare i limiti di volume e quantitàdi proteina caratteristici del tipo di strip che si sta utilizzando Volumi maggiori entrata prefereneziale di molecole a basso peso molecolare (prima acquapoi altriionie per ultimeproteinead alto PM). Volumi minori il gel non si rigonfia alle opportune dimensioni. Le dimensioni dei pori della matrice non sono controllati e pari a quelli prestabiliti. Questo porta ad una difficolta nell analizzare proteine ad alto PM.
32 Reidratazione Le IPG strips sono reidratate over night La soluzione di reidratazione è applicata alle scanalature del supporto In ciascuna scanalatura viene posta una strip Ogni strip viene coperta con olio di paraffina per minimizzare l evaporazione e la cristallizzazione dell urea e per evitare il contatto con la CO 2 che, se adsorbita dal gel, può provocare un acidificazione della matrice con conseguente errata VALUTAZIONE dei punti isoelettrici Immobiline DryStrip reswelling tray
33 Reidratazione strip holder Ettan IPGPhor (Amersham Bioscience)
34
35 Prima dimensione:ief Il punto Isoelettrico di una proteina Le proteine sono molecole anfipatichedotate di gruppi acidi e basici. ph<pi ph=pi ph>pi Ogni proteina ha un particolare punto isoelettrico. La carica netta della proteina dipende dal ph dell ambiente in cui essa si trova. Quando il ph èuguale al pi della proteina, la carica netta diventa ZERO.
36 Prima dimensione:ief ph basso: Le proteine vengono protonate Carica positiva Anodo Anodo IPG strip Campo elettrico Proteine acide ph alto: Le proteine vengono deprotonate carica negativa Le proteine cariche migrano all interno del gradiente di ph Catodo Quando le proteine raggiungono il valore di ph corrispondente al proprio pi, la loro carica netta diviene zero ed esse focalizzano come bande discrete Catodo Proteine basiche
37 Isoelettrofocalizzazione Non esiste un protocollo di isolelettrofocalizzazione universale ogni singolo passo deve/può essere ottimizzato in funzione del campione in esame Aumento progressivo dei voltaggi in modo tale che nelle prime fasi della IEF gli ioni presenti nel campione (ioni presenti nel campione, lysis buffer o controioni dei gruppiacidio basicidel gel) venganotrasportatifuoridalgel Temperatura: 20 C: più bassa l urea cristallizza, più alta (>37 C) l urea modifica le proteine Multiphor II Ettan IPGphor II
38 / V V V V V V V V V 3h 2h 2h 2h 2h 2h 2h 2h 48h La definizione dei metodi e di fondamentale importanza al fine di riprodurre al meglio le stesse condizioni in corse effettuate separatamente compensando eventuali variazioni dei voltaggi applicati dovute a variazioni della conducibilità(diversa resistenza dei campioni)
39 Passaggio dalla I alla II dimensione La transizione dalla prima alla seconda dimensione coinvolge l equilibratura della striscia in tampone contenente SDS e la riduzione ed alchilazione dei pondi disolfuro mediante l uso di DDT (ditiotreitolo) e IAM (iodoacetamide) al fine di bloccare i gruppi SH delle proteine prevenendo la formazione di ponti disolfuro durante la seconda dimensione S-S TBP or DTT - DTE H 2 O H + S-S TBP + H O - 2 H + S - - S TBP =O I NH 2 O = SH S HI =NH2 O
40 Equilibrio Tampone di Equilibrio (Tris-HCl 50 mm ph 8.4) mantiene il ph della strip nel range appropriato per l elettroforesi. Urea (6 M) Riduce gli effetti dell elettroendosmosi aumentando la viscosità del tampone. L elettroendosmosi(eeo) è dovuta alla presenza di cariche negative fissate sulla IPG strip. EEO causa un flusso di acqua che ostacola la migrazione delle proteine e può interferire con il trasferimento delle stesse dalla strip al gel della seconda dimensione Glycerol(30 %) Riduce gli effetti dell elettroendosmosie facilita il trasferimento delle proteine dalla strip al gel per la seconda dimensione. SDS (2 %) Denatura le proteine e le carica negativamente. Step 1: Ditiotreitolo(DTT) (2 %) 15 minuti Riduce i ponti disolfuro preservando lo stato denaturato delle proteine. Step 2: Iodoacetammide(IAA) (2.5 %) 10 minuti Alchila i gruppi tiolicidelle proteine prevenendo la riossidazionedei ponti disolfuricidurante l elettroforesi. Blu di Bromofenolo(BFB) (tracce) Colorante consente di seguire l andamento della migrazione.
41 II Dimensione: : SDS-PAGE Trasferimento della strip equilibrata sul gel SDS-PAGE ETTAN Daltsix MINI PROTEAN
42 Visualizzazione degli spot Al termine della seconda dimensione si procede alla colorazione del gel La scelta della colorazione dipenderà soprattutto dalla quantità di proteine caricate Le colorazioni non devono interferire con i processi successivi (es. spettrometria di massa) Nitrato di Argento meno di 1 ng sensibilità CommassieBrilliantBlue (CBB) Colloidale G-250: circa 5 10 ng Coomassie Brilliant Blue (CBB) R-250 : circa ng Coloranti fluorescenti (SYPRO Ruby o Deep Purple) Colorantispecificiper proteinemodificatepost-traduzionalmente(pro Diamond e Emerald per fosfo- e glicoproteine, rispettivamente.
43 Esempio di elettroforesi bidimensionale ad elevata risoluzione E. coli 2-D map Lisato totale I dimensione: strip 18cm ph 3-10 NL II dimensione: gel di poliacrilammide con gradiente 9 16 %T colorato con Nitrato d argento.
44 Analisi d immagine Al termine della separazione delle proteine mediante 2DE, al fine di procedere all analisi d espressione differenziale, è indispensabile effettuare: 1. La digitalizzazione delle mappe bidimensionali 2. Il confronto degli elettroferogrammi ottenuti Algoritmi specifici permettono di rilevare gli spot (detection), rimuovere il rumore di fondo (background noise subtraction), allineare e confrontare (matching( matching) ) i gel, creando immagini sintetiche, e valutando i differenti livelli di espressione proteica sfuttando basi statistiche
45 Analisi d immagine Strumenti per l analisi d immagine Phosphoimager Marcaturacon 32 P e 35 S Fluoroimager Marcatura in fluorescenza Densitometro o Photo Scanner
46 Detection
47 Analisi d immagine A B C GEL SINTETICO A+B+C+D+E E D
48 Proteomica differenziale Mediante l utilizzo dei metodi di indagine proteomica è possibile effettuare un analisi quali/quantitativa delle proteine differenzialmente espresse.
49 Analisi d immagine ph 10 Non linear IPG 3-10 ph 3 ph 10 Non linear IPG 3-10 ph Mr kda 10 Differenze quantitative Differenze qualitative
50 chefare con le proteine separate mediante 2D-PAGE???
51 Taglio degli spot proteici
52 Digestione delle proteine Transfer Gel Piece to Test Tube Mass prep station Destain Dehydrate Rehydrate with Trypsin Solution Incubate at 37 C for16 h
53 Deposizione sul target plate del MALDI
54 Digestione delle proteine Per avere informazioni sull identità della proteina è necessario romperla in frammenti più piccoli!
55 Digestione delle proteine proteina ammino acido
56 Digestione delle proteine proteina Arginina Lisina
57 Digestione delle proteine Tripsina Riconosce e taglia le proteine quando sono presenti ammino acidi basici Arginina Lisina
58 Digestione delle proteine Arginina Lisina
59 Digestione delle proteine Arginina Lisina
60 Digestione delle proteine
61 Digestione delle proteine
62 Digestione delle proteine Una digestione triptica delle proteine fornisce frammenti più piccoli che possono essere analizzati mediante spettrometria di massa
63 Spettrometria di massa Metodica con la quale è possibile pesare una molecola dopo che essa è stata ionizzata, ovvero dopo che ad essa è stata impartita una carica elettrica. Analisi delle proteine
64 Voyager Spec #1[BP = , 24303] E Mass (m/z) 0 0 % Intensity DE GEL G5 SEQUENZE NUCLEOTIDICHE DA BANCA DATI gatctgaaat gttcgtcgat gggttcgtac aagggcctgt ESCISSIONE SPOT DIGESTIONE TRIPTICA SEQUENZE PROTEICHE DA BANCA DATI PEPTIDI PROTEOLITICI TEORICI RATETGMKAT MARIANNAPI GGAPADMCTA ADMRDGGFAD Voyager Spec #1[BP = , 24303] E Mass (m/z) 0 0 % Intensity Peptide mass fingerprint
Genomica e Proteomica
 Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
FOCALIZZAZIONE ISOELETTRICA (IEF)
 FOCALIZZAZIONE ISOELETTRICA (IEF) ELETTROFORESI DI PROTEINE CRITERI DI SEPARAZIONE PAGE nativa densità di carica (pi), dimensioni, forma PAGE-SDS solo dimensioni IEF solo in base al punto isoelettrico
FOCALIZZAZIONE ISOELETTRICA (IEF) ELETTROFORESI DI PROTEINE CRITERI DI SEPARAZIONE PAGE nativa densità di carica (pi), dimensioni, forma PAGE-SDS solo dimensioni IEF solo in base al punto isoelettrico
ELETTROFORESI DI PROTEINE
 ELETTROFORESI DI PROTEINE ELETTROFORESI DI PROTEINE Molto più complessa della separazione elettroforetica di DNA. forma delle proteine fortissime variazioni cariche delle proteine La > parte dei campioni
ELETTROFORESI DI PROTEINE ELETTROFORESI DI PROTEINE Molto più complessa della separazione elettroforetica di DNA. forma delle proteine fortissime variazioni cariche delle proteine La > parte dei campioni
5- Estrazione ed analisi di DNA
 5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
3. ELETTROFORESI DI PROTEINE
 3. ELETTROFORESI DI PROTEINE Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU-16 ore) Marco Scocchi ( BIO/10-11) ELETTROFORESI PRINCIPI GENERALI Migrazione di particelle
3. ELETTROFORESI DI PROTEINE Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU-16 ore) Marco Scocchi ( BIO/10-11) ELETTROFORESI PRINCIPI GENERALI Migrazione di particelle
Permette l identificazione di specifiche proteine antigeniche in una soluzione complessa
 WESTERN BLOTTING Permette l identificazione di specifiche proteine antigeniche in una soluzione complessa Tecnica di trasferimento delle proteine da un gel ad una membrana associata ad utilizzo di anticorpi
WESTERN BLOTTING Permette l identificazione di specifiche proteine antigeniche in una soluzione complessa Tecnica di trasferimento delle proteine da un gel ad una membrana associata ad utilizzo di anticorpi
Corso di insegnamento di Biochimica e Biotecnologie degli Alimenti. Tecniche elettroforetiche. Lezione n. XXIV-04.06.14
 Corso di insegnamento di Biochimica e Biotecnologie degli Alimenti Tecniche elettroforetiche Lezione n. XXIV-04.06.14 L ELETTROFORESI E la separazione di molecole cariche in soluzione Principio Si basa
Corso di insegnamento di Biochimica e Biotecnologie degli Alimenti Tecniche elettroforetiche Lezione n. XXIV-04.06.14 L ELETTROFORESI E la separazione di molecole cariche in soluzione Principio Si basa
Modulo 3. Lavorare con le proteine
 Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 13 Cromatografia ed elettroforesi Concetti chiave: Il comportamento cromatografico di una proteina è influenzato da alcune
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 13 Cromatografia ed elettroforesi Concetti chiave: Il comportamento cromatografico di una proteina è influenzato da alcune
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
v = velocità di migrazione della proteina in un campo elettrico E = forza del campo elettrico z = carica netta della proteina 3500 V catod o
 La prima e : Isoelectric focusing (IEF) v=e z f 1 step1 v = velocità di migrazione della proteina in un campo elettrico E = forza del campo elettrico z = carica netta della proteina Tot 76 kvh f = coefficiente
La prima e : Isoelectric focusing (IEF) v=e z f 1 step1 v = velocità di migrazione della proteina in un campo elettrico E = forza del campo elettrico z = carica netta della proteina Tot 76 kvh f = coefficiente
cromatografia Elettroforesi
 Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
ELETTROFORESI DI PROTEINE
 ELETTROFORESI DI PROTEINE Molto più complessa della separazione elettroforetica di DNA. forma delle proteine fortissime variazioni cariche delle proteine La > parte dei campioni di PROTEINE è più piccola
ELETTROFORESI DI PROTEINE Molto più complessa della separazione elettroforetica di DNA. forma delle proteine fortissime variazioni cariche delle proteine La > parte dei campioni di PROTEINE è più piccola
TECNICHE ELETTROFORETICHE
 TECNICHE ELETTROFORETICHE L elettroforesi e un metodo di separazione che si basa sulla diversa mobilita degli ioni (o di sostanze elettricamente cariche), quando posti all interno di un campo elettrico
TECNICHE ELETTROFORETICHE L elettroforesi e un metodo di separazione che si basa sulla diversa mobilita degli ioni (o di sostanze elettricamente cariche), quando posti all interno di un campo elettrico
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE
 CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
Elettroforesi di Tamara Benincasa
 Elettroforesi di Tamara Benincasa L elettroforesi è una metodologia utilizzata in laboratorio attraverso la quale molecole biologiche (ammino acidi, peptidi, proteine, nucleotidi ed acidi nucleici), dotate
Elettroforesi di Tamara Benincasa L elettroforesi è una metodologia utilizzata in laboratorio attraverso la quale molecole biologiche (ammino acidi, peptidi, proteine, nucleotidi ed acidi nucleici), dotate
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI
 METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI SEPARAZIONE IN PROTEOMICA
 METODI DI SEPARAZIONE IN PROTEOMICA ELETTROFORESI DI PROTEINE INTATTE MONODIMENSIONALE BIDIMENSIONALE CROMATOGRAFIA MONODIMENSIONALE DI PROTEINE INTATTE GEL FILTRAZIONE AFFINITA CROMATOGRAFIA MONO o BIDIMENSIONALE
METODI DI SEPARAZIONE IN PROTEOMICA ELETTROFORESI DI PROTEINE INTATTE MONODIMENSIONALE BIDIMENSIONALE CROMATOGRAFIA MONODIMENSIONALE DI PROTEINE INTATTE GEL FILTRAZIONE AFFINITA CROMATOGRAFIA MONO o BIDIMENSIONALE
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
PURIFICAZIONE DELLE PROTEINE
 PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
Elettroforesi proteine ed acidi nucleici
 Elettroforesi proteine ed acidi nucleici Flavia Frabetti Tecnici di laboratorio 2010/2011 ELETTORFORESI metodo fisico di separazione che sfrutta la mobilità elettroforetica di molecole cariche, sottoposte
Elettroforesi proteine ed acidi nucleici Flavia Frabetti Tecnici di laboratorio 2010/2011 ELETTORFORESI metodo fisico di separazione che sfrutta la mobilità elettroforetica di molecole cariche, sottoposte
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
V R V t. Proteine ad alto peso molecolare. Proteine a peso molecolare intermedio. Proteine a basso peso molecolare. Kd + piccolo.
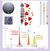 V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
L elettroforesi è una tecnica che consiste nella migrazione differenziata in un campo elettrico, di molecole elettricamente cariche.
 L elettroforesi è una tecnica che consiste nella migrazione differenziata in un campo elettrico, di molecole elettricamente cariche. L elettroforesi è una tecnica che viene usata per separare molecole
L elettroforesi è una tecnica che consiste nella migrazione differenziata in un campo elettrico, di molecole elettricamente cariche. L elettroforesi è una tecnica che viene usata per separare molecole
Apparato elettroforesi
 Elettroforesi Tecniche che permettono di separare diverse macromolecole cariche tramite l applicazione di un campo elettrico. Apparato elettroforesi Fonte: Internet Utilizzata in biochimica e biologia
Elettroforesi Tecniche che permettono di separare diverse macromolecole cariche tramite l applicazione di un campo elettrico. Apparato elettroforesi Fonte: Internet Utilizzata in biochimica e biologia
Analisi di proteine:
 Analisi di proteine: Elettroforesi e Western Blot Seminario Metodologico per il Corso di Didattica Libera Marilena Dinardo [email protected] Le proteine sono il prodotto dei geni: sono le
Analisi di proteine: Elettroforesi e Western Blot Seminario Metodologico per il Corso di Didattica Libera Marilena Dinardo [email protected] Le proteine sono il prodotto dei geni: sono le
WESTERN BLOT o IMMUNOFISSAZIONE
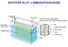 WESTERN BLOT o IMMUNOFISSAZIONE BLOTTING Trasferimento di macromolecole su una membrana immobilizzante. Southern DNA - da Edward Southern 1970 Northern Western RNA Proteine SCOPO DEL WESTERN BLOTTING Consente
WESTERN BLOT o IMMUNOFISSAZIONE BLOTTING Trasferimento di macromolecole su una membrana immobilizzante. Southern DNA - da Edward Southern 1970 Northern Western RNA Proteine SCOPO DEL WESTERN BLOTTING Consente
MATERIALE DIDATTICO. A supporto sono rese disponibili le slides delle lezioni
 MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
GENERALITA SULLA CROMATOGRAFIA
 GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
METODICHE DI IMMUNOCHIMICA
 METODICHE DI IMMUNOCHIMICA IMMUNOCHIMICA permette la determinazione quantitativa di proteine in tessuti e omogenati INTERAZIONI ANTIGENE-ANTICORPO L immunochimica si basa sulle interazioni antigene-anticorpo
METODICHE DI IMMUNOCHIMICA IMMUNOCHIMICA permette la determinazione quantitativa di proteine in tessuti e omogenati INTERAZIONI ANTIGENE-ANTICORPO L immunochimica si basa sulle interazioni antigene-anticorpo
Estrazione di proteine - Scelta della fonte biologica
 Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
2. Tecniche immunochimiche: Western blotting; ELISA; sandwich ELISA 3. Tecniche spettroscopiche: spettrofotometria UV/vis; spettrofluorimetria
 1. Tecniche elettroforetiche: SDS-PAGE 2. Tecniche immunochimiche: Western blotting; ELISA; sandwich ELISA 3. Tecniche spettroscopiche: spettrofotometria UV/vis; spettrofluorimetria Testo consigliato Keith
1. Tecniche elettroforetiche: SDS-PAGE 2. Tecniche immunochimiche: Western blotting; ELISA; sandwich ELISA 3. Tecniche spettroscopiche: spettrofotometria UV/vis; spettrofluorimetria Testo consigliato Keith
La struttura covalente delle proteine (la sequenza amminoacidica)
 La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
Tecniche elettroforetiche:
 Tecniche elettroforetiche: Gel di agarosio, Nativa, SDS-PAGE, Isoelettrofocalizzazione, 2D-PAGE L elettroforesi è una tecnica che consiste nella migrazione differenziata in un campo elettrico, di molecole
Tecniche elettroforetiche: Gel di agarosio, Nativa, SDS-PAGE, Isoelettrofocalizzazione, 2D-PAGE L elettroforesi è una tecnica che consiste nella migrazione differenziata in un campo elettrico, di molecole
COS E LA PROTEOMICA? The total PROTEIN complement of a GENOME Proteoma proteine codificate modificazioni post-traduzionali
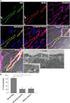 COS E LA PROTEOMICA? The total PROTEIN complement of a GENOME (M. Wilkins et al. Electrophoresis 1995,16 1090-95) La Proteomica è lo studio del PROTEOMA Ud'A [Biochimica Applicata 1] dia n. 1 Proteoma
COS E LA PROTEOMICA? The total PROTEIN complement of a GENOME (M. Wilkins et al. Electrophoresis 1995,16 1090-95) La Proteomica è lo studio del PROTEOMA Ud'A [Biochimica Applicata 1] dia n. 1 Proteoma
Perche usare Gel di Poliacrilammide per separare le proteine?
 Perche usare Gel di Poliacrilammide per separare le proteine? I gel di poliacrilammide hanno una trama piu compatta I pori hanno dimensioni minori che nei gel di agarosio Le proteine sono molto piu piccole
Perche usare Gel di Poliacrilammide per separare le proteine? I gel di poliacrilammide hanno una trama piu compatta I pori hanno dimensioni minori che nei gel di agarosio Le proteine sono molto piu piccole
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Polymerase chain reaction - PCR. Biotecnologie applicate all ispezione degli alimenti di origine animale
 Prof.ssa Tiziana Pepe Polymerase chain reaction - PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali [email protected] Metodologia
Prof.ssa Tiziana Pepe Polymerase chain reaction - PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali [email protected] Metodologia
Elettroforesi - ++ In assenza di moti diffusivi/convettivi gli analiti neutri non possono spostarsi nel mezzo.
 Elettroforesi Con il termine elettroforesi si indica una famiglia di tecniche in cui la separazione di analiti viene effettuata sfruttandone la diversa migrazione sotto l azione di un campo elettrico:
Elettroforesi Con il termine elettroforesi si indica una famiglia di tecniche in cui la separazione di analiti viene effettuata sfruttandone la diversa migrazione sotto l azione di un campo elettrico:
Elettroforesi - ++ In assenza di moti diffusivi/convettivi gli analiti neutri non possono spostarsi nel mezzo.
 Elettroforesi Con il termine elettroforesi si indica una famiglia di tecniche in cui la separazione di analiti viene effettuata sfruttandone la diversa migrazione sotto l azione di un campo elettrico:
Elettroforesi Con il termine elettroforesi si indica una famiglia di tecniche in cui la separazione di analiti viene effettuata sfruttandone la diversa migrazione sotto l azione di un campo elettrico:
ELETTROFORESI. Tecnica analitica che consente di separare molecole cariche grazie all applicazione di un campo elettrico.
 ELETTROFORESI ELETTROFORESI Tecnica analitica che consente di separare molecole cariche grazie all applicazione di un campo elettrico. Anioni ANODO (+) Cationi CATODO (-) v = velocità di migrazione μ =
ELETTROFORESI ELETTROFORESI Tecnica analitica che consente di separare molecole cariche grazie all applicazione di un campo elettrico. Anioni ANODO (+) Cationi CATODO (-) v = velocità di migrazione μ =
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE Cromatografia è il termine generico che indica una serie di tecniche di separazione di molecole simili in base alle loro proprietà chimiche e fisiche. Questo metodo di separazione
TECNICHE CROMATOGRAFICHE Cromatografia è il termine generico che indica una serie di tecniche di separazione di molecole simili in base alle loro proprietà chimiche e fisiche. Questo metodo di separazione
SDS-PAGE/Western blot
 SDS-PAGE/Western blot preparare 2 gels: 7.5% di acrilamide, SPACERS 1.5 mm. Uno verrà utilizzato per il trasferimento su nitrocellulosa, l altro colorato con il blu di coomassie. caricare i campioni dell
SDS-PAGE/Western blot preparare 2 gels: 7.5% di acrilamide, SPACERS 1.5 mm. Uno verrà utilizzato per il trasferimento su nitrocellulosa, l altro colorato con il blu di coomassie. caricare i campioni dell
LUMINESCENZA. semiconduttore
 LUMINESCENZA LUMINESCENZA Elettroluminescenza Radioluminescenza Chemiluminescenza Bioluminescenza Termoluminescenza Triboluminescenza Sonoluminescenza Fotoluminescenza corrente elettrica in gas ionizzato
LUMINESCENZA LUMINESCENZA Elettroluminescenza Radioluminescenza Chemiluminescenza Bioluminescenza Termoluminescenza Triboluminescenza Sonoluminescenza Fotoluminescenza corrente elettrica in gas ionizzato
Spettrometria di massa (principi fondamentali)
 Spettrometria di massa (principi fondamentali) Rilevamento con spettrometria di massa (MS) Una tecnica più raffinata del PID è la spettrometria di massa che prevede l analisi in massa di ioni formati (con
Spettrometria di massa (principi fondamentali) Rilevamento con spettrometria di massa (MS) Una tecnica più raffinata del PID è la spettrometria di massa che prevede l analisi in massa di ioni formati (con
Tecniche elettroforetiche:
 Tecniche elettroforetiche: Gel di agarosio, Nativa, SDS-PAGE, Isoelettrofocalizzazione, 2D-PAGE L elettroforesi è una tecnica che consiste nella migrazione differenziata in un campo elettrico, di molecole
Tecniche elettroforetiche: Gel di agarosio, Nativa, SDS-PAGE, Isoelettrofocalizzazione, 2D-PAGE L elettroforesi è una tecnica che consiste nella migrazione differenziata in un campo elettrico, di molecole
determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D Spettrofotometro cuvetta monocromatore rivelatore
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D Spettrofotometro cuvetta monocromatore rivelatore
SCOPO DEL WESTERN BLOTTING
 WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING Tecnica che consente di visualizzare/individuare UNA proteina tra milioni, grazie all utilizzo di anticorpi
WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING Tecnica che consente di visualizzare/individuare UNA proteina tra milioni, grazie all utilizzo di anticorpi
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE
 EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
Metodologie citogenetiche. Metodologie molecolari. Formulare la domanda Utilizzare la metodica appropriata
 In base al potere di risoluzione della tecnica Metodologie citogenetiche Metodologie molecolari Formulare la domanda Utilizzare la metodica appropriata 1 DNA RNA PROTEINE DNA Cromosomi (cariotipo, FISH,
In base al potere di risoluzione della tecnica Metodologie citogenetiche Metodologie molecolari Formulare la domanda Utilizzare la metodica appropriata 1 DNA RNA PROTEINE DNA Cromosomi (cariotipo, FISH,
Cosa determina l assorbanza di un cromoforo?
 Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
MODULO: TECNICHE DI ANALISI Matrix Assisted Laser Desorption Ionisation MALDI. C. Daniel
 MODULO: TECNICHE DI ANALISI Matrix Assisted Laser Desorption Ionisation MALDI C. Daniel La spettrometria di massaèampiamente usata per l analisi delle biomolecole (proteine, polisaccaridi) ma èsempre stata
MODULO: TECNICHE DI ANALISI Matrix Assisted Laser Desorption Ionisation MALDI C. Daniel La spettrometria di massaèampiamente usata per l analisi delle biomolecole (proteine, polisaccaridi) ma èsempre stata
ESTRAZIONE PURIFICAZIONE. Modificazione chimica ANALISI STRUMENTALE
 Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Southern blot. !Per. determinare la presenza o assenza di specifici frammenti genici. !Studio. della struttura e dell organizzazione di un gene
 Southern blot!per determinare la presenza o assenza di di specifici frammenti genici!studio della struttura e dell organizzazione di di un gene Southern blot Procedura Isolare DNA genomico Digerirlo con
Southern blot!per determinare la presenza o assenza di di specifici frammenti genici!studio della struttura e dell organizzazione di di un gene Southern blot Procedura Isolare DNA genomico Digerirlo con
