EVEROLIMUS - AFINITOR
|
|
|
- Mario Conti
- 10 anni fa
- Просмотров:
Транскрипт
1 giunta regionale Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 1/10 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED EVEROLIMUS - AFINITOR Indicazione in esame: Everolimus (Afinitor ) è indicato per il trattamento del carcinoma mammario avanzato con stato recettoriale ormonale positivo, HER2/neu negativo, in combinazione con exemestane, in donne in postmenopausa in assenza di malattia viscerale sintomatica dopo recidiva o progressione a seguito di trattamento con un inibitore dell aromatasi non steroideo. A cura del Gruppo Farmaci Innovativi del Coordinamento della Rete Oncologica Veneta Raccomandazione n. 4 data di redazione: gennaio 2015 Documento approvato nella seduta del 29 gennaio 2015 della Commissione Tecnica Regionale Farmaci, ex DGR n. 952/2013
2 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 2/10 Gruppo Farmaci Innovativi del Coordinamento della Rete Oncologica Veneta Membri (votanti) CONTE PierFranco, Direttore UOC Oncologia Medica 2 - IOV Padova (Coordinatore) BASSAN Franco, Direttore UOC Oncologia Medica - Azienda ULSS 4 Alto Vicentino DEL GIUDICE Augusta, Associazione Noi e il cancro Volontà di Vivere ONLUS - Padova FERRARESE Annalisa, Direttore SOC Farmacia ospedaliera - Azienda ULSS 18 Rovigo GASPARETTO Teresa, Responsabile Ricerca Innovazione e Health Technology Assessment (HTA) - Regione Veneto GORI Stefania, Direttore UOC Oncologia - Ospedale Sacro Cuore Don Calabria, Negrar (VR) LEONE Roberto, Professore Associato di Farmacologia - Università degli Studi di Verona MORANDI Paolo, UOC Oncologia Medica - Azienda ULSS 12 Veneziana Ospedale Dell Angelo, Mestre PERTILE Paolo, Ricercatore Dipartimento di Scienze Economiche - Università degli Studi di Verona SAUGO Mario, Servizio Epidemiologico Regionale - Regione Veneto SCANNAPIECO Gianluigi, Direttore Sanitario - Azienda Ospedaliera Padova SCROCCARO Giovanna, Dirigente Settore Farmaceutico-Protesica-Dispositivi Medici - Regione Veneto TORTORA Giampaolo, Direttore Oncologia Medica A du - Azienda Ospedaliera Universitaria Integrata Verona TOTTOLO Paolo, Medico di Medicina Generale - Azienda ULSS 9 Treviso ZAGONEL Vittorina, Direttore UOC Oncologia Medica 1 - IOV Padova Segreteria Scientifica ADAMI Silvia Coordinamento Regionale Unico sul Farmaco (CRUF) Regione Veneto BORTOLAMI Alberto Coordinamento Tecnico-Scientifico Rete Oncologica Veneta CONTE PierFranco Coordinatore Tecnico-Scientifico Rete Oncologica Veneta SCROCCARO Giovanna Dirigente Settore Farmaceutico Protesica Dispositivi Medici - Regione Veneto Coordinamento Organizzativo Rete Oncologica Veneta MARCHESE Fortunata Settore Farmaceutico Protesica Dispositivi Medici RONI Chiara Farmacista Il presente documento è stato realizzato dal Gruppo Farmaci Innovativi del Coordinamento della Rete Oncologica Veneta con il supporto metodologico del Coordinamento Regionale Unico sul Farmaco ed è stato approvato dalla Commissione Tecnica Regionale Farmaci. Riferimenti Coordinamento Rete Oncologica Veneta Coordinamento Regionale Unico sul Farmaco [email protected]
3 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 3/10 SCHEDA DEL FARMACO NOME COMMERCIALE Principio Attivo Ditta Produttrice ATC Formulazione Dosaggio Categoria Terapeutica Inibitori della proteina chinasi AFINITOR Everolimus Novartis Farma spa L01XE10 Compresse 5-10 mg Indicazione in Esame Afinitor è indicato per il trattamento del carcinoma mammario avanzato con stato recettoriale ormonale positivo, HER2/neu negativo, in combinazione con exemestane, in donne in postmenopausa in assenza di malattia viscerale sintomatica dopo recidiva o progressione a seguito di trattamento con un inibitore dell aromatasi non steroideo. Classificazione ai fini della rimborsabilità Classe di rimborsabilità: H. Ai fini delle prescrizioni a carico del SSN i centri utilizzatori dovranno compilare la scheda raccolta dati informatizzata di arruolamento che indica i pazienti eleggibili e la scheda di follow-up e applicare le condizioni negoziali secondo le indicazioni pubblicate sul sito dell'agenzia, piattaforma web - all'indirizzo Classificazione ai fini della fornitura Medicinale soggetto a prescrizione medica limitativa, da rinnovare volta per volta, vendibile al pubblico su prescrizione di centri ospedalieri o di specialisti - Oncologo, internista (RNRL). Ulteriori condizioni negoziali Ulteriori condizioni negoziali Payment-by-result, con rimborso per le pazienti Prezzo SSR* 30 cpr da 5 mg = 2.144,34 30 cpr da 10 mg = 3.049,73 Registro AIFA SI. Il paziente è eleggibile se: diagnosi di carcinoma mammario, con stadio della malattia localmente avanzato non candidabile a trattamento locoregionale con intento curativo o metastatico; status dei recettori ormonali (ER, PgR) positivo; status Her2/neu, valutato tramite analisi immunoistochimica e FISH, essere negativo; donne in menopausa, in assenza di metastasi viscerali sintomatiche e con funzionalità epatica normale (se compromessa, non oltre il grado Child Pugh B Il medicinale può essere usato in prima linea, in terapia metastatica, in pazienti con recidiva durante o dopo trattamento adiuvante con inibitore dell aromatasi non steroideo. Il medicinale può essere usato fino alla quarta linea, in terapia metastatica, in pazienti con progressione durante o dopo un precedente trattamento con un inibitore dell aromatasi non steroideo. *Prezzo SSN al netto degli sconti negoziali e dell IVA 10%;
4 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 4/10 SINTESI DELLE RACCOMANDAZIONI Quesito clinico N. 1 Nelle pazienti in postmenopausa con carcinoma mammario HR+/HER2- in assenza di malattia viscerale sintomatica, è indicato il trattamento di 1 linea con Exemestane + Everolimus se la recidiva di malattia si verifica durante o entro 1 anno dal termine del trattamento adiuvante includente un antiaromatasico non steroideo? Raccomandazione RACCOMANDATO IN CASI SELEZIONATI Raccomandazione formulata sulla base di: rapporto benefici/rischi: incerto evidenze considerate di qualità: bassa alternative terapeutiche: disponibili costo rispetto alle alternative: superiore alla maggior parte delle alternative; inferiore a chemio+bevacizumab Utilizzo atteso: sulla base della raccomandazione formulata, si prevede un tasso di utilizzo compreso tra il 10% e il 30% dei pazienti candidabili alla terapia. Votazione del Gruppo di Lavoro (13 votanti presenti): 13 Raccomandato in casi selezionati. Commento: La qualità delle evidenze è stata ritenuta di grado basso in quanto questa tipologia di pazienti costituiva una minoranza della popolazione arruolata (<20%) e il comparator utilizzato (exemestane) non era il più appropriato. Non sono disponibili studi di confronto diretto verso fulvestrant. Per questi pazienti, nella pratica clinica esistono alternative soddisfacenti, di minore costo (con l eccezione di paclitaxel+bevacizumab) e maggiore tollerabilità (fulvestrant, capecitabina, paclitaxel, paclitaxel+ bevacizumab). Quesito clinico N. 2 Nelle pazienti in post menopausa con carcinoma mammario HR+/HER2- in assenza di malattia viscerale sintomatica, è indicato il trattamento di 1 linea con Exemestane + Everolimus se la recidiva di malattia si verifica dopo 1 anno dal termine di un trattamento adiuvante comprendente un antiaromatasico non steroideo? Raccomandazione RACCOMANDATO IN CASI SELEZIONATI Raccomandazione formulata sulla base di: rapporto benefici/rischi: incerto evidenze considerate di qualità: bassa alternative terapeutiche: disponibili costo rispetto alle alternative: superiore Utilizzo atteso: sulla base della raccomandazione formulata, si prevede un tasso di utilizzo compreso tra il 10% e il 30% dei pazienti candidabili alla terapia. Votazione del Gruppo di Lavoro (13 votanti presenti): 13 Raccomandato in casi selezionati. Commento: La qualità delle evidenze è stata ritenuta di grado basso in quanto questa tipologia di pazienti costituiva una minoranza della popolazione arruolata e il comparator utilizzato (exemestane) non era il più appropriato. Anche per questa tipologia di pazienti, nella pratica clinica esistono alternative soddisfacenti, di minore costo (con l eccezione di paclitaxel+bevacizumab) e maggiore tollerabilità (fulvestrant, capecitabina, paclitaxel, paclitaxel + bevacizumab).
5 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 5/10 Quesito clinico N. 3 Nelle pazienti in post menopausa con carcinoma mammario HR+/HER2- metastatico in assenza di malattia viscerale sintomatica e pretrattate con un antiaromatasico non steroideo, è indicato il trattamento con Exemestane in combinazione con Everolimus in seconda linea? Raccomandazione MODERATAMENTE RACCOMANDATO Raccomandazione formulata sulla base di: rapporto benefici/rischi: incerto evidenze considerate di qualità: moderata alternative terapeutiche: disponibili ma meno soddisfacenti costo rispetto alle alternative: superiore Utilizzo atteso: sulla base della raccomandazione formulata, si prevede un tasso di utilizzo compreso tra il 30% e il 60% dei pazienti candidabili alla terapia. Votazione del Gruppo di Lavoro (13 votanti presenti): 13 Moderatamente raccomandato. Commento: La qualità delle evidenze è stata ritenuta di grado moderato in quanto il comparator utilizzato non è stato considerato come il più appropriato. Per questa tipologia di pazienti, le alternative disponibili (fulvestrant, capecitabina, paclitaxel, paclitaxel+bevacizumab) sono meno soddisfacenti, in quanto per questa linea di trattamento il beneficio è minore a fronte di una maggiore tossicità. Quesito clinico N. 4 Nelle pazienti in post menopausa con carcinoma mammario HR+/HER2- metastatico in assenza di malattia viscerale sintomatica e pretrattate con un antiaromatasico non steroideo, è indicato il trattamento con Exemestane in combinazione con Everolimus in III e IV linea? Raccomandazione MODERATAMENTE RACCOMANDATO Raccomandazione formulata sulla base di: rapporto benefici/rischi: incerto evidenze considerate di qualità: moderata alternative terapeutiche: disponibili ma meno soddisfacenti costo rispetto alle alternative: superiore Utilizzo atteso: sulla base della raccomandazione formulata, si prevede un tasso di utilizzo compreso tra il 30% e il 60% dei pazienti candidabili alla terapia. Votazione del Gruppo di Lavoro (13 votanti presenti): 13 Moderatamente raccomandato. Commento: La qualità delle evidenze è stata ritenuta di grado moderato in quanto il comparator utilizzato non è stato considerato come il più appropriato. Per questa tipologia di pazienti, maggiormente rappresentata nello studio registrativo, le alternative disponibili (fulvestrant, capecitabina, paclitaxel,paclitaxel+bevacizumab) sono meno soddisfacenti, in quanto per questa linea di trattamento il beneficio è minore a fronte di una maggiore tossicità.
6 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 6/10 SINTESI DELLE EVIDENZE DISPONIBILI, QUALITA METODOLOGICA DEGLI STUDI E COSTI Everolimus è un inibitore selettivo del mtor e viene somministrato per via orale al dosaggio di 10 mg/die. L approvazione di everolimus si è basata sui risultati di un unico studio sponsorizzato, BOLERO-2, un RCT internazionale di fase III, in doppio cieco e multicentrico, il cui obiettivo era dimostrare la superiorità di everolimus in combinazione con exemestane verso il solo exemestane, in donne in postmenopausa affette da cancro avanzato della mammella ER positivo e refrattario a precedenti trattamenti con letrozolo o anastrozolo. Le pazienti incluse nello studio dovevano avere almeno una lesione evidente oppure lesioni ossee principalmente litiche, un ECOG performance status da 0 a 2, un adeguata funzionalità d organo e valori ematologici adeguati. Le pazienti che avevano assunto in precedenza altri trattamenti endocrini antitumorali e un singolo ciclo di chemioterapia per la fase avanzata della patologia sono state, comunque, incluse nello studio. I precedenti trattamenti includevano letrozolo o anastrozolo (100%), tamoxifene (48%), fulvestrant (16%) e chemioterapia (68%), con una mediana di tre precedenti linee di terapia. In questo studio, 724 pazienti sono state randomizzate (in rapporto 2:1) a ricevere everolimus per via orale (10 mg/die) o placebo, entrambi in associazione con exemestane per via orale 25 mg/die. L end-point primario dello studio era la PFS, valutata secondo i criteri RECIST e basata sulla valutazione dello sperimentatore. Le analisi di supporto per la PFS sono state basate sulla revisione radiologica centralizzata indipendente. Gli end-point secondari comprendevano la OS, il tasso di risposta obiettiva, il tasso di beneficio clinico, il tempo al peggioramento dell ECOG Performance Status, la sicurezza e la qualità di vita. Sia nell analisi ad interim che nella analisi finale, la superiorità dell associazione everolimus+exemestane rispetto al controllo in relazione all endpoint primario di efficacia è stata dimostrata. In particolare, nell analisi finale, l associazione di everolimus con exemestane ha dimostrato di migliorare la sopravvivenza libera da progressione con una PFS mediana di 7.8 mesi contro 3.2 mesi del gruppo con il solo exemestane (HR = 0.45, p<0.0001) secondo la valutazione dello sperimentatore e di 11,0 mesi vs 4,1 mesi (HR = 0.38, p<0,0001) secondo la valutazione della commissione indipendente. Sono stati recentemente presentati a un congresso europeo i risultati finali dello studio BOLERO-2, dai quali non si evincono differenze staticamente significative in termini di OS fra i due bracci di trattamento (everolimus+exemestane: 31 mesi vs controllo 26 mesi; HR: 0,89 p= ns). Il Panel ritiene che il guadagno di sopravvivenza globale riscontrato sia comunque rilevante dal punto di vista clinico. Il profilo di tollerabilità è sfavorevole: la terapia con everolimus più exemestane è stata associata a una maggiore incidenza di eventi avversi rispetto al solo exemestane. Gli eventi avversi più comuni, di grado 3/4, sono stati: stomatiti (8% nel gruppo con everolimus più exemestane vs. 1% nel gruppo con il solo exemestane), anemia (6% vs. <1%), dispnea (6% vs. <1%), iperglicemia (4% vs. <1%), stanchezza (4% vs. <1%) e polmonite (3% vs. 0%). Per quanto riguarda la qualità della vita, un recente studio ha mostrato un tempo al deterioramento della qualità della vita globale maggiore nel braccio everolimus+exemestane rispetto al controllo (rispettivamente 8,3 mesi vs 5,8 mesi, p=0.0084). La qualità delle evidenze è stata ritenuta complessivamente di grado moderato in quanto, come evidenziato anche da EMA, non ci sono studi di confronto diretto verso le migliori alternative disponibili (es. fulvestrant). Inoltre, nel braccio di controllo è stato registrato un tasso di risposta obiettiva del 0.4% che rappresenta una percentuale di molto inferiore rispetto a quella attesa (15%). C è quindi la possibilità che i pazienti del braccio di controllo abbiano ricevuto un trattamento sub-ottimale. Il costo della terapia con everolimus in associazione a exemestane varia a seconda della linea di trattamento, a causa della diversa durata della terapia. Il farmaco, considerando gli accordi negoziali, ha un costo stimabile tra e a paziente, che risulta essere superiore alle alternative disponibili (chemioterapie e fulvestrant) come evidenziato dalle Tabelle 1-4.
7 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 7/10 Tabella 1. Prima linea terapeutica in pazienti con recidiva entro un anno Farmaco Schedula somm. ciclo ciclo* Durata Everolimus + Exemestane EVE:10 mg/die + EXE: 25 mg/die Somm lordo accordi netto accordi mesi Fulvestrant 1 mese: 500 mg+500 mg 1,14 die ogni 28 die; Succ: 500 mg 1,14 die ogni 28 die Capecitabina mg/m2 BID 1-14 giorni ogni 21# 0 1 mese: 936 Successivi: mesi mesi Paclitaxel 90 mg/m2 giorni 1,8,15 ogni 28# mesi Bevacizumab + Paclitaxel BEVA: 10 mg/kg 1,15 ogni 28 + PAC: 90 mg/m2 giorni 1,8,15 ogni 28# mesi ** ** * comprensivo IVA 10% e di spreco di prodotto. Per il costo ciclo si sono considerati 28 giorni di terapia. ciclo al lordo di accordi negoziali. complessivo incluso dei costi di somministrazione #Superficie corporea 1,7m 2. Peso corporeo 65 kg.**bevacizumab ha lo stesso costo data la tipologia dell accordo indipendente dalla risposta clinica). Tabella 2. prima linea terapeutica in pazienti con recidiva dopo un anno Farmaco Schedula somm. ciclo ciclo* Durata Everolimus + Exemestane EVE:10 mg/die + EXE: 25 mg/die Somm lordo accordi netto accordi mesi Fulvestrant 1 mese: 500 mg+500 mg 1,14 die ogni 28 die; Succ: 500 mg 1,14 die ogni 28 die Capecitabina mg/m2 BID 1-14 giorni ogni 21# 0 1 mese: 936 Successivi: mesi mesi Paclitaxel 90 mg/m2 giorni 1,8,15 ogni 28# mesi * comprensivo IVA 10% e di spreco di prodotto. Per il costo ciclo si sono considerati 28 giorni di terapia. ciclo al lordo di accordi negoziali. complessivo incluso dei costi di somministrazione #Superficie corporea 1,7m 2.
8 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 8/10 Tabella 3. Seconda linea terapeutica Farmaco Schedula somm. ciclo Everolimus + Exemestane EVE:10 mg/die + EXE: 25 mg/die ciclo* Durata Somm lordo accordi netto accordi mesi Fulvestrant 1 mese: 500 mg+500 mg 1,14 die ogni 28 die; Succ: 500 mg 1,14 die ogni 28 die Capecitabina mg/m2 BID 1-14 giorni ogni 21# 0 1 mese: 936 Successivi: mesi mesi Paclitaxel 90 mg/m2 giorni 1,8,15 ogni 28# mesi * comprensivo IVA 10% e di spreco di prodotto. Per il costo ciclo si sono considerati 28 giorni di terapia. ciclo al lordo di accordi negoziali. complessivo incluso dei costi di somministrazione # Superficie corporea 1,7m 2. Tabella 4. Terza-quarta linea terapeutica Farmaco Schedula somm. ciclo Everolimus + Exemestane EVE:10 mg/die + EXE: 25 mg/die ciclo* Durata Somm lordo accordi netto accordi mesi Fulvestrant 1 mese: 500 mg+500 mg 1,14 die ogni 28 die; Succ: 500 mg 1,14 die ogni 28 die Capecitabina mg/m2 BID 1-14 giorni ogni 21# 0 1 mese: 936 Successivi: mesi mesi Paclitaxel 90 mg/m2 giorni 1,8,15 ogni 28# mesi * comprensivo IVA 10% e di spreco di prodotto. Per il costo ciclo si sono considerati 28 giorni di terapia. ciclo al lordo di accordi negoziali. complessivo incluso dei costi di somministrazione # Superficie corporea 1,7m 2.
9 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 9/10 BIBLIOGRAFIA AIOM AIRTUM. I numeri del cancro in Italia 2013 Yardley DA. Combining mtor Inhibitors with Chemotherapy and Other Targeted Therapies in Advanced Breast Cancer: Rationale, Clinical Experience, and Future Directions. Breast Cancer: Basic and Clinical Research 2013: Riassunto delle caratteristiche del prodotto. Afinitor. Linee guida AIOM. Neoplasie della mammella. Edizione 2013 (aggiornamento a luglio 2013). Baselga J. et al.; Everolimus in Postmenopausal Hormone-Receptor-Positive Advanced Breast Cancer. The New England Journal of Medicine 2012; 366: Yardley D. et al.; Everolimus Plus Exemestane in Postmenopausal Patients with HR+ Breast Cancer: BOLERO-2 Final Progression-Free Survival Analysis. Advances in Therapy 2013; 30: Campone M et al. Effect of visceral metastases on the efficacy and safety of everolimus in postmenopausal women with advancedbreast cancer: subgroup analysis from the BOLERO-2 study. Eur J Cancer 2013; 49: Gnant M et al. Effect of everolimus on bone marker levels and progressive disease in bone in BOLERO-2. J Natl Cancer Inst 2013; 105: Pritchard KI et al. Safety and efficacy of everolimus with exemestane vs. exemestane alone in elderly patients with HER2-negative, hormone receptor-positive breast cancer in BOLERO-2. Clin Breast Cancer. 2013; 13(6): Beck JT et al. Everolimus plus exemestane as first-line therapy in HR+, HER2- advanced breast cancer in BOLERO-2. Breast Cancer Res Treat 2014; 143(3): Noguchi S et al. Efficacy of everolimus with exemestane versus exemestane alone in Asian patients with HER2- negative, hormone-receptor-positive breast cancer in BOLERO-2. Breast Cancer Afinitor-H-C-1038-II-20 : EPAR - Assessment Report Variation. Piccart M et al. Everolimus plus exemestane for hormone receptor-positive (HR+), human epidermal growth factor receptor-2-negative (HER2 ) advanced breast cancer (BC): overall survival results from BOLERO-2. Eur J Cancer 2014; 50 (Supplement 3): S1. Abstract 1LB. Bachelot T, et al. Comparative efficacy of everolimus plus exemestane vs fulvestrant for hormone receptor positive advanced breast cancer following progression/recurrence after endocrine therapy: a network meta-analysis. Breast Cancer Res Treat 2014; 143: Rugo HS1, et al. Incidence and time course of everolimus-related adverse events in postmenopausal women with hormone receptor-positive advanced breast cancer: insights from BOLERO-2. Ann Oncol. 2014;25(4): Burris, et al. Health-related quality of life of patients with advanced breast cancer treated with everolimus plus exemestane versus placebo plus exemestane in the phase 3, randomized, controlled, BOLERO-2 trial. Cancer 119: Avis 3 aprile SMC (872/13).
10 Allegato D al Decreto n. 119 del 12 maggio 2015 pag. 10/10 METODOLOGIA I quesiti clinici riferiti alla indicazione oggetto di analisi vengono predisposti dal Gruppo di Lavoro sulla base del contesto clinico di riferimento. Il Gruppo di Lavoro ha deciso di votare, per ciascun quesito clinico, quattro aspetti: 1. Giudizio sulle alternative terapeutiche (da linee guida / da esperienza clinica): sulla base dell analisi del contesto clinico le alternative terapeutiche sono considerate: DISPONIBILI DISPONIBILI MA MENO SODDISFACENTI ASSENTI O DISPONIBILI MA INSODDISFACENTI Le alternative considerate sono le migliori alternative disponibili e possono essere rappresentate sia dal comparator da studio clinico che dalla terapia normalmente utilizzata nella pratica clinica per la medesima indicazione. 2. Giudizio sulla qualità delle evidenze: la qualità delle evidenze è classificata (secondo il metodo GRADE) in quattro categorie: ALTA MODERATA BASSA MOLTO BASSA Partendo dalla qualità teoricamente alta di uno studio randomizzato, la qualità si può abbassare per la presenza di limiti legati a bias nella conduzione e analisi dello studio, scelta del gruppo di controllo, trasferibilità, incoerenza dei risultati/eterogeneità, stime imprecise o dati insufficienti, pubblicazione selettiva dei dati. 3. Giudizio sul bilancio benefici/rischi: dopo aver identificato e classificato gli outcome clinici come importanti ed essenziali, importanti ma non essenziali e non importanti, viene assegnato un giudizio sui risultati di efficacia clinica disponibili che vengono considerati, in funzione dell importanza degli outcome clinici e dell entità dei risultati: MOLTO RILEVANTI (Outcome clinici importanti ed essenziali ed entità del risultato clinicamente rilevante) RILEVANTI (Outcome clinici importanti ma non essenziali ed entità del risultato clinicamente rilevante oppure Outcome clinici importanti ed essenziali ed entità del risultato solo moderatamente rilevante) POCO RILEVANTI (Outcome clinici non importanti benché con entità del risultato clinicamente rilevante) MARGINALI (Qualsiasi Outcome clinico ed entità del risultato clinicamente non rilevante) Viene inoltre espresso un giudizio sulla tollerabilità, considerata: BUONA DISCRETA SCARSA Sulla base del giudizio espresso su efficacia e tollerabilità viene quindi espresso un giudizio complessivo sul bilancio benefici/rischi, considerato: MOLTO FAVOREVOLE FAVOREVOLE INCERTO SFAVOREVOLE 4. Giudizio sul costo rispetto alle alternative: il costo della terapia, calcolato al netto degli eventuali sconti derivanti dagli accordi negoziali e dei meccanismi di condivisione del rischio, viene considerato, rispetto alle alternative (se presenti): INFERIORE SOVRAPPONIBILE SUPERIORE Ogni componente del Gruppo di Lavoro effettua la propria valutazione in merito a ciascun punto sopra descritto e, utilizzando un algoritmo decisionale condiviso, definisce il livello di raccomandazione del quesito in oggetto. In particolare, sono previsti quattro possibili livelli di raccomandazione: RACCOMANDATO (R) utilizzabile nella maggioranza dei pazienti MODERATAMENTE RACCOMANDATO (MR) Si nutrono dei dubbi sul fatto che il farmaco debba essere utilizzato nella maggioranza dei pazienti, ma si ritiene che il suo impiego debba essere tenuto in considerazione RACCOMANDATO IN CASI SELEZIONATI (RS) utilizzabile solo in casi selezionati di pazienti NON RACCOMANDATO (NR) si sconsiglia l utilizzo del farmaco Il livello di raccomandazione viene definito a maggioranza; in caso di pareggio o incertezza, la decisione viene assunta collegialmente. Sulla base della raccomandazione formulata, il Gruppo di Lavoro prevede una percentuale di utilizzo atteso che viene esplicitata per singola raccomandazione. In caso di quesiti su popolazioni non considerate all interno degli studi clinici, il Gruppo di Lavoro sceglie tra le opzioni NR o RS, di volta in volta, valutata anche la presenza o meno di alternative.
MINI SCHEDA HTA EVEROLIMUS (AFINITOR ) INDICAZIONE CARCINOMA MAMMARIO
 1/7 MINI SCHEDA HTA EVEROLIMUS (AFINITOR ) INDICAZIONE CARCINOMA MAMMARIO Nome Commerciale AFINITOR Principio Attivo everolimus Ditta Produttrice Novartis Farma spa ATC L01XE10 Formulazione Compresse Dosaggio
1/7 MINI SCHEDA HTA EVEROLIMUS (AFINITOR ) INDICAZIONE CARCINOMA MAMMARIO Nome Commerciale AFINITOR Principio Attivo everolimus Ditta Produttrice Novartis Farma spa ATC L01XE10 Formulazione Compresse Dosaggio
La valutazione multidisciplinare in sanità dalla teoria alla applicazione pratica: modello di valutazione in oncologia
 Motore Sanità - Summer School Il futuro del SSN tra modelli organizzativi, sostenibilità ed innovazione La valutazione multidisciplinare in sanità dalla teoria alla applicazione pratica: modello di valutazione
Motore Sanità - Summer School Il futuro del SSN tra modelli organizzativi, sostenibilità ed innovazione La valutazione multidisciplinare in sanità dalla teoria alla applicazione pratica: modello di valutazione
Le raccomandazioni regionali all utilizzo dei farmaci ad alto costo
 Le raccomandazioni regionali all utilizzo dei farmaci ad alto costo Verona, 18 settembre, 2015 Pierfranco Conte, Alberto Bortolami Coordinamento Rete Oncologica del Veneto - ROV Compiti della Rete Oncologica
Le raccomandazioni regionali all utilizzo dei farmaci ad alto costo Verona, 18 settembre, 2015 Pierfranco Conte, Alberto Bortolami Coordinamento Rete Oncologica del Veneto - ROV Compiti della Rete Oncologica
PERTUZUMAB - PERJETA
 giunta regionale Allegato C al Decreto n. 119 del 12 maggio 2015 pag. 1/9 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED PERTUZUMAB - PERJETA Indicazione in esame: Pertuzumab (Perjeta
giunta regionale Allegato C al Decreto n. 119 del 12 maggio 2015 pag. 1/9 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED PERTUZUMAB - PERJETA Indicazione in esame: Pertuzumab (Perjeta
Quali strategie per un utilizzo razionale dei farmaci oncologici innovativi? L esperienza della Regione Veneto
 FARMACI ONCOLOGICI INNOVATIVI: SCENARIO ATTUALE E LORO VALUTAZIONE Quali strategie per un utilizzo razionale dei farmaci oncologici innovativi? L esperienza della Regione Veneto Roberto Leone Dipartimento
FARMACI ONCOLOGICI INNOVATIVI: SCENARIO ATTUALE E LORO VALUTAZIONE Quali strategie per un utilizzo razionale dei farmaci oncologici innovativi? L esperienza della Regione Veneto Roberto Leone Dipartimento
SINOSSI DELLO STUDIO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO
 SINOSSI DELLO STUDIO TITOLO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO SPONSOR Sequenza ottimale di ormonoterapia in pazienti con carcinoma mammario metastatico ricadute dopo terapia
SINOSSI DELLO STUDIO TITOLO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO SPONSOR Sequenza ottimale di ormonoterapia in pazienti con carcinoma mammario metastatico ricadute dopo terapia
CABAZITAXEL - JEVTANA
 giunta regionale Allegato F al Decreto n. 139 del 3 giugno 2015 pag. 1/7 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED CABAZITAXEL - JEVTANA Indicazione in esame: in combinazione
giunta regionale Allegato F al Decreto n. 139 del 3 giugno 2015 pag. 1/7 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED CABAZITAXEL - JEVTANA Indicazione in esame: in combinazione
Tavola Rotonda Monitoraggio consumo farmaci, innovazione e PDTA
 Tavola Rotonda Monitoraggio consumo farmaci, innovazione e PDTA PierFranco Conte, Silvia Adami, Alberto Bortolami, Chiara Roni, Giovanna Scroccaro Coordinamento Rete Oncologica del Veneto - ROV Università
Tavola Rotonda Monitoraggio consumo farmaci, innovazione e PDTA PierFranco Conte, Silvia Adami, Alberto Bortolami, Chiara Roni, Giovanna Scroccaro Coordinamento Rete Oncologica del Veneto - ROV Università
A cura del Gruppo Regionale Farmaci Oncologici (GReFO) (pubblicato a maggio 2014) Aggiornata alla pubblicazione della negoziazione AIFA (luglio 2014)
 Raccomandazioni evidence-based Pertuzumab Nel carcinoma mammario avanzato HER2/neu positivo (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 26 Settembre
Raccomandazioni evidence-based Pertuzumab Nel carcinoma mammario avanzato HER2/neu positivo (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 26 Settembre
Everolimus (AFINITOR )
 Raccomandazioni evidence-based Everolimus (AFINITOR ) Nel carcinoma mammario avanzato dopo fallimento di terapia con inibitore dell aromatasi non steroideo A cura del gruppo di lavoro Farmaci Innovativi
Raccomandazioni evidence-based Everolimus (AFINITOR ) Nel carcinoma mammario avanzato dopo fallimento di terapia con inibitore dell aromatasi non steroideo A cura del gruppo di lavoro Farmaci Innovativi
SCHEDA FARMACO. Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Alberto Bortolami Coordinamento Rete Oncologica del Veneto Istituto Oncologico Veneto
 Alberto Bortolami Coordinamento Rete Oncologica del Veneto Istituto Oncologico Veneto Metodologia Farmaci Innovativi Metodologia Percorso Valutativo (dr. Alberto Bortolami-Coordinamento Rete Oncologica)
Alberto Bortolami Coordinamento Rete Oncologica del Veneto Istituto Oncologico Veneto Metodologia Farmaci Innovativi Metodologia Percorso Valutativo (dr. Alberto Bortolami-Coordinamento Rete Oncologica)
CRIZOTINIB - XALKORI
 giunta regionale Allegato A al Decreto n. 253 del 28 agosto 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED CRIZOTINIB - XALKORI Indicazione in esame: é indicato per
giunta regionale Allegato A al Decreto n. 253 del 28 agosto 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED CRIZOTINIB - XALKORI Indicazione in esame: é indicato per
SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Nintedanib (VARGATEF)
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Nintedanib (VARGATEF)
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Nintedanib (VARGATEF)
NSCLC - stadio iiib/iv
 I TUMORI POLMONARI linee guida per la pratica clinica NSCLC - stadio iiib/iv quale trattamento per i pazienti anziani con malattia avanzata? Il carcinoma polmonare è un tumore frequente nell età avanzata.
I TUMORI POLMONARI linee guida per la pratica clinica NSCLC - stadio iiib/iv quale trattamento per i pazienti anziani con malattia avanzata? Il carcinoma polmonare è un tumore frequente nell età avanzata.
MINI SCHEDA HTA CRIZOTINIB (XALKORI )
 1/7 MINI SCHEDA HTA CRIZOTINIB (XALKORI ) Nome Commerciale XALKORI Principio Attivo Crizotinib Ditta Produttrice Pfizer Italia Srl ATC L01XE16 Formulazione Capsule rigide Dosaggio 200 mg 250 mg Altri antineoplastici
1/7 MINI SCHEDA HTA CRIZOTINIB (XALKORI ) Nome Commerciale XALKORI Principio Attivo Crizotinib Ditta Produttrice Pfizer Italia Srl ATC L01XE16 Formulazione Capsule rigide Dosaggio 200 mg 250 mg Altri antineoplastici
NAB PACLITAXEL - ABRAXANE
 giunta regionale Allegato A al Decreto n. 291 del 7 ottobre 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED NAB PACLITAXEL - ABRAXANE Indicazione in esame: in associazione
giunta regionale Allegato A al Decreto n. 291 del 7 ottobre 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED NAB PACLITAXEL - ABRAXANE Indicazione in esame: in associazione
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Specialità: Herceptin (Roche spa) Forma farmaceutica:
 TRASTUZUMAB per l'indicazione: in associazione ad un inibitore dell aromatasi nel trattamento di pazienti in postmenopausa affetti da carcinoma mammario metastatico positivo per i recettori ormonali, non
TRASTUZUMAB per l'indicazione: in associazione ad un inibitore dell aromatasi nel trattamento di pazienti in postmenopausa affetti da carcinoma mammario metastatico positivo per i recettori ormonali, non
Neoplasie della mammella - 2
 Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
Espressione di geni specifici per un determinato tumore
 Espressione di geni specifici per un determinato tumore Paziente A: Non ha il cancro Espressione dei geni: Nessuna Biopsia Geni associati al cancro allo stomaco Paziente B: Ha un tumore allo stomaco Bassa
Espressione di geni specifici per un determinato tumore Paziente A: Non ha il cancro Espressione dei geni: Nessuna Biopsia Geni associati al cancro allo stomaco Paziente B: Ha un tumore allo stomaco Bassa
MINI SCHEDA HTA AXITINIB (INLYTA )
 1/6 MINI SCHEDA HTA AXITINIB (INLYTA ) FARMACO IN ESAME Nome commerciale Inlyta Principio Attivo Axitinib Ditta Produttrice Pfizer Italia srl ATC L01XE17 Formulazione Compresse rivestite Dosaggio 1 mg
1/6 MINI SCHEDA HTA AXITINIB (INLYTA ) FARMACO IN ESAME Nome commerciale Inlyta Principio Attivo Axitinib Ditta Produttrice Pfizer Italia srl ATC L01XE17 Formulazione Compresse rivestite Dosaggio 1 mg
16th World Conference on Lung Cancer (WCLC): highlights
 16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
HTA e farmaci: il ruolo dell AIFA
 HTA e farmaci: il ruolo dell AIFA Simona Montilla 12 luglio 2013 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non impegnano in alcun modo l AIFA
HTA e farmaci: il ruolo dell AIFA Simona Montilla 12 luglio 2013 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non impegnano in alcun modo l AIFA
Panitumumab. Raccomandazioni evidence-based. Carcinoma colon-rettale metastatico (I linea di terapia)
 Raccomandazioni evidence-based Panitumumab Carcinoma colon-rettale metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 36 Ottobre 2014 Direzione
Raccomandazioni evidence-based Panitumumab Carcinoma colon-rettale metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 36 Ottobre 2014 Direzione
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE. n. 749 del 26-10-2015 O G G E T T O
 REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 749 del 26-10-2015 O G G E T T O Istituzione Commissione per la valutazione della richiesta di farmaci non erogabili
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 749 del 26-10-2015 O G G E T T O Istituzione Commissione per la valutazione della richiesta di farmaci non erogabili
La terapia medica primaria e adiuvante e il follow-up: le principali novità. a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati (Ferrara)
 Protocollo diagnostico-terapeutico per le Pazienti con carcinoma mammario La terapia medica primaria e adiuvante e il follow-up: le principali novità a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati
Protocollo diagnostico-terapeutico per le Pazienti con carcinoma mammario La terapia medica primaria e adiuvante e il follow-up: le principali novità a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati
dopo il fallimento di terapia con antiaromatasico A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Everolimus Nel carcinoma mammario avanzato dopo il fallimento di terapia con antiaromatasico A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso
Raccomandazioni evidence-based Everolimus Nel carcinoma mammario avanzato dopo il fallimento di terapia con antiaromatasico A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso
CARTA INTESTATA DEL CENTRO CLINICO
 CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
Trastuzumab emtansine (TDM-1)
 Raccomandazioni evidence-based Trastuzumab emtansine (TDM-1) nel carcinoma della mammella avanzato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.33 (Pubblicato a ) Aggiornato
Raccomandazioni evidence-based Trastuzumab emtansine (TDM-1) nel carcinoma della mammella avanzato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.33 (Pubblicato a ) Aggiornato
Chairmen: Sabino De Placido, Luca Gianni
 Chairmen: Sabino De Placido, Luca Gianni P R O G R A M M A S C I E N T I F I C O P R E L I M I N A R E COORDINATORI SCIENTIFICI SABINO DE PLACIDO Università Degli Studi di Napoli Federico II, Napoli LUCA
Chairmen: Sabino De Placido, Luca Gianni P R O G R A M M A S C I E N T I F I C O P R E L I M I N A R E COORDINATORI SCIENTIFICI SABINO DE PLACIDO Università Degli Studi di Napoli Federico II, Napoli LUCA
Il ruolo di CA15-3 nel monitoraggio della terapia nel carcinoma mammario metastatico: un caso clinico
 Il ruolo di CA15-3 nel monitoraggio della terapia nel carcinoma mammario metastatico: un caso clinico C. Cocco 1, B. Caruso 1, E. Fiorio 2 1 Laboratorio Analisi (sede di BT) 2 Oncologia (sede di BT), AOUI,
Il ruolo di CA15-3 nel monitoraggio della terapia nel carcinoma mammario metastatico: un caso clinico C. Cocco 1, B. Caruso 1, E. Fiorio 2 1 Laboratorio Analisi (sede di BT) 2 Oncologia (sede di BT), AOUI,
Sinossi di studio clinico Codice: GECP06/01 Pag. 1 di 5
 Codice: GECP06/01 Pag. 1 di 5 Studio aperto randomizzato multicentrico di fase III di confronto tra il trattamento con Erlotinib (Tarceva ) e la chemioterapia nei pazienti affetti da carcinoma non a piccole
Codice: GECP06/01 Pag. 1 di 5 Studio aperto randomizzato multicentrico di fase III di confronto tra il trattamento con Erlotinib (Tarceva ) e la chemioterapia nei pazienti affetti da carcinoma non a piccole
BANDO AIFA 2012 PER LA RICERCA INDIPENDENTE SUI FARMACI
 BANDO AIFA 2012 PER LA RICERCA INDIPENDENTE SUI FARMACI SCHEMA DI PRESENTAZIONE DELLA LETTERA DI INTENTI La presentazione della lettera di intenti dovrà avvenire entro le ore 12.00 del 23 aprile 2012,
BANDO AIFA 2012 PER LA RICERCA INDIPENDENTE SUI FARMACI SCHEMA DI PRESENTAZIONE DELLA LETTERA DI INTENTI La presentazione della lettera di intenti dovrà avvenire entro le ore 12.00 del 23 aprile 2012,
SEBASTIANO FILETTI. Dipartimento di Medicina Interna e Specialità Mediche. Università di Roma Sapienza, Roma
 SEBASTIANO FILETTI Dipartimento di Medicina Interna e Specialità Mediche Università di Roma Sapienza, Roma La malattia tiroidea è in aumento negli ultimi anni. Quali le ragioni? Dati epidemiologici provenienti
SEBASTIANO FILETTI Dipartimento di Medicina Interna e Specialità Mediche Università di Roma Sapienza, Roma La malattia tiroidea è in aumento negli ultimi anni. Quali le ragioni? Dati epidemiologici provenienti
Governo del Farmaco. Azienda Ospedaliera di Verona
 Governo del Farmaco Elementi organizzativi e tecnologie: Esperienze a confronto Venezia 23 Febbraio 2009 Giovanna Scroccaro Azienda Ospedaliera di Verona Governo del Farmaco Elementi organizzativi e tecnologie:
Governo del Farmaco Elementi organizzativi e tecnologie: Esperienze a confronto Venezia 23 Febbraio 2009 Giovanna Scroccaro Azienda Ospedaliera di Verona Governo del Farmaco Elementi organizzativi e tecnologie:
Coordinatori Catia Angiolini, Giovanni L. Pappagallo alias Gigi. -Le evidenze derivanti dalla letteratura Marta Pestrin
 3- QUESITO CLINICO Nelle pazienti con carcinoma mammario HR positivo/her2 negativo in postmenopausa è opportuno considerare un trattamento ormonale con Fulvestrant rispetto ad AI? Coordinatori Catia Angiolini,
3- QUESITO CLINICO Nelle pazienti con carcinoma mammario HR positivo/her2 negativo in postmenopausa è opportuno considerare un trattamento ormonale con Fulvestrant rispetto ad AI? Coordinatori Catia Angiolini,
IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA
 IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA Francesca Caprari Direttore Affari Istituzionali e Relazioni Esterne Celgene srl L inizio Il Registro AIFA
IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA Francesca Caprari Direttore Affari Istituzionali e Relazioni Esterne Celgene srl L inizio Il Registro AIFA
DECRETI E DELIBERE DI ALTRE AUTORITÀ
 DECRETI E DELIBERE DI ALTRE AUTORITÀ AGENZIA ITALIANA DEL FARMACO DETERMINA 17 giugno 2013. Classificazione del medicinale per uso umano «Kristexxa», secondo procedura centralizzata. (Determina n. 583/2013).
DECRETI E DELIBERE DI ALTRE AUTORITÀ AGENZIA ITALIANA DEL FARMACO DETERMINA 17 giugno 2013. Classificazione del medicinale per uso umano «Kristexxa», secondo procedura centralizzata. (Determina n. 583/2013).
 Agenzia Italiana del Farmaco Bando di assegnazione di finanziamento per la Ricerca indipendente sui farmaci Area 2 - Studi comparativi fra farmaci e strategie farmacologiche Art. 48, commi 5 lett. g) e
Agenzia Italiana del Farmaco Bando di assegnazione di finanziamento per la Ricerca indipendente sui farmaci Area 2 - Studi comparativi fra farmaci e strategie farmacologiche Art. 48, commi 5 lett. g) e
GRAVIDANZA DOPO CANCRO: QUANDO? Giovanna Scarfone - Stefania Noli Fondazione IRCCS Ca Granda Opsedale Maggiore Policlinico, Milano
 GRAVIDANZA DOPO CANCRO: QUANDO? Giovanna Scarfone - Stefania Noli Fondazione IRCCS Ca Granda Opsedale Maggiore Policlinico, Milano Timing e outcome della gravidanza dopo carcinoma Inquadramento ed Entità
GRAVIDANZA DOPO CANCRO: QUANDO? Giovanna Scarfone - Stefania Noli Fondazione IRCCS Ca Granda Opsedale Maggiore Policlinico, Milano Timing e outcome della gravidanza dopo carcinoma Inquadramento ed Entità
SINOSSI. Studio di Fase II: Obiettivo primario Determinare l attività antitumorale della combinazione in termini di tempo alla progressione
 SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
MODELLO ORGANIZZATIVO REGIONALE PER LA GESTIONE DEL RISCHIO CLINICO.
 ALLEGATO A MODELLO ORGANIZZATIVO REGIONALE PER LA GESTIONE DEL RISCHIO CLINICO. il sistema organizzativo che governa le modalità di erogazione delle cure non è ancora rivolto al controllo in modo sistemico
ALLEGATO A MODELLO ORGANIZZATIVO REGIONALE PER LA GESTIONE DEL RISCHIO CLINICO. il sistema organizzativo che governa le modalità di erogazione delle cure non è ancora rivolto al controllo in modo sistemico
STUDIO OSSERVAZIONALE SULLA TERAPIA DELLA PATOLOGIA MAMMARIA INDOTTA DALLA MONOTERAPIA CON ANTIANDROGENO PURO PER ADENOCARCINOMA PROSTATICO
 STUDIO OSSERVAZIONALE SULLA TERAPIA DELLA PATOLOGIA MAMMARIA INDOTTA DALLA MONOTERAPIA CON ANTIANDROGENO PURO PER ADENOCARCINOMA PROSTATICO FAX: 0916552413 SITO WEB: www.gstu.it E-MAIL: [email protected] CRITERI
STUDIO OSSERVAZIONALE SULLA TERAPIA DELLA PATOLOGIA MAMMARIA INDOTTA DALLA MONOTERAPIA CON ANTIANDROGENO PURO PER ADENOCARCINOMA PROSTATICO FAX: 0916552413 SITO WEB: www.gstu.it E-MAIL: [email protected] CRITERI
Nuovi regimi terapeutici nel trattamento del mieloma multiplo in pazienti non candidabili a trapianto
 Nuovi regimi terapeutici nel trattamento del mieloma multiplo in pazienti non candidabili a trapianto Antonio Palumbo Divisione di Ematologia Universitaria, Ospedale Molinette, Torino Per più di quattro
Nuovi regimi terapeutici nel trattamento del mieloma multiplo in pazienti non candidabili a trapianto Antonio Palumbo Divisione di Ematologia Universitaria, Ospedale Molinette, Torino Per più di quattro
Il Direttore della Direzione Regionale Programmazione Sanitaria -Risorse Umane e Sanitarie
 Oggetto: Aggiornamento della determinazione 1875 del Modalità di erogazione dei farmaci classificati in regime di rimborsabilità in fascia H e in regime di fornitura OSP2, così come modificata dalla determinazione
Oggetto: Aggiornamento della determinazione 1875 del Modalità di erogazione dei farmaci classificati in regime di rimborsabilità in fascia H e in regime di fornitura OSP2, così come modificata dalla determinazione
Il ruolo di AIFA nella Ricerca Clinica. Luca Pani [email protected]
 Il ruolo di AIFA nella Ricerca Clinica Luca Pani [email protected] Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non possono essere considerate o citate
Il ruolo di AIFA nella Ricerca Clinica Luca Pani [email protected] Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non possono essere considerate o citate
La gestione del rischio clinico nei reparti ospedalieri e nelle RSA
 Coordinamento Regionale Unico sul Farmaco Risultati indagine regionale: La gestione del rischio clinico nei reparti ospedalieri e nelle RSA Dr.ssa Silvia Adami Venezia, 28-02-2014 2 Programma S. Adami:
Coordinamento Regionale Unico sul Farmaco Risultati indagine regionale: La gestione del rischio clinico nei reparti ospedalieri e nelle RSA Dr.ssa Silvia Adami Venezia, 28-02-2014 2 Programma S. Adami:
Documento PTR n.212 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n.212 relativo a: PAZOPANIB Aprile 2014 Pazopanib Indicazioni registrate
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n.212 relativo a: PAZOPANIB Aprile 2014 Pazopanib Indicazioni registrate
BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma mammario metastatico in combinazione con paclitaxel.
 BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma mammario metastatico in combinazione con paclitaxel. (09-09-2008) Specialità: Avastin(Roche spa) Forma farmaceutica:
BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma mammario metastatico in combinazione con paclitaxel. (09-09-2008) Specialità: Avastin(Roche spa) Forma farmaceutica:
L'ESPERIENZA DEL PROGETTO EMILI: PREVENZIONE NELLE DONNE CON TUMORE MAMMARIO ATTRAVERSO L'EDUCAZIONE ALIMENTARE E AL MOVIMENTO
 L'ESPERIENZA DEL PROGETTO EMILI: PREVENZIONE NELLE DONNE CON TUMORE MAMMARIO ATTRAVERSO L'EDUCAZIONE ALIMENTARE E AL MOVIMENTO Latina, 26 Maggio 2012 Dott.ssa Federica Sebastiani Dipartimento di Oncologia.
L'ESPERIENZA DEL PROGETTO EMILI: PREVENZIONE NELLE DONNE CON TUMORE MAMMARIO ATTRAVERSO L'EDUCAZIONE ALIMENTARE E AL MOVIMENTO Latina, 26 Maggio 2012 Dott.ssa Federica Sebastiani Dipartimento di Oncologia.
Il punto di vista del clinico
 Il punto di vista del clinico Giulio Metro S.C. Oncologia Medica Ospedale Santa Maria della Misericordia, Azienda Ospedaliera di Perugia Registri di monitoraggio AIFA: stato dell arte ed esperienze a confronto
Il punto di vista del clinico Giulio Metro S.C. Oncologia Medica Ospedale Santa Maria della Misericordia, Azienda Ospedaliera di Perugia Registri di monitoraggio AIFA: stato dell arte ed esperienze a confronto
Perfare MASSIMIZZARE IL VALORE DELL ATTUALE GAMMA DI PRODOTTI
 Perfare Perfare Percorsi aziendali di formazione e assistenza operativa MASSIMIZZARE IL VALORE DELL ATTUALE GAMMA DI PRODOTTI Costruire un piano di azioni concrete per ottenere il massimo valore dall attuale
Perfare Perfare Percorsi aziendali di formazione e assistenza operativa MASSIMIZZARE IL VALORE DELL ATTUALE GAMMA DI PRODOTTI Costruire un piano di azioni concrete per ottenere il massimo valore dall attuale
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO
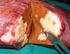 LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO SANITARIA N. 6 VICENZA PROVVEDIMENTO DEL DIRIGENTE RESPONSABILE
 REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO SANITARIA N. 6 VICENZA PROVVEDIMENTO DEL DIRIGENTE RESPONSABILE Servizio Risorse Umane e Relazioni Sindacali delegato dal Direttore Generale dell Azienda con
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO SANITARIA N. 6 VICENZA PROVVEDIMENTO DEL DIRIGENTE RESPONSABILE Servizio Risorse Umane e Relazioni Sindacali delegato dal Direttore Generale dell Azienda con
Comitato Scientifico: Gianni Amunni Oscar Bertetto Antonio Frassoldati Roberto Labianca Riccardo Masetti Paolo Pronzato
 Coordinamento Scientifico Pierfranco Conte Valentina Guarneri Comitato Scientifico: Gianni Amunni Oscar Bertetto Antonio Frassoldati Roberto Labianca Riccardo Masetti Paolo Pronzato A cura di OVER SRL
Coordinamento Scientifico Pierfranco Conte Valentina Guarneri Comitato Scientifico: Gianni Amunni Oscar Bertetto Antonio Frassoldati Roberto Labianca Riccardo Masetti Paolo Pronzato A cura di OVER SRL
Trials clinici. Disegni di studio
 Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Rassegna Stampa. Comunicato stampa. Intermedia s.r.l. per la comunicazione integrata
 Rassegna Stampa Comunicato stampa TUMORE DEL SENO: FUNZIONA LA TERAPIA "ACCELERATA" "IL 94% DEI PAZIENTI GUARISCE CON I TEMPI DI CURA PIU' BREVI" Intermedia s.r.l. per la comunicazione integrata Via Malta,
Rassegna Stampa Comunicato stampa TUMORE DEL SENO: FUNZIONA LA TERAPIA "ACCELERATA" "IL 94% DEI PAZIENTI GUARISCE CON I TEMPI DI CURA PIU' BREVI" Intermedia s.r.l. per la comunicazione integrata Via Malta,
SCHEDA FARMACO. (a cura di UOS Farmacoeconomia e HTA, Area Centro)
 SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Dabrafenib (Tafinlar)
SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Dabrafenib (Tafinlar)
Terapia in fase Avanzata
 IL CARCINOMA DEL COLON-RETTO 14 OTTOBRE 2011, ROMA Terapia in fase Avanzata Maria Sofia Rosati Oncologia A Policlinico Umberto I Roma Numeri.. e persone!! ***Solo il 56% *50% dei pz con CRC è over 70 degli
IL CARCINOMA DEL COLON-RETTO 14 OTTOBRE 2011, ROMA Terapia in fase Avanzata Maria Sofia Rosati Oncologia A Policlinico Umberto I Roma Numeri.. e persone!! ***Solo il 56% *50% dei pz con CRC è over 70 degli
Accesso ai farmaci innovativi e controllo della spesa a livello regionale
 FARMACI INNOVATIVI Qualità efficacia appropriatezza 9 ottobre 2009 Camera dei Deputati Palazzo Marini (Roma) Accesso ai farmaci innovativi e controllo della spesa a livello regionale Stefania Melena Direzione
FARMACI INNOVATIVI Qualità efficacia appropriatezza 9 ottobre 2009 Camera dei Deputati Palazzo Marini (Roma) Accesso ai farmaci innovativi e controllo della spesa a livello regionale Stefania Melena Direzione
Finanziamento di Progetti di Ricerca in Oncologia. Bando interno per l anno 2013
 < Finanziamento di Progetti di Ricerca in Oncologia Bando interno per l anno 2013 La Direzione Scientifica emana per l anno 2013 un bando interno per finanziare mediante il budget della Ricerca Corrente
< Finanziamento di Progetti di Ricerca in Oncologia Bando interno per l anno 2013 La Direzione Scientifica emana per l anno 2013 un bando interno per finanziare mediante il budget della Ricerca Corrente
Quando il dolore è ancora un problema. XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013
 Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
PRESENTAZIONE DEL PDTA ELABORATO DAL GRUPPO U.O.C. CHIRURGIA TORACICA UNIVERSITA DEGLI STUDI DI PADOVA AZIENDA OSPEDALIERA DI PADOVA
 PRESENTAZIONE DEL PDTA ELABORATO DAL GRUPPO FEDERICO REA U.O.C. CHIRURGIA TORACICA UNIVERTA DEGLI STUDI DI PADOVA AZIENDA OSPEDALIERA DI PADOVA PDTA Percorso Diagnostico Terapeutico ed Assistenziale Rappresenta
PRESENTAZIONE DEL PDTA ELABORATO DAL GRUPPO FEDERICO REA U.O.C. CHIRURGIA TORACICA UNIVERTA DEGLI STUDI DI PADOVA AZIENDA OSPEDALIERA DI PADOVA PDTA Percorso Diagnostico Terapeutico ed Assistenziale Rappresenta
16/05/2012. La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino. Roma, 10 Maggio 2012
 La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino Roma, 10 Maggio 2012 1 Dichiarazione di trasparenza/interessi: Carlo Tomino, dirigente Le opinioni espresse in questa
La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino Roma, 10 Maggio 2012 1 Dichiarazione di trasparenza/interessi: Carlo Tomino, dirigente Le opinioni espresse in questa
Carcinoma della prostata: INCIDENZA
 Outcomes in Localized Prostate Cancer: National Prostate Cancer Registry of Sweden Follow-up Study JNCI - J Natl Cancer Inst. 2010 Jul 7;102(13):919-20 Trento, 13/11/2010 Di cosa si tratta? E' uno studio
Outcomes in Localized Prostate Cancer: National Prostate Cancer Registry of Sweden Follow-up Study JNCI - J Natl Cancer Inst. 2010 Jul 7;102(13):919-20 Trento, 13/11/2010 Di cosa si tratta? E' uno studio
Grazie dell attenzione
 Grazie dell attenzione http://www.registri-tumori.it/pdf/aiom2012/i_numeri_del_cancro_2012.pdf In Italia circa 2.250mila persone (4% del totale della popolazione) vivono avendo avuto una precedente
Grazie dell attenzione http://www.registri-tumori.it/pdf/aiom2012/i_numeri_del_cancro_2012.pdf In Italia circa 2.250mila persone (4% del totale della popolazione) vivono avendo avuto una precedente
Il ruolo dell ISF: dall informazione al marketing Raffaella Michieli
 Il ruolo dell ISF: dall informazione al marketing Raffaella Michieli Metodi di cura Per i Medici il Farmaco è il pane quotidiano 85% dei contatti in MG esita in una prescrizione farmacologica Fonte H.S.
Il ruolo dell ISF: dall informazione al marketing Raffaella Michieli Metodi di cura Per i Medici il Farmaco è il pane quotidiano 85% dei contatti in MG esita in una prescrizione farmacologica Fonte H.S.
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? 2. Come nasce la sperimentazione clinica e che tipi di studi esistono?
 STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
Aggiornamenti su RAS: mutazioni di KRAS ed NRAS nel carcinoma del colon retto. Carmelo Lupo
 Aggiornamenti su RAS: mutazioni di KRAS ed NRAS nel carcinoma del colon retto Carmelo Lupo RAS-RAF signaling Activation of the RAS-RAF signaling cascade occurs via the following sequential steps 1 : Activation
Aggiornamenti su RAS: mutazioni di KRAS ed NRAS nel carcinoma del colon retto Carmelo Lupo RAS-RAF signaling Activation of the RAS-RAF signaling cascade occurs via the following sequential steps 1 : Activation
Anticorpi monoclonali Anti-EGFR. -Ruolo Biologico -Evidenze terapeutiche -Problemi -Sviluppi futuri. Valentina Anrò
 Anticorpi monoclonali Anti-EGFR -Ruolo Biologico -Evidenze terapeutiche -Problemi -Sviluppi futuri Valentina Anrò Ruolo Biologico Epidermal Growth Factor Receptor Extracellular Domain Transmembrane Domain
Anticorpi monoclonali Anti-EGFR -Ruolo Biologico -Evidenze terapeutiche -Problemi -Sviluppi futuri Valentina Anrò Ruolo Biologico Epidermal Growth Factor Receptor Extracellular Domain Transmembrane Domain
Premessa. Tratto da American Heart Journal 2004; 147: 705-712
 Effetti del cambiamento di terapia con statine sul raggiungimento delle concentrazioni lipidiche ottimali: lo studio Measuring Effective Reductions in Cholesterol Using Rosuvastatin Therapy (MERCURY I)
Effetti del cambiamento di terapia con statine sul raggiungimento delle concentrazioni lipidiche ottimali: lo studio Measuring Effective Reductions in Cholesterol Using Rosuvastatin Therapy (MERCURY I)
Autorità Nazionale Anticorruzione e per la valutazione e la trasparenza delle amministrazioni pubbliche
 Autorità Nazionale Anticorruzione e per la valutazione e la trasparenza delle amministrazioni pubbliche Metodologia dell attività di vigilanza e controllo dell Autorità in relazione agli obblighi di pubblicazione
Autorità Nazionale Anticorruzione e per la valutazione e la trasparenza delle amministrazioni pubbliche Metodologia dell attività di vigilanza e controllo dell Autorità in relazione agli obblighi di pubblicazione
Accesso ai farmaci innovativi: alternative all AIC
 Accesso ai farmaci innovativi: alternative all AIC Maria Lebboroni Servizio di Farmacia Ospedaliera ULSS 9 Treviso Premessa Sperimentazione clinica Immissione in commercio (AIC) normativa farmacovigilanza
Accesso ai farmaci innovativi: alternative all AIC Maria Lebboroni Servizio di Farmacia Ospedaliera ULSS 9 Treviso Premessa Sperimentazione clinica Immissione in commercio (AIC) normativa farmacovigilanza
I nuovi anticoagulanti orali nella fibrillazione atriale non valvolare: le linee guida per la prescrizione
 I nuovi anticoagulanti orali nella fibrillazione atriale non valvolare: le linee guida per la prescrizione Anna Maria Marata Area Valutazione del Farmaco ASSR Regione Emilia Romagna 9 Dicembre 2013 October
I nuovi anticoagulanti orali nella fibrillazione atriale non valvolare: le linee guida per la prescrizione Anna Maria Marata Area Valutazione del Farmaco ASSR Regione Emilia Romagna 9 Dicembre 2013 October
Cetuximab e mutazione K-Ras nel tumore del colon-retto
 Università di Pisa Dipartimento di Farmacia Corso di laurea in CTF Corso: Basi biochimiche dell azione dei farmaci Cetuximab e mutazione K-Ras nel tumore del colon-retto Pisa, 27/03/2014 Samuela Fabiani
Università di Pisa Dipartimento di Farmacia Corso di laurea in CTF Corso: Basi biochimiche dell azione dei farmaci Cetuximab e mutazione K-Ras nel tumore del colon-retto Pisa, 27/03/2014 Samuela Fabiani
nel carcinoma del pancreas esocrino metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Nab-paclitaxel nel carcinoma del pancreas esocrino metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 40 Febbraio
Raccomandazioni evidence-based Nab-paclitaxel nel carcinoma del pancreas esocrino metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 40 Febbraio
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI
 UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
BANDO. Premi di Ricerca SIOMMMS per giovani ricercatori
 BANDO Premi di Ricerca SIOMMMS per giovani ricercatori Regolamento Per il biennio 2014/2016 la SIOMMMS (Società Italiana dell Osteoporosi, del Metabolismo Minerale e delle Malattie Metaboliche dello Scheletro)
BANDO Premi di Ricerca SIOMMMS per giovani ricercatori Regolamento Per il biennio 2014/2016 la SIOMMMS (Società Italiana dell Osteoporosi, del Metabolismo Minerale e delle Malattie Metaboliche dello Scheletro)
Studio di ricerca clinica sul dolore da endometriosi. Il dolore che Lei sente è reale... anche se gli altri non possono vederlo.
 Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
PDTA e farmaci innovativi nel carcinoma della mammella
 PDTA e farmaci innovativi nel carcinoma della mammella Maria Vittoria Dieci, PierFranco Conte Università di Padova Dipartimento di Scienze Chirurgiche, Oncologiche e Gastroenterologiche IOV Istituto Oncologico
PDTA e farmaci innovativi nel carcinoma della mammella Maria Vittoria Dieci, PierFranco Conte Università di Padova Dipartimento di Scienze Chirurgiche, Oncologiche e Gastroenterologiche IOV Istituto Oncologico
REGIONE DEL VENETO ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. DELIBERAZIONE DEL DIRETTORE GENERALE N. 85 DEL 13/03/2013
 REGIONE DEL VENETO ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. DELIBERAZIONE DEL DIRETTORE GENERALE N. 85 DEL 13/03/2013 OGGETTO: Approvazione convenzione con la Società Pierre Fabre Pharma srl di Milano per
REGIONE DEL VENETO ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. DELIBERAZIONE DEL DIRETTORE GENERALE N. 85 DEL 13/03/2013 OGGETTO: Approvazione convenzione con la Società Pierre Fabre Pharma srl di Milano per
Comparabilità fra le somministrazioni successive effetto di trascinamento ( carry-over ) effetto di periodo
 Metodo epidemiologici per la clinica _efficacia / 2 Gli studi crossover Periodo 1 Periodo 2 R A N D O M A B A B Valutazione Tempo 1 0 1 1 2 0 2 1 Gli studi crossover Metodo epidemiologici per la clinica
Metodo epidemiologici per la clinica _efficacia / 2 Gli studi crossover Periodo 1 Periodo 2 R A N D O M A B A B Valutazione Tempo 1 0 1 1 2 0 2 1 Gli studi crossover Metodo epidemiologici per la clinica
ARTICOLO SCIENTIFICO: ANALISI E VALUTAZIONE CRITICA DELLE INFORMAZIONI. critical appraisal BOSCARO GIANNI 1
 ARTICOLO SCIENTIFICO: ANALISI E VALUTAZIONE CRITICA DELLE INFORMAZIONI critical appraisal BOSCARO GIANNI 1 BOSCARO GIANNI 2 Analisi Statistica analisi descrittiva: descrizione dei dati campionari con grafici,
ARTICOLO SCIENTIFICO: ANALISI E VALUTAZIONE CRITICA DELLE INFORMAZIONI critical appraisal BOSCARO GIANNI 1 BOSCARO GIANNI 2 Analisi Statistica analisi descrittiva: descrizione dei dati campionari con grafici,
Terapia del dolore in oncologia La rilevazione del dolore
 Terapia del dolore in oncologia La rilevazione del dolore B. Micheloni UOC Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar 4 Dicembre 2014 Definizione di dolore Spiacevole esperienza sensoriale
Terapia del dolore in oncologia La rilevazione del dolore B. Micheloni UOC Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar 4 Dicembre 2014 Definizione di dolore Spiacevole esperienza sensoriale
Dr.ssa Enola Maria Vezzani
 III ZOOM Journal Club 2013 NH Hotel Bologna 21 Febbraio 2014 Radioterapia loco-regionale nelle pazienti sottoposte a chemioterapia neoadiuvante Dr.ssa Enola Maria Vezzani U.O Radioterapia Oncologica di
III ZOOM Journal Club 2013 NH Hotel Bologna 21 Febbraio 2014 Radioterapia loco-regionale nelle pazienti sottoposte a chemioterapia neoadiuvante Dr.ssa Enola Maria Vezzani U.O Radioterapia Oncologica di
ANALISI DI ALCUNI INDICATORI DI FOLLOW-UP NEL TUMORE DELLA MAMMELLA NELL ASL DELLA PROVINCIA DI VARESE ANNO 2009
 ANALISI DI ALCUNI INDICATORI DI FOLLOW-UP NEL TUMORE DELLA MAMMELLA NELL ASL DELLA PROVINCIA DI VARESE ANNO 2009 A cura di: Dr.ssa M. Gambino, Dr.ssa Ass. San. L. Balconi, Dr. S. Pisani U. O. S. Sorveglianza
ANALISI DI ALCUNI INDICATORI DI FOLLOW-UP NEL TUMORE DELLA MAMMELLA NELL ASL DELLA PROVINCIA DI VARESE ANNO 2009 A cura di: Dr.ssa M. Gambino, Dr.ssa Ass. San. L. Balconi, Dr. S. Pisani U. O. S. Sorveglianza
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza
 Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
SCHEDA PER LA RILEVAZIONE DELLA CUSTOMER SATISFACTION
 SCHEDA PER LA RILEVAZIONE DELLA CUSTOMER SATISFACTION FAC-SIMILE Nota: Il presente questionario, predisposto a cura dell Ufficio Formazione/ Direzione/altro Ufficio responsabile, è compilato a cura di
SCHEDA PER LA RILEVAZIONE DELLA CUSTOMER SATISFACTION FAC-SIMILE Nota: Il presente questionario, predisposto a cura dell Ufficio Formazione/ Direzione/altro Ufficio responsabile, è compilato a cura di
Il paradosso del Veneto
 Audizione in Quinta Commissione del Consiglio Regionale del Veneto Venezia, 12 Luglio 2013 Il paradosso del Veneto Enzo Bonora Presidente - Sezione Veneto Trentino Alto Adige Società Italiana di Diabetologia
Audizione in Quinta Commissione del Consiglio Regionale del Veneto Venezia, 12 Luglio 2013 Il paradosso del Veneto Enzo Bonora Presidente - Sezione Veneto Trentino Alto Adige Società Italiana di Diabetologia
Guida Compilazione Piani di Studio on-line
 Guida Compilazione Piani di Studio on-line SIA (Sistemi Informativi d Ateneo) Visualizzazione e presentazione piani di studio ordinamento 509 e 270 Università della Calabria (Unità organizzativa complessa-
Guida Compilazione Piani di Studio on-line SIA (Sistemi Informativi d Ateneo) Visualizzazione e presentazione piani di studio ordinamento 509 e 270 Università della Calabria (Unità organizzativa complessa-
