Farmacovigilanza La segnalazione on line
|
|
|
- Viola Chiesa
- 4 anni fa
- Visualizzazioni
Transcript
1 Farmacovigilanza La segnalazione on line Pesaro 13 novembre 2017 U.O. Farmacovigilanza Ospedaliera e Territoriale paola.paolucci2@sanita.marche.it
2 Operatore Sanitario Operatori sanitari e cittadini inviano le segnalazioni usando moduli cartacei che vengono raccolti dal Responsabile di FV (RFV) Il Responsabile di FV controlla che le segnalazioni siano complete; le invia ad AIFA, attraverso la Rete Nazionale di FV, e al Centro Regionale via o fax. Cittadini h 7 giorni Responsabile di FV Rete Nazionale di FV (AIFA) L AIFA analizza periodicamente le segnalazioni raccolte e le condivide a livello europeo e mondiale attraverso EudraVigilance e VigiBase
3
4
5
6
7 Difficili da compilare in modo corretto Il segnalatore può omettere o sbagliare dati importanti (non ha un feedback diretto) Complicati da trasferire al RFV e al CR I moduli cartacei devono essere inviati via fax, via , via posta ordinaria Onerosi da gestire per il RFV Controllare che i dati siano corretti e se non lo sono deve richiamare il segnalatore, inserire manualmentela segnalazione in RNF entro 7 giorni Formazione degli operatori per la codifica MedDRA Archiviazione delle schede cartacee originali
8 Evoluzione della Rete Nazionale di Farmacovigilanza verso un sistema più efficiente Nuova piattaforma tecnologica di riferimento Nuove funzionalità
9 Segnalazione online è un sistema attraverso il quale operatori sanitari e pazienti possono inviare via web in modo volontario casi di sospette reazioni avverse da farmaci all'autorità regolatrice è previsto anche dalla nuova normativa europea in materia di farmacovigilanza
10 Inghilterra Spagna Olanda Danimarca Croazia
11 Operatore Sanitario Operatori sanitari e cittadini, registrati o non inviano via web le segnalazioni collegandosi a VigiFarmaco e compilando un modulo online VigiFarmaco h 7 giorni Rete Nazionale di FV (AIFA) Cittadini Il Responsabile di FV: -riceve di notifica delle nuove segnalazioni -si collega a VigiFarmaco per validare e codificare la scheda -invia in automatico XML la scheda nella Rete Nazionale di FV. Responsabile di FV
12
13 Sito compatibile con tutti i browser (ultime versioni) Preferibile Mozilla Firefox JavaScript aggiornato
14 Estensione alla tecnologia mobile (Android, ios) Dialogo della piattaforma con altri sistemi per una più veloce e diretta segnalazione: Anagrafi vaccinali Cartelle cliniche ospedaliere informatizzate Software di MMG Sviluppo della piattaforma come strumento di informazione di ritorno ai segnalatori Miglioramento delle prestazioni dell autocodifica
15 Registrazione (segnalatori, RFV e CR) Invio delle segnalazioni Validazione e codifica Invio in RNF RFV e CR Archiviazione schede cartacee
16
17 VigiFarmaco Registrazione (1/2) I segnalatori possono usare la piattaforma con o senza registrazione Se si registrano trovano i propri dati già inseriti in ogni segnalazione Gli operatori (Responsabili di FV, Centri Regionali) devono registrarsi per operare in VigiFarmaco
18 I fase (tutti): registrazione personale VigiFarmaco Registrazione (2/2) come cittadino o operatore sanitario dati richiesti: nome, cognome, , ASL di appartenenza, struttura sanitaria di riferimento II fase (RFV/CR): richiesta e assegnazione del ruolo III fase (RFV/CR): gestione del profilo RFV e CR
19 VigiFarmaco Invio della segnalazione Cittadini e operatori sanitari possono segnalare con o senza registrazione (dati precompilati) Moduli diversi per operatori sanitari e cittadini Guida alla compilazione a fianco I campi obbligatori sono solo quelli previsti dalla normativa (indicati con un asterisco).
20 VigiFarmaco Invio della segnalazione Al termine della segnalazione il sistema gestisce automaticamente l invio di un di notifica al segnalatore, al relativo Responsabile di Farmacovigilanza e al Centro regionale(ed eventuali collaboratori) I segnalatori possono scaricare il pdf della segnalazione Successivamente il segnalatore e il RFV ricevono dal sistema l avviso tramite dell avvenuto inserimento in RNF(informazione di ritorno)
21 La segnalazione viene fatta in 5 fasi successive: Dati del paziente Dati della reazione avversa VigiFarmaco Invio della segnalazione Dati dei trattamenti (sospetti, concomitanti e altri prodotti) Dettagli del segnalatore + informazioni aggiuntive (es. Reparto) Anteprima per verifica/modifica e invio Compilazione dei campi: Dati inseriti con menu a tendina (funzione dell autocompletamento) o come testo libero Possibilità di modificare o eliminare quanto inserito tramite appositi pulsanti
22 Paziente Per motivi di privacy riportare prima la lettera iniziale del nome e del cognome. L indicazione della data di nascita, invece che dell età, è importante per segnalazioni di reazioni avverse a vaccino: infatti, le vaccinazioni dell età evolutiva vengono somministrate, di norma, ad età prestabilite. Le iniziali, insieme alla data di nascita, consentono di distinguere i casi, operazione necessaria soprattutto in occasione di segnalazioni di cluster di reazioni avverse da vaccini derivanti da una stessa struttura. La data di insorgenza della reazione insieme alle date di inizio e fine terapia - cartella SM/PA sospetto - consentono di stabilire la correlazione temporale tra assunzione del farmaco e reazione avversa. La data di nascita l età sono indicazioni tra loro esclusive.
23
24 Reazione avversa Oltre alla descrizione della reazione è prevista anche la sua diagnosi ed i risultati di eventuali accertamenti diagnostici. Esami di laboratorio e strumentali : risultati, rilevanti ai fini della reazione avversa, degli esami effettuati e date a cui si riferiscono. La sola citazione dell esame senza conoscere il risultato non è dirimente. Una reazione è grave solo se: è fatale; ha provocato o prolungato l ospedalizzazione; ha provocato invalidità grave o permanente; ha messo in pericolo la vita del paziente. Sono gravi le anomalie congenite e i difetti alla nascita in neonati le cui madri avevano assunto farmaci sospetti in gravidanza. La scheda sarà compilata con i dati della madre. Sarà allegata una relazione clinica con dati anamnestici, dettagli sulla reazione a carico del neonato e l esito della stessa Se l esito è decesso, è necessario indicare la data del decesso e la causa.
25
26
27 Farmaco: SM/PA sospetto E importante riportare il nome commerciale del farmaco e non il principio attivo per consentire accertamenti legati alla produzione e per consentire alle aziende farmaceutiche di assolvere agli obblighi di farmacovigilanza previsti dalla legge. Nel caso dei farmaci generici, al nome del principio attivo deve essere aggiunto il nome dell azienda per permettere l identificazione del medicinale coinvolto. Deve essere indicato il dosaggio e l unità posologica per permettere l individuazione della confezione, e la data di scadenza. Riportare informazioni relative all eventuale miglioramento della reazione avversa dopo la sospensione del farmaco. Per segnalazione di reazioni a vaccini riportare l ora della somministrazione, il numero di dose o richiamo e la sede della vaccinazione. Dall indicazione terapeutica per la quale il farmaco è stato assunto potrebbero emergere spiegazioni alternative all insorgenza della reazione osservata.
28
29
30
31 SM/PA concomitante L informazione di eventuali farmaci concomitanti va acquisita soprattutto in relazione alle possibili interazioni. Nel caso di segnalazione di reazioni avverse a vaccini è necessario riportare anche i vaccini somministrati nelle 4 settimane precedenti alla somministrazione. E necessario inserire le informazioni sul dosaggio e sulla via di somministrazione.
32 Segnalatore Il segnalatore deve essere chiaramente identificabile,anche se i suoi dati sono tutelati, in primo luogo perchè spesso c è la necessità di contattare il segnalatore per chiarimenti o follow-up ed inoltre non sono accettabili schede anonime. Qualora la fonte venga riportata come Altro deve essere specificato chiaramente la tipologia di segnalatore E importare inserire se disponibili dati quali e cellulare, al fine di permettere diverse soluzioni per contattare il segnalatore.
33
34
35
36
37
38 Importanza della qualità dei dati Finalità delle reazioni spontanee Consentire la precoce identificazione di segnali di allerta. A tale scopo è fondamentale poter contare su dati completi e qualitativamente validi. La qualità nell inserimento delle segnalazioni Ulteriori passi in avanti si stanno realizzando per migliorare le attività di analisi e di elaborazione dei dati, ma la tecnologia non basta ed il sistema restituisce nella forma e nei modi desiderati solo ciò che è stato in precedenza inserito. Il rischio dei dati incompleti Le schede incomplete o qualitativamente scadenti non consentono di effettuare una corretta valutazione del singolo caso, e rendono poco utili i rapporti di sicurezza inviati dalle Aziende Farmaceutiche
39
40 Grazie per l'attenzione
Allegato 1 - Guida alla compilazione della scheda di segnalazione di reazione avversa
 Allegato 1 - Guida alla compilazione della scheda di segnalazione di reazione avversa Vengono di seguito riportate alcune precisazioni, tratte dalle linee guida presenti nel sito dell'aifa relativamente
Allegato 1 - Guida alla compilazione della scheda di segnalazione di reazione avversa Vengono di seguito riportate alcune precisazioni, tratte dalle linee guida presenti nel sito dell'aifa relativamente
Ministero della Salute
 Ministero della Salute DECRETO: NUOVO MODELLO DI SEGNALAZIONE DI REAZIONE AVVERSA A FARMACI E VACCINI IL MINISTRO DELLA SALUTE VISTO il decreto legislativo. 18 febbraio 1997, n. 44; VISTO il decreto legislativo
Ministero della Salute DECRETO: NUOVO MODELLO DI SEGNALAZIONE DI REAZIONE AVVERSA A FARMACI E VACCINI IL MINISTRO DELLA SALUTE VISTO il decreto legislativo. 18 febbraio 1997, n. 44; VISTO il decreto legislativo
La segnalazione via web con la piattaforma Vigifarmaco. Ugo Moretti Centro Regionale di Farmacovigilanza del Veneto Università di Verona
 La segnalazione via web con la piattaforma Vigifarmaco Ugo Moretti Centro Regionale di Farmacovigilanza del Veneto Università di Verona Direttiva 2010/84/UE Articolo 107 bis 1. Ciascuno Stato membro registra
La segnalazione via web con la piattaforma Vigifarmaco Ugo Moretti Centro Regionale di Farmacovigilanza del Veneto Università di Verona Direttiva 2010/84/UE Articolo 107 bis 1. Ciascuno Stato membro registra
CEFPAS 24 Marzo 2015 Silvana Mansueto
 CENTRO DI FARMACOVIGILANZA Centro di consulenza ed informazione sugli effetti tossici da farmaci in gravide e neonati da erbe medicinali e dai prodotti da esse derivati A.O.U. "Policlinico - Vittorio Emanuele"
CENTRO DI FARMACOVIGILANZA Centro di consulenza ed informazione sugli effetti tossici da farmaci in gravide e neonati da erbe medicinali e dai prodotti da esse derivati A.O.U. "Policlinico - Vittorio Emanuele"
Scheda unica di segnalazione di sospetta reazione avversa
 DIPARTIMENTO ASSISTENZA FARMACEUTICA Scheda unica di segnalazione di sospetta reazione avversa Dott.ssa Elisa Iori Responsabile di farmacovigilanza Assicura la qualità dei dati delle schede Gestisce il
DIPARTIMENTO ASSISTENZA FARMACEUTICA Scheda unica di segnalazione di sospetta reazione avversa Dott.ssa Elisa Iori Responsabile di farmacovigilanza Assicura la qualità dei dati delle schede Gestisce il
La segnalazione spontanea di una sospetta reazione avversa consente di raccogliere importanti informazioni sulla sicurezza dei medicinali e di
 La segnalazione spontanea di una sospetta reazione avversa consente di raccogliere importanti informazioni sulla sicurezza dei medicinali e di individuare precocemente possibili segnali di allarme correlati
La segnalazione spontanea di una sospetta reazione avversa consente di raccogliere importanti informazioni sulla sicurezza dei medicinali e di individuare precocemente possibili segnali di allarme correlati
La nuova normativa in breve
 La nuova normativa in breve Le nuove disposizioni di legge in tema di sicurezza dei medicinali promettono di cambiare significativamente la farmacovigilanza Nel luglio 2012 sono entrate in vigore due nuove
La nuova normativa in breve Le nuove disposizioni di legge in tema di sicurezza dei medicinali promettono di cambiare significativamente la farmacovigilanza Nel luglio 2012 sono entrate in vigore due nuove
MINISTERO DELLA SALUTE DECRETO 12 Dicembre 2003 Nuovo modello di segnalazione di reazione avversa a farmaci e vaccini. Decreta:
 MINISTERO DELLA SALUTE DECRETO 12 Dicembre 2003 Nuovo modello di segnalazione di reazione avversa a farmaci e vaccini. IL MINISTRO DELLA SALUTE Visto il decreto legislativo 18 febbraio 1997, n. 44; Visto
MINISTERO DELLA SALUTE DECRETO 12 Dicembre 2003 Nuovo modello di segnalazione di reazione avversa a farmaci e vaccini. IL MINISTRO DELLA SALUTE Visto il decreto legislativo 18 febbraio 1997, n. 44; Visto
VigiFarmaco piattaforma informatica: nuova modalità per segnalare le reazioni avverse da farmaci.
 VigiFarmaco piattaforma informatica: nuova modalità per segnalare le reazioni avverse da farmaci. Azienda Ulss n.13 Mirano (Ve) Servizio farmaceutico territoriale Settembre 2015 https://vigifarmaco.it
VigiFarmaco piattaforma informatica: nuova modalità per segnalare le reazioni avverse da farmaci. Azienda Ulss n.13 Mirano (Ve) Servizio farmaceutico territoriale Settembre 2015 https://vigifarmaco.it
LA NUOVA PIATTAFORMA DELLA SEGNALAZIONE ONLINE DELLE REAZIONI AVVERSE: VIGIFARMACO
 CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari LA NUOVA PIATTAFORMA DELLA SEGNALAZIONE ONLINE DELLE REAZIONI AVVERSE:
CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari LA NUOVA PIATTAFORMA DELLA SEGNALAZIONE ONLINE DELLE REAZIONI AVVERSE:
Manuale d uso di VigiFarmaco: segnalazione online di sospette reazioni avverse a farmaci e vaccini
 Pagina 1 di 10 Manuale d uso di VigiFarmaco: segnalazione online di sospette reazioni avverse a farmaci e vaccini INTRODUZIONE Perché vanno segnalate le reazioni avverse dei farmaci? Al momento della commercializzazione
Pagina 1 di 10 Manuale d uso di VigiFarmaco: segnalazione online di sospette reazioni avverse a farmaci e vaccini INTRODUZIONE Perché vanno segnalate le reazioni avverse dei farmaci? Al momento della commercializzazione
FARMACOVIGILANZA PROCEDURA PER LA SEGNALAZIONE DELLE SOSPETTE REAZIONI AVVERSE DA FARMACI E VACCINI
 FARMACOVIGILANZA PROCEDURA PER LA SEGNALAZIONE DELLE SOSPETTE REAZIONI AVVERSE DA FARMACI E VACCINI Definizioni Farmacovigilanza: complesso delle attività correlate a rilevazione, gestione, comprensione
FARMACOVIGILANZA PROCEDURA PER LA SEGNALAZIONE DELLE SOSPETTE REAZIONI AVVERSE DA FARMACI E VACCINI Definizioni Farmacovigilanza: complesso delle attività correlate a rilevazione, gestione, comprensione
Direttiva 2010/84/UE
 Il Progetto web reporting Direttiva 2010/84/UE Articolo 107 bis 1. Ciascuno Stato membro registra tutti i sospetti effetti collaterali negativi che si verificano nel suo territorio e che gli vengono comunicati
Il Progetto web reporting Direttiva 2010/84/UE Articolo 107 bis 1. Ciascuno Stato membro registra tutti i sospetti effetti collaterali negativi che si verificano nel suo territorio e che gli vengono comunicati
SEGNALAZIONE DELLE SOSPETTE REAZIONI AVVERSE DA FARMACI. Un impegno etico per la. sicurezza del farmaco. Prevenire è meglio che curare
 Azienda U.S.L. 5 Spezzino U.O. Farmaceutica Territoriale Direttore Dr. Alessandro Sarteschi Prevenire è meglio che curare Le segnalazioni devono essere inviate a: Servizio Farmacovigilanza e Centro Documentazione
Azienda U.S.L. 5 Spezzino U.O. Farmaceutica Territoriale Direttore Dr. Alessandro Sarteschi Prevenire è meglio che curare Le segnalazioni devono essere inviate a: Servizio Farmacovigilanza e Centro Documentazione
Decreta: N.B.: E' OBBLIGATORIA SOLTANTO LA COMPILAZIONE DEI SEGUENTI CAMPI: 2; 4; 7; 8; 12; 22; 24; 25.
 GAZZETTA UFFICIALE N.210 DEL 9 SETTEMBRE 1997 MINISTERO DELLA SANITA' DECRETO 7 AGOSTO 1997 - SOSTITUZIONE DEL MODELLO A ALLEGATO AL DECRETO MINISTERIALE 20 APRILE 1991 RECANTE APPROVAZIONE DEI MODELLI
GAZZETTA UFFICIALE N.210 DEL 9 SETTEMBRE 1997 MINISTERO DELLA SANITA' DECRETO 7 AGOSTO 1997 - SOSTITUZIONE DEL MODELLO A ALLEGATO AL DECRETO MINISTERIALE 20 APRILE 1991 RECANTE APPROVAZIONE DEI MODELLI
CASO CLINICO. Arianna Deidda
 CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari CASO CLINICO Arianna Deidda Vaccini & Vaccinovigilanza Cagliari,
CENTRO REGIONALE FARMACOVIGILANZA - Regione Sardegna Unità Complessa di Farmacologia Clinica Azienda Ospedaliero Universitaria Cagliari CASO CLINICO Arianna Deidda Vaccini & Vaccinovigilanza Cagliari,
La nuova scheda informatica per l operatore sanitario e per il cittadino
 La Scheda di segnalazione di sospetta ADR e gli aspetti normativi Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia-Romagna AUSL Piacenza 20 e 22
La Scheda di segnalazione di sospetta ADR e gli aspetti normativi Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia-Romagna AUSL Piacenza 20 e 22
Dipartimento Interaziendale Farmaceutico UO Farmacia Ospedaliera. La gestione delle segnalazione di reazione avversa (ADR) a farmaco
 Pag. 1/6 La gestione delle segnalazione di reazione avversa (ADR) a farmaco 1. Lista di distribuzione...1 2. Emissione...1 3. Scopo...1 4. Campo di applicazione...1 5. Riferimenti...2 6. Definizioni...2
Pag. 1/6 La gestione delle segnalazione di reazione avversa (ADR) a farmaco 1. Lista di distribuzione...1 2. Emissione...1 3. Scopo...1 4. Campo di applicazione...1 5. Riferimenti...2 6. Definizioni...2
Sorveglianza sulle reazioni avverse da vaccino 24/05/2016
 Sorveglianza sulle reazioni avverse da vaccino 24/05/2016 Sorveglianza sulle reazioni avverse da vaccino Nell ambito dei Fondi AIFA 2008-2009 è stato condotto dal 2011 un progetto interregionale sulla
Sorveglianza sulle reazioni avverse da vaccino 24/05/2016 Sorveglianza sulle reazioni avverse da vaccino Nell ambito dei Fondi AIFA 2008-2009 è stato condotto dal 2011 un progetto interregionale sulla
SEGNALAZIONE SPONTANEA DI SOSPETTE REAZIONI AVVERSE A FARMACI GUIDA PER IL CITTADINO
 SEGNALAZIONE SPONTANEA DI SOSPETTE REAZIONI AVVERSE A FARMACI GUIDA PER IL CITTADINO Strumento semplice, pratico ed economico che ha come obiettivo la salute del paziente e consente di rilevare potenziali
SEGNALAZIONE SPONTANEA DI SOSPETTE REAZIONI AVVERSE A FARMACI GUIDA PER IL CITTADINO Strumento semplice, pratico ed economico che ha come obiettivo la salute del paziente e consente di rilevare potenziali
La nuova legislazione sulla Farmacovigilanza. Il nuovo flusso delle segnalazioni. Carmela Santuccio. Roma, 13 settembre 2012
 La nuova legislazione sulla Farmacovigilanza Il nuovo flusso delle segnalazioni Carmela Santuccio Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione
La nuova legislazione sulla Farmacovigilanza Il nuovo flusso delle segnalazioni Carmela Santuccio Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione
Il ruolo del Responsabile aziendale di farmacovigilanza, i flussi, le DDL e il supporto nella segnalazione
 Il ruolo del Responsabile aziendale di farmacovigilanza, i flussi, le DDL e il supporto nella segnalazione La cultura della farmacovigilanza per la sicurezza del paziente Bologna 26 gennaio, 2, 9 e 16
Il ruolo del Responsabile aziendale di farmacovigilanza, i flussi, le DDL e il supporto nella segnalazione La cultura della farmacovigilanza per la sicurezza del paziente Bologna 26 gennaio, 2, 9 e 16
IL FARMACISTA COME SEGNALATORE:
 Direzione Generale Sanità e Servizi Sociali IL FARMACISTA COME SEGNALATORE: la scheda, la corretta compilazione, esempi di segnalazioni di ADR CORSO PER FARMACISTI CONVENZIONATI: LA CULTURA DELLA FARMACOVIGILANZA
Direzione Generale Sanità e Servizi Sociali IL FARMACISTA COME SEGNALATORE: la scheda, la corretta compilazione, esempi di segnalazioni di ADR CORSO PER FARMACISTI CONVENZIONATI: LA CULTURA DELLA FARMACOVIGILANZA
La gestione degli eventi avversi e dei SAE
 Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
Prot. Az.Osp. n e Prot.Az.USL n Ferrara, Rif.: I, L 1/12
 Dipartimento Farmaceutico Interaziendale Università degli Studi di Ferrara COORDINAMENTO DI FARMACOVIGILANZA INTERAZIENDALE Prot. Az.Osp. n. 12175 e Prot.Az.USL n. 24666 Ferrara, 18.03.2008. Rif.: I, 3.5
Dipartimento Farmaceutico Interaziendale Università degli Studi di Ferrara COORDINAMENTO DI FARMACOVIGILANZA INTERAZIENDALE Prot. Az.Osp. n. 12175 e Prot.Az.USL n. 24666 Ferrara, 18.03.2008. Rif.: I, 3.5
Rev. N. 1 del 04/04/2019 Pagina 1
 PROCEDURA GESTIONALE PG ADF 001 Titolo: VIGILANZA SUI FARMACI, VACCINI, PRODOTTI A BASE DI PIANTE OFFICINALI E INTEGRATORI ALIMENTARI Rev. N. 1 del 04/04/2019 Pagina 1 AREA DEL FARMACO INDICE: Campo di
PROCEDURA GESTIONALE PG ADF 001 Titolo: VIGILANZA SUI FARMACI, VACCINI, PRODOTTI A BASE DI PIANTE OFFICINALI E INTEGRATORI ALIMENTARI Rev. N. 1 del 04/04/2019 Pagina 1 AREA DEL FARMACO INDICE: Campo di
PRINCIPIO ATTIVO NON SOGGETTO A NOTE AIFA PRESCRIVIBILE CON PIANO TERAPEUTICO
 PRINCIPIO ATTIVO NON SOGGETTO A NOTE AIFA PRESCRIVIBILE CON PIANO TERAPEUTICO Principio attivo Centri autorizzati Roflumilast (R03DX07) Centri ospedalieri o specialisti pneumologo, geriatra, internista,
PRINCIPIO ATTIVO NON SOGGETTO A NOTE AIFA PRESCRIVIBILE CON PIANO TERAPEUTICO Principio attivo Centri autorizzati Roflumilast (R03DX07) Centri ospedalieri o specialisti pneumologo, geriatra, internista,
-Applicazione della terminologia MeDRA alla codifica delle ADR -La FV negli studi osservazionali e nei registri dei farmaci sottoposti a monitoraggio
 Centro Regionale di Farmacovigilanza -Applicazione della terminologia MeDRA alla codifica delle ADR -La FV negli studi osservazionali e nei registri dei farmaci sottoposti a monitoraggio Seminario multi-tematico
Centro Regionale di Farmacovigilanza -Applicazione della terminologia MeDRA alla codifica delle ADR -La FV negli studi osservazionali e nei registri dei farmaci sottoposti a monitoraggio Seminario multi-tematico
VACCINO VIGILANZA E SEGNALAZIONE REAZIONI AVVERSE
 VACCINO VIGILANZA E SEGNALAZIONE REAZIONI AVVERSE Il concetto di farmacovigilanza si fonda sull assunto che nessun farmaco può essere considerato completamente sicuro ma risulta tale solo quando il rischio
VACCINO VIGILANZA E SEGNALAZIONE REAZIONI AVVERSE Il concetto di farmacovigilanza si fonda sull assunto che nessun farmaco può essere considerato completamente sicuro ma risulta tale solo quando il rischio
Roma, 3 settembre 2015 Al Presidente Dell Istituto Superiore di Sanità SEDE Oggetto: comunicazione di precisazioni non essenziali al Protocollo dello
 Roma, 3 settembre 2015 Al Presidente Dell Istituto Superiore di Sanità SEDE Oggetto: comunicazione di precisazioni non essenziali al Protocollo dello studio di coorte PITER (Piattaforma Italiana per lo
Roma, 3 settembre 2015 Al Presidente Dell Istituto Superiore di Sanità SEDE Oggetto: comunicazione di precisazioni non essenziali al Protocollo dello studio di coorte PITER (Piattaforma Italiana per lo
Centro Regionale di Farmacovigilanza. Mauro Melis Dipartimento di Scienze Mediche e Chirurgiche Unità di Farmacologia Università di Bologna
 Centro Regionale di Farmacovigilanza Mauro Melis Dipartimento di Scienze Mediche e Chirurgiche Unità di Farmacologia Università di Bologna Delineato un processo di monitoraggio continuo, fatto di analisi
Centro Regionale di Farmacovigilanza Mauro Melis Dipartimento di Scienze Mediche e Chirurgiche Unità di Farmacologia Università di Bologna Delineato un processo di monitoraggio continuo, fatto di analisi
Il ruolo del Responsabile aziendale di Farmacovigilanza
 Il ruolo del Responsabile aziendale di Farmacovigilanza Bologna, 8 novembre 2013 Dott.ssa Mirna Magnani La farmacovigilanza ha 4 obiettivi principali: 1. riconoscere, il pi rapidamente possibile, nuove
Il ruolo del Responsabile aziendale di Farmacovigilanza Bologna, 8 novembre 2013 Dott.ssa Mirna Magnani La farmacovigilanza ha 4 obiettivi principali: 1. riconoscere, il pi rapidamente possibile, nuove
IL RUOLO DEL RESPONSABILE AZIENDALE DI FARMACOVIGILANZA E IL SUPPORTO NELLA SEGNALAZIONE A LIVELLO LOCALE
 Corso regionale di farmacovigilanza per farmacisti convenzionati: LA CULTURA DELLA FARMACOVIGILANZA PER LA SICUREZZA DEL PAZIENTE Piacenza, 29 aprile 2010 IL RUOLO DEL RESPONSABILE AZIENDALE DI FARMACOVIGILANZA
Corso regionale di farmacovigilanza per farmacisti convenzionati: LA CULTURA DELLA FARMACOVIGILANZA PER LA SICUREZZA DEL PAZIENTE Piacenza, 29 aprile 2010 IL RUOLO DEL RESPONSABILE AZIENDALE DI FARMACOVIGILANZA
Guida pratica per la segnalazione on-line di sospette Reazioni Avverse a farmaci e a vaccini
 Guida pratica per la segnalazione on-line di sospette Reazioni Avverse a farmaci e a vaccini Tale guida rappresenta un supporto per agevolare e incoraggiare gli operatori sanitari e i cittadini alla segnalazione
Guida pratica per la segnalazione on-line di sospette Reazioni Avverse a farmaci e a vaccini Tale guida rappresenta un supporto per agevolare e incoraggiare gli operatori sanitari e i cittadini alla segnalazione
Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013
 Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Servizio FV Interno OEI : dott.ssa MT Calcagno, dott.ssa M.Torsegno Indice - Definizioni di Farmacovigilanza
Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Servizio FV Interno OEI : dott.ssa MT Calcagno, dott.ssa M.Torsegno Indice - Definizioni di Farmacovigilanza
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica
 Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
Vademecum per il monitoraggio della Legge n. 648 del 23/12/1996 Aggiornamento Aprile 2018
 Vademecum per il monitoraggio della Legge n. 648 del 23/12/1996 Aggiornamento Aprile 2018 1. Per quali farmaci è previsto il monitoraggio ai sensi della L. n. 648/96? La Legge n.648 del 23 Dicembre 1996
Vademecum per il monitoraggio della Legge n. 648 del 23/12/1996 Aggiornamento Aprile 2018 1. Per quali farmaci è previsto il monitoraggio ai sensi della L. n. 648/96? La Legge n.648 del 23 Dicembre 1996
Guida all uso del report: Sospette Reazioni Avverse (Casa Farmaceutica)
 Guida all uso del report: Sospette Reazioni Avverse (Casa Farmaceutica) Versione 1.0 Giugno 2012 1 Indice Suggerimenti per il management del computer...3 Sospette reazioni avverse...5 Report Sospette Reazioni
Guida all uso del report: Sospette Reazioni Avverse (Casa Farmaceutica) Versione 1.0 Giugno 2012 1 Indice Suggerimenti per il management del computer...3 Sospette reazioni avverse...5 Report Sospette Reazioni
Elementi di vigilanza nella gestione dei gas medicinali
 La gestione sanitaria dei gas medicinali Corso per formatori delle Aziende sanitarie 15 novembre 2012 e 17 gennaio 2013 Elementi di vigilanza nella gestione dei gas medicinali Elisa SANGIORGI Servizio
La gestione sanitaria dei gas medicinali Corso per formatori delle Aziende sanitarie 15 novembre 2012 e 17 gennaio 2013 Elementi di vigilanza nella gestione dei gas medicinali Elisa SANGIORGI Servizio
Farmacovigilanza. Obbligo segnalazioni avverse entro 48h. Il Decreto in Gazzetta Ufficiale
 Farmacovigilanza. Obbligo segnalazioni avverse entro 48h. Il Decreto in Gazzetta Ufficiale Il provvedimento recepisce le direttive europee sulla farmacovigilanza. Tempi ridotti a 36 ore per segnalazione
Farmacovigilanza. Obbligo segnalazioni avverse entro 48h. Il Decreto in Gazzetta Ufficiale Il provvedimento recepisce le direttive europee sulla farmacovigilanza. Tempi ridotti a 36 ore per segnalazione
a cura della Dott.ssa Cinzia Scolari
 pag 5 8 a cura della Dott.ssa Cinzia Scolari pag 5 Giuseppe MARZULLI Direttore Sanitario A.O. Bolognini Seriate Avolte ho l impressione che ci sia una convinzione latente sulla non pericolosità dei medicinali
pag 5 8 a cura della Dott.ssa Cinzia Scolari pag 5 Giuseppe MARZULLI Direttore Sanitario A.O. Bolognini Seriate Avolte ho l impressione che ci sia una convinzione latente sulla non pericolosità dei medicinali
VIGER LA FARMACOVIGILANZA IN GERIATRIA. Progetto Regionale Farmacovigilanza
 VIGER LA FARMACOVIGILANZA IN GERIATRIA Progetto Regionale Farmacovigilanza COS È IL PROGETTO VIGER Il progetto VIGER (Vigilanza in Geriatria) è un progetto di farmacovigilanza finalizzato alla valutazione
VIGER LA FARMACOVIGILANZA IN GERIATRIA Progetto Regionale Farmacovigilanza COS È IL PROGETTO VIGER Il progetto VIGER (Vigilanza in Geriatria) è un progetto di farmacovigilanza finalizzato alla valutazione
FARMACOVIGILANZA SEGNALAZIONE DI REAZIONI AVVERSE RICONDUCIBILI ALL'USO DI MEDICINALI.
 Caf Latium - Professione & Sviluppo Marzo 2006. FARMACOVIGILANZA SEGNALAZIONE DI REAZIONI AVVERSE RICONDUCIBILI ALL'USO DI MEDICINALI. I farmacisti (come operatori sanitari, oltre ai medici) sono tenuti
Caf Latium - Professione & Sviluppo Marzo 2006. FARMACOVIGILANZA SEGNALAZIONE DI REAZIONI AVVERSE RICONDUCIBILI ALL'USO DI MEDICINALI. I farmacisti (come operatori sanitari, oltre ai medici) sono tenuti
Corso di aggiornamento in FARMACOVIGILANZA. Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013
 Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Farmacovigilanza La scienza e le attività collegate alla identificazione, valutazione, conoscenza
Corso di aggiornamento in FARMACOVIGILANZA Ospedale Evangelico Internazionale Genova, 12 e 17 Giugno 2013 Farmacovigilanza La scienza e le attività collegate alla identificazione, valutazione, conoscenza
RAPPORTO DI FARMACOVIGILANZA
 RAPPORTO DI FARMACOVIGILANZA REGIONE PIEMONTE A cura di Settore Assistenza Farmaceutica, Integrativa e Protesica Assessorato alla Sanità della Regione Piemonte Centro Regionale di Farmacovigilanza della
RAPPORTO DI FARMACOVIGILANZA REGIONE PIEMONTE A cura di Settore Assistenza Farmaceutica, Integrativa e Protesica Assessorato alla Sanità della Regione Piemonte Centro Regionale di Farmacovigilanza della
RIPAM ANAC PER L ASSUNZIONE DI 35 UNITA DI PERSONALE A TEMPO INDETERMITATO
 RIPAM ANAC PER L ASSUNZIONE DI 35 UNITA DI PERSONALE A TEMPO INDETERMITATO DA INQUADRARE NELLA CATEGORIA A - PARAMETRO RETRIBUTIVO F1 GUIDA PER LA COMPILAZIONE DELLA DOMANDA ONLINE Per ottimizzare i tempi
RIPAM ANAC PER L ASSUNZIONE DI 35 UNITA DI PERSONALE A TEMPO INDETERMITATO DA INQUADRARE NELLA CATEGORIA A - PARAMETRO RETRIBUTIVO F1 GUIDA PER LA COMPILAZIONE DELLA DOMANDA ONLINE Per ottimizzare i tempi
La nuova normativa di Farmacovigilanza [Regolamento Unione Europea N. 1235/2010 e Direttiva 2010/84/UE] in vigore in Italia da Luglio 2012 introduce
![La nuova normativa di Farmacovigilanza [Regolamento Unione Europea N. 1235/2010 e Direttiva 2010/84/UE] in vigore in Italia da Luglio 2012 introduce La nuova normativa di Farmacovigilanza [Regolamento Unione Europea N. 1235/2010 e Direttiva 2010/84/UE] in vigore in Italia da Luglio 2012 introduce](/thumbs/65/53226195.jpg) La normativa europea in materia di farmacovigilanza è stata modificata con l adozione nel 2010, del Regolamento UE 1235/2010, la cui applicazione è operativa dal 2 luglio 2012, e della Direttiva 2010/84/UE,
La normativa europea in materia di farmacovigilanza è stata modificata con l adozione nel 2010, del Regolamento UE 1235/2010, la cui applicazione è operativa dal 2 luglio 2012, e della Direttiva 2010/84/UE,
AVVIO DI FAITH. NOME UTENTE: Viene proposto l ultimo utente utilizzato; nella versione Dimostrativa troverete Amministratore ;
 AVVIO DI FAITH Cliccare sull icona presente sul desktop del Vostro computer. A questo punto verrà visualizzata la finestra di autenticazione dove inserire: NOME UTENTE: Viene proposto l ultimo utente utilizzato;
AVVIO DI FAITH Cliccare sull icona presente sul desktop del Vostro computer. A questo punto verrà visualizzata la finestra di autenticazione dove inserire: NOME UTENTE: Viene proposto l ultimo utente utilizzato;
PRESIDENZA DEL CONSIGLIO DEI MINISTRI SCUOLA NAZIONALE DELL AMMINISTRAZIONE
 PRESIDENZA DEL CONSIGLIO DEI MINISTRI SCUOLA NAZIONALE DELL AMMINISTRAZIONE CONCORSO PUBBLICO, PER ESAMI, PER L AMMISSIONE DI 148 ALLIEVI AL CORSO- CONCORSO SELETTIVO DI FORMAZIONE DIRIGENZIALE PER IL
PRESIDENZA DEL CONSIGLIO DEI MINISTRI SCUOLA NAZIONALE DELL AMMINISTRAZIONE CONCORSO PUBBLICO, PER ESAMI, PER L AMMISSIONE DI 148 ALLIEVI AL CORSO- CONCORSO SELETTIVO DI FORMAZIONE DIRIGENZIALE PER IL
Guida rapida per l utilizzatore Browser
 ANticoagulant THEraphy MAnagement Guida rapida per l utilizzatore Browser Copyright 2010 Instrumentation Laboratory SpA Le informazioni contenute in questo documento sono proprietà di Instrumentation Laboratory
ANticoagulant THEraphy MAnagement Guida rapida per l utilizzatore Browser Copyright 2010 Instrumentation Laboratory SpA Le informazioni contenute in questo documento sono proprietà di Instrumentation Laboratory
PROCEDURA DI ACCESSO IN CONDIZIONI ORDINARIE
 MODELLO DI PERCORSO REGIONALE UNIFICATO PER L ACCESSO ALL UTILIZZO TERAPEUTICO DI MEDICINALI SOTTOPOSTI A SPERIMENTAZIONE CLINICA (EXPANDED-ACCESS/USO COMPASSIONEVOLE) Il protocollo da sottoporre all impresa
MODELLO DI PERCORSO REGIONALE UNIFICATO PER L ACCESSO ALL UTILIZZO TERAPEUTICO DI MEDICINALI SOTTOPOSTI A SPERIMENTAZIONE CLINICA (EXPANDED-ACCESS/USO COMPASSIONEVOLE) Il protocollo da sottoporre all impresa
Sistema Gestionale Bando Ordinanza 544 (rendicontazione)
 Sistema Gestionale Bando Ordinanza 544 (rendicontazione) Guida al Sistema Servizi Informatici Versione 23 Sommario della presentazione Il sistema informatico per la gestione delle domande La pagina iniziale
Sistema Gestionale Bando Ordinanza 544 (rendicontazione) Guida al Sistema Servizi Informatici Versione 23 Sommario della presentazione Il sistema informatico per la gestione delle domande La pagina iniziale
NEL PIENO DELLE DANZE: FARMACOVIGILANZA. Veronica Franchina
 CORSO INTRODUZIONE ALLA RICERCA CLINICA MILANO 14-15 GIUGNO 2018 NEL PIENO DELLE DANZE: FARMACOVIGILANZA Veronica Franchina Coordinatore di ricerca clinica, U.O.C. Oncologia Medica A.O. Papardo Messina
CORSO INTRODUZIONE ALLA RICERCA CLINICA MILANO 14-15 GIUGNO 2018 NEL PIENO DELLE DANZE: FARMACOVIGILANZA Veronica Franchina Coordinatore di ricerca clinica, U.O.C. Oncologia Medica A.O. Papardo Messina
VigiFarmaco: la segnalazione online delle reazioni avverse da farmaco
 VigiFarmaco: la segnalazione online delle reazioni avverse da farmaco Introduzione...2 Che cos è la farmacovigilanza?...2 Che cos è la segnalazione spontanea?...2 Che cos è il nuovo sistema di segnalazione
VigiFarmaco: la segnalazione online delle reazioni avverse da farmaco Introduzione...2 Che cos è la farmacovigilanza?...2 Che cos è la segnalazione spontanea?...2 Che cos è il nuovo sistema di segnalazione
FAQ per la gestione delle segnalazioni nell ambito della Rete Nazionale di Farmacovigilanza
 FAQ per la gestione delle segnalazioni nell ambito della Rete Nazionale di Farmacovigilanza Il 22 novembre 2017 sono entrate in vigore le nuove disposizioni relative al simplified electronic reporting
FAQ per la gestione delle segnalazioni nell ambito della Rete Nazionale di Farmacovigilanza Il 22 novembre 2017 sono entrate in vigore le nuove disposizioni relative al simplified electronic reporting
SCHEDA DI SEGNALAZIONE ALLE AUTORITA COMPETENTI DI SOSPETTA DIMINUZIONE DI EFFICACIA
 SCHEDA DI SEGNALAZIONE ALLE AUTORITA COMPETENTI DI SOSPETTA DIMINUZIONE DI EFFICACIA DATI IDENTIFICATIVI DELL AUTORE DELLA SEGNALAZIONE (*) Nome e cognome Indirizzo Telefono e-mail Qualifica/occupazione
SCHEDA DI SEGNALAZIONE ALLE AUTORITA COMPETENTI DI SOSPETTA DIMINUZIONE DI EFFICACIA DATI IDENTIFICATIVI DELL AUTORE DELLA SEGNALAZIONE (*) Nome e cognome Indirizzo Telefono e-mail Qualifica/occupazione
REGISTRO CAMPAGNA VACCINAZIONE ANTINFLUENZALE MANUALE UTENTE : MMG - PDF - Operatori DPM
 REGISTRO CAMPAGNA VACCINAZIONE ANTINFLUENZALE MANUALE UTENTE : MMG - PDF - Operatori DPM 1 ver.1.2 - ottobre 2016 Sommario pag. 3 pag. 5 pag. 6 pag. 14 Accesso al portale Funzioni del Portale Registrazione
REGISTRO CAMPAGNA VACCINAZIONE ANTINFLUENZALE MANUALE UTENTE : MMG - PDF - Operatori DPM 1 ver.1.2 - ottobre 2016 Sommario pag. 3 pag. 5 pag. 6 pag. 14 Accesso al portale Funzioni del Portale Registrazione
LA RETE NAZIONALE DI FARMACOVIGILANZA
 Primo Corso Regionale di Farmacovigilanza LA RETE NAZIONALE DI FARMACOVIGILANZA Dott.ssa Carmela Santuccio AIFA - Ufficio Farmacovigilanza Bologna 21 Febbraio 2008 Rete Nazionale di Farmacovigilanza: sistema
Primo Corso Regionale di Farmacovigilanza LA RETE NAZIONALE DI FARMACOVIGILANZA Dott.ssa Carmela Santuccio AIFA - Ufficio Farmacovigilanza Bologna 21 Febbraio 2008 Rete Nazionale di Farmacovigilanza: sistema
Normativa Regolamento UE 1235/2010 Direttiva 2010/84/UE
 Implementazione delle nuove linee guida dell AIFA e principali modifiche introdotte dalla nuova normativa europea di Farmacovigilanza CEFPAS 24 marzo 2015 Claudia La Cavera Normativa Regolamento UE 1235/2010
Implementazione delle nuove linee guida dell AIFA e principali modifiche introdotte dalla nuova normativa europea di Farmacovigilanza CEFPAS 24 marzo 2015 Claudia La Cavera Normativa Regolamento UE 1235/2010
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria
 Corso di formazione sul campo a cura della sezione regionale SIFO Liguria DIPARTIMENTO DEL FARMACO S.C. FARMACEUTICA Settore Assistenza Farmaceutica Pec : farmacia@pec.asl4.liguria.it Email :farm.terr@asl4.liguria.it
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria DIPARTIMENTO DEL FARMACO S.C. FARMACEUTICA Settore Assistenza Farmaceutica Pec : farmacia@pec.asl4.liguria.it Email :farm.terr@asl4.liguria.it
La Farmacovigilanza: coinvolgimento degli operatori delle strutture sanitarie private della Regione Emilia-Romagna"
 La Farmacovigilanza: coinvolgimento degli operatori delle strutture sanitarie private della Regione Emilia-Romagna" Daniela Carati Centro Regionale di Farmacovigilanza Servizio Politica del Farmaco (Responsabile
La Farmacovigilanza: coinvolgimento degli operatori delle strutture sanitarie private della Regione Emilia-Romagna" Daniela Carati Centro Regionale di Farmacovigilanza Servizio Politica del Farmaco (Responsabile
AVVISO PUBBLICO SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA B PRESENTAZIONE DELLA DOMANDA CITTADINO
 AVVISO PUBBLICO SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA B PRESENTAZIONE DELLA DOMANDA CITTADINO FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante
AVVISO PUBBLICO SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA B PRESENTAZIONE DELLA DOMANDA CITTADINO FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante
SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA A FASI DA ESEGUIRE ON-LINE
 SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA A PRESENTAZIONE DELLA DOMANDA DELEGATO FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante apposito link presente
SELEZIONE DEI BENEFICIARI DEL PROGRAMMA REDDITO MINIMO DI INSERIMENTO CATEGORIA A PRESENTAZIONE DELLA DOMANDA DELEGATO FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante apposito link presente
Prot. n Frosinone,31/01/2018 FARMAINFORMA. Informazione sui Farmaci e la Farmacovigilanza Numero Speciale Gennaio 2018
 Prot. n. 10373 Frosinone,31/01/2018 FARMAINFORMA Informazione sui Farmaci e la Farmacovigilanza Numero Speciale Gennaio 2018 La numerosità delle segnalazioni di ADR è un criterio cardine per definire un
Prot. n. 10373 Frosinone,31/01/2018 FARMAINFORMA Informazione sui Farmaci e la Farmacovigilanza Numero Speciale Gennaio 2018 La numerosità delle segnalazioni di ADR è un criterio cardine per definire un
Piano di eliminazione del Morbillo e della Rosolia Congenita. Analisi dei dati e monitoraggio del Piano e dei suoi risultati
 Piano di eliminazione del Morbillo e della Rosolia Congenita Analisi dei dati e monitoraggio del Piano e dei suoi risultati 1 Analizzare i dati: Usare l informazione per decidere bene Unità di analisi:
Piano di eliminazione del Morbillo e della Rosolia Congenita Analisi dei dati e monitoraggio del Piano e dei suoi risultati 1 Analizzare i dati: Usare l informazione per decidere bene Unità di analisi:
La Rete Nazionale di Farmacovigilanza e gli aspetti normativi
 La Rete Nazionale di Farmacovigilanza e gli aspetti normativi Andrea Marchi Servizio Politica del Farmaco Direzione Generale Sanità e Politiche Sociali Regione Emilia Romagna Bologna 26 gennaio e 2, 9,
La Rete Nazionale di Farmacovigilanza e gli aspetti normativi Andrea Marchi Servizio Politica del Farmaco Direzione Generale Sanità e Politiche Sociali Regione Emilia Romagna Bologna 26 gennaio e 2, 9,
Tutorial per la raccolta dati anagrafici degli atleti iscritti al C.F.T.
 Tutorial per la raccolta dati anagrafici degli atleti iscritti al C.F.T. Raccolta dati anagrafici degli atleti iscritti alle attività dei CFT Il Centro Federale Territoriale chiede alle società di appartenenza
Tutorial per la raccolta dati anagrafici degli atleti iscritti al C.F.T. Raccolta dati anagrafici degli atleti iscritti alle attività dei CFT Il Centro Federale Territoriale chiede alle società di appartenenza
La ricetta veterinaria informatizzata nell allevamento bovino. Ferrara, 21/06/2018
 La ricetta veterinaria informatizzata nell allevamento bovino Ferrara, 21/06/2018 La sperimentazione negli allevamenti bovini della Regione E-R Veterinari LP che hanno partecipato alla fase sperimentale
La ricetta veterinaria informatizzata nell allevamento bovino Ferrara, 21/06/2018 La sperimentazione negli allevamenti bovini della Regione E-R Veterinari LP che hanno partecipato alla fase sperimentale
FASI DA ESEGUIRE ON-LINE
 FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante apposito link presente sul portale della Regione Basilicata e rilascio delle credenziali di accesso necessarie per procedere alla candidatura
FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante apposito link presente sul portale della Regione Basilicata e rilascio delle credenziali di accesso necessarie per procedere alla candidatura
GESTIONE DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA A FARMACI (ADR), DEI DIFETTI E DELLE NOTE INFORMATIVE IMPORTANTI SUI FARMACI
 PA.DF.01 0 1 di 33 PROCEDURA AZIENDALE GESTIONE DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA A FARMACI (ADR), DEI DIFETTI E DELLE NOTE INFORMATIVE IMPORTANTI SUI FARMACI PA.DF.01 0 2 di 33 INDICE PREMESSA
PA.DF.01 0 1 di 33 PROCEDURA AZIENDALE GESTIONE DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA A FARMACI (ADR), DEI DIFETTI E DELLE NOTE INFORMATIVE IMPORTANTI SUI FARMACI PA.DF.01 0 2 di 33 INDICE PREMESSA
FARMACOVIGILANZA PICCOLO IMPEGNO PER ACCRESCERE LA SICUREZZA DEI FARMACI
 Sede legale: Via G. Cusmano, 24 90141 PALERMO C.F. e P. I.V.A.: 05841760829 Dipartimento Farmaceutico Via Pindemonte 88 90128 PALERMO dipfarmaco@asppalermo.org FARMACOVIGILANZA PICCOLO IMPEGNO PER ACCRESCERE
Sede legale: Via G. Cusmano, 24 90141 PALERMO C.F. e P. I.V.A.: 05841760829 Dipartimento Farmaceutico Via Pindemonte 88 90128 PALERMO dipfarmaco@asppalermo.org FARMACOVIGILANZA PICCOLO IMPEGNO PER ACCRESCERE
REGIONE SARDEGNA CONCORSO UNICO PER L ASSUNZIONE DI 20 DIRIGENTI A TEMPO INDETERMINATO
 REGIONE SARDEGNA CONCORSO UNICO PER L ASSUNZIONE DI 20 DIRIGENTI A TEMPO INDETERMINATO DECRETO N.P. 27540/48 DEL 28 SETTEMBRE 2017 GUIDA PER LA COMPILAZIONE DELLA DOMANDA ONLINE Per ottimizzare i tempi
REGIONE SARDEGNA CONCORSO UNICO PER L ASSUNZIONE DI 20 DIRIGENTI A TEMPO INDETERMINATO DECRETO N.P. 27540/48 DEL 28 SETTEMBRE 2017 GUIDA PER LA COMPILAZIONE DELLA DOMANDA ONLINE Per ottimizzare i tempi
Dott. Roberto Baldini Dirigente Farmacista Responsabile S.S. Gestione Dispositivi Medici U. O. C. Farmacia IRCCS A.O.U. San Martino IST Genova
 Corso aggiornamento sezione regionale SIFO Liguria Dott. Roberto Baldini Dirigente Farmacista Responsabile S.S. Gestione Dispositivi Medici U. O. C. Farmacia IRCCS A.O.U. San Martino IST Genova Corso SIFO
Corso aggiornamento sezione regionale SIFO Liguria Dott. Roberto Baldini Dirigente Farmacista Responsabile S.S. Gestione Dispositivi Medici U. O. C. Farmacia IRCCS A.O.U. San Martino IST Genova Corso SIFO
Farmacovigilanza e Vigilanza Dispositivi medici
 Farmacovigilanza e Vigilanza Dispositivi medici Vigilanza Pre e post market Farmacovigilanza e Vigilanza Dispositivi Medici Partecipanti Pazienti ed utilizzatori, segnalatori, promotori commerciali e non
Farmacovigilanza e Vigilanza Dispositivi medici Vigilanza Pre e post market Farmacovigilanza e Vigilanza Dispositivi Medici Partecipanti Pazienti ed utilizzatori, segnalatori, promotori commerciali e non
Integrazione con i servizi di cooperazione operativa della REGIONE LAZIO- ADD-ON MESIR
 DATI PRODUTTORE Via Di Collodi, 6/C 50141 Firenze www.millewin.it COME CONTATTARE L ASSISTENZA TECNICA Dal Lunedì al Venerdì dalle ore 8.30 alle ore 19.30, con orario continuato Sabato dalle ore 9.00 alle
DATI PRODUTTORE Via Di Collodi, 6/C 50141 Firenze www.millewin.it COME CONTATTARE L ASSISTENZA TECNICA Dal Lunedì al Venerdì dalle ore 8.30 alle ore 19.30, con orario continuato Sabato dalle ore 9.00 alle
ANDAMENTO DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA AI FARMACI NELLA ASL DI LATINA
 ANDAMENTO DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA AI FARMACI NELLA ASL DI LATINA PRIMO SEMESTRE 2017 USD Assistenza Farmaceutica e Territoriale Responsabile: Dott.ssa Loredana Arenare Farmacisti
ANDAMENTO DELLA SEGNALAZIONE DI SOSPETTA REAZIONE AVVERSA AI FARMACI NELLA ASL DI LATINA PRIMO SEMESTRE 2017 USD Assistenza Farmaceutica e Territoriale Responsabile: Dott.ssa Loredana Arenare Farmacisti
Invio promemoria ricetta dematerializzata al paziente
 Invio promemoria ricetta dematerializzata al paziente in FastAmb Medico di Famiglia BestSoft SOFTWARE IN SANITÀ Via Bono Cairoli 28/A - 20127 Milano (MI) Help desk: 02 29529140 Num. Verde da fisso: 800
Invio promemoria ricetta dematerializzata al paziente in FastAmb Medico di Famiglia BestSoft SOFTWARE IN SANITÀ Via Bono Cairoli 28/A - 20127 Milano (MI) Help desk: 02 29529140 Num. Verde da fisso: 800
Comunicazioni Obbligatorie
 Comunicazioni Obbligatorie Sistema informatico on-line di supporto Guida alla compilazione del form di accreditamento 1 Indice dei contenuti 1. GUIDA ALL ACCREDITAMENTO... 3 1.1. CREDENZIALI DI ACCESSO
Comunicazioni Obbligatorie Sistema informatico on-line di supporto Guida alla compilazione del form di accreditamento 1 Indice dei contenuti 1. GUIDA ALL ACCREDITAMENTO... 3 1.1. CREDENZIALI DI ACCESSO
La cartella clinica informatizzata:
 La cartella clinica informatizzata: come cambia il management sanitario La cartella clinica informatizzata Presentazione e gestione di casi (lezione interattiva) Tricase, 14/02/2014 Trasparenza Illustrerò
La cartella clinica informatizzata: come cambia il management sanitario La cartella clinica informatizzata Presentazione e gestione di casi (lezione interattiva) Tricase, 14/02/2014 Trasparenza Illustrerò
SPUNTI DI FARMACOVIGILANZA
 SPUNTI DI FARMACOVIGILANZA farmacoviilanza 10/14/2009 1 Farmacoviilanza Raccolta sistematica ed analisi di un insieme articolato di informazioni Coinvole a diversi livelli tutta la comunità: pazienti,
SPUNTI DI FARMACOVIGILANZA farmacoviilanza 10/14/2009 1 Farmacoviilanza Raccolta sistematica ed analisi di un insieme articolato di informazioni Coinvole a diversi livelli tutta la comunità: pazienti,
GUIDA ALLA CANDIDATURA
 GUIDA ALLA CANDIDATURA BANDO CONCORSO PUBBLICO PER TITOLI ED ESAMI PER IL CONFERIMENTO DI N. 2 POSTI A TEMPO INDETERMINATO, IN QUALITA DI AUSILIARIO DEL TRAFFICO - CATEGORIA C1 DEL CCNL AUTORIMESSE VIGENTE.
GUIDA ALLA CANDIDATURA BANDO CONCORSO PUBBLICO PER TITOLI ED ESAMI PER IL CONFERIMENTO DI N. 2 POSTI A TEMPO INDETERMINATO, IN QUALITA DI AUSILIARIO DEL TRAFFICO - CATEGORIA C1 DEL CCNL AUTORIMESSE VIGENTE.
REGIONE PUGLIA CENTRO REGIONALE PER LA FARMACOVIGILANZA
 REGIONE PUGLIA CENTRO REGIONALE PER LA FARMACOVIGILANZA Dati sulla segnalazione spontanea delle reazioni avverse a farmaci (ADR) in Regione Puglia nell anno 2016 Nella presente relazione vengono illustrati
REGIONE PUGLIA CENTRO REGIONALE PER LA FARMACOVIGILANZA Dati sulla segnalazione spontanea delle reazioni avverse a farmaci (ADR) in Regione Puglia nell anno 2016 Nella presente relazione vengono illustrati
Istruzioni per l estrazione dell elenco pazienti per i quali compilare le schede di valutazione della fragilità... 2
 Sommario Istruzioni per l estrazione dell elenco pazienti per i quali compilare le schede di valutazione della fragilità... 2 Compilazione Schede di Valutazione della Fragilità:... 6 Istruzioni per l estrazione
Sommario Istruzioni per l estrazione dell elenco pazienti per i quali compilare le schede di valutazione della fragilità... 2 Compilazione Schede di Valutazione della Fragilità:... 6 Istruzioni per l estrazione
PROCEDURA MODELLO UNICO: PRESCRIZIONE MANUALE OPERATIVO
 PROCEDURA MODELLO UNICO: PRESCRIZIONE MANUALE OPERATIVO 2 PROCEDURA MODELLO UNICO: PRESCRIZIONE SOMMARIO ACCESSO AL SISTEMA SANIARP... 3 PRESCRIZIONE DEL PIANO TERAPEUTICO... 5 Ricerca del paziente ed
PROCEDURA MODELLO UNICO: PRESCRIZIONE MANUALE OPERATIVO 2 PROCEDURA MODELLO UNICO: PRESCRIZIONE SOMMARIO ACCESSO AL SISTEMA SANIARP... 3 PRESCRIZIONE DEL PIANO TERAPEUTICO... 5 Ricerca del paziente ed
PRESIDENZA DEL CONSIGLIO DEI MINISTRI
 PRESIDENZA DEL CONSIGLIO DEI MINISTRI CONCORSO PUBBLICO, PER TITOLI E PER ESAMI, PER IL RECLUTAMENTO DI N. 12 (DODICI) UNITÀ DI PERSONALE NON DIRIGENZIALE A TEMPO INDETERMINATO, DI CUI N. 2 (DUE) PER IL
PRESIDENZA DEL CONSIGLIO DEI MINISTRI CONCORSO PUBBLICO, PER TITOLI E PER ESAMI, PER IL RECLUTAMENTO DI N. 12 (DODICI) UNITÀ DI PERSONALE NON DIRIGENZIALE A TEMPO INDETERMINATO, DI CUI N. 2 (DUE) PER IL
Casi clinici. Esempi dalla realtà di Rimini. Presentazione di alcuni casi clinici (esempi dalla realtà di Rimini)
 Casi clinici Università di Bologna CReVIF Dipartimento di Farmacologia Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia- Romagna AUSL Piacenza
Casi clinici Università di Bologna CReVIF Dipartimento di Farmacologia Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia- Romagna AUSL Piacenza
Centri Federali Territoriali. Tutorial per le Società Raccolta dati anagrafici degli atleti iscritti al C.F.T.
 Centri Federali Territoriali Tutorial per le Società Raccolta dati anagrafici degli atleti iscritti al C.F.T. Raccolta dati anagrafici degli atleti iscritti alle attività dei CFT Il Centro Federale Territoriale
Centri Federali Territoriali Tutorial per le Società Raccolta dati anagrafici degli atleti iscritti al C.F.T. Raccolta dati anagrafici degli atleti iscritti alle attività dei CFT Il Centro Federale Territoriale
L utilizzo di uno schema scritto è raccomandato e agevola gli operatori che devono effettuare l indagine anamnestica.
 f. ANAMNESI La raccolta dell anamnesi è un passo essenziale in ogni atto medico, ma soprattutto prima di intraprendere la somministrazione di un vaccino. L anamnesi ha lo scopo di mettere in evidenza alcuni
f. ANAMNESI La raccolta dell anamnesi è un passo essenziale in ogni atto medico, ma soprattutto prima di intraprendere la somministrazione di un vaccino. L anamnesi ha lo scopo di mettere in evidenza alcuni
PRESENTAZIONE DOMANDA
 PRESENTAZIONE DOMANDA Bando Garanzia Giovani Disabili (GGD) 2015-2017 Istituzione dell Elenco dei Soggetti Attuatori dei servizi per il lavoro previsti dalla Garanzia Giovani Disabili Fondo Regionale Disabili
PRESENTAZIONE DOMANDA Bando Garanzia Giovani Disabili (GGD) 2015-2017 Istituzione dell Elenco dei Soggetti Attuatori dei servizi per il lavoro previsti dalla Garanzia Giovani Disabili Fondo Regionale Disabili
MODELLO 4 - compilazione modello 4
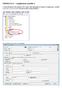 MODELLO 4 - compilazione modello 4 L informatizzazione del modello 4 deve essere fatta utilizzando la funzione Compilazione modello 4 presente nel menu di SIVE all interno della cartella Modello 4 La maschera
MODELLO 4 - compilazione modello 4 L informatizzazione del modello 4 deve essere fatta utilizzando la funzione Compilazione modello 4 presente nel menu di SIVE all interno della cartella Modello 4 La maschera
FASI DA ESEGUIRE ON-LINE
 FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante apposito link presente sul portale della Regione Basilicata e rilascio delle credenziali di accesso necessarie per procedere alla candidatura
FASI DA ESEGUIRE ON-LINE a) registrazione del candidato mediante apposito link presente sul portale della Regione Basilicata e rilascio delle credenziali di accesso necessarie per procedere alla candidatura
Manuale Utente SAP ITS. 3.1 Gestione EMCS Gestione delle Spedizioni V.02
 Manuale Utente SAP ITS 3.1 Gestione EMCS 3.1.2 Gestione delle Spedizioni V.02 Introduzione Il progetto EMCS (Excise Movement and Control System) introduce una nuova gestione della comunicazione relativa
Manuale Utente SAP ITS 3.1 Gestione EMCS 3.1.2 Gestione delle Spedizioni V.02 Introduzione Il progetto EMCS (Excise Movement and Control System) introduce una nuova gestione della comunicazione relativa
Farmacovigilanza attiva e passiva. Dott.ssa Anna Marra
 Farmacovigilanza attiva e passiva Dott.ssa Anna Marra Sorveglianza Passiva / Attiva Eventi Spontaneamente segnalati Attivamente cercati (indagati) Aspecificità In funzione di un obiettivo Fattori culturali,
Farmacovigilanza attiva e passiva Dott.ssa Anna Marra Sorveglianza Passiva / Attiva Eventi Spontaneamente segnalati Attivamente cercati (indagati) Aspecificità In funzione di un obiettivo Fattori culturali,
Informazioni di ritorno ai segnalatori: uno strumento utile in Farmacovigilanza. AIFA - Agenzia Italiana del Farmaco
 Informazioni di ritorno ai segnalatori: uno strumento utile in Farmacovigilanza AIFA - Agenzia Italiana del Farmaco Informazione di ritorno Nel 2012 l AIFA ha attivato un progetto ad hoc per la predisposizione
Informazioni di ritorno ai segnalatori: uno strumento utile in Farmacovigilanza AIFA - Agenzia Italiana del Farmaco Informazione di ritorno Nel 2012 l AIFA ha attivato un progetto ad hoc per la predisposizione
Il registro nazionale dell ADHD. Modalità di prescrizione e distribuzione Metilfenidato e Atomoxetina
 Il registro nazionale dell ADHD Modalità di prescrizione e distribuzione Metilfenidato e Atomoxetina Domenica Di Benedetto U.O. FARMACIA Azienda Ospedaliera SAN PAOLO (MI) Milano, 11Dicembre 2007 ISTITUTO
Il registro nazionale dell ADHD Modalità di prescrizione e distribuzione Metilfenidato e Atomoxetina Domenica Di Benedetto U.O. FARMACIA Azienda Ospedaliera SAN PAOLO (MI) Milano, 11Dicembre 2007 ISTITUTO
