TRASFORMAZIONE E DINAMICA DEGLI INQUINANTI : Programma
|
|
|
- Annabella Ippolito
- 5 anni fa
- Visualizzazioni
Transcript
1 TRASFORMAZIONE E DINAMICA DEGLI INQUINANTI : Programma Argomento Testo* Cap. Pag. Cinetica chimica Velocità di reazione. Definizione di ordine, pseudo-ordine e moleco- F.P larità. Equazioni cinetiche integrate di ordine 0, 1, 2 e 3 rispetto ad un solo componente, di ordine 2 rispetto a due componenti. Autocatalisi. Dipendenza della Kcin dalla temperatura secondo Arrhenius. Biochemical oxygen demand (BOD) e metodo di Fujimoto. (Appunti) Metodi di determinazione dell'ordine: tempo frazionario, isolamento, proporzioni costanti, velocità iniziali. Correlazione tra grandezze fisiche e concentrazioni, con esempi Teoria delle collisioni. Meccanismo di Lindemann-Hinshelwood per reazioni di primo ordine. Relazione tra costanti cinetiche e Keq.. Teoria del complesso atti- E.C vato, dipendenza della Kcin.da H e S di attivazione Reazioni complesse: parallele, consecutive e reversibili (di ordine 1). F.P Condizioni di stato stazionario. Applicazione consecutive: profilo 186, 375 concentrazione di O 2 in un corso d'acqua in presenza di BOD. (Appunti) Reazioni a catena ed esplosive (cenni). A Catalisi enzimatica (meccanismo di Michaelis-Menten). E.C Cenni sulla teoria di Debye-Huckel Dipendenza della Kcin.dalla forza ionica (reazioni tra specie cariche). F.P Diffusione molecolare e modello di Pasquill Equazioni di Fick per la diffusione; modello di Pasquill per la diffusio- E.C ne e il trasporto di un pennacchio di fumo lungo la direzione del vento. V Equilibri elettrochimici Reazioni di ossido-riduzione. Celle elettrochimiche. Forza elettromo- E.C trice : convenzione sul segno e relazione con G e Keq.. Equazione di Nernst. Semicelle. Potenziali standard di riduzione. Dipendenza della f.e.m. dalla temperatura e relazione con S di reazione. (Appunti) Elettrochimica dinamica Densità di corrente. Sovratensione. Densità di corrente di scambio. A Derivazione dell'equazione di Butler-Volmer. Variazione della densità di corrente in funzione della sovratensione. Diagramma di Tafel. Velocità di sviluppo di gas e di deposizione di metallo al catodo. Diminuzione della DDP in una cella operativa in funzione della corrente e della resistenza interna. Corrosione dal punto di vista termodinamico e cinetico. Corrente di corrosione. Potenziale di corrosione. Dipendenza della corrente di corrosione da superfici elettrodiche, densità della corrente di scambio e forza elettromotrice. F.P. J.W. Moore and R.G. Pearson, Kinetics and Mechanism, J. Wiley & Sons, New York, E.C. - D. Eisenberg and D. Crothers, Physical Chemistry with applications to the life sciences, The Benjamin/Cummings Publishing Company, Menlo Park, V. - P.A. Vesilind, J.J. Pierce, R.F. Weine, Environmental Engineering, 3^ Ediz., Butterworth- Heinemann, Boston, A1 - P.W. Atkins, Physical Chemistry, 3^ Ed. Inglese, Oxford University Press. 1 A2 - P.W. Atkins, The Elements of Physical Chemistry, Oxford University Press.
2 Basi di quantomeccanica e spettroscopia. Onde, particelle, equazioni di De Broglie e Schrödinger. Livelli quantizzati di una particella confinata in una scatola. Funzioni d'onda dell'atomo di idrogeno. Legame covalente. Orbitali molecolari. Basi di spettroscopia vibrazionale (IR, Raman) e visibile-ultravioletta (eccitazione di elettroni,fluorescenza). Utilizzo di metodi computazionali per valutare energia totale, energie orbitaliche e distribuzione di carica, frequenze vibrazionali, stati elettronici eccitati, energie di ionizzazione, affinità elettroniche. ESERCITAZIONI DI LABORATORIO - Cinetica di reazione seguita mediante conduttimetria, a temperature diverse. Elaborazione dati per determinare costante cinetica ed energia di attivazione. - Utilizzo di metodi teorici (attraverso il del pacchetto di programmi Gaussian 03, ambiente Unix) per determinare geometrie molecolari di equilibrio, frequenze vibrazionali, struttura elettronica, energie di transizione elettronica (assorbimento UV-visibile), energie di ionizzazione, affinità elettroniche. 2
3 CINETICA: parte della scienza del moto (dinamica, nel gergo fisico). In chimica indica la velocità di una reazione. La cinetica chimica studia la velocità di reazione, i fattori che la influenzano e il meccanismo con cui la reazione avviene. È evidente la differenza tra il punto di vista dinamico della cinetica chimica e quello statico della termodinamica. La termodinamica si interessa solo dello stato iniziale e finale (entrambi in condizioni di equilibrio) di un sistema, ma non della variabile tempo. La cinetica si interessa della velocità con cui lo stato iniziale (reagenti) si trasforma in stato finale (prodotti). Lo stato di equilibrio può essere trattato anche in termini cinetici, come lo stato in cui le velocità della reazione diretta e inversa sono uguali. Il contrario non è vero: la conoscenza delle condizioni di equilibrio (bilancio netto nullo) non dice se le velocità che si controbilanciano sono entrambe grandi o piccole. È ovvio che la conoscenza della velocità con cui procede una reazione è di per sé di fondamentale importanza dal punto di vista applicativo. Non meno importante, dal punto di vista chimico, è il fatto che la determinazione sperimentale dell'equazione cinetica è lo strumento più efficace per definire il meccanismo di reazione, ovvero, la sequenza di singoli eventi reattivi (stadi elementari, nel gergo) attraverso i quali avviene la reazione netta indicata dalla stechiometria. Es. di stechiometrie simili, eq. cin. diverse, meccanismi diversi: H 2 + I 2 H 2 + Br 2 2 HI 2 HBr d [ HI ] = k [ H 2 ][ I 2 ] dt 1/ 2 d [ HBr] k[ H2][ Br2 ] = dt 1+ k'[ HBr]/[ Br ] 2 3
4 SISTEMA DI REAZIONE Sistema aperto: è il caso più complicato (e non considerato qui) perché la variazione di concentrazione di ciascuna specie non dipende solo dalla cinetica della reazione chimica, ma anche dal bilancio delle portate in entrata e uscita. Sistema chiuso : la variazione di concentrazione nel tempo di ciascuna specie dipende solo dalla cinetica della reazione chimica. VELOCITA' DI REAZIONE Per una reazione generica a A + b B c C + d D la velocità (v) può essere espressa come: v = d[a]/dt o d[b]/dt o d[c]/dt o d[d]/dt. - preceduta da segno negativo per i reagenti, in modo che v sia sempre positiva; - in funzione della concentrazione (proprietà intensiva) e non del numero di moli (che dipende dalle dimensioni del sistema). - deve essere espressa come derivata perché cambia nel tempo ; Nota: a seconda che la v sia riferita ad una specie o ad un'altra, il suo valore cambia per effetto dei diversi coefficienti stechiometrici: (1/a) v A = (1/b) v B = (1/c) v C = (1/d) v D 4
5 EFFETTO DELLA CONCENTRAZIONE Ad una certa T = cost., la v è funzione di alcune o tutte le specie coinvolte nella reazione. Se un prodotto compare nell'equazione cinetica, il suo effetto si dice autoinibizione o autocatalisi a seconda che diminuisca o aumenti la v. Lo stesso effetto si definisce inibizione o catalisi quando è determinato da una specie che non è né un reagente né un prodotto. Non è prevedibile a priori l'equazione cinetica (la funzione esistente tra v e le concentrazioni) se si conosce solo la stechiometria di reazione : H 2 + I 2 2 HI v = k [H 2 ] [I 2 ] H 2 + Br 2 2 HBr v = k [H 2 ] [Br 2 ] ½ / (1 + k' [HBr] / [Br 2 ] ) Anche se le due reazioni hanno stechiometria analoga, hanno equazioni cinetiche molto diverse perchè avvengono con diversi meccanismi. ORDINE DI REAZIONE Equazioni cinetiche di forma monomiale (produttoria di una k e potenze di concentrazioni) non sono infrequenti e sono le meno complesse da trattare: d [A] / d t = k [A] n a [B] n b [C] n c Nota: dimensioni di k [conc.] (n 1) tempo 1 tranne che per n = 1, il valore numerico dipende dalle unità scelte per la concentrazione, oltre a quelle di tempo. Solo per questo tipo di equazioni cinetiche è definito l'ordine di reazione n = n a +n b + n c +, dove n a, n b, n c sono detti ordini parziali rispetto alle singole specie. 5
6 La reazione tra idrogeno e iodio è di secondo ordine, per quella tra idrogeno e bromo non esiste il concetto di ordine. Così come dalla stechiometria non è possibile prevedere l'equazione cinetica, ovviamente non è possibile prevedere l'ordine, né tanto meno gli ordini parziali coincidono necessariamente con i coefficienti stechiometrici. L'ordine deve essere trovato sperimentalmente. Se in particolari condizioni si verifica che una o più concentrazioni rimangono (circa) costanti durante la reazione, il loro valore può esere incluso nella costante cinetica k. In questo caso, la reazione è detta essere di pseudo-ordine n, dove n è la somma degli esponenti delle concentrazioni che cambiano. Questo caso si verifica in presenza di un catalizzatore (che partecipa alla reazione, ma si rigenera), quando un componente è in forte eccesso rispetto agli altri (la conc. consumata o prodotta è trascurabile rispetto a quella iniziale), o in presenza di un effetto tampone (ioni H +, OH ). Ad esempio, per l'inversione del saccarosio d [S] / d t = k [S] [H 2 O] [H + ] : l'ordine è 3, ma in ambiente acquoso tamponato si ha pseudo-ordine 1. MOLECOLARITÀ Mentre il concetto di ordine è empirico, quello di molecolarità è teorico. La molecolarità è definita come il numero di specie (molecole, atomi, ioni, ) che prendono parte ad un unico processo reattivo (stadio elementare). Non si conoscono reazioni con molecolarità > 3. Una reazione mono-, bi- o trimolecolare è anche di ordine 1, 2 o 3, rispettivamente, ma non è (necessariamente) vero il contrario. 6
7 ORDINE n RISPETTO A 1 SOLO REAGENTE Equaz. cinet. non integrata n v = K [A] Equaz. cinet. integrata 1 1 ( - 1 ) = K t (n-1) [A o] n -1 [A] n -1 Tempo di dimezz. n -1 t 2-1 1/ 2 = (n-1) K [A o ] n -1 n = 0 v v = K [A] [A o ] - [A] = K t t 1/2 = [A o ] /2K t 1 / 2 [A o ] 0 [A] 0 -K t 0 1/2K [A o ] n = 1 v v = k[a] ln[a] ln[a o] ln [A]/[A o] = - K t t 1/2 t 1/ 2 = ln2/k 0 [A] 0 -K t 0 [A o ] 7
8 ORDINE n RISPETTO A 1 SOLO REAGENTE Equaz. cinet. non integrata n v = K [A] Equaz. cinet. integrata 1 1 ( - 1 ) = K t (n-1) [A o] n -1 [A] n -1 Tempo di dimezz. n -1 t 2-1 1/ 2 = (n-1) K [A o ] n -1 v n = 2 v = k [A] 2 1/[A] 1/[A] - 1/[A o] = k t t 1/2 t 1 / 2 = 1/[A o]k K 1/K 1/[A o] 0 [A] 0 t 0 1/[A o] n = 3 v v = k [A] 3 1/[A] 2 1/[A] 2-1/[A0] 2 = 2k t t 1/2 t 1/ 2 = 3/2K[A o] 2 1/[A o] 2 2 K 3/2K 0 [A] 0 t 0 1/[A o] 2 Nota - La relazione t ½ / Ao in forma logaritmica vale anche per n = 1: ln t ½ = ln cost. (n 1) ln Ao, ovvero, diagrammando ln t ½ contro ln Ao si trova una retta con pendenza (n 1). 8
9 TEMPO DI DIMEZZAMENTO conc. A o n = 1 t = (ln 2) / k 1/2 Il tempo di dimezz. non dipende dalla conc. iniz. A o ' A o /2 ' A o /2 0 t 1/2 t conc. A o n = 1 t = 1/2 n (n-1) k A o n-1 A o /2 A o /4 t 1 /2 t ' = 2 t 1/2 1/2 n = 2 t ' 1 /2 0 t ln t 1/2 = f (n-k) (n-1) ln A o (anche per n=1) 9
10 Ordine 2 rispetto ad 1 reagente: metodo dei tempi frazionari IDROLISI ALCALINA DI NITROBENZOATO DI ETILE Dati conc./ tempo : t (s) [A]x10 2 5,00 3,55 2,75 2,25 1,85 1,60 1,48 1,40 Molarità x [A 0 ]x10 2 5,00 4,50 4,00 3,50 3,00 t 1/ tempo (s) 400 t 1/2 300 pend.=1/k= 11,03 M.s k = M-1s /[A] 10
11 ORDINE 2 RISPETTO A 2 REAGENTI (1 + 1) A + B + Prodotti v = d [A] / d t = k [A] [B] ln ( Ao / Bo. B / A ) = (B o -A o ) k t n-propil Br + S 2 O n-propil S 2 O 3- + Br - B = B o A o + A Pendenza = k (B o - A o ) Nota: per B 0 =A 0 si ha una forma indeterminata, ma si ricade nel caso di v = k [A] 2 ORDINE 2 : AUTOCATALITICA A + B + v = d [A] / d t = k [A] [B] ln ( Ao / Bo. B / A ) = (B o + A o ) k t B = (A o +B o )/[1+(A o /B o ) e k(ao+bo) t ] B = B o + A o A Nota: B o piccolo ma 0 11
12 k A EFFETTO DELLA TEMPERATURA SULLA VELOCITÀ DI REAZIONE Equazione (empirica) di Arrhenius : 0 0 d ln k E = d T RT a 2 E ln k = a + ln A RT E ln k = a + cost. RT k = A. e - (Ea / RT) T con : E a = energia di attivazione A = fattore preesponenziale Con una E a media di circa kj/mol), la k aumenta di un fattore 2-3 per un aumento di T = 10 C (a T amb.), mentre aumenta circa volte se Ea dimezza. ln k ln A... - Ea/R... Per determinare E a ed A, si misurano i valori di k a T diverse e si diagramma ln k contro 1/T: la pendenza della retta è E a / R e l'intercetta (estrapolata) è ln A. 1/ T 12
13 ESERCITAZIONE: determinazione dei parametri di Arrhenius La costante cinetica per la decomposizione (reazione di ordine 2) dell'acetaldeide (CH 3 CHO) è stata misurata nell'intervallo di T K. T (K) K (M -1 s -1 ) ln k (1/Ms) /T Il diagramma di ln k contro 1/T mostra una buona correlazione lineare. La migliore interpolazione (metodo dei minimi quadrati) ha una pendenza -E a /R = -2.21x10 4 e intercetta (1/T= 0) ln A = 27.0 E a = (2.21x 10 4 K) x (8.314 J K -1 mol -1 ) = 184 kj mol -1 A = e 27.0 M -1 s -1 = 5.3 x M -1 s -1 Nota: le dimensioni di A sono quelle della costante k. 13
14 Solubility of Oxygen T ( C) Sat. conc. (mg/l) Da: P.A. Vesilind et al., Environmental Engineering, Cap. 4. Membrana Catodo O 2 KCl O 2 sciolto in H 2 O Anodo La conc. di saturazione di O 2 in acqua diminuisce con la T. Può essere misurata con una sonda polarografica dotata di un anodo di Ag circondato da un catodo di Au, immersi in una soluzione di KCl. La parete inferiore è costituita da una membrana di teflon, permeabile all'ossigeno. Si hanno le reazioni elettrochimiche: catodo: O H 2 O + 4 e 4 OH anodo: 4 Ag + 4 Cl 4 AgCl + 4 e con una corrente proporzionale alle molecole di O 2 che entrano in contatto col catodo. Definizione di B.O.D. Il BOD (domanda biochimica d ossigeno) rappresenta la massa di ossigeno che viene utilizzata in n giorni dai microorganismi per decomporre ossidativamente a 20 C le sostanze organiche presenti in 1 litro d acqua: BOD n (di solito BOD 5 ) = BOD in n (5) giorni 14
15 BOD (Biochemical Oxygen Demand) L eliminazione del carbonio organico (OR) dalle acque reflue è affidata a microorganismi (MO) aerobi che, in presenza di O 2, si accrescono a spese di OR, con produzione di CO 2 e di altri composti con alto numero di ossidazione, come sali di SO 4 - -, NO 3 -, PO ,... ν 1 O 2 + ν 2 OR ν 3 MO + ν 4 CO d [O 2 ]/dt. 1/ν 1 = d [OR]/dt. 1/ν 2 = d [MO] /dt. 1/ν 3 La massa (conc.) dei microorganismi si accresce nel tempo a spese di OR secondo la legge cinetica della catalisi enzimatica (meccanismo di Michaelis-Menten) : d ρ MO /dt = µ. ρ MO. ρ OR /(K + ρ OR ) con ρ i = c i M i ; µ t 1 (vel. specif. per unità di conc. MO) e dalla stechiometria, con y = ν 3,M /ν 2,M : d ρ OR /dt = 1/y. d ρ MO /dt // dρ O 2 /dt = (ν 1,M/ν 2,M ). d ρ OR /dt Se K>> ρ OR d ρ OR /dt = µ/(y K). ρ MO. ρ OR = K OR. ρ OR cinetica di ordine 1 (K OR t 1 ) : ρ OR = ρ OR (0). e K OR.t BOD t (mg/l) = ρ O 2 (0) - ρ O 2 (t) (O 2 consumato al tempo t) ρ O 2 (0) ρ O2 = (ν 1,M/ν 2,M ).(ρ OR (0) ρ OR ) = (ν 1,M /ν 2,M ). ρ OR (0). (1 e K OR.t ) BOD t = L 0 (1 - e K OR.t ) ; ρ O 2 = L 0. e K OR.t dove L 0 = BOD = ρ O 2 (0) = (ν 1,M/ν 2,M ). ρ OR (0) = ossigeno (mg/l) necessario per ossidare tutto il carbonio organico iniziale. ρ O 2 in funzione del tempo si trova da (L 0 BOD t ), che richiede la determinazione di L o la pendenza del diagramma lineare ln ρ O 2 / t fornisce la K OR. 15
16 Metodo di Fujimoto t (giorni) BOD (mg/l) Lo = mg/l 30 BOD (t+t') BOD (t) t (giorni) L = 27,95 BOD ln (L) Diagrammando ln(l) contro t K OR = 0,263 g -1 16
17 ESERCIZIO - METODO DELLE VELOCITA' INIZIALI La velocità iniziale viene determinata sperimentalmente come c/ t. Occorre trovare un indicatore che segnali il consumo di un c prefissato (e piccolo). Per la reazione : 2 Fe(CN) I - 2 Fe(CN 6 ) I 2 v = d[i 2 ]/dt = k [Fe(CN) ] a [I - ] b [Fe(CN 6 ) 4 - ] c [I 2 ] d Con [I 2 ] iniziale = 0 ( d = 0) si trova (25 C) : Cin. N Concentrazione iniziale (M) Fe(CN) I - Fe(CN 6 ) 4 - Vel. Iniz. (M/ora) da cui si deduce che a=2, b=1, c=-1 ( n = 2) e k = 10-3 / (10-3 ) 2. (10-3 ) 1. (10-3 ) -1 = 10 3 M -1 ore -1 17
18 UTILIZZO DI PROPRIETA' FISICHE AL POSTO DELLA CONC. L'indagine cinetica e la determinazione dei parametri che la caratterizzano partono dalla elaborazione di dati sperimentali di concentrazione in funzione del tempo. Tale analisi chimica del sistema spesso non è né semplice né rapida. Tuttavia può in molti casi essere convenientemente sostituita dalla misura di una proprietà fisica (λ) dell'intero sistema (ad es., indice di rifrazione, assorbanza nell'ir o UV o visibile, ecc.) nel tempo. Gli unici requisiti sono: 1) variazione di λ grande rispetto alla sensibilità dello strumento di misura; 2) additività di λ (λ totale =somma λ parziali); 3) deve esistere una relazione matematica precisa tra concentrazione e λ (ma in pratica l'unica utilizzabile è la proporzionalità). Si può esaminare il caso più semplice di reazione: A B (in presenza di solvente) poiché sarà facilmente comprensibile che i risultati possono essere estesi a qualsiasi reazione più complessa. Se la reazione va a completezza, a un tempo t (qualsiasi) : λ = k A [A] + k B ([Ao] [A]) + k B [Bo] + λ SOL a t = 0 : λo = k A [Ao] + k B [Bo] + λ SOL a t = : λ = k B [Ao] + k B [Bo] + λ SOL λ λ = k A [A] + k B ([Ao] [A]) k B [Ao] = (k A k B ) [A] λo λ = k A [Ao] k B [Ao] = (k A k B ) [Ao] (λ λ ) / (λo λ ) = A / Ao Nota : non è richiesto che le varie k di proporzionalità siano uguali tra di loro e non importa conoscerle perché nel rapporto si elidono. Non si può risalire al valore assoluto di [A], ma solo al rapporto [A]/[Ao]. Per una reazione di ordine 1: ln (A / Ao) = ln [(λ λ ) / (λo λ )] = k t ma (se pure in modo meno diretto) la relazione è utilizzabile anche per n 1. Per una reazione di equilibrio A B : λeq = k A [A eq ] + k B [Ao A eq ] + k B [Bo] + λ SOL da cui, con le relazioni precedenti, si trova: (λ λ eq ) / (λo λ eq ) = (A A eq ) / (Ao A eq ) risultato direttamente utilizzabile per reazioni reversibili di ordine 1. 18
19 UTILIZZO DI PROPRIETA' FISICHE AL POSTO DELLA CONC. (CH 3 ) 3 COOC(CH 3 ) 3 2 (CH 3 ) 2 CO + C 2 H 6 Decomposition of di-t-butyl peroxyde at C time (min) P (mm Hg) P - P K x 10 4 (s -1 ) a n = 1 (A /A 0 ) = (P - P) / (P - P 0 ) P 3 P av ± 0.07 a rate constants evaluated for successive 3-min intervals 5.8 NB: per ottenere la pendenza (- k) basta diagrammare (P - P) contro t. ln (Pinf.-P) 5.6 k = min -1 = 3,48 x 10-4 s pend.= -k = /min t (min) 19
20 O C CH 2 Br + N O C CH 2 N + Br I prodotti sono specie cariche : nel tempo aumenta la conduttanza (C ) v = k [A] [B] con Ao=Bo v = k [A] 2 (1/A) (1/Ao) = k t (Ao/A) = (C Co) / (C C) (1/Ao) (Ao/A) (1/Ao) = k t (1/Ao) (C Co) / (C C) (1/Ao) = k t c'è una relazione lineare tra 1 / (C C) e t, con pendenza = k Ao / (C Co) Nota : occorre quindi conoscere anche concentrazione e conduttanza a t = 0. 1/(C - C) ) k Ao / (C - Co) 20
21 TEORIA DELLE COLLISIONI A + B Prodotti (stadio elementare bimolecolare) In prima approssimazione si assume che le molecole abbiano simmetria sferica e che tutti gli urti bimolecolari diano luogo alla formazione dei prodotti. σ AB = σ A + σ B ; massa ridotta: µ = (m A m B ) / (m A + m B ) <v> = velocità media relativa = ( 8 K B T / π µ ) ½ Vs -1 = π σ 2 AB ( 8 K B T / π µ ) ½ Numero di urti di 1 sola molecola A con tutte le B al secondo = = ( 8 π K B T / µ ) ½ σ 2 AB n B molec. s 1 (n B = molec. B/cm 3 2,7 x per gas a T e P standard, µ= g, σ =10-7 cm ) Numero di collisioni bimolecolari (al secondo e cm 3 ): Z AB = ( 8 π K B T / µ ) ½ σ 2 AB n A n B ( urti bimolec. cm 3 s 1 ) v 10 8 M s 1 = k. n A n B k M -1 s -1 (n A = n B M a T e P amb.) Costante cinetica prevista troppo alta (ordine di grandezza del fattore preesp.) Numero di collisioni bimolec. utili = Z AB ' = q. Z AB (con q = p. e E i /RT ) - p (fattore sterico) tiene conto della probabilità che l'orientazione consenta la reazione; difficilmente valutabile a priori (compreso tra 10-5 e 1). - Equazione di Boltzmann (termod.statistica) : N / No = e E i / K B T è la frazione di molecole la cui energia supera la soglia E i alla temperatura T. 21
22 E a = energia di attivazione [energia / mol] ; R = K B.N A VELOCITA' DI REAZIONE = Z AB ' = p. ( 8 π R T / NA µ )½ σ 2 AB e Ea /RT n A n B e - Ea /RT 10-9 con una E a media = 50 kj mol -1, T = 298 K k p M -1 s -1 (consistente con dati sperimentali ) ENERGIA DI ATTIVAZIONE E PROFILO DI REAZIONE E a H E a ' (reaz. inversa) 22
23 REAZIONI UNIMOLECOLARI Meccanismo di Lindemann-Hinshelwood Le reazioni unimolecolari seguono una cinetica di ordine 1, con una costante che non dipende dalla T (il superamento dell'e a non è dovuto a collisioni). E' il caso della disintegrazione radioattiva. - dn = n k dt - dn/n = k dt - dc/c = k dt (con n = moli, c = concentrazione) Per molte cinetiche di ordine 1, invece, la k dipende da T secondo Arrhenius. Non procedono quindi attraverso un unico stadio elementare. Sono state spiegate dal meccanismo proposto da Lindemann-Hinshelwood : A + A A + A* k 1 A + A* A + A k 2 A* P k 3 Solo la specie A*, attivata per collisione, dà luogo allo stadio monomolecolare: v = -d[a] /dt = d[p] /dt = k 3 [A*]. La specie A*, molto reattiva, è in condizioni di stato stazionario: d[a*]/dt = 0. d[a*]/dt = k 1 [A] 2 k 2 [A] [A*] k 3 [A*] = 0 [A*] (k 2 [A] + k 3 ) = k 1 [A] 2 [A*] = k 1 [A] 2 / (k 2 [A] + k 3 ) v = k 3 [A*] = k 3 k 1 [A] 2 / (k 2 [A] + k 3 ) Casi limite : k 2 [A] >> k 3 v = k 3 k 1 /k 2 [A] (ordine 1) k 2 [A] << k 3 v = k 1 [A] 2 (ordine 2) La k 2 è tanto grande che non si riesce ad abbassare [A] fino a verificare l'ordine 2, ma abbastanza da non seguire l'ordine 1. 23
24 MECCANISMO DI REAZIONE, STADI ELEMENTARI Uno degli obiettivi di uno studio cinetico è la determinazione del meccanismo di reazione, che consiste in una sequenza di stadi elementari. Gli stadi elementari hanno le seguenti caratteristiche: 1) uno stadio elementare risulta da processi che avvengono o in una singola molecola o da collisioni reattive tra due o, talvolta, tre particelle; 2) in uno stadio elementare non vi sono intermedi stabili tra reagenti e prodotti; 3) l'equazione cinetica per uno stadio elementare può essere dedotta dalla stechiometria; 4) la somma degli stadi elementari che costituiscono il meccanismo deve dare come risultato la reazione netta; 5) la costante di equilibrio per ciascuno stadio elementare è il rapporto tra le costanti cinetiche diretta e inversa; 6) la costante di equilibrio per la reazione netta (somma degli stadi elementari) è il rapporto tra la produttoria delle costanti cinetiche dirette e la produttoria delle costanti cinetiche inverse dei singoli stadi: K eq = Π k i / Π k -i 24
25 1) A + B k 1 k -1 C d [C]/d t = k 1 [A] [B] - k -1 [C] k 2 2) C D k -2 A + B D d [D]/d t = k 2 [C] - k -2 [D] ( reazione netta ) 5) All'equilibrio: d [C]/d t = k 1 [A] [B] - k -1 [C] = 0 > [C] [A] [B] = K 1eq= d [D]/d t = k 2 [C] - k -2 [D] = 0 > [D] [C] = K 2eq = k 1 k -1 k 2 k -2 6) K 1eq K 2eq = k 1 k 2 k -1 k -2 = [C] [D] [A] [B] [C] = [D] [A] [B] = K eq = Π k i Π k -i 25
26 COORDINATA DI REAZIONE, PUNTO DI SELLA H a + H b H c H a H b + H c Minimo Sella (o stato di transizione) Energia Coordinata di reazione Minimo Distanza H b H c Energia Distanza H a H b Superficie di energia potenziale per la semplice reazione H a + H b H c H a H b + H c. L'energia è rappresentata (in direzione verticale) in funzione delle distanze H a H b e H b H c. Notare che la distanza H a H b è grande all'inizio della reazione e va diminuendo via via che il sistema si sposta lungo la coordinata di reazione, fino a raggiungere la distanza di equilibrio della molecola H 2. La sella si trova in un massimo di energia lungo la coordinata di reazione, ma (come tutti gli altri punti) in un minimo rispetto alle direzioni perpendicolari. La specie instabile che si trova in questo stato di transizione tra reagenti e prodotti è definita complesso attivato. 26
27 TEORIA DEL COMPLESSO ATTIVATO Assume che la velocità di reazione dipenda dalla concentrazione del complesso attivato, in equilibrio con i reagenti. Per lo stadio elementare bimolecolare A + B (A-B) C la costante di equilibrio è K = [A-B ] / ([A] [B]) -d[a]/dt = (coef. trasm., κ) x (vel. passaggio barriera, ν) x [A-B ] Si può dimostrare che la frequenza ν (s -1 ) di passaggio attraverso la barriera è ν = E / h = K B T / h, con K B = 1, J K -1 per molecola e h = cost. Planck = 6, J s ν s -1 (T amb.). -d[a]/dt = κ (K B T / h) [A-B ] = κ (K B T / h) K [A] [B] 1) velocità proporzionale alla concentrazione di ciascun reagente ; 2) k cinetica = κ (K B T / h) K, dove la K di eq. può essere correlata alle proprietà termodinamiche del complesso attivato. Sostituendo K = e ( G / RT) = e ( S / R H / RT) : k cin. = κ (K B T / h). e ( S / R). e ( H / RT) Relazione con la k cin. secondo Arrhenius: d ln k/dt = 1/ T + H / RT 2 = (RT + H ) / RT 2 Arrhenius : d ln k/dt = Ea / RT 2 Ea = H + RT k cin. = κ (K B T / h). e ( S / R). e. e (Ea / RT) = A. e (Ea/RT) Nota : il fattore preesponenziale A dipende dall'entropia standard di attivazione (è l'equivalente della probabilità di opportuna orientazione nella teoria delle collisioni), l'energia di attivazione Ea è poco diversa dall'entalpia standard di attivazione (a T amb., RT 2,4 kj mol -1, mentre un valore medio di Ea è circa kj mol -1 ). 27
28 REAZIONI PARALLELE (ordine 1) Meccanismo A k 1 U A k 2 V A k 3 W t - d [A] /dt = k [A] dove k = (k 1 + k 2 +k 3 ) [A] = [Ao] e kt d [U] /dt = k 1 [Ao] e kt [U] = [Uo] + ( k 1 [Ao] / k) (1 - e kt ) e analoghe soluzioni per V e W, dove compaiono k 2 e k 3. Ad ogni t : [A] + [U] + [V] + [W] = [Ao] t ½ (dimezzamento di A e di metà comparsa dei prodotti) = (ln 2 )/ k Con Uo = Vo = Wo = 0, ad ogni t si ha U : V : W = k 1 : k 2 : k 3 t 1 e k t Si può dimostrare la relazione tra la Ea per la scomparsa di A e quelle per la comparsa dei prodotti : E 1 k 1 + E 2 k 2 + E 3 k 3 E a = k 1 + k 2 + k 3 28
29 REAZIONI CONSECUTIVE, o IN SERIE (ordine 1) Meccanismo A B k 1 k 2 B C k 1 = 0.1 min -1 K 2 = 0.05 min -1 con [Bo] = [ Co] = 0 [A] + [B] + [C] =[Ao] ad ogni tempo. t (min) -d[a] /dt = k 1 [A] ** d[b] /dt = k 1 [A] k 2 [B] ** d[c] /dt = k 2 [B] [A] = [Ao] e k1 t (A scompare secondo una cinetica di ordine 1) Dall'equaz. differenz. non omogenea d[b] /dt + k 2 [B] = k 1 Ao e k 1 t [B] = k 1 [Ao] (k 2 - k 1 ) (e - k 1 t - e -k 2 t ) [C] = [Ao] - [A] - [B] = [Ao] 1 + con [Bo] = [Co] = 0 1 k 1 - k 2 (k 2 e - k 1 t - k 1 e - k 2 t ) [ ] Ponendo d [B]/dt = 0 si ottiene il tempo (t max ) al quale la concentrazione di B è massima : t max = ln (k 2 / k 1) ( k 2 - k 1 ) Poiché d 2 [C]/d t 2 = k 2 d [B]/dt, in corrispondenza di [B] max la concentrazione di C ha un flesso (d 2 [C]/d t 2 = 0) 29
30 REAZIONI CONSECUTIVE APPLICAZIONE : Concentrazione di ossigeno in un corso d'acqua in funzione del B.O.D. velocità di trasferimento di O 2 dall'aria all'acqua : dρ os = k 2 (ρ sa ρ os) (con k dt 2 prop. A / V = 1/ p) p A velocità di consumo di O 2 : dρ os dt = k 1. L 0 e - k 1t dρ os dt - k = k 2 (ρ sa ρ os) k 1.L 0 e 1 t ovvero : d(ρ sa ρ os) dt - k = k 1.L 0 e 1 t k 2 (ρ sa ρ os) > (ρ sa ρ os) come l'intermedio B nelle consecutive A k 1 k B 2 C, quindi l'equaz. cinetica integrata è : ρ O 2 ρ sa (ρ sa ρ os) = k 1 L 0 - k (e 1 t - k e 2 t ) k 2 k 1 e il tempo corrispondente alla minima ρ os è : t min = Profilo della concentrazione di O 2 nel tempo ln k 2 k1 k 2 k 1 In un corso d'acqua con una certa v, a t min corrisponde la distanza v.t min dal punto in cui si immettono le acque reflue. 0 0 t min t Nota: il valore di ρ min dipende anche da L 0 (t min solo da k 1 e k 2 ). 30
31 REAZIONI REVERSIBILI DI ORDINE 1 A k k' B [B o ] = 0 [B] = ([Ao]- [A]) - d[a]/dt = k [A] k' [B] = k [A] k' ([A o ] [A]) - d[a]/((k+k') [A] k' [A o ]) = dt - 1 (k+k') ln A ln ((k+k') [A] - k'[a o ]) = t Ao k [A o ] = (k+k') t (k+k') [A] - k'[a o ] Nota: non direttamente utilizzabile in questa forma. All'equilibrio: k [A e ] = k'[b e ] = k'([a o ] [A e ]) A e = k'[a o ]/(k+k') Dividendo num. e den. dell'argomento del logaritmo per (k+k'): ln k [A o ] / (k+k') [A] - [A e ] = (k+k') t e scrivendo k[a o ] come [A o ] - [A e ] ln k[a o ] + k'[a o ] k'[a o ] [A] - [A e ] = (k+k') t Diagrammando ln 1/([A]-[A e ]) contro il tempo si ottiene una retta di pendenza (k+k'). E' facile anche sfruttare la relazione: (λ λ eq ) / (λo λ eq ) = (A A eq ) / (Ao A eq ). Dalla relazione k / k' = ([A o ]-[A e ]) / [A e ] si ottengono i valori di k e k' separatamente. Nota: E a E a ' = H di reazione. 31
32 CATALISI ENZIMATICA Meccanismo v max E + S k 2 k 1 k -1 ES v in ordine 0 ES k -2 k 3 k -3 EP EP P + E (veloce) ordine 1 [S] Il meccanismo (Michaelis-Menten) prevede che la velocità di formazione del prodotto coincida con quella del complesso EP (3 stadio veloce) V = K 2 [ES] Stato stazionario per l'intermedio ES d[es] / dt = 0 k 1 [E] [S] k -1 [ES] k 2 [ES] + k -2 [EP] = 0 ; [E] = [Eo] [ES] [EP] All'inizio della reazione, [EP] e [P] 0 si possono trascurare le reaz. inverse del 2 e 3 stadio il risultato finale vale per le velocità iniziali. [ES] = ( k 1 [Eo] [S] ) / (k -1 + k 2 + k 1 [S] ) v max (fissata [Eo]) e k M (costante di Michaelis) sono i parametri caratterizzanti. Possono essere terminati con il metodo del "doppio reciproco" : v in = 1 /v k 2 [Eo] [S] k -1 + k 2 k 1 + [S] = v max [S] k M + [S] 1 1 k v = + M. v max v max 1 [S] 1 v max ) k M v max 1 / [S] 32
33 CATALISI ENZIMATICA ESERCIZTAZ. NUMERICA 3 [S] mm Dati sperim. V in µm s -1 6 v x 10 (M/s) 2 ½ v max 1,0 2,0 3,0 4,0 5,0 1,1 1,8 2,3 2,6 2,9 1 k M [S] x 1000 (M) 1/ v v max = 5 x 10-6 M s -1 k M = 3,5 x 10-3 M k M /v max = 709 s 1/v max / [S] 33
34 REAZIONI A CATENA Classificazione degli stadi di reazione : INIZIALE :.. Cl 2 Cl + Cl DI PROPAGAZIONE :. CH 3 + CH 3CH 3 CH 4 + CH 3 CH. 2. O.. + H 2O OH + OH. (ramificato ) RITARDANTE (sottrae prodotto, ma non interrompe la catena) :.. H + HBr H 2 + Br TERMINALE :.. CH 3 + CH 3 CH 3 CH 3 DI INIBIZIONE (reazione con le pareti o con radicali estranei alla reazione):.. CH 3 + R CH 3 R 34
35 MECCANISMO DI FORMAZIONE DI HBr H 2 (g) + Br 2 (g) 2 HBr (g) INIZ. Br 2 2 Br. v = k 1 [Br 2 ] PROPAG. Br. + H 2 HBr + H. v = k 2 [Br. ] [H 2 ] H. + Br 2 HBr + Br. v = k 2 ' [H. ] [Br 2 ] RITARD. H. + HBr H 2 + Br. v = k 3 [H. ] [HBr] TERM. Br. + Br. (+M) Br 2 (+M*) v = k 4 [Br. ] 2 H. + H. H 2 H. + Br. HBr } trascurabili d [HBr]/dt = k 2 [Br. ] [H 2 ] + k 2 ' [H. ] [Br 2 ] - k 3 [H. ] [HBr] L'ipotesi di stato stazionario rispetto a [H. ] e [Br. ] : d[h] /dt = k 2 [Br. ] [H 2 ] - k 2 ' [H. ] [Br 2 ] - k 3 [H. ] [HBr] = 0 d [Br]/dt = 2 k 1 [Br 2 ] - k 2 [Br. ] [H 2 ] + k 2 ' [H. ] [Br 2 ] + k 3 [H. ] [HBr] 2 k 4 [Br. ] 2 = 0 porta a : d [ HBr] d t 3 / 2 k [ H 2 ][ Br2 ] = [ Br ] + k'[ HBr] 2 35
36 REAZIONI ESPLOSIVE esplosione termica 1 atm = Pa H 2 (g) + ½ O 2 (g) H 2 O (g) esplosione per ramificazione probabile meccanismo H 2 + O 2 HO 2 + H iniziale O 2 + H O + OH O + H 2 OH + H } propagazione ramificata H 2 + OH H 2 O + H propagazione - A pressioni basse i propagatori raggiungono le pareti. - A pressioni medio/alte, reazioni termolecolari del tipo O 2 + H + M HO 2 + M* rallentano la propagazione. 36
37 Teoria di Debye-Hückel Φ(r) a r = κ -1 I = Σ i c i z i2 (forza ionica) κ I 1/2 ρ (r) = B. e κr / r [4πr 2 ρ(r) ] rel or ρ(r) ] rel Potenziale elettrostatico ione isolato : Φ = Ze/ε r Potenziale elettrostatico ione schermato : Φ = (Ze/ε r).e κr fattore di schermo 37
38 Dipendenza della k cinetica dalla forza ionica Forza ionica : µ = ½ Σ i c i z i2. Dalla teoria di Debye-Hückel, con µ 10-2 : ln γ i = z i2 α µ/(1 + β a i µ ) z i2 α µ (βa 0,7 ) Per una reazione bimolecolare A + B Prodotti : [AB # ] = K eq# [A] [B] (γ A γ B / γ AB # ) k = k o. (γ A γ B / γ AB # ) (teoria complesso attivato) log k log k o + 2 z A z B α µ log ( k / ko ) In H 2 O e T = 25 C : α = 0,509 (con log dec.) pendenza = 2 α z A z B z A z B 38
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Per la cinetica del 1 ordine si ha:
 1. Si consideri la seguente reazione: CH 3 CHO (g) CH 4(g) + CO (g) Determinare l ordine di reazione e calcolare la costante di velocità della suddetta reazione a 518 C noti i seguenti dati sperimentali:
1. Si consideri la seguente reazione: CH 3 CHO (g) CH 4(g) + CO (g) Determinare l ordine di reazione e calcolare la costante di velocità della suddetta reazione a 518 C noti i seguenti dati sperimentali:
Definiamo Entalpia la funzione: DH = DU + PDV. Variando lo stato del sistema possiamo misurare la variazione di entalpia: DU = Q - PDV.
 Problemi Una mole di molecole di gas ideale a 292 K e 3 atm si espandono da 8 a 20 L e a una pressione finale di 1,20 atm seguendo 2 percorsi differenti. Il percorso A è un espansione isotermica e reversibile;
Problemi Una mole di molecole di gas ideale a 292 K e 3 atm si espandono da 8 a 20 L e a una pressione finale di 1,20 atm seguendo 2 percorsi differenti. Il percorso A è un espansione isotermica e reversibile;
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
Lezione di Combustione
 Lezione di Combustione Introduzione Da un punto di vista chimico-fisico la combustione è un processo reattivo fortemente esotermico Generalmente le temperature in gioco sono particolarmente elevate e dipendono
Lezione di Combustione Introduzione Da un punto di vista chimico-fisico la combustione è un processo reattivo fortemente esotermico Generalmente le temperature in gioco sono particolarmente elevate e dipendono
Leggi dei gas. PV = n RT SISTEMI DI PARTICELLE NON INTERAGENTI. perché le forze tra le molecole sono differenti. Gas perfetti o gas ideali
 Perché nelle stesse condizioni di temperatura e pressione sostanze differenti possono trovarsi in stati di aggregazione differenti? perché le forze tra le molecole sono differenti Da che cosa hanno origine
Perché nelle stesse condizioni di temperatura e pressione sostanze differenti possono trovarsi in stati di aggregazione differenti? perché le forze tra le molecole sono differenti Da che cosa hanno origine
Calcolo di integrali
 7 Maggio 2012 - Lab. di Complementi di Matematica e Calcolo Numerico Calcolo di integrali Indice 1 Teoria cinetica dei gas: la distribuzione delle velocità di Maxwell [1] 1 2 Lavoro associato a una trasformazione
7 Maggio 2012 - Lab. di Complementi di Matematica e Calcolo Numerico Calcolo di integrali Indice 1 Teoria cinetica dei gas: la distribuzione delle velocità di Maxwell [1] 1 2 Lavoro associato a una trasformazione
GAS IDEALI E MACCHINE TERMICHE. G. Pugliese 1
 GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
5.1 RUOLO DELLA TERMODINAMICA E DELLA CINETICA 3 5.3 LEGGE DI VELOCITÀ, COSTANTE DI VELOCITÀ E ORDINE DI REAZIONE 7
 Cap. 5 CINETICA E MECCANISMO DELLE REAZIONI DISCONTINUE I N D I C E pag. PREMESSA 3 5.1 RUOLO DELLA TERMODINAMICA E DELLA CINETICA 3 5.2 VELOCITÀ DI REAZIONE E SUA MISURA 4 5.3 LEGGE DI VELOCITÀ, COSTANTE
Cap. 5 CINETICA E MECCANISMO DELLE REAZIONI DISCONTINUE I N D I C E pag. PREMESSA 3 5.1 RUOLO DELLA TERMODINAMICA E DELLA CINETICA 3 5.2 VELOCITÀ DI REAZIONE E SUA MISURA 4 5.3 LEGGE DI VELOCITÀ, COSTANTE
LA MOLE LA MOLE 2.A PRE-REQUISITI 2.3 FORMULE E COMPOSIZIONE 2.B PRE-TEST
 LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05
 I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto:
 Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI
 DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
ELETTROCHIMICA. Uso di reazioni chimiche per produrre corrente elettrica (Pile)
 ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
Esercizio 1. CO 2 heat capacity
 Esercizio 1 CO 2 heat capacity Quando 2.0 moli di CO 2 sono riscaldate alla pressione costante di 1.25 atm la loro temperatura passa da 250 K a 277 K. La capacità termica molare a P costante della CO 2
Esercizio 1 CO 2 heat capacity Quando 2.0 moli di CO 2 sono riscaldate alla pressione costante di 1.25 atm la loro temperatura passa da 250 K a 277 K. La capacità termica molare a P costante della CO 2
STATO LIQUIDO. Si definisce tensione superficiale (γ) il lavoro che bisogna fare per aumentare di 1 cm 2 la superficie del liquido.
 STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
Biosensori Sensori Chimici. nicola.carbonaro@centropiaggio.unipi.it
 Biosensori Sensori Chimici nicola.carbonaro@centropiaggio.unipi.it Principali applicazioni dei Sensori chimici Ruolo fondamentale degli ioni nella maggior parte dei processi biologici Sensori elettrochimici
Biosensori Sensori Chimici nicola.carbonaro@centropiaggio.unipi.it Principali applicazioni dei Sensori chimici Ruolo fondamentale degli ioni nella maggior parte dei processi biologici Sensori elettrochimici
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Chimica Fisica I. a.a. 2012/2013 S. Casassa
 a.a. 2012/2013 S. Casassa 1 Note Tecniche 2 Testi consigliati: G.K. Vemulapalli, Chimica Fisica", EdiSES, Napoli (1995). D.A. Mc Quarrie e J.D. Simon, Chimica Fisica: un approccio molecolare", Zanichelli,
a.a. 2012/2013 S. Casassa 1 Note Tecniche 2 Testi consigliati: G.K. Vemulapalli, Chimica Fisica", EdiSES, Napoli (1995). D.A. Mc Quarrie e J.D. Simon, Chimica Fisica: un approccio molecolare", Zanichelli,
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
Selezione test GIOCHI DELLA CHIMICA
 Selezione test GIOCHI DELLA CHIMICA CLASSE A Velocità - Equilibrio - Energia Regionali 2010 36. Se il valore della costante di equilibrio di una reazione chimica diminuisce al crescere della temperatura,
Selezione test GIOCHI DELLA CHIMICA CLASSE A Velocità - Equilibrio - Energia Regionali 2010 36. Se il valore della costante di equilibrio di una reazione chimica diminuisce al crescere della temperatura,
Gas perfetti e sue variabili
 Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
Celle a combustibile Fuel cells (FC)
 Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Cenni di Teoria Cinetica dei Gas
 Cenni di Teoria Cinetica dei Gas Introduzione La termodinamica descrive i sistemi termodinamici tramite i parametri di stato (p, T,...) Sufficiente per le applicazioni: impostazione e progettazione di
Cenni di Teoria Cinetica dei Gas Introduzione La termodinamica descrive i sistemi termodinamici tramite i parametri di stato (p, T,...) Sufficiente per le applicazioni: impostazione e progettazione di
Equazioni dierenziali ordinarie del prim'ordine
 21 Maggio 2012 - Lab. di Complementi di Matematica e Calcolo Numerico Equazioni dierenziali ordinarie del prim'ordine Indice 1 Integrazione di un'equazione cinetica 2 2 Cinetica di adsorbimento di Langmuir
21 Maggio 2012 - Lab. di Complementi di Matematica e Calcolo Numerico Equazioni dierenziali ordinarie del prim'ordine Indice 1 Integrazione di un'equazione cinetica 2 2 Cinetica di adsorbimento di Langmuir
Esercizi di Chimica (2 a prova in itinere)
 Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA.
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
LEGGI DEI GAS / CALORI SPECIFICI. Introduzione 1
 LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA
 Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici.
 LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
Ripasso sulla temperatura, i gas perfetti e il calore
 Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
Elettrochimica. 1. Celle elettrolitiche. 2. Celle galvaniche o pile
 Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
Formulario di Termodinamica
 Formulario di Termodinamica Punto triplo dell acqua: T triplo = 273.16 K. Conversione tra gradi Celsius e gradi Kelvin (temperatura assoluta): t( C) = T (K) 273.15 Conversione tra Caloria e Joule: 1 cal
Formulario di Termodinamica Punto triplo dell acqua: T triplo = 273.16 K. Conversione tra gradi Celsius e gradi Kelvin (temperatura assoluta): t( C) = T (K) 273.15 Conversione tra Caloria e Joule: 1 cal
Temperatura. V(t) = Vo (1+at) Strumento di misura: termometro
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
Il trasporto di materia. Principi di Ingegneria Chimica Ambientale
 Il trasporto di materia Principi di Ingegneria Chimica Ambientale 1 Considerazioni preliminari Il nostro studio sarà limitato a: miscele binarie miscele diluite (ossia in cui la frazione molare di uno
Il trasporto di materia Principi di Ingegneria Chimica Ambientale 1 Considerazioni preliminari Il nostro studio sarà limitato a: miscele binarie miscele diluite (ossia in cui la frazione molare di uno
Correnti e circuiti a corrente continua. La corrente elettrica
 Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
LO STATO GASSOSO. Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi
 LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
DETERMINATION OF THE ACIDIC PROPERTIES OF MODIFIED SILICAS BY THERMOGRAVIMETRIC ANALYSIS
 DETERMINATION OF THE ACIDIC PROPERTIES OF MODIFIED SILICAS BY THERMOGRAVIMETRIC ANALYSIS Antonella Gervasini, Simona Bennici e Paolo Carniti Dipartimento di Chimica Fisica ed Elettrochimica, Università
DETERMINATION OF THE ACIDIC PROPERTIES OF MODIFIED SILICAS BY THERMOGRAVIMETRIC ANALYSIS Antonella Gervasini, Simona Bennici e Paolo Carniti Dipartimento di Chimica Fisica ed Elettrochimica, Università
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti.
 Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Al Prof. Mario Beccari, professore ordinario di Impianti Chimici, va il mio ringraziamento per aver elaborato gli argomenti riportati qui.
 Al Prof. Mario Beccari, professore ordinario di Impianti Chimici, va il mio ringraziamento per aver elaborato gli argomenti riportati qui. Nota per gli studenti. Sono stati usati simboli diversi da quelli
Al Prof. Mario Beccari, professore ordinario di Impianti Chimici, va il mio ringraziamento per aver elaborato gli argomenti riportati qui. Nota per gli studenti. Sono stati usati simboli diversi da quelli
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Fisica Generale 1 per Chimica Formulario di Termodinamica e di Teoria Cinetica
 Fisica Generale 1 per Chimica Formulario di Termodinamica e di Teoria Cinetica Termodinamica Equazione di Stato: p = pressione ; V = volume ; T = temperatura assoluta ; n = numero di moli ; R = costante
Fisica Generale 1 per Chimica Formulario di Termodinamica e di Teoria Cinetica Termodinamica Equazione di Stato: p = pressione ; V = volume ; T = temperatura assoluta ; n = numero di moli ; R = costante
TERMODINAMICA DI UNA REAZIONE DI CELLA
 TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI
 TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia
 Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
SOLUZIONE ESERCIZIO 1.1
 SOLUZIONE ESERCIZIO 1.1 La temperatura di fusione ed il coefficiente di espansione termica di alcuni metalli sono riportati nella tabella e nel diagramma sottostante: Metallo Temperatura di fusione [ C]
SOLUZIONE ESERCIZIO 1.1 La temperatura di fusione ed il coefficiente di espansione termica di alcuni metalli sono riportati nella tabella e nel diagramma sottostante: Metallo Temperatura di fusione [ C]
Simulazione test di ingresso Ingegneria Industriale Viterbo. Quesiti di Logica, Chimica e Fisica. Logica
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 1-4 - 10-22 - 46-94 -... A) 188 B) 190 C) 200 D) 47 L2
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 1-4 - 10-22 - 46-94 -... A) 188 B) 190 C) 200 D) 47 L2
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
RICHIAMI DI TERMOCHIMICA
 CAPITOLO 5 RICHIAMI DI TERMOCHIMICA ARIA TEORICA DI COMBUSTIONE Una reazione di combustione risulta completa se il combustibile ha ossigeno sufficiente per ossidarsi completamente. Si ha combustione completa
CAPITOLO 5 RICHIAMI DI TERMOCHIMICA ARIA TEORICA DI COMBUSTIONE Una reazione di combustione risulta completa se il combustibile ha ossigeno sufficiente per ossidarsi completamente. Si ha combustione completa
Dissociazione elettrolitica
 Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
CORSO DI FISICA TECNICA e SISTEMI ENERGETICI
 CORSO DI FISICA TECNICA e SISTEMI ENERGETICI Esercitazione 2 Proff. P. Silva e G. Valenti - A.A. 2009/2010 Ottimizzazione di un gruppo frigorifero per il condizionamento Dati di impianto: Potenza frigorifera
CORSO DI FISICA TECNICA e SISTEMI ENERGETICI Esercitazione 2 Proff. P. Silva e G. Valenti - A.A. 2009/2010 Ottimizzazione di un gruppo frigorifero per il condizionamento Dati di impianto: Potenza frigorifera
FARMACODINAMICA RECETTORI ED EFFETTORI
 FARMACODINAMICA I recettori per i farmaci Prof. Renato Bernardini RECETTORI ED EFFETTORI Farmaco (Φαρµακον) = principio attivo Recettore = macromolecole deputate alla trasmissione di un segnale chimico
FARMACODINAMICA I recettori per i farmaci Prof. Renato Bernardini RECETTORI ED EFFETTORI Farmaco (Φαρµακον) = principio attivo Recettore = macromolecole deputate alla trasmissione di un segnale chimico
SCALA DEI PESI ATOMICI RELATIVI E MEDI
 SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
MASSE ATOMICHE. 1,000 g di idrogeno reagiscono con 7,9367 g di ossigeno massa atomica ossigeno=2 x 7,9367=15,873 g (relativa all'idrogeno)
 MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
Indice generale. Prefazione
 26-10-2009 10:41 Pagina VI Prefazione Ringraziamenti dell Editore Guida alla lettura XIII XV XVII Capitolo 0 Lessico della chimica 1 0.1 La chimica 1 0.1.1 Classificazioni della materia 2 0.1.2 Proprietà
26-10-2009 10:41 Pagina VI Prefazione Ringraziamenti dell Editore Guida alla lettura XIII XV XVII Capitolo 0 Lessico della chimica 1 0.1 La chimica 1 0.1.1 Classificazioni della materia 2 0.1.2 Proprietà
Università telematica Guglielmo Marconi. Chimica
 Università telematica Guglielmo Marconi Chimica 1 Termodinamica 1 Argomenti Nell unità didattica dedicata alla termodinamica verranno affrontati i seguenti argomenti: L energia interna di un sistema Le
Università telematica Guglielmo Marconi Chimica 1 Termodinamica 1 Argomenti Nell unità didattica dedicata alla termodinamica verranno affrontati i seguenti argomenti: L energia interna di un sistema Le
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
La fisica di Feynmann Termodinamica
 La fisica di Feynmann Termodinamica 3.1 TEORIA CINETICA Teoria cinetica dei gas Pressione Lavoro per comprimere un gas Compressione adiabatica Compressione della radiazione Temperatura Energia cinetica
La fisica di Feynmann Termodinamica 3.1 TEORIA CINETICA Teoria cinetica dei gas Pressione Lavoro per comprimere un gas Compressione adiabatica Compressione della radiazione Temperatura Energia cinetica
Corso di Laurea in FARMACIA
 Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
I SISTEMI DI UNITA DI MISURA
 Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
ANALISI MULTIVARIATA
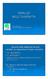 ANALISI MULTIVARIATA Marcella Montico Servizio di epidemiologia e biostatistica... ancora sulla relazione tra due variabili: la regressione lineare semplice VD: quantitativa VI: quantitativa Misura la
ANALISI MULTIVARIATA Marcella Montico Servizio di epidemiologia e biostatistica... ancora sulla relazione tra due variabili: la regressione lineare semplice VD: quantitativa VI: quantitativa Misura la
Elettrolita forte = specie chimica che in soluzione si dissocia completamente (l equilibrio di dissociazione è completamente spostato verso destra)
 A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 6: Equilibri in soluzione: equilibri acido/base, idrolisi e tamponi (6 h)
A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 6: Equilibri in soluzione: equilibri acido/base, idrolisi e tamponi (6 h)
SDD - Seconde Equilibrio e ph. Equilibrio e ph. Obiettivo
 1 Obiettivo Capire che cosa è il ph, apprendere le leggi fondamentali che lo controllano e capire qualitativamente le applicazioni delle soluzioni tampone. Prerequisiti Il concetto di equilibrio (che comunque
1 Obiettivo Capire che cosa è il ph, apprendere le leggi fondamentali che lo controllano e capire qualitativamente le applicazioni delle soluzioni tampone. Prerequisiti Il concetto di equilibrio (che comunque
3 Variabile intensiva coniugata alla quantità di moto 1
 EQUILIBRIO ERMODINAMICO LOCALE Contents 1 Variabili termodinamiche locali 1 2 Quantità di moto 1 3 Variabile intensiva coniugata alla quantità di moto 1 4 Densità delle variabili estensive 2 5 Equilibrio
EQUILIBRIO ERMODINAMICO LOCALE Contents 1 Variabili termodinamiche locali 1 2 Quantità di moto 1 3 Variabile intensiva coniugata alla quantità di moto 1 4 Densità delle variabili estensive 2 5 Equilibrio
ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016. CLASSI SECONDE ITI, SEZ. H,G, Disciplina:CHIMICA E LABORATORIO
 ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016 CLASSI SECONDE ITI, SEZ. H,G, Disciplina:CHIMICA E LABORATORIO PROGETTAZIONE DIDATTICA ANNUALE Elaborata conformemente alle linee
ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016 CLASSI SECONDE ITI, SEZ. H,G, Disciplina:CHIMICA E LABORATORIO PROGETTAZIONE DIDATTICA ANNUALE Elaborata conformemente alle linee
UNIVERSITA DEGLI STUDI DI PADOVA DIPARTIMENTO DI INGEGNERIA IDRAULICA, MARITTIMA E GEOTECNICA
 UNIVERSITA DEGLI STUDI DI PADOVA DIPARTIMENTO DI INGEGNERIA IDRAULICA, MARITTIMA E GEOTECNICA CORSO DI COSTRUZIONI IDRAULICHE A.A. 00-0 PROF. LUIGI DA DEPPO ING. NADIA URSINO ESERCITAZIONE N : Progetto
UNIVERSITA DEGLI STUDI DI PADOVA DIPARTIMENTO DI INGEGNERIA IDRAULICA, MARITTIMA E GEOTECNICA CORSO DI COSTRUZIONI IDRAULICHE A.A. 00-0 PROF. LUIGI DA DEPPO ING. NADIA URSINO ESERCITAZIONE N : Progetto
Chimica. Ingegneria Meccanica, Elettrica e Civile Simulazione d'esame
 Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
Voltammetria ciclica (CV)
 Voltammetria ciclica (CV) La voltammetria ciclica è un evoluzione di quella a scansione lineare, realizzata imponendo all elettrodo una scansione di potenziale triangolare: In questo caso il primo tratto
Voltammetria ciclica (CV) La voltammetria ciclica è un evoluzione di quella a scansione lineare, realizzata imponendo all elettrodo una scansione di potenziale triangolare: In questo caso il primo tratto
K [H 2 O] 2 = K w = [H 3 O + ][OH ]
![K [H 2 O] 2 = K w = [H 3 O + ][OH ] K [H 2 O] 2 = K w = [H 3 O + ][OH ]](/thumbs/27/10717050.jpg) Autoionizzazione dell acqua L acqua pura allo stato liquido è un debole elettrolita anfiprotico. L equilibrio di dissociazione è: 2H 2 O H 3 O + + OH - [H 3 O + ][OH ] K = [H 2 O] 2 Con K
Autoionizzazione dell acqua L acqua pura allo stato liquido è un debole elettrolita anfiprotico. L equilibrio di dissociazione è: 2H 2 O H 3 O + + OH - [H 3 O + ][OH ] K = [H 2 O] 2 Con K
ENERGIA NELLE REAZIONI CHIMICHE
 ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
Prova scritta di Fisica Generale I Corso di studio in Astronomia 22 giugno 2012
 Prova scritta di Fisica Generale I Corso di studio in Astronomia 22 giugno 2012 Problema 1 Due carrelli A e B, di massa m A = 104 kg e m B = 128 kg, collegati da una molla di costante elastica k = 3100
Prova scritta di Fisica Generale I Corso di studio in Astronomia 22 giugno 2012 Problema 1 Due carrelli A e B, di massa m A = 104 kg e m B = 128 kg, collegati da una molla di costante elastica k = 3100
modulo: CHIMICA DEI POLIMERI
 CORSO PON Esperto nella progettazione, caratterizzazione e lavorazione di termoplastici modulo: CHIMICA DEI POLIMERI Vincenzo Venditto influenza delle caratteristiche strutturali, microstrutturali e morfologiche
CORSO PON Esperto nella progettazione, caratterizzazione e lavorazione di termoplastici modulo: CHIMICA DEI POLIMERI Vincenzo Venditto influenza delle caratteristiche strutturali, microstrutturali e morfologiche
COMPITO DI CHIMICA DEL 19-04-2013
 COMPITO DI CHIMICA DEL 19-04-2013 1) Una certa quantità di solfato di ferro (II), sciolta in una soluzione acquosa di acido solforico, viene trattata con 1.0 10-3 mol di permanganato di potassio. Si ottengono
COMPITO DI CHIMICA DEL 19-04-2013 1) Una certa quantità di solfato di ferro (II), sciolta in una soluzione acquosa di acido solforico, viene trattata con 1.0 10-3 mol di permanganato di potassio. Si ottengono
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
La mobilità degli elementi chimici
 La mobilità degli elementi chimici Gli ioni contenuti nella parte sinistra del diagramma sono quelli che in soluzione si presentano sotto forma di cationi semplici. Gli ioni nella parte centrale del diagramma
La mobilità degli elementi chimici Gli ioni contenuti nella parte sinistra del diagramma sono quelli che in soluzione si presentano sotto forma di cationi semplici. Gli ioni nella parte centrale del diagramma
Programmazione di CHIMICA ANALITICA E STRUMENTALE. Classe: 4 a A CHIMICI
 R E P U B B L I C A I T A L I A N A I.T.I. MINERARIO G. ASPRONI - IGLESIAS A.S. 2014-2015 Programmazione di CHIMICA ANALITICA E STRUMENTALE Classe: 4 a A CHIMICI INSEGNANTE TEORICO Silvia Chinedda INSEGNANTE
R E P U B B L I C A I T A L I A N A I.T.I. MINERARIO G. ASPRONI - IGLESIAS A.S. 2014-2015 Programmazione di CHIMICA ANALITICA E STRUMENTALE Classe: 4 a A CHIMICI INSEGNANTE TEORICO Silvia Chinedda INSEGNANTE
I GAS GAS IDEALI. PV=nRT. Pressione Volume numero di moli Temperatura Costante dei gas. P V n T R. n, T= cost Legge di Boyle
 I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012)
 CORSO DI LAUREA IN SCIENZE BIOLOGICHE Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012) 1) Bilanciare la seguente ossidoriduzione: KMnO 4 + H 2 O 2 + H 2 SO 4 MnSO 4 + K 2 SO 4 + O 2 + H
CORSO DI LAUREA IN SCIENZE BIOLOGICHE Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012) 1) Bilanciare la seguente ossidoriduzione: KMnO 4 + H 2 O 2 + H 2 SO 4 MnSO 4 + K 2 SO 4 + O 2 + H
Il Metodo Scientifico
 Unita Naturali Il Metodo Scientifico La Fisica si occupa di descrivere ed interpretare i fenomeni naturali usando il metodo scientifico. Passi del metodo scientifico: Schematizzazione: modello semplificato
Unita Naturali Il Metodo Scientifico La Fisica si occupa di descrivere ed interpretare i fenomeni naturali usando il metodo scientifico. Passi del metodo scientifico: Schematizzazione: modello semplificato
Programmi relativi ai quesiti delle prove di ammissione ai corsi di. Odontoiatria e Protesi Dentaria, in Medicina Veterinaria e ai corsi di
 Programmi relativi ai quesiti delle prove di ammissione ai corsi di Odontoiatria e Protesi Dentaria, in Medicina Veterinaria e ai corsi di laurea delle professioni sanitarie Per l ammissione ai corsi è
Programmi relativi ai quesiti delle prove di ammissione ai corsi di Odontoiatria e Protesi Dentaria, in Medicina Veterinaria e ai corsi di laurea delle professioni sanitarie Per l ammissione ai corsi è
7 Esercizi e complementi di Elettrotecnica per allievi non elettrici. Circuiti elementari
 7 Esercizi e complementi di Elettrotecnica per allievi non elettrici Circuiti elementari Gli esercizi proposti in questa sezione hanno lo scopo di introdurre l allievo ad alcune tecniche, semplici e fondamentali,
7 Esercizi e complementi di Elettrotecnica per allievi non elettrici Circuiti elementari Gli esercizi proposti in questa sezione hanno lo scopo di introdurre l allievo ad alcune tecniche, semplici e fondamentali,
L H 2 O nelle cellule vegetali e
 L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
LEZIONE 5-6 GAS PERFETTI, CALORE, ENERGIA TERMICA ESERCITAZIONI 1: SOLUZIONI
 LEZIONE 5-6 G PERFETTI, CLORE, ENERGI TERMIC EERCITZIONI 1: OLUZIONI Gas Perfetti La temperatura è legata al movimento delle particelle. Un gas perfetto (ovvero che rispetta la legge dei gas perfetti PV
LEZIONE 5-6 G PERFETTI, CLORE, ENERGI TERMIC EERCITZIONI 1: OLUZIONI Gas Perfetti La temperatura è legata al movimento delle particelle. Un gas perfetto (ovvero che rispetta la legge dei gas perfetti PV
Correnti e circuiti a corrente continua. La corrente elettrica
 Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
C V. gas monoatomici 3 R/2 5 R/2 gas biatomici 5 R/2 7 R/2 gas pluriatomici 6 R/2 8 R/2
 46 Tonzig La fisica del calore o 6 R/2 rispettivamente per i gas a molecola monoatomica, biatomica e pluriatomica. Per un gas perfetto, il calore molare a pressione costante si ottiene dal precedente aggiungendo
46 Tonzig La fisica del calore o 6 R/2 rispettivamente per i gas a molecola monoatomica, biatomica e pluriatomica. Per un gas perfetto, il calore molare a pressione costante si ottiene dal precedente aggiungendo
Lo stato gassoso e le caratteristiche dei gas
 Lo stato gassoso e le caratteristiche dei gas 1. I gas si espandono fino a riempire completamente e ad assumere la forma del recipiente che li contiene 2. Igasdiffondonounonell altroesonoingradodimescolarsiintuttiirapporti
Lo stato gassoso e le caratteristiche dei gas 1. I gas si espandono fino a riempire completamente e ad assumere la forma del recipiente che li contiene 2. Igasdiffondonounonell altroesonoingradodimescolarsiintuttiirapporti
1 atm = 760 mm Hg = 760 torr = 101300 N/m 2 =101300 Pa. Anodo = Polo Positivo Anione = Ione Negativo. Catodo = Polo Negativo Catione = Ione Positivo
 1) Concetti Generali 1. Unità di Misura: A. Pressione 1 atm = 760 mm Hg = 760 torr = 101300 N/m 2 =101300 Pa. B. Calore 1 joule = 10 7 Erg. 1 caloria = 4,185 joule. Anodo = Polo Positivo Anione = Ione
1) Concetti Generali 1. Unità di Misura: A. Pressione 1 atm = 760 mm Hg = 760 torr = 101300 N/m 2 =101300 Pa. B. Calore 1 joule = 10 7 Erg. 1 caloria = 4,185 joule. Anodo = Polo Positivo Anione = Ione
Esercitazione 8. Gli equilibri acido-base: Ka, Kb. L autoprotolisi dell acqua. Misura del ph Soluzioni tampone 1,0 10-14
 Esercitazione 8 Misura del ph Soluzioni tampone Gli equilibri acido-base: Ka, Kb HA + H 2 O! H 3 O + + A - Ka = [H 3 O+ ][A - ] [HA] A - + H 2 O! OH - + HA Kb = [OH- ][HA] [A - ] Ka Kb = [ H 3 O + ] [
Esercitazione 8 Misura del ph Soluzioni tampone Gli equilibri acido-base: Ka, Kb HA + H 2 O! H 3 O + + A - Ka = [H 3 O+ ][A - ] [HA] A - + H 2 O! OH - + HA Kb = [OH- ][HA] [A - ] Ka Kb = [ H 3 O + ] [
I FENOMENI TERMICI. I fenomeni termici Fisica Medica Lauree triennali nelle Professioni Sanitarie. P.Montagna ott-07. pag.1
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano pag.1
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano pag.1
Studio di funzione. Tutti i diritti sono riservati. E vietata la riproduzione, anche parziale, senza il consenso dell autore. Funzioni elementari 2
 Studio di funzione Copyright c 2009 Pasquale Terrecuso Tutti i diritti sono riservati. E vietata la riproduzione, anche parziale, senza il consenso dell autore. Funzioni elementari 2 Studio di funzione
Studio di funzione Copyright c 2009 Pasquale Terrecuso Tutti i diritti sono riservati. E vietata la riproduzione, anche parziale, senza il consenso dell autore. Funzioni elementari 2 Studio di funzione
