UNIVERSITA DEGLI STUDI DI GENOVA
|
|
|
- Roberta Marchetti
- 9 anni fa
- Просмотров:
Транскрипт
1 UNIVERSITA DEGLI STUDI DI GENOVA Facoltà di Scienze M.F.N. Dipartimento di Fisica Corso di Laurea Magistrale in FISICA TERAPIA INNOVATIVA CON ITTRIO-90 PER LA CURA DEI TUMORI EPATICI Tesi di Laurea di: Erica MURRU Relatori Prof. Sandro Squarcia Prof. Maria Claudia Bagnara Correlatore Prof. Paolo Prati Anno accademico
2 INDICE PREMESSA... 2 INTRODUZIONE... 5 CAPITOLO 1: CHE COSA È LA MEDICINA NUCLEARE? LA MEDICINA NUCLEARE LA GAMMA CAMERA LA SPECT LA PET CAPITOLO 2: LA TERAPIA RADIOEMBOLIZZANTE CON 90 Y ASPETTI CLINICI CARATTERISTICHE DELLE MICROSFERE DI 90 Y SELEZIONE DEL PAZIENTE PERCORSO DEL PAZIENTE STUDIO PREVISIONALE: SPECT CON MAA VERIFICA DI CONTROLLO: SPECT E PET/TC POST TERAPIA ASPETTI DI FISICA MEDICA E RADIOPROTEZIONE CAPITOLO 3: LA DOSIMETRIA RELAZIONI DOSIMETRICHE SIR-SPHERES THERASPHERE VOXEL DOSIMETRY CAPITOLO 4: MISURE DI ATTIVITÀ IL CALIBRATORE DI ATTIVITÀ CONTROLLI DI QUALITÀ SUI CALIBRATORI DI ATTIVITÀ CALIBRAZIONE DELLA VIAL CONTENENTE LE MICROSFERE DI 90 Y CAPITOLO 5: I RISULTATI SPERIMENTALI METODO EMPIRICO METODO DELLA BSA METODO PARTITIVO VOXEL DOSIMETRY VERIFICA ATTIVITÀ SOMMINISTRATA ED ELABORAZIONI POST-TRATTAMENTO DATABASE PAZIENTI CONCLUSIONI APPENDICE BIBLIOGRAFIA
3 PREMESSA In questa tesi vengono trattati, dal punto di vista della Fisica Medica e Sanitaria, i vari processi di una terapia innovativa per la cura di tumori epatici non operabili, in pazienti portatori di HCC (carcinoma epatocellulare) o di metastasi epatiche da carcinoma colorettale. Tale terapia viene solitamente indicata come Terapia Radioembolizzante Transarteriale (TARE) o Radioterapia Interna Selettiva (SIRT) con Ittrio-90 ( 90 Y). Il principio è la somministrazione locale intra-arteriosa di microsfere di vetro o resina del diametro di µm, nelle quali vi è incorporato il radionuclide 90 Y (che emette radiazioni β), con modalità analoga ad altre terapie mediche che utilizzano microsfere a rilascio di farmaco. La TARE La TARE, introdotta nel capitolo successivo, può essere, nei suoi aspetti più generali, così sintetizzata: Step 1: valutazione di fattibilità della terapia Durante la prima fase viene effettuata la valutazione di fattibilità della terapia, con: esami clinici di routine, tra cui una AngioTC (TAC con mezzo di contrasto che visualizza l anatomia dei vasi arteriosi e la loro vascolarizzazione); esame angiografico epatico e di altri distretti arteriosi afferenti al tumore, effettuato dal radiologo interventista in sala angiografica, per valutare l anatomia vascolare della regione di interesse ed eventualmente embolizzare arterie extraepatiche afferenti alle lesioni target (bersaglio); nella stessa sede, simulazione del trattamento radioembolizzante con l'iniezione di Macroaggregati di Albumina (MAA) marcati con Tecnezio-99m ( 99m Tc-MAA) nel o nei rami arteriosi target effettuata dal medico nucleare; entro un ora, esecuzione di scintigrafie in Medicina Nucleare, allo scopo di rilevare la presenza di accumuli extraepatici del radiofarmaco, che potrebbero controindicare il trattamento TARE; studio fisico-dosimetrico personalizzato per il paziente in questione al fine di calcolare l attività di sfere marcate con 90 Y da somministrare al paziente per il trattamento della neoplasia, effettuato dal fisico medico, sulla base dei dati dell esame AngioTC, delle scintigrafie e delle informazioni cliniche rilevanti. Step 2: esecuzione del trattamento TARE Entro un mese dallo studio preliminare va effettuata la seconda fase, che è la terapia vera e propria, cioè: il medico nucleare, affiancato dal radiologo interventista, somministra il quantitativo prescritto di microsfere marcate con 90 Y, tramite cateterismo 2
4 vascolare selettivo intraepatico, secondo i dati strumentali e dosimetrici ottenuti nella fase 1; durante e al termine della procedura il fisico medico effettua misure radiometriche per scopi di radioprotezione; La quantità di attività di radionuclide da somministrare, calcolata a partire dallo studio dosimetrico individualizzato pre-trattamento, deve essere preparata in medicina nucleare secondo le procedure indicate dal fisico medico. L impianto deve essere effettuato presso una sala di Radiologia Interventistica in quanto va eseguito durante una procedura di cateterismo con controllo angiografico. Step 3: verifica del trattamento TARE Il giorno successivo il paziente effettua in Medicina Nucleare l esame SPECT (basato sulla radiazione di bremsstrahlung dell 90 Y) e l esame 90 Y-PET-TC (basato sulla radiazione prodotta dall 90 Y), per la verifica della procedura terapeutica e lo studio fisico-dosimetrico retrospettivo effettuato dal fisico medico. Step 4: follow up L esito della terapia viene seguito nel tempo con una serie di procedure cliniche e diagnostiche sul paziente. Scopo del lavoro di tesi All inizio del lavoro si è cercato di raccogliere in Letteratura quante più informazioni possibili riguardo questa terapia innovativa, anche sulla base delle esperienze di altri ospedali. Si è passati poi ad analizzare tutte le procedure adottate e i risultati ottenuti riguardanti i trattamenti fino a quel momento effettuati all Ospedale San Martino di Genova (ancora in maniera poco sistematica e non approfondita) per poter standardizzare le linee guida di questa terapia e rendere più efficaci alcuni dei suoi processi. Per questo si è costruito un database completo di tutti i dati rilevanti per questa ricerca (vedi Capitolo 5, paragrafo 5.6). Scopo del lavoro di tesi è stato quindi quello di approfondire gli aspetti, di interesse per il fisico medico, connessi con la terapia TARE, e collaborare con il reparto di Fisica Medica e Sanitaria dell IRCCS San Martino-IST (presso il quale si è svolto il lavoro) alla messa a punto della metodica di routine: raccolta e archiviazione dei dati clinici, fisici e dosimetrici dei pazienti trattati presso l IRCCS dal 2014 in poi e aggiornamento con quelli trattati durante il periodo del lavoro di tesi (2015); messa a punto di fogli Excel da utilizzare per l effettuazione dello studio fisicodosimetrico, implementando due diverse metodiche dosimetriche; apparecchiature: operazioni di taratura del calibratore di attività per l isotopo 90 Y, il cui uso non è normalmente previsto per tali strumenti; operazioni di 3
5 taratura e ottimizzazione della gamma camera e del tomografo PET per l utilizzo con l 90 Y, il cui uso non è normalmente previsto per tali strumenti; partecipazione a tutte le fasi, compresa quella nella sala dell intervento, per alcuni trattamenti; per alcuni pazienti, elaborazione delle immagini di Medicina Nucleare per effettuare lo studio fisico-dosimetrico pre-trattamento e la verifica retrospettiva. 4
6 INTRODUZIONE I tumori del fegato e la TARE Il fegato, situato nella parte destra dell addome, è il più grande organo del corpo ed è fondamentale per uno stato di buona salute di una persona: rimuove le sostanze di scarto dal sangue e produce la bile e molti enzimi necessari alla digestione. I tumori primari del fegato (cioè quelli nati nell organo stesso e non provocati da cellule staccatesi da altri tumori e migrate fino al fegato, le cosiddette metastasi) hanno per lo più inizio dalle cellule interne dell organo, chiamate epatociti. In questo caso si parla di carcinoma epatocellulare; questi tumori tendono a diffondersi alle ossa e ai polmoni. Più spesso, tuttavia, le neoplasie che colpiscono il fegato sono secondarie, cioè derivano da tumori che nascono altrove (per esempio nel colon). Una volta che si è accertata la presenza di un tumore del fegato, il medico effettua la stadiazione, cioè la definizione del grado di malignità e di espansione del tumore finalizzata alla programmazione della cura. Questa fase è particolarmente importante nel caso del tumore del fegato in quanto si decide se è possibile o meno procedere per via chirurgica. Nella maggior parte dei casi, infatti, questi tumori non possono essere rimossi con il bisturi (la diagnosi è tardiva perché i sintomi sono silenti, e il fegato è già troppo compromesso). La terapia radioembolizzante transarteriale può essere utilizzata proprio in pazienti con tumori epatici primitivi per i quali la rimozione chirurgica del tumore non è possibile o in pazienti con metastasi secondarie al fegato che non rispondono più alla chemioterapia. La TARE si caratterizza per essere una procedura gestita in maniera multidisciplinare, con la presenza di competenze chirurgiche, gastroenterologiche, radiologiche, medico-nucleari e fisiche, tali da rendere possibile l esecuzione del trattamento in maniera sicura ed efficace. Dal momento che ogni paziente costituisce un caso a sé è difficile stabilire a priori i benefici del trattamento TARE in maniera generale, ma si può affermare che tale terapia potrebbe ridurre la dimensione del tumore, stabilizzare la malattia e quindi prolungare la sopravvivenza dei pazienti, aumentando le possibilità di affrontare la rimozione chirurgica del tumore o di essere sottoposti a un trapianto. Il primo studio sul trattamento radioembolizzante con 90 Y dell'epatocarcinoma è stato condotto dal gruppo multidisciplinare per la diagnosi e la cura del carcinoma epatocellulare (HCC) dell'istituto Tumori di Milano negli anni ed è stato pubblicato su Hepatology 1 nel maggio Questa ricerca ha riportato una risposta obiettiva pari al 40,4% e una risposta completa al 9,6%. Tali percentuali dimostrano l'efficacia di questa procedura nella terapia dell'hcc negli stadi intermedio e 1 : Hepatology è il manifesto ufficiale dell AASLD (American Association for the Study of Liver Diseases). Questa rivista contiene gli ultimi risultati della ricerca, nonché altri dati scientifici rilevanti. 5
7 avanzato: stadio B e C della classificazione BCLC 2. In particolare da detta ricerca emerge l'efficacia di 90 Y-TARE nel trattamento dello stadio avanzato dell' HCC (stadio C della classificazione BCLC) con trombosi portale; risulta invece controindicata la Chemioembolizzazione Trans-Arteriosa (TACE). In Letteratura, esistono anche altre esperienze positive circa l'utilizzo di 90 Y-TARE. In una recente valutazione metanalitica, svolta da Price e Karapetis nel 2009, si identificano due trial randomizzati che paragonano 90 Y-TARE al trattamento chemioterapico nei pazienti con il carcinoma del colon retto avanzato metastatico al fegato. Successivamente, è stato pubblicato uno studio randomizzato su 44 pazienti che ha dimostrato un raddoppio del tempo a progressione epatica della malattia, grazie alla TARE rispetto alla sola CT (Chemioterapia). Essendo tale studio limitato ad un numero circoscritto di pazienti ne è stato disegnato uno su larga scala con l obiettivo di confrontare il trattamento TARE con l attuale gold-standard. Pertanto nel 2010 è iniziato lo studio anglo-australiano SIRFLOX-FOXFIRE che in 4 anni ha reclutato 1000 pazienti e che presto (1-2 anni) dovrebbe dare una risposta definitiva. Numerosità In Italia l'incidenza dell'hcc è di circa 110 nuovi casi su un milione all anno, per cui in Liguria possiamo stimare la presenza di circa 160 nuovi casi in un anno. Considerato però che la 90 Y-TARE è riservata a solo 2 dei complessivi 5 stadi in cui si può presentare la malattia, e che nell'ambito dei 2 stadi vi è una ulteriore selezione sulla base della valutazione clinica del singolo paziente, è stimabile che il trattamento possa interessare a non più di 10 casi all anno. Quanto appena affermato è da riferirsi ai soli primi due anni dell'esperienza. Infatti nel caso di ulteriori conferme dell efficacia del trattamento è evidente che la richiesta potrebbe aumentare (difficilmente potrebbe superare i 25 casi all anno). Attualmente è ancora abbastanza contenuto il numero di Centri in Italia in grado di fornire la prestazione: oltre all IRCCS San Martino-IST, vi è solo l IRCCS Mi - Ist. Tumori, l A.O.U. Sant' Orsola Malpighi di Bologna, il Policlinico A. Gemelli di Roma, l A.O. S. Maria Goretti di Latina, e l IRCCS Na - Ist. Tumori. Va comunque considerato che altri Centri in Italia si stanno organizzando per fornire la procedura in modo standardizzato. 2 : Barcellona Clinic Liver Cancer (BCLC) è un sistema di stadiazione che consente la stratificazione dei pazienti portatori di HCC in gruppi (0, A, B, C, D) sulla base delle caratteristiche della neoplasia. 6
8 CAPITOLO 1: Che cosa è la Medicina Nucleare? 1.1 La Medicina Nucleare La medicina nucleare è quella branca della medicina che utilizza sostanze radioattive (radiofarmaci) in diagnostica e in terapia. Le metodiche diagnostiche consistono nello studio e nell analisi della fissazione di un radionuclide legato a una molecola carrier (di trasporto), che segue l'attività metabolica di un tessuto o si fissa a quest'ultimo mediante l'interazione con opportuni recettori. La terapia radiometabolica si effettua impiegando sostanze radioattive che, legandosi ai tessuti patologici con meccanismi simili ai radionuclidi usati in campo diagnostico, consentono di irraggiarli in maniera selettiva e con un'elevata dose di radiazione ad alto LET (come le particelle beta meno o alpha) risparmiando in larga misura i tessuti sani. Le apparecchiature utilizzate per la produzione di immagini (gamma camera per le scintigrafie e PET per le tomografie ad emissione di positroni) utilizzano dei cristalli a scintillazione che consentono la visualizzazione della zone di fissazione del radionuclide all'interno dell'organismo. Tali cristalli emettono luce quando vengono colpiti dalla radiazione gamma, emessa direttamente dal radiofarmaco che viene iniettato al paziente o generata per annichilazione dei positroni emessi dai radiofarmaci per la PET (in quest'ultimo caso vengono ricercati gli eventi di coincidenza). La luce così rilevata è poi convertita in un segnale elettrico-digitale per l'analisi computerizzata. Mediante acquisizioni tomografiche è inoltre possibile lo studio tridimensionale del particolare organo da studiare (PET e SPECT). Il radionuclide più utilizzato in diagnostica con gamma camera è il 99m Tc, che emette radiazioni gamma con energia di 140 kev (ottimali per la gamma camera) ed ha un'emivita di circa 6 ore, compatibile con la durata degli esami ma comunque abbastanza breve da consentire una limitata irradiazione del paziente e della popolazione. Il 99m Tc viene prodotto tramite un generatore 99 Mo/ 99m Tc che ne garantisce un'ottima disponibilità. Altri radionuclidi di comune utilizzo per diagnostica con la gamma camera sono: Indio-111; Iodio-123, 125 e 131 (quest ultimo presenta inoltre una componente beta meno, sfruttata per la terapia radiometabolica). I radiofarmaci beta più emittenti, per la diagnostica con la metodica PET, sono in gran parte legati al Fluoro-18, che emette radiazione gamma con energia di 511 kev (secondaria all annichilazione del positrone, come tutti i beta più emettitori) ed ha un'emivita di circa 2 ore. Un altro radionuclide utilizzato per diagnostica PET ma prodotto con generatore è il Ga-68. I centri che dispongono di un ciclotrone utilizzano anche molecole marcate con Carbonio-11 o Azoto-13. Essi decadono in 7
9 tempi brevi (tempi di dimezzamento nell'ordine dei minuti) e quindi necessitano di questa macchina nelle vicinanze per il loro ottenimento. I radiofarmaci più utilizzati, per la terapia medico-nucleare sono: I-131 per la terapia delle malattie tiroidee; Samario-153, Stronzio-89 e Radio-223 per la terapia delle metastasi ossee; Ittrio-90 per il trattamento dei linfomi ed altri tumori, per il trattamento locale delle artropatie infiammatorie croniche (radiosinoviortesi); Renio-186 e Erbio-169 per altre terapie radiometaboliche. 1.2 La Gamma Camera La gamma camera (vedi Figura 1) è costituita da due elementi fondamentali: il collimatore e un sistema di localizzazione fotonica. Il collimatore è costituito da una lastra di materiale assorbente (solitamente piombo) in cui sono praticati dei fori. In tal modo, possono passare attraverso i fori esclusivamente i raggi che si muovono nella direzione scelta, mentre i restanti verranno assorbiti. Esistono collimatori con diverse geometrie di fori. Lo spessore dei setti fra i fori e la lunghezza degli stessi determina da un lato la definizione spaziale del sistema e dall'altro l'efficienza di rilevazione (quanti fotoni del totale che raggiungono il collimatore sono rilevati dalla gamma camera). Differenti spessori e lunghezze sono quindi necessarie, a seconda dell'energia dei fotoni incidenti (fotoni più energetici attraversano un maggiore spessore di piombo), per raggiungere il miglior compromesso fra quantità di "rumore" presente nell'immagine finale (dovuta ad interazioni con fotoni non voluti, ad esempio che hanno subito scatter compton) e intensità di segnale. 8
10 La gamma camera Figura 1 Principi di funzionamento Questa macchina utilizza la radioattività per differenti scopi: diagnosticare la presenza di un tumore o delle sue metastasi, studiare il funzionamento del cuore o del fegato, verificare la presenza di un embolo che ostruisce un vaso sanguigno, etc. Con un'unica iniezione di tracciante radioattivo si può anche studiare tutto il corpo. La radioattività è debole e quindi non pericolosa, e la sostanza radioattiva viene eliminata entro qualche giorno. Il tracciante più comunemente utilizzato è il tecnezio. Esso viene inserito in composti sintetizzati in modo tale da essere assimilato specificamente dal tessuto da indagare. Ad esempio, volendo studiare le ossa, il tecnezio viene unito a molecole contenenti fosfato, che è un elemento di base nella formazione delle ossa. Il composto marcato così ottenuto, dopo essere stato iniettato nel corpo del paziente, si fisserà sulle ossa. Essendo radioattivo, il tecnezio emette raggi gamma rivelabili tramite la gamma camera multitesta che viene fatta muovere lentamente al di sopra del paziente disteso. Le molecole marcate con il tecnezio appaiono sullo schermo di un computer come punti scintillanti. La presenza eventuale di una concentrazione anomala in dei punti, ad esempio di un osso, evidenzia un'iperattività che spesso è sinonimo di lesione o malattia. 9
11 Applicazioni La gamma camera consente di effettuare vari tipi di acquisizione: Planar Imaging Planar Imaging Dinamico SPECT Imaging Planar Imaging Si tratta, tra questi, del più semplice protocollo di acquisizione dell'immagine. In questo caso i rivelatori sono mantenuti in posizione fissa rispetto al paziente, e i dati che si ottengono, dunque, arrivano da un'unica angolazione. L'immagine creata mediante questo tipo di acquisizione è simile ad una radiografia a raggi X. Tale protocollo si applica generalmente per gli esami delle ossa. Planar Imaging Dinamico Dal momento che la gamma camera, in un'analisi di tipo planare, viene mantenuta in posizione fissa, è possibile osservare il movimento del radiotracciante attraverso il corpo del paziente tramite l acquisizione di una serie successiva d'immagini planari, in un determinato periodo di tempo. Ciascuna proiezione è il risultato dell'insieme dei dati ottenuti durante un breve intervallo di tempo, tipicamente 1-10 secondi. Se si effettuano diverse proiezioni in un tempo più lungo, allora è possibile vedere l'animazione del movimento del tracciante e, su questa base, effettuare l'analisi dei dati. Il planar imaging dinamico è comunemente usato per misurare il flusso attraverso i filtri glomerulari renali. SPECT Imaging Ruotando la gamma camera attorno al paziente, essa acquisterà una serie di proiezioni della distribuzione del tracciante ottenute sotto differenti angolazioni. Mettendole insieme, è possibile operare la ricostruzione di un'immagine tridimensionale della distribuzione del radiofarmaco nel corpo. 1.3 La SPECT La SPECT (Single Photon Emission Computed Tomography), come già accennato, non è altro che una gamma camera utilizzata con tecnica tomografica in cui l'acquisizione dei dati si effettua mediante la rotazione delle testate di rivelazione della stessa attorno al corpo del paziente. Ad ogni diversa angolazione, viene acquisita un'immagine planare (planar imaging) detta proiezione; l'insieme di tali proiezioni consente poi di ottenere delle informazioni più realistiche, in tre dimensioni (SPECT imaging), visualizzabili sotto forma di sezioni transassiali - immagini radiologiche relative a sottili strati (di spessore inferiore a 1 cm) delle strutture corporee indagate, ricavate secondo piani assiali, cioè trasversali rispetto all asse corporeo maggiore - ottenute tramite utilizzo di appositi algoritmi di 10
12 ricostruzione. Analogamente alla PET, come vedremo, la tomografia computerizzata a singola emissione di fotoni permette di ottenere delle informazioni funzionali su un organo specifico o su tutto il corpo del paziente. La radiazione interna è amministrata per mezzo di un farmaco marcato con un isotopo radioattivo, o elemento tracciante (tipicamente il tecnezio). Esso può essere iniettato, ingerito, o inalato. L'isotopo radioattivo decade mediante emissione dei raggi gamma che, in seguito alla rivelazione, forniscono un'immagine di ciò che avviene all'interno del corpo del paziente. La SPECT sfrutta dunque una tecnologia simile alla PET ma più semplice: in questo caso infatti si impiegano dei radiofarmaci marcati con isotopi che emettono direttamente, e non secondariamente, radiazioni gamma. Come il nome stesso suggerisce (TC a emissione di singoli fotoni), i raggi gamma emessi dal tracciante radioattivo sono la sola fonte delle informazioni che si ottengono: essi vengono raccolti nella gamma camera e poi analizzati al fine di ricostruire un'immagine della struttura di provenienza. In questo modo è possibile determinare il funzionamento di un organo o di un'altra particolare struttura corporea. 1.4 La PET La tomografia a emissione di positroni (o PET, dall'inglese Positron Emission Tomography) (vedi Figura 2), come già detto, è una tecnica di diagnostica in medicina nucleare che utilizza la produzione di bioimmagini (immagini del corpo). Anche la PET fornisce informazioni di tipo fisiologico-funzionale, a differenza della TC (tomografia computerizzata) e della RM (risonanza magnetica) che invece forniscono solo informazioni di tipo morfologico del distretto anatomico esaminato. Con l'esame PET si ottengono mappe dei processi funzionali all'interno del corpo. Tomografo PET Figura 2 11
13 Principi di funzionamento La procedura inizia con l'iniezione di un radiofarmaco formato da un radio-isotopo tracciante con emivita breve legato chimicamente a una molecola attiva a livello metabolico (vettore), ad esempio il fluorodesossiglucosio ( 18 F-FDG). Dopo un tempo di attesa, durante il quale la molecola metabolicamente attiva (spesso uno zucchero) raggiunge una determinata concentrazione all'interno dei tessuti organici da analizzare, il soggetto viene posizionato nello scanner. L'isotopo di breve vita media decade, emettendo un positrone. Dopo un percorso che può raggiungere al massimo pochi millimetri, il positrone si annichila con un elettrone, producendo una coppia di fotoni gamma entrambi di energia 511 KeV ed emessi in direzioni opposte tra loro (fotoni back to back) (vedi Figura 3). Figura 3: Acquisizione dei raggi γ sulla PET Questi fotoni sono rilevati quando raggiungono uno scintillatore, nel dispositivo di scansione, e creano un lampo luminoso, rilevato attraverso dei tubi fotomoltiplicatori. Punto cruciale della tecnica è la rilevazione simultanea di coppie di fotoni: i fotoni che non raggiungono il rilevatore in coppia, cioè entro un intervallo di tempo di pochi nanosecondi, non sono presi in considerazione. Dalla misurazione della posizione in cui i fotoni colpiscono il rilevatore, si possono ricostruire gli ipotetici punti del corpo da cui sono stati emessi. Lo scanner utilizza la rilevazione delle coppie di fotoni per mappare la densità dell'isotopo nel corpo, sotto forma di immagini di sezioni (generalmente trasverse) separate fra loro di 5 mm circa. La mappa risultante rappresenta i tessuti in cui la molecola campione si è 12
14 maggiormente concentrata e viene letta e interpretata da uno specialista in medicina nucleare al fine di determinare la diagnosi ed il conseguente trattamento. I radionuclidi utilizzati nella scansione PET sono generalmente isotopi con breve tempo di dimezzamento, come 11 C (~20 min), 13 N (~10 min), 15 O (~2 min) e soprattutto 18 F (~110 min). Per via del loro basso tempo di dimezzamento, questi radioisotopi devono essere prodotti da un ciclotrone posizionato in prossimità dello scansionatore PET. Tali radionuclidi sono incorporati in composti normalmente assimilati dal corpo umano, come il glucosio, l'acqua o l'ammoniaca, e quindi iniettati nel corpo da analizzare per tracciare i luoghi nei quali vanno a distribuirsi. I composti così contrassegnati vengono chiamati radiotraccianti o radiofarmaci. Applicazioni La PET è usata estensivamente in oncologia clinica (per avere rappresentazioni dei tumori e per la ricerca di metastasi) e nelle ricerche cardiologiche e neurologiche. Metodi di indagine alternativi sono la tomografia computerizzata a raggi X (TC), l imaging a risonanza magnetica (MRI), la risonanza magnetica funzionale (RMF) e la tomografia computerizzata a ultrasuoni. Ad ogni modo, mentre gli altri metodi di scansione, come la TAC e la RMN, permettono di identificare alterazioni organiche e anatomiche nel corpo umano, le scansioni PET sono in grado di rilevare alterazioni a livello biologico molecolare che spesso precedono l'alterazione anatomica, attraverso l'uso di marcatori molecolari che presentano un diverso ritmo di assorbimento a seconda del tessuto interessato. Con una scansione PET è possibile visualizzare e quantificare con discreta precisione il cambio di afflusso sanguigno nelle varie strutture anatomiche (attraverso la misurazione nelle varie zone d interesse della concentrazione dell'emettitore di positroni iniettato). Spesso, e sempre più frequentemente, le scansioni della Tomografia a Emissione di Positroni sono raffrontate con le scansioni a Tomografia Computerizzata, fornendo informazioni sia anatomiche e morfologiche, sia metaboliche e funzionali (in sostanza, su come il tessuto o l'organo siano conformati e su come stiano operando). Per sopperire alle difficoltà tecniche e logistiche, conseguenti allo spostamento del paziente per eseguire i due esami, ed alle imprecisioni che ne deriverebbero, ci si avvale oramai esclusivamente dei tomografi PET-TAC (PET/TC), nei quali un sistema di rilevazione PET ed un tomografo TAC di ultima generazione sono assemblati in un unico gantry e controllati da un'unica consolle di comando. L'introduzione del tomografo PET-TAC ha consentito un grande miglioramento dell'accuratezza e dell'interpretabilità delle immagini (vedi Figura 4) ed una notevole riduzione dei tempi di esame. 13
15 Immagini TAC e PET sovrapposte Figura 4 La PET gioca un ruolo sempre maggiore nella verifica della risposta a determinate terapie; specialmente in particolari terapie anti-cancro. La PET è usata anche in studi pre-clinici sugli animali, dove invece le indagini ripetute sullo stesso soggetto sono consentite. Queste ricerche si sono dimostrate particolarmente valide nella ricerca sul cancro, dove si registra un aumento della qualità statistica dei dati e una sostanziale diminuzione del numero di animali richiesti per ogni singolo studio. Una limitazione alla diffusione della PET è il costo dei ciclotroni per la produzione dei radionuclidi di breve tempo di dimezzamento. Pochi ospedali e università possono permettersi l'acquisto e il mantenimento di questi costosi apparati e quindi la maggior parte dei centri PET è rifornita da produttori esterni. Questo vincolo limita l'uso della PET clinica principalmente all'utilizzo dei soli traccianti contrassegnati con il 18 F, che,avendo un tempo di dimezzamento di 110 minuti, può essere trasportato a una distanza piuttosto ragionevole prima di essere utilizzato. Anche il 68 Ga, ottenibile grazie a un generatore, permette di ottenere traccianti in maniera abbastanza agevole. 14
16 CAPITOLO 2: La Terapia Radioembolizzante con 90 Y 2.1 Aspetti clinici La Terapia Radioembolizzante Transarteriale (TARE) o Radioterapia Interna Selettiva (SIRT) con 90 Y, come già detto, è una terapia radiante loco-regionale che si effettua per i tumori epatici. Questa prevede la somministrazione locale intra-arteriosa di microsfere di vetro o resina del diametro di µm, nelle quali vi è incorporato il radionuclide 90 Y (che emette radiazioni β). La somministrazione avviene nella sala di Radiologia Interventistica, sotto controllo radiologico e con l ausilio del medico nucleare. I benefici e gli effetti tossici di questa radioembolizzazione derivano dalle radiazioni portate dall 90 Y e non dall ischemia; infatti le microsfere vanno a localizzarsi e a esplicitare la loro funzione preferenzialmente a livello del microcircolo tumorale evitando così di provocare un effetto macroembolico. Infatti alla base di tale radioembolizzazione risiede un concetto importante: i tumori epatici sviluppano una vascolarizzazione che è per almeno il 90% di tipo arterioso, mentre il parenchima epatico sano è supportato per il 70-80% dal sistema portale. Questa differente vascolarizzazione è un vantaggio per le terapie loco-regionali trans-arteriose; si può somministrare alte dosi di radiazioni con il massimo risparmio di parenchima sano. L arteria o le arterie in cui le microsfere vengono iniettate definiscono il volume di tessuto epatico esposto alla radiazione. Una volta raggiunta la microcircolazione tumorale, l 90 Y emette radiazioni β con una penetrazione tissutale media di circa 5.3 mm; questo vuol dire che la maggior parte delle radiazioni interesserà il tessuto tumorale risparmiando il parenchima sano. Poiché le microsfere andranno a localizzarsi preferenzialmente nelle arterie intra- e peri-tumorali è possibile somministrare un elevata attività radiante superiore a 50 Gy fino anche a 150 Gy (è sufficiente una dose di 120 Gy nella maggior parte dei casi). Tutto ciò è in contrasto con la radioterapia epatica esterna, limitata nella dose per problemi di tossicità ai tessuti adiacenti al tumore e che potrebbe provocare insufficienza epatica a più del 50% dei pazienti. 15
17 Arterie del fegato Figura 5 Il fegato è diviso in due lobi, destro e sinistro, e più in particolare in otto segmenti: I, II, III, IV, V, VI, VII, VIII. L'arteria epatica è il vaso arterioso principale che irrora il fegato (vedi Figura 5). Tale arteria origina dal tronco celiaco, ove viene chiamata arteria epatica comune, e in seguito si porta anteriormente e lateralmente. Durante il suo decorso emette quali suoi rami le arterie gastriche sinistra e destra e l arteria gastroduodenale. A questo punto viene denominata arteria epatica propria. Successivamente curva superiormente e posteriormente davanti alla vena porta, ramificandosi in arteria epatica destra ed arteria epatica sinistra. L'arteria epatica destra ha un decorso sinuoso, passa posteriormente al condotto coledoco, emette subito, quale sua ramificazione, l'arteria cistica, poi entra nel parenchima epatico destro, piega orizzontalmente e si divide in due ulteriori rami, uno procede anterosuperiormente ed irrora i segmenti I, V, VIII, ciascuno con un ramo, l'altro decorre lateralmente e posteriormente e fornisce rami arteriosi per il VI, VII segmento. L'arteria epatica sinistra, di minor calibro, risale superiormente, entra nel parenchima epatico sinistro e qui si divide in tre ramificazioni, una laterale per il IV segmento, una superiore per il III e una mediale per il II. Le arterie segmentali sono di tipo terminale. Il fegato possiede altresì due sistemi venosi, quello portale e quello delle vene epatiche. La vena porta ha il compito di convogliare al fegato il sangue proveniente dalla digestione intestinale e dalla milza, costituendo un sistema detto appunto sistema della vena porta o sistema portale. Poco prima di entrare nel parenchima epatico, la vena porta, si divide in sinistra e destra, con la destra di calibro maggiore. Invece le tre vene epatiche (sinistra, media e destra), tributarie della vena cava inferiore, costituiscono il secondo sistema venoso del fegato. 16
18 Indicazioni 90 Y-TARE è indicato nel trattamento dell'hcc, non metastatico, nello stadio B e C della classificazione BCLC. Talvolta viene praticata anche nella gestione dei pazienti con metastasi epatiche da cancro colorettale o comunque, sulla base dei risultati favorevoli ottenuti, nei seguenti casi: la malattia è limitata al fegato; se la malattia non è limitata al fegato, le metastasi extraepatiche non devono essere disseminate in più organi e devono essere di piccole dimensioni ( < 2cm ); la malattia nel suo complesso deve essere relativamente indolente grazie alle terapie antineoplastiche sistemiche. 2.2 Caratteristiche delle microsfere di 90 Y Le microsfere marcate con 90 Y non sono considerate un vero e proprio radiofarmaco, pur essendo utilizzate di fatto - con le stesse modalità, ma vengono invece definite come dispositivo medico, in quanto non interagiscono a livello cellulare. Il radionuclide 90 Y L 90 Y è un isotopo radioattivo dell ittrio prodotto dal decadimento dello 90 Sr, che costituisce circa il 5% degli isotopi radioattivi derivanti dalla fissazione dell uranio. L 90 Y va incontro a decadimento β - con un emivita radioattiva di circa 2,7 giorni, cioè un po più di 64 ore, e un energia di decadimento di 2,28 MeV. Il decadimento produce anche una piccola quota di fotoni di energia pari a 1,7 MeV (corrispondente allo 0,01% dell energia emessa). L interazione degli elettroni emessi con la materia può portare ad una radiazione di bremsstrahlung (Raggi X). Tabella 1 Come si può vedere anche dalla tabella 1, l 90 Y è sostanzialmente un emettitore β puro. Tabella 1 : D. Delacroix et al; Radionuclide and radiation protection data handbook; radiation protection dosimetry Vol. 98, Number 1,
19 Le Sfere Le sfere in commercio sono di due tipi: le SIR-Spheres e le TheraSphere; le loro caratteristiche, riassunte nella tabella 2, sono leggermente differenti. Characteristics SIR-Spheres TheraSphere Material Resin Glass Sphere diameter (μm) Activity in single vial (GBq) 3 six sizes: 3,5,7,10,15.20 Number of spheres per vial (range in million) Activity per sphere (Bq) Specific gravity Low High Embolic effect Moderate Mild Splitting one vial for two or more patients Possible Not possible Tabella 2 Le Therasphere (MDS Nordion, Ottawa, Canada) sono microsfere di vetro caricate con 90 Y con un diametro compreso tra 20 µm e 30 µm e attività di circa 2500 Bq per microsfera. Le fiale sono disponibili in sei diverse attività: 3 GBq, 5 GBq, 7 GBq, 10 GBq, 15 GBq, 20 GBq, contenenti rispettivamente 1.2, 2, 2.8, 4, 6 e 8 milioni di microsfere. Le SIR-Spheres (Sirtex, Lane Cove, Australia) sono microsfere di resina caricate con 90 Y con diametro compreso tra 20 µm e 60 µm e attività di 50 Bq per microsfera. Ogni fiala ha attività di circa 3 GBq e contiene milioni di microsfere, sospese in 5 ml di acqua sterile. Una volta iniettate, le microsfere rilasciano più del 94% della dose in 11 giorni. Le differenze principali tra i due tipi di microsfere consistono nelle dimensioni delle microsfere, nell attività per singola microsfera e nel numero di microsfere iniettate; infatti a parità di attività, il numero di microsfere SIR-Spheres iniettate è molto maggiore. Viste queste caratteristiche non è insolito per SIR-Spheres raggiungere la saturazione del letto vascolare con stasi. Inoltre nelle microsfere di vetro il radiofarmaco è incorporato nella matrice, mentre in quelle di resina è adeso, ma in pratica in entrambi i casi rimane solidamente intrappolato nel punto di infissione. Per questo motivo l escrezione di 90 Y tramite le urine e le feci è praticamente nulla nel primo caso e comunque trascurabile nel secondo. Tabella 2 : Carlo Chiesa et al. EANM procedure guideline for the treatment of liver cancer and liver metastases with intraarterial radioactive compounds. Published online: 15 April
20 2.3 Selezione del paziente La selezione del paziente e l'indicazione al trattamento con 90 Y-TARE avvengono nel corso di una apposita riunione del Gruppo Interdisciplinare di Patologia (GIP) su richiesta di uno dei medici referenti del paziente. Poiché è auspicabile evitare di effettuare interventi chirurgici al paziente nei giorni immediatamente consecutivi alla terapia, tra i criteri di esclusione al trattamento va considerato anche il rischio di complicanze (connesse o non) che richiederebbero l intervento chirurgico nei giorni successivi e metterebbe in pericolo di radiazioni anche i medici. Il paziente quindi deve essere in buone condizioni generali e non necessitare di assistenza sanitaria particolare. Una caratteristica del trattamento 90 Y-TARE è che la procedura viene applicata con metodo one-shot. 2.4 Percorso del paziente Come già anticipato nella Premessa, la terapia 90 Y-TARE è suddivisa sostanzialmente in quattro momenti: Step 1: valutazione di fattibilità della terapia Durante la prima fase della procedura avviene, sia per il paziente portatore di HCC che per quello con metastasi epatiche da carcinoma colorettale, la valutazione di fattibilità della procedura con necessità di ricovero per almeno due giorni: vengono eseguiti l'esame angiografico epatico e la simulazione del trattamento radioembolizzante con l'iniezione di Macroaggregati di Albumina (MAA) marcati con 99m Tc nel o nei rami arteriosi "target" (il 99m Tc-MAA, un colloide, che nel flusso ematico dovrebbe comportarsi in maniera analoga alle sfere terapeutiche). In precedenza il paziente ha già effettuato un esame TAC con mezzo di contrasto (AngioTC), per studiarne l anatomia e la vascolarizzazione. Un esperto in Fisica Medica provvede quindi ad effettuare lo studio fisico-dosimetrico, sulla base di tutti i dati così raccolti, per pianificare il piano di trattamento. L angiografia (vedi Figura 6) qui effettuata viene definita diagnostica e ha lo scopo di studiare l anatomia vascolare del paziente, identificare varianti anatomiche e isolare la circolazione epatica occludendo vasi extraepatici che potrebbero determinare un inavvertita diffusione delle microsfere agli organi non target. La scelta di effettuare o no l embolizzazione preventiva di un arteria è lasciata al radiologo interventista che deciderà in base alle caratteristiche anatomiche, al flusso sanguigno e al sito di infusione prescelto. L embolizzazione profilattica di un arteria deve essere eseguita in maniera superselettiva mediante rilascio di spirali metalliche, in corrispondenza dell origine dell arteria da embolizzare, in modo da consentire il ripristino del flusso dei rami a valle attraverso i molteplici circoli collaterali tipici della circolazione gastroenterica. In tal modo il rischio di ischemia indotta dall embolizzazione è minimo. 19
21 Angiografia Figura 6 Una volta effettuata l angiografia diagnostica, un micro-catetere viene posizionato nel sito di infusione prescelto e vengono iniettati 4-5 mci di Macroaggregati di Albumina (MAA) marcati con 99m Tc. Poiché le dimensioni dei MAA (10-60 µm) sono paragonabili a quelle delle microsfere di 90 Y, si presume che le due distribuzioni siano molto simili, permettendo cosi di prevedere la distribuzione delle microsfere al momento del trattamento vero e proprio. Infatti, dai risultati, si può dire che le distribuzioni dei MAA e dell 90 Y non siano differenti nel 71% dei casi, differenti nel 23% dei casi e incerte nel 6% dei casi (vedi Figura 7). IMMAGINE Tc-99m MAA SPECT/TC Figura 7 IMMAGINE Y-90 SPECT/TC A questo segue l immediata esecuzione in Medicina Nucleare di una scintigrafia planare e una SPECT (basate sulla radiazione gamma prodotta dal 99m Tc), che verranno integrate con le immagini di AngioTC, allo scopo di rilevare la presenza e la significatività di accumuli extraepatici di radiofarmaco, shunt polmonari e/o 20
22 gastrointestinali non evidenziabili con la sola angiografia e che potrebbero controindicare il trattamento (vedi Capitolo2, paragrafo 2.5). L attività da somministrare a un determinato paziente viene personalizzata con uno studio preliminare da parte di uno specialista in Fisica Medica, ai sensi del D.Lgs 187/00: i dati raccolti con l esame AngioTC e la SPECT, con altre informazioni cliniche rilevanti, vengono elaborati in uno studio fisico-dosimetrico personalizzato per il paziente in questione, al fine di calcolare l attività di sfere marcate con 90 Y da somministrare per il trattamento della neoplasia, sulla base della prescrizione effettuata del medico nucleare. Valori tipici di attività sono compresi tra 0,5 e 3 GBq di 90 Y. Come vedremo nel Capitolo 3, per questo calcolo si possono utilizzare varie procedure, anche a seconda delle differenti prescrizioni date dalle due diverse ditte di provenienza delle microsfere di 90 Y. Al termine dello Step 1, è utile un confronto fra tutte le figure coinvolte, per arrivare a uno studio completo e confermare la fattibilità del trattamento; in caso positivo si passerà alla seconda fase, che avverrà non oltre 3-4 settimane dall angiografia diagnostica poiché tempi maggiori potrebbero permettere una riorganizzazione della vascolarizzazione con variazioni rispetto a quanto visto nell angiografia valutativa. Step 2: esecuzione del trattamento TARE Questa fase prevede il ricovero del paziente per poter procedere alla radioembolizzazione: in pratica si ripete la procedura angiografica iniettando, questa volta, la dose di 90 Y precedentemente calcolata e preparata. Si esegue il cateterismo selettivo dell arteria epatica posizionando il micro catetere coassiale ad alto flusso nella sede di infusione prescelta, e, una volta in sede, lo si connette con il sistema outlet del kit di somministrazione. L utilizzo del catetere ad alto flusso permette, da un lato, una somministrazione a pressione costante consentendo una migliore sospensione delle microsfere, dall altro, la riduzione della resistenza al flusso del sistema di somministrazione che impedirebbe la fuoriuscita completa delle microsfere e provocherebbe il loro accumulo nel kit di somministrazione e nel catetere. D altra parte è comunque necessario che la velocità di infusione sia minore della velocità del flusso in arteria, in quanto un flusso di iniezione superiore al flusso nel vaso potrebbe causare un reflusso delle microsfere e una somministrazione ad aree non target. Questa velocità può essere monitorata mediante l iniezione di mezzo di contrasto prima dell infusione vera e propria. Therasphere o SIR-Spheres, a seconda del caso, spediscono insieme alla fiala con la dose di 90 Y il kit necessario per l infusione, formato da un sistema di tubi sterili monouso e da una parte di accessori riutilizzabili, nonché da contenitori schermati (in plexiglas, essendo l 90 Y un beta emettitore puro) (vedi Figura 8). 21
23 Kit di somministrazione Figura 8 Il kit di somministrazione deve essere disposto su un carrello o un tavolo posizionato accanto al paziente, cioè vicino al raccordo di entrata del catetere di infusione (vedi Figura 9). INIEZIONE DELLE MICROSFERE Figura 9 Le tecniche di infusione di Therasphere e SIR-Spheres differiscono. Le SIR-Spheres necessitano di un monitoraggio fluoroscopico perché, dato il numero e le dimensioni delle particelle, è più facile raggiungere la saturazione del vaso prescelto e la stasi; si utilizza quindi in alternanza anche un infusione di mezzo di contrasto, facendo attenzione a non fare entrare in contatto le SIR-Spheres con il mezzo contrasto. Questo permette all operatore di monitorare adeguatamente l iniezione e verificare che non si raggiunga la saturazione vascolare. Un infusione tipica di SIR-Spheres 22
24 richiede circa minuti, mentre quella di Therasphere dura meno di 5 minuti in quanto si può procedere più velocemente (la stasi vascolare non è ipotizzabile quindi non è necessario un monitoraggio fluoroscopico). Durante la procedura la Fisica Medica e Sanitaria è sempre presente ed effettua rilevazioni radiometriche tramite una camera a ionizzazione (vedi Figura 10), per verificare le modalità di somministrazione e dare eventuali indicazioni per il frazionamento della dose. Al termine della procedura effettua controlli radiometrici con contaminametro (contatore proporzionale) sugli operatori, sui rifiuti prodotti e entro la sala dell intervento, per motivi di radioprotezione e consentire il successivo impiego della sala, nonché misure dirette sul paziente con camera a ionizzazione per rilasciare il benestare al rientro del paziente in reparto (vedi Capitolo 2, paragrafo 2.7). Figura 10: Camera a ionizzazione Step 3: verifica del trattamento TARE Il giorno successivo il paziente si reca in Medicina Nucleare ed effettua un indagine scintigrafica (basata sulla radiazione di bremsstrahlung provocata dalle particelle emesse dall 90 Y) e un esame 90 Y-PET-TC (basato sulla radiazione minoritaria prodotta dall 90 Y per internal pair production) per la valutazione del risultato della procedura (vedi Capitolo 2, paragrafo 2.6) Step 4: follow up In seguito vengono programmati controlli periodici di follow up. Per il paziente portatore di HCC sottoposto a 90 Y-TARE, è previsto il controllo AngioTC per la definizione del risultato secondo i criteri classificativi codificati dalla modified Response Evaluation Criteria In Solid Tumor 3 (mrecist) a 1, 6, 12 mesi, associato ogni volta all esame del dosaggio del valore di alfa-fetoproteina per il monitoraggio della malattia neoplastica. Questo è in aggiunta agli esami ematochimici e strumentali previsti per la patologia epatica e metabolica di base. Invece per il paziente portatore di metastasi epatiche da carcinoma colorettale, sottoposto a 90 Y-TARE, è previsto il controllo AngioTC per la definizione del risultato secondo i criteri classificativi codificati dalla mrecist a 2 e 4 mesi e il dosaggio del 3 : Linea guida proposta come metodo per la determinazione della risposta di un particolare trattamento. 23
25 valore del CEA (un marcatore tumorale). Si deve anche specificare che questa terapia non è indolore, ma si possono riscontrare effetti collaterali comuni: fatica, dolori addominali, nausea, febbre, transitorie elevazioni transaminasi. Con probabilità più ristretta (2-8%) si possono verificare ulteriori eventi avversi: dolori addominali cronici e la presenza di radiazioni fuori bersaglio o radiazioni attenuate in tessuti adiacenti ad esso, che potrebbero provocare gastrite da radiazioni (ulcerazione gastrointestinale, emorragie gastrointestinali, pancreatite), polmonite da radiazioni con relativo versamento pleurico, malattie epatiche indotte dalle radiazioni (epatite, fibrosi epatica, ipertensione portale, colecistite, radionecrosi, insufficienza epatica). 2.5 Studio previsionale: SPECT con MAA Lo studio pre-terapia con somministrazione di Macroaggregati di Albumina (MAA) marcati con 99m Tc viene effettuato essenzialmente per simulare, senza creare effetti danneggianti, la terapia vera e propria, al fine di escludere eventuali assorbimenti del tracciante da parte dei polmoni e di altri organi extraepatici, visualizzabili appunto analizzando le immagini scintigrafiche della distribuzione del 99m Tc, e per poter eseguire i calcoli dosimetrici e determinare l attività di 90 Y da iniettare. Qualora la distribuzione dei MAA non fosse ottimale, l equipe medica coinvolta deve decidere la fattibilità della terapia, eventualmente, ripetendo la procedura angiografica dopo ulteriori embolizzazioni. Entro un ora dalla somministrazione dei MAA, viene effettuato un esame scintigrafico con acquisizione di immagini planari segmentarie del corpo intero, completate da un acquisizione tomografica SPECT dell addome. Le immagini prodotte da questi esami si basano sulla radiazione prodotta dal 99m Tc ( 99m Tc prodotto tramite un generatore 99 Mo/ 99m Tc). Il tecnezio è infatti molto utilizzato in questi tipi di applicazioni in quanto è un emettitore di raggi gamma (di energia 140 kev, ottimali per la gamma camera), ha una breve emivita (6,01 ore) e ha la capacità di legarsi a numerose molecole di interesse biochimico. La finestra di acquisizione della gamma camera è allora selezionata a 140 ±10% kev e i collimatori che si utilizzano sono quelli ad alta energia (HE) Verifica di controllo: SPECT e PET/TC post terapia Entro 24 h dal trattamento di radioembolizzazione transarteriale con microsfere marcate con 90 Y (TARE) la bio-distribuzione delle microsfere può essere verificata, come già detto, tramite una scintigrafia, ottenuta sfruttando la radiazione di frenamento (bremsstrahlung) delle particelle - emesse dal 90 Y, nonché con una tomografia PET/TC, ottenuta sfruttando la produzione di coppie (internal pair production) nel decadimento dell 90 Y, che avviene con un branching ratio quasi 4 : Kao et al. Personalized predictive lung dosimetry by technetium-99m macroaggregated albumin SPECT/CT for yttrium-90 radioembolization. EJNMMI Research,
26 trascurabile, pari a (31.86 ± 0.47)x10-6, nella transizione allo stato eccitato dello 90 Zr (vedi Figura 11). Figura 11: Decadimento dell 90 Y Viene quindi effettuato un esame scintigrafico con esecuzione di immagini planari segmentarie del corpo intero, completate da un acquisizione tomografica SPECT dell addome, e successivamente un acquisizione PET/TC dell addome. La scintigrafia post-terapia viene eseguita per due ragioni. In primo luogo, alcune microsfere potrebbero essersi inaspettatamente localizzate al di fuori del fegato, nonostante una precedente simulazione di distribuzione favorevole ottenuta con la somministrazione dei 99m Tc-MAA (per motivazioni cliniche o di procedura). L accumulo di microsfere marcate con 90 Y in organi diversi dal fegato, come già visto, può causare gravi complicazioni, quindi essere a conoscenza della presenza di sfere al di fuori del fegato permette di adottare provvedimenti preventivi nella cura di queste complicazioni. In secondo luogo, la distribuzione delle microsfere nel tessuto epatico tumorale (e non) dovrebbe essere un importante fattore predittivo dell efficacia del trattamento, permettendo una stima, basata sulle immagini stesse, della dose di radiazione effettivamente assorbita dai vari tessuti. Purtroppo, il basso yield e la natura continua dello spettro di bremsstrahlung dei fotoni (da 0 a 2,3 MeV) limitano la precisione quantitativa di questo tipo di indagini. Per ogni MBq, circa fotoni di bremsstrahlung con energia superiore a 50 kev sono prodotti dall interazione dei β - con i tessuti organici, quindi è necessaria un acquisizione in una finestra energetica particolarmente ampia, cioè ampia abbastanza da poter massimizzare la sensibilità della tecnica. L assenza di un fotopicco impedisce infatti l uso di una singola finestra di acquisizione, indispensabile anche per la sottrazione 25
27 dei fotoni di scatter e per la correzione per l attenuazione. Inoltre la penetrazione di fotoni a più alta energia attraverso i setti del collimatore porta a un ulteriore perdita di contrasto dell immagine. La fattibilità della PET con l 90 Y è stata recentemente dimostrata sia in fantoccio che in paziente e, in questo caso, potrebbe essere un alternativa interessante alla SPECT da bremsstrahlung. Per ogni MBq di attività, l 90 Y emette circa 32 positroni al secondo con una energia massima di 758 kev. Di conseguenza, le coppie di fotoni di annichilazione vengono prodotte circa 700 volte meno spesso dei fotoni di bremsstrahlung. Tuttavia, l esame PET con 90 Y può consentire la rilevazione di attività extraepatica in maniera più precisa e una stima più accurata di dose al tumore e al fegato, poiché la risoluzione spaziale dovrebbe essere, ed è, comparabile a quella, molta buona, della PET con 18 F, che ha un energia massima di positroni di 633 kev. Inoltre la PET può essere associata direttamente alla TAC (apparecchiatura ibrida PET/TC, oramai allo stato dell arte), consentendo di visualizzare anche in maniera morfologica la distribuzione di attività. Simulazione del trattamento TARE tramite fantoccio e calibrazione della gamma camera e del tomografo PET/TC Abbiamo cercato di simulare la terapia radioembolizzante con microsfere di 90 Y tramite l uso di un fantoccio, essenzialmente per calibrare la gamma camera e il tomografo PET da noi utilizzati per le verifiche post-trattamento. Nel particolare abbiamo acquisito le immagini PET e SPECT relative al fantoccio riempito con 90 Y e valutato quali potessero essere le impostazioni migliori per queste misurazioni, come ad esempio la larghezza della finestra di energia. Abbiamo così creato un protocollo di acquisizione ottimale per questi tipi di esami e da poter utilizzare nel futuro. Il fantoccio da noi usato (il NEMA IEC Body Phantom Set TM ) (vedi Figura 12) simula appunto il torace di una persona: è costituito dal corpo centrale (body) riempito completamente con acqua distillata per circa 9,5 litri, da una struttura cilindrica centrale contenente palline di polistirolo e acqua, che riproduce le funzionalità dei polmoni, e da delle sfere, anch esse riempite d acqua, che simulano i vari organi. Le spesse pareti del fantoccio sono in plexiglas, ottimo schermante per i beta emettitori. 26
28 Figura 12: Fantoccio NEMA I volumi delle sei sfere all interno del fantoccio si ricavano pesando le siringhe, relative a ciascuna sfera, contenenti l acqua estratta da esse stesse; da queste misure si deve poi sottrare il peso della tara (siringa vuota). I valori dei volumi così ottenuti sono: 0,53 cc, 1,16 cc, 2,60 cc, 5,54 cc, 11,52 cc, 26,54 cc. Considerando la sfera più grande come il fegato, abbiamo in quella ( zona calda ) iniettato una attività di 1000 kbq per ogni grammo di cloruro di 90 Y, che è il valore mediano delle concentrazioni di attività somministrate ai paziente finora trattati (attività iniettata/volume lobo target del fegato). Si deve inoltre iniettare nel corpo centrale ( zona tiepida ) una concentrazione di attività di 56 kbq/g, cioè in rapporto 1:18 rispetto alla concentrazione della zona calda, per simulare la radiazione di fondo sviluppatesi nel background 5. Si può, infine, introdurre in tutte le parti del fantoccio contaminate dal radioisotopo 90 Y un quantitativo di DTPA (una polvere bianca che si discioglie in acqua) pari a una concentrazione di 1g/l, al fine di evitare l adesione dell ittrio alle pareti di plexiglas del fantoccio 6. Calibrazione della gamma camera tramite fantoccio Per quanto riguarda la gamma camera usata per questo tipo di radioisotopo, cioè per rilevare la radiazione di bremsstrahlung che scaturisce dall interazione delle particelle β, prodotte dal decadimento dell 90 Y, con il corpo del paziente, non si trovano in Letteratura riferimenti ben precisi, uniformi e univocamente determinati, ma molti esperimenti simili che forniscono solo le indicazioni più rilevanti. Noi ci siamo soffermati sulle pubblicazioni più recenti trovate in Letteratura e sviluppato più misurazioni tramite fantoccio, al fine di trovare il settaggio più efficiente per questo tipo di esame e determinare il protocollo di acquisizione adeguato. La radiazione di bremsstrahlung ha uno spettro di energia continuo e molto ampio; si estende fino alla più alta emissione di energia dei raggi beta (2,3 MeV) senza 5 : Elschot M, Nijsen JFW, Dam AJ, de Jong HWAM. Quantitative Evaluation of Scintillation Camera Imaging Characteristics of Isotopes Used in Liver Radioembolization. PLoS ONE, : Pasciak et al. A Comparison of Techniques for 90Y PET/CT Image-Based Dosimetry Following Radioembolization with Resin Microspheres. Frontiers in Oncology, May
29 presentare un pronunciato fotopicco, pertanto è difficile stabilire a priori quale sia la finestra energetica di acquisizione migliore. Il problema principale per l'imaging dell 90 Y è che i fotoni con energia inferiore a 60 kev sono attenuati nel corpo del paziente, quelli con energie superiori ai 300 kev derivano dalla penetrazione attraverso i setti del collimatore o sono da questi scatterati e la più alta percentuale dei fotoni con energia compresa nell intervallo kev sono retrodiffusi dal vano dietro il cristallo. Inoltre l'interazione tra i fotoni di bremsstrahlung e il piombo (Pb) fa rilevare un picco di raggi X intorno ai 75 kev. Questi fotoni degradano la qualità delle immagini e l accuratezza quantitativa delle misure; in linea teorica però si può asserire che la finestra di energia kev sia quella ottimale in quanto ha una dispersione primaria più bassa rispetto agli altri range e quindi garantisce una miglior precisione di misura 7. Una finestra più sottile diminuirebbe la sensibilità del sistema e il rapporto segnale-rumore, mentre una finestra più estesa produrrebbe degli artefatti. Si può anche stabilire quali siano i collimatori migliori da utilizzare in questi tipi di misurazione. Ne esistono di vari tipi, ma per questi esami i più utilizzati sono: i MEAP o MEGP (Medium Energy All Purpose o Medium Energy General Purpose), collimatori standard per fotoni a medie energie, oppure i LEHR (Low Energy High Resolution), collimatori per fotoni a bassa energia in cui si vuole un alta risoluzione spaziale a scapito dell efficienza di rivelazione. Una volta posizionato il fantoccio nella gamma camera (vedi Figura 13), abbiamo effettuato le seguenti misurazioni: 1) scintigrafia planare whole-body con collimatori MEGP e con le seguenti impostazioni: zoom 1, 2,2 mm/pixel, matrice di 256x1024, speed testate 10cm/sec, durata di acquisizione 600sec, tre finestre di energia a 75 ± 25% kev, 130 ± 25% kev, 220 ± 25% kev; 2) scintigrafia planare statica (riservata al solo torace in questi tipi di esami) con collimatori MEGP e con le seguenti impostazioni: zoom 1, 2,2 mm/pixel, matrice di 256x256, durata di acquisizione 600sec, tre finestre di energia a 75 ± 25% kev, 130 ± 25% kev, 220 ± 25% kev; 3) scintigrafia planare statica con collimatori MEGP e con le seguenti impostazioni: zoom 1, 2,2 mm/pixel, matrice di 256x256, durata di acquisizione 600sec, due finestre di energia a 75 ± 33% kev, 155 ± 33% kev; 4) scintigrafia planare statica con collimatori LEHR e con le seguenti impostazioni: zoom 1, 2,2 mm/pixel, matrice di 256x256, durata di acquisizione 600 sec, due finestre di energia a 75 ± 33% kev, 155 ± 33% kev; 5) SPECT con collimatori MEGP e con le seguenti impostazioni: zoom 1, 4 mm/pixel, matrice di 64x64, raggio di rotazione 23cm, 6 per ogni step di 7 : Roshan et al. Advances in SPECT for Optimizing the Liver Tumors Radioembolization Using Yttrium-90 Microspheres. World Journal of Nuclear Medicine, Volume 14, May
30 rotazione, 30sec/step, durata di acquisizione 30 minuti, due finestre di energie a 75 ± 33% kev, 155 ± 33% kev. Figura 13: Fantoccio nella gamma camera Millenium Dai grafici dei conteggi in funzione dell energia corrispondenti alle misurazioni descritte ai punti 1 e 2 (vedi di seguito) si può vedere chiaramente dove sono posizionate le tre finestre di acquisizione prescelte rispetto all andamento dei grafici stessi; la prima, quella di energia più bassa contiene il picco a 75 kev dei fotoni provenienti dall interazione con il piombo dei collimatori, quella centrale è posizionata all interno del plateau e la terza, di molti meno conteggi, contiene i fotoni scatterati una o anche più volte dal sistema di rivelazione. 29
31 Inoltre, dalle immagini acquisite da queste misurazioni si può notare, come da previsione, che la miglior chiarezza di immagine ed efficienza si ha tramite la finestra di energia centrale, cioè quella centrata in 130 kev (tra 97,5 kev e 162,5 kev). Si riportano queste immagini qui sotto (le prime due, ognuna per ogni testata della gamma camera, si riferiscono alla finestra centrale, le seconde due a quella del piombo e le terze due a quella delle alte energie ). 30
32 Analizzando quindi queste immagini e questi grafici, abbiamo deciso di standardizzare questo tipo di misurazione impostando l acquisizione dei dati tramite la finestra del piombo e la finestra compresa tra 104 kev e 206 kev, cioè quella centrale studiata in partenza ma leggermente modificata, un po allargata, in modo da contenere il numero più elevato possibile di conteggi corrispondenti ai fotoni delle energie del plateau. Dalla finestra centrale, infatti, si può trarre il maggior numero di informazioni sia qualitative che quantitative; è dove si rileva una nitidezza di immagine superiore e dove si può procedere con l identificazione delle aree irraggiate dall 90 Y (in questo caso la sfera più grande) e con l analisi della distribuzione dell attività all interno di esse, tramite i conteggi da acquisire nelle ROI di intaresse. La finestra del piombo può essere utile per considerazioni di scatter e per avere un supplemento di dati da poter confrontare. Questa finestra di energia può essere visionata nel seguente grafico: I grafici relativi alla misurazione effettuata seguendo i parametri descritti al punto 3 e comprensivi delle due nuove finestre di acquisizione appena definite sono: Inoltre le immagini registrate con queste impostazioni e riguardanti le scintigrafie planari statiche sempre del punto 3 sono le seguenti: 31
33 Usando invece i collimatori LEHR (vedi punto 4) si sono ottenute le seguenti scintigrafie: 32
34 Si può affermare che i collimatori da usare in questi esami devono essere i MEGP in quanto, anche se i rate dei conteggi per ogni testata della gamma camera sono minori rispetto a quelli relativi ai conteggi acquisiti con i collimatori LEHR (circa 5 kcps rispetto a quasi 30 kcps), l efficienza di rivelazione è sicuramente maggiore. Infine, a seguito di tutte queste considerazioni e per verificare il corretto e funzionale andamento di questo protocollo, abbiamo effettuato l acquisizione più completa che si possa fare con la gamma camera, l esame SPECT, descritto nelle sue impostazioni al punto 5. Le immagini fuse SPECT ricavate si riportano di seguito. 33
35 Immagini fuse sui tre assi (frontale, sagitale,assiale) Calibrazione del tomografo PET/TC tramite fantoccio I positroni emessi per internal pair production dall 90 Y si annichilano con gli elettroni, producendo una coppia di fotoni gamma entrambi di energia 511 KeV ed emessi in direzioni opposte tra loro; quindi la finestra di acquisizione è standard, e già di default impostata a 511 ± 15% kev. Siccome il protocollo di acquisizione di questa macchina non consente la selezione dell isotopo 90 Y, si utilizzano le impostazioni riguardanti il 22 Na che ha decadimento β + e una lunga emivita (circa 2,6 anni). Per verificare questo tipo di misurazione con questi tipi di parametri, abbiamo introdotto il nostro fantoccio nella PET e acquisito le immagini tomografiche per circa 40 minuti. Il buon risultato ottenuto è il seguente: 34
36 Immagini fuse PET/TC Come si vede da queste scansioni, la ricostruzione delle immagini PET (in alto a sinistra), cioè la loro sovrapposizione con quelle della TAC (in basso a sinistra), porta a delle immagini fuse (in alto a destra) che rilevano in modo chiaro i punti di addensamento dell 90 Y e in particolare quelli nella sfera più grande ben identificata dalla TAC. 2.7 Aspetti di fisica medica e radioprotezione La struttura di Fisica Medica e Sanitaria è responsabile degli aspetti di radioprotezione riguardanti i lavoratori e i pazienti connessi all uso di microsfere marcate con 90 Y per il trattamento delle malattie neoplastiche del fegato tramite la terapia radiante selettiva. Nonostante tale tipo di prodotto sia registrato come dispositivo medico e non come radiofarmaco, di fatto ne ha le caratteristiche, in quanto viene somministrata una sostanza radioattiva al paziente. Pertanto la pratica, definita come medico-radiologica ai sensi della normativa vigente, è da considerarsi anche assimilabile ad una terapia medico nucleare. Caratteristiche del radionuclide 90 Y: decadimento beta meno puro, con sola emissione di raggi beta di alta energia senza emissioni di raggi gamma primari; la radiazione minoritaria da internal pair production è trascurabile a fini radioprotezionistici; 35
37 energia media delle particelle beta 0,937 MeV, energia massima 2,28 MeV; tempo di dimezzamento 2,67 giorni = 64,1 h; percorso medio dei raggi beta nei tessuti 2,5 mm (massimo 11 mm): di conseguenza la radiazione beta viene attenuata dai tessuti organici del paziente e da modeste schermature; massima azione a livello della massa tumorale, bassa esposizione dei tessuti vicini; la radiazione beta ad alta energia, quando viene attenuata, produce radiazione X secondaria di frenamento (bremsstrahlung) in quantità più o meno intensa a seconda della densità del materiale attraversato responsabile dell attenuazione; la radiazione che emerge dal corpo del paziente al quale è stato somministrato 90 Y è quindi radiazione X di frenamento di modesta intensità (il rate di dose da esposizione è paragonabile a quello di un paziente che effettua una scintigrafia, dell ordine di qualche decina di μsv/h a contatto) (vedi tabella 3); la manipolazione diretta dell isotopo, a causa della radiazione beta, può dare livelli di radiazione molto elevati alle mani e contaminazioni della cute degli operatori, pertanto deve essere assolutamente evitato il contatto diretto (a contatto con siringa non schermata: 40 msv/h) (vedi tabella 4). RATE DI DOSE IN PROSSIMITA DEL PAZIENTE Measure Contact Dose Rate (msv/h) Dose Rate at 0,3 m (msv/h) Resin Glass Resin Glass Average 0,079 0,190 0,011 0,020 Minimum 0,001 0,020 0,0002 0,010 Maximum 0,870 0,700 0,070 0,100 Tabella 3 Tabella 3 : J Vasc Interv Radiol 2012; 23:
38 RATE DI DOSE A DIVERSE DISTANZE DALLA SORGENTE Tabella 4 Come si vede nella Tabella 4, infatti, il rate di dose è molto elevato in prossimità della sorgente, ma diminuisce il maniera significativa all aumentare dell azione dei materiali schermanti e della distanza da essa a causa della bassa capacità di penetrazione delle particelle β. Detenzione e impiego di 90 Y I quantitativi di 90 Y previsti dalla legge, validi per tutte le pratiche con 90 Y di Medicina Nucleare effettuate nello stesso impianto, sono: massimo 6000 MBq per la detenzione di 90 Y in una consegna; massimo MBq di 90 Y per l impiego annuale. Norme di sicurezza Ai sensi di legge le terapie radiometaboliche non espressamente indicate nella legge D.Lgs 187/00 devono essere effettuate in regime di ricovero protetto con raccolta delle deiezioni dei pazienti e quindi ciò riguarda anche la terapia radiante selettiva con microsfere di 90 Y. Il modesto impatto radioprotezionistico di tale pratica, però, non necessiterebbe di restrizioni così particolarmente stringenti, pertanto le associazioni AIMN 8 e AIFM 9 si stanno attivando con una segnalazione al Ministero della Salute, affinché si esprima circa l inclusione di tale pratica tra le esenzioni dal particolare regime di ricovero previsto dall aggiornamento del D.Lgs 187/00, così come già riconosciuto per la terapia con cloruro di 223 Ra. L iter legislativo per la terapia radiante con microsfere di 90 Y è quindi ancora in corso. Di fatto, attualmente, Tabella 4 : D. Delacroix et al; Radionuclide and radiation protection data handbook; radiation protection dosimetry Vol. 98, Number 1, : Associazione Italiana di Medicina Nucleare. 9 : Associazione Italiana di Fisica Medica. 37
39 a livello nazionale, è comune per gli Esperti Qualificati ritenere che i requisiti di legge possano essere sufficientemente ottemperati con un ricovero protetto semplificato. Questo si traduce con il ricovero presso uno dei reparti individuati ed autorizzati dagli Esperti Qualificati, con i seguenti accorgimenti: la procedura deve essere effettuata soltanto su pazienti autosufficienti, che non necessitano di assistenza sanitaria particolare e per i quali è trascurabile il rischio di complicanze post-trattamento che richiederebbero un intervento chirurgico nei giorni successivi; ricovero in camera singola; accessi alla camera e assistenza al paziente regolamentati da specifiche raccomandazioni; monitoraggio del paziente e dell attività escreta dal paziente; smaltimento di eventuali rifiuti radioattivi secondo quanto previsto dalla normativa, ai sensi dell art. 154 del D.Lgs 230/95; programma di informazione e formazione specifico per il personale sanitario del reparto di degenza; dimissioni del paziente regolamentate (valutazioni dosimetriche alla dimissione e rilascio di opportune istruzioni e norme di comportamento al paziente). Infatti, considerate le caratteristiche fisiche del radionuclide 90 Y, le proprietà radiometaboliche dei radiofarmaci ad esso associati e le modalità di gestione dei pazienti già trattati, tramite valutazioni dosimetriche e di impatto ambientale, si è evidenziato che i rischi di esposizione e contaminazione connessi a tali pratiche siano modesti e quindi che la dose stimata sia per i parenti e le persone che assistono il paziente che per i lavoratori aziendali non classificati, cioè non convolti strettamente nella procedura, sia trascurabile, o comunque inferiore ai limiti consentiti. Percorso delle sfere di 90 Y Le sfere radioattive vengono consegnate direttamente presso il settore di Terapia Radiometabolica della Medicina Nucleare, dove vengono poste entro una cassaforte schermata. La preparazione della dose terapeutica da somministrare avviene entro la zona controllata e opportunamente schermata del reparto di medicina nucleare (camera calda). Poi il trasporto del materiale radioattivo fino alla sala dell intervento viene effettuato secondo la procedura concordata con l Esperto Qualificato e alla presenza di personale della Fisica Medica e Sanitaria che deve eseguire i relativi controlli radiometrici. La somministrazione del preparato, che è un impianto di microsfere marcate con 90 Y, avviene presso una sala di Radiologia Interventistica attraverso un infusione nell arteria epatica, secondo una procedura studiata dai medici nucleari e dai fisici medici che minimizza la dose agli operatori. La sala dell intervento viene preparata preventivamente per poter contenere e rimuovere 38
40 facilmente eventuali contaminazioni ambientali che si potrebbero verificare durante la procedura. Gli operatori, tutti classificati come radio-esposti, durante la preparazione e la somministrazione dell 90 Y devono indossare idonei dispositivi di protezione individuali: abiti e calzature da lavoro, guanti in materiale plastico monouso, dosimetri personali. L impianto di microsfere è effettuato alla presenza di personale della Fisica Medica e Sanitaria, che ha l incarico di effettuare i controlli radiometrici, verificare la corretta gestione dei rifiuti radioattivi e autorizzare il rilascio della sala al termine della procedura. Subito dopo la somministrazione, periodicamente durante il ricovero, e al momento della dimissione del paziente, verranno effettuati controlli radiometrici su di esso e sugli escreti da parte della Fisica e Sanitaria. Prima della somministrazione del radiofarmaco, al paziente o ai familiari vengono consegnate ed illustrate le istruzioni per la riduzione della dose alla popolazione (D.Lgs 187/00). I rifiuti solidi contaminati prodotti durante la fase di preparazione e somministrazione del radiofarmaco vengono raccolti in appositi contenitori schermati per i beta-emettitori all interno del reparto di Radiologia Interventistica, ivi lasciati decadere, e poi smaltiti in regime di esenzione ai sensi dell art. 154 del D.Lgs 230/95, previo controllo radiometrico da parte della Fisica Medica e Sanitaria. Tutti i rifiuti (potenzialmente infetti e non) prodotti durante l intervento sono raccolti in appositi contenitori (biobox) e sottoposti a controllo radiometrico prima dello smaltimento; nel caso si riscontrassero contaminazioni, i contenitori devono essere stoccati in depositi idonei e poi smaltiti in regime di esenzione ai sensi dell art. 154 del D.Lgs 230/95. Analogamente sono trattati i materiali destinati al riutilizzo (anch essi potrebbero essere contaminati), come i box per la somministrazione e la biancheria utilizzata dal personale: controllo, stoccaggio per decadimento, lavaggio/ricondizionamento, riutilizzo. Le camere in cui vengono ricoverati i pazienti che hanno effettuato la terapia TARE con microsfere di 90 Y non necessitano di allestimenti particolari: devono essere camere singole, possibilmente con bagno dedicato, all interno di un reparto autorizzato dall Esperto Qualificato (previo sopralluogo e programma di formazione-informazione al personale del reparto da parte della Fisica Medica e Sanitaria). Il rate di dose in prossimità del paziente è modesto (circa 10-6 (msv/h)/mbq a 1 m), pertanto non sono necessarie particolari schermature della stanza. Eventuali terapie su pazienti incontinenti o non autosufficienti dovrebbero essere preventivamente concordate con la Fisica Medica e Sanitaria. L escrezione urinaria di 90 Y per tali tipologie di pazienti è molto modesta e il sistema idrico ospedaliero consente una notevole diluizione degli escreti nel punto di scarico, pertanto non si ritiene necessario provvedere alla raccolta delle deiezioni, che verranno semplicemente monitorate. Quindi sulla base dell analisi dei rischi, si ritiene che le camere in cui vengono ricoverati i pazienti che hanno effettuato la terapia TARE con microsfere di 90 Y devono essere classificate come "zone sorvegliate", ai sensi dell'art. 82 del D.Lgs 230/95, limitatamente al periodo di 39
41 permanenza di tali pazienti. Di conseguenza l accesso a tali stanze e la gestione di tali pazienti è regolamentato dalle norme interne di protezione e sicurezza. Percorso in caso di complicanze Nel caso di complicanze post-procedurali, che richiederebbero un intervento chirurgico Toraco-Addominale in urgenza, i responsabili della Fisica Medica e Sanitaria dell ospedale in questione, tempestivamente avvisati, devono definire per quel caso specifico il periodo di tempo, successivo al trattamento con microsfere di 90 Y, per il quale sono necessarie misure protezionistiche per gli operatori sanitari. I Medici che dovrebbero eseguire l intervento chirurgico e tutto il personale che sarebbe coinvolto in tale procedura, devono essere precedentemente e opportunamente addestrati a gestire l'evento. Ovviamente la Fisica Medica e Sanitaria dovrebbe, anche in questi casi, partecipare all intervento, effettuando le relative valutazioni dosimetriche. Le modalità di intervento, al fine di prevenire le esposizioni o di limitarne le conseguenze sui lavoratori e sulla popolazione, sono: rispettare scrupolosamente le norme interne di protezione e sicurezza; prestare grande attenzione alle modalità operative; utilizzare sempre i mezzi di protezione previsti (soprattutto i guanti, da sostituire frequentemente); limitare al minimo necessario le procedure di assistenza diretta ai pazienti, operando con precisione e rapidità; effettuare frequenti controlli di contaminazione alle mani, soprattutto al termine di operazioni che prevedono la manipolazione di sorgenti radioattive e, nel caso sia necessario, procedere con la massima tempestività alle operazioni di decontaminazione personale. Inoltre, siccome si deve essere in grado di fornire il servizio H24, risulta necessario poter disporre di un database sempre aggiornato con tutti i dati relativi ai casi eseguiti. Questo serve sia per motivi strettamente assistenziali sia per il proseguimento degli studi di ricerca. E necessaria, quindi, la collaborazione della maggior parte degli operatori coinvolti nel progetto per poter organizzare un database completo e inserire tutti i parametri salienti delle diverse parti di competenza. 40
42 CAPITOLO 3: La dosimetria 3.1 Relazioni dosimetriche Lo schema sviluppato dal Medical Internal Radiation Dose (MIRD), comitato della Medicina Nucleare, è l attuale riferimento dosimetrico per le terapie che fanno uso di radionuclidi, compresa quella con le microsfere di 90 Y. Il rate della dose in un generico tessuto di massa m è: D = k A m < E > e, integrando, la dose risulta: D = k<e>a 0 dove: m e ln(2)t/t 1/2 0 T 1/2 k < E > β ln(2) ( Gykg ) ( 109 dis J sgbq MeV = ( dis s ) (86400 day e quindi: D[Gy] = 50 A 0[GBq] m[kg] dt = A 0 m k < E > T 1/2 ln (2) ) ( x10 13 J ) MeV day ) ( ) 50 Gykg ln (2) Lo shunt polmonare viene studiato attraverso la distribuzione dei 99m Tc-MAA, che predicono la distribuzione delle microsfere di 90 Y, e valutato tramite il rapporto: L = C Lung C Lung +C Liver Lo shunt polmonare viene valutato dal medico nucleare che analizza le scintigrafie dell esame SPECT, affrontato dopo la somministrazione dei Macroaggregati di Albumina marcati con 99m Tc. Anche se potrebbe essere un calcolo approssimativo, ci si sofferma sullo studio delle immagini SPECT planari, quella anteriore e quella posteriore, cioè le due fette diametralmente opposte e frontali al corpo del paziente (vedi Figura 14). Si disegnano in entrambe le immagini le ROI sul fegato e sui polmoni, tramite un appropriato programma si ricavano i conteggi su ciascuna di queste ROI e si utilizza la media geometrica per ottenere la media dei conteggi delle ROI delle due immagini sia per quanto riguarda il fegato che per i polmoni. A questo punto si può calcolare il valore di L e trarne tutte le considerazioni dosimetriche con il fisico di riferimento. Si possono verificare in questo modo anche possibili shunt su altri organi, come stomaco e intestino, che potrebbero controindicare il trattamento. GBq 41
43 Figura 14: Immagini planari SPECT, anteriore e posteriore Ad esempio per il paziente PICCA si sono registrati i seguenti dati: CALCOLO SHUNT POLMONARE (DA PLANARE) ORGANO ANT POST MediaG % POLMONE ,0% FEGATO ,0% ALTRO % I pazienti per i quali si calcola un valore di L più alto del 20% non si ritengono qualificati per questo tipo di terapia in quanto incorrerebbero in una polmonite da radiazioni; in tutti gli altri casi si segue la seguente tabella (Tabella 5): 42
44 TABLE-Activity Reduction Recommendations for 90Y Resin Microspheres in Patients With Increased Lung Shunting. 99m Tc-MAA Lung Shunt (%) Activity of 90Y Resin Microspheres <10 Deliver full activity of 90Y resin microspheres Reduce activity of 90Y resin microspheres by 20% Reduce activity of 90Y resin microspheres by 40% >20 Do not treat with 90Y resin microspheres unless Tabella 5 Invece le dosi assorbite singolarmente dal tumore, dai polmoni e dal fegato normale (fegato sano) (vedi Figura 15) possono essere calcolate come segue: A Total = A NormalLiver + A Tumor + A Lung dalla definizione di L si ha: A Lung = A Total L e quindi la dose ai polmoni è data da: D Lung = 50 A Total m Lung L Figura 15: Ipotetica distribuzione della dose; coinvolge sia il tumore che il fegato sano e i polmoni. Tabella 5 : Andrew Kennedy, Douglas Coldwell, Bruno Sangro, Harpreet Wasan and Riad Salem. Radioembolization for the Treatment of Liver Tumors General Principles. American Journal of Clinical Oncology, Volume 35, Number 1, February
45 Inoltre la frazione tra l attività unitaria di radiazione sul tumore e quella sul tessuto sano è data da: T N = ( A Tumor m Tumor )/( A NormalLiver m NormalLiver ) e, tramite alcuni passaggi algebrici, si può scrivere la dose sul fegato normale, cioè sano, e la dose sul tumore come quanto segue: D NormalLiver = D Tumor = 50 A Total (1 L) m NormalLiver + T N m Tumor 50 A Total (1 L) = T D 1 T N (m NormalLiver+ T N m Tumor) N NormalLiver Il rapporto T N = ( A Tumor m Tumor )/( A NormalLiver m NormalLiver ) serve per stimare la quantità di attività relativa che andrebbe ad intaccare il fegato sano e si ricava elaborando le immagini dei MAA. Si disegna una VOI all interno del tumore e una in una zona del fegato colpita comunque dai MAA ma al di fuori del tumore. Poi, tramite un adeguato programma, si quantificano i conteggi rilevati nelle VOI e i loro volumi; dai volumi si risale alle masse attraverso le densità, che si considerano per tutti i tessuti pari a 1 g/cc=1 g/ml, e così si ottengono tutti i dati della formula. 3.2 SIR-Spheres Sono tre i metodi prescritti da SIR-Spheres per determinare l attività da somministrare: 1) Il metodo empirico: A[GBq]=Liver Involvement Activity LSM LPM E basato su valori di attività standard, eventualmente modificati da fattori che tengono conto dell estensione del tumore, ad esempio se si manifesta o no su entrambi i lobi del fegato, e dell entità dello shunt polmonare, analizzato tramite le immagini SPECT del pretrattamento con i 99m Tc-MAA. Questi fattori sono sintetizzati nella Tabella 6. 44
46 Tabella 6 2) Il metodo della body surface area (BSA): BSA[m 2 ] = height[m] weight[kg] A[GBq] = BSA Tumor Volume Total Liver Volume dove A è l attività da iniettare e BSA è l area di superficie corporea (m 2 ). Il calcolo dipende quindi solo dal volume epatico, il volume del tumore e le dimensioni fisiche del paziente. La formula si riferisce a un infusione su tutto il fegato per cui andrà corretta nel caso di un infusione limitata, ad esempio, a un solo lobo: A lobe [GBq] = [BSA ( V tumor lobe V total lobe )] [ V total liver V tumor liver ] Tabella 6 : Andrew S. Kennedy et al. Recommendations of the American Association of Physicists in Medicine on dosimetry, imaging, and quality assurance procedures for 90Y microsphere brachytherapy in the treatment of hepatic malignancies. Published: 1 August
47 I valori tipici delle attività che si ottengono sono nell intervallo 1.0 GBq 2.5 GBq. Queste attività possono essere ridotte se la funzione epatica risulta compromessa o se lo shunt polmonare, come detto prima, è abbastanza elevato. Si deve inoltre porre attenzione alle attività calcolate che superano i 3 GBq e procedere con tutte le verifiche del caso. Le SIR-Spheres sono spedite in fiale standard di 3 GBq calcolati in relazione al giorno del trattamento; a questo punto, a partire dalla fiala originale, verranno preparate nel laboratorio di Medicina Nucleare una o più fiale con la dose desiderata per il paziente in questione. Quindi a differenza di TheraSphere, come vedremo, la dose per il paziente va preparata in laboratorio. Ha il vantaggio di essere manipolabile con la possibilità di poterla frazionare e ottenere così più fiale con dosi differenti, ad esempio per iniezioni multiple per tumori multifocali; oppure con una stessa fiala è possibile trattare più pazienti nella stessa giornata. La possibilità di frazionare la dose è collegata al gran numero di microsfere e al loro minor peso specifico. Se da una parte rappresenta un grosso vantaggio, dall altra la manipolazione delle SIR-Spheres può essere fonte di incidenti di contaminazione o anche di errori nella preparazione della dose. 3) Il metodo partitivo: questo modello si basa sulla risoluzione dell equazioni, già citate prima, che esprimono A Total in funzione di D Lung = 20 Gy e D NormalLiver = 80 Gy (70 Gy se il paziente è cirrotico); questi valori di dose sono i due limiti di radiazione per polmoni e fegato sano. Poi, per rispettare entrambi i vincoli, si sceglie come attività da somministrare la più bassa tra le due. Nessuno di questi modelli è basato su forti fondamenti scientifici e le varie modificazioni delle attività progettate da ognuno di questi modelli sono ancora materia di ricerca. 3.3 TheraSphere L attività prescritta da TheraSphere è calcolata risolvendo l equazione della dose per l attività: A[GBq] = D[Gy] m[kg] 50 dove A è l attività; il volume di fegato target in cm 3 è calcolato con la CT e convertito poi in massa con un fattore di conversione di 1 g/ml (il valore della densità). La massa di fegato target si riferisce alla massa tissutale persuasa dal vaso in cui avverrà l infusione. Da TheraSpheres sono selezionate tipicamente dosi tra gli 80 e i 120 Gy a seconda delle caratteristiche del tumore. Le TheraSphere non possono essere ordinate per una dose specifica e ben determinata, per cui per ogni paziente è necessario ordinare la fiala più appropriata (disponibile in sei attività diverse, come riportato sopra) e, tenendo conto del tempo di decadimento dell 90 Y, calcolare 46
48 in che data l attività della fiala scelta sarà quella voluta. Considerando il decadimento dell 90 Y, una stessa attività può essere somministrata con un diverso numero di microsfere permettendo di scegliere questa quantità caso per caso, a seconda del tipo di effetto embolico ricercato. In altre parole, se l 90 Y all interno di una fiala è lasciato decadere per un notevole tempo, l attività per microsfera diminuisce in maniera considerevole. Questo permette l infusione di un elevato numero di microsfere anche con bassa attività; tale stratagemma si è rivelato utile per tumori di grosse dimensioni, permettendo una migliore distribuzione delle microsfere. 3.4 Voxel Dosimetry Analizzando le immagini SPECT relative all infusione dei 99m Tc-MAA e la sovrapposizione di queste con quelle della TAC, si può stimare la dose di 90 Y che sarà assorbita dal tumore e dagli altri tessuti circostanti durante la fase del trattamento vero e proprio. Voxel = volume di un pixel Per ogni voxel j la dose assorbita è: D j = A j S = NDs j S dove: A j è l attività cumulativa nel tempo espressa in GBq s (uguale al numero di decadimenti): A j = 1.443A j T 1/2 dove: A j è l attività che si deposita inizialmente in ogni voxel e T 1/2, in questo caso, è il tempo di dimezzamento dell 90 Y, che vale 64,1 h. Inoltre si assume che la biodistribuzione dei 99m Tc-MAA e quella delle microsfere di 90 Y siano uguali e che quindi in ogni voxel l attività dell 90 Y (A j ( 90 Y)) sia direttamente proporzionale ai conteggi dei 99m Tc-MAA (C j ( 99m Tc)), determinati precedentemente tramite l analisi della SPECT: A j ( 90 Y) / A tot ( 90 Y) = C j ( 99m Tc) / C tot ( 99m Tc) Mentre S è il fattore di MIRD; è espresso in Gy/GBq s e rappresenta il livello di assorbimento della dose da parte di ciascun voxel per unità di decadimento. Esso è dato dall energia β media (E β MEAN ) emessa dall 90 Y in ogni voxel e ivi completamente depositata diviso la massa degli stessi voxel: S = D j / 1 decay = E β MEAN ( 90 Y) / voxel mass 47
49 S = 937 KeV = Gy/GBq s [(4.42mm) g cm3] 48
50 CAPITOLO 4: Misure di attività 4.1 Il Calibratore di attività Figura 16: Illustrazione schematica dei componenti che costituiscono il calibratore di attività Il calibratore di attività (o di dose) (vedi Figura 16) è lo strumento base della medicina nucleare, è indispensabile per misurare la radioattività dei radioisotopi e le dosi dei radiofarmaci. È facile e veloce da usare. E poco preciso nella determinazione della purezza radiochimica di un radiofarmaco a causa della sua scarsa sensibilità nel registrare fedelmente le piccole radioattività coinvolte nel controllo di qualità di un radiofarmaco. Il calibratore di attività da noi utilizzato, il Capintec CRC-25R, ma in generale ogni calibratore, consiste in una camera a ionizzazione a pozzetto, al cui interno sono alloggiati un cilindro metallico di protezione, un inserto in plastica, e un contenitore di plastica porta-campioni dove si posizionano al suo interno le fiale e le siringhe oggetto di misura (vedi Figura 17). La camera di ionizzazione è riempita con un gas inerte ad alta pressione, solitamente argon, la cui funzione è quella di ionizzarsi al passaggio delle cariche, ottimizzando il più possibile l efficienza di rivelazione dello strumento. Normalmente è anche provvisto di una schermatura, di solito di piombo, che circonda la parete esterna del pozzetto per proteggere l operatore dalle radiazioni emesse dai campioni e minimizzare gli effetti della radiazione di fondo. 49
51 Figura 17: Componenti della camera a pozzetto del calibratore di attività Il calibratore è in genere collocato all interno della cella di manipolazione e collegato ad un unità di elaborazione dati esterna che permette di condurre test diagnostici e procedure di autocalibrazione. L unità di elaborazione permette inoltre di assegnare a ogni radioisotopo un fattore di calibrazione direttamente legato alla risposta della camera e all energia dei fotoni emessi, il cui valore è riportato in tabelle riconosciute a livello internazionale. Una volta memorizzati nello strumento tali fattori, è sufficiente, durante la misurazione, selezionare il radioisotopo in questione per ottenere la misura della sua attività. Nell ambito della medicina nucleare, il range di attività che tipicamente devono essere misurate è tra 1 MBq e 10 GBq con un accuratezza di almeno il ± 5%. 4.2 Controlli di qualità sui calibratori di attività Il calibratore di attività è sottoposto a controlli di qualità obbligatori, regolati dal D.Lgs 230/95, al fine di garantire sia il suo corretto funzionamento sia la sua affidabilità. Periodicamente, nel corso della vita dello strumento, occorre sottoporlo ad una serie di controlli di qualità: controlli di qualità giornalieri o prove di corretto funzionamento ogni giorno di impiego; controlli di qualità periodici o prove di taratura periodicamente e secondo necessità. Controlli di qualità giornalieri I controlli di qualità giornalieri sono costituiti da prove di corretto funzionamento, effettuate all inizio di ogni giornata lavorativa (di effettivo utilizzo), prima dell inizio delle attività (attendere almeno 30 minuti dopo l accensione), dal personale addetto 50
52 del reparto. Va verificato il corretto funzionamento del calibratore di attività effettuando il controllo dei seguenti parametri: ALIMENTAZIONE FONDO PRECISIONE STABILITÀ COSTANZA I primi due test possono essere avviati e direttamente eseguiti per mezzo di un apposita funzione presente nell unità di controllo del calibratore, oppure verificati nel dettaglio secondo le seguenti procedure: ALIMENTAZIONE L elevata corrente di ionizzazione, che si viene a creare nel volume sensibile del calibratore, può produrre una diminuzione della tensione tra gli elettrodi della camera a ionizzazione con conseguente perdita del regime lineare di funzionamento della camera stessa. Per questo motivo è fondamentale che l alimentazione sia stabile nel tempo. I moderni calibratori possiedono circuiti di controllo che permettono di verificare costantemente lo stato della tensione di alimentazione, tipicamente dell ordine dei 150 V V. FONDO Il monitoraggio continuo del fondo di radiazione viene utilizzato come indicatore; è utile infatti per verificare che il rumore elettronico dello strumento non sia in peggioramento e/o che non vi sia presente una contaminazione delle superfici interne del pozzetto o del porta-campione. Sin dal primo mese di utilizzo del calibratore dopo l accettazione, vanno raccolti i dati del fondo: il loro valore medio e la loro deviazione standard forniranno il punto di riferimento per questo controllo. Si deve cioè: 1) rimuovere tutte le sorgenti radioattive dal calibratore di attività e dalle sue immediate vicinanze. Si registra il valore di attività valutato selezionando una scala di riferimento (tipicamente quella del 99m Tc); 2) tolleranza: il valore del fondo misurato deve rientrare in tre deviazioni standard dal valore di fondo medio determinato all accettazione. Inoltre si può valutare la precisione: PRECISIONE Questo controllo ha lo scopo di confermare che l incertezza di una singola misurazione sia determinata principalmente dalla natura casuale del decadimento radioattivo. Un valore più grande del previsto indica la possibile presenza di un altra imprevista fonte di incertezza. Quindi: 51
53 1) inserire una sorgente di taratura (di solito 137 Cs) nel calibratore e registrare dieci letture sequenziali ad intervalli di 1 minuto; 2) calcolare la media delle misure e lo scarto di ciascuna misura dal valore medio; 3) tolleranza: lo scarto massimo di ciascuna misura dal valor medio dell attività misurata deve essere minore del ± 1%. Controlli di qualità periodici e prove di stato I controlli di qualità periodici sono costituiti da prove di taratura, effettuate secondo le periodicità prefissate a cura del personale preposto. Oltre alle verifiche dei controlli giornalieri, vanno effettuati i controlli di: STABILITÀ DI CONTEGGIO (CON SORGENTE CHECK) RISPOSTA RELATIVA E COSTANZA LINEARITÀ DELLA RISPOSTA ACCURATEZZA CALIBRAZIONI SUSSIDIARIE (GEOMETRIA) STABILITÀ DI CONTEGGIO (CON SORGENTE CHECK) L obiettivo è controllare la costanza della risposta del sistema esaminando la riproducibilità nel misurare la stessa sorgente su un lungo periodo di tempo. Questa prova dà un indice della riproducibilità della lettura dell elettrometro e dell integrità della camera a ionizzazione nel suo complesso. Idealmente, si dovrebbe misurare ogni giorno, prima dell utilizzo del calibratore, almeno una sorgente a tempo di dimezzamento relativamente lungo posta in una geometria riproducibile. Di solito si opta per l utilizzo del 137 Cs a causa della sua lunga emivita e della sua purezza radionuclidica, anche se possono essere utilizzati altri radionuclidi quali 57 Co, 60 Co, 133 Ba o 226 Ra. La procedura è quella che segue: 1) misurare la sorgente check utilizzando l impostazione appropriata per quel determinato radionuclide; 2) misurare il fondo di radiazione con le stesse impostazioni e sottrarlo all attività misurata al punto 1, oppure effettuare questa misura avendo già confermato il corretto funzionamento del circuito di sottrazione automatico del fondo; 3) per ogni sorgente utilizzata, registrare l attività misurata, l identità del radionuclide della sorgente check, la data del controllo e l impostazione di calibrazione utilizzata; 4) tolleranza: ± 2% sui risultati attesi, relativamente alle misure analoghe precedenti. 52
54 RISPOSTA RELATIVA E COSTANZA Questo controllo è progettato per garantire che le impostazioni del calibratore per particolari radionuclidi non siano cambiate. La procedura è sostanzialmente la stessa di quella usata per misurare la risposta della sorgente check. Il controllo andrà fatto su più sorgenti costituite dai radionuclidi di uso comune. La procedura è quella che segue: 1) misurare le sorgenti scelte utilizzando l impostazione del calibratore per l attività di un radionuclide di uso comune scelto come riferimento (ad esempio 137 Cs ); 2) misurare il fondo di radiazione alle stesse impostazioni e sottrarlo all attività misurata al punto 1, oppure effettuare questa misura avendo già confermato il corretto funzionamento del circuito di sottrazione automatico del fondo; il valore misurato non sarà quindi una corretta attività espressa nelle unità di misura selezionate, ma un semplice valore di riferimento la cui costanza può essere verificata ogni giorno di utilizzo; 3) tolleranza: ± 2% sui risultati attesi. LINEARITÀ DELLA RISPOSTA Questo controllo valuta se, per uno stesso radionuclide, può essere usata la stessa impostazione di calibrazione per indicarne l attività corretta su tutto il range di impiego del calibratore. In altri termini, non è altro che la costanza del rapporto tra la risposta fornita dal calibratore di dose ed il valore effettivo dell attività sottoposta a misura. È importante che la linearità del calibratore di attività per il radionuclide in questione sia verificata in tutto il range del suo uso tra la massima attività somministrata e 1 MBq (in genere, l attività massima somministrata di 99m Tc è circa 150 GBq). Ci sono più metodi possibili, qui ne verrà illustrato uno. Occorre prestare molta attenzione alla potenziale esposizione alle radiazioni degli operatori per lo svolgimento di questa prova. In ciascuna di queste prove, viene utilizzato il 99m Tc, la cui emivita vale 6,01 ore. Metodo del tempo di decadimento: 1) prendere una siringa o vial contenente un campione appena eluito di 99m Tc avente almeno la massima attività normalmente riscontrata nella pratica clinica quotidiana e posizionarlo nel calibratore. Selezionare il range di misura che normalmente si utilizza per la misurazione e il dosaggio dell attività del radionuclide. Sottrarre il fondo per ottenere l attività netta in MBq. Annotare la data e l ora al minuto più vicino; 2) ripetere il test ad intervalli di circa due ore durante la giornata lavorativa, ricordandosi di cambiare, se necessario, il range di misura. Continuare nei giorni successivi fino a quando l attività analizzata è inferiore a 1 MBq (se il calibratore può essere collegato in uscita ad un dispositivo di acquisizione 53
55 dati, si può lasciare la vial al suo interno e le misure saranno registrate automaticamente nell intero periodo di campionamento, riducendo così al minimo l esposizione alle radiazioni per l operatore); 3) convertire le ore e le date registrate in ore trascorse dalla prima misura; 4) i valori annotati, corretti per il decadimento, dovrebbero produrre il valore iniziale di attività del campione misurato. Ogni scostamento può essere attribuito ad un difetto di linearità; 5) tolleranza: ± 2%. ACCURATEZZA Questo controllo permette di garantire che i valori di attività determinati dal calibratore di attività siano riconducibili e paragonabili agli standard nazionali e internazionali all interno delle incertezze da essi indicate. Le sorgenti da utilizzare per questo scopo devono essere fornite di un certificato di calibrazione con specificato il livello d incertezza (di solito 1-5%). Ad ogni controllo di accuratezza, devono essere utilizzati almeno due radionuclidi, selezionati dalla lista di radionuclidi comunemente utilizzati. Idealmente, le sorgenti utilizzate saranno dello stesso volume e contenute negli stessi tipi di contenitori di quelli utilizzati nella routine. Si deve quindi: 1) inserire le sorgenti di taratura di 137 Cs, di 133 Ba o di 57 Co nel calibratore e registrare per ciascuna dieci letture sequenziali ad intervalli di 1 minuto. Sottrarre il fondo a ciascuna misura per ottenere le attività nette; 2) calcolare la media di tutte le misurazioni dello stesso radioisotopo per ognuno di essi e confrontare le medie ricavate con quelle indicate dal costruttore; 3) tolleranza: tenendo conto delle incertezza delle attività delle sorgenti di prova e dei loro decadimenti, gli scarti massimi tra i valori medi delle attività misurate e le attività certificate devono essere entro il ± 5%. CALIBRAZIONI SUSSIDIARIE (GEOMETRIA) Questo controllo serve per garantire che i fattori di calibrazione del calibratore per contenitori e volumi che sono diversi da quelli utilizzati nelle normali modalità cliniche, siano corretti. Per dimostrare ciò si deve: 1) prendere due aliquote della stessa soluzione di radionuclide e sistemarle in due contenitori. Uno di questi deve essere dello stesso tipo di quelli con cui vengono eseguiti i controlli di qualità e deve contenere quindi la massa di riferimento (o volume di calibrazione), l altro contenitore è quello per il quale è necessario il controllo di calibrazione (in alternativa l attività presente in questo contenitore può essere determinata per differenza, eseguendo cioè misure sul contenitore standard dal quale è stata prelevata la soluzione radioattiva da misurare prima e dopo il prelievo); 54
56 2) misurare l attività in entrambi i contenitori, sottrarre il fondo e correggere per il decadimento a un tempo di riferimento comune. Calcolare la concentrazione di attività per unità di massa (o volume) per ogni contenitore; 3) tolleranza: le due concentrazioni di attività così calcolate non devono differire di oltre il 5%. 4.3 Calibrazione della vial contenente le microsfere di 90 Y Nel nostro istituto utilizziamo principalmente le microsfere di 90 Y prodotte dalla Sirtex, le SIR-Spheres. Esse sono inviate dal produttore all interno di una vial (fiala), schermata con plexiglas, in cui si trovano sospese in acqua apirogena per preparazioni iniettabili per un totale di 5 ml per circa 3 GBq (81 mci) di attività, con un indeterminazione del 5% (vedi Figura 18). Questo permette di quantificare in termini di volume l attività necessaria per l iniezione ai singoli pazienti. L attività delle microsfere, piuttosto che il loro peso o volume, determina il numero di microsfere che verranno iniettate. Le microsfere sono preparate per l uso il giorno stesso della calibrazione a distanza di non più di 24 ore dal loro arrivo in Medicina Nucleare. Oltre le 24 ore, il numero di microsfere necessarie per fornire l attività desiderata aumenterebbe di circa il 30% e potrebbe superare, in alcuni pazienti, la capacità vascolare dei tumori. Le microsfere sono tipicamente realizzate circa 48 ore prima dell ora prevista per il trattamento o della data di calibrazione per tenere conto dei tempi di trasporto. Vial da 5 ml in cui sono contenute le microsfere Figura 18 Secondo le linee guida internazionali, l attività di un radiofarmaco a fini terapeutici dovrebbe essere accuratamente determinata e l errore di misura non dovrebbe superare il 5% in quanto si ha sempre più la necessità di calcolare con precisione la dose efficace per i pazienti da trattare e, in particolare, la dose agli organi bersaglio. A causa della grande rilevanza clinica, la metodologia di misura dell attività dell 90 Y, o di altri radionuclidi aventi una grande abbondanza di emissione β, è stata spesso 55
57 affrontata in Letteratura. Tuttavia, la metodologia di misurazione per l 90 Y è più impegnativa che quella per emettitori γ puri in quanto la misura dell attività di un emettitore β puro dipende principalmente dalla radiazione di bremsstrahlung e quindi le condizioni geometriche, una variabile non costante, con le quali viene misurata nel calibratore sono di estrema importanza. La distribuzione dei fotoni corrispondenti alla radiazione di bremsstrahlung è infatti criticamente dipendente da: volume della sorgente; geometria del contenitore della sorgente (dal raggio, nel nostro caso, di contenitori cilindrici); geometria dei dispositivi porta-campione all interno del calibratore; materiale del contenitore della sorgente; omogeneità della sospensione delle microsfere. Proprio per questi motivi il fattore di calibrazione per l 90 Y non può essere univocamente trovato, ma dovrebbe essere ogni volta, per ciascuna situazione, determinato. Per quanto riguarda le microsfere di 90 Y prodotte dalla Sirtex si è cercato di trovarlo nella maniera più precisa possibile le prime tre volte di utilizzo di questo dispositivo medico. In questi casi infatti, per eseguire le operazioni di calibrazione nel modo più accurato possibile, i certificati di calibrazione consegnateci insieme ai radiofarmaci sono stati forniti con un indeterminazione più piccola del solito, del 2%. Si è quindi introdotto nel calibratore di dose la prima di queste vial e determinato il fattore suddetto per quella specifica vial. Ripetendo poi le stesse misurazioni per le altre due vial si è potuto ottenere il fattore di calibrazione medio. Di seguito si riportano tutti questi passaggi. 56
58 IRCCS AOU San Martino-IST - HFS4 - U.O. FISICA MEDICA E SANITARIA TERAPIA RADIOMETABOLICA - 90Y-SIR SPHERES CALIBRAZIONE CAPINTEC CALIBRATORE: CAPINTEC MOD. CRC25R S/N INV La lettura, apparentemente in MBq, viene indicata come X48; va moltiplicata per 10 e per un fattore correttivo: Attività ( MBq ) LETTURA ( X 48 ) 10 TARATURA GEOMETRIA "RECEPTION VIAL" F rec_vial (FLACONE DA TRASPORTO) 15/04/ :57 misura RECEPTION VIAL 317 X48 unità arbitrarie (indicato MBq) attivita' nominale iniziale sorgente a determinata ora 3,364 GBq 90,92 mci attivita' nominale sorgente ora misura 3,365 GBq 90,95 mci concentrazione nominale ora misura 0,67 GBq/ml 18,11 mci/ml Fattore correttivo (calib): F rec_vial 1,062 REC_VIAL TARATURA GEOMETRIA "RECEPTION VIAL" F rec_vial (FLACONE DA TRASPORTO) 29/04/ :22 misura RECEPTION VIAL 317 X48 unità arbitrarie (indicato MBq) attivita' nominale iniziale sorgente a determinata ora 3,299 GBq 89,16 mci attivita' nominale sorgente ora misura 3,303 GBq 89,27 mci concentrazione nominale ora misura 0,66 GBq/ml 17,84 mci/ml Fattore correttivo (calib): F rec_vial 1,042 REC_VIAL TARATURA GEOMETRIA "RECEPTION VIAL" F rec_vial (FLACONE DA TRASPORTO) F CORR 14/05/ :05 misura RECEPTION VIAL 319 X48 unità arbitrarie (indicato MBq) attivita' nominale iniziale sorgente a determinata ora 3,384 GBq 91,46 mci attivita' nominale sorgente ora misura 3,381 GBq 91,38 mci concentrazione nominale ora misura 0,66 GBq/ml 17,84 mci/ml Fattore correttivo (calib): F rec_vial 1,060 REC_VIAL GEOMETRIA LETTURA F CORR RECEPTION VIAL SIRT moltiplicare lettura (MBq) X 10 X F REP_VIAL 1,054 Per le misure successive abbiamo utilizzato il medesimo calibratore di dose, il Capintec CRC-25R, precedentemente descritto, cercando di seguire le stesse condizioni e la stessa geometria predisposte durante la calibrazione di questo radiofarmaco. Il procedimento di misura consiste nel estrarre un certo volume di ittrio dalla vial preparata dalla Sirtex, che conterrà la quantità di radiofarmaco per un singolo paziente, e introdurlo nella vial di somministrazione, di forma differente dall altra vial (con il fondo a V, v-vial). A questo punto basterà rimisurare la prima vial, includendo già il fattore moltiplicativo medio di calibrazione, per determinare l attività all interno della nuova vial di somministrazione. Naturalmente è fondamentale che venga mantenuta sempre la stessa posizione della vial di misura all interno del calibratore di dose. Inoltre, l omogeneità del campione può incidere sulla misurazione della sua attività: in generale è necessario risospendere le SIR- Spheres agitando il contenitore per 10 s, introdurlo nel calibratore e aspettare circa 5 s prima di misurare l attività. Di solito non si riesce a prelevare subito il volume che corrisponda in modo soddisfacente all attività da somministrare, ma si devono eseguire varie prove fino a trovare il valore desiderato. Una misurazione, che ho potuto seguire in prima persona, è la seguente: 57
59 TARATURA GEOMETRIA "RECEPTION VIAL" F rec_vial (FLACONE DA TRASPORTO) 21/04/ :33 misura RECEPTION VIAL 317 X48 indicato in MBq attività calcolata sorgente ora misura 3,34 GBq 90,3 mci attivita' nominale sorgente ora misura 3,51 GBq 94,9 mci scarto misura/nominale -4,8% concentrazione calcolata ora misura 0,668 GBq/ml 18,1 mci/ml Fattore correttivo ( ) F rec_vial 1,054 REC_VIAL CALCOLO VOLUMI NOMINALI DA PRELEVARE 1 PREPARAZIONE: Paziente 21/04/ :00 ORA DI RIFERIMENTO PAZIENTE attività nominale (teorica) da prelevare 0,97 GBq 26,2 mci volume nominale da prelevare 1,5 ml prelevo volume nominale da REC_VIAL 21/04/ :53 misura residuo in RECEPTION VIAL 217 X48 indicato in MBq calcolo attività residua in REC_VIAL 2,29 GBq 61,8 mci calcolo attivita' iniz. in REC_VIAL ora mis 3,33 GBq 90,0 mci calcolo attività prelevata in siringa 5 ml 1,04 GBq 28,2 mci calcolo attività prelevata ora paziente 1,01 GBq 27,3 mci scarto da progetto 4% 58
60 CAPITOLO 5: I risultati sperimentali Abbiamo analizzato i casi dei pazienti trattati in questi ultimi due anni ( ) all Ospedale San Martino. Ci siamo concentrati su quelli per i quali abbiamo utilizzato le microsfere di 90 Y prodotte dalla Sirtex in quanto molto più numerosi e con un studio preliminare dosimetrico più aperto e modificabile, quindi in continua progressione. Come visto e descritto al CAPITOLO 3, paragrafo 3.2, si possono utilizzare vari metodi per determinare l attività di ittrio da somministrare ai pazienti. 5.1 Metodo empirico Solo i primi due pazienti, quando la pratica di questa terapia era solo all inizio e non era ancora stata standardizzata, nel 2009, sono stati trattati con il metodo empirico. Questo metodo è molto approssimativo, è basato solo su attività tabellate a seconda della stima del livello di sviluppo del tumore, e per questo fu presto abbandonato. 5.2 Metodo della BSA Con l evoluzione della ricerca si è poi passati ad usare il metodo della BSA che considera, oltre al volume del tumore e a quello dell intero fegato, l altezza e il peso dei pazienti. Anche se ancora abbastanza empirico, è tuttora il metodo indicato e consigliato dalla casa produttrice delle microsfere di 90 Y, cioè secondo il bugiardino (techinical datasheet) della Sirtex e quindi quello al quale i medici e i fisici devono attenersi. Ad esempio per il Signor PICCA, dopo l invio da parte dei medici nucleari di tutti i suoi dati clinici (volume del fegato, volume delle lesioni, ect.), estrapolati da elaborazioni sulla TAC, abbiamo calcolato il valore dello shunt polmonare (L) tramite le immagini SPECT planari pre-terapia (vedi CAPITOLO 3, paragrafo 3.1) e determinato, con il metodo della BSA, l attività da iniettare a questo paziente durante la terapia. CALCOLO SHUNT POLMONARE (DA PLANARE) ORGANO ANT POST MediaG % POLMONE ,0% FEGATO ,0% ALTRO % 59
61 altezza 174 cm peso 72 kg BSA 1,86 m2 Volumetrie basate su elaborazione TC del: 19/09/2014 V sx volume lobo sinistro (sano+lesioni) 203 cc V dx volume lobo destro (sano+lesioni) 1227 cc V total_liver volume fegato totale (sano + lesioni) 1430 cc Lesioni: T sx sul lobo destro volume lesioni lobo sinistro 0 cc T dx volume lesioni lobo destro 2,54 cc TARGET lobo/segmento da trattare destro V tumor_lobe volume lesioni (entro il lobo) 2,54 cc V total_lobe volume del lobo TARGET, incluse lesioni 1227 cc V NL volume fegato sano (tutto il fegato, meno lesioni) 1428 cc Captazioni basate su elaborazione MAA del: 31/10/2014 Volume polmonare equivalente V L 1000 cc densità tutti i tessuti (se >10%: ridurre attività; 1,0 g/cc Shunt polmonare (Lung Shunting) LS se >20%: STOP ) 3,0% METODO BSA (TRATTAMENTO LOBARE) SI L'attività viene adattata sulla base delle dimensioni del paziente e dell'estensione del tumore A lobe V [ GBq] BSA 0.2 V tumor_ lobe total_ lobe V V total_ lobe total_ liver Attività da somministrare al lobo TARGET A lobe 1,1 GBq Shunt polmonare L (Lung Shunting) (se >10%: ridurre attività; se >20%:STOP 3,0% Necessaria riduzione della dose (per L)? NO 0% Richiesta riduzione della dose per motivazione clinica? NO 0% Attività da impiantare (con eventuali riduzione): 1,1 GBq 5.3 Metodo partitivo Abbiamo inoltre sviluppando retrospettivamente, per alcuni pazienti, la procedura e i calcoli indicati dal metodo partitivo, sicuramente molto più preciso e particolareggiato rispetto a quello della BSA. Si devono risolvere le equazioni per A Total, limitando le dosi ai polmoni e al fegato sano, cioè imponendo D Lung = 20Gy e D NormalLiver = 80Gy e scegliendo l A Total minore ottenuta in modo da rispettare entrambi i vincoli. Per risolvere le equazioni di 60
62 questo metodo ci si deve prima ricavare i valori di L e T dalle analisi effettuate dopo N la somministrazione dei MAA. Il limite del metodo partitivo è che può essere usato sono nei casi in cui il tumore è localizzato in un area ben circoscritta e chiaramente definita; questo accade più di frequente in pazienti portatori di HCC dove il tumore può presentarsi solo come singola massa piuttosto che nei pazienti con metastasi secondarie al fegato dove si possono trovare molte lesioni diffuse, difficili da delineare. A Total = D Lungm Lung 50 L A Total = D NormalLiver[( T N m Tumour)+m NormalLiver ] 50(1 L) Procedimento: 1) si fondono (corregistrano), cioè si sovrappongono per tutti e tre gli assi, le immagini TAC (anatomiche) con quelle SPECT relative alla distribuzione dei Macroaggregati di Albumina marcati con 99m Tc (funzionali, di Medicina Nucleare) con l ausilio del medico nucleare; 2) si disegnano per alcune fette (di spessore 2,50 mm) una ROI interna al tumore e una esterna ad esso colpita comunque dal 99m Tc per quella particolare infusione; 3) si ricavano, tramite un programma (noi abbiamo utilizzato Xeleris), i conteggi medi per pixel di ogni ROI, si fa una media dei dati raccolti e si calcola il valore T N come il rapporto tra la media dei conteggi medi per pixel sul tumore e la media dei conteggi medi per pixel sul non tumore (Normal Liver, NL); 4) si calcola il valore di L seguendo la procedura precedentemente descritta, cioè tramite le immagini planari SPECT dei Magroaggregati di Albumina marcati con 99m Tc; 5) si risolvono le equazioni, già citate, riguardanti il metodo partitivo; 6) si paragonano i risultati ottenuti con quelli del metodo della BSA. 61
63 Ad esempio per il paziente PICCA : 1) fusione tra le immagini TAC e quelle SPECT: Fusione immagini TAC e SPECT 62
64 Immagini fuse sui tre assi (frontale, sagitale e assiale) Immagini fuse su sei "fette" TAC 63
65 2) disegno delle ROI sul tumore (ROI rosa) e sul non tumore (ROI blu) per una determinata fetta : Disegno delle ROI 3) acquisizione dei conteggi per le ROI sul tumore e per quelle sul non tumore per tutte e tre le fette prese in considerazione e calcolo di T N : 64
66 "PICCA" MAA DEL 31 OTTOBRE 2014 Name tumour_1_nm Name tumour_2_nm Name tumour_3_nm Avg count Avg count Avg count Max count Max count Max count Min count 11.0 Min count 16.0 Min count 36.0 Total count Total count Total count Area (pxls) Area (pxls) Area (pxls) Area (mm2) Area (mm2) Area (mm2) Name NL_1_NM Name NL_2_NM Name NL_3_NM Avg count Avg count Avg count Max count Max count Max count Min count 62.0 Min count 68.0 Min count 81.0 Total count Total count Total count Area (pxls) Area (pxls) Area (pxls) Area (mm2) Area (mm2) Area (mm2) T = N = T/N = 0,563 4) calcolo di L: CALCOLO SHUNT POLMONARE (DA PLANARE) ORGANO ANT POST MediaG % POLMONE ,0% FEGATO ,0% ALTRO % 65
67 5) risultati del metodo partitivo: METODO PARTITIVO (TRATTAMENTO SELETTIVO) SI Metodica MIRD multicompartimentale L'attività viene massimizzata nel rispetto delle dosi-limite ai polmoni e fegato sano Dose limite al polmone D L (< 25 Gy; preferibilmente < 20 Gy) 20 Gy Attività totale che corrisponde alla dose limite al polmone: 13,42 GBq Dose limite al fegato sano (media) D NT (<80 Gy; <70 Gy se cirrosi) 80 Gy Attività totale che corrisponde alla dose limite al fegato sano: Attività da impiantare con rispetto vincoli: 2,37 GBq 2,4 GBq 6) confronto tra il metodo della BSA e quello partitivo: ATTIVITA' PRESCRITTA, CONCORDATA CON IL MEDICO NUCLEARE METODO BSA PARTITIVO CONCORDATO ATTIVITA' DA IMPIANTARE 1,1 GBq 2,4 GBq 1,1 GBq Dose media lobo/segmento trattato 43 Gy 93 Gy 43 Gy Dose media fegato in toto 37 Gy 80 Gy 37 Gy Dose media fegato sano 80 Gy 37 Gy Dose media lesione 48 Gy 22 Gy Dose media polmone 2 Gy 4 Gy 2 Gy Ipotesi residuo in box post-trattamento: 10% Attività da preparare (al lordo del residuo) 1,21 GBq Paragonando i due metodi e i risultati da questi ottenuti si può affermare che il metodo partitivo è molto più preciso dell altro perché considera anche la distribuzione del 99m Tc, usata come simulazione del trattamento, e non si basa solo su dati clinici generali del paziente. D altra parte però, siccome il metodo partitivo determina la massima attività tollerabile per non danneggiare i polmoni e il fegato sano, da come risultati attività molto più elevate di quelle calcolate con il metodo BSA e quindi si deve essere sicuri che la dose da iniettare vada prevalentemente sul tumore e che il confronto con la distribuzione dei MAA sia attendibile. 66
68 5.4 Voxel dosimetry La teoria che, in un prossimo futuro, si cercherà di mettere in pratica in modo consolidato è la voxel dosimetry perché sicuramente la più completa e la più precisa. Seguendo questo metodo si ricava, analizzando le immagini SPECT relative all infusione dei 99m Tc-MAA e la loro sovrapposizione con quelle della TAC, l attività di 90 Y pixel per pixel che si depositerà sul tumore e sugli altri tessuti circostanti ad esso. Inoltre, calcolando il fattore di MIRD (S) si può risalire al valore della dose assorbita dagli organi punto per punto, e più specificatamente nei punti di interesse. In questo modo si può prevedere la distribuzione della dose assorbita, necessaria per lo studio dosimetrico dell 90 Y precedente alla terapia (vedi CAPITOLO 3, paragrafo 3.4). Un esempio dell elaborazioni delle immagini tramite il metodo della voxel dosimetry potrebbe essere il seguente (Figura 19): Figura 19 Si vede, tramite i vari colori e i loro rispettivi valori, il grado di assorbimento della dose da parte di ogni regione del fegato (b) e (c). Nelle due immagini TAC invece si vedono le dimensioni diminuite del tumore dopo la terapia con 90 Y (d) rispetto a prima di questa (a). 67
69 Si può anche sviluppare il grafico (vedi Figura 20) che definisce la quantità di dose assorbita in funzione della percentuale di volume di tumore considerato: Figura 20: Grafico della quantità di dose assorbita in funzione della percentuale di volume di tumore considerato. Questa procedura è per ora poco diffusa negli ospedali perché ancora frutto di ricerca, legata alla disponibilità di software non disponibili, per il momento, su larga scala e sicuramente un metodo molto più laborioso e dispendioso di tempo rispetto agli altri. 5.5 Verifica attività somministrata ed elaborazioni posttrattamento Si può, alla fine di ogni intervento, verificare l attività di 90 Y realmente somministrata ai pazienti raccogliendo tutte le misure effettuate prima, durante e dopo l operazione. Infatti, per ogni paziente trattato, i fisici sanitari dell Ospedale San Martino di Genova sono soliti compilare un questionario, dove inseriscono tutti i dati dosimetrici e radiometrici di ogni terapia effettuata per poterli elaborare statisticamente, per condurre considerazioni radioprotezionistiche (eventuali prescrizioni nella gestione del paziente durante il ricovero) e per stimare l attività effettivamente somministrata. In alcuni casi, per i pazienti trattati nel 2015, ho potuto assistere personalmente agli interventi, effettuare tutte le misure di radioprotezione, nonché prendere parte a tutte le considerazione dosimetriche. Il questionario del paziente analizzato prima è risultato il seguente: 68
70 IRCCS AOU San Martino-IST - HFS4 - U.O. FISICA MEDICA E SANITARIA MODHFS-4108-B rev TERAPIA RADIOMETABOLICA - 90Y-SIR SPHERES RACCOLTA DATI SUL CAMPO TREATMENT DAY/ID: 05/11/2014 SIR PM Place (city): Hospital: Measurement instrument (brand, type): Patient reference time (Name) Prescribed activity (GBq) for patient 1,1 GBq Patient reference time 15:30 Prepared activity (GBq) at patient reference time 1,00 GBq Application time 16:30 Delivered activity (GBq) 0,88 GBq Deviation from prescription -20% Pre application dose rate reference time 15:45 Dose rate in contact with V-Vial shield (µsv/hr) Dose rate at 1 meter of the V- Vial shield (µsv/hr) 175 µsv/hr 1,7 µsv/hr Dose rate in contact with the application box (µsv/hr) 60 µsv/hr Average value for lateral sides Dose rate at 1 meter off the box (µsv/hr) 1,7 µsv/hr From higher dose rate side Dose rate at 30 cm off the box (µsv/hr) 9,8 µsv/hr From higher dose rate side Application Post application dose rate reference time 17:30 Dose rate in contact with the patient (µsv/hr) 30 µsv/hr Just after application Dose rate at 1 meter of the patient (µsv/hr) 2 µsv/hr Background measured Dose rate at catheter (max) 550 µsv/hr During application Dose rate at catheter (max) 10 µsv/hr Residual activity after application Residual dose rate in contact with the application box (µsv/hr) 6,5 µsv/hr Average value for lateral sides Residual activity estimated end of application (GBq) 0,11 GBq Residual percent activity end of application 11% Dose Calibrator Type: Capintec CRC 25R GENOVA IRCCS AOU San Martino-IST Ionization chamber Victoreen 451B "PICCA" Questa tabella viene compilata dal fisico sanitario che, presente in sala operatoria, effettua le misure radiometriche. Si inseriscono il valore dell attività prescritta per quel determinato paziente, l ora presunta dell intervento e l attività preparata in riferimento a quell ora, considerando il decadimento dell 90 Y fino a quel momento. Nel FORM vanno compilate solo le celle a sfondo azzurro perché le altre contengono formule. Inoltre si introducono i dati relativi all ora esatta della pratica terapeutica, 69
71 alle misurazioni dei rate di dose antecedenti la terapia a contatto del box contenente la fiala di 90 Y e in altre situazioni e l ora in cui vengono effettuate. Vengono presi anche i valori dei rate di dose subito dopo l intervento come il rate di dose a contatto con il paziente o quello vicino al suo catetere di iniezione. Con questi dati si può calcolare l attività realmente somministrata al paziente sottraendo all attività preparata, scalata per il decadimento dell 90 Y tra l ora di riferimento della terapia e quella effettiva, l attività residua. L attività residua si ricava dividendo il rate della dose residua a contatto del box per il fattore che converte i rate della dose in attività ((µsv/hr)/gbq), precedentemente calcolato per il caso specifico. Poi si moltiplica anche qui per l esponenziale che tiene conto del decadimento dell 90 Y tra l ora delle misure post intervento e quella dell inizio della procedura. La formula per il decadimento radioattivo è: A dec = A 2 (t 1 t 2 )/T 1/2 dove T 1/2 dell 90 Y=2,671 giorni Mentre il fattore di conversione si ottiene ad esempio dividendo il valore del rate della dose a contatto con il box misurato prima dell intervento per il valore dell attività preparata ricalcolata in base all ora delle misurazioni dei rate di dose come quella precedente. Abbiamo inoltre confrontato le immagini SPECT fuse pre-terapia della biodistribuzione dei MAA marcarti con 99m Tc con quelle post-terapia della biodistribuzione dell 90 Y, ottenute sempre con la SPECT e riferite entrambe al trattamento precedentemente descritto: 70
72 Immagini fuse della distruzione dei MAA pre-terapia Immagini fuse della distribuzione dell' 90 Y post-terapia 71
73 Si può notare che, anche se non sono perfettamente identiche (situazione abbastanza difficile da trovare viste le diverse caratteristiche fisiche dei due radionuclidi), sono in gran parte simili. Si deve anche specificare che il medico nucleare, sulla base dei risultati del pre-trattamento, può modificare, se lo ritiene necessario, le modalità di iniezione del radiofarmaco per migliorare il più possibile il percorso e i punti di fissazione delle microsfere di 90 Y durante la terapia. In questo caso infatti, essendo un trattamento lobare destro (cioè la radiazione deve colpire tutto il lobo e non solo una specifica lesione), si evidenzia, giustamente, nelle immagini post-trattamento, una più estesa distribuzione dell ittrio su quel lobo. 5.6 Database pazienti Rielaborando e raccogliendo tutti i dati, clinici e dosimetrici, dei pazienti finora trattati con questa terapia si può costruire un database completo utile agli studi di ricerca. Quello che ho fatto io, con il mio lavoro di tesi, è stato revisionare e raccogliere tutte le informazioni rilevanti riguardanti i pazienti sottoposti a 90 Y-TARE (dal 2014), cercare di migliorare e ottimizzare alcune procedure, soprattutto quella sullo studio dosimetrico, e aggiornare il database con i dati dei pazienti che ho potuto seguire in prima persona (2015). A proposito degli aspetti clinici si possono rilevare l età, il sesso e le patologie più diffuse tra questi pazienti; vengono indicati anche il tipo di trattamento che è stato effettuato, se lobare o segmentario, e il tipo di somministrazione, in quale arteria epatica si deve sviluppare l iniezione e se viene frazionata la dose durante l iniezione. 72
74 Dati clinici 73
75 Per quanto riguarda i risultati dosimetrici si possono, per ogni caso, confrontare i valori di attività ottenuti con il metodo della BSA con quelli ottenuti con il metodo partitivo (stimando il valore T/N) e calcolare le dosi assorbite dalle lesioni, dall intero fegato e dai polmoni in funzione dell attività, approvata dal medico nucleare, realmente somministrata. Si può infatti fare una stima dell attività residua, persa per ragioni di procedura (rimasta nella siringa di somministrazione) e di decadimento, dalle misure dei pazienti già trattati e utilizzarla nelle future valutazioni dosimetriche pre-intervento (circa il 10% dell attività concordata). Infine in Appendice si riporta il database completo di tutti i dati, clinici e dosimetrici, di tutti i pazienti curati al San Martino con questa terapia (una quindicina), illustrando anche i valori morfologici del fegato, estrapolati dagli esami TAC in Medicina Nucleare, come i volumi dei due lobi del fegato e quelli delle lesioni. 74
76 ID paziente BSA L (shunt polmonare) Attività calcolata con il metodo della BSA (GBq) Dose Lobo/Segmento trattato (Gy) Dose Fegato totale (Gy) Dose polmone (Gy) Attività calcolata con il metodo partitivo (GBq) Attività concordata da somministrare (GBq) Attività concordata da preparare al lordo del residuo (GBq) Delivered activity (GBq) Residual activity estimated end of application (GBq) Dati dosimetrici SIR FCA 1,58 0,1% 0, ,6 0,0 2,18 0,50 0,55 0,41 0,02 SIR FR (A) 1,73 2,4% 1, ,9 1,2 4,31 1,02 1,122 0,79 0,04 SIR FR (B) 1,73 2,4% 0, ,1 0,1 4,31 0,27 0,297 0,24 0,01 SIR CAM 1,52 2,2% 0, ,7 0,3 1,89 0,50 0,55 0,54 0,01 SIR GR 1,70 0,1% 1, ,8 0,1 2,10 1,58 1,738 1,43 0,01 SIR AC 1,71 0,1% 0, ,7 0,0 3,39 0,60 0,66 0,60 0,06 SIR FE (A) 1,45 3,0% 1, ,2 1,6 2,62 1,20 1,32 0,45 0,11 SIR FE (B) 1,45 3,0% 1, ,2 1,6 2,62 1,20 1,32 0,57 0,07 SIR SA 1,45 3,5% 0, ,4 1,0 5,05 0,60 0,66 0,69 0,08 SIR PM (1) 1,86 11,0% 1, ,3 6,2 2,59 1,10 1,21 0,88 0,11 SIR RG (A) 2,20 1,5% 1, ,0 1,1 4,41 1,52 1,672 1,48 0,10 SIR RG (B) 2,20 1,5% 0, ,6 0,4 4,41 0,43 0,473 0,40 0,06 SIR LA (1) 1,68 3,7% 0, ,7 1,8 2,24 0,97 1,067 0,968 0,03 SIR VD 1,69 1,8% 0, ,0 0,6 3,52 0,71 0,781 0,688 0,04 SIR SP 1,77 1,7% 1, ,3 1,0 3,42 1,30 1,43 1,23 0 SIR VA 1,67 1,1% 1, ,1 0,7 4,53 1,25 1,375 1,20 0,09 SIR LA (2) 1,52 3,3% 0, ,8 1,0 2,38 0,67 0,737 0,61 0,03 SIR PM (2) (A) 1,88 10,0% 1, ,2 7,5 2,50 1,27 1,397 1,08 0,11 SIR PM (2) (B) 1,88 1,5% 0, ,3 0,1 2,29 0,31 0,341 0,25 0,09 SIR PM (3) 1,90 3,0% 0, ,6 1,3 2,49 0,82 0,902 0,69 0,10 SIR CG 1,98 2,2% 1, ,3 1,6 4,48 1,53 1,683 1,36 0,20 75
77 CONCLUSIONI La terapia con consegna in arteria epatica di microsfere di 90 Y è una promettente nuova cura per i tumori al fegato. Infatti, le risposte finora ottenute sono sufficientemente elevate da rendere probabile l ipotesi che questo trattamento possa avere un grande impatto sulla sopravvivenza di questi pazienti. Dai dati e le analisi post-terapia si rilevano, per un numero discreto di pazienti, la diminuzione dei volumi tumorali e l aumento del tempo a progressione del tumore; questo permette il miglioramento della qualità e delle aspettative di vita di questi pazienti. Si stanno però ancora analizzando statisticamente gli effetti di questo trattamento e, soprattutto, verificando se questa terapia combinata con altre, come la chemioterapia, possa essere più efficiente per la guarigione del paziente. Inoltre il miglioramento della costruzione delle immagini e della metodologia per il calcolo dosimetrico stanno cominciando a produrre stime della dose sempre più accurate e personalizzate. Un esempio di come il tumore possa regredire dopo questo tipo di intervento è evidenziabile con le seguenti immagini: TAC SCAN PRE-SIRT TAC SCAN 6 MESI POST-SIRT 76
78 ID paziente CdC provenienza PATOLOGIA Tipo trattamento Note cliniche Data prevista trattamento ANNO nato il SESSO ETA' APPENDICE SIR FCA H04D METASTASI DA CCR LOBARE, LOBO DESTRO 15/04/ /03/1959 F 55 SIR FR (A) H04D HCC EPATOCARCINOMA LOBARE, LOBO DESTRO SIR FR (B) H04D HCC EPATOCARCINOMA LOBARE, LOBO SINISTRO lesione ripartita tra i due lobi; trattamento suddiviso tra i due lobi lesione ripartita tra i due lobi; trattamento suddiviso tra i due lobi 15/04/ /08/1963 M 51 15/04/ /08/1963 M 51 SIR CAM H04D METASTASI DA CCR LOBARE, LOBO SINISTRO 29/04/ /09/1954 F 60 SIR GR H04D METASTASI DA COLANGIOCARCINOMA CELLULARE (LOBARE, LOBO SINISTRO il fegato è costituito dal solo lobo sinistro perché il destro è stato asportato 29/04/ /05/1936 F 78 SIR AC H04D HCC EPATOCARCINOMA SEGMENTARIO,SEGMENTI: S-VII e S-VIII 14/05/ /01/1964 M 50 SIR FE (A) H04D METASTASI DA CCR LOBARE, LOBO DESTRO SIR FE (B) H04D METASTASI DA CCR LOBARE, LOBO DESTRO SIR SA H04D METASTASI DA NEUROENDOCRINO LOBARE, LOBO DESTRO La dose dovrà essere ripartita 50%-50% in due 29/05/2014 vasi differenti (due somministrazioni) /03/1952 F 62 La dose dovrà essere ripartita 50%-50% in due 29/05/2014 vasi differenti (due somministrazioni) /03/1952 F 62 La lesione da 111 cc non capta i MAA, si tratta 29/05/2014 il resto del lobo destro /05/1934 F 80 SIR PM (1) H04D METASTASI DA CCR LOBARE, LOBO DESTRO 05/11/ /10/1953 M 61 SIR RG (A) H04D METASTASI LOBARE, LOBO DESTRO SIR RG (B) H04D METASTASI LOBARE, LOBO SINISTRO SIR LA (1) H04D METASTASI da K-pancreatico LOBARE, LOBO DESTRO SIR VD H2AD HCC primitivo multifocale (esteso) LOBARE, LOBO SINISTRO volume bersaglio: fegato in toto (infatti viene trattato anche il lobo sinistro) 05/11/ /06/1968 M 46 volume bersaglio: fegato in toto (infatti viene trattato anche il lobo destro) 05/11/ /06/1968 M 46 in due dosi 50%-50%:1-arteria epatica destra antero-mediale; 2-arteria postero-laterale 11/12/ /03/1950 F 64 singola somministrazione: nell'arteria epatica 11/12/2014 sinistra /09/1960 M 54 SIR SP H04D METASTASI DA CCR con secondarietà epatiche LOBARE, LOBO DESTRO 08/01/ /12/1963 M 52 SIR VA H04D METASTASI DA COLANGIOCARCINOMA CELLULARE (LOBARE, LOBO DESTRO 08/01/ /05/1978 M 37 SIR LA (2) H04D METASTASI da K-pancreatico LOBARE, LOBO SINISTRO 21/04/ /03/1950 F 65 SIR PM (2) (A) H04D METASTASI DA CCR LOBARE, LOBO DESTRO 21/04/ /10/1953 M 62 SIR PM (2) (B) H04D METASTASI DA CCR SEGMENTARIO, SEGMENTI: S-IV teriografia in arteria epatica comune (rami per S-I21/04/ /10/1953 M 62 SIR PM (3) H04D METASTASI DA CCR LOBARE, LOBO SINISTRO (SII) cc + 10 cc (SIV)+ 31 cc (SI) + 2 cc (SIV) +1 cc (SI30/06/ /10/1953 M 62 SIR CG H04D METASTASI DA CCR LOBARE, LOBO DESTRO rteria epatica dx: rami per seg. SVII ed SVIII Due s 30/06/ /11/1958 M 57 77
79 ID paziente BSA Data TAC Vsx Vdx Vtotal_liver Tsx Tdx Vtotal_lobe VNL Data MAA L (shunt polmonare) Attività calcolata con il metodo della BSA (GBq) Dose Lobo/Segmento trattato (Gy) Dose Fegato totale (Gy) Dose polmone (Gy) Attività calcolata con il metodo partitivo (GBq) Attività concordata da somministrare (GBq) Attività concordata da preparare al lordo del residuo (GBq) Data effettiva trattamento Delivered activity (GBq) Residual activity estimated end of application (GBq) Data controlli post SIR FCA 1,58 03/04/ /04/2014 0,1% 0, ,6 0,0 2,18 0,50 0,55 15/04/2014 0,41 0,02 16/04/2014 SIR FR (A) 1, ,8 122, ,3 31/03/2014 2,4% 1, ,9 1,2 4,31 1,02 1,122 15/04/2014 0,79 0,04 16/04/2014 SIR FR (B) 1, ,8 122, ,2 31/03/2014 2,4% 0, ,1 0,1 4,31 0,27 0,297 15/04/2014 0,24 0,01 16/04/2014 SIR CAM 1,52 27/03/ ,5 928,4 1144,9 57, , /04/2014 2,2% 0, ,7 0,3 1,89 0,50 0,55 29/04/2014 0,54 0,01 30/04/2014 SIR GR 1, , ,9 04/04/2014 0,1% 1, ,8 0,1 2,10 1,58 1,738 29/04/2014 1,43 0,01 30/04/2014 SIR AC 1, , ,4 18/04/2014 0,1% 0, ,7 0,0 3,39 0,60 0,66 14/05/2014 0,60 0,06 15/05/2014 SIR FE (A) 1, , ,4 27/05/2014 3,0% 1, ,2 1,6 2,62 1,20 1,32 29/05/2014 0,45 0,11 30/05/2014 SIR FE (B) 1, , ,4 27/05/2014 3,0% 1, ,2 1,6 2,62 1,20 1,32 29/05/2014 0,57 0,07 30/05/2014 SIR SA 1, /05/2014 3,5% 0, ,4 1,0 5,05 0,60 0,66 29/05/2014 0,69 0,08 30/05/2014 SIR PM (1) 1,86 19/09/ , ,4 0 2, ,9 31/10/ ,0% 1, ,3 6,2 2,59 1,10 1,21 05/11/2014 0,88 0,11 06/11/2014 SIR RG (A) 2,20 07/10/ /10/2014 1,5% 1, ,0 1,1 4,41 1,52 1,672 05/11/2014 1,48 0,10 06/11/2014 SIR RG (B) 2,20 07/10/ /10/2014 1,5% 0, ,6 0,4 4,41 0,43 0,473 05/11/2014 0,40 0,06 06/11/2014 SIR LA (1) 1,68 19/11/ , ,3 09/12/2014 3,7% 0, ,7 1,8 2,24 0,97 1,067 11/12/2014 0,968 0,03 12/12/2014 SIR VD 1,69 17/11/ , ,2 10/12/2014 1,8% 0, ,0 0,6 3,52 0,71 0,781 11/12/2014 0,688 0,04 12/12/20114 SIR SP 1,77 26/11/ /12/2014 1,7% 1, ,3 1,0 3,42 1,30 1,43 08/01/2015 1, /01/2015 SIR VA 1, /12/2014 1,1% 1, ,1 0,7 4,53 1,25 1,375 08/01/2015 1,20 0,09 09/01/2015 SIR LA (2) 1,52 30/01/ , ,2 12/03/2015 3,3% 0, ,8 1,0 2,38 0,67 0,737 21/04/2015 0,61 0,03 22/04/2015 SIR PM (2) (A) 1,88 20/03/ , ,8 21/04/ ,0% 1, ,2 7,5 2,50 1,27 1,397 22/04/2015 1,08 0,11 23/04/2015 SIR PM (2) (B) 1,88 20/03/ , ,2 21/04/2015 1,5% 0, ,3 0,1 2,29 0,31 0,341 22/04/2015 0,25 0,09 23/04/2015 SIR PM (3) 1,90 25/06/ /06/2015 3,0% 0, ,6 1,3 2,49 0,82 0,902 30/06/2015 0,69 0,10 01/07/2015 SIR CG 1,98 13/05/ /06/2015 2,2% 1, ,3 1,6 4,48 1,53 1,683 30/06/2015 1,36 0,20 01/07/
80 BIBLIOGRAFIA - Mazzaferro V, Sposito C, Bhoori S, Romito R, et al. Yttrium-90 radioembolization of intermediate-advanced hepatocarcinoma: a phase 2 study. Hepatology, 2013 May. - Llovet JM, Bru C, Bruix J. Prognosis of Hepatocellular Carcinoma: The BCLC Staging Sistem. Seminars in Liver Disease, Lau WY, Sangro B, Chen PJ, Cheng SQ. et al. Treatment for hepatocellular carcinoma with portal vein thrombosis: the emerging role for radioembolization using yttium-90. Oncology, Kim YH, Kim do Y. Yttrium 90 radioembolization for hepatocellular carcinoma: what we know and what we need to know. Oncology, Bolondi L, Piscaglia F. Yttrium 90 radioembolization: the horizon is changing for patients with intermediate and advanced hepatocellular carcinoma. Hepatology, 2013 May. - Memon K, Lewandowski RJ, Riaz A, Salem R. Yttrium 90 microspheres for the treatment of hepatocellular carcinoma. Recent Results Cancer Res, Yu N, Srinivas SM, Difilippo FP, Shrikanthan S. et al. Lung dose calculation with SPECT/TC for 90Yttrium radioembolization of liver cancer. Int. J. Radiat. Oncol. Biol. Phys Mar. - Shi J, Lai EC, Li N. et al. Surgical treatment of hepatocellular carcinoma with portal vein tumor thrombus. Ann. Of Surg. Oncology, 2010 Aug. - Townsend A, Price T, Karapetis C. Selective internal radiation therapy for liver metastases from colorectal cancer. Cochrane Database Syst Rev, 2009 Oct 7. - Zhen-Wei Peng, Rong-Ping Guo et al. Hepatic Resection versus transcatheter arterial chemoembolization for the treatment of hepatocellular carcinoma with portal vein tumor thrombus. Cancer, 2012 Oct 1. - Inoue Y., Hasegawa K, Makuuchi M. et al. Is there any difference in survival according to the portal tumor thrombectomy method in patients with hepatocellular carcinoma? Surgery, 2009 Jan. - Lencioni R, Llovet JM. Modified RECIST (mrecist) assessment for hepatocellular carcinoma. Sem. Liver Dis D. Delacroix et al; Radionuclide and radiation protection data handbook; Radiation protection dosimetry Vol. 98, Number 1, Yung Hsiang Kao et al. General Theory of Predictive Dosimetry for Yttrium- 90,Radioembolization to Sites Other than the Liver. Received: 22 July 2013 / Accepted: 10 September 2013 / Published online: 15 November Andrew Kennedy, Douglas Coldwell, Bruno Sangro, Harpreet Wasan and Riad Salem. Radioembolization for the Treatment of Liver Tumors General 79
81 Principles. American Journal of Clinical Oncology, Volume 35, Number 1, February Francesco Giammarile, Lisa Bodei, Carlo Chiesa, Glenn Flux, Flavio Forrer, Françoise Kraeber-Bodere, Boudewijn Brans, Bieke Lambert, Mark Konijnenberg, Françoise Borson-Chazot & Jan Tennvall and Markus Luster, the Therapy, Oncology and Dosimetry Committees. EANM procedure guideline for the treatment of liver cancer and liver metastases with intra-arterial radioactive compounds. Published online: 15 April C. Chiesa, M. Mira, M. Maccauro, R. Romito, C. Spreafico, C. Sposito, S. Bhoori, C. Morosi, S. Pellizzari, A. Negri, E. Civelli, R. Lanocita, T. Camerini, C. Bampo, M. Carrara, E. Seregni, A. Marchianò, V. Mazzaferro, E. Bombardieri. A dosimetric treatment planning strategy in radioembolization of hepatocarcinoma with 90Y glass microspheres. The quarterly journal of nuclear medicine and molecular imaging, William A. Dezarn, Jeffery T. Cessna, Larry A. DeWerd, Wenzheng Feng, Vanessa L. Gates, James Halama, Andrew S. Kennedy, Subir Nag, Mehrdad Sarfaraz, Varun Sehgal, Reed Selwyn, Michael G. Stabin, Bruce R. Thomadsen, Lawrence E. Williams, Riad Salem. Recommendations of the American Association of Physicists in Medicine on dosimetry, imaging, and quality assurance procedures for 90Y microsphere brachytherapy in the treatment of hepatic malignancies. Received: 8 April 2011; revised: 16 June 2011; accepted for publication: 17 June 2011; published: 1 August Marta Cremonesi, Carlo Chiesa, Lidia Strigari, Mahila Ferrari, Francesca Botta, Francesco Guerriero, Concetta De Cicco, Guido Bonomo, Franco Orsi, Lisa Bodei, Amalia Di Dia, Chiara Maria Grana and Roberto Orecchia. Radioembolization of hepatic lesions from a radiobiology and dosimetric perspective. Published: 19 August Kao et al. Personalized predictive lung dosimetry by technetium-99m macroaggregated albumin SPECT/CT for yttrium-90 radioembolization. EJNMMI Research, Elschot M, Nijsen JFW, Dam AJ, de Jong HWAM. Quantitative Evaluation of Scintillation Camera Imaging Characteristics of Isotopes Used in Liver Radioembolization. PLoS ONE, Pasciak et al. A Comparison of Techniques for 90Y PET/CT Image-Based Dosimetry Following Radioembolization with Resin Microspheres. Frontiers in Oncology, May Roshan et al. Advances in SPECT for Optimizing the Liver Tumors Radioembolization Using Yttrium-90 Microspheres. World Journal of Nuclear Medicine, Volume 14, May
Dall invisibile al visibile: le immagini diagnostiche in medicina
 CT [ 18 F]FDG PET Dall invisibile al visibile: le immagini diagnostiche in medicina Claudio Landoni Dipartimento di Scienza della Salute Come eravamo. Fino alla fine dell 800 indagare la struttura di un
CT [ 18 F]FDG PET Dall invisibile al visibile: le immagini diagnostiche in medicina Claudio Landoni Dipartimento di Scienza della Salute Come eravamo. Fino alla fine dell 800 indagare la struttura di un
Lezione 25 Radiazioni Ionizzanti. Rivelatori di Particelle 1
 Radiazioni Ionizzanti Rivelatori di Particelle 1 Diagnostica con radiazioni ionizzanti Diagnostica: Radiografia Tac Medicina nucleare (SPECT e PET) Rivelatori di Particelle 2 Diagnostica La diagnostica
Radiazioni Ionizzanti Rivelatori di Particelle 1 Diagnostica con radiazioni ionizzanti Diagnostica: Radiografia Tac Medicina nucleare (SPECT e PET) Rivelatori di Particelle 2 Diagnostica La diagnostica
Le neuroimmagini: come la scienza e la tecnologia ci aiutano a studiare le funzioni del cervello. Event funded by FP7-Eu project DECIDE
 Le neuroimmagini: come la scienza e la tecnologia ci aiutano a studiare le funzioni del cervello Event funded by FP7-Eu project DECIDE Le neuroimmagini: visualizzazione in vivo del cervello Il termine
Le neuroimmagini: come la scienza e la tecnologia ci aiutano a studiare le funzioni del cervello Event funded by FP7-Eu project DECIDE Le neuroimmagini: visualizzazione in vivo del cervello Il termine
andate, insegnate, guarite.
 andate, insegnate, guarite. Fondazione Istituto San Raffaele G.Giglio di Cefalù Servizio di Medicina Nucleare Servizio accoglienza: 0921 920553 Centro prenotazioni: 0921 920564 Servizio di Medicina Nucleare:
andate, insegnate, guarite. Fondazione Istituto San Raffaele G.Giglio di Cefalù Servizio di Medicina Nucleare Servizio accoglienza: 0921 920553 Centro prenotazioni: 0921 920564 Servizio di Medicina Nucleare:
L acquisizione e l elaborazione delle immagini di Medicina Nucleare
 L acquisizione e l elaborazione delle immagini di Medicina Nucleare UNIVERSITÀ DEGLI STUDI DI MILANO Materiale didattico a cura della Dott.ssa Michela Lecchi Medicina Nucleare: strumentazione gamma camera
L acquisizione e l elaborazione delle immagini di Medicina Nucleare UNIVERSITÀ DEGLI STUDI DI MILANO Materiale didattico a cura della Dott.ssa Michela Lecchi Medicina Nucleare: strumentazione gamma camera
SPECT (Gamma Camera)
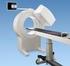 SPECT-PET Nella tomografia a raggi-x si usa la misura del coefficiente di attenuazione del tessuti per dedurre informazioni diagnostiche sul paziente. La tomografia ad emissione d altra parte utilizza
SPECT-PET Nella tomografia a raggi-x si usa la misura del coefficiente di attenuazione del tessuti per dedurre informazioni diagnostiche sul paziente. La tomografia ad emissione d altra parte utilizza
FISICA delle APPARECCHIATURE per MEDICINA NUCLEARE
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per MEDICINA NUCLEARE (lezione, 15.05.13) Marta Ruspa 1 Requisiti
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per MEDICINA NUCLEARE (lezione, 15.05.13) Marta Ruspa 1 Requisiti
Dottor LOMUSCIO Giuseppe Responsabile di Struttura Semplice Dipartimentale UO Medicina Nucleare - Azienda Ospedaliera BUSTO ARSIZIO - Varese
 Dottor LOMUSCIO Giuseppe Responsabile di Struttura Semplice Dipartimentale UO Medicina Nucleare - Azienda Ospedaliera BUSTO ARSIZIO - Varese L adesione alle Linee Guida NON sarà assicurare al Paziente
Dottor LOMUSCIO Giuseppe Responsabile di Struttura Semplice Dipartimentale UO Medicina Nucleare - Azienda Ospedaliera BUSTO ARSIZIO - Varese L adesione alle Linee Guida NON sarà assicurare al Paziente
Introduzione. Obiettivi
 Tecniche di studio RM per la quantificazione di flusso intracerebrale e sue applicazioni. Dr TSRM Giorgi Riccardo Fondazione I.R.C.C.S. Istituto Neurologico Carlo Besta di Milano Introduzione Una delle
Tecniche di studio RM per la quantificazione di flusso intracerebrale e sue applicazioni. Dr TSRM Giorgi Riccardo Fondazione I.R.C.C.S. Istituto Neurologico Carlo Besta di Milano Introduzione Una delle
Diagnostica medico-nucleare delle patologie polmonari
 Diagnostica medico-nucleare delle patologie polmonari Distretto vascolare Distretto ventilatorio Deficit combinato-matched Deficit non combinato-mismatched Embolia polmonare Associata ad alta mortalità
Diagnostica medico-nucleare delle patologie polmonari Distretto vascolare Distretto ventilatorio Deficit combinato-matched Deficit non combinato-mismatched Embolia polmonare Associata ad alta mortalità
Foto stroboscopica di una palla lasciata cadere da ferma (palla rossa) nello stesso istante in cui un altra (palla gialla) è sparata orizzontalmente
 Il sistema cardiocircolatorio Foto stroboscopica di una palla lasciata cadere da ferma (palla rossa) nello stesso istante in cui un altra (palla gialla) è sparata orizzontalmente verso destra. Come si
Il sistema cardiocircolatorio Foto stroboscopica di una palla lasciata cadere da ferma (palla rossa) nello stesso istante in cui un altra (palla gialla) è sparata orizzontalmente verso destra. Come si
PET: caratteristiche tecniche e funzionamento
 CORSO (TC-) PET - RADIOTERAPIA: METODICHE A CONFRONTO NELLA REALTA DELL AZIENDA PET: caratteristiche tecniche e funzionamento Elisa Grassi Servizio di Fisica Sanitaria ASMN Il nostro viaggio Tomografia
CORSO (TC-) PET - RADIOTERAPIA: METODICHE A CONFRONTO NELLA REALTA DELL AZIENDA PET: caratteristiche tecniche e funzionamento Elisa Grassi Servizio di Fisica Sanitaria ASMN Il nostro viaggio Tomografia
La radioattività. La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche.
 La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
Fegato (inclusi dotti biliari intraepatici)
 14 Fegato (inclusi dotti biliari intraepatici) 14 (Esclusi i sarcomi ed i tumori metastatici al fegato) C22.0 Fegato C22.1 Dotti biliari intraepatici RIASSUNTO DELLE MODIFICHE In questa edizione le categorie
14 Fegato (inclusi dotti biliari intraepatici) 14 (Esclusi i sarcomi ed i tumori metastatici al fegato) C22.0 Fegato C22.1 Dotti biliari intraepatici RIASSUNTO DELLE MODIFICHE In questa edizione le categorie
Medicina Nucleare sistematica: Terapia Radiometabolica
 UNIVERSITÀ DEGLI STUDI DI FERRARA Corso di Laurea Magistrale in Medicina e Chirurgia Corso Integrato di Diagnostica per Immagini e Radioprotezione (A.A. 2015-16) Diagnostica per Immagini e Radioterapia
UNIVERSITÀ DEGLI STUDI DI FERRARA Corso di Laurea Magistrale in Medicina e Chirurgia Corso Integrato di Diagnostica per Immagini e Radioprotezione (A.A. 2015-16) Diagnostica per Immagini e Radioterapia
M. Marengo CALIBRATORI DI ATTIVITA E LORO USO IN MEDICINA NUCLEARE. Medical Physics Department S.Orsola Malpighi University Hospital, Bologna, Italy
 M. Marengo CALIBRATORI DI ATTIVITA E LORO USO IN MEDICINA NUCLEARE Medical Physics Department S.Orsola Malpighi University Hospital, Bologna, Italy [email protected] Maniglia del centratore per i
M. Marengo CALIBRATORI DI ATTIVITA E LORO USO IN MEDICINA NUCLEARE Medical Physics Department S.Orsola Malpighi University Hospital, Bologna, Italy [email protected] Maniglia del centratore per i
Le radiazioni in medicina. Dott.ssa Rossella Vidimari Fisico dirigente di I livello Struttura Complessa di Fisica Sanitaria A. O. U.
 Le radiazioni in medicina Dott.ssa Rossella Vidimari Fisico dirigente di I livello Struttura Complessa di Fisica Sanitaria A. O. U. di Trieste Fisica Nucleare Fisica delle Particelle Elementari Astrofisica
Le radiazioni in medicina Dott.ssa Rossella Vidimari Fisico dirigente di I livello Struttura Complessa di Fisica Sanitaria A. O. U. di Trieste Fisica Nucleare Fisica delle Particelle Elementari Astrofisica
UNIVERSITA DEGLI STUDI DI BARI
 UNIVERSITA DEGLI STUDI DI BARI FACOLTA DI MEDICINA E CHIRURGIA Sezione di Diagnostica per Immagini DIRETTORE: Prof. Giuseppe Angelelli METASTASI OSSEE: imaging Arnaldo Scardapane Le ossa sono una delle
UNIVERSITA DEGLI STUDI DI BARI FACOLTA DI MEDICINA E CHIRURGIA Sezione di Diagnostica per Immagini DIRETTORE: Prof. Giuseppe Angelelli METASTASI OSSEE: imaging Arnaldo Scardapane Le ossa sono una delle
DIAGNOSTICA PER IMMAGINI CASA DI CURA PRIVATA SANATRIX
 DIAGNOSTICA PER IMMAGINI CASA DI CURA PRIVATA SANATRIX DIAGNOSTICA PER IMMAGINI Il servizio di Diagnostica per Immagini di Clinica Sanatrix si avvale di apparecchiature che, utilizzando varie forme di
DIAGNOSTICA PER IMMAGINI CASA DI CURA PRIVATA SANATRIX DIAGNOSTICA PER IMMAGINI Il servizio di Diagnostica per Immagini di Clinica Sanatrix si avvale di apparecchiature che, utilizzando varie forme di
DATAZIONI PER PER LUMINESCENZA
 Stima della dose annua: La dose annua è dovuta alle particelle alfa, beta, ai raggi gamma e ai raggi cosmici. Mentre il contributo delle particelle alfa è interamente dovuto ai radionuclidi delle serie
Stima della dose annua: La dose annua è dovuta alle particelle alfa, beta, ai raggi gamma e ai raggi cosmici. Mentre il contributo delle particelle alfa è interamente dovuto ai radionuclidi delle serie
Laboratorio di Fisica Biomedica
 Laboratorio di Fisica Biomedica Fasci di raggi X Argomenti trattati Tecniche di rivelazione dei raggi X Qualita dell immagine radiografica Radiografia con fasci quasi monocromatici Radiografia con mezzi
Laboratorio di Fisica Biomedica Fasci di raggi X Argomenti trattati Tecniche di rivelazione dei raggi X Qualita dell immagine radiografica Radiografia con fasci quasi monocromatici Radiografia con mezzi
PATOLOGIE DELL AORTA
 PATOLOGIE DELL AORTA LE ISCHEMIE MESENTERICHE EMBOLIA: Occlusione acuta soprattutto in pazienti cardiopatici con disturbi del ritmo o alterazioni valvolari reumatiche. L'EMBOLO si arresta dove il calibro
PATOLOGIE DELL AORTA LE ISCHEMIE MESENTERICHE EMBOLIA: Occlusione acuta soprattutto in pazienti cardiopatici con disturbi del ritmo o alterazioni valvolari reumatiche. L'EMBOLO si arresta dove il calibro
Domande relative alla specializzazione in: Medicina nucleare
 Domande relative alla specializzazione in: Medicina nucleare Domanda #1 (codice domanda: n.961) : Quale tra queste condizioni è controindicazione assoluta al trattamento radiometabolico del dolore da metastasi
Domande relative alla specializzazione in: Medicina nucleare Domanda #1 (codice domanda: n.961) : Quale tra queste condizioni è controindicazione assoluta al trattamento radiometabolico del dolore da metastasi
Cenni di fisica moderna
 Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
SPETTROMETRIA GAMMA SPETTROMETRIA GAMMA
 La spettrometria gamma è un metodo di analisi che consente la determinazione qualitativa e quantitativa dei radionuclidi gamma-emettitori presenti in un campione di interesse. Il successo di questo metodo
La spettrometria gamma è un metodo di analisi che consente la determinazione qualitativa e quantitativa dei radionuclidi gamma-emettitori presenti in un campione di interesse. Il successo di questo metodo
Linee guida per il planning nel carcinoma del polmone. Radiotherapy and Oncology 71 (2004)
 Linee guida per il planning nel carcinoma del polmone Radiotherapy and Oncology 71 (2004) 139-146 Linee guida per il planning nel carcinoma del polmone Posizionamento del paziente Acquisizione delle immagini
Linee guida per il planning nel carcinoma del polmone Radiotherapy and Oncology 71 (2004) 139-146 Linee guida per il planning nel carcinoma del polmone Posizionamento del paziente Acquisizione delle immagini
UNIVERSITÁ DEGLI STUDI DI PADOVA
 Fisica Sanitaria Interazione di raggi X con la materia (diffusione, effetto compton, fotoelettrico, produzione di coppie, fotodisintegrazione). Spessore emivalente, decivalente. Interazione delle particelle
Fisica Sanitaria Interazione di raggi X con la materia (diffusione, effetto compton, fotoelettrico, produzione di coppie, fotodisintegrazione). Spessore emivalente, decivalente. Interazione delle particelle
Radiologia Interventistica Oncologica Informazioni per il Paziente
 Radiologia Interventistica Oncologica Informazioni per il Paziente Radiologia Interventistica: l alternativa alla chirurgia www.cirse.org Cardiovascular and Interventional Radiological Society of Europe
Radiologia Interventistica Oncologica Informazioni per il Paziente Radiologia Interventistica: l alternativa alla chirurgia www.cirse.org Cardiovascular and Interventional Radiological Society of Europe
Interpretativa Generale Non previsto INTRODUZIONE ALLA DIAGNOSTICA PER IMMAGINI
 INTRODUZIONE ALLA DIAGNOSTICA PER IMMAGINI Indirizza lo studente alla conoscenza delle varie macchine impiegate nella diagnostica per immagini (radiologia convenzionale, ultrasonografia, tomografia computerizzata,
INTRODUZIONE ALLA DIAGNOSTICA PER IMMAGINI Indirizza lo studente alla conoscenza delle varie macchine impiegate nella diagnostica per immagini (radiologia convenzionale, ultrasonografia, tomografia computerizzata,
L imaging morfologico. Maja Ukmar. U.C.O di Radiologia Azienda Ospedaliero-Universitaria Ospedali Riuniti Trieste
 LA DIAGNOSTICA PER IMMAGINI NEL TREATMENT PLANNING DELLA RADIOTERAPIA L imaging morfologico Maja Ukmar U.C.O di Radiologia Azienda Ospedaliero-Universitaria Ospedali Riuniti Trieste Radiogramma diretto
LA DIAGNOSTICA PER IMMAGINI NEL TREATMENT PLANNING DELLA RADIOTERAPIA L imaging morfologico Maja Ukmar U.C.O di Radiologia Azienda Ospedaliero-Universitaria Ospedali Riuniti Trieste Radiogramma diretto
Giornate Epato-Gastroenterologiche Cuneesi Vicoforte 19 febbraio 2010 Marco Tabone Gastroenterologia A.O. Mauriziano
 Terapia radiointerstiziale nell epatocarcinoma avanzato Giornate Epato-Gastroenterologiche Cuneesi Vicoforte 19 febbraio 2010 Marco Tabone Gastroenterologia A.O. Mauriziano Premessa HCC è sensibile alle
Terapia radiointerstiziale nell epatocarcinoma avanzato Giornate Epato-Gastroenterologiche Cuneesi Vicoforte 19 febbraio 2010 Marco Tabone Gastroenterologia A.O. Mauriziano Premessa HCC è sensibile alle
Università degli Studi di Torino Facoltà di Medicina e Chirurgia
 Università degli Studi di Torino Facoltà di Medicina e Chirurgia RUOLO DELLA RISONANZA MAGNETICA DI PERFUSIONE E DI DIFFUSIONE NELLA VALUTAZIONE PRECOCE DELLA RISPOSTA AL TRATTAMENTO RADIOCHIRURGICO DELLE
Università degli Studi di Torino Facoltà di Medicina e Chirurgia RUOLO DELLA RISONANZA MAGNETICA DI PERFUSIONE E DI DIFFUSIONE NELLA VALUTAZIONE PRECOCE DELLA RISPOSTA AL TRATTAMENTO RADIOCHIRURGICO DELLE
ECOGRAFIA CLINICA UNA DIAGNOSTICA SOSTENIBILE DANIELA CATALANO
 ECOGRAFIA CLINICA UNA DIAGNOSTICA SOSTENIBILE DANIELA CATALANO Università di Catania Dipartimento di Medicina Clinica e Sperimentale PRECISION MEDICINE PER UNA ONCOLOGIA SOSTENIBILE DALLA DIAGNOSTICA ALLA
ECOGRAFIA CLINICA UNA DIAGNOSTICA SOSTENIBILE DANIELA CATALANO Università di Catania Dipartimento di Medicina Clinica e Sperimentale PRECISION MEDICINE PER UNA ONCOLOGIA SOSTENIBILE DALLA DIAGNOSTICA ALLA
VALUTAZIONE PER IMMAGINI
 VALUTAZIONE PER IMMAGINI PERIN B., L. DAVI DIPARTIMENTO IMMAGINI Imaging aneurismi Angio-TC Angiografia Ecografia Angio-RM AORTA ADDOMINALE: PATOLOGIA ANEURISMATICA Contributo ecografia Eco (color-doppler)
VALUTAZIONE PER IMMAGINI PERIN B., L. DAVI DIPARTIMENTO IMMAGINI Imaging aneurismi Angio-TC Angiografia Ecografia Angio-RM AORTA ADDOMINALE: PATOLOGIA ANEURISMATICA Contributo ecografia Eco (color-doppler)
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
Ruolo del Fisico Medico in Italia
 Ruolo del Fisico Medico in Italia Povo, Facoltà di Scienze, 23 maggio 2012 Relatore: Lamberto Widesott Fisico Medico U.O. Protonterapia di Trento Portavoce Associazione Italiana di Fisica Medica (AIFM)
Ruolo del Fisico Medico in Italia Povo, Facoltà di Scienze, 23 maggio 2012 Relatore: Lamberto Widesott Fisico Medico U.O. Protonterapia di Trento Portavoce Associazione Italiana di Fisica Medica (AIFM)
Una rivoluzione nella diagnosi e nel trattamento del cancro: la PET
 Una rivoluzione nella diagnosi e nel trattamento del cancro: la PET Introdotta circa tre decadi fa da Phelps e Hoffman la Tomografia ad Emissione di Positroni (PET) solo recentemente è divenuta lo strumento
Una rivoluzione nella diagnosi e nel trattamento del cancro: la PET Introdotta circa tre decadi fa da Phelps e Hoffman la Tomografia ad Emissione di Positroni (PET) solo recentemente è divenuta lo strumento
Medicina Nucleare sistematica: Infettivologia Nucleare
 UNIVERSITÀ DEGLI STUDI DI FERRARA Corso di Laurea Magistrale in Medicina e Chirurgia Corso Integrato di Diagnostica per Immagini e Radioprotezione (A.A. 2015-16) Diagnostica per Immagini e Radioterapia
UNIVERSITÀ DEGLI STUDI DI FERRARA Corso di Laurea Magistrale in Medicina e Chirurgia Corso Integrato di Diagnostica per Immagini e Radioprotezione (A.A. 2015-16) Diagnostica per Immagini e Radioterapia
PROTOCOLLO SPERIMENTALE DI IMPIEGO CLINICO MN3
 PROTOCOLLO SPERIMENTALE DI IMPIEGO CLINICO MN3 DIAGNOSTICA CON ANALOGHI DELLA SOMATOSTATINA MARCATI CON 68 Ga DI TUMORI CON PROBABILE ESPRESSIONE DI RECETTORI SSTR2 e/o 5, DA INDIRIZZARE AL TRATTAMENTO
PROTOCOLLO SPERIMENTALE DI IMPIEGO CLINICO MN3 DIAGNOSTICA CON ANALOGHI DELLA SOMATOSTATINA MARCATI CON 68 Ga DI TUMORI CON PROBABILE ESPRESSIONE DI RECETTORI SSTR2 e/o 5, DA INDIRIZZARE AL TRATTAMENTO
LA SCINTIGRAFIA CEREBRALE
 LA SCINTIGRAFIA CEREBRALE Sergio Baldari, Alfredo Campennì Medicina Nucleare Dipartimento di Scienze Radiologiche Università degli Studi di Messina - A.O.U. Policlinico G. Martino Donazione di organi e
LA SCINTIGRAFIA CEREBRALE Sergio Baldari, Alfredo Campennì Medicina Nucleare Dipartimento di Scienze Radiologiche Università degli Studi di Messina - A.O.U. Policlinico G. Martino Donazione di organi e
Ampolla di Vater. (Non sono inclusi i tumori carcinoidi ed altri tumori neuroendocrini) RIASSUNTO DELLE MODIFICHE
 Ampolla di Vater (Non sono inclusi i tumori carcinoidi ed altri tumori neuroendocrini) C24.1 Ampolla di Vater RIASSUNTO DELLE MODIFICHE Èstata eliminata la distinzione fra T3 e T4 sulla base della profondità
Ampolla di Vater (Non sono inclusi i tumori carcinoidi ed altri tumori neuroendocrini) C24.1 Ampolla di Vater RIASSUNTO DELLE MODIFICHE Èstata eliminata la distinzione fra T3 e T4 sulla base della profondità
LA PRODUZIONE DEI RAGGI X
 UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali. Meccanismo di azione e interazioni farmacologiche
 A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it [email protected]
A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it [email protected]
VALUTAZIONE DI UN SISTEMA AUTOMATIZZATO CLIA PER LA DETERMINAZIONE DEL L ANTIGENE CARBOIDRATICO 19-9
 VALUTAZIONE DI UN SISTEMA AUTOMATIZZATO CLIA PER LA DETERMINAZIONE DEL L ANTIGENE CARBOIDRATICO 19-9 Chantal Di Segni, Giuseppina Gennarini, Serena Rita Zarrillo, Emanuela Anastasi, Antonio Angeloni Dipartimento
VALUTAZIONE DI UN SISTEMA AUTOMATIZZATO CLIA PER LA DETERMINAZIONE DEL L ANTIGENE CARBOIDRATICO 19-9 Chantal Di Segni, Giuseppina Gennarini, Serena Rita Zarrillo, Emanuela Anastasi, Antonio Angeloni Dipartimento
CIED e Radioterapia. Mara Severgnini, Fisica Medica A.O.U. Ospedali Riuniti di Trieste
 CIED e Radioterapia Mara Severgnini, Fisica Medica A.O.U. Ospedali Riuniti di Trieste Dispositivi Cardiaci Impiantabili e radioterapia Pacemaker Defibrillatori Le radiazioni provocano danni: distruzione
CIED e Radioterapia Mara Severgnini, Fisica Medica A.O.U. Ospedali Riuniti di Trieste Dispositivi Cardiaci Impiantabili e radioterapia Pacemaker Defibrillatori Le radiazioni provocano danni: distruzione
Dotti biliari extraepatici
 16 Dotti biliari extraepatici (Non sono inclusi i sarcomi ed i tumori carcinoidi) C24.0 Dotti biliari extraepatici C24.8 Lesione sovrapposta dell albero biliare C24.9 Albero biliare, NAS RIASSUNTO DELLE
16 Dotti biliari extraepatici (Non sono inclusi i sarcomi ed i tumori carcinoidi) C24.0 Dotti biliari extraepatici C24.8 Lesione sovrapposta dell albero biliare C24.9 Albero biliare, NAS RIASSUNTO DELLE
CHE COS E LA COLONSCOPIA VIRTUALE
 CHE COS E LA COLONSCOPIA VIRTUALE La colonscopia virtuale (CV) è un esame non invasivo del colon che si esegue attraverso una tomografia assiale computerizzata (TAC) dell addome dopo aver disteso il colon
CHE COS E LA COLONSCOPIA VIRTUALE La colonscopia virtuale (CV) è un esame non invasivo del colon che si esegue attraverso una tomografia assiale computerizzata (TAC) dell addome dopo aver disteso il colon
GINOCCHIO DOLOROSO Semeiotica radiologica normale e patologica.
 GINOCCHIO DOLOROSO Semeiotica radiologica normale e patologica www.fisiokinesiterapia.biz DIAGNOSTICA PER IMMAGINI ECOGRAFIA RX TOMOGRAFIA COMPUTERIZZATA RISONANZA MAGNETICA ECOGRAFIA Cavo popliteo SI
GINOCCHIO DOLOROSO Semeiotica radiologica normale e patologica www.fisiokinesiterapia.biz DIAGNOSTICA PER IMMAGINI ECOGRAFIA RX TOMOGRAFIA COMPUTERIZZATA RISONANZA MAGNETICA ECOGRAFIA Cavo popliteo SI
Seconda Parte Specifica per la tipologia di scuola - Statistica sanitaria e Biometria - 22/07/2016
 Domande relative alla specializzazione in: Statistica sanitaria e Biometria Scenario 1: In uno studio prospettivo condotto per valutare la relazione tra l'uso di estrogeni e rischio di cancro alla mammella,
Domande relative alla specializzazione in: Statistica sanitaria e Biometria Scenario 1: In uno studio prospettivo condotto per valutare la relazione tra l'uso di estrogeni e rischio di cancro alla mammella,
La Scintigrafia Miocardica: cos è e che dati fornisce. Dott. G. Bertuccio S.C. Medicina Nucleare ASLTO5
 La Scintigrafia Miocardica: cos è e che dati fornisce Dott. G. Bertuccio S.C. Medicina Nucleare ASLTO5 Una corretta definizione.. q La Scintigrafia Miocardica è un importante test diagnostico di II livello,
La Scintigrafia Miocardica: cos è e che dati fornisce Dott. G. Bertuccio S.C. Medicina Nucleare ASLTO5 Una corretta definizione.. q La Scintigrafia Miocardica è un importante test diagnostico di II livello,
Decadimento a. E tipico dei radioisotopi con Z > 82 (Pb), nei quali il rapporto tra il numero dei neutroni e quello dei protoni è troppo basso.
 Decadimento a Nel decadimento vengono emesse particelle formate da 2 protoni e 2 neutroni ( = nuclei di 4He) aventi velocità molto elevate (5-7% della velocità della luce) E tipico dei radioisotopi con
Decadimento a Nel decadimento vengono emesse particelle formate da 2 protoni e 2 neutroni ( = nuclei di 4He) aventi velocità molto elevate (5-7% della velocità della luce) E tipico dei radioisotopi con
Informazioni per il PAZIENTE Scintigrafia Totale Corporea e/o polmonare con traccianti positivi cod
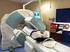 Informazioni per il PAZIENTE Scintigrafia Totale Corporea e/o polmonare con traccianti positivi cod. 92.15.4 Che cosa è la scintigrafia polmonare con traccianti positivi? E un esame che si propone di studiare
Informazioni per il PAZIENTE Scintigrafia Totale Corporea e/o polmonare con traccianti positivi cod. 92.15.4 Che cosa è la scintigrafia polmonare con traccianti positivi? E un esame che si propone di studiare
IL SISTEMA CIRCOLATORIO UMANO
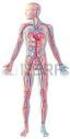 Funzione Vasi sanguigni Aorta Vene cave IL SISTEMA CIRCOLATORIO Arterie polmonari UMANO Vene polmonari Struttura Circolazione Sistematica e polmonare FUNZIONI Distribuzione delle sostanze nutritive dall
Funzione Vasi sanguigni Aorta Vene cave IL SISTEMA CIRCOLATORIO Arterie polmonari UMANO Vene polmonari Struttura Circolazione Sistematica e polmonare FUNZIONI Distribuzione delle sostanze nutritive dall
Sviluppo futuro della ricerca clinica Mario Scartozzi
 HER2Club in gastric cancer Sviluppo futuro della ricerca clinica Mario Scartozzi La ricerca clinica per lo sviluppo di nuove strategie terapeutiche nei pazienti affetti da carcinoma gastrico metastatico
HER2Club in gastric cancer Sviluppo futuro della ricerca clinica Mario Scartozzi La ricerca clinica per lo sviluppo di nuove strategie terapeutiche nei pazienti affetti da carcinoma gastrico metastatico
RASSEGNA STAMPA giovedì 6 giugno 2013
 RASSEGNA STAMPA giovedì 6 giugno 2013 Audipress n.d. Primo Piano 06-GIU-2013 da pag. 6 5 giugno 2013 Fondazione Giovanni Paolo II, primo centro ad utilizzare la Radiochirurgia con tecnica VMAT Non esistono
RASSEGNA STAMPA giovedì 6 giugno 2013 Audipress n.d. Primo Piano 06-GIU-2013 da pag. 6 5 giugno 2013 Fondazione Giovanni Paolo II, primo centro ad utilizzare la Radiochirurgia con tecnica VMAT Non esistono
I rivelatori. Osservare il microcosmo. EEE- Cosmic Box proff.: M.Cottino, P.Porta
 I rivelatori Osservare il microcosmo Cose prima mai viste L occhio umano non riesce a distinguere oggetti con dimensioni inferiori a 0,1 mm (10-4 m). I primi microscopi vennero prodotti in Olanda alla
I rivelatori Osservare il microcosmo Cose prima mai viste L occhio umano non riesce a distinguere oggetti con dimensioni inferiori a 0,1 mm (10-4 m). I primi microscopi vennero prodotti in Olanda alla
UNIVERSITÀ - OSPEDALE di PADOVA MEDICINA NUCLEARE COS' E`?
 UNIVERSITÀ - OSPEDALE di PADOVA MEDICINA NUCLEARE SCINTIGRAFIA OSTEO-ARTICOLARE Franco Bui, Diego Cecchin COS' E`? E' una delle metodiche di imaging medico nucleare più comunemente utilizzate. Sfrutta
UNIVERSITÀ - OSPEDALE di PADOVA MEDICINA NUCLEARE SCINTIGRAFIA OSTEO-ARTICOLARE Franco Bui, Diego Cecchin COS' E`? E' una delle metodiche di imaging medico nucleare più comunemente utilizzate. Sfrutta
I FACOLTA DI MEDICINA E CHIRURGIA CORSO DI LAUREA SPECIALISTICA DELLE PROFESSIONI SANITARIE TECNICHE DIAGNOSTICHE Sede di Latina
 I FACOLTA DI MEDICINA E CHIRURGIA CORSO DI LAUREA SPECIALISTICA DELLE PROFESSIONI SANITARIE TECNICHE DIAGNOSTICHE Sede di Latina Presidente del corso Prof. Esterina Pascale Vice-Presidente Prof. Annarita
I FACOLTA DI MEDICINA E CHIRURGIA CORSO DI LAUREA SPECIALISTICA DELLE PROFESSIONI SANITARIE TECNICHE DIAGNOSTICHE Sede di Latina Presidente del corso Prof. Esterina Pascale Vice-Presidente Prof. Annarita
L unità di misura della dose nel S.I. è il Gray
 LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
IMAGING RADIOLOGICO NEL CARCINOMA GASTRICO LOCALMENTE AVANZATO
 IMAGING RADIOLOGICO NEL CARCINOMA GASTRICO LOCALMENTE AVANZATO Silvia Venturini S.O.C. Radiologia Centro di Riferimento Oncologico Aviano (PN) Fino al 2006 intervento chirurgico unica opzione terapeutica
IMAGING RADIOLOGICO NEL CARCINOMA GASTRICO LOCALMENTE AVANZATO Silvia Venturini S.O.C. Radiologia Centro di Riferimento Oncologico Aviano (PN) Fino al 2006 intervento chirurgico unica opzione terapeutica
ADENOCARCINOMA DEL RETTO
 ADENOCARCINOMA DEL RETTO GASTOENTEROLOGO- PATOLOGO CHIRURGO-RADIOLOGO- PATOLOGO GIOG ONCOLOGO-PATOLOGO- RADIOLOGO RADIOTERAPISTA 1. esame endoscopico richiesto dal Curante e/o per screening programmato.
ADENOCARCINOMA DEL RETTO GASTOENTEROLOGO- PATOLOGO CHIRURGO-RADIOLOGO- PATOLOGO GIOG ONCOLOGO-PATOLOGO- RADIOLOGO RADIOTERAPISTA 1. esame endoscopico richiesto dal Curante e/o per screening programmato.
Training in Trombosi Società Italiana per lo Studio dell Emostasi e della Trombosi. Introduzione. Cremona settembre 2016
 Training in Trombosi Società Italiana per lo Studio dell Emostasi e della Trombosi Cremona 19-23 settembre 2016 Introduzione Anna Falanga Ospedale Papa Giovanni XXIII Bergamo www.siset.org Chi Siamo S
Training in Trombosi Società Italiana per lo Studio dell Emostasi e della Trombosi Cremona 19-23 settembre 2016 Introduzione Anna Falanga Ospedale Papa Giovanni XXIII Bergamo www.siset.org Chi Siamo S
Chirurgia - tumori del fegato e delle vie biliari
 Chirurgia - tumori del fegato e delle vie biliari La chirurgia del fegato e delle vie biliari comprende una notevole varietà di interventi, che vanno dalle più semplici e routinarie colecistectomie, con
Chirurgia - tumori del fegato e delle vie biliari La chirurgia del fegato e delle vie biliari comprende una notevole varietà di interventi, che vanno dalle più semplici e routinarie colecistectomie, con
Numero di nuovi casi con tumore del colon sottoposti a chirurgia
 Codice Interno Definizione Significato Denominatore Carcinoma Colon-Retto CRC obj1 Percentuale di casi con trattamento chirurgico per tumore del colon entro 60 gg dall endoscopia Descrive la proporzione
Codice Interno Definizione Significato Denominatore Carcinoma Colon-Retto CRC obj1 Percentuale di casi con trattamento chirurgico per tumore del colon entro 60 gg dall endoscopia Descrive la proporzione
Unità didattica 10. Decima unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
5. DAP - AREA FISICA. 5.1 Onde Meccaniche Rumore Ultrasuoni. Analisi statistica sul campo (con presenza operatore):
 Versione 2002 - aggiornamento 8 gennaio 2002 20 5. DAP - AREA FISICA 5.1 Onde Meccaniche 5.1.1 Rumore 5.1.01.01 Misura di livello sonoro con fonometro 52,00 5.1.01.02 Determinazione dei tempi di riverbero
Versione 2002 - aggiornamento 8 gennaio 2002 20 5. DAP - AREA FISICA 5.1 Onde Meccaniche 5.1.1 Rumore 5.1.01.01 Misura di livello sonoro con fonometro 52,00 5.1.01.02 Determinazione dei tempi di riverbero
AL POSTO DELLA BIOPSIA EPATICA UN ESAME NON INVASIVO Operativa all Ospedale San Paolo di Savona l Elastometria Epatica mediante FibroScan
 CARTELLA STAMPA Martedì 6 novembre 2007 ore 11,00 Sala riunioni U.O. Medicina Interna e Gastroenterologia V piano retrocorpo Ospedale San Paolo di Savona Direttore Dipartimento Scienze Mediche Dott. Giorgio
CARTELLA STAMPA Martedì 6 novembre 2007 ore 11,00 Sala riunioni U.O. Medicina Interna e Gastroenterologia V piano retrocorpo Ospedale San Paolo di Savona Direttore Dipartimento Scienze Mediche Dott. Giorgio
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna [email protected] Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna [email protected] Si definiscono radiazioni ionizzanti tutte le
Trattamento radioterapico in paziente affetto da carcinoma della giunzione Esofago- gastrica: confronto tra piano VMAT e IMRT step and shoot.
 Trattamento radioterapico in paziente affetto da carcinoma della giunzione Esofago- gastrica: confronto tra piano VMAT e IMRT step and shoot. S. Terrevazzi, C. Gumina, E. Mariani, G. Montanari, A. Podhradska,
Trattamento radioterapico in paziente affetto da carcinoma della giunzione Esofago- gastrica: confronto tra piano VMAT e IMRT step and shoot. S. Terrevazzi, C. Gumina, E. Mariani, G. Montanari, A. Podhradska,
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
Centro di Radioterapia e Medicina Nucleare di Cagliari
 Centro di Radioterapia e Medicina Nucleare di Cagliari Stampato nel mese di giugno 2008 a cura dell Azienda Sanitaria Locale di Cagliari L apertura del nuovo Centro di Radioterapia e Medicina Nucleare
Centro di Radioterapia e Medicina Nucleare di Cagliari Stampato nel mese di giugno 2008 a cura dell Azienda Sanitaria Locale di Cagliari L apertura del nuovo Centro di Radioterapia e Medicina Nucleare
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
Corso di Laurea Magistrale In Scienze Delle Professioni Sanitarie Tecniche-Area Tecnico- Diagnostica
 Corso di Laurea Magistrale In Scienze Delle Professioni Sanitarie Tecniche-Area Tecnico- Diagnostica CORSO INTEGRATO DI SCIENZE PROFESSIONALIZZANTI 1 II ANNO- I Semestre Insegnamenti: Anatomia Patologica
Corso di Laurea Magistrale In Scienze Delle Professioni Sanitarie Tecniche-Area Tecnico- Diagnostica CORSO INTEGRATO DI SCIENZE PROFESSIONALIZZANTI 1 II ANNO- I Semestre Insegnamenti: Anatomia Patologica
Informazioni per il PAZIENTE Scintigrafia linfatica e linfoghiandolare segmentaria nelle lesioni mammarie (ricerca del linfonodo sentinella ) cod.
 Informazioni per il PAZIENTE Scintigrafia linfatica e linfoghiandolare segmentaria nelle lesioni mammarie (ricerca del linfonodo sentinella ) cod. 92.16.1 Che cosa è la scintigrafia linfatica e linfoghiandolare
Informazioni per il PAZIENTE Scintigrafia linfatica e linfoghiandolare segmentaria nelle lesioni mammarie (ricerca del linfonodo sentinella ) cod. 92.16.1 Che cosa è la scintigrafia linfatica e linfoghiandolare
LA VALUTAZIONE DEL RISCHIO SANITARIO. Stefano De Crescenzo A.S.S.T. Niguarda - D.G. Welfare Regione Lombardia
 LA VALUTAZIONE DEL RISCHIO SANITARIO Stefano De Crescenzo A.S.S.T. Niguarda - D.G. Welfare Regione Lombardia Obiettivi intervento fornire: alcune semplici indicazioni sugli effetti delle basse dosi alcuni
LA VALUTAZIONE DEL RISCHIO SANITARIO Stefano De Crescenzo A.S.S.T. Niguarda - D.G. Welfare Regione Lombardia Obiettivi intervento fornire: alcune semplici indicazioni sugli effetti delle basse dosi alcuni
Sistemi di Elaborazione delle Informazioni
 Intro Sistemi di Elaborazione delle Informazioni prof. Salvatore Siracusa [email protected] ww2.unime.it/sei La storia delle immagini biomediche, iniziata poco più di cento anni fa con la scoperta dei
Intro Sistemi di Elaborazione delle Informazioni prof. Salvatore Siracusa [email protected] ww2.unime.it/sei La storia delle immagini biomediche, iniziata poco più di cento anni fa con la scoperta dei
PUCCIO A.M. PUCE R. OLTREMARINI G. REBECCHI I. GIORDANO G. ISTITUTO PALAZZOLO FONDAZIONE DON GNOCCHI-MILANO PREMESSA:
 PUCCIO A.M. PUCE R. OLTREMARINI G. REBECCHI I. GIORDANO G. ISTITUTO PALAZZOLO FONDAZIONE DON GNOCCHI-MILANO PREMESSA: Le correnti elettriche, i campi elettrici ed elettromagnetici sono forme di energia
PUCCIO A.M. PUCE R. OLTREMARINI G. REBECCHI I. GIORDANO G. ISTITUTO PALAZZOLO FONDAZIONE DON GNOCCHI-MILANO PREMESSA: Le correnti elettriche, i campi elettrici ed elettromagnetici sono forme di energia
Torace Standard Studio del parenchima e del mediastino
 Torace Standard Stuo del parenchima e del meastino Posizione del paziente Intervallo Direzione Fov acquisizione Tempo rotazione Configurazione dei detettori PARAMETRI DI ACQUISIZIONE Supino Torace intero
Torace Standard Stuo del parenchima e del meastino Posizione del paziente Intervallo Direzione Fov acquisizione Tempo rotazione Configurazione dei detettori PARAMETRI DI ACQUISIZIONE Supino Torace intero
RICERCA E SVILUPPO DI NUOVI FARMACI
 RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
Magnete in caduta in un tubo metallico
 Magnete in caduta in un tubo metallico Progetto Lauree Scientifiche 2009 Laboratorio di Fisica Dipartimento di Fisica Università di Genova in collaborazione con il Liceo Leonardo da Vinci Genova - 25 novembre
Magnete in caduta in un tubo metallico Progetto Lauree Scientifiche 2009 Laboratorio di Fisica Dipartimento di Fisica Università di Genova in collaborazione con il Liceo Leonardo da Vinci Genova - 25 novembre
LA TOMOGRAFIA COMPUTERIZZATA.
 LA TOMOGRAFIA COMPUTERIZZATA PRINCIPI GENERALI DELLA TC La TC è un procedimento radiografico digitalizzato che permette di rappresentare sezioni assiali di spessore finito del corpo umano tramite immagini
LA TOMOGRAFIA COMPUTERIZZATA PRINCIPI GENERALI DELLA TC La TC è un procedimento radiografico digitalizzato che permette di rappresentare sezioni assiali di spessore finito del corpo umano tramite immagini
CATETERISMO CARDIACO, CORONAROGRAFIA, ANGIOGRAFIA PERIFERICA CONSENSO INFORMATO CARDIOLOGIA INTERVENTISTICA PER EMODINAMICA E
 Dipartimento Cardio-Toraco-Vascolare e Area Critica Cardiologia Interventistica Dott. Antonio Manari - Direttore CONSENSO INFORMATO PER EMODINAMICA E CARDIOLOGIA INTERVENTISTICA CATETERISMO CARDIACO, CORONAROGRAFIA,
Dipartimento Cardio-Toraco-Vascolare e Area Critica Cardiologia Interventistica Dott. Antonio Manari - Direttore CONSENSO INFORMATO PER EMODINAMICA E CARDIOLOGIA INTERVENTISTICA CATETERISMO CARDIACO, CORONAROGRAFIA,
GUIDA ALL UTENTE ESTERNO UO MEDICINA NUCLEARE PO SARONNO
 Pagina 1 di 5 INDICE 1. Presentazione della UO pag.2 1.1 Orari, ubicazione e struttura pag.2 1.2 Attività pag.3 2. Caratteristica del servizio pag.3 2.1 Modalità di accesso alla prestazione pag.3 2.2 Turni
Pagina 1 di 5 INDICE 1. Presentazione della UO pag.2 1.1 Orari, ubicazione e struttura pag.2 1.2 Attività pag.3 2. Caratteristica del servizio pag.3 2.1 Modalità di accesso alla prestazione pag.3 2.2 Turni
Campobasso. Dalla Fondazione Giovanni Paolo II trattamenti radioterapici avanzati per i tumori del testa-collo
 Campobasso. Dalla Fondazione Giovanni Paolo II trattamenti radioterapici avanzati per i tumori del testa-collo Il lavoro scientifico che riporta la fattibilità di questa complessa strategia è stato pubblicato
Campobasso. Dalla Fondazione Giovanni Paolo II trattamenti radioterapici avanzati per i tumori del testa-collo Il lavoro scientifico che riporta la fattibilità di questa complessa strategia è stato pubblicato
esecuzione e di basso costo, rileva alterazioni parenchimali, interstiziali, pleuriche, dei linfatici, del circolo polmonare, del cuore e delle
 Studio radiografico del torace L indagine radiografica standard del torace, di semplice esecuzione e di basso costo, rileva alterazioni parenchimali, interstiziali, pleuriche, dei linfatici, del circolo
Studio radiografico del torace L indagine radiografica standard del torace, di semplice esecuzione e di basso costo, rileva alterazioni parenchimali, interstiziali, pleuriche, dei linfatici, del circolo
DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE
 DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE Istruzioni per la compilazione Per la corretta esecuzione della manovra e per
DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE Istruzioni per la compilazione Per la corretta esecuzione della manovra e per
MISURA DELLA MASSA DELL ELETTRONE
 MISURA DELLA MASSA DELL ELETTRONE di Arianna Carbone, Giorgia Fortuna, Nicolò Spagnolo Liceo Scientifico Farnesina Roma Interazioni tra elettroni e fotoni Per misurare la massa dell elettrone abbiamo sfruttato
MISURA DELLA MASSA DELL ELETTRONE di Arianna Carbone, Giorgia Fortuna, Nicolò Spagnolo Liceo Scientifico Farnesina Roma Interazioni tra elettroni e fotoni Per misurare la massa dell elettrone abbiamo sfruttato
MAMMELLE. Protocollo d esame RM
 MAMMELLE Protocollo d esame RM Queste diapositive fanno parte di un corso completo e sono a cura dello staff di rm-online.it E vietata la riproduzione anche parziale Cenni Anatomici Questionario tipico
MAMMELLE Protocollo d esame RM Queste diapositive fanno parte di un corso completo e sono a cura dello staff di rm-online.it E vietata la riproduzione anche parziale Cenni Anatomici Questionario tipico
Regolamento Didattico. Scuola di Specializzazione in Chirurgia toracica
 Regolamento Didattico Scuola di Specializzazione in Chirurgia toracica Piano degli studi I anno S.S.D. CFU Materie di base, inglese scientifico e ricerca BIO/16, MED/08, BIO/09, MED/07, BIO/14, MED/15,
Regolamento Didattico Scuola di Specializzazione in Chirurgia toracica Piano degli studi I anno S.S.D. CFU Materie di base, inglese scientifico e ricerca BIO/16, MED/08, BIO/09, MED/07, BIO/14, MED/15,
Relazione sull attività scientifica svolta nel quadrimestre 1 giugno-30 settembre 2007 dalla Dott.ssa Ilaria Zanotti
 Relazione sull attività scientifica svolta nel quadrimestre 1 giugno-3 settembre 27 dalla Dott.ssa Ilaria Zanotti Il lavoro scientifico svolto nel corso del quadrimestre di assegnazione della borsa di
Relazione sull attività scientifica svolta nel quadrimestre 1 giugno-3 settembre 27 dalla Dott.ssa Ilaria Zanotti Il lavoro scientifico svolto nel corso del quadrimestre di assegnazione della borsa di
ESAME PET :CARATTERISTICHE TECNICO PRATICHE
 ESAME PET :CARATTERISTICHE TECNICO PRATICHE CTSRM PATRIZIA SANGALLI REGGIO EMILIA 27 Novembre 2004 11 Dicembre 2004 TSRM SIMONA COLA TSRM GIUSEPPE BIGI La Tomografia ad Emissione di Positroni (PET) è una
ESAME PET :CARATTERISTICHE TECNICO PRATICHE CTSRM PATRIZIA SANGALLI REGGIO EMILIA 27 Novembre 2004 11 Dicembre 2004 TSRM SIMONA COLA TSRM GIUSEPPE BIGI La Tomografia ad Emissione di Positroni (PET) è una
Imaging perioperatorio e chirurgia radioguidata di recidiva locoregionale di carcinoma differenziato della tiroide (G. Manca) Caso Clinico 2
 Imaging perioperatorio e chirurgia radioguidata di recidiva locoregionale di carcinoma differenziato della tiroide (G. Manca) Caso Clinico 2 Paziente di sesso femminile, 28 anni Agosto 2008: riscontro
Imaging perioperatorio e chirurgia radioguidata di recidiva locoregionale di carcinoma differenziato della tiroide (G. Manca) Caso Clinico 2 Paziente di sesso femminile, 28 anni Agosto 2008: riscontro
Neoplasia del Pancreas: Ruolo dell EUS
 Neoplasia del Pancreas: Ruolo dell EUS Fabia Attili MD, PhD Digestive Endoscopy Unit Cancro del pancreas I numeri: 10^ più comune neoplasia 4^ causa di mortalità per cancro American Cancer Society 2006:
Neoplasia del Pancreas: Ruolo dell EUS Fabia Attili MD, PhD Digestive Endoscopy Unit Cancro del pancreas I numeri: 10^ più comune neoplasia 4^ causa di mortalità per cancro American Cancer Society 2006:
La Diagnostica per Immagini nella Patologia Tumorale del Colon
 Giornate Mediche Fiorentine Firenze 2/3/4 dicembre 2016 La Diagnostica per Immagini nella Patologia Tumorale del Colon Andrea Stiatti e Alessandro Bartolozzi Diagnostica per Immagini nella patologia tumorale
Giornate Mediche Fiorentine Firenze 2/3/4 dicembre 2016 La Diagnostica per Immagini nella Patologia Tumorale del Colon Andrea Stiatti e Alessandro Bartolozzi Diagnostica per Immagini nella patologia tumorale
