ALOGENURI ALCHILICI. Composti organici che presentano uno o più atomi di alogeno legati ad uno o più atomi di carbonio tetraedrico.
|
|
|
- Uberto Mantovani
- 5 anni fa
- Visualizzazioni
Transcript
1 ALOGENUI ALILII omposti organici che presentano uno o più atomi di alogeno legati ad uno o più atomi di carbonio tetraedrico. NomenclaturaIUPA : Alogeno =Sostituente 2 cloro 2 metil propano trans 1 bromo 3 cloro cicloesano Esempi: Br l l l 3 AATTEISTIE Scarsa presenza in natura non solubili in acqua in genere sono più pesanti dell acqua composti polari (interazione dipolo-dipolo) scarsamente biodegradabili l 2 F 2 Freon 12 l l DDT appresentazione strutturale : geometria tetraedrica l l Effetti conformazionali a a a a a b l b l a anti gauche
2 IN VETINA Gli alogenuri alchilici e lo strato di ozono. I propellenti volatili utilizzati negli spray sono un gruppo di alogenuri alchilici detti freon. Vantaggi: non infiammabilità, chimicamente inerti, non tossici, non lasciano residuo. Svantaggi: raggiungono l atmosfera. l 2 F 2 hλ lf 2 + l l +O 3 O 2 + lo Lo strato di Ozono fa da filtro per le radiazioni ultraviolette più energetiche, proteggendo la vita sulla terra. Oggi i lorofluoro carburi (F) sono banditi.
3 STUTTUA e EATTIVITA regione nucleofila δ+ δ regione elettrofila SOSTITUZIONE NULEOFILA - ' = alchile x = l, Br, I.. O - N - S - O N + - eattività rescente per l < Br < I ELIMINAZIONE '' ''' ' base '' ''' ' + β eliminazione o 1, 2 eliminazione
4 SOSTITUZIONE : Fatti Sperimentali acetone Br + NaI I + NaBr velocità : = 3 -> > ( 3 ) 2 - >( 3 ) ,01 velocità = k 2 [ 2 5 Br ]. [ NaI ] reazione del 1 ordine in ciascun reagente ; del 2 ordine globale k 2 rappresenta l E att e l Orientazione ( fattore entropico) Una Spiegazione plausibile : Più bassa elettro negatività dei radicali alchilici rispetto al Maggiore ingombro sterico acetone acquoso Br + 2 O O + Br velocità : ( 3 ) 3 - >> ( 3 ) 2 - > velocità = k 1 [ ( 3 ) 3 Br ] reazione del 1 ordine globale STUDI sulla VELOITA di EZIONE hanno evidenziato, per i due tipi di reazioni due percorsi, ovvero, DUE MEANISMI DIVESI : SN2 (sostituzione nucleofila bimolecolare) SN1 (sostituzione nucleofila monomolecolare)
5 Il meccanismo SN 2 Ener. * La formazione e la rottura dei legami avviene simultaneamente: reazione ad un unico stadio, uno solo stato di transizione E att. Stato di Transizione: il punto di massima energia che il sistema raggiunge per arrivare ai prodotti. I I Br oppure Br onfigurazione dello stato di transizione: INVESIONE O ITENZIONE? Br I cis I - trans 3 3 Br I trans I - cis 3 3 La velocità diminuisce all aumentare dell ingombro sterico.
6 NULEOFILIITA La velocità della reazione SN2 è fortemente dipendente dal nucleofilo usato: MeO 3 J + Nu - 3 -Nu + J - 3 OO - l - Br - 3 O - SN - N - J - S Differenti Nucleofili, a parità di atomo attaccante, seguono: la Base di Bronsted più Forte è anche il Nucleofilo più forte. Nucleofili che appartengono allo stesso Gruppo (l, Br, J oppure O, S) seguono: la Polarizzabilità aumenta scendendo (atomi più grandi sono più polarizzabili). EFFETTO SOLVENTE L effetto generalmente è scarso per i solventi APOLAI (i più usati). I solventi polari protici con nucleofili Anionici, stabilizzandoli, diminuiscono la velocità. GUPPO USENTE J > Br > l perchè segue l energia di legame l > Br > J ma anche la stabilità dell anione : J - > Br - > l - Il migliore gruppo uscente risulta essere la base coniugata dell acido di Bronsted più forte.
7 Il meccanismo SN 1 Si può postulare un meccanismo alternativo a due stadi : Formazione del legame antecedente la rottura inverosimile ottura del legame che precede la rottura verosimile 1 stadio: rottura eterolitica + 2 stadio: formazione del legame fra il nucleofilo e il arbocatione + Nu - Nu Il 1 stadio risulta essere fortemente ENDOTEMIO: = Kcal/ mol ( separazione di cariche di segno opposto). Forte effetto del SOLVENTE ostante dielettrica ε (capacità di tenere separate le cariche) 2 O 3 O 3 SO 3 OO ON( 3 ) Solvatazione O O O O O O Ad Es. la ionizzazione del 3 J in 2 O mostra un = + 63 Kcal/mol. Quindi abbiamo un effetto stabilizzante di 164 Kcal/mol.
8 Energia E 2 * E 1 * Nu oordinata d i eazione 1 stadio fortemente endotermico; 2 stadio fortemente esotermico Stereochimica della SN 1 Il ABOATIONE INTEMEDIO ha geometria trigonale planare. Quindi subisce l attacco del nucleofilo da entrambe le facce dando origine a ISOMEI al 50 % (AEMIZZAZIONE se si parte da un alogenuro otticamente attivo). Nu Nu Nu 3 3 Ionizzazione (lenta) veloce 3 3
9 Stabilità dei ABOATIONI 3º > 2º > 1º > super 1º Effetto Induttivo : diseguale condivisione degli e - di legame fra atomi di diversa elettronegatività L è più elettronegativo del Il arbonio del arbocatione ibridato SP2 è più elettronegativo del carbonio SP3 del radicale avendo maggior carattere S Postulato di ammond Lo stato di transizione di una reazione fortemente endotermica rifletterà la situazione energetica e strutturale dei prodotti in grado maggiore che non dei reagenti. Questo comporta che ogni sostituente che tende a stabilizzare il prodotto di questa reazione stabilizzerà anche lo stato di transizione che porta ad esso. Viceversa per le reazioni fortemente esotermiche. Attraverso questo postulato possiamo spiegare la competizione tra i due percorsi ( SN2 e SN1) per un alogenuro 1, 2, 3 : il 3 - J avrebbe uno stato di transizione troppo elevato con la SN1, essendo un carbocatione molto instabile, mentre ha uno stato di transizione più basso nella SN2. Il Postulato di ammond lo dobbiamo avere presente in TUTTI i meccanismi di reazione che vedremo.
10 iarrangiamenti molecolari 3 3 O, 2 O Br 3 2 O O normale riarrangiato + 1º º 3 Quando per trasposizione si può ottenere un arbocatione più stabile, si possono osservare prodotti di riarrangiamento. Effetto Solvente : Notevole (stabilizzazione o destabilizzazione dell intermedio carbocationico) Gruppo Uscente : J > Br > l - come nella SN2 Nucleofilicità : essendo il arbocatione molto energetico reagisce con qualsiasi Nucleofilo presente, indipendentemente dalla diversa nucleofilicità.
11 EAZIONI di ELIMINAZIONE '' ''' ' base '' ''' ' + β eliminazione o 1, 2 eliminazione Fatti sperimentali: la facilità di questa reazione varia con la struttura dell alogenuro della Base di Bronsted e del Solvente, è sempre in competizione con le reazioni di Sostituzione Br 3 3 Br Br + KO + KO + KO O O O lenta 2 5 O veloce KBr 2 70% 30% 100% 2 100% + KBr egola di SAYTZEFF Quando un alogenuro alchilico può dare più di un alchene predomina l alchene più sostituito Br O KO % 25% 3 Lo stato di transizione riflette la stabilità dell alchene finale (il più sostituito).
12 Il Meccanismo di Eliminazione Bimolecolare E 2 V = k 2 ( ) ( Base ) 3 l 2 5 O KO 3 Alchene più sostituito 3 l 2 5 O KO 3 Alchene meno sostituito onfigurazione dello stato di transizione: Trans oplanare B
13 Il Meccanismo monomolecolare E 1 on solvente fortemente ionizzante e scaldando si osserva : V = k 1 ( ) Br 2 O - DMSO % + Br 3 2 O 3 2 ompetizione tra Sostituzione ed Eliminazione Di fondamentale importanza risulta essere la Basicità secondo Bronsted del Nucleofilo : J - < Br - < l - << F - < 3 OO - < S - < N -- << O - < O - << N 2- < 3 - Basi Molto deboli deboli forti molto forti Variabile SN 2 E 2 J > Br > l J > Br > l Gruppo alchilico 1 > 2 > 3 3 > 2 > 1 Nucleofilo - Aumento della velocità all aumentare della nucleofilia Aumento della velocità all aumentare della basicità
14 omposti Organometallici Legame fra un Atomo di ed un atomo Metallico Tale legame può essere visto O quasi totalmente OVALENTE (ad es. con il Silicio Si ) O quasi totalmente IONIO (ad es. con il Litio Li ) Si ( 3 ) 3 Li eattivi di Grignard : rivestono un ruolo importante nella sintesi organica perché facili da preparare. δ+ δ Mg Etere Etilico anidro δ δ+ Mg I composti Organo metallici sono sorgenti di ABANIONI ovvero di nucleofili al arbonio
È la presenza dell alogeno che conferisce alla molecola la reattività caratteristica
 aratteristica strutturale degli alogenuri ALOGENO È la presenza dell alogeno che conferisce alla molecola la reattività caratteristica + - 2 2 Br elettronegativo, con parziale carica negativa questo NON
aratteristica strutturale degli alogenuri ALOGENO È la presenza dell alogeno che conferisce alla molecola la reattività caratteristica + - 2 2 Br elettronegativo, con parziale carica negativa questo NON
R-X ALOGENURI ALCHILICI. F Cl Br I. Nomenclatura. In genere si indicano con. + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo
 ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
H H. R R δ+ R H. δ Cl
 Alogenuri alchilici: nomenclatura e reattività Nomenclatura: due possibilità a) Per gli alogenuri più semplici: residuo alchilico + nome dell alogeno (Es metilbromuro, etilbromuro). b) Per molecole più
Alogenuri alchilici: nomenclatura e reattività Nomenclatura: due possibilità a) Per gli alogenuri più semplici: residuo alchilico + nome dell alogeno (Es metilbromuro, etilbromuro). b) Per molecole più
Reattività degli alogenuri alchilici
 Reattività degli alogenuri alchilici 1 3 Meccanismo della Reazione di Sostituzione Nucleofila 4 5 Meccanismo unimolecolare: sostituzione nucleofila unimolecolare (SN1) Un alogenuro che reagisca con questo
Reattività degli alogenuri alchilici 1 3 Meccanismo della Reazione di Sostituzione Nucleofila 4 5 Meccanismo unimolecolare: sostituzione nucleofila unimolecolare (SN1) Un alogenuro che reagisca con questo
Alogenuri alchilici. Alogenuri alchilici: funzioni. Varietà di funzione dei composti alogenati. Figura
 Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati Alogenuri alchilici: nomenclatura Alogenuri alchilici o aloalcani Bromo Alogenuri alchilici: struttura
Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati Alogenuri alchilici: nomenclatura Alogenuri alchilici o aloalcani Bromo Alogenuri alchilici: struttura
Reattività degli alogenuri alchilici: Reazioni di sostituzione nucleofila alifatica Reazioni di eliminazione
 Reattività degli alogenuri alchilici: Reazioni di sostituzione nucleofila alifatica Reazioni di eliminazione Queste reazioni hanno rilevanza prevalentemente per la sintesi organica Nucleofilo OH - Alogenuri
Reattività degli alogenuri alchilici: Reazioni di sostituzione nucleofila alifatica Reazioni di eliminazione Queste reazioni hanno rilevanza prevalentemente per la sintesi organica Nucleofilo OH - Alogenuri
Gli Alogenuri Alchilici
 Gli Alogenuri Alchilici l l F Br F F l F F l l 1,2-Dicloroetano (solvente) Aloetano (anestetico) Freon 12 (fluido refrigerante) egole IUPA per la Nomenclatura degli Alogenuri Alchilici 1.Trovare e nominare
Gli Alogenuri Alchilici l l F Br F F l F F l l 1,2-Dicloroetano (solvente) Aloetano (anestetico) Freon 12 (fluido refrigerante) egole IUPA per la Nomenclatura degli Alogenuri Alchilici 1.Trovare e nominare
Capitolo 7 Composti organici alogenati
 himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
Unità didattica 6. Cosa è una sostutizione? Reazioni di Sostituzione degli Alogenuri Alchilici
 Cosa è una sostutizione? Unità didattica 6 Reazioni di Sostituzione degli Alogenuri Alchilici Capitolo 7 e 8 di Brown e Poon L atomo o il gruppo che è sostituito o eliminato in queste reazioni è detto
Cosa è una sostutizione? Unità didattica 6 Reazioni di Sostituzione degli Alogenuri Alchilici Capitolo 7 e 8 di Brown e Poon L atomo o il gruppo che è sostituito o eliminato in queste reazioni è detto
Figura. Alogenuri alchilici
 Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati Alogenuri alchilici: funzioni Alogenuri alchilici: funzioni Alogenuri alchilici: nomenclatura Alogenuri
Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati Alogenuri alchilici: funzioni Alogenuri alchilici: funzioni Alogenuri alchilici: nomenclatura Alogenuri
Alogenuri alchilici. Alogenuri alchilici: funzioni. Varietà di funzione dei composti alogenati. Figura
 Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati 1 Alogenuri alchilici: funzioni Alogenuri alchilici: funzioni 2 Alogenuri alchilici: nomenclatura Alogenuri
Figura Alogenuri alchilici Alogenuri alchilici: funzioni Varietà di funzione dei composti alogenati 1 Alogenuri alchilici: funzioni Alogenuri alchilici: funzioni 2 Alogenuri alchilici: nomenclatura Alogenuri
Le reazioni degli alogenuri alchilici: le sostituzioni nucleofile e le eliminazioni
 Le reazioni degli alogenuri alchilici: le sostituzioni nucleofile e le eliminazioni δ - X δ X = F, l, o I Dato il carattere elettrofilo del carbonio alogeno sostituito, buona parte della chimica degli
Le reazioni degli alogenuri alchilici: le sostituzioni nucleofile e le eliminazioni δ - X δ X = F, l, o I Dato il carattere elettrofilo del carbonio alogeno sostituito, buona parte della chimica degli
S N. Reazioni di Sostituzione Nucleofila. Nucleofilo: Nu: + C X C + Nu + X - Sostituzione Nucleofila:
 Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1
 REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Alogenuri. alchilici. arilici. vinilici. l atomo di alogeno è legato ad un carbonio sp 2. l atomo di alogeno è legato ad un carbonio sp 3
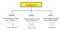 Alogenuri alchilici l atomo di alogeno è legato ad un carbonio sp 3 Br 2-bromo-pentano vinilici l atomo di alogeno è legato ad un carbonio sp 2 Cl cloruro di vinile arilici l atomo di alogeno è legato
Alogenuri alchilici l atomo di alogeno è legato ad un carbonio sp 3 Br 2-bromo-pentano vinilici l atomo di alogeno è legato ad un carbonio sp 2 Cl cloruro di vinile arilici l atomo di alogeno è legato
Stabilità. 1. più sostituito = più stabile. 2. trans più stabile del cis; E più stabile del Z. II. Relazione struttura-reattività R C R R R
 Alcheni 1 II. Relazione struttura-reattività 1. più sostituito = più stabile Stabilità R R R R R > > R R, R 2 2 > R 2 > R R 2 2 2. trans più stabile del cis; E più stabile del Z repulsione trans-2-butene
Alcheni 1 II. Relazione struttura-reattività 1. più sostituito = più stabile Stabilità R R R R R > > R R, R 2 2 > R 2 > R R 2 2 2. trans più stabile del cis; E più stabile del Z repulsione trans-2-butene
La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio.
 La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio. Proteine, zuccheri, lipidi, DNA.. farmaci arta, fibre, plastica s2p2 Z=6 2p 1s 2
La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio. Proteine, zuccheri, lipidi, DNA.. farmaci arta, fibre, plastica s2p2 Z=6 2p 1s 2
Reattività degli alogenuri alchilici
 Reattività degli alogenuri alchilici 1 Sono composti organici che contengono almeno un legame carbonio-alogeno (C X) X (F, Cl, Br, I) Il carbonio è sp3 Possono contenere più legami C X: composti polialogenati.
Reattività degli alogenuri alchilici 1 Sono composti organici che contengono almeno un legame carbonio-alogeno (C X) X (F, Cl, Br, I) Il carbonio è sp3 Possono contenere più legami C X: composti polialogenati.
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
Reazioni di eliminazione
 Reazioni di eliminazione Reazioni di eliminazione Gli alogenuri alchilici oltre ad essere buoni substrati per reazioni di sostituzione nucleofila alifatica sono anche buoni substrati per reazioni di eliminazione.
Reazioni di eliminazione Reazioni di eliminazione Gli alogenuri alchilici oltre ad essere buoni substrati per reazioni di sostituzione nucleofila alifatica sono anche buoni substrati per reazioni di eliminazione.
La barriera rotazionale attorno ad un doppio legame è di 50 Kcal / mol Due polimeri
 omposti organici che presentano uno o più doppi legami carbonio arbonio arattere non polare Molto poco solubili in acqua Densità più bassa dell acqua Grande presenza in natura NomenclaturaIUPA : Si identifica
omposti organici che presentano uno o più doppi legami carbonio arbonio arattere non polare Molto poco solubili in acqua Densità più bassa dell acqua Grande presenza in natura NomenclaturaIUPA : Si identifica
Gli alogenuri alchilici R-X X= Cl, Br, F, I. Alogeno alcani o alogenuri alchilici
 Gli alogenuri alchilici R-X X= Cl, Br, F, I Alogeno alcani o alogenuri alchilici 1 CH 3 CH 2 CH 2 Cl cloropropano /cloruro dipropile CH 3 CH 3 C Cl 2,2-dimetil-1-cloroetano / terbutilcloruro CH 3 Cl 1-clorocicloesano
Gli alogenuri alchilici R-X X= Cl, Br, F, I Alogeno alcani o alogenuri alchilici 1 CH 3 CH 2 CH 2 Cl cloropropano /cloruro dipropile CH 3 CH 3 C Cl 2,2-dimetil-1-cloroetano / terbutilcloruro CH 3 Cl 1-clorocicloesano
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Idrocarburi Alifatici
 Idrocarburi Alifatici Alcano R-C 2 -C 2 -R C n 2n+2 Questo è il massimo rapporto /C per un dato numero di atomi di carbonio. Alchene R-C=C-R C n 2n Ogni doppio legame riduce il numero di atomi di idrogeno
Idrocarburi Alifatici Alcano R-C 2 -C 2 -R C n 2n+2 Questo è il massimo rapporto /C per un dato numero di atomi di carbonio. Alchene R-C=C-R C n 2n Ogni doppio legame riduce il numero di atomi di idrogeno
REAZIONI DEGLI ALCHENI
 REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
Alogenuri Alchilici R-Cl R-Br R-I R-F
 Alogenuri Alchilici R-Cl R-Br R-I I R-FR Alogenoalcani I composti contenenti un atomo di alogeno legato covalentemente ad un atomo di carbonio ibridato sp 3 sono chiamati alogenoalcani o alogenuri alchilici.
Alogenuri Alchilici R-Cl R-Br R-I I R-FR Alogenoalcani I composti contenenti un atomo di alogeno legato covalentemente ad un atomo di carbonio ibridato sp 3 sono chiamati alogenoalcani o alogenuri alchilici.
REATTIVITÀ DI R-XR M + R
 ... X.. M. M. M. M. M 2e- trasferiti dalla superficie metallica in 1 o 2 stadi EATTIVITÀ DI -X... X. -.. Ṙ.. - M + M + δ- δ+ -M nucleofilo -X elettrofilo 1) EAZIONE DI WUTZ -X + - Na + - + Na + X - 2)
... X.. M. M. M. M. M 2e- trasferiti dalla superficie metallica in 1 o 2 stadi EATTIVITÀ DI -X... X. -.. Ṙ.. - M + M + δ- δ+ -M nucleofilo -X elettrofilo 1) EAZIONE DI WUTZ -X + - Na + - + Na + X - 2)
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Reazioni di Eliminazione: E1 e E2 Sintesi di alcheni (olefine) 1 E1 Eliminazione Unimolecolare Processo del tutto analogo alla S N 1 2 Reattività dei carbocationi 1. Sostituzione 2. Eliminazione 3. Addizione
Reazioni di Eliminazione: E1 e E2 Sintesi di alcheni (olefine) 1 E1 Eliminazione Unimolecolare Processo del tutto analogo alla S N 1 2 Reattività dei carbocationi 1. Sostituzione 2. Eliminazione 3. Addizione
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
Alogenuri alchilici R X 1
 Alogenuri alchilici R X 1 1. Alogenuri alchilici Sono composti organici che contengono almeno un legame carbonio-alogeno (C X) X (F, Cl, Br, I) Il carbonio è sp 3 Possono contenere più legami C X: composti
Alogenuri alchilici R X 1 1. Alogenuri alchilici Sono composti organici che contengono almeno un legame carbonio-alogeno (C X) X (F, Cl, Br, I) Il carbonio è sp 3 Possono contenere più legami C X: composti
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Composti organici del silicio
 Composti organici del silicio e B C N O F Ne P S Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 2 3d 0 Il silicio è un elemento della seconda riga della tavole periodica, è più grande, meno elettronegativo e più polarizzabile
Composti organici del silicio e B C N O F Ne P S Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 2 3d 0 Il silicio è un elemento della seconda riga della tavole periodica, è più grande, meno elettronegativo e più polarizzabile
Reazioni degli Alcani
 Reazioni degli Alcani Alogenazione: una reazione di sostituzione: un atomo di H viene sostituito da un atomo di Cl CH + 4 Cl 2 Cl + HCl La reazione di alogenazione degli alcani è una reazione che porta
Reazioni degli Alcani Alogenazione: una reazione di sostituzione: un atomo di H viene sostituito da un atomo di Cl CH + 4 Cl 2 Cl + HCl La reazione di alogenazione degli alcani è una reazione che porta
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Composti AROMATICI. Il Puzzle del Benzene. + Br 2 dà reazione di sostituzione elettrofila C 6. Br + H 2 H 12
 Composti AMATICI Dallo studio degli olii essenziali viene scoperta una nuova classe di composti con un elevato rapporto C /, chiamati AMATICI per il piacevole odore. Il Puzzle del Benzene C 6 6 relativamente
Composti AMATICI Dallo studio degli olii essenziali viene scoperta una nuova classe di composti con un elevato rapporto C /, chiamati AMATICI per il piacevole odore. Il Puzzle del Benzene C 6 6 relativamente
Alchini (C n H 2n-2 ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio doppi.
 himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
REAZIONI E LORO MECCANISMI
 REAZIONI E LORO MECCANISMI Rivisitazione dei concetti di Omolisi, Eterolisi Reagenti Nucleofili e Reagenti Elettrofili Addizione elettrofila Sostituzione nucleofila Eliminazione Reazioni radicaliche Reazioni
REAZIONI E LORO MECCANISMI Rivisitazione dei concetti di Omolisi, Eterolisi Reagenti Nucleofili e Reagenti Elettrofili Addizione elettrofila Sostituzione nucleofila Eliminazione Reazioni radicaliche Reazioni
SOSTITUZIONI NUCLEOFILA SU CARBONI SATURI
 SOSTITUZIONI NUCLEOFILA SU CABONI SATUI Es di cleofili: H 2 O, OH, CO 2 H, e lo loro basi coniugate (OH -, O -, COO - ) H 2 S, SH e basi coniugate; NH 3, NH 2 -, le ammine e i loro derivati CN -, C i carbanioni,
SOSTITUZIONI NUCLEOFILA SU CABONI SATUI Es di cleofili: H 2 O, OH, CO 2 H, e lo loro basi coniugate (OH -, O -, COO - ) H 2 S, SH e basi coniugate; NH 3, NH 2 -, le ammine e i loro derivati CN -, C i carbanioni,
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 SSTITUZINI NUCLEFILE H H H H H + HBr + H H 2 H Br SUBSTRATI alogenuri, eteri, epossidi, esteri solfonici Possibili meccanismi S N 1, S N 2, S N 2, S n i 1 Generalità Gruppo uscente (LG) deve essere una
SSTITUZINI NUCLEFILE H H H H H + HBr + H H 2 H Br SUBSTRATI alogenuri, eteri, epossidi, esteri solfonici Possibili meccanismi S N 1, S N 2, S N 2, S n i 1 Generalità Gruppo uscente (LG) deve essere una
Reazioni degli Alogenuri Alchilici. Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici.
 Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
Complessi alchilici e arilici
 Complessi alchilici e arilici Composti organometallici con legami singoli M-C. E M-C = 125-270 KJ/mole in un generico complesso L x M-CR y (M metallo di transizione) E E-C = 140-360 KJ/mole in un generico
Complessi alchilici e arilici Composti organometallici con legami singoli M-C. E M-C = 125-270 KJ/mole in un generico complesso L x M-CR y (M metallo di transizione) E E-C = 140-360 KJ/mole in un generico
ALCHENI: Reazioni del doppio legame
 ALCENI: REATTIVITÀ ALCENI: Reazioni del doppio legame Reazione di addizione Addizioni ioniche Addizioni con meccanismo concertato ADDIZIONI IONICE ADDIZIONE DI ACIDI ALOGENIDRICI ADDIZIONE DI ACQUA ROTTURA
ALCENI: REATTIVITÀ ALCENI: Reazioni del doppio legame Reazione di addizione Addizioni ioniche Addizioni con meccanismo concertato ADDIZIONI IONICE ADDIZIONE DI ACIDI ALOGENIDRICI ADDIZIONE DI ACQUA ROTTURA
Unità didattica 7 (segue) Reattività del benzene. Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili
 Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Reazioni Stereospecifiche e Stereoselettive
 Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Complementi di Chimica Organica. Composti Aromatici: Benzene C 6 H 6 (1825) (1865) Friedrich August Kekulé
 Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Reazioni Organiche 1
 Reazioni Organiche 1 Scrivere le equazioni per le reazioni organiche Le equazioni delle reazioni organiche sono indicate da una freccia singola ( ) tra materiale di partenza e prodotto a meno che non siano
Reazioni Organiche 1 Scrivere le equazioni per le reazioni organiche Le equazioni delle reazioni organiche sono indicate da una freccia singola ( ) tra materiale di partenza e prodotto a meno che non siano
Reazioni Radicaliche
 Reazioni Radicaliche Preparazione di alogenoalcani: alogenazione di alcani Gli alcani sono composti molto poco reattivi a causa del fatto che gli atomi che li costituiscono formano legami forti e praticamente
Reazioni Radicaliche Preparazione di alogenoalcani: alogenazione di alcani Gli alcani sono composti molto poco reattivi a causa del fatto che gli atomi che li costituiscono formano legami forti e praticamente
Unità didattica 3. Generalità sulle reazioni chimiche organiche. Gli alcheni:
 Generalità sulle reazioni chimiche organiche Unità didattica 3 Generalità sulle reazioni chimiche organiche Gli alcheni: Struttura, nomenclatura, reattività Possiamo catalogare le reazioni chimiche organiche
Generalità sulle reazioni chimiche organiche Unità didattica 3 Generalità sulle reazioni chimiche organiche Gli alcheni: Struttura, nomenclatura, reattività Possiamo catalogare le reazioni chimiche organiche
Sostituzione nucleofila Addizione a gruppi carbonilici Addizione a doppi legami attivati
 himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
PIANO DI STUDIO DELLA DISCIPLINA CHIMICA ORGANICA
 CHIMICA ORGANICA PIANO DELLE 5 CHIMICA, MATERIALI E BIOTECNOLOGIE SETTORE TECNOLOGICO Anno 2018/2019 DA n. 1 L'atomo e le teorie di legame Periodo: Settembre -Ottobre Rappresentare una specie chimica organica
CHIMICA ORGANICA PIANO DELLE 5 CHIMICA, MATERIALI E BIOTECNOLOGIE SETTORE TECNOLOGICO Anno 2018/2019 DA n. 1 L'atomo e le teorie di legame Periodo: Settembre -Ottobre Rappresentare una specie chimica organica
IDROCARBURI INSATURI: GLI ALCHENI HANNO ALMENO UN DOPPIO LEGAME NELLA STRUTTURA NOMENCLATURA: RADICE COME NEGLI IDROCARBURI, DESINENZA -ENE
 IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
Alcheni: : struttura e reattività. Alcheni. Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n. H 2n. Alcheni in biologia
 Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
COMPOSTI AROMATICI POLICICLICI
 CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
Unità didattica 8. Alcoli ed eteri sono gli analoghi organici dell acqua. Alcoli eteri epossidi e composti solforati
 Unità didattica 8 Alcoli eteri epossidi e composti solforati Alcoli ed eteri sono gli analoghi organici dell acqua Un alcol si definisce primario, secondario o terziario a seconda del tipo di carbonio
Unità didattica 8 Alcoli eteri epossidi e composti solforati Alcoli ed eteri sono gli analoghi organici dell acqua Un alcol si definisce primario, secondario o terziario a seconda del tipo di carbonio
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Reazioni di sostituzione nucleofila alifatica
 Reazioni di sostituzione nucleofila alifatica Reazioni di sostituzione nucleofila In queste reazioni un nucleofilo viene sostituito da un altro nucleofilo: Tuttavia, poiché un nucleofilo è anche una base,
Reazioni di sostituzione nucleofila alifatica Reazioni di sostituzione nucleofila In queste reazioni un nucleofilo viene sostituito da un altro nucleofilo: Tuttavia, poiché un nucleofilo è anche una base,
Contenuti della lezione:
 Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Aromaticità. Addizione elettrofila alcheni
 Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Alcoli e Tioli. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Eteri, Epossidi, Solfuri
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Eteri, Epossidi, Solfuri Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Eteri, Epossidi, Solfuri Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
RADICALI: struttura e geometria. Organic Chemistry, 2 ed. David Klein, Wiley
 RADICALI: struttura e geometria Rottura di legame eterolitica Rottura di legame omolitica Due elettroni Un elettrone Organic Chemistry, 2 ed. David Klein, Wiley RADICALI: struttura e geometria Rottura
RADICALI: struttura e geometria Rottura di legame eterolitica Rottura di legame omolitica Due elettroni Un elettrone Organic Chemistry, 2 ed. David Klein, Wiley RADICALI: struttura e geometria Rottura
Cos è la chimica organica
 Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Alcheni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
6. I gruppi funzionali
 6. I gruppi funzionali Si definisce GRUPP FUZIALE (W) un eteroatomo (o un aggruppamento di atomi) che, sostituito ad un idrogeno (o a un legame -) di un alcano, ne modifica la caratteristiche chimicofisiche
6. I gruppi funzionali Si definisce GRUPP FUZIALE (W) un eteroatomo (o un aggruppamento di atomi) che, sostituito ad un idrogeno (o a un legame -) di un alcano, ne modifica la caratteristiche chimicofisiche
Esercitazione n Reazioni degli alogenuri alchilici.
 Esercitazione n. 1 - Reazioni degli alogenuri alchilici. 1. Dare definizione ed un esempio per ciascuno dei seguenti termini: Non sottovalutate questo tipo di esercizio: è importante saper esporre in modo
Esercitazione n. 1 - Reazioni degli alogenuri alchilici. 1. Dare definizione ed un esempio per ciascuno dei seguenti termini: Non sottovalutate questo tipo di esercizio: è importante saper esporre in modo
Cos è la chimica organica
 Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Aldeidi e Chetoni. Proprietà Chimico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami H Bassi pesi molecolari sono solubili in acqua
 Aldeidi e hetoni ' Gruppo carbonilico Aldeide hetone Proprietà himico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami Bassi pesi molecolari sono solubili in acqua Nomenclatura IUPA :
Aldeidi e hetoni ' Gruppo carbonilico Aldeide hetone Proprietà himico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami Bassi pesi molecolari sono solubili in acqua Nomenclatura IUPA :
1. COS È LA CHIMICA ORGANICA?
 Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab.
 I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
N H CH 3 H 3 C. Ammine. Struttura. Classificazione. Nomenclatura. Reattività
 Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
AMMINE. con acidi RNH 2. con O come elettrofilo RNH 2 + H + + R NH 3 NESSUNA REAZIONE. atomo basico, atomo nucleofilo
 AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
Alcheni. Formula: C n H 2n Nome: prefisso+ene. C=C 1.34 Ang 172 kcal/mol Il legame π 63 kcal/mol
 Alcheni Formula: C n 2n Nome: prefisso+ene C=C 1.34 Ang 172 kcal/mol Il legame π 63 kcal/mol ISOMERIA GEOMETRICA NOMENCLATURA Esempio di alchene terminale La catena viene numerata assegnando al carbonio
Alcheni Formula: C n 2n Nome: prefisso+ene C=C 1.34 Ang 172 kcal/mol Il legame π 63 kcal/mol ISOMERIA GEOMETRICA NOMENCLATURA Esempio di alchene terminale La catena viene numerata assegnando al carbonio
7. Reazioni degli alcani
 7. Reazioni degli alcani Gli alcani sono anche detti paraffine da parum affinis (poco reattive). In realtà, una loro reazione (la combustione) è il motore del mondo 7.1. La combustione degli alcani Reazione
7. Reazioni degli alcani Gli alcani sono anche detti paraffine da parum affinis (poco reattive). In realtà, una loro reazione (la combustione) è il motore del mondo 7.1. La combustione degli alcani Reazione
Composti carbonilici
 Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Stabilità del benzene (entalpie di idrogenazione) Energia di risonanza
 La chimica del benzene e dei suoi derivati I derivati del benzene vengono chiamati composti aromatici poiché inizialmente vennero isolati dal catrame nel 1800 ed erano caratterizzati da un odore aromatico.
La chimica del benzene e dei suoi derivati I derivati del benzene vengono chiamati composti aromatici poiché inizialmente vennero isolati dal catrame nel 1800 ed erano caratterizzati da un odore aromatico.
Reattività degli Alcheni. Addizione elettrofila
 Reattività degli Alcheni Addizione elettrofila Reattività degli alcheni Abbiamo visto che il gruppo funzionale che caratterizza un alchene è il doppio legame carbonio-carbonio. Tutti i composti che presentano
Reattività degli Alcheni Addizione elettrofila Reattività degli alcheni Abbiamo visto che il gruppo funzionale che caratterizza un alchene è il doppio legame carbonio-carbonio. Tutti i composti che presentano
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE
 SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Composti Metallorganici
 omposti etallorganici Fe 1952: risoluzione della struttura del Ferrocene (diciclopentadienilferro) 1 monoapto, 2 diapto, 3 triapto, etc.., fino a 8 octoapto Indeterminazione della classificazione basata
omposti etallorganici Fe 1952: risoluzione della struttura del Ferrocene (diciclopentadienilferro) 1 monoapto, 2 diapto, 3 triapto, etc.., fino a 8 octoapto Indeterminazione della classificazione basata
PIANO DI STUDIO DELLA DISCIPLINA
 ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it Rev. 1.1 del 26/07/17 https://isisfacchinetti.gov.it CHIMICA ORGANICA PIANO DELLE
ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it Rev. 1.1 del 26/07/17 https://isisfacchinetti.gov.it CHIMICA ORGANICA PIANO DELLE
ALCHENI CICLOALCHENI. C n H 2n. C n H 2n-2 C C. Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio
 ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Prof.ssa Stacca Prof.ssa Stacca
 La bassa differenza di elettronegatività tra C e H fa sì che i legami presenti negli alcani siano legami covalenti quasi omopolari; di conseguenza gli alcani sono composti apolari. La bassa differenza
La bassa differenza di elettronegatività tra C e H fa sì che i legami presenti negli alcani siano legami covalenti quasi omopolari; di conseguenza gli alcani sono composti apolari. La bassa differenza
Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Alchini. Suffisso: -ino. d. H 3 CCH 2 CC CH
 Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
Il Legame Chimico e la Struttura Molecolare
 A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
