SECONDA UNIVERSITA DEGLI STUDI DI NAPOLI FACOLTA DI MEDICINA E CHIRURGIA L ENDOSCOPIA CON VIDEOCAPSULA: Cenni storici sulle tecniche di endoscopia
|
|
|
- Tommasina Brescia
- 5 anni fa
- Visualizzazioni
Transcript
1 SECONDA UNIVERSITA DEGLI STUDI DI NAPOLI FACOLTA DI MEDICINA E CHIRURGIA L ENDOSCOPIA CON VIDEOCAPSULA: Cenni storici sulle tecniche di endoscopia La storia dell endoscopia, intesa come aspirazione a guardare all interno del corpo umano utilizzando come accesso gli orifizi naturali, affonda le sue radici in tempi assai remoti. La prima notizia relativa all esplorazione delle cavità naturali del corpo umano risale a quando un medico di Francoforte, Dott. Phillip Bozzini, nel 1806 presentò il suo guida luce. Con questo strumento la luce emessa da una candela di cera, per mezzo di un sistema composto da uno specchio, tubi e speculi, veniva diretta in modo tale da arrivare ad illuminare le cavità del corpo umano. Negli anni successivi apparvero altri sistemi di illuminazione simili, come ad esempio quello inventato da Segalas in Francia nel 1821 e quello di Fischer negli Stati Uniti nel 1827.Un successivo sviluppo del sistema, costruito in scala più vasta, fu quello creato dal francese Charrière, dopo i dati raccolti da Desormeaux, in cui la candela veniva sostituita da una lampada a gas (alimentata da una miscela di alcool etilico e turpentino), ottenendo l'effetto di una migliore intensità di luce. Poiché questi primi endoscopi erano rudimentali e difficili da maneggiare, il dermatologo viennese Grunfeld nel 1873 incominciò a far uso della fiamma del gas e della luce prodotta da una buona lampada di paraffina ( a volte persino della luce solare), dirigendole verso le cavità del corpo umano, per mezzo di uno specchio frontale concavo inventato da Hoffmann nel Inoltre Grunfeld, fu il primo che riuscì ad eliminare piccole ulcerazioni ed in seguito,anche altri medici adottarono lo stesso metodo, sperimentando l'utilizzo di luce elettrica. Nel 1867 un dentista di Breslau, Bruck, introdusse per la prima volta in una cavità umana una lampada con filamento di platino raffreddato ad acqua. Oltre ad illuminare la laringe, egli tentò anche di trans-illuminare la vescica attraverso l'intestino e la vagina. Tuttavia il suo metodo si rilevò inadeguato. I primi spericolati tentativi risalgono infatti alla seconda metà dell 800 attraverso l utilizzazione di strumenti estremamente rudimentali che è difficile solo immaginare. La vera data di nascita dell'endoscopia moderna risale al 1879, quando Max Nitze presentò a Vienna il suo specchio vescicale ossia il cistoscopio. La vescica veniva illuminata con un filamento di platino incandescente del tipo di quello di Bruck e l'osservazione veniva resa possibile da un sistema ottico con ampio campo di visione, calcolato da Beneche (ottico dell'università di Berlino). Poiché le apparecchiature necessarie per l'alimentazione elettrica ed il raffreddamento ad acqua del filamento di platino erano molto complesse, furono pochissimi a fare uso di questo strumento e Solo con la miniaturizzazione della lampada incandescente, inventata da Edison nel 1879, che rese possibile nel 1887 lo sviluppo del metodo endoscopico di esplorazione delle cavità umane; Dittel e Nitze furono i primi a presentare un endoscopie illuminato con una piccola lampada mignon, inoltre, per poter esplorare tutta la vescica attraverso una semplice rotazione dello strumento, Nitze completò il suo sistema ottico aggiungendo un prisma che permetteva di deviare la visione lateralmente. Negli anni successivi, e parallelamente alla diffusione di strumenti solo diagnostici, furono presentati dei progetti, tuttora ancora validi, di cistoscopi con dispositivo di lavaggio e di endoscopi per interventi terapeutici, per menzionarne qualcuno: strumenti con canali per il passaggio di sonde e con dispositivi di deflessione (leva di Albarran), uretere-cistoscopi, pinze vescicali etc...
2 Gli endoscopi presentati tra il 1887 e il 1907 andarono soggetti a continue migliorie a livello meccanico e così altre cavità naturali e artificiali furono aperte all'endoscopia; Nel 1908 un medico di Zeiss, Rìngleb, insieme a Rohr, migliorò il vecchio sistema di Seneche. Queste nuove ottiche endoscopiche risultavano di gran lunga più luminose e, soprattutto davano un immagine corretta sia verticalmente che lateralmente. Nel 1911 il gastroscopie di Sussmann, flessibile in fase di introduzione, veniva irrigidito in un secondo momento per mezzo di un sistema meccanico. Nel 1913 per la prima volta nella storia della medicina, Beer usò la corrente ad alta frequenza, scoperta nel 1890 da Arsonval. Questa scoperta aumentò notevolmente le possibilità di intervento terapeutico endoscopico. Nel 1926 Bovie produsse un generatore ad alta frequenza che rendeva possibile l'incisione sott'acqua. In seguito Stern presentò il primo resettoscopio per la resezione della prostata. Nonostante tutte queste modifiche, il principale problema per l endoscopia rimaneva ancora quello alla lampada incandescente miniaturizzata, in quanto essa non rendevano possibile un ulteriore miglioramento dell'immagine, poiché la luminosità non poteva essere aumentata senza ridurne la durata. Però, verso la fine degli anni '50 apparvero negli Stati Uniti le prime fibre ottiche per la trasmissione di luce, applicate all'endoscopia ( le prime fibre vennero prodotte negli anni '30 da Lanini, Baird, Mansell e Kanapy ed il loro utilizzo nella ricerca spaziale ne aveva determinato l'ulteriore sviluppo). Queste fibre di vetro rivestite, del diametro di 20/70 micron e raggruppate in fasci flessibili, permettevano di illuminare cavità anche a grandi distanze senza diminuzione dell'intensità e con una minima dispersione di calore e cosi nel 1963 si ebbero i primi endoscopi detti a luce fredda, tuttora di uso corrente. Gli ultimi sviluppi di una certa importanza nel campo dell'endoscopia risalgono al 1967/68, con le ottiche di Hopkìns e Lumina; nel sistema ottico di Hopkins gli spazi tra una lente e l'altra vengono colmati da bacchette di vetro e le lenti stesse hanno forma tubolare. Questo ha dato origine all'espressione " ottiche ad antenna" o "ottiche a bacchetta". Le ottiche Lumina sono invece costituite da un sistema che comprende lenti e tubi costruiti con un nuovo tipo di vetro per ottiche, sottoposto a speciale trattamento. Per esigenze anatomiche, il raggio centrale dell'ottica di un endoscopie deve essere in genere deviato lateralmente. La deviazione del raggio centrale può essere ottenuta con diversi tipi di prisma la funzione di questi prismi è di correggere l'immagine verticalmente e lateralmente per l'osservatore.
3 La moderna endoscopia L inizio della moderna endoscopia può essere ascritto all introduzione dei fibroendoscopi, presentati per la prima volta da Hirschowitz nel Tali strumenti, completamente flessibili, costituiscono un tipo di endoscopi completamente differente da tutti quelli proposti fino ad allora. Nei fibroscopi le fibre ottiche non solo trasmettono la luce ma anche l'immagine ottica. Le fibre utilizzate sono ancora più sottili di quelle impiegate per la sola trasmissione della luce e la disposizione delle fibre deve essere coerente ed allineata. Nei fibroscopi l'immagine dell'oggetto viene proiettata sulla superficie delle fibre di vetro per mezzo di una lente e poi viene trasmessa dalle fibre stesse e osservata all'altra estremità dall'operatore tramite un oculare. Si ottiene così uno schermo che è più o meno approssimativo in rapporto allo spessore delle fibre usate. Le fibre rotte sono facilmente visibili sotto forma di puntini che interferiscono sull'immagine. I fibroscopi potevano essere usati per l'esplorazione di cavità naturali difficilmente raggiungibili con gli strumenti rigidi.l'estremità distale dei fibroscopi può essere inclinata tramite un meccanismo collocato nell'estremità prossimale, che permette, durante l'inserzione di guidare lo strumento attraverso lo stomaco e l'intestino e di esaminare così in modo minuzioso aree ben definite. Lo strumento è dotato di uno o due canali operativi che consentono interventi di piccola chirurgia utilizzando accessori flessibili e di altri due piccoli canali di servizio che inviano sull'estremità distale, a mezzo di una pompa, acqua sotto pressione per poter lavare l'obiettivo dello strumento e aria per poterlo asciugare, La stessa aria serve anche per poter dilatare la cavità in esplorazione e garantire una migliore osservazione. Dopo l'invenzione dell'endoscopio flessibile, l endoscopia digestiva è stata effettuata su vasta scala, con notevole riduzione dei disagi per i pazienti e si è determinato un enorme ampliamento delle possibilità diagnostiche e la messa a punto delle prime applicazioni terapeutiche della metodica. A parte alcune eccezioni come la broncoscopia e la coledoco-scopia, il principale campo di applicazione e di sviluppo dell endoscopia è rimasto l'esplorazione del tratto gastro-intestinale ed in rapporto alle porzioni di intestino da esaminare ed alle diverse possibilità di impiego sono stati creati specifici tipi di strumenti quali esofago-gastroscopi, duodenoscopi, sigmoidoscopi o colonscopi. L ulteriore, fondamentale punto di svolta dell endoscopia moderna è stato l introduzione della videoendoscopia, che ha segnato la definitiva consacrazione dell endoscopia come una delle tecniche più importanti per la diagnosi ed il trattamento di molte patologie dell apparato digerente. Infatti, la possibilità che non solo operatore ma anche tutti i collaboratori potessero seguire tutte le fasi dell indagine su di un monitor ha determinato una vera rivoluzione nel modo di insegnare e di eseguire le procedure endoscopiche. In effetti la video endoscopia ha rappresentato quel salto di qualità che ha poi reso possibili tutte le ulteriori evoluzioni tecnologiche della metodica, sia in campo diagnostico, come la magnificazione, la virtual cromo endoscopy, l endoscopia ad immunofluorescenza, solo per citarne alcune, sia in campo terapeutico, come le tecniche di resezione endoscopica delle neoplasie superficiali gastrointestinali. I problemi di esplorazione del piccolo intestino Gli enormi sviluppi tecnologici dell endoscopia non sono serviti, però, a superare il limite rappresentato dall impossibilità di esplorare, se non in minima parte, il tratto più esteso del tubo digerente, cioè il piccolo intestino. Anche con gli attuali strumenti, l endoscopia del tratto digestivo superiore consente al massimo l esplorazione di tutte le porzioni del duodeno, mentre mediante l endoscopia del tratto digestivo inferiore può essere possibile l intubazione della valvola ileo cecale per via retrograda e la visualizzazione solo
4 dell ultima ansa ileale. Questi tratti corrispondono ad una piccolissima percentuale dell intera estensione del piccolo intestino, che quindi è rimasto come una specie di buco nero inesplorabile. Per molto tempo questo handicap della tecnica endoscopica è stato considerato trascurabile dal punto di vista clinico, tenuto conto che il peso complessivo della patologia che può colpire il piccolo intestino è ben poca cosa rispetto alla frequenza ed alla gravità delle malattie che possono essere riscontrate a livello gastro-duodenale o del colon. In sostanza si è ritenuto che l intestino tenue, a dispetto della sua notevole estensione, fosse in realtà poco importante in termini di impatto clinico così che la difficoltà di studio di questo distretto non dovessero rappresentare un grande problema. Un tale atteggiamento si è progressivamente modificato nel tempo alla luce del miglioramento delle conoscenze sulla fisiopatologia dell intestino tenue e sulla rilevanza clinica da attribuirsi ad alcune affezioni a carico di questo tratto intestinale, a partire dai sanguinamenti, da alcuni tipi di neoplasie rivelatesi non così rare come si riteneva in passato, come i tumori di natura mesenchimale, o, soprattutto la malattia di Crohn. Per tale motivo si è cominciato a valutare come ingiustamente trascurato il piccolo intestino ed a percepire l esigenza di mettere a punto della tecniche endoscopiche volte ad esplorare in maniera più adeguata tale segmento intestinale. Con gli strumenti endoscopici convenzionali l unica possibilità di migliorare lo studio del tenue era affidata all utilizzo intraoperatorio. In tal modo l endoscopio viene introdotto attraverso una tomia dell intestino e fatto procedere con l aiuto del chirurgo che avvolge l intestino sull endoscopio. Ovviamente si tratta di una procedura applicabile nei casi in cui, in assenza di una diagnosi preoperatoria, si è costretti ad effettuare una laparotomia esplorativa ed a tentare di giungere ad una diagnosi durante lo stesso intervento. Pertanto sono stati progettati strumenti endoscopici molto più lunghi di quelli convenzionali (enteroscopi) nel tentativo di estendere il tratto di intestino da poter esplorare. L enteroscopia costituiva in ogni caso una tecnica molto complessa, molto difficile da realizzare perché la possibilità di avanzamento dello strumento nel piccolo intestino è molto limitata per la notevole mobilità delle anse del tenue. In realtà l enteroscopia è stata una tecnica che ha avuto uno scarso sviluppo ed è rimasta limitata a pochissimi centri. Inoltre si trattava di una metodica molto dispendiosa in termini di tempo, di tolleranza da parte dei pazienti e che poteva consentire solo un esplorazione parziale del piccolo intestino. Più recentemente sono stati proposti ulteriori strumentazioni per realizzare la cosiddetta push enteroscopy, in particolare gli enteroscopi a singolo o a doppio pallone che, certamente hanno la possibilità di addentrarsi più agevolmente nel lume del piccolo intestino, ancorandosi di volta in volta alla sua parete, attraverso il gonfi aggio e lo sgonfiaggio dei palloni attaccati all enteroscopio. Anche utilizzando tali strumenti l esplorazione del tenue rimane una metodica molto complessa, che richiede molto tempo comunque non può assicurare la visualizzazione dell intero piccolo intestino. Si tratta quindi di una metodica da riservare ai casi in cui c è da effettuare un trattamento endoscopico per una lesione già identificata, ma non può essere proposto come una tecnica diagnostica per l intestino tenue.
5 L ENDOSCOPIA CON VIDEO CAPSULA La capsula endoscopica Nel 1966, al pubblico cinematografico fu proposto un film destinato a far discutere... "Viaggio Allucinante" (tit. or., Fantastic Voyage). Il film, tratto da un racconto di Isaac Asimov, descriveva una funambolica tecnologia grazie alla quale era possibile miniaturizzare - riducendolo a dimensioni dei microbi - una sorta di minisommergibile con tanto di equipaggio umano, in grado di essere introdotto nel corpo per effettuare al suo interno esami diagnostici ed operazioni di microchirurgia.lo stesso Asimov, aveva sottolineato che l'insieme narrativo era pura fantasia: un espediente letterario per descrivere le meraviglie e le possibilità che si sarebbero manifestate disponendo di una simile tecnologia. Circa 35 anni dopo, una versione meno suggestiva ma altrettanto emozionante di questa tecnologia ha visto la luce: la capsula endoscopica. La capsula endoscopica nota anche con il nome di wireless endoscopy o capsula enteroscopica, rappresenta uno dei più recenti sviluppi tecnologici in endoscopia. La capsula endoscopica permette di aumentare l'incidenza diagnostica soprattutto per quanto riguarda la patologia a carico dell'intestino tenue. La capsula è stata ideata nel 1981 da un ingegnere israeliano, Gavriel Iddan, il quale pensò di creare un piccolo vettore in miniatura in grado di attraversare tutto l'apparato gastrointestinale, trasportato dai movimenti legati alla peristalsi con la possibilità di trasmettere in tempo reale le immagini del suo percorso. Nel 1994, dopo lo sviluppo del prototipo e la verifica di fattibilità, sono state registrate le prime immagini trasmesse dallo stomaco di maiale, a queste fino al 1996, seguirono numerosi trials sempre sull'animale. Un ulteriore avanzamento tecnologico del prototipo ha visto la riduzione delle dimensioni della capsula ed un aumento della capacità di trasmissione e della durata di registrazione ed una maggiore risoluzione delle immagini; questi miglioramenti tecnologici hanno portato all'impiego della capsula in soggetti umani. Infatti nell agosto 1999, fu ingoiata la prima capsula endoscopica (M2A Capsule Endoscopy; Given Imaging, Yogneam, Israel). La metodica fu presenta nella primavera del 2000 con un articolo pubblicato su Nature e nel corso della Digestive Disease Week statunitense e nel 2001 ha ricevuto l'approvazione della FDA (Food and Drug Administration) statunitense e ne è stato autorizzato l uso clinico. Nello stesso anno anche in Europa ha avuto inizio la sperimentazione del sistema diagnostico. In estrema sintesi la procedura si basa sull uso di una microtelecamera contenuta in una capsula monouso, delle dimensioni comparabili con quelle di una capsula di farmaco, che viene ingerita con qualche sorso d acqua e che, spinta dalla peristalsi, viene espulsa per la via naturale dopo aver percorso tutto il tubo digerente, lungo il quale raccoglie una serie di immagini video.
6 La struttura della video capsula Il sistema di video endoscopia con capsula consta di tre unità: una capsula deglutibile, un registratore per incamerare le immagini, un apposito computer (workstation) per elaborare e visualizzare le immagini raccolte. La Capsula L enterocapsula è monouso, costituita di materiale biocompatibile sigillato in maniera speciale resistente ai succhi gastrici ed alla pressione. Le dimensioni sono di 11 mm x 26 mm, (più o meno le dimensioni di una capsula di antibiotico o di una grossa pillola di vitamine), il peso è 3.7 g. All'interno è contenuta una cupola ottica, un fermo per la lente, la lente, un sistema di illuminazione a LED (Light Emitted Diode), un sistema d acquisizione immagini a colori a CMOS (Complementary Metal Oxide Semiconductor), in grado di acquisire due immagini ogni secondo per circa otto ore per un totale di oltre immagini,inoltre presenta due batterie, un trasmettitore miniaturizzato ASIC (Application Specific Integrated Circuit) ed un'antenna. La struttura della video capsula è schematizzata nella Fig 1 1. cupola ottica 2. fermo per la lente 3. lente 4. illuminazione a LED (Light Emitted Diode) 5. acquisizione immagini a CMOS (Complementary Metal Oxide Semiconductor) 6. batterie 7. trasmettitore ASIC (Application Specific Integrated Circuit) 8. antenna Il registratore Le immagini riprese ed inviate dalla video capsula vengono e raccolte da una serie di sensori (simili agli elettrodi dell'ecg) fissati con appositi adesivi alla cute dell addome. Le immagini vengono quindi trasmesse ad una unita esterna, un registratore costituito da una smart-card (analoga a quelle utilizzate nelle fotocamere digitali) che ha le dimensioni di un lettore portatile di CD e che è collocato con una cintura intorno alla vita del paziente. Attualmente e disponibile un nuovo dispositivo, denominato antenna jacket che viene indossato dal paziente come un gilet senza dover fissare gli elettrodi sull epidermide. Tale dispositivo, oltre ad immagazzinare le immagini del tratto gastrointestinale è dotato di circuiti attraverso i quali è possibile ottenere numerosi parametri del paziente senza l'utilizzo di cavi, come ad esempio la valutazione del polso, della pressione arteriosa e della temperatura corporea
7 La Workstation Al termine della registrazione, la cui durata complessiva, come detto, in rapporto alla durata delle batterie è di circa 8 ore, viene rimossa la cintura con il registratore, che viene collegato ad un computer (work station), con un software dedicato per analizzare ed interpretare le immagini acquisite e ricercare reperti patologici. Il tempo necessario per tale operazione può variare da 50 minuti a circa 2 ore, in relazione al quesito anamnestico, alla complessità del quadro endoscopico e all esperienza dell esaminatore. Nella Fig 2 sono rappresentati il registratore ed il computer La Video capsula per il colon La PillCam COLON misura 11x31 mm, possiede ai due poli due lenti ed è provvista di due videocamere. Ha dimensioni maggiori nell'asse longitudinale per accogliere batterie di maggiore capacità che implicano la possibilità di più tempo di indagine Registra 4 immagini/sec per una durata massima di 10 h. Dopo l ingestione la capsula rimane attiva per 3 min per poi entrare in stand-by per 1 h e 45 min, periodo al termine del quale si riattiva. Al momento della riattivazione, nel 97,5% dei casi essa si trova già nel piccolo intestino. Grazie alle 2 telecamere, la visuale è doppia rispetto a quella della capsula per il tenue e ciò consente una migliore visualizzazione del colon. Le più recenti evoluzioni della videocapsula colica dispongono di un dispositivo di spegnimento dall'esterno che quindi può consentire un più lungo tempo di utilizzo nei segmenti voluti. La video capsula per l esofago Tra i più recenti sviluppi nel campo della endoscopia capsulare va annoverata anche la capsula esofagea (PillCam ESO ).Anche la capsula esofagea è dotata ai due poli di due lenti e due videocamere, che consentono l'acquisizione di più fotogrammi da entrambi i lati. L esofago per le sue caratteristiche anatomiche e funzionali non rappresenta certamente il viscere più adatto per l impiego dell endoscopia con video capsula,in quanto si tratta di un segmento intestinale molto corto con un transito piuttosto veloce ; inoltre, solo l insufflazione consente di distenderne adeguatamente il lume e di osservarne bene le pareti., ed essendo come ovvio, quest ultima preclusa con la vce, non ci si può attendere una qualità d immagine neppure lontanamente comparabile con quelle eseguite con le tecniche di endoscopia convenzionale. Nonostante ciò è stato ipotizzato un possibile impiego della vce per la valutazione ed il follow up di alcune patologie proprie dell esofago quali l esofago di Barrett e le varici esofagee.
8 Cenni sulle fasi della procedura L indagine prevede una preparazione per la pulizia intestinale nelle 24 ore precedenti l esame. L utilizzo della preparazione (PEG, NaP) sembra migliorare la visione della mucosa in corso di VCE. L associazione di sostanze tensioattive forniscono un ulteriore vantaggio all uso della VCE. Il problema della preparazione dell intestino assume un importanza cruciale per l impiego della video capsula nello studio del colon. Infatti, con l endoscopia convenzionale, anche in presenza di una toilette intestinale non ottimale, utilizzando il lavaggio e l aspirazione è possibile riuscire a condurre a termine una soddisfacente esplorazione del colon. Invece utilizzando la video capsula, come risulta intuibile, non è possibilità migliorare la pulizia del viscere nel corso dell esame e quindi risulta indispensabile ottenere una preparazione intestinale perfetta. Sono stati proposti diversi schemi di preparazione con ricorso a prodotti differenti ed a diverse restrizioni dietetiche, ma si discute ancora molto nell intento di ricercare la migliore soluzione per evitare che l indagine possa risultare inaffidabile sul piano diagnostico. Una opzione che viene sempre più frequentemente proposta, per ottenere la massima garanzia di una adeguata pulizia del colon è la preparazione intestinale con l'idrocolon pulizia (colon washing). Si tratta di una metodica che certamente puo risultare di notevole aiuto nella diagnostica, però comporta problemi di carattere organizzativo e di lievitazione dei costi. In tutti i casi l utilizzo della video capsula necessita di un digiuno di almeno 8 ore prima dell assunzione della stessa. Inoltre, prima dell utilizzo, vanno posizionati i sensori ed il registratore dei dati sul paziente e dopo l attivazione della capsula, il paziente viene invitato ad ingerirla con un sorso d acqua. La capsula si sposta in maniera naturale attraverso il tratto gastrointestinale sfruttando i movimenti peristaltici, ed il paziente non avverte nessun fastidio e può svolgere tutte le normali attività, anzi gli viene consigliato di camminare o salire e scendere le scale per facilitare il transito della videocapsula. Vi sono poche precauzioni da ricordare, tra cui evitare campi elettromagnetici (andare in luoghi con il metal detector, utilizzare il telefono cellulare ecc.). Per quanto riguarda l alimentazione del paziente, due ore dopo l ingestione della capsula possono essere assunti liquidi quali succhi di frutta, tè, caffè (non latte né antiacidi in quanto possono oscurare la ripresa); uno spuntino leggero può essere consumato circa 4 ore dopo l ingestione della capsula ed infine dopo 8 ore può essere ripresa l alimentazione normale. La durata dell esame è di circa 8 ore(periodo della durata delle batterie), dopo di che il paziente restituisce il registratore al dottore o all infermiere, il quale viene collegato ad un Pc al quale trasferisce tutte le immagine registrate. La capsula endoscopica è a perdere(cioè dopo l esame non puo essere riutilizzata) e sarà espulsa naturalmente con le feci; nel caso raro in cui ciò non avvenga (a livello mondiale la percentuale di non rilascio spontaneo della capsula è dello 0.5 % circa), la video capsula dovrà essere rimossa endoscopicamente o chirurgicamente.
9 Vantaggi e limiti dell endoscopia con videocapsula I vantaggi teorici della capsula endoscopica sono notevoli. Innanzitutto l ottima compliance da parte del paziente che risulta essere intuibile perché, per quanto l'endoscopia tradizionale sia quasi sempre ben tollerata, è innegabile che la semplice ingestione di una capsula sia decisamente preferibile. Anche i costi dovrebbero essere accettabili; infatti sebbene la capsula sia a perdere, la spesa per ogni esame non è molto più alta di quello di un'endoscopia tradizionale. Inoltre dall introduzione nella pratica clinica già si sono registrati notevoli sviluppi tecnologici, che stanno portando progressivamente ad un ampliamento delle indicazioni. Nondimeno la possibilità che tale metodica, possa divenire l alternativa agli esami endoscopici convenzionali, come la gastroscopia o la colonscopia è ancora lontana dal divenire realtà. Esistono, infatti, ancora numerosi limiti tecnici da superare prima che la VCE possa diventare una procedura indicata per lo studio dell intero intestino e delle sue patologie e quindi come detto, sostituire gran parte delle tecniche endoscopiche convenzionali, anche se è ipotizzabile che ciò possa accadere in un futuro non molto lontano. I limiti maggiori riguardano attualmente la possibilità di esplorare la parete gastrica. Infatti, il lume ampio, la particolare motilità che fa muovere disordinatamente la capsula con registrazioni in direzioni casuali, l insufficiente illuminazione, e la rapidita di transito, permettetono un'esplorazione solo parziale di questo organo e poco affidabile. Tali difficoltà, seppure in minor misura, sono presenti anche al colon, dove in più si aggiungono le problematiche inerenti ai tempi lunghi di transito e quindi problemi di durata delle batterie; Inoltre per il colon, come visto in precedenza, si pone il problema della toilette intestinale, che dovrebbe essere perfetta per consentire una buona e completa visione. Altro limite importante per la videocapsula rispetto alle tecniche classiche di endoscopia, è l impossibilità di eseguire prelievi bioptici o qualunque procedura di tipo operativo Le attuali indicazioni all endoscopia con videocapsula Da tutto quanto detto si comprende come, attualmente le indicazioni consolidate dell endoscopia con video capsula, debbano riguardare eminentemente la diagnostica delle patologie dell intestino tenue che seppur rare rispetto ad altre porzioni del tratto gastro-intestinale, sono estremamente difficile da diagnosticare. D altra parte l intestino tenue rappresenta il viscere ideale per la progressione della video capsula, in quanto il lume non troppo ampio, la peristalsi regolare che consente un transito in tempi abbastanza costanti e commisurati con la durata delle batterie, permettono alla video capsula, di procedere senza rotolamenti e di fornire una completa visione delle pareti di questo tratto intestinale, riprendendole in avanti o indietro a seconda dell'orientamento d'ingresso. La visualizzazione dello sfondato cecale conferma il raggiungimento del grosso intestino. Come è stato sottolineato in precedenza, invece, le tecniche di endoscopia convenzionale in tale ambito risultano molto complesse, mal tollerate dai pazienti, tanto da richiedere la sedazione profonda, se non la narcosi e comunque consentono di esplorare solo parzialmente in tenue.
10 Le indicazioni all impiego della video capsula nello studio del tenue L endoscopia con video capsula deve essere considerata l indagine di scelta per la valutazione del piccolo intestino con applicazioni cliniche che, però, seppure importanti, rimangono limitate ad un ben preciso ambito e cioè la diagnosi delle patologie a carattere non occlusivo in quanto in presenza di un sospetto altamente fondato di occlusione, come si dirà più dettagliatamente in seguito, l impiego della video capsula dovrebbe essere controindicato essendo un possibile fattore aggravante per l occlusione. Differente è il discorso per lo studio di malattie potenzialmente stenosanti, come il morbo di Crohn che, invece, seppure a determinate condizioni, rappresenta una delle possibili applicazioni. In sintesi, a trarre vantaggio dall impiego di questo nuovo strumento diagnostico, sono soprattutto quelle lesioni intestinali che non possono essere evidenziate con le tecniche di endoscopia convenzionale. E in tale ambito che l utilizzazione della video capsula diventa preziosa, risultando in grado di risolvere problemi diagnostici non altrimenti risolvibili. Tali indicazioni possono essere così di seguito schematizzate: Definite Sanguinamento gastrointestinale di origine oscura (EGDS e Colonscopia negative) Morbo di Crohn Celiachia Tumori dell intestino tenue Sorveglianza delle sindromi poliposiche. In corso di validazione Sorveglianza del trapianto dell intestino tenue
11 Sanguinamento gastrointestinale di origine oscura Nell ambito della valutazione delle emorragie gastrointestinali oscure la VCE è stata proposta come tecnica efficace per identificare la fonte di sanguinamento, definito come "anemia da carenza di ferro ricorrente o persistente, positivo al test del sangue occulto fecale FOBT (Faecal Occult BloodTest). Si calcola che circa il 33-52% dei casi di sanguinamento occulto e il 4-5% dei casi di sanguinamento oscuro non trovino una spiegazione neanche dopo l esecuzione di gastroscopia e colonscopia Approssimativamente il 5% dei sanguinamenti gastrointestinali si verificano tra il legamento di Treitz e la valvola ileocecale. Una delle cause di tali sanguinamenti è costituita dalle angiodisplasie gastrointestinali. Tale reperto rappresenta una entità patologica e clinica caratterizzata da ectasie vascolari che possono rompersi od ulcerarsi provocando una emorragia acuta o, più frequentemente, un sanguinamento cronico. E stato calcolato che le angiodisplasie del piccolo intestino incidano per 30% to 40% come causa di sanguinamento occulto gastrointestinale e rappresentano la più comune fonte di sanguinamento nei pazienti anziani. L enteropatia da uso di farmaci anti-infiammatori non steroidei e le malattie infiammatorie croniche intestinali possono essere associate con erosioni, ulcere e di stenosi del piccolo intestino e perciò possono essere causa di sanguinamento occulto. Altre possibili cause comprendono i tumori, che sono considerate la più comune fonte di sanguinamento occulto gastro intestinale (SOGI) nei pazienti con meno di 50 anni. Si tratta di tipi diversi di neoplasie, soprattutto tumori di natura mesenchimale, come leiomiomi o GIST, quindi tumori neuroendocrini (carcinoidi), linfomi e infine, meno frequentemente, adenocarcinomi. Specialmente nei pazienti giovani bisogna poi considerare le ulcerazioni associate a diverticolo di Meckel. Altre cause più rare di SOGI, possono essere rappresentate infine da enteropatia da radiazioni, ulcere di Dieulafoy e varici del piccolo intestino. La VCE si pone come la metodica più indicata per la diagnosi di tali sanguinamenti con elevata accuratezza diagnostica, superiore a quella delle altre metodiche d immagine (push-enteroscopia, clisma del tenue, clisma TC del tenue, RMN del tenue). Una metanalisi di 14 studi prospettici per un totale di 396 pazienti con SOGI ha evidenziato come la videocapsula dimostrasse una più alta performance per l identificazione di lesioni clinicamente significative (56%) rispetto alla push enteroscopy (26%) In comparazione con il criterio standard dell enteroscopia intraoperatoria per l identificazione della fonte di sanguinamento, la VCE ha evidenziato una sensibilità del 95% and una specificità del 75% in uno studio prospettico, di due centri su 47 pazienti. Rispetto all angio TAC ed all angiografia standard, la VCE identificava un numero maggiore di lesioni fonte di sanguinamento (72% con la VCE vs 24% con l angio TAC ed il 56% con l angiografia). L elevata performance diagnostica (91.9%) della VCE praticata in urgenza (entro 48 ore dopo l accesso in reparto) in pazienti con sanguinamento occulto acuto gastrointestinale di entità lieve e moderata suggerisce che un intervento diagnostico precoce con la video capsula può migliorare il successo diagnostico. I vantaggi della video capsula includono la non invasività della procedura, l accettabilità da parte dei pazienti, la sicurezza e l affidabilità diagnostica in questo specifico campo di applicazione. Le limitazioni, oltre alla più volte citata incapacità di effettuare un intervento terapeutico, consistono nella possibilità di non localizzare con precisione la sede della lesione, i risultati falsi positivi, la potenzialità di un transito troppo veloce con la conseguenza di non vedere le lesioni e infine la vita limitata delle batterie che può causare uno studio incompleto. Se attraverso l endoscopia con video capsula vengono evidenziate lesioni significative, il paziente dovrebbe essere avviato ad uno specifico trattamento. I tassi di risanguinamento dopo uno studio negativo con VCE sono generalmente bassi (6%- 11%). Se la videocapsula non riesce ad identificare la causa del SOGI, può essere presa in considerazione una seconda indagine con la VCE, sebbene i risultati non sono univoci. In uno studio prospettico relativo a 76 pazienti con persistente SOGI e una prima valutazione con videocapsula non diagnostica, un second look
12 con la VCE risultava positivo nel 49% dei pazienti. La rivalutazione con video capsula ha più possibilità di risultare diagnostica se il decorso clinico del paziente era virato da un sanguinamento occulto ad un sanguinamento palese o quando si fosse determinata una caduta del emoglobina uguale o maggiore di 4 punti. In un piccolo studio prospettico su 20 pazienti con anemia da carenza di ferro (45) una seconda VCE evidenziò un rilievo positivo o sospetto nel 35% dei casi e determinò una modifica del trattamento nel 10% dei casi. Morbo di Crohn Vi è un trend crescente di pazienti con la malattia di Crohn che vengono sottoposti all'esame con VCE sulla base del fatto che tale indagine permette la diretta visualizzazione della mucosa del piccolo intestino e può essere utile nell identificazione di lesioni superficiali non visualizzate con l endoscopia convenzionale e con metodiche di immagini radiologiche. La VCE potrebbe in effetti essere utile nella prima diagnosi di morbo di Crohn (MC), per la diagnosi di recidiva, per definire l estensione della malattia, per valutare la risposta alla terapia, e per giungere ad una diagnosi differenziale tra MC e RCU o colite indeterminata. I risultati di studi retrospettivi, di case series e di studi prospettici hanno dimostrato che la videocapsula è utile per la diagnosi di MC in caso di enteroscopia o di ileoscopia retrograda negative o non riuscite. Il rendimento diagnostico della video capsula risulta molto variabile (dal 10% al 71%) a seconda delle diverse esperienze cliniche. La video capsula ha mostrato di essere più sensibile nella diagnosi di MC del piccolo intestino rispetto alle metodiche radiologiche ed endoscopiche convenzionali. In pazienti con malattia lieve o moderata ed enteroscopia normale la videocapsula può evidenziare alterazioni del piccolo intestino che non ricadessero nell ambito delle possibilità diagnostiche della stessa enteroscopia. Uno studio prospettico su 42 pazienti ha comparato la video capsula con l enteroscopia, la TAC con enterografia e la colonscopia con ileo scopia retrograda nella valutazione del MC del piccolo intestino. Di queste 4 tecniche la VCE ha avuto la sensibilità più alta (83%) con la più bassa specificità (53%) e la colonscopia con ileoscopia ha avuto la più alta specificità (100%) con una sensibilità del 74%. Uno studio su 39 pazienti, la maggior parte con diagnosi nota di MC ha riportato una sensibilità ed una specificità rispettivamente dell 89.6% e del 100%. Pochi studi hanno valutato i benefici della VCE nella valutazione della colite indeterminata. Uno studio ha evidenziato che 5 di 22 pazienti con colite risultavano avere lesioni di continuo della mucosa alla VCE. In tal modo fu possibile porre diagnosi di MC. Il principale limite della VCE nella valutazione del MC del piccolo intestine è dato dalla mancanza di criteri uniformi per porre la diagnosi di MC. Ancora una volta va sottolineata l impossibilità di effettuare prelievi ed interventi terapeutici. Un ulteriore limite nel caso del morbo di Crohn è rappresentato dalla possibilità che la capsula possa essere ritenuta. La presenza di lesioni di continuo della mucosa non è necessariamente indicativa di MC. Diverse patologie possono, infatti, causare ulcerazioni della mucosa come infezioni, ischemia, esiti di radiazioni e danni da farmaci, particolarmente gli anti-infiammatori non steroidei. In più è stato evidenziato che fino al 14% dei soggetti sani possono avere lesioni di continuo della mucosa o altre lesioni non specifiche. La ritenzione della capsula nei pazienti con MC determinate dalla presenza di stenosi del piccolo intestino, che si verificano dall 1 al 13 % dei pazienti con diagnosi nota di MC. Le capsule ritenute possono richiedere un intervento chirurgico in pazienti che altrimenti non avrebbero avuto necessità di un intervento. Una valutazione radiologica (TAC o clisma seriato del tenue) preliminare alla video capsula è consigliato, perché nei pazienti con MC asintomatici si possono osservare stenosi in una percentuale fino
13 al 22%. I pazienti affetti da MC con sintomi di ostruzione o con evidenza endoscopica o radiologica di stenosi del piccolo intestino non dovrebbero essere sottoposti ad indagine con VCE. In caso di ritenzione di capsule a monte di una stenosi da MC si potrebbe utilizzare un trattamento con anti-infiammatori anche se non vi sono studi pubblicati su tale tema. Per prevenire l evenienza della ritenzione della VCE nei pazienti con MC è stato proposto l uso della cosiddetta patency capsule. La " patency capsule è una capsula che ha la stessa dimensione della capsula video. Viene utilizzata preliminarmente all esame con VCE. Contiene un identificatore a radiofrequenza (RFID) che permette di essere rilevata da un sistema di scansione. Quando il passaggio è ostruito da una stenosi, la capsula patency subisce un'alterazione del proprio profilo che ne facilita il passaggio nel lume in ore dopo l'ingestione. L utilizzo della patency, come metodica capace di scongiurare il rischio che la VCE venga ritenuto e tutt oggi discusso. Infine bisogna sottolineare come una inattesa ritenzione della capsula, nel senso che una valutazione radiologica preliminare non aveva evidenziato stenosi significative, non può essere considerata una complicanza in senso stretto, perché in realtà consente di fare una diagnosi di stenosi non rilevata con altre tecniche. Valutazione degli effetti collaterali di antinfiammatori non steroidei (FANS) Diversi studi hanno dimostrato che sono frequenti lesioni intestinali in pazienti trattati con FANS. Il quadro clinico può includere sanguinamento palese o occulto, dolore addominale, od ostruzione intestinale nei casi di stenosi. Le lesioni più frequentemente riscontrate sono ulcere ed erosioni. Sorveglianza delle sindromi poliposiche La sorveglianza endoscopica nelle sindromi poliposiche risulta di notevole importanza; di fatto queste forme sono gravate da un elevato rischio di evoluzione neoplastica. Il contributo dell enteroscopia con videocapsula risulta particolarmente importante in quanto consente un esaustiva valutazione del piccolo intestino. Celiachia L utilizzo della videocapsula nella celiachia consente di evidenziare la distribuzione delle aree di atrofia dei villi, caratteristica di questa malattia e le eventuali altre alterazioni mucosali associate. La VCE può mostrarsi particolarmente interessante per il work-up diagnostico dei pazienti con celiachia che si presentano con sintomi atipici o anemia cronica da carenza di ferro. Inoltre nei pazienti con diagnosi nota di malattia celiaca, la VCE è indicata nei casi in cui si presenti una recidiva sintomatica nonostante l'osservanza di una dieta senza glutine. In questa situazione, la VCE potrebbe rivelare un modello di digiunite ulcerosa o linfoma a cellule T.
14 Tumori dell intestino tenue La VCE identifica in modo efficace i tumori dell'intestino tenue che sono rilevabili con i classici esami radiologici (impatto diagnostico uguale al 52,6%) Le possibili indicazioni della videocapsula per lo studio del colon La Videocapsula come gia detto, non sostituisce la colonscopia convenzionale (che costituisce ancora il gold standard per individuare le neoplasie del colon), ma rappresenta uno strumento aggiuntivo e complementare. Le principali indicazioni sono rappresentate dalla colonscopia incompleta, dai pazienti a rischio per manovre endoscopiche, e specialmente dalla non compliance alla colonscopia stessa. Il New England Journal of Medicine ha pubblicato lo scorso anno uno studio multicentrico sulla videocapsula endoscopica (Capsule Endoscopy versus Colonoscopy for the Detection of Polyps and Cancer ) che nelle intenzioni dei suoi produttori voleva verificare se la videocapsula poteva essere un' alternativa alla colonscopia tradizionale nella diagnosi delle lesioni del colon. Sono stati trattati 300 pazienti con patologia del colon conclamata o sospetta e i risultati sono stati che la videocapsula ha una sensibilità del 64 per cento nell'identificare polipi di dimensioni pari o superiori a 6 mm; del 73 per cento in caso di adenomi in stadio avanzato di 6 mm o più grandi; del 74 per cento nel caso di tumori e la sensibilità si è rivelata migliore con una preparazione più accurata dell'intestino. L'editoriale che commenta l'articolo osserva che la bassa sensibilità della videocapsula nell'identificare adenomi di piccole dimensioni è fonte di preoccupazione. Per questa ragione e per la necessità di una migliore pulizia intestinale si conclude che la capsula endoscopica non può attualmente essere raccomandata per questa indicazione. Controindicazioni all esame con Videocapsula Assolute Ostruzione o pseudostruzione intestinale Gravidanza Relative Pacemaker* o defibrillatori Neuropatia diabetica severa Pregressa chirurgia addominale maggiore Patologie motorie intestinali Disordini della deglutizione Diverticolo di Zenker Diverticolosi severa del tubo digerente
15 La capsula deve essere usata con cautela in pazienti con nota o sospetta ostruzione gastrointestinale,fistole, e disturbi della deglutizione. Dati recenti suggeriscono che il segnale in radiofrequenza della VCE non interferisce con pacemaker cardiaco. La sicurezza in gravidanza non è stata ancora stabilita. Prospettive Future Sembra probabile che nei prossimi anni lo studio e la sperimentazione in endoscopia saranno incentrati sulla videocapsula e anche se queste sono state inizialmente sviluppate per esaminare il piccolo intestino, vi sono già prototipi in corso di valutazione per l'esofago, lo stomaco ed il colon. I recenti miglioramenti tecnici includono l incremento di acquisizione d immagini (frame per secondo) una maggiore risoluzione e un più ampio angolo di visione. Inoltre, riveste un ruolo fondamentale la durata energetica delle batterie. Una caratteristica innovativa adottata in capsule (PillCam Colon 2) della seconda generazione è la variazione dei frame rate con movimento della capsula. Il frame rate della capsula in movimento è di circa 35 al secondo, tuttavia si riduce a 2 al secondo quando la capsula è ferma. Una soluzione alternativa alla vita della batteria è la ricarica delle batterie da un alimentatore extracorporeo. Un problema particolare è il tempo necessario per analizzare i dati rilevati dalla capsula del piccolo intestino. Questo è di solito min anche se una riduzione del tempo è stata realizzata con miglioramenti in software e ci possono essere ulteriori risparmi di tempo con l'esperienza. Inoltre in futuro, saranno sviluppate piccole capsule che possono essere usate nei bambini e nei pazienti con nota o sospetta stenosi del piccolo intestino. Bibliografia 1. Mishkin D, Chuttani R, Croffie J, et al. ASGE Technology Status Evaluation Report: wireless capsule endoscopy. Gastrointest Endosc 2006;63: Triester S, Leighton J, Leontiadis G, et al. A meta-analysis of the yield of capsule endoscopy compared to other diagnostic modalities in patients with obscure gastrointestinal bleeding. Am J Gastroenterol 2005;100: Hartmann D, Schmidt H, Bolz G, et al. A prospective two-center study comparing wireless capsule endoscopy with intraoperative enteroscopy in patients with obscure GI bleeding. Gastrointest Endosc 2005; 61: Saperas E, Dot J, Videla S, et al. Capsule endoscopy versus computed tomography or standard angiography for the diagnosis of obscure gastrointestinal bleeding. Am J Gastroenterol 2007;102:731-7.
16 5. Li F, Gurudu S, De Petris G, et al. Retention of the capsule endoscope: a single-center experience of 1000 capsule endoscopy procedures. Gastrointest Endosc 2008;68: Petersen B, Hussain N, Marine J, et al. Endoscopy in patients with implanted electronic devices. Gastrointest Endosc 2007;65: Macdonald J, Porter V, McNamara D. Negative capsule endoscopy in patients with obscure GI bleeding predicts low rebleeding rates. Gastrointest Endosc 2008;68: Lai L,WongGLH,ChowDKL, et al. Long-term follow-up of patients with obscure gastrointestinal bleeding after negative capsule endoscopy. Am J Gastroenterol 2006;101: Viazis N, Papaxoinis K, Vlachogiannakos J, et al. Is there a role for second-look capsule endoscopy in patients with obscure GI bleeding after a nondiagnostic first test? Gastrointest Endosc 2009;69: Bar-Meir S, Eliakim R, Nadler M, et al. Second capsule endoscopy for patients with severe iron deficiency anemia. Gastrointest Endosc 2004;60: Caunedo A, Rodrigues-Tellex M, Garcia-Montes J, et al. Usefulness of capsule endoscopy in patients with suspected small bowel disease. Rev Esp Enferm Dig 2004;96: Dubcenco E, Jeejeebhoy KN, Tang SJ, et al. The value of capsule endoscopy in the diagnosis and management of Crohn s disease: report of two cases. Gastrointest Endosc 2004;59: Hara AK, Leighton JA, Sharma VK, et al. Small bowel: preliminary comparison of capsule endoscopy with barium study and CT. Radiology 2004;230: Herrerias JM, Caunedo A, Rodriguez-Tellez M, et al. Capsule endoscopy in patients with suspected Crohn s disease and negative endoscopy. Endoscopy 2003;35: Mow WS, Lo SK, Targan SR, et al. Initial experience with wireless capsule enteroscopy in the diagnosis and management of inflammatory bowel disease. Clin Gastroenterol Hepatol 2004;2: Fireman Z, Mahajna E, Broide E, et al. Diagnosing small bowel Crohn s disease with wireless capsule endoscopy. Gut 2003;52:390-2.
17 17. Arguelles-Arias F, Caunedo A, Romero J, et al. The value of capsule endoscopy in pediatric patients with a suspicion of Crohn s disease. Endoscopy 2004;36: Costamagna G, Shah SK, Riccioni ME, et al. A prospective trial comparing small bowel radiographs and video capsule endoscopy for suspected small bowel disease. Gastroenterology 2002;123: Eliakim R, Fischer D, Suissa A, et al. Wireless capsule video endoscopy is a superior diagnostic tool in comparison to barium follow-through and computerized tomography in patients with suspected Crohn s disease. Eur J Gastroenterol Hepatol 2003;15: Eliakim R, Suissa A, Yassin K, et al. Wireless capsule video endoscopy compared to barium followthrough and computerized tomography in patients with suspected Crohn s diseasedfinal report. Dig Liver Dis 2004;36: ASGE guideline: endoscopy in the diagnosis and treatment of inflammatory bowel disease Voderholzer WA, Ortner M, Rogalla P, et al. Diagnostic yield of wireless capsule enteroscopy in comparison with computed tomography enteroclysis. Endoscopy 2003;35: Voderholzer WA, Beinhoelzl J, Rogalla P, et al. Small bowel involvement in Crohn s disease: a prospective comparison of wireless capsule endoscopy and computed tomography enteroclysis. Gut 2005; 54: Chong AKH, Taylor A, Miller A, et al. Capsule endoscopy vs. push enteroscopy and enteroclysis in suspected small-bowel Crohn s disease. Gastrointest Endosc 2005;61: Goldstein JL, Eisen GM, Lewis B, et al. Video capsule endoscopy to prospectively assess small bowel injury with celecoxib, naproxen plus omeprazole, and placebo. Clin Gastroenterol Hepatol 2005;3: Marmo R, Rotondano G, Piscopo R, et al. Capsule endoscopy versus enteroclysis in the detection of small-bowel involvement in Crohn s disease: a prospective trial. Clin Gastroenterol Hepatol 2005;3: Solem CA, Loftus EV, Fletcher JG, et al. Small bowel (SB) imaging in Crohn s disease (CD): a prospective, blinded, 4-way comparison trial [abstract]. Gastroenterology 2005;128(Suppl):A Dubcenco E, Jeejeebhoy KN, Petroniene R, et al. Capsule endoscopy findings in patients with established and suspected small-bowel Crohn s disease: correlation with radiologic, endoscopic, and histologic findings. Gastrointest Endosc 2005;62:
18 28. Yousfi MM, De Petris G, Leighton JA, et al. Diaphragm disease after use of nonsteroidal antiinflammatory agents: first report of diagnosis with capsule endoscopy. J Clin Gastroenterol 2004;38: Faigel DO, Fennerty MB. Cutting the cord for capsule endoscopy. Gastroenterology 2002;123: Cheifetz AS, Kornbluth AA, Legnani PE, et al. Incidence and outcome of the retained video capsule endoscope (CE) in Crohn s disease (CD) is it a therapeutic complication? [abstract]. Am J Gastroenterol 2004;99:S262. ECOENDOSCOPIA ED FNA ECOENDO-GUIDATO Vincenzo Napolitano INTRODUZIONE L ecoendoscopia, nota anche come endoultrasonografia (EUS), è una metodica di indagine che sfrutta le potenzialità diagnostiche degli ultrasuoni per esplorare distretti e strutture difficili da esaminare (come il pancreas) o addirittura irraggiungibili (come il mediastino) con l ecografia convenzionale transcutanea. In sostanza, utilizzando l endoscopia come veicolo, la scansione ultrasonografica viene effettuata dall interno del lume intestinale (esofago, stomaco, duodeno, retto, colon). Ciò comporta due vantaggi fondamentali: il primo è che si evitano gli ostacoli al passaggio degli ultrasuoni costituiti dallo spessore della parete toracica o addominale, dal gas intestinale e dall aria contenuta dai polmoni; il secondo è che la vicinanza della sonda con le strutture anatomiche da esplorare, consente di utilizzare frequenze molto più elevate rispetto all ecografia convenzionale, con un notevole incremento del potere di risoluzione. E importante, quindi, sottolineare che l ecoendoscopia è a tutti gli effetti un indagine ecografica, condotta con il supporto della tecnica endoscopica. L ecoendoscopia nasce all inizio degli anni 80 dello scorso secolo, con la creazione dei primi, rudimentali prototipi di strumenti, derivati dall assemblaggio di una sonda ecografica miniaturizzata ad un endoscopio a fibre ottiche. A causa dell inadeguatezza delle apparecchiature disponibili, però, l ecoendoscopia ha vissuto una lunga fase pionieristica in cui è rimasta appannaggio di pochissimi centri distribuiti tra Giappone, Europa ed USA, cui si deve il merito di aver testato le potenzialità
19 diagnostiche ed i possibile campi di applicazione della metodica, cominciando a delineare l anatomia ecografica trans-viscerale. Solo a partire dai primi anni 90 l ecoendoscopia, a seguito del moltiplicarsi delle esperienze, rese possibili anche dalla disponibilità di strumenti finalmente più maneggevoli e quindi più idonei ad un uso routinario, ha cominciato ad assumere un ruolo definito nella pratica clinica. Ulteriori, continui sviluppi in campo tecnologico, con l introduzione in commercio di strumenti sempre più sofisticati, con caratteristiche e potenzialità di impiego diverse gli uni dagli altri, hanno consentito poi, negli anni più recenti, di ampliare te le applicazioni cliniche dell EUS, che costituisce, oggi, una tra le tecniche endoscopiche più importanti. LE STRUTTURE ANATOMICHE ESPLORABILI CON L ECOENDOSCOPIA La prima struttura esplorabile per mezzo ecoendoscopia è costituita dalla parete gastrointestinale, di cui L EUS è in grado di fornire una rappresentazione molto precisa e dettagliata, impossibile da ottenersi con altre metodiche di indagine. Utilizzando la frequenza di 7,5 MHz l imaging ecografico della parete gastrointestinale, appare costituito da cinque strati concentrici, alternativamente iper ed ipoecogeni a mano a mano che si procede dall interno verso l esterno del lume. Questa alternanza di strati è il prodotto del differente grado di assorbimento degli ultrasuoni da parte dei tessuti che compongono la parete e dell interfaccia tra di essi. Il dato veramente importante, però, è che per i diversi strati ecografici è stata dimostrata con studi in vitro una corrispondenza, se pur grossolana, con gli strati anatomici. In particolare i primi due strati interni, rispettivamente iper ed ipoecogeno corrispondono alla mucosa, il terzo strato iperecogeno alla sottomucosa, il quarto strato ipoecogeno alla muscolare propria ed infine il quinto strato iperecogeno alla sierosa.(figura 1). Ciò è valido sia per l esofago che per lo stomaco e per il retto, anche se qualche differenza può riscontrarsi in rapporto allo spessore della parete, variabile in corrispondenza dei diversi visceri. A livello dell esofago, per esempio, la cui parete è molto sottile, spesso si identificano solo 3 strati in quanto la mucosa e la sottomucosa possono risultare non distinguibili. Al contrario, a livello della parete gastrica il quarto strato, che rappresenta la muscolare propria, può apparire distinto in due sottostrati, corrispondenti alla componente circolare e longitudinale della muscolare stessa, divisi da una sottilissima banda iperecogena. Oltre alla parete gastrointestinale, l ecoendoscopia consente di valutare gli organi e le strutture circostanti, entro il limite consentito dalle frequenze utilizzate, la cui gamma, con gli strumenti attualmente disponibili, può variare da 5 a 20 MHz. Con la frequenza di 7,5 MHz, che può essere considerata quella standard per l ecoendoscopia, la massima profondità di penetrazione degli ultrasuoni è di circa 10 cm con una distanza focale (dove la risoluzione risulta ottimale) di circa 3 cm. Pertanto, attraverso l esofago sarà possibile valutare adeguatamente tutte le strutture localizzate nel mediastino posteriore, in particolare l aorta toracica, la vena azygos, le arterie polmonari oltre che le diverse stazioni linfonodali (Fig. 2); dallo stomaco procedendo dal fondo verso l antro, sarà possibile, tra l altro, visualizzare la milza, il surrene di sinistra, il tripode celiaco, la coda ed il corpo del pancreas fino alla regione istmica, i vasi splenici fino alla confluenza portale, il fegato di sinistra, la colecisti (Fig. 3); dal lume duodenale, ancora la colecisti, la testa del pancreas, la via biliare extraepatica, compresa la regione papillare e, parzialmente, il fegato di destra. Ovviamente, tenendo presente che incrementando il potere di risoluzione si riduce parallelamente la profondità di penetrazione degli ultrasuoni, si comprende come, utilizzando frequenze più elevate, per esempio 20MHz, si otterrà una rappresentazione ancora più magnificata della parete, in cui si potranno identificare addirittura 9 strati, ma risulterà impossibile visualizzare strutture localizzate subito all esterno di essa. L impiego di questo tipo di frequenze, infatti, come si dirà successivamente, è destinato allo studio delle lesioni di parete più superficiali. GLI STRUMENTI Le apparecchiature ecoendoscopiche hanno subito negli anni una notevole evoluzione tecnologica, che dura tuttora. Attualmente vi è in commercio un ampia gamma di strumenti con caratteristiche differenti, per rispondere alle esigenze di una diagnostica sempre più sofisticata, oltre che delle
20 emergenti applicazioni di carattere operativo dell ecoendoscopia. Gli strumenti possono essere distinti in due categorie fondamentali: ecoendoscopi dedicati e sonde cieche. Gli ecoendoscopi dedicati, all apparenza, sono molto simili ad un endoscopio flessibile, con le relative funzioni, nella cui estremità distale è incorporato un trasduttore ad ultrasuoni (Fig. 4). Gli ecoendoscopi dedicati si distinguono a loro volta in due fondamentali categorie: strumenti a scansione radiale e strumenti a scansione lineare. Il piano di scansione ecografica risulta perpendicolare nei primi e parallelo nei secondi, rispetto all asse lungo dello strumento. Gli ecoendoscopi a scansione radiale prodotti dalla Olympus, per circa un decennio, hanno rappresentato l unica strumentazione disponibile e, successivamente, con versioni sempre più aggiornate, il tipo di apparecchiatura più diffusa. Utilizzano un trasduttore meccanico rotante a 360, immerso in un bagno di olio e contenuto in un cappuccio di materiale plastico (Fig. 5). Il trasduttore è attivato da un motore che, nei modelli più datati, era posizionato sull impugnatura dello strumento, che. per questo motivo, risultata particolarmente pesante e poco maneggevole. Nelle versioni più recenti l apparato motore è stato trasferito al cavo di connessione tra lo strumento e l ecoprocessore, alleggerendo l impugnatura, che è del tutto simile a quella dei normali endoscopi, tranne che per l aggiunta dei pulsanti che comandano le funzioni ecografiche (Fig. 6). La presenza del trasduttore in posizione distale fa sì che la visione endoscopica con questi strumenti non sia frontale, ma obliqua, con una angolazione più o meno accentuata in rapporto all ingombro della sonda ecografica che, comunque, nelle versioni più aggiornate, risulta notevolmente ridotto. I primi strumenti introdotti in commercio erano dotati di una singola frequenza di lavoro di 7.5 MHz. Quindi sono stati prodotti ecoendoscopi con possibilità di utilizzo di una doppia frequenza (principalmente 7.5 e 12 MHz). Attualmente sono commercializzati strumenti multifrequenza di 5, e 20 MHz. La scansione radiale, che consente di ottenere un imaging ecografico a 360 di tutte le strutture che, ad ogni dato livello, sono comprese in un piano assiale circostante la sonda, costituisce la modalità ideale per una valutazione di insieme, oltre che per semplificare l orientamento e per rendere più agevole la comprensione dell anatomia ecoendoscopica. Gli ecoendoscopi a scansione radiale rappresentano, in effetti, gli strumenti standard per l ecoendoscopia diagnostica. Del tutto recentemente, accanto agli strumenti radiali con trasduttore meccanico rotante, sono stati introdotti in commercio, ad opera di diverse industrie (Olympus, Fujinon, Pentax), modelli di eco endoscopi elettronici a scansione radiale nei quali il trasduttore ad ultrasuoni è disposto a costituire una sorta di anello sulla parte più distale dello strumento (fig 7). A parte alcuni particolari tecnici, come l angolo di visione endoscopica (frontale o lievemente obliquo) e lievi differenze nel calibro degli strumenti, i diversi modelli presentano caratteristiche molto simili. In particolare sono in grado di fornire una scansione radiale a 360 di elevata qualità, propria dell imaging elettronico e sono dotati delle funzioni doppler (color, power, doppler pulsato), come gli strumenti elettronici lineari, descritti di seguito. Si deve alla Pentax, nel 1991 la produzione del primo ecoendoscopio lineare elettronico, che ha avuto poi nel tempo numerose evoluzioni, seguita poi dalla Olympus e, del tutto recentemente, dalla Fujinon. Restando sui principi generali, senza addentrarci in dettagli tecnici, tutti questi strumenti sono dotati di un trasduttore elettronico tipo convex che produce un piano di scansione parallelo all asse dello strumento e quindi delle immagini settoriali (Fig. 8). Ne consegue che l orientamento risulta molto meno agevole e la possibilità di ottenere una valutazione diagnostica di insieme piuttosto problematica, oltre a richiedere un tempo molto più lungo. Il vantaggio di questi apparecchi, però, è costituito dal fatto che, se non introduciamo nel canale operativo dello strumento un ago, potremo seguirne agevolmente il tragitto, che verrà a cadere sempre nell ambito del piano di scansione ecografica (Fig. 9)). L impiego degli ecoendoscopi a scansione lineare è stato, pertanto, prevalentemente destinato all effettuazione dell ago aspirato sotto guida ecoendoscopica, procedura che ha trovato una sempre più ampia diffusione e che viene attualmente effettuata di routine in tutti i centri in cui si pratichi una diagnostica ecoendoscopica avanzata. Si tratta ovviamente di una metodica che richiede uno specifico training ed un adeguata esperienza. Alcuni strumenti sono dotati, come i duodenoscopi, di un elevatore che consente di modificare l angolo di uscita dell ago per meglio
21 orientarlo sulla lesione bersaglio da campionare. Attualmente, in rapporto ai potenziali sviluppi dell ecoendoscopia anche in campo terapeutico, sono presenti in commercio anche ecoendoscopi a scansione lineare con ampio canale operativo (fino a 3.8 mm), che consentono il transito non solo dagli aghi, ma anche di altri devices come delle protesi (Fig. 10). Ulteriore vantaggio degli ecoendoscopi elettronici a scansione lineare è la disponibilità del segnale doppler che permette di identificare agevolmente i vasi arteriosi e venosi così da rendere più sicura la procedura dell ago aspirato. Anche con tali strumenti la visione endoscopica è obliqua e ciò rende necessaria, ancora di più che con gli strumenti a scansione radiale, una particolare perizia ed una particolare attenzione nell effettuazione delle diverse manovre nel corso dell indagine, dall introduzione dello strumento, al passaggio del piloro, all approccio alle seconda porzione duodenale. Il calibro abbastanza considerevole (dai 13 ai 14 mm) e la lunghezza (in particolare in alcuni modelli) del tratto rigido distale dello strumento, non visibile endoscopicamente, costituisce, infatti, causa di difficoltà. La fonte degli ultrasuoni è costituita, a seconda delle industrie produttrici, da un ecoprocessore dedicato o da ecotomografi convenzionali compatibili. Le stesse fonti sono in grado di supportare anche i nuovi strumenti elettronici radiali. SONDE CIECHE Oltre agli eco endoscopi dedicati, lo strumentario per la diagnostica endosonografica comprende anche sonde ecografiche non dotate di visione endoscopica e che presentano caratteristiche che le rendono particolarmente adatte a specifiche forme di impiego. Nell ambito di questa categoria di strumenti, quelli che hanno trovato la più ampia applicazione e la maggiore diffusione, sono le cosiddette minisonde. Si tratta di lunghi sondini di pochi millimetri di calibro, tanto da poter transitare agevolmente attraverso il canale operativo di un endoscopio standard, nella cui estremità è contenuto un trasduttore ad ultrasuoni, generalmente di tipo meccanico rotante. La minisonda è collegata ad uno specifico apparato motore, che gestisce la rotazione del trasduttore e, attraverso tale apparato, ad un ecoprocessore. Introdotte in commercio circa a metà degli anni 90 e diffusesi, all inizio, soprattutto in Giappone, nel corso degli anni anche le minisonde hanno subito una notevole evoluzione tecnologica. Oggi sono disponibili molti modelli prodotti da diverse industrie (Olympus, Aloka, Fujinon), con frequenze che possono spaziare da 7.5 fino a 30 MHz (ciascun tipo di minisonda è dotata di una singola frequenza di lavoro). Particolarmente ampia è la gamma di tali strumenti prodotta dall Olympus, che comprende anche minisonde che possono essere filoguidate e quindi introdotte nella via biliare o nel dotto pancreatico, realizzando quel particolare tipo di indagine definita IDUS (intraductal ultrasonography) (Fig. 11). Fanno parte di tale gamma anche minisonde a scansione elicoidale che, attraverso il sussidio di uno specifico software possono fornire delle imaging 3D. L impiego delle minisonde è destinato principalmente allo studio di piccole lesioni della parete gastrointestinale, che non possono essere identificate facilmente o studiate adeguatamente con gli ecoendoscopi dedicati. In tali casi, dopo aver evidenziato la lesione endoscopicamente la minisonda può essere indirizzata, sempre sotto visione, direttamente in prossimità della lesione stessa. Le minisonde di gran lunga più utilizzate sono quelle con elevate frequenze di lavoro (12 e 20 MHz). Ovviamente ciò comporta che, a fronte di un elevato potere di risoluzione, la penetrazione degli ultrasuoni è molto limitata. Pertanto, con tali strumenti non è possibile valutare le strutture circostanti la parete, in particolare i linfonodi regionali e quindi essi non possono essere considerati un alternativa agli ecoendoscopi dedicati. Le minisonde hanno una durata limitata, generalmente compresa tra i 50 ed i 100 esami e dipendente anche dalla sede anatomica in cui vengono più frequentemente impiegate. L usura, oltre che la possibilità di rottura della minisonda, sarà maggiore nel duodeno o nel colon, quando l endoscopio sarà soggetto a multiple angolature piuttosto che nell esofago, dove l asse dell endoscopio, e quindi della stessa minisonda, risulta generalmente rettilineo. GLI AGHI PER FNA ECOENDOGUIDATO
22 Gli aghi per l FNA ecoendoguidato sono specificamente destinati a tale tipo di impiego ed hanno quindi delle peculiari caratteristiche. Anche relativamente a questo tipo di accessorio, sono oggi disponibili numerosi modelli, sia monouso che multiuso. Gli aghi per FNA- EUS guidato sono, in realtà, dei devices formati da diversi componenti (fig. 12), in particolare: 1) l impugnatura, mobile, con cui viene comandata dall esterno la fuoriuscita dell ago e può anche essere gestito il movimento della guaina la cui estremità, prima di ogni procedura, deve essere posizionata alcuni mm al di fuori del canale operativo dello strumento; ciò per evitare che nella fase di estrusione lo stesso ago possa danneggiare l ecoendoscopio. Nei modelli più recenti la corsa dello stantuffo mobile con cui si determina la fuoriuscita, dell ago può essere regolata con un sistema a vite di blocco, in modo da poter predefinire quale sarà la massima penetrazione dell ago stesso nei tessuti, in rapporto alla distanza della lesione bersaglio dal trasduttore. Con tale accorgimento, durante l esecuzione della puntura, si eviterà di andare oltre la lesione raggiungendo accidentalmente strutture adiacenti, in particolare vasi, con conseguente rischio di complicanze. L impugnatura viene connessa all imbocco del canale operativo dello strumento con un meccanismo luer-locked in modo da solidarizzare l ago con l ecoendoscopio.- 2) la guaina, all interno della quale scorre l ago, ha la triplice funzione di assicurare al sistema la giusta rigidità e, al tempo stesso, la sufficiente flessibilità, oltre a proteggere il canale operativo da possibili danni. Le guaine possono essere un materiale plastico o metallico a struttura spiraliforme. Questo ultimo tipo si fa preferire per la maggiore flessibilità, fondamentale soprattutto quando la puntura deve essere effettuata a strumento non rettilineo. La guaina e l impugnatura rappresentano le parti riutilizzabili dei sistemi pluriuso. 3) L ago vero e proprio. Gli aghi sono disponibili in 3 misure:19, 22 e 25 G. Gli aghi da 22G sono quelli più largamente impiegati, in quanto assicurano una buona penetrazione, scarso rischio di complicanze, adeguatezza del campione, con la possibilità di ottenere micro biopsie. L utilizzazione degli aghi di differente calibro è indicata in particolari situazioni. Per esempio gli aghi da 25G, che sono senza dubbio i meno traumatici, possono essere impiegati per il prelievo da linfonodi allo scopo di ridurre il materiale ematico. Gli aghi da 19 G possono risultare utili in caso di lesioni molto compatte, come i tumori mesenchimali, anche se non è dimostrato che il maggiore calibro dell ago migliori la qualità del campione, o per aspirare lesioni cistiche a contenuto particolarmente denso. All interno dell ago è sempre presente un mandrino che ha la funzione di migliorarne la rigidità durante la puntura e di evitare che lo stesso ago raccolga lungo il suo percorso materiale e cellule estranee all area da campionare. E evidente che una volta raggiunta la lesione bersaglio il mandrino deve essere estratto per effettuare l espirazione.. 4) Il sistema di aspirazione, costituito da una siringa in cui si sia predeterminato il vuoto e connessa ad un rubinetto che viene aperto dopo aver agganciato il sistema all ago. In tal modo la pressione negativa si trasmette all ago determinando il meccanismo di aspirazione. E importante chiudere il rubinetto prima di estrarre l estremità dell ago dalla lesione per evitare di aspirare, nella fase di ritiro, materiale che può inquinare il campione. Per concludere il discorso sugli aghi, un breve cenno all ago per biopsia (tru-cut). Tale accessorio consente di effettuare un prelievo istologico ottenendo, con un sistema a ghigliottina del tutto simile ai sistemi analoghi utilizzati anche in ecografica convenzionale, una piccola carota di tessuto. Per il calibro e le caratteristiche di tale ago la procedura di prelievo risulta molto più complessa e con un maggior rischio di complicanze. CENNI SULLA PROCEDURA La procedura dell ecoendoscopia, sia relativamente alla preparazione del paziente, che alla tecnica di esecuzione dell indagine, in linea di massima, non si discosta da quella prevista per gli esami endoscopici effettuati in sedo-analgesia. Per tale motivo in questo paragrafo ci si soffermerà in particolare sulle caratteristiche specifiche della procedura dell ecoendoscopia.
23 E opportuno distinguere l ecoendoscopia del tratto digestivo superiore da quella colo-rettale. Ecoendoscopia del tratto digestivo superiore: L indagine viene di norma eseguita in sedo-analgesia, utilizzando la classica associazione di un oppiaceo (e.g. meperidina) e di una benzodiazepina (e.g. midazolam), non perché l esame provochi un maggior discomfort per il paziente rispetto alla semplice EGDS, ma perché richiede un tempo di esecuzione piuttosto lungo (mediamente compreso tra i 15 ed i 30 ). Le indagini diagnostiche preliminari richieste al paziente saranno, pertanto, le stesse previste per un endoscopia diagnostica condotta in sedo-analgesia. Allo stesso modo, in caso di ecoendoscopia associata ad FNA, la preparazione sarà quella utilizzata per gli esami endoscopici operativi. Molti operatori, però, preferiscono effettuare la manovra della puntura utilizzando la sedazione profonda con Propofol, che richiede un regime di ricovero almeno in DH e la consulenza e l assistenza dell anestesista. Va sottolineata l opportunità, prima di effettuare l indagine, di raccogliere un consenso informato specifico per l ecoendoscopia. Relativamente alla tecnica di indagine, il paziente, come per l EGDS, viene posizionato di norma in decubito laterale sinistro con la testa flessa sul collo. Nella fase di introduzione dello strumento, per le caratteristiche strutturali degli ecoendoscopi, descritte nel relativo paragrafo, è necessaria una particolare cautela. E preferibile, anche se non costituisce una regola fissa, dare inizio all esplorazione ultrasonografica dopo essersi posizionati distalmente rispetto all organo da esaminare, effettuando le scansioni ecografiche a mano a mano che l apparecchio viene progressivamente ritirato. Per poter ottenere un buon imaging è necessaria un adeguata finestra acustica. Bisogna quindi aspirare tutta l aria contenuta nel viscere ed introdurre un mezzo idoneo al passaggio degli ultrasuoni rappresentato, nel caso dell ecoendoscopia, dall acqua. Per l esplorazione di visceri a lume tubulare, come l esofago o il duodeno, l acqua viene instillata in un palloncino di lattice applicato sulla sonda, che deve essere gonfiato fino ad ottenere un adeguato contatto con la parete, senza esercitare, però, un eccessiva compressione. Nel caso di visceri ad ampio lume, come lo stomaco, l acqua viene introdotta direttamente nel lume, possibilmente con l ausilio di una pompa a portata costante, così da evitare vortici e formazione di microbolle di aria (Fig. 13). Generalmente ml di acqua sono sufficienti per ottenere una buona distensione della parete, così da consentirne un adeguata valutazione. L impiego di quantità maggiori di acqua di norma non risulta necessario è può, anzi, incrementare il rischio di una ab ingestis. E ovvio che tali indicazioni sono valide in linea di principio, perché in molte situazioni può essere utile utilizzare le due tecniche in maniera combinata. In ogni caso è necessaria un estrema cautela nell introdurre acqua libera nel lume dell esofago dove un rischio di una ab ingestis è particolarmente accentuato. L acqua libera va aspirata dal lume prima di procedere alla valutazione delle strutture esterne alla parete gastrica, alfine di ridurne la distanza dal trasduttore. Per lo studio degli organi circostanti la parete gastrointestinale è necessaria la conoscenza dell anatomia ecoendoscopica, in particolare bisogna essere in grado di identificare alcuni reperi anatomici, fondamentali per un corretto ed adeguato orientamento. Il più importante di tali reperi è costituito dall aorta, sia nel mediastino, che in addome. Ovviamente, se si utilizza uno strumento radiale, il vaso, in sede mediastinica e sottodiaframmatica, a livello dell emergenza dell arteria celiaca, verrà visualizzato in sezione trasversale. Se si utilizza, invece, uno strumento lineare, si otterrà una sezione longitudinale dell aorta. (Fig. 14) L ecoendoscopia colorettale Per quanto riguarda l endosonografia del colon, destinata principalmente allo studio delle lesioni precoci mediante l impiego delle minisonde in corso di colonscopia, la procedura non presenta elementi di specificità rispetto all esame endoscopico. Per quanto riguarda l endosonografia del retto (si preferisce usare questo termine in luogo di ecoendoscopia in quanto l ecografia trans rettale viene realizzata anche con sonde rigide dedicate), si tratta di un indagine poco fastidiosa per il paziente e, di norma, ben tollerata. Per tale motivo, se non in casi del tutto particolari, non è richiesta la sedo
24 analgesia. Essendo generalmente l indagine limitata al retto, per la preparazione intestinale viene generalmente considerato sufficiente far praticare al paziente dei clisteri, anche utilizzando dei clismi pronti. Anche nel caso della ecoendoscopia del retto è necessaria un adeguata conoscenza dell anatomia ecografica della pelvi, sia per consentire il corretto orientamento, sia per descrivere i rapporti di eventuali lesioni della parete con le strutture circostanti. Quando l indagine venga condotta per la valutazione di lesioni neoplastiche del retto, è opportuno cominciare l esame, quando possibile, dalla giunzione retto sigmoidea per visualizzare i vasi ipogastrici e valutare eventuali linfonodi presenti a tale livello. L FNA ecoendo guidato Si tratta di una procedura che viene ormai eseguita routinariamente in molti centri di ecoendoscopia e che consente di migliorare l eccuratezza diagnostica della metodica, attraverso il prelievo di materiale per una valutazione citologica o anche istologica, quando si riescono a campionare microfrustoli di tessuto. Si è già parlato degli strumenti e degli accessori, in particolare gli aghi, necessari per effettuare tale manovra. Per quanto riguarda la tecnica di indagine, il primo tempo consiste nel ricercare la posizione ottimale per effettuare la puntura. A tale scopo è opportuno far sì che la lesione bersaglio venga a trovarsi al centro dell immagine, alla distanza più breve possibile dal trasduttore. E importante accertarsi preventivamente che lungo il prevedibile percorso che l ago dovrà fare per raggiungere la lesione, non si frappongano dei vasi sanguigni. A tal proposito risulta molto utile il ricorso alle funzioni doppler. Può essere altresì utile misurare la distanza tra il trasduttore ed il margine distale della lesione per predeterminare, quando il modello di ago lo consenta, la lunghezza massima di fuoriuscita dell ago stesso. Una volta completate queste manovre e dopo aver cercato di visualizzare ecograficamente la parte distale della guaina, accertandosi che protruda di qualche mm dal canale operativo dello strumento, si potrà procedere alla puntura. La puntura può essere effettuata con lo stiletto completamente inserito nell ago, oppure si può ritirarlo di qualche mm al momento di pungere, per aumentare la forza di penetrazione dell ago. In tal caso, però, una volta entrati nella lesione bisognerà spingere nuovamente lo stiletto per pulire l ago da eventuali cellule di parete raccolte durante il tragitto. A questo punto si rimuoverà lo stiletto, si avviterà sull ago la siringa sotto vuoto e si aprirà il rubinetto, attivando l aspirazione. Si effettueranno, quindi, numerosi movimenti di va e vieni dell ago all interno della lesione, variando di tanto in tanto l angolo di penetrazione, così da campionare aree diverse. Completato il campionamento, con un movimento rapido si ritirerà l ago nella guaina, non prima di aver richiuso il rubinetto. Sfilato l ago dallo strumento, si passerà infine al trattamento del materiale campionato, valutandone innanzitutto la congruità per stabilire l eventuale necessità di ulteriori passaggi. Per tale valutazione, come per la corretta preparazione ed il fissaggio del materiale, può risultare molto utile la presenza del citopatologo in sala, sia per migliorare significativamente l accuratezza diagnostica (i campionamenti inadeguati si riducono almeno del 20-30%), sia per ridurre il numero di passaggi, con una parallela riduzione di rischio. L FNA ecoendo guidato, se eseguito da un operatore con un adeguato training, costituisce una procedura efficace e con un tasso di complicanze molto basso. Esistono, comunque differenti gradi di difficoltà della tecnica, in rapporto alla sede ed alle caratteristiche delle lesioni da campionare. Le lesioni può semplici da pungere sono considerate le grosse masse mediastiniche, a difficoltà intermedia viene considerata la puntura delle lesioni pancreatiche. Le maggiori difficoltà sono correlate, infine, alla puntura delle neoformazioni intraparietali gastriche di natura stromale. Le possibili complicanze consistono nell emorragia e nell infezione. Il rischio di infezione riguarda in particolare la puntura delle lesioni cistiche del pancreas e delle lesioni perirettali. E raccomandato in tali casi far eseguire ai pazienti una profilassi antibiotica. LE APPLICAZIONI CLINICHE DELL ECOENDOSCOPIA
25 A conclusione di questo capitolo, ci soffermeremo brevemente sulle principali applicazioni cliniche dell ecoendoscopia. L indicazione clinica forse più nota, oltre che la prima ad essere stata proposta, riguarda la stadiazione loco regionale delle neoplasie della parete gastrointestinale. E stato già detto che l ecoendoscopia consente di identificare, nell ambito della parete gastrointestinale, degli strati che corrispondono abbastanza fedelmente a quelli anatomici. Da ciò scaturisce la possibilità di determinare con precisione la profondità di infiltrazione parietale del tumore (T), che appare come una massa ipoecogena disomogenea (Fig. 15), in rapporto al numero degli strati parietali che risultano interrotti e/o distrutti dalla neoplasia, ottenendo una stadiazione ultrasonografica direttamente comparabile con quella TNM (Fig. 16). L accuratezza per la stadiazione T, secondo i dati della letteratura, è compresa tra l 80 ed il 90%). L ecoendoscopia risulta anche molto efficace nella valutazione del parametro N (accuratezza compresa tra il 70 e l 80%), sia per l elevato potere di risoluzione, che consente di identificare i linfonodi fino a dimensioni minime di 3 mm, sia per la possibilità di ipotizzarne, sulla base delle caratteristiche dell ecotessitura, la natura benigna o maligna (Fig. 17). L impiego dell FNA può ulteriormente migliorare l accuratezza (fino ad oltre il 90%) per la diagnosi di metastasi linfonodali. A parte l accuratezza diagnostica, l importanza dell ecoendoscopia risiede nel suo elevato impatto clinico, cioè nella possibilità di determinare la modifica della strategia terapeutica in rapporto alla situazione del singolo paziente. Recentemente, con la diffusione delle tecniche di resezione endoscopica (mucosectomia, dissezione sottomucosa), si sta registrando un notevole interesse per le neoplasie in stadio early che, quando confinate alla sola mucosa, possono beneficiare di tali forme di trattamento. L endosonografia, con l impiego delle minisonde ad altra frequenza, si è dimostrata essere molto affidabile per un adeguata selezione dei pazienti. L ecoendoscopia ha contribuito in maniera determinante a migliorare la diagnosi delle lesioni sottomucose che vengono evidenziate, spesso incidentalmente, in corso di esami endoscopici, ma sulla cui natura la sola valutazione endoscopica non può fornire informazioni sufficienti. L ecoendoscopia, invece, oltre a discriminare con notevole precisione le compressioni ab estrinseco dalle vere lesioni sottomucose, può consentire di ottenere una diagnosi differenziale di queste ultime, attraverso l identificazione dello strato di origine e le caratteristiche dell ecotessitura. Particolarmente importante il ruolo che l ecoendoscopia nella diagnostica dei tumori mesenchimali della parete gastrointestinale, che appaiono generalmente come masse ipoecogene, originanti dal IV strato della parete (muscolare propria). Sulla base di un accurata valutazione dell imaging endoscopico, integrato, in alcuni casi con il ricorso all FNA, è, infatti, possibile differenziare i leiomiomi (Fig. 18) che sono quasi sempre benigni, da altra forme neoplasie mesenchimali, come i gastrointestinal stromal tumors, che possono avere un comportamento maligno e richiedono, pertanto un differente management. Una ulteriore applicazione dell ecoendoscopia riguarda la diagnosi, la stadiazione ed il follow up dei linfomi gastrici primitivi. Oltre alle patologie della parete gastrointestinale, l altro grande campo di applicazione dell ecoendoscopia, riguarda la patologia bilio pancreatica. Relativamente alla patologia delle vie biliari, la prima indicazione riguarda la diagnosi della micro litiasi, in cui l accuratezza della metodica risulta superiore non solo all ecografia convenzionale per via trans cutanea, ma anche alla stessa colangiormn (Fig. 19). Pertanto, l ecoendoscopia viene consigliata nei casi di calcolosi della colecisti con fondato sospetto clinico di calcolosi coledocica associata e colangiormn negativa, prima di effettuare una colecistectomia per via video laparoscopica. Inoltre, trova indicazione nei casi di pancreatite acuta idiopatica, la cui causa, in molti casi, è da ricercarsi in una microlitiasi misconosciuta. Un ulteriore impiego dell ecoendoscopia riguarda la diagnostica delle stenosi della via biliare e la stadiazione delle neoplasie del coledoco e della papilla di Vater. In tali casi può risultare utile il ricorso all ultrasonografia intraduttale con le minisonde filoguidate. L dea dell ecoendoscopia nacque inizialmente per migliorare lo studio del pancreas, spesso non esplorabile adeguatamente con l ecografia del convenzionale. Quindi, la patologia del pancreas ha
26 costituito da sempre uno dei principali settori di interesse dell ecoendoscopia che, a metà degli anni 90 dello scorso secolo era considerata la metodica singolarmente più accurata per la diagnosi e la stadiazione delle neoplasie solide del pancreas, che si presentano come delle masse ipoecogene a margini irregolari (Fig. 20). L attuale evoluzione delle tecniche di imaging radiologico, ha determinato un parziale ridimensionamento dell ecoendoscopia che rimane comunque essenziale per l identificazione dei piccoli tumori e per la diagnosi di un eventuale infiltrazione dell asse vascolare mesenterico-portale. L ecoendoscopia conserva, altresì, un posto centrale nell algoritmo diagnostico delle neoplasie del pancreas in funzione dell FNA ecoendoguidato, che costituisce la tecnica più sicura e più accurata per ottenete la tipizzazione istologica della lesione. Ancora più importante è il ruolo della metodica, spesso ancora in associazione all FNA, nella diagnosi differenziale dei tumori cistici, patologia emergente proprio per il grande contributo fornito dall ecoendoscopia al miglioramento delle conoscenze su queste lesioni, prima poco diagnosticate e poco considerate. Non va inoltre trascurata, tra le indicazioni dell ecoendoscopia, quella riguardante la diagnostica dei tumori neuroendocrini e, infine, le pancreatiti croniche, specialmente ad incerta eziologia. Un ultimo accenno va riservato all ecoendoscopia operativa che già oggi è una realtà. Alcune indicazioni, infatti, come il drenaggio delle pseudo cisti pancreatiche o la neorolisi del plesso celiaco per il trattamento del dolore pancreatico, sono ormai consolidate nella pratica clinica. Altre come i drenaggi biliari e/o pancreatici, con relativo posizionamento di protesi sotto guida eco endoscopica, in caso di fallimento delle altre tecniche di uso comune, sono in ia di definizione. Infine, sono in fase di sperimentazione diverse altre possibili applicazioni terapeutiche, la cui reale fattibilità dipende solo da ulteriori, ma prevedibili evoluzioni tecnologiche delle apparecchiature. BIBLIOGRAFIA 1. Di Magno EP, Buxton JL, Regan PT, Hattery RR, Wilson DA, Suarez JR et al.: Ultrasonic endoscope. Lancet 1980; 1: Caletti G, Bolondi L, Labò G.: Ultrasonic endoscopy: the gastrointestinal wall. Scand J of Gastroenterol 1984; 19 Suppl: Rosch T, Classen M.: A new ultrasound probe for endosonographic imaging of the upper GI tract. Endoscopy 1990; 22: Kimmey MB, Martin RW, Silverstein FE.: Clinical application of linear ultrasound probes. Endoscopy 1992; 24 Suppl 1: Klapman JB, Logrono R, Dye CE.: Clinical impact of on-site cytopathology interpretation on endoscopic ultrasound fine needle aspiration. Am J Gastroenterol 2003; 98: Fusaroli P, Caletti G.: Endoscopic ultrasonography. Endoscopy 2005; 37: Wiersema MJ, Vilmann P, Giovannini M, Chang KJ, Wiersema LM.: Endosonographyguided fine- needle aspiration biopsy: diagnostic accuracy and complication assessment. Gastroenterology 1997; 112: Murata Y, Suzuki S, Ohta M, Mitsunaga A, Kazuhiko H, Yoshida K et al.: Small ultrasonic probes for determination of the depth of superficial esophageal cancer. Gastrointest Endosc 1996; 44: Rosch T.: Endoscopic staging of esophageal cancer: a review of literature results. Gastrointest Endosc Clin North Am 1995; 5:
27 10. Wang HP.: Endoscopic ultrasound staging of gastric malignancy. Digestive Endoscopy 2004; 16 (Suppl,):S Murata Y, Napoleon B, Odegaard S.: High- frequency endoscopic ultrasonography in the evaluation of superficial esophageal cancer. Endoscopy 2003; 35: Ichikawa T, Kudo M, Matsui S, Okada M, Kitano M.: Endoscopic ultrasonography with three miniature probes of different frequencyis an accurate diagnostic tool forendoscopic submucosal dissection. Hepatogastroenterology 2007; 54: Caletti G, Fusaroli P, Togliani T.: EUS in MALT lymphoma. Gastrointest Endosc 2002; 56 (Suppl): S21-S Chak A.: EUS in submucosal tumors. Gastrointest Endosc 2002; 56 Suppl; S43-S Okubo K, Yamao K, Nakamura T, Tajika M, Sawaki A, Hara K et al.: Endoscopic ultrasoundguided fine-needle aspiration biopsy for the diagnosis of gastrointestinal stromal tumors in the stomach. J Gastroenterol 2004; 39: Polkowski m, Regula J, Tilszer A, Butruk E, Sotoudehmanesh R, Kolahdoozan S et al.: Endoscopic ultrasound versus endoscopic retrograde cholangiography for patients with intermediate probability of bile duct stones: a randomized trial comparing two management strategies. Endoscopy 2007; 39: Tandon M, Topazian M.: Endoscopic ultrasound in idiophatic acute pancreatitis. Am J Gastroenterol 2001; 96: Ahamad NA, Lewis JD, Ginsberg GG, Rosato EF, Morris JB, Kochman ML.: EUS in preoperative staging of pancreatic cancer. Gastrointest Endosc 2000; 52: Hunt GC, Faigel DO.: Assessment of EUS for diagnosing, staging, and determining respectability of pancreatic cancer: a review. Gatrointest Endosc 2002; 55: Yovino S, Darwin P, Daly B, Garofalo M, Moesinger R.: Predicting unresectability in pancreatic cancer patients: the additive effects of CT and endoscopic ultrasound. J Gastrointest Surg 2007;11: Mortensen MB, Edwin B, Hunerbein M, Liedman B, Nielsen HO, Hovendal C.: Impact of endoscopic ultrasonography (EUS) on surgical decision-making in upper gastrointestinal tract cancer: an international multicentric study. Surg. Endosc 2007; 21: Volmar KE, Vollmer RT, Jowell PS, Nelson RC, Xie HB.: Pancreatic FNA in 1000 cases: a comparison of imaging modalities. Gastrointest Endosc 2005; 61: Eloubeidi M, Tamhane A, Varadarajulu S.: Frequency of major complications after EUSguided FNA of solid pancreatic masses: a prospective evaluation. Gastrointest Endosc 2006; 63:
28 24. Brugge WR. The role of EUS in the diagnosis of cystic lesions of the pancreas. Gastrointest Endosc 2000; 52:S Fockens P.: EUS in drainage of pancreatic pseudocysts. Gatrointest Endosc 2002;56 (Suppl): S93-S Gunaratnam NT, Sarma AV, Norton ID, Wiersema MJ.: A prospective study on EUS-guided celiac plexus neurolysis for pancreatic cancer pain. Gastrointest Endosc 2001; 54: Sriram PVJ, Fritscher-Ravens A.: Interventional EUS: Future Perpesctives. Techniques in Gastrointestinal Endoscopy 2007; 9:
29 LE TECNICHE DI RESEZIONE ENDOSCOPICA Introduzione Negli ultimi anni la medicina si pone sempre più l obiettivo di prevenire più che di curare la malattia o, almeno, di giungere ad una diagnosi quanto più precoce possibile in modo da poter utilizzare trattamenti sempre meno invasivi e meno invalidanti per i pazienti. Questa trattazione sarà incentrata proprio su quelle nuove tecniche endoscopiche che stanno assumendo un ruolo fondamentale nella diagnosi e nel trattamento delle lesioni pre-neoplastiche e delle neoplasie precoci del tubo digerente. La applicazioni dell endoscopia, prima nella diagnosi e poi anche nella terapia di queste lesioni è dovuta principalmente alle ricerche svolte nei paesi orientali, soprattutto in Giappone. In questi paesi, infatti, alcune neoplasie gastrointestinali, come il cancro dello stomaco o dell esofago, in rapporto a fattori razziali ma, soprattutto a fattori ambientali, specialmente le abitudini di carattere alimentare, rivestono carattere di endemicità. Per tale motivo sono stati organizzati dei programmi di screening di massa allo scopo di favorire la prevenzione secondaria o la diagnosi precoce di queste neoplasie e quindi migliorare la prognosi dei pazienti. Ciò ha portato ad un affinamento delle tecniche di diagnosi, in particolare di quelle endoscopiche. Per meglio definire la problematica che ci apprestiamo a trattare ci riferiamo, a titolo di esempio, all evoluzione del cancro del colon retto. La principale e più accreditata teoria sullo sviluppo del cancro colorettale è la cosiddetta sequenza adenoma-carcinoma che prevede la trasformazione maligna a partire da una lesione adenomatosa attraverso alterazioni che determinano un aumento progressivo delle dimensioni, dei livelli di displasia e delle potenzialità invasive della lesione neoplastica. Fino agli anni 70 si riteneva che il precursore delle neoplasie del colo-retto fosse rappresentato unicamente da una lesione polipoide della mucosa, cioè da una formazione protrudente di conformazione sessile o peduncolata con caratteristiche istologiche di tipo adenomatoso, la cui evoluzione verso l adenocarcinoma, come è noto, richiede mediamente un periodo di tempo variabile tra i 5 ed i 7 anni. Alla fine degli anni 70 e durante gli anni 80, gli studiosi giapponesi dimostrarono, invece, che il cancro colo rettale, in un numero non del tutto trascurabile di casi, non derivava dall evoluzione di un polipo adenomatoso ma esordiva direttamente sotto forma di lesioni piatte o depresse, che potevano infiltrare gli strati della parete al di sotto della mucosa, già a partire da dimensioni di pochi millimetri. In seguito, grazie alla maggiore esperienza, allo sviluppo di nuove tecniche di diagnosi endoscopiche avanzate, che in seguito descriveremo brevemente, e di nuove apparecchiature che garantivano un maggiore potere risolutivo dell immagine endoscopica, gli autori giapponesi hanno riportato un incidenza sempre crescente di lesioni colo-rettali piatte e depresse, che è stata dimostrata attestarsi addirittura intorno al 40% di tutte le lesioni precoci. I miglioramenti nella diagnosi hanno fatto sì che in quei paesi, si sia registrato un sorprendente incremento delle neoplasie diagnosticate in fase molto precoce e, di conseguenza si è assistito allo sviluppo di tecniche terapeutiche di tipo endoscopico con l intento di ottenere un trattamento mini invasivo di tali lesioni, almeno in casi selezionati. Recentemente gli Autori occidentali, utilizzando le metodiche giapponesi, hanno dimostrato che le lesioni non polipoidi piatte e depresse rappresentano una realtà sempre più rilevante anche nella popolazione Occidentale. Per tali motivi le classificazioni endoscopiche delle neoplasie precoci gastrointestinali messe a punto dagli autori giapponesi sono state fatte proprie anche dagli europei. La tabella 1 illustra l ultimo aggiornamento di questa classificazione elaborato in occasione di una consensus conference tenutasi a Parigi e pubblicato nel Essa distingue lesioni polipoidi o protrudenti e lesioni non polipoidi o non protrudenti. Le prime sono
30 caratterizzate da altezza della lesione maggiore di un terzo del suo diametro, mentre le lesioni non polipoidi sono definite come qualsiasi irregolarità della mucosa con altezza inferiore a un terzo del diametro. Tabella 1 L importanza clinica di questa classificazione è data dalla possibilità di correlare la classificazione macroscopica con la profondità di infiltrazione, in particolare con il rischio di invasione sottomucosa, che è cruciale per la scelta della terapia. Infatti, l evoluzione di una lesione neoplastica del tubo digestivo passa da una fase non invasiva, limitata alla mucosa, ad una invasiva che coinvolge dapprima la sottomucosa per poi interessare gli altri strati della parete. La fase non invasiva compre le neoplasie intaepiteliali di basso e di alto grado, le neoplasie intraghiandolari confinate alla lamina propria e le neoplasie intramucose che superano la lamina propria ed infiltrano ma senza oltrepassare la muscolaris mucosae, il superamento di quest ultima con la progressiva infiltrazione dello strato sottomucoso rappresenta il punto di passaggio alla fase invasiva. I lavori scientifici dimostrano che le forme precoci, non invasive, non presentano metastasi linfonodali pertanto sono candidabili ad una resezione endoscopica, mentre le neoplasie con interessamento esteso della sottomucosa si accompagnano a metastasi linfonodali nel 6-12% per le neoplasie del colon retto, fino al 20% per le neoplasie dello stomaco e fino al 30% di quelle esofagee. Pertanto tali neoplasie, salve alcune eccezioni, richiedono una resezione chirurgica con dissezione linfonodale per un trattamento con intenti curativi. Nella fig. 1 viene illustrata la stadiazione delle neoplasie precoci riferita allo stomaco in relazione al rischio di metastasi linfonodali.
31 Ritornando alla classificazione di Parigi, le lesioni di tipo III non sono trattabili tramite resezione endoscopica, in quanto suggeriscono la presenza di invasione sottomucosa profonda. Le lesioni di tipo I e IIc comportano un rischio maggiore di invasione sottomucosa, rispetto alle lesioni IIa, IIb o di tipo misto. In queste lesioni, la valutazione istologica del campione ottenuto tramite resezione endoscopica, che rappresenta l ultimo step della diagnosi, stabilirà la profondità dell invasione e quindi potrà dire se la resezione avrà avuto un valore curativo. Ovviamente, prima di poter valutare ed eventualmente trattare una neoplasia precoce è necessario prima identificarla, predirne la natura e la profondità dell infiltrazione parietale; per fare ciò bisogna ricorrere ad alcune tecniche accessorie rappresentate dalla cromoendoscopia, dalla magnificazione di immagine e dall ecoendoscopia ad alta frequenza. LA CROMOENDOSCOPIA Per cromoendoscopia si intende l impiego di sostanze che, applicate sulla mucosa del canale digerente, rendono più visibile o meglio contrastate aree di alterazione morfo-strutturale della superficie in corso di esame endoscopico. (Fig. 2)
32 Queste sostanze appartengono a tre classi fondamentali: Coloranti vitali assorbiti dalle cellule per diffusione o assorbimento attivo ( liquido di Lugol, blu di metilene, cristal violetto ) Coloranti di contrasto non assorbiti dalle cellule, accentuano la topografia tissutale accumulandosi tra i solchi intercellulari e nelle fossette ghiandolari rendendo più visibile l architettura della mucosa ( indaco carminio e acido acetico ) Coloranti reattivi reagiscono alle modificazioni della secrezione acida e sono utili per l identificazione precoce del cancro gastrico e della infezione da H. pylori ( rosso Congo e rosso fenolo ). Questi coloranti vengono applicati sulla mucosa direttamente con una siringa connessa con il canale operativo dello strumento o mediante l impiego di cateteri spray. Le aree che usualmente è consigliabile colorare sono le aree di discromia ( pallore focale o eritema ), le aree di irregolarità della superficie mucosa ( rilevate o depresse ) e le aree in cui il pattern vascolare della mucosa appare interrotto. Il liquido di Lugol, utilizzato in concentrazione 0.1% - 3%, reagisce con il glicogeno dell epitelio squamoso non cheratinizzato. L epitelio squamoso esofageo normale si colora in marrone bruno intenso con aspetto a pelle di serpente mentre il Barrett, la displasia o il cancro precoce restano discolorati per la deplezione di glicogeno. Usato in passato per lo studio del Barrett, è oggi molto meno utilizzato per le reazioni sistemiche legate allo iodio. Il blu di metilene ( BM ) ( 0.5% - 1% ) viene captato attivamente dalle cellule cilindriche mucipare dei tessuti assorbenti come il piccolo intestino ed il colon. In questo tipo di colorazione è opportuno pre-applicare agenti mucolitici ( N-acetil-cisteina ) sull area di mucosa da colorare. Dopo circa 2 minuti dalla colorazione, le aree di metaplasia intestinale, displasia o cancro appaiono come aree a scarsa intensità cromatica o che si colorano in modo disomogeneo mentre la mucosa esofagea e gastrica normale rimane non colorata. Il blu di metilene è utilizzato nell esofago e nello stomaco per la diagnosi di metaplasia intestinale e per la ricerca di aree di displasia e cancro, mentre nel colon per la individuazione dei foci di cripte aberranti ( ACF ). Il cristal violetto è un colorante vitale captato dalle ghiandole del LieberKuhn e consente una precisa identificazione delle dimensioni e distribuzione spaziale delle cripte ( orifici ghiandolari ). Il suo impiego è riservato alle aree di sospetta infiltrazione neoplastica sottomucosa.
33 L indaco carminio ( IC ), impiegato a diluizioni di %, è un colorante blu di contrasto che accentua la microarchitettura mucosa riempiendo i solchi e le fossette ghiandolari, rendendo visibili i bordi e la forma della lesione. E il colorante di riferimento per la cromoendoscopia del colon e per la visualizzazione della distribuzione spaziale degli orifici ghiandolari ( pit pattern ). Rappresenta anche la sostanza di gran lunga più utilizzata per la colorazione preliminare delle lesioni da trattare con resezione endoscopica in quanto ne consente una precisa definizione dei margini. ALTA RISOLUZIONE E MAGNIFICAZIONE DELL IMMAGINE Per risoluzione ottica si intende la capacità di discriminare i dettagli della superficie mucosa, cioè la capacità di visualizzare distintamente come separati due oggetti che sono molto vicini. La risoluzione è una funzone della densità dei pixel ( maggiore è la densità dei pixel, maggiore è la risoluzione dell immagine ). I video endoscopi convenzionali hanno dei CCD ( charged-coupled devices ) con densità di pixel variabile tra e Gli apparecchi ad alta risoluzione hanno invece una densità di pixel che può giungere fino ad con notevole miglioramento della qualità dell immagine. Negli strumenti di nuova generazione, l alta risoluzione è combinata con la capacità di magnificazione ottica, cioè di ingrandire un immagine fino a 150 volte attraverso l impiego di un sistema di lenti mobili controllate dall operatore. Questi strumenti a magnificazione ottica, detti anche zoom, hanno il vantaggio di poter essere usati come endoscopi standard durante le indagini di routine senza attivare la capacità di zoom. Altri strumenti possono eseguire una magnificazione elettronica che consente una visualizzazione ancora più dettagliata della lesione. Il problema è che questi strumenti sono dedicati a tale metodica e quindi il loro uso deve essere mirato allo studio di lesioni già identificate e da sottoporre a specifica valutazione. La principale, potenziale applicazione della magnificazione di immagine, soprattutto in associazione con la cromo endoscopia, che consentire di esaltare ulteriormente i particolari della lesione, è rappresentata dalla identificazione precoce delle lesioni neoplastiche superficiali gastrointestinali Questa metodica consente una dettagliata visualizzazione della microstruttura superficiale della mucosa gastrointestinale determinata dalla disposizione spaziale degli orifizi delle cripte ghiandolari (pit pattern). La classificazione dei pit pattern è applicabile alle lesioni precoci, sia dell esofago che dello stomaco e del colon retto. La più nota di tali classificazioni, universalmente adottata per la caratterizzazione delle lesioni non polipoidi del colon-retto è quella di Kudo. Essa prevede 5 tipi di pit pattern con le seguenti caratteristiche (fig. 3 ): tipo I: orifizi ghiandolari rotondeggianti a distribuzione regolare, corrisponde alla mucosa normale o a lesioni di tipo iperplastico tipo II: pit stellati o a croce di dimensioni poco più grandi della norma, tipici di lesioni iperplastico/infiammatorie tipo IIIL: pit tubulari larghi o allungati, leggermente ricurvi o rotondeggianti, corrisponde a lesioni di tipo adenomatoso tipo IIIS: pit tubulari piccoli, tondeggianti o lievemente deformati, compatti e più piccoli della norma, può corrispondere ad una lesione adenomatosa o in alcuni casi a carcinomi di tipo depresso tipo IV: pit cerebriformi, tubulari larghi e tortuosi, caratteristico di lesioni adenomatose di tipo protrudente tipo V: pit irregolare per forma, disposizione e dimensioni o destrutturato, tipico dell adenocarcinoma
34 Il pit di tipo V in particolare è stato suddiviso in due gruppi, un tipo VI con pattern irregolare per forma, dimensione e disposizione ed un tipo VN non strutturato con assenza del pit pattern. In base a questa distinzione è stata proposta da Fujii una classificazione clinica del pit pattern che distingue: lesioni non neoplastiche: pit pattern I e II sec. Kudo lesioni neoplastiche non invasive: pit pattern IIIs, IIIL, IV e VI sec. Kudo lesioni neoplastiche invasive: pit pattern VN sec. Kudo La correlazione esistente tra morfologia dei pit pattern valutati con magnificazione endoscopica e reperto istologico è stata inequivocabilmente dimostrata da due importantissimi lavori di Kudo e Kato pubblicati nel Pertanto i dati disponibili fino ad oggi sembrano indicare con chiarezza una buona correlazione tra pattern magnificato e tipo istologico della lesione [4] [5] [6] e, come abbiamo visto nella classificazione proposta da Fuji, sembrano suggerire anche una correlazione tra le caratteristiche dei pit pattern e l infiltrazione parietale da parte della lesione. Va precisato, comunque, che i dati circa la capacità di differenziare le forme neoplastiche confinate alla mucosa o alla porzione più superficiale della sottomucosa, da quelle invasive attraverso lo studio dei pit pattern non sono ancora sufficienti. E noto, peraltro, che la definizione dell infiltrazione della sottomucosa è essenziale perché una resezione endoscopica possa avere un intento curativo. L Ecoendoscopia ad alta frequenza L unica metodica che ha la potenzialità di valutare direttamente il grado dell infiltrazione parietale è costituita dall ecografia endoscopica o eco endoscopia. L ecografia endoscopica è una combinazione di endoscopia ed ultrasuoni ad alta frequenza. Un piccolo trasduttore ultrasonico del diametro di mm è montato sulla punta di un endoscopio e può effettuare una scansione radiale, generando un immagine di
35 360 orientata perpendicolarmente all asse lungo dello strumento o una scansione lineare generando un immagine diretta parallelamente all asse lungo dell endoscopio. Il primo tipo di scansione ha il vantaggio di dare una migliore panoramica della parete intestinale e delle strutture adiacenti extraluminali, mentre il secondo permette soprattutto di eseguire procedure operative come ad esempio la puntura con ago sottile. Le frequenze utilizzate variano dai 5 MHz ai 20 MHz e dal momento che la frequenza utilizzata è inversamente proporzionale al potere di penetrazione del fascio ultrasonoro si deduce che basse frequenze permettono di visualizzare meglio le strutture extraluminali (linfonodi, organi adiacenti), mentre le alte frequenze consentono uno studio dettagliato della parete del viscere. Negli ecoendoscopi di ultima generazione la produzione degli ultrasuoni è elettronica, ciò ha permesso l utilizzo anche del color-doppler. Poiché gli organi cavi gastroenterici contengono aria, l accoppiamento acustico del trasduttore ecografico alla parete intestinale viene ottenuta attraverso l uso di un palloncino ripieno d acqua attorno alla punta dello strumento oppure attraverso l istillazione di acqua all interno dell organo cavo. L aspetto ecoendoscopico della parete dei visceri gastrointestinali utilizzando le frequenze più basse consiste in cinque strati distinti, alternati, iperecogeno e ipoecogeno, tale pattern parietale corrisponde approssimativamente agli strati istologici pertanto i due strati più interni (iperecogeno e ipoecogeno) rappresentano l interfaccia lume/mucosa superficiale e mucosa profonda/muscularis mucosae; il terzo strato, iperecogeno, corrisponde alla sottomucosa; il quarto, ipoecogeno, alla muscularis propria ed il quinto (iperecogeno) alla sierosa (dove presente) che tuttavia risulta mal distinguibile dal tessuto iperecogeno circostante. L utilizzo di alte frequenze (20-30 MHz) consente un maggior dettaglio della parete del viscere con l identificazione di 9 strati alternati iperecogeni/ipoecogeni, con la possibilità di riconoscere 3 sottostrati nella mucosa e di riconoscere anche la muscolaris mucosae, il cui superamento costituisce la discriminante per distinguere le lesioni non invasive da quelle invasive (Fig 4) La valutazione della stratificazione parietale, nel caso di una neoplasia del tubo digerente permette di definire precisamente quali e quanti strati sono interessati dall infiltrazione producendo una stadiazione del parametro T direttamente comparabile con quella anatomo patologica. Limitatamente al grado di infiltrazione parietale ed alla stadiazione delle neoplasie precoci vi è la possibilità di distinguere le lesioni
36 limitate alla mucosa (EUS-T1m), da quelle con infiltrazione della sottomucosa (EUS-T1sm). Gli ultimi sviluppi tecnologici hanno consentito inoltre la miniaturizzazione delle parti ecografiche con la produzione di minisonde che possono essere introdotte attraverso il canale operativo degli endoscopi tradizionali (fig 5). Le minisonde, che presentano frequenze dai 12 ai 30 MHz possono essere molto utili per lo studio delle neoplasie precoci anche perchè possono essere posizionate sotto visione endoscopica ad di sopra della lesione da analizzare senza determinare eccessiva compressione. LE TECNICHE TERAPEUTICHE Le tecniche endoscopiche che saranno descritte in seguito possono costituire un trattamento efficace e definitivo delle neoplasie precoci solo quando il rischio di diffusione della malattia al linfonodi sia trascurabile. Sempre gli autori giapponesi hanno dimostrato che se il tumore è confinato solo alla mucosa il rischio di metastasi linfonodali è vicino allo 0%, mentre se il tumore infiltra completamente anche la sottomucosa tale rischio si avvicina al 30% e quindi un trattamento endoscopico non è più sufficiente. Ritornando alle tecniche diagnostiche prima descritte, la cromo endoscopia e la magnificazione sono importanti per identificare le lesioni precoci, per valutare quelle più a rischio e per evidenziare le aree maggiormente sospette di degenerazione tumorale. Tali tecniche, però, non consentono di valutare l estensione in profondità della lesione, indispensabile, come è stato detto, per selezionare i pazienti che possono beneficiare di una terapia endoscopica. Questo ruolo spetta invece all ecoendoscopia, specialmente, ad alta frequenza che consente di escludere la presenza di un tumore invasivo e di identificare le lesioni confinate allo strato mucoso in una percentuale molto elevata di casi (compresa in letteratura tra l 80 ed il 90%). Pertanto, prima di procedere ad un intervento di resezione endoscopica dovrà sempre essere effettuata un ecoendoscopia. In ogni caso la successiva resezione endoscopica avrà innanzitutto un valore diagnostico offrendo alla valutazione dell anatomopatologo l intera lesione per la precisa definizione del livello dell infiltrazione e per decidere, quindi, se l intervento sarà stato curativo o meno.
37 LA MUSECTOMIA ENDOSCOPICA Introdotta a metà circa degli anni 90 in Giappone, la mucosectomia nasce come una metodica dedicata alla asportazione di neoplasie del tubo digerente localizzate negli stadi superficiali della parete gastrointestinale. Proprio agli inizi degli anni 90 il crescente uso dell endoscopia per lo screening di massa del cancro gastrico porta in Giappone alla diagnosi di un numero enorme di tumori gastrici in fase precoce (i cosiddetti early gastric cancer ), a bassissimo rischio di diffusione linfonodale, per i quali l intervento chirurgico poteva rappresentare un overtreatment mentre poteva essere indicata una asportazione endoscopica che consentisse la rimozione en-bloc o in pochi frammenti di tutta la lesione identificata. In questo contesto clinico nascono le differenti idee tecniche, i primi accessori e la prima definizione di EMR Endoscopic Mucosal Resection. La differenza sostanziale tra l EMR e la polipectomia classica, consiste nel fatto che mentre la polipectomia mira a rimuovere formazioni polipoidi rilevate rispetto al piano mucoso e quindi facilmente incarcerabili con un ansa da polpectomia, l EMR viene applicata a lesioni cosiddette piatte e/o comunque scarsamente rilevate sul piano mucoso e quindi non facilmente aggredibili con la semplice ansa diatermica. Inoltre nel caso dell EMR il concetto di rimozione mucosa si estende anche allo strato superficiale della sottomucosa al fine di poter ottenere un frammento di tessuto sul quale possa essere possibile esprimere un adeguata stadiazione locale di tipo oncologico. Infatti in questo contesto, la stratificazione della parete gastrointestinale è l elemento chiave per l applicazione di questa tecnica alle patologie neoplastiche superficiali. La marcatura della lesione Il primo step della procedura è la marcatura della lesione che serve a delimitare con precisione l area da resecare e deve rappresentare la guida dell endoscopista per l intera durata dell intervento endoscopico. La tecnica di marcatura è sostanzialmente identica in tutti i tratti dell apparato digerente e qualsiasi sia la morfologia e le dimensioni della lesione da asportare. Si può utilizzare la punta dell ansa diatermica o a sonda APC per produrre dei piccoli spot biancastri di coagulazione a circa 5 mm dal margine della lesione per tutta la sua circonferenza: questo consente di delimitare un area di resezione leggermente più grande della reale dimensione della lesione mucosa al fine di garantire la completa resezione. Fig 6 L infiltrazione sottomucosa
38 A proposito della iniezione i concetti più importanti da sottolineare sono: 1) dove iniettare, 2) quando iniettare, 3) cosa iniettare. Per il primo punto deve essere subito chiaro che la iniezione sottomucosa deve cominciare sempre dal punto più distale della lesione e non dal punto più vicino all endoscopio. Infatti in quest ultimo caso l iniezione determina un ribaltamento della lesione in una posizione che diventa più facile da visualizzare frontalmente con l endoscopio, difficile da iniettare ulteriormente sul versante più lontano e difficile da aggredire con l ansa o con gli altri accessori che si rendessero necessari per la resezione endoscopica. Una volta iniziata l iniezione dal punto più distale se il sollevamento avviene correttamente, ed è visibile ad occhio nudo il progressivo scollamento della mucosa rispetto ai piani sottostanti, si potrà procedere in direzione prossimale anche iniettando la zona centrale della lesione e quindi l area più vicina all endoscopio. Si raccomanda di far penetrare di 1-2 mm l ago, con un angolo di circa rispetto alla mucosa, in modo da raggiungere la sottomucosa senza andare troppo oltre. Fig 7 Se non dovesse verificarsi lo scollamento è probabile che la lesione infiltri profondamente la sottomucosa e sia quindi in uno stadio non più aggredibile per via endoscopica. Questo è quello che Kato ha definito qualche anno fa come il non lifting sign [28], la cui sensibilità e specificità si è dimostrata alta nell indicare una infiltrazione neoplastica profonda e quindi di una impossibilità a procedere con l asportazione endoscopica. Quando iniettare è uno dei quesiti posti da che si avvicina per la prima volta a questa metodica. Teoricamente non esiste un limite all infiltrazione specie se si usa soluzione salina. Anche 70 o 80 ml o ancora di più soluzione salina non rappresentano di per sé un problema ma alcune considerazioni vanno fatte. La prima è relativa alla diluizione con adrenalina. Non esistono lavori di confronto che dicono qual è la diluizione ottimale di adrenalina in fisiologica o che dicano se la diluizione 1:10000 previene più efficacemente il sanguinamento rispetto a 1: In genere ciascun endoscopista usa una diluizione differente senza un vero razionale scientifico ma in base ad abitudini consolidate o a convenzioni personali. Quello che risulta importante, specie in soggetti anziani e cardiopatici, è la quantità globale di adrenalina iniettata nella sottomucosa che comunque non dovrebbe superare una fiala (1 ml) nei pazienti anziani o cardiopatici e le due fiale (2 ml) in tutti gli altri pazienti. Anche se molto raramente, sono stati descritti infatti dei casi di aritmia anche fatali in seguito all iniezione di adrenalina. Infine l ultimo aspetto da considerare nella sottomucosa.
39 Questo argomento è stato oggetto di numerosi studi negli ultimi anni che hanno preso in considerazione differenti tipi di liquidi iniettabili endoscopicamente. La sostanza ideale da iniettare dovrebbe essere trasparente, permanere a lungo nella sottomucosa, non essere istolesiva, avere proprietà emostatiche ed essere anche economica. La soluzione salina, che storicamente è stata utilizzata nella maggior parte degli studi ha tutte queste caratteristiche con l eccezione che si dissolve in pochi minuti venendo assorbita dal torrente ematico e non ha nessuna capacità emostatica. Tra le sostanze prese in considerazione vi sono il detrosio, la glucosata ipertronica al 33%, l hemagel, l acido ialuronico, l idriossipropilmetilcellulosa ed altre ancora. Tra le sostanze che permangono più a lungo nella sottomucosa hanno un viscosità aumentata rispetto alla soluzione salina e quindi possono essere iniettate con una certa difficoltà se si usano aghi a canale piccolo da 23 G. Per tale motivo è suggeribile l utilizzo di un ago da 20 o 19 G quando si vuole iniettare l acido ialuronico o la idrossipropilmeticellulosa. Le tecniche di resezione Nonostante il principio sia lo stesso, le varianti tecniche della manovra endoscopica di rimozione di lesioni neoplastiche del tubo digerente sono numerosissime, ma solo in alcuni casi utilizzate routinariamente nella pratica clinica. Una prima grossolana classificazione di queste tecniche ne prevede la distinzione in due gruppi principali quelle in cui si utilizza un cappuccio cosiddetta Suck and cut e quelle in cui non è previsto l uso del cappuccio lift and cut. In realtà negli ultimi tempi sono state descritte anche delle tecniche in cui è previsto l uso del cappuccio ma non per aspirare al suo interno il tessuto da rimuovere, ma quale strumento per visualizzare meglio la lesione da asportare e per focalizzare bene il raggio di azione e la superficie di taglio su cui si sta lavorando (Fig 8). Metodiche lift and cut La tecnica più semplice di questo gruppo è quella inject and cut: si procede a sollevare la lesione con infiltrazione sottomucosa per creare un bled che viene poi catturato con l ansa diatermica e resecato con corrente da taglio [29.
40 L aggiunta di indaco carminio alla soluzione da iniettare fornisce un colore verde-bluastro alla sottomucosa espansa ed è di aiuto nel valutare la profondità durante e dopo la resezione. Lesioni di grosse dimensioni tipicamente richiedono la resezione in pezzi (piecemeal) che, quando possibile, dovrebbe essere effettuata in singole sessione. L impiego di uno strumento a doppio canale facilita notevolmente la tecnica inject and cut: in questo caso una pinza da biopsia viene utilizzata per tirare la lesione target all interno di un ansa diatermica preventivamente aperta ed introdotta nel secondo canale operativo dello strumento. L ansa viene quindi serrata e la lesione resecata. Metodiche suck and cut Altre tecniche prevedono l impiego di cilindretti trasparenti montati sul distale dell endoscopio entro cui aspirare la lesione sollevata (EMRC Endoscopic Mucosal Resection with Cap) o l applicazione di anelli elastici prima della resezione (EMRL Endoscopic Mucosal Resection with ligation ) [30]. La EMRC richiede l impiego di uno speciale cilindretto trasparente di plastica cap che viene applicato alla Dopo marcatura diatermica dei margini periferici della lesione, si procede alla infiltrazione sottomucosa con fisiologica o con soluzione di epinefrina diluita (1:10.000). Una particolare ansa diatermica viene pre-caricata nella scanalatura del bordo del cilindretto e tutta l area sollevata con infiltrazione viene aspirata all interno del cap. L ansa viene quindi serrata attorno a questo pseudo polipo creato artificialmente con la suzione, il tessuto intrappolato viene spinto fuori dal cilindretto con l ansa e la resezione viene eseguita con corrente miscelata(figura 5). Sono disponibili cilindretti di diverse dimensioni e conformazione, in base al diametro dell endoscopio; quello più grosso ha un diametro di 18 mm ed è stato disegnato per consentire resezioni en bloc. La tecnica EMRL è simile alla cap-assisted EMRC ed utilizza un legatore endoscopico per voraci esofagee applicato su uno strumento a canale singolo. La lesione da resecare viene aspirata nella camera dl legatore e legata con anello elastico (con o senza infiltrazione sottomucosa) prima di eseguire la resezione standard. LA DISSEZIONE SOTTOMUCOSA Il trattamento endoscopico delle lesioni preneoplastiche e/o neoplastiche in fase precoce del tubo digerente si è modificato ed evoluto negli ultimi 20 anni passando dalla fase della ablazione termica e/o con laser alla asportazione endoscopica con ansa sino alla mucosectomia endoscopica con cappuccio proposta per la prima volta da Inoue nel 1991[31]. Negli ultimi cinque sei anni questo percorso si è arricchito di una tecnica più complessa che mira alla asportazione en bloc e profonda, fino a raggiungere la tonaca muscolare, di lesioni early di dimensioni notevoli, anche superiori ai 3 4 cm. Tale tecnica, definita ESD ( Endoscopic Submucosal Dissection ), è basata sull uso di aghi dedicati che incidendo mucosa e sottomucosa possono consentire una resezione chirurgica radicale di lesioni altrimenti non asportabili o asportabili in più frammenti con le altre metodiche disponibili[32]. Vantaggi della ESD rispetto alla EMR L EMR ha rappresentato un momento di grande progresso endoscopico nel trattamento delle lesioni early del tubo digerente. Tale tecnica ha però dimostrato delle limitazioni sostanziali che sono state in parte superate dall ESD. Il problema principale risiede nelle dimensioni della lesione da asportare e nella precisione dell asportazione, nel senso del controllo della sezione di taglio rispetto ai margini laterali ed alla infiltrazione del piano mucoso
41 sottomucoso. Per ciò che riguarda le dimensioni, è stato dimostrato che lesioni maggiori di 2 cm, di aspetto flat o depresso possono essere asportate en bloc con le tecniche di EMR solo in una piccola percentuale mentre nella maggioranza dei casi necessitano di una resezione piecemeal. Questi limiti sono legati alle dimensioni dei cappucci e delle anse che impediscono di resecare in un unico pezzo lesioni superiori ad un certo diametro. L asportazione piecemeal si associa purtroppo ad una difficile ricostruzione ed orientamento dei frammenti con conseguente difficoltà per i patologi di stabilire livelli di infiltrazione ed indennità dei margini di resezione. Tutto questo, oltre ad associarsi ad una percentuale di recidiva che può arrivare anche al 30% ( e che è figlia di una resezione incompleta con presenza di foci neoplastiche ) impedisce una adeguata stadiazione della malattia e quindi una corretta valutazione della appropriatezza del gesto endoscopico e del rischio di diffusione linfonodale della malattia. Al contrario dell EMD, l ESD si basa su un concetto tipicamente chirurgico: una volta individuata e caratterizzata una lesione, l ago diatermico verrà utilizzato come un bisturi per incidere la mucosa sana intorno alla lesione ed esporre la sottomucosa che verrà progressivamente resecata sino ad ottenere il pezzo intero di parete interessata dal processo neoplastico [33] (Fig 9). Indicazioni Quello delle indicazioni per l ESD rimane un tema complicato, in continua evoluzione e su cui non sono state emanate linee guida dalle società scientifiche di endoscopia europee o americane. Alcune linee guida sono disponibili grazie alla Società Giapponese di Endoscopia anche se, a nostro modo di vedere, queste linee guida non possono sempre essere applicate pedissequamente nella nostra realtà per due motivi principali: uno è la discrepanza di definizione e terminologia, l altro è il livello di expertise che i giapponesi hanno in questo ambito e che è ben lontano da quello dei colleghi occidentali. Se tecnicamente per un giapponese può essere adeguato asportare en bloc una lesione di 5 o 6 cm questo è quasi impossibile allo stato attuale per la stragrande maggioranza degli endoscopisti occidentali. Traducendo ed adattando le regole giapponesi alle nostre esigenze è ragionevole immaginare che l ESD possa essere indicata per le lesioni depresse o con ulcera centrale minori di 2 cm a patto che la stadiazione con EUS ad alta frequenza e il lifting sign siano negativi. In presenza di lesioni maggiori di 2 cm l esperienza del singolo operatore, la sede e la morfologia della lesione dovranno guidare la scelta del tipo di approccio endoscopico o chirurgico qualora la terapia endoscopica non fosse proponibile. Accessori e strumenti Per l esecuzione dell ESD sono necessari aghi da sclerosi, aghi da precut e da dissezione sottomucosa, cappucci distanziatori o focalizzatori, clip metalliche e pinze da coagulazione. Gli aghi da sclerosi utilizzati sono quelli tradizionali da 23 Gauge e servono per l iniezione sottomucosa di fisiologica o altre soluzioni.
42 Quando si utilizzano soluzioni iniettabili ad elevata viscosità ( che permangono più a lungo nella sottomucosa ) quali acido ialuronico, colla di fibrina o HPMC può essere indicato l uso di aghi di dimensioni maggiori ( 21 Gauge ). Gli aghi diatermici per la dissezione sottomucosa sono disponibili in versioni differenti. Tutti sono stati sviluppati sul modello dell ago da precut e si distinguono in IT knife, TT knife, Hook knife e Flex knife (Fig 10). Ognuno di questi aghi ha delle specifiche peculiarità ed è stato sviluppato da esperti giapponesi. Ad oggi non esistono evidenze in letteratura per poter dire che un ago è più efficace o più sicuro di un altro o che un ago ha indicazione per una sede ( esofago, stomaco, colon ) piuttosto che per un altra. Di contro si può però dire che il più utilizzato in assoluto e quello su cui sono disponibili più dati scientifici è l IT knife che si caratterizza per avere in punta una pallina di ceramica che impedisce la trasmissione dell impulso monopolare in profondità garantendo così una certa sicurezza rispetto al rischio di perforazione. I cappucci per l ESD sono differenti da quelli utilizzati per l EMR. Infatti essi non servono ad aspirare tessuto al loro interno ma servono a tenere distanziati i due lembi di mucosa attraverso i quali si accede alla sottomucosa. L utilizzo dei cappucci distanziatori è maggiore nelle fasi più avanzate della dissezione quando una buona parte della lesione è stata incisa e tende a ricadere su se stessa occupando la zona che deve ancora essere resecata. In questa situazione il cappuccio agisce come un secondo braccio consentendo la separazione dei lembi e la focalizzazione dei movimenti dei knife rispetto al piano di taglio sottomucoso. Le clip sono un altro strumento molto utile nel corso dell ESD. In particolare vengono utilizzate per l emostasi e soprattutto per la chiusura di eventuali perforazioni che si verificano in corso di dissezione. Fig 11 Le pinze di coagulazione a caldo sono utilizzate per coagulare grossi vasi della sottomucosa evitando così che possano sanguinare sporcando il campo d azione. Tecnica Prevede quattro steps fondamentali: la marcatura, l iniezione sottomucosa, l incisione circonferenziale della mucosa con esposizione della sottomucosa ed infine la dissezione sottomucosa. Marcatura:
43 questo step è necessario nell esofago e nello stomaco dove i margini della lesione possono diventare poco chiari dopo la fase dell iniezione sottomucosa. Nel colon, se la lesione è ben evidente e sollevata rispetto al piano mucoso, può non essere necessaria. La marcatura si esegue utilizzando l APC o la punta di uno dei knife e formando dei piccoli spot di coagulo tutt intorno alla lesione, a 1 2 mm dal margine della lesione, creando così una linea di demarcazione sul cui versante esterno dovrà essere eseguita l incisione della mucosa. Iniezione sottomucosa: E uno step fondamentale. L ago deve essere infisso a 45 gradi rispetto al piano mucoso ed ad una certa profondità per essere sicuri di raggiungere la sottomucosa. Qualunque siano le dimensioni della lesione da asportare si consiglia di non iniettare mai tutta la superficie della lesione ma di cominciare dai bordi che saranno quelli che verranno resecati per primi. L iniezione della zona centrale dovrà essere fatta in un secondo tempo quando tutta la circonferenza mucosa è stata incisa e ha inizio la vera e propria dissezione sottomucosa. Non vi è un limite alla quantità di soluzione da iniettare così come non vi sono volumi appropriati per sede o dimensione della lesione. Bisogna agire con buon senso e fermarsi quando si vede la formazione di un buon cuscino sottomucoso. L iniezione di eccessiva quantità di soluzione, specie nel colon, può modificare il piano di inclinazione e di orientamento della mucosa rendendo difficile un corretto approccio alla lesione. Incisione della mucosa: Si inizia creando ai due lati opposti della lesione due piccole soluzioni di continuo nella mucosa sino alla esposizione della sottomucosa. Per fare ciò si può usare l ago da precut o uno degli altri aghi con l eccezione dell IT la cui punta è ricoperta e quindi taglia solo sul versante laterale. Partendo da queste due soluzioni di continuo si procederà con il knife scelto per continuare a incidere la mucosa nelle due direzioni sino a raggiungere la soluzione di continuo contro laterale e quindi completare la circonferenza del taglio. In questa fase conviene utilizzare una corrente di taglio tipo endo cut ma ad un dosaggio inferiore ( 80 watt ) a quello normalmente utilizzato per la polipectomia. L incisione della mucosa dovrà avvenire dal punto più distale della lesione verso il punto più prossimale. Infatti i knife sono manovrati al meglio e controllati in maniera ottimale solo quando il movimento dell endoscopio è in retrazione. Quasi impossibile o comunque meno sicuro ed efficace è l esecuzione del taglio in avanzamento. Dissezione sottomucosa: Si esegue posizionando il knife nel solco creato dall incisione della sottomucosa ed orientando il senso del taglio verso il piano sottomucoso e quindi su un piano sottostante e parallelo alla lesione. Mantenere questa direzione di taglio è estremamente difficile e necessita di movimenti di torsione sull endoscopio per far si che il knife sia correttamente orientato. Il knife, durante le operazioni di dissezione dovrebbe essere sempre mantenuto tangenziale e non verticale rispetto al piano di taglio o alla sottomucosa. Infatti l ago in posizione verticale non raggiunge una adeguata profondità di taglio nella sottomucosa, è difficile da muovere nella direzione voluta e non consente una adeguata visione dell area su cui si sta esercitando il taglio. Inoltre la distanza tra la punta dell endoscopio e la punta dell ago deve essere breve perché altrimenti si perde ( come per molti altri accessori in endoscopia ) il corretto e completo controllo dei movimenti. Anche se la sottomucosa è ben esposta rispetto alla posizione del knife si consiglia sempre di eseguire tagli brevi e controllati. Questo consentirà sempre un adeguato controllo della direzione e del taglio e la corretta visualizzazione dei vasi sottomucosi che andranno coagulati prima di procedere ulteriormente con la dissezione. Nelle fasi più avanzate della dissezione il cappuccio distanziatore sarà necessario per una migliore esposizione del piano sottomucoso. In linea di massima i movimenti del knife avverranno in retrazione e non in avanzamento e spesso richiederanno lo strumento in retrovisione.
44 I movimenti in direzione laterale sono possibili e diventano necessari nelle fasi più avanzate della dissezione. I movimenti laterali del knife avverranno in maniera diversa a seconda che si utilizzi il gastroscopio o il colonscopio. Infatti nel caso del gastroscopio il knife uscirà sul versante sinistro del quadrante ed i movimenti saranno più facili da sinistra verso destra. Nel caso del colonscopio il knife uscirà dal canale sul versante destro e sarà più semplice tagliare da destra verso sinistra. Questi accorgimenti sono molto utili per ottenere un taglio efficace della sottomucosa ed un controllo adeguato della direzione sia sul piano orizzontale che su quello verticale. Quando risulta difficile orientare correttamente il taglio con il knife, l endoscopio andrà ruotato quanto più possibile sul piano assiale e con una inclinazione che consenta di mantenere una posizione frontale rispetto alla lesione. Nel corso della dissezione, man mano che si espone il piano sottomucoso, si evidenzieranno i vasi sottomucosi. Questi vanno coagulati adeguatamente con la pinza da coagulo o con il knife per impedire sanguinamenti che sporcano il piano operatorio e rallentano le procedure di dissezione. Il setting dell elettrobisturi nell ESD è molto simile a quello della polipectomia standard anche se alcuni autori giapponesi ritengono più adeguato un setting su valori più bassi ( endo cut 80 watt e coagulazione soft 40 o 60 watt ) per ridurre il rischio di sanguinamento. Complicanze e loro gestione Le complicanze dell ESD sono rappresentate dal sanguinamento, dalla perforazione e dal dolore. Il sanguinamento è l evento più frequente e si verifica in una percentuale di casi variabile tra il 5% e l 8%. E più frequente per le lesioni gastriche rispetto a quelle del colon e nell ambito dello stomaco il terzo superiore dell organo è più a rischio di sanguinamento rispetto al corpo distale ed all antro. Nel corso della procedura sanguinamenti minori sono molto frequenti e dipendono dal taglio dei vasi sottomucosi. Tali sanguinamenti devono essere controllati immediatamente usando il knife e la corrente di coagulo soft o la pinza da coagulazione per evitare che l eccessiva presenza di sangue sporchi il campo operatorio impedendo la corretta identificazione dei landmark anatomici. Si raccomanda soprattutto in questa fase di evitare di usare eccessive quantità di acqua per il lavaggio del punto di sanguinamento perché comunque l acqua si mescola con il sangue, necessita di essere aspirata e può contribuire a creare una zona sporca che ridice la visibilità endoscopica. Le clips sono una utile risorsa per il controllo del sanguinamento anche se si suggerisce ( fin quando è possibile ) di limitarne l uso nelle fasi iniziali dell ESD per evitare che la presenza delle clip disturbi l azione del knife. I sanguinamenti tardivi ( > 72 ore ) sono in genere più rari, di minore entità e tendono ad autolimitarsi senza necessità di terapie endoscopiche. La perforazione è una complicanza che si riscontra più frequentemente nell ESD in confronto con l EMR con una percentuale variabile tra il 3% e il 5%. I dati della letteratura indicano che il rischio di perforazione non correla con le dimensioni della lesione trattata ma con la presenza di ulcera o depressione. Quando identificata precocemente la perforazione può essere trattata in maniera conservativa utilizzando le clips metalliche per approssimare i bordi della soluzione di continuo e chiuderla. Dai dati della letteratura si deduce che più del 75% dei casi di perforazione in corso di ESD sono trattati con successo mediante posizionamento di clips e terapia conservativa ( sondino, nutrizione parenterale totale e copertura antibiotica ad ampio spettro ) [34]. LA POLIPECTOMIA ENDOSCOPICA In una trattazione incentrata sulle resezioni endoscopiche non è possibile non inserire la forma più semplice di resezione e cioè la polipectomia, anche perché, per quanto riguarda il colon, i polipi rappresentano comunque, nella massima parte dei casi, i precursori del cancro e quindi il tempestivo trattamento dei polipi consente la prevenzione secondaria dello stesso cancro. E noto che il rischio di cancerizzazione dei polipi del colon è funzione di una serie di fattori. Il primo di essi è dato dal tipo istologico. I polipi epiteliali del colon si distinguono in adenomi tubulari, tubulo villosi e villosi. I polipi villosi sono quelli a rischio più elevato.
45 Un altro fattore è costituito dalle dimensioni. Il rischio di cancerizzazione è molto basso nei polipi dimensioni inferiori ai 5 mm ed aumenta progressivamente con l incremento delle dimensioni, soprattutto se eccedenti i 2 cm. Importante è anche il numero dei polipi. Più il numero è elevato, più aumenta la probabilità che uno di essi possa degenerare. Infine, un sicuro indice di aumentato rischio è costituito dalla insorgenza di displasia. La displasia è una condizione caratterizzata dalla comparsa di alterazioni cellulari a carico del citoplasma e del nucleo, che segnano un evidente accelerazione verso la trasformazione in senso carcinomatoso.. La colonscopia gioca un ruolo fondamentale nella diagnosi di tali lesioni e presenta inoltre la prerogativa esclusiva di poter consentire l effettuazione della resezione per via endoscopica della maggior parte dei polipi. Anche per quanto riguarda i polipi, in fase di valutazione è possibile utilizzare metodiche avanzate, quali la cromo-magnificazione, per evidenziare i segni di una iniziale e focale degenerazione in senso adenocarcinomatoso La polipectomia è una tecnica introdotta nella pratica endoscopica fin dal Da allora è andata incontro ad una diffusione crescente, beneficiando dalla rapidità e della facilità di esecuzione e dal ridotto tasso di complicanze ad essa connesse, quando eseguita correttamente. La tecnica con cui realizzare la polipectomia può essere diversa in dipendenza dalle dimensioni e dalla morfologia della lesione da trattare. Sul piano morfologico i polipi si distinguono in due fondamentali categorie: polipi sessili e polipi peduncolati. Un polipo si definisce sessile quando è attaccato alla parete, cioè quando la base di impianto sulla mucosa è estesa quanto il polipo stesso. Il polipo peduncolato, invece, è connesso alla mucosa della parete del colon per mezzo, appunto, di un peduncolo, che può essere più o meno lungo e più o meno sottile. Per i polipi sessili di piccoli dimensioni (fino a 3 mm) può essere sufficiente l asportazione con una comune pinza di biopsia, oppure si può ricorrere alla tecnica della biopsia a caldo (hot biopsy) per evitare eventuali emorragie. I polipi di maggiori dimensioni vengono asportati utilizzando un particolare strumento, che viene inserito nel canale operativo del colonscopio, chiamato ansa diatermica. L ansa diatermica è costituita da un filo metallico conformato come un cappio che può essere allargato e stretto per mezzo di un manipolo. Il cappio può essere di forme diverse: ovale, esagonale, asimmetrica. Può essere costituita da un monofilamento o da più filamenti intrecciati. La polipectomia dei polipi peduncolati è relativamente facile. Il polipo viene catturato con l ansa allargata. Quindi l ansa diatermica viene stretta intorno al peduncolo come un cappio e viene quindi attraversata da una corrente elettrica capace di recidere i tessuti (corrente di taglio) e di provocarne coagulazione, importante per prevenire il sanguinamento (corrente di coagulo monopolare). Durante la resezione l impiego dei i due tipi di corrente deve essere integrato nella maniera più idonea. A volte i polipi peduncolati possono avere un peduncolo particolarmente spesso. In questi caso, per maggiore sicurezza, in particolare ai fini di prevenire un eventuale sanguinamento post polipectomia può essere opportuno l impiego di un endo loop. Si tratta di un laccio un materiale plastico che viene stretto alla base de peduncolo. Fig 11. Successivamente verrà effettuata la resezione con l ansa diatermica al di sopra dell endo loop che rimarrà a stringere il peduncolo, fino alla sua eliminazione spontanea. Un altra tecnica per prevenire il sanguinamento può essere rappresentata dal posizionamento sul peduncolo di una o più endoclips. Per quanto riguarda i polipi sessili prima di effettuare una polipectomia con ansa diatermica, è sempre opportuno praticare uno scollamento del polipo dai piani sottostanti con una soluzione salina con eventuale aggiunta di adrenalina e di un colorante (lifting). Tale manovra ha lo scopo di peduncolizzare il polipo
46 sollevandolo sul piano mucoso, in modo che utilizzando l ansa diatermica non si provochi un danno della parete, con il rischio di una conseguente perforazione. In effetti viene messa in atto la stessa procedura che costituisce il tempo preliminare della mucosectomia endoscopica, utilizzata per asportare le lesioni superficiali piatte. Una volta sollevato il polipo si utilizza l ansa diatermica con la stessa tecnica dei polipi peduncolati. Questo è il motivo per cui, almeno per quanto riguarda i polipi sessili, è giustificato considerare la polipectomia come una resezione endoscopica a tutti gli effetti. La procedura dell infiltrazione può essere impiegata anche in caso di polipi con un peduncolo corto allo scopo di aumentare la distanza del polipo dalla parete. In qualche caso può essere indicato usare sia il lifting che il posizionamento di un endo loop. Anche nel caso di polipi peduncolati, quindi, a causa della misura, forma o localizzazione la polipectomia può presentare particolari difficoltà per la rimozione endoscopica configurando quella che viene definita polipectomia difficile. Quando si effettua una polipectomia endoscopica bisogna sempre mirare ad asportare la lesione in maniera completa e in un pezzo unico (en block). Questo è importante anche perché l anatomo patologo al quale verrà inviato il polipo asportato, avrà la possibilità di esaminare la lesione nella sua interezza. In questo modo, in caso di eventuale cancerizzazione, sarà possibile valutare adeguatamente il limite dell infiltrazione e stabilire se il trattamento endoscopico sarà stato sufficientemente radicale. In caso di polipi voluminosi, però, non è sempre possibile realizzare una resezione en block. In tali circostanze si può effettuare una resezione in fasi successive, asportando la lesione a pezzi (piece meal). Tale tecnica, quando possibile, dovrebbe essere evitata perché non consente una buona valutazione istologica della lesione asportata. La polipectomia endoscopica può essere causa di complicanze quali: l emorragia in circa il 2% dei casi; la perforazione nello 0.3%; il dolore post polipectomia nell 1%. Conclusioni Nell ambito delle diverse branche mediche l endoscopia è tra quelle che ha maggiormente beneficiato degli enormi progressi in campo tecnologico che si sono registrati negli ultimi anni. Ciò ha consentito una notevole espansione delle applicazione cliniche dell endoscopia sia in campo diagnostico e terapeutico soprattutto nel campo delle lesioni precoci gastrointestinali. Si tratta di un settore che riscuote sempre maggiore interesse in quanto la diagnosi precoce delle neoplasie gastrointestinali consente un sempre più ampio ricorso a tecniche di intervento mini invasive che salvaguardano la qualità di vita del paziente. In campo endoscopico oggi disponiamo di strumenti e di accessori che consentono di effettuare procedure diagnostiche e terapeutiche assolutamente impensabili solo fino a pochi anni orsono. Attualmente tali procedure come dimostrano i dati della letteratura ed anche la casistica descritta, seppure numericamente limitata, appaiono sufficientemente sicure ed adeguate al tenere un trattamento definitivo in pazienti selezionati. È evidente che per poter effettuare questo tipo di procedure è necessaria una adeguata esperienza e la disponibilità di tutte le strumentazioni per poter completare tutto l iter diagnostico terapeutico. Quindi è opportuno che esse siano appannaggio di centri di riferimento in grado di poter sfruttare al meglio le potenzialità che oggi la tecnologia è in grado di garantire.
47 ESOFAGO DI BARRETT Definizione anatomica dell ESOFAGO L Esofago è un organo dell apparato digerente della lunghezza di circa cm e larghezza di 2-3 cm. Collega la faringe allo stomaco e presenta una duplice funzione: consente il passaggio del cibo (bolo alimentare) fino allo stomaco dove avverrà la digestione; impedisce il reflusso dallo stomaco insieme ad acido e succhi gastrici. Le pareti dell esofago sono formate da strati, o tonache, sovrapposte: mucosa, sottomucosa, tonaca muscolare, tonaca avventizia. La mucosa esofagea è uno strato spesso, di colore grigio-rosato o rossastro nelle giunzioni gastro-esofagea; a riposo presenta numerosi solchi e creste, tali da occluderne il lume. Si tratta però di modificazioni temporanee della mucosa esofagea che scompaiono quando questa è distesa, ad esempio durante il passaggio del bolo alimentare. La mucosa è costituita da tre strati : epitelio di rivestimento, tonaca propria e muscolaris mucosae. La patologia esofagea può essere di tipo funzionale (disordini motori, diverticoli esofagei, esofagite emalattia da reflusso gastro-esofageo); e di tipo neoplastico (Esofago di Barret). Definizione anatomo-patologica ESOFAGO di BARRET Dal punto di vista anatomo-patologico, si definisce Esofago di Barrett la metaplasia intestinale della mucosa squamosa esofagea. Macroscopicamente il segmento colpito appare caratterizzato da una o
48 più lingue o chiazze di mucosa vellutata rossa, che si estendono al di sopra della giunzione gastro-esofagea, definita dall apice delle pliche gastriche. Tale mucosa metaplastica si alterna a una residua mucosa squamosa (esofagea) che, invece, appare liscia e pallida (fig.1). (Fig.1) L Esofago di Barrett è una condizione patologica nella quale l epitelio pavimentoso stratificato dell esofago viene in parte sostituito da epitelio intestinale. Attualmente, l epitelio colonnare, caratterizzato dalla presenza delle globlet cells, è considerato patognomonico della malattia,in quanto l unico ad avere una potenziale evoluzione maligna. 1 Oltre alle alterazioni della mucosa, l Esofago di Barrett è spesso caratterizzato anche da modifiche dei tessuti di derivazione mesenchimale, come, per esempio dalla duplicazione della muscolaris mucosae, e si pensa che tali modifiche possano essere correlate allo 1 The AGA Institute Medical Position. Statement on the Management of Barrett s Esophagus. Gastroenterology, 2011; 140:
49 sviluppo dell adenocarcinoma invasivo sul segmento esofageo malato. 2 In condizioni fisiologiche, la giunzione gastro-esofagea, rappresentata dal margine prossimale delle pliche gastriche, coincide con la Linea Z, che corrisponde alla giunzione squamo colonnare, ovvero all interfaccia tra l epitelio squamoso stratificato dell esofago e l epitelio cilindrico della mucosa gastrica. Nell Esofago di Barrett invece, si verifica la risalita, più o meno marcata, della linea Z, rispetto alla giunzione gastro-esofagea. Classificazione L Esofago di Barret deve il suo nome al Dott. Barret, chirurgo inglese che per primp, negli anni 50, descrisse la malattia come Sindrome dell esofago corto, per il caratteristico aspetto del lume esofageo che, a causa della metaplasia, appariva accorciato. L Esofago di Barret può essere suddiviso in base alla lunghezza del tratto esofageo interessato dalla metaplasia in tre tipi principali: Long Barret : se il segmento interessato misura più di 3 cm; Short Barret : se è compreso tra 1 e 3 cm; Ultra-Short Barret : se misura meno di 1 cm. Epidemiologia L'esofago di Barrett non è una patologia molto frequente. Secondo studi epidemiologici condotti negli USA, la prevalenza clinica nella popolazione generale sarebbe dello 0,026% anche se, sulla base di riscontri autoptici, essa dovrebbe ritenersi molto superiore. E stimata
50 essere intorno all'1% di tutti i pazienti che si sottopongono ad esofagogastroduodenoscopia ed è valutata tra l'8 ed il 20% nei pazienti con sintomi da reflusso gastroesofageo. Scende, però, al 3-7% quando la diagnosi venga posta solo in presenza di epitelio colonnare specializzato. L'età media al momento della diagnosi è intorno ai 50 anni, anche se il range è molto ampio (da 1 mese a 88 anni); il rapporto tra sesso maschile e sesso femminile è di 3:1 con una netta prevalenza per la razza bianca. La prevalenza dell'eb registra, almeno nei paesi occidentali, un costante trend di crescita, parallelo a quello della MRGE. Anche l'incidenza dell'adenocarcinoma esofageo è in progressivo aumento rispetto a quella del carcinoma squamoso, sia negli USA che nei paesi dell'europa occidentale, tanto che l'adenocarcinoma rappresenta ormai circa il 50% di tutte le neoplasie epiteliali dell'esofago. Secondo i dati desunti da studi retrospettivi, la prevalenza di adenocarcinoma esofageo nei pazienti con EB risulta aggirarsi intorno al 10%; sulla base di studi prospettici l'incidenza di adenocarcinoma varia tra 1/52 e 1/285 pazienti per anno di follow-up con un rischio stimato da 30 a 125 volte superiore a quello della popolazione generale. La diagnosi di adenocarcinoma nei pazienti con EB viene posta mediamente trai 60 ed i 70 anni e quindi a circa anni dopo la diagnosi di EB. Eziopatogenesi Dal punto di vista eziopatogenetico, la principale causa dell Esofago di Barrett è la Malattia da reflusso gastro-esofageo, un affezione che riguarda il 30% della popolazione adulta del mondo occidentale e che,
51 a lungo andare, provoca un infiammazione più o meno grave della parete dell esofago dovuta al contatto con materiale acido di provenienza dallo stomaco. Le cellule staminali situate nella porzione più profonda dell epitelio sono così stimolate a differenziarsi in modo tale da poter tollerare quest insulto. Da qui lo sviluppo della metaplasia. Non è ancora del tutto chiaro il motivo per cui solo alcuni individui esposti a questi fattori di rischio sviluppino la patologia, ma sicuramente entrano in gioco delle alterazioni genetiche ed epigenetiche a carico delle cellule staminali. Allo stesso modo non sono ben conosciuti i meccanismi per cui in un subset di pazienti dalla metaplasia si passi alla displasia, fino all insorgenza dell adenocarcinoma. Diagnosi La diagnosi dell Esofago di Barrett è il risultato di un accurato iter diagnostico che parte da un attenta anamnesi e arriva alla valutazione istologica delle lesioni. L'endoscopia è l'indagine di scelta per la diagnosi dell'eb, per la possibilità di evidenziare la mucosa metaplasica rosa salmone, che si differenzia bene rispetto alla mucosa di color madreperlaceo dell esofago. L endoscopia, però, da sola, non consente di distinguere tra i diversi tipi di epitelio metaplastico e quindi di identificare la metaplasia intestinale (epitelio colonnare specializzato), che è il tipo di epitelio responsabile della potenzialità evolutiva dell EB. Anche nella diagnosi di displasia l endoscopia convenzionale raramente può essere utile in quanto le alterazioni displastiche, quasi mai si rendono evidenti attraverso specifiche alterazioni endoscopiche. Un utile integrazione all'esame endoscopico può derivare da una tecnica complementare, rappresentata dalla cromoendoscopia.
52 Tale tecnica consiste nell impiego di sostanze che, applicate sulla mucosa del canale digerente, rendono più visibile o meglio contrastate aree di alterazione morfo-strutturale della superficie in corso di esame endoscopico. Queste sostanze appartengono a tre classi fondamentali: - Coloranti vitali assorbiti dalle cellule per diffusione o assorbimento attivo ( liquido di Lugol, blu di metilene, cristal violetto ). - Coloranti di contrasto non assorbiti dalle cellule, accentuano la topografia tissutale accumulandosi tra i solchi intercellulari e nelle fossette ghiandolari rendendo più visibile l architettura della mucosa ( indaco carminio e acido acetico ). - Coloranti reattivi reagiscono alle modificazioni della secrezione acida e sono utili per l identificazione precoce del cancro gastrico e della infezione da H. pylori ( rosso Congo). Per confermare la metaplasia ed identificare un eventuale displasia anche in assenza di lesioni endoscopiche visibili,è però necessario, completare l esame endoscopico con l effettuazione di prelievi bioptici multipli. Si può parlare a tal proposito del Protocollo di Seattle, secondo cui si dovrebbero effettuare biopsie multiple sui quattro quadranti della parete del viscere, le prime sulla giunzione gastroesofagea, le altre a distanza di 2 cm, in verticale, le une dalle altre (1 cm in caso di displasia sospetta o già accertata), fino ad arrivare al margine prossimale della mucosa metaplastica e, infine, all esofago apparentemente indenne. Si dovrebbero, inoltre, fornire all anatomopatologo informazioni riguardanti la localizzazione della linea Z e il
53 rapporto tra questa e la giunzione gastro-esofagea 3 4. Il Protocollo di Seattle si è rivelato un ottima strategia per la valutazione di tutto il segmento esofageo patologico, per l identificazione, la localizzazione e la quantificazione delle goblet cells ovvero delle cellule caliciformi tipiche della mucosa intestinale e per la ricerca di un eventuale displasia. L identificazione sulle biopsie delle goblet cells è fondamentale per porre diagnosi di EB al punto che secondo le linee guida dell American College of Gastroenterology, la mancata dimostrazione delle vere goblet cells esclude automaticamente la diagnosi di Barrett 5. Non tutti, però, condividono questa impostazione, Nell UK e in Giappone, infatti, il reperimento di tali cellule non è considerato necessario per porre diagnosi di Barrett, in quanto numerosi studi evidenziano che anche l epitelio privo di goblet cells può evolvere in adenocarcinoma. Pertanto, secondo le linee guida della British Society of Gastroenterology, i pazienti che presentano solo metaplasia cardiale e/o fundica, dovrebbero essere trattati allo stesso modo di quelli con metaplasia intestinale, in termini di terapia e sorveglianza endoscopica 6. Da quanto detto, risulta evidente l importanza del prelievo o meglio, dei prelievi, che l endoscopista dovrà effettuare nel sospetto di metaplasia. Altro elemento importante è la diagnosi di displasia, la cui presenza modifica il management del Barrett. Per molto tempo non vi è stato accordo fra gli anatomopatologi per la diagnosi di displasia. Attualmente, sia in Europa, che nei Paesi Asiatici, viene utilizzata la Classificazione di Vienna, che definisce il campione bioptico come: 3 Harrison R et al. Detection of intestinal metaplasia in Barrett s esophagus: an observational comparator study suggests the need for a minimum of eight biopsies. Am J Gastroenterol, 2007; 102: Chandrasoma P, Der R, Dalton P. Distribution and significance of epithelial types in columnarlined esophagus. Am J Surg Pathol, 2001; 25: Wang K K e Sampliner R E. Practice Parameters Committee of the American College of Gastroenterology. Updated guidelines 2008 for the diagnosis, surveillance and therapy of Barrett s esophagus. Am J Gastroenterol 2008; 103: Odze RD. Barrett esophagus: histology and pathology for the clinician. Nat Rev Gastroenterol Hepatol, 2009; 6:
54 1) Negativo per displasia, 2) Displasia indefinita, se il campione presenta dei fenomeni rigenerativi difficilmente distinguibili dai fenomeni displastici veri e propri, oppure artefatti tecnici che ne inficiano le caratteristiche citologiche. Non sono stati ancora accettati, ad oggi, dei markers molecolari che possano aiutare gli anatomo-patologi in questa distinzione: Ki67, PCNA, Ciclina D1, p53 non si sono rivelati sufficientemente specifici in questo senso. 3) Displasia di basso grado, non invasiva, 4) Displasia severa non invasiva, con atipie citologiche e architetturali più marcate rispetto a quella di basso grado, aspetto villoso, maggiore complessità e ramificazione delle cripte, disposizione cellulare di tipo back to back. 5) Displasia invasiva. Molto sottile è il confine che separa la displasia invasiva dall adenocarcinoma in situ. L ultimo step della progressione in senso neoplastico è l adenocarcinoma invasivo, intramucoso o sottomucoso a seconda dell interessamento della muscolaris mucosae. Il rischio di progressione della displasia di basso grado in displasia severa o in adenocarcinoma viene stimato tra il 2 e il 12%, mentre il rischio di progressione della displasia severa in cancro risulta compreso tra il 16 e il 59%. Altra considerazione importante è che non solo il grado ma anche l estensione della displasia è direttamente proporzionale al rischio di trasformazione maligna 7 8. Ritornando alla diagnosi endoscopica il presupposto è la precisa definizione della giunzione squamo-colonnare rispetto a quella gastro-esofagea 7 Buttar NS et al. Extent of high-grade dysplasia in Barrett s esophagus correlates with risk of adenocarcinoma. Gastroenterology, 2001; 120: Srivastava A et al. Extent of low-grade dysplasiais a risk factor for the development of esophageal adenocarcinoma in Barrett s esophagus. Am J Gastroenterol, 2007; 102:
55 Effettuata questa valutazione è possibile determinare la lunghezza dell esofago di Barrett, sottraendo la distanza della linea squamo-colonnare dalla giunzione esofago-gastrica. La classificazione di Praga, elaborata nel 2006 da Sharma et al., ha reso possibile la classificazione endoscopica dell esofago di Barrett, introducendo il criterio C, cioè la massima estensione circonferenziale, espressa in centimetri, a partire dalla giunzione gastroesofagea, e il criterio M, ovvero la massima estensione in lunghezza del sospetto epitelio colonnare, calcolata come distanza in centimetri tra la giunzione gastro-esofagea e l apice dell eventuale lingua metaplastica (fig. 5). (Fig. 5: immagini esemplificative della classificazione di Praga) Sintomi La storia clinica dei pazienti è generalmente, ma non necessariamente,
56 è quella di una malattia da reflusso gastroesofageo, responsabile dell infiammazione e, quindi, della metaplasia della mucosa esofagea 9. Le manifestazioni dell esofagite da reflusso comprendono una serie di sintomi, tipici e atipici (tab. n 3), che possono presentarsi in maniera variabile. Sintomi dell'esofagite da reflusso Tipici Atipici pirosi dolore toracico simil-anginoso bronco-pneumopatie abingestiis rigurgito disfagia raucedine cronica odinofagia asma scialorrea Tra i sintomi tipici, la pirosi e il rigurgito sono i più frequenti. La prima è avvertita generalmente come sensazione di bruciore in sede retro-sternale, che può estendersi fino alla base del collo e irradiarsi posteriormente nella regione inter-scapolare; il secondo, invece, consiste nella risalita di materiale gastrico in bocca. Entrambi insorgono, di solito, nel periodo post-prandiale o quando il paziente è in posizione supina e possono essere scatenati dall ingestione di alimenti capaci di ridurre il tono dello sfintere esofageo inferiore (cioccolata, pomodoro, menta, caffè, cipolla) o di irritare la mucosa già infiammata del viscere (agrumi, alcol, bevande troppo calde o troppo fredde). Per valutare l'entità e le caratteristiche del reflusso e delle alterazioni motorie che ne sono alla base, al momento della diagnosi dell Esofago di Barrett, vanno sempre effettuate la manometria e la PH-metria. 9 Jankowski J, Barr H, Wang K, Delaney B. Diagnosis and management of Barrett s oesophagus. Brith Med J, 2010; 341:
57 - La ph-metria esofagea delle 24 ore (secondo la tecnica proposta da DeMeester e Johnson) è l esame più sensibile e specifico per documentare l acidità del microambiente esofageo e rappresenta il goldstandard per la diagnosi di reflusso gastro-esofageo patologico. Si tratta di un esame che non richiede ricovero e consente una registrazione circadiana degli episodi di reflusso nel rispetto della fisiologia esofagea. Un elettrodo sensibile alla concentrazione idrogenionica (introdotto per via nasale) viene posizionato 5 cm a monte del margine superiore dello Sfintere Esofageo Inferiore (SEI) e collegato con un registratore. Per tutta la durata della registrazione, il paziente svolge le normali attività quotidiane. L indagine (generalmente ben tollerata) permette una correlazione tra le variazioni del ph esofageo e la comparsa di sintomi clinici registrati su apposito diario. Prima della procedura, il paziente deve sospendere l assunzione di qualsiasi tipo di farmaco. È considerato Reflusso Gastro-Esofago (RGE) ogni caduta di ph al di sotto di 4. Per valutare la presenza e la gravità di un reflusso gastroesofageo patologico vengono valutati una serie di parametri, tra i quali la percentuale del tempo totale di esposizione a ph< 4 della mucosa esofagea, il numero complessivo di episodi di RGE, il numero di reflussi con durata > 5 min. Opzioni Terapeutiche Volendo sintetizzare quanto è stato detto fino ad ora si può dire che l Esofago di Barret è da considerarsi, nella stragrande maggioranza dei casi, una condizione acquisita, secondaria alla MRGE cronica e caratterizzata dalla presenza di metaplasia intestinale in esofago, con potenzialità evolutiva verso l adenocarcinoma, attraverso un percorso che vede nella displasia severa l ultimo step.
58 Per questo motivo l approccio ideale dell EB dovrebbe prevedere, oltre al trattamento del reflusso, che è la causa prima della lesione e dei sintomi, l eliminazione della metaplasia e la sua sostituzione con un epitelio neosquamoso libero da malattia e quindi non più a rischio di cancerizzazione Il conseguimento di tali risultati potrebbe consentire di risolvere il problema della sorveglianza endoscopica, che comporta dei costi certamente non trascurabili ed impatta, spesso molto negativamente, sulla qualità di vita dei pazienti. In effetti, almeno fino a pochissimo tempo fa, un trattamento diretto della metaplasia non era concretamente disponibile e la terapia dell esofago di Barrett è coincisa con quella del reflusso nei casi non complicati o della displasia severa e/o dell adenocarcinoma. La Terapia del reflusso Terapia Medica: E basata sull utilizzo dei farmaci inibitori della pompa protonica (IPP), omeprazolo e derivati, introdotti nella pratica clinica alla fine degli anni '80 del secolo scorso. Tali farmaci, impiegati ad alte dosi (almeno 40 mg di omeprazolo die), sono in grado di determinare oltre che la rapida scomparsa dei sintomi, la guarigione delle lesioni esofagitiche, anche severe (ulcere), in un'alta percentuale di casi. Gli IPP, seppure con un meccanismo indiretto, tendono a contrastare anche gli effetti del reflusso duodenogastroesofageo. Il più importante di questi meccanismi risiede nella notevole riduzione del volume globale del refluito, indotta dal farmaco attraverso il blocco della secrezione acida. Il blocco della secrezione acida gastrica è altresì efficace nel depotenziare l'azione dei sali biliari che in genere non sono responsabili di una lesività diretta ma favoriscono quella del reflusso acido attraverso la detersione della mucosa esofagea ed ancora l'azione, diretta, degli acidi biliari coniugati che esplicano il loro effetto lesivo a
59 ph acido. Comunque, anche nei confronti del reflusso acido, il trattamento prolungato con IPP ad alte dosi non sembrerebbe assicurare una protezione completa; dopo un follow-up superiore ai 5 anni, oltre un terzo dei pazienti continuano a presentare alterazioni del tracciato ph-metrico (percentuale patologica di tempo totale di esposizione a ph inferiore a 4). In ogni caso, la terapia con IPP deve essere necessariamente protratta per periodi di tempo indefiniti, ciò che costituisce un indubbio problema, in particolare nei pazienti con lunga aspettativa di vita. Terapia Chirurgica La terapia chirurgica, rappresentata dagli interventi di plastica antireflusso, è considerata dai più meno costosa e sicuramente più efficace nel controllo del reflusso alcalino e della sintomatologia reflux-like rispetto ai PPI. Indipendentemente dai risultati sul reflusso, né la terapia chirurgica, né tanto meno quella medica, si sono dimostrate in grado di determinare, se non episodicamente e in modo molto parziale, la regressione della metaplasia. Terapia della displasia severa e dell adenocarcinoma All estremo opposto rispetto alla terapia del reflusso vi è il trattamento della displasia severa, che spesso non può essere distinta dal carcinoma in situ. D altra parte è steto segnalato che in oltre il 40% dei pazienti sottoposti ad intervento per diagnosi di sola displasia severa, coesisteva, sul campione chirurgico, un adenocarcinoma. Per tale motivo il trattamento standard della displasia severa nell EB, una volta confermata la diagnosi, nei pazienti a rischio chirurgico non elevato, è stato considerato l esofagectomia. Come si vede queste modalità di trattamento non vanno ad incidere direttamente sull Esofago di Barrett e sulla sua possibile evoluzione. E vero che una terapia efficace e duratura del reflusso dovrebbe poter evitarne la progressione, ma prove certe in tal senso non esistono e lo dimostra il fatto che dopo un trattamento antireflusso i pazienti con Barrett devono continuare a sottoporsi ad un regime di sorveglianza. E va sottolineato, infine, che la sorveglianza non è in grado di per sé di prevenire l insorgenza della displasia severa o dell adenocarcinoma, ma solo di permetterne una diagnosi tempestiva e quanto più precoce possibile.
60 I potenziali trattamenti endoscopici Per questo motivo nel tempo sono state proposte una serie di modalità di trattamento locale diretto dell esofago di Barrett, integrative od alternative rispetto alle terapie prima descritte. E facilmente intuibile come la via ottimale di approccio per tali trattamenti sia stata identificata in quella endoscopica, attraverso l utilizzo di diverse tecniche mirate alla resezione e/o all ablazione dell epitelio danneggiato. Va sottolineato che quasi tutti i trattamenti endoscopici proposti e che saranno di seguito brevemente discussi, sono stati primariamente impiegati in pazienti con displasia severa ad alto rischio chirurgico per l età avanzata o la presenza di comorbilità. Alcuni di questi trattamenti hanno poi dimostrati di poter rappresentare una valida alternativa alla terapia chirurgica resettiva non solo nei pazienti ad alto rischio chirurgico, per il trattamento della displasia severa o dell adenocarcinoma intramucoso, in cui il rischio di metastasi linfonodale è da considerarsi prossimo allo zero e quindi la completa escissione della lesione primitiva può risultare curativa. A nostro avviso, però, la principale indicazione di un trattamento endoscopico nell EB, su cui ne andrebbe misurata l efficacia e la sicurezza, è rappresentata dalla completa asportazione dell epitelio metaplastico, con la conseguente prevenzione dell evoluzione in senso neoplastico e l eliminazione di un programma di sorveglianza. Le varie tecniche endoscopiche possono essere suddivise, in base al principio di funzionamento, in: - meccaniche: mucosectomia, sottomucosectomia; - chimiche: terapia fotodinamica (PDT); - termiche: elettrocoagulazione multipolare (MPEC), Argon plasma coagulation (APC), crioablazione, terapia laser con CO2 (ancora in sperimentazione). Va precisato già in premessa che, relativamente alla displasia severa e/o all adenocarcinoma in stadio early, le tecniche di ablazione non meccaniche, presentano il notevole limite di asportate il tessuto patologico attraverso la sua distruzione. Ciò rende impossibile la valutazione anatomopatologica sul campione asportato, per cui non è dato sapere se l intervento effettuato possa aver avuto un intento curativo. Questa possibilità può essere offerta solo dalle tecniche meccaniche, che, non a caso, vengono considerate innanzitutto l ultimo step dell iter
61 diagnostico, sempre che la lesione venga asportata en block. Pertanto solo le tecniche meccaniche di resezione endoscopica possono costituire, in casi selezionati (lesione limitata alla mucosa, senza interessamento linfatico e vascolare), un effettiva alternativa al trattamento chirurgico. MUCOSECTOMIA ENDOSCOPICA: La mucosectomia endoscopica, consistente nell asportazione, previa infiltrazione e scollamento, della mucosa esofagea; è una tecnica semplice, ripetibile, consolidata, indicata in caso di lesioni focali, nodulari o piane, non ulcerate. Le tecniche convenzionali di resezione endoscopica della mucosa comprendono la mucosectomia con ansa ( lift and cut ), la mucosectomia strip biopsy, la mucosectomia con cap e la mucosectomia con legatura elastica. - MUCOSECTOMIA STANDARD LIFT AND CUT : è la tecnica più semplice e consiste nell individuazione dei margini della lesione con colorazione vitale con indaco-carminio, con o senza demarcazione periferica ai margini della lesione (5 mm) mediante ago diatermico, hot biopsy con branche chiuse o punta di ansa chiusa, si esegue poi l iniezione sottomucosa con soluzioni saline e/o colloidali con o senza adrenalina (1: ) per separare e sollevare la lesione mucosa dalla muscolare propria. Infine, si intrappola la lesione nell ansa aperta e con l ausilio di una modica aspirazione si procede a strozzatura ed elettro-resezione cercando di mantenere all interno della presa tutti i margini della lesione precedentemente individuati. (fig) - MUCOSECTOMIA STRIP BIOPSY : è una tecnica, relativamente
62 semplice, richiede l impiego di un gastroscopio a doppio canale e l aiuto di due assistenti. Previa delimitazione dei margini mediante colorazione vitale con indaco-carminio, si procede alla marcatura periferica della lesione (5 mm dai margini) mediante un ago diatermico. Dopo, si inietta al centro della lesione soluzione fisiologica con adrenalina 1: per sollevare lo strato sottomucoso mediante un ago da sclerosi. Si inseriscono nei due canali operatori un ansa e una pinza da presa. La pinza viene fatta scorrere dentro l occhiello dell ansa aperta e poi richiusa leggermente sulla pinza. Si afferra la lesione con la pinza sollevando delicatamente la lesione e si fa scorrere sulla lesione l ansa aperta con una live pressione. Calibrata l ansa in modo da comprendere tutti i margini della lesione precedentemente segnalati si procede all elettro-resezione. Dopo il recupero, il campione viene appiattito e fissato con aghi sottili su polistirolo o sughero e si verifica l inclusione nel pezzo di tutti i segni della marcatura. In caso di incompleta resezione si ripete la procedura e poi si ricostruisce l architettura e l orientamento dei pezzi considerando la forma originaria della lesione e i segni della marcatura. - MUCOSECTOMIA CON CAP : richiede l uso di un cap di plastica trasparente da apporre alla punta dello strumento. All interno del cap vi è un solco entro cui posizionare l ansa aperta. Dopo l iniezione sottomucosa, il cap viene spinto sulla lesione che viene quindi completamente aspirata al suo interno e resecata (fig). - MUCOSECTOMIA CON LEGATURA ELASTICA :In questa tecnica si adopera un dispositivo per legatura elastica per varici. Con o senza iniezione sottomucosa, la lesione viene aspirata nel cilindro del dispositivo e viene legata con un anello elastico. Successivamente si esegue l elettro-resezione con ansa da polipectomia.
63 In premessa alla descrizione delle diverse tecniche endoscopiche è stato già sottolineato che la mucosectomia endoscopica va considerata, prima che un opzione terapeutica risolutiva, una metodica di diagnostica avanzata, in grado di fornire preziose informazioni riguardanti il grado di differenziazione e lo stadio di un eventuale neoplasia. E stato anche detto che in determinate condizioni essa costituisce una modalità di trattamento affidabile su una singola lesione focale. Nel caso dell EB, però, è noto che molto spesso la displasia è multifocale; ciò rende ragione dell elevata incidenza di recidiva dopo mucosectomia endoscopica che può giungere al 47% per la frequente presenza di lesioni sincrone misconosciute o di lesioni metacrone. Il problema potrebbe essere risolto con l estensione della mucosectomia a tutta la mucosa metaplastica e quindi potenzialmente displastica. A parte le difficoltà di ottenere una mucosectomia realmente completa, soprattutto in casi di segmenti lunghi di Barrett le mucosectomie estese si associano ad un incidenza di stenosi pari al 50% della popolazione trattata. Si comprende, pertanto, come il ruolo da riservarsi alla mucosectomia sia quello di un primo step del trattamento, volto ad eliminare le irregolarità mucose focali (lesioni endoscopicamente visibili) affidando poi il compito di realizzare l ablazione del residuo tessuto metaplastico con altre tecniche endoscopiche. SOTTOMUCOSECTOMIA ENDOSCOPICA : La sottomucosectomia endoscopica, è una metodica indaginosa, proponibile solo per lesioni estese oltre i limiti delle possibilità di asportazione en block della mucosectomia (20 mm) e localizzate a livello della giunzione esofago-gastrica, dove la parete intestinale è meno sottile che nell esofago e quindi il rischio di perforazione, correlato a questa tecnica, risulti relativamente più contenuto. Previa individuazione dei limiti della lesione con indaco-carminio si procede a marcatura periferica della lesione con ago diatermico e si effettua l infiltrazione della sottomucosa con fluidi di varia
64 composizione (soluzioni saline e/o colloidali, con o senza adrenalina 1: , polietilenglicole, glicerolo, ialuronato di sodio, idrossimetilpropilcellulosa etc.). Dopo tale tempo preliminare, che è sostanzialmente simile a quello della mucosectomia, si procede all incisione circonferenziale della mucosa unendo i fori precedentemente creati. Successivamente, attraverso ripetute iniezioni sottomucose tese sollevare la lesione dai piani profondi, si procede cautamente nella dissezione lungo il piano sottomucoso. Fino alla completa resezione della lesione. Il pezzo recuperato viene quindi appiattito e fissato con aghi sottili su polistirolo o sughero e si verifica la presenza di tutti i segni della marcatura. Dopo la fissazione, il campione viene sottoposto a sezioni seriali ad intervalli di 2 mm parallele ad una linea che comprende il margine di resezione più vicino cosicché possono essere valutati adeguatamente sia i margini verticali che quelli laterali. Viene valutata la profondità dell invasione neoplastica (T), il grado di differenziazione (grading) e l infiltrazione linfatica e vascolare. Questo tipo di resezione consente una diagnosi istologica completa ed accurata della lesione. La dissezione sottomucosa è una tecnica complessa, che necessita di molto tempo e che non è ancora del tutto standardizzata. Richiede l impiego di bisturi (knives) differenti in relazione alle diverse caratteristiche della lesione o ai diversi momento dell intervento e di accessori che vengono continuamente aggiornati, nell intento di rendere la tecnica di escuzione più agevole. Si comprende pertanto come la dissezione sottomucosa è una procedura che necessita di un lungo training e di una notevole esperienza, soprattutto per un impiego a livello dell esofago. Per tutte queste ragioni è evidente che il ricorso a tale tecnica ell esofago di Barrett debba essere limitato a casi e situazioni estremamente selezionati. In ogni caso la dissezione sottomucosa non è assolutamente indicata nella rimozione di tessuto non neoplastico con interessamento esclusivo della mucosa. TERAPIA FOTODINAMICA (PDT) : La terapia fotodinamica (PDT) è stata riconosciuta dalla FDA (US Food and Drug Administration) per il trattamento dell esofago di Barrett
65 con displasia di alto grado. E una tecnica chimica basata sull utilizzo di un farmaco fotosensibilizzante che, quando viene eccitato da un fascio di luce, produce radicali liberi che portano a morte le cellule. Trascorse 48 ore dall iniezione intravenosa del farmaco foto sensibilizzante (in genere il Photofrin), il paziente viene sottoposto ad endoscopia. Il Photofrin iniettato rende tutti i tessuti (compresa la mucosa di Barrett) sensibili alla luce. Durante l endoscopia una luce laser viene indirizzata sulla mucosa di Barrett, causticandola. I pazienti vengono successivamente trattati con IPP a dosaggio pieno per controllare il RGE e favorire la normale riepitelizzazione dell'esofago. Inizialmente la PDT è stata proposta per curare l adenocarcinoma intramucoso insorto sul Barrett; successivamente sono stati condotti diversi studi finalizzati a valutare l impatto della procedura sulla displasia, sia lieve che severa, e sulla metaplasia. Il più significativo tra questi si è svolto negli U.S.A e, su circa 100 pazienti con HGD, ha dimostrato una percentuale di remissione completa del 77% e una percentuale di progressione verso il cancro dopo PDT del 13%, concludendo che la terapia fotodinamica riduce significativamente ma non elimina il rischio di evoluzione cancerosa 10. Ulteriori studi hanno riscontrato una regressione della metaplasia pari solo al 52%, associata a un rischio significativo di recidive e di stenosi post-trattamento, verificatesi in circa la metà dei soggetti trattati. Infine, i costi poco 10 Overholt BF, Wang KK, Burdick JS et al. Five-year efficacy and safety of photodynamic therapy with Photofrin in Barrett s highgrade dysplasia. Gastroenterologist, 2007; 66:
66 contenuti e la difficoltà di applicazione, oltre alle problematiche sopraccitate, ne hanno determinato l esclusione dalla pratica clinica prima in Europa e poi negli U.S.A. 11. ELETTROCOAGULAZIONE MULTIPOLARE (MPEC): L Elettrocoagulazione multipolare (MPEC) è una tecnica termica che si serve di un passaggio di corrente elettrica tale da provocare un rialzo termico a livello della mucosa esofagea. L'aumento della temperatura è cosi rapido ed intenso da provocare la coagulazione delle cellule con conseguente necrosi. La necessità di porre l elettrodo a stretto contatto con la parete del viscere aumenta, però, il rischio di perforazione. ARGON PLASMA COAGULATION (APC) : L Argon Plasma Coagulation (APC) è una metodica no-touch che sfrutta una corrente monopolare ad alta frequenza veicolata dal gas Argon ionizzato. Il principale vantaggio è sicuramente il costo contenuto, ma anche gli svantaggi non sono trascurabili, essendo una tecnica operatore-dipendente che richiede elevati tempi di applicazione e che, essendo no-touch, non garantisce un applicazione uniforme dell energia erogata su tutta la superficie da trattare. L incidenza di complicanze maggiori, quali perforazioni, stenosi e sanguinamenti, non 11 Sampliner RE. Endoscopic Therapy for Barrett s Esophagus. Clinical Gastroenterology and Hepatology, 2009; 7:
67 è irrilevante, in particolar modo in caso di long Barrett e, soprattutto, è stata stimata una percentuale di recidiva pari al 12%, nonostante la terapia di mantenimento con PPI! A tutt oggi, quindi, l APC è ritenuta utile nel trattamento di short Barrett, di piccole isole metaplastiche o displastiche, di residui derivanti da un incompleta ablazione ottenuta con altre tecniche e in caso di mancata disponibilità di altri dispositivi più costosi. CRIOTERAPIA : La crioterapia rientra tra le tecniche di ablazione termica e si avvale di sostanze, come l azoto liquido o il diossido di carbonio, capaci di raggiungere bassissime temperature determinando, così, il danneggiamento della mucosa patologica (l azoto liquido raggiunge temperature inferiori a -196 C). La metodica si è rivelata soddisfacente, portando all eradicazione completa della metaplasia o della displasia in circa l 80% dei casi 12, ma purtroppo gravata da un rischio di perforazione piuttosto alto dovuto all insufflazione di notevoli volumi di gas necessari per la procedura. Gli studi a disposizione, inoltre, non randomizzati, senza gruppo di controllo e con follow-up troppo brevi, non possono essere considerati del tutto affidabili nè dirimenti. TERAPIA LASER CON CO2 : 12 Sampliner RE. Endoscopic Therapy for Barrett s Esophagus. Clinical Gastroenterology and Hepatology, 2009; 7:
68 La terapia laser con CO2 si sta dimostrando una tecnica precisa e capace di agire in profondità, ma al momento è ancora in fase di sperimentazione su modelli animali. ABLAZIONE CON RADIOFREQUENZA Tutte le tecniche endoscopiche fin qui esaminate presentano delle prerogative positive, ma tutte, parimenti, presentano delle notevoli limitazioni che ne condizionano le possibilità di impiego nell esofago di Barrett in ordine al raggiungimento degli obiettivi in precedenza indicati. In particolare, per quanto riguarda l ablazione della metaplasia, nessuna delle summenzionate tecniche risulta soddisfacente, o per la notevole incidenza di complicanze (stenosi, perforazione), o per l impossibilità di ottenere l eliminazione completa (relativamente all estensione od alla profondità), con la conseguenza di un alto tasso di recidiva. Questo stato di cose sembra essersi modificato con l avvento di una nuova metodica di trattamento endoscopico, rappresentata dall ablazione con radiofrequenza (RFA). Tale tecnica costituisce il principale oggetto di questa trattazione e ad essa, pertanto, verrà dedicata un attenzione più approfondita. ABLAZIONE CON RADIOFREQUENZA ( HALO 360 SYSTEM) La radiofrequenza: è una tecnica che utilizza il calore per distruggere
69 un tessuto danneggiato o tumorale. L ablazione (o coagulazione) con radiofrequenza è una tecnica in cui il tessuto viene riscaldato fino a quando non è più vitale. E un tipo molto specifico di ablazione, in cui viene erogata l'energia termica in modo molto preciso e controllato. Il tessuto dell esofago di Barrett è molto sottile (pochi micron) ed è quindi un buon candidato per la rimozione con energia ablativa a radiofrequenza. Lo scopo delle terapie ablative è quello di produrre, come esito del processo riparativo, la ricostituzione del rivestimento epiteliale squamoso e ciò si può realizzare solo se la cicatrizzazione avviene in ambiente anacido. Il risultato di una completa e stabile riepitelizzazione costituirebbe finalmente la soluzione di tutte le problematiche connesse alla prevenzione dell'adenocarcinoma. Il trattamento ablativo dovrebbe contemperare le seguenti esigenze: garantire la totale distruzione, anche in profondità, della mucosa metaplastica evitando la persistenza di residue aree di MI che possano riscontrarsi anche al di sotto dell'epitelio squamoso neoformato; ridurre il più possibile i disagi per il paziente (necessità di trattamenti ripetuti) e le complicanze (dolore, perforazione, emorragia, stenosi); è importante considerare, infatti, che in questo caso il trattamento riguarda una lesione ancora benigna. L ablazione con radiofrequenze si è rivelata fin da subito una tecnica semplice e sicura, tanto che attualmente negli U.S.A. ha sostituito quasi completamente l utilizzo di tutte le altre metodiche e anche
70 nel trattamento dell Esofago di Barrett, complicato e non. Tale tecnica è effettuata con un sistema prodotto dall azienda BARRX MEDICAL chiamato HALO 360 SYSTEM. Informazioni tecniche L HALO 360 SYSTEM è costituito da un catetere filo guidato, dotato all estremità di un emettitore di radiofrequenze (RF) a pallone (fig.8), e un generatore di RF (fig. 9). (Fig.8: sonda per l emissione di RF) Il catetere a pallone per l emissione di RF è ricoperto da 60 microelettrodi circonferenziali a polarità alternata, che formano un emettitore di RF cilindrico lungo 3 cm. I microelettrodi emettono impulsi di radiofrequenza di una potenza pari a 10 J/cm² in presenza di metaplasia, 12 J/cm² in caso di displasia e breve durata (< 1 sec.), determinando una necrosi circonferenziale, uniforme e superficiale di 0,5 1 mm. Il diametro del pallone da usare viene scelto in base a una preventiva
71 misurazione del diametro esofageo con uno specifico catetere di prova, che serve a far sì che il pallone deputato al trattamento, possa aderire perfettamente e uniformemente a tutta la mucosa da ablare. Attualmente sono disponibili palloni di 6 diverse misure: 18, 22, 25, 28, 31 e 34 mm. (Fig.9: generatore per l emissione di RF) Il generatore è invece costituito da una serie di pulsanti di facile utilizzo per la gestione della temperatura, della potenza di emissione di calore ; da connettori vari e da un pedalino per la gestione esterna dell apparecchio durante la procedura da parte del chirurgo. Quando è indicato? L HALO 360 SYSTEM è un sistema utilizzato in primis nel trattamento dell Esofago di Barret, ma può essere utile anche neel ulcera esofagea, malformazioni artero- venose, gastric antral vascular ectasia (GAVE).
72 Modalità d uso (fig.11) L ablazione con radiofrequenza è un intervento chirurgico effettuato in sedo analgesia profonda. La procedura prevede una serie di fasi successive, che devono essere eseguite tutte in maniera corretta e precisa. Per ottenere il miglior risultato dal trattamento con radiofrequenza è indispensabile che il pallone dell Halo 360 su cui sono collocati gli elettrodi, una volta gonfiato aderisca nella giusta maniera alla parete esofagea, mantenendo un adeguato contatto su tutta la superficie, senza esercitare un eccessiva pressione. Solo in questo modo sarà possibile, infatti, che l energia erogata possa determinare l effetto voluto, e cioè una necrosi circonferenziale, uniforme e superficiale (0,5 1 mm) riguardante l epitelio colonnare superficiale, la lamina propria e parte della muscolaris mucosae, senza coinvolgimento della sottomucosa (fig. 10) 13. (Fig.10: Sonda posta a contatto con l esofago terminale) In considerazione del fatto che il calibro dell esofago può essere variabile, così come è variabile la compliance della parete, è pertanto necessario che si scelga il pallone di calibro più adatto per il singolo paziente. Non a caso il sistema prevede la possibilità di utilizzare palloni di calibro differente tra i quali scegliere preventivamente quello giusto. L energia viene erogata, previa detersione del viscere con acetilcisteina e acqua e valutazione endoscopica con NBI (Narrow Band Imaging - immagine a banda ristretta che sfrutta la luce sulla banda del verde e del blu), a partire da circa 1 cm al di sopra del 13
73 margine prossimale dell epitelio patologico fino a 1 cm al di sotto del margine distale. L ablazione con Halo 360 è indicata in caso di metaplasia, LGD o HGD circonferenziale > 2cm o di multiple isole o lingue di tessuto patologico 14. In presenza di aree circonferenziali < 2cm, lingue piccole, isole diffuse, linea Z irregolare o localizzazione giunzionale è indicato l utilizzo dell Halo 90, un catetere montato sulla punta dell endoscopio, dotato di un elettrodo di superficie lungo 30 o 40 mm e largo 13 mm, ideato allo scopo di eliminare le lesioni focali o i residui post-trattamento con Halo 360. Affinché l ablazione risulti completa, dopo la prima applicazione di RF è importante rimuovere dall esofago tutti i coaguli prima di procedere all applicazione successiva. La tecnica è sicura e ripetibile: dopo un periodo di almeno 2 mesi dalla prima ablazione, è possibile riproporre il trattamento con Halo ma più spesso è sufficiente l Halo 90 - per rimuovere eventuali residui di malattia. Generalmente sono sufficienti da 1 a 4 sedute per ottenere la bonifica completa della mucosa esofagea. Dopo il trattamento endoscopico, il paziente deve proseguire la terapia di mantenimento con PPI per controllare il reflusso gastro esofageo, che è il primum movens della patologia. In alternativa, può scegliere di sottoporsi a plastica antireflusso. 14 Pouw RE, Sharma VK, Bergman JJ, Fleisher DE. Radiofrequency ablation for total Barrett s eradication: a description of the endoscopic technique, its clinical results and future prospects. Endoscopy, 2008; 40:
74 (fig.11.) Trattamento endoscopico con RFA nei vari tipi di Barrett. Quando è controindicata e Quali sono le più importanti avvertenze? L ablazione con Radiofrequenza nell Esofago di Barrett è controindicato in alcune situazioni quali: gravidanza soggetti che hanno effettuato radioterapia dell esofago varici esofagee a rischio sanguinamento esofagite eosinofila. Gli effetti collaterali,più diffusi, previsti dopo il trattamento invece, sono: dolore toracico
75 mal di gola odinofagia disfagia febbre Quelli invece meno diffusi sono: lacerazioni della mucosa sanguinamenti acuti minori formazione di stenosi emorragie trasfusioni dovute a gravi emorragie Molto importante è l attenzione che il medico deve avere nei confronti di pazienti con vomiti post trattamento, poiché questo può comportare perforazioni esofagee, aspirazioni e morte. L ablazione con radiofrequenza col sistema HALO non va utilizzato nei seguenti casi: soggetti trattati precedentemente con altre tecniche ablative soggetti che hanno meno di 18 anni esofago di barrett con una lunghezza che supera i 6 cm stenosi esofagee che impediscono il passaggio dell endoscopio soggetti trattati precedentemente con mucosectomia o sottomucosectomia nodularità della mucosa esofagea displasia. Studi scientifici Numerosi studi hanno dimostrato la superiorità dell ablazione con
76 radiofrequenza, sia rispetto alla sorveglianza, che rispetto alle altre metodiche. Tra i più importanti, si annovera lo studio condotto da Shaheen et al. tra 19 centri degli Stati Uniti. 101 pazienti sono stati sottoposti a RFA; di questi, 43 affetti da HGD (displasia alto grado) e 58 da LGD (displasia basso grado) : dopo 12 mesi, la displasia era stata eradicata nell 85% dei casi trattati e solo nel 24% nel gruppo di controllo. Tra i 101 pazienti trattati si sono verificati solo 5 casi di stenosi, risolte con un massimo di due dilatazioni endoscopiche 15. Un ulteriore studio è stato condotto alla Mayo Clinic da Sharma et al.: l ablazione completa della displasia si è avuta nel 95% di 39 pazienti con LGD e nel 79% di 24 pazienti con HGD sottoposti ad Halo System. Altro studio prospettico condotto da Sharma et al.: tra 10 pazienti con LGD, la guarigione si è registrata nel 100% dei casi, con una percentuale di stenosi pari allo 0%! Concludiamo questa breve analisi dei dati della letteratura con le linee guida dell American Gastroenterological Association (AGA) del 2011 in riferimento all evidence-based relativamente al ruolo delle terapie endoscopiche nell Esofago di Barrett: Le tecniche endoscopiche attualmente utilizzate per eradicare l esofago di Barrett comprendono RFA, PDT, crioterapia, laserterapia e mucosectomia. Le tecniche utilizzate più frequentemente, da sole o in combinazione, sono la radiofrequenza e la mucosectomia. Le evidenze relative all efficacia di 15 Pouw RE, Sharma VK, Bergman JJ, Fleisher DE. Radiofrequency ablation for total Barrett s eradication: a description of the endoscopic technique, its clinical results and future prospects. Endoscopy, 2008; 40:
77 tali tecniche sono emerse rapidamente nell ultima decade (Quality of evidence: moderata). Sebbene la RFA e la PDT non sono mai state confrontate direttamente in trials controllati, la RFA sembra avere un efficacia almeno comparabile con un numero sicuramente inferiore di eventi avversi rispetto alla PDT(Quality of Evidence: Moderata) Relativamente all ablazione della metaplasia nell intento di ottenere la ricostituzione di un epitelio con le caratteristiche del normale rivestimento squamoso in tutta l estensione della mucosa esofagea, senza la persistenza di foci di residua metaplasia al di sotto dell epitelio neoformato è stato evidenziato: la RFA può determinare la reversione verso l epitelio squamoso in un elevata percentuale di pazienti con Barrett in differenti stadi di evoluzione. I dati ad oggi dimostrano che la reversione verso l epitelio squamoso può persistere fino a 5 anni di follow up. (Quality of Evidence: Alta) Non vi sono trial controllati in grado di dimostrare che i trattamenti di ablazione endoscopica, inclusi la radiofrequenza e la crioterapia, siano più efficaci o più convenienti in termini costo/beneficio, rispetto alla sorveglianza, nel ridurre il rischio di cancerizzazione dei pazienti con EB senza displasia (Quality of evidence: molto bassa) La terapia con radiofrequenza nel Barrett con displasia lieve porta alla reversione verso un normale epitelio squamoso in oltre il 90% dei casi. (Quality of Evidence: Alta) La terapia con radiofrequenza in pazienti con displasia severa riduce la progressione verso il cancro, come dimostrato in un trial randomizzato sham-controllato. Ulteriori studi non controllati hanno evidenziato una simile riduzione della progressione neoplastica ed hanno sostenuto che la RFA è in grado di ottenere la reversione verso l epitelio squamoso in un ampia percentuale di casi (Quality of evidence: Alta).
78 Gli stessi successi sono stati dimostrati anche a Roma da una sperimentazione condotta dall equipe del Prof. Paolo Trentino presso il Policlinico Umberto I. Tra i pazienti, reclutati da numerosi centri di tutta la Penisola tra cui il Servizio di Chirurgia endoscopica della Seconda Università di Napoli, e condotti nella Capitale per il trattamento, alcuni presentavano solo metaplasia, altri metaplasia e displasia. La regressione completa della patologia rappresentava l endopoint primario; tra quelli secondari c erano invece la minima incidenza di complicanze e la dimostrazione dell efficienza della procedura in termini economici. Tra novembre 2009 e ottobre 2011 sono stati trattati 33 pazienti, di cui 26 maschi e 4 femmine, di età compresa tra i 54 e gli 84 anni. Macroscopicamente, il Barrett appariva circonferenziale in 13 casi, non circonferenziale nei restanti 20. Dal punto di vista istologico, 22 pazienti presentavano solo metaplasia, 6 LGD, 3 HGD, 2 adenocarcinoma intramucoso. La procedura è stata eseguita 69 volte (da una a 4 volte per ogni paziente). I risultati sono stati ancora una volta entusiasmanti: nonostante 17 casi siano ancora in trattamento, ad oggi si sono registrate ben 15 remissioni complete e 1 unico fallimento. Entro la prima settimana si sono verificate complicanze in 12 casi, ma tutte transitorie e di entità trascurabile: dolore retrosternale, febbre, odinofagia, e in un solo caso si è avuto sanguinamento dopo 12 giorni dal IV trattamento! -I risultati ottenuti, che fanno ipotizzare una percentuale di remissione completa, sia della metaplasia che della
79 displasia, superiore al 90% dopo un follow-up di 5 anni, hanno inequivocabilmente dimostrato l efficacia del trattamento con radiofrequenza nella prevenzione dell adenocarcinoma, la superiorità dei suoi effetti terapeutici rispetto alla sorveglianza endoscopica e la bassissima incidenza di complicanze maggiori. Pertanto, anche se attualmente la pratica clinica promuove il ricorso all Halo System nei soli casi di displasia, la ricerca scientifica si sta muovendo in direzione preventiva per affermare i vantaggi indiscussi di una metodica che, senza complicanze o costi eccessivi, può effettivamente eliminare la metaplasia iniziale ed impedire l eventuale evoluzione cancerosa della malattia.
80 L ablazione con radiofrequenze nell Esofago di Barrett senza displasia Nonostante il rischio lifetime di evoluzione maligna della metaplasia semplice sia relativamente basso, pari al 5% nei maschi e al 3% nelle femmine, gli studi riportati nei capitoli precedenti hanno dimostrato inequivocabilmente i vantaggi dell utilizzo di una tecnica sicura ed efficace quale l Halo System nel combattere una patologia cronica con potenziale evoluzione maligna. L ablazione con radiofrequenze sembra rispecchiare il profilo di una terapia ideale, con percentuali di guarigione completa superiori al 90% a 5 anni di follow-up, bassissima incidenza di complicanze maggiori (vicina allo 0%) e costi contenuti. Oltre a questi, un altro vantaggio da tenere in debita considerazione è la quasi totale assenza di recidive dovuta alla riepitelizzazione dell esofago con epitelio neosquamoso, del tutto simile al rivestimento fisiologico della mucosa esofagea normale. Tutte le aberrazioni molecolari tipiche delle cellule metaplastiche scompaiono nel nuovo epitelio (cosa che, invece, non avviene con altre tecniche di ablazione come la terapia fotodinamica) e, soprattutto, l RFA sembra risolvere il problema del cosiddetto buried Barrett (o buried glands ), per cui si intende qualsiasi tipo di epitelio colonnare residuo coperto da tessuto neosquamoso superficiale e privo di comunicazione con
81 l epitelio di superficie 16. Ed effettivamente, la questione delle buried glands pone non pochi problemi nella gestione del paziente trattato per metaplasia, dal momento che queste ghiandole nascoste sotto il neoepitelio possono rimanere misconosciute alle biopsie di controllo ed evolvere verso la displasia e l adenocarcinoma. Tutte le altre metodiche endoscopiche si sono rivelate fallimentari in questo senso, con percentuali di buried Barrett che andavano dal 7.4 al 27,3% 17 e solo l RFA ha mostrato una percentuale accetabile (0,4%): uno studio di 12 mesi condotto nel 2008 ha reclutato 10 pazienti (7 casi di metaplasia, 2 di LGD e 1 di HGD); dopo il trattamento con RFA, per ogni paziente sono state eseguite biopsie mirate a 3 mesi e a 12 mesi: alla fine del follow-up (XII mese) tutti i 10 pazienti avevano riportato la remissione completa; l unico caso di buried glands si era registrato nella prima biopsia dopo il trattamento in un soggetto di sesso maschile, di 54 anni, con una metaplasia iniziale circonferenziale di 8cm: la procedura, quindi, è stata ripetuta con Halo 360 e, alla fine dei 12 mesi, anche il buried Barrett era scomparso. Complessivamente, dunque, su un totale di 247 biopsie post-ablazione, solo una ha rivelato la persistenza della patologia 18. Tra le altre cose, bisogna ricordare che l Halo System è una tecnica 16 Hernandez JC, Reicher S, Chung D, Pham BV, Tsail F, Disibio G, French S, Eysselein VE. Pilot series of radiofrequency ablation of Barrett s esophagus with or without neoplasia. Endoscopy, 2008; 40: Hornick J, Blount P, Sanchez C et al. Biologic properties of columnar epithelium underneath reepithelialized squamous mucosa in Barrett s esophagus. Am J Surg Pathol, 2005; 29: Hernandez JC, Reicher S, Chung D, Pham BV, Tsail F, Disibio G, French S, Eysselein VE. Pilot series of radiofrequency ablation of Barrett s esophagus with or without neoplasia. Endoscopy, 2008; 40:
82 di ablazione superficiale che, indipendentemente dall operatore, non può creare insulto alla sottomucosa (come invece può avvenire usando l APC, la PDT o la EMR) e questo riduce ulteriormente il rischio di complicanze. Ablazione dell EB non displastico o sorveglianza? Dopo aver passato in rassegna i vantaggi innovativi e i risultati entusiasmanti dell RFA, condicio sine qua non per la sua affermazione nella pratica clinica, è opportuno soffermarsi sul razionale della terapia: perché preferire l ablazione del Barrett non displastico alla sorveglianza? Innanzitutto bisogna considerare il punto di vista e lo stato d animo del paziente, consapevole di essere affetto da una malattia cronica che quasi certamente non regredirà da sola e che forse evolverà verso una condizione maligna altamente aggressiva. La sorveglianza endoscopica rappresenta per lui un appuntamento fisso, sicuramente fastidioso, a cui presentarsi regolarmente, e che, nonostante tutto, un giorno improvvisamente potrà rivelargli la presenza di una malattia mortale. In secondo luogo, la diagnosi di metaplasia è raramente una diagnosi di certezza: il protocollo di Seattle non riesce a caratterizzare l intera superficie di un Barrett, molto spesso non c è accordo tra gli anatomo-patologi nel riconoscere la displasia e tutte le tecniche di rimozione endoscopica non sono in grado di dare informazioni precise sulla profondità di invasione e sull infiltrazione dei vasi
83 sanguigni e linfatici: questo significa che, una volta che la metaplasia si è trasformata in displasia o adenocarcinoma, diventa difficile effettuare una corretta stadiazione e proporre un adeguato trattamento. Infine, le analisi costi/benefici condotte finora suggeriscono la netta superiorità dell ablazione endoscopica rispetto ai costi elevati della sorveglianza, che invece comporta una spesa annuale negli U.S.A. -pari a 290 milioni di dollari per una strategia che in termini di sopravvivenza ha rivelato, attraverso studi di coorte e casocontrollo, solo risultati contrastanti 19. Al contrario, è stato dimostrato che, se la percentuale di displasia residua dopo ablazione endoscopica è inferiore al 40% e se il costo complessivo della procedura non supera i $ per singolo paziente (come avviene con l Halo System), allora il trattamento può essere considerato più cost-effective rispetto alla sorveglianza. Infine, in assenza di displasia, la strategia più efficiente prevede l ablazione endoscopica, da eseguire con una tecnica che garantisca la risoluzione completa in più del 40% dei casi, seguita dalla sorveglianza solo per quei pazienti in cui la metaplasia non sia stata eradicata completamente. Tra le tecniche di ablazione endoscopica, poi, la RFA è sicuramente la più vantaggiosa in termini di costi ed efficacia: basti pensare che, 19 Inadomi JM, Samsouk MA, Madanik RD, Jennifer s, Thomas P. A Cost-Utility Analysis of Ablative Therapy for Barrett s Esophagus. Gastroenterology, 2009; 136:
84 rispetto alla sorveglianza, raccoglie un ICER (incremental cost -effectiveness ratio) di soli 5839 $ per QALY (quality-adjusted life year) guadagnato, mentre con la terapia fotodinamica l ICER si attesta intorno ai $ 20! Comunque, a prescindere da qualsiasi analisi economica e da tutti i vantaggi dimostrati, la comunità scientifica è d accordo nel preferire le strategie in grado di ridurre lo sviluppo di un cancro a quelle che, invece, possono portare solo a una diagnosi precoci. 20 Inadomi JM, Samsouk MA, Madanik RD, Jennifer s, Thomas P. A Cost-Utility Analysis of Ablative Therapy for Barrett s Esophagus. Gastroenterology, 2009; 136:
85 Conclusioni In conclusione si può affermare con certezza, dati gli studi scientifici riportati nei paragrafi precedenti, che l Ablazione con Radiofrequenza dell Esofago di Barrett è una tecnica molto efficiente sia in termini di rischio- efficacia, sia in termini di costobeneficio. A tal proposito vorrei concludere con una domanda rivolta al SSN: Perché, dopo circa due anni dalla richiesta d acquisto di tale dispositivo (HALO 360 SYSTEM), da parte del reparto di Chirurgia., ancora oggi i pazienti Campani non possono usufruire di tale procedura nella propria regione, nonostante ci siano dottori formati ed in grado di poter effettuare senza alcun problema tale tipo di intervento? In attesa non di una risposta, ma di fatti concreti, ci auguriamo e speriamo che anche i nostri dottori abbiano la possibilità di portare a termine la cura dei propri pazienti e di non essere più costretti a far si che gli stessi vengano trasferite in altre strutture ospedaliere, costringendoli ad ulteriori spese e disagi.!
86 Il Cancro dell esofago Incidenza. Il tumore dell esofago è una neoplasia relativamente rara, si colloca al nono posto nel mondo con incidenza di 3-4 casi ogni abitanti. Presenta una notevole variabilità nella distribuzione geografica, con maggiore incidenza in alcuni paesi quali Cina, Iran,Portorico e Singapore ove la mortalità è più elevata e l incidenza è pari a 30/ abitanti; in Europa e in USA rappresenta l 1% di tutti i tumori maligni e la sesta causa di morte per neoplasia nell uomo. Negli ultimi decenni, sia in USA che in Canada ed Europa Occidentale si è registrato un incremento di incidenza per tumore dell esofago da correlare all istotipo adenocarcinoma. In Italia si verificano circa nuovi casi/anno; le regioni del nord sono queòòe con la maggior incidenza. Sesso. Il tumore dell esofago colpisce principalmente il sesso maschile con rapporto 3/1. Età. L incidenza aumenta progressivamente dopo i anni; l età media di insorgenza è intorno ai 66 anni. Razza. La variante squamocellulare è 6 volte più frequente nei maschi neri rispetto ai bianchi, l adenocarcinoma 3 volte più frequente nei bianchi rispetto ai neri. Sede Anatomica. Il 15% dei carcinomi esofagei origina dal 1/3 superiore dell esofago, il 50% dal 1/3 medio, il rimanente 35% dal 1/3 inferiore; in quest ultima sede è nettamente prevalente l adenocarcinoma associato ad esofago di Barrett. Eziologia. Fattori di rischio dominanti sono il consumo di tabacco e alcol per i soggetti maschi; nelle donne l aumento di incidenza negli ultimi anni è associato ad un più elevato consumo di sigarette. L alcol aumenta il rischio di carcinoma squamoso dell esofago ma non quello dell adenocarcinoma. I fumatori hanno un rischio 5-10 volte maggiore rispetto ai non fumatori; il rischio è strettamente correlato al numero di sigarette consumate e agli anni complessivi di abitudine al fumo. Il rischio di sviluppare il carcinoma squamoso dell esofago nei soggetti che consumano contemporaneamente bevande alcoliche e sigarette aumenta fino a 100 volte. Dieta. Numerosi studi hanno messo in evidenza l'importanza della dieta e delle carenze nutrizionali nell'insorgenza del carcinoma esofageo: assunzione di frutta e verdura, arricchimento della dieta con beta carotene, vitamina E e selenio sembrano svolgere un ruolo protettivo, mentre un carente stato nutrizionale e un aumentata assunzione di carni rosse a incrementarne il rischio. Acalasia. Malattia caratterizzata da alterata motilità della muscolatura esofagea associata a mancato rilasciamento dello sfintere esofageo inferiore; il 14-16% dei soggetti affetti da acalasia sviluppa un tumore squamoso dell esofago dopo un periodo medio di 20 anni. Lesioni da caustici. Circa l 1-7% dei pazienti affetti da carcinoma esofageo presenta un anamnesi di ingestione di caustici Il periodo di tempo che intercorre tra ingestione di caustici e insorgenza di carcinoma esofageo è di anni; la maggioranza di queste neoplasie insorge nel 1/3 medio dell esofago. Esofago di Barrett. L esofagite da reflusso predispone all'insorgenza dell esofago di Barrett, che è caratterizzato dalla sostituzione dell'epitelio squamoso pluristratificato, che normalmente riveste l esofago distale, con epitelio colonnare metaplasico; si può riscontrare la presenza di uno o di tutti i seguenti tipi di epiteli: di tipo fundico, cardiale e metaplasia intestinale. La displasia e il carcinoma sono particolarmente associati alla metaplasia intestinale. L esofago di Barrett rappresenta da solo il fattore di rischio più importante di adenocarcinoma esofageo; il rischio di cancro è 2-3 volte superiore nei pazienti con esofago di Barrett rispetto ai pazienti con malattia da reflusso gastroesofageo di lunga data ma senza Barrett.
87 Tipi Istologici: Il 90% dei tumori esofagei è costituito da carcinomi squamocellulari e da denocarcinoma; quest ultimo rappresenta oltre l'80% dei tumori insorti su esofago di Barrett. L incidenza del tipo istopatologico di tumore esofageo nelle diverse aree geografiche dipende da molte variabili, inclusi stile di vita e fattori socio-economici. Il carcinoma squamocellulare è associato all'ingestione di sostanze caustiche, all'acalasia e al carcinoma epidermoide della testa/collo. Dal punto di vista molecolare, l istotipo squamoso è differente dall adenocarcinoma esofageo e dall adenocarcinoma del cardias e dello stomaco ed ha un comportamento biologico più aggressivo. Per questo motivo il carcinoma dell esofago medio-toracico ha una prognosi peggiore rispetto all adenocarcinoma del cardias e dell esofago distale. Diagnosi e stadiazione della malattia Nel sospetto di una neoplasia esofagea, gli esami iniziali di scelta sono l esofagogramma con doppio contrasto e/o l esofagoscopia. Lo studio radiologico mostra elevata sensibilità solo nelle forme tardive mentre ha una bassa specificità nelle forme precoci. L esame endoscopico, a differenza dell esofagogramma, ha elevata specificità e sensibilità nella diagnosi, anche delle forme precoci e consente la conferma diagnostica attraverso le biopsie multiple della lesione sospetta con un accuratezza del 94%. L ecoendoscopia rappresenta ancora la metodica più accurata per la valutazione dell infiltrazione parietale della neoplasia e l interessamento dei linfonodi regionali con una accuratezza dell 85% nella determinazione del T e del 79% nell interessamento linfonodale (stadiazione loco regionale). Per tale motivo l ecoendoscopia risulta utile nella selezione dei pazienti potenzialmente candidati a terapie neoadiuvanti mentre presenta molti limiti nella valutazione della risposta al trattamento neoadiuvante. La Tomografia Computerizzata (TC) del torace e dell addome rappresenta in ogni caso l esame di scelta per una completa stadiazione e la valutazione anche di eventuali metastasi a distanza. La Risonanza Magnetica (RM) mostra ha un accuratezza simile alla TC e quindi non aggiunge informazioni aggiuntive rispetto alla TC, che certamente è un indagine più largamente diffusa. La PET può essere di utilità per il rilevamento delle metastasi a distanza ma è soprattutto utile per la valutazione della risposta ai trattamenti neoadiuvanti.. Classificazione TNM e suddivisione in stadi Dal punto di vista anatomo-topografico ed endoscopico l esofago si suddivide nelle seguenti porzioni: Esofago cervicale. Inizia dal bordo inferiore della cartilagine cricoide e termina allo stretto toracico superiore (circa 18cm. dagli incisivi superiori) Esofago toracico superiore. Si estende dallo stretto toracico sino alla biforcazione tracheale ( circa 24cm. dagli incisivi superiori) Esofago toracico medio. E compreso tra biforcazione tracheale ed esofago distale appena sopra la giunzione gastro-esofagea ( circa 32cm. dagli incisivi superiori) Esofago toracico inferiore. Include la porzione intra-addominale dell esofago e la giunzione esofago-gastrica ( circa 40cm. dagli incisivi superiori)
88 Terapia Chirurgica La terapia chirurgica rappresenta ancora la principale forma di trattamento del cancro dell esofago, Il trattamento chirurgico può essere effettuato direttamente nei casi in cui è possibile ottenere una resezione R0. In caso di neoplasie ancora resecabili, ma in stadio
89 più avanzati (da T2 N1 in avanti) la terapia chirurgica viene fatta precedere da in trattamento radio chemioterapico (terapia neoadiuvante) Secondo la sede della malattia la resezione dell esofago deve essere più o meno estesa. Si può andare da resezioni parziali fino all esofagectomia totale. L esofagectomia, comunque, è ancora oggi uno degli interventi chirurgici più impegnativi, sia in termini di morbilità che di mortalità operatoria. Per questo motivo è importante che questa procedura venga effettuata in centri di riferimento che abbiano un adeguata esperienza e che venga praticata in pazienti attentamente selezionati, ovvero in coloro che possono effettivamente beneficiare della resezione per ottenere un prolungamento significativo di quantità e qualità di vita. Quindi un accurata stadiazione preoperatoria è premessa essenziale per il buon esito a distanza della terapia chirurgica. L esofagectomia può essere eseguita per via transtoracica con duplice accesso (laparotomia mediana e toracotomia destra) in caso di resezione parziale dell esofago con anastomosi intratoracica, o con triplice accesso (toracotomia destra seguito da laparotomia e cervicotomia), in caso di esofagectomia totale con anastomosi (esofago gastrica o esofago-colica) in sede cervicale. L altra possibilità è quella di effettuare l esofagectomia a torace chiuso con stripping dell esofago per via trans mediastinica. In questo caso l accesso è quello addominale, attraverso cui si realizza la preparazione dello stomaco da trasporre in torace e la preparazione dell esofago mediastinico per via trans iatale. Il secondo accesso è dato dalla cervicotomia sinistra, attraverso cui si effettua lo stripping dell esofago e l anastomosi tra lo stomaco trasposto ed il piccolo moncone esofageo residuo. Tutto il tempo addominale (preparazione dello stomaco) e la preparazione dell esofago mediastinico per via trans iatale, può essere realizzato anche attraverso un approccio mini invasivo laparoscopico. In questo modo si riduce notevolmente l impatto dell intervento sul paziente, evitando anche la laparotomia. La scelta di utilizzare anche un accesso trans toracico risponde all esigenza di effettuare una linfadenectomia completa, che non è possibile utilizzando la via trans iatale. La scelta dell approccio chirurgico è anche di natura filosofica. Infatti, ci sono chirurghi che credono nella possibilità di una chirurgia radicale curativa e ritengono che un asportazione completa dei linfonodi regionali possa migliorare la sopravvivenza. Altri, invece, sostengono che il cancro dell esofago, tranne che nelle forme molto iniziali, confinate alla mucosa, sia sempre una malattia sistemica. Per questo motivo qualunque intervento avrebbe carattere palliativo e quindi va privilegiato sempre un approccio meno invasivo quali quello a torace chiuso. In effetti, i risultati fino ad oggi non hanno dimostrato che una linfadenectomia estesa migliori la prognosi. Trattamenti alternativi alla chirurgia Con i recenti sviluppi dell endoscopia operativa, le tecniche endoscopiche possono offrire delle alternative alla chirurgia o nelle forme di neoplasie molto superficiali o, al contrario, nelle forme troppo avanzate a scopo palliativo. Nelle neoplaise in stadio precoce (early cancer) confinate alla mucosa è oggi possibile effettuare una resezione endoscopica ad intento curativo. CURE PALLIATIVE: Dilatazione per via endoscopica Non è un trattamento definitivo ma un atto preliminare, di valutazione alla protesizzazione, alla PEG; la dilazione può diventare inefficace dopo 1-2 settimane e pertanto si deve considerare un momento del trattamento o una terapia da eseguire in associazione ad altri trattamenti Terapie ablative endoscopiche Ablazione laser
90 Molto utilizzata per la disostruzione. Il trattamento può essere effettuato con migliori possibilità di successo per recidive di limitate dimensioni. Rivolta maggiormente a pazienti con tumore inoperabile piuttosto che a pazienti con recidiva superficiale. L ablazione mediante laserterapia non è in grado di fornire subito l immediatezza dell alimentazione risolvendo la disfagia: sono necessarie almeno 2 o 3 sedute per ottenere risultati soddisfacenti ma è necessario ripetere il trattamento ogni 2-3 settimane. Il trattamento laser rimane un trattamento costoso e disponibile in pochi Centri specializzati. Ablazione con argon plasma coagulation (APC) Combinazione di gas argon ed energia monopolare che conduce energia senza venir a contatto con i tessuti, favorendo la coagulazione e la necrosi. L APC non ha la profondità del laser, viene però utilizzata nelle emorragie digestive, per necrotizzare i tessuti, utile per ampie superfici, presenta minori costi, una maggiore facilità di impiego, è sicura e ha una minor curva di apprendimento. Rispetto al laser può essere utilizzato con successo e scarse complicanza nel trattamento palliativo di piccole lesioni ma non può servire come terapia disostruttiva. Posizionamento di stent Protesi Costituisce il mezzo più idoneo e immediato per migliorare il sintomo disfagia. Attualmente si utilizzano le protesi metalliche autoespansibili, più costose che hanno soppiantato le protesi in plastica o silicone, impiegate in passato, per facilità di utilizzo e minor complicanze. Indicazioni principali: lesioni stenosanti vegetanti e infiltranti dell esofago toraco-cardiale, fistole esofago-tracheali, fistole mediastiniche. I problemi dopo il posizionamento di una protesi si verificano quando la parte distale della protesi si trova in uno spazio vuoto come a livello cardiale con conseguente rischio di spostamento della protesi stessa (dislocazione della protesi). Problematiche dovute alla protesi si possono presentare inoltre dopo 2-3 mesi con lo occlusione della protesi per presenza di tessuto esuberante (iperplastico) in corrispondenza del margine prossimale della protesi: non si tratta di tessuto neoplastico ma spesso di un tessuto reattivo Ipertrofico. PEG (gastrostomia endoscopica percutanea) Tecnica che consente il posizionamento di una sonda nutrizionale a livello gastrico o digiunale con accesso transparietale in epigastrio, senza ricorrere a laparotomia; risulta più veloce ed economica rispetto alla tecnica chirurgica e si riserva principalmente come soluzione nutrizionale temporanea o definitiva. La procedura viene realizzata con l ausilio dell endoscopia, che rappresenta la guida per effettuare l accesso percutaneo allo stomaco, per seguire tutte le fasi del passaggio della sonda per l alimentazione e per controllarne il posizionamento Il cancro gastrico Epidemiologia Il cancro dello stomaco è ancora oggi tra le neoplasie più frequenti con un incidenza, a livello mondiale, di circa nuovi casi ogni anno. Tuttavia il trend è in diminuzione. Le popolazioni più colpite sono quella giapponese, coreana, cinese, cilena e della Costa Rica. In Europa le popolazioni più colpite sono quella ungherese, finlandese, austriaca ed islandese. L Italia si colloca tra i Paesi con livelli di incidenza e di mortalità intermedi. La CLASSIFICAZIONE DI LAUREN individua due principali istotipi, intestinale e diffuso risultando di particolare interesse per la correlazione con il dato epidemiologico
91 Il carcinoma di tipo intestinale ha il picco d incidenza nei maschi al di sopra dei 60 anni di età, è quasi sempre associato alla preesistenza di lesioni precancerose ed è legato a fattori ambientali. E la forma più frequente nelle popolazioni dove è alta l'incidenza di cancro dello stomaco, caratteristica questa che lo ha fatto definire epidemico Il carcinoma di tipo diffuso ha una frequenza equivalente nei due sessi, manifestandosi però su una popolazione più giovane, non è condizionato da fattori ambientali e la sua omogenea distribuzione nelle varie popolazioni lo ha fatto definire endemico. I fattori di rischio del cancro dello stomaco Un fattore di rischio ormai ben documentato è costituito dalle abitudini alimentari: gli aminoacidi introdotti con la dieta, gli idrocarburi policiclici che si ritrovano nelle carni affumicate o troppo cotte o negli oli usati ripetutamente per friggere, le micotossine come la B2 presente nelle muffe, le diete ricche di carboidrati con alto contenuto di amido o ipersodiche cioè con alimenti troppo salati. Altri fattori sono quelli ambientali come, ad esempio, il contatto lavorativo con il petrolio ed i suoi derivati, il carbone. Negli ultimi decenni un ruolo eziopatogenetico fondamentale è stato attribuito all infezione da Helicobacter pylori che, modificando il micro-ambiente della mucosa gastrica induce gastriti superficiali o gastriti atrofiche multifocali. La gastrite cronica atrofica diffusa può associarsi alla metaplasia intestinale e quindi alla displasia che può esitare nel cancro. Il tipo di cancro dello stomaco correlato ai citati fattori di rischio è il carcinoma gastrico di tipo intestinale, la cui incidenza, quindi, può essere influenzata intervenendo nel modificare le situazioni dietetico ambientali. Non a caso questo tipo di cancro gastrico è quello che ha registrato un decremento d'incidenza mentre il tipo diffuso si è ridotto in modo marginale. Verosimilmente ciò è dovuto al fatto che il cancro di tipo diffuso è sostanzialmente indipendente dai fattori ambientali ed è invece correlato ad un danno genetico Diagnosi del cancro dello stomaco La diagnosi clinica è ancora troppo spesso tardiva in quanto i sintomi sono aspecifici e riconducibili ad una generica gastrite mentre il calo ponderale, il dolore, la nausea ed il rapido riempimento gastrico meglio indirizzano verso un sospetto. La diagnosi strumentale riconosce un buon valore alla radiografia con doppio contrasto ma l esame fondamentale è la gastroscopia che consente di ottenere una diagnosi più precoce e la conferma diagnostica attraverso il prelievo bioptico. Per quanto riguarda la stadiazione l indagine di prima scelta è sempre rappresentata dalla TC multistrato, con e senza mezzo di contrasto, che permette di valutare il grado di infiltrazione parietale, le stazioni linfonodali e le metastasi a distanza. L ecografia addominale, per la sua diffusione e per il fatto di costituire l indagine di prima linea in un elevato numero di casi, può rappresentare l esame che suggerisce la diagnosi, in particolare quando la lesione sia abbastanza voluminosa. Effettuando l indagine previo riempimento del lume gastrico con acqua, si può anche valutare bene lo spessore della parete e quindi il grado di infiltrazione parietale della neoplasia. L ecografia è considerata comunque una metodica di bassa sensibilità per la diagnosi, mentre risulta invece estremamente efficace nella valutazione di eventuali localizzazioni secondarie epatiche. Per tale applicazione l ecografia risulta ancora la metodica di imaging più accurata. L eco-endoscopia trova applicazione soprattutto per ottenere una più precisa definizione del grado di infiltrazione parietale, con una accuratezza intorno al 90%, specialmente utile per valutare l'early gastric cancer. La Risonanza Magnetica non fornisce informazioni aggiuntive rispetto alla TC. La PET o meglio la PET-TC non viene in genere impiegata nella stadiazione iniziale ma trova
92 una specifica indicazione, nella valutazione a distanza dopo chemioterapia adiuvante o comunque nel follow up oncologico.. Stadiazione del cancro dello stomaco Anche per il cancro dello stomaco la prognosi della malattia è direttamente correlata alla stadiazione. Per il cancro dello stomaco si utilizza la classificazione TNM, di seguito riportata Stadiazione T Stadio T1: il tumore è limitato alla mucosa e/o alla sottomucosa. Nell ambito dello stadio T1 andrebbero considerate a parte le neoplasie confinate alla mucosa (il varo early gastric cancer), che possono essere trattati con la sola escissione locale. Stadio T2: il tumore invade la muscolare propria. Stadio T3 il tumore infiltra la sierosa Stadio T4 Il tumore infiltra gli organi adiacenti Stafiazione N Stadio N0 non sono presenti metastasi linfonodali Stadio N1 da 1 a 6 linfonodi interessati da metastasi Stadio N2 da 7 a 15 linfonodi interessati da metastasi Stadio N3 oltre 15 linfonodi interessati Stadiazione M Stadio M0: non sono presenti metastasi a distanza Stadio M1: sono presenti metastasi a distanza Terapia del cancro dello stomaco Per il cancro allo stomaco l'unica terapia realmente efficace è quella chirurgica. Gli interventi chirurgici, in casi selezionati possono essere oggi effettuati anche con tecnica videolaparoscopica. Per gli aspetti legati al trattamento chirurgico negli anni la discussione scientifica si è concentrata prevalentemente sulla necessità di asportare in modo completo lo stomaco o solo in parte in base alla localizzazione ed allo stadio della malattia. Oggetto di dibattito è stata anche l estensione della linfadenectomia e se l esportazione anche dei linfonodi più lontani comportasse un reale beneficio oncologico. Per il primo aspetto si è giunti alla conclusione che nelle forme di tumore vicine al cardias l'intervento di scelta sia la gastrectomia totale mentre nelle forme più vicine al piloro, è possibile eseguire con uguale risultato oncologico una resezione parziale, ovvero una gastroresezione. Questa conclusione si è dimostrata importante in quanto una gastroresezione permette una qualità di vita del paziente sicuramente migliore rispetto ad una gastrectomia. Per quanto riguarda la linfoadenectomia attualmente si è giunti alla conclusione che la sua estensione dovrebbe essere adeguata in funzione della stadiazione anatomopatologica, più che per un significato curativo. Pertanto l opinione nettamente prevalente è quella di effettuare una linfadenectomia nè troppo limitata nè troppo estesa; la prima, infatti, potrebbe risultare inefficace sia in termini oncologici, che di stadiazione, mentre la seconda comporterebbe un rischio di complicanze postoperatorie troppo elevate. Le novità nella chirurgia del tumore gastrico sono costituite dalla terapia endoscopica, dalla laparoscopia e dalla chirurgia robotica. In casi selezionati le nuove tecniche endoscopiche permettono di eseguire un'asportazione locale della neoplasia per via endoscopica senza necessità di intervento chirurgico.
93 La laparoscopia sta trovando applicazione anche nella chirurgia dei tumori dello stomaco. Le esperienze sono ancora preliminari ed i dati non ancora consolidati ma pare tuttavia che l'intervento eseguito per via laparoscopica permetta di ottenere gli stessi risultati oncologici della chirurgia tradizionale con un decorso postoperatorio migliore per il paziente Un ulteriore progresso è l'utilizzo del robot al fine di eseguire con maggiore precisione i gesti chirurgici della tecnica tradizionale. La chirurgia gioca un ruolo anche nella diagnosi della malattia, infatti la laparoscopia ha ormai conquistato un ruolo ben definito nella stadiazione preintervento La chirurgia ha inoltre un ruolo importante nella palliazione con esecuzione, in genere per via laparoscopica, di una gastro-entero-anstomosi che permette di mantenere il transito alimentare, migliorando sensibilmente la qualità di vita del paziente. La terapia del cancro gastrico, è andata progressivamente cambiando negli anni e, da un primo approccio esclusivamente chirurgico (la prima resezione gastrica risale al 1881 ad opera di Billroth), si è oggi arrivati a quello che si definisce in oncologia un approccio multidisciplinare, dove oltre alla chirurgia, la chemioterapia, la radioterapia ed altre terapie, come quelle endoscopiche, vengono variamente combinate col fine di ottenere i migliori risultati ed il minor numero possibile di effetti indesiderati avendo sempre ben chiaro che la qualità della vita è un obiettivo altrettanto importante se non prioritario rispetto alla sopravvivenza. Limitando le osservazioni all' aspetto chirurgico, è importante ricordare che lo stadio della malattia al momento della diagnosi, ovvero la sua diffusione locale e a distanza, costituisce il principale fattore determinante la prognosi e, allo stato attuale delle conoscenze, l'asportazione chirurgica della neoplasia è indispensabile a prescindere da altre eventuali terapie per ottenere la guarigione. Lo schema sottostante illustra le principali modalità resezione gastrica: un resezione subtotale per i tumori localizzati in sede distale (antro); gastrectomia totale per i tumori di corpo, fondo e regione sottocardiale; gastroresezione polare superiore in casi selezionati di neoplasie sottocardiali.
94 Cancro del colon retto Epidemiologia Secondo i dati dei registri tumori, jn Italia nel periodo il tumore del colon-retto è risultato al 4 posto in termini di frequenza fra le neoplasie diagnosticate negli uomini rappresentando l 11% del totale dei tumori, e al 3 posto nelle donne rappresentando l 12% del totale. Esiste una discreta variabilità geografica dell nel nostro Paese tra aree con i tassi più alti (entro nord) ed aree con tassi più bassi (sud e isole). Per quanto riguarda gli andamenti nel tempo, il tumore del colon-retto mostra una tendenza all aumento dimentre la mortalità appare in riduzione negli ultimi trent anni; tale osservazione è principalmente correlata alla maggiore efficacia delle terapie, alla possibilità di porre diagnosi precoci ed all introduzione dello screening. E in genere unadell età media: raramente compare al di sotto dei 45 anni raggiungendo un picco d incidenza nelle persone di età superiore ai 75 anni. La distribuzione di insorgenza lungo il grosso intestino è varia: nel 16% dei casi si localizza al cieco e colon ascendente, nell 8% al traverso e flessura splenica, nel 6% al colon discendente, nel 20% al sigma e nel 50% nel retto. Fattori di rischio I fattori di rischio sono: 1. di tipo ereditario (es poliposi familiare o altre patologie come la sindrome di Lynch consistente nella tendenza ereditaria a sviluppare carcinomi del colon in assenza di poliposi), 2. Di tipo non ereditario (es malattie infiammatorie croniche come retto-colite ulcerosa e morbo di Crohn; età per l incidenza superiore tra le persone di età compresa tra i 60 e i 70 anni ), 3. alimentare (dieta ipercalorica e ricca in grassi animali dieta povera di scorie). Nella massima parte dei casi, comunque,(in oltre il 90% dei casi) i tumori maligni del colon derivano da preesistenti polipi. La probabilità che un polipo del colon evolva verso una forma invasiva di cancro dipende dalla sua dimensione: minore del 2 % per dimensioni inferiori a 1,5 cm, dal 2 al 10 % per dimensioni di 1,5-2,5 cm, maggiore del 10 % per dimensioni superiori a 2,5 cm. Manifestazioni cliniche La diagnosi didel colon può essere secondaria ad accertamenti eseguiti per la comparsa di sintomi o può essere il risultato della partecipazione ad una campagna di screening. Una serie di fattori (quali la sede anatomica d insorgenza, estensione, presenza o assenza di fenomeni ostruttivi o emorragici) condizionano la comparsa della sintomatologia clinica, peraltro estremamente varia nelle sue manifestazioni. Poiché le neoplasie in stadio iniziale tendono a produrre sintomi scarsi, poco specifici e quindi spesso trascurati (modifiche delle abitudini intestinali, vaga dolorabilità addominale, perdita di peso senza causa apparente, stanchezza persistente) è necessario che sempre maggiori sforzi siano indirizzati verso il potenziamento delle campagne di screening per la diagnosi precoce del tumore del colon retto. Comunque, per le localizzazioni del colon di destra più spesso prevalgono i sintomi aspecifici mentre per il colon di sinistra tendono a prevalere i disturbi legati alla sub
95 occlusione intestinale associati a dolori addominali, che dipendono dall ostruzione provocata dal tumore. I sintomi più frequenti in rapporto alla sede sono i seguenti: COLON DESTRO Anemia Calo ponderale (perdita di peso) Variazioni dell alvo (con tendenza alla diarrea) Dolore addominale Massa addominale palpabile Ematochezia (perdita di sangue misto alle feci) COLON SINISTRO Alterazioni dell alvo (con tendenza alla stitichezza) Dolore addominale Occlusione intestinale Anemia Ematochezia (perdita di sangue misto alle feci) SIGMA Stipsi (stitichezza) Difficoltà all evacuazione Ematochezia (perdita di sangue misto alle feci) Dolore addominale Diagnosi: Per lo screening la metodica più diffusa è quella della ricerca del sangue occulto nelle feci che va effettuata in tre determinazioni successive ad una distanza di qualche giorno l una dall altra. In caso di positività è necessario proseguire l iter diagnostico con indagini più approfondite. Obbligatoria in ogni caso di sospetto tumore del grosso intestino resta l esecuzione dell esplorazione rettale, capace di escludere la presenza di una neoformazione localizzata a livello del retto e di rilevare un eventuale sanguinamento macroscopico. Esistono poi diverse indagini strumentali, caratterizzate da diversi livelli di invasività, che possono aiutare nel percorso diagnostico: CLISMA OPACO A DOPPIO CONTRASTO: è una tecnica radiologica effettuata dopo aver fatto ingerire o aver introdotto nel retto e nel colon a monte attraverso un clistere un mezzo di contrasto. Per consentire una maggiore adesione del mezzo di contrasto baritato alla parete del l intestino si introduce attraverso il clistere una certa quantità di gas (anidrite carbonica). Si tratta di una metodica che ha perso molto della sua importanza con l avvento
96 della colonscopia che, oltre alla visualizzazione della lesione consente una diagnosi di natura.. COLONSCOPIA: è un esame che permette di visualizzare la parete interna dell intestino attraverso l impiego di una sonda a fibre ottiche inserita attraverso l ano e fatta risalire fino, se possibile, alla valvola ileo-cecale. Come si è detto, oltre alla visione diretta della lesione la colonscopia consente inoltre di effettuare di prelevare un frammento di tessuto (biopsia) da inviare all esame microscopico per una conferma della diagnosi. Per un ottimale esecuzione è necessaria un accurata preparazione del paziente che deve sottoporsi all esame in condizioni di perfetta pulizia intestinale. Se la coloscopia è l indagine essenziale per la diagnosi esistono poi una serie di metodiche che possono anche contribuire all identificazione della lesione ma vengono impiegate soprattutto per la stadiazione pretrattamento della malattia o per il follow up dopo l intervento: ECOGRAFIA: è la metodica più semplice e meno invasiva. Occasionalmente può costituire anche la prima indagine che fa sospettare la malattia, ma viene impiegata soprattutto per valutare l eventuale presenza di metastasi epatiche. TC (TOMOGRAFIA COMPUTERIZZATA O TAC): E una tecnica di imaging radiologico del tutto indolore che impiega raggi X. Costituisce la metodica di prima scelta per la stadiazione, sia loco regionale, che a distanza TC (TOMOGRAFIA COMPUTERIZZATA O TAC): E la tecnica di imaging radiologico più diffusa e costituisce la metodica di prima scelta per la stadiazione, sia loco regionale (linfonodi), che a distanza. ECOENDOSCOPIA TRANS-RETTALE:RISONANZA MAGNETICA (RM): metodica di imaging radiologico che utilizza le onde magnetiche. In termini di performance e di accuratezza relativamente alla stadiazione a distanza la metodica è simile alla TC. La RM, però è molto accurata per la stadiazione loco regionale del cancro del retto, in particolare relativamente ai linfonodi del mesoretto (stadio N) e gli stadi più avanzati di T. In tal senso la RM può essere considerata complementare rispetto all ecoendoscopia. PET (Tomografia ad emissione di positroni): tecnica diagnostica che sfrutta l impiego di sostanze radioattive per seguire il percorso all interno del corpo umano di composti naturali come il glucosio,fonte insostituibile di energia per tutte le cellule dell organismo umano. Le cellule tumorali si riproducono più velocemente di quelle sane, quindi richiedono più energia. Per tale motivo la tecnica, oltre a far identificare la lesione neoplastica attraverso un area di ipercaptazione del radiocomposto, fornisce anche una valutazione funzionale circa l attività della lesione attraverso una minore o maggiore intensitù della captazione. Attualmente la metodica viene sempre più spesso effettuata in associazione alla TC (PET-TC) che consente una localizzazione più precisa della lesione. E una metodica che trova applicazione soprattutto nel follow up, per valutare la risposta a trattamenti chemio o radioterapici. La determinazione sul sangue del marcatore CEA (antigene carcino-embrionario), di scarsa utilità nella diagnosi precoce e nello screening, è, però, importante per valutare la gravità della malattia (la sua concentrazione è direttamente collegata all estensione del cancro), nel monitoraggio della risposta al trattamento farmacologico (scende infatti se la chemioterapia è efficace) e per la verifica della ripresa della malattia (risale in caso di ricadute).
97 Terapia La terapia di scelta del tumore del colon-retto è la chirurgia in tutti i casi in cui il tumore sia asportabile ed il paziente sia operabile, anche quando siano presenti metastasi epatiche in numero limitato. L intervento chirurgico consiste nell asportazione di un tratto di colon e ricostruzione della continuità del canale alimentare. A seconda della sede del tumore si eseguiranno tipologie differenti di intervento chirurgico.le tecniche chirurgiche possono essere effettuate sia per via laparotomica che laparoscopica.localizzazione dei tumori del colon: EMICOLECTOMIA DESTRA E l intervento che si effettua per il trattamento dei tumori del cieco e del colon destro. L approccio con tecnica open prevede una laparotomia mediana xifo-.sotto ombelicale Legatura del le arterie coliche di destra (ileocolica e colica destra) all emergenza dall a. mesenterica superiore.. Resezione di cm di tenue terminale, cieco colon ascendente e angolo colico dx. La continuità dell intestino si ricostruisce attraverso un astomosi tra ileo e colon trasverso(ileo-trasverso stomia) manuale o meccanica, più spesso latero-laterale per la differenza di calibro tra i due visceri. COLECTOMIA SEGMENTARIA Per tumori del colon trasverso si esegue una colectomia segmentaria del trasverso che prevede la legatura dell arteria colica media e la resezione di un segmento di colon traverso previa preparazione ed abbassamento degli angoli colici destro e sinistro EMICOLECTOMIA SINISTRA E l intervento che si effettua per i tumori del colon sinistro. L intervento con tecnica open prevede una laparotomia xifo-pubica. L emicolectomia sinistra tipica prevede la resezione del 1/3 distale del colon traverso, dell angolo colico sx, del colon discendente e del sigma previa legatura dell arteria e della vena mesenterica inferiore a livello del margine inferiore del pancreas. La ricostruzione della continuità del canale alimentare viene ottenuta
98 mediante anastomosi tra il colon trasverso ed il retto. L anastomosi può essere effettuata sia manualmente che mediante cucitrice meccanica e può essere realizzata mediante accostamento diretto dei due monconi (termino-terminale) o può essere di tipo lateroterminale. Nel caso di anastomosi confezionale con cucitrici meccaniche circolari (tipo CEEA) la cucitrice stessa può essere introdotta per via trans anale. Nel caso di neoplasie del retto la resezione deve interessare una parte più o meno estesa di questo segmento a seconda della sede della lesione. Anche tumori che interessano la parte distale del retto possono essere resecati risparmiando gli sfinteri anali sempre che il limite inferiore della lesione sia localizzato ad almeno 2-3 cm dal piano degli sfinteri. Correlazione tra tipo di trattamento e stadio della neoplasia La prognosi nei soggetti con cancro del colon-retto dipende strettamente dal grado di invasione tissutale locale, dall'infiltrazione degli organi vicini e dalla presenza di metastasi ai linfonodi o ad altri organi. Si possono utilizzare diversi sistemi di stadiazione, che correlano strettamente con la prognosi e la sopravvivenza a 5 anni. La classificazione di Dukes, proposta dal dottor Cuthbert E. Dukes nel 1932, pone l'accento sulla infiltrazione tissutale, sul coinvolgimento linfonodale e sulla presenza di metastasi a distanza. Questa classificazione è stata per molti anni quella più diffusamente utilizzata ma attualmente si utilizzano maggiormente la classificazione TNM che consente una più accurata definizione del gradi di infiltrazione parietale tra le lesioni con interessamento di mucosa-sottomucosa, muscolare e sierosa. Esiste ancora un altra classificazione (la classificazione di Astler-Coller modificata, che è quella preferita dagli anatomo-patologi Un accurata valutazione mediante le indagini diagnostiche preoperatorie può consentire di prevedere abbastanza precisamente lo stadio della malattia e programmare il trattamento, anche se la definizione finale dello stadio può essere ottenuta solo attraverso l esame istologico postoperatorio. Di seguito sono riportato le diverse classificazioni e nella successiva tabella è indicato il trattamento correlato ai differenti stadi. Duke s Astler- Coller modificat a Classificazion e TNM Classificazion e numerica Descrizione anatomopatologic a Sopravvivenz a a 5 anni A A T1 N0 M0 I Interessa la mucosa >90% e la sottomucosa A B1 T2 N0 M0 I Si estende allo strato >90% muscolare B B2 T3 N0 M0 IIA Si estende alla 70-85% tonaca muscolare B B3 T4 N0 M0 IIB Si estende alla 55-65% sierosa C C1 T1-2 N1 M0 IIIA Metastasi a % linfonodi regionali C C2 T3-4 N1 M0 IIIB 45-55% C C3 Tx N2 M0 IIIc Metastasi a 4 o più 20-30% linfonodi regionali
99 D D Tx Nx M1 IV Metastasi a distanza 5% Il trattamento del tumore del colon a seconda dello stadio Stadio 0 (Tis o T1m, N0, M0) descrizione Trattamento Tumore in situ o intramucoso Escissione locale/resezione segmentaria per lesioni non suscettibili di escissione locale Stadio I : T1 N0 M0 (A1), T2 N0 M0 (B1) descrizione Trattamento Il tumore è limitato alla parete intestinale Resezione chirurgica
100 Stadio II : T3 N0 M0 (B2), T4 N0 M0 (B3) descrizione Trattamento Il tumore ha superato i limiti della parete intestinale B2 (o IIA) T3 N0 M0 Diffusione: il tumore invade la sierosa o i tessuti pericolici o perirettali non ricoperti dal peritoneo Resezione chirurgica (valutare terapia adiuvante solo nell ambito di protocolli di ricerca) B3 (o IIB) T4 N0 M0 Diffusione: il tumore invade direttamente altri organi e/o strutture e/o il peritoneo viscerale Resezione chirurgica (valutare terapia adiuvante solo nell ambito di protocolli di ricerca)
101 Stadio III : T1-2 N1 M0, T3-4, N1 M0, ogni T N2 M0) descrizione/b> trattamento Il tumore si è esteso airegionali C1 (o IIIA) T1-2 N1 M0 Chirurgia seguita da trattamento chemioterapico adiuvante C2 (o IIIB) T3-4 N1 M0 Chirurgia seguita da trattamento chemioterapico C3 (o IIIC) Ogni T N2 M0 Chirurgia seguita da trattamento chemioterapico adiuvante Stadio IV (D secondo Dukes, ogni T, ogni N, M+) descrizione trattamento Il tumore ha prodottoa distanza Chirurgia palliativa/chemioterapia palliativa/terapia di supporto
102 Chirurgia laparoscopica Nella medicina moderna è andato affermandosi sempre di più il concetto della salvaguardia della qualità della vita. A differenza di quanto accadeva in passato quando l obiettivo fondamentale, se non unico, era costituito dalla sconfitta della malattia a qualunque costo, oggi si tende, invece, a conciliare l efficacia del trattamento con il l esigenza di rispettare il più possibile l integrità fisica e, conseguentemente, anche psichica del paziente. Questo concetto ha trovato la sua massima espressione in ambito chirurgico con l affermarsi, anche grazie all evoluzione tecnologica, di quella che viene definita la chirurgia gentile. La più evidente espressione della chirurgia gentile è costituita dalla chirurgia cosiddetta mini invasiva. Per chirurgia mini invasiva si può intendere un trattamento chirurgico di portata limitata (ad esempio la quadrantectomia per la terapia del cancro della mammella o le resezioni endoscopiche per il trattamento locale delle lesioni superficiali gastrointestinali) oppure il concetto di mini invasività si intende riferito al tipo di approccio che viene utilizzato. E questo il caso della chirurgia laparoscopica che consiste, appunto, nell effettuare interventi sugli organi addominali senza praticare una più o meno ampia incisione della parete addominale (laparotomia), ma solo dei piccoli fori in cui vengono fatti passare strumenti chirurgici particolari, i cui movimenti possono essere gestiti dal chirurgo dall esterno. Quindi, la tecnica operatoria e la difficoltà degli interventi condotti per via laparoscopica, non differisce da quelli condotti per via laparotomia. In altre parole un intervento chirurgico non è meno complesso se viene effettuato per via laparoscopica, ma i vantaggi derivanti da questo approccio sono numerosi. Il primo, più importante vantaggio dipende dall assenza della ferita chirurgica. Conseguenza diretta di ciò è la drastica riduzione delle complicanze correlate alla laparotomia, immediate come le infezioni o più tardive, come la formazione di ernie (laparoceli). Evitando la laparotomia si evita anche l ampia apertura del peritoneo e ciò comporta una più rapida ripresa della peristalsi. Inoltre la mancanza della ferita chirurgica determina anche una notevole riduzione del dolore post operatorio. Per questi motivi il paziente ha una più rapida mobilizzazione, può essere dimesso più precocemente e quindi può ritornare in tempi molto più brevi alle proprie occupazioni. Anche in termini di costi globali la chirurgica laparoscopica risulta pertanto più vantaggiosa rispetto alla chirurgia convenzionale a dispetto di un maggiore costo iniziale per le apparecchiature e lo strumentario. La chirurgia laparoscopica nasce alla fine degli anni 80 dello scorso secolo con la prima colecistectomia effettuata da un chirurgo francese. Dopo le iniziali perplessità che accompagnano sempre l introduzione del nuovo l approccio laparoscopico ha conquistato sempre maggiori favori e, con il rapido evolversi della apparecchiature e dello strumentario, ha visto ampliarsi sempre di più le proprie indicazioni. A partire della colecistectomia che, in rpincipio, sembrava l unico ntervento da potersi effettuare per questa via, l approccio laparoscopico è stato proposto proposto per numerosi altri interventi quali l appendicectomia, la chirurgia di parete (ernie, laparoceli), la chirurgia delle patologie funzionali dell esofago (malattia da reflusso gastroesofageo, acalasia) e così via. In una prima fase sono rimasti esclusi gli interventi per patologia oncologica, per il possibile rischio di diffusione di cellule neoplastiche, soprattutto l inseminazione di tali cellule nella parete addominale, con la possibile insorgenza di metastasi a tale livello. Grazie alla creazione di nuovi presidi atti a proteggere ed isolare la parete stessa nel momento in cui l organo sede della neoplasia viene portato all esterno, anche quest ultimo tabù è venuto a cadere e, in particolare per la chirurgia dei tumori del colon, l approccio mini invasivo è da considerarsi ormai lo standard. Attualmente si fa molto prima ad indicare gli interventi che non vengono eseguiti per via laparoscopica che quelli in cui tale approccio è indicato. Come detto in precedenza, l elemento fondamentale della laparoscopia è la mancanza della incisione laparotomia, che è sostituita da multiple microincisioni (di 5, 10 mm), di cui una quasi sempre a livello dell ombelico, per consentire il passaggio nella cavità addominale di cannule (trocars), attraverso cui vengono introdotti un ottica e gli appositi strumenti chirurgici.
103 Affinché sia possibile operare, però, è indispensabile disporre di uno spazio adeguato per poter visualizzare il campo operatorio e per poter utilizzare gli strumenti chirurgici. In condizioni normali la cavità peritoneale, a cui bisogna accedere, rappresenta uno spazio virtuale. Ciò significa che i visceri sono in contatto con la superficie interna della parete addominale. Pertanto, in chirurgia laparoscopica, prima di ogni altra manovra è necessario trasformare la cavità peritoneale da spazio virtuale in spazio reale, idoneo ad operare. Per fare questo bisogna realizzare quello che è denominato pneumoperitoneo e cioè immettere del gas all interno della cavità peritoneale in modo da distanziare adeguatamente la parete addominale dai visceri ed ottenere un adeguato campo operatorio. Il gas utilizzato è la CO2 (anidride carbonica) che è stata preferita ad altri gas ed all aria in quanto poco infiammabile e facilmente riassorbibile e diffusibile in modo da ridurre notevolmente il rischio di possibili complicanze emboliche (emboli gassosi). Per poter realizzare un adeguato pneumoperitoneo è necessario generalmente raggiungere una pressione compresa tra i 10 ed i 12 mmhg. Da quanto detto si intuisce che uno dei componenti fondamentali di un apparecchiatura per laparoscopia e rappresentato da un sistema di insufflazione con l indicazione della pressione raggiunta ed il mantenimento della pressione standard attraverso l avvio automatico quando la pressione dovesse scendere ed il blocco quando si raggiunge il livello pressorio predeterminato. La realizzazione del pneumoperitoneo rappresenta, quindi, il tempo preliminare comune a tutti gli interventi in laparoscopia. Il pneumoperitoneo può essere ottenuto attraverso due modalità: una modalità a cielo coperto utilizzando uno specifico presidio detto ago di Veress ed una a cielo aperto (cosiddetta tecnica di Hasson), che consiste nell accedere alla cavità peritoneale con una manovra chirurgica realizzando una mini incisione a strati la parete addominale e raggiungendo il peritoneo parietale sotto visione, con l ausilio piccoli divaricatori. L incisione viene in genere effettuata a livello dell ombelico; attraverso di essa sarà posizionato il primo trocar che sarà utilizzato prima per realizzare il pneumoperitoneo e quindi per veicolare l ottica a al interno della cavità addominale. Lutilizzo dell ago di Veress offre sicuramente il vantaggio della rapidità ma, anche effettuando la manovra di introduzione dell ago con tutti gli accorgimenti necessari (trazione verso l alto la parete addominale in prossimità dell ombelico, dove viene infisso l ago; decorso obliqui e non perpendicolare rispetto alla parete addominale dello stesso ago), vi è comunque una certa percentuale di rischio di complicanze. Le possibili complicanze consistono principalmente nella perforazione di un tratto di intestino, nella lesione di un organo parenchimale, come il pancreas, o peggio nella lesione di uno dei grossi vasi addominali, come la vena cava inferiore o l aorta, con conseguenze potenzialmente molto grevi. La tecnica aperta comporta certamente un tempo maggiore ma riduce notevolmente l incidenza di possibili complicanze. Una volta ottenuto il pneumoperitoneo, si posiziona il primo trocar (in genere di 12 o 12 mm, a livello dell ombelico) attraverso il quali viene introdotta l ottica. L ottica è un sottile cilindro metallico contenente un sistema di lenti e che viene collegato ad una fonte di luce fredda ed a una telecamera, che trasmette le immagini raccolte all interno della cavità addominale a dei monitor. In tal modo l operatore, gli assistenti al campo e tutto il personale interessato ha la possibilità di seguire le varie fasi della procedura chirurgica. La visione del campo operatorio che è possibile ottenere con questo sistema è nettamente migliore rispetto alla chirurgia convenzionale, con immagini magnificate e ad alta risoluzione. La fonte luminosa, il sistema di acquisizione e trasmissione delle immagini, insieme all insufflatore costituiscono la base di un apparecchiatura per chirurgia laparoscopica. Apparecchiature accessorie sono rappresentate da un sistema di aspirazione e di lavaggio, che vengono collegati ad uno specifico strumento ed un sistema di archiviazione delle immagini, estremamente utile, se non indispensabile per la documentazione della procedura. Introdotta l ottica si procede ad una esplorazione preliminare della cavità addominale e quindi si posizionano gli ulteriori trocars, in numero variabile a seconda del tipo di intervento da effettuare. L introduzione di tali trocars avviene sotto controllo visivo dall interno grazie all ottica già posizionata nella cavità peritoneale e quindi in maniera molto più sicura. Completato il posizionamento dei trocars si da inizio
104 all intervento vero e proprio secondo tempi e modalità ben codificati e che in genere ricalcano molto da vicino quelli dei corrispondenti interventi condotti per via laparotomia. Per poter operare, ovviamente, è necessario disporre di un adeguato strumentario chirurgico. Esso si compone di una serie di strumenti standard, che non differiscono nella sostanza da quelli utilizzati in chirurgia open, se non per il fatto di essere più lunghi e di poter essere articolati dall esterno. Si tratta sostanzialmente di pinze da presa, da trazione, di forbici, di dissettori, portaghi, applicatori di clips ecc. Vi è un corrispettivo dell elettrobisturi rappresentato da un sottile strumento metallico ricoperto da una guaina isolante, tranne che nella sua parte terminale, conformata ad uncino. Oltre allo strumentario standard esistono poi degli strumenti speciali, molti dei quali sono stati specificamente concepiti per la chirurgia mini invasiva e magari sono stati poi adattati anche alla chirurgia convenzionale. Tra questi strumenti speciali vanno sicuramente considerate le cucitrici meccaniche endolaparoscopiche. Le cucitrici meccaniche non sono state certamente inventate con la chirurgia mini invasiva ma l utilizzazione in tale campo di impiego ne ha favorito un enorme sviluppo e perfezionamento. D altra parte, proprio la possibilità di utilizzare tali presidi in chirurgia laparoscopica ha consentito il grande salto di qualità per tale approccio. Esistono ormai innumerevoli tipi di cucitrici meccaniche, soprattutto di tipo lineare, utilizzabili in laparoscopia, di differente lunghezza, snodabili, con la possibilità di utilizzare più cariche e con diversa conformazione dei punti metallici in relazione allo spessore ed alla consistenza dei tessuti da suturare. Anche altri strumenti hanno avuto grande importanza per lo sviluppo della chirurgia laparoscopica facilitando moltissimo l esecuzione di manovre particolarmente difficili per via laparoscopica, come la legatura e sezione dei vasi sanguigni. Ci riferiamo in particolare al dissettore ad ultrasuoni e al dissettore a radiofrequenza. Il dissettore ad ultrasuoni lavora a frequenze elevatissime (superiori a 20 Khz), che a contatto con i tessuti parenchimatosi comportano l emulsione delle cellule ricche di acqua risparmiando strutture vascolari, nervose, biliari e linfatiche. In pratica è uno strumento che serve a sezionare in successivi, piccoli step strutture parenchimali evitando il sanguinamento dei tessuti. I principali campi di applicazione sono costituiti dalla chirurgia resettiva di fegato, milza, rene, pancreas. Il coagulatore a radiofrequenza si basa sul principio della generazione di onde elettromagnetiche ad altissima frequenza. Tali onde determinano la rapida oscillazione degli ioni cellulari con la conseguente produzione di elevatissime temperature. In tal modo è possibile ottenere la completa coagulazione di vasi sanguigni fino ad un calibro di 7 mm. Infine va menzionato il cosiddetti bisturi ad ultrasuoni (bisturi armonico) che è dotato di una lama in titanio capace di oscillare con un breve movimento longitudinale ad elevatissima frequenza (circa al secondo). L attrito provocato da tali oscillazioni produce da un lato l esplosione delle cellule per la vaporizzazione delle molecole d acqua in esse contenute e dall altro la distruzione dei tessuti fibrosi. E uno strumento di grande utilità nella dissezione di strutture fibroadipose (omento, briglie aderenziali, mesi ileali e colici) contenenti vasi di un diametro fino a 5 mm. Accanto ai notevoli vantaggi della chirurgia laparoscopia, che sono stati prima indicati, esistono anche degli inconvenienti correlati a tale tecnica determinati dalle alterazioni fisiopatologiche da essa prodotte. Gran parte di queste possibili conseguenze sono legate al pneumoperitoneo e possono essere così sintetizzate: Alterazioni della funzionalità cardiaca o o o riduzione del ritorno venoso tachicardia aumento delle resistenze periferiche
105 Alterazioni del ritmo cardiaco (25 45% dei casi) Alterazioni del circolo periferico e splancnico Alterazioni della funzionalità polmonare Embolia gassosa Ipertermia Da ciò deriva che una preventiva valutazione, affidata in particolare all anestesista, della funzionalità cardio respiratoria è fondamentale, prima di sottoporre un paziente ad un intervento per via laparoscopica allo scopo di prevedere e quindi prevenire i possibili rischi. Come è stato detto la chirurgia laparoscopica ha ampliato enormemente il suo campo di applicazione negli ultimi anni e per molti tipi di intervento costituisce ormai la modalità elettiva di esecuzione. Tra le indicazioni che potrebbero essere definite assolute alla laparoscopia, oltre, ovviamente, alla colecistectomia è certamente da annoverare la chirurgia del reflusso gastroesofageo. In questo campo l intervento chirurgico che ha avuto la più ampia diffusione è la plastica antireflusso a 360 secondo Nissen, nella versione semplificata proposta dal suo allievo Rossetti e che si presta in maniera ottimale all esecuzione per via laparoscopica. Questo intervento in estrema sintesi consiste nel confezionare intorno alla porzione distale, intra addominale dell esofago un cappio utilizzando la parete anteriore del fondo gastrico, senza sezionare i vasi brevi. Il cappio viene ottenuto facendo ruotare posteriormente e quindi a destra dell esofago, precedentemente mobilizzato sezionando la membrana freno esofagea, la parete anteriore del fondo gastrico. La parte della parete gastrica ruotata intorno all esofago viene, infine, suturata al davanti dell esofago stesso mediante il posizionamento di due punti, con la restante parete anteriore del fondo gastrico posta a sinistra dell esofago. In tal modo viene chiuso il cappio. Normalmente per effettuare tale intervento, oltre al primo trocar, introdotto in sede periombelicale dopo aver instaurato il pneumoperitoneo mediante l ago di Veress, vengono posizionati altri quattro trocars: il primo da 5 mm all ipocondrio destro al di sotto del margine costale sull emiclaveare; il secondo da 5 mm in sede sottoxifoidea sinistra alla sinistra del legamento rotondo; il terzo da 10 mm all ipocondrio sinistro al di sotto del margine costale sull emiclaveare; il quarto da 10 mm sull ombelicale traversa alla sinistra del trocar ombelicale. Rappresentazione schematica della plastica antireflusso sec. Nissen- Rossetti
106 Rappresentazione schematica del posizionamento dei trocars per l intervento di plastica antireflusso per via laparoscopica
LA VIDEO CAPSULA ENDOSCOPICA(VCE)
 LA VIDEO CAPSULA ENDOSCOPICA(VCE). LA VIDEOCAPSULA ENDOSCOPICA L'ultima evoluzione dell endoscopia gastrointestinale è rappresentata dalla video capsula endoscopica (VCE). La metodica fu presentata nella
LA VIDEO CAPSULA ENDOSCOPICA(VCE). LA VIDEOCAPSULA ENDOSCOPICA L'ultima evoluzione dell endoscopia gastrointestinale è rappresentata dalla video capsula endoscopica (VCE). La metodica fu presentata nella
LA VIDEO CAPSULA ENDOSCOPICA(VCE)
 LA VIDEO CAPSULA ENDOSCOPICA(VCE). LA VIDEOCAPSULA ENDOSCOPICA L'ultima evoluzione dell endoscopia gastrointestinale è rappresentata dalla video capsula endoscopica (VCE). La metodica fu presentata nella
LA VIDEO CAPSULA ENDOSCOPICA(VCE). LA VIDEOCAPSULA ENDOSCOPICA L'ultima evoluzione dell endoscopia gastrointestinale è rappresentata dalla video capsula endoscopica (VCE). La metodica fu presentata nella
GMB scaricato da
 II UNIVERSITA DI NAPOLI Facoltà di Medicina e Chirurgia Dipartimento di internistica clinica e sperimentale Magrassi-Lanzara Dipartimento assistenziale di Scienze mediche e chirurgiche Scuola di specializzazione
II UNIVERSITA DI NAPOLI Facoltà di Medicina e Chirurgia Dipartimento di internistica clinica e sperimentale Magrassi-Lanzara Dipartimento assistenziale di Scienze mediche e chirurgiche Scuola di specializzazione
SECONDA UNIVERSITA DEGLI STUDI DI NAPOLI FACOLTA DI MEDICINA E CHIRURGIA L ENDOSCOPIA CON VIDEOCAPSULA:
 1 SECONDA UNIVERSITA DEGLI STUDI DI NAPOLI FACOLTA DI MEDICINA E CHIRURGIA L ENDOSCOPIA CON VIDEOCAPSULA: Cenni storici sulle tecniche di endoscopia La storia dell endoscopia, intesa come aspirazione a
1 SECONDA UNIVERSITA DEGLI STUDI DI NAPOLI FACOLTA DI MEDICINA E CHIRURGIA L ENDOSCOPIA CON VIDEOCAPSULA: Cenni storici sulle tecniche di endoscopia La storia dell endoscopia, intesa come aspirazione a
Castel di Sangro, 9 marzo L'endoscopia è un metodo di esplorazione che permette di visualizzare l'interno (dal greco endon ) del corpo.
 La Diagnosi Endoscopica Castel di Sangro, 9 marzo 2009 L'endoscopia è un metodo di esplorazione che permette di visualizzare l'interno (dal greco endon ) del corpo. L'endoscopia può essere utilizzata sia
La Diagnosi Endoscopica Castel di Sangro, 9 marzo 2009 L'endoscopia è un metodo di esplorazione che permette di visualizzare l'interno (dal greco endon ) del corpo. L'endoscopia può essere utilizzata sia
CLUB ITALIANO CAPSULA ENDOSCOPICA Sezione di studio della Società Italiana di Gastroenterologia
 GE_PO_16_M_01v01 PAG. 1 di 5 CLUB ITALIANO CAPSULA ENDOSCOPICA Sezione di studio della Società Italiana di Gastroenterologia CONSENSO INFORMATO PER L ESECUZIONE DELL ENTEROSCOPIA CON CAPSULA Given Video
GE_PO_16_M_01v01 PAG. 1 di 5 CLUB ITALIANO CAPSULA ENDOSCOPICA Sezione di studio della Società Italiana di Gastroenterologia CONSENSO INFORMATO PER L ESECUZIONE DELL ENTEROSCOPIA CON CAPSULA Given Video
L ANGOLO ENDOSCOPICO: ISTRUZIONI PER L USO. V. Napolitano INDICAZIONI ALL ENDOSCOPIA
 L ANGOLO ENDOSCOPICO: ISTRUZIONI PER L USO INDICAZIONI ALL ENDOSCOPIA V. Napolitano Seconda Università degli Studi di Napoli Dipartimento di Chirurgia Generale e Specialistica Dir. Prof. C. Pignatelli
L ANGOLO ENDOSCOPICO: ISTRUZIONI PER L USO INDICAZIONI ALL ENDOSCOPIA V. Napolitano Seconda Università degli Studi di Napoli Dipartimento di Chirurgia Generale e Specialistica Dir. Prof. C. Pignatelli
APPROPRIATEZZA e ADEGUATEZZA nelle richieste degli esami endoscopici
 APPROPRIATEZZA e ADEGUATEZZA nelle richieste degli esami endoscopici APPROPRIATEZZA uso appropriato, pertinenza ad eseguire una endoscopia seguendo come parametri la fedele osservanza delle indicazioni
APPROPRIATEZZA e ADEGUATEZZA nelle richieste degli esami endoscopici APPROPRIATEZZA uso appropriato, pertinenza ad eseguire una endoscopia seguendo come parametri la fedele osservanza delle indicazioni
ENTEROSCOPIA CON VIDEO CAPSULA
 Pag. 1 di 5 Copia per l assistita/o Gentile Signora/e, questo foglio informativo è stato realizzato per dare alle persone che debbono affrontare un percorso di cura che prevede l espressione del proprio
Pag. 1 di 5 Copia per l assistita/o Gentile Signora/e, questo foglio informativo è stato realizzato per dare alle persone che debbono affrontare un percorso di cura che prevede l espressione del proprio
DIPARTIMENTO CHIRURGICO GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA. PEG Gastrostomia. Endoscopica Percutanea
 DIPARTIMENTO CHIRURGICO GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA PEG Gastrostomia Endoscopica Percutanea Che cosa è? La gastrostomia endoscopica percutanea (PEG) è una procedura che comporta il posizionamento
DIPARTIMENTO CHIRURGICO GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA PEG Gastrostomia Endoscopica Percutanea Che cosa è? La gastrostomia endoscopica percutanea (PEG) è una procedura che comporta il posizionamento
CHE COS E LA COLONSCOPIA VIRTUALE
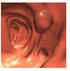 CHE COS E LA COLONSCOPIA VIRTUALE La colonscopia virtuale (CV) è un esame non invasivo del colon che si esegue attraverso una tomografia assiale computerizzata (TAC) dell addome dopo aver disteso il colon
CHE COS E LA COLONSCOPIA VIRTUALE La colonscopia virtuale (CV) è un esame non invasivo del colon che si esegue attraverso una tomografia assiale computerizzata (TAC) dell addome dopo aver disteso il colon
La stipsi un problema risolvibile diagnosi ed indicazioni terapeutiche
 U.O. di Chirurgia Generale (Dir.: G. Munegato) Ospedale S. Maria dei Battuti CONEGLIANO (TV) diagnosi ed indicazioni terapeutiche 1^ Settimana Nazionale per la Diagnosi e la Cura della Stipsi 14 18 Novembre
U.O. di Chirurgia Generale (Dir.: G. Munegato) Ospedale S. Maria dei Battuti CONEGLIANO (TV) diagnosi ed indicazioni terapeutiche 1^ Settimana Nazionale per la Diagnosi e la Cura della Stipsi 14 18 Novembre
Sistema Videocapsulare Endoscopico OMOM
 Sistema Videocapsulare Endoscopico OMOM 5 Sistema Videocapsulare Endoscopico Smart Capsule 2 Nuova videocapsula endoscopica Specifiche tecniche Caratteristiche Fisiche Dimensione Peso Materiale ø 11 x
Sistema Videocapsulare Endoscopico OMOM 5 Sistema Videocapsulare Endoscopico Smart Capsule 2 Nuova videocapsula endoscopica Specifiche tecniche Caratteristiche Fisiche Dimensione Peso Materiale ø 11 x
Alessandro Pezzoli U.O di Gastroenterologia ed Endoscopia digestiva Az. Osp. Sant Anna Ferrara
 Alessandro Pezzoli U.O di Gastroenterologia ed Endoscopia digestiva Az. Osp. Sant Anna Ferrara Le emergenze-urgenze in endoscopia digestiva, Ferrara 3/12/2010 Sanguinamento: ematochezia e rettoragia Occlusione
Alessandro Pezzoli U.O di Gastroenterologia ed Endoscopia digestiva Az. Osp. Sant Anna Ferrara Le emergenze-urgenze in endoscopia digestiva, Ferrara 3/12/2010 Sanguinamento: ematochezia e rettoragia Occlusione
neoplasie del colon risultati dello screening A.O. Salvini Dott. Claudio Gozzini U.O. Gastroenterologia Presidio Ospedaliero Rho
 neoplasie del colon risultati dello screening A.O. Salvini Dott. Claudio Gozzini U.O. Gastroenterologia Presidio Ospedaliero Rho cancro colorettale nel mondo tasso di mortalità alto medio basso dati non
neoplasie del colon risultati dello screening A.O. Salvini Dott. Claudio Gozzini U.O. Gastroenterologia Presidio Ospedaliero Rho cancro colorettale nel mondo tasso di mortalità alto medio basso dati non
Work up diagnostico e terapeutico
 EMORRAGIE DIGESTIVE DISTALI Work up diagnostico e terapeutico F. Cosentino Emorragie del tratto gastrointestinale inferiore Definizioni Approccio iniziale del paziente Concetti chiave Colonscopia ed indagini
EMORRAGIE DIGESTIVE DISTALI Work up diagnostico e terapeutico F. Cosentino Emorragie del tratto gastrointestinale inferiore Definizioni Approccio iniziale del paziente Concetti chiave Colonscopia ed indagini
materiale biocompatibile resistente all acidità dei succhi gastrici
 Dipartimento di Medicina Specialistica U. O. Gastroenterologia ed Endoscopia Digestiva Ospedale G.B. Morgagni Forlì L enteroscopia con videocapsula Angelo De Padova Università degli studi di Ferrara Scuola
Dipartimento di Medicina Specialistica U. O. Gastroenterologia ed Endoscopia Digestiva Ospedale G.B. Morgagni Forlì L enteroscopia con videocapsula Angelo De Padova Università degli studi di Ferrara Scuola
PROGRAMMA DEL CORSO DI CHIRURGIA GENERALE (CANALE A) Prof. Giuseppe Noya. Il trauma:
 PROGRAMMA DEL CORSO DI CHIRURGIA GENERALE (CANALE A) Prof. Giuseppe Noya Il trauma: - Valutazione iniziale e prime terapie chirurgiche del traumatizzato - Trauma del bambino, nell adulto e in gravidanza
PROGRAMMA DEL CORSO DI CHIRURGIA GENERALE (CANALE A) Prof. Giuseppe Noya Il trauma: - Valutazione iniziale e prime terapie chirurgiche del traumatizzato - Trauma del bambino, nell adulto e in gravidanza
APPROPRIATEZZA DELLE RICHIESTE DI ENDOSCOPIA DIGESTIVA. Confronto con il lavoro del 2006 della provincia di REGGIO EMILIA
 APPROPRIATEZZA DELLE RICHIESTE DI ENDOSCOPIA DIGESTIVA Confronto con il lavoro del 2006 della provincia di REGGIO EMILIA GRUPPO DI LAVORO MMG Endoscopisti ASMN, ASL, Privato accreditato Gastroenterologi
APPROPRIATEZZA DELLE RICHIESTE DI ENDOSCOPIA DIGESTIVA Confronto con il lavoro del 2006 della provincia di REGGIO EMILIA GRUPPO DI LAVORO MMG Endoscopisti ASMN, ASL, Privato accreditato Gastroenterologi
APPROPRIATEZZA DELLE RICHIESTE DI ENDOSCOPIA DIGESTIVA
 APPROPRIATEZZA DELLE RICHIESTE DI ENDOSCOPIA DIGESTIVA Confronto con il lavoro del 2006 della provincia di REGGIO EMILIA GRUPPO DI LAVORO MMG Endoscopisti ASMN, ASL, Privato accreditato Gastroenterologi
APPROPRIATEZZA DELLE RICHIESTE DI ENDOSCOPIA DIGESTIVA Confronto con il lavoro del 2006 della provincia di REGGIO EMILIA GRUPPO DI LAVORO MMG Endoscopisti ASMN, ASL, Privato accreditato Gastroenterologi
Neoplasia del Pancreas: Ruolo dell EUS
 Neoplasia del Pancreas: Ruolo dell EUS Fabia Attili MD, PhD Digestive Endoscopy Unit Cancro del pancreas I numeri: 10^ più comune neoplasia 4^ causa di mortalità per cancro American Cancer Society 2006:
Neoplasia del Pancreas: Ruolo dell EUS Fabia Attili MD, PhD Digestive Endoscopy Unit Cancro del pancreas I numeri: 10^ più comune neoplasia 4^ causa di mortalità per cancro American Cancer Society 2006:
ACCETTAZIONE, ACCOGLIENZA, VOLUME DI ATTIVITA
 ACCETTAZIONE, ACCOGLIENZA, VOLUME DI ATTIVITA Dott. Mauro Spandre Servizio di Gastroenterologia ed Endoscopia Digestiva Ospedale S Giovanni A.S. SIGMOIDOSCOPIA (1) Esplorazione del retto e del sigma con
ACCETTAZIONE, ACCOGLIENZA, VOLUME DI ATTIVITA Dott. Mauro Spandre Servizio di Gastroenterologia ed Endoscopia Digestiva Ospedale S Giovanni A.S. SIGMOIDOSCOPIA (1) Esplorazione del retto e del sigma con
Malattia diverticolare del colon
 Malattia diverticolare del colon la diverticolosi è molto frequente anche in individui asintomatici ma soprattutto nelle fasce d età più avanzata rara sotto i 40 anni, 5% nei cinquantenni, oltre il 75%
Malattia diverticolare del colon la diverticolosi è molto frequente anche in individui asintomatici ma soprattutto nelle fasce d età più avanzata rara sotto i 40 anni, 5% nei cinquantenni, oltre il 75%
FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA.
 FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA. Gentile Paziente, La gastroscopia è un esame endoscopico che permette la visualizzazione della mucosa dell esofago, dello
FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA. Gentile Paziente, La gastroscopia è un esame endoscopico che permette la visualizzazione della mucosa dell esofago, dello
L APPROPIATEZZA DELLE INDAGINI AGLI ESAMI ENDOSCOPICI
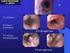 L APPROPIATEZZA DELLE INDAGINI AGLI ESAMI ENDOSCOPICI Dott. Andrea Prati Responsabile U.O. Semplice di Urodinamica U.O. di Urologia P.O.di Fidenza S.Secondo (Parma) Un esame appropriato è l ESAME più indicato,possibilmente
L APPROPIATEZZA DELLE INDAGINI AGLI ESAMI ENDOSCOPICI Dott. Andrea Prati Responsabile U.O. Semplice di Urodinamica U.O. di Urologia P.O.di Fidenza S.Secondo (Parma) Un esame appropriato è l ESAME più indicato,possibilmente
Enteroscopia con video capsula vs procedure convenzionali nella diagnosi delle malattie dell intestino tenue: un meta-analisi degli studi controllati
 Enteroscopia con video capsula vs procedure convenzionali nella diagnosi delle malattie dell intestino tenue: un meta-analisi degli studi controllati Disegno dello studio Revisione sistematica quantitativa.
Enteroscopia con video capsula vs procedure convenzionali nella diagnosi delle malattie dell intestino tenue: un meta-analisi degli studi controllati Disegno dello studio Revisione sistematica quantitativa.
Arrigo Arrigoni Carlo Senore
 UTILIZZO DELLA COLONSCOPIA VIRTUALE Arrigo Arrigoni Carlo Senore Torino, 21 novembre 2018 LA COLONSCOPIA VIRTUALE (CTC) HA SOSTITUITO IL CLISMA COLON DC I trial SIGGAR (Halligan et al. 2013; Atkin et al.
UTILIZZO DELLA COLONSCOPIA VIRTUALE Arrigo Arrigoni Carlo Senore Torino, 21 novembre 2018 LA COLONSCOPIA VIRTUALE (CTC) HA SOSTITUITO IL CLISMA COLON DC I trial SIGGAR (Halligan et al. 2013; Atkin et al.
Congresso ACEMC Roma 5 luglio 2012 DIGESTIVE. Azienda Ospedaliero-Universitaria di Parma SSD Radiologia Urgenza ed Emergenza
 Congresso ACEMC Roma 5 luglio 2012 L IMAGING LIMAGING NELLE EMORRAGIE DIGESTIVE Massimo Valentino Azienda Ospedaliero-Universitaria di Parma SSD Radiologia Urgenza ed Emergenza IL PAZIENTE CON SOSPETTA
Congresso ACEMC Roma 5 luglio 2012 L IMAGING LIMAGING NELLE EMORRAGIE DIGESTIVE Massimo Valentino Azienda Ospedaliero-Universitaria di Parma SSD Radiologia Urgenza ed Emergenza IL PAZIENTE CON SOSPETTA
AZIENDA OSPEDALIERA S. MARIA DEGLI ANGELI PORDENONE Pordenone Via Montereale, 24 CF e P. IVA Tel Fax 0434.
 AZIENDA OSPEDALIERA S. MARIA DEGLI ANGELI PORDENONE 33170 Pordenone Via Montereale, 24 CF e P. IVA 01302970932 Tel. 0434.3991 Fax 0434.399398 DIPARTIMENTO DI CHIRURGIA GENERALE S.C. GASTROENTEROLOGIA ED
AZIENDA OSPEDALIERA S. MARIA DEGLI ANGELI PORDENONE 33170 Pordenone Via Montereale, 24 CF e P. IVA 01302970932 Tel. 0434.3991 Fax 0434.399398 DIPARTIMENTO DI CHIRURGIA GENERALE S.C. GASTROENTEROLOGIA ED
STRUTTURA COMPLESSA DI GASTROENTEROLOGIA
 FOGLIO INFORMATIVO E CONSENSO INFORMATO PER ECOENDOSCOPIA Gentile Paziente, L ecoendoscopia è una procedura diagnostica e terapeutica che impiega un approccio ecografico ed endoscopico combinato, nella
FOGLIO INFORMATIVO E CONSENSO INFORMATO PER ECOENDOSCOPIA Gentile Paziente, L ecoendoscopia è una procedura diagnostica e terapeutica che impiega un approccio ecografico ed endoscopico combinato, nella
L occlusione intestinale: l apporto l gastroenterologo
 L occlusione intestinale: l apporto l del gastroenterologo Alessandro Pezzoli U.O di Gastroenterologia ed Endoscopia digestiva Az ospedaliera Sant Anna Ferrara Società Med Chir 24/3/2012 Occlusione intestinale
L occlusione intestinale: l apporto l del gastroenterologo Alessandro Pezzoli U.O di Gastroenterologia ed Endoscopia digestiva Az ospedaliera Sant Anna Ferrara Società Med Chir 24/3/2012 Occlusione intestinale
Linee guida per la corretta utilizzazione delle metodiche endoscopiche
 Linee guida per la corretta utilizzazione delle metodiche endoscopiche Le linee guida adottate derivano da quelle redatte dall'american Society for Gastrointestinal Endoscopy sulla base di revisione critica
Linee guida per la corretta utilizzazione delle metodiche endoscopiche Le linee guida adottate derivano da quelle redatte dall'american Society for Gastrointestinal Endoscopy sulla base di revisione critica
Servizi di gastroenterologia dell Ente Ospedaliero Cantonale
 Servizi di gastroenterologia dell Ente Ospedaliero Cantonale Cos è la gastroenterologia? La gastroenterologia (dal greco gaster -stomaco-, enteron -intestino- e logos -scienza-) è la specialità della medicina
Servizi di gastroenterologia dell Ente Ospedaliero Cantonale Cos è la gastroenterologia? La gastroenterologia (dal greco gaster -stomaco-, enteron -intestino- e logos -scienza-) è la specialità della medicina
70 CONGRESSO ITALIANO DI PEDIATRIA
 70 CONGRESSO ITALIANO DI PEDIATRIA ECOGRAFIA IN PEDIATRIA PALERMO 12 GIUGNO 2014 MALATTIE INFIAMMATORIE CRONICHE INTESTINALI modalità di esecuzione dell esame e semeiotica ecografica Mauro Massimetti MALATTIE
70 CONGRESSO ITALIANO DI PEDIATRIA ECOGRAFIA IN PEDIATRIA PALERMO 12 GIUGNO 2014 MALATTIE INFIAMMATORIE CRONICHE INTESTINALI modalità di esecuzione dell esame e semeiotica ecografica Mauro Massimetti MALATTIE
Gli score endoscopici nelle IBD. Roberto Faggiani
 Gli score endoscopici nelle IBD Roberto Faggiani Ruolo dell endoscopia nelle IBD Diagnosi differenziale Valutazione di attività ed estensione di malattia Manovre terapeutiche Sorveglianza e screening neoplasia
Gli score endoscopici nelle IBD Roberto Faggiani Ruolo dell endoscopia nelle IBD Diagnosi differenziale Valutazione di attività ed estensione di malattia Manovre terapeutiche Sorveglianza e screening neoplasia
Ricordate di iscrivervi alla Sezione SIRM di Radiologia Addominale Gastroenterologica
 Ricordate di iscrivervi alla Sezione SIRM di Radiologia Addominale Gastroenterologica http://www.sirm.org/homepage/sezioni-studio/addominale http://www.sirmgastrointestinal.weebly.com/ ROBERTO DI MIZIO
Ricordate di iscrivervi alla Sezione SIRM di Radiologia Addominale Gastroenterologica http://www.sirm.org/homepage/sezioni-studio/addominale http://www.sirmgastrointestinal.weebly.com/ ROBERTO DI MIZIO
Come diagnosticare MRE nel 2018
 Patologia benigna del giunto GastroEsofageo: verso un approccio integrato multi disciplinare Come diagnosticare MRE nel 2018 Ruolo della Endoscopia come test diagnostico iniziale Dott.ssa Maria Giuseppina
Patologia benigna del giunto GastroEsofageo: verso un approccio integrato multi disciplinare Come diagnosticare MRE nel 2018 Ruolo della Endoscopia come test diagnostico iniziale Dott.ssa Maria Giuseppina
RUOLO DELL ECOGRAFIA NELLA DIAGNOSI E NEL FOLLOW-UP DELLE MALATTIE INFIAMMATORIE INTESTINALI
 RUOLO DELL ECOGRAFIA NELLA DIAGNOSI E NEL FOLLOW-UP DELLE MALATTIE INFIAMMATORIE INTESTINALI Alice Colucci Rho, 22 Settembre 2007 Iter diagnostico nelle IBD à Clinica algie addominali, alterazioni dell
RUOLO DELL ECOGRAFIA NELLA DIAGNOSI E NEL FOLLOW-UP DELLE MALATTIE INFIAMMATORIE INTESTINALI Alice Colucci Rho, 22 Settembre 2007 Iter diagnostico nelle IBD à Clinica algie addominali, alterazioni dell
LA MALATTIA DIVERTICOLARE COMPLICATA IL RUOLO DELLA RADIOLOGIA NELLA DIAGNOSI E NEL TRATTAMENTO
 AZIENDA OSPEDALIERA UNIVERSITARIA INTEGRATA VERONA Ospedale Civile Maggiore U.O. Radiologia Direttore: Dott.ssa Stefania Montemezzi LA MALATTIA DIVERTICOLARE COMPLICATA IL RUOLO DELLA RADIOLOGIA NELLA
AZIENDA OSPEDALIERA UNIVERSITARIA INTEGRATA VERONA Ospedale Civile Maggiore U.O. Radiologia Direttore: Dott.ssa Stefania Montemezzi LA MALATTIA DIVERTICOLARE COMPLICATA IL RUOLO DELLA RADIOLOGIA NELLA
DR.SANDRO BOSCHETTO UOSD GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA OSP.S.CAMILLO DE LELLIS RIETI. Roma 25 gennaio 2019 NH Villa Carpegna
 DR.SANDRO BOSCHETTO UOSD GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA OSP.S.CAMILLO DE LELLIS RIETI Roma 25 gennaio 2019 NH Villa Carpegna INQUADRAMENTO -MALATTIA AUTOIMMUNE GENETICAMENTE CORRELATA -RARA
DR.SANDRO BOSCHETTO UOSD GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA OSP.S.CAMILLO DE LELLIS RIETI Roma 25 gennaio 2019 NH Villa Carpegna INQUADRAMENTO -MALATTIA AUTOIMMUNE GENETICAMENTE CORRELATA -RARA
Guida ai Servizi Ospedalieri
 REGIONE CALABRIA AZIENDA SANITARIA PROVINCIALE di VIBO VALENTIA Endoscopia Digestiva Diagnostica e Chirurgica Dr. A.Chirico Dr. V.Grasso Dr. L.Purita Guida ai Servizi Ospedalieri - CARTA DI ACCOGLIENZA
REGIONE CALABRIA AZIENDA SANITARIA PROVINCIALE di VIBO VALENTIA Endoscopia Digestiva Diagnostica e Chirurgica Dr. A.Chirico Dr. V.Grasso Dr. L.Purita Guida ai Servizi Ospedalieri - CARTA DI ACCOGLIENZA
CONSENSO INFORMATO PER ESOFAGO-GASTRO-DUODENOSCOPIA
 PAGINA 1 DI 6 SERVIZIO DI ENDOSCOPIA DIGESTIVA Padiglione Regina Elena Piano 3 - Via M. Fanti, n 6 - Milano CONSENSO INFORMATO PER ESOFAGO-GASTRO-DUODENOSCOPIA Data Gentile Signore/a, Nella relazione di
PAGINA 1 DI 6 SERVIZIO DI ENDOSCOPIA DIGESTIVA Padiglione Regina Elena Piano 3 - Via M. Fanti, n 6 - Milano CONSENSO INFORMATO PER ESOFAGO-GASTRO-DUODENOSCOPIA Data Gentile Signore/a, Nella relazione di
In base alle informazioni ricevute, in piena consapevolezza e libertà decisionale esprimo: il mio consenso a sottopormi alla procedura di:
 Il sottoscritto Dott... dichiara di avere fornito informazioni complete e comprensibili al Sig/Sig.ra al riguardo della necessità/opportunità di sottoporsi a ECOENDOSCOPIA DIAGNOSTICA E OPERATIVA In base
Il sottoscritto Dott... dichiara di avere fornito informazioni complete e comprensibili al Sig/Sig.ra al riguardo della necessità/opportunità di sottoporsi a ECOENDOSCOPIA DIAGNOSTICA E OPERATIVA In base
Il paziente ha un sospetto sanguinamento del tratto intermedio e la videocapsula è negativa
 CHE FARE SE... Il paziente ha un sospetto sanguinamento del tratto intermedio e la videocapsula è negativa Clelia MARMO, UOC Fisiopatologia Chirurgica Apparato Digerente, AOU S.U.N. - Napoli Riccardo MARMO,
CHE FARE SE... Il paziente ha un sospetto sanguinamento del tratto intermedio e la videocapsula è negativa Clelia MARMO, UOC Fisiopatologia Chirurgica Apparato Digerente, AOU S.U.N. - Napoli Riccardo MARMO,
Emostasi endoscopica
 II UNIVERSITA DI NAPOLI Facoltà di Medicina e Chirurgia Dipartimento di internistica clinica e sperimentale Magrassi-Lanzara Dipartimento assistenziale integrato di chirurgia generale e specialistica Servizio
II UNIVERSITA DI NAPOLI Facoltà di Medicina e Chirurgia Dipartimento di internistica clinica e sperimentale Magrassi-Lanzara Dipartimento assistenziale integrato di chirurgia generale e specialistica Servizio
Reperti non neoplastici nella colonoscopia di screening
 Reperti non neoplastici nella colonoscopia di screening reperti nello screening reperti nello screening Italia survey 2012 adenoma avanzato: 24% carcinoma: 5% patologia non neoplastica:? il quadro clinico
Reperti non neoplastici nella colonoscopia di screening reperti nello screening reperti nello screening Italia survey 2012 adenoma avanzato: 24% carcinoma: 5% patologia non neoplastica:? il quadro clinico
DILATAZIONI DILATAZIONI MECCANICHE 11/11/2016. Meccaniche Pneumatiche DILATAZIONI MECCANICHE. Sonde di Savary
 Per stenosi si intende un restringimento del lume intestinale che comporta un ostacolo al transito, più o meno accentuato, in rapporto all entità del restringimento stesso. Una stenosi del lume esofageo
Per stenosi si intende un restringimento del lume intestinale che comporta un ostacolo al transito, più o meno accentuato, in rapporto all entità del restringimento stesso. Una stenosi del lume esofageo
AZIENDA OSPEDALIERA S. MARIA DEGLI ANGELI PORDENONE Pordenone Via Montereale, 24 CF e P. IVA Tel Fax 0434.
 AZIENDA OSPEDALIERA S. MARIA DEGLI ANGELI PORDENONE 33170 Pordenone Via Montereale, 24 CF e P. IVA 01302970932 Tel. 0434.3991 Fax 0434.399398 DIPARTIMENTO DI CHIRURGIA GENERALE S.C. GASTROENTEROLOGIA ED
AZIENDA OSPEDALIERA S. MARIA DEGLI ANGELI PORDENONE 33170 Pordenone Via Montereale, 24 CF e P. IVA 01302970932 Tel. 0434.3991 Fax 0434.399398 DIPARTIMENTO DI CHIRURGIA GENERALE S.C. GASTROENTEROLOGIA ED
REPORT SCIENTIFICO 20 CNMD Napoli 2014
 REPORT SCIENTIFICO 20 CNMD Napoli 2014 PRESENZE COMPLESSIVE REGISTRATE NELLE GIORNATE CONGRESSUALI 1741 1 REPORT SCIENTIFICO 20 CNMD Napoli 2014 Parte originale Parte non originale Gradimento Minicorsi
REPORT SCIENTIFICO 20 CNMD Napoli 2014 PRESENZE COMPLESSIVE REGISTRATE NELLE GIORNATE CONGRESSUALI 1741 1 REPORT SCIENTIFICO 20 CNMD Napoli 2014 Parte originale Parte non originale Gradimento Minicorsi
DIAGNOSTICA ENDOSCOPICA DEL TRATTO DIGESTIVO
 Arcispedale S. Maria Nuova VILLA VERDE GRUPPO DI LAVORO INTERAZIENDALE PER L APPROPRIATEZZA CLINICA DIAGNOSTICA ENDOSCOPICA DEL TRATTO DIGESTIVO E GESTIONE DELLE SITUAZIONI CLINICHE DI PIÙ FREQUENTE RISCONTRO
Arcispedale S. Maria Nuova VILLA VERDE GRUPPO DI LAVORO INTERAZIENDALE PER L APPROPRIATEZZA CLINICA DIAGNOSTICA ENDOSCOPICA DEL TRATTO DIGESTIVO E GESTIONE DELLE SITUAZIONI CLINICHE DI PIÙ FREQUENTE RISCONTRO
&diritti GESTIONE. L endoscopia con videocapsula: tecnologia e razionale d uso. Il libro bianco dell endoscopista F. Cosentino, G. Battaglia, E.
 GESTIONE &diritti di un Servizio di Endoscopia Digestiva Il libro bianco dell endoscopista F. Cosentino, G. Battaglia, E. Ricci L endoscopia con videocapsula: tecnologia e razionale d uso Roberto de Franchis
GESTIONE &diritti di un Servizio di Endoscopia Digestiva Il libro bianco dell endoscopista F. Cosentino, G. Battaglia, E. Ricci L endoscopia con videocapsula: tecnologia e razionale d uso Roberto de Franchis
Emorragie occulte oscure
 Emorragie occulte oscure L endoscopia con videocapsula, entrata nella pratica clinica nel 2001, ha avuto nel corso di questi anni una vastissima diffusione. Sono state eseguite finora nel mondo oltre 200.000
Emorragie occulte oscure L endoscopia con videocapsula, entrata nella pratica clinica nel 2001, ha avuto nel corso di questi anni una vastissima diffusione. Sono state eseguite finora nel mondo oltre 200.000
intestinale per neoplasia E. Codognotto
 L occlusione Locclusione e la perforazione intestinale per neoplasia E. Codognotto Introduzione Il carcinoma del colon è la terza neoplasia per frequenza 20% nuove diagnosi: ca localmente avanzato P f
L occlusione Locclusione e la perforazione intestinale per neoplasia E. Codognotto Introduzione Il carcinoma del colon è la terza neoplasia per frequenza 20% nuove diagnosi: ca localmente avanzato P f
IldocumentoGOLD completo(w ORKSHOPREPORTS)èconsultabilesulsitowww.goldcopd.it
 GUIDA RAPIDA PER LA GESTIONE AMBULATORIALE DELLA BPCO Basatasuprogettoglobaleperladiagnosi,gestionee prevenzionebpco (Aggiornamento2007) IldocumentoGOLD completo(w ORKSHOPREPORTS)èconsultabilesulsitowww.goldcopd.it
GUIDA RAPIDA PER LA GESTIONE AMBULATORIALE DELLA BPCO Basatasuprogettoglobaleperladiagnosi,gestionee prevenzionebpco (Aggiornamento2007) IldocumentoGOLD completo(w ORKSHOPREPORTS)èconsultabilesulsitowww.goldcopd.it
Le certezze e i dubbi del medico d urgenza
 GESTIONE IN DEA DEL PAZIENTE CON DOLORE ADDOMINALE Torino, 20 febbraio 2010 Azienda Ospedaliera Ordine Mauriziano Le certezze e i dubbi del medico d urgenza Luisa Arnaldi SC Medicina d Urgenza Ospedale
GESTIONE IN DEA DEL PAZIENTE CON DOLORE ADDOMINALE Torino, 20 febbraio 2010 Azienda Ospedaliera Ordine Mauriziano Le certezze e i dubbi del medico d urgenza Luisa Arnaldi SC Medicina d Urgenza Ospedale
NORME DI PREPARAZIONE PER INDAGINI ENDOSCOPICHE DEL TRATTO DIGESTIVO SUPERIORE ESOFAGOGASTRODUODENOSCOPIA
 NORME DI PREPARAZIONE PER INDAGINI ENDOSCOPICHE DEL TRATTO DIGESTIVO SUPERIORE ESOFAGOGASTRODUODENOSCOPIA IL GIORNO DELL ESAME Digiuno dalla mezzanotte E consentita l assunzione di farmaci nelle terapie
NORME DI PREPARAZIONE PER INDAGINI ENDOSCOPICHE DEL TRATTO DIGESTIVO SUPERIORE ESOFAGOGASTRODUODENOSCOPIA IL GIORNO DELL ESAME Digiuno dalla mezzanotte E consentita l assunzione di farmaci nelle terapie
LA DIAGNOSTICA PER IMMAGINI NELLA PANCREATITE ACUTA
 SCUOLA REGIONALE DI FORMAZIONE SPECIFICA IN MEDICINA GENERALE, CORSO 2010/2013. PATOLOGIA DEL PANCREAS LA DIAGNOSTICA PER IMMAGINI NELLA PANCREATITE ACUTA Elisabetta Ascari Fabio Bassi Medicina III Gastroenterologia
SCUOLA REGIONALE DI FORMAZIONE SPECIFICA IN MEDICINA GENERALE, CORSO 2010/2013. PATOLOGIA DEL PANCREAS LA DIAGNOSTICA PER IMMAGINI NELLA PANCREATITE ACUTA Elisabetta Ascari Fabio Bassi Medicina III Gastroenterologia
CLASSI DI PRIORITÀ. Visita Gastroenterologica
 Visita Gastroenterologica CLASSI DI PRIORITÀ Classe U Urgente Accesso diretto al PSA o DEA Emorragia digestiva in atto Dolori addominali ricorrenti e/o sindrome clinica per sospetto addome acuto Corpi
Visita Gastroenterologica CLASSI DI PRIORITÀ Classe U Urgente Accesso diretto al PSA o DEA Emorragia digestiva in atto Dolori addominali ricorrenti e/o sindrome clinica per sospetto addome acuto Corpi
1 Corso ANOTE/ANIGEA Esaregionaledel Sud «OBIETTIVO QUALITÀ»
 1 Corso ANOTE/ANIGEA Esaregionaledel Sud. «OBIETTIVO QUALITÀ» PROGRAMMAZIONE DELLO SCREENING DEL CCR: L INFERMIERE NELLA SEGRETERIA SCREENING Pietro Vaccaro Premessa Identificare una malattia prima che
1 Corso ANOTE/ANIGEA Esaregionaledel Sud. «OBIETTIVO QUALITÀ» PROGRAMMAZIONE DELLO SCREENING DEL CCR: L INFERMIERE NELLA SEGRETERIA SCREENING Pietro Vaccaro Premessa Identificare una malattia prima che
LA BIOPSIA LIQUIDA Informazioni per i pazienti. A cura di: Alessandro Inno e Giulio Metro
 Informazioni per i pazienti A cura di: Alessandro Inno e Giulio Metro maggio 2017 Gruppo di lavoro coordinato da Stefania Gori UOC Oncologia Medica - Ospedale Sacro Cuore-Don Calabria - Negrar (VR) Alessandro
Informazioni per i pazienti A cura di: Alessandro Inno e Giulio Metro maggio 2017 Gruppo di lavoro coordinato da Stefania Gori UOC Oncologia Medica - Ospedale Sacro Cuore-Don Calabria - Negrar (VR) Alessandro
ROBERTO DI MIZIO DIRETTORE SERVIZIO DI RADIOLOGIA OSPEDALE PENNE ASL PESCARA
 ROBERTO DI MIZIO DIRETTORE SERVIZIO DI RADIOLOGIA OSPEDALE PENNE ASL PESCARA 1 ILEO MECCANICO DELL INTESTINO TENUE STRATEGIA DELL IMAGING 2 In caso di addome acuto, il radiologo svolge un duplice compito:
ROBERTO DI MIZIO DIRETTORE SERVIZIO DI RADIOLOGIA OSPEDALE PENNE ASL PESCARA 1 ILEO MECCANICO DELL INTESTINO TENUE STRATEGIA DELL IMAGING 2 In caso di addome acuto, il radiologo svolge un duplice compito:
Il nuovo Handbook della IARC
 Il nuovo Handbook della IARC Dott.ssa Paola Armaroli S.S.D. Epidemiologia Screening CPO AOU Città della Salute e della Scienza di Torino Via Cavour, 31,10123 Torino PROGRAMMA REGIONALE DISCREENING COLORETTALE
Il nuovo Handbook della IARC Dott.ssa Paola Armaroli S.S.D. Epidemiologia Screening CPO AOU Città della Salute e della Scienza di Torino Via Cavour, 31,10123 Torino PROGRAMMA REGIONALE DISCREENING COLORETTALE
ALLEGATO 1: REQUISITI INTRA-PROCEDURALI DELLA GASTROSCOPIA
 ALLEGATO 1: REQUISITI INTRA-PROCEDURALI DELLA GASTROSCOPIA Grado di raccomandazione Evidenza del beneficio Forza metodologica/evidenza scientifica a supporto Implicazioni 1A Chiara Trial randomizzati senza
ALLEGATO 1: REQUISITI INTRA-PROCEDURALI DELLA GASTROSCOPIA Grado di raccomandazione Evidenza del beneficio Forza metodologica/evidenza scientifica a supporto Implicazioni 1A Chiara Trial randomizzati senza
Dott. Fabrizio Maggiorelli U.O. Medicina d Urgenza e Pronto Soccorso Azienda ospedaliero Universitaria Pisana
 Pisa 26 febbraio 2016 L APPROCCIO CLINICO Dott. Fabrizio Maggiorelli U.O. Medicina d Urgenza e Pronto Soccorso Azienda ospedaliero Universitaria Pisana Non si tratta di una malattia ma di vari processi
Pisa 26 febbraio 2016 L APPROCCIO CLINICO Dott. Fabrizio Maggiorelli U.O. Medicina d Urgenza e Pronto Soccorso Azienda ospedaliero Universitaria Pisana Non si tratta di una malattia ma di vari processi
L'enteroscopia. a cura di: Marcello Ingrosso
 S.I.E.D. Società Italiana Endoscopia Digestiva L'enteroscopia a cura di: Marcello Ingrosso U.O.C. di Endoscopia Digestiva Chirurgica Centro di Ricerca e Formazione ad Alta Tecnologia Facoltà di Medicina
S.I.E.D. Società Italiana Endoscopia Digestiva L'enteroscopia a cura di: Marcello Ingrosso U.O.C. di Endoscopia Digestiva Chirurgica Centro di Ricerca e Formazione ad Alta Tecnologia Facoltà di Medicina
Approfondimenti scientifici
 Approfondimenti scientifici 8 Introduzione () Negli ultimi decenni, con l endoscopia gastrointestinale, i ricercatori e i clinici hanno avuto la precedentemente esclusa possibilità dell accesso diretto
Approfondimenti scientifici 8 Introduzione () Negli ultimi decenni, con l endoscopia gastrointestinale, i ricercatori e i clinici hanno avuto la precedentemente esclusa possibilità dell accesso diretto
Sanguinamento rettale nei pazienti con malattia diverticolare
 Sanguinamento rettale nei pazienti con malattia diverticolare Gianmichele Meucci Unità Operativa di Gastroenterologia e di Endoscopia digestiva (Direttore: Dott. F. Cosentino) Ospedale San Giuseppe -Milano
Sanguinamento rettale nei pazienti con malattia diverticolare Gianmichele Meucci Unità Operativa di Gastroenterologia e di Endoscopia digestiva (Direttore: Dott. F. Cosentino) Ospedale San Giuseppe -Milano
PERCORSO DIAGNOSTICO TERAPEUTICO DELLA MALATTIA PEPTICA
 Rev.: 0 Pag. 1/5 AUTORIZZAZIONI REV. DATA REDATTO VERIFICATO APPROVATO 26/06/02 DR. Matergi, Dr. Biscontri, Igiene e Dr. Diversi, Dr. Lavagni, Organizzazione dei Dr. Magnanelli Servizi Sanitari Rev.: 0
Rev.: 0 Pag. 1/5 AUTORIZZAZIONI REV. DATA REDATTO VERIFICATO APPROVATO 26/06/02 DR. Matergi, Dr. Biscontri, Igiene e Dr. Diversi, Dr. Lavagni, Organizzazione dei Dr. Magnanelli Servizi Sanitari Rev.: 0
COLITE ULCEROSA MODERNI ORIENTAMENTI DI CURA ENDOSCOPIA. Carlo Manfrini
 COLITE ULCEROSA MODERNI ORIENTAMENTI DI CURA ENDOSCOPIA Carlo Manfrini RUOLO DELL'ENDOSCOPIA DIAGNOSI DIFFERENZIALE SEDE,ESTENSIONE, ATTIVITA' VALUTAZIONE MODIFICAZIONI INDOTTE DA TERAPIA SCREENING DISPLASIA
COLITE ULCEROSA MODERNI ORIENTAMENTI DI CURA ENDOSCOPIA Carlo Manfrini RUOLO DELL'ENDOSCOPIA DIAGNOSI DIFFERENZIALE SEDE,ESTENSIONE, ATTIVITA' VALUTAZIONE MODIFICAZIONI INDOTTE DA TERAPIA SCREENING DISPLASIA
II UNIVERSITA DI NAPOLI
 II UNIVERSITA DI NAPOLI DIPARTIMENTO DI INTERNISTICA CLINICA E SPERIMENTALE Magrassi Lanzara Facoltà di Medicina e Chirurgia Cattedra di Chirurgia endoscopica Prof. Angelo Pezzullo Scuola di specializzazione
II UNIVERSITA DI NAPOLI DIPARTIMENTO DI INTERNISTICA CLINICA E SPERIMENTALE Magrassi Lanzara Facoltà di Medicina e Chirurgia Cattedra di Chirurgia endoscopica Prof. Angelo Pezzullo Scuola di specializzazione
6 a Conferenza Nazionale GIMBE Verso un approccio di sistema alla Clinical Governance
 6 a Conferenza Nazionale GIMBE Verso un approccio di sistema alla Clinical Governance Bologna, 11 febbraio 2011 Prescrizione delle colonscopie nella zona di Ancona: quali inappropriatezze? Matteo Marcosignori
6 a Conferenza Nazionale GIMBE Verso un approccio di sistema alla Clinical Governance Bologna, 11 febbraio 2011 Prescrizione delle colonscopie nella zona di Ancona: quali inappropriatezze? Matteo Marcosignori
Il paziente con sospetta occlusione intestinale
 Il Team Medico-Infermieristico nella Medicina Interna del terzo millennio Corso di Ecografia Bedside Carpi, 17 ottobre 2014 Il paziente con sospetta occlusione intestinale Esterita Accogli Centro di Ecografia
Il Team Medico-Infermieristico nella Medicina Interna del terzo millennio Corso di Ecografia Bedside Carpi, 17 ottobre 2014 Il paziente con sospetta occlusione intestinale Esterita Accogli Centro di Ecografia
Colonscopia di Sorveglianza dopo resezione del tumore del colon e dopo polipectomia Francesco Cupella
 Colonscopia di Sorveglianza dopo resezione del tumore del colon e dopo polipectomia Francesco Cupella L IGNORANZA E PIU VICINA ALLA VERITA CHE IL PREGIUDIZIO Candidati alla sorveglianza endoscopica postresezione
Colonscopia di Sorveglianza dopo resezione del tumore del colon e dopo polipectomia Francesco Cupella L IGNORANZA E PIU VICINA ALLA VERITA CHE IL PREGIUDIZIO Candidati alla sorveglianza endoscopica postresezione
Manifestazioni cliniche della Celiachia
 Manifestazioni cliniche della Celiachia Alessandro Pezzoli U.O. di Gastroenterologia ed Endoscopia digestiva Ospedale Sant Anna Ferrara Riunione AIC 5/4/2014 Malattia celiaca o enteropatia da glutine Condizione
Manifestazioni cliniche della Celiachia Alessandro Pezzoli U.O. di Gastroenterologia ed Endoscopia digestiva Ospedale Sant Anna Ferrara Riunione AIC 5/4/2014 Malattia celiaca o enteropatia da glutine Condizione
LA GESTIONE DEI PAZIENTI CON CANCRI pt1: ANALISI DI UNA CASISTICA DI SCREENING
 LA GESTIONE DEI PAZIENTI CON CANCRI pt1: ANALISI DI UNA CASISTICA DI SCREENING BACKGROUND -I tumori pt1 sono divisi in alto e basso rischio di mts linfonodali -Fattori predittivi: invasione linfo-vascolare
LA GESTIONE DEI PAZIENTI CON CANCRI pt1: ANALISI DI UNA CASISTICA DI SCREENING BACKGROUND -I tumori pt1 sono divisi in alto e basso rischio di mts linfonodali -Fattori predittivi: invasione linfo-vascolare
Stazione metropolitana Toledo - Arch. Óscar Tusquets. Congresso Nazionale. Palazzo Reale. delle Malattie Digestive Febbraio 2016
 Stazione metropolitana Toledo - Arch. Óscar Tusquets 22 Napoli, Congresso Nazionale Palazzo Reale delle Malattie Digestive 24-27 Febbraio 2016 CONGRESSO TAVOLA SINOTTICA NAZIONALE 24 FEBBRAIO delle Malattie
Stazione metropolitana Toledo - Arch. Óscar Tusquets 22 Napoli, Congresso Nazionale Palazzo Reale delle Malattie Digestive 24-27 Febbraio 2016 CONGRESSO TAVOLA SINOTTICA NAZIONALE 24 FEBBRAIO delle Malattie
Dott. Andrea Nucci Endoscopia Digestiva SGDD
 Dott. Andrea Nucci Endoscopia Digestiva SGDD COLONSCOPIA In paz molto anziani i vantaggi attesi dalla C. di screening non superano i potenziali rischi Ipotensione 9%, desaturazione 27% vs 19% Più alta
Dott. Andrea Nucci Endoscopia Digestiva SGDD COLONSCOPIA In paz molto anziani i vantaggi attesi dalla C. di screening non superano i potenziali rischi Ipotensione 9%, desaturazione 27% vs 19% Più alta
IBD Sorveglianza endoscopica: come, quando e per quanto tempo
 IBD Sorveglianza endoscopica: come, quando e per quanto tempo Giampaolo Angelini Verona, 23 novembre 2010 Sorveglianza endoscopica nelle IBD Perché? Maggior rischio di CRC in UC e CD colico Rischio cumulativo
IBD Sorveglianza endoscopica: come, quando e per quanto tempo Giampaolo Angelini Verona, 23 novembre 2010 Sorveglianza endoscopica nelle IBD Perché? Maggior rischio di CRC in UC e CD colico Rischio cumulativo
Il follow-up secondo le nuove linee guida
 Il follow-up secondo le nuove linee guida Prof. Franco Bazzoli U.O. Gastroenterologia Dipartimento di scienze mediche e chirurgiche Università di Bologna Obiettivi della sorveglianza Ridurre la morbilità
Il follow-up secondo le nuove linee guida Prof. Franco Bazzoli U.O. Gastroenterologia Dipartimento di scienze mediche e chirurgiche Università di Bologna Obiettivi della sorveglianza Ridurre la morbilità
Diagnostic accuracy of bedside abdominal ultrasound in patients with suspected diverticulitis.
 E. Donnarumma, C. Perani, C. Gigli, E. De Curtis, L. Naldi, F. di Mare, A. Bribani, G. Cerini, S. Gualtieri, A. Radaeli, P. Nazerian, S. Grifoni. Study group On behalf of US SIMEU Diagnostic accuracy of
E. Donnarumma, C. Perani, C. Gigli, E. De Curtis, L. Naldi, F. di Mare, A. Bribani, G. Cerini, S. Gualtieri, A. Radaeli, P. Nazerian, S. Grifoni. Study group On behalf of US SIMEU Diagnostic accuracy of
IL PROGRAMMA FS Arrigo Arrigoni S.C.GASTROENTEROLOGIA 2 Azienda Citta della Salute e della Scienza di Torino. Torino, 13 novembre 2013
 PROGRAMMA REGIONALE DI SCREENING COLORETTALE PREVENZIONE SERENA WORKSHOP 2013 IL PROGRAMMA FS Arrigo Arrigoni S.C.GASTROENTEROLOGIA 2 Azienda Citta della Salute e della Scienza di Torino Torino, 13 novembre
PROGRAMMA REGIONALE DI SCREENING COLORETTALE PREVENZIONE SERENA WORKSHOP 2013 IL PROGRAMMA FS Arrigo Arrigoni S.C.GASTROENTEROLOGIA 2 Azienda Citta della Salute e della Scienza di Torino Torino, 13 novembre
I rapporti con i professionisti: il retraining degli endoscopisti. Emilio Di Giulio SIED
 IL CCM PER LA PREVENZIONE - PREVENZIONE SECONDARIA DEI TUMORI DELLA MAMMELLA, CERVICE UTERINA E COLONRETTO Ministero del Lavoro, Salute e Politiche Sociali, CCM - Centro Nazionale per la Prevenzione ed
IL CCM PER LA PREVENZIONE - PREVENZIONE SECONDARIA DEI TUMORI DELLA MAMMELLA, CERVICE UTERINA E COLONRETTO Ministero del Lavoro, Salute e Politiche Sociali, CCM - Centro Nazionale per la Prevenzione ed
Corso Integrato Medicina Clinica-Chirurgica
 Corso Integrato Medicina Clinica-Chirurgica Insegnamenti (SSD): Medicina Interna MED/09 Chirurgia Generale MED/18 Chirurgia Pediatrica MED/20 Pediatria generale e Specialistica MED/38 Scienze Infermieristiche
Corso Integrato Medicina Clinica-Chirurgica Insegnamenti (SSD): Medicina Interna MED/09 Chirurgia Generale MED/18 Chirurgia Pediatrica MED/20 Pediatria generale e Specialistica MED/38 Scienze Infermieristiche
(Patrocini richiesti) Corso di Aggiornamento ECM
 (Patrocini richiesti) Città di Castiglione delle Stiviere Corso di Aggiornamento ECM Ospedale OGGI - GASTRONEWS NOVITÀ IN GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA Castiglione delle Stiviere (MN) 21 maggio
(Patrocini richiesti) Città di Castiglione delle Stiviere Corso di Aggiornamento ECM Ospedale OGGI - GASTRONEWS NOVITÀ IN GASTROENTEROLOGIA ED ENDOSCOPIA DIGESTIVA Castiglione delle Stiviere (MN) 21 maggio
IMAGING delle MICI. Carlo Amodio
 IMAGING delle MICI Carlo Amodio IMAGING DELLE MICI RX intestino tenue con bario RX enteroclisi doppio contrasto Ecografia intestinale Entero -TC Enterografia RM RM enteroclisi IMAGING DELLE M.I.C.I. PATOMORFOSI
IMAGING delle MICI Carlo Amodio IMAGING DELLE MICI RX intestino tenue con bario RX enteroclisi doppio contrasto Ecografia intestinale Entero -TC Enterografia RM RM enteroclisi IMAGING DELLE M.I.C.I. PATOMORFOSI
Trattamenti endoscopici sull intestino tenue con l enteroscopia a doppio pallone: possibilità e limiti della metodica
 Trattamenti endoscopici sull intestino tenue con l enteroscopia a doppio pallone: possibilità e limiti della metodica Endoscopic interventions in the small bowel using double balloon enteroscopy: feasibility
Trattamenti endoscopici sull intestino tenue con l enteroscopia a doppio pallone: possibilità e limiti della metodica Endoscopic interventions in the small bowel using double balloon enteroscopy: feasibility
www.fisiokinesiterapia.biz
 NUOVE METODICHE DIAGNOSTICHE Nuove Metodiche diagnostiche Breath tests Videocapsula Endoscopia a Doppio Pallone Endoscopia Virtuale Endoscopia nuove tecniche narrow banding magnificazione e colorazione
NUOVE METODICHE DIAGNOSTICHE Nuove Metodiche diagnostiche Breath tests Videocapsula Endoscopia a Doppio Pallone Endoscopia Virtuale Endoscopia nuove tecniche narrow banding magnificazione e colorazione
Daniele Regge Gabriella Iussich La colonscopia virtuale
 Springer Daniele Regge Gabriella Iussich La colonscopia virtuale Guida pratica all esame, dalle indicazioni all interpretazione dei dati Daniele Regge Gabriella Iussich Direzione Operativa di Radiodiagnostica
Springer Daniele Regge Gabriella Iussich La colonscopia virtuale Guida pratica all esame, dalle indicazioni all interpretazione dei dati Daniele Regge Gabriella Iussich Direzione Operativa di Radiodiagnostica
LE STENOSI ANASTOMOTICHE DIGESTIVE TRATTAMENTI A CONFRONTO
 LE STENOSI ANASTOMOTICHE DIGESTIVE TRATTAMENTI A CONFRONTO Dr. Giorgio Benedetti SSD Gastroenterologia OC PN Riunione SIED/AIGO Udine, 12 Aprile 2010 LE STENOSI ANASTOMOTICHE DIGESTIVE LE STENOSI DELLE
LE STENOSI ANASTOMOTICHE DIGESTIVE TRATTAMENTI A CONFRONTO Dr. Giorgio Benedetti SSD Gastroenterologia OC PN Riunione SIED/AIGO Udine, 12 Aprile 2010 LE STENOSI ANASTOMOTICHE DIGESTIVE LE STENOSI DELLE
Luigi Aronne. Malattia diverticolare Etiopatogenesi Condizioni ambientali Dieta povera di fibre Sviluppo socioeconomico Alterata motilità del colon
 Malattia Diverticolare Descrizione della patologia (Cruvelheir 1849) Primo studio completo (Graser 1899) Base anatomica (1904) Primo intervento per diverticolite complicata ( Luigi Aronne Definizione Diverticoli
Malattia Diverticolare Descrizione della patologia (Cruvelheir 1849) Primo studio completo (Graser 1899) Base anatomica (1904) Primo intervento per diverticolite complicata ( Luigi Aronne Definizione Diverticoli
ESAME RADIOGRAFICO DELL APPARATO DIGERENTE
 ESAME RADIOGRAFICO DELL APPARATO DIGERENTE Che cos'è? INFORMAZIONI E' l'esame radiografico del tubo digerente superiore (esofago, stomaco, duodeno) e delle anse intestinali, ottenuto mediante opacizzazione
ESAME RADIOGRAFICO DELL APPARATO DIGERENTE Che cos'è? INFORMAZIONI E' l'esame radiografico del tubo digerente superiore (esofago, stomaco, duodeno) e delle anse intestinali, ottenuto mediante opacizzazione
ISPECO S.r.l Ispezioni Controlli [METODI DI INDAGINE CND INERENTI I FASCI TUBIERI DI SCAMBIATORI]
![ISPECO S.r.l Ispezioni Controlli [METODI DI INDAGINE CND INERENTI I FASCI TUBIERI DI SCAMBIATORI] ISPECO S.r.l Ispezioni Controlli [METODI DI INDAGINE CND INERENTI I FASCI TUBIERI DI SCAMBIATORI]](/thumbs/99/141303063.jpg) 2014 S.r.l Ispezioni Controlli [METODI DI INDAGINE CND INERENTI I FASCI TUBIERI DI SCAMBIATORI] Descrizione dei metodi di indagine CND inerente i fasci tubieri di scambiatori I controlli CND sui fasci
2014 S.r.l Ispezioni Controlli [METODI DI INDAGINE CND INERENTI I FASCI TUBIERI DI SCAMBIATORI] Descrizione dei metodi di indagine CND inerente i fasci tubieri di scambiatori I controlli CND sui fasci
PROGRAMMA REGIONALE DI SCREENING COLORETTALE PREVENZIONE SERENA WORKSHOP 2018 INDICATORI DIAGNOSTICI: IL PROGRAMMA CON SIGMOIDOSCOPIA.
 PROGRAMMA REGIONALE DI SCREENING COLORETTALE PREVENZIONE SERENA WORKSHOP 2018 INDICATORI DIAGNOSTICI: IL PROGRAMMA CON SIGMOIDOSCOPIA Renato Fasoli S.C. Gastroenterologia ed Endoscopia Digestiva - Ospedale
PROGRAMMA REGIONALE DI SCREENING COLORETTALE PREVENZIONE SERENA WORKSHOP 2018 INDICATORI DIAGNOSTICI: IL PROGRAMMA CON SIGMOIDOSCOPIA Renato Fasoli S.C. Gastroenterologia ed Endoscopia Digestiva - Ospedale
Piccolo intestino. (Esclusi i linfomi, i tumori carcinoidi ed i sarcomi viscerali) C17.8 Lesione sovrapposta del piccolo intestino
 11 Piccolo intestino (Esclusi i linfomi, i tumori carcinoidi ed i sarcomi viscerali) C17.0 Duodeno C17.1 Digiuno C17.2 Ileo C17.8 Lesione sovrapposta del piccolo intestino C17.9 Piccolo intestino, NAS
11 Piccolo intestino (Esclusi i linfomi, i tumori carcinoidi ed i sarcomi viscerali) C17.0 Duodeno C17.1 Digiuno C17.2 Ileo C17.8 Lesione sovrapposta del piccolo intestino C17.9 Piccolo intestino, NAS
PRIMA DELL INCIDENTE:
 PRIMA DELL INCIDENTE: La prevenzione secondaria Dott.ssa Karen Borgonovo UO Oncologia Medica ASST BG Ovest Direttore: Dr S. Barni La prevenzione secondaria Mira ad effettuare una diagnosi precoce in modo
PRIMA DELL INCIDENTE: La prevenzione secondaria Dott.ssa Karen Borgonovo UO Oncologia Medica ASST BG Ovest Direttore: Dr S. Barni La prevenzione secondaria Mira ad effettuare una diagnosi precoce in modo
- Prof. NOBILI - Prof. S.CUCCHIARA - Prof. L.STRONATI - Prof. D.ALVARO - Prof. D. COZZI ITALIANO
 Piano formativo del Master di II llo in GASTROENTEROLOGIA EPATOLOGIA E NUTRIZIONE IN ETA PEDIATRICA Dipartimento PEDIATRIA Facoltà Medicina e Chirurgia Direttore del Master: Consiglio Didattico Scientifico
Piano formativo del Master di II llo in GASTROENTEROLOGIA EPATOLOGIA E NUTRIZIONE IN ETA PEDIATRICA Dipartimento PEDIATRIA Facoltà Medicina e Chirurgia Direttore del Master: Consiglio Didattico Scientifico
