Appunti del Corso di Patologia e Fisiopatologia Generale del Professor E. Albano
|
|
|
- Simone Deluca
- 5 anni fa
- Visualizzazioni
Transcript
1 Università degli Studi del Piemonte Orientale A. Avogadro Corso di Laurea in Medicina e Chirurgia Appunti del Corso di Patologia e Fisiopatologia Generale del Professor E. Albano - PARTE 1 - A.A. 2013/2014
2 INDICE FISIOPATOLOGIA L INFIAMMAZIONE... 3 Gli attori del processo infiammatorio... 3 La fase vascolare... 4 Infiammazione sierosa... 6 Infiammazione siero-fibrinosa... 6 Infiammazione catarrale... 6 Infiammazione purulenta... 6 Infiammazione emorragica... 6 I mediatori del processo infiammatorio... 7 Attivazione della risposta infiammatoria... 7 Sostanze che mediano l infiammazione Diapedesi leucocitaria Selectine, loro recettori e loro attività Ruolo delle piastrine nel processo di diapedesi leucocitaria Fagocitosi Terminazione dell infiammazione Infiammazione cronica RISPOSTE SISTEMICHE ALL INFIAMMAZIONE Leucocitosi Risposta di fase acuta Effetti metabolici Patogenesi della sindrome infiammatoria sistemica (SIRS) e dello shock settico Patogenesi dell ARDS (Adult Respiratory Distress Syndrome) Febbre Fisiopatologia della febbre Evoluzione del processo febbrile LA FIBROSI La cirrosi epatica MECCANISMI DI RIPARAZIONE DEL DANNO TISSUTALE Riparazione delle ferite dermo-epidermiche e del tessuto epiteliale Reclutamento della risposta infiammatoria Neoangiogenesi Riparazione Riparazione delle fratture ossee Guarigione del tessuto nervoso Gli esiti del processo di riparazione
3 L INFIAMMAZIONE L infiammazione è la risposta al danno da parte dei tessuti vascolarizzati. Il suo scopo è quello di reclutare materiale difensivo nella sede danneggiata. Non è quindi uno stato, bensì un processo e come tale presenta una dinamica propria. Inoltre, si integra con la risposta immunitaria ed è filogeneticamente molto antica. Le interazioni tra le due entità avvengono sia nella fase di riconoscimento della noxa patogena, sia nella fasi effettrici e di riparazione. Il processo infiammatorio è noto da tempi immemorabili per quanto concerne il suo quadro sintomatologico(tumor, dolor, calor, functio lesa). Inoltre, esistono dei modelli costantemente riprodotti nei processi infiammatori acuti. es. polmonite acuta: alveoli che presentano dilatazione dei vasi e pieni di essudato(tante cellule). es. miocardite acuta: il tessuto danneggiato risulta profondamente infiltrato da cellule infiammatorie. L infiammazione presenta una sua particolare evoluzione; se la causa del danno è eliminata si determina infiammazione acuta e poi guarigione, mentre, la causa perdura nel tempo, si determina infiammazione cronica. Gli attori del processo infiammatorio Le cellule che vengono coinvolte nel processo infiammatorio sono quelle che è possibile ritrovare nei vasi sanguigni, soprattutto a livello del distretto capillare. Tra questi vi sono cellule endoteliali, leucociti, suddivisibili in granulociti(eosinofili, basofili e neutrofili) e agranulociti(monociti e linfociti), globuli rossi e piastrine. Neutrofili: presentano citoplasma acidofilo con numerosi granuli distinti in primari, con ricco contenuto di proteine ad azione difensiva come lisozima, enzimi litici e mieloperossidasi, secondari, con proteine ad azione difensiva come lisozima e lattoferrina, e terziari, contenenti diversi enzimi litici. Il contenuto viene riversato all esterno con vescicole, dove esegue diverse funzioni. 3
4 Monociti: numericamente meno numerosi, hanno vita lunga e possono anche proliferare; sono divisi in monociti circolanti, grosse cellule dal grande nucleo e dal citoplasma grigiastro ricco di granuli contenenti enzimi litici e un vasto corredo di mitocondri, in grado di modificare il loro assetto differenziativo producendo grande varietà di mediatori, e una seconda popolazione che non viene reclutata subito, ma è coinvolta nei processi della risposta ripartiva(non è ancora chiara la loro funzione). I macrofagi tissutali derivano dai monociti che possono differenziarsi in diverse tipologie di macrofagi. Ognuna di queste varianti ha caratteristiche diverse e costituiscono sentinelle che si attivano in risposta al danno. Mastocita basofili: poco numerosi, ma molto specializzati. Precursori di cellule presenti nel tessuto noti come mastcellule, dove si localizzano le IgE e si attivano in caso di allergie ed infiammazioni rilasciando soprattutto istamina. Eosinofilo: rappresentano il 2% delle cellule del sangue; partecipano alla difesa dei parassiti e alla regolazione del processo immunitario. Linfociti: cellule chiave nelle risposta immunitaria, interagiscono con i monociti nella risposta infiammatoria. Plasmacellule: ricche di reticolo endoplasmatico rugoso necessario alla sintesi di anticorpi. Piastrine: mancano di nucleo; si attivano dopo il danno legandosi fra loro e liberando il contenuto dei loro granuli. Partecipano alla sintesi di mediatori coinvolti nella terminazione dei processi infiammatori. Importanti per la riparazione tissutale: interagiscono con cellule endoteliali, che presentano molecole di adesione se infiammate. Cellule endoteliali: libera fattori proinfiammatori ed esprime molecole di adesione e regola il tono vascolare e quindi la quantità di sangue che affluisce. Le cellule derivano da un precursore comune. La sintesi è regolata dalle stesse risposte infiammatorie. La fase vascolare I vasi sanguigni rappresentano il punto chiave del processo infiammatorio. Dopo un taglio sulla cute si possono osservare i segni clinici dell infiammazione, come ad esempio prendiamo il rubor(rossore). Circa secondi dopo la lesione, l area appare arrossata, per attivazione di istiociti e mastociti; si osserva quindi una zona di iperemia dovuta a vasodilatazione (in seguito all apertura di sfinteri precapillari con conseguente aumento del flusso sanguigno)e attorno alla zona lesa appare un alone arrossato. Dopo 1-3 minuti la zona si presenta ancora arrossata, ma la parte centrale è pallida e da essa fuoriesce del liquido (la pressione tende a ridurre l iperemia). Un aspetto importante è dato dall innervazione: dalle fibre sensitive che innervano gli sfinteri precapillari, stimolate dalla lesione, liberano sostanza P e/o ATP, condizione che determina apertura dello sfintere. Si ha inoltre attivazione di istiociti e mastcellule, che degranulano liberando istamina, la quale determina vasodilatazione. A livello dei capillari si ha aumento del flusso sanguigno con 4
5 espansione del letto capillare stesso, che determina quindi il quadro di iperemia. Questa variazione del microcircolo modifica i livelli di pressione dei capillari ed è responsabile del cosiddetto tumor, ossia dell aumento della permeabilità. È importante tenere conto delle forze implicate nella filtrazione e nel riassorbimento dei liquidi lungo i capillari e le venule (legge di Starling degli scambi idrici capillari). In particolare, si ha partecipazione della pressione laterale o idrostatica e della pressione oncotica. Il liquido che fuoriesce forma l essudato infiammatorio. Per evidenziare il tumor si effettua un esperimento: dopo aver iniettato in circolo dell inchiostro di china si osserva dove si posizionano le particelle di nerofumo; è possibile notare che esse si localizzano negli spazi sottoendoteliali. Quindi, non solo aumenta il numero di capillari inondati di sangue, ma si determina anche un fenomeno per cui si ha passaggio di particelle; ciò avviene grazie alla contrazione delle cellule endoteliali, che delimitano dei varchi tra esse stesse. In questo modo si ha aumento della permeabilità capillare. Ci sono cause ed entità diverse per quanto riguarda l aumento della permeabilità: Casi lievi, di breve durata, per squilibri idrostatici, che vedono transitori aumenti della permeabilità Ferite e ustioni di modesto grado sono caratterizzate da aumenti di permeabilità più massicci Casi gravi (ustioni termiche, ipossia, sindrome da schiacciamento) in cui è possibile riscontrare danni all epitelio, elevata fuoriuscita di liquidi e passaggio di componenti proteici; possono fuoriuscire anche le cellule. La formazione dell essudato è dovuta ad alterazioni a livello degli equilibri idroelettrolitici, con aumento della permeabilità capillare. Si ha una distinzione tra trasudato ed essudato: Trasudato: ha peso specifico inferiore a 1,012 (simile a quello dell acqua), è caratterizzato da un basso contenuto proteico. Si forma per alterazione degli equilibri idroelettrolitici, ma senza aumento della permeabilità vascolare(es. idrotorace) Essudato: ha peso specifico superiore a 1,020, la quantità di proteine totali è maggiore che nel trasudato. La sua formazione deriva dalla variazione degli equilibri idroelettrolitici e dall aumento della permeabilità capillare(es. pleurite acuta) La finalità del processo infiammatorio è il trasferimento dal sangue all interstizio di sostanze tramite l essudato. Alcune forme di essudato infiammatorio prevedono anche il passaggio di cellule, che è un fenomeno attivo. Grazie ai segnali che determinano il trasferimento delle cellule dal sangue agli spazi intercellulari si forma l infiltrato infiammatorio. Le cellule che possono essere coinvolte sono leucociti, talvolta eritrociti (ad esempio nella polmonite lobare), per aumento della permeabilità vascolare, passaggio di proteine e cellule della serie bianca e rossa (microemorragia). La composizione cellulare dell infiltrato infiammatorio non è costante nel tempo. In generale, la prima tipologia di cellule coinvolta è data dai granulociti neutrofili, che compaiono nell essudato già nelle prime ore. La loro presenza nell essudato è transitoria, essi infatti sono destinati a essere rimpiazzati (dopo l attivazione vanno incontro ad apoptosi) da altri tipi cellulari. Nelle fasi avanzate si assiste al reclutamento dei monociti, che differenziano in cellule macrofagiche a lunga sopravvivenza. I monociti-macrofagi possono essere anche responsabili della perpetuazione cronica dell infiammazione. Successivamente intervengono cellule specializzate, i linfociti (il loro reclutamento può avvenire o meno, se avviene esso è tardivo). Spesso nelle infiammazioni acute i linfociti non sono reclutati, oppure vengono reclutati tardi. 5
6 La formazione dell essudato si suddivide in 3 fasi: Iniziale transitoria, che dura circa 30 minuti e dipende dall istamina. Immediata prolungata, che inizia subito e può durare anche diversi giorni; si deve alla lesione dell endotelio. Ritardata prolungata,che dura da 4 a 24 ore e può essere caratterizzata da dolore. Infiammazione sierosa Processo flogistico caratterizzato da essudato limpido, povero di cellule e fibrina che nella cute si può accumulare fra epitelio e derma a formare bolle o flittene in conseguenza a stimoli di natura fisica o chimica(conseguenza della permeabilità capillare modificata). Infiammazione siero-fibrinosa Processo flogistico caratterizzato da essudato ricco di fibrina, derivata dalla trasformazione del fibrinogeno(es. miocardite fibrinosa da infezione virale). Porta ad alterazione della superficie sierosa stessa. Infiammazione catarrale Interessa mucose che producono muco per la presenza di cellule caliciformi mucipare, quali le vie aeree superiori, l apparato gastroenterico e l apparato urogenitale, con la formazione di un essudato ricco di muco che possiede attività battericida poiché contiene ferritina, lisozima ed IgA secretorie. Infiammazione purulenta Caratterizzata dalla presenza di essudato ricco di cellule flogistiche, chiamato pus. Ha consistenza cremosa, colore giallastro e ph acido(circa 5,7) dovuto alla presenza di acido lattico. È prodotto in presenza di batteri detti piogeni(es. meningite purulenta). Il pus tende a raccogliersi in cavità a formare ascessi. Si forma per necrosi colliquativa del tessuto e circoscritta da una membrana costituita da tessuto di granulazione detta membrana piogena. Se l essudato purulento non è circoscritto si forma un flémmone, mentre se si raccoglie in cavità preformate, quali pleura, peritoneo ecc.., si crea un empiema. Infiammazione emorragica L infiltrato flogistico è caratterizzato dalla presenza, oltre che di leucociti, anche di un elevata quantità di globuli rossi, provocata da una lesione diretta dei capillari ad opera di una noxa patogena(es. polmonite acuta). 6
7 I mediatori del processo infiammatorio I mediatori coinvolti nel processo infiammatorio sono responsabili della formazione di un intricata rete di segnali. Molti dei mediatori hanno funzioni pleiotrope, ossia svolgono più attività contemporaneamente. Si possono immaginare come parole, che assumono un significato diverso a seconda della frase. Molti di essi sono strettamente interdipendenti nell interazione tra immunità innata e specifica. L immunità innata coinvolge molte cellule e costituisce la prima risposta. L immunità specifica coinvolge poche cellule in quella che è la seconda risposta. Attivazione della risposta infiammatoria L attivazione della risposta infiammatoria può essere scatenata mediante due diversi meccanismi: segnali derivanti da agenti infettivi: PAMPs (Patogen Associated Molecular Patterns) segnali derivanti dal danno cellulare: DAMPs (Damage Associated Molecular Patterns). I PAMPs e i DAMPs sono recepiti dai PRR (Pattern Recognition Receptors), recettori a bassa affinità che determinano l attivazione delle risposte cellulari, con rilascio di mediatori della risposta infiammatoria. Esempi di PAMPs: Lipoproteine Glicolipoproteine Lipopolisaccaridi Acido lipoteicoico Flagellina DNA e RNA a doppio o singolo filamento Peptidoglicani Peptidi formilati (formil-metionina) Glicidi contenenti mannosio Zimosano Lipidi ossidati I PRR possono essere recettori solubili: - collettine: lectina legante il mannosio (MBL), proteine A e D del surfactante (SP-A, SP-D), dectina 1 e 2, ficoline - fattori del complemento - pentrassine corte: proteina C reattiva (CRP), proteina sierica dell amiloide (SAP) 7
8 - pentrassine lunghe: PTX2-4, pentrassine neurali. Sono prodotte in periferia e legano cellule in apoptosi oppure organismi patogeni. recettori di membrana (a 7 eliche): - recettori dei peptidi formilati (FRP1, FRP2) - recettori lectinici: recettori del mannosio - recettori Toll-like - recettori scavenger (spazzini): CD14, CD36, RAGE, LOX1, SR-A, SR-B recettori citoplasmatici: - recettori NOD (NOD1 e 2) - recettori RIG-1-like (RLR): RIG-1, MDA5 - AIM-2 - NOD-like (NLPR1-14) La famiglia dei Toll-Like Receptors (TLR) nell uomo è formata da 9 membri e devono il loro nome alla somiglianza con i recettori Toll, scoperti nelle mosche. Essi possono esistere in forma monomerica oppure in forma dimerica e possono agire come recettori singoli oppure combinati con altre proteine di membrana, come ad esempio CD14. I TLR hanno una vasta capacità di risposta a un gran numero di PAMPs, con un relativo grado di specificità. Gruppi di TLR riconoscono gruppi di PAMPs e DAMPs. Dall interazione tra TLR4 e CD14 si scatena una via di trasduzione del segnale che culmina con l attivazione di NFkB, via attivata in risposta al riconoscimento da parte di CD14 del complesso di LBP(Binding Protein) con LPS(lipopolisaccaridi batterici, soprattutto gram - ). La porzione intracellulare del TLR va incontro a una modificazione conformazionale, con conseguente reclutamento di Myd88. Si forma un complesso con due chinasi, IRAK-1 e IRAK-4, che fosforilano TRAF6. La proteina TRAF6 fosforilata forma un complesso con TAK1 e TAK2, che determina attivazione di NFkB. Ci può essere il coinvolgimento di un altra via, per cui si attiva una cascata di chinasi che mantiene i segnali proinfiammatori. Alcuni TLR trasducono il segnale attraverso una via indipendente, che coinvolge TIRF: si ha aggregazione intracellulare, si attiva TRF3, ciò porta alla trascrizione degli interferoni primari. Alcuni TLR, come il 7 e il 9, non si trovano sulla membrana cellulare, ma negli endosomi (che si formano per i processi di micropinocitosi cellulare); essi riconoscono mrna a doppio filamento e DNA con sequenze CpG, determinando attivazione di una via di trasduzione di allarme e di una che dà attivazione degli interferoni primari, determinando così resistenza alle infezioni virali. È importante sottolineare il ruolo cruciale del sistema di NFkB, attivato in risposta a segnali provenienti da patogeni o danno cellulare, esplicati sotto forma di mediatori proinfiammatori. Evento cruciale è la fosforilazione di IKK1 e IKK2, complessati con NEMO nella forma inattiva. Dopo la fosforilazione, queste chinasi fosforilano il complesso di inibizione di NFkB, chiamato IkB; si liberano i dimeri p65-p50 di NFkB, che migrano nel nucleo, attivando così l espressione genica di: mediatori proinfiammatori molecole di adesione molecole per la produzione di prostaglandine, NO Questo programma si attua in cellule monocitarie ed endoteliali. Mutazioni a carico di CD14 danno diminuzione della risposta a lipopolisaccaridi. Mutazioni a carico di TLR4 o IRAK-4 determinano riduzione della risposta a batteri e aumento della gravità 8
9 dell infiammazione. Polimorfismi genetici a carico di NEMO di PKA sono alla base di una ridotta capacità di risposta a virus o batteri. Tra i PRR citoplasmatici si annoverano i recettori NOD, i recettori RIG e i recettori RLR. I RLR riconoscono sequenze di RNA a doppia elica o frammenti di DNA, attraverso il recettore MDA5. L attivazione di questa via si ha nella risposta a virus. I recettori RLR legano le molecole di RNA attraverso attività enzimatica elicasica, ubiquitinazione e legame alla membrana mitocondriale; si attivano meccanismi di trasduzione che coinvolgono chinasi (IKK1, TRIF, ecc.), che determinano attivazione di fattori di trascrizione per interferoni (α e β). Gli IFN-α e β promuovono la trascrizione di geni antivirali, determinando blocco della proliferazione cellulare, resistenza all infezione virale, attivazione di RNAsi, il risultato è il contenimento della diffusione virale. Questo meccanismo, filogeneticamente antico, è indipendente dall immunità. Un esempio è dato dal meccanismo di controllo del raffreddore. I recettori della famiglia NOD e NOD-like appartengono a un ulteriore sistema di allarme, che è l inflammosoma. Esso è un complesso di recettori intracellulari che comprende un membro della famiglia delle proteine NALP, cui appartengono NOD1 e NOD2, la proteina adattatrice ASC e la molecola effettrice, costituita dall enzima proteolitico che attiva IL-1 (ICE) e molecole correlate. Si ha attivazione di tale complesso in seguito al riconoscimento di DAMPs: HMGB1(High-Mobility Group Box 1 protein), da parte di TLR-2/-4 e RAGE. HMGB1 è una proteina nucleare che viene rilasciata durante la lisi nucleare. Acido urico Cromatina e DNA (TLR-9) Heat shock proteins (TLR-2, CD14) Galetine (CD2/3) Thioredoxina Prodotti di degradazione della matrice extracellulare Miosina non muscolare (IgM) Fosfolipidi ossidati Proteine formilate mitocondriali Proteine rilasciate durante la necrosi cellulare (ad esempio SAP130, riconosciuta dal recettore CLEC4E presente sulla membrana cellulare macrofagica) Le proteine recettoriali si possono aggregare a formare un complesso intracitoplasmatico che può legare ASC, la quale complessa con caspasi 1. Il risultato è l attivazione della caspasi 1, che è in grado di attivare una proteina presente in forma inerte nel citoplasma (IL-1β o IL-18). IL-1β ha un ruolo importante nell attivare la risposta infiammatoria, da sola scatena segnali di allarme (in modo simile a PAMPs e DAMPs). La risposta infiammatoria può essere enormemente amplificata, poiché una singola cellula che riconosce un PAMP rilascia grandi quantità di IL-1-. Questo avviene in pochi millisecondi, a differenza della risposta mediata da NFkB, che passa per il nucleo. IL-1 innesca una via di trasduzione del segnale uguale a quella del TLR. Quindi ne mima gli effetti, in modo amplificato, determinando così l attivazione di un grande numero di cellule infiammatorie. Questi tipi di segnali sono indispensabili nella risposta adattativa. Quando una cellula dendritica riconosce un antigene in presenza di attivazione di recettori per DAMPs e PAMPs, si attiva e scatena una risposta, inducendo una risposta immunitaria di tipo adattativo molto rapida. Il riconoscimento di un antigene quando non si ha attivazione mediata da PAMPs/DAMPs determina anergia. Questo è importante nelle malattie autoimmuni. 9
10 Sostanze che mediano l infiammazione Per quanto riguarda i mediatori dell infiammazione, si distinguono quelli generati dalle cellule e quelli provenienti dal plasma: Dalle cellule: - Istamina - Ossido nitrico - PAF - Eicosanoidi - Enzimi (proteasi) - Derivati dell ossigeno - Citochine/chemochine - Sostanza P Tra le amine vasoattive è importante l istamina, un mediatore della risposta vascolare primaria. L istamina è contenuta nei granuli primari dei mastociti, all interno dei quali è legata a catene di glicosaminoglicani con serotonina e chimasi; deriva dall amminoacido istidina per una reazione di decarbossilazione. I complessi contenuti nei granuli dei mastociti sono rilasciati subito dopo l attivazione cellulare. Gli stimoli che causano la degranulazione e quindi la liberazione di istamina sono: Agenti fisici (trauma, calore) Reazioni immunologiche: i mastociti possiedono il recettore per le IgE Presenza di anafilotossine (C3a, C5a) Presenza di prodotti liberati da neutrofili, monociti e piastrine IL-1 L azione dell istamina si esplica attraverso la stimolazione dei recettori H1 (e H2), presenti sulla membra a di cellule endoteliali, macrofagi, ecc. Le cellule endoteliali: si contraggono, aumentando la permeabilità dei vasi; producono ossido nitrico (NO), che raggiunge le cellule muscolari lisce, inducendo vasodilatazione; espongono molecole di adesione per i leucociti. 10
11 L istamina stimola le fibre nervose, inducendo prurito. Questa sostanza ha effetti rapidi ma transitori, infatti è rapidamente inattivata dall enzima istaminasi, rilasciato da neutrofili ed eosinofili. Se non c è liberazione di altri mediatori, gli effetti cessano presto. L ossido nitrico (NO) è sintetizzato a partire dall amminoacido arginina grazie all azione di una famiglia di enzimi che prende il nome di NO sintasi (NOS). Nelle cellule endoteliali è presente un isoenzima cosititutivo, enos, attivato dal calcio. La produzione basale di NO è responsabile del tono vasale; l aumento di NO derivante da enos è responsabile della vasodilatazione che caratterizza le prime fasi dell infiammazione. Nei macrofagi attivati viene indotto un altro isoenzima NOS, denominato inos (NOS inducibile): inos non è regolata dal calcio ed è in grado di sintetizzare NO in quantità molto elevate. In queste condizioni NO non funziona solo come vasodilatatore, ma formando nitroperossido che contribuisce all azione battericida: NO + O2 - ONOO - NO può inoltre legarsi all amminoacido tirosina, formando nitrotirosina. I metaboliti dell acido arachidonico possono essere prodotti dagli enzimi cicloossigenasi 1 e 2 (COX1 e COX2) oppure per ossidazione mediata dagli enzimi lipossigenasi. Nell infiammazione hanno una funzione importante soprattutto PGH2, PGG, PGE2 e PGF2, che esplicano un ruolo di supporto all azione dell istamina, rendendo gli effetti più duraturi e persistenti. Le prostaglandine stimolano la permeabilità vascolare, determinano vasodilatazione, inducono chemiotassi, attivano le cellule endoteliali e i macrofagi, partecipano alla risposta sistemica all infiammazione (risposta febbrile). Per quanto riguarda COX, distinguiamo: COX1: atta alla produzione basale di prostaglandine, è ubiquitaria COX2: responsabile della produzione di prostaglandine durante la risposta infiammatoria. È un enzima inducibile (attraverso NFkB). La sintesi di prostaglandine si combina con l attività delle 5-lipossigenasi (raramente di 15- lipossigenasi). L ossidazione in posizione 5 dell acido arachidonico determina la produzione di leucotrieni, molecole con struttura non ciclizzata che spesso sono coniugate con glutatione; a seconda dell amminoacido proveniente dalla molecole di glutatione si ha: LTA LTD LTC Ci sono anche LTE e LTB. I leucotrieni LTE4, LTD4 e LTC4 stimolano l aumento della permeabilità capillare e la contrazione del muscolo liscio bronchiale. LTB4 stimola inoltre la chemiotassi dei neutrofili. Leucotrieni e prostaglandine erano detti SRS-A (Slow Reacting Susbstances of Anaphylaxis). Il lisofosfolipide che si forma in seguito all azione dell enzima fosfolipasi A2 forma il PAF(Platelet Activating Factor, fattore di attivazione delle piastrine). Il PAF deriva dall acetilazione in posizione 2 del liso-paf, derivante dalla fosfatidilcolina. Il PAF è responsabile di una vasta gamma di effetti: 11
12 agisce sulle cellule dell epitelio renale, stimolando la sintesi di prostaglandine. stimola, a livello di monociti-macrofagi, l aggregazione, la chemiotassi, l aumento della distensione, la differenziazione, la produzione di anione superossido e la produzione di prostaglandine e trombossano. stimola la chemiotassi degli eosinofili. stimola l attivazione e l aggregazione a livello delle piastrine. stimola la contrazione delle cellule muscolari lisce dei vasi. stimola aggregazione, chemiotassi e marginazione dei neutrofili. stimola la contrazione delle cellule endoteliali a livello venulare. stimola la contrazione delle cellule del mesangio. Le citochine sono mediatori proteici capaci di mettere in comunicazione tra loro le cellule. Sono segnali scambiati tra le cellule e agiscono in maniera autocrina/paracrina; possono avere effetti endocrini. Comprendono molti composti chimici diversi, tra cui: Proteine che agiscono come fattori di crescita localmente o a livello del midollo emopoietico (GM-CSF) Interferoni, primari (α e β), secondari (γ) Interleuchine: un gruppo di mediatori proteici che mettono in comunicazione cellule diverse. Oltre alle interleuchine propriamente dette c è il TNF-α e -β. Vi sono anche le chemochine, responsabili della regolazione della motilità cellulare. Considerando le citochine in base alla loro funzione, abbiamo: Citochine emopoietiche: GM-CSF Citochine dell immunità specifica: IL-2, IFN-γ, IL-4 Citochine infiammatorie primarie: IL-1, TNF-α, IL-6 Citochine infiammatorie secondarie: IL-12, chemochine Citochine antinfiammatorie: TGF-β, IL-10 Interleuchina-1 (IL-1) è una citochina infiammatoria primaria viene liberata dall inflammosoma a partire da un precursore intracellulare. Partecipa a un complesso sistema di attivazione, che comprende recettori e molecole antagoniste. Agisce a livello del suo recettore specifico, che è IL-1R. Questo recettore funziona se è presente il corecettore ACP. 12
13 Il complesso costituito da IL-1R e ACP recluta la proteina intracellulare Myd88, si ha la cascata vista nei TLR che culmina nell attivazione di NFkB. Esistono IL-1α e IL-1β, esse possiedono funzioni simili. Il complesso di attivazione è regolato dal fatto che esiste un recettore Decoy, privo della porzione intracellulare (per splicing alternativo); Decoy è un recettore che antagonizza gli effetti di IL-1, infatti quando l interleuchina si lega ad esso non si ha trasduzione del segnale. Se il recettore Decoy è espresso sulla membrana, esso compete con IL-1R, limitando il messaggio attivato da IL-1. Quando la risposta infiammatoria termina, si osserva un aumento dell espressione del recettore Decoy. Il recettore Decoy può essere idrolizzato, si genera così una forma solubile che lega IL-1, la quale quindi non può interagire con IL-1R. Esiste una molecola antagonista di IL-1, IL-1ra (IL-1 Receptor Antagonist), che lega IL-1R con elevata affinità, spiazzando così IL-1 (funge da antagonista competitivo). Aumenta nel corso dello spegnimento della risposta infiammatoria. Gli effetti di IL-1 comprendono: A livello delle cellule infiammatorie: attivazione dei granulociti neutrofili Attivazione dei macrofagi, che producono NO, citochine, prostaglandine Sulla parete vascolare, determina ipotensione, sindrome di permeabilità capillare, espressione di molecole di adesione, produzione di prostaglandine, PAF Stimola la produzione di anticorpi da parte delle cellule B Stimola la produzione di linfochine da parte delle cellule T Nel fegato induce la produzione di proteine di fase acuta (attraverso la produzione di IL-6) Determina aumento del riassorbimento osseo Stimola il rilascio di amminoacidi dalle proteine muscolari Determina, a livello dei fibroblasti, proliferazione, aumento della sintesi di collageno e procollagenasi Agisce sul midollo emopoietico determinando neutrofilia e linfopenia Agisce sul sistema nervoso centrale, è responsabile dei sintomi legati alla febbre (astenia, perdita di appetito, sonnolenza) Il Tumor Necrosis Factor α (TNF-α) è essenzialmente una citochina pro infiammatoria primaria, largamente prodotta dalle cellule infiammatorie (granulociti, monociti, linfociti T attivati, NK e NKT), e dalle cellule parenchimali quando alterate da danni. Il livello ematico di TNF-α aumenta di diversi ordini di grandezza nel corso di infiammazione sistemica. Vi sono 2 pool di TNF-α: uno è immediatamente disponibile, ed è legato al rilascio di molecole di TNF-α poste sulla membrane delle cellule (mediato dall enzima TACE, una proteasi); l altro prevede la produzione di nuovo TNF-α. Il TNF-α agisce su due tipi di recettori: TNFRI (p55) e TNFRII (p65). Si tratta di recettori trimerici, che innescano la via di attivazione di NFkB. Il TNF-α ha un importante ruolo nelle vie di sopravvivenza cellulare. L eventuale risposta citotossica mediata da TNF-α deriva dalla somma di stimoli diversi. Gli effetti di TNF-α e IL-1 sono largamente sovrapponibili: Stimolano il rilascio di derivati lipidici Stimolano la sintesi di citochine, quindi la sopravvivenza cellulare Stimolano il rilascio di altre citochine e di chemochine Stimolano la migrazione dei leucociti Stimolano la liberazione di mediatori vasodilatatori Stimolano l immunità adattativa: attivano i linfociti Th1, il che costituisce un ulteriore stimolo alla produzione di TNF-α e IL-1 Stimolano il rilascio di IL-6 13
14 Interleuchina-6 (IL-6) è una citochina primaria, ma il suo compito è relativamente subordinato a TNF-α e IL-1. Essa ha un ruolo complesso, perché agisce sia favorendo la sopravvivenza sia stimolando la risposta di organi periferici, come il fegato. In particolare, IL-6: Agisce come fattore di crescita emopoietico e per la differenziazione megacariocitaria Stimola la proliferazione dei linfociti B Amplifica la stimolazione dell endotelio a produrre molecole adesive e chemochine Induce la produzione di proteine di fase acuta Induce la febbre. Il recettore per IL-6 è costituito da due componenti: IL-6Ra è il vero e proprio recettore Proteina adattatrice GP-130. La trasduzione del segnale porta all attivazione di JAK3, che fosforila Stat; il dimero Stat-Stat entra nel nucleo e attiva la trascrizione genica. Lo stesso recettore di IL-6, se tagliato, può comportarsi da recettore solubile, antagonizzando gli effetti di IL-6. Le citochine primarie partecipano alla produzione di quelle secondarie: i macrofagi stimolati da TNF-α e IFN-γ rilasciano IL-12, che attiva macrofagi e cellule endoteliali; i macrofagi stimolati da TNF e IL-1 rilasciano chemochine e fattori di crescita. Le chemochine (chemiotactic cytokine) sono una famiglia di circa 50 piccole proteine basiche (8-10 kda), dotate di attività chemiotattica e che condividono caratteristiche strutturali. In base alla posizione dei residui di cisteina, che formando ponti disolfuro determinano la struttura tridimensionale che interagisce con i diversi tipi di recettori, si distinguono 4 sottofamiglie di chemochine: Chemochine CXC: i due residui di cisteina sono intervallati da 1 amminoacido. es. IL-8, IP-10, SDF1, BCA-1. Chemochine CC: i due residui cisteinici sono adiacenti. es. MCP, MIP. Chemochine CX3C: vi sono 3 amminoacidi tra i due residui di cisteina. es. frattalchina. Chemochina C: linfotactina. Possiede solo uno dei residui di cisteina di riferimento. La caratteristica di tali molecole è legata al fatto che riconoscono gruppi di recettori simili: Il recettore per CXC è detto CXCR Il recettore per CC è detto CCR Il recettore per CX3C è detto CX3CR Spesso una citochina riconosce più recettori. La proprietà che caratterizza tutte le citochine è quella di indurre la motilità di diversi gruppi di cellule. A seconda del tipo cellulare interessato, le cellule presentano recettori diversi: Il neutrofilo esprime soprattutto CXCR1, CXCR4 Il linfocita T helper esprime, tra gli altri, CCR1, CXCR4, CCR2 Il linfocita B esprime CCR2, CCR6, CXCR5 Il linfocita T attivato esprime soprattutto CCR (2, 5, 6, 7, 10) La cellula dendritica esprime soprattutto CCR1, CCR4 14
15 Il monocita esprime CXCR4, CXCR1, CX3CR3, CCR2 Il macrofago esprime CCR5, CXCR4 I recettori per le chemochine sono dei GPCR. Si ha attivazione della via mediata da fosfolipasi C, DAG, IP3 e PKC. A valle, le chemochine determinano polimerizzazione dei filamenti di actina, adesione, riarrangiamento del citoscheletro, differenziazione e proliferazione, attivando così un macchinario per la motilità e quindi per il passaggio dei leucociti dal sangue all interstizio. I mediatori presenti nel plasma sono invece: Sistema delle chinine Sistema del complemento Sistema della coagulazione Sistema della fibrinolisi Il sistema delle chinine è legato all attivazione di cascate proteolitiche che liberano peptidi, soprattutto bradichinina e callidina, mediante taglio proteolitico del chininogeno ad alto peso molecolare (High Molecular Weight Kininogen). Le chinine inducono risposte vascolari quali aumento della permeabilità, attivazione delle cellule endoteliali, rilascio di istamina e citochine da parte delle cellule infiammatorie. Possiedono il duplice ruolo di invio di segnali di allarme e di attivazione dell infiammazione. Il sistema delle chinine è filogeneticamente antico e svolge un ruolo di supporto nei confronti degli altri sistemi. Esso ha un ruolo importante negli stimoli dolorifici, infatti le chinine sono recepite da terminazioni nocicettive del sistema nervoso periferico. Le chinine sono mediatori a breve vita, infatti vengono rapidamente inattivate per taglio proteolitico dalle carbossipeptidasi 1 e 2. Ruolo chiave nella produzione di chinine è assunto dalla proteasi callicreina, che si forma a partire dalla precallicreina per taglio proteolitico. Il fattor XII della coagulazione o fattore di Hageman taglia la precallicreina, attivandola a callicreina. Il fattor XII è suscettibile al contatto con superfici cariche negativamente, esso percepisce la variazione di carica elettrostatica sull endotelio. Il fattor XII si lega a superfici cariche negativamente e si attiva a fattor XIIa, che è una proteasi. Taglia molecole coinvolte nella cascata coagulativa (attiva il fattor XI) e agisce sulla precallicreina, dando callicreina. I due sistemi della coagulazione e delle chinine dialogano anche attraverso altri modi. La callicreina attiva il plasminogeno in plasmina, che degrada la fibrina. La plasmina è una proteasi aspecifica, essa inoltre attiva il C3 a C3b. Il sistema del complemento è un sistema a cascata molto più complesso di quello delle chinine; include oltre 20 componenti e costituisce un importante punto di interrelazione tra immunità innata e specifica. I soggetti con problemi a livello del sistema del complemento presentano deficit della risposta infiammatoria e gravi infezioni. Nel quadro dell infiammazione, questo sistema promuove il riconoscimento e la fagocitosi da parte delle cellule di microorganismi estranei o di costituenti cellulari. Esso è atto alla rimozione degli immunocomplessi e alcune molecole prodotte nel corso della cascata del complemento hanno ruolo di opsonine. Nella risposta infiammatoria, il complemento è importante per formare C3 e C5 convertasi. Questo perché C5 e C3 attivati hanno un ruolo nel favorire l attivazione delle cellule infiammatorie e la fagocitosi, infatti C3a e C5a sono anafilotossine. I segnali mediati da citochine inducono una aumentata espressione dei recettori C3aR e C5aR da parte di cellule endoteliali e fagociti; a loro 15
16 volta i segnali indotti dal legame delle anafilotossine ai recettori determina l incremento dell espressione di citochine e altri mediatori proinfiammatori, causando aumento della permeabilità, vasodilatazione e diapedesi dei leucociti. C3a, C4a e C5a sono attivatori aspecifici per mastcellule, piastrine, granulociti. Il complemento partecipa al processo infiammatorio mediante la produzione di peptidi come C3b, C4b, C3d, molecole che determinano attivazione dei granulociti neutrofili ed eosinofili e delle cellule dendritiche e NK. Le proteasi leucocitarie sono rilasciate negli spazi intercellulari, spesso in seguito a degranulazione. Esse creano il terreno operativo per le cellule infiammatorie. Il sistema delle proteasi comprende un gran numero di fattori, che si classificano in base al meccanismo catalitico: Serin-proteasi: elastasi, catepsina G, proteinasi 3, triptasi, attivatore del plasminogeno, chimasi, granzima A e B Metallo-proteasi: collagenasi interstiziale (MMP-1), collagenasi neutrofila (MMP-8), gelatinasi 72 kda (MMP-2), gelatinasi 92 kda (MMP-9), stromelisina 1-3 (MMP-3, -10, - 11), matrilisina (MMP-7), metalloelastasi (MMP-12) Cisteina-proteasi: catepsina S, catepsina L, catepsina B, catepsina H Aspartico-proteasi: catepsina D Principali azioni biologiche delle proteasi leucocitarie: Degradazione di molecole della matrice extracellulare Degradazione di proteine plasmatiche Conversione del plasminogeno in plasmina Attività antimicrobica Induzione della secrezione di citochine Degradazione di mediatori dell infiammazione Degradazione di recettori Attivazione leucocitaria e piastrinica Induzione della secrezione di muco Conversione e attivazione di proenzimi I mediatori dell infiammazione possiedono tre ruoli principali: Vasodilatazione: - Istamina, serotonina (secrete da mastociti e piastrine) - Prostaglandine (secrete da tutte le cellule) Vasopermeabilità immediata: - Istamina, serotonina (mastociti, piastrine) - Bradichinina (plasma) - LTC4, LTD4, LTE4 (leucociti, mastociti) - PAF (endotelio, piastirne, ecc.) - C3a, C4a, C5a (plasma) - Proteasi (neutrofili, cellule in necrosi) Vasopermeabilità ritardata: - Citochine (macrofagi, cellule NK) Chemiotassi: - LTB4, HETE (mastociti, leucociti) - C3a, C4a, C5a (plasma) 16
17 - PAF (endotelio, piastirne, ecc.) - Chemochine (macrofagi, neutrofili, ecc.) - Prodotti batterici Opsonizzazione: - C3b (plasma) - Proteine di fase acuta (plasma) - IgG, IgM (plasma) Danno cellulare: - Radicali liberi, ROS (leucociti attivati, macrofagi) - Enzimi leucocitari (leucociti attivati) - Enzimi lisosomiali (cellule necrotiche) - Enzimi batterici (batteri) Dolore: - Bradichinina (plasma) - Prostaglandine (tutte le cellule) Diapedesi leucocitaria Le cellule che partecipano alla migrazione leucocitaria hanno una capacità motoria intrinseca che permette loro di muoversi in una specifica direzione grazie a segnali chemiotattici. E possibile studiare la capacità migratoria delle cellule con la Camera di Boyden, costituita da due compartimenti separati da una membrana semipermeabile con pori; nella camera superiore si trova la sospensione cellulare, in quella inferiore si inocula la sostanza di cui si vuole valutare la capacità chemiotattica. Si valuta il numero di cellule che passano dalla camera superiore a quella inferiore. Si può quantizzare, con questo strumento, la capacità delle diverse sostanze di indurre chemiotassi. Tali sostanze sono: Peptidi batterici formilati PAF Leucotriene B4 C3a, C5a, C4a IL-1β, TNF-α Chemochine Il processo di migrazione leucocitaria è complesso. Tra i fattori che lo favoriscono si ha il rallentamento del flusso sanguigno che avviene in seguito a vasodilatazione e aumento della permeabilità vascolare. Nel normale flusso, i leucociti sono vicini alla parete endoteliale, ma non è permessa la loro adesione. Nel caso dell infiammazione (fase vascolare), la marginalizzazione è accentuata. Uscendo liquido dal plasma, gli eritrociti tendono a impilarsi formano i rouleaux e i leucociti si legano all endotelio attivato. Il meccanismo di diapedesi prevede anche l attivazione dell endotelio, che espone una serie di molecole di adesione e libera segnali che mediano l adesione leucocitaria. Ad esempio, se si espongono le cellule 17
18 endoteliali a IL-1, la quota di leucociti che si legano all endotelio aumenta. L adesione leucocitaria presenta diverse fasi: 1)I leucociti vanno incontro a una serie di contatti transitori con l endotelio che prendono il nome di tethering (titillamento). Questi contatti transitori permettono lo scambio di messaggi tra leucociti ed endotelio, grazie ai quali si ha attivazione dell endotelio stesso, che espone molecole di adesione; anche i leucociti esprimono nuove molecole di superficie. Importante è il rilascio di citochine e chemochine. 2)Si ha un progressivo rallentamento dei leucociti; il rotolamento di queste cellule sull endotelio determina la formazione di nuovi contatti e nuovi scambi. 3)Si arriva a un punto di arresto, in cui il leucocita ormai adeso all endotelio si ferma e stimola l endotelio a creare dei varchi tra le giunzioni cellula-cellula e anche attraverso le singole cellule. 4)Il leucocita si infila nei varchi neoformati (diapedesi vera e propria), arrivando così nell interstizio. Le molecole di adesione leucocitaria sono esposte sulla membrana delle cellule endoteliali e sono riconosciute da recettori posti su quella dei leucociti. Si possono suddividere in 2 categorie di proteine: Selectine: questo gruppo comprende E- selectina e P-selectina. Si legano a CD11 e CD18 e sono molecole altamente glicosilate. Vi è anche una L-selectina, sulla membrana leucocitaria. Superfamiglia delle immunoglobuline: comprende ICAM-1, ICAM-2 e VCAM-1. Esse sono riconosciute da integrine leucocitarie. Selectine, loro recettori e loro attività I glicani sialilati di tipo Lewis X sono espressi in grande quantità quando il leucocita è attivato. P- ed E-selectina sono responsabili del fenomeno di tethering. ICAM e VCAM sono molecole che necessitano di essere sintetizzate espressamente (via NFkB) e che determinano un ulteriore attivazione dell endotelio da parte delle citochine primarie. Sono responsabili della trasduzione di segnali intracellulari che permettono il dialogo tra leucociti ed endotelio. Si ha che: tutti i leucociti esprimono LFA-1 (Leukocyte Function Antigen-1) o CD11a/CD18; esso è un recettore per ICAM-1/-2 i monociti e i linfociti, inoltre, esprimono l integrina α4β1 o VLA-4, controrecettore per VCAM-1 i granulociti neutrofili e i monociti, inoltre, esprimono l integrina β2 on MAC-1 o CD11b/CD18, che può legare ICAM-1 La diversa cronologia di espressione è legata al diverso ruolo delle molecole di adesione nel regolare la diapedesi. Ruolo delle piastrine nel processo di diapedesi leucocitaria L esposizione di segnali di allarme sull endotelio (endothelial distress) costituisce un meccanismo di attivazione piastrinica. L esposizione di P-selectina e di fattore di Von Willebrand (vwf) favorisce l attivazione delle piastrine. Il legame tra piastrine e leucocita risulta essere addirittura più 18
19 potente di quello tra piastrina ed endotelio. Le piastrine rilasciano importanti molecole-segnale, come il fattore tissutale, e favoriscono il rilascio di citochine e chinine. Gli stimoli alla migrazione leucocitaria nei siti infiammatori: Esiste un modello di indirizzo dei leucociti. L attivazione cellulare nella formazione dell essudato infiammatorio avviene secondo una sequenza temporale ben precisa: Le cellule interagiscono tra loro in modo complesso, con comportamenti diversi. I neutrofili sono i primi a essere coinvolti (attirati da P-selectina, ICAM-1); quando sono attivati e si trovano nell interstizio rilasciano il contenuto dei granuli, tra cui figurano ROS, citochine proinfiammatorie; hanno attività citotossica e fagocitaria nei confronti di patogeni e materiale cellulare. I granulociti neutrofili rilasciano fattore LL37 e catepsina G, che sono responsabili del mantenimento della condizione di attivazione endoteliale e del richiamo di monociti nell interstizio. Nell evoluzione del processo infiammatorio si ha poi la fase in cui si attirano in modo crescente i monociti, che presentano caratteristiche e attività funzionali duttili e articolate. I macrofagi possono sopravvivere a lungo; i monociti possono differenziare ad altri tipi cellulari, ad esempio a cellule dendritiche. Ci sono due tipologie di attivazione dei monociti, con caratteristiche funzionali opposte: in relazione a stimoli proinfiammatori i monociti si attivano in senso M1: la loro attività consiste nel rilascio di ROS, NO, IL-1, IL-6, IL-12, IL-23; essi distruggono cellule (sono citotossici). La risposta di tipo M1 è stimolata da TNF e IFN-γ (rilasciato dai linfociti Th1) e da segnali di allarme (PAMPs, LPS). la risposta in senso M2 è ritenuta essere quella che caratterizza i macrofagi quando essi collaborano alla riparazione tissutale e al rimodellamento della matrice extracellulare (per il rilascio, tra le altre cose, di TGF-β). IL-4 e IL-13 (rilasciate dai linfociti Th2), IL-10, CSF-1 e immunocomplessi+il-1/lps stimolano la risposta M2. Si osserva poca produzione di NO e di citochine infiammatorie; si ha aumento del rilascio di recettore Decoy, che antagonizza gli effetti di IL-1. Le cellule macrofagiche M2 possiedono capacità fagocitarie e di APC (presentazione dell antigene). Esse inoltre permettono di uccidere o di circoscrivere parassiti pluricellulari; sono coinvolte nelle manifestazioni allergiche. La polarizzazione dei macrofagi in un senso piuttosto che nell altro è il risultato di stimoli ambientali diversi; alcune risposte, inoltre, hanno carattere sia M1 sia M2. 19
20 Fagocitosi I fagociti inglobano microrganismi, cellule e detriti cellulari e li degradano nell apparato lisosomiale. La fagocitosi inoltre è importante per la presentazione dell antigene. È un processo in cui sono coinvolti numerosi segnali. Per inglobare, il fagocita emette estrusioni coperte da membrana, avvolgendo così il materiale da fagocitare. Questo processo è stimolato da segnali innescati dal contatto fagocita-materiale. Si forma quindi un vacuolo di fagocitosi, in cui i granuli riversano il loro contenuto (proteasi, idrolasi, molecole antibatteriche). Il fagocita può inglobare più bersagli contemporaneamente. Inizialmente, si ha il riconoscimento da parte della membrana del fagocita di potenziali bersagli. Ciò è mediato da PRR e recettori scavenger; il meccanismo è potenziato dall interazione di proteine solubili che svolgano la funzione di opsonizzazione o buttering ( rendere più appetibile ); tali proteine possono essere immunoglobuline (IgG, soprattutto), molecole del complemento (C3b, C5b) che rimangono adese alla superficie su cui si sono formate, oppure opsonine non specifiche. La fagocitosi può avvenire anche senza opsonizzazione. I fagociti possiedono sulla membrana numerosi recettori ad alta affinità. Le risposte intracellulari comportano la migrazione dei granuli e la degranulazione. Si attivano proteine G legate al recettore per l opsonina, si attiva PLC, si ha liberazione di DAG e IP3, con attivazione di PKC che fosforila numerosi substrati; l aumento del calcio intracellulare determina modificazione del citoscheletro, degranulazione, fusione dei granuli primari e secondari e dei lisosomi con il fagosoma. Passano così enzimi: proteasi, proteine cationiche, lattoferrina, idrolasi, lisozima, ecc. I segnali attivati dall aumento del calcio intracellulare e dall attività di PKC regolano il burst ossidativo dei fagociti i quali, se stimolati, vanno incontro ad aumento del consumo di ossigeno non associato ad aumento dell attività metabolica, ma correlato alla formazione di complessi multiproteici associati alla membrana del fagosoma: si tratta dell enzima NADPH ossidasi. Si usa NADPH grazie all azione di una flavoproteina che trasferisce elettroni all ossigeno. L enzima NADPH ossidasi è una macchina molecolare che genera anione superossido O2 -, che viene riversato nel fagosoma. Il sistema serve a produrre quantità massicce di anione superossido. Si deve usare molto ossigeno, è richiesto aumento del flusso ematico; il NADPH è generato dalla via del pentoso fosfato. Il significato funzionale alla base dell attività della NADPH ossidasi 20
21 risiede nel fatto che l anione superossido viene convertito, all interno del fagosoma, in H2O2, che a sua volta è substrato dell enzima mieloperossidasi (MPO), che catalizza una reazione di alogenazione: l alogeno è soprattutto cloro e lo ione ipoclorito che si forma determina danni nei microrganismi con cui entra in contatto. Nel corso dell attivazione dei macrofagi ci possono essere dei problemi, che sfociano in alterazioni della fagocitosi. L attivazione può avvenire prima che il vacuolo si sia chiuso, si ha quindi il fenomeno del rigurgito durante il pasto: si formano numerosi vacuoli e si ha rilascio del contenuto dei granuli, soprattutto enzimi. Nella cosiddetta fagocitosi frustrata, invece, il bersaglio da fagocitare è troppo grande, si hanno più fagociti con più vacuoli ma ciò non è sufficiente, perciò il contenuto dei granuli fuoriesce negli spazi intercellulari; questo fenomeno accade spesso. In alcune condizioni, dove predominano bersagli indigeriti o ci sono difetti nel meccanismo stesso, l attivazione dei fagociti può determinare danno tissutale, per azione soprattutto di ROS ed enzimi litici. Questo è ben visibile in casi di infiammazione cronica. In alcune condizioni, alla base delle alterazioni della fagocitosi vi sono dei difetti genetici, e la capacità di eliminare uno o più batteri risulta compromessa. Ad esempio, nella CGD (Chronic Granulomatous Disease, malattia granulomatosa cronica), alla base della quale vi è una mutazione a carico di NADPH ossidasi, il complesso è meno attivo o addirittura inattivo, perciò la generazione di ROS è deficitaria e il soggetto affetto da CGD risulta essere incapace di uccidere microrganismi catalasi positivi (si producono piccole quantità di H2O2, che viene rapidamente degradata, per cui la MPO non forma ione ipoclorito). Aumenta il rischio di infezione da S. aureus. Nella deficienza di adesione leucocitaria (LAD) di tipo 1 e di tipo 2, si hanno problemi a livello di CD18 nel primo caso e nella fucosilazione dei carboidrati nel secondo; il risultato è una maggior predisposizione a infezioni causate da batteri gram negativi, S. aureus e altri, a causa di difetti nel reclutamento dei leucociti tali per cui i fagociti non riescono a migrare nell interstizio. La LAD1, ad esempio, è caratterizzata da estrema neutrofilia con assenza di essudato purulento. 21
22 Terminazione dell infiammazione L infiammazione è un processo che si deve spegnere poiché un meccanismo che sia potenzialmente in grado di innesca il processo infiammatorio può anche determinare un profondo danno tissutale. Nella terminazione del processo infiammatorio è importante il fenomeno dell efferocitosi, in cui i macrofagi eliminano i corpi apoptotici. L apoptosi dei polimorfonucleati (PMN) porta alla loro progressiva diminuzione durante il processo infiammatorio e costituisce un segnale per la risposta dei macrofagi, che riconoscono i segnali find me and eat me ed eliminano così i corpi apoptotici. Si osserva che il numero dei macrofagi aumenta alla fine del processo infiammatorio. I corpi apoptotici sono riconosciuti da un set di recettori, essi infatti esprimono molecole di fosfatidilserina, cui si legano fattori extracellulari come β2-gpi e GAS-6, che hanno i loro recettori sui macrofagi. Si ha una variazione nell assetto funzionale del macrofago, diminuiscono i segnali che determinano rilascio di citochine proinfiammatorie, a favore di una riprogrammazione del macrofago, che rilascia citochine con attività antinfiammatoria: IL-10 è la tipica citochina antinfiammatoria. Si liberano anche altri mediatori, capaci di determinare la terminazione del processo infiammatorio. La fagocitosi dei corpi apoptotici serve anche perché quando i granulociti vanno incontro ad apoptosi vengono espressi recettori come CCR5, che costituisce una trappola per chemochine proinfiammatorie (CCL3, CCL5), che attraggono i granulociti neutrofili. Si eliminano dall ambiente circostante anche altre chemochine proinfiammatorie: i macrofagi rilasciano MMP-12, che agisce su chemochine come CXCL8 e CXCL3, inattivandole; MMP-2 modifica CXCL7, si formano dei peptidi che bloccano le chemochine (per legame con i recettori CCR1-3). Si ha così una progressiva eliminazione di fagociti, parallelamente a una riprogrammazione dei macrofagi in senso antinfiammatorio (M2) e a una diminuzione del livello di chemochine. Forse si ha anche il reclutamento di un ulteriore popolazione di monociti, osservazioni nel miocardio hanno dimostrato che il rilascio di CX3CL1 determina il richiamo di una popolazione di monociti CD14 - /CD16 +, si tratta di macrofagi con aumentata capacità di eliminazione di corpi apoptotici e aumentata tendenza a determinare la fine dell infiammazione e la guarigione del tessuto. Nello spegnimento della risposta infiammatoria sono coinvolti alcuni mediatori lipidici, che derivano da acido arachidonico (AA), acido docosanesanoico (DHA, C22:6) e acido eicosapentenoico (HPA, C20:5); questi ultimi due appartengono alla categoria degli acidi ω-3. Dall acido arachidonico derivano le lipossine. I neutrofili attivati producono LTB4 a partire da LTA4, che deriva dall azione della 5- lipossigenasi (5-LOX) sull acido arachidonico (AA). Dato che i neutrofili non possiedono attività LTC4-sintetasica, essi passano LTB4 alle piastrine, che invece la possiedono; esse, inoltre, possono produrre 22
23 lipossina-a a partire da LTB4 dei neutrofili, grazie all azione della 12-LOX. Le 15-epilipossine, -A e -B, derivano dall acido arachidonico per azione della COX-2. L acido acetilsalicilico, principio attivo dell Aspirina, determina acetilazione di COX-2, che diventa così una 15-lipossigenasi, che addiziona ossigeno all acido arachidonico generando derivati ossigenati, che sono alla base delle epilipossine; si possono così generare mediatori antinfiammatori. In particolare, le epilipossine: determinano diminuzione dei segnali dolorifici, del rilascio e dell attività delle citochine, dell adesione all endotelio e della migrazione dei polimorfonucleati promuovono l attività antifibrotica e l eliminazione dei corpi apoptotici dei PMN da parte dei macrofagi I mediatori lipidici importanti nello spegnimento dell infiammazione, oltre a lipossine ed epilipossine, sono le resolvine (D ed E), le protectine e le maresine (maresina: macrophage mediator in resolvin inflammation). La lipossina A agisce sui recettori AXL (FPR1), blocca la migrazione dei granulociti e favorisce quella dei monociti, diminuisce l adesione dei neutrofili, la formazione di ROS, l attività di NFkB e il rilascio di CXCL8. Le resolvine interagiscono con i recettori ChemR23, riducendo l attività di NFkB nei macrofagi; competono con il legame di LTB4 a BTL1 dei neutrofili, inibendone l attività chemiotattica. Queste molecole inducono l espressione di CCR5. Determinano inoltre, a livello delle cellule dendritiche, una diminuzione della produzione di IL-12. Protectine e resolvine sono sintetizzate da macrofagi stimolati a mutare il loro pattern differenziativo. Alla terminazione del processo infiammatorio partecipano numerose altre molecole. L adenosina, che lega i recettori A2, determina aumento della sintesi di IL-10, stimola la fine dell attività funzionale dei macrofagi, dà riduzione del rilascio di citochine proinfiammatorie, blocca il rilascio di IL-12 da parte delle cellule dendritiche. L infiammazione ha ripercussioni a livello del sistema nervoso centrale: per afferenze dovute alla stimolazione di recettori dolorifici (anche verso l ipotalamo), per azione sull ipotalamo di citochine proinfiammatorie (IL-1 e TNF-α, che determinano il quadro della febbre). A causa dell attivazione dell ipotalamo si ha rilascio di CRH, che agisce sull adenoipofisi, che produce ACTH, che agisce sulla ghiandola surrenale, che libera cortisolo. Il cortisolo ha effetti importanti sulla modulazione della risposta infiammatoria: a livello periferico, agisce sulle cellule infiammatorie (e dell immunità 23
24 adattativa), l interazione tra cortisolo e recettore intracellulare dà il complesso HR, che si attiva rilasciando HSP ed entrando nel nucleo, dove si lega a sequenze di DNA responsive e modula la sintesi proteica, ad esempio di lipocortina, annessina A1, fosfatasi di MAPK: Lipocortina e annessina A1 bloccano la risposta infiammatoria perché a livello intracellulare inibiscono l enzima fosfolipasi A2 (PLA2), perciò non si libera acido arachidonico La fosfatasi di MAPK è responsabile del blocco di chinasi come JNK e p38mapk, che sono ingaggiate da TLR e IL-1R. Il complesso HR interferisce con NFkB, sopprimendone l attività. Annessina A1 rappresenta un segnale diffusibile, capace di bloccare la trasmigrazione leucocitaria e l attivazione delle mastcellule e di aumentare la fagocitosi di corpi apoptotici. L incapacità di risolvere l infiammazione acuta è responsabile delle sviluppo di fenomeni infiammatori cronici. Infiammazione cronica L infiammazione cronica deriva da un prolungamento di un infiammazione acuta che non è riuscita a eliminare l agente flogogeno; si instaura quindi in presenza di agenti flogogeni non eliminabili facilmente (es. tubercolosi, corpi estranei, autoimmunità). L infiammazione cronica è in genere definibile come istoflogosi, nel senso che presenta una spiccata componente tessutale, a differenza dell infiammazione acuta o angioflogosi, in cui prevale la componente endoteliale. Nell infiammazione cronica viene meno il coinvolgimento vascolare e predomina l infiltrato parvicellulare, costituito soprattutto da linfociti e monociti, con pochi polimorfonucleati. Si osservano spesso alterazione e danno parenchimale, talvolta in associazione con meccanismi di riparazione tissutale. Nella polmonite cronica, ad esempio, si osservano tessuto fibroso, danno alveolare, ispessimento dei setti interalveolari residui; altri esempi di infiammazione cronica associata a patologie sono l aterosclerosi, l obesità, l artrite reumatoide, la bronchite cronica, ecc. Le caratteristiche principali dei processi infiammatori cronici sono: Formazione dell infiltrato Distruzione dei tessuti Attivazione dei meccanismi di riparazione Le cellule dell infiammazione cronica sono: macrofagi, linfociti, cellule predisposte alla riparazione tissutale (fibroblasti). I macrofagi sono cellule di derivazione monocitaria in grado di moltiplicarsi e di differenziarsi. Le funzioni dei macrofagi sono: la fagocitosi, la stimolazione dei fibroblasti attraverso il rilascio di specifiche citochine, l amplificazione del processo di chemiotassi mediante alcuni mediatori (ad esempio CCL2) e l interazione con i linfociti in qualità di cellule presentanti l antigene (APC). I monociti-macrofagi sono estremamente versatili e producono un gran numero di molecole: Molecole ad attività antibatterica: - Idrolasi acide - Fosfatasi - Lisozima - Catepsina G - Defensine 24
25 - ROS - NO Fattori della coagulazione: - Attivatore del plasminogeno - Fattor III - Fattor V - Fattor VIII Fattori del complemento: - Fattore B - C3 - Properdina Mediatori proinfiammatori: - IL-1 - IL-6 - TNF-α - IL-12 - IFN-β Mediatori antinfiammatori: - IL-10 - TGF-β - Prostaglandina E2 Agenti chemiotattici: - PAF - Chemochine (CCL2, CCL3, CCL5, CXCL8) Fattori di crescita midollari: - M-CSF - GM-CSF Fattori angiogenetici: - PDGF - EGF - FGF - VEGFs Enzimi attivi sulla matrice extracellulare: - Elastasi - Metalloproteasi Nelle infiammazioni croniche convivono vari processi: Attivazione dell infiammazione e distruzione cellulare: si hanno macrofagi M1 Riparazione dei tessuti e deposizione di matrice extracellulare: vi sono macrofagi M2 Non è ancora chiaro come i due tipi di risposta convivano: o esistono due popolazioni di macrofagi diverse, oppure esistono fenotipi macrofagici che hanno entrambe le caratteristiche. I linfociti T sono distinguibili in CD4 + (T helper) e CD8 + (citotossici). Tra i linfociti Th CD4 + distinguiamo: Linfociti Th1: secernono IFN-γ, TNF-α, IL-1; attivano in senso M1 i macrofagi Linfociti Th17: producono IL-17, IL-22; sostengono risposte di tipo proinfiammatorio nei macrofagi Linfociti Th2: producono IL-4, IL-5, IL-13; determinano polarizzazione dei macrofagi in senso M2 Linfociti Tregolatori: producono IL-10, che tende a spegnere l infiammazione. In malattie autoimmuni e nell aterosclerosi, la presentazione dell antigene a linfociti Th1 determina aumento della stimolazione dei macrofagi, che a loro volta attivano i linfociti, per cui il processo si perpetua. 25
26 In presenza di parassiti e reazioni allergiche, la secrezione di IL-4, IL-5 e IL-13 caratterizza il fenotipo dei linfociti Th2; ciò permette di segregare il microrganismo. La differenziazione a Th1 o Th2 dipende dallo stimolo, che è la presentazione dell antigene, e da citochine, e condizione la differenziazione dei macrofagi. Nell infiammazione cronica aumentano i linfociti Th1 e Th17, mentre diminuiscono i Treg e talvolta i Th2. Ruolo del linfocita Th1 nell infiammazione cronica: Nelle infiammazioni croniche i macrofagi possono assumere aspetti particolari e caratteristici: Cellule epitelioidi, di forma allungata(20-40 μm di diametro), hanno un ciclo vitale della durata di 1-4 settimane. Sono in grado di differenziarsi ed eventualmente di sdifferenziarsi. La membrana plasmatica appare ricca di estroflessioni che, intersecandosi con quelle delle cellule adiacenti, conferiscono un aspetto a palizzata. Le cellule epitelioidi hanno scarsa attività fagocitaria, mentre sembrano essere orientate verso la secrezione in particolare di fattori di crescita utili per la differenziazione delle cellule macrofagiche. Cellule giganti multinucleate( μm di diametro) si distinguono in due tipi a seconda della disposizione dei nuclei: - Cellule di Langhans: qui i nuclei sono disposti a ferro di cavallo in periferia - Cellule da corpo estraneo: i nuclei, nel citoplasma, sono in posizione centrale o casuale. Le cellule multinucleate possono originare per divisione del nucleo senza divisione cellulare o per fusione di elementi macrofagici indotta dal MMF (Macrophage Forming Factor). Il ruolo delle cellule multinucleate non è ben noto, infatti esse hanno una scarsa attività fagocitaria e non sembrano neppure essere delle cellule orientate verso la secrezione. Tratto caratteristico dell infiammazione cronica è la distruzione tissutale, che è provocata da macrofagi (soprattutto se attivati e polarizzati in collaborazione con linfociti T) e dagli effetti dell agente lesivo. Si osserva un quadro di necrosi caseosa, che comporta perdita della struttura del tessuto (ad esempio nel granuloma ghiandolare). In risposta alla distruzione del tessuto si innesca un processo di riparazione, che si protrae nel tempo dando luogo ad aumento della deposizione di collagene e della formazione di tessuto fibroso; ciò avviene anche per effetto di specifiche citochine. Come risultato, calano la cellularità e la vascolarizzazione. La fibrosi, esito comune di molti processi infiammatori cronici, può avere gravi conseguenze anatomo-funzionali. I fibroblasti sono gli elementi cellulari responsabili della reazione fibrotica che generalmente si associa e conclude il processo infiammatorio cronico. Si possono riconoscere almeno 3 tipi di fibroblasti, che sembrano rappresentare la stessa cellula ma in momenti differenti: I fibroblasti attivi sono cellule di forma allungata e nucleo ovalare con reticolo endoplasmatico rugoso e apparato di Golgi ben sviluppati e numerose vescicole di secrezione I fibroblasti quiescenti o fibrociti hanno un nucleo più denso e organuli scarsamente sviluppati I fibroblasti contrattili o miofibroblasti presentano dense zone di adesione cellulare tipo desmosomi, fibrille ben sviluppate e membrana nucleare frastagliata. La liberazione di citochine pro-fibrogenetiche come TGF-β da parte dei macrofagi stimola l attivazione dei miofibroblasti. 26
27 Dal punto di vista istopatologico si hanno essenzialmente due tipi di istoflogosi: Interstiziale: il processo infiammatorio è diffuso Granulomatosa: è una risposta infiammatoria focale e ben delimitata, caratterizzata dall accumulo e dalla proliferazione di leucociti mononucleati associati o meno a linfociti. Il granuloma è una forma di infiltrato infiammatorio cronico organizzato caratteristicamente in una forma rotondeggiante. Le reazioni granulomatose sono distinte in: Granulomi da ipersensibilità: dovuti a noxae con attività antigenica che inducono una reazione di ipersensibilità di tipo IV Granulomi da corpo estraneo: la noxa in questo caso non attiva nessuna risposta immunitaria, ma rimane all interno del fagocita, distruggendolo o attivando il rilascio dei granuli. Il materiale estraneo non eliminabile dal macrofago (ad es. schegge, cristalli, asbesto), quindi viene segregato nel granuloma. La risposta prevede alcune fasi: 1) Accumulo di macrofagi attivati in senso M1, che circondano il corpo estraneo 2) I macrofagi spengono l attività infiammatoria e circoscrivono il corpo estraneo, spesso fondendosi in cellule giganti, segregando il corpo estraneo attraverso la stimolazione di una risposta fibrogenetica. Esempi di granulomi da corpo estraneo: il primo è in risposta a un filo di sutura, il secondo è dovuto a silicosi polmonare. Si notano l intensa attività fibrotica e l assenza di risposta infiammatoria. Nel granuloma infiammatorio, lo stimolo che ha provocato l attivazione della risposta infiammatoria resta antigenicamente attivo e si ha reazione linfocitaria (generalmente mediata da linfociti CD4 + ). Nel caso del granuloma tubercolare si osservano le tipiche caratteristiche della risposta infiammatoria cronica. Si osserva un ampia area di necrosi caseosa o coagulativa, a causa anche del danno ipossico; la zona necrotica è circondata da uno strato di cellule macrofagiche epitelioidi (che spesso contengono il micobatterio). Talvolta i micobatteri non possono essere eliminati e possono proliferare all interno dei macrofagi. Se la risposta CD4 e CD8 non rende competenti i macrofagi e i linfociti CD8 + non eliminano i micobatteri si ha espansione dell area di necrosi, con la convergenza dei granulomi, che formano la cosiddetta caverna tubercolare: si osservano cellule giganti (nella figura, di tipo Langhans) circondate da cellule epitelioidi, e all esterno i linfociti. La Coccidosi polmonare è un tipico granuloma, che presenta spesso due sferule di C.Immitis fagocitate da una cellula gigante tipo Langhans. 27
28 RISPOSTE SISTEMICHE ALL INFIAMMAZIONE Il processo infiammatorio è volto a distruggere, diluire, rimuovere o almeno circoscrivere l agente lesivo. Per fare ciò, mobilita le difese dell organismo e attiva i meccanismi di riparazione; è una risposta difensiva, ma può anche causare danni nei tessuti interessati. Inoltre, è una risposta locale, ma può produrre effetti sistemici, che sono: Leucocitosi Risposta di fase acuta Effetti metabolici Febbre Leucocitosi La leucocitosi è tipica in corso di processi infiammatori. È caratterizzata da cambiamenti quantitativi e qualitativi. Normalmente, i leucociti sono presenti in numero di per mm 3 ; in caso di leucocitosi si arriva a leucociti/mm 3. Il meccanismo dipende da una mobilitazione del pool marginato e del pool di riserva midollare. Le citochine coinvolte sono GM-CSF, G-CSF, M-CSF, Multi- CSF (IL-3). Meno comunemente si verifica una leucopenia (ad es. in febbre tifoide, brucellosi, tubercolosi), riconducibile a effetti di metaboliti batterici sul pool proliferante. Per quanto concerne i cambiamenti qualitativi, il più comune è la neutrofilia (aumento dei neutrofili)che possono arrivare a costituire il 90% dei leucociti circolanti. Meno comunemente si riscontrano linfocitosi (i linfociti superano il 20-30%), monocitosi (aumento dei monociti, senza leucocitosi) o eosinofilia. Le citochine coinvolte (GM-CSF, M-CSF, IL-5) hanno effetti tipospecifici. Il fenomeno della leucocitosi, nei suoi aspetti, è legato al fatto che, in risposta a stimoli infiammatori, vengono reclutate le riserve presenti nei tessuti: una quota importante è marginalizzata nei vasi polmonari e viene immessa in circolo; i monociti presenti a livello splenico possono essere liberati nel giro di pochi minuti. Risposta di fase acuta La risposta di fase acuta consiste in una modificazione della composizione delle proteine plasmatiche caratterizzata dall aumento di certe proteine a scapito di altre, in seguito a riprogrammazione della sintesi proteica, in particolare a livello epatico; le proteine che caratterizzano la reazione di fase acuta sono funzionali all infiammazione. In molti casi gli aumenti dei livelli delle proteine in questione sono marcati, e possono fungere da marcatori diagnostici. Le citochine infiammatorie primarie (IL-1, TNF-α, IL-6) modulano la sintesi epatica di proteine di fase acuta, che migliorano l efficienza dei meccanismi dell infiammazione e, in particolare, della fagocitosi. Le proteine di fase acuta comprendono: Proteine la cui concentrazione aumenta del 50%: - Ceruloplasmina: lega il rame, ha attività antiossidante 28
29 - Proteine del complemento (C1q, C3, C4): coinvolte in fagocitosi, modulazione della chemiotassi leucocitaria, legame delle cellule apoptotiche - Fibronectina: per la riparazione tissutale - Componente P sierica dell amiloide (SAP) Proteine la cui concentrazione aumenta da 2 a 4 volte: - Glicoproteina α1 acida - α1-antitripsina: inibisce le proteasi - α1-antichimotripsina - Fibrinogeno - Aptoglobina: legata al trasporto dell emoglobina - Proteina legante il mannosio (MBP): atta al riconoscimento di agenti infettivi e cellule apoptotiche - Proteina legante il C4 (C4BP) Proteine la cui concentrazione aumenta di alcune centinaia di volte e anche più di mille volte: - Proteina C reattiva (CRP): atta al riconoscimento di agenti infettivi e di cellule apoptotiche - Siero amiloide A (SAA): per il riconoscimento di cellule alterate e cellule apoptotiche Proteine la cui concentrazione diminuisce: - Albumina - Transferrina - Apo AI - Apo AII - Alfafetoproteina - Glicoproteina α2 HS Effetti metabolici Numerosi sono gli aspetti metabolici associati alle reazioni di fase acuta e, in generale, al processo infiammatorio. L infiammazione, infatti, è un processo dispendioso dal punto di vista energetico. Si verifica una rielaborazione dell assetto metabolico, che permette all organismo di fornire energia nelle reazioni coinvolte nell infiammazione: Aumentano i livelli plasmatici di ormoni: glucagone, insulina, ACTH, cortisolo, catecolamine, GH, tiroxina, aldosterone, vasopressina Aumenta il catabolismo proteico, ciò comporta debolezza muscolare per perdita della massa magra con conseguente astenia Aumento della gluconeogenesi Alterazioni del metabolismo lipidico: aumento di VLDL e trigliceridi, calo di HDL Resistenza all insulina, che è un ormone che aumenta nel corso dell infiammazione. Questo evento dipende da modificazioni a livello intracellulare, poiché sebbene i recettori siano funzionanti e la quantità di insulina sia normale/alta, la trasduzione del segnale è ridotta a causa dell azione di mediatori proinfiammatori (IL-6, IL-1, TNFα), i quali promuovono la fosforilazione in 29
30 serina di IRS-1 e IRS-2, che normalmente funzionano se fosforilate in tirosina e quindi ora sono incapaci di svolgere il normale compito di proteine adattatrici; TNF-α e IL-6, inoltre, stimolano l attivazione di JNK e IKB, che sono attivate anche da stress del reticolo e da ROS e inibiscono IRS. SOCS1 e SOCS3, attivate da IL-6, ubiquitinano, inibendo, IRS. Aumento della sintesi di proteine di fase acuta Variazioni nella distribuzione ionica: ad esempio diminuisce il livello di ferro disponibile, per calo della sintesi di ferrtina (questo è un meccanismo batteriostatico Patogenesi della sindrome infiammatoria sistemica (SIRS) e dello shock settico Patogenesi dell ARDS (Adult Respiratory Distress Syndrome) L ARDS è una patologia caratterizzata da diffusa lesione a livello dell epitelio respiratorio, con edema alveolare diffuso, per elevati livelli circolanti di TNFα. I granulociti passano negli alveoli e si attivano, ciò compromette l attività respiratoria per calo degli scambi alveolari dei gas. Febbre La febbre consiste in un aumento della temperatura corporea per modificazione della regolazione dei centri termoregolatori ipotalamici. È una delle manifestazioni più comuni del processo infiammatorio e in genere dei processi che prevedono aumenti dei livelli di citochine (infezioni, neoplasie). 30
31 Gli stimoli che determinano variazioni nel settaggio dei centri ipotalamici dipendono dall attività di citochine primarie (IL-1) sulle cellule endoteliali che circondano i centri stessi, si produce PGE2 che attraversa la barriera ematoencefalica e attiva i nuclei paraventricolare e dell area preottica. Per questo motivo gli inibitori di COX sono antipiretici. Fisiopatologia della febbre Per quanto riguarda il processo di termogenesi chimica, esso risulta essere legato all attività degli ormoni tiroidei e delle catecolamine, che, nel tessuto adiposo bruno, determinano aumento della sintesi di UCP, proteina che determina il disaccoppiamento della produzione di ATP dalla respirazione cellulare a livello mitocondriale, aumenta il consumo di ossigeno e l energia viene dispersa sotto forma di calore; nel muscolo scheletrico si verificano contrazioni involontarie e inefficaci, si ha il brivido. Il pallore tipico dello stato febbrile consegue alla vasocostrizione periferica, che garantisce una minor termodispersione. Evoluzione del processo febbrile L evoluzione del processo febbrile avviene in 3 fasi: Ascesa o effervescenza: caratterizzata da aumento della temperatura, brivido Equilibrio o fastigio: il centro termoregolatore è settato a una temperatura alta, che si mantiene costante; assenza di brivido e pallore, ma si modifica l assetto metabolico Discesa o defervescenza: caratterizzata, tra le altre cose, da sudorazione profusa, termodispersione, vasodilatazione A seconda dell innzalzamento termico, distinguiamo: Febbre bassa o febbricola: innalzamento di 1 C rispetto alla norma Febbre media: aumento di 1-2 C rispetto alla norma Febbre alta: innalzamento di 2-3 C rispetto alla norma Febbre altissima o iperpiressia: temperatura superiore a 41,5 C È importante considerare l andamento della curva termica, in particolare per formulare una diagnosi. 31
32 L andamento riflette i periodi di crescita del plasmodio all interno degli eritrociti: ogni accesso febbrile corrisponde alla lisi dei globuli rossi, con passaggio del plasmodio in circolo Ci sono febbri periodiche ereditarie, dovute ad alterazioni nella risposta alle citochine. Esse presentano curve termiche particolari, con aumenti transitori che si hanno in certi periodi dell anno. La febbre presenta delle condizioni favorevoli e sfavorevoli. Quelle favorevoli sono: A temperature elevate è minore la proliferazione e la virulenza di numerse specie batteriche e virali patogene, poiché la febbre permette aumento dell efficacia di IFN Le temperature elevate favoriscono la funzionalità delle difese immunitarie dell ospite (aumento dell attività fagocitica e battericida dei neutrofili e citotossica dei linfociti) Quelle a sfavore, invece: Alterazioni del ricambio idroelettrolitico (disidratazione e acidosi metabolica) Alterazioni del metabolismo energetico (elevato consumo calorico associato a scarca introduzione di alimenti: depauperamento delle scorte di glicogeno, dimagrimento, aumentato catabolismo delle proteine muscolari fino all atrofia muscolare) Aumento frequenza cardiaca e respiratoria Disturbi neurologici (sonnolenza e in caso di temperature molto elevate convulsioni e delirio) 32
33 LA FIBROSI La fibrosi o sclerosi è una condizione caratterizzata dall aumento di tessuto connettivale stromale, in particolare di collagene di tipo I, all interno di organi parenchimatosi. Nei Paesi Occidentali questa patologia è molto rilevante, poiché costituisce circa il 45% di causa di morte. Diversi sono gli esempi di patologie fibrotiche: malattie interstiziali polmonari cirrosi epatica e fibrosi pancreatica aterosclerosi morbo di Crohn ed insufficienze intestinali croniche insufficienza cardiaca nefropatia diabetica sclerodermia degenerazione maculare della retina La fibrosi risulta essere strettamente correlata ai processi di riparazione; in particolare, si determina inattivazione impropria del processo riparativo, che procede autonomamente, senza controllo o inibizione; è lecito pensare quindi, come questi processi subiscano modificazione. Le malattie fibrosanti o sclerosanti croniche sono caratterizzate da un alterazione dell equilibrio fra la riparazione del danno e lo sviluppo della fibrosi. L evoluzione fibrotica è determinata da fattori che portano il sistema a deviare dal suo normale percorso; uno di questi fattori è l infiammazione cronica, che determina attivazione dei fibroblasti, stimolazione dell angiogenesi e sbilanciata attivazione delle metalloproteasi. Numero sono le ipotesi avanzate riguardo alla contemporanea esistenza delle attività riparatorie e fibrotiche; una di queste è relativo alla possibilità che esistano caratteristiche di differenziazione macrofagica intermedie. La cirrosi epatica Per quanto concerne il fegato, la cirrosi epatica è sinonimo di fibrosi. In caso di fibrosi, il fegato si presenta molto duro e compatto, con possibile presenza di calcificazioni oltre che di abbondante collagene. La deposizione di materiale fibrotico si ha inizialmente a livello degli spazi sottoendoteliali e successivamente si osserva la formazione di travate fibrose che dissecano i lobuli epatici alterandone la struttura anatomica. Si determina quindi un alterazione del processo rigenerativo con formazione di pseudolobuli, non irrorati da vasi sanguigni. In particolare le cellule stellate, stimolate dal danno epatico cronico, proliferano e differenziano in miofibroblasti, i quali procedono al rilascio di collagene e matrice extracellulare. I processi di infiammazione sono teoricamente reversibili: sperimentalmente si è osservato che sospendendo lo stimolo infiammatorio era possibile una reversione della fibrosi. 33
34 MECCANISMI DI RIPARAZIONE DEL DANNO TISSUTALE La risposta al danno tissutale si esplica attraverso meccanismi con scopi precisi Arrestare la (eventuale) perdita di sangue: emostasi Combattere l aggressione da parte di agenti dannosi (soprattutto batteri): infiammazione Ricostruire i tessuti danneggiati: riparazione I tipi cellulari coinvolti nei meccanismi di riparazione sono molteplici, e possono variare in relazione al tipo di danno: Riparazione delle ferite dermo-epidermiche e del tessuto epiteliale La guarigione delle ferite cutanee prevede una cronologia precisa di eventi che avvengono anche contemporaneamente. Reclutamento della risposta infiammatoria Il primo passo consiste nel reclutamento della risposta infiammatoria. Vengono richiamati e persistono nel tessuto macrofagi e mastcellule. I macrofagi sono indispensabili, sono coinvolti nella terminazione del processo infiammatorio e nella pulizia del terreno. Importante è il ruolo del processo emostatico: rapidamente si forma un coagulo, che una volta essiccato darà l escara. L escara ha una duplice funzione: Protegge la ferita Costituisce il terreno su cui si muovono le cellule durante la coagulazione Si ha quindi degradazione di tale tipo tessuto: i macrofagi rilasciano metalloproteasi, che digeriscono la matrice extracellulare del coagulo e determinano la liberazione di fattori di crescita presenti nella matrice stessa. I macrofagi, in questo contesto, hanno capacità riparativa e fibrogenetica, rilasciano mediatori per il reclutamento dei miofibroblasti e partecipano alla neoangiogenesi; hanno caratteristiche di tipo M2. L evento caratterizzante della riparazione delle ferite cutanee è la formazione del tessuto di granulazione. Esso ha aspetto giallo-biancastro, molle, riccamente vascolarizzato. È un tessuto particolare, caratterizzato dalla deposizione di nuova matrice connettivale (acido ialuronico, ecc.) e un ampio letto vascolare, costituito da capillari neoformati. 34
35 Neoangiogenesi La neoangiogenesi è legata all ipossia che si instaura nell area interna della ferita. Si attiva la risposta dei macrofagi, che secernono citochine e messaggeri proangiogenetici; il bersaglio è l endotelio dei vasi circostanti. Si induce così attivazione delle cellule endoteliali, che emettono pseudopodi e degradano la membrana basale; viene stimolata la motilità delle cellule endoteliali stesse; il bottone di cellule endoteliali si sposta; una cellula leader emette pseudopodi e controlla l ambiente circostante. La cellula leader avanza all interno della matrice ed è seguita da altre cellule endoteliali in proliferazione. Si forma una struttura a canalicolo, che costituisce il nuovo lume vascolare. Importanti sono gli stimoli ricevuti dalle cellule endoteliali: si tratta di segnali chemiotattici mediati principalmente dai VEGF e da altre molecole quali semaforine, nectrine e altre proteine della matrice; si esprimono recettori per EPO, endotelina, ecc. I nuovi vasi, quindi, si anastomizzano tra loro formando nuovi capillari; questi ultimi inizialmente sono costituiti da sole cellule endoteliali, successivamente si aggiungono i periciti, che circondano l endotelio, determinano la formazione della membrana basale endoteliale, consentono la formazione di capillari più resistenti. Gli stimoli ipossici sono mediati da HIF: I fattori di crescita vascolari implicati sono diversi: 35
36 Si considerano anche MMP (metalloproteasi), inibitori delle MMP e attivatori delle MMP: si tratta di molecole determinanti, che sono prodotte da macrofagi ed endotelio. Le MMP sono secrete come proenzimi e sono attivate mediante taglio proteolitico soprattutto grazie alla plasmina. Insieme al plasminogeno si rilascia inoltre l attivatore tissutale del plasminogeno. Le proteine TIMP sono inibitori tissutali delle MMP. Riparazione Importanti eventi caratterizzano l evoluzione verso la cicatrice: regressione dei capillari che si restringono, arresto del flusso ed apoptosi delle cellule del sangue. Questo avviene in virtù di un equilibrio tra fattori proangiogenetici e fattori antiangiogenetici; tra questi ultimi vi sono: Proteine di matrice: endostatina, arrestene, frammenti di fibronectina o di trombospondina, ecc. Prodotti di secrezione, non derivanti dalla matrice: angiostatina, frammenti di plasminogeno, vasostatina, ecc. Si ha il coinvolgimento di modificatori della matrice extracellulare. Prima laminina e fibronectina, che sono importanti nel tessuto di granulazione perché costituiscono un punto di attacco per integrine di macrofagi e miofibroblasti. C è una grande quantità di mucopolisaccaridi e proteoglicani, che legano i GF e ne favoriscono la presentazione ai recettori presenti sulle cellule. I fattori di crescita in questione sono PDGF, VEGF, TGF-β e FGF. FGF stimola la proliferazione e la differenziazione di cellule connettivali ed epiteliali. Questi fattori di cresciti sono anche in grado di stimolare la motilità cellulare. Attori importanti del processo riparativo sono i miofibroblasti, che derivano dalla migrazione dei fibroblasti, dalla proliferazione delle cellule nel tessuto in riparazione, da precursori mesenchimali circolanti di origine midollare. La loro azione è importante anche per la retrazione della ferita. Essi secernono componenti della matrice extracellulare (collagene prima di tipo III, poi di tipo I). Formano una prima trama organizzata di collagene, poi l intervento delle MMP determina l orientamento secondo le linee di forza e la cicatrice si irrobustisce. Aspetto fondamentale della formazione del tessuto cicatriziale è la migrazione delle cellule epiteliali. Nella riparazione delle ferite cutanee essa è precoce, inizia nelle prime ore. La velocità è un fattore essenziale per la guarigione, è importante che si crei rapidamente una barriere di protezione dalle infezioni e che prevenga la fuoriuscita di liquido. I due processi principali in cui sono coinvolte le cellule del tessuto di granulazione sono la proliferazione, sostenuta da cellule contenute nelle nicchie staminali, e l espansione-mobilizzazione. L attività di proliferazione è sostenuta dalle stesse 36
37 citochine di prima, in particolare da EGF; quella di mobilizzazione è sostenuta da HGF (Hepatocyte Growth Factor, fattori di crescita anche per altri tipi cellulari) o scattern factor. Per i movimenti sono essenziali le integrine, in particolare integrina α3β1 e integrina α2,3,4β1: si tratta di molecole dimeriche, che si legano a laminina e fibronectina e determinano ancoraggio e liberazione di segnali che coinvolgono le placche di adesione focale, reclutano le FAK e le chinasi Src che trasducono un segnale per la sopravvivenza e la liberazione di fattori di crescita; queste integrine sono espresse da miofibroblasti, cellule endoteliali ed epiteliali. Per quanto riguarda gli organi parenchimatosi, si deve una componente determinante, che è quella data dalle cellule staminali, essenziali per ripristinare il numero originale di cellule. Diverse sono le tipologia dei processi di guarigione delle ferite cutanee: Guarigione per prima intenzione: i margini sono strettamente adiacenti, la cicatrice risulta essere modesta, praticamente assente. Si ha restitutio ad integrum velocemente Guarigione per seconda intenzione: i margini sono distanti, i tempi sono allungati, il risultato è la formazione di una cicatrice più o meno evidente, le dimensioni dipendono dall entità del danno. Le cicatrici determinano menomazioni strutturali, il tessuto è rigido, poco vascolarizzato, meno funzionale (ciò è evidente soprattutto nel caso di organi parenchimatosi). I fattori che condizionano la guarigione delle ferite possono essere: Fattori locali: - Tipo, dimensioni e localizzazione della ferita - Apporto ematico - Infezione - Movimento - Radiazioni ionizzanti - Radiazioni ultraviolette - Variazioni della temperatura - Rimozione della noxa o presenza di corpi estranei - Contatto tra i lembi della ferita Fattori sistemici: - Età - Stato circolatorio - Stato metabolico - Ormoni: glucocorticoidi, ACTH, GH, estrogeni, paratormone, calcitonina - Malattie concomitanti - Alimentazione: vitamina C, vitamina K, amminoacidi, calcio, zinco Ci possono essere alterazioni nei processi di guarigione e di cicatrizzazione, che talvolta sfociano nella formazione dei cheloidi, ossia cicatrici ipertrofiche, ricche di tessuto connettivale, caratterizzate dalla diffusa presenza di fibroblasti e da un rallentato turnover della matrice extracellulare. I cheloidi possono dare luogo a compressioni, può risultare difficile compiere certi movimenti o si può avere schiacciamento di organi. Ci sono basi genetiche che predispongono alla comparsa di cheloidi. 37
38 Riparazione delle fratture ossee Il tessuto osseo è organizzato in maniera peculiare; esso è caratterizzato da svariate popolazioni cellulari (osteoblasti, osteoclasti, cellule di origine mesenchimale che fungono da precursori degli osteoblasti). È un tessuto soggetto a continuo rimodellamento. Nelle fasi iniziali della guarigione di una ferita ossea, si ha un coagulo ematico che consegue alla rottura dei capillari dell osteoide. Il coagulo è intraperiostale o coinvolge le strutture limitrofe; esso viene invaso da macrofagi e poi da miofibroblasti; si forma il tessuto di granulazione. A questo punto vengono richiamate o si formano dai miofibroblasti le cellule condrocitarie, responsabili della deposizione di ECM ricca di collagene di tipo II e X; la composizione della ECM risulta essere quella della cartilagine. La deposizione di tessuto cartilagineo richiede circa una settimana e determina la sostituzione del tessuto fibroso con un callo fibrocartilagineo, che spesso risulta ridondante. Al suo interno si instaurano modificazioni che determinano la successiva ossificazione: nelle zone circostanti il callo si reclutano osteoclasti, atti al rimodellamento della matrice; i callo diventa cartilagineo e aumentano continuità e resistenza. Poi si osservano nuclei di calcificazione endocondrale, formati da osteoblasti. Le cellule periostali invadono la matrice e, dopo un mese, si forma un callo osseo costituito da osso compatto ma non organizzato. Successivamente si ha il rimaneggiamento osseo e si formano nuovi osteoni; questo processo richiede mesi e dipende dai carichi meccanici che l osso subisce. Il coordinamento delle attività di osteoblasti e osteoclasti dipende da citochine e da specifiche proteine, le proteine morfogenetiche dell osso (BMP). I segnali indotti dalle BMPs sono 38
39 Guarigione del tessuto nervoso È da sottolineare che vi sono importanti differenze a seconda che ci si riferisca a sistema nervoso centrale oppure periferico. Sebbene vi sia una capacità di rigenerazione assonale, nel SNC ciò è inibito dalla secrezione di glicoproteine acide da parte degli astrociti (che sono di derivazione tipo monocitica). Nel SNC, le lesioni neuronali evolvono in deposizioni fibromieliniche. Nel SNP è possibile la riparazione dei nervi lesionati. La lesione degli assoni causa la degenerazione anterograda e retrograda del neurone. La degenerazione retrograda, o Walleriana, determina la dissoluzione della struttura assonale. Se la lesione è vicina al soma si può avere apoptosi del neurone, mentre se è lontana dal soma il nucleo può essere risparmiato. L evento successivo è il distacco delle cellule di Schwann, che causa demielinizzazione; i macrofagi fagocitano e degradano la glia. Nel corpo neuronale si crea un rigonfiamento, detto ovoide di mielina, in cui si accumulano vescicole e mitocondri; dopo qualche giorno escono dei filamenti dendritici, ricchi di recettori per molecole della matrice extracellulare (semaforine, eccetera). I recettori tastano il terreno circostante alla ricerca del tracciato lasciato dal precedente neurite; il dendrite che lo trova sopravvive e si allunga velocemente (2-3 mm/die), mentre gli altri degenerano. La crescita continua finché il neurone non ripristina il collegamento con la struttura successiva. Si ha poi, nell arco di settimane, la riorganizzazione delle cellule di Schwann, che avvolgono il neurone e producono mielina, permettendo il ripristino della struttura precedente. I mediatori coinvolti sono FGF, altri fattori di crescita, NGF, neuropoietine, semaforine, ephrine. Essi possono infatti essere usati come stimolanti per la reinnervazione. Gli esiti del processo di riparazione La riparazione del danno tissutale prevede: Rigenerazione delle cellule e delle strutture dei parenchimi (eventualmente) Riparazione dello stroma connettivale, sia per compensare le eventuali perdite sia per rimpiazzare deficit degenerativi Si instaura un equilibrio tra due processi: Replicazione connettivale, che dà luogo alla cicatrice Rigenerazione della struttura originaria Ci si sposta a favore di un evento piuttosto che di un altro a seconda del tipo di tessuto: 39
Mediatori di infiammazione. Lezione del 21 Novembre 2014
 Mediatori di infiammazione Lezione del 21 Novembre 2014 Che cos è un mediatore? Un mediatore è una qualunque molecola generata in un focolaio infiammatorio che modula in qualche modo la risposta flogistica
Mediatori di infiammazione Lezione del 21 Novembre 2014 Che cos è un mediatore? Un mediatore è una qualunque molecola generata in un focolaio infiammatorio che modula in qualche modo la risposta flogistica
Marginazione polimorfonucleati
 Marginazione polimorfonucleati STIMOLI ATTIVANTI IL-1, TNFa SELETTINE MOLECOLE DI ADESIONE FASE DELL ADESIONE INIZIALE LASSA E-SELETTINA sulle cellule endoteliali P-SELETTINA cellule endoteliali e piastrine.
Marginazione polimorfonucleati STIMOLI ATTIVANTI IL-1, TNFa SELETTINE MOLECOLE DI ADESIONE FASE DELL ADESIONE INIZIALE LASSA E-SELETTINA sulle cellule endoteliali P-SELETTINA cellule endoteliali e piastrine.
Il SISTEMA DEL COMPLEMENTO. proteine plasmatiche che svolgono. flogosi sono due meccanismi assai
 SISTEMA DEL COMPLEMENTO Il SISTEMA DEL COMPLEMENTO consiste in una serie numerosa di proteine plasmatiche che svolgono un ruolo fondamentale nella risposta immunitaria come nell infiammazione (immunità
SISTEMA DEL COMPLEMENTO Il SISTEMA DEL COMPLEMENTO consiste in una serie numerosa di proteine plasmatiche che svolgono un ruolo fondamentale nella risposta immunitaria come nell infiammazione (immunità
Immunità cellulo-mediata
 Immunità cellulo-mediata Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari Immunità cellulo-mediata
Immunità cellulo-mediata Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari Immunità cellulo-mediata
I MEDIATORI CHIMICI DELLA FLOGOSI
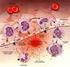 I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
Leucociti circolanti 5-10% 2-3% 60-70% 20-25% 0.1%
 Leucociti circolanti 5-10% 2-3% 60-70% 20-25% 0.1% 5% CFU=unità formante colonie Le cellule effettrici più numerose del SI innato sono cellule derivate dal midollo osseo che circolano nel sangue e migrano
Leucociti circolanti 5-10% 2-3% 60-70% 20-25% 0.1% 5% CFU=unità formante colonie Le cellule effettrici più numerose del SI innato sono cellule derivate dal midollo osseo che circolano nel sangue e migrano
Infiammazione (flogosi)
 Infiammazione (flogosi) Reazione di un tessuto vascolarizzato ad un danno locale Componente vascolare Componente cellulare Infiammazione acuta Calor Rubor Tumor Dolor Functio laesa Equilibrio dei fluidi
Infiammazione (flogosi) Reazione di un tessuto vascolarizzato ad un danno locale Componente vascolare Componente cellulare Infiammazione acuta Calor Rubor Tumor Dolor Functio laesa Equilibrio dei fluidi
INTRODUZIONE ALLE REAZIONI FLOGISTICHE
 INTRODUZIONE ALLE REAZIONI FLOGISTICHE INCONTRO FRA CELLUA E NOXA PATOGENA: SEQUENZA DEGLI EVENTI noxa patogena adattamento cellula danno irreversibile danno reversibile - stress proteins - enzimi di riparazione
INTRODUZIONE ALLE REAZIONI FLOGISTICHE INCONTRO FRA CELLUA E NOXA PATOGENA: SEQUENZA DEGLI EVENTI noxa patogena adattamento cellula danno irreversibile danno reversibile - stress proteins - enzimi di riparazione
Immunologia e Immunopatologia. LINFOCITI T HELPER: Citochine dell Immunità Specifica
 Immunologia e Immunopatologia LINFOCITI T HELPER: Citochine dell Immunità Specifica Linfociti T effettori T helper: regolazione dell immunità specifica Attivazione macrofagi Secrezione Ab, scambio isotipico
Immunologia e Immunopatologia LINFOCITI T HELPER: Citochine dell Immunità Specifica Linfociti T effettori T helper: regolazione dell immunità specifica Attivazione macrofagi Secrezione Ab, scambio isotipico
I principali mediatori chimici dell infiammazione
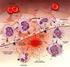 I principali mediatori chimici dell infiammazione Mediatori plasmatici Danno endoteliale! Il Fattore di Hageman ha un ruolo centrale nell attivazione dei mediatori plasmatici Mediatori plasmatici: IL SISTEMA
I principali mediatori chimici dell infiammazione Mediatori plasmatici Danno endoteliale! Il Fattore di Hageman ha un ruolo centrale nell attivazione dei mediatori plasmatici Mediatori plasmatici: IL SISTEMA
Basi cellulari della risposta immune. Cellule linfoidi. F 9a. Precursori cellule ematiche
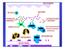 Basi cellulari della risposta immune F 9a Cellule linfoidi Precursori cellule ematiche Feto (fegato) Adulto (midollo osseo) F 9a F 9a F 9a F 9a Idiotipo: disegno antigenico della regione ipervariabile
Basi cellulari della risposta immune F 9a Cellule linfoidi Precursori cellule ematiche Feto (fegato) Adulto (midollo osseo) F 9a F 9a F 9a F 9a Idiotipo: disegno antigenico della regione ipervariabile
Meccanismi effettori della RISPOSTA IMMUNITARIA
 Meccanismi effettori della RISPOSTA IMMUNITARIA RUOLO delle APC LE CELLULE APC PROFESSIONALI ATTIVITA DEL LINFOCITA Th Innesco della Risposta Immunitaria AZIONE DEI LINFOCITI T Attivazione dei linfociti
Meccanismi effettori della RISPOSTA IMMUNITARIA RUOLO delle APC LE CELLULE APC PROFESSIONALI ATTIVITA DEL LINFOCITA Th Innesco della Risposta Immunitaria AZIONE DEI LINFOCITI T Attivazione dei linfociti
Meccanismi effettori dei linfociti T citotossici
 Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
Struttura degli anticorpi
 Struttura degli anticorpi (220 aa) (440 aa) Le classi di anticorpi Ig A, IgD, IgE, IgG, IgM IgM Risposta primaria Attivazione della fagocitosi attivazione del complemento IgM monomeriche insieme alle IgD
Struttura degli anticorpi (220 aa) (440 aa) Le classi di anticorpi Ig A, IgD, IgE, IgG, IgM IgM Risposta primaria Attivazione della fagocitosi attivazione del complemento IgM monomeriche insieme alle IgD
Immunita innata: cellule e meccanismi coinvolti
 Immunita innata: cellule e meccanismi coinvolti Immunita innata Immunita innata Prima linea di difesa Seconda linea di difesa Componenti dell Immunita innata Sistema immunitario innato Prima linea Seconda
Immunita innata: cellule e meccanismi coinvolti Immunita innata Immunita innata Prima linea di difesa Seconda linea di difesa Componenti dell Immunita innata Sistema immunitario innato Prima linea Seconda
Definizione: dal latino Inflammare (sinonimo: Flogosi)
 INFIAMMAZIONE Definizione: dal latino Inflammare (sinonimo: Flogosi) Processo biologico Processo biologico complesso, alla cui genesi difensivo e riparativo contribuiscono avente lo scopo di diluire, modificazioni
INFIAMMAZIONE Definizione: dal latino Inflammare (sinonimo: Flogosi) Processo biologico Processo biologico complesso, alla cui genesi difensivo e riparativo contribuiscono avente lo scopo di diluire, modificazioni
Schema delle citochine
 Schema delle citochine 13 gennaio 2011 1 Risposta innata TNF - Tumor Necrosis Factor Fonti principali: fagociti attivati, NK e mastociti. Struttura e recettore: inizialmente proteina di membrana, poi tagliata
Schema delle citochine 13 gennaio 2011 1 Risposta innata TNF - Tumor Necrosis Factor Fonti principali: fagociti attivati, NK e mastociti. Struttura e recettore: inizialmente proteina di membrana, poi tagliata
Piccole proteine (15-30kDal) Riconosciute da recettori Secrete da diversi tipi cellulari
 Piccole proteine (15-30kDal) Riconosciute da recettori Secrete da diversi tipi cellulari La gran parte delle citochine sono per convenzione chiamate interleuchine ad indicare che queste sono prodotte dai
Piccole proteine (15-30kDal) Riconosciute da recettori Secrete da diversi tipi cellulari La gran parte delle citochine sono per convenzione chiamate interleuchine ad indicare che queste sono prodotte dai
Immunologia e Immunologia Diagnostica ATTIVAZIONE CELLULE B E IMMUNITÀ UMORALE
 Immunologia e Immunologia Diagnostica ATTIVAZIONE CELLULE B E IMMUNITÀ UMORALE Le fasi della risposta umorale 1. Riconoscimento dell antigene (legame BCR) 2. Stimoli addizionali (T helper, citochine, complemento)
Immunologia e Immunologia Diagnostica ATTIVAZIONE CELLULE B E IMMUNITÀ UMORALE Le fasi della risposta umorale 1. Riconoscimento dell antigene (legame BCR) 2. Stimoli addizionali (T helper, citochine, complemento)
COME FUNZIONA IL SISTEMA IMMUNITARIO
 COME FUNZIONA IL COME FUNZIONA IL SISTEMA IMMUNITARIO I vertebrati possiedono complessi meccanismi difensivi che costituiscono il sistema immunitario, che li protegge dall invasione di microrganismi patogeni,
COME FUNZIONA IL COME FUNZIONA IL SISTEMA IMMUNITARIO I vertebrati possiedono complessi meccanismi difensivi che costituiscono il sistema immunitario, che li protegge dall invasione di microrganismi patogeni,
Immunità naturale o aspecifica o innata
 Immunità naturale o aspecifica o innata E' la resistenza che ogni individuo possiede nei confronti dei patogeni indipendentemente da ogni precedente contatto E dovuta al riconoscimento di strutture tipicamente
Immunità naturale o aspecifica o innata E' la resistenza che ogni individuo possiede nei confronti dei patogeni indipendentemente da ogni precedente contatto E dovuta al riconoscimento di strutture tipicamente
Le difese dell organismo IL SISTEMA IMMUNITARIO
 Le difese dell organismo IL SISTEMA IMMUNITARIO Responsabile dell IMMUNITA Capacità dell org di resistere ed eventualmente eliminare sostanze estranee o cellule anormali 12 1 IL SISTEMA IMMUNITARIO Sistema
Le difese dell organismo IL SISTEMA IMMUNITARIO Responsabile dell IMMUNITA Capacità dell org di resistere ed eventualmente eliminare sostanze estranee o cellule anormali 12 1 IL SISTEMA IMMUNITARIO Sistema
Immunologia e Immunologia Diagnostica IL SISTEMA IMMUNITARIO E L IMMUNITÀ INNATA
 Immunologia e Immunologia Diagnostica IL SISTEMA IMMUNITARIO E L IMMUNITÀ INNATA Informazioni sul Corso Descrizione del Corso Modulo di Ivano Condò Corso Integrato di Biochimica Clinica e Immunologia Coordinatore:
Immunologia e Immunologia Diagnostica IL SISTEMA IMMUNITARIO E L IMMUNITÀ INNATA Informazioni sul Corso Descrizione del Corso Modulo di Ivano Condò Corso Integrato di Biochimica Clinica e Immunologia Coordinatore:
Infiammazione acuta Infiammazione cronica
 Infiammazione (flogosi) Reazione di un tessuto vascolarizzato ad un danno locale Componente vascolare Componente cellulare Infiammazione acuta Infiammazione cronica Infiammazione acuta Calor Rubor Tumor
Infiammazione (flogosi) Reazione di un tessuto vascolarizzato ad un danno locale Componente vascolare Componente cellulare Infiammazione acuta Infiammazione cronica Infiammazione acuta Calor Rubor Tumor
IMMUNITA RIMOZIONE DELL AGENTE INFETTIVO. Riconoscimento da parte di effettori preformati non
 IMMUNITA INFEZIONE Immunità innata specifici RIMOZIONE DELL AGENTE INFETTIVO Riconoscimento da parte di effettori preformati non (risposta immediata 0-4 ore) Risposta indotta precoce Riconoscimento, Reclutamento
IMMUNITA INFEZIONE Immunità innata specifici RIMOZIONE DELL AGENTE INFETTIVO Riconoscimento da parte di effettori preformati non (risposta immediata 0-4 ore) Risposta indotta precoce Riconoscimento, Reclutamento
Formazione dell essudato
 Formazione dell essudato Û della permeabilità vascolare azione lesiva diretta dell agente flogogeno sulla parete vascolare azione vasopermeabilizzante dei mediatori della flogosi (selettivamente a livello
Formazione dell essudato Û della permeabilità vascolare azione lesiva diretta dell agente flogogeno sulla parete vascolare azione vasopermeabilizzante dei mediatori della flogosi (selettivamente a livello
La risoluzione dell infiammazione comincia dopo poche ore dall inizio dell infiammazione stessa.
 La risoluzione dell infiammazione comincia dopo poche ore dall inizio dell infiammazione stessa. NOXAE FLOGOGENE - Infezioni (batteriche, virali ecc) - Stimoli fisici (caldo, freddo, radiazioni) - Stimoli
La risoluzione dell infiammazione comincia dopo poche ore dall inizio dell infiammazione stessa. NOXAE FLOGOGENE - Infezioni (batteriche, virali ecc) - Stimoli fisici (caldo, freddo, radiazioni) - Stimoli
COME FANNO LE CELLULE SOFFERENTI AD ATTIVARE IL PROCESSO INFIAMMATORIO?
 COME FANNO LE CELLULE SOFFERENTI AD ATTIVARE IL PROCESSO INFIAMMATORIO? Quando le cellule sono dai danneggiate reversibilmente possono ancora decidere se suicidarsi (morire per apoptosi, che ha comunque
COME FANNO LE CELLULE SOFFERENTI AD ATTIVARE IL PROCESSO INFIAMMATORIO? Quando le cellule sono dai danneggiate reversibilmente possono ancora decidere se suicidarsi (morire per apoptosi, che ha comunque
Proprietà Esotossine Endotossine
 Principali differenze tra Esotossine ed Endotossine Proprietà Esotossine Endotossine Proprietà chimiche Modalità d azione Immunogenicità Potenzialità del tossoide Proteine secrete nell ambiente extracellulare
Principali differenze tra Esotossine ed Endotossine Proprietà Esotossine Endotossine Proprietà chimiche Modalità d azione Immunogenicità Potenzialità del tossoide Proteine secrete nell ambiente extracellulare
Lessico di base Antigene: ogni macromolecola estranea all organismo che viene riconosciuta specificamente dal sistema immunitario e che innesca una
 Lessico di base Antigene: ogni macromolecola estranea all organismo che viene riconosciuta specificamente dal sistema immunitario e che innesca una risposta immunitaria. Anticorpo (immunoglobulina solubile):
Lessico di base Antigene: ogni macromolecola estranea all organismo che viene riconosciuta specificamente dal sistema immunitario e che innesca una risposta immunitaria. Anticorpo (immunoglobulina solubile):
IMMUNITA IMMUNITA INNATA O NATURALE IMMUNITA ACQUISITA
 IMMUNITA IMMUNITA INNATA O NATURALE IMMUNITA ACQUISITA Immunità naturale: barriera che l'organismo eredita dai genitori e protegge da molti agenti patogeni Fattori coinvolti: razza, sesso, stato di nutrizione,
IMMUNITA IMMUNITA INNATA O NATURALE IMMUNITA ACQUISITA Immunità naturale: barriera che l'organismo eredita dai genitori e protegge da molti agenti patogeni Fattori coinvolti: razza, sesso, stato di nutrizione,
FLOGOSI CRONICA: CAUSE
 FLOGOSI CRONICA FLOGOSI CRONICA: CAUSE inadeguatezza della risposta flogistica acuta nell eliminare la noxa caratteristiche della noxa che inducono reazione cronica 1- infezioni a basso potenziale proflogistico
FLOGOSI CRONICA FLOGOSI CRONICA: CAUSE inadeguatezza della risposta flogistica acuta nell eliminare la noxa caratteristiche della noxa che inducono reazione cronica 1- infezioni a basso potenziale proflogistico
Complesso Maggiore di Istocompatibilita (MHC)
 Complesso Maggiore di Istocompatibilita (MHC) Scoperta dell MHC I geni dell MHC sono stati inizialmente identificati come responsabili del rapido rigetto dei tessuti trapiantati. I geni dell MHC sono polimorfi:
Complesso Maggiore di Istocompatibilita (MHC) Scoperta dell MHC I geni dell MHC sono stati inizialmente identificati come responsabili del rapido rigetto dei tessuti trapiantati. I geni dell MHC sono polimorfi:
Argomento della lezione
 Argomento della lezione Le molecole d adesione intercellulare: definizione Le famiglie delle molecole d adesione: Selectine Integrine ICAM Espressione e funzione MOLECOLE DI ADESIONE INTERCELLULARE Le
Argomento della lezione Le molecole d adesione intercellulare: definizione Le famiglie delle molecole d adesione: Selectine Integrine ICAM Espressione e funzione MOLECOLE DI ADESIONE INTERCELLULARE Le
Immunologia e Immunologia Diagnostica COMPLESSO MAGGIORE DI ISTOCOMPATIBILITÀ E PRESENTAZIONE DELL ANTIGENE
 Immunologia e Immunologia Diagnostica COMPLESSO MAGGIORE DI ISTOCOMPATIBILITÀ E PRESENTAZIONE DELL ANTIGENE Il Complesso Maggiore di Istocompatibilità (MHC) Scoperta dell MHC I geni dell MHC sono stati
Immunologia e Immunologia Diagnostica COMPLESSO MAGGIORE DI ISTOCOMPATIBILITÀ E PRESENTAZIONE DELL ANTIGENE Il Complesso Maggiore di Istocompatibilità (MHC) Scoperta dell MHC I geni dell MHC sono stati
Esotossina: definizione Prodotto del metabolismo di alcuni batteri che viene riversato nel mezzo in cui essi sono posti a sviluppare Glicoproteine ad
 Esotossine ed Endotossine prof. Vincenzo Cuteri Esotossina: definizione Prodotto del metabolismo di alcuni batteri che viene riversato nel mezzo in cui essi sono posti a sviluppare Glicoproteine ad attività
Esotossine ed Endotossine prof. Vincenzo Cuteri Esotossina: definizione Prodotto del metabolismo di alcuni batteri che viene riversato nel mezzo in cui essi sono posti a sviluppare Glicoproteine ad attività
MODULO 2: infiammazione e immunità innata
 MODULO 2: infiammazione e immunità innata Lezione 2-7: Infiammazione: definizione caratteristiche generali Infiammazione acuta: eventi vascolari eventi cellulari Dott.ssa Chiara Porta: Chiara.porta@unipmn.it
MODULO 2: infiammazione e immunità innata Lezione 2-7: Infiammazione: definizione caratteristiche generali Infiammazione acuta: eventi vascolari eventi cellulari Dott.ssa Chiara Porta: Chiara.porta@unipmn.it
Immunologia e Immunopatologia ATTIVAZIONE DEI LINFOCITI T
 Immunologia e Immunopatologia ATTIVAZIONE DEI LINFOCITI T Le fasi dell immunità specifica cellulo-mediata 1. Attivazione dei linfociti T 2. Differenziamento linfociti T effettori 3. Reazioni immunitarie
Immunologia e Immunopatologia ATTIVAZIONE DEI LINFOCITI T Le fasi dell immunità specifica cellulo-mediata 1. Attivazione dei linfociti T 2. Differenziamento linfociti T effettori 3. Reazioni immunitarie
La risoluzione dell infiammazione comincia dopo poche ore dall inizio dell infiammazione stessa.
 La risoluzione dell infiammazione comincia dopo poche ore dall inizio dell infiammazione stessa. NOXAE FLOGOGENE - Infezioni (batteriche, virali ecc) - Stimoli fisici (caldo, freddo, radiazioni) - Stimoli
La risoluzione dell infiammazione comincia dopo poche ore dall inizio dell infiammazione stessa. NOXAE FLOGOGENE - Infezioni (batteriche, virali ecc) - Stimoli fisici (caldo, freddo, radiazioni) - Stimoli
Cellule infiammatorie
 Cellule infiammatorie Le principali cellule coinvolte nella risposta infiammatoria sono: - Granulociti - Macrofagi e cellule derivate - Linfociti e Plasmacellule Mastociti - Fibroblasti Le vie attraverso
Cellule infiammatorie Le principali cellule coinvolte nella risposta infiammatoria sono: - Granulociti - Macrofagi e cellule derivate - Linfociti e Plasmacellule Mastociti - Fibroblasti Le vie attraverso
MEDIATORI CHIMICI DELL INFIAMMAZIONE
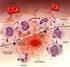 MEDIATORI CHIMICI DELL INFIAMMAZIONE Sono sostanze presenti nell organismo in forma di precursori inattivi o sequestrati in siti intracellulari dove non possono esplicare la loro azione. In seguito ad
MEDIATORI CHIMICI DELL INFIAMMAZIONE Sono sostanze presenti nell organismo in forma di precursori inattivi o sequestrati in siti intracellulari dove non possono esplicare la loro azione. In seguito ad
CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA. Prof. Roberto Testi Indirizzo
 CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA COORDINATORE Prof. Roberto Testi Indirizzo e-mail: roberto.testi@uniroma2.it SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte. Immunopatologia 1 LIBRI
CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA COORDINATORE Prof. Roberto Testi Indirizzo e-mail: roberto.testi@uniroma2.it SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte. Immunopatologia 1 LIBRI
Migrazione dei leucociti attraverso la parete endoteliale delle venule postcapillari (dove il flusso ematico è più lento) nei tessuti adiacenti
 I leucociti I leucociti Sono anche detti globuli bianchi ed il sangue li veicola verso gli organi dove esercitano le loro funzioni (difesa immunitaria) Perciò la maggior parte dei leucociti si trova al
I leucociti I leucociti Sono anche detti globuli bianchi ed il sangue li veicola verso gli organi dove esercitano le loro funzioni (difesa immunitaria) Perciò la maggior parte dei leucociti si trova al
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Il termine complemento è stato coniato da Jules Bordet circa un secolo fa e si riferisce alla funzione delle proteine che lo compongono: esse
 Il termine complemento è stato coniato da Jules Bordet circa un secolo fa e si riferisce alla funzione delle proteine che lo compongono: esse complementano la funzione degli anticorpi nell eliminazione
Il termine complemento è stato coniato da Jules Bordet circa un secolo fa e si riferisce alla funzione delle proteine che lo compongono: esse complementano la funzione degli anticorpi nell eliminazione
I macrofagi fagocitano i microbi e le sostanze estranee riconoscendo alcune caratteristiche generali di queste. Se la particella da fagocitare è
 Gli anticorpi sono in grado di eliminare i microbi mediante meccanismi diretti come la neutralizzazione, l immobilizzazione e la formazione di immunocomplessi o indiretti quali l attivazione delle proteine
Gli anticorpi sono in grado di eliminare i microbi mediante meccanismi diretti come la neutralizzazione, l immobilizzazione e la formazione di immunocomplessi o indiretti quali l attivazione delle proteine
Gli Ac sono il 20% delle proteine sieriche; oggi sono chiamati immunoglobuline: Ig Le Ig sono nel plasma, nel muco, nei secreti ghiandolari e negli
 ANTICORPI ANTICORPI: molecole ( glicoproteine ) prodotte in risposta ad un antigene e capaci di formare un legame specifico con la sostanza che ne ha indotto la formazione. espressi sulla superficie dei
ANTICORPI ANTICORPI: molecole ( glicoproteine ) prodotte in risposta ad un antigene e capaci di formare un legame specifico con la sostanza che ne ha indotto la formazione. espressi sulla superficie dei
Mediatori Chimici. Fegato. Cellulari (prodotti dalle cellule infiammatorie. Preformati in granuli secretori. Neosintetizzati
 Cellulari (prodotti dalle cellule infiammatorie Fegato Fonte principale Mediatori Chimici Preformati in granuli secretori Neosintetizzati Mediatore Istamina Serotonina Enzimi lisosomiali Prostaglandine
Cellulari (prodotti dalle cellule infiammatorie Fegato Fonte principale Mediatori Chimici Preformati in granuli secretori Neosintetizzati Mediatore Istamina Serotonina Enzimi lisosomiali Prostaglandine
La risposta umorale è mediata da anticorpi secreti dalle plasmacellule
 Risposta umorale La risposta umorale è mediata da anticorpi secreti dalle plasmacellule La risposta umorale è mediata da anticorpi secreti dalle plasmacellule Antigeni leganti il BCR sono internalizzati,
Risposta umorale La risposta umorale è mediata da anticorpi secreti dalle plasmacellule La risposta umorale è mediata da anticorpi secreti dalle plasmacellule Antigeni leganti il BCR sono internalizzati,
INSEGNAMENTO: IMMUNOLOGIA ED IMMUNOPATOLOGIA (GP005810)
 INSEGNAMENTO: IMMUNOLOGIA ED IMMUNOPATOLOGIA (GP005810) Corso di Laurea in Medicina e Chirurgia MU02 - Sede di Terni Docente titolare del corso: Dott.ssa Emanuela Rosati PROGRAMMA ORGANIZZAZIONE DEL SISTEMA
INSEGNAMENTO: IMMUNOLOGIA ED IMMUNOPATOLOGIA (GP005810) Corso di Laurea in Medicina e Chirurgia MU02 - Sede di Terni Docente titolare del corso: Dott.ssa Emanuela Rosati PROGRAMMA ORGANIZZAZIONE DEL SISTEMA
Ariel
 Informazioni utili E-mail: usare anche saverio.minucci@ieo.it Libri: Abbas-Lichtman: le basi dell immunologia Pier-Lickzak-Wetzler: immunologia-infezione-immunità Test finale: 2 domande aperte Una a piacere
Informazioni utili E-mail: usare anche saverio.minucci@ieo.it Libri: Abbas-Lichtman: le basi dell immunologia Pier-Lickzak-Wetzler: immunologia-infezione-immunità Test finale: 2 domande aperte Una a piacere
TRAFFICO INTRACELLULARE E COMUNICAZIONE TRA LE CELLULE
 TRAFFICO INTRACELLULARE E COMUNICAZIONE TRA LE CELLULE Carboidrati proteine Glicolipide Regione ad α-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di
TRAFFICO INTRACELLULARE E COMUNICAZIONE TRA LE CELLULE Carboidrati proteine Glicolipide Regione ad α-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di
L infiammazione (o flogosi) costituisce una risposta dei tessuti vascolarizzati a stimoli endogeni o esogeni che causano danno.
 L infiammazione (o flogosi) costituisce una risposta dei tessuti vascolarizzati a stimoli endogeni o esogeni che causano danno. INFIAMMAZIONE - Processo locale (con ripercussioni generali) - che si sviluppa
L infiammazione (o flogosi) costituisce una risposta dei tessuti vascolarizzati a stimoli endogeni o esogeni che causano danno. INFIAMMAZIONE - Processo locale (con ripercussioni generali) - che si sviluppa
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre
 Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
FATTORI DI CRESCITA COME MESSAGGERI
 RECETTORI ASSOCIATI A PROTEINE CHINASI Sono proteine che hanno sia funzione di recettore che attività enzimatica chinasica. L interazione con il ligando specifico stimola l attività della chinasi e il
RECETTORI ASSOCIATI A PROTEINE CHINASI Sono proteine che hanno sia funzione di recettore che attività enzimatica chinasica. L interazione con il ligando specifico stimola l attività della chinasi e il
Jay Phelan, Maria Cristina Pignocchino. Scopriamo la biologia
 Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 11 Il sistema immunitario 3 1. Le tre linee di difesa contro i patogeni Il sistema immunitario protegge l organismo attraverso tre
Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 11 Il sistema immunitario 3 1. Le tre linee di difesa contro i patogeni Il sistema immunitario protegge l organismo attraverso tre
IMMUNITA. L obiettivo finale è quello di proteggere l organismo da agenti infettivi e/o antigeni estranei
 IMMUNITA L uomo ha acquisito nel corso dell evoluzione tutta una serie di meccanismi difensivi che costituiscono il sistema immunitario, il quale mediante una risposta specifica e coordinata verso tutte
IMMUNITA L uomo ha acquisito nel corso dell evoluzione tutta una serie di meccanismi difensivi che costituiscono il sistema immunitario, il quale mediante una risposta specifica e coordinata verso tutte
ANTIGENE: molecola estranea, appartenente ad un batterio o ad un altro invasore, capace di indurre una risposta immunitaria.
 LA RISPOSTA IMMUNITARIA ANTIGENE: molecola estranea, appartenente ad un batterio o ad un altro invasore, capace di indurre una risposta immunitaria. ANTICORPO (o IMMUNOGLOBULINA, Ig): molecola proteica
LA RISPOSTA IMMUNITARIA ANTIGENE: molecola estranea, appartenente ad un batterio o ad un altro invasore, capace di indurre una risposta immunitaria. ANTICORPO (o IMMUNOGLOBULINA, Ig): molecola proteica
Molecole Adesione. 1. Introduzione. Molecole di adesione
 Molecole Adesione 1. Introduzione Molecole di adesione Permettono alle cellule di comunicare una con l altra e con il loro ambiente. Le interazioni tra molecole di adesione e i loro ligandi orchestrano
Molecole Adesione 1. Introduzione Molecole di adesione Permettono alle cellule di comunicare una con l altra e con il loro ambiente. Le interazioni tra molecole di adesione e i loro ligandi orchestrano
I leucociti o globuli bianchi sono cellule coinvolte nella risposta immunitaria. Grazie al loro intervento il corpo umano si difende dagli attacchi
 GLOBULI BIANCHI I leucociti sono cellule del sangue provviste di nucleo e si trovano nel circolo sanguigno, nel sistema linfatico e nei tessuti. La loro caratteristica assenza di pigmentazione gli conferisce
GLOBULI BIANCHI I leucociti sono cellule del sangue provviste di nucleo e si trovano nel circolo sanguigno, nel sistema linfatico e nei tessuti. La loro caratteristica assenza di pigmentazione gli conferisce
Caratteristiche generali della reazione infiammatoria
 Caratteristiche generali della reazione infiammatoria Localizzazione tessuti interstiziali cavità interne del corpo: cavo pleurico, cavo peritoneale, cavo pericardico, vaginale del testicolo, cavità articolari
Caratteristiche generali della reazione infiammatoria Localizzazione tessuti interstiziali cavità interne del corpo: cavo pleurico, cavo peritoneale, cavo pericardico, vaginale del testicolo, cavità articolari
Interleuchine (linfochine)
 Interleuchine (linfochine) F 45 Interleuchina-1 (Il-1) - E prodotta soprattutto dai macrofagi attivati - Stimola i linfociti T a produrre Il-2 - Partecipa all attivazione dei B - Induce proliferazione
Interleuchine (linfochine) F 45 Interleuchina-1 (Il-1) - E prodotta soprattutto dai macrofagi attivati - Stimola i linfociti T a produrre Il-2 - Partecipa all attivazione dei B - Induce proliferazione
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
Il sistema immunitario ha sviluppato un sistema altamente specializzato per la cattura degli antigeni e per la loro presentazione ai linfociti.
 Come riescono pochi linfociti specifici per un antigene microbico a localizzare il microbo? Come riesce il sistema immunitario a produrre le cellule effettrici e le molecole piùadatte a debellare un determinato
Come riescono pochi linfociti specifici per un antigene microbico a localizzare il microbo? Come riesce il sistema immunitario a produrre le cellule effettrici e le molecole piùadatte a debellare un determinato
Immunità mediata da cellule T
 Immunità mediata da cellule T Le cellule T effettrici della risposta immune adattativa cellulare ed umorale Incontro delle cellule T naïve con l antigene avviene negli organi linfatici periferici Le cellule
Immunità mediata da cellule T Le cellule T effettrici della risposta immune adattativa cellulare ed umorale Incontro delle cellule T naïve con l antigene avviene negli organi linfatici periferici Le cellule
Il sangue è un tessuto connettivo. La caratteristica inusuale del sangue è che la matrice extracellulare è un liquido, per cui i sangue è un tessuto
 Il sangue è un tessuto connettivo. La caratteristica inusuale del sangue è che la matrice extracellulare è un liquido, per cui i sangue è un tessuto connettivo fluido. Costituisce l 8% del peso corporeo
Il sangue è un tessuto connettivo. La caratteristica inusuale del sangue è che la matrice extracellulare è un liquido, per cui i sangue è un tessuto connettivo fluido. Costituisce l 8% del peso corporeo
Immunità mediata da cellule T
 Immunità mediata da cellule T Le cellule T effettrici della risposta immune adattativa cellulare ed umorale Incontro delle cellule T naïve con l antigene avviene negli organi linfatici periferici Le cellule
Immunità mediata da cellule T Le cellule T effettrici della risposta immune adattativa cellulare ed umorale Incontro delle cellule T naïve con l antigene avviene negli organi linfatici periferici Le cellule
FACOLTA DI SCIENZE MOTORIE CORSO DI MEDICINA DELLO SPORT E TRAUMATOLOGIA. Prof. Franca Carandente. Appunti delle lezioni LEZIONE 1 L INFIAMMAZIONE
 FACOLTA DI SCIENZE MOTORIE CORSO DI MEDICINA DELLO SPORT E TRAUMATOLOGIA Prof. Franca Carandente Appunti delle lezioni LEZIONE 1 L INFIAMMAZIONE 1 L INFIAMMAZIONE O FLOGOSI E LA RISPOSTA DI UN TESSUTO
FACOLTA DI SCIENZE MOTORIE CORSO DI MEDICINA DELLO SPORT E TRAUMATOLOGIA Prof. Franca Carandente Appunti delle lezioni LEZIONE 1 L INFIAMMAZIONE 1 L INFIAMMAZIONE O FLOGOSI E LA RISPOSTA DI UN TESSUTO
Le immunoglobuline: struttura e funzioni
 PFA APPROPRIATEZZA NELL USO DELLE IMMUNOGLOBULINE Savona 2007 Le immunoglobuline: struttura e funzioni Francesco Indiveri,M.D. Clinica di medicina interna ad orientamento immunologico Di.M.I- Università
PFA APPROPRIATEZZA NELL USO DELLE IMMUNOGLOBULINE Savona 2007 Le immunoglobuline: struttura e funzioni Francesco Indiveri,M.D. Clinica di medicina interna ad orientamento immunologico Di.M.I- Università
La risposta immune innata
 La risposta immune innata Le tre fasi della risposta ad un agente infettivo La prima linea di difesa In molti casi, I microrganismi potenzialmente patogeni (che scatenano una malattia nell individuo colpito
La risposta immune innata Le tre fasi della risposta ad un agente infettivo La prima linea di difesa In molti casi, I microrganismi potenzialmente patogeni (che scatenano una malattia nell individuo colpito
ESSUDAZIONE CELLULARE
 ESSUDAZIONE CELLULARE La fase del processo infiammatorio che segue immediatamente la formazione della componente liquida dell essudato è la diapedesi, ovvero l uscita dei leucociti dai vasi verso il tessuto
ESSUDAZIONE CELLULARE La fase del processo infiammatorio che segue immediatamente la formazione della componente liquida dell essudato è la diapedesi, ovvero l uscita dei leucociti dai vasi verso il tessuto
ESSUDAZIONE CELLULARE
 ESSUDAZIONE CELLULARE La fase del processo infiammatorio che segue immediatamente la formazione della componente liquida dell essudato è la diapedesi, ovvero l uscita dei leucociti dai vasi verso il tessuto
ESSUDAZIONE CELLULARE La fase del processo infiammatorio che segue immediatamente la formazione della componente liquida dell essudato è la diapedesi, ovvero l uscita dei leucociti dai vasi verso il tessuto
IL COMPLEMENTO Sistema di numerose proteine plasmatiche, molte con attività proteolitica, capaci di attivarsi a cascata
 IL COMPLEMENTO Sistema di numerose proteine plasmatiche, molte con attività proteolitica, capaci di attivarsi a cascata I componenti del complemento mediano funzioni che portano indirettamente o direttamente
IL COMPLEMENTO Sistema di numerose proteine plasmatiche, molte con attività proteolitica, capaci di attivarsi a cascata I componenti del complemento mediano funzioni che portano indirettamente o direttamente
Psoriasi, le molecole segnale...
 Psoriasi, le molecole segnale... Fino all identificazione dei Th17 la psoriasi è stata considerata una patologia autoimmune classificata come Th1, con particolare attenzione alla citochina TNFα, il gold
Psoriasi, le molecole segnale... Fino all identificazione dei Th17 la psoriasi è stata considerata una patologia autoimmune classificata come Th1, con particolare attenzione alla citochina TNFα, il gold
Rischio infettivo meccanismo di difesa contro le infezioni
 Rischio infettivo meccanismo di difesa contro le infezioni I MECCANISMI DI DIFESA Ogni individuo possiede dei meccanismi di difesa che gli permettono di opporre una resistenza più o meno efficace nei confronti
Rischio infettivo meccanismo di difesa contro le infezioni I MECCANISMI DI DIFESA Ogni individuo possiede dei meccanismi di difesa che gli permettono di opporre una resistenza più o meno efficace nei confronti
FUNZIONE CELLULARE E TRAFFICO INTRACELLULARE
 FUNZIONE CELLULARE E TRAFFICO INTRACELLULARE Carboidrati proteine Glicolipide Regione ad a-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di membrana
FUNZIONE CELLULARE E TRAFFICO INTRACELLULARE Carboidrati proteine Glicolipide Regione ad a-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di membrana
Alberts et al., L ESSENZIALE DI BIOLOGIA MOLECOLARE DELLA CELLULA, Zanichelli editore S.p.A. Copyright 2005
 La conversione dell informazione da una forma ad un altra è il punto critico della trasmissione e prende il nome di: TRASDUZIONE DEL SEGNALE Nella comunicazione cellulare: Molecola segnale Proteina recettore
La conversione dell informazione da una forma ad un altra è il punto critico della trasmissione e prende il nome di: TRASDUZIONE DEL SEGNALE Nella comunicazione cellulare: Molecola segnale Proteina recettore
Meccanismi di difesa immunitari Risposta umorale (produzione anticorpale)
 Risposta umorale (produzione anticorpale) Tutte le proteine virali sono immunogene. Nel corso dell infezione virale vengono prodotte tutte le tipologie anticorpali: IgM, che si manifestano precocemente
Risposta umorale (produzione anticorpale) Tutte le proteine virali sono immunogene. Nel corso dell infezione virale vengono prodotte tutte le tipologie anticorpali: IgM, che si manifestano precocemente
RISPOSTA IMMUNITARIA UMORALE. Attivazione dei linfociti B e produzione degli anticorpi. dott.ssa Maria Luana Poeta
 RISPOSTA IMMUNITARIA UMORALE Attivazione dei linfociti B e produzione degli anticorpi dott.ssa Maria Luana Poeta Fasi delle risposta immunitaria adattativa Antigeni riconosciuti dai Linfociti B Risposta
RISPOSTA IMMUNITARIA UMORALE Attivazione dei linfociti B e produzione degli anticorpi dott.ssa Maria Luana Poeta Fasi delle risposta immunitaria adattativa Antigeni riconosciuti dai Linfociti B Risposta
CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA. SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte. Immunopatologia
 CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA DOCENTI Proff.ri Vera Del Gobbo (coordinatore); Roberto Testi Dott.ri Florence Malisan; Ivano Condò SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte.
CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA DOCENTI Proff.ri Vera Del Gobbo (coordinatore); Roberto Testi Dott.ri Florence Malisan; Ivano Condò SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte.
INFIAMMAZIONE ACUTA. Dott.ssa Chiara Ferranti
 INFIAMMAZIONE ACUTA Dott.ssa Chiara Ferranti FASE VASCOLARE: vasodilatazione La vasodilatazione inizia precocemente dopo lo stimolo lesivo grazie alla liberazione di mediatori vasoattivi L istamina rilasciata
INFIAMMAZIONE ACUTA Dott.ssa Chiara Ferranti FASE VASCOLARE: vasodilatazione La vasodilatazione inizia precocemente dopo lo stimolo lesivo grazie alla liberazione di mediatori vasoattivi L istamina rilasciata
SECONDI MESSAGGERI. Ca++
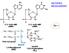 SECONDI MESSAGGERI Ca++ Recettori di membrana associati a proteine G che attivano la fosfolipasi C II messaggeri: - derivati del fosfatidil inositolo - Ca ++ Sintesi dei secondi messaggeri DAG e IP dal
SECONDI MESSAGGERI Ca++ Recettori di membrana associati a proteine G che attivano la fosfolipasi C II messaggeri: - derivati del fosfatidil inositolo - Ca ++ Sintesi dei secondi messaggeri DAG e IP dal
24 marzo 2015 IMMUNITA INNATA
 24 marzo 2015 IMMUNITA INNATA -Immunità Innata- Come Avviene il Riconoscimento di microbi Strutture molecolari condivise da classi di microbi LPS, Mannosio, RNA ds, CpG seq,, N-formil metion., Recettori
24 marzo 2015 IMMUNITA INNATA -Immunità Innata- Come Avviene il Riconoscimento di microbi Strutture molecolari condivise da classi di microbi LPS, Mannosio, RNA ds, CpG seq,, N-formil metion., Recettori
PATOLOGIA CELLULARE LESIONI LETALI
 PATOLOGIA CELLULARE LESIONI LETALI www.fisiokinesiterapia.biz DANNO CELLULARE REVERSIBILE E IRREVERSIBILE IPOSSIA/ISCHEMIA (carenza di ossigeno/insufficiente perfusione dei tessuti) AGENTI FISICI (traumi,
PATOLOGIA CELLULARE LESIONI LETALI www.fisiokinesiterapia.biz DANNO CELLULARE REVERSIBILE E IRREVERSIBILE IPOSSIA/ISCHEMIA (carenza di ossigeno/insufficiente perfusione dei tessuti) AGENTI FISICI (traumi,
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI
 Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
linfociti ISTOLOGIA UNIPG a e b, piccolo e medio linfocito (Giemsa). c, immagine al MES.
 linfociti a e b, piccolo e medio linfocito (Giemsa). c, immagine al MES. Medio e piccolo linfocita Nucleo: sferico 20-30% Granuli specifici: nessuno Pochi mesi-anni Linfocito Linfocito al MES Sopravvivenza:
linfociti a e b, piccolo e medio linfocito (Giemsa). c, immagine al MES. Medio e piccolo linfocita Nucleo: sferico 20-30% Granuli specifici: nessuno Pochi mesi-anni Linfocito Linfocito al MES Sopravvivenza:
infiammazione e tumore: obiettivo della lezione
 infiammazione e tumore: obiettivo della lezione introduzione all INFIAMMAZIONE introduzione alla TUMORIGENESI il legame tra infiammazione e cancro --- esempi oggi Fasi dell infiammazione: reclutamento
infiammazione e tumore: obiettivo della lezione introduzione all INFIAMMAZIONE introduzione alla TUMORIGENESI il legame tra infiammazione e cancro --- esempi oggi Fasi dell infiammazione: reclutamento
PROCESSO IL PROCESSO INFIAMMATORIO INFIAMMATORIO. Protagonisti. Infiammazione cronica
 IL PROCESSO INFIAMMATORIO PROCESSO INFIAMMATORIO Successione di modificazioni che avvengono in un tessuto vivente in risposta alla lesione, purché questa non sia di grado tale da distruggere la struttura
IL PROCESSO INFIAMMATORIO PROCESSO INFIAMMATORIO Successione di modificazioni che avvengono in un tessuto vivente in risposta alla lesione, purché questa non sia di grado tale da distruggere la struttura
Immunologia (2 CFU) CI Biochimica Clinica e Immunologia (coordinatore: Silvia Biocca) Ivano Condò Florence Malisan
 Immunologia (2 CFU) CI Biochimica Clinica e Immunologia (coordinatore: Silvia Biocca) Ivano Condò Florence Malisan Sito per il deposito files lezioni: http:// Testi consigliati: J.R. Regueiro Gonzales
Immunologia (2 CFU) CI Biochimica Clinica e Immunologia (coordinatore: Silvia Biocca) Ivano Condò Florence Malisan Sito per il deposito files lezioni: http:// Testi consigliati: J.R. Regueiro Gonzales
CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA. SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte. Immunopatologia
 CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA DOCENTI Proff.ri Vera Del Gobbo (coordinatore); Roberto Testi Dott.ri Florence Malisan; Ivano Condò SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte.
CORSO INTEGRATO DI IMMUNOLOGIA ED IMMUNOPATOLOGIA DOCENTI Proff.ri Vera Del Gobbo (coordinatore); Roberto Testi Dott.ri Florence Malisan; Ivano Condò SVOLGIMENTO DEL CORSO: I parte. Immunologia II parte.
Immunità umorale = immunità mediata dagli anticorpi
 Immunità umorale = immunità mediata dagli anticorpi ADCC Tre vie di attivazione del complemento 24 L attivazione del complemento avviene attraverso la proteolisi (clivaggio) sequenziale dei diversi frammenti
Immunità umorale = immunità mediata dagli anticorpi ADCC Tre vie di attivazione del complemento 24 L attivazione del complemento avviene attraverso la proteolisi (clivaggio) sequenziale dei diversi frammenti
Studio del potere interferonizzante di un vaccino IBR Marker Live
 Studio del potere interferonizzante di un vaccino IBR Marker Live Annalisa Stefani, Stefano Nardelli In collaborazione con INTRODUZIONE Per VACCINOsi intende una preparazione antigenica, costituita o dal
Studio del potere interferonizzante di un vaccino IBR Marker Live Annalisa Stefani, Stefano Nardelli In collaborazione con INTRODUZIONE Per VACCINOsi intende una preparazione antigenica, costituita o dal
IPERSENSIBILITÀ DI TIPO III O MEDIATA DA IMMUNOCOMPLESSI
 MALATTIE AUTOIMMUNI REAZIONI DI TIPO II POSSONO AVVENIRE ANCHE QUANDO LA TOLLERANZA AL SELF VIENE INTERROTTA E VENGONO PRODOTTI Ab CONTRO I TESSUTI PROPRI DELL ORGANISMO ES. AUTOANTICORPI CONTRO LE CELLULE
MALATTIE AUTOIMMUNI REAZIONI DI TIPO II POSSONO AVVENIRE ANCHE QUANDO LA TOLLERANZA AL SELF VIENE INTERROTTA E VENGONO PRODOTTI Ab CONTRO I TESSUTI PROPRI DELL ORGANISMO ES. AUTOANTICORPI CONTRO LE CELLULE
come gli altri connettivi in senso lato il sangue è un tessuto di origine mesenchimale
 come gli altri connettivi in senso lato il sangue è un tessuto di origine mesenchimale Funzioni del sangue Trasporta gas disciolti Distribuisce sostanze nutritive Trasporta i prodotti del catabolismo Consegna
come gli altri connettivi in senso lato il sangue è un tessuto di origine mesenchimale Funzioni del sangue Trasporta gas disciolti Distribuisce sostanze nutritive Trasporta i prodotti del catabolismo Consegna
IMMUNOPATOLOGIA. Antigeni omologhi che differiscono in individui delle stessa specie per il loro background genetico.
 IMMUNOPATOLOGIA Il sistema immunitario ci protegge contro sostanze estranee, invasioni microbiche e tumori, ma occasionalmente le risposte immunitarie possono anche danneggiare i tessuti dell ospite normale
IMMUNOPATOLOGIA Il sistema immunitario ci protegge contro sostanze estranee, invasioni microbiche e tumori, ma occasionalmente le risposte immunitarie possono anche danneggiare i tessuti dell ospite normale
Immunità umorale = immunità mediata dagli anticorpi ADCC
 Immunità umorale = immunità mediata dagli anticorpi ADCC 1 2 Necessari 2 segnali per attivare i linfociti B Primo segnale: BCR Secondo segnale = - Antigeni timo-dipendenti (TD):. cellule T adiuvanti (T
Immunità umorale = immunità mediata dagli anticorpi ADCC 1 2 Necessari 2 segnali per attivare i linfociti B Primo segnale: BCR Secondo segnale = - Antigeni timo-dipendenti (TD):. cellule T adiuvanti (T
Il sistema immunitario
 MASSAGGIATORE E OPERATORE DELLA SALUTE I ANNO CORSO DI IGIENE 1 Docente: Dott.ssa Tatiana Caccia Lezione n. 3 Il sistema immunitario I meccanismi di difesa di un organismo di solito avvengono in tre fasi
MASSAGGIATORE E OPERATORE DELLA SALUTE I ANNO CORSO DI IGIENE 1 Docente: Dott.ssa Tatiana Caccia Lezione n. 3 Il sistema immunitario I meccanismi di difesa di un organismo di solito avvengono in tre fasi
