Simmetria molecolare e i gruppi di simmetria puntuali. Daniele Toffoli March 21, / 87
|
|
|
- Leopoldo Fumagalli
- 4 anni fa
- Visualizzazioni
Transcript
1 Simmetria molecolare e i gruppi di simmetria puntuali Daniele Toffoli March 21, / 87
2 Outline 1 Elementi e operazioni di simmetria 2 Isomerismo ottico 3 Gruppi puntuali di simmetria I 4 Gruppi puntuali di simmetria II 5 Assegnazione sistematica del gruppo puntuale di simmetria 6 Esempi Daniele Toffoli March 21, / 87
3 Elementi e operazioni di simmetria 1 Elementi e operazioni di simmetria 2 Isomerismo ottico 3 Gruppi puntuali di simmetria I 4 Gruppi puntuali di simmetria II 5 Assegnazione sistematica del gruppo puntuale di simmetria 6 Esempi Daniele Toffoli March 21, / 87
4 Elementi e operazioni di simmetria Elementi di simmetria e operazioni di simmetria Definizioni Operazione di simmetria Operazione su un oggetto tale che l oggetto viene portato in una configurazione equivalente a quella iniziale. Indistinguibile Elemento di simmetria Entita geometrica, rispetto alla quale una o piu operazioni di simmetria possono essere definite. Asse di rotazione. Piano di simmetria. Punto (centro) di inversione. Daniele Toffoli March 21, / 87
5 Elementi e operazioni di simmetria Elementi di simmetria e operazioni di simmetria Definizioni Elementi e operazioni elemento operazione/i notazione Piano di simm. riflessione σ centro di inv. inversione rispetto al punto i Asse di rot. rot. attorno all asse C n Asse improprio rot. + rif. in un piano S n Daniele Toffoli March 21, / 87
6 Elementi e operazioni di simmetria Piani di simmetria e riflessioni Considerazioni generali Piani di simmetria Il piano deve passare attraverso l oggetto. Se il piano coincide con il piano XY: x x x y = y = y z z z Daniele Toffoli March 21, / 87
7 Elementi e operazioni di simmetria Piani di simmetria e riflessioni Considerazioni generali Piani di simmetria Atomi sul piano non vengono spostati. Atomi dello stesso tipo fuori dal piano occorrono in coppie. Se una molecola ha un solo atomo di una data specie, l atomo deve stare sull intersezione di tutti i piani di simmetria della molecola. Operazioni generate: σ 2n+1 = σ σ 2n = E Daniele Toffoli March 21, / 87
8 Elementi e operazioni di simmetria Piani di simmetria e riflessioni Esempi Molecole senza piani di simmetria: numero dispari di tutti i tipi di atomi non planari SFClO Molecole con un numero infinito di piani di simmetria: molecole lineari. Molecole con un piano di simmetria: F 2 SO, Cl 2 SO... Molecule con due piani di simmetria: H 2 O, CH 2 Cl 2 (AB 2 C 2 tetraedriche) Molecole con tre piani di simmetria: NH 3 (AB 3 piramidali, eccetto che nello stato di transizione planare) Daniele Toffoli March 21, / 87
9 Elementi e operazioni di simmetria Piani di simmetria e riflessioni Esempi Molecole con quattro piani di simmetria AB 3 planari (SO 2 3, CO 2 3, BF 3,...) Molecole con cinque piani di simmetria Sistemi planari quadrati AB 4 (PtCl 2 4, AuCl 4 ) Molecole con sei piani di simmetria Sistemi AB 4 tetraedrici: AB 1 B 2, AB 1 B 3, AB 1 B 4, AB 2 B 3, AB 2 B 4, AB 3 B 4. Daniele Toffoli March 21, / 87
10 Elementi e operazioni di simmetria Piani di simmetria e riflessioni Esempi Molecole con nove piani di simmetria Sistemi AB 6 ottaedrici. Tre piani equivalenti: AB 1 B 2 B 3 B 4, AB 2 B 4 B 5 B 6, AB 1 B 3 B 5 B 6. Sei piani equivalenti, del tipo AB 5 B 6 che biseca B 1 B 2 e B 3 B 4,... Daniele Toffoli March 21, / 87
11 Elementi e operazioni di simmetria Centro di inversione e operazione di inversione Considerazioni generali centro di inversione Se l origine coincide con il centro: x x x y = y = y z z z Solo un atomo puo essere al centro (l unico non trasformato). Tutti gli altri atomi devono occorrere in coppie. Genera due operazioni: i 2n+1 = i i 2n = E Daniele Toffoli March 21, / 87
12 Elementi e operazioni di simmetria Centro di inversione e operazione di inversione Esempi Molecole ottaedriche AB 6. Molecole planari quadrate AB 4. Molecole planari trans AB 2 C 2. Molecole lineari ABA. Etilene, Benzene. Molecole AB 4 tetraedriche non hanno un centro di inversione. Daniele Toffoli March 21, / 87
13 Elementi e operazioni di simmetria Assi di rotazione e rotazioni proprie Considerazioni generali Assi di rotazione di ordine n Il simbolo usato (anche per la corrispondente operazione) e C n. Un asse C n genera n operazioni: C n, C 2 n, C 3 n,..., C n n = E. Un numero arbitrario di atomi puo giacere sull asse Se un atomo non giace sull asse ci devono essere n-1 altri atomi dello stesso tipo. n atomi in totale (atomi in posizioni equivalenti). Daniele Toffoli March 21, / 87
14 Elementi e operazioni di simmetria Assi di rotazione e rotazioni proprie Considerazioni generali Operazioni di rotazione C 2 genera due operazioni C 2, C 2 2 =E Un asse C 3 genera tre operazioni: C 3, C 2 3 =C 1 3, C3 3 =E. Un asse C 4 genera quattro operazioni: C 4, C 2 4 =C 2, C 3 4 =C 1 4, C4 4 =E. Un asse C 6 genera sei operazioni: C 6, C 3, C 2, C 2 3, C 1 6, E. Daniele Toffoli March 21, / 87
15 Elementi e operazioni di simmetria Assi di rotazione e rotazioni proprie Esempi Molecole senza assi di rotazione: SFClO, F 2 SO, Cl 2 SO,... Molecole con un asse di rotazione C : molecole lineari (tutti gli atomi giacciono sull asse) Molecole con un asse di rotazione C 2 : H 2 O, CH 2 Cl 2,... Molecule con tre assi C 2 : Etilene, C 2 H 4, molecole AB 4 tetraedriche. Daniele Toffoli March 21, / 87
16 Elementi e operazioni di simmetria Assi di rotazione e rotazioni proprie Esempi Molecole con assi di rotazioni C 3 : Molecole AB 3 piramidali e planari. Asse passante per A e al piano dei tre B. Molecole AB 4 tetraedriche: Quattro assi C 3, passanti per i legami A B Molecole AB 6 ottaedriche: Quattro assi passanti per i centri di due facce triangolari opposte e l atomo A. Daniele Toffoli March 21, / 87
17 Elementi e operazioni di simmetria Assi di rotazione e rotazioni proprie Esempi Molecole planari AB 3 Tre assi C 2 coincidenti con i legami A B: Conseguenza della presenza di un asse C 2 all asse verticale C 3. Le operazioni relative al C 3 replicano altri elementi di simmetria. Daniele Toffoli March 21, / 87
18 Elementi e operazioni di simmetria Assi di rotazione e rotazioni proprie Esempi Molecole con assi di ordine superiore Ione PtCl 2 4 : Asse verticale C 4 al piano molecolare. Quattro assi C 2 nel piano dello ione molecolare. Anione ciclopentadienile, C 5 H 5 Asse verticale C 5. Benzene Asse di ordine 6, al piano molecolare Sei assi C 2 nel piano molecolare (due set). Daniele Toffoli March 21, / 87
19 Elementi e operazioni di simmetria Assi di rotazione e rotazioni proprie Relazioni generali con altre operazioni di simmetria Assi e piani contenenti l asse C n, n = 2, 3, 5, 7 C n, n=2: Assi e piani verticali sono portati su se stessi. C n, n=3,5,7: Vengono generati altri n-1 assi e piani verticali. Assi e piani contenenti l asse C n, n = 4, 6, 8 L esistenza di un piano verticale o asse C 2 richiede la presenza di un totale di n 2 di tali elementi. Daniele Toffoli March 21, / 87
20 Elementi e operazioni di simmetria Assi impropri e rotazioni improprie Considerazioni generali Rotazione impropria di ordine n Il simbolo usato (anche per la corrispondente operazione) e S n. L operazione avviene in due steps: Rotazione di 2π n rispetto all asse. Riflessione in un piano all asse. Esiste anche quando C n e σ h non sono elementi di simmetria dell oggetto. L ordine di C n e σ h non e importante. Daniele Toffoli March 21, / 87
21 Elementi e operazioni di simmetria Assi impropri e rotazioni improprie Considerazioni generali Molecole AB 4 tetraedriche Tre assi S 4 : Coincidenti con gli assi C 2. Daniele Toffoli March 21, / 87
22 Elementi e operazioni di simmetria Operazioni generate dall elemento S n Considerazioni generali Asse improprio di ordine pari Assumiamo C n lungo Z, σ nel piano XY: [C n, σ] = 0. Un asse improprio S n genera le operazioni S n, S 2 n, S 3 n,..., S n n. S n n=(c n σ) n =C n nσ n =E, S n+1 n =S n,... S m n =C m n quando m e pari Operazioni generate da S 6 : S 6, S 2 6, S3 6, S4 6, S5 6, S6 6 S 2 6 =C 3; S 3 6 =S 2=i; S 4 6 =C2 3 ; S6 6 =E. La presenza di S 2n richiede l esistenza di un asse C n. Daniele Toffoli March 21, / 87
23 Elementi e operazioni di simmetria Operazioni generate dall elemento S n Considerazioni generali Asse improprio di ordine dispari Richiede la presenza sia di σ h che di C n come elementi indipendenti: S n n=(c n σ) n =C n nσ n =σ. S n =C n σ, C n e anche elemento di simmetria. S n genera 2n operazioni: S 5 =C 5 σ; S 2 5 =C2 5 ; S3 5 =C3 5 σ; S4 5 =C 1 5 ; S5 5 =σ S 6 5 =C 5; S 7 5 =C2 5 σ; S8 5 =C3 5 ; S9 5 =C 1 5 σ; S10 5 =E Daniele Toffoli March 21, / 87
24 Elementi e operazioni di simmetria Prodotti di operazioni di simmetria Approccio matriciale C 2 (z)=c 2 (y)c 2 (x) C 2 (x) = C 2 (y) = C 2 (z) = C 2 (z) = = Daniele Toffoli March 21, / 87
25 Elementi e operazioni di simmetria Prodotti di operazioni di simmetria Approccio matriciale σ d =C 4 (z)σ(xz) σ(xz) = C 4 (z) = σ d = σ d = = Daniele Toffoli March 21, / 87
26 Elementi e operazioni di simmetria Prodotti di operazioni di simmetria Approccio matriciale C 2 =C 4(z)C 2 (y) C 2 (y) = C 4 (z) = C 2 = C 2 = = Daniele Toffoli March 21, / 87
27 Elementi e operazioni di simmetria Prodotti di operazioni di simmetria Approccio matriciale C 2 (z)σ(xy)=σ(xy)c 2 (z)=i C 2 (z) = σ(xy) = i = i = = Daniele Toffoli March 21, / 87
28 Elementi e operazioni di simmetria Elementi di simmetria equivalenti e atomi equivalenti Elementi di simmetria equivalenti Elementi che sono tra loro relazionati da operazioni di simmetria del gruppo puntuale. Esempio: Molecola trigonale planare AB 3 I tre assi C 2 sono tra loro relazionati da rotazioni C 3 e C 2 3. I tre assi C 2 sono equivalenti. I tre piani verticali sono equivalenti: Intersecano il piano molecolare lungo gli assi C 2. Relazionati tra loro dalle rotazioni C 3 e C 2 3. Daniele Toffoli March 21, / 87
29 Elementi e operazioni di simmetria Elementi di simmetria equivalenti e atomi equivalenti Elementi di simmetria equivalenti Esempio: AB 4 planare quadrata Possiede quattro assi C 2 nel piano molecolare: C 2 e C 2 : assi B A B. C 2 e C 2 bisecano gli angoli BAB. Possiede quattro piani di simmetria verticali: Intersecano σ h lungo gli assi C 2. C 2 e C 2 sono equivalenti (per rotazione C 4). C 2 e C 2 sono equivalenti tra loro. C 2 e C 2 non sono elementi equivalenti. I piani verticali sono equivalenti a coppie: {σ v, σ v } e {σ d, σ d }. Daniele Toffoli March 21, / 87
30 Elementi e operazioni di simmetria Elementi di simmetria equivalenti e atomi equivalenti Elementi di simmetria equivalenti I tre piani σ v in AB 3 (sia planare che trigonale piramidale) sono equivalenti: NH 3, BF 3,... I due piani σ v in H 2 O non sono equivalenti. I sei assi C 2 nel piano molecolare del Benzene non sono tutti equivalenti: Assi C 2 che bisecano legami C C opposti. Assi C 2 che passano per C opposti. I sei piani σ v non sono tra loro equivalenti. Daniele Toffoli March 21, / 87
31 Elementi e operazioni di simmetria Elementi di simmetria equivalenti e atomi equivalenti Set di atomi equivalenti Appartengono necessariamente alla stessa specie chimica. Sono scambiati tra loro a seguito di una qualsiasi operazione di simmetria del gruppo puntuale. Esempi Tutti gli atomi di H in CH 4, C 6 H 6, C 2 H 4, ciclopropano,... Tutti gli atomi di F in SF 6. Tutti gli atomi di C in Cr(CO) 6. Tutti gli atomi di O in Cr(CO) 6. I tre atomi di F in posizione equatoriale in PF 5. I due atomi di F in posizione assiale in PF 5. Daniele Toffoli March 21, / 87
32 Elementi e operazioni di simmetria Elementi di simmetria e operazioni Principi generali Prodotti Il prodotto di due rotazioni proprie e una rotazione propria (gruppo delle rotazioni). Il prodotto di due riflessioni in piani A e B che si intersecano ad un angolo φ AB e equivalente a una rotazione attorno all asse di intersezione, di un angolo 2φ AB. Esistono quindi in totale n = 2π 2φ AB piani verticali. Dati C n e un piano verticale, esistono n di questi piani, separati di un angolo φ = 2π 2n. Un asse C n con n pari e un piano σ C n richiedono l esistenza di i: C2n n σ = σc 2n n = C 2σ = σc 2 = i C2n n i = ic 2n n = C 2i = ic 2 = σ. Daniele Toffoli March 21, / 87
33 Elementi e operazioni di simmetria Elementi di simmetria e operazioni Principi generali Prodotti Il prodotto di due rotazioni C 2 rispetto a due assi C 2 che si intersecano ad un angolo θ, e una rotazione rispetto ad un asse al piano degli assi C 2 di un angolo 2θ. Daniele Toffoli March 21, / 87
34 Elementi e operazioni di simmetria Elementi di simmetria e operazioni Principi generali Regole di commutazione Due rotazioni rispetto allo stesso asse: C k n C l n = C (k+l) n Riflessioni rispetto a piani perpendicolari: σ(xy)σ(yz) = σ(yz)σ(xy) ˆσ(xy) = ˆσ(yz) = ˆσ(xy)ˆσ(yz) = = C 2 (y) Daniele Toffoli March 21, / 87
35 Elementi e operazioni di simmetria Elementi di simmetria e operazioni Principi generali Regole di commutazione Inversione e ogni riflessione o rotazione Due rotazioni C 2 attorno ad assi perpendicolari: C 2 (x)c 2 (y) = C 2 (y)c 2 (x) Ĉ 2 (x) = Ĉ 2 (y) = Ĉ 2 (x)ĉ 2 (y) = = C 2 (z) Rotazione e riflessione in un piano all asse di rotazione. Daniele Toffoli March 21, / 87
36 Isomerismo ottico 1 Elementi e operazioni di simmetria 2 Isomerismo ottico 3 Gruppi puntuali di simmetria I 4 Gruppi puntuali di simmetria II 5 Assegnazione sistematica del gruppo puntuale di simmetria 6 Esempi Daniele Toffoli March 21, / 87
37 Isomerismo ottico Isomerismo ottico Generalita Operazioni generatrici Ogni operazione di simmetria puo essere espressa in termini di rotazioni proprie o improprie: σ = Eσ = C 1 1 σ = S 1 i = S 2 Supponiamo σ = σ(xy) e C 2 =C 2 (z) ˆσ(xy)Ĉ2(z) = = = î Daniele Toffoli March 21, / 87
38 Isomerismo ottico Molecole dissimmetriche Definizione e proprieta Molecole dissimmetriche vs asimmetriche Molecole asimmetriche: molecole che non posseggono elementi di simmetria (gruppo puntuale C 1 ) Molecole dissimmetriche: molecole non sovrapponibili alla loro immagine speculare. Tutte le molecole asimmetriche sono dissimmetriche. La proposizione inversa non e necessariamente vera. Condizione necessaria e sufficiente: Molecole dissimmetriche non hanno elementi di simmetria S n. Daniele Toffoli March 21, / 87
39 Isomerismo ottico Isomerismo ottico Molecole dissimmetriche non hanno elementi di simmetria S n Proposizione inversa Se esiste un asse S n la molecola non puo essere dissimmetrica. Se esiste S n di ordine dispari, allora σ e un elemento di simmetria. Se esiste S n di ordine pari e σ non esiste indipendentemente: S n = C n σ = C 1 n S n = C 1 C n σ = σ n Una rotazione non puo cambiare la struttura, ma riorienta solamente la molecola. Daniele Toffoli March 21, / 87
40 Isomerismo ottico Isomerismo ottico Molecole dissimmetriche non hanno elementi di simmetria S n Proposizione diretta Se la molecola non e dissimmetrica, esiste un asse S n. L immagine speculare deve essere prodotta dalle operazioni di simmetria del gruppo. Non possono essere semplici rotazioni proprie = operazioni S n. Assi S n con n dispari generano una operazione di riflessione. Asse S 2 : S 2 = C 2 σ = i = σ = C2 1 i Ĉ2 1 (z)î = = = ˆσ(xy) Daniele Toffoli March 21, / 87
41 Isomerismo ottico Isomerismo ottico Molecole dissimmetriche non hanno elementi di simmetria S n Molecole con assi S 2 non sono dissimmetriche Daniele Toffoli March 21, / 87
42 Isomerismo ottico Isomerismo ottico Molecole dissimmetriche non hanno elementi di simmetria S n Proposizione diretta Se la molecola non e dissimmetrica, esiste un asse S n. Asse S 4 : S 4 = C 4 σ = σ = C4 1 S Ĉ4 1 (z)ŝ 4 = = = ˆσ(xy) Daniele Toffoli March 21, / 87
43 Isomerismo ottico Isomerismo ottico Molecole dissimmetriche non hanno elementi di simmetria S n Molecole con assi S 4 non sono dissimmetriche 1,3,5,7-tetrametilcicloottatetraene. Daniele Toffoli March 21, / 87
44 Gruppi puntuali di simmetria I 1 Elementi e operazioni di simmetria 2 Isomerismo ottico 3 Gruppi puntuali di simmetria I 4 Gruppi puntuali di simmetria II 5 Assegnazione sistematica del gruppo puntuale di simmetria 6 Esempi Daniele Toffoli March 21, / 87
45 Gruppi puntuali di simmetria I L insieme soddisfa gli assiomi di Daniele gruppo. Toffoli March 21, / 87 Gruppi di simmetria puntuali Generalita Set completi di operazioni di simmetria Per una data molecola, possiamo compilare una lista di tutte le operazioni di simmetria compatibili con gli elementi di simmetria molecolare Molecola planare AB 3 E,C 3, C 1 3, C 2, C 2, C 2, σ v, σ v, σ v, σ h, S 3, S 2 3. Questo insieme e chiuso rispetto all operazione di moltiplicazione (composizione) di operazioni.
46 Gruppi puntuali di simmetria I Gruppi di simmetria puntuali Generalita Set completi di operazioni di simmetria L operazione E esiste in ogni set. La moltiplicazione (composizione) di operazioni e associativa Ogni operazione possiede un inversa: σ 1 = σ, i 1 = i (C m n ) 1 =C n m n L operazione S m n possiede sempre un inversa: n m inv. p p S (n m) n p d S (n m) n d p C (n m) n d d S (2n m) n Daniele Toffoli March 21, / 87
47 Gruppi puntuali di simmetria I Gruppi di simmetria puntuali Notazione per i gruppi puntuali: simboli di Schönflies Gruppi senza assi di rotazione propri o impropri Gruppo C 1 : {E} Nessun elemento di simmetria: molecole asimmetriche. Gruppo C s : {E, σ}. σ come unico elemento di simmetria. Gruppo C i : {E, i}. i come unico elemento di simmetria. Daniele Toffoli March 21, / 87
48 Gruppi puntuali di simmetria I Gruppi di simmetria puntuali Notazione per i gruppi puntuali: simboli di Schönflies Gruppi con un asse di rotazione proprio o improprio Gruppo C n : {C n, Cn 2,..., Cn n 1, E} C n come unico elemento di simmetria. Gruppo ciclico (abeliano) di ordine n. Gruppo S n (n > 2 pari): {S n, C n, S 3 2 n,..., Sn n 1, E}. Consiste di n operazioni, includendo quelle generate da C n Gruppo C nh (S n, n dispari) Consiste di 2n operazioni, includendo quelle generate da C n e σ h. 2. Daniele Toffoli March 21, / 87
49 Gruppi puntuali di simmetria I Gruppi di simmetria puntuali Notazione per i gruppi puntuali: simboli di Schönflies Gruppi con due o piu elementi di simmetria Gruppo D n Asse C n e n assi C 2 a C n. Gruppo di ordine 2n: {C n, C 2 n,..., E} e le n rotazioni C 2. Gruppo C nh Consiste di 2n operazioni, ottenute aggiungendo all asse verticale C n un piano σ h. n operazioni aggiuntive: {Eσ h, C n σ h S n,..., C m n σ h,...} C m n σ h =σ h C m n. Gruppo C nv n dispari: set di n piani σ v equivalenti. n pari: set di n 2 piani equivalenti σ v e n 2 piani σ d (piani diedri). Daniele Toffoli March 21, / 87
50 Gruppi puntuali di simmetria I Gruppi di simmetria puntuali Notazione per i gruppi puntuali: simboli di Schönflies Gruppo D nh : ottenuto aggiungendo σ h a D n σ h C n origina n 1 (n pari) operazioni S m n (incl. C n ). 2 σ h C n origina n 1 (n dispari) operazioni S m n. σ h C 2 =C 2 σ h =σ v che contiene C 2 : Ĉ 2 (x)ˆσ h = = = σ(xz) σ h C 2 =σ v = C 2 =σ h σ v C n, σ h, n(σ v ) sono anche generatori. E, n-1 C m n, n C 2, n σ v, n-1 rotazioni improprie, σ h (4n elementi). Daniele Toffoli March 21, / 87
51 Gruppi puntuali di simmetria I Gruppi di simmetria puntuali Notazione per i gruppi puntuali: simboli di Schönflies Gruppo D nd : ottenuto aggiungendo nσ d a D n σ d : piani diedri, bisecano coppie di assi C 2. n operazioni generate da prodotti del tipo σ d C 2. Operazioni generate da asse S 2n collineare con C n. 4n elementi (operazioni) in totale. Daniele Toffoli March 21, / 87
52 Gruppi puntuali di simmetria I Gruppi di simmetria puntuali Notazione per i gruppi puntuali: simboli di Schönflies Gruppi delle molecole lineari: C v e D h Asse molecolare e asse C piani verticali σ v Molecole che possiedono un centro di inversione: Del tipo A B A (A atomo o gruppo di atomi) Elementi di simmetria addizionali sono i, σ h, C 2 all asse molecolare e che passano per il centro. Gruppo D h. Molecole senza centro di inversione: Del tipo A B C. Non ci sono altri elementi di simmetria Gruppo C v. Daniele Toffoli March 21, / 87
53 Gruppi puntuali di simmetria II 1 Elementi e operazioni di simmetria 2 Isomerismo ottico 3 Gruppi puntuali di simmetria I 4 Gruppi puntuali di simmetria II 5 Assegnazione sistematica del gruppo puntuale di simmetria 6 Esempi Daniele Toffoli March 21, / 87
54 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Solidi platonici Sono le simmetrie dei poliedri convessi regolari (gli assi di simmetria sono alle loro facce) Tetraedro: quattro facce triangolari: quattro assi C 3 che si intersecano nel centro del solido. I cinque poliedri convessi regolari Hanno le seguenti caratteristiche: Le facce (equivalenti) sono poligoni regolari. I vertici sono equivalenti. I lati sono equivalenti. Daniele Toffoli March 21, / 87
55 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Solidi platonici I poliedri convessi regolari sono al massimo 5 In un vertice del poliedro devono convergere almeno tre poligoni regolari non coplanari (Somma degli angoli < 360 ). Tre triangoli equilateri. Quattro triangoli equilateri. tetraedro ottaedro Daniele Toffoli March 21, / 87
56 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Solidi platonici I poliedri convessi regolari sono al massimo 5 Cinque triangoli equilateri. Tre quadrati. icosaedro cubo Daniele Toffoli March 21, / 87
57 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Solidi platonici I poliedri convessi regolari sono al massimo 5 Tre pentagoni. dodecaedro Daniele Toffoli March 21, / 87
58 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Tetraedro Elementi e operazioni di simmetria Tre assi S 4 coincidenti con gli assi x, y, z. Operazioni generate: S 4, S 2 4 =C 2, S 3 4. Tre assi C 2 collineari con gli assi S 4. Quattro assi C 3. Operazioni generate: C 3, C 2 3 =C 1 3. Tetraedro inscritto in un cubo Daniele Toffoli March 21, / 87
59 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Tetraedro Elementi e operazioni di simmetria Sei piani σ d. Gruppo T d. 24 operazioni (raggruppate in classi): E, 8C 3,3C 2,6S 4, 6σ d Tetraedro inscritto in un cubo Daniele Toffoli March 21, / 87
60 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Ottaedro Elementi e operazioni di simmetria Tre assi S 4 passanti per vertici opposti. Operazioni generate: S 4, S 2 4 =C 2, S 3 4. Tre assi C 2 collineari con gli assi S 4. Tre assi C 4 collineari con gli assi S 4 e C 2. Operazioni generate: C 4, C 2 4 =C 2, C 3 4 Sei assi C 2 che bisecano lati opposti. Operazioni generate: C 2. Ottaedro Daniele Toffoli March 21, / 87
61 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Ottaedro Elementi e operazioni di simmetria Quattro assi S 6 passanti per coppie di facce opposte. Operazioni generate: S 6, C 3 S 3 6 =i, C 1 3, S5 6. Quattro assi C 3 collineari con gli assi S 6. Centro di inversione, i. Tre piani di simmetria σ h che passano per quattro vertici. Operazioni generate: σ h. Ottaedro Daniele Toffoli March 21, / 87
62 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Ottaedro Elementi e operazioni di simmetria 6 piani σ d che passano per coppie di vertici opposti e bisecano coppie di lati opposti. Operazioni generate: σ d. Gruppo O h. 48 operazioni (raggruppate in classi): E, 8C 3,6C 4,6C 2, 3C 2 (=C 2 4 ),i, 6S 4, 8S 6, 3σ h, 6σ d Ottaedro Daniele Toffoli March 21, / 87
63 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Cubo Gruppo O h come tutti i solidi transizionali Cubo: facce penetrate da assi C 4 e vertici da assi C 3. Ottaedro: facce penetrate da assi C 3 e vertici da assi C 4. Daniele Toffoli March 21, / 87
64 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Dodecaedro e icosaedro Elementi e operazioni di simmetria Sei assi S 10 Dodecaedro: passanti per coppie opposte di facce pentagonali. Icosaedro: passanti per vertici opposti. Operazioni generate: S 10, S 2 10 =C 5, S 3 10, S4 10 =C2 5, S5 10 =i, S6 10 =C3 5, S7 10, S 8 10 =C4 5,S9 10, E. Daniele Toffoli March 21, / 87
65 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Dodecaedro e icosaedro Elementi e operazioni di simmetria Dieci assi S 6 Dodecaedro: passanti per coppie opposte di vertici. Icosaedro: passanti per coppie opposte di facce. Operazioni generate: S 6, S 2 6 =C 3, S 3 6 =i, S4 6 =C2 3, S5 6. Daniele Toffoli March 21, / 87
66 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Dodecaedro e icosaedro Elementi e operazioni di simmetria Sei assi C 5 collineari con gli assi S 10. Dieci assi C 3 collineari con gli assi S 6 Quindici assi C 2 che bisecano lati opposti. Operazioni generate: C 2. Quindici piani σ: Ogniuno contiene 2C 2 e 2C 5. Daniele Toffoli March 21, / 87
67 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Dodecaedro e icosaedro Elementi e operazioni di simmetria Gruppo I h. 120 operazioni (raggruppate in classi): E, 12C 5, 12C 2 5, 20C 3, 15C 2, i, 12S 10, 12S 3 10, 20S 6, 15σ Daniele Toffoli March 21, / 87
68 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Sottogruppi rotazionali puri di T d, O h, I h Gruppi T, O, I Prodotti di rotazioni sono rotazioni. Ottenuti rimuovendo da T d, O h, I h, le operazioni di riflessione e di rotazioni improprie. Gruppo T operazioni (raggruppate in classi): E, 4C 3, 4C 2 3, 3C 2 Gruppo O operazioni (raggruppate in classi): E, 8C 3,6C 4,6C 2, 3C 2 (=C 2 4 ) Gruppo I operazioni (raggruppate in classi): E, 12C 5, 12C 2 5, 20C 3, 15C 2 Daniele Toffoli March 21, / 87
69 Gruppi puntuali di simmetria II Simmetrie con piu assi di ordine elevato Gruppo T h Operazioni Ottenuto aggiungendo un set di piani σ h che contengono gli assi C 2. operazioni (raggruppate in classi): E, 4C 3, 4C 2 3, 3C 2, i, 4S 6, 4S 5 6, 3σ h Daniele Toffoli March 21, / 87
70 Assegnazione sistematica del gruppo puntuale di simmetria 1 Elementi e operazioni di simmetria 2 Isomerismo ottico 3 Gruppi puntuali di simmetria I 4 Gruppi puntuali di simmetria II 5 Assegnazione sistematica del gruppo puntuale di simmetria 6 Esempi Daniele Toffoli March 21, / 87
71 Assegnazione sistematica del gruppo puntuale di simmetria Classificazione del gruppo puntuale di una molecola Procedura sistematica 1 Gruppi delle molecole lineari (C v o D h ), o gruppi con piu assi di ordine superiore (gruppi speciali): quattro assi C 3 : T, T h, T d, O, O h dieci assi C 3 : I sei assi C 5 : I h 2 Non ci sono assi di rotazione propria o impropria. piano di simmetria: gruppo C s centro di inversione: gruppo C i. Nessun elemento: gruppo C 1. 3 Esiste un asse di rotazione impropria di ordine pari, S n, n = 4, 6, 8. Nessun piano di simmetria o assi di rotazione propri non relazionati a S n : gruppo S n. Solo operazioni generate da S n. Relativamente raro. Daniele Toffoli March 21, / 87
72 Assegnazione sistematica del gruppo puntuale di simmetria Classificazione del gruppo puntuale di una molecola Procedura sistematica 4 Esiste C n (asse verticale), ma non n C 2 : Non ci sono altri elementi di simmetria: gruppo C n Esistono n σ v : gruppo C nv Esiste σ h : gruppo C nh 5 Esiste C n (asse verticale) con n C 2 : Non ci sono altri elementi di simmetria: gruppo D n Esiste σ h : gruppo D nh ( nσ v ) Esistono n σ d : gruppo D nd Daniele Toffoli March 21, / 87
73 Assegnazione sistematica del gruppo puntuale di simmetria Classificazione del gruppo puntuale di una molecola Procedura sistematica Daniele Toffoli March 21, / 87
74 Esempi 1 Elementi e operazioni di simmetria 2 Isomerismo ottico 3 Gruppi puntuali di simmetria I 4 Gruppi puntuali di simmetria II 5 Assegnazione sistematica del gruppo puntuale di simmetria 6 Esempi Daniele Toffoli March 21, / 87
75 Esempi Esempi H 2O Gruppo C 2v 1 Non ci sono assi di rotazione S n. 2 1 asse di rotazione propria C 2 : Sul piano molecolare Passa per O e biseca la linea H H. 3 2 σ contengono l asse C 2 : Il piano molecolare. Il piano che passa per O e biseca la linea H H Daniele Toffoli March 21, / 87
76 Esempi Esempi NH 3 Gruppo C 3v 1 Non ci sono assi di rotazione S n. 2 1 asse di rotazione propria C 3 : Passa per l atomo di N al piano dei tre H. 3 C 3 all intersezione di 3 σ v : Ogni σ v contiene N e un legame N H. Daniele Toffoli March 21, / 87
77 Esempi Esempi allene Gruppo D 2d 1 Asse di rotazione S 4 : Coincide con l asse molecolare (asse C 2 verticale). 2 Due assi C 2 ortogonali all asse verticale C 2 (Gruppo di tipo D). 3 Non ci sono assi di rotazione C n con n > 2. 4 Non ci sono piani σ h 5 2 piani di simmetria verticali. Daniele Toffoli March 21, / 87
78 Esempi Esempi H 2O 2 Configurazione di equilibrio non planare: gruppo C 2. 1 Non ci sono assi di rotazione S n. 2 1 asse verticale C 2. 3 Non ci sono piani di simmetria 4 Ulteriori elementi di simmetria: θ = 0 : configurazione cis-planare. θ = 90 : configurazione trans-planare. Daniele Toffoli March 21, / 87
79 Esempi Esempi H 2O 2 Configurazione cis-planare: gruppo C 2v. 1 Non ci sono assi di rotazione S n. 2 1 asse verticale C piani di simmetria verticali mutuamente ortogonali: Piano molecolare. Piano che biseca la linea H H. Daniele Toffoli March 21, / 87
80 Esempi Esempi H 2O 2 Configurazione trans-planare: gruppo C 2h. 1 Non ci sono assi di rotazione S n. 2 1 asse verticale C 2. 3 Non ci sono piani di simmetria verticali. 4 1 σ h (piano della molecola). Daniele Toffoli March 21, / 87
81 Esempi Esempi Cicloottatetraene Gruppo D 2d. 1 1 asse di rotazione impropria S asse di rotazione C 2 coincidente con S 4. 3 Non possiede assi C n con n > assi C 2 al C 2 verticale (gruppo di tipo D 2 ). 5 2 piani di simmetria verticali: bisecano coppie di doppi legami e angoli tra i C 2. Daniele Toffoli March 21, / 87
82 Esempi Esempi 1,3,5,7-Tetrametilcicloottatetraene Gruppo S asse di rotazione impropria S 4. 2 Non esistono altri elementi di simmetria. I gruppi metilici abbassano la simmetria del sistema. Daniele Toffoli March 21, / 87
83 Esempi Esempi Benzene Gruppo D 6h. 1 1 asse di rotazione impropria S 6, ortogonale al piano dell anello. 2 Altri elementi di simmetria: Asse di rotazione propria C 6, coincidente con S 6. 6 assi C 2 nel piano dell anello. 1 σ h (il piano molecolare). Centro di inversione (il centro dell anello). 3 piani verticali (passano per vertici opposti). 3 piani diedri (passano per legami C C opposti). Daniele Toffoli March 21, / 87
84 Esempi Esempi PF 5 (trigonale bipiramidale) Gruppo D 3h. 1 I legami P F eq. sono tra loro equiv. 2 I legami P F ass. sono tra loro equiv. 3 1 asse di rotazione C 3, al piano eq. Asse F ass P F ass. 4 Altri elementi di simmetria: 3 assi C 2 (legami P F equat.). 3 piani di simmetria verticali. 1 piano σ h (il piano equat.). Daniele Toffoli March 21, / 87
85 Esempi Esempi Ferrocene (Configurazione staggered) Gruppo D 5d. 1 Asse di rotazione impropria di ordine dispari, S Asse di rotazione propria C 5, coincidente con S assi C piani di simmetria verticali (passano tra gli assi C 2 ). Daniele Toffoli March 21, / 87
86 Esempi Esempi Ferrocene (Configurazione eclissata) Gruppo D 5h. 1 Non possiede assi di rotazione impropria. 2 Asse di rotazione propria C assi C piani di simmetria verticali (passano tra gli assi C 2 ). 5 1 piano σ h. Daniele Toffoli March 21, / 87
87 Esempi Esempi Ferrocene (altre configurazioni) Gruppo D 5 1 Non possiede assi di rotazione impropria. 2 1 asse di rotazione propria C assi C 2. 4 Non possiede piani di simmetria verticali. 5 Non possiede un piano σ h Daniele Toffoli March 21, / 87
Corso di Chimica Inorganica II (A-L) Laurea Triennale in Chimica (L-27) GRUPPO: insieme di elementi correlati dalle seguenti regole:
 APPUNTI DI TEORIA DEI GRUPPI Corso di Chimica Inorganica II (A-L) Laurea Triennale in Chimica (L-27) Dr. Andrea G. Marrani DEFINIZIONI GRUPPO: insieme di elementi correlati dalle seguenti regole: 1) PRODOTTO
APPUNTI DI TEORIA DEI GRUPPI Corso di Chimica Inorganica II (A-L) Laurea Triennale in Chimica (L-27) Dr. Andrea G. Marrani DEFINIZIONI GRUPPO: insieme di elementi correlati dalle seguenti regole: 1) PRODOTTO
CHIMICA FISICA III (Modulo A)
 CHIMICA FISICA III (Modulo A) Prof. Giovanna Fronzoni, Dipartimento di Scienze Chimiche e Farmaceutiche fronzoni@units.it Testi consigliati : P. Atkins, J. De Paula : Chimica Fisica (per la parte generale
CHIMICA FISICA III (Modulo A) Prof. Giovanna Fronzoni, Dipartimento di Scienze Chimiche e Farmaceutiche fronzoni@units.it Testi consigliati : P. Atkins, J. De Paula : Chimica Fisica (per la parte generale
Simmetria Molecolare
 Simmetria Molecolare Chimica Generale ed Inorganica Chimica Inorganica 1 prof. Dario Duca simmetria: artefatti e natura elemento di simmetria operazione di simmetria piano di riflessione riflessione elementi
Simmetria Molecolare Chimica Generale ed Inorganica Chimica Inorganica 1 prof. Dario Duca simmetria: artefatti e natura elemento di simmetria operazione di simmetria piano di riflessione riflessione elementi
Lavoro di Gruppo - III
 Lavoro di Gruppo - III Fulvio Bisi 1 Anna Torre 1 1 Dipartimento di Matematica - Università di Pavia Stage Orientamento 2016-16 giugno Bisi-Torre (Dip. Mate UniPV) Lavoro di Gruppo III Stage 16 giu 2016
Lavoro di Gruppo - III Fulvio Bisi 1 Anna Torre 1 1 Dipartimento di Matematica - Università di Pavia Stage Orientamento 2016-16 giugno Bisi-Torre (Dip. Mate UniPV) Lavoro di Gruppo III Stage 16 giu 2016
1. SIMMETRIA. 1.1 Operazioni ed elementi di simmetria puntuale
 1. SIMMETRIA Molte proprietà molecolari sono determinate dalla simmetria delle molecole stesse, come del resto molte proprietà dei solidi sono determinate dalla simmetria del loro reticolo cristallino.
1. SIMMETRIA Molte proprietà molecolari sono determinate dalla simmetria delle molecole stesse, come del resto molte proprietà dei solidi sono determinate dalla simmetria del loro reticolo cristallino.
Gli esercizi assegnati all esame saranno varianti di alcuni degli esercizi seguenti
 Gli esercizi assegnati all esame saranno varianti di alcuni degli esercizi seguenti 1.1) Su un piano α (trasparente) sia tracciato un triangolo equilatero. Si consideri un piano β parallelo ad α e raggi
Gli esercizi assegnati all esame saranno varianti di alcuni degli esercizi seguenti 1.1) Su un piano α (trasparente) sia tracciato un triangolo equilatero. Si consideri un piano β parallelo ad α e raggi
DIEDRI. Un diedro è convesso se è una figura convessa, concavo se non lo è.
 DIEDRI Si definisce diedro ciascuna delle due parti di spazio delimitate da due semipiani che hanno la stessa origine, compresi i semipiani stessi. I due semipiani prendono il nome di facce del diedro
DIEDRI Si definisce diedro ciascuna delle due parti di spazio delimitate da due semipiani che hanno la stessa origine, compresi i semipiani stessi. I due semipiani prendono il nome di facce del diedro
Geometria molecolare
 Geometria molecolare Le molecole possono essere rappresentate disponendo gli atomi in posizioni definite nello spazio in modo da costruire una figura geometrica Il modo più semplice per assegnare la geometria
Geometria molecolare Le molecole possono essere rappresentate disponendo gli atomi in posizioni definite nello spazio in modo da costruire una figura geometrica Il modo più semplice per assegnare la geometria
Le simmetrie dei poliedri regolari
 Le simmetrie dei poliedri regolari Le isometrie del piano e dello spazio sono state classificate da due illustri matematici. Per quanto riguarda il piano, il teorema di Chasles, del 8, afferma che nel
Le simmetrie dei poliedri regolari Le isometrie del piano e dello spazio sono state classificate da due illustri matematici. Per quanto riguarda il piano, il teorema di Chasles, del 8, afferma che nel
Introduzione alla Simmetria Molecolare
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Introduzione alla Simmetria Molecolare Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Introduzione alla Simmetria Molecolare Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Simmetrie nei Poliedri Regolari
 Simmetrie nei Poliedri Regolari Francesca Benanti Dipartimento di Matematica ed Informatica Università degli Studi di Palermo, Via Archirafi 34, 90123 Palermo Tel: 09123891105 Email: fbenanti@math.unipa.it
Simmetrie nei Poliedri Regolari Francesca Benanti Dipartimento di Matematica ed Informatica Università degli Studi di Palermo, Via Archirafi 34, 90123 Palermo Tel: 09123891105 Email: fbenanti@math.unipa.it
LA GEOMETRIA DELLO SPAZIO: CENNI DI TEORIA ED ESERCIZI
 LA GEOMETRIA DELLO SPAZIO: CENNI DI TEORIA ED ESERCIZI SPAZIO: l insieme di tutti i punti. PUNTI ALLINEATI: punti che appartengono alla stessa retta PUNTI COMPLANARI: punti che appartengono allo stesso
LA GEOMETRIA DELLO SPAZIO: CENNI DI TEORIA ED ESERCIZI SPAZIO: l insieme di tutti i punti. PUNTI ALLINEATI: punti che appartengono alla stessa retta PUNTI COMPLANARI: punti che appartengono allo stesso
Geometria euclidea dello spazio Presentazione n. 5 Poliedri Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia
 Geometria euclidea dello spazio Presentazione n. 5 Poliedri Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia Poliedri Un poliedro è un solido delimitato da una superficie formata da
Geometria euclidea dello spazio Presentazione n. 5 Poliedri Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia Poliedri Un poliedro è un solido delimitato da una superficie formata da
Prisma retto. Generatrice. Direttrice. Prisma obliquo. Nel caso le generatrici non siano parallele. Generatrice
 Oggetti (identificati) nello spazio Una porzione di piano delimitata da una linea spezzata chiusa si chiama poligono, un solido delimitato da un numero finito di facce piane si chiama poliedro. In un poliedro
Oggetti (identificati) nello spazio Una porzione di piano delimitata da una linea spezzata chiusa si chiama poligono, un solido delimitato da un numero finito di facce piane si chiama poliedro. In un poliedro
Formule di Lewis e geometria molecolare
 Formule di Lewis e geometria molecolare Formalismo simbolico di Lewis Rappresentazione degli elettroni di valenza; permette di seguire gli elettroni di valenza durante la formazione di un legame Consiste
Formule di Lewis e geometria molecolare Formalismo simbolico di Lewis Rappresentazione degli elettroni di valenza; permette di seguire gli elettroni di valenza durante la formazione di un legame Consiste
METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA. Lezione n 12
 METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA Lezione n 12 PARTE SECONDA GEOMETRIA SOLIDA UNA PREMESSA Diversi esperti di Didattica della Matematica ritengono che l approccio migliore, per la
METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA Lezione n 12 PARTE SECONDA GEOMETRIA SOLIDA UNA PREMESSA Diversi esperti di Didattica della Matematica ritengono che l approccio migliore, per la
I solidi. Un solido è una parte di spazio delimitata da una superficie chiusa. I solidi delimitati da poligoni vengono chiamati poliedri.
 I solidi Un solido è una parte di spazio delimitata da una superficie chiusa. I solidi delimitati da poligoni vengono chiamati poliedri. I solidi che hanno superfici curve vengono chiamati solidi rotondi.
I solidi Un solido è una parte di spazio delimitata da una superficie chiusa. I solidi delimitati da poligoni vengono chiamati poliedri. I solidi che hanno superfici curve vengono chiamati solidi rotondi.
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici. Capitolo 10
 Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
Applicazioni della teoria dei gruppi alla simmetria molecolare
 Università degli studi di Padova Scuola di Scienze Progetto Lauree Scientifiche Applicazioni della teoria dei gruppi alla simmetria molecolare Alessia Trovò Enrico Nale Andrea Sabatino Prof. Riccardo Colpi
Università degli studi di Padova Scuola di Scienze Progetto Lauree Scientifiche Applicazioni della teoria dei gruppi alla simmetria molecolare Alessia Trovò Enrico Nale Andrea Sabatino Prof. Riccardo Colpi
Piano Lauree Scientifiche - Progetto Archimede. Dai poliedri platonici ai poliedri archimedei per espansione
 Piano Lauree Scientifiche - Progetto Archimede Dai poliedri platonici ai poliedri archimedei per espansione Consideriamo il quadrato verde AEHD faccia del cubo ABCDEFGH. Vogliamo traslare questa faccia
Piano Lauree Scientifiche - Progetto Archimede Dai poliedri platonici ai poliedri archimedei per espansione Consideriamo il quadrato verde AEHD faccia del cubo ABCDEFGH. Vogliamo traslare questa faccia
Previsione delle geometrie molecolari (Cap. 8)
 Previsione delle geometrie molecolari (Cap. 8) La forma delle molecole La teoria VSEPR Previsione della geometria molecolare Momento di dipolo di molecole poliatomiche Isomeria Ordine di legame 6 0 La
Previsione delle geometrie molecolari (Cap. 8) La forma delle molecole La teoria VSEPR Previsione della geometria molecolare Momento di dipolo di molecole poliatomiche Isomeria Ordine di legame 6 0 La
APPUNTI DI GEOMETRIA SOLIDA
 APPUNTI DI GEOMETRIA SOLIDA Geometria piana: (planimetria) studio delle figure i cui punti stanno tutti su un piano Geometria solida: (stereometria) studio delle figure i cui punti non giacciono tutti
APPUNTI DI GEOMETRIA SOLIDA Geometria piana: (planimetria) studio delle figure i cui punti stanno tutti su un piano Geometria solida: (stereometria) studio delle figure i cui punti non giacciono tutti
IL GRUPPO SO(3) , b a a R 2φ g R 1. a 2 + b 2 e i2φ N. Valendo a 2 + b 2 = 1, abbiamo dunque tr(r 2φ g R 1. Se diagonalizziamo R 2φ g R 1.
 IL GRUPPO SO3). Semplicità di SO3) Usando l omomorfismo suriettivo ρ : SU2) SO3) che abbiamo già descritto, possiamo dimostrare che SO3) è un gruppo semplice. In effetti, per far questo ci basta mostrare
IL GRUPPO SO3). Semplicità di SO3) Usando l omomorfismo suriettivo ρ : SU2) SO3) che abbiamo già descritto, possiamo dimostrare che SO3) è un gruppo semplice. In effetti, per far questo ci basta mostrare
1. conoscere i concetti fondamentali della geometria sintetica del piano (poligoni, circonferenza
 Terzo modulo: Geometria Obiettivi 1. conoscere i concetti fondamentali della geometria sintetica del piano (poligoni, circonferenza e cerchio, ecc.). calcolare perimetri e aree di figure elementari nel
Terzo modulo: Geometria Obiettivi 1. conoscere i concetti fondamentali della geometria sintetica del piano (poligoni, circonferenza e cerchio, ecc.). calcolare perimetri e aree di figure elementari nel
un legame covalente due legami covalenti? tre legami covalenti due legami covalenti un legame covalente
 e C N un legame covalente due legami covalenti? tre legami covalenti O F Ne 1s 2s 2p due legami covalenti un legame covalente C 1s 2s 2p ibridazione quattro legami covalenti Cariche Formali Usando le strutture
e C N un legame covalente due legami covalenti? tre legami covalenti O F Ne 1s 2s 2p due legami covalenti un legame covalente C 1s 2s 2p ibridazione quattro legami covalenti Cariche Formali Usando le strutture
Come vedere la matematica in ciò che ci circonda
 1/46 Come vedere la matematica in ciò che ci circonda Savona 19 Dicembre 2001 2/46 2/46 2/46 2/46 2/46 2/46 3/46 Sono entrambi parti di un paraboloide Un paraboloide si ottiene facendo ruotare una parabola
1/46 Come vedere la matematica in ciò che ci circonda Savona 19 Dicembre 2001 2/46 2/46 2/46 2/46 2/46 2/46 3/46 Sono entrambi parti di un paraboloide Un paraboloide si ottiene facendo ruotare una parabola
Poliedri regolari. - Le condizioni (a), (b) e (c) della definizione data non sono sovrabbondanti: Riferimenti bibliografici: (a) e (c) non (b)
 Riferimenti bibliografici: Poliedri regolari - Forme Maria Dedò Ed. Zanichelli - Le condizioni (a), (b) e (c) della definizione data non sono sovrabbondanti: (a) e (c) non (b) Definizione: Un poliedro
Riferimenti bibliografici: Poliedri regolari - Forme Maria Dedò Ed. Zanichelli - Le condizioni (a), (b) e (c) della definizione data non sono sovrabbondanti: (a) e (c) non (b) Definizione: Un poliedro
CONCETTO DI GRUPPO QP= R
 http://www. TEORIA DEI GRUPPI (prima parte) CONCETTO DI GRUPPO In linea generale, possiamo definire un "gruppo" come un insieme di elementi fra di loro in relazione mediante alcune regole ben determinate.
http://www. TEORIA DEI GRUPPI (prima parte) CONCETTO DI GRUPPO In linea generale, possiamo definire un "gruppo" come un insieme di elementi fra di loro in relazione mediante alcune regole ben determinate.
Definizione Chiamiamo poliedro la regione di spazio limitata che ha per bordo una superficie poliedrale.
 1 Poliedri Definizione Un sottoinsieme connesso dello spazio è detto superficie poliedrale se è l unione di un numero finito di poligoni P j (poligoni che si diranno facce del poliedro) in modo che risultino
1 Poliedri Definizione Un sottoinsieme connesso dello spazio è detto superficie poliedrale se è l unione di un numero finito di poligoni P j (poligoni che si diranno facce del poliedro) in modo che risultino
Piano Lauree Scientifiche - Progetto Archimede. Costruzione di poliedri SCHEDA 4
 Piano Lauree Scientifiche - Progetto Archimede Costruzione di poliedri SCHEDA 4 Espansione di un cubo Consideriamo il quadrato verde AEHD faccia del cubo ABCDEFGH. Vogliamo traslare questa faccia esternamente
Piano Lauree Scientifiche - Progetto Archimede Costruzione di poliedri SCHEDA 4 Espansione di un cubo Consideriamo il quadrato verde AEHD faccia del cubo ABCDEFGH. Vogliamo traslare questa faccia esternamente
La FORMA delle MOLECOLE
 La FORMA delle MOLECOLE Quando una molecola è costituita da due soli atomi, non vi è alcun dubbio sulla sua forma: gli atomi sono semplicemente disposti uno accanto all altro. Le molecole formate da tre
La FORMA delle MOLECOLE Quando una molecola è costituita da due soli atomi, non vi è alcun dubbio sulla sua forma: gli atomi sono semplicemente disposti uno accanto all altro. Le molecole formate da tre
Rette e piani nello spazio
 Geometria Euclidea Solida 1 Rette e piani nello spazio Sappiamo già che il punto, la retta ed il piano sono enti geometrici primitivi e, come tali, non sono definibili. Definizione : Dicesi spazio l insieme
Geometria Euclidea Solida 1 Rette e piani nello spazio Sappiamo già che il punto, la retta ed il piano sono enti geometrici primitivi e, come tali, non sono definibili. Definizione : Dicesi spazio l insieme
I poliedri SMS E. MAJORANA ROMA CLASSI 3F 3 H
 I poliedri SMS E. MAJORANA ROMA CLASSI 3F 3 H Cosa è un poliedro? Definizioni: Un poliedro è la parte di spazio delimitata da poligoni posti su piani diversi in modo tale che ogni lato sia comune a due
I poliedri SMS E. MAJORANA ROMA CLASSI 3F 3 H Cosa è un poliedro? Definizioni: Un poliedro è la parte di spazio delimitata da poligoni posti su piani diversi in modo tale che ogni lato sia comune a due
GEOMETRIA MOLECOLARE. Ibridazione La teoria VSEPR
 GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
Forme molecolari - Teoria VSEPR Teoria della repulsione dei doppietti elettronici di valenza
 Lezione 8 1. Teoria VSEPR 2. Il legame chimico 3. Legame covalente - Valence Bond 4. Legami e 5. Sovrapposizione di orbitali atomici 6. Intro IBRIDAZIONE Forme molecolari - Teoria VSEPR Teoria della repulsione
Lezione 8 1. Teoria VSEPR 2. Il legame chimico 3. Legame covalente - Valence Bond 4. Legami e 5. Sovrapposizione di orbitali atomici 6. Intro IBRIDAZIONE Forme molecolari - Teoria VSEPR Teoria della repulsione
GEOMETRIA. Studio dei luoghi /relazioni tra due variabili. Studio delle figure (nel piano/spazio) Problemi algebrici sulle figure geometriche
 GEOMETRIA ANALITICA EUCLIDEA Studio dei luoghi /relazioni tra due variabili Studio delle figure (nel piano/spazio) Funzioni elementari Problemi algebrici sulle figure geometriche Grafici al servizio dell
GEOMETRIA ANALITICA EUCLIDEA Studio dei luoghi /relazioni tra due variabili Studio delle figure (nel piano/spazio) Funzioni elementari Problemi algebrici sulle figure geometriche Grafici al servizio dell
Metodi basati sulla meccanica quantistica
 Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
ISTITUTO SAN GABRIELE CLASSI 4 S - 4 SA PROF. ANDREA PUGLIESE GEOMETRIA EUCLIDEA NELLO SPAZIO
 ISTITUTO SAN GABRIELE CLASSI 4 S - 4 SA PROF. ANDREA PUGLIESE GEOMETRIA EUCLIDEA NELLO SPAZIO GEOMETRIA NELLO SPAZIO Gli enti fondamentali sono punto, retta, piano, e spazio. Con le lettere maiuscole (A,B,C,...)
ISTITUTO SAN GABRIELE CLASSI 4 S - 4 SA PROF. ANDREA PUGLIESE GEOMETRIA EUCLIDEA NELLO SPAZIO GEOMETRIA NELLO SPAZIO Gli enti fondamentali sono punto, retta, piano, e spazio. Con le lettere maiuscole (A,B,C,...)
GEOMETRIA MOLECOLARE
 GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
Metodi basati sulla meccanica quantistica
 Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Esercizi sulle Geometrie Molecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
GEOMETRIA MOLECOLARE. La struttura di Lewis non fornisce alcuna indicazione sulla forma delle molecole in
 GEOMETRIA MOLECOLARE La struttura di Lewis non fornisce alcuna indicazione sulla forma delle molecole in quanto dipende dagli ANGOLI DI LEGAME cioè gli angoli tra le linee che congiungono i nuclei degli
GEOMETRIA MOLECOLARE La struttura di Lewis non fornisce alcuna indicazione sulla forma delle molecole in quanto dipende dagli ANGOLI DI LEGAME cioè gli angoli tra le linee che congiungono i nuclei degli
Teoria dei gruppi. Daniele Toffoli. June 5, 2017
 Teoria dei gruppi Daniele Toffoli June 5, 017 1 Definizione di gruppo Consideriamo un set G di elementi distinti G = {G 1, G,, G g }. L insieme G è detto costituire un gruppo, se sono soddisfatti i seguenti
Teoria dei gruppi Daniele Toffoli June 5, 017 1 Definizione di gruppo Consideriamo un set G di elementi distinti G = {G 1, G,, G g }. L insieme G è detto costituire un gruppo, se sono soddisfatti i seguenti
CONVITTO NAZIONALE CARLO ALBERTO Scuole annesse: Primaria Secondaria I grado Liceo Scientifico
 CONVITTO NAZIONALE CARLO ALBERTO Scuole annesse: Primaria Secondaria I grado Liceo Scientifico Baluardo Partigiani n 6 28100 - Novara Tel. 0321/620047 - Fax. 0321/620622 Email: novc010008@istruzione.it
CONVITTO NAZIONALE CARLO ALBERTO Scuole annesse: Primaria Secondaria I grado Liceo Scientifico Baluardo Partigiani n 6 28100 - Novara Tel. 0321/620047 - Fax. 0321/620622 Email: novc010008@istruzione.it
Le sezioni piane del cubo
 Le sezioni piane del cubo Versione provvisoria 11 dicembre 006 1 Simmetrie del cubo e sezioni speciali Sezioni speciali si presentano in corrispondenza di piani perpendicolari agli assi di simmetria del
Le sezioni piane del cubo Versione provvisoria 11 dicembre 006 1 Simmetrie del cubo e sezioni speciali Sezioni speciali si presentano in corrispondenza di piani perpendicolari agli assi di simmetria del
1 Congruenza diretta e inversa
 1 Congruenza diretta e inversa PROPRIETÀ. La congruenza tra due figure piane mantiene inalterata la lunghezza dei segmenti e l ampiezza degli angoli; ciò che cambia è la posizione delle figure nel piano.
1 Congruenza diretta e inversa PROPRIETÀ. La congruenza tra due figure piane mantiene inalterata la lunghezza dei segmenti e l ampiezza degli angoli; ciò che cambia è la posizione delle figure nel piano.
Esercizi sulle Geometrie Molecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Geometria euclidea. Alessio del Vigna. Lunedì 15 settembre
 Geometria euclidea Alessio del Vigna Lunedì 15 settembre La geometria euclidea è una teoria fondata su quattro enti primitivi e sulle relazioni che tra essi intercorrono. I quattro enti primitivi in questione
Geometria euclidea Alessio del Vigna Lunedì 15 settembre La geometria euclidea è una teoria fondata su quattro enti primitivi e sulle relazioni che tra essi intercorrono. I quattro enti primitivi in questione
Geometria euclidea. Alessio del Vigna
 Geometria euclidea Alessio del Vigna La geometria euclidea è una teoria fondata su quattro enti primitivi e sulle relazioni che tra essi intercorrono. I quattro enti primitivi in questione sono il punto,
Geometria euclidea Alessio del Vigna La geometria euclidea è una teoria fondata su quattro enti primitivi e sulle relazioni che tra essi intercorrono. I quattro enti primitivi in questione sono il punto,
Simmetria nei cristalli
 Simmetria nei cristalli Un operazione di simmetria lascia invariato un cristallo, ovvero il cristallo trasformato è sovrapponibile al cristallo originario. Tali operazioni possono essere classificate in
Simmetria nei cristalli Un operazione di simmetria lascia invariato un cristallo, ovvero il cristallo trasformato è sovrapponibile al cristallo originario. Tali operazioni possono essere classificate in
Geometria nello spazio
 Geometria nello spazio Def. Lo spazio è l insieme di infiniti elementi A, B, C detti punti; esso è dotato di sottoinsiemi non vuoti a, b, c detti rette e α, β, γ detti piani.. POSTULATI DI INCIDENZA. Dati
Geometria nello spazio Def. Lo spazio è l insieme di infiniti elementi A, B, C detti punti; esso è dotato di sottoinsiemi non vuoti a, b, c detti rette e α, β, γ detti piani.. POSTULATI DI INCIDENZA. Dati
Teoria VSEPR Geometria molecolare
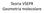 Teoria VSEPR Geometria molecolare la teoria VSEPR la forma delle molecole Massima distanza possibile! Teoria della repulsione delle coppie di elettroni di valenza VSEPR Struttura delle molecole Le regioni
Teoria VSEPR Geometria molecolare la teoria VSEPR la forma delle molecole Massima distanza possibile! Teoria della repulsione delle coppie di elettroni di valenza VSEPR Struttura delle molecole Le regioni
Lezione introduttiva allo studio della GEOMETRIA SOLIDA
 Lezione introduttiva allo studio della GEOMETRIA SOLIDA Geometria solida Lo spazio euclideo è un insieme infinito di elementi detti punti e contiene sottoinsiemi propri ed infiniti : le rette e i piani..
Lezione introduttiva allo studio della GEOMETRIA SOLIDA Geometria solida Lo spazio euclideo è un insieme infinito di elementi detti punti e contiene sottoinsiemi propri ed infiniti : le rette e i piani..
IBRIDAZIONE e GEOMETRIA MOLECOLARE
 IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
Laboratorio di informatica
 Laboratorio di informatica GEOMETRIA DELLO SPAZIO Introduzione a Geogebra 3D La versione 5 di Geogebra prevede anche la possibilità di lavorare in ambiente 3D. Basta aprire Visualizza - Grafici 3D: sullo
Laboratorio di informatica GEOMETRIA DELLO SPAZIO Introduzione a Geogebra 3D La versione 5 di Geogebra prevede anche la possibilità di lavorare in ambiente 3D. Basta aprire Visualizza - Grafici 3D: sullo
Elementi di strutturistica cristallina III
 Chimica fisica superiore Modulo 1 Elementi di strutturistica cristallina III Sergio Brutti Reticoli tri-dimensionali Consideriamo nuovamente i 14 reticoli di Bravais Basi cristalline Analogamente che al
Chimica fisica superiore Modulo 1 Elementi di strutturistica cristallina III Sergio Brutti Reticoli tri-dimensionali Consideriamo nuovamente i 14 reticoli di Bravais Basi cristalline Analogamente che al
Le cupole geodetiche
 Le cupole geodetiche Una cupola geodetica é una struttura semisferica composta da aste che si intersecano in triangoli. Dal punto di vista matematico possiamo definire cupola geodetica un tipo di triangolazione
Le cupole geodetiche Una cupola geodetica é una struttura semisferica composta da aste che si intersecano in triangoli. Dal punto di vista matematico possiamo definire cupola geodetica un tipo di triangolazione
Indice. Parte prima Metodi. XI Gli autori
 XI Gli autori XIII Prefazione Parte prima Metodi 5 Capitolo 1 Elementi di geometria proiettiva 5 1.1 Gli enti geometrici 6 1.2 Convenzioni 7 1.3 L operazione di proiezione 9 1.4 L ampliamento proiettivo
XI Gli autori XIII Prefazione Parte prima Metodi 5 Capitolo 1 Elementi di geometria proiettiva 5 1.1 Gli enti geometrici 6 1.2 Convenzioni 7 1.3 L operazione di proiezione 9 1.4 L ampliamento proiettivo
I N F I N I T I T R I A N G O L I. (Tk) D I T A R T A G L I A. (possibili applicazioni in geometria (k + 2) - dimensionale)
 I N F I N I T I T R I A N G O L I (Tk) D I T A R T A G L I A (possibili applicazioni in geometria (k + 2) - dimensionale) Gruppo B. Riemann * Francesco Di Noto, Michele Nardelli *Gruppo amatoriale per
I N F I N I T I T R I A N G O L I (Tk) D I T A R T A G L I A (possibili applicazioni in geometria (k + 2) - dimensionale) Gruppo B. Riemann * Francesco Di Noto, Michele Nardelli *Gruppo amatoriale per
Esame di Stato di Liceo Scientifico Corso di Ordinamento
 Corso di Ordinamento Soluzione dei Temi di Matematica proposti nella Sessione Ordinaria 006 Sessione Ordinaria 006 Corso di Ordinamento Sommario Problema Punto a) Punto b) Punto c) Punto Finale 4 Problema
Corso di Ordinamento Soluzione dei Temi di Matematica proposti nella Sessione Ordinaria 006 Sessione Ordinaria 006 Corso di Ordinamento Sommario Problema Punto a) Punto b) Punto c) Punto Finale 4 Problema
IBRIDAZIONE. MODELLO DELL ORBITALE di LEGAME
 IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
Punti, linee e piani nello spazio
 Punti, linee e piani nello spazio DEFINIZIONE. La geometria dello spazio o geometria dei solidi o ancora geometria solida è il settore della geometria che si occupa dei corpi a tre dimensioni (lunghezza,
Punti, linee e piani nello spazio DEFINIZIONE. La geometria dello spazio o geometria dei solidi o ancora geometria solida è il settore della geometria che si occupa dei corpi a tre dimensioni (lunghezza,
Regola di Wade. Figura 3.39 Struttura del cluster [Ru 6 (CO) 18
 Regola di Wade Figura 3.39 Struttura del cluster [Ru 6 (CO) 18 18 ] 2- Regola di Wade Gruppo 6 Gruppo 7 Gruppo 8 Gruppo 9 Gruppo 10 Cr, Mo, W Mn, Tc, Re Fe, Ru Os Co, Rh, Ir Ni, Pd, Pt M(CO) 2-2 -1 0 1
Regola di Wade Figura 3.39 Struttura del cluster [Ru 6 (CO) 18 18 ] 2- Regola di Wade Gruppo 6 Gruppo 7 Gruppo 8 Gruppo 9 Gruppo 10 Cr, Mo, W Mn, Tc, Re Fe, Ru Os Co, Rh, Ir Ni, Pd, Pt M(CO) 2-2 -1 0 1
Simmetria e Teoria dei Gruppi Prodotti di operazioni di simmetria
 Prodotti di operazioni di simmetria H O C, σ v, σ v C σ v σ v σ v C = σ v Tavola di moltiplicazione Il prodotto di due operazioni di simmetria è un operazione di simmetria a operazione Simmetria e Teoria
Prodotti di operazioni di simmetria H O C, σ v, σ v C σ v σ v σ v C = σ v Tavola di moltiplicazione Il prodotto di due operazioni di simmetria è un operazione di simmetria a operazione Simmetria e Teoria
Simmetrie nei poliedri
 Simmetrie nei poliedri Livello scolare: 1 biennio Abilità interessate Individuare e riconoscere nel mondo reale le figure. geometriche note e descriverle con la terminologia specifica. Analizzare con strumenti
Simmetrie nei poliedri Livello scolare: 1 biennio Abilità interessate Individuare e riconoscere nel mondo reale le figure. geometriche note e descriverle con la terminologia specifica. Analizzare con strumenti
La Teoria del Legame di Valenza
 La Teoria del Legame di Valenza Un legame covalente tra due atomi A e B viene spiegato in termini di sovrapposizione tra due orbitali atomici appartenenti ai due atomi e descrittivi dei due elettroni di
La Teoria del Legame di Valenza Un legame covalente tra due atomi A e B viene spiegato in termini di sovrapposizione tra due orbitali atomici appartenenti ai due atomi e descrittivi dei due elettroni di
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria :
 Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
I vertici e i lati di ogni poligono vengono detti rispettivamente vertici e spigoli del poliedro.
 1 I poliedri diagonale DEFINIZIONE. Un poliedro è la parte di spazio delimitata da poligoni posti su piani diversi in modo tale che ogni lato sia comune a due di essi. I poligoni che delimitano il poliedro
1 I poliedri diagonale DEFINIZIONE. Un poliedro è la parte di spazio delimitata da poligoni posti su piani diversi in modo tale che ogni lato sia comune a due di essi. I poligoni che delimitano il poliedro
IBRIDAZIONE. Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale.
 IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
LA GEOMETRIA DELLO SPAZIO
 LA GEOMETRIA ELLO SPAZIO 1 alcola l area e il perimetro del triangolo individuato dai punti A ; 0; 4, ; 1; 5 e 0; ;. ( ) ( ) ( ) 9 ; + 6 Stabilisci se il punto A ( 1;1; ) appartiene all intersezione dei
LA GEOMETRIA ELLO SPAZIO 1 alcola l area e il perimetro del triangolo individuato dai punti A ; 0; 4, ; 1; 5 e 0; ;. ( ) ( ) ( ) 9 ; + 6 Stabilisci se il punto A ( 1;1; ) appartiene all intersezione dei
DEL LEGAME DI VALENZA
 Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata TEORIA DEL LEGAME DI VALENZA Teoria del
Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata TEORIA DEL LEGAME DI VALENZA Teoria del
Stereochimica di alcani e cicloalcani. Stereochimica. Conformazioni, conformeri
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
Prontuario di geometria euclidea nello spazio. Per la scuola secondaria di I grado
 Prontuario di geometria euclidea nello spazio Per la scuola secondaria di I grado N. B. Gli argomenti presentati sono una sintesi di quelli trattati in classe e non sostituiscono ma integrano il libro
Prontuario di geometria euclidea nello spazio Per la scuola secondaria di I grado N. B. Gli argomenti presentati sono una sintesi di quelli trattati in classe e non sostituiscono ma integrano il libro
DIDATTICA DELLA GEOMETRIA Lezione n 3
 DIDATTICA DELLA GEOMETRIA Lezione n 3 PERCORSI NELLA GEOMETRIA SOLIDA LA RELAZIONE DI EULERO f+v=s+2 Possiamo fare un po di algebra con la Geometria solida! Quanti vertici ha un prisma a base triangolare?
DIDATTICA DELLA GEOMETRIA Lezione n 3 PERCORSI NELLA GEOMETRIA SOLIDA LA RELAZIONE DI EULERO f+v=s+2 Possiamo fare un po di algebra con la Geometria solida! Quanti vertici ha un prisma a base triangolare?
Quando si parla di diedro tra due semipiani, si intende. quello convesso (che non contiene il prolungamento. sono paralleli i rispettivi piani
 Diedri Siano dati due semipiani nello spazio, α e β, aventi per origine la stessa retta r. Essi dividono lo spazio in due regioni, ciascuna delle quali si chiama diedro. I due semipiani sono le facce del
Diedri Siano dati due semipiani nello spazio, α e β, aventi per origine la stessa retta r. Essi dividono lo spazio in due regioni, ciascuna delle quali si chiama diedro. I due semipiani sono le facce del
Elementi di Euclide. Libro II. Algebra Geometrica. Proposizione 4: (x + y) 2 = x 2 + 2xy + y 2.
 PAS 2014 GEOMETRIA Programma di massima: Elementi di logica elementare. La geometria degli Elementi di Euclide. De nizioni, assiomi e postulati. La geometria del triangolo. Criteri di uguaglianza. Teorema
PAS 2014 GEOMETRIA Programma di massima: Elementi di logica elementare. La geometria degli Elementi di Euclide. De nizioni, assiomi e postulati. La geometria del triangolo. Criteri di uguaglianza. Teorema
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Le Proprietà Periodiche degli Elementi
 Le Proprietà Periodiche degli Elementi Il Legame Chimico Energia nel sistema biatomico. Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame
Le Proprietà Periodiche degli Elementi Il Legame Chimico Energia nel sistema biatomico. Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame
GEOMETRIA NELLO SPAZIO
 pag. 1 GEOMETRIA NELLO SPAZIO 1. Sintesi geometria piana Il punto, ente privo di dimensioni La retta, ente con una sola dimensione Il piano, ente con due dimensioni a) Punto e retta sul piano Per un punto
pag. 1 GEOMETRIA NELLO SPAZIO 1. Sintesi geometria piana Il punto, ente privo di dimensioni La retta, ente con una sola dimensione Il piano, ente con due dimensioni a) Punto e retta sul piano Per un punto
Negli esercizi che seguono ci sono alcune cose da specificare:
 DISCLAIMER Negli esercizi che seguono ci sono alcune cose da specificare: ) voi dovete interpretare i simboli V e A (R) sempre come R. Questo oggetto sarà chiamato alle volte piano affine e alle volte
DISCLAIMER Negli esercizi che seguono ci sono alcune cose da specificare: ) voi dovete interpretare i simboli V e A (R) sempre come R. Questo oggetto sarà chiamato alle volte piano affine e alle volte
Completa la seguente tabella. 2/2/2019 terze - Documenti Google
 2/2/2019 terze - Documenti Google Completa la seguente tabella https://docs.google.com/document/d/1mfhzgafma4qvlhpwxed95bcgzl35z-_la1ksibjkeye/edit 1/9 2/2/2019 terze - Documenti Google https://docs.google.com/document/d/1mfhzgafma4qvlhpwxed95bcgzl35z-_la1ksibjkeye/edit
2/2/2019 terze - Documenti Google Completa la seguente tabella https://docs.google.com/document/d/1mfhzgafma4qvlhpwxed95bcgzl35z-_la1ksibjkeye/edit 1/9 2/2/2019 terze - Documenti Google https://docs.google.com/document/d/1mfhzgafma4qvlhpwxed95bcgzl35z-_la1ksibjkeye/edit
Le figure solide. Due rette nello spaio si dicono sghembe se non sono complanari e non hanno alcun punto in comune.
 Le figure solide Nozioni generali Un piano nello spazio può essere individuato da: 1. tre punti A, B e C non allineati. 2. una retta r e un punto A non appartenente ad essa. 3. due rette r e s incidenti.
Le figure solide Nozioni generali Un piano nello spazio può essere individuato da: 1. tre punti A, B e C non allineati. 2. una retta r e un punto A non appartenente ad essa. 3. due rette r e s incidenti.
PNI 2006 QUESITO 1. Che la somma dei primi 64 termini della progressione geometrica di ragione 2 e primo termine 1. Tale somma vale: QUESITO 2
 www.matefilia.it La somma dei chicchi di grano è data da: PNI 2006 QUESITO 1 S = 1 + 2 + 2 2 + 2 + + 2 Che la somma dei primi 64 termini della progressione geometrica di ragione 2 e primo termine 1. Tale
www.matefilia.it La somma dei chicchi di grano è data da: PNI 2006 QUESITO 1 S = 1 + 2 + 2 2 + 2 + + 2 Che la somma dei primi 64 termini della progressione geometrica di ragione 2 e primo termine 1. Tale
CAPITOLO 4 STRUTTURE MOLECOLARI
 APITL 4 STRUTTURE MLELARI 4.1 (a) Di seguito è mostrata la struttura di Lewis di P 3. Nella teoria VSEPR il numero di coppie di elettroni attorno all atomo centrale è fondamentale per determinare la struttura.
APITL 4 STRUTTURE MLELARI 4.1 (a) Di seguito è mostrata la struttura di Lewis di P 3. Nella teoria VSEPR il numero di coppie di elettroni attorno all atomo centrale è fondamentale per determinare la struttura.
VIAGGIO NELLA (A)SIMMETRIA. La visione di un chimico : Simmetria e rottura di simmetria nelle molecole
 VIAGGIO NELLA (A)SIMMETRIA La visione di un chimico : Simmetria e rottura di simmetria nelle molecole CHE COSA E LA SIMMETRIA? 1 Corrispondenza precisa di forma o di posizione tra tutti gli elementi di
VIAGGIO NELLA (A)SIMMETRIA La visione di un chimico : Simmetria e rottura di simmetria nelle molecole CHE COSA E LA SIMMETRIA? 1 Corrispondenza precisa di forma o di posizione tra tutti gli elementi di
D. 1 Il prodotto di a = 12,37 e b = 25,45
 Settembre 005 Aritmetica D. Il prodotto di a =,7 e b = 5,45 A 4, 867 B 4, 65 C 45, 650 D 4, 865 E 4, 8655 D. L inverso del numero numero: A 5 B 5 + 5 C + 5 D E D. I numeri 5 è il,4,5,0,00, si ordinano
Settembre 005 Aritmetica D. Il prodotto di a =,7 e b = 5,45 A 4, 867 B 4, 65 C 45, 650 D 4, 865 E 4, 8655 D. L inverso del numero numero: A 5 B 5 + 5 C + 5 D E D. I numeri 5 è il,4,5,0,00, si ordinano
CHIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO. energia superiore. energia inferiore. orbitale s
 CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
1 Punti, linee e piani nello spazio
 1 Punti, linee e piani nello spazio DEFINIZIONE. La geometria dello spazio o geometria dei solidi o ancora geometria solida è il settore della geometria che si occupa dei corpi a tre dimensioni (lunghezza,
1 Punti, linee e piani nello spazio DEFINIZIONE. La geometria dello spazio o geometria dei solidi o ancora geometria solida è il settore della geometria che si occupa dei corpi a tre dimensioni (lunghezza,
Scuole italiane all estero (Calendario australe) 2007 Suppletiva QUESITO 1
 www.matefilia.it Scuole italiane all estero (Calendario australe) 2007 Suppletiva QUESITO 1 Si vuole che delle due radici dell equazione x 2 + 2(h + 1)x + m 2 h 2 = 0 una risulti doppia dell altra. Quale
www.matefilia.it Scuole italiane all estero (Calendario australe) 2007 Suppletiva QUESITO 1 Si vuole che delle due radici dell equazione x 2 + 2(h + 1)x + m 2 h 2 = 0 una risulti doppia dell altra. Quale
A T T E N Z I O N E. Ministero dell Istruzione, dell Università e della Ricerca
 Pag. 1/5 Sessione suppletiva 01 $$$$$..1/1 Seconda prova scritta *$$$$$1115* *$$$$$1115* *$$$$$1115* *$$$$$1115* A T T E N Z I O N E Il plico relativo a questa prova contiene due temi: il primo destinato
Pag. 1/5 Sessione suppletiva 01 $$$$$..1/1 Seconda prova scritta *$$$$$1115* *$$$$$1115* *$$$$$1115* *$$$$$1115* A T T E N Z I O N E Il plico relativo a questa prova contiene due temi: il primo destinato
Maturità Scientifica 2014 Problema 1 Corso di Ordinamento. Problema 1
 Maturità Scientifica Problema Corso di Ordinamento Problema Pagina di Maturità Scientifica Problema Corso di Ordinamento dal grafico Γ della funzione integrale ( ) ( ) g = f t dt dobbiamo dedurre le principali
Maturità Scientifica Problema Corso di Ordinamento Problema Pagina di Maturità Scientifica Problema Corso di Ordinamento dal grafico Γ della funzione integrale ( ) ( ) g = f t dt dobbiamo dedurre le principali
SPAZIO E FIGURE: ROMPIAMO LE SCATOLE
 SPAZIO E FIGURE: ROMPIAMO LE SCATOLE 1) Procurati una scatola vuota e bada che sia richiusa bene. Apri i lati necessari ad ottenere il suo sviluppo. Quanti lati è necessario aprire come minimo? 2) Lavora
SPAZIO E FIGURE: ROMPIAMO LE SCATOLE 1) Procurati una scatola vuota e bada che sia richiusa bene. Apri i lati necessari ad ottenere il suo sviluppo. Quanti lati è necessario aprire come minimo? 2) Lavora
piastrelle piastrelle piastrelle
 Perché le celle delle api hanno una struttura esagonale regolare? Università delle Liberetà 2008 09 appunti di marinella bassi 1 2 Il tessuto di molti vegetali e il pigmento della retina nei nostri occhi
Perché le celle delle api hanno una struttura esagonale regolare? Università delle Liberetà 2008 09 appunti di marinella bassi 1 2 Il tessuto di molti vegetali e il pigmento della retina nei nostri occhi
FIGURE SOLIDE OSSERVANDO LE FIGURE DELLO SPAZIO CHE CI CIRCONDANO NOTIAMO CHE:
 FIGURE SOLIDE OSSERVANDO LE FIGURE DELLO SPAZIO CHE CI CIRCONDANO NOTIAMO CHE: IL CUBO IL PARALLELEPIPEDO LA PIRAMIDE HANNO LA SUPERFICIE COSTITUITA DA POLIGONI (QUADRATO, RETTANGOLO, TRIANGOLO) E PRENDONO
FIGURE SOLIDE OSSERVANDO LE FIGURE DELLO SPAZIO CHE CI CIRCONDANO NOTIAMO CHE: IL CUBO IL PARALLELEPIPEDO LA PIRAMIDE HANNO LA SUPERFICIE COSTITUITA DA POLIGONI (QUADRATO, RETTANGOLO, TRIANGOLO) E PRENDONO
LA MATEMATICA DEI POLIEDRI REGOLARI
 LA MATEMATICA DEI POLIEDRI REGOLARI Essi simbolizzano il desiderio di Armonia e di ordine dell uomo, ma nello stesso tempo la loro perfezione desta in noi il senso della nostra impotenza. I poliedri regolari
LA MATEMATICA DEI POLIEDRI REGOLARI Essi simbolizzano il desiderio di Armonia e di ordine dell uomo, ma nello stesso tempo la loro perfezione desta in noi il senso della nostra impotenza. I poliedri regolari
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR)
 TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta della struttura elettronica delle molecole, come quella
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta della struttura elettronica delle molecole, come quella
