ESR, RISONANZA DI SPIN ELETTRONICA
|
|
|
- Modesto Pozzi
- 7 anni fa
- Visualizzazioni
Transcript
1 ESR, RISONANZA DI SPIN ELETTRONICA La tecnica ESR, anche detta EPR risonanza paragnetica elettronica, misura la dose di radiazione nucleare ricevuta dal campione alla stessa stregua della TL, anche se la terminologia è storicamente diversa. Per la TL si usa di solito parlare di PALEODOSE, mentre per la ESR si parla di dose accumulata, AD, o dose totale, TD. Anche in questo caso l età è data dal rapporto tra la dose accumulata e la dose annuale: età =(dose accumulata)/ (dose annuale). Anche per l ESR il tempo zero corrisponde al momento della crescita del cristallo. L ESR misura direttamente il numero di elettroni intrappolati, senza bisogno di svuotare le trappole come nel caso di TL o OSL. Centro di colore nel cloruro di sodio
2 PRINCIPIO FISICO DELL ESR L elettrone ha una proprietà intrinseca chiamata SPIN. Lo spin ha due stati possibili legati alla sua orientazione rispetto ad un generico asse nello spazio. Può essere orientato parallelamente o anti-parallelamente, spin su o spin giù. Questi due stati diversi determinano molte proprietà di atomi e molecole. Nell atomo di elio ci sono due elettroni con spin antiparalleli nello stesso stato elettronico energeticamente più basso, lo stato 1s. Il principio di Pauli è la proprietà degli elettroni di dover occupare stati diversi. Nello stato 1s ci possono essere solo due elettroni, uno con spin su, uno con spin giù. Un terzo elettrone, nell atomo di Litio, deve quindi occupare uno stato diverso, lo stato 2s che si trova a più alta energia. E in questo modo che spieghiamo la struttura della tavola periodica degli elementi: uno stato s può contenere 2 elettroni, uno stato p ne può contenere 6, uno stato d ne può contenere 10, etc.
3 Effetto Zeeman, ESR In un atomo, l orbita elettronica è descritta, dal numero quantico principale n, associato all energia, e dai numeri quantici l, m l, associati al momento angolare e alla sua componente lungo un asse prefissato. Essendo l elettrone carico, a questo moto orbitale sarà associato un momento di dipolo magnetico orbitale che tenderà ad orientarsi in presenza di un campo magnetico, esterno. Un effetto simile si ha per lo spin dell elettrone a cui è associato un momento di dipolo magnetico intrinseco che pure lui tende a orientarsi in un campo magnetico esterno. L energia degli stati dipende dall orientazione di orbita e spin rispetto al campo magnetico, i livelli si separano e la riga della transizione elettromagnetica (alle frequenze Vis-UV) tra una coppia di stati si divide in più righe: effetto Zeeman.
4 L effetto Zeeman osserva quindi una struttura fine nelle righe di assorbimento o luminescenza che si hanno per transizioni ottiche tra due stati elettronici lontani in energia. Si parla di struttura fine perché la separazione tra i livelli magnetici è molto inferiore alla separazione dei due livelli elettronici coinvolti nella transizione. Le tecniche spettroscopiche nel UV-Vis-IR permettono di studiare la natura dei centri paramagnetici attivi in ESR.
5 L ESR invece rivela la transizione tra sottolivelli magnetici appartenenti allo stesso stato elettronico. In assenza di un campo magnetico esterno i due stati di spin dell elettrone hanno la stessa energia. In un campo magnetico i due stati si separano in energia e la separazione è proporzionale al campo magnetico. Un elettrone che occupa lo stato più basso in energia può transire a quello più alto assorbendo un fotone e rovesciando la direzione dello spin. Il fotone deve avere un energia, h, pari alla differenza di energia tra i due stati. Con i campi magnetici ottenibili in laboratorio facendo passare corrente in una bobina, la frequenza della transizione è nell intervallo delle microonde. La differenza di energia tra i due livelli, ΔE, è data da: ΔE = g µ B H = h ν (1) dove: g è il fattore di Landè, µ B è il magnetone di Bohr, µ B = x erg/gauss, H è il campo magnetico esterno, h = è la costante di Planck, h= x erg/sec, ν è la frequenza della transizione.
6 La cavità dello spettrometro ESR contiene un campo magnetico uniforme e il campo delle microonde. Nella pratica la sorgente a microonde ha frequenza fissa e viene invece cambiata in maniera continua l intensità del campo magnetico. Quando il campo ha il giusto valore per avere una risonanza tra la frequenza delle microonde e quella della transizione elettronica, si ha assorbimento di potenza elettromagnetica direttamente misurata dallo strumento che fornisce la potenza. L assorbimento è proporzionale al numero di elettroni che transiscono e quindi al numero di trappole occupate presenti nel cristallo, a sua volta proporzionale alla dose accumulata indotta dalle radiazioni nucleari.
7 Il rapporto tra la frequenza di risonanza ed il relativo campo magnetico è misurato dal fattore g che vale 2 per una transizione pura di spin, ma può assumere valori diversi legati al moto spaziale dell elettrone. Ogni tipo di trappola ha il suo tipico fattore g. La misura fornisce quindi il tipo ed numero di trappole presenti. Nel grafico sotto è riportata la derivata dell assorbimento che si ottiene sovrapponendo un (debole) campo magnetico alternato a quello continuo. Questa tecnica dà risultati più precisi. Il campione, contenuto in una fiala di quarzo, è posto nella cavità risonante delle microonde nella zona di campo magnetico uniforme. La misura dura pochi minuti.
8 In ogni materiale ci possono essere differenti tipi di trappole che danno segnale ESR utile per la datazione, insieme ad altri centri che assorbono le microonde pur non avendo niente a che fare con trappole riempite da elettroni prodotti da decadimenti radioattivi. Ogni centro ha assorbimento ad un valore tipico del fattore g, noto da studi spettroscopici ESR e Zeeman. Nella calcite si distinguono bene due tipi di trappole per l elettrone. La trappola importante per la datazione è quella che assorbe a g = Le sorgenti di microonde più utilizzate sono: Banda X f = 9 GHz Banda Q f = 35 GHz Un centro con g=2 risuona rispettivamente a H = 0.32 T = 3200 gauss e a H = 1.25 T.
9 Un comune forno a microonde consiste delle parti seguenti: un magnetron, un circuito elettronico di controllo e alimentazione del magnetron, una guida d'onda, una camera (o tecnicamente cavità) di cottura. una rete metallica (sullo sportello) Il magnetron, alimentato in corrente continua ad alta tensione (2 000 V), genera un campo elettrico alternato nella frequenza delle microonde, normalmente 2,45 GHz (lunghezza d'onda di 12 cm) con una potenza solitamente compresa tra 100 W ed 1 kw, che la guida d'onda invia alla camera di cottura. L'acqua, i grassi, e i carboidrati che costituiscono il cibo assorbono l'energia delle microonde in un processo chiamato riscaldamento dielettrico: le molecole sono in generale dipoli elettrici, ovvero hanno una estremità con carica elettrica positiva e un'altra con carica negativa; sono per questo sensibili al campo elettrico (alternato), che cambiando continuamente il suo verso induce le molecole a modificare ripetutamente la loro orientazione in base alla frequenza del campo. Questo movimento genera calore attraverso forze di attrito con le molecole vicine e si ha quindi un riscaldamento. Le microonde riscaldano con più efficienza l'acqua, ma in misura minore anche grassi, zuccheri e ghiaccio.
10 I campioni vengono preparati in maniera simile a quelli per le misure di termoluminescenza. Ridotti in polvere dopo aver tolto i primi 2 mm di superficie riscaldati a 120 dopo l irraggiamento artificiale per eliminare i centri instabili. Questo riscaldamento, nella calcite, rimuove i centri che danno segnale a g = che interferisce con quello usato per la datazione a g = Le trappole che danno segnale ESR non sono di solito svuotate dall esposizione alla luce. Evidentemente sono diverse da quelle che danno TL. In qualche minerale invece lo sono e l ESR in questo caso può essere usato per datare materiali non bruciati in cui lo zero del tempo è il momento di seppellimento al riparo della luce, come già descritto per la TL. Il limite superiore di età databile è, come per la TL, dato dalla saturazione e dalla stabilità delle trappole. Può raggiungere anche il milione di anni.
11 La stabilità nel tempo delle trappole è fortemente dipendente dalla temperatura perché l elettrone per sfuggire alla trappola deve superare una barriera di potenziale. Si può valutare misurando come il segnale decade riscaldando il campione per giorni a temperature crescenti in un intervallo tra 150 e 200 C ed usando la legge di Arrhenius per estrapolare la vita della trappola a temperature più basse. La legge di Arrhenius descrive i processi attivati termicamente. Se E è l energia della barriera che l elettrone deve superare per lasciare la trappola, la probabilità dell evento è data da P = P 0 exp(-e/(kt)) e il tempo medio di permanenza è dato da = 0 exp(e/(kt)) e dove T è la temperatura assoluta misurata in gradi Kelvin (K). T(K) = T( C) , e k è la costante di Boltzmann (a T ambiente kt = ev). 0 è una costante da determinare misurando a diverse T. Un plot di ln( ) in funzione di 1/T dovrebbe dare una retta che permette di estrapolare il valore di alla temperatura desiderata (quella effettiva che il campione ha avuto nel tempo trascorso che si vuol datate). Questo tempo può essere di centinaia di migliaia o di milioni di anni a T ambiente T= 293 K, ma può ridursi a pochi giorni a a T= 450 K. Notare che dipende fortemente dalla temperatura della sepoltura e che le temperature più alte sentite anche per tempi relativamente brevi hanno il maggior effetto. La stima di non può quindi che essere molto approssimativa.
12
13
14 Ossa e denti Lo smalto dei denti è cristallino e contiene pochissima materia organica. Le ossa e la dentina, invece, hanno un contenuto minerale intorno al 50%. La loro struttura evolve per millenni o centinaia di millenni prima di raggiungere una mineralizzazione completa. Lo smalto è quindi più adatto a fornire una datazione precisa. Il minerale è idrossiapatite ed il segnale (molto intenso) ESR è a g = con un tempo di vita dell ordine di 10 7 anni. Bastano poche decine di milligrammi per datare denti antichi (con alta dose).
15 Se il reperto è solo un pezzo di smalto, la dose annuale è dominata dalla radiazione alfa e beta del terreno. Il contributo alfa è eliminabile rimuovendo uno strato superficiale sottile ( m). La dose beta va calcolata tenendo conto che una parte della radiazione beta dal terreno può non essere completamente attenuata dallo strato di smalto, se troppo sottile. Se il reperto è un dente intero o uno strato di smalto con attaccato del cemento o della dentina, una componente importante della dose annuale viene dalla radioattività del cemento e della dentina. Il contenuto di uranio di cemento e dentina, nei denti fossili, è infatti molto maggiore di quello dello smalto e può raggiungere valori molto alti di centinaia di ppm. Nei denti vivi, o di data recente, il contenuto di uranio è invece molto basso, meno di un ppm.
16 Bisognerebbe quindi sapere quando e a che ritmo l uranio presente è stato inglobato. Nei denti grandi (es. rinoceronte) si trova meno uranio nella regione centrale. In questo caso si può ricostruire un modello dell accumulo di uranio nel tempo, soprattutto se è disponibile una datazione indipendente come per esempio quella data dalle serie dell uranio.
17 Spesso si usano due modelli estremi: 1) Early uptake, cioè si ipotizza che tutto l uranio presente sia stato assorbito all inizio. 2) Linear uptake, cioè si ipotizza che ci sia stato un assorbimento lineare nel tempo. I due modelli forniscono due date estreme, che approssimano la data del reperto per difetto e per eccesso, rispettivamente.
18
19
20 Ossa e dentina Questi non sono sistemi chiusi: oltre al problema del ritmo di incorporazione dell uranio, c è qui un altro grosso problema. Dopo la morte si instaura un lunghissimo processo di mineralizzazione colla perdita della componente organica. Il minerale si modifica ed i centri ESR attivi cambiano nel tempo. Se non se ne tiene debitamente conto si rischia di sottostimare la data. Altri materiali databile con la tecnica ESR sono i coralli e le conchiglie di molluschi, i quarzi ed in generale i materiali databili con il metodo della termoluminescenza.
21
Spettroscopia. 05/06/14 SPET.doc 0
 Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
Radiazioni ionizzanti
 Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Radiazioni ionizzanti 11/3/2005 Struttura atomica Atomo Nucleo Protone 10 10 m 10 14 m 10 15 m ev MeV GeV 3 3,0 0,3 0 0 0 Atomo Dimensioni lineari
Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Radiazioni ionizzanti 11/3/2005 Struttura atomica Atomo Nucleo Protone 10 10 m 10 14 m 10 15 m ev MeV GeV 3 3,0 0,3 0 0 0 Atomo Dimensioni lineari
CHIMICA: studio della struttura e delle trasformazioni della materia
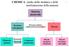 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Lezione n. 28. EPR Esempi ed applicazioni in campo biochimico e medico. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 28 EPR Esempi ed applicazioni in campo biochimico e medico 02/03/2008 Antonino Polimeno 1 Risonanza paramagnetica elettronica (1) - La Risonanza
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 28 EPR Esempi ed applicazioni in campo biochimico e medico 02/03/2008 Antonino Polimeno 1 Risonanza paramagnetica elettronica (1) - La Risonanza
Spettroscopia. Spettroscopia
 Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
Modelli atomici Modello atomico di Rutheford Per t s d u i diare la t s rutt ttura t a omica Ruth th f or (
 Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Lezione 1 ELEMENTI DI FISICA NUCLEARE APPLICATA ALLA MEDICINA
 Lezione 1 ELEMENTI DI FISICA NUCLEARE APPLICATA ALLA MEDICINA RADIAZIONE=PROPAGAZIONE DI ENERGIA NELLO SPAZIO L energia può essere associata: a particelle materiali (radiazione corpuscolare), a vibrazioni
Lezione 1 ELEMENTI DI FISICA NUCLEARE APPLICATA ALLA MEDICINA RADIAZIONE=PROPAGAZIONE DI ENERGIA NELLO SPAZIO L energia può essere associata: a particelle materiali (radiazione corpuscolare), a vibrazioni
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
the power of ten Prof.ssa Patrizia Gallucci
 https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
LO SPIN DELL'ELETTRONE. Lezioni d'autore
 LO SPIN DELL'ELETTRONE Lezioni d'autore VIDEO Momento magnetico e momento angolare (I) L immagine dell atomo di idrogeno, con la carica negativa in orbita chiusa intorno al protone, suggerisce l effetto
LO SPIN DELL'ELETTRONE Lezioni d'autore VIDEO Momento magnetico e momento angolare (I) L immagine dell atomo di idrogeno, con la carica negativa in orbita chiusa intorno al protone, suggerisce l effetto
Cara&erizzazione della composizione e stru&ura delle molecole a&raverso misure di spe&roscopia. Proff. C. Ferrante e D. Pedron
 Cara&erizzazione della composizione e stru&ura delle molecole a&raverso misure di spe&roscopia Proff. C. Ferrante e D. Pedron 1 Radiazione Ele,romagne0ca Propagazione nello spazio e nel tempo: L onda si
Cara&erizzazione della composizione e stru&ura delle molecole a&raverso misure di spe&roscopia Proff. C. Ferrante e D. Pedron 1 Radiazione Ele,romagne0ca Propagazione nello spazio e nel tempo: L onda si
Formazione di orbitali π. La differenza di energia tra due orbitali π è minore di quella tra due orbitali. Orbitali di non legame, n
 Spettroscopia Studia le interazione tra le radiazioni elettromagnetiche e la materia. Come sono fatti questi sistemi? La formazione dei legami chimici viene spiegata in termini di interazioni di orbitali
Spettroscopia Studia le interazione tra le radiazioni elettromagnetiche e la materia. Come sono fatti questi sistemi? La formazione dei legami chimici viene spiegata in termini di interazioni di orbitali
DATAZIONI PER PER LUMINESCENZA
 Stima della dose annua: La dose annua è dovuta alle particelle alfa, beta, ai raggi gamma e ai raggi cosmici. Mentre il contributo delle particelle alfa è interamente dovuto ai radionuclidi delle serie
Stima della dose annua: La dose annua è dovuta alle particelle alfa, beta, ai raggi gamma e ai raggi cosmici. Mentre il contributo delle particelle alfa è interamente dovuto ai radionuclidi delle serie
a) Discutere lo spettro osservato e ricavare la costante rotazionale B e la frequenza vibrazionale ν 0 ;
 Esercizio 2 Un gas di molecole biatomiche viene illuminato da radiazione elettromagnetica dando in uscita uno spettro di diffusione e di assorbimento. La radiazione inviata con lunghezza d onda λ 0 = 4358Å
Esercizio 2 Un gas di molecole biatomiche viene illuminato da radiazione elettromagnetica dando in uscita uno spettro di diffusione e di assorbimento. La radiazione inviata con lunghezza d onda λ 0 = 4358Å
STRUTTURA ATOMICA. Per lo studio della struttura dell atomo ci si avvale della Spettroscopia.
 STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
PROPRIETÀ MAGNETICHE DELLA MATERIA. ovvero: comportamento della materia in presenza di un campo magnetico
 PROPRIETÀ MAGNETICHE DELLA MATERIA ovvero: comportamento della materia in presenza di un campo magnetico dinamometro Fenomenologia All'interno di un solenoide percorso da corrente si crea un campo magnetico
PROPRIETÀ MAGNETICHE DELLA MATERIA ovvero: comportamento della materia in presenza di un campo magnetico dinamometro Fenomenologia All'interno di un solenoide percorso da corrente si crea un campo magnetico
Astronomia Lezione 4/11/2011
 Astronomia Lezione 4/11/2011 Docente: Alessandro Melchiorri e.mail:alessandro.melchiorri@roma1.infn.it Slides: oberon.roma1.infn.it/alessandro/ Libri di testo: - An introduction to modern astrophysics
Astronomia Lezione 4/11/2011 Docente: Alessandro Melchiorri e.mail:alessandro.melchiorri@roma1.infn.it Slides: oberon.roma1.infn.it/alessandro/ Libri di testo: - An introduction to modern astrophysics
Fisica Atomica - Giugno 2017
 Fisica Atomica - Giugno 2017 1. Sapendo che l energia di seconda ionizzazione dell atomo di calcio è 95000 cm 1 e che i livelli elettronici dello ione Ca + sono ben approssimati dai difetti quantici δ
Fisica Atomica - Giugno 2017 1. Sapendo che l energia di seconda ionizzazione dell atomo di calcio è 95000 cm 1 e che i livelli elettronici dello ione Ca + sono ben approssimati dai difetti quantici δ
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Risonanza magnetica nucleare
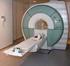 Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.)
 RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.) e una tecnica non invasiva impiega radiazioni a bassa frequenza (non ionizzanti!) ν 10-100 MHz (radiofrequenze) sfrutta la
RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.) e una tecnica non invasiva impiega radiazioni a bassa frequenza (non ionizzanti!) ν 10-100 MHz (radiofrequenze) sfrutta la
Atomo. Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale)
 Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
SPETTROMETRIA DI ASSORBIMENTO ATOMICO
 SPETTROMETRIA DI ASSORBIMENTO ATOMICO E una metodica spettroscopica atta alla determinazione qualiquantitativa di metalli. E basata sull assorbimento di radiazioni elettromagnetiche da parte di atomi nell
SPETTROMETRIA DI ASSORBIMENTO ATOMICO E una metodica spettroscopica atta alla determinazione qualiquantitativa di metalli. E basata sull assorbimento di radiazioni elettromagnetiche da parte di atomi nell
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Fenomeni quantistici
 Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Spettro delle onde elettromagnetiche. Ottica: luce visibile leggi della riflessione e rifrazione
 Spettro delle onde elettromagnetiche Ottica: luce visibile leggi della riflessione e rifrazione Introduzione Abbiamo visto che la propagazione della radiazione elettromagnetica nel vuoto è regolata dalle
Spettro delle onde elettromagnetiche Ottica: luce visibile leggi della riflessione e rifrazione Introduzione Abbiamo visto che la propagazione della radiazione elettromagnetica nel vuoto è regolata dalle
Radiazione elettromagnetica
 Spettroscopia Radiazione elettromagnetica: energia che si propaga in un mezzo fenomeno ondulatorio dovuto alla propagazione simultanea nello spazio di un campo elettrico (E) e di uno magnetico (M) perpendicolari
Spettroscopia Radiazione elettromagnetica: energia che si propaga in un mezzo fenomeno ondulatorio dovuto alla propagazione simultanea nello spazio di un campo elettrico (E) e di uno magnetico (M) perpendicolari
Lezione 24 Radiazioni Ionizzanti
 Generalità Lezione 24 Radiazioni Ionizzanti Con il termine radiazione si descrivono fenomeni molto diversi fra loro: Emissione di luce da una lampada Emissione di calore da una fiamma Particelle elementari
Generalità Lezione 24 Radiazioni Ionizzanti Con il termine radiazione si descrivono fenomeni molto diversi fra loro: Emissione di luce da una lampada Emissione di calore da una fiamma Particelle elementari
Lo Spettro Elettromagnetico
 Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Unità didattica 10. Decima unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
METODI DI DATAZIONE PER L'ARCHEOLOGIA
 METODI DI DATAZIONE PER L'ARCHEOLOGIA Obiettivi formativi Acquisire le conoscenze necessarie per un utilizzo consapevole delle principali tecniche di indagine fisica, con particolare riguardo per le datazioni.
METODI DI DATAZIONE PER L'ARCHEOLOGIA Obiettivi formativi Acquisire le conoscenze necessarie per un utilizzo consapevole delle principali tecniche di indagine fisica, con particolare riguardo per le datazioni.
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
UNITÀ DIDATTICA II CRONOLOGIE E SISTEMI DI DATAZIONE IL LAVORO SUL CAMPO: TECNICHE DI SCAVO IL MATRIX DI HARRIS
 UNITÀ DIDATTICA II IL LAVORO SUL CAMPO: TECNICHE DI SCAVO IL MATRIX DI HARRIS GESTIONE DEI DATI E DEI REPERTI : DALLO SCAVO AL POST-SCAVO MANUFATTI... ED ECOFATTI: APPROCCIO TIPOLOGICO E SISTEMI DI CLASSIFICAZIONE
UNITÀ DIDATTICA II IL LAVORO SUL CAMPO: TECNICHE DI SCAVO IL MATRIX DI HARRIS GESTIONE DEI DATI E DEI REPERTI : DALLO SCAVO AL POST-SCAVO MANUFATTI... ED ECOFATTI: APPROCCIO TIPOLOGICO E SISTEMI DI CLASSIFICAZIONE
FISICA delle APPARECCHIATURE per RADIOTERAPIA
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Effetto Zeeman anomalo
 Effetto Zeeman anomalo Direzione del campo B esempio: : j=3/2 Direzione del campo B j=1+1/2 = 3/2 s m j =+3/2 m j =+1/2 l m j =-1/2 m j =-3/2 La separazione tra i livelli é diversa l e µ l antiparalleli
Effetto Zeeman anomalo Direzione del campo B esempio: : j=3/2 Direzione del campo B j=1+1/2 = 3/2 s m j =+3/2 m j =+1/2 l m j =-1/2 m j =-3/2 La separazione tra i livelli é diversa l e µ l antiparalleli
Legge di Gauss per il magnetismo. La struttura magnetica più semplice in natura è il dipolo magnetico
 Legge di Gauss per il magnetismo La struttura magnetica più semplice in natura è il dipolo magnetico Φ B = ර B d ԦA = 0 legge di Gauss per i campi magnetici Φ E = ර E d ԦA = q i ε 0 legge di Gauss per
Legge di Gauss per il magnetismo La struttura magnetica più semplice in natura è il dipolo magnetico Φ B = ර B d ԦA = 0 legge di Gauss per i campi magnetici Φ E = ර E d ԦA = q i ε 0 legge di Gauss per
Risonanza magnetica di spin: ESR (o EPR) nucleare: RMN/NMR
 Risonanza magnetica di spin: ESR (o EPR) nucleare: RMN/NMR 1944-prima osservazione della ESR 1938-prima osservazione della NMR Tecniche spettroscopiche oggi standard Applicazioni di caratterizzazione e
Risonanza magnetica di spin: ESR (o EPR) nucleare: RMN/NMR 1944-prima osservazione della ESR 1938-prima osservazione della NMR Tecniche spettroscopiche oggi standard Applicazioni di caratterizzazione e
Risonanza Magnetico Nucleare
 Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Risonanza Magnetico Nucleare 21/3/2005 RMN ovvero NMR Spettroscopia RMN permette di - acquisire immagini 2D e 3D di parti del corpo umano ottima risoluzione
Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Risonanza Magnetico Nucleare 21/3/2005 RMN ovvero NMR Spettroscopia RMN permette di - acquisire immagini 2D e 3D di parti del corpo umano ottima risoluzione
CORSO DI LAUREA IN OTTICA E OPTOMETRIA
 CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
I 4 NUMERI QUANTICI. I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali.
 I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
I NUMERI QUANTICI. per l = orbitale: s p d f
 I NUMERI QUANTICI I numeri quantici sono quattro. I primi tre servono a indicare e a distinguere i diversi orbitali. Il quarto numero descrive una proprietà tipica dell elettrone. Esaminiamo in dettaglio
I NUMERI QUANTICI I numeri quantici sono quattro. I primi tre servono a indicare e a distinguere i diversi orbitali. Il quarto numero descrive una proprietà tipica dell elettrone. Esaminiamo in dettaglio
Le radiazioni ionizzanti e la radioprotezione
 Le radiazioni ionizzanti e la radioprotezione Radiazioni Radiazioniionizzanti ionizzanti Il termine radiazione viene abitualmente usato per descrivere fenomeni apparentemente assai diversi tra loro,
Le radiazioni ionizzanti e la radioprotezione Radiazioni Radiazioniionizzanti ionizzanti Il termine radiazione viene abitualmente usato per descrivere fenomeni apparentemente assai diversi tra loro,
SPETTROSCOPIA UV-VIS LEZIONE 9
 SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
Docente: Alessandro Melchiorri Slides delle lezioni: oberon.roma1.infn.it/alessandro/astro2014
 Astronomia Lezione 31/10/2014 Docente: Alessandro Melchiorri e.mail:alessandro.melchiorri@roma1.infn.it Slides delle lezioni: oberon.roma1.infn.it/alessandro/astro2014 Cosa possiamo imparare sulle stelle
Astronomia Lezione 31/10/2014 Docente: Alessandro Melchiorri e.mail:alessandro.melchiorri@roma1.infn.it Slides delle lezioni: oberon.roma1.infn.it/alessandro/astro2014 Cosa possiamo imparare sulle stelle
Principi di Base di MR
 Principi di Base di MR Spin Proprietà fondamentale come la massa e la carica elettrica Protoni, elettroni e neutroni hanno tutti spin ½ Quando posta in un campo magnetico B 0, una particella con spin può
Principi di Base di MR Spin Proprietà fondamentale come la massa e la carica elettrica Protoni, elettroni e neutroni hanno tutti spin ½ Quando posta in un campo magnetico B 0, una particella con spin può
Richiami. Esercizio 1.1. La radiazione elettromagnetica del corpo nero ha la seguente densità di energia per unità di frequenza
 Parte I Problemi Richiami Esercizio 1.1. La radiazione elettromagnetica del corpo nero ha la seguente densità di energia per unità di frequenza u ν = 8π hν c 3 ν e βhν 1, dove c è la velocità della luce
Parte I Problemi Richiami Esercizio 1.1. La radiazione elettromagnetica del corpo nero ha la seguente densità di energia per unità di frequenza u ν = 8π hν c 3 ν e βhν 1, dove c è la velocità della luce
Analisi chimiche per i beni culturali
 Analisi chimiche per i beni culturali Nicola Ludwig ricevimento: in via Noto giovedì dopo lezione Nicola.Ludwig@unimi.it Istituto di Fisica Generale Applicata, via Celoria 16 Programma L obiettivo del
Analisi chimiche per i beni culturali Nicola Ludwig ricevimento: in via Noto giovedì dopo lezione Nicola.Ludwig@unimi.it Istituto di Fisica Generale Applicata, via Celoria 16 Programma L obiettivo del
FISICA delle APPARECCHIATURE per MEDICINA NUCLEARE
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per MEDICINA NUCLEARE (lezione I, 07.05.13) Marta Ruspa 1 L
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per MEDICINA NUCLEARE (lezione I, 07.05.13) Marta Ruspa 1 L
Spettro di corpo nero, temperatura di brillanza e temperatura di antenna
 Spettro di corpo nero, temperatura di brillanza e temperatura di antenna Aniello Mennella Università degli Studi di Milano Dipartimento di Fisica Cosa trattiamo oggi Lo spettro di corpo nero Perché il
Spettro di corpo nero, temperatura di brillanza e temperatura di antenna Aniello Mennella Università degli Studi di Milano Dipartimento di Fisica Cosa trattiamo oggi Lo spettro di corpo nero Perché il
G. Bracco -Appunti di Fisica Generale
 Equazioni di Maxwell ε 0 E= ρ B= 0 E= - B / t B = μ 0 J+ ε 0 μ 0 E / t= μ 0 (J+ ε 0 E / t) il termine ε 0 E / t è la corrente di spostamento e fu introdotto da Maxwell per rendere consistenti le 4 equazioni
Equazioni di Maxwell ε 0 E= ρ B= 0 E= - B / t B = μ 0 J+ ε 0 μ 0 E / t= μ 0 (J+ ε 0 E / t) il termine ε 0 E / t è la corrente di spostamento e fu introdotto da Maxwell per rendere consistenti le 4 equazioni
La struttura dell atomo
 La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
La struttura della materia
 La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
E. SCHRODINGER ( )
 E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
OVERVIEW. Teoria atomica e tavola periodica. Legami e interazioni degli atomi
 OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi stato fondamentale stati eccitati
 4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
LASER. Light Amplification by Stimulated Emission of Radiation. Introduzione. Assorbimento, emissione spontanea, emissione stimolata
 LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
2. La Struttura dei Composti Organici e le caratteristiche chimico-fisiche
 2. La Struttura dei Composti Organici e le caratteristiche chimico-fisiche 6. Spettroscopia Giuseppe G. Carbonara La struttura dei composti organici 6. Spettroscopia I. Analisi elementare II. Spettri di
2. La Struttura dei Composti Organici e le caratteristiche chimico-fisiche 6. Spettroscopia Giuseppe G. Carbonara La struttura dei composti organici 6. Spettroscopia I. Analisi elementare II. Spettri di
NATURA DELLA LUCE. 1/4 - NATURA DELLA LUCE - C. Calì - DIEET-UNIPA (2007-rev_10/11) Pubblicato in
 NATURA DELLA LUCE Nel corso del tempo diverse sono state le teorie formulate per spiegare la luce ed il suo comportamento. La teoria corpuscolare, messa a punto da Newton, è basata sull'ipotesi che la
NATURA DELLA LUCE Nel corso del tempo diverse sono state le teorie formulate per spiegare la luce ed il suo comportamento. La teoria corpuscolare, messa a punto da Newton, è basata sull'ipotesi che la
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Sommario della lezione 2. Materia e definizioni. Struttura dell atomo
 Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
Fisica 2 per biotecnologie: Prova Scritta 30 Gennaio 2012
 Fisica 2 per biotecnologie: Prova Scritta 30 Gennaio 2012 Scrivere immediatamente, ED IN EVIDENZA, sui due fogli protocollo consegnati (ed eventuali altri fogli richiesti) la seguente tabella: NOME :...
Fisica 2 per biotecnologie: Prova Scritta 30 Gennaio 2012 Scrivere immediatamente, ED IN EVIDENZA, sui due fogli protocollo consegnati (ed eventuali altri fogli richiesti) la seguente tabella: NOME :...
ATOMI E PARTICELLE SUBATOMICHE
 ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
Rappresentazione dell atomo. Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano.
 Rappresentazione dell atomo Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano. Informazioni importanti circa la dimensione dell atomo e la distribuzione della massa
Rappresentazione dell atomo Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano. Informazioni importanti circa la dimensione dell atomo e la distribuzione della massa
La Produzione dei Raggi X
 La Produzione dei Raggi X Master: Verifiche di Qualità in Radiodiagnostica, Medicina Nucleare e Radioterapia Lezione 2 Dr. Rocco Romano (Dottore di Ricerca) Facoltà di Farmacia, Università degli Studi
La Produzione dei Raggi X Master: Verifiche di Qualità in Radiodiagnostica, Medicina Nucleare e Radioterapia Lezione 2 Dr. Rocco Romano (Dottore di Ricerca) Facoltà di Farmacia, Università degli Studi
INTRODUZIONE AI METODI OTTICI
 INTRODUZIONE AI METODI OTTICI Con l espressione Metodi Ottici s intende l insieme delle tecniche analitiche nelle quali interviene una radiazione elettromagnetica. Per avere una sufficiente comprensione
INTRODUZIONE AI METODI OTTICI Con l espressione Metodi Ottici s intende l insieme delle tecniche analitiche nelle quali interviene una radiazione elettromagnetica. Per avere una sufficiente comprensione
FISICA APPLICATA 2 DIPOLI ELETTRICI E MAGNETICI
 FISICA APPLICATA 2 DIPOLI ELETTRICI E MAGNETICI DOWNLOAD Il pdf di questa lezione (ele2.pdf) è scaricabile dal sito http://www.ge.infn.it/ calvini/tsrm/ 26/11/2012 DIPOLO ELETTRICO La configurazione costituita
FISICA APPLICATA 2 DIPOLI ELETTRICI E MAGNETICI DOWNLOAD Il pdf di questa lezione (ele2.pdf) è scaricabile dal sito http://www.ge.infn.it/ calvini/tsrm/ 26/11/2012 DIPOLO ELETTRICO La configurazione costituita
Chimica e computer Principi di spettroscopia IR
 Chimica e computer Principi di spettroscopia IR Marco Bortoli, Laura Orian Dipartimento di Scienze chimiche Università degli Studi di Padova Via Marzolo 1 35131 Padova La spettroscopia è lo studio dell
Chimica e computer Principi di spettroscopia IR Marco Bortoli, Laura Orian Dipartimento di Scienze chimiche Università degli Studi di Padova Via Marzolo 1 35131 Padova La spettroscopia è lo studio dell
SOSTANZE PERICOLOSE. 1 Il numero di massa di un elemento è uguale
 SOSTANZE PERICOLOSE 1 Il numero di massa di un elemento è uguale a Alla somma del numero dei protoni + quello dei mesoni b alla somma del numero dei protoni, + quello dei neutroni del suo atomo c Alla
SOSTANZE PERICOLOSE 1 Il numero di massa di un elemento è uguale a Alla somma del numero dei protoni + quello dei mesoni b alla somma del numero dei protoni, + quello dei neutroni del suo atomo c Alla
La misura della temperatura
 Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Dalla struttura fine delle transizioni atomiche allo spin dell elettrone
 Dalla struttura fine delle transizioni atomiche allo spin dell elettrone Evidenze sperimentali Struttura fine delle transizioni atomiche (doppietto( del sodio) Esperimento di Stern-Gerlach Effetto Zeeman
Dalla struttura fine delle transizioni atomiche allo spin dell elettrone Evidenze sperimentali Struttura fine delle transizioni atomiche (doppietto( del sodio) Esperimento di Stern-Gerlach Effetto Zeeman
Cenni sulla struttura della materia
 Cenni sulla struttura della materia Tutta la materia è costituita da uno o più costituenti fondamentali detti elementi Esistono 102 elementi, di cui 92 si trovano in natura (i rimanenti sono creati in
Cenni sulla struttura della materia Tutta la materia è costituita da uno o più costituenti fondamentali detti elementi Esistono 102 elementi, di cui 92 si trovano in natura (i rimanenti sono creati in
03/04/2019 METODI SPETTROSCOPICI - 3. Risonanza magnetica elettronica (EPR O ESR) CHIMICA ANALITICA UNIVERSITÀ DEGLI STUDI DI TERAMO
 UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI - 3 La risonanza magnetica elettronica è una branca della spettroscopia nella quale
UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI - 3 La risonanza magnetica elettronica è una branca della spettroscopia nella quale
Teoria Atomica Moderna. Chimica generale ed Inorganica: Chimica Generale. sorgenti di emissione di luce. E = hν. νλ = c. E = mc 2
 sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
mvr = n h e 2 r = m v 2 e m r v = La configurazione elettronica r = e 2 m v 2 (1) Quantizzazione del momento angolare (2) 4 πε.
 La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
Lezione 19 Fisica nucleare
 Lezione 19 Fisica nucleare Nucleo Il nucleo atomico è costituito da nucleoni (N), ovvero: protoni (p) e neutroni (n). Il numero di p è caratteristico di ogni elemento; è detto numero atomico ed è indicato
Lezione 19 Fisica nucleare Nucleo Il nucleo atomico è costituito da nucleoni (N), ovvero: protoni (p) e neutroni (n). Il numero di p è caratteristico di ogni elemento; è detto numero atomico ed è indicato
Scintillatori. Stage Residenziale 2012
 Scintillatori Stage Residenziale 2012 Rivelatori a Scintillazione Passaggio di radiazione attraverso materiale scintillante eccitazione di atomi e molecole del materiale emissione di luce raccolta e trasmessa
Scintillatori Stage Residenziale 2012 Rivelatori a Scintillazione Passaggio di radiazione attraverso materiale scintillante eccitazione di atomi e molecole del materiale emissione di luce raccolta e trasmessa
LO SPETTRO ELETTROMAGNETICO
 LO SPETTRO ELETTROMAGNETICO 1 LO SPETTRO ELETTROMAGNETICO cresce Visibile Raggi γ Raggi X UV IR Micro onde cresce Onde radio Medio corte medie e lunghe Eccitazione dei nuclei atomici Lontano Vicino Lontano
LO SPETTRO ELETTROMAGNETICO 1 LO SPETTRO ELETTROMAGNETICO cresce Visibile Raggi γ Raggi X UV IR Micro onde cresce Onde radio Medio corte medie e lunghe Eccitazione dei nuclei atomici Lontano Vicino Lontano
CONFIGURAZIONE ELETTRONICA. In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo.
 CONFIGURAZIONE ELETTRONICA In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo. ORBITA : Zona intorno al nucleo di diversa energia dove ruotano
CONFIGURAZIONE ELETTRONICA In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo. ORBITA : Zona intorno al nucleo di diversa energia dove ruotano
Onde e oscillazioni. Fabio Peron. Onde e oscillazioni. Le grandezze che caratterizzano le onde
 Onde e oscillazioni Lezioni di illuminotecnica. Luce e Onde elettromagnetiche Fabio Peron Università IUAV - Venezia Si parla di onde tutte le volte che una grandezza fisica varia la sua entità nel tempo
Onde e oscillazioni Lezioni di illuminotecnica. Luce e Onde elettromagnetiche Fabio Peron Università IUAV - Venezia Si parla di onde tutte le volte che una grandezza fisica varia la sua entità nel tempo
Onde e oscillazioni. Fabio Peron. Onde e oscillazioni. Le grandezze che caratterizzano le onde
 Onde e oscillazioni Lezioni di illuminotecnica. Luce e Onde elettromagnetiche Fabio Peron Università IUAV - Venezia Si parla di onde tutte le volte che una grandezza fisica varia la sua entità nel tempo
Onde e oscillazioni Lezioni di illuminotecnica. Luce e Onde elettromagnetiche Fabio Peron Università IUAV - Venezia Si parla di onde tutte le volte che una grandezza fisica varia la sua entità nel tempo
Lezione n. 19. L equazione. di Schrodinger L atomo. di idrogeno Orbitali atomici. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Effetto Stark (1) H 0 nlm > = E n nlm > (4) Ricordiamo che. E n = me4 2 h 2 n 2 = E 1
 Effetto Stark Studiamo l equazione di Schrödinger per l atomo di idrogeno in presenza di un campo elettrico costante e diretto lungo l asse z, E = E k. La hamiltoniana di Schrödinger per l atomo di idrogeno
Effetto Stark Studiamo l equazione di Schrödinger per l atomo di idrogeno in presenza di un campo elettrico costante e diretto lungo l asse z, E = E k. La hamiltoniana di Schrödinger per l atomo di idrogeno
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
Semiconduttori. Bande di energia. Un cristallo è formato da atomi disposti in modo da costituire una struttura periodica regolare
 Semiconduttori Bande di energia Un cristallo è formato da atomi disposti in modo da costituire una struttura periodica regolare Quando gli atomi formano un cristallo, il moto degli elettroni dello strato
Semiconduttori Bande di energia Un cristallo è formato da atomi disposti in modo da costituire una struttura periodica regolare Quando gli atomi formano un cristallo, il moto degli elettroni dello strato
Lezione 9/11/2012. Docente: Alessandro Melchiorri
 Astronomia Docente: Alessandro Melchiorri e.mail:alessandro.melchiorri@roma1.infn.it Lezione 9/11/2012 Sito web per slides lezioni: oberon.roma1.infn.it:/alessandro/astro2012/ Le lezioni astronomia012_*.pdf
Astronomia Docente: Alessandro Melchiorri e.mail:alessandro.melchiorri@roma1.infn.it Lezione 9/11/2012 Sito web per slides lezioni: oberon.roma1.infn.it:/alessandro/astro2012/ Le lezioni astronomia012_*.pdf
Violazione della Parità
 Violazione della Parità Raffaele Pontrandolfi Corso di Astrosica e Particelle Elementari Motivazione Per spiegare l asimmetria nell universo tra particelle e antiparticelle bisogna trovare dei processi
Violazione della Parità Raffaele Pontrandolfi Corso di Astrosica e Particelle Elementari Motivazione Per spiegare l asimmetria nell universo tra particelle e antiparticelle bisogna trovare dei processi
DISTRIBUZIONI DISTRIBUZIONE DI GAUSS
 DISTRIBUZIONI ESPERIENZA a: DISTRIBUZIONE DI GAUSS SCOPO: Costruzione di una distribuzione di Gauss dai valori di una grandezza fisica ottenuti da una misura dominata da errori casuali. Studio dell influenza
DISTRIBUZIONI ESPERIENZA a: DISTRIBUZIONE DI GAUSS SCOPO: Costruzione di una distribuzione di Gauss dai valori di una grandezza fisica ottenuti da una misura dominata da errori casuali. Studio dell influenza
4. MODELLO DI EINSTEIN
 4. MODELLO DI EISTEI Einstein fu il primo ad elaborare un modello per la descrizione dell interazione radiazione-materia (molecole) tenendo conto della quantizzazione delle energie molecolari e della radiazione.
4. MODELLO DI EISTEI Einstein fu il primo ad elaborare un modello per la descrizione dell interazione radiazione-materia (molecole) tenendo conto della quantizzazione delle energie molecolari e della radiazione.
Gli accoppiamenti di spin. e i sistemi di spin nucleari
 Gli accoppiamenti di spin e i sistemi di spin nucleari l momento magnetico di un nucleo interagisce con i momenti magnetici dei nuclei vicini. sistono due tipi di interazioni: nterazione diretta, anisotropa
Gli accoppiamenti di spin e i sistemi di spin nucleari l momento magnetico di un nucleo interagisce con i momenti magnetici dei nuclei vicini. sistono due tipi di interazioni: nterazione diretta, anisotropa
Fascio di antenna, spettro di corpo nero, temperatura di brillanza e temperatura di antenna
 Fascio di antenna, spettro di corpo nero, temperatura di brillanza e temperatura di antenna Aniello Mennella Università degli Studi di Milano Dipartimento di Fisica Cosa trattiamo oggi Fascio di antenna,
Fascio di antenna, spettro di corpo nero, temperatura di brillanza e temperatura di antenna Aniello Mennella Università degli Studi di Milano Dipartimento di Fisica Cosa trattiamo oggi Fascio di antenna,
INTRODUZIONE ALLA SPETTROMETRIA
 INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
Nuclei con N e Z pari ed eccitazioni collettive
 Nuclei con N e Z pari ed eccitazioni collettive Si osserva che e possibile avere dei 2 + ma l energia e troppo alta. Consideriamo allora una combinazione lineare di stati che siaccoppiano a 2 + 2 + Rompere
Nuclei con N e Z pari ed eccitazioni collettive Si osserva che e possibile avere dei 2 + ma l energia e troppo alta. Consideriamo allora una combinazione lineare di stati che siaccoppiano a 2 + 2 + Rompere
