RICERCA DEGLI ANIONI
|
|
|
- Alessandra Carli
- 5 anni fa
- Visualizzazioni
Transcript
1 RICERCA DEGLI ANIONI
2 RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI BROMURI IODURI Ricerca: SOLFATI OSSALATI TIOSOLFATI NITRITI NITRATI ARSENIATI 1
3 Analisi degli anioni per via secca ACETATI (CH 3 COO - ) Derivano dall acido acetico - acido monoprotico debole (Ka = ) Reazione con bisolfato di potassio (KHSO 4 ) La sostanza triturata in mortaio con KHSO 4 ed una goccia di acqua sviluppa CH 3 COOH riconoscibile dall odore caratteristico di aceto CH 3 COONa + KHSO 4 CH 3 COOH + KNaSO 4 2
4 CARBONATI (CO 3 ) Analisi degli anioni per via secca Derivano dall acido carbonico (Ka 1 = , Ka 2 = ) Reazione con acqua di barite [Ba(OH) 2 ] Si tratta la polvere con HCl dil. Si raccoglie la CO 2 che si sviluppa in una seconda provetta contenente Ba(OH) 2. Un precipitato bianco, solubile in HCl, conferma la presenza di CO 3. CO H + H 2 CO 3 CO 2 + H 2 O CO 2 + Ba OH - BaCO 3(s) + H 2 O Precipitato bianco Si prepara una provetta contenente l acqua di barite. In una seconda provetta si pone la sostanza da analizzare e si aggiunge HCl 2N. Si collegano le due provette tramite un tubo di vetro piegato ad U (tubo a squadra) e si scalda debolmente la provetta contenente la sostanza da analizzare. Se sono presenti gli ioni carbonato, la soluzione di idrossido di bario si intorbida. N.B. Per aggiunta di HCl il precipitato formatosi si Sostanza da Acqua di barite analizzare + HCl + scioglie. riscaldamento 3
5 TARTRATI (C 4 O 6 H 4 ) Analisi degli anioni per via secca Derivano dall acido tartarico (Ka 1 = , Ka 2 = ) Calcinazione Una piccola quantità di polvere viene calcinata in una capsula di porcellana. Si sviluppa un odore caratteristico di zucchero bruciato che conferma la presenza dei tartrati. COONa 2 CHOH CHOH COOK 2 CO CO + 2 C + 4 H 2 O + K 2 O + Na 2 O 4
6 IONE AMMONIO (NH 4+ ) Analisi dei cationi per via secca Reazione con idrossido di sodio (NaOH) Si tratta la polvere con NaOH dil. e si riscalda leggermente. Si libera NH 3 gassosa riconoscibile dall odore o mediante una cartina indicatrice. NH 4 Cl + NaOH NH 3 + H 2 O + Na + + Cl - 5
7 Analisi degli anioni per via secca SOLFITI (SO 3 ) Derivano dall acido solforoso H 2 SO 3 (Ka 1 = , Ka 2 = ) Reazione con bicromato di potassio (K 2 Cr 2 O 7 ) Si tratta la polvere con HCl dil. e si scalda leggermente. Si sviluppa SO 2 che si fa reagire con una cartina imbevuta di K 2 Cr 2 O 7 posta all imboccatura della provetta. La colorazione verde che compare sulla cartina (dovuta alla riduzione del cromo) conferma la presenza di SO 3. Na 2 SO 3 + 2H + SO 2 + H 2 O + 2 Na + 3 SO 2 + Cr 2 O H + 2 Cr SO 4 + H 2 O verde 6
8 Analisi degli anioni per via umida SOLUZIONE ALCALINA SOSTANZA + Na 2 CO Si scioglie in 10 ml di H 2 O e si riscalda all ebollizione per 10 min. Al termine si filtra, si allontana il precipitato e si utilizza il filtrato per eseguire i saggi di riconoscimento degli anioni Precipitano i cationi dei metalli pesanti o colorati come carbonati, idrossidi o ossidi insolubili, mentre passano in soluzione gli anioni come sali sodici solubili (Interconversione) Es. CaSO 4(s) + Na 2 CO 3 CaCO 3 (s) + 2 Na + + SO 4 MnCl 2 + Na 2 CO 3 MnCO 3 (s) + 2 Na Cl - Ø Ø Trasformare i sali poco solubili in sali sodici solubili Allontanare i cationi dei metalli pesanti o colorati (Fe, Ni, Mn, ecc.) che potrebbero interferire. 7
9 Analisi degli anioni per via umida N.B. Generalmente prima di ogni saggio la soluzione alcalina deve essere acidificata e riscaldata per allontanare i carbonati, come CO 2, che danno interferenza nella maggior parte dei saggi CO 3 + H + HCO H + H 2 CO 3 CO 2 + H 2 O SOLFATI (SO 4 ) Reazione con cloruro di bario (BaCl 2 ) Soluzione alcalina + HCl dil. (scacciare bene i gas) + soluzione di BaCl 2. Si ottiene un precipitato bianco insolubile in HCl. BaCl 2 + SO 4 BaSO 4(s) + 2Cl - Precipitato bianco 8
10 Analisi degli anioni per via umida TIOSOLFATI (S 2 O 3 ) Derivano dall acido tiosolforico H 2 S 2 O 3 Reazione con bicromato di potassio (K 2 Cr 2 O 7 ) Si tratta la soluzione alcalina con HCl dil. e si scalda leggermente. Si sviluppa SO 2 che si fa reagire con una cartina imbevuta di K 2 Cr 2 O 7 posta all imboccatura della provetta. La colorazione verde che compare sulla cartina (dovuta alla riduzione del cromo) conferma la presenza di S 2 O 3. S 2 O H + SO 2 + H 2 O + S 3 SO 2 + Cr 2 O H + 2 Cr SO 4 + H 2 O verde Reazione con argento nitrato (AgNO 3 ) Un po di soluzione alcalina neutralizzata con HNO 3 dil. e trattata con un leggero eccesso di AgNO 3 dà un precipitato bianco di Ag 2 S 2 O 3 che subito diventa giallo, poi bruno e infine nero per formazione di Ag 2 S. S 2 O 3 + AgNO 3 Ag 2 S 2 O 3(s) + NO 3 - Ag 2 S 2 O 3 + H 2 O H 2 SO 4 + Ag 2 S(s) 9
11 OSSALATI (C 2 O 4 ) Reazione con cloruro di calcio (CaCl 2 ) Si acidifica la soluzione alcalina con CH 3 COOH fino a ph = 5 (scacciare bene i gas). Si aggiunge una soluzione di CaCl 2 : un precipitato bianco denota la presenza di ossalati C 2 O 4 + CaCl 2 CaC 2 O 4(s) + 2Cl - Precipitato bianco (si forma lentamente e a caldo) Analisi degli anioni per via umida Conferma: Si lava il precipitato con H 2 O e si scioglie in H 2 SO 4 dil. Si riscalda e si aggiunge goccia a goccia una soluzione di KMnO 4 : si osserva scoloramento. 2 MnO C 2 O H + 2 Mn CO H 2 O viola incolore 10
12 Analisi degli anioni per via umida NITRITI (NO 2 ) Reazione con solfato di ferro II Si prepara una soluzione satura di FeSO 4 e la si acidifica con H 2 SO 4 dil. Su questa soluzione si stratifica dall alto un po della soluzione alcalina. Si ottiene una colorazione bruna di solfato di ferro nitrosile sotto forma di anello. 1) NO 2 + H + HNO 2 2) 3 HNO 2 H 2 O + HNO NO 3) FeSO 4 + NO [Fe(NO)]SO 4 solfato di ferro nitrosile bruno 11
13 NITRATI (NO 3- ) Reazione con solfato di ferro II Analisi degli anioni per via umida Si acidifica la soluzione alcalina con H 2 SO 4 dil. Si aggiunge qualche granellino di FeSO 4. Si immerge la pipetta contenente H 2 SO 4 conc. sino a raggiungere il fondo della provetta e si stratifica. Nella zona di separazione tra i due liquidi (dovuta alla diversa densità) si forma un anello bruno. NO H Fe 2+ 3 Fe 3+ + NO + 2 H 2 O con solfato ferroso in eccesso FeSO 4. NO solfato di ferro nitrosile (bruno) N.B. Se sono presenti ioni bromuri o ioduri l acido solforico libera bromo o iodio che interferiscono. In tal caso si preferisce effettuare la reazione con la lega di Devarda (Zn + Al + Cu) 3 NO OH H 2 O + 8 Al 3NH Al(OH) 4 - N.B. lo ione NH 4 + interferisce liberando ammoniaca in ambiente alcalino 12
14 ARSENIATI (AsO 4 3- ) (Si deve aver trovato As 5+ nella ricerca dei cationi) a) Reazione con miscela magnesiaca (MgCl 2, NH 4 Cl, NH 4 OH) Analisi degli anioni per via umida Si acidifica la soluzione alcalina con HCl (scacciare bene i gas), si aggiunge NH 4 OH fino a reazione basica quindi si aggiunge la miscela magnesiaca. Si forma (a caldo) un precipitato bianco di arseniato ammonico magnesiaco solubile in acidi. Na 3 AsO 4 + MgCl 2 + NH 4 Cl MgNH 4 AsO NaCl bianco b) Reazione con argento nitrato Si acidifica la soluzione alcalina con HNO 3 dil.(scacciare bene i gas), si aggiunge CH 3 COONa in eccesso (per tamponare) quindi si aggiunge AgNO 3. Si forma un precipitato rosso mattone insolubile in acido acetico. Na 3 AsO AgNO 3 Ag 3 AsO NaNO 3 rosso c) Reazione con molibdato di ammonio Si acidifica la soluzione alcalina con HNO 3 dil. (scacciare bene i gas), si aggiunge (NH 4 ) 2 MoO 4 e si riscalda a lungo. Si forma un precipitato giallo cristallino di arseno molibdato di ammonio. H 3 AsO (NH 4 ) 2 MoO HNO 3 12 H 2 O + 21 NH 4 NO 3 + (NH 4 ) 3 AsO 4 x 12 MoO 3 giallo 13
15 Analisi degli anioni per via umida ALOGENURI (Cl -, Br -, I - ) Cloruri Reazione con argento nitrato (AgNO 3 ) Si acidifica la soluzione alcalina con HNO 3 dil. (scacciare bene i gas), quindi si aggiunge AgNO 3. Si ottiene un precipitato bianco caseoso (insolubile in HNO 3 dil., solubile in ammoniaca dil.) Cl - + Ag + AgCl(s) Kps = AgCl (s) + 2 NH 4 OH (dil.) Ag(NH 3 ) Cl H 2 O N.B. AgCl riprecipita per acidificazione con acido nitrico dil. Ag(NH 3 ) Cl H + AgCl(s) + 2 NH
16 Bromuri Analisi degli anioni per via umida a) Reazione con argento nitrato (AgNO 3 ) Si acidifica la soluzione alcalina con HNO 3 dil. (scacciare bene i gas), quindi si aggiunge AgNO 3. Si ottiene un precipitato giallo chiaro caseoso (insolubile in HNO 3 dil., solubile in ammoniaca conc.) Br - + Ag + AgBr(s) Giallo chiaro Kps = AgBr (s) + 2 NH 4 OH (conc.) Ag(NH 3 ) Br H 2 O N.B. AgBr riprecipita per acidificazione con acido nitrico dil. Ag(NH 3 ) Br H + AgBr(s) + 2 NH
17 Analisi degli anioni per via umida Bromuri b) Reazione con sodio ipoclorito (NaClO) Si acidifica la soluzione alcalina con H 2 SO 4 dil. (scacciare bene i gas), quindi si aggiunge cloroformio e NaClO gtt a gtt (agitare energicamente dopo ogni aggiunta). In presenza di Br - la fase cloroformica si colora in rosso vinoso che passa a giallo in eccesso di NaClO). 2 Br - + ClO H + Br 2 + Cl - + H 2 O Rosso vinoso N.B. in eccesso di NaClO: 3 ClO - ClO Cl - Cl - + ClO H + Br 2 + Cl 2 2 BrCl Cl 2 + H 2 O Giallo vinoso 16
18 Analisi degli anioni per via umida Ioduri a) Reazione con argento nitrato (AgNO 3 ) Si acidifica la soluzione alcalina con HNO 3 dil. (scacciare bene i gas), quindi si aggiunge AgNO 3. Si ottiene un precipitato giallo caseoso (insolubile in HNO 3 dil. e in ammoniaca conc.) I - + Ag + AgI (s) Giallo Kps =
19 Analisi degli anioni per via umida Ioduri b) Reazione con sodio ipoclorito (NaClO) Si acidifica la soluzione alcalina con H 2 SO 4 dil. (scacciare bene i gas), quindi si aggiunge cloroformio e NaClO gtt a gtt (agitare energicamente dopo ogni aggiunta). In presenza di I - la fase cloroformica si colora in viola e, successivamente, diventa incolore in eccesso di NaClO). 2 I - + ClO H + I 2 + Cl - + H 2 O Viola I Cl H 2 O 2 HIO Cl H + Incolore 18
20 Analisi degli anioni per via umida Ridissoluzione selettiva degli alogenuri di argento Soluzione alcalina (Cl -, Br -, I - ) 1) HNO 3 dil. (scacciare bene i gas) 2) AgNO 3 (fino a completa ppt) soluzione (controllare che la ppt sia completa) Precipitato (Ag I, AgBr, AgCl) NH 3 dil. soluzione [Ag(NH 3 ) 2+ ] + Cl - HNO 3 dil. Residuo (Ag I e AgBr) NH 3 conc. Precipitato bianco (AgCl) [Ag(NH 3 ) 2+ ] + Br - Residuo bianco (Ag I) HNO 3 dil. H 2 O Precipitato giallo (AgBr) Residuo giallo (AgI) 19
21 Analisi degli anioni per via umida Ossidazione selettiva degli alogenuri di argento con NaClO Soluzione alcalina (Br - e I - ) 1) H 2 SO 4 dil. 2) Cloroformio (10 gtt) 3) NaClO (gocca a goccia) Fase organica (viola) E 0 : Br 2 /2Br - : 1 volt I 2 /2I - : 0.5 volt 2 I - + ClO H + I 2 + Cl - + H 2 O Viola NaClO (goccia a goccia) Fase organica (rosso vinoso) 2 Br - + ClO H + Br 2 + Cl - + H 2 O Rosso vinoso NaClO (goccia a goccia) Fase organica (giallo vinoso) Br 2 + Cl 2 2 BrCl Giallo vinoso 20
22 VIA SECCA ACETATI (CH 3 COO ) Reazione con bisolfato di potassio (KHSO 4 ) La sostanza triturata in mortaio con KHSO 4 ed una goccia di acqua sviluppa CH 3 COOH riconoscibile dall odore caratteristico di aceto. Reazione con acqua di barite [Ba(OH) 2 ] CARBONATI (CO 3= ) Si prepara una provetta contenente l acqua di barite. In una seconda provetta si pone la sostanza da analizzare e si aggiunge HCl 2N. Si collegano le due provette tramite un tubo di vetro piegato ad U (tubo a squadra) e si scalda debolmente la provetta contenente la sostanza da analizzare. Se sono presenti ioni CO 3 2, la soluzione di idrossido di bario si intorbida per formazione del carbonato di bario. Per aggiunta di HCl il precipitato formatosi si scioglie. Calcinazione TARTRATI (C 4 O 6 H 4 2 ) Una piccola quantità di polvere viene calcinata in una capsula di porcellana. Si sviluppa un odore caratteristico di zucchero bruciato che conferma la presenza dei tartrati. Reazione con idrossido di sodio (NaOH) IONE AMMONIO (NH 4+ ) Si tratta la polvere con NaOH dil. e si riscalda leggermente. Si libera NH 3 gassosa riconoscibile dall odore o mediante una cartina indicatrice. 21
23 VIA UMIDA SOLFATI (SO 4 2 ) Reazione con cloruro di bario (BaCl 2 ) Soluzione alcalina + HCl dil. (scacciare bene i gas) + soluzione di BaCl 2. Si ottiene un precipitato bianco (solfato di bario) insolubile in HCl. OSSALATI (C 2 O 2 4 ) Reazione con cloruro di calcio (CaCl 2 ) Si acidifica la soluzione alcalina con CH 3 COOH fino a ph = 5 (scacciare bene i gas). Si aggiunge una soluzione di CaCl 2 : un precipitato bianco (ossalato di calcio) denota la presenza di ossalati. Conferma: Si lava il precipitato con H 2 O e si scioglie in H 2 SO 4 dil. Si riscalda e si aggiunge goccia a goccia una soluzione di KMnO 4 : si osserva scoloramento. Reazione con solfato di ferro NITRITI (NO 2 ) Si prepara una soluzione satura di FeSO 4 e la si acidifica con H 2 SO 4 dil. Su questa soluzione si stratifica dall alto un po della soluzione alcalina. Si ottiene una colorazione bruna di solfato di ferro nitrosile sotto forma di anello. Reazione con solfato di ferro NITRATI (NO 3 ) Si acidifica la soluzione alcalina con H 2 SO 4 dil. Si aggiunge FeSO 4. Si immerge la pipetta contenente H 2 SO 4 conc. sino a raggiungere il fondo della provetta e si stratifica. Nella zona di separazione tra i due liquidi (dovuta alla diversa densità) si forma un anello bruno. TIOSOLFATI (S 2 O 3= ) Reazione con nitrato di argento Un po di soluzione alcalina viene neutralizzata con HNO 3 dil. e trattata con un leggero eccesso di AgNO 3. La formazione di un precipitato bianco (tiosolfato di argento) che poi diventa bruno denoterà la presenza di tiosolfati. 22
24 ALOGENURI (Cl, Br, I ) Cloruri Si acidifica la soluzione alcalina con HNO 3 dil. (scacciare bene i gas), quindi si aggiunge AgNO 3. Si ottiene un precipitato bianco caseoso di AgCl (insolubile in HNO 3 dil., solubile in ammoniaca dil.) Cl + Ag + AgCl Bromuri 1) Si acidifica la soluzione alcalina con HNO 3 dil. (scacciare bene i gas), quindi si aggiunge AgNO 3. Si ottiene un precipitato giallo chiaro caseoso di AgBr (insolubile in HNO 3 dil., solubile in ammoniaca conc.) Br - + Ag + AgBr 2) Si acidifica la soluzione alcalina con H 2 SO 4 dil. (scacciare bene i gas), quindi si aggiunge cloroformio e NaClO gtt a gtt (agitare energicamente dopo ogni aggiunta). In presenza di Br - la fase cloroformica si colora in rosso vinoso (rosso arancio) che passa a giallo in eccesso di Cl ). Ioduri 2 Br - + ClO + 2 H + Br 2 + Cl + H 2 O 3 ClO ClO Cl Rosso vinoso Cl + ClO + 2 H + Br 2 + Cl 2 2 BrCl Giallo vinoso Cl 2 + H 2 O 1) Si acidifica la soluzione alcalina con HNO 3 dil. (scacciare bene i gas), quindi si aggiunge AgNO 3. Si ottiene un precipitato giallo caseoso di AgI (insolubile in HNO 3 dil. e in ammoniaca conc.) I + Ag + 2) Si acidifica la soluzione alcalina con H 2 SO 4 dil. (scacciare bene i gas), quindi si aggiunge cloroformio e NaClO gtt a gtt (agitare energicamente dopo ogni aggiunta). In presenza di I la fase cloroformica si colora in viola (rosso arancio) che passa a giallo in eccesso di Cl ). 2 I + ClO + 2 H + I 2 + Cl + H 2 O I Cl H 2 O 2 HIO Cl + 10 H + Viola Incolore AgI 23
25 Ridissoluzione selettiva degli alogenuri di argento Soluzione alcalina (Cl, Br, I ) Ossidazione selettiva degli alogenuri di argento con NaClO Soluzione alcalina (Br e I ) 1) HNO 3 dil. (scacciare bene i gas) 2) AgNO 3 (fino a completa ppt) 1) H 2 SO 4 dil. 2) Cloroformio (10 gtt) 3) NaClO (goccia a goccia) soluzione (controllare che la ppt sia completa) Precipitato (Ag I, AgBr, AgCl) NH 3 dil. Fase organica (viola) 2 I + ClO + 2 H + I 2 + Cl + H 2 O Viola NaClO (goccia a goccia) soluzione [Ag(NH 3 ) 2+ ] + Cl HNO 3 dil. Precipitato bianco (AgCl) Residuo (Ag I e AgBr) NH 3 conc. [Ag(NH 3 ) 2+ ] + Br Residuo bianco (Ag I) HNO 3 dil. Precipitato giallo (AgBr) H 2 O Residuo giallo (AgI) Fase organica (rosso vinoso) 2 Br + ClO + 2 H + Br 2 + Cl + H 2 O Rosso vinoso NaClO (goccia a goccia) Fase organica (giallo vinoso) Br 2 + Cl 2 2 BrCl Giallo vinoso 24
RICERCA RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO
 RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
Reazioni analitiche dello ione acetato
 Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) 3 bianco gelatinoso.
 Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
ANALISI CHIMICA QUALITATIVA
 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
II Gruppo: CH 3 - C + H 2 O CH 3 - C + H 2 S CH 3 - C + NH 4 OH TAA
 II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
Fe(OH) 3. Mn(OH) 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
Fe(OH) 3. Mn(OH) 2. bianco. MnO 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
SOSTANZE INORGANICHE
 SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
METODO DI VOLHARD. Nel metodo di Volhard gli ioni argento sono titolati con una soluzione standard di ione tiocianato: Ag + + SCN - AgSCN
 METODO DI VOLHARD Il metodo viene impiegato per la determinazione di ioni alogenuro quali I -, Cl -, Br -. Un eccesso noto di soluzione standard di nitrato di argento AgNO 3 viene aggiunto al campione
METODO DI VOLHARD Il metodo viene impiegato per la determinazione di ioni alogenuro quali I -, Cl -, Br -. Un eccesso noto di soluzione standard di nitrato di argento AgNO 3 viene aggiunto al campione
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
(Si identificano Ag +, Hg 2. , Pb 2+ ) - 1 GRUPPO - Reattivo Generale: HCl 2N. Soluzione. Precipitato. Soluzione. Residuo. Soluzione.
 Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
ANALISI ORGANICA Saggi preliminari
 ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
Esame (0) - solubilità dei composti e reaz - Codice Prova:
 1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
DI ANALISI CHIMICA QUALITATIVA NON SISTEMATICA DI ALCUNI IONI
 Schemaconreazioniok.3 PERCORSI DIDATTICI per studenti del 2 anno I.T.A.S. G. Raineri Piacenza NOTE DI ANALISI CHIMICA QUALITATIVA NON SISTEMATICA DI ALCUNI IONI Ernesto Colombani SEQUENZA DELLE OPERAZIONI
Schemaconreazioniok.3 PERCORSI DIDATTICI per studenti del 2 anno I.T.A.S. G. Raineri Piacenza NOTE DI ANALISI CHIMICA QUALITATIVA NON SISTEMATICA DI ALCUNI IONI Ernesto Colombani SEQUENZA DELLE OPERAZIONI
ESERCIZI DI RIEPILOGO GENERALE
 ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
TUTORAGGIO CHIMICA A.A. 2018/2019 Tutoraggio Chimica (Prof. L. Pilia) Nicola Melis
 TUTORAGGIO CHIMICA 18.12.2018 1 Es. 1: Il fluoruro di calcio si discioglie in piccole quantità in acqua. Calcolare il valore di K ps sapendo che [Ca 2+ ] = 2,3*10-4 CaF 2 (s) Ca 2+ (aq) + 2 F - (aq) Es.
TUTORAGGIO CHIMICA 18.12.2018 1 Es. 1: Il fluoruro di calcio si discioglie in piccole quantità in acqua. Calcolare il valore di K ps sapendo che [Ca 2+ ] = 2,3*10-4 CaF 2 (s) Ca 2+ (aq) + 2 F - (aq) Es.
Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI.
 Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
bario cloruro biidrato (200 mg; PM ) ferro(iii) cloruro esaidrato (200 mg; PM ) rame(ii) acetato monoidrato (200 mg; PM 181.
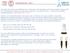 Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
IV Gruppo: H 2 S 2 H + + S = I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. rosa-salmone. nero.
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Esercitazione 3. Tipi di soluzioni. Cristallizzazione. Ricristallizzazione. Preparazione del nitrato di potassio
 Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
IV Gruppo: I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. nero. rosa-salmone. NiS
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Equilibri in soluzione acquosa unità 1, modulo G del libro
 Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
+ NO 2 + 3H 2 O = Ce +3 + NO 3 + 2H 3 O +, b) 0.478 g
 1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
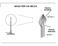 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2014/2015
 Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00
![CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00 CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00](/thumbs/68/59131328.jpg) CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2016/2017
 Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
ESERCIZI I PARTE. 1 Bilanciamento
 ESERCIZI I PARTE 1 1 Bilanciamento 1. H 3 PO 3 + CuO Cu 3 (PO 3 ) 2 +3H 2 O ) 2. Cs 2 O + H 2 O CsOH 3. P 2 O 5 + H 2 O HPO 3 4. NaCl + H 2 SO 4 Na 2 SO 4 + HCl 5. NaF + Mg(OH) 2 MgF 2 + NaOH 6. Al(OH)
ESERCIZI I PARTE 1 1 Bilanciamento 1. H 3 PO 3 + CuO Cu 3 (PO 3 ) 2 +3H 2 O ) 2. Cs 2 O + H 2 O CsOH 3. P 2 O 5 + H 2 O HPO 3 4. NaCl + H 2 SO 4 Na 2 SO 4 + HCl 5. NaF + Mg(OH) 2 MgF 2 + NaOH 6. Al(OH)
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Sostanze organiche: determinazioni qualitative
 Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Analizziamo i casi più frequenti. Acido forte Base forte Acido debole Base debole Idrolisi Tampone
 Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA
 CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
SOLUZIONE del COMPITO N 2
 SOLUZIONE del COMPITO N 2 Es.1) Bilanciare le seguenti equazioni ed assegnare il nome a ciascun reagente e prodotto: 3Fe(s) + 4H 2 O(g) FeO(s) + Fe 2 O 3 (S) + 4 H 2 (g) [N.B. FeO + Fe 2 O 3 = Fe 3 O 4
SOLUZIONE del COMPITO N 2 Es.1) Bilanciare le seguenti equazioni ed assegnare il nome a ciascun reagente e prodotto: 3Fe(s) + 4H 2 O(g) FeO(s) + Fe 2 O 3 (S) + 4 H 2 (g) [N.B. FeO + Fe 2 O 3 = Fe 3 O 4
Numero di ossidazione
 Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
SOLUZIONI COMPITO A DI CHIMICA DEL
 SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
1 Gruppo: Ag + ; Hg 2 2+ ; Pb ++ Reattivo precipitante: HCl dil (2N).
 1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
L ANALISI CHIMICA 2 SOSTANZA INCOGNITA. Analisi degli anioni e dei cationi. Riconoscimento della sostanza
 L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
NOMENCLATURA E REAZIONI
 NOMENCLATURA E REAZIONI Gli elementi chimici si dividono in: METALLI e NON METALLI I METALLI, perdendo elettroni, originano IONI POSITIVI (o CATIONI) I NON METALLI, acquistando elettroni, originano IONI
NOMENCLATURA E REAZIONI Gli elementi chimici si dividono in: METALLI e NON METALLI I METALLI, perdendo elettroni, originano IONI POSITIVI (o CATIONI) I NON METALLI, acquistando elettroni, originano IONI
Analisi di farmaci inorganici XI esercitazione di laboratorio
 Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
Problema 1 Mg + 2HCl H 2 + MgCl 2. di Mg 1 Mg 1 H 2 quindi 0,823 moli di H 2 di H 2
 REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
PROVA SCRITTA DI CHIMICA GENERALE ED INORGANICA Scienze e Tecnologie per l Ambiente
 10 Dicembre 2008 eventuale presenza di momento dipolare per I - 3 e per gli anioni dei sali: nitrato di sodio, perclorato di potassio. 2) a) Calcolare il ph di una soluzione di carbonato di sodio 0.10
10 Dicembre 2008 eventuale presenza di momento dipolare per I - 3 e per gli anioni dei sali: nitrato di sodio, perclorato di potassio. 2) a) Calcolare il ph di una soluzione di carbonato di sodio 0.10
NUMERO DI OSSIDAZIONE NOMENCLATURA CHIMICA
 NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI
 CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune con uno o più atomi in
CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune con uno o più atomi in
Equilibri acido-base
 Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
PROVA SCRITTA DI CHIMICA GENERALE ED INORGANICA Scienze e Tecnologie per l Ambiente 3 Febbraio 2010
 3 Febbraio 2010 eventuale presenza di momento dipolare per le molecole: PH 3, BrF 5, ione perclorato. 2) Calcolare il ph a 25 C di una soluzione acquosa 0.10 M di acido cloracetico (indicare con HA) sapendo
3 Febbraio 2010 eventuale presenza di momento dipolare per le molecole: PH 3, BrF 5, ione perclorato. 2) Calcolare il ph a 25 C di una soluzione acquosa 0.10 M di acido cloracetico (indicare con HA) sapendo
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE
 PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
REAZIONI IN SOLUZIONE
 REAZIONI IN SOLUZIONE - ACIDO-BASE SCAMBIO DI PROTONI HA + B A - + BH + - REDOX SCAMBIO DI ELETTRONI A OX + B RED A RED + B OX - REAZIONI DI SOLUBILIZZAZIONE AgCl (s) Ag + (aq) + Cl- (aq) - REAZIONI DI
REAZIONI IN SOLUZIONE - ACIDO-BASE SCAMBIO DI PROTONI HA + B A - + BH + - REDOX SCAMBIO DI ELETTRONI A OX + B RED A RED + B OX - REAZIONI DI SOLUBILIZZAZIONE AgCl (s) Ag + (aq) + Cl- (aq) - REAZIONI DI
CH 3 COOH 100% 20% Acido Acetico Glaciale. Acido Acetico Diluito. Pericolo. Attenzione H226 H314 H315 H319. n. Cas Cod. Ph.Eur.
 Acido Acetico Glaciale n. Cas 64-19-7 Cod. Ph.Eur. 1000400 CH 3 COOH 100% H226 H314 n. Cas 64-19-7 Cod. Ph.Eur. 1000402 Acido Acetico Diluito CH 3 COOH Attenzione 20% H315 H319 SOL n. Cas 7647-01-0 Cod.
Acido Acetico Glaciale n. Cas 64-19-7 Cod. Ph.Eur. 1000400 CH 3 COOH 100% H226 H314 n. Cas 64-19-7 Cod. Ph.Eur. 1000402 Acido Acetico Diluito CH 3 COOH Attenzione 20% H315 H319 SOL n. Cas 7647-01-0 Cod.
Corso di Laurea in Chimica e Tecnologia Farmaceutiche Esame di Chimica Analitica e Complementi di Chimica Modulo di Chimica Analitica 8 Novembre 2012
 Modulo di Chimica Analitica 8 Novembre 2012 1. Una soluzione viene preparata sciogliendo1210 mg di K 3 Fe(CN) 6 in 775 ml di acqua. Calcolare: a) la concentrazione analitica di K 3 Fe(CN) 6 b) la concentrazione
Modulo di Chimica Analitica 8 Novembre 2012 1. Una soluzione viene preparata sciogliendo1210 mg di K 3 Fe(CN) 6 in 775 ml di acqua. Calcolare: a) la concentrazione analitica di K 3 Fe(CN) 6 b) la concentrazione
REAZIONI IN SOLUZIONE
 REAZIONI IN SOLUZIONE - ACIDO-BASE [ SCAMBIO DI PROTONI HA + B D A - + BH + - REDOX [ SCAMBIO DI ELETTRONI A OX + B RED D A RED + B OX - REAZIONI DI SOLUBILIZZAZIONE AgCl (s) D Ag + (aq) + Cl- (aq) - REAZIONI
REAZIONI IN SOLUZIONE - ACIDO-BASE [ SCAMBIO DI PROTONI HA + B D A - + BH + - REDOX [ SCAMBIO DI ELETTRONI A OX + B RED D A RED + B OX - REAZIONI DI SOLUBILIZZAZIONE AgCl (s) D Ag + (aq) + Cl- (aq) - REAZIONI
BaSO. BaSO 4 è una costante quindi: K ps = prodotto di solubilità
 Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2015/2016
 Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Programma d esame PARTE PRIMA
Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Programma d esame PARTE PRIMA
ACIDI E BASI. c) il ph a metà della titolazione Risposta: a) [HCOOH] = 9.20x10 2 moli/litro; b) ph = 8.22; c) ph = 3.75
![ACIDI E BASI. c) il ph a metà della titolazione Risposta: a) [HCOOH] = 9.20x10 2 moli/litro; b) ph = 8.22; c) ph = 3.75 ACIDI E BASI. c) il ph a metà della titolazione Risposta: a) [HCOOH] = 9.20x10 2 moli/litro; b) ph = 8.22; c) ph = 3.75](/thumbs/56/39183185.jpg) ACIDI E BASI 1) 20.0 ml di una base debole BOH 0.5 M (Kb=3.0 x 10 5 ) sono stati titolati con HCl 1.2 M. Calcolare: a) il ph iniziale b) dopo l aggiunta di 4.0 ml della soluzione di HCl. c) all equivalenza
ACIDI E BASI 1) 20.0 ml di una base debole BOH 0.5 M (Kb=3.0 x 10 5 ) sono stati titolati con HCl 1.2 M. Calcolare: a) il ph iniziale b) dopo l aggiunta di 4.0 ml della soluzione di HCl. c) all equivalenza
RICERCA DELLA FUNZIONE CARBOSSILICA
 RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
Equilibri acido-base
 Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
Reazioni in soluzione acquosa
 Reazioni in soluzione acquosa Soluzioni, solvente e soluto Elettroliti Dissoluzione e solvatazione di elettroliti Equazioni chimiche Equazioni ioniche Concentrazione di soluzioni Reazioni di precipitazione
Reazioni in soluzione acquosa Soluzioni, solvente e soluto Elettroliti Dissoluzione e solvatazione di elettroliti Equazioni chimiche Equazioni ioniche Concentrazione di soluzioni Reazioni di precipitazione
PROVA SCRITTA DI CHIMICA GENERALE ED INORGANICA Scienze e Tecnologie per l Ambiente 1 Febbraio 2013
 1 Febbraio 2013 1) a) Scrivere le formule di Lewis, l ibridizzazione dell'atomo centrale, la geometria molecolare ed eventuale presenza di momento dipolare per SF 6 e per gli anioni dei sali: fosfato di
1 Febbraio 2013 1) a) Scrivere le formule di Lewis, l ibridizzazione dell'atomo centrale, la geometria molecolare ed eventuale presenza di momento dipolare per SF 6 e per gli anioni dei sali: fosfato di
2 H 2 + O 2 2 H 2 O 2 Na + 2 H 2 O 2 Na + + H OH
 Le equazioni chimiche devono essere BILANCIATE, cioè devono indicare le quantità di sostanze che partecipano alla reazione: 1) Legge di conservazione della massa: in una reazione chimica non si creano
Le equazioni chimiche devono essere BILANCIATE, cioè devono indicare le quantità di sostanze che partecipano alla reazione: 1) Legge di conservazione della massa: in una reazione chimica non si creano
Reazioni in Soluzioni Acquose. Capitolo 4
 Reazioni in Soluzioni Acquose Capitolo 4 Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza presente
Reazioni in Soluzioni Acquose Capitolo 4 Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza presente
Sostanze organiche: determinazioni qualitative
 Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
1 - Titolazioni acido-base e ph
 1 - Titolazioni acido-base e ph Procedimento (m.m. di NH 3 = 17,03) Moli di NaOH consumate (1,04 x 10-3 ) Moli di HCl iniziali (7,75 x 10-3 ) Moli di NH 3 (6,71 x 10-3 ) Massa di NH 3 (114,3 mg) Concentrazione
1 - Titolazioni acido-base e ph Procedimento (m.m. di NH 3 = 17,03) Moli di NaOH consumate (1,04 x 10-3 ) Moli di HCl iniziali (7,75 x 10-3 ) Moli di NH 3 (6,71 x 10-3 ) Massa di NH 3 (114,3 mg) Concentrazione
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol)
 STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formazione di...
 scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
ossidazione/riduzione, ossidante/riducente
 ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox +6-1 -1 +3-1 K 2 Cr 2 O 7 (aq) + HI(aq) KI(aq) + CrI 3 (aq) + I 2 (s) + H 2 O(l) 0 K 2 Cr 2 O 7 (aq) + 6HI(aq) KI(aq) + 2CrI
ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox +6-1 -1 +3-1 K 2 Cr 2 O 7 (aq) + HI(aq) KI(aq) + CrI 3 (aq) + I 2 (s) + H 2 O(l) 0 K 2 Cr 2 O 7 (aq) + 6HI(aq) KI(aq) + 2CrI
I gas nobili esistono (solo) allo stato di gas monoatomico
 I gas nobili esistono (solo) allo stato di gas monoatomico In condizioni normali non formano composti, dimostrando che i loro atomi non tendono a legarsi (inerzia chimica) Legame chimico G. N. Lewis (1916):
I gas nobili esistono (solo) allo stato di gas monoatomico In condizioni normali non formano composti, dimostrando che i loro atomi non tendono a legarsi (inerzia chimica) Legame chimico G. N. Lewis (1916):
H N. Mn 2+ +.. Fe 3+ +.. H 2 O
 CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni
 2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI
 COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
ESERCIZI DI STECHIOMETRIA
 ESERCIZI DI STECHIOMETRIA NOMENCLATURA Dare il nome ai seguenti composti: Al(NO 3 ) 3 Ba(OH) 2 BF 3 Ca(ClO) 2 CaCO 3 CaS Cu 2 SO 4 CaO CaSO 4 CaCl 2 CO CrCl 3 Fe(OH) 2 FePO 4 Fe 2 O 3 HClO HF PH 3 H 2
ESERCIZI DI STECHIOMETRIA NOMENCLATURA Dare il nome ai seguenti composti: Al(NO 3 ) 3 Ba(OH) 2 BF 3 Ca(ClO) 2 CaCO 3 CaS Cu 2 SO 4 CaO CaSO 4 CaCl 2 CO CrCl 3 Fe(OH) 2 FePO 4 Fe 2 O 3 HClO HF PH 3 H 2
CORSO DI LAUREA IN BIOLOGIA ECOLOGICA. Esercitazioni di Laboratorio di Chimica Generale ed Inorganica
 CORSO DI LAUREA IN BIOLOGIA ECOLOGICA Esercitazioni di Laboratorio di Chimica Generale ed Inorganica Anno Accademico 2002-2003 1 ESERCITAZIONE Titolazione di una soluzione di HCl con una soluzione di NaOH
CORSO DI LAUREA IN BIOLOGIA ECOLOGICA Esercitazioni di Laboratorio di Chimica Generale ed Inorganica Anno Accademico 2002-2003 1 ESERCITAZIONE Titolazione di una soluzione di HCl con una soluzione di NaOH
ESERCIZI. 1. Completa le seguenti reazioni e, se necessario, bilanciale: b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore!
 ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
Nomenclatura delle sostanze chimiche
 Nomenclatura delle sostanze chimiche SOSTANZE CHIMICHE!1 ELEMENTI Metalli Non metalli COMPOSTI Ossidi Anidridi Idrossidi Acidi Sali Idruri - ossiacidi - idracidi METALLI!2 Duttili Malleabili Buoni conduttori
Nomenclatura delle sostanze chimiche SOSTANZE CHIMICHE!1 ELEMENTI Metalli Non metalli COMPOSTI Ossidi Anidridi Idrossidi Acidi Sali Idruri - ossiacidi - idracidi METALLI!2 Duttili Malleabili Buoni conduttori
Riconoscimento sostanza incognita FU
 1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
Esame di Chimica Generale (M-Z) A.A (25 gennaio 2012)
 CORSO DI LAUREA IN SCIENZE BIOLOGICHE Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012) 1) Bilanciare la seguente ossidoriduzione: KMnO 4 + H 2 O 2 + H 2 SO 4 MnSO 4 + K 2 SO 4 + O 2 + H
CORSO DI LAUREA IN SCIENZE BIOLOGICHE Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012) 1) Bilanciare la seguente ossidoriduzione: KMnO 4 + H 2 O 2 + H 2 SO 4 MnSO 4 + K 2 SO 4 + O 2 + H
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Prova scritta CTF del 20- Gen NO 2
 Prova scritta CTF del 20Gen2011 1) Il Legame Covalente 2) Bilanciare in ambiente acido la seguente reazione di ossido riduzione: MnO 4 + NO 2 = Mn 2+ + NO 3 3) Applicando la teoria della repulsione delle
Prova scritta CTF del 20Gen2011 1) Il Legame Covalente 2) Bilanciare in ambiente acido la seguente reazione di ossido riduzione: MnO 4 + NO 2 = Mn 2+ + NO 3 3) Applicando la teoria della repulsione delle
ossidazione/riduzione, ossidante/riducente
 ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox 0 +5 +2 +4 Cu(s) + HNO 3 (aq) Cu(NO 3 ) 2 + NO 2 (g) + H 2 O(l) Determinazione dei numeri di ossidazione Cu(s) + 2HNO 3 (aq)
ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox 0 +5 +2 +4 Cu(s) + HNO 3 (aq) Cu(NO 3 ) 2 + NO 2 (g) + H 2 O(l) Determinazione dei numeri di ossidazione Cu(s) + 2HNO 3 (aq)
(appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio.
 ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
