- determinazione colorimetrica della concentrazione di una miscela proteica
|
|
|
- Adriano Contini
- 5 anni fa
- Visualizzazioni
Transcript
1 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2017/2018 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela proteica - Determinazione spettrofotometrica della concentrazione di una proteina pura - Determinazione spettrofotometrica dell attività enzimatica - Calcolo dell attività specifica Studente:.. Matricola:.
2 1. Cromatografia a scambio ionico In questo tipo di cromatografia, l adsorbimento delle particelle sulla fase stazionaria è determinato da interazioni di tipo elettrostatico (gruppi con cariche di segno opposto). Le proteine, che possiedono gruppi ionizzabili, possano portare una carica netta positiva o negativa, utilizzabile per il loro isolamento dalle miscele che le contengono. La carica netta che le proteine presentano dipende dal loro pk e dal ph della soluzione secondo l'equazione di Henderson-Hasselbalch. Le separazioni a scambio ionico sono condotte in colonne impaccate con una resina scambiatrice di ioni. Si tratta cioè di una resina in cui una matrice solida di supporto, in forma di sferule porose, che presenta gruppi funzionali carichi ad essa covalentemente legati. Negli scambiatori anionici la resina espone gruppi carichi positivamente (in generale, gruppi basici) che attraggono molecole cariche negativamente, e ne favoriscono l adsorbimento sulla fase solida, mentre le molecole neutre o cariche positivamente vengono eluite precocemente dalla colonna. Negli scambiatori cationici la situazione è invertita poiché la resina espone gruppi carichi negativamente (in generale, gruppi acidi) che attraggono molecole cariche positivamente. La resina DEAE Sepharose, utilizzata in questa esperienza di laboratorio, è costituita da una matrice di agarosio a cui è covalentemente legato il gruppo dietilamminoetile (pk~ 8.5) ed è equilibrata in tampone sodio-fosfato 10 mm, ph 8.0. Il campione da analizzare mediante cromatografia a scambio ionico è rappresentato da una miscela proteica costituita dalle seguenti proteine: pepsina, ribonucleasi A e alcool deidrogenasi.
3 La pepsina è un enzima, appartenente alla classe delle idrolasi ed alla sottoclasse EC Esso è contenuto nel succo gastrico ed ha la proprietà di scindere le proteine in grossi frammenti peptidici. La pepsina viene prodotta dalle cellule parietali dello stomaco sotto forma di pepsinogeno, pro-enzima inattivo con peso molecolare pari a ca., che si trasforma in pepsina in seguito a un processo catalizzato dalla pepsina stessa provocato dal ph acido del compartimento gastrico. L enzima maturo ha un peso molecolare di 36 kda e un punto isolelettrico pari a 2,2. La ribonucleasi pancreatica bovina (RNasi A) è un enzima di 124 residui, la cui stabilità è conferita da legami idrogeno intracatena e da quattro ponti disolfurici tra gli otto residui cisteinici. Ha una struttura compatta e molto stabile ed è in grado di scindere l RNA mediante una reazione di transesterificazione seguita dall idrolisi di un legame fosfodiesterico. Ha un peso molecolare pari a circa 14 kda e un punto isoelettrico di 8,64. Il suo coefficiente di estinzione molare è 0,71 per una soluzione 1 mg/ml a 278 nm. L alcool deidrogenasi (ADH) (o anche NAD-dipendente alcool deidrogenasi; NADH-Aldeide deidrogenasi; ecc.) è un enzima che catalizza preferenzialmente la conversione di alcool primari non ramificati nella loro corrispondente aldeide (EC ossidoreduttasi; riconosce gruppi-oh; NAD o NADP dipendente; primo membro del gruppo). L enzima nativo da lievito ha un peso molecolare di circa 140 kda, costituito da 4 subunità di 35 kda ognuna. Il suo punto isoelettrico è pari a 5,45. In seguito alla separazione cromatografica delle tre proteine descritte bisognerà identificarle in base alla posizione di eluizione di ognuna di esse.
4 METODICA dopo avere rimosso il tampone presente sulla resina, caricare 1 ml di miscela proteica; lavare la resina con 10 ml di tampone sodio-fosfato 10 mm, ph 7,0; eluire con un gradiente salino di NaCl : da 0 M a 0,3 M in tampone 10 mm sodiofosfato ph 7,0 (30 ml di tampone sodio-fosfato 10 mm, ph 7,0 e 30 ml di tampone sodio-fosfato 10 mm ph 7,0 contenente 0.3 M NaCl); Lavare con 20 ml di tampone sodio-fosfato 10 mm ph 7,0 contenente 1 M NaCl leggere i valori di assorbanza a 280 nm delle singole frazioni eluite dalla colonna e riportare in grafico i dati ottenuti. Frazioni Abs 280 nm Frazioni Abs 280 nm
5 Su un foglio di carta millimetrata costruire il cromatogramma mettendo in grafico con i valori di assorbanza (espressi come Optical Density = O.D.) ottenuti. Per convenzione si riportano in ordinata i valori di assorbanza misurati (O.D.280nm) e in ascissa il volume espresso come numero di frazione. O.D. 280 nm Fraction Number Osservare i picchi ottenuti ed identificare quello corrispondente alla ADH Collezionare tutto il contenuto delle frazioni con ADH in un unica provetta, chiuderla con parafilm e conservarla in frigorifero.
6 2. Determinazione spettrofotometrica della concentrazione proteica di: una proteina pura (metodo diretto ) e di una miscela proteica (metodo colorimetrico indiretto) Le tecniche Spettroscopiche o Spettrofotometriche si basano sull interazione, cioè lo scambio di energia, della radiazione elettromagnetica con la materia. Tale energia radiante può essere rappresentata come 1) un onda elettromagnetica fatta di un insieme fluttuante di campi elettrici e magnetici che si propagano nello spazio in modo periodico o 2) come una serie di pacchetti discreti d energia, i fotoni. La lunghezza d onda ( ) è definita come la distanza tra due punti dell onda aventi la stessa fase. L energia di questa onda elettromagnetica varia in funzione delle differenti lunghezze d onda. Lo spettro elettromagnetico rappresenta l insieme delle radiazioni ed è costituito da una serie di fotoni o d onde elettromagnetiche d energia crescente. Esso viene diviso in regioni caratteristiche corrispondenti a campi ben definiti di energia.
7 Spettroscopia UV/Visibile La regione dello spettro maggiormente usata per rilevare proteine in soluzione riguarda lunghezze d onda che vanno approssimativamente tra i 120~400 nm per l ultravioletto (anche se la zona utilizzata è più ristretta) e i 400~800 nm per il visibile. L interazione dell energia radiante a determinate lunghezze d onda con la materia viene rivelata da un apposito strumento, lo spettrofotometro. Ogni sostanza avrà una propria caratteristica lunghezza d onda a cui assorbirà la luce incidente e la misura di tale assorbimento in funzione della lunghezza d onda costituisce una sorta di impronta digitale della sostanza.
8 Dalla misura dell assorbanza di una soluzione proteica si possono ricavare due tipi di informazioni differenti a seconda del campione - una informazione qualitativa, cioè verificare se nella soluzione sono presenti questo tipo di molecole - Una informazione di concentrazione se trattasi di specie pura. Per la misurazione della concentrazione di una specie pura in soluzione, esiste un equazione che permette di calcolare la concentrazione di una sostanza in soluzione ed è la legge di Lambert-Beer, la quale può essere enunciata come segue: la quantità di luce assorbita da una soluzione è funzione della concentrazione della sostanza assorbente e della lunghezza del cammino ottico. L equazione risulta essere: A = l c A = Assorbanza misurate come densità ottiche (OD), cioè il valore che si legge sullo spettrofotometro; = Coeficiente di estinzione (Molare o mg/ml), cioè corrisponde all assorbanza misurata alla lunghezza d onda a cui la sostanza mostra il massimo di assorbimento, quando il campione è in concentrazione di 1M o 1 mg/ml e il cammino ottico è di 1 cm. l = cammino ottico, cioè lo spessore del campione, ovvero la distanza percorsa dallla luce nell attraversare il campione. La proteina di riferimento più usata è l albumina serica bovina il cui coefficiente di estinzione in mg/ml è di 0,67 OD280nm.
9 Determinazione della concentrazione proteica di una miscela (proteica): metodo indiretto Quando la soluzione è una miscela di proteine diverse, non è possibile applicare la spettrofotometria diretta per determinarne la concentrazione. Le varie specie proteiche avranno, infatti, ciascuna coefficienti di estinzione diversi. In questo caso si procede per via indiretta tramite metodo colorimetrico descritto in seguito. In questa procedura, la BSA rappresenta la proteina di riferimento in quanto è possibile determinarne la concentrazione esatta per via spettrofotometrica. La soluzione che vi sarà fornita è ad una concentrazione di 0,5 mg/ml. Reazione Colorimetrica di Bradford In soluzione acida, il colorante triarilmetano (Coomassie Blu) si lega alle proteine sviluppando una colorazione misurabile mediante uno spettrofotometro. Il massimo valore di assorbanza presentato dal colorante in soluzione è di 465 nm (λ max del colorante) ma quello del complesso colorante proteina (blu) subisce uno spostamento a 595 nm (λ max del complesso). Lo sviluppo di colore quindi si accompagna ad un aumento dell assorbanza del campione a 595 nm che è proporzionale alla quantità di proteine totali presenti nel campione. Per conoscere i valori di assorbanza a 595 nm dei complessi colorante-proteine (funzione della concentrazione proteica poiché il colorante è in largo eccesso) è necessario procedere alla costruzione della cosidetta retta di taratura del saggio. Essa si costruisce facendo reagire il reattivo di Bradford (Coomassie Blu in soluzione acida) con quantità note e crescenti ( g) di una soluzione di BSA di cui si è determinata la concentrazione con il metodo diretto. Preparare 600 l di soluzione contenente proteine (vedere schema) ed aggiungere 400 l del reattivo di Bradford. Mescolare e leggere l assorbanza della soluzione a 595 nm
10 Tubo Campione H 2 O Reattivo OD 595nm g 1 Bianco 600 l 400 l BSA 1 g = 2 l l 400 l 1 3 BSA 2 g = 4 l l 400 l 2 4 BSA 4 g = 8 l l 400 l 4 5 BSA 8 g = 16 l l 400 l 8 6 Miscela di carico 2 l 598 l 400 l 7 Miscela di carico 5 l 595 l 400 l - leggere contro bianco o sottrarre a ogni lettura (tubi 2-7) l assorbanza del bianco; - Costruire la retta di taratura ponendo in grafico su carta millimetrata i valori di assorbanza (ordinate) registrati contro i relativi g di BSA (ascisse); - Determinare la quantità di proteine presenti nella miscela (tubi 6-7), calcolando sulla retta di taratura a quanti g di proteina corrispondono le letture ottenute: g proteine/2 l miscela g proteine/5 l miscela = mg/ml = mg/ml La concentrazione proteica in mg/ml sarà una media aritmetica dei valori ottenuti La quantità di proteine totali si calcola moltiplicando il valore della concentrazione espressa in mg/ml per il volume del campione
11 Dosaggio spettrofotometrico della concentrazione della ADH eluita da colonna (metodo diretto) Poiché l ADH eluito da colonna cromatografica è omogeneo, la determinazione della sua concentrazione può essere effettuata direttamente per via spettrofotometrica servendoci del suo coefficiente di estinzione E1% = 14.6 (280 nm in acqua). 1. Dosaggio di attivita enzimatica Lo scopo di questa parte della esercitazione è quella di calcolare le unità enzimatiche di ADH attraverso un saggio di attività spettrofotometrico. Verrà dunque descritta la procedura: i) per la messa a punto di una miscela di saggio in cui l enzima ADH esplichi la sua attività catalitica e ii) per il calcolo delle unità enzimatiche. L ADH catalizza l ossidazione di alcoli primari in presenza del coenzima NAD +, ad un ph ottimale di 8.0; durante la reazione inversa le aldeidi sono ridotte in presenza di NADH ad un ph ottimale intorno alla neutralità. La variazione di assorbanza a 340 nm (variazione del rapporto forma ossidata e ridotta NAD + /NADH) per unità di tempo è misura dell attività enzimatica. ADH CH3-CH2-OH + NAD + O=CH-CH3 + NADH +H + Una unità enzimatica (U) è definita come la quantità di enzima richiesta per convertire 1 µmol di substrato in prodotto in 1 min in condizioni di temperatura definite (generalmente 25 o 30 C) e ad un valore di forza ionica e ph ottimale. Attraverso il saggio spettrofotomentrico si dovrà determinare la quantità (espressa in micromoli) di NADH che si forma in un minuto.
12 Saggio di attività dell alcool deidrogenasi: 1. miscela di reazione: 2 mm NAD +, 20 mm Etanolo in tampone sodio-fosfato M, ph 8. Mescolare 2.5 ml di tampone sodio-fosfato 0.1 M, ph 8, 0.4 ml di NAD M, 2 ml di etanolo 0.1 M e portare a 10 ml con H 2 O; 2. allestire i saggi di attività mescolando in una cuvetta 1 ml di miscela di reazione e: μl di miscela proteica pari a circa. g; μl di ADH purificata pari a circa. g; μl di ADH (controllo positivo) pari a circa. g registrare l incremento di assorbanza a 340 nm in funzione del tempo; 3. calcolare le µmoli di NADH formate in 1 ml di miscela di reazione: dividere l incremento di assorbanza per minuto ( A/min) per il coefficiente di estinzione millimolare (µmoli/ml) del NADH (OD a 340 nm 6. 22); 4. calcolare le unità di attività enzimatica/ml di soluzione saggiata, tenendo conto dei µl delle frazioni utilizzati per il saggio. (Una unità enzimatica è la quantità di enzima che converte in prodotto una µmole di substrato per minuto nelle condizioni ottimali di ph e temperatura per il saggio). moli NADH/ml x V finale (1000 l) U/ml = l utilizzati nel saggio Campione 5 l ADH (controllo positivo) Volume finale della miscela di reazione 1 ml 2 l Miscela di carico 1 ml 340nm 1 min U misurate U/ml Unità totali 5 l Miscela di carico 1 ml l ADH da colonna l ADH da colonna 1 ml 1 ml
13 Trascrivere i valori della quantità di proteine totali e unità enzimatiche totali ottenuti per ogni campione Calcolare l attività specifica dei singoli campioni Calcolare la resa (%) del processo di purificazione (Resa= Unità dopo cromatografia diviso unità iniziali) Calcolare il fattore di purificazione Campione Proteine totali U totali Attività specifica (attività/proteine) Resa Fattore di purificazione ADH Controllo positivo) Miscela di carico ADH da colonna
- determinazione colorimetrica della concentrazione di una miscela proteica. - Determinazione spettrofotometrica dell attività enzimatica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2012/2013 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2012/2013 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
- determinazione colorimetrica della concentrazione di una miscela proteica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2013/2014 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2013/2014 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE
 CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
A = εlc c = A/εl c = 0.2/38000 M -1 cm -1 1 cm c = M = 5 μm
 COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2006/2007. Corso di: Laboratorio di Biologia II Chimica Biologica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2006/2007 Corso di: Laboratorio di Biologia II Chimica Biologica Dott. Marcello MEROLA Parziale purificazione dell enzima Alcool Deidrogenasi
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2006/2007 Corso di: Laboratorio di Biologia II Chimica Biologica Dott. Marcello MEROLA Parziale purificazione dell enzima Alcool Deidrogenasi
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
Cosa determina l assorbanza di un cromoforo?
 Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer:
 Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer: Introduzione: La spettrofotometria o fotometria è una tecnica analitica che sfrutta il fenomeno dell'assorbimento
Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer: Introduzione: La spettrofotometria o fotometria è una tecnica analitica che sfrutta il fenomeno dell'assorbimento
V R V t. Proteine ad alto peso molecolare. Proteine a peso molecolare intermedio. Proteine a basso peso molecolare. Kd + piccolo.
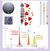 V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
Spettroscopia nell ultravioletto e nel visibile
 Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
Seminario di Cacciatore Rosalia
 Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
Fondamenti di spettroscopia. Spettrofotometria UV/Vis (Tecnica analitica)
 Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
Spettroscopia di assorbimento UV-Vis
 Spettroscopia di assorbimento UV-Vis Metodi spettroscopici La spettroscopia studia i fenomeni alla base delle interazioni della radiazione con la materia Le tecniche spettroscopiche sono tutte quelle tecniche
Spettroscopia di assorbimento UV-Vis Metodi spettroscopici La spettroscopia studia i fenomeni alla base delle interazioni della radiazione con la materia Le tecniche spettroscopiche sono tutte quelle tecniche
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2007/2008. Corso di: Laboratorio di Biologia II Chimica Biologica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2007/2008 Corso di: Laboratorio di Biologia II Chimica Biologica Dott. Marcello MEROLA Parziale purificazione dell enzima Alcool Deidrogenasi
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2007/2008 Corso di: Laboratorio di Biologia II Chimica Biologica Dott. Marcello MEROLA Parziale purificazione dell enzima Alcool Deidrogenasi
La cinetica enzimatica: Calcolo della K m e V max
 La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
Spettrofotometria. Foto di Clotilde B. Angelucci
 Spettrofotometria Foto di Clotilde B. Angelucci Le radiazioni elettromagnetiche e lo spettro Una radiazione elettromagnetica è caratterizzata dalla sua frequenza (ν) o dalla sua lunghezza d onda (λ). Queste
Spettrofotometria Foto di Clotilde B. Angelucci Le radiazioni elettromagnetiche e lo spettro Una radiazione elettromagnetica è caratterizzata dalla sua frequenza (ν) o dalla sua lunghezza d onda (λ). Queste
FORMULARIO DI CHIMICA
 ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica
 Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
La legge. Il colorimetro. L esperienza. Realizzato da. August Beer ( ) Johann Heinrich Lambert ( )
 LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
Dosaggio delle proteine
 Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Corso di Tecniche biomolecolari applicate Modulo Analisi di Macromolecole
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Corso di Tecniche biomolecolari applicate Modulo Analisi di Macromolecole 1. Elettroforesi su gel di poliacrilammide (PAGE nativa) L esperimento consiste
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Corso di Tecniche biomolecolari applicate Modulo Analisi di Macromolecole 1. Elettroforesi su gel di poliacrilammide (PAGE nativa) L esperimento consiste
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Curriculum Biologia della Nutrizione Anno Accademico 2012/2013 Corso di Chimica Biologica e laboratorio Dott. Eliodoro Pizzo Materiale Didattico Laboratorio
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Curriculum Biologia della Nutrizione Anno Accademico 2012/2013 Corso di Chimica Biologica e laboratorio Dott. Eliodoro Pizzo Materiale Didattico Laboratorio
ε (M -1 cm -1 ) Composto 260 nm 340 nm NAD ~ 0 NADPH
 1 Una soluzione contenente una miscela di NADPH e NAD + viene analizzata spettrofotometricamente. L assorbanza di tale miscela, misurata in una cuvetta da 1 cm di lunghezza, è pari a: A260 nm = 0,85 A340nm
1 Una soluzione contenente una miscela di NADPH e NAD + viene analizzata spettrofotometricamente. L assorbanza di tale miscela, misurata in una cuvetta da 1 cm di lunghezza, è pari a: A260 nm = 0,85 A340nm
Spettrofotometria UV-vis
 Spettrofotometria UV-vis Radiazione elettromagnetica: è una forma di trasmissione di energia in cui un campo elettrico e un campo magnetico si propagano attraverso onde nello spazio e nel tempo Interazione
Spettrofotometria UV-vis Radiazione elettromagnetica: è una forma di trasmissione di energia in cui un campo elettrico e un campo magnetico si propagano attraverso onde nello spazio e nel tempo Interazione
Chimica Analitica e Laboratorio 2. Modulo di Spettroscopia Analitica
 Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Determinazione della costante di dissociazione di un acido debole 2 Metodi di determinazione del pk d Potenziometria K d = + [ H ][ A
Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Determinazione della costante di dissociazione di un acido debole 2 Metodi di determinazione del pk d Potenziometria K d = + [ H ][ A
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
Corso di Tecniche biomolecolari applicate Modulo Analisi di Macromolecole
 Laboratorio Giorno 1 Corso di Tecniche biomolecolari applicate Modulo Analisi di Macromolecole Docente: Dott. Andrea Strazzulli Attività: Determinazione della concentrazione proteica di un campione. Parte
Laboratorio Giorno 1 Corso di Tecniche biomolecolari applicate Modulo Analisi di Macromolecole Docente: Dott. Andrea Strazzulli Attività: Determinazione della concentrazione proteica di un campione. Parte
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Spettroscopia molecolare: interazioni luce-materia
 Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
Determinazioni quantitative in farmacologia
 Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
GENERALITA SULLA CROMATOGRAFIA
 GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea
 la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea Analisi delle sue proprietà fisiche e biologiche Come viene modulata la sua espressione
la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea Analisi delle sue proprietà fisiche e biologiche Come viene modulata la sua espressione
La spettrofotometria è una tecnica analitica, qualitativa e quantitativa e permette il riconoscimento e la quantizzazione di una sostanza in base al
 SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
TECNICHE ANALITICHE DI RIVELAZIONE PER PROTEINE TECNICHE SPETTROSCOPICHE: Rivelazione in base all interazione fra proteine e radiazione
 TECNICHE ANALITICHE DI RIVELAZIONE PER PROTEINE TECNICHE SPETTROSCOPICHE: Rivelazione in base all interazione fra proteine e radiazione elettromagnetica. Determinazione della concentrazione (quantificazione)
TECNICHE ANALITICHE DI RIVELAZIONE PER PROTEINE TECNICHE SPETTROSCOPICHE: Rivelazione in base all interazione fra proteine e radiazione elettromagnetica. Determinazione della concentrazione (quantificazione)
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
Formazione di orbitali π. La differenza di energia tra due orbitali π è minore di quella tra due orbitali. Orbitali di non legame, n
 Spettroscopia Studia le interazione tra le radiazioni elettromagnetiche e la materia. Come sono fatti questi sistemi? La formazione dei legami chimici viene spiegata in termini di interazioni di orbitali
Spettroscopia Studia le interazione tra le radiazioni elettromagnetiche e la materia. Come sono fatti questi sistemi? La formazione dei legami chimici viene spiegata in termini di interazioni di orbitali
TIPI di CROMATOGRAFIA
 Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Analisi delle Proteine
 Analisi delle Proteine Elementi che costituiscono le proteine: idrogeno, carbonio, azoto, ossigeno e zolfo; tra cui l azoto è l elemento più distintivo nei cibi, l azoto varia da 13,4% a 19,1%. L analisi
Analisi delle Proteine Elementi che costituiscono le proteine: idrogeno, carbonio, azoto, ossigeno e zolfo; tra cui l azoto è l elemento più distintivo nei cibi, l azoto varia da 13,4% a 19,1%. L analisi
O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%.
 Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
04/04/2017 CLASSIFICAZIONE METODI SPETTROSCOPICI CHIMICA ANALITICA UNIVERSITÀ DEGLI STUDI DI TERAMO
 UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI I metodi spettroscopici si basano sulla interazione e misura della radiazione elettromagnetica
UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI I metodi spettroscopici si basano sulla interazione e misura della radiazione elettromagnetica
LABORATORIO DI CHIMICA FISICA I. Dr Ester Chiessi
 LABORATORIO DI CHIMICA FISICA I. Dr Ester Chiessi STUDIO CINETICO DELLA REAZIONE DI IDROLISI DELL ACETATO DI p- NITROFENILE IN SOLUZIONE ACQUOSA ALCALINA La reazione di idrolisi dell acetato di p-nitrofenile
LABORATORIO DI CHIMICA FISICA I. Dr Ester Chiessi STUDIO CINETICO DELLA REAZIONE DI IDROLISI DELL ACETATO DI p- NITROFENILE IN SOLUZIONE ACQUOSA ALCALINA La reazione di idrolisi dell acetato di p-nitrofenile
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO
 IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
SPETTROFOTOMETRIA UV/VIS
 SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
l'analisi dello spettro permette di individuare la natura della sostanza in esame
 L'analisi spettrofotometrica consiste nella misurazione di radiazioni elettromagnetiche per ottenere informazioni sia qualitative che quantitative: ogni sostanza assorbe o emette radiazioni di lunghezza
L'analisi spettrofotometrica consiste nella misurazione di radiazioni elettromagnetiche per ottenere informazioni sia qualitative che quantitative: ogni sostanza assorbe o emette radiazioni di lunghezza
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE
 RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
CINETICA ENZIMATICA - velocità di reazione
 [P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
[P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
Radiazione elettromagnetica
 Spettroscopia Radiazione elettromagnetica: energia che si propaga in un mezzo fenomeno ondulatorio dovuto alla propagazione simultanea nello spazio di un campo elettrico (E) e di uno magnetico (M) perpendicolari
Spettroscopia Radiazione elettromagnetica: energia che si propaga in un mezzo fenomeno ondulatorio dovuto alla propagazione simultanea nello spazio di un campo elettrico (E) e di uno magnetico (M) perpendicolari
differente ripartizione delle sostanze tra due fasi immiscibili
 Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
Scheda n.15. Vania Bresolin Cinetica enzimatica. Determinazione dell attività specifica di un enzima
 Scheda n.15 Vania Bresolin Cinetica enzimatica Determinazione dell attività specifica di un enzima ITAS Santorre di Santarosa Istituto Tecnico, settore Tecnologico Indirizzo Chimica, Materiali e Biotecnologie
Scheda n.15 Vania Bresolin Cinetica enzimatica Determinazione dell attività specifica di un enzima ITAS Santorre di Santarosa Istituto Tecnico, settore Tecnologico Indirizzo Chimica, Materiali e Biotecnologie
MA + H + MAH + Materiale: 500 cc di soluzione di NaOH 0.01 M 500 cc di soluzione di HCl 0.01 M fresca Metil-arancio (MA) Etanolo Acqua distillata
 Cambiamenti nell aspetto degli spettri di assorbimento elettronico del metilarancio in funzione del ph a seguito della reazione di protonazione del metilarancio. Scopo dell esperimento è osservare la variazione
Cambiamenti nell aspetto degli spettri di assorbimento elettronico del metilarancio in funzione del ph a seguito della reazione di protonazione del metilarancio. Scopo dell esperimento è osservare la variazione
LABORATORIO DI CHIMICA FISICA PER IL CORSO DI LAUREA IN SCIENZA DEI MATERIALI A.A. 2010/2011 DR. ESTER CHIESSI
 LABORATORIO DI CHIMICA FISICA ER IL CORSO DI LAUREA IN SCIENZA DEI MATERIALI A.A. 21/211 DR. ESTER CHIESSI DETERMINAZIONE DEI ARAMETRI TERMODINAMICI DI EQUILIBRIO DI UNA REAZIONE CHIMICA: LA FORMAZIONE
LABORATORIO DI CHIMICA FISICA ER IL CORSO DI LAUREA IN SCIENZA DEI MATERIALI A.A. 21/211 DR. ESTER CHIESSI DETERMINAZIONE DEI ARAMETRI TERMODINAMICI DI EQUILIBRIO DI UNA REAZIONE CHIMICA: LA FORMAZIONE
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Cromatografia di scambio ionico su colonna
 S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Cromatografia di scambio ionico su colonna La cromatografia è un metodo di
S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Cromatografia di scambio ionico su colonna La cromatografia è un metodo di
PROGETTO di ALTERNANZA SCUOLA LAVORO
 PROGETTO di ALTERNANZA SCUOLA LAVORO Formazione sul rischio specifico chimico e biologico Progettazione e sintesi di composti organici di interesse farmaceutico; determinazione quali-quantitativa Attività
PROGETTO di ALTERNANZA SCUOLA LAVORO Formazione sul rischio specifico chimico e biologico Progettazione e sintesi di composti organici di interesse farmaceutico; determinazione quali-quantitativa Attività
Tecniche spettrofotometriche e cromatografiche
 Tecniche spettrofotometriche e cromatografiche Biochimica e biotecnologie degli alimenti Lezione 3 Tecniche spettroscopiche Le radiazioni elettromagnetiche vengono rappresentate sia come un'onda elettromagnetica
Tecniche spettrofotometriche e cromatografiche Biochimica e biotecnologie degli alimenti Lezione 3 Tecniche spettroscopiche Le radiazioni elettromagnetiche vengono rappresentate sia come un'onda elettromagnetica
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI
 METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
CORSO di DIDATTICA LIBERA METODICHE SPETTROFOTOMETRICHE E LORO APPLICAZIONI FARMACOLOGICHE
 CORSO di DIDATTICA LIBERA METODICHE SPETTROFOTOMETRICHE E LORO APPLICAZIONI FARMACOLOGICHE Anna Cozzoli Sezione di Farmacologia Facoltà di Farmacia Bari, 11 Dicembre 2012 APPLICAZIONI DELLE METODICHE SPETTROFOTOMETRICHE
CORSO di DIDATTICA LIBERA METODICHE SPETTROFOTOMETRICHE E LORO APPLICAZIONI FARMACOLOGICHE Anna Cozzoli Sezione di Farmacologia Facoltà di Farmacia Bari, 11 Dicembre 2012 APPLICAZIONI DELLE METODICHE SPETTROFOTOMETRICHE
PURIFICAZIONE E CARATTERIZZAZIONE BIOCHIMICA DI UNA TREALASI DI INSETTO ESPRESSA COME PROTEINA ETEROLOGA IN Escherichia coli.
 PURIFICAZIONE E CARATTERIZZAZIONE BIOCHIMICA DI UNA TREALASI DI INSETTO ESPRESSA COME PROTEINA ETEROLOGA IN Escherichia coli. La trealasi (α,α-trealosio glucoidrolasi EC 3.2.1.28) è un enzima che catalizza
PURIFICAZIONE E CARATTERIZZAZIONE BIOCHIMICA DI UNA TREALASI DI INSETTO ESPRESSA COME PROTEINA ETEROLOGA IN Escherichia coli. La trealasi (α,α-trealosio glucoidrolasi EC 3.2.1.28) è un enzima che catalizza
cromatografia Esplorando le proteine
 Cromatografia Flavia Frabetti Tecnici di laboratorio 2010/2011 Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per
Cromatografia Flavia Frabetti Tecnici di laboratorio 2010/2011 Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
Elettroforesi = migrazione in campo elettrico
 Elettroforesi = migrazione in campo elettrico Molte molecole di interesse biologico possiedono gruppi ionizzabili. In opportune condizioni di ph presentano una carica elettrica + o e quindi sono in grado
Elettroforesi = migrazione in campo elettrico Molte molecole di interesse biologico possiedono gruppi ionizzabili. In opportune condizioni di ph presentano una carica elettrica + o e quindi sono in grado
La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione.
 Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Esercitazioni di Chimica Biologica AA PURIFICAZIONE DI UNA PROTEINA DI FUSIONE GST-CATECOLO 1,2 DIOSSIGENASI
 Esercitazioni di Chimica Biologica AA 2005-06 PURIFICAZIONE DI UNA PROTEINA DI FUSIONE GST-CATECOLO 1,2 DIOSSIGENASI Viene utilizzato il pellet cellulare congelato ottenuto dalla crescita di cellule di
Esercitazioni di Chimica Biologica AA 2005-06 PURIFICAZIONE DI UNA PROTEINA DI FUSIONE GST-CATECOLO 1,2 DIOSSIGENASI Viene utilizzato il pellet cellulare congelato ottenuto dalla crescita di cellule di
Cara&erizzazione della composizione e stru&ura delle molecole a&raverso misure di spe&roscopia. Proff. C. Ferrante e D. Pedron
 Cara&erizzazione della composizione e stru&ura delle molecole a&raverso misure di spe&roscopia Proff. C. Ferrante e D. Pedron 1 Radiazione Ele,romagne0ca Propagazione nello spazio e nel tempo: L onda si
Cara&erizzazione della composizione e stru&ura delle molecole a&raverso misure di spe&roscopia Proff. C. Ferrante e D. Pedron 1 Radiazione Ele,romagne0ca Propagazione nello spazio e nel tempo: L onda si
5- Estrazione ed analisi di DNA
 5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
Metodi spettroscopici
 Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
Chimica Analitica e Laboratorio 2. Modulo di Spettroscopia Analitica
 Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Spettroscopia UV-visibile 2 Trasmittanza - assorbanza La trasmittanza di un mezzo è la frazione di radiazione incidente trasmessa T =
Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Spettroscopia UV-visibile 2 Trasmittanza - assorbanza La trasmittanza di un mezzo è la frazione di radiazione incidente trasmessa T =
IMMUNODOSAGGI o DOSAGGI IMMUNOLOGICI E.L.I.S.A.
 IMMUNODOSAGGI o DOSAGGI IMMUNOLOGICI E.L.I.S.A. Alcune applicazioni degli anticorpi in ricerca (tecniche immunochimiche) Scopo sperimentale: IDENTIFICARE un determinato antigene (tecnica QUALITATIVA) QUANTIFICARE
IMMUNODOSAGGI o DOSAGGI IMMUNOLOGICI E.L.I.S.A. Alcune applicazioni degli anticorpi in ricerca (tecniche immunochimiche) Scopo sperimentale: IDENTIFICARE un determinato antigene (tecnica QUALITATIVA) QUANTIFICARE
Modulo 3. Lavorare con le proteine
 Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Quantizzazione del DNA con spettrofotometro
 Quantizzazione del DNA ed elettroforesi 1 Quantizzazione del DNA con spettrofotometro Al termine della metodica di estrazione, occorre quantificare il DNA isolato. Un metodo per quantificare in modo preciso
Quantizzazione del DNA ed elettroforesi 1 Quantizzazione del DNA con spettrofotometro Al termine della metodica di estrazione, occorre quantificare il DNA isolato. Un metodo per quantificare in modo preciso
Estrazione di acido salicilico con acetato di n-butile
 S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Estrazione di acido salicilico con acetato di n-butile L estrazione liquido-liquido
S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Estrazione di acido salicilico con acetato di n-butile L estrazione liquido-liquido
cromatografia Elettroforesi
 Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
LABORATORIO PLS CHIMICA DEI MATERIALI SINTESI E CARATTERIZZAZIONE DI NANOPARTICELLE D ORO (NANOGOLD)
 PIANO NAZIONALE LAUREE SCIENTIFICHE (PNLS1) La Scienza per una Migliore Qualità della Vita LABORATORIO PLS CHIMICA DEI MATERIALI SINTESI E CARATTERIZZAZIONE DI NANOPARTICELLE D ORO (NANOGOLD) Responsabile:
PIANO NAZIONALE LAUREE SCIENTIFICHE (PNLS1) La Scienza per una Migliore Qualità della Vita LABORATORIO PLS CHIMICA DEI MATERIALI SINTESI E CARATTERIZZAZIONE DI NANOPARTICELLE D ORO (NANOGOLD) Responsabile:
SIMULAZIONE ESAME DI CHIMICA ANALITICA PER BIOTECNOLOGIE 2018/19 Tempo concesso: 45 min (+ 5 min per ricopiare sulla scheda ottica)
 SIMULAZIONE ESAME DI CHIMICA ANALITICA PER BIOTECNOLOGIE 2018/19 Tempo concesso: 45 min (+ 5 min per ricopiare sulla scheda ottica) 1) Quali, fra le seguenti operazioni, non può essere utilizzata per preparare
SIMULAZIONE ESAME DI CHIMICA ANALITICA PER BIOTECNOLOGIE 2018/19 Tempo concesso: 45 min (+ 5 min per ricopiare sulla scheda ottica) 1) Quali, fra le seguenti operazioni, non può essere utilizzata per preparare
fase stazionaria fase mobile
 Cromatografia Insieme di tecniche che hanno lo scopo di separare una miscela nei suoi componenti, per permetterne il riconoscimento qualitativo e quantitativo. Sono basate sulla distribuzione dei vari
Cromatografia Insieme di tecniche che hanno lo scopo di separare una miscela nei suoi componenti, per permetterne il riconoscimento qualitativo e quantitativo. Sono basate sulla distribuzione dei vari
Analisi quantitativa dell interazione proteina-proteina
 Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Determinazione del contenuto di licopene
 Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
Lezione n. 20. Visibile. La spettroscopia UV/Visibile. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 20 Principi generali delle spettroscopie ottiche La spettroscopia UV/Visibile Visibile Antonino Polimeno 1 Spettroscopie ottiche (1) - Le tecniche di misura
Chimica Fisica Biotecnologie sanitarie Lezione n. 20 Principi generali delle spettroscopie ottiche La spettroscopia UV/Visibile Visibile Antonino Polimeno 1 Spettroscopie ottiche (1) - Le tecniche di misura
Determinazione dell attività enzimatica
 Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
METODI SPETTROSCOPICI
 METODI SPETTROSCOPICI D.C. Harris, Elementi di chimica analitica, Zanichelli Capitoli 7 e 8 Spettroscopia: originariamente era quella branca della scienza in cui si studiava come la luce (visibile) può
METODI SPETTROSCOPICI D.C. Harris, Elementi di chimica analitica, Zanichelli Capitoli 7 e 8 Spettroscopia: originariamente era quella branca della scienza in cui si studiava come la luce (visibile) può
Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo
 UNIVERSITÀ DEGLI STUDI DI PAVIA CORSO DI LAUREA INTERFACOLTÀ IN BIOTECNOLOGIE Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo Relatore:
UNIVERSITÀ DEGLI STUDI DI PAVIA CORSO DI LAUREA INTERFACOLTÀ IN BIOTECNOLOGIE Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo Relatore:
Cromatografia a scambio ionico HPLC per la determinazione di cationi ed anioni nelle acque potabili
 Cromatografia a scambio ionico HPLC per la determinazione di cationi ed anioni nelle acque potabili Azienda Sanitaria Provinciale di Catania Team Aziendale HTA LOGO ENTE Il gruppo di lavoro Francesco Barletta
Cromatografia a scambio ionico HPLC per la determinazione di cationi ed anioni nelle acque potabili Azienda Sanitaria Provinciale di Catania Team Aziendale HTA LOGO ENTE Il gruppo di lavoro Francesco Barletta
Fondamenti di spettrofotometria. Spettroscopia UV/Vis
 Fondamenti di spettrofotometria Spettroscopia UV/Vis Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi dell interazione
Fondamenti di spettrofotometria Spettroscopia UV/Vis Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi dell interazione
