DISPENSE DI LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III
|
|
|
- Gianluigi Torre
- 5 anni fa
- Visualizzazioni
Transcript
1 DISPENSE DI LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a- ESERCITAZIONE (D.P.I.: Occhiali guanti) Ø SAGGIO AL COCCIO (SOTTO CAPPA) Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE METALLORGANICHE Ø SAGGIO ALLA FIAMMA (SOTTO CAPPA) Ø SOLUBILITA SOSTANZE INORGANICHE COMPORTAMENTO ALLA CALCINAZIONE L'osservazione del comportamento di una sostanza alla calcinazione consente di distinguere fra sostanze inorganiche, organiche e metallorganiche. Si tratta di un saggio preliminare molto utile per giungere alla completa identificazione di una sostanza incognita. La calcinazione si effettua ponendo qualche milligrammo di sostanza in una capsula di porcellana e scaldando alla fiamma di un bunsen per qualche minuto. Per quanto i fenomeni osservabili siano molteplici, è bene distinguere due situazioni principali: si osserva formazione di particelle carboniose sostanza organica od organometallica Talvolta, la carbonizzazione non é molto evidente; ciò succede con composti organici che hanno tendenza a sublimare o composti metallo-organici con un contenuto molto basso di carbonio. Per distinguere tra composti organici ed organometallici si cerca, nel residuo carbonioso, la presenza di ceneri, cioè prodotti inorganici formati durante la calcinazione. - sostanza organometallica: si riscontra la presenza di cationi metallici. La ricerca viene effettuata tramite i comuni metodi dell'analisi inorganica qualitativa (vedi oltre). - sostanza organica: la ricerca dei cationi risulta negativa. In questo caso il residuo carbonioso si presenta nero-lucido; per prolungato riscaldamento esso può scomparire completamente lasciando la piastrina pulita oppure rimanere come una massa nera lucida rigonfia.
2 non si osserva formazione di residuo carbonioso sostanza inorganica In genere la sostanza non subisce alcuna alterazione, anche a temperature elevate. Talvolta però si osserva: - cambiamento di colore (termocromismo) (ZnO, TiO 2 ) - fusione (acido borico) - sublimazione con o senza fusione (NH 4 Cl, HgCl 2, Hg 2 Cl 2, HgI 2, zolfo, I 2 ). SOLUBILITA SOSTANZE ORGANICHE 1) SOLUBILITÀ IN SOLVENTE INERTI I solventi inerti generalmente impiegati sono: acqua Et 2 O 30 mg circa di sostanza (una punta di spatola) vengono introdotti in una provetta: si aggiunge 1 ml di solvente e si agita con una bacchetta di vetro. Se, dopo 3 o 4 minuti di agitazione, il composto non si è sciolto completamente, lo si considera insolubile in quel solvente. N.B.: Solubilità in acqua: la sostanza viene prima saggiata in acqua a freddo e, solo se necessario, a caldo. Se risulta solubile, possiamo avere tre possibilità (misurazione del ph): a) soluzione acquosa acida al tornasole: composto acido b) soluzione acquosa basica al tornasole: composto basico c) soluzione acquosa neutra al tornasole: composti neutri oppure acidi e basi deboli. Solamente nel caso in cui la sostanza sia risultata insolubile o scarsamente solubile in acqua, allora si procede a saggiarne la solubilità in solventi reattivi (soluzioni acquose diluite di alcali ed acidi): NaHCO 3 sol. satura Na 2 CO 3 2N NaOH 2N HCl 2N Le prove di solubilità nei solventi reattivi devono essere effettuate a temperatura ambiente per evitare processi di saponificazione, idrolisi ed altri. NaHCO 3 sol. satura: si sciolgono tutti i composti a carattere acido forte (acidi carbossilici, acidi solfonici, nitrofenoli). Na 2 CO 3 2N: si sciolgono, oltre ai precedenti, tutti i composti contenenti un gruppo funzionale acido di media forza (fenoli attivati, barbiturici, saccarina).
3 NaOH 2N: si sciolgono tutti i composti a carattere acido, sia forte che debole. Così si sciolgono, oltre ai precedenti, composti 1,3-dicarbonilici, solfonammidi, immidi, fenoli ed enoli. Se il composto è risultato insolubile sia in acqua che in alcali diluiti, allora si prova la solubilità in: HCl 2N: si sciolgono in generale i composti basici, come le ammine alifatiche e aromatiche; in generale, tuttavia, non è possibile distinguere tra basi deboli e basi forti. Molti composti di interesse farmaceutico presentano carattere anfotero e quindi risultano solubili sia in NaOH 2N che in HCl 2N (è il caso degli amminoacidi e dei sulfamidici). Per composti insolubili in acqua e nelle soluzioni acquose diluite basiche o acide si può valutare la solubilità in: H 2 SO 4 conc.: si sciolgono tutti i composti a carattere basico debolissimo (alcooli, eteri, aldeidi e chetoni), idrocarburi insaturi, idrocarburi aromatici attivati. Sono insolubili in acido solforico concentrato le paraffine, semplici idrocarburi aromatici non attivati e loro alogeno derivati. SOLUBILITA SOSTANZE METALLORGANICHE Le sostanze organometalliche iscritte nella F.U. possono essere costituite da: sali di acidi organici con cationi metallici sali di ammine o di ammonio quaternario con anioni inorganici Sul campione vengono effettuate prove di solubilità in acqua (con misura del ph se eventualmente solubile) ed etanolo.
4 ESAMI PRELIMINARI OSSERVAZIONE DELLE CARATTERISTICHE ORGANOLETTICHE Le proprietà organolettiche delle varie sostanze (stato fisico, colore, odore, sapore) sono indicate nelle singole monografie della F.U. sotto la voce caratteri. Nelle tabelle I-X i composti sono preliminarmente raggruppati in base allo stato fisico in sostanze liquide e solide. Nella tabella I, contenente i composti di natura inorganica, sono riportate eventuali indicazioni relative al colore. Infatti, tra le proprietà fisiche delle sostanze a carattere ionico, il colore è quella più utile ai fini del riconoscimento qualitativo, in quanto il composto assume il colore degli ioni costituenti. SAGGI ALLA FIAMMA Per effettuare il saggio si pulisca il filo di platino arroventandolo alla fiamma ed immergendolo poi in una provetta contenente 1-2 ml di HCl 2N; l'operazione va ripetuta sino a quando il filo non impartisce più alcuna colorazione alla fiamma. Quindi si pone su di un vetrino da orologio poca sostanza in esame e, con il filo bagnato di HCl 2N, si raccoglie una piccola quantità di composto. Si porta il filo alla base del mantello della fiamma, dove la temperatura è sensibilmente più bassa (in presenza di più sostanze si evidenzierà prima la colorazione della più volatile). zona ossidante zona di ossidazione inferiore zona riducente In tabella sono riportate le colorazioni tipiche di alcuni elementi: Sali di Colore della fiamma Li Ca K Na Rosso carminio (poco persistente) Rosso mattone (a sprazzi) Viola pallido (fucsia al vetrino al cobalto) Giallo (intenso e persistente) Ba Verde chiaro (attenzione BaSO 4 ) Cu Verde-azzurro B Verde smeraldo
5 SOLUBILTA SOSTANZE INORGANICHE 1) SOLUBILITÀ IN SOLVENTE INERTE: ACQUA Il saggio si esegue ponendo una piccola quantità di sostanza nel tubo da saggio con 1-2 ml di acqua deionizzata. In caso di insolubilizzazione parziale o completa scaldare su bagno maria. Si potranno avere due casi: sostanze solubili in acqua (vedi allegata Tabella IIIA) sostanze insolubili in acqua (vedi allegata Tabella IIIB) SOLUBILITA IN ACQUA DEI SALI PIU COMUNI SOLUBILI IN ACQUA sali alcalini ed ammoniacali nitrati, nitriti cloruri (eccetto AgCl, Hg 2 Cl 2, PbCl 2, CuCl) acetati (CH 3 COOAg poco solubile) solfati (eccetto BaSO 4, CaSO 4, PbSO 4, HgSO 4, Ag 2 SO 4, SrSO 4 ) perclorati (KClO 4 poco solubile) POCO SOLUBILI carbonati fosfati idrossidi ossidi ossalati borati solfuri fluoruri solfiti arseniti arseniati cromati (di metalli pesanti) 2) SOLUBILITÀ IN SOLVENTI REATTIVI 2.A) SOSTANZE INORGANICHE IDROSOLUBILI (TABELLA IIIA) - determinazione del ph con cartina universale Il valore di ph può indicare la presenza di acidi, sali acidi, sali ad idrolisi acida, idrossidi, sali basici, sali ad idrolisi basica, sali ad idrolisi neutra. - trattamento con HCl 2N (due provette) Ad una piccola quantità di sostanza nel tubo da saggio si addizionano 1-2 ml di HCl 2N. La solubilità del campione in HCl 2N può essere accompagnata da fenomeni di importanza analitica: Con effervescenza: CO 2, incolore ed inodore, verificabile per gorgogliamento in acqua di barite carbonati e bicarbonati SO 2, visibile su cartina allo iodio solfiti e tiosolfati 5
6 Senza effervescenza: I 2, evidenziabile con cartina alla salda d amido iodati ossidi, sali basici, idrossidi di cationi diversi da Ag +, Pb 2+, Hg 2 2+, Sb 3+ e Bi 3+ - (prima provetta) trattamento con BaCl 2 precipitazione dei solfati di magnesio, sodio, zinco, ecc. - (seconda provetta) trattamento NaOH 2N Addizionare alla stessa soluzione acida precedentemente ottenuta 1-2 ml di NaOH 2N precipitazione degli idrossidi insolubili (quelli anfoteri tornano in soluzione) - acidificazione di una nuova soluzione acquosa del composto con HNO 3 conc. e trattamento con AgNO 3 Si solubilizza il composto in esame in acqua e si addizionano due gocce di HNO 3 concentrato. Si agita e si tratta la soluzione con AgNO 3 (usare i guanti!!) precipitazione degli alogenuri di argento. 2.B) SOSTANZE INORGANICHE NON IDROSOLUBILI (TABELLA IIIB) - trattamento con HCl 2N del campione: (vedi sopra) - trattamento con NaOH 2N (sulla stessa provetta o su un altra provetta) precipitazione degli idrossidi di metalli alcalino-terrosi o dissoluzione di I 2. 6
7 Ephedrine Ephedrine hydrochloride?
8 L-Ascorbic acid propil 4-idrossibenzoato Sulfaguanidine
9 Acido salicilico ph sol. Acquosa: Salicilato di sodio?
10 Acido ace;lsalicilico Resorcinolo Caffeina Isoniazide
11 Dapsone Timolo Mentolo Canfora
12 COMPORTAMENTO INORGANICI AL COCCIO: - OSSIDO DI ZINCO: - SODIO TIOSOLFATO: - AMMONIO CLORURO: - POTASSIO IODURO: - ACIDO BORICO/TETRABORATO DI SODIO
13 SUBLIMAZIONE Sublimazione del cloruro di ammonio, acido salicilico, timolo/mentolo, Iodio D.P.I.: Occhiali, guanti, facciale filtrante Occorrente: 1 vetrino da orologio, becher, spatola, piastra scaldante. Accendere la piastra riscaldante a circa C. Mettere 2-3 spatolate di sostanza da purificare nel becher e coprire con il vetrino da orologio. Mettere il tutto sulla piastra riscaldante calda (utilizzando le pinze di metallo) e scaldare per ottenere la sublimazione. Con le pinze di metallo allontanare dalla piastra l apparecchio per la sublimazione e poggiarlo sul cubo/ parallelepipedo di legno (attenzione non poggiarlo sul banco, l escursione termica troppo rapida potrebbe rompere il becher). Lasciar raffreddare l apparecchio sublimatorerecuperare in il sublimato grattandolo dalle pareti del vetrino da orologio con la spatola e raccoglierlo in un vetrino pulito. La sublimazione può essere effettuata anche in una provetta, su un vetrino coperto da un imbuto, su due vetrini o in un sublimatore a dito freddo.
14 CRISTALLIZZAZIONE Acido salicilico Acido benzoico Acido acetilsalicilico D.P.I.: Occhiali, guanti Occorrente: beuta da 25 ml; bacchetta di vetro; pinze di legno; imbutino di vetro; carta da filtro; portaprovette e una provetta, 3-4 spatolate abbondanti di ac. Benzoico, vengono poste in una beuta da 25 ml. Nella beuta deve essere aggiunta una quantità di acqua tale da lasciare abbondante corpo di fondo a freddo ma portata all ebollizione deve essere in grado di sciogliere la sostanza. NOTA: Non riempire mai la beuta più di 1/3 del suo volume. Per ottenere questo si aggiunge una piccola quantità di H 2 O. Si riscalda all ebollizione su piastra la sospensione agitando continuamente prendendo la beuta con una pinza di legno (non di metallo). Se all ebollizione la sostanza non risulta disciolta, si deve aggiungere ancora acqua in piccole quantità, riportare il tutto all ebollizione, finché la dissoluzione è completa. A dissoluzione completata all ebollizione allontanare la beuta dalla piastra ed attendere il lento raffreddamento. Si osserva la precipitazione di acido benzoico in scaglie iridescenti. Si prepara il filtro a pieghe, lo si pone nell imbuto e l imbuto a sua volta si pone su una provetta pulita. Si raccoglie in maniera quantitativa tutto il cristallizzato sul filtro a pieghe e il filtrato (acque madri di cristallizzazione) nella provetta. Il cristallizzato si lava con H 2 O distillata fredda (2 lavaggi da circa 1-2 ml). Si lascia asciugare a T ambiente; quando il cristallizzato è secco si controlla la purezza determinando il pf. Le acque di cristallizzazione si scartano nel recipiente per lo smaltimento delle soluzioni.
15 CRISTALLIZZAZIONE CRISTALLIZZAZIONE DELL ACIDO SALICILICO DA ACQUA. Pesare 1 g di acido salicilico grezzo nella beuta smerigliata da 100 ml e aggiungere 30 ml di H 2 O distillata. Porre su piastra scaldante, montando sulla beuta la canna refrigerante (o condensatore) e mandare a reflusso (100 C) la soluzione. Preparare a parte una beuta a collo non smerigliato con 10 ml di H 2 O distillata ed introdurvi l imbuto di vetro portante un filtro a pieghe. Porlo sulla piastra e tenerlo al caldo Eseguire la filtrazione a caldo e raffreddare, si osserva la formazione di un precipitaro bianco. Filtrare il precipitato, essiccare il solido purificato e controllarne la purezza misurando il p.f. (teorico 122,5 C) CRISTALLIZZAZIONE DA SOLVENTE MISTO (aspirina da H 2 O/Etanolo). Pesare 5 g di aspirina grezza nella beuta smerigliata da 100 ml e aggiungere 15 ml di Etanolo. Porre su piastra scaldante all ebollizione. Quando tutto il solido è passato in soluzione, allontanare cautamente dalla fonte di calore. Versare 40 ml di H 2 O distillata e lasciare raffreddare (porre la beuta in ghiaccio). Filtrare il precipitato, essiccare il solido purificato e controllarne la purezza misurando il p.f. (teorico 130 C).
LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III
 LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a - 2 a ESERCITAZIONE Ø SAGGIO AL COCCIO Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE METALLORGANICHE Ø SAGGIO ALLA FIAMMA Ø SOLUBILITA
LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a - 2 a ESERCITAZIONE Ø SAGGIO AL COCCIO Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE METALLORGANICHE Ø SAGGIO ALLA FIAMMA Ø SOLUBILITA
Riconoscimento sostanza incognita FU
 Riconoscimento sostanza incognita FU 1. Calcinazione: Carbonizza e non lascia residuo o caramellizza: Sostanza organica Determinazione p.f. Determinazione p.f. 1 determinazione primo capillare 2 determinazione
Riconoscimento sostanza incognita FU 1. Calcinazione: Carbonizza e non lascia residuo o caramellizza: Sostanza organica Determinazione p.f. Determinazione p.f. 1 determinazione primo capillare 2 determinazione
Riconoscimento sostanza incognita FU
 1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO
 RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
(Si identificano Ag +, Hg 2. , Pb 2+ ) - 1 GRUPPO - Reattivo Generale: HCl 2N. Soluzione. Precipitato. Soluzione. Residuo. Soluzione.
 Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
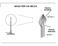 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
Reazioni analitiche dello ione acetato
 Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Saggi preliminari. Esame organolettico Combustione Saggi di solubilità Comportamento chimico
 Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI.
 Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
Fasi di identificazione di una sostanza
 Fasi di identificazione di una sostanza Serie di operazioni attraverso le quali è possibile ottenere i dati sul comportamento chimico e fisico del composto, che poi devono essere confrontati con quelli
Fasi di identificazione di una sostanza Serie di operazioni attraverso le quali è possibile ottenere i dati sul comportamento chimico e fisico del composto, che poi devono essere confrontati con quelli
Saggi preliminari. Esame organolettico Combustione Saggi di solubilità Comportamento chimico
 Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
TERZA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 TERZA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Terza Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbossilica Ricerca del Carattere Acido Saggio di Angeli e Rimini
TERZA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Terza Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbossilica Ricerca del Carattere Acido Saggio di Angeli e Rimini
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2016/2017
 Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Sostanze organiche: determinazioni qualitative
 Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni
 Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
RICERCA RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
ACIDO ACETILSALICILICO. Fenomeni visibili con FeCl 3 dopo idrolisi
 ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica
 NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
OSSIDAZIONI CON PERMANGANATO DI POTASSIO
 OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2014/2015
 Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Titolo: Raccomandazioni per la conservazione di campioni
 Sigla documento: Acidità e Alcalinità Vol. 500 ml Polietilene, vetro Refrigerazione (4 C) Aldeidi (Composti carbonilici) Vol. 500 ml Vetro scuro Refrigerazione (4 C) Anidride carbonica (Biossido di carbonio)
Sigla documento: Acidità e Alcalinità Vol. 500 ml Polietilene, vetro Refrigerazione (4 C) Aldeidi (Composti carbonilici) Vol. 500 ml Vetro scuro Refrigerazione (4 C) Anidride carbonica (Biossido di carbonio)
3011 Sintesi dell acido eritro-9,10-diidrossistearico dall acido oleico
 311 Sintesi dell acido eritro-9,1-diidrossistearico dall acido oleico COOH KMnO 4 HO COOH NaOH HO C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Riferimento in letteratura: Lapworth,
311 Sintesi dell acido eritro-9,1-diidrossistearico dall acido oleico COOH KMnO 4 HO COOH NaOH HO C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Riferimento in letteratura: Lapworth,
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
ESPERIENZA 4. Permanganometria
 ESPERIENZA 4 Permanganometria Il permanganato di potassio è uno dei titolanti più frequentemente usati nell analisi volumetrica per via redox. Può essere usato in soluzione acida, neutra o leggermente
ESPERIENZA 4 Permanganometria Il permanganato di potassio è uno dei titolanti più frequentemente usati nell analisi volumetrica per via redox. Può essere usato in soluzione acida, neutra o leggermente
Analisi di farmaci inorganici XI esercitazione di laboratorio
 Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
Esercitazione 6. Chimica biologica del Fe. Il Ferro ) 2 (SO 4 6H 2. Fe(NH 4
 Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
RICERCA DELLA FUNZIONE CARBOSSILICA
 RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA
 CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
Sintesi verde malachite
 Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
SECONDA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 SECONDA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Seconda Esperienza di Laboratorio Riconoscimento del doppio legame Saggio con KMnO 4 (Baeyer) Riconoscimento della struttura aromatica Saggio di
SECONDA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Seconda Esperienza di Laboratorio Riconoscimento del doppio legame Saggio con KMnO 4 (Baeyer) Riconoscimento della struttura aromatica Saggio di
Sostanze organiche: determinazioni qualitative
 Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
Isolamento della caffeina dalle foglie di tè
 SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
Attività laboratoriale di «Trasformazione dei prodotti»
 Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
1 Gruppo: Ag + ; Hg 2 2+ ; Pb ++ Reattivo precipitante: HCl dil (2N).
 1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI
 COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
SOSTANZE INORGANICHE
 SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
Chimica Inorganica e Laboratorio
 Chimica Inorganica e Laboratorio Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni L esperienza 2 consiste nell osservazione della variazione periodica delle proprietà di due gruppi, le
Chimica Inorganica e Laboratorio Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni L esperienza 2 consiste nell osservazione della variazione periodica delle proprietà di due gruppi, le
CHIMICA ORGANICA - laboratorio AA 2012/13
 CHIMICA ORGANICA - laboratorio AA 2012/13 Esperienza 1 SEPARAZIIONE ACIIDO--BASE.. CROMATOGRAFIIA ssu STRATO SOTTIILE ((TLC)).. L esperienza si propone di separare tre composti mediante estrazione da solvente
CHIMICA ORGANICA - laboratorio AA 2012/13 Esperienza 1 SEPARAZIIONE ACIIDO--BASE.. CROMATOGRAFIIA ssu STRATO SOTTIILE ((TLC)).. L esperienza si propone di separare tre composti mediante estrazione da solvente
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
QUARTA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 QUARTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quarta Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbonilica Formazione di 2,4-dinitrofenilidrazoni (reazione
QUARTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quarta Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbonilica Formazione di 2,4-dinitrofenilidrazoni (reazione
II Gruppo: CH 3 - C + H 2 O CH 3 - C + H 2 S CH 3 - C + NH 4 OH TAA
 II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE
 PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
SESTA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 SESTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Settima Esperienza di Laboratorio Prove di solubilità Riconoscimento degli α-amminoacidi Saggio della ninidrina Riconoscimento dei Sulfamidici Misura
SESTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Settima Esperienza di Laboratorio Prove di solubilità Riconoscimento degli α-amminoacidi Saggio della ninidrina Riconoscimento dei Sulfamidici Misura
Prima esperienza di Laboratorio. Alcune reazioni del rame
 Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
ANALISI CHIMICA QUALITATIVA
 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
Occorrente: mascherina; guanti; spatola, capillari chiusi per pf, coccio di porcellana porosa.
 PRIMA ESERCITAZIONE DETERMINAZIONE PUNTO DI FUSIONE CON IL METODO DEL CAPILLARE Occorrente: mascherina; guanti; spatola, capillari chiusi per pf, coccio di porcellana porosa. METODO DEL CAPILLARE CON IL
PRIMA ESERCITAZIONE DETERMINAZIONE PUNTO DI FUSIONE CON IL METODO DEL CAPILLARE Occorrente: mascherina; guanti; spatola, capillari chiusi per pf, coccio di porcellana porosa. METODO DEL CAPILLARE CON IL
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo)
 4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formazione di...
 scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) H 2 SO 4. Quantità: Acido salicilico 5.0 g (PM = 138.
 ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
Leggere attentamente il file sulla sicurezza prima di accedere al laboratorio
 Didattica della Chimica organica (2 CFU, 16h) PAS/TFA A012/A013 16 ore: 4 ore Lezioni frontali: Lunedì 9 febbraio 2015, ore 15.00-16.30 mercoledì 11 febbraio 2015, ore 15.00-16.30 Aula A1 III piano edificio
Didattica della Chimica organica (2 CFU, 16h) PAS/TFA A012/A013 16 ore: 4 ore Lezioni frontali: Lunedì 9 febbraio 2015, ore 15.00-16.30 mercoledì 11 febbraio 2015, ore 15.00-16.30 Aula A1 III piano edificio
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2017/2018
 Facoltà di Farmacia e Medicina Anno Accademico 2017/2018 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2017/2018 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
bario cloruro biidrato (200 mg; PM ) ferro(iii) cloruro esaidrato (200 mg; PM ) rame(ii) acetato monoidrato (200 mg; PM 181.
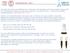 Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) 3 bianco gelatinoso.
 Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
L ANALISI CHIMICA 2 SOSTANZA INCOGNITA. Analisi degli anioni e dei cationi. Riconoscimento della sostanza
 L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
ESTRAZIONE DI UN COMPOSTO ACIDO, UNO BASICO E UNO NEUTRO DA UNA FASE INIZIALE ORGANICA
 ESTRAZIONE DI UN COMPOSTO ACIDO, UNO BASICO E UNO NEUTRO DA UNA FASE INIZIALE ORGANICA L'obiettivo dell esperienza è quello di separare una miscela costituita da un composto organico con caratteristiche
ESTRAZIONE DI UN COMPOSTO ACIDO, UNO BASICO E UNO NEUTRO DA UNA FASE INIZIALE ORGANICA L'obiettivo dell esperienza è quello di separare una miscela costituita da un composto organico con caratteristiche
Chimica Generale. Reazioni Chimiche. Reazioni Chimiche
 Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
EQUILIBRI SOLUBILITA. AgNO 3 + H 2 O. Ag + + NO 3- + H 2 O. Provetta 1 : Ag + + NO 3- + H 2 O NaCl + H 2 O Na + + Cl - + H 2 O
 a) Mettere in due provette ca. 2 ml della soluzione di AgNO 3, poi aggiungere in una 34 gocce di NaCl e nell altra 3 4 gocce di K 2 CrO 4 AgNO 3, NaCl, K 2 CrO 4 sono solubili in acqua. In soluzione avremo:
a) Mettere in due provette ca. 2 ml della soluzione di AgNO 3, poi aggiungere in una 34 gocce di NaCl e nell altra 3 4 gocce di K 2 CrO 4 AgNO 3, NaCl, K 2 CrO 4 sono solubili in acqua. In soluzione avremo:
 ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
Esercitazione 3. Tipi di soluzioni. Cristallizzazione. Ricristallizzazione. Preparazione del nitrato di potassio
 Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
ANALISI ORGANICA Saggi preliminari
 ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico.
 Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2013/2014
 Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina I.
Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina I.
Sintesi dell acetanilide
 Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
PRINCIPIO TESTATO: reazioni di sintesi, doppio scambio con precipitazione, eso-endotermiche e di ossido-riduzione.
 TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
Calcoli stechiometrici in soluzione (Cap. 12)
 Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
Riconoscimento dei Glucidi (Glucosio):
 Riconoscimento dei Glucidi (Glucosio): Materiale occorrente: Soluzione di Glucosio Liquido di Feheling A (soluzione di solfato rameico pentaidrato (CuSO 4 5 H 2 O)) Liquido di Feheling B (soluzione di
Riconoscimento dei Glucidi (Glucosio): Materiale occorrente: Soluzione di Glucosio Liquido di Feheling A (soluzione di solfato rameico pentaidrato (CuSO 4 5 H 2 O)) Liquido di Feheling B (soluzione di
Smistamento sistema+co H. Staudinger
 Smistamento sistema+co H. Staudinger onsente mediante procedimen+ sistema+ci lo smistamento in gruppi di una miscela incognita sulla base delle diverse cara8eris+che chimico-fisiche dei componen+ Frazione
Smistamento sistema+co H. Staudinger onsente mediante procedimen+ sistema+ci lo smistamento in gruppi di una miscela incognita sulla base delle diverse cara8eris+che chimico-fisiche dei componen+ Frazione
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
ACIDO ACETILSALICILICO. Fenomeni visibili con FeCl 3 dopo idrolisi
 ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
(appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio.
 ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
+ NO 2 + 3H 2 O = Ce +3 + NO 3 + 2H 3 O +, b) 0.478 g
 1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Esperienza n. 5 Preparazione di (NH 4 ) 2 [Cu(C 2 O 4 ) 2 ] 2H 2 O
![Esperienza n. 5 Preparazione di (NH 4 ) 2 [Cu(C 2 O 4 ) 2 ] 2H 2 O Esperienza n. 5 Preparazione di (NH 4 ) 2 [Cu(C 2 O 4 ) 2 ] 2H 2 O](/thumbs/73/68788801.jpg) Esperienza n. 5 Preparazione di (NH ) 2 [Cu(C 2 O ) 2 ] 2H 2 O OBBIETTIVI Lo scopo di questa esperienza è quello di preparare il sale complesso (NH)2[Cu(C2O)2] 2H2O. INTRODUZIONE Il (NH)2[Cu(C2O)2] 2H2O
Esperienza n. 5 Preparazione di (NH ) 2 [Cu(C 2 O ) 2 ] 2H 2 O OBBIETTIVI Lo scopo di questa esperienza è quello di preparare il sale complesso (NH)2[Cu(C2O)2] 2H2O. INTRODUZIONE Il (NH)2[Cu(C2O)2] 2H2O
Smistamento sistematico H. Staudinger
 Smistamento sistematico H. Staudinger Consente mediante procedimenti sistematici lo smistamento in gruppi di una miscela incognita sulla base delle diverse caratteristiche chimico-fisiche dei componenti.
Smistamento sistematico H. Staudinger Consente mediante procedimenti sistematici lo smistamento in gruppi di una miscela incognita sulla base delle diverse caratteristiche chimico-fisiche dei componenti.
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
O CH 3 C COOH OH H + O
 Chimica rganica - Laboratorio A.A. 2012/13 Esperienza Sintesi dell acido acetilsalicilico (aspirina) 2 H CH 3 C CH 3 C H + C CH 3 CH 3 Reazione collaterale: H H H + H + H H Introduzione L aspirina è uno
Chimica rganica - Laboratorio A.A. 2012/13 Esperienza Sintesi dell acido acetilsalicilico (aspirina) 2 H CH 3 C CH 3 C H + C CH 3 CH 3 Reazione collaterale: H H H + H + H H Introduzione L aspirina è uno
REAZIONI ACIDO-BASE OSSERVARE, DESCRIVERE E DARE UNA SPIEGAZIONE DEI FENOMENI CHIMICI AVVENUTI
 ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
ANALISI dei MEDICINALI II Corso di Laurea in Farmacia (matricole dispari) a.a Prof. Antonio Lavecchia
 ANALISI dei MEDICINALI II Corso di Laurea in Farmacia (matricole dispari) a.a. 2017-2018 Prof. Antonio Lavecchia Testi Consigliati Guida all analisi di composti d'interesse farmaceutico, F. Savelli, Ed.
ANALISI dei MEDICINALI II Corso di Laurea in Farmacia (matricole dispari) a.a. 2017-2018 Prof. Antonio Lavecchia Testi Consigliati Guida all analisi di composti d'interesse farmaceutico, F. Savelli, Ed.
3016 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico
 6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
