LFA.P26 Rev.1 del
|
|
|
- Evelina Grassi
- 9 anni fa
- Просмотров:
Транскрипт
1 U.O. FARMACIA STEWARDSHIP ANTIFUNGINA E LINEE GUIDA DI TERAPIA NELL ADULTO LFA.P26 Rev.1 del Pag. 1/68 Dipartimento di Malattie Infettive Dipartimento Farmaceutico Elaborato da : Prof Spinello Antinori U.O.C. Malattie Infettive III Approvato da Qualifica Data invio per Data approvazione approvazione Dr Giuliano Rizzardini Direttore Dipartimento di 23/9/ /12/2014 Malattie Infettive Direttore U.O.C. Malattie Infettive I Prof Massimo Galli Direttore U.O.C. Malattie Infettive III 23/9/ /12/2014 Dr Massimo Medaglia Direttore U.O.C. Farmacia 23/9/ /12/2014 Documento attivo da : gennaio 2015 Cadenza Revisione: ogni 3 anni o prima nel caso di importanti risultati provenienti da studi clinici che modifichino in maniera sostanziale la terapia di una delle patologie di seguito riportate. Disponibilità del documento : dall avvenuta approvazione su Intranet per tutto il personale dell AO. E vietata la sua diffusione sotto qualsiasi forma o mezzo al di fuori dell Azienda L Sacco.
2 Introduzione e razionale Le infezioni fungine invasive (di seguito IFI) rappresentano una patologia osservata con frequenza crescente in ambito nosocomiale. L incremento dell incidenza è conseguente soprattutto all aumento della popolazione di soggetti immunocompromessi, in particolare con infezione da HIV, sottoposti a terapie immunosoppressive o affetti da neoplasie con neutropenia indotta da chemioterapia. Inoltre, i pazienti ospedalizzati in unità di terapia intensiva (ICU) nella maggior parte dei casi presentano numerosi dei fattori di rischio (vedi paragrafo candidemia) comunemente associati alla possibile comparsa di infezioni fungine invasive (Eggimann et al. Ann Intensive Care 2011). Accanto a queste considerazioni di ordine epidemiologico si deve tenere conto del fatto che nel corso degli ultimi anni si è verificata la disponibilità di nuove molecole antifungine (echinocandine, azoli di terza generazione). Tali farmaci rappresentano un prezioso ausilio per il Medico nel trattamento delle IFI ma in molti casi presentano dei costi nettamente superiori rispetto ai farmaci in uso da più tempo. Da ultimo va menzionato il fenomeno della farmacoresistenza che seppur ancora limitato comincia a essere osservato anche nella terapia antimicotica con un possibile impatto negativo sull outcome del paziente (Alexander et al. Clin Infect Dis 2013). Queste considerazioni richiedono pertanto da parte del Medico un uso razionale dei farmaci antimicotici che derivi da evidenze cliniche forti (quando disponibili ) non disgiunte da considerazioni di ordine economico. Esistono in letteratura numerose linee guida (Allegato A) alle quali si rimanda per una trattazione più approfondita dell argomento e dalle quali sono state attinte e in parte rielaborate le principali informazioni. Questo documento rappresenta l aggiornamento delle precedenti linee guida interne di terapia antifungina con il passaggio dalla politica di restrizione prescrittiva all introduzione e implementazione di una vera stewardship antifungina. Programma di Stewardship antifungina Le precedenti linee guida a uso interno (aziendali) avevano introdotto un programma di restrizione prescrittiva dei farmaci antimicotici a costo elevato che avveniva attraverso la compilazione di un apposito documento di richiesta del farmaco stesso a firma dello specialista infettivologo. L analisi delle singole schede effettuata a posteriori ha permesso di evidenziare alcune criticità: per esempio, scelta del farmaco non conforme colle indicazioni fornite dalle linee guida aziendali; dose del farmaco non appropriata; criteri diagnostici (specialmente in caso di aspergillosi invasiva) non rispettati. Inoltre, la sola indicazione prescrittiva non essendo richiesto un followup
3 della stessa, non permetteva per esempio una valutazione sulla possibilità di semplificare (da formulazione parenterale a formulazione orale) o descalare (da farmaco ad alto costo a farmaco a basso costo) la terapia antimicotica iniziale. Le criticità precedentemente menzionate non si discostano da quanto segnalato dalla letteratura internazionale che riporta un uso inappropriato dei farmaci antifungini in percentuali variabili da 27% a 74% (LopezMedrano et al. Clin Microbiol Infect 2013; Mondain et al. Infection 2013; Zilberg et al. BMC Infect Dis 2010). Più recentemente uno studio condotto in un ospedale di Madrid ha mostrato come il 33.3% delle prescrizioni inappropriate fosse conseguente a una consulenza da parte dello specialista in malattie infettive (Valerio et al. JAC 2014). Questi dati sottolineano l importanza che lo specialista infettivologo abbia specifiche competenze in micologia in considerazione della crescente difficoltà posta dalla diagnosi e terapia delle infezioni fungine invasive. In quest ottica l implementazione di un programma specifico di stewardship antifungina costituisce una possibile risposta con l obiettivo di migliorare il management e l outcome dei pazienti affetti da IFI da un lato e dall altro di impiegare in maniera oculata le risorse economiche disponibili (Reed et al. Diagn Microbiol Infect Dis 2013; Alfandari et al. Med Mad Infect 2014; AnandaRajah et al Curr Opin Infect Dis 2012). In accordo con le indicazioni per un programma di stewardship antifungina si è proceduto alla formulazione di linee guida adattate al contesto locale (il presente documento che sostituisce la versione precedente). Identificazione di un Team multidisciplinare responsabile dell implementazione e applicazione delle nuove linee guida composto da alcuni medici specialisti infettivologi, due farmacisti, un microbiologo e un farmacologo clinico (vedi allegato B). Il compito del Team sarà il seguente: il Microbiologo oltre a comunicare (con le usuali pratiche aziendali) all UO interessata il risultato preliminare di emocoltura positiva per miceti o di positività di uno dei biomarcatori fungini effettuati (antigene criptococcico, antigene galattomannano) allerta (in analogia con il sistema già in uso per gli eventi sentinella) i responsabili del Team infettivologico (uno per U.O.). A questo punto uno specialista infettivologo si reca nell UO di cui è identificato come consulente (allegato B). Dopo la valutazione, se richiesto, viene compilata (attualmente in forma cartacea, successivamente si prevede di farlo direttamente da Intranet) da parte del Medico infettivologo la Scheda di monitoraggio farmaci antimicotici innovativi (MFA.P72 allegata alle presenti Linee Guida e scaricabile dai documenti della Farmacia nella Intranet aziendale) da inviare all U.O. Farmacia per la richiesta del farmaco soggetto a restrizione prescrittiva. L'approvvigionamento non segue il flusso standard, tramite procedura informatica EncoGPI, ma avviene esclusivamente previa compilazione della scheda di monitoraggio.la prescrizione prevede una fornitura del farmaco per un massimo di 57 giorni (quest ultima situazione nel caso in cui il 5 giorno cada di sabato o domenica) al termine dei quali il consulente
4 (eventualmente allertato dal Farmacista) valuta nuovamente il paziente e verifica l opportunità/necessità di proseguire con la medesima terapia, sospendere la terapia antifungina o deescalare la stessa. Al termine della terapia per ogni paziente verranno raccolte (a cura del consulente infettivologo) informazioni relative all outcome (una delle misure che verranno poi utilizzate per la valutazione dell efficacia del programma di stewardship antifungina). Il Team multispecialistico si riunirà obbligatoriamente ogni 6 mesi (di norma il secondo mercoledì del mese) su convocazione da parte dell U.O. Farmacia per la verifica del consumo globale dei farmaci antifungini, dei DDD (defined daily doses) (entrambi a cura del Farmacista), del numero di richieste all UO Microbiologia/numero di risultati positivi, (a cura del Microbiologo), dell aderenza alle linee guida e per la valutazione dell outcome. Al termine verrà redatto un breve report che verrà inviato alla Direzione Generale e a tutte le U.O. Di seguito vengono prese in considerazione le principali IFI con le indicazioni e/o raccomandazioni per la diagnosi delle stesse oltre che per la terapia. Infezioni da Candida spp. Candidemia L infezione del torrente ematico (bloodstream infection) da Candida spp. rappresenta una causa importante di morbilità e mortalità nei pazienti ospedalizzati. Candida spp. è il terzo/quarto patogeno in ordine di frequenza come causa di infezione nosocomiale ematica con una mortalità grezza del 4050 % e una mortalità attribuibile intorno al 2030 %. Numerosi studi condotti in Europa, Stati Uniti e Italia hanno mostrato un incremento significativo dell incidenza di questa patologia. Questo dato è confermato anche nel nostro nosocomio come indicato nella figura 1 che riporta l incidenza osservata nel periodo (Milazzo et al. Mycopathologia 2014)
5 Figura 1. Incidenza di candidemia presso l AOPolo Universitario L Sacco nel periodo In tabella 1 sono riportate le comorbilità e i fattori di rischio identificati in numerosi studi associati al possibile sviluppo di candidemia. Tabella 1 Fattori di rischio e comorbilità associati allo sviluppo di candidemia nei pazienti ospedalizzati Terapia antibiotica a largo spettro (numero di farmaci e durata) Steroidi (terapia e profilassi) Estremi della vita (< 1 > 70 anni) Neoplasie Chemioterapia Colonizzazione (> 2 siti) Terapia con farmaci che riducono l acidità gastrica Catetere venoso centrale Nutrizione parenterale totale Neutropenia ( 500/µL) Chirurgia (gastrointestinale) Ventilazione meccanica Insufficienza renale/emodialisi Malnutrizione Mucosite Ustioni (> 50% della superficie corporea) Ricovero in ICU > 10 giorni GvHD (graft versus host disease) acuta e cronica Trapianto di cellule staminali e di organo solido APACHE II score > 20 L epidemiologia, con particolare riferimento all incidenza di candidemia e alla distribuzione delle specie di Candida (Candida albicans vs nonalbicans spp.), varia in modo considerevole da paese a paese ma anche a seconda del reparto di provenienza, della patologia sottostante e dell età del paziente (tabella 2). Tra le circa 100 specie di Candida conosciute più del 90 % degli episodi di candidemia sono attribuibili a Candida albicans, C.
6 glabrata, C. parapsilosis, C. tropicalis e C. krusei. Alcuni studi documentano come l isolamento di C. albicans si riduca con l aumento dell età del paziente, dopo una precedente esposizione agli azoli e nei pazienti in terapia intensiva. Tra le specie di Candida nonalbicans, C. glabrata viene isolata nel 20 % degli episodi di candidemia negli Stati Uniti e nel 15 % in Europa (Guinea, Clin Microbiol Infect 2014); C. parapsilosis è la seconda specie più frequentemente isolata dalle emocolture in Europa e tende a formare biofilm sulla superficie e sul lume dei cateteri; come è noto i microrganismi che producono biofilm rappresentano spesso dei microrganismi difficili da eradicare, C.tropicalis è una causa rilevante di infezioni nei pazienti con neoplasie e sembra essere più virulenta rispetto a C.albicans nei pazienti con neoplasie ematologiche. C.krusei pur essendo una causa infrequente di candidemia (< 3%) deve essere tenuta in particolare considerazione in quanto presenta una resistenza intrinseca al fluconazolo (vedi tabella 3) ed è associata ad una mortalità più elevata rispetto a C.albicans. Infine deve essere menzionato che C.lusitaniae si caratterizza per la resistenza (iniziale o a rapido sviluppo nei confronti di amfotericina B). Tabella 2 Epidemiologia di candidemia a seconda della patologia sottostante e dell età del paziente Categoria C.albicans C.glabrata C.parapsilosis C.tropicalis Patologia o condizione % % % % sottostante Chirurgia Terapia intensiva Tumori solidi Neoplasie ematologiche Immaturità fetale Infezione da HIV Gruppi d età < 1 anno anni anni > 70 anni Popolazione totale Riprodotta da Tortorano AM et al. Eur J Clin Microbiol Infect Dis 2004: 23: Nella nostra realtà ospedaliera relativa al quinquennio , Candida albicans costituisce ancora la specie predominante (64% dei casi) seguita da C. glabrata (19.1%), C. tropicalis (6.7%) e C. parapsilosis (4.5%). Inoltre, C. glabrata risulta particolarmente frequente in terapia intensiva e nei reparti di Medicina (27.8% e 36.8%, rispettivamente) (Figura 2) rispetto ai reparti chirurgici e alle malattie infettive (Milazzo et al. Mycopathologia 2014).
7 Figura 2 Frequenza di isolamenti da emocoltura di Candida spp. suddivisi per tipologia di reparti (chirurgia, medicina, malattie infettive, ICU) presso l AOPolo Universitario L Sacco nel periodo (fonte: Milazzo L et al. Mycopathologia 2014) Tabella 3 Suscettibilità (attesa) in vitro delle principali specie di Candida Specie AMB 5FC FLU ITR VOR POS Echinocandine C. albicans S S S S S S S C. glabrata SI S SDDR SDDR SI S S C. krusei S R R SDDR SI S S C. lusitaniae SR S S S S S S C. parapsilosis S S S S S S SI C.tropicalis S S S S S S S C. guilliermondii S S S S S S R AMB= amfotericina B; 5FC= fluorocitosina; FLU= fluconazolo; ITR= itraconazolo; VOR= voriconazolo; POS= posaconazolo; S= suscettibile; I= intermedio; SDD= suscettibile dosedipendente; R= resistente Diagnosi di candidemia: L emocoltura rappresenta il gold standard per la diagnosi di candidemia; 2 flaconi di emocoltura (10 ml) dovrebbero essere raccolti nel sospetto di candidemia prima di iniziare la terapia antifungina. Questo approccio è in grado di dimostrare circa il 90% degli episodi di candidemia. Poiché il 3040% di tutti gli
8 episodi di candidemia è associato alla presenza di cateteri venosi centrali è buona norma in questi casi effettuare emocolture sia da vena periferica sia dal catetere venoso centrale. L isolamento di Candida spp. anche da una singola emocoltura richiede sempre l inizio di terapia antimicotica. Circa il 2530 % delle infezioni disseminate si caratterizzano per emocolture negative. E inoltre consigliabile effettuare un fundus oculi in quanto possono essere evidenziate alterazioni compatibili con una diagnosi di candidemia. Il fundus va effettuato anche in assenza di disturbi del visus per escludere la presenza di endoftalmite e corioretinite. Metodi non colturali La ricerca di 1,3βdglucano in pazienti con fattori di rischio e quadro clinico compatibile di candidemia/candidosi invasiva sembra essere molto promettente anche se la maggior parte degli studi sono stati effettuati in pazienti ricoverati in reparti di terapia intensiva (Hanson et al. Plos One 2012; Posteraro et al. Crit Care 2011). L elevato potere predittivo negativo (> 99%) permette, laddove il test venga impiegato, una esclusione pressoché certa della diagnosi di candidemia (con la possibilità di sospendere una terapia antimicotica iniziata empiricamente). Rimane una questione aperta quale sia il valore soglia (cutoff) più appropriato per incrementare sia i valori predittivi positivi e negativi sia per discriminare l infezione dalla colonizzazione. In generale vengono considerati significativi valori > 80 pg/ml Poiché tale test non viene effettuato presso il nostro laboratorio di Microbiologia il suo impiego attualmente non può essere consigliato. Va ricordato che l utilità di questa indagine è stata dimostrata in contesti in cui il risultato dell esame è disponibile in tempo reale (Posteraro et al. Crit Care 2011; Hanson et al. Plos One 2012; Eggimann et al. Crit Care 2011). Impiego di punteggi predittivi per la diagnosi di candidemia/candidosi invasiva nei pazienti ospedalizzati in terapia intensiva Nel corso degli anni sono stati proposti diversi score clinici predittivi dello sviluppo di candidemia/candidosi invasiva nei pazienti ospedalizzati in terapia intensiva. I più noti sono l indice di colonizzazione da Candida (ICC) e la sua variante cosiddetta corretta (cicc) proposto da Pittet (Pittet et al. Ann Surg 1994); il Candida score di Leon (Leon et al. Crit Care Med 2009) e lo score di OstroskyZeichner (OstroskyZeichner et al. Mycoses 2011). Un indice di colonizzazione > 0.4 ha un valore predittivo positivo del 66% e un valore predittivo negativo del 100%. Il calcolo degli indici di colonizzazione viene effettuato applicando le formule sotto riportate: ICC= Numero di aree corporee colonizzate da Candida/Numero di regioni sottoposte a screening;
9 cicc= Numero di regioni corporee con elevata colonizzazione (>10 5 CFU/mL)/Numero di regioni corporee colonizzate da Candida. Il Candida score di Leon assegna un punteggio alle seguenti condizioni: colonizzazione multifocale da Candida (1 punto); nutrizione parenterale (1 punto); chirurgia maggiore (1 punto); sepsi grave (2 punti). Un punteggio 3 è considerato altamente predittivo di candidosi invasiva. Il modello di OstroskyZeichner sviluppato in pazienti che abbiano una ospedalizzazione di almeno 4 giorni si basa sulla presenza dei seguenti fattori : terapia antibiotica sistemica (giorni 13) o presenza di CVC (giorni 13) e almeno due dei seguenti: nutrizione parenterale totale (giorni 13), dialisi (giorni 13), chirurgia maggiore (giorni70), pancreatite (giorni 7 0), impiego di steroidi (giorni 73) o impiego di terapie immunosoppressive (giorni 70). Si caratterizza per un potere predittivo positivo del 10% e un potere predittivo negativo del 97%. Come si vede tutti questi score presentano un elevato potere predittivo negativo ma hanno bassi valori in relazione al potere predittivo positivo. Pertanto, benché siano stati utilizzati per la cosiddetta preemptive therapy nei pazienti ospedalizzati in ICU, il loro ruolo più significativo consiste nell elevato potere di esclusione di tale patologia piuttosto che come biomarcatori di malattia. Farmaci impiegabili nella terapia della candidemia/candidosi invasiva Sono utilizzabili farmaci appartenenti alle seguenti classi: 1) Polieni (amfotericina B deossicolato; formulazioni liposomiche di amfotericina B); 2 ) Triazoli (fluconazolo; itraconazolo; voriconazolo); 3) Echinocandine (caspofungina, anidulafungina, micafungina). Scelta del farmaco Deve tenere conto delle caratteristiche del paziente (neutropenico vs nonneutropenico), della funzionalità renale (insufficienza renale; dialisi) ed epatica (cirrosi epatica) e di eventuali altre comorbilità. Inoltre devono essere considerate pregresse esposizioni a farmaci antimicotici (soprattutto profilassi), le condizioni generali del paziente (paziente critico), l efficacia dimostrata e l eventuale tossicità attesa del farmaco nonché le possibili interazioni farmacologiche. Paziente non neutropenico Per il paziente non neutropenico le linee guida statunitensi (Pappas et al.,clin Infect Dis 2009) collocano sullo stesso piano fluconazolo e le echinocandine (AI). Viene privilegiato l impiego delle echinocandine nel paziente con
10 pregressa esposizione agli azoli e con situazione clinica instabile o grave. Le più recenti linee guida europee (Ullmann et al., Clin Microbiol Infect 2012) raccomandano sempre come prima scelta l impiego di una echinocandina (AI) benché vi sia un solo studio comparativo con dimostrazione di superiorità di una singola echinocandina (anidulafungina) nei confronti del fluconazolo (Reboli et al NEJM 2007). Sulla scorta della non attività nei confronti di C. krusei e della possibile inefficacia verso C. glabrata il fluconazolo nelle linee guida europee viene raccomandato solo marginalmente (CI) (per esempio nelle infezioni provocate da C. parapsilosis microrganismo verso cui le echinocandine presentano valori di MIC elevati). Nelle linee guida europee amfotericina B liposomiale (LAMB) viene raccomandata moderatamente (BI) nel trattamento della candidemia benché nello studio di confronto con micafungina l efficacia clinica dei due agenti sia risultata sovrapponibile. Tale raccomandazione deriva unicamente dalla maggiore nefrotossicità di LAMB rispetto a micafungina. Una recente revisione di 7 studi clinici relativi a 1915 pazienti ha dimostrato che 2 strategie terapeutiche erano associate ad miglioramento della sopravvivenza (> 10%) : rimozione di catetere venoso centrale (OR 0.50; IC 95%.35.72; P=.0001) e terapia con una echinocandina (OR 0.65; IC 95%.45.94; P=.02) (Andes et al. Clin Infect Dis 2012). Sulla scorta delle raccomandazioni riportate dalle principali linee guida, nello studio sopracitato e in considerazione dell epidemiologia locale (Milazzo et al. Mycopathologia 2014) si ritiene indicato impiegare una echinocandina nella terapia iniziale (vedi figura 3flowchart) conseguente all isolamento di un lievito da emocoltura (esclusi i pazienti con infezione da HIV per i quali si sospetti e/o sia più probabile una diagnosi di criptococcosi). Il paziente verrà valutato successivamente (nell ottica della stewardship antifungina) per verificare l andamento clinico e la possibilità di strategia di semplificazione terapeutica (stepdown) con fluconazolo (endovena o orale). Non vi sono indicazioni certe su quando possa essere effettuato (in termini di giorni) lo stepdown a fluconazolo.le linee guida ESCMID, nel caso di ceppo sensibile a fluconazolo e con paziente stabile e in grado di assumere la terapia per os, danno indicazione (BII) dopo 10 giorni di terapia parenterale con echinocandina. In realtà questa raccomandazione è mutuata dagli studi registrativi delle tre echinocandine (Mora Duarte et al. NEJM 2002; Reboli et al. NEJM 2007; Pappas et al. Clin Infect Dis 2007) e la scelta temporale è del tutto empirica. Uno studio clinico recente ha dimostrato l efficacia e la fattibilità di uno stepdown precoce (meno di 7 giorni) in pazienti inizialmente trattati con anidulafungina. Sulla scorta di questi dati viene proposto di valutare lo stepdown dopo 57 giorni di terapia con echinocandina.
11 In figura 3 è riportata la flowchart relativa all isolamento preliminare di lievito da emocoltura con le indicazioni posologiche da adottare in attesa dell identificazione di specie. Isolamento di lievito da emocoltura (in attesa di identificazione) * Microbiologo Paziente non neutropenico Immediata comunicazione al Team dedicato alla stewardship Echinocandina Caspofungina 70 mg ev (LD) poi 50 mg/die ev Anidulafungina 200 mg ev (LD) poi 100 mg/die ev Micafungina 100 mg/die ev Rivalutazione del paziente dopo 57 giorni Paziente clinicamente stabile (senza febbre, parametri cardiocircolatori nella norma; indici infiammatori in riduzione); isolamento di C. parapsilosis; C. albicans, C.tropicalis o C.glabrata sensibile a fluconazolo Stepdown Fluconazolo (os o ev) 400 mg/die * N.B. Nel paziente HIVnegativo un isolamento di lievito da emocoltura deve essere considerato in prima istanza (in attesa dell identificazione di genere e specie) trattarsi di Candida; al contrario nel paziente HIVsieropositivo con valori di linfociti CD4+ < 200/µL e in assenza dei fattori di rischio per candidemia l isolato è più verosimilmente Cryptococcus neoformans. Tale dato è importante in quanto come è noto le echinocandine sono inefficaci nei confronti di C.neoformans. LD = loading dose
12 Per quanto riguarda la scelta dell echinocandina in tabella 4 sono riassunte le principali caratteristiche e le indicazioni registrative delle tre echinocandine. Nessuna delle tre echinocandine richiede modificazioni posologiche in presenza di insufficienza renale; la sola caspofungina richiede una riduzione della posologia Tabella 4 Principali caratteristiche delle tre echinocandine disponibili Principio attivo Anidulafungina Caspofungina Micafungina Nome commerciale Ecalta Pfizer CancidasMSD MycamineAstellas Pharma Indicazioni terapeutiche (registrazione) Candidiasi invasiva nell adulto non neutropenico# Candidiasi invasiva (anche neutropenico) Terapia empirica neutropenia febbrile Aspergillosi invasiva in pazienti adulti intolleranti o refrattari a amfotericina B/itraconazolo Candidiasi invasiva (anche neutropenico e paziente pediatrico) Profilassi delle infezioni da Candida in pazienti sottoposti a trapianto allogenico di cellule staminali ematopoietiche o in pazienti che si prevede possano manifestare neutropenia (conta assoluta dei neutrofili < 500 cellule/µl) per 10 o più giorni. Candidosi esofagea Loading dose (dose carico) 1 giorno Dose/die 200 mg 100 mg 70 mg* 50 mg No 100 mg Modifiche dose in caso di malattia renale Modifiche dose in caso di malattia epatica Interazioni farmacologiche Ciclosporina Tacrolimus Micofenolato mofetil Induttori CP450 (es. rifampicina) Nessun aggiustamento necessario Nessun aggiustamento necessario No No No No Nessun aggiustamento necessario ChildPugh 79: aumento significativo AUC ridurre la dose di mantenimento a 35 mg/die Si Si No Riduce i livelli di caspofungina Nessun aggiustamento necessario Nessun aggiustamento necessario Costo ospedale (+IVA) 100 mg= 354,32 50mg= 441,31; 70 mg= 561, mg= 402,06 * Nei pazienti con peso corporeo 80 kg è indicato mantenere la dose giornaliera di 70 mg # Il 24 luglio 2014 è stato espresso parere favorevole da parte dell CHMP (Committee for Medicinal Products for Human use) ad adottare un cambio nelle indicazioni che è stato recepito da EMA e da AIFA come segue: Trattamento della candidiasi invasiva nei pazienti adulti. Si ricorda quanto riportato nella scheda tecnica: La decisione di utilizzare Mycamine deve tenere conto del rischio potenziale di sviluppare tumori epatici (paragrafo 4.4 Avvertenze speciali e precauzioni di impiego). Mycamine deve perciò essere usata solo l utilizzo di altri antifungini non è appropriato. No No No No giornaliera in presenza di cirrosi epatica con ChildPugh compreso tra 79; la dose giornaliera di caspofungina deve essere aumentata (da 50 a 75 mg) nel caso di somministrazione di induttori epatici del citocromo P450 (rifampicina; carbamazepina; fenitoina; nevirapina; efavirenz). Inoltre caspofungina riduce l AUC di tacrolimus del 20%. Per i pazienti che abbiano intrapreso una terapia con echinocandina e le cui condizioni cliniche siano
13 migliorate e l isolato di Candida sia verosimilmente suscettibile agli azoli (ad esempio C.albicans, C.parapsilosis, C.tropicalis) è raccomandato lo switch a fluconazolo. Una volta identificato il lievito a livello di specie e sulla scorta delle suscettibilità attese dei microrganismi di più frequente isolamento possono essere disegnati 4 scenari: 1) Isolamento di Candida albicans : si tratta di una specie sensibile agli azoli (salvo casi di pregressi trattamenti prolungati) alle echinocandine e ai polieni; valgono pertanto le considerazioni sopra riportate legate in particolare alle condizioni cliniche del paziente. 2) Isolamento di Candida glabrata : si tratta di una specie la cui sensibilità agli azoli è variable (vedi tabella 3) ; pertanto è preferibile utilizzare una echinocandina e l eventuale switch a fluconazolo deve essere effettuato solo in presenza di un isolato suscettibile agli azoli. 3) Isolamento di Candida krusei: si tratta di una specie intrinsecamente resistente agli azoli; in questo caso è opportuno iniziare e proseguire la terapia con una echinocandina. 4) Isolamento di Candida parapsilosis: si tratta di una specie sensibile agli azoli e come è noto viene frequentemente isolata nelle candidemie associate a catetere venoso centrale; vi sono alcuni dati della letteratura che indicano una ridotta suscettibilità degli isolati di C.parapsilosis alle echinocandine; pur non essendoci studi clinici ad hoc alcuni esperti in genere raccomandano di non utilizzare le echinocandine per il trattamento di questa specie. E sempre opportuno effetuare lo switch a fluconazolo Followup microbiologico: una volta pervenuto l esito di emocoltura positiva per Candida è necessario dopo l inizio della terapia effettuare emocolture seriate per dimostrare l avvenuta negativizzazione. Non vi sono dati certi sul criterio temporale da adottare (i.e. con che frequenza) per l esecuzione di emocolture di controllo. Nelle linee guida ESCMID viene data indicazione di effettuarle giornalmente fino alla negativizzazione (BIII) (Cornely et al. Clin Microbiol Infect 2012). Un atteggiamento più pragmatico potrebbe essere quello di effettuarle ogni due giorni fino alla dimostrazione di avvenuta negativizzazione. Durata della terapia: in assenza di localizzazioni secondarie dimostrabili è opportuno proseguire la terapia antimicotica per 2 settimane dopo la negativizzazione di emocoltura
14 Paziente neutropenico Nel paziente neutropenico la candidemia rappresenta un infezione generalmente grave e talora caratterizzata da un quadro clinico similsepsi con insufficienza multiorgano che mette in pericolo la vita del paziente. Non vi sono studi clinici randomizzati controllati che abbiamo specificamente valutato il trattamento dei pazienti neutropenici con le echinocandine; quanto è noto deriva dall analisi dei diversi sottogruppi nei vari studi registrativi relativi alle tre echinocandine (MoraDuarte et al. N Engl J Med 2002; Pappa set al. Clin Infect Dis 2007; Kuse et al. Lancet 2007; Reboli et al. N Engl J Med 2007) in cui il numero dei pazienti neutropenici arruolati variava, a seconda dello studio da < 3% a circa 10%. Per quanto attiene anidulafungina nello studio comparativo con fluconazolo furono arruolati un numero esiguo di pazienti con neutropenia (< 3%) per poter avere dati affidabili e per questo motivo anidulafungina non aveva ottenuto l approvazione per il trattamento della candidemia nel paziente neutropenico (è in vigore nella nuova scheda tecnica 26 agosto 2014 la modifica di EMA approvata da AIFA con la seguente dizione: Trattamento della candidiasi invasiva nei pazienti adulti.). Anche per il paziente neutropenico pur con una forza dell evidenza inferiore (con l eccezione delle linee guida ESCMID) rispetto al nonneutropenico due (caspofungina e micafungina) delle tre echinocandine sono considerate il trattamento di scelta della candidemia. Amfotericina B liposomiale è considerata sullo stesso piano delle echinocandine (e raccomandata con eguale forza) nelle linee guida IDSA (Pappas et al. Clin Infect Dis 2009), ECIL (Maertens et al. Bone Marrow Transpl 2011) e in quelle della DGHO (Mousset et al. Ann Hematol 2014) mentre in quelle ESCMID per la maggiore nefrotossicità la forza della sua raccomandazione è inferiore (Ullmann et al. Clin Microbiol Infect 2012) (Tabella 5). Tabella 5 Indicazioni e raccomandazioni (a seconda delle principali linee guida) all impiego dei farmaci antifungini nella terapia della candidemia nel paziente neutropenico Farmaco IDSA,2009 ECIL,2011 ESCMID,2012 AGIHO/DGHO 2014 Anidulafungina AIII BII BII BI Caspofungina AII BII AII BI Micafungina AII BII AII BI Amfotericina B AII BII BII BI liposomiale Fluconazolo BII CIII CII Voriconazolo BII CII IDSA, Infectious Diseases Society of America; ECIL, European Conference on Infections in leukaemia; ESCMID, European Society of Clinical Microbiology and Infectious Diseases; AGIHO/DHGO, Infectious Diseases Working party of the German Society of Hematology and Oncology
15 Per quanto riguarda il costo della terapia in tabella 6 sono riportate delle simulazioni a seconda del farmaco impiegato. Tabella 6 Costo della terapia per candidemia a seconda del farmaco/schema utilizzato (simulazione per 2 o 3 settimane di terapia) in un ipotetico paziente Farmaco Periodo 2 settimane 3 settimane Fluconazolo 800 mg (LD) poi 400 mg/die ev Anidulafungina Micafungina Caspofungina Amfotericina B liposomiale (3 mg/kg/die) 18, ,8 5628, ,37 (peso 50 kg) 150 mg/die 6508,32 (peso 70 kg) ^200mg/die= 8677,76 (peso 80 kg) 250^^ mg/die= ,2 26, , , ,54 150mg/die= 9762, mg/die= , mg/die=16.270,8 Echinocandina+switch (fluconazolo) *Anid+flu= 2843,03 (ev) 2837,36 (os) Caspo+flu= 3217,67 (ev) 3212 (os) Mica+flu= 2822,89 (ev) 2817,22 (os) Anid+flu= 2851,5 (ev) 2840,1(os) Caspo+flu= 3226,14 (ev) 3214,8 (os) Mica+flu= 2831,36 (ev) 2820,02 (os) ^ La dose giornaliera è 210 mg ; ^^ la dose giornaliera è 240 mg. * E considerata 1 settimana di echinocandina+ 1 settimana di fluconazolo; E considerata 1 settimana di echinocandina+ 2 settimana di fluconazolo N.B. I costi delle terapie sono riferiti al solo costo di acquisto del medicinale da parte dell ospedale E evidente come uno switch dopo 7 giorni da echinocandina a fluconazolo permetta un risparmio di circa il 50% rispetto ad una terapia per 14 giorni con l echinocandina. Non vi è una differenza significativa invece nell utilizzo di fluconazolo in formulazione orale rispetto alla formulazione parenterale. Tuttavia quando ciò sia possibile (nessuna altra terapia parenterale) la formulazione orale va preferita perché riduce il rischio di complicanze legate all accesso venoso periferico (flebite, infezione). In una ipotetica terapia della durata di 14 giorni anidulafungina presenta un costo lievemente inferiore rispetto a micafungina (di circa 300 euro) mentre i due farmaci si equivalgono (in termini di costo complessivo) quando si effettui lo switch a fluconazolo dopo una settimana.
16 Durata della terapia: in assenza di localizzazioni secondarie dimostrabili è opportuno proseguire la terapia antimicotica per 2 settimane dopo negativizzazione di emocoltura (almeno 2 sequenziali) e scomparsa delle manifestazioni cliniche con recupero dalla neutropenia. Gestione del catetere venoso centrale (pazienti non neutropenici e neutropenici) Non vi sono studi clinici randomizzati controllati che abbiano valutato l impatto della rimozione del catetere venoso centrale (CVC) sull outcome della candidemia. Tuttavia tutte le linee guida concordano che in presenza di candidemia accertata il CVC dovrebbe essere rimosso. I dati a favore della rimozione del CVC (soprattutto nel paziente non neutropenico) documentano che la rimozione si associa a minore durata di candidemia e riduzione della mortalità sia negli adulti sia nei bambini (Andes et al. Clin Infect Dis 2012). Nel caso in cui la rimozione del CVC non sia possibile è indicato impiegare farmaci antimicotici attivi sul biofilm (echinocandine o amfotericina B liposomiale). Ecocardiografia Si riconosce l indicazione ad effettuare l esecuzione di ecocardiografia nei pazienti con candidemia persistente (definita come persistenza di emocoltura positiva dop almeno 96 ore di terapia antifungina adeguata) per escludere endocardite. Nei pazienti protesi valvolare cardiaca che vanno incontro a un episodio di candidemia è consigliato effettuare una nuovo esame ecocardiografico (dopo un primo esame negativo) a distanza di 6 mesi per la possibilità di endocardite tardiva (Falcone et al. Medicine 2009). Fundus oculi E opportuno eseguire l esame del fundus oculare in tutti i pazienti con diagnosi di candidemia (anche in assenza di disturbi visivi) per escludere un quadro di corioretinite o di endoftalmite. Si tratta di complicanze che richiedono una terapia più prolungata e soprattutto non devono essere trattate con echinocandine per la scarsa penetrazione di questi farmaci a livello dell occhio.
17 Candiduria Nei pazienti ambulatoriali senza fattori di rischio la identificazione di Candida da urinocoltura riflette in genere un problema di contaminazione e si suggerisce di ripetere l esame. Non è in genere indicata alcuna terapia antimicotica salvo i casi di confermata positività e dopo esclusione di candidiasi genitale (vaginale o al glande). Nei pazienti ospedalizzati portatori di catetere vescicale è indicata la rimozione e/o sostituzione del catetere vescicale e il trattamento antifungino nel caso in cui siano presenti sintomi indicativi di cistite. Il trattamento della candiduria è raccomandato solo nei pazienti a rischio di malattia disseminata (neutropenici; neonati con basso peso alla nascita ;pazienti ricoverati in ICU con segni di sepsi; pazienti che verranno sottoposti a manovre urologiche). I neutropenici e i neonati con basso peso alla nascita devono essere trattati secondo gli schemi della candidiasi invasiva; per i pazienti sottoposti a procedure urologiche è indicato fluconazolo mg/die alcuni giorni prima e dopo la manovra. La candiduria sintomatica causata da ceppi di Candida fluconazolosensibili può essere trattata con fluconazolo 200 mg per os per 2 settimane. Per i ceppi resistenti a fluconazolo si può impiegare amfotericina B deossicolato 0,30,6 mg/kg/die per 17 giorni. Candidosi esofagea La candidosi esofagea è una condizione di frequente riscontro soprattutto nei pazienti con infezione da HIV; la diagnosi richiede la dimostrazione macroscopica di Candida spp. con esofagogastroduodenoscopia (EGDS); tuttavia non si ritiene sempre indispensabile eseguire EGDS ma la diagnosi può essere presunta in presenza di candidosi orofaringea e disfagia con scomparsa della sintomatologia in seguito ad appropriata terapia antimicotica. Il fluconazolo rappresenta il farmaco di scelta (per via orale) alla dose di 200 mg al giorno per 1421 giorni; nel caso di intolleranza alla terapia orale/disfagia importante il farmaco (almeno inizialmente) può essere somministrato per via parenterale. Nei pazienti HIVsieropositivi in assenza di un recupero immunitario è frequente la recidiva della candidosi mucosa (orofaringea e esofagea); in generale una ridotta suscettibilità agli azoli si osserva nei pazienti con pregressi trattamenti e grave immunodepressione ; anche in questi casi prima di utilizzare altri farmaci è opportuno provare ad impiegare dosi più elevate di fluconazolo (ceppi di Candida con
18 suscettibilità dosedipendente) ( mg/die). In caso di mancata risposta anche ai dosaggi più elevati si può ricorrere alla somministrazione di amfotericina B deossicolato (0,30,7 mg/kg/die). Come ulteriori opzioni possono essere considerati l impiego di voriconazolo 200 mg ogni 12 ore per 1421 giorni oppure una delle echinocandine disponibili ai seguenti dosaggi: caspofungina 50 mg/die, micafungina 150 mg/die, anidulafungina 200 mg/die (per la scelta valgono le stesse considerazioni di ordine economico fatte per il trattamento della candidemia ma si ricorda che soltanto per micafungina esiste l indicazione terapeutica registrativa). Gli studi effettuati per la candidosi esofagea indicano una frequenza maggiore di recidiva dopo trattamento con le echinocandine rispetto al fluconazolo. L impiego della terapia HAART quando possibile è sempre raccomandata per controbattere una condizione di grave immunodepressione che è alla base delle recidive di candidosi. Altre localizzazioni dell infezione da Candida spp. Candida spp. possono localizzarsi, soprattutto come conseguenza di candidemia, a livello dell occhio (corioretinite, endoftalmite), delle meningi (meningite), dell endocardio (endocardite) o dell apparato osteoarticolare (osteomielite, artrite settica). Si tratta di forme cliniche infrequenti e per questo motivo non esistono dati provenienti da studi clinici controllati che indichino quale sia la migliore terapia da impiegare. In molti casi le raccomandazioni derivano da casistiche numericamente limitate o da singoli casi clinici più raramente da metaanalisi. Come indicazione generale si ricorda di non impiegare le echinocandine nel caso di localizzazione oculare o al sistema nervoso centrale per la scarsa penetrazione di questi farmaci a tale livello. Nella tabella 7 vengono riportate schematicamente le indicazioni fornite nelle principali linee guida (IDSA, ESCMID,DMYKG) che verranno utilizzate e adattate da parte del consulente infettivologo in base alle caratteristiche del paziente.
19 Tabella 7 Terapia antifungina nelle localizzazioni rare da Candida spp. Localizzazione d organo Meningite LAMB 35 mg/kg +/ FC 25 mg/kg (x4/die) (per alcune settimane) seguito da fluconazolo mg/die (BIII) Endoftalmite/corioretinite DAMB mg/kg/die +FC 25 mg/kg (x 4/die) (AIII) Fluconazole 612 mg/kg/die (BIII) Endocardite LAMB 35 mg/kg +/ FC 25 mg/kg (x4/die) o DAMB mg +/ FC 25 mg/kg (x4/die) o una echinocandina* (BIII) Rimozione di pacemaker e ICDs fortemente raccomandata. Trattare per 46 settimane dopo la rimozione del device Osteomielite Fluconazolo 400 mg/die per 612 mesi o LAMB 35 mg/kg/die per diverse settimane seguito da fluconazolo per 612 mesi (BIII) Artrite settica Fluconazolo 400 mg/die per almeno 6 settimane o LAMB 35 mg/kg/die per alcune settimane seguito da fluconazolo (BIII) IDSA 2009 ESCMID 2012 DMYKG 2011 Commenti LAMB 3 mg/kg + FC 150 mg/kg/die per 10 settimane seguito da fluconazolo 3 mg/kg/die per 5 settimane (BIII) o LAMB 3 mg/kg/die per 4 settimane + fluconazolo 6 mg/kg/die per 4 settimane Fluconazolo mg/die (AII) o voriconazolo 12/6 mg/kg/die ev seguito da 400 mg/die per os (AII) (In entrambi i casi se è stato isolato un ceppo sensibile) LAMB +/ FC per 68 settimane seguite da fluconazolo (BII) Caspofungina+/ FC (CII) Fluconazolo 400 mg/die per 612 mesi (AII) O LAMB 3 mg/kg/die o ABLC 5 mg/kg/die per 26 settimane seguito da fluconazolo 400 mg/die per 511 mesi (AII) LAMB 3 mg/kg/die o ABLC 5 mg/kg/die per 2 settimane seguiti da fluconazolo 400 mg/die per > 4 settimane (AII) Fluconazolo 400 mg/die per > 6 settimane (BII) DAMB mg/kg+fc 25 mg/kg (x4)/d (BIII) o LAMB 3 mg/kg/die (BIII) o Fluconazole mg/die (BIII) Fluconazolo mg/die (BIII) Voriconazolo 48 mg/kg x 2/die (BIII) DAMB mg/kg/die (BII) + FC 25 mg/kg (x 4/die)(BIII) Fluconazolo mg/die (BII) Voriconazolo 48 mg/kg x 2/die (BII) Fluconazolo mg/die (BII) Voriconazolo 48 mg/kg x 2/die (BII) In generale vi è accordo, anche in assenza di studi clinici controllati, ad impiegare in prima istanza nella terapia della meningite amfotericina B Non impiegare le echinocandine poiché non raggiungono concentrazioni di farmaco adeguate nell occhio Non vi sono studi clinici controllati randomizzati; le echinocandine e L AMB sono considerati dagli esperti i farmaci da preferire per questa patologia; la chirurgia è considerata indispensabile sulla base di metaanalsi (casi clinici). E necessaria una terapia prolungata per molti mesi Fluconazolo e/o amfotericina B liposomiale sono i farmaci di scelta Aspergillosi Aspergillus spp. sono funghi filamentosi diffusi ubiquitariamente in natura specialmente nel terreno; sono responsabili di infezioni invasive caratterizzate da elevata letalità soprattutto nei pazienti gravemente immunocompromessi. I conidi inalati attraverso le vie respiratorie trovano nei macrofagi alveolari la prima linea di
20 difesa ma sono soprattutto i granulociti neutrofili le cellule dominanti nella risposta immunitaria difensiva nei confronti delle ife. Le popolazioni di pazienti a rischio di sviluppare l aspergillosi invasiva (AI) sono aumentate come conseguenza dell incremento delle pratiche trapiantologiche e dell impiego di terapie immunosoppressive; in tabella 8 sono riportate le popolazioni a rischio di AI; in generale i pazienti ematologici sono quelli a maggior rischio di sviluppare AI. Tabella 8 Popolazioni di pazienti a rischio di sviluppare aspergillosi invasiva (AI) Popolazione a rischio Commento Neutropenici Neutropenia grave (< 100 neutrofili/µl) e prolungata (> 10 gg) I pazienti a più elevato rischio sono quelli che ricevono chemioterapia citotossica per leucemia acuta e anemia aplastica Riceventi trapianto allogenico di cellule staminali emopoietiche (AlloHSCT) Riceventi trapianto autologo di cellule staminali emopoietiche (AlloHSCT) Rischio elevato nel 1 mese dopo regime di condizionamento 16 mese durante la parziale immunoricostituzione permane un rischio di AI > 6 mesi riduzione del rischio (se non vi è necessità di regimi immunosoppressori per GvHD) Rischio inferiore di AI rispetto agli allotrapianti Rischio più elevato nei trapianti con cellule CD34+ Rischio maggiore nei soggetti sottoposti a più di un HSCT e quelli con precedenti trattamenti con terapie immunosoppressive per malattia refrattaria Trapiantati di organo solido (vedi anche allegato C) I soggetti sottoposti a trapianti di polmone sono a rischio più elevato Il principale fattore di rischio è rappresentato dall intensità del regime immunosoppressivo per Pazienti sottoposti a terapie immunosoppressive per malattie autoimmunitarie controllare il rigetto Dosi elevati di steroidi per via sistemica (> 20 mg/die di prednisone per > 3 settimane); inibitori della calcineurina; AIDS Pazienti gravemente immunodepressi (< 50 linfociti CD4+/µL) CGD Difetto ereditario della fagocitosi neutrofila L AI è la principale causa di morte in questi soggetti La diagnosi di AI senza apparenti fattori di rischio deve portare alla valutazione per una possibile CGD Altre patologie primitive del sistema immunitario Sindrome di Job AIDS, sindrome da immunodeficienza acquisita; AI, aspergillosi invasiva; CGD, malattia cronica granulomatosa; HSCT, trapianto allogenico di cellule staminali emopoietiche L aspergillosi può localizzarsi in qualsiasi organo di un paziente immunocompromesso ma la forma polmonare costituisce quella più frequente in assoluto. L angioinvasione prodotta dalle ife è responsabile di trombosi vascolare e infarto tessutale con necrosi coagulativa. Il quadro clinico dell AI polmonare è aspecifico essendo caratterizzato dalla comparsa di infiltrati polmonari, febbre elevata, tosse e meno frequentemente dolore toracico
21 ed emoftoe. L aspergillosi invasiva può meno frequentemente localizzarsi al sistema nervoso centrale (meningite, meningoencefalite, lesioni occupanti spazio, lesioni infartuali con o senza emorragie), al cuore (miocardite, endocardite, pericardite), all occhio (endoftalmite e cheratite), all osso (osteomielite) al parenchima renale. Si tratta quasi sempre di forme disseminate anche se localizzazioni primitive possono essere osservate in seguito a contaminazione diretta (per esempio interventi di neurochirurgia o di cardiochirurgia per sostituzioni valvolari). A livello polmonare si riconoscono poi alcune peculiari forme invasive (aspergillosi tracheobronchiale e aspergillosi polmonare cronica necrotizzante), la colonizzazione di lesioni cavitarie preesistenti (aspergilloma polmonare) e una forma su base allergica (aspergillosi broncopolmonare allergica). Diagnosi di aspergillosi invasiva Secondo i criteri dell EORTC la diagnosi definitiva di AI richiede la dimostrazione diretta di Aspergillus su materiale ottenuto mediante biopsia (De Pauw et al. Clin Infect Dis 2008). La diagnosi di AI probabile può essere posta in base ad un criterio epidemiologico (relativo al paziente, ad esempio neutropenia prolungata) associato a un criterio microbiologico e/o radiologico (noduli polmonari) (tabella 9). Tabella 9 Criteri EORTC per la diagnosi di malattia fungina probabile Fattori dell ospite Criteri clinici Criteri micologici Neutropenia recente (< 500/µL) di durata > 10 giorni temporalmente correlata all esordio della malattia fungina Ricevente di trapianto allogenico di cellule staminale Impiego prolungato di steroidi compresi i pazienti con aspergillosis broncopolmonare allergica (dose media giornaliera 0,3 mg/kg di prednisone > 3 settimane) Malattia localizzata alle basse vie respiratorie (presenza di 1 dei 3 segni seguenti): Lesioni dense, ben circoscritte, con o senza segno dell alone (Halo sign) Segno della luna crescente (aircrescent sign) Cavitazione Tracheobronchite Ulcerazione, noduli, placche, pseudomembrane osservate alla broncoscopia Infezione sinonasale Imaging che mostra sinusite + 1 dei seguenti 3 segni dolore acuto localizzato (inclusa irradiazione all occhio) Ulcere nasali con escare mucose Estensione dai seni paranasali Esame diretto (citologia o coltura) Muffe su escreato, lavaggio broncoalveolare, brushing bronchiale o campioni aspirati dai seni nasali Presenza di elementi fungini indicativi di muffa Isolamento in coltura di una muffa (Aspergillus spp; Fusarium spp; Mucormicosi; Scedosporium spp.) Saggi microbiologici indiretti (rilevazione di antigeni o componenti della parete) Aspergillosi (antigene galattomannano rilevato su plasma, siero, liquido di lavaggio broncoalveolare o liquor) Infezioni invasive fungine (esclusa criptococcosi e zigomicosi) βdglucano rilevato su siero
22 Trattamento con altri farmaci immunosoppressivi per le cellule T (ciclosporina; antitnfa; anticorpi monoclonali (ad sempio alentuzumab) o analoghi nucleosidici nei precedenti 90 giorni all osso Infezione del SNC 1 dei 2 segni lesioni focali (imaging) Enhancement meningeo alla TC o RMN Candidiasi disseminata Almeno 1 delle 2 entità dopo un episodio di candidemia nelle 2 settimane precedenti Piccole lesioni a bersaglio (bull s eye) a livello di fegato o milza Essudati retinici (esame oftalmoscopico) L introduzione della TC a strato sottile e l impiego dell antigene galattomannano (GM) su siero hanno notevolmente migliorato la capacità diagnostica di AI. Nei pazienti ad alto rischio è consigliabile pertanto eseguire TC a strato sottile e determinazione dell antigene galattomannano (almeno due determinazioni separate). Per quanto riguarda l antigene galattomannano sono considerati positivi valori superiori a 0,5. La dimostrazione di due risultati sequenziali con un OD 0.5 porta la specificità del saggio a valori del 98 % nei pazienti ematologici. L incidenza di falsi positivi varia dal 5 % negli adulti fino all 83 % nei neonati prematuri. In questi ultimi, i risultati falsi positivi sono in parte ascrivibili a traslocazione intestinale di galattomannano; un meccanismo simile è stato ipotizzato nei pazienti neoplastici con gravi mucositi farmacoindotte. Altre condizioni associate a risultati falsi positivi descritte in letteratura sono le seguenti: somministrazione endovena di piperacillinatazobactam e somministrazione orale o endovena di amoxicillinaclavulanato; terapia di condizionamento con ciclofosfamide; reattività crociata in pazienti con altre infezioni fungine (penicilliosi marneffei; istoplasmosi; criptococcosi); patologie autoimmunitarie o a patogenesi autoimmunitaria (trapiantati di fegato con epatite autoimmune; GVHD cronica). La somministrazione di farmaci antifungini (per esempio per la profilassi primaria nei pazienti ematologici) riduce notevolmente la sensibilità diagnostica dell antigene galattomannano. Va inoltre ricordato che la sensibilità diagnostica di questo test è bassa (3050%) nei trapiantati di organo solido, nei pazienti ospedalizzati in ICU e nei pazienti con BPCO. Poiché il GM è una molecola solubile la sua determinazione può essere effettuate anche su altri fluidi biologici (per esempio lavaggio broncoalveolare e liquor cefalorachidiano). Due metaanalisi hanno dimostrato che la ricerca di GM su BAL è più sensibile ma meno specifica rispetto al siero (Guo et al. Chest 2010; Zou et al. Plos One 2012). Non è stato stabilito con certezza un valore soglia per indicare la positività del GM su BAL ma nella maggior parte degli studi viene utilizzato un valore superiore a 0.5 (Guinea et al. Mycopathologia 2014). La più bassa
23 specificità del GM su BAL è stata osservata nei pazienti affetti da BPCO come conseguenza probabilmente dell elevata colonizzazione da parte di Aspergillus in questa popolazione di pazienti. E importante ricordare che il dato microbiologico va sempre interpretato nel contesto del quadro clinico e ciò è tanto più vero quando si utilizzano biomarcatori come GM. Nella tabella 10 sono schematizzati la forza e la qualità dell evidenza relativi al GM secondo le linee guida dell ESCMID di prossima pubblicazione (Lagrou et al. ESCMID 2014). L utilizzo di altri biomarcatori fungini (1,3βdglucanomarcatore panfungino) e della PCR per Aspergillus, proposti in molti studi, non viene presa in considerazione in quanto entrambe le metodiche non sono disponibili presso il nostro laboratorio. Tabella 10 Evidenze nell impiego di galattomannano (GM) su vari liquidi biologici per la diagnosi di AI secondo le linee guida ESCMID 2014 Galattomannano su plasma (siero) Popolazione Intervento Qualità /forza dell evidenza Commento Neutropenia prolungata e pazienti sottoposti a AlloHSCT in assenza di profilassi nei confronti di muffe GM su sangue per diagnosi di aspergillosi invasiva AI Pazienti con neoplasia ematologica Neutropenici Non neutropenici GM su sangue AII BII Richiesti 2 determinazioni consecutive con un OD index 0.5 per la più elevata accuratezza diagnostica. Il monitoraggio prospettico deve essere effettuato con la valutazione clinica e HRCT Minore sensibilità nei pazienti non neutropenici Pazienti ricoverati in ICU GM su sangue CII Migliore performance nei pazienti neutropenici Pazienti sottoposti a trapianto di organo solido GM su sangue CII Bassa sensibilità, buona specificità; la maggior parte degli studi condotti nei trapiantati di polmone Galattomannano su lavaggio broncoalveolare Tutti i pazienti Galattomannano su liquor GM su BAL per diagnosi di aspergillosi polmonare AII Marcatore con ottima efficacia; il miglior cutoff compreso tra 0.5 e 1.0 (< 0.5 esclude la diagnosi) GM su CSF per diagnosi di aspergillos cerebrale BII Non esiste un cutoff validato Fonte: Lagrou K et al. Diagnostic group 2014 ESCMID Aspergillus guidelines (parzialmente modificata)
24 Monitoraggio microbiologico L antigene galattomannano (GM) sul siero è stato proposto come un marcatore surrogato di risposta alla terapia antifungina in quanto diversi Autori hanno evidenziato una riduzione dei livelli sierici nei pazienti che rispondono alla terapia o al contrario un graduale incremento o la ricomparsa nei pazienti con mancata risposta o recidiva della malattia. In uno studio prospettico un incremento dell OD di 1.0 rispetto al baseline valutato dopo 7 giorni era predittivo di fallimento della terapia e potenzialmente giustifica una modificazione del regime antifungino. Terapia dell aspergillosi invasiva I farmaci registrati con indicazione all impiego nell aspergillosi invasiva sono : 1) Polieni (amfotericina B deossicolato; amfotericine liposomiche); 2) i triazolici a spettro allargato (voriconazolo, itraconazolo, posaconazolo) ; 3) tra le echinocandine per ora solo caspofungina. Scelta del farmaco Sulla scorta di uno studio clinico randomizzato che ha valutato comparativamente voriconazolo (6 mg/kg due volte al giornodose carico seguito da 4 mg/kg due volte al giorno) vs amfotericina B deossicolato (11,5 mg/kg/die ev) in cui l analisi di un outcome composito mise in evidenza una differenza del 21 % (53 % vs 32%) a favore di voriconazolo quest ultimo è considerato il farmaco di scelta per il trattamento dell aspergillosi invasiva (sia per IDSA sia per ESCMID). Amfotericina B liposomiale è considerata la migliore alternativa a voriconazolo nei pazienti intolleranti o refrattari a voriconazolo. In base ai risultati dello studio AmbiLoad in cui vennero confrontati due dosaggi iniziali (3 mg/kg/die vs 10 mg/kg/die) con risultati analoghi (46 % vs 50%) ma maggiore tossicità nel braccio ad alte dosi, il dosaggio di 3 mg/kg/die è quello considerato raccomandabile anche se nella pratica clinica si ricorre spesso ad un dosaggio più elevato (5 mg/kg/die) in considerazione della gravità della malattia. Vi è accordo da parte degli esperti ribadito anche da una recente Consensus italiana (GITMO) a non impiegare più amfotericina B deossicolato a causa della ben nota nefrotossicità e delle reazioni infusionali che ne richiedono riduzione della dose o sospensione con una riduzione attesa della risposta (Girmenia et al. Clin Infect Dis 2009). Per quanto riguarda gli altri farmaci caspofungina rappresenta una possibile alternativa terapeutica con percentuali di risposta riportate del 3240 %; anche itraconazolo somministrato per via endovenosa e posaconazolo (per os) possono essere considerate alternative impiegabili in caso di intolleranza o refrattarietà alle terapie di prima linea. E comunque buona norma non impiegare itraconazolo o posaconazolo nel caso in cui il regime iniziale sia stato con voriconazolo per il medesimo meccanismo d azione e per la possibile resistenza crociata. In tabella 11 sono riportati in maniera riassuntiva i farmaci utilizzabili e i relativi dosaggi.
25 Va segnalato che è in corso di verifica da parte di FDA ed EMA l approvazione di isavuconazolo con l indicazione per il trattamento sia di aspergillosi invasiva sia di mucormicosi. Nelle linee guida ESCMID relative all aspergillosi invasiva isavuconazolo ha ricevuto un punteggio AII per la terapia di aspergillosi polmonare invasiva in attesa della pubblicazione dello studio clinico randomizzato e controllato. Tabella 11 Raccomandazioni per la terapia dell aspergillosi invasiva Condizione clinica Terapia di I scelta Terapia alternativa Commenti Aspergillosis invasiva polmonare Aspergillosi invasiva dei seni Aspergillosi tracheobronchiale Aspergillosi polmonare cronica necrotizzante Aspergillosi del SNC Infezione del cuore (endocardite, pericardite miocardite) Osteomielite e artrite settica Endoftalmite e cheratite Voriconazolo 6 mg/kg/ev ogni 12 ore, 1 giorno, quindi 4 mg/kg/ev ogni 12 ore; dose orale 200 mg ogni 12 ore Richiede una terapia chirurgica e medica E indispensabile una resezione chirurgica dei tessuti devitalizzati Indicata terapia intraoculare/sistemica + intervento oftalmologico (vitrectomia parziale) Amfotericina B liposomiale (35 mg/kg/ev/die Caspofungina 70 mg ev 1 giorno, poi 50 mg ev Itraconazolo 200 mg/ev ogni 12 ore per 2 giorni quindi 200 mg/die Posazonazolo 200 mg ogni 6 ore per os, quindi con stabilizzazione della malattia 400 mg ogni 12 ore per os Simile all aspergillosi polmonare invasiva Simile all aspergillosi polmonare invasiva Simile all aspergillosi polmonare invasiva In assenza di dati clinici provenienti da studi randomizzati non è raccomandato l impiego routinario di terapia di combinazione; la terapia di combinazione può essere presa in considerazione in caso di mancata risposta (clinicoradiologica e microbiologica) o di peggioramento; in questi casi è opportuno impiegare farmaci che agiscono su un diverso bersaglio (caspofungina+ azolico; azolico+ amfotericina B liposomiale) Nella forma polmonare cronica che richiede una terapia della durata di mesi è opportuno impiegare un triazolico orale Esperienza limitata a singoli casi soprattutto con AMFB deossicolato. Esperienza limitata a singoli casi soprattutto con AMFB deossicolato. Terapia topica indicata per la cheratite; la terapia sistemica sembra essere importante nella cura dei casi di endoftalmite Terapia di combinazione La disponibilità di nuovi farmaci antifungini con differenti bersagli d azione e profili di tossicità favorevoli e dati di studi in vitro e in vivo su modelli animali con evidenze favorevoli hanno fatto porre la speranza che la terapia di combinazione potesse migliorare l outcome di pazienti con diagnosi di aspergillosi invasiva. Nonostante vi siano alcune evidenze dai dati pubblicati che la terapia di combinazione dell aspergillosi invasiva possa migliorare la prognosi nei pazienti ematologici (tabella 12) vi sono delle limitazioni metodologiche (numero limitato di pazienti trattati; numero limitato di pazienti con diagnosi certa o probabile; assenza di studi prospettici randomizzati) che allo stato attuale non permettono di indicare la terapia di combinazione come una
26 terapia raccomandata. Una recente analisi, che ha preso in considerazione anche i trials non pubblicati ha evidenziato che la terapia di combinazione per l aspergillosi invasiva non è più efficace della monoterapia e il suo impiego non è giustificato per l incremento dei costi (MartinPena et al. Clin Infect Dis 2014). La terapia antifungina di combinazione non può quindi essere raccomandata per il trattamento dell aspergillosi invasiva; si ritiene pertanto che possa essere presa in considerazione solo in alcuni eccezionali casi singoli come terapia di salvataggio quando vi siano indicazioni di un rapido e drammatico peggioramento clinico e radiologico della malattia, sia stata esclusa una sindrome da immunoricostituzione, le concentrazioni dei farmaci di prima scelta siano comprese nel range terapeutico. Tabella 12 Studi clinici di terapia di combinazione nel trattamento di aspergillosi invasiva Autore, tipologia studio Aliff, Cancer 2003; 97: Retrospettivo Marr, Clin Infect Dis 2004; 39: ; Marr, Clin Infect Dis 2005; 40: Sequenziale Kontoyannis, Cancer 2003; 98: Retrospettivo Singh, Transplantation 2006; 81: Sequenziale Kontoyannis, Cancer 2005; 103: Sequenziale Maertens, Cancer 2006; 107: Terapia di salvataggio Calliot, Cancer 2007; 110: Raad, Leukemia 2008;22: Terapia di salvataggio Mihu, Cancer 2010; 116:52906 Terapia di salvataggio (retrospettivo) farmaci Pazienti % di aspergillosi certa/probabile Caspofungina+ AMBc vs LAMB AMBc seguita da caspo+lamb/ablc vs AMBc seguita da voriconazolo Caspo+ LAMB 48 (50% HCST; 50% leucemici) LAMB vs caspo+voriconazolo Itraconazolo+ AMB lipidica vs AMB lipidica Caspo+AMB o caspo+triazoli LAMB (10 mg/kg) vs L AMB (3 mg/kg)+ caspo Posaconazolo vs HD (>7,5 mg)lamb+ caspo vs HDLAMB LAMB vs AMB+echinocandine vs echinocandine Risultati 30 (leucemici) C=20%; P=13% Risposta favorevole 60%; aspergillosi certa 83% 47 (HSCT) C= 58% vs 75 %; P=42 % vs 25% 87 (100% trapianto organo solido) 11/101 (100% neoplasie ematologiche) 53 (85% ematologici; 53% neutropenici) refrattari o intolleranti alla monoterapia 30 (100% neoplasie ematologiche 53 pazienti ematologici vs 38 vs 52 (controlli storici) Sopravvivenza a 3 mesi migliore con la terapia di combinazione; nessuna differenza sulla sopravvivenza a 12 mesi CP=48% Risposta globale 42% (22% diagnosi certa) C= 51,1% vs 55%; P=48,9% vs 45% C= 36% vs 39%; P= 64% vs 61% C=24.5%;P=62.5% CP= 100% C= 2140% (nei 3 gruppi); P=6079% 159 pazienti ematologici C=36% (nei 3 gruppi); P=64% AMBc= amfotericina B deossicolato; LAMB= amfotericina B liposomiale; C= certa; P=probabile Outcome favorevole 70% combo vs 51% L AMB (ns) Nessuna differenza risposta alla fine terapia; morti simili nei due gruppi (46% vs 45%) 55% con risposta favorevole (13.7% completa) Risposta alla fine trattamento 67% combo vs 27% (p=0.028); sopravvivenza a 12 settimane 100% vs 80% Risposta favorevole globale 40% posaconazolo, 8% HD LAMB, 11% combo (P< 0.001) Nessuna differenza nella risposta: Combo 9%, Ech 13%, LAMB 3%
27 Aspergillosi broncopolmonare allergica (ABPA) Si tratta di una patologia polmonare causata da una reazione di ipersensibilità nei confronti di Aspergillus fumigatus che può complicare il decorso clinico di pazienti affetti da asma bronchiale e fibrosi cistica (Agarwal et al. Clin Exp Allergy 2013). Occasionalmente l ABPA può insorgere in pazienti affetti da altre patologie polmonari (BPCO, bronchiectasia idiopatica, bronchiectasia posttubercolare, bronchiectasia secondaria a sindrome di Kartagener, malattia cronica granulomatosa e sindrome da iperige). Secondo una stima recente ne sarebbero affetti a livello mondiale circa 4,8 milioni di individui con asma attiva e di questi circa 1 milione nella sola Europa (Denning et al. Med Mycol 2013). Clinicamente i pazienti presentano asma non controllata, broncospasmo, emottisi e tosse produttiva. Altri sintomi riportati sono febbricola, calo ponderale e astenia. In tabella 13 sono riportati i criteri diagnostici per ABPA proposti dal gruppo di lavoro dell ISHAM. Tabella 13 Nuovi criteri proposti per la diagnosi di aspergillosi broncopolmonare allergica (ABPA) Condizioni predisponenti Asma bronchiale, fibrosi cistica Criteri obbligatori (entrambi devono essere presenti) Positività a cutireazione nei confronti di Aspergillus di tipo I (ipersensibilità cutanea immediata verso antigene di Aspergillus) o elevati livelli di IgE contro Aspergillus fumigatus Livelli elevati di IgE totali (> 1000 IU/mL)* Altri criteri (almeno 2 di 3) Presenza di precipitine o anticorpi IgG nei confronti di A.fumigatus Alterazioni radiografiche polmonari compatibili con ABPA Valori di eosinofili totali > 500/µL (nei pazienti non trattati con steroidi il dato può essere anche storico) * Se nel paziente sono soddisfatti tutti gli altri criteri può essere considerato accettabile anche un valore di IgE < 1000 IU/mL. Un quadro radiografico compatibile con ABPA può essere transitorio (i.e., addensamento, noduli, tramtrack opacities (opacità su linee parallele), toothpaste/fingeringlove opacities (dita nel guanto espressione di broncocele) o permanente (i.e. linee parallele e ombre ad anello, bronchi ectasie e fibrosi pleuropolmonare) La terapia dell ABPA si avvale di farmaci ad attività antiinfiammatoria (corticosteroidi per via sistemica) per sopprimere l attività immunitaria e di farmaci antifungini per ridurre la carica fungina a livello delle vie aeree. Gli obiettivi della terapia sono il controllo dell asma, la prevenzione e il trattamento delle esacerbazioni acute e l arresto dello sviluppo di bronchi ectasie. La patologia è di pertinenza squisitamente pneumologia. Per quanto riguarda la terapia antifungina quest ultima richiede l impiego di itraconazolo 200 mg due volte al giorno (con TDM) per almeno 16 settimane.
28 Criptococcosi La criptococcosi è una grave infezione micotica osservata prevalentemente in paziente immunocompromessi (La Hoz et al. Drugs 2013); è causata da Cryptococcus neoformans (sierotipi A, D e AD) e C. gattii (sierotipi B e C); quest ultimo responsabile di infezioni soprattutto in soggetti immunocompetenti è presente nelle aree tropicali e subtropicali anche se più recentemente è stata descritta una epidemia in Canada (Isola di Vancouver, British Columbia) che sembra essersi diffusa anche nelle regioni settentrionali degli USA (Harris et al. Clin Infect Dis 2011). Il fungo è responsabile soprattutto di quadri di meningite e meningoencefalite in particolare nei pazienti affetti da AIDS. Al di fuori del paziente con infezione da HIV è possibile osservare la criptococcosi nei soggetti affetti da numerose patologie (tabella 14 ) che comportano una riduzione della capacità di risposta cellulomediata del sistema immunitario. Tabella 14 Patologie e condizioni predisponenti associate allo sviluppo di criptococcosi Infezione da HIV (conta dei linfociti CD4+ 200/µL) Terapia steroidea cronica Trapianto di organo solido Trapianto di cellule staminali emopoietiche Neoplasie ematologiche (linfoma di Hodgkin; linfoma non Hodgkin) Terapie biologiche (etanercept; infliximab; alemtuzumab) Neoplasie Diabete mellito Cirrosi epatica Linfocitopenia CD4+ idiopatica Insufficienza renale cronica Malattie del connettivo (LES; sarcoidosi; sindrome da iperigm e/o IgE) L infezione inizia generalmente a carico dell apparato respiratorio causando raramente sintomi a questo livello; quindi il fungo si dissemina per via ematogena e raggiunge il sistema nervoso centrale dove provoca come detto un quadro di meningite o di meningoencefalite. I sintomi meningei (cefalea, rigor nucalis, vomito, segni ipertonicoantalgici), soprattutto nei pazienti gravemente immunocompromessi possono mancare (in parte o del tutto) e sono presenti complessivamente nel 25 % dei casi. Spesso l unico sintomo presente è la cefalea che si caratterizza per la persistenza e la non responsività ai farmaci antidolorifici; è pertanto necessario quando sia nota la condizione di immunodepressione un elevato indice di sospetto della malattia. Diagnosi di meningite criptococcica E necessario eseguire la puntura lombare con esame chimicofisico del LCR, colorazione con inchiostro di china, ricerca dell antigene criptococcico e coltura per miceti. L esame chimicofisico del LCR in genere si caratterizza per la presenza di un liquor limpido con una spiccata
29 ipoglicorrachia, modesta iperproteinorrachia e scarsa cellularità; nei pazienti affetti da AIDS; tanto maggiore è il grado di immunodepressione tanto minore sarà la cellularità sul liquor. La diagnosi di certezza richiede l isolamento del micete dal liquor; tuttavia una diagnosi presuntiva può essere effettuata rapidamente con la colorazione con inchiostro di china (India ink) e con la ricerca dell antigene criptococcico; il primo, soprattutto nei pazienti affetti da AIDS, presenta una sensibilità dell 80 %; l antigene criptococcico (test rapido la cui risposta è disponibile nel giro di poche ore) presenta una sensibilità del 9798 % e una specificità del %. L antigene criptococcico può essere ricercato anche sul siero (con sensibilità e specificità sovrapponibile a quella osservata sul liquor nei pazienti con meningite criptococcica), su liquido di lavaggio broncoalveolare e urina. L antigene viene titolato ed è considerato positivo un titolo uguale o superiore a 1:41:8. E opportuno sempre eseguire anche emocoltura e urinocoltura per miceti per documentare una infezione disseminata. Altri metodi di diagnosi Cryptococcus neoformans può essere documentato anche su biopsie provenienti da cute, midollo osseo, polmone, linfonodi; si utilizzano colorazioni specifiche per miceti (GrocottGomori, PAS) e la colorazione con mucicarminio per la capsula. Monitoraggio microbiologico Nella meningite criptococcica e necessario documentare una negativizzazione della liquorcoltura (almeno una anche se sarebbero richieste 2 esami consecutivi negativi) prima di deescalare la terapia iniziale (vedi dopo). Terapia La meningite criptococcica non trattata conduce invariabilmente a morte; è necessario pertanto istituire una terapia antimicotica il più precocemente possibile; l obiettivo principale è rappresentato dalla necessità di sterilizzare il LCR il più rapidamente possibile con una terapia di associazione; tradizionalmente la terapia prevede una fase di induzione di 2 settimane impiegando amfotericina B deossicolato più flucitosina; la necessità di impiegare dosi crescenti di amfotericina B deossicolato per raggiungere il dosaggio appropriato (0,71 mg/kg) e i frequenti effetti collaterali durante l infusione (febbre elevata; artralgie; flebiti) oltre alla nota nefrotossicità fanno oggi preferire l impiego di amfotericina B liposomiale pur essendo quest ultima più costosa; il costo del farmaco verrebbe ammortizzato da una durata inferiore della degenza. La terapia di combinazione è considerata sempre la prima scelta nel trattamento della meningite criptococcica anche al di fuori del paziente con infezione da HIV (Perfect et al. Clin Infect Dis 2010). Le linee guida dell IDSA, aggiornate nel 2010, hanno a questo proposito individuato tre scenari possibili: paziente con infezione da HIV; paziente sottoposto a trapianto d organo; paziente HIVsieronegativo non sottoposto a trapianto. Nel primo e nell ultimo scenario viene sempre
30 indicato dalle linee guida l impiego iniziale di amfotericina B deossicolato con possibilità di modificare con una formulazione liposomica nel caso di insufficienza renale mentre nel paziente trapiantato di organo solido l opzione iniziale è considerata una formulazione liposomica di amfotericina. Sulla scorta della nostra esperienza e per quanto sopra riportato in relazione alla tossicità di amfotericina B deossicolato si ritiene di indicare come trattamento privilegiato in tutti gli scenari clinici l impiego dall inizio di amfotericina B liposomiale anche a discapito di amfotericina B in complessi lipidici (ABLC) che pur avendo un costo inferiore alla prima, si caratterizza per molti degli effetti collaterali associati alla formulazione deossicolato. Nei pazienti con una elevata carica micotica sul LCR (definita in base al CFU o al titolo dell antigene criptococcico) la dose di amfotericina B liposomiale può essere incrementata fino a 6 mg/kg/die. Alla fase di induzione segue una terapia di consolidamento per almeno 8 settimane con fluconazolo ad alte dosi (612 mg/kg/die). Nei pazienti immunocompromessi è poi necessario effettuare una terapia di mantenimento (di durata variabile a seconda della tipologia di paziente) sempre con fluconazolo. Nei pazienti trapiantati viene suggerito di proseguire la terapia di mantenimento per 612 mesi poiché i tassi di recidiva tardiva non superano l 13% (Singh et al. Transplantation 2005; Baddley et al. Am J Transplant 2013). E possibile anche nei pazienti con infezione da HIV sospendere la terapia di mantenimento dopo avere ottenuto una significativa immunoricostituzione in seguito all istituzione di una terapia antiretrovirale efficace (vedi tabella 15). Benché non vi siano studi con numerosità del campione significativa vi è accordo che dopo aver ricevuto almeno 1 anno di terapia di mantenimento con triazoli, una conta dei linfociti CD4+ > 100/µL e un controllo della replicazione di HIV per > 3 mesi si possa sospendere la terapia cronica antifungina (Mussini et al. Clin Infect Dis 2004). La persistente positività dell antigene criptococcico su siero (a titoli non elevati) in assenza di segni clinici di malattia (e con esami colturali negativi) non costituisce in questi pazienti una controindicazione alla sospensione della terapia antimicotica di mantenimento (Antinori, Am J Med 2007). Per la localizzazione polmonare (con sintomi da lieve a moderato), dopo aver escluso con la puntura lombare il coinvolgimento cerebrale, può essere considerata la terapia con il solo fluconazolo (400 mg/die) per almeno 612 mesi. Nei casi gravi (per esempio con quadro di ARDS) è indicato il trattamento come nei pazienti con coinvolgimento cerebrale.
31 Sindrome infiammatoria da immunoricostituzione (IRIS) Nel corso degli ultimi anni è stata descritta sia nei pazienti con infezione da HIV sia nei trapiantati di organo solido la possibile comparsa in seguito ad una ricostituita capacità di risposta immunitaria, di una sindrome infiammatoria denominata IRIS (sindrome infiammatoria da immunoricostituzione). Tale sindrome può presentarsi con un peggioramento del quadro clinico dopo iniziale miglioramento indotto dalla terapia antifungina(forma paradossa) oppure con la comparsa exnovo detta anche smascheramento (unmasking) di una infezione latente. Clinicamente la IRIS può presentarsi con il quadro clinico di una meningite asettica, con lesioni cerebrali espansive, idrocefalo, noduli polmonari, linfadenite e cellulite oppure con una meningite con liquorcoltura positiva ed elevata cellularità (nel caso di unmasking IRIS) Nel paziente trapiantato la IRIS viene osservata in seguito alla rapida riduzione della terapia immunosoppressiva in associazione all inizio della terapia antifungina. In questi pazienti si ritiene che il quadro possa essere precipitato dalla transizione da una risposta prevalentemente di tipo Th2 (indotta dai farmaici immunosoppressori) ad una risposta Th1 (proinfiammatoria). Nei pazienti con infezione da HIV una rapida risalita dei valori dei linfociti CD4+ indotta dalla terapia antiretrovirale rappresenta l evento scatenante questa sindrome. In questi ultimi la prevalenza della comparsa di IRIS è globalmente del 19,5% ed è responsabile della morte del paziente nel 20.8% (Muller et al. Lancet Infect Dis 2010). Il momento migliore per iniziare la terapia antiretrovirale nei pazienti HIVsieropositivi in cui venga posta diagnosi di meningite criptococcica resta non definito con precisione. Poiché si tratta di pazienti gravemente immunocompromessi l inizio precoce della terapia antiretrovirale è generalmente consigliato ma va considerato anche il rischio di complicanze e morte indotto dalla IRIS. Per tale motivo la maggior parte delle linee guida consigliano di iniziare la terapia antiretrovirale dopo almeno 210 settimane dall inizio della terapia antifungina. Uno studio recente condotto in Sudafrica e Uganda su pazienti con meningite criptococcica AIDScorrelata (trattata per 14 giorni con amfotericina B 0,71 mg/kg/die + fluconazolo 800 mg/die seguiti da fluconazolo) che iniziavano la terapia antirtrovirale precocemente (1 o 2 settimane dopo la diagnosi) o dopo 5 settimane dalla diagnosi ha mostrato a 26 settimane un eccesso di morti con l inizio precoce della terapia antiretrovirale (45% vs 30% HR 1.73; IC 95% ;P=0.03) (Boulware et al. N Engl J Med 2014). Diversi studi hanno valutato i possibili fattori di rischio per la comparsa di IRIS nei pazienti con criptococcosi AIDSassociata. A parte l inizio precoce della terapia antiretrovirale (peraltro non dimostrato in alcuni studi), la presenza di fungemia, valori elevati di antigenemia e una ridotta risposta infiammatoria iniziale nel
32 liquor (conta dei globuli bianchi < 25/µL e protidorrachia < 50 mg/dl) sono altri fattori di rischio indicativi di una infezione micotica grave e/o con elevata carica micotica. Sulla base di questi dati sembra pertanto opportuno dilazionare di almeno 4 settimane l inizio della terapia antiretrovirale e comunque non intraprenderla prima di avere dimostrato la sterilizzazione della liquorcoltura. E opportuno ricordare che la diagnosi di IRIS resta una diagnosi di esclusione e in ogni caso devono essere effettuate tutte le indagini microbiologiche utili per escludere o confermare una recidiva di malattia criptococcica o la presenza di nuove patologie opportunistiche. Non esiste una definizione condivisa di IRIS ma si consiglia di fare riferimento alle definizioni di forma paradossa e a quella di patologia associata alla terapia antiretrovirale (che comprende l unmasking IRIS) proposte dall International Network for the Study of HIVassociated IRIS (INSHI) (Haddow et al. Lancet Infect Dis 2010). Antigenemia criptococcica e preemptive therapy. La possibile presenza di antigenemia criptococcica isolata in pazienti HIVsieropositivi asintomatici ma con grave immunocompromissione era una situazione clinica nota anche prima dell introduzione delle terapie antiretrovirali altamente efficaci (HAART). Tuttavia la sua rilevanza da un punto di vista prognostico è emersa chiaramente, soprattutto nei Paesi a risorse limitate, dopo l introduzione della HAART. Uno studio condotto in Sudafrica ha dimostrato che avere uno screening per l antigene criptococcico negativo sul plasma 2 settimane prima dell inizio della terapia antiretrovirale è associato ad un valore predittivo negativo del 100% per lo sviluppo di meningite criptococcica nel primo anno di terapia antiretrovirale. Al contrario la sua positività si associa alla comparsa di meningite criptococcica in più di un quarto dei pazienti con un adjusted hazard di morte del 3.2% (Jarvis et al. Clin Infect Dis 2009). Poiché l antigene criptococcico è rilevabile nel siero con una mediana di 3 settimane prima della comparsa di meningite criptococcica, l esecuzione del test e il trattamento dei soggetti risultati positivi rappresenta un potenziale metodo per ridurre la letalità associata a questa patologia che rimane elevata anche in epoca HAART. Nel 2011 l OMS ha dichiarato che l inizio precoce della terapia antiretrovirale costituisce la strategia preventiva più efficace per ridurre l incidenza e l elevata letalità della meningite criptococcica.come raccomandazione condizionale l OMS ha indicato lo screening routinario e il trattamento dell antigenemia criptococcica prima dell inizio della terapia antiretrovirale nei pazienti naive con valori di linfociti CD4+ inferiori a 100/uL in aree con elevata prevalenza (circa il 3%) di antigenemia criptococcica. Diversi Paesi a cosiddette risorse limitate (Sudafrica, Mozambico, Ruanda) hanno implementato questa strategia ma il suo impiego è stato
33 evocato anche nei Paesi a risorse elevate (Rajasingham et al. Clin Infect Dis 2012). Uno studio condotto a Londra in pazienti con nuova diagnosi di infezione da HIV e conta dei linfociti CD4+ < 100/µL ha indicato una prevalenza pari al 5% (Patel et al J Infect 2013). Più recentemente i CDC hanno condotto uno studio retrospettivo sul siero di 1872 pazienti con infezione da HIV e conta dei linfociti CD4+ < 100/µL raccolti dal 1986 al 2012 dal Multicenter AIDS Cohort Study (MACS) dimostrando una prevalenza globale di antigene mia criptococcica negli Stati Uniti del 2.9% (IC 95% 2.2%3.7%) (McKenney et al. MMWR 2014). Sulla base di questi dati i CDC suggeriscono l implementazione di una strategia di screening che sarebbe costeffective. Non si dispongono di dati sulla prevalenza dell antigenemia criptococcica nella popolazione italiana di pazienti HIVsieropositivi ma è verosimile che non si discosti di molto da quanto segnalato negli Stati Uniti. Si suggerisce pertanto di effettuare tale screening in tutti i pazienti con diagnosi di infezione da HIV late presenter (linfociti CD /µL) prima di intraprendere la terapia antiretrovirale e di effettuare una terapia preempitive con fluconazolo secondo quanto riportato nell algoritmo in figura 4. Riscontro di positività per HIV (i.e., antihiv+) Linfociti CD4+ < /µL CRAg screening Negativo Terapia HAART Positivo Sintomi Puntura lombare Asintomatico* CM Fluconazolo 800 mg/die x 2 settimane Trattare la meningite criptococcica secondo linee guida Inizio HAART dopo 2 settimane Fluconazolo 400 mg/die x 8 settimane Figura 4 Algoritmo per l implementazione dello screening per la ricerca di antigene criptococcico (CrAg) e la terapia preemptive. * E consigliabile effettuare la puntura lombare in tutti i pazienti con risultato positivo per l antigene criptococcico su siero. Inoltre è sempre consigliabile eseguire almeno 1 emocoltura per miceti. CM= meningite criptococcica; HAART= Highly active antiretroviral therapy. Fonte Jarvis et al. JIAPAC 2012
34 Tabella 15 Schemi di terapia della criptococcosi Localizzazione Terapia di I scelta Alternative Sistema nervoso centrale (meningite criptococcica) Induzione (minimo 2 settimane) Amfotericina B liposomiale 34 mg/kg/die ev + flucitosina 100 mg/kg/die ev (refratto in 4 somministrazioni) * oppure Amfotericina B liposomiale 34 mg/kg/die per 46 settimane (schema senza flucitosina) oppure Amfotericina B deossicolato 0,71 mg/kg/die ev + flucitosina 100 mg/kg/die (refratto in 4 somministrazioni) Consolidamento: minimo 8 settimane Fluconazolo 400 mg/die per os o Fluconazolo 800 mg/die per os (dosaggio consigliato nel caso in cui non sia stata utilizzata flucitosina nella terapia di induzione) Mantenimento : fluconazolo 200 mg/die per os La terapia di mantenimento può essere sospesa nei pazienti che presentino immunoricostituzione in seguito a terapia HAART (CD4> 100/µL > 6mesi) Fluconazolo mg/die ev + flucitosina 100 mg/kg/die (refratto in 4 somministrazioni) per 610 settimane Fluconazolo mg /die per 1012 settimane (quando impiegato da solo va utilizzata la dose massima tollerata e comunque si suggerisce di utilizzare almeno 1200 mg/die in considerazione dell effetto statico del farmaco) * Itraconazolo 200 mg x2/die per os Polmone * Schema consigliato Fluconazolo 400 mg/die per os per 612 mesi Itraconazolo 400 mg/die per os per 612 mesi Amfotericina B deossicolato 0,5 mg/kg/die ev (dose totale 12 g)
35 Mucormicosi (Zigomicosi) Mucormicosi è il termine utilizzato per descrivere le infezioni causate da funghi appartenenti all ordine Mucorales. Zigomicosi, usato in precedenza e come sinonimo è considerato meno accurato per descrivere questa grave patologia in base alla recente riclassificazione tassonomica che ha abolito gli Zygomycetes come classe (Spelberg et al. Clin Microbiol Rev 2005, KwonChung Clin Infect Dis 2012). Gli zigomiceti sono microrganismi ubiquitari e termotolleranti presenti soprattutto come saprofiti nel materiale organico ; producono in maniera significativa spore che vengono inalate. I membri dell ordine Mucorales causano le forme più gravi di zigomicosi che oggi vengono come detto preferibilmente riferite come mucormicosi. I miceti appartenenti al genere Entomophthorales sono responsabili di forme a decorso cronico a carico della mucosa nasale e dei tessuti sottocutanei osservate per lo più in individui immunocompetenti in aree tropicali e subtropicali. La mucormicosi è considerata una infezione emergente, soprattutto nei pazienti ematologici in particolare tra coloro che sono stati sottoposti a profilassi antifungina come cosiddette breakthrough infection (tabella 16). I generi responsabili della maggior parte dei casi di mucormicosi sono : Rhizopus, Mucor, Lichtheimia (in precedenza nota come Absidia), Cunninghamella, Rhizomucor, Apophysomyces e Saksenaea. Nei pazienti ematologici la localizzazione più frequente è quella polmonare ma possono essere coinvolti altri siti (seni paranasali, encefalo, cute, tratto digerente) e talora si osservano quadri di malattia disseminata (più di un sito coinvolto). Tabella 16 Fattori predisponenti per mucormicosi nei pazienti con neoplasie ematologiche e/o sottoposti a trapianto di cellule staminali Neutropenia prolungata (> 3 settimane) e grave (< 200 neutrofili/µl) Monocitopenia (< 100/µL) Somministrazione prolungata (> 3 settimane) di alte dosi di corticosteroidi (prednisone o equivalente > 1mg/kg/die) Sovraccarico di ferro (valutato con elevati indici di ferro, o con colorazione su biopsia osteomidollare) Trapianto di cellule staminali ad alto rischio (Donatore non correlato; donatore aploidentico; da cordone ; depleto di cellule T) GvHD grave e suo trattamento (specialmente con corticosteroidi) Recidiva di leucemia Precedente esposizione a farmaci antifungini attivi verso Aspergillus (specialmente voriconazolo)? Iperglicemia prolungata (a digiuno > 200 mg/dl); iperglicemia associata a terapia con corticosteroidi; diabete mellito GvHD, graft versus host disease Fonte : Kontoyannis et al. Blood 2011
36 Tabella 17 Condizioni predisponenti associate a mucormicosi Diabete mellito Chetoacidosi Trapianto allogenico di cellule staminali Trapianto di organo solido Emocromatosi in terapia con deferoxamina Neutropenia Diagnosi La diagnosi di mucormicosi si basa su un elevato indice di sospetto (condizioni predisponenti, vedi tabella 16 e 17), segni e sintomi clinici di presentazione, imaging ed esame istopatologico e colturale di campioni clinici appropriati. I campioni utilizzabili per la diagnosi istopatologica e colturale sono rappresentati da scraping cutaneo da lesioni della cute; scraping e aspirato da lesioni dei seni (forma rinocerebrale); lavaggio broncoalveolare; materiale proveniente dal naso; biopsie tissutali in pazienti con forme gastrointestinali e/o disseminate. Il materiale raccolto (seni nasali o escreato) e le biopsie devono essere analizzati impiegando KOH al 10% o FungiFluor ; gli elementi fungini possono essere scarsi nei campioni citologici e quando presenti possono essere frammentati. Le caratteristiche su materiale citologico sono quelle di ife rifrangenti (615 µm), cellule ingrossate e talora ife distorte. L esame istopatologico mostra un processo infiammatorio suppurativo con focali aree di infiammazione granulomatosa; le ife (diametro 630 µm) appaiono nonsettate o paucisettate e irregolarmente ramificate (con angoli > 90 ); è caratteristica l angioinvasione con trombosi e infarto. Le colorazioni con ematossilinaeosina (EE) devono essere completate con colorazioni specifiche per miceti (Grocott Gomori argento o PAS). Questi funghi sono come è noto di difficile dimostrazione in coltura e negli ultimi anni sono stati impiegati con successo metodi molecolari per l identificazione. La crescita in coltura è rapida e si verifica in genere in 24 ore a temperature di 2537 C. La coltura da un sito sterile conferma la diagnosi di mucormicosi e permette la precisa identificazione di genere e di specie. Non sono disponibili test antigenici specifici per la rilevazione delle infezioni causate dai miceti responsabili di mucormicosi. L 13 βdglucano, un componente della parete fungina di molti miceti (e quindi considerato un antigene panfungino) è assente in Mucorales. L antigene galattomannano può essere occasionalmente positivo
37 in corso di mucormicosi ma un risultato negativo (su siero e BAL) in un paziente a rischio e con un quadro compatibile di infezione fungina invasiva incrementa la verosimiglianza di mucormicosi invasiva. Per quanto riguarda la diagnosi radiologica alcune modificazioni sembrano essere osservate più frequentemente nei pazienti affetti da mucormicosi rispetto ad altre infezioni da funghi filamentosi. Il segno dell alone ( halo sign ) e quello della semiluna ( air crescent sign ) sono generalmente considerati come indicativi di infezione fungina a carico delle basse vie respiratorie. Il cosiddetto segno dell alone inverso (cioè un area di opacità a vetro smerigliato circondata da un anello di consolidamento) sembra essere più tipica della mucormicosi rispetto all aspergillosi invasiva. In uno studio non controllato su 189 pazienti il segno dell alone inverso era presente nel 19% dei casi di mucormicosi, in meno dell 1% di aspergillosi invasiva e in nessun paziente con fusariosi. Terapia Di tutti i farmaci antifungini disponibili amfotericina B mostra la migliore attività in vitro nei confronti della maggior parte delle specie responsabili di mucormicosi. Alcune specie però, ad esempio Cunninghamella e Rhizopus, presentano valori di MIC più elevati. Gli azoli con la sola eccezione di posaconazolo non sono attivi nei confronti degli zigomiceti. Posaconazolo è stato utilizzato come terapia di salvataggio della zigomicosi in due studi di 91 e 24 pazienti con percentuali di successo riportate rispettivamente del 60 % e 79 %. Le echinocandine risultano almeno in vitro inattive nei confronti degli zigomiceti. Amfotericina B deossicolato è stata considerata per molti anni il trattamento di scelta della mucormicosi con dosaggi raccomandati compresi tra 1 e 1,5 mg/kg/die; diversi studi recenti supportano l impiego di amfotericina B liposomiale come trattamento di prima scelta della mucormicosii. Una revisione di 120 pazienti ematologici ha mostrato tassi di sopravvivenza del 67 % nei pazienti trattati con amfotericina B liposomiale rispetto al 39 % dei trattati con amfotericina B deossicolato (p=0.02). In un altro studio retrospettivo italiano su 59 pazienti ematologici con zigomicosi certa o probabile le percentuali di risposta erano del 58 % nei trattati con amfotericina B liposomiale contro il 23 % nei trattati con amfotericina B deossicolato. Benchè la dose e la durata della terapia con amfotericina B liposomiale non sia stata stabilita con certezza si tende ad impiegarla a dosaggi più elevati (5 10 mg/kg/die) di quelli usualmente utilizzati. Le più recenti linee guida sia dell ESCMID sia dell ECIL concordano nel considerare amfotericina B liposomiale (a dosi uguali o superiori a 5 mg/kg/die) la terapia di prima scelta per il trattamento della mucormicosi (Skiada et al. Haematologica 2013; Cornely et al. Clin Microbiol Infect 2014). L amfotericina B in complessi lipidici (5 mg/kg/die) può rappresentare una alternativa se è stata esclusa una localizzazione cerebrale. Nei pazienti con localizzazione al sistema nervoso centrale viene raccomandato l impiego di una dose maggiore (10 mg/kg/die) di amfotericina B liposomiale per un periodo iniziale di almeno 28 giorni.
38 La terapia medica deve essere associata a debridement chirurgico del tessuto necrotico da parte di un chirurgo esperto nel trattamento di questa patologia. Uno studio retrospettivo relativo a 30 pazienti combinato con l analisi della letteratura relativa a 225 pazienti affetti da mucormicosi ha mostrato che il debridement chirurgico polmonare riduceva la mortalità da 62% a 11%. Due recenti revisioni della letteratura (Roden et al. Clin Infect Dis 2005; Zaoutis et al. Pediatr Infect Dis J 2007) hanno documentato migliori tassi di sopravvivenza con un approccio combinato di terapia chirurgica e medica. Per i pazienti refrattari o intolleranti alla terapia con gli antifungini di prima scelta il posaconazolo è considerato il farmaco di scelta per la terapia di salvataggio (200 mg quattro volte al giorno o 400 mg due volte al giorno). Una volta stabilizzata la malattia (almeno 3 settimane di terapia parenterale con LAMB) può essere impiegato posaconazolo per os 200 mg quattro volte al giorno come terapia di mantenimento. Per migliorare l assorbimento e quindi le concentrazioni plasmatiche di posaconazolo è importante dare alcune indicazioni ai pazienti: assunzione con un pasto a elevato contenuto lipidico; con bevande acide; sospendere terapie che riducono l acidità gastrica (soprattutto gli inibitori di pompa protonica). E inoltre necessario monitorare le concentrazioni plasmatiche di posaconazolo dopo 7 giorni di terapia per assicurarsi che i livelli del farmaco siano almeno > 1µg/mL ( ma idealmente > 2 µg/ml poiché la MIC 90 per Mucorales è > 1 µg/ml). In figura 5 sono riportate le opzioni raccomandate per il trattamento della mucormicosi
39 Mucormicosi invasiva Debridement chirurgico Normale funzione renale Funzione renale alterata Amfotericina B liposomiale 510 mg/kg/die ev o Amfotericina B complessi lipidici 5 mg/kg/die ev Posaconazolo 200 mg x 4/die Quadro refrattario /intolleranza o Malattia stabile/migliorata Figura 5 Algoritmo diagnosticoterapeutico per la mucormicosi
40 Istoplasmosi L istoplasmosi è una infezione causata da miceti dimorfi: Histoplasma capsulatum var. capsulatum (endemico negli Stati Uniti, America centromeridionale, Africa e Asia) e da H.capsulatum var. duboisii (endemico esclusivamente in Africa dove coesiste con l altra varietà). La distribuzione geografica di questi miceti è influenzata dalle caratteristiche del suolo, dall umidità e dal clima; le deiezioni di uccelli e di pipistrelli favoriscono la crescita del microrganismo nel terreno aumentandone la sporulazione. Nel nostro Paese sono segnalati casi autoctoni in persone che vivono nella pianura padana e riattivazioni in pazienti immunocompromessi (soprattutto HIVsieropositivi) che hanno vissuto o soggiornato in aree endemiche (Antinori et al. Medicine 2006; Antinori Am J Trop Med Hyg 2014). Nel soggetto immunocompetente l istoplasmosi può essere osservata come patologia polmonare in genere autolimitante soprattutto in viaggiatori con fattori di rischio specifici (speleologi). Diagnosi La diagnosi richiede la dimostrazione del micete in coltura (emocoltura, liquorcoltura, urinocoltura) o su materiale bioptico (cute, midollo osseo, altri campioni). Negli Stati Uniti è disponibile un saggio per la rilevazione dell antigene di istoplasma su sangue e urina. Terapia In tabella 18 sono riportate le indicazioni alla terapia antifungina per l istoplasmosi secondo quanto riportato nelle linee guida statunitensi. Tabella 18 Indicazioni alla terapia antifungina in corso di istoplasmosi Indicazioni certe, efficacia certa o probabile Infezione polmonare acuta diffusa con sintomi da moderatamente gravi a gravi Infezione polmonare cronica cavitaria Infezione disseminata progressiva Infezione del sistema nervoso centrale Indicazioni incerte, efficacia non nota Infezione polmonare acuta focale (asintomatica o con sintomi lievi che persistono > 1 mese) Linfoadenite mediastinica Granuloma mediastinico Sindromi infiammatorie trattate con steroidi Non raccomandata, efficacia incerta o inefficacia Fibrosi mediastinica Noduli polmonari Broncolitiasi Sindrome oculare presunta
41 I farmaci antifungini che mostrano attività nell istoplasmosi sono l amfotericina B deossicolato, amfotericina B liposomiale, amfotericina B in complessi lipidici e itraconazolo; non vi sono evidenze relative all impiego delle echinocandine. In tabella 19 sono riassunte le indicazioni con i farmaci e i dosaggi indicati per l istoplasmosi nelle linee guida dell IDSA (le uniche disponibili per questa infezione micotica). Tabella 19 Terapia dell istoplasmosi secondo le indicazioni delle linee guida statunitensi Manifestazione clinica Trattamento Livello di evidenza/forza della raccomandazione Istoplasmosi acuta polmonare moderatamente grave o grave AIII Lieve o moderata Amfotericina B liposomiale (35 mg/kg/die) o amfotericina B deossicolato (0,71 mg/kg/die) ev per 12 settimane poi itraconazolo 200 mg per os ogni 12 ore Sintomi < 4 settimane= nessuna Sintomi > 4 settimane= itraconazolo 200 mg x2 per os per 612 settimane Istoplasmosi cronica cavitaria Itraconazolo 200 mg x2 per os per 12 mesi Pericardite Itraconazolo 200 mg per os 12 volte al giorno per 612 settimane se viene impiegato anche prednisone Istoplasmosi progressiva disseminata (PDH) Amfotericina B liposomiale (3 mg/kg/die) ev per 2 settimane poi itraconazolo 200 mg ogni 12 ore per os per 12 mesi Istoplasmosi del SNC Amfotericina B liposomiale (5 mg/kg/die) ev per 46 settimane poi itraconazolo 200 mg x 23 volte die per os per almeno 12 mesi Fonte: Wheat JL et al. Clin Infect Dis 2007;45:80725 AIII BIII AII BIII AI BIII Terapia antifungina empirica e terapia preemptive Nella pratica clinica quotidiana l impiego di terapia antifungina su base empirica o preemptive supera di gran lunga quella utilizzata per il trattamento di infezioni certe (Valerio et al. J Antimicrob Chemother 2014). I motivi sono diversi ma in larga misura dettati dalle ben note difficoltà diagnostiche associate alle infezioni fungine pur se temperate negli ultimi anni da alcune innovazioni (biomarcatori fungini; TC a strato sottile; PCR) ; dalla gravità delle infezioni stesse caratterizzate da elevata letalità soprattutto nei pazienti immunocompromessi; dalla dimostrazione (nella candidemia) che l inizio tardivo della terapia si associa ad un incremento significativo della letalità (Morelle t al. Antimicrob Agents Chemother 2005) ; dagli studi, effettuati negli anni 80 nei pazienti neutropenici
42 febbrili non responsivi alla terapia antibiotica a largo spettro (Pizzo et al. Am J Med 1982; EORTC, Am J Med 1989)) che ha reso questa pratica lo standard of care. Nella nostra pratica si ravvisano due tipologie di scenari clinici per i quali appare appropriato prendere in considerazione una terapia antifungina empirica/preemptive: il paziente ricoverato in terapia intensiva (con quadro di sepsi/shock settico e BPCO in terapia steroidea cronica, addensamenti polmonari e insufficienza respiratoria) e il paziente neutropenico febbrile (ematologico). I due approcci (terapia empirica e terapia preemptive) vengono oggi indicati anche come feverdriven (quello empirico) e diagnosticdriven (quello preemptive). Paziente in rianimazione (ICUUTI). Il primo problema da considerare è quello relativo alla candidemia (per i dettagli si rimanda al capitolo relativo presente in questo documento). La terapia empirica deve essere guidata da una attenta valutazione clinica del paziente in quanto i fattori di rischio associati a candidemia ricorrono quasi sempre e quasi tutti nel paziente con febbre/sepsi ricoverato in ICU. L opzione della preemptive therapy è vincolata all impiego di biomarcatori (1,3βdglucano) non disponibili (né presso la nostra UO di Microbiologia né in altri laboratori esterni) oppure utilizzando i punteggi derivanti dagli score proposti (Candida score, indice di colonizzazione, regole predittive di OstroskyZeichner) che mostrano un elevato potere predittivo negativo ma un basso potere predittivo positivo. A scopo esemplificativo si riporta in tabella 20 le performance ottenute comparativamente nello studio di Posteraro e collaboratori che hanno valutato 1,3βdglucano, Candida score e indice di colonizzazione nella diagnosi di candidemia nel paziente in ICU. Tabella 20 Performance di 1,3βdglucano (BG), Candida score (CS) e indice di colonizzazione per la diagnosi di candidosi invasiva in 95 pazienti Sensibilità (%) 95%CI Specificità (%)95%CI PPV (%)95%CI NPV (%)95%CI BG con cutoff di 80 mg/ml 92.9 ( ) 93.7 ( ) 98.7 ( ) 98.7 ( ) CS ( ) 88.6 ( ) 57.1 ( ) 97.2 ( ) Indice di colonizzazione ( ) 69.6 ( ) 27.3 ( ) 91.7 ( ) Fonte : Posteraro et al. Critical Care 2011; 15:R249 I fattori che spingono verso una terapia empirica o preemptive nel paziente con sepsi/shock settico in ICU sono legati alla dimostrazione che l inizio dopo 12,24 o 48 ore dall esecuzione di idonee emocolture (poi risultate positive per Candida spp.) si associa ad un incremento significativo della letalità nei pazienti con candidemia (Morell et al. Antimicrob Agents Chemother 2005; Clin Infect Dis 2006). Nell allegato D è riportato un algoritmo per la terapia empirica proposto da Eggiman e collaboratori che valuta i diversi score proposti e a cui si può fare riferimento
43 nella decisione clinica. In questo caso la scelta dell antimicotico dovrà ricadere sempre sull impiego di una echinocandina o di amfotericina B liposomiale. Sempre nel pazienti in ICU un problema emergente segnalato dalla letteratura internazionale è quello dell aspergillosi invasiva polmonare (AIP) e dell interpretazione di Aspergillus spp. isolato dalle secrezioni respiratorie al di fuori dei gruppi a rischio tradizionali. I dati epidemiologici riportano un incidenza di AIP in ICU variabile da 0.3 a 6.9% (Koulenti et al. Curr Opin Infect Dis 2014). Uno studio retrospettivo statunitense condotto su un database (4 anni) ha identificato 412 casi di AI in ICU su oltre 6424 casi di AI (prevalenza 6.4%) con una prevalenza in ICU pari a % (su 2,470,118 pazienti) (Baddley et al. BMC Infect Dis 2013). I pazienti avevano un età media di 63.9 anni presentavano insufficienza respiratoria acuta nel 76% dei casi, erano in terapia steroidea nel 77% dei casi e avevano insufficienza renale nel 41% dei casi. Secondo questo studio l AI in ICU si associa a elevata letalità e a un incremento dei costi ospedalieri con un 3.5% di incremento e 1.3 giorni di maggior permanenza in ospedale per ogni giorno di ritardo nell inizio di terapia antifungina (Baddley et al. BMC Infect Dis 2013). I pazienti con BPCO in terapia steroidea e lesioni polmonari rappresentano la categoria a maggior rischio di AI in ICU ma la diagnosi è oltremodo difficile. L identificazione di Aspergillus spp. in campioni respiratori si associa a una vera infezione nel 72% dei pazienti neutropenici, nel 55% dei trapiantati di organo solido e nel 22% dei pazienti con BPCO (Guinea et al. Clin Microbiol Infect 2010). In ogni caso l isolamento di Aspergillus spp. da campioni respiratori in pazienti ospedalizzati in ICU costituisce un marcatore prognostico sfavorevole indipendentemente dal fatto che si tratti di colonizzazione o infezione (Khasawneh et al. J Crit Care 2006).Per quanto concerne le diverse specie uno studio ha indicato come l isolamento di A.terreus sia associato più frequentemente a una vera infezione rispetto alle altre specie (Caston et al. Chest 2007). In assenza di criteri certi (escluse le biopsie o l isolamento da siti sterili) nel paziente in ICU sono stati proposti alcuni criteri diversi da quelli dell EORTC (che funzionano meno bene o poco rispetto al paziente ematologico ) sono stati proposti e successivamente validati in uno studio prospettico dei criteri per la diagnosi putativa di aspergillosi polmonare invasiva nei pazienti in ICU (Vandewoude et al. Crit Care 2006; Blot et al. Am J Respir Crit Care Med 2012) che vengono riportati nell allegato E. Possono essere impiegati come ausilio per la decisione clinica nei pazienti con isolamento di Aspergillus spp. da campioni provenienti dalle vie respiratorie. Il problema di questo algoritmo (che è l unico validato in uno studio clinico) è relativo al fatto che richiede come prerequisito l isolamento di Aspergillus ed è noto che la patologia può essere osservata anche in pazienti senza isolamento del fungo dalle vie respiratorie. In questo caso le opzioni terapeutiche sono rappresentate da voriconazolo e amfotericina B
44 liposomiale : La scelta di una molecola rispetto all altra (tenendo presente che voriconazolo è considerato prima scelta) dipenderà da eventuali farmaci concomitanti che siano metabolizzati da CYP3A4 o 2C9 o che possano prolungare l intervallo QT (in questo caso si privilegerà LAMB), dalla presenza di insufficienza epatica grave (Child C sempre LAMB) o di insufficienza renale grave (privilegiare voriconazolo), Paziente neutropenico. Anche in questa condizione l approccio può essere quello di terapia empirica (fever driven) o preemptive (diagnostic driven). Nel primo caso la decisione di intraprendere la terapia empirica è basata sulla mancata risposta a idonea terapia antibiotica a 96 ore in paziente febbrile (> 38 C) e con neutropenia grave (< 500/µL). Nel secondo caso la scelta è dettata dalla positività di un biomarcatore (GM) o dalla TC torace (o da entrambi). L impiego in questo setting di 1,3Bdglucano e di PCR (reazione polimerasica a catena) per Aspergillus spp. rimangono controversi. I farmaci impiegabili sono amfoerticina B (oggi pressoché esclusivamente la formulazione liposomiale) e caspofungina. Entrambi sono registrati con questa indicazione. La scelta deve tenere tuttavia conto di numerose variabili, soprattutto il fatto che tra i due farmaci amfotericina B è l antimicotico dotato dello spettro di attività più allargato (attivo pressoché contro tutti i miceti escluso Aspergillus terreus e Candida lusitaniae). Una recentissima revisione Cochrane che ha preso in esame 32 studi clinici (per un totale di 4287 pazienti) ha mostrato che la profilassi o la terapia empirica con amfotericina B è in grado di ridurre in maniera significativa la mortalità complessiva (RR 0.69, IC 95 % ) (Gotzche et al. Cochrane 2014); inoltre, l incidenza di infezioni fungine si riduceva significativamente con la somministrazione di amfotericina B (RR0.41, IC ), fluconazolo (RR 0.39, IC 95% ) e itraconazolo (RR 0.53, IC 95% ). da ultimo amfotericina B e fluconazolo riducevano la mortalità ascrivibile a infezioni fungine (RR 0.45, IC 95% per amfotericina B; RR 0.42, IC 95% per fluconazolo). Un altra revisione Cochrane altrettanto recente che ha confrontato amfotericina B e voriconazolo ha mostrato come amfotericina B liposomiale sia significativamente più efficace di voriconazolo nella terapia empirica delle infezioni fungine nel paziente neutropenico e sia quindi da preferire (Jorgensen KJ et al. Cochrane 2014).
45 Monitoraggio terapeutico dei farmaci antifungini (Therapeutic drug monitoring) L importanza e la necessità di effettuare il monitoraggio delle concentrazioni terapeutiche (di seguito TDM) di alcuni farmaci antifungini è riconosciuta in maniera crescente tanto che diverse Società scientifiche hanno prodotto documenti in tal senso (Hamada et al. J Infect Chemother 2013; Ashbee et al. JAC 2014; CendejasBueno et al. 2014). Benché sia tuttora dibattuto il fatto di considerare la TDM come un indagine routinaria (come avviene ad esempio per alcuni farmaci antibatterici) il suo impiego, soprattutto nel caso dei triazoli attivi nei confronti delle muffe (itraconazolo, voriconazolo, posaconazolo), è generalmente indicato. Allo stato attuale non vi sono invece indicazioni al suo impiego per i polieni (amfotericina B deossicolato, amfotericina B liposomiale e amfotericina B in complessi lipidici) e per le echinocandine (micafungina, anidulafungina, caspofungina). Il voriconazolo presenta negli adulti una farmacocinetica nonlineare (secondo MichaelisMertens) che appare correlata a meccanismi saturabili di eliminazione. E generalmente considerato un farmaco con un elevata biodisponibilità dopo somministrazione orale sia negli adulti sia nei bambini (8086%) anche se dati più recenti sembrano indicare talora valori inferiori al 60% (Pascual et al. Clin Infect Dis 2012). Il voriconazolo viene metabolizzato attraverso meccanismi ossidativi che coinvolgono il citocromo P450 (soprattutto gli isoenzimi CYP3A4, CYP2C19 e CYP2C9). Il CYP2C19 si associa a numerosi polimorfismi clinicamente rilevanti che sono stati correlati a differenze anche notevoli della clearance del farmaco. I fattori a supporto dell impiego della TDM in maniera routinaria nella terapia con voriconazolo derivano soprattutto dalla dimostrazione, sia in condizioni sperimentali sia in studi clinici, della relazione concentrazioneefficacia e concentrazionetossicità. Inoltre, la variabilità farmacocinetica di voriconazolo è notevole, estesamente documentata e come conseguenza di ciò è stato determinato che una piccola quota di pazienti che ricevono la dose indicata presenta un esposizione al farmaco associata con un elevata probabilità di successo e una bassa probabilità di tossicità. In uno studio prospettico controllato e randomizzato è stato dimostrato un outcome migliore nei pazienti che ricevevano voriconazolo adeguato alle concentrazioni rispetto a quelli che ricevevano la dose fissa del farmaco (Park et al. Clin Infect Dis 2012). E indicato mantenere una through concentration tra 1.0 e 5.5 mg/l. Secondo quanto riportato nelle linee guida britanniche la concentrazione per minimizzare la tossicità di voriconazolo (fotopsia, incremento dei valori degli enzimi epatici, neurotossicità) dovrebbe essere < 46 mg/l (Ashbee et al. JAC 2014). Nel caso in cui la MIC (ottenuta con il metodo CLSI) del microrganismo responsabile sia nota il rapporto (through concentration:mic target) deve essere compresa tra 25. Poiché le concentrazioni di voriconazolo si modificano
46 più rapidamente rispetto a itraconazolo e posaconazolo viene considerato ragionevole effettuare la prima determinazione entro 25 giorni. La medesima strategia va messa in atto qualora si modifichi il dosaggio del farmaco e quando si effettui uno switch dalla somministrazione parenterale a quella orale. Per quanto riguarda itraconazolo, farmaco oggi impiegato meno frequentemente del passato per la terapia e profilassi delle IFI, si ritiene necessario eseguire la TDM nella maggior parte dei pazienti ; il farmaco ha una farmacocinetica non lineare e lo steady state viene raggiunto non prima di 2 settimane. Viene consigliato di effettuare un primo prelievo dopo 1 settimana e monitorare quindi i valori a intervalli regolari. Misurando le concentrazioni con HPLC/spettrofotometria di massa è necessario mantenere concentrazioni di 0.51 mg/l. Anche per posaconazolo, in considerazione della notevole variabilità farmacocinetica dimostrata nella pratica clinica e dell evidenza frequente di concentrazioni sub ottimali impiegando le dosi raccomandate, è consigliabile eseguire la TDM. Secondo la BSMM nel caso di impiego per profilassi viene considerata ragionevole una concentrazione target di 0.7 mg/l anche se le evidenze a supporto di questo valore sono relativamente deboli. Per quanto riguarda la terapia di infezioni fungine certe la minima concentrazione target è di 1 mg/l. La prima determinazione va effettuata dopo almeno 1 settimana di impiego del farmaco (quando si raggiunge lo steady state); nel caso in cui si modifichi la terapia sono necessari altri 7 giorni prima che il nuovo steady state sia raggiunto. Per le echinocandine non vi sono indicazioni all impiego della TDM. Al di fuori degli azoli l unico altro farmaco per cui sarebbe indicato l utilizzo della TDM è la flucitosina, che fa parte della terapia iniziale di combinazione della meningite criptococcica. La dose standard di flucitosina è pari a mg/kg/die suddivisa in 34 somministrazioni giornaliere. E richiesta una riduzione della dose giornaliera in presenza di insufficienza renale (clearance creatinina 2650 ml/min, 75 mg/kg/die; clearance creatinina 1325 ml/min, 37 mg/kg/die; clearance creatinina < 13 ml/min, non somministrare). Il rischio di mielotossicità da flucitosina è notevole quando la concentrazione di picco è > 100 mg/l; pertanto la concentrazione di picco (misurata 2 ore dopo una dose orale) dovrebbe rimanere nell intervallo compreso fra mg/l. Poiché la flucitosina ha una breve emivita la sua prima determinazione dovrebbe avvenire entro 72 ore dall inizio della terapia e successivamente dovrebbe essere effettuata regolarmente (ogni modifica della funzionalità renale influisce sulle concentrazioni). In tabella 21 sono riassunte schematicamente le indicazioni, i livelli target e le strategie da adottare per gli aggiustamenti della dose. Infine si ricorda che presso la nostra AO è possibile effettuare la TDM di voriconazolo e posaconazolo contattando il Dr Dario Cattaneo dell UO Farmacologica clinica (vedi allegato B).
47 Tabella 21 Sintesi delle differenti raccomandazioni per l impiego della TDM nella terapia/profilassi antifungina Indicazione alla TDM Tempo di esecuzione (dopo la prima dose) Concentrazioni terapeutiche Fluconazolo Itraconazolo Voriconazolo Posaconazolo Flucitosina Insufficienza renale; pediatria Pazienti immunocmpromessi che ricevono il farmaco per la profilassi; pazienti che ricevono il farmaco per la terpia di IFI o aspergillosi broncopolmonare allergica Verifica raggiungimento target terapeutico; modifiche della dose o switch a terapia orale; malassorbimento; tossicità epatica, neurologica, oculare; interazioni farmacologiche Verifica raggiungimento target terapeutico; malassorbimento; interazioni farmacologiche 45 giorni 15 giorni 57 giorni 57 giorni 3 giorni AUC/ MIC> 25 Profilassi: Cmin> 0,5 mg/l (o µg/ml) Terapia: Cmin> 12 mg/l (o µg/ml) Cmin: 14 mg/l (o µg/ ml) Soglia di tossicità Cmin > 46 mg/l (o Strategie per aggiustamento dose nei pazienti con concentrazioni inferiori al target desiderato Incrementare dose giornaliera (da 200 mg x2/die a 300 mg x2/die) Somministrae sospensione orale anziché le capsule Se si impiega la sospensione orale verificare l assunzione a stomaco vuoto Se si impiegano le capsule non utilizzare antagonisti H2 o inibitori di pompa µg/ml) Incrementare la dose ev del 50% finoa un massimo di 6 mg/kg x 2/die (adulti); incrementare la dose orale da 200 mg x2/die a 300 mgx27die Verifica raggiungimento target terapeutico, mielotossicità; insufficienza renale Profilassi : Cmin > 0.5 Cmin mg/l mg/l (o µg/ml) Terapia: mg/l (o µg/ml) Cmax > 100 mg/l Incrementare la dose da 600 mg/die a 800 mg/die; somministrae la dose totale ogni 6 ore; somministrae a stomaco pieno; somministrae con un pasto ad alto contenuto grasso; sospendere farmaci che sopprimono l acidità gastrica; sospendere farmaci che interferiscono Suscettibilità agli antifungini di Candida spp e Aspergillus spp. Incrementare la dose del 50% Due organizzazioni hanno sviluppato metodi di riferimento per saggiare gli isolati fungini e hanno stabilito i relativi breakpoints per l interpretazione della suscettibilità agli antifungini: l EUCAST (European Committee on Antimicrobial Susceptibility testing) e l AFST (Antifungal Susceptibility Testing Subcommiteees) del CLSI (Clinical Laboratory Standards Institute). Inizialmente le 2 organizzazioni hanno prodotto valori di breakpoints differenti :in genere più bassi per EUCAST rispetto a CLSI. Più recentemente i breakpoints del CLSI sono stati rivisti e in larga misura armonizzati con quelli di EUCAST. Le principali differenze sono le seguenti: EUCAST in considerazione della notevole variabilità dei valori di MIC osservati nel tempo e tra i diversi laboratori per caspofungina nei confronti di Candida spp., non ritiene fornire a questo riguardo valori di breakpoints, suggerisce nel frattempo di impiegare anidulafungina come marcatore di suscettibilità a caspofungina (EspinellIngroff et al. Antimicrob Agents Chemother 2013). Uno studio pubblicato nel 2014 condotto su circa 4300 ceppi di Candida spp. ha confermato che anidulafungina costituisce un accurato marcatore surrogato in grado di predire suscettibilità o resistenza di Candida spp. a caspofungina (Pfaller et al. J Clin Microbiol 2014). I breakpoints indicati da EUCAST per anidulafungina e micafungina sono di alcune diluizioni più bassi per Candida spp. rispetto a quelli generati da CLSI (come conseguenza metodologica poiché i metodi impiegati da EUCAST danno valori di MIC più bassi) (Arendrup et al.
48 Drug Resist Updat 2013; Pfaller et al. Drug Resist Updat 2011). Per EUCAST sia C. parapsilosis sia C. guilliermondi non sono mai considerate specie totalmente suscettibili alle echinocandine ma con suscettibilità intermedia. In tabella 22 sono riportati i valori di breakpoints per Candida spp. secondo EUCAST e CLSI. Tabella 22 Valori comparativi dei breakpoints per le principali specie di Candida secondo i riferimenti EUCAST e CLSI Specie Anidulafungina Caspofungina Micafungina Fluconazolo Voriconazolo Posaconazolo Candida EUCAST: NS albicans EUCAST : S 0.03 CLSI: S 0.25 CLSI:S 0.25;R>0.5 EUCAST : S CLSI: S 0.25;R>0.5 EUCAST : S 2;R>4 CLSI: S 2;R>4 EUCAST : S 0.12 CLSI: S 0.12;R>0.5 EUCAST :S 0.06 CLSI: NS C. glabrata EUCAST: S 0.06 CLSI. S 0.12 EUCAST: NS CLSI. S 0.12; R>0.25 EUCAST: S 0.03 CLSI. S 0.06;R>0.125 EUCAST: S 0.002;R>32 CLSI. S 0.002;R>32 EUCAST: EI CLSI: EUCAST: EI CLSI: NS C. krusei EUCAST: S 0.06 CLSI: S 0.25;R>0.5 EUCAST: NS CLSI: S 0.25;R>0.5 EUCAST: EI CLSI: S 0.25;R>0.5 EUCAST: EI CLSI:S 0.5;R>1 EUCAST: EI CLSI: NS C. papapsilosis EUCAST : S 0.002;R>4 CLSI:S 2;R>4 EUCAST: NS CLSI:S 2;R>4 EUCAST : S 0.002;R>2 CLSI:S 2;R>4 EUCAST : S 2;R>4 CLSI:S 2;R>4 EUCAST : S 0.12 CLSI:S 0.12;R>0.5 EUCAST : S 0.06 CLSI: NS C.tropicalis EUCAST : S 0.06; CLSI: S 0.25;R>0.5 EUCAST: NS CLSI: S 0.25;R>0.5 EUCAST: EI CLSI: S 0.25;R>0.5 EUCAST : S 2;R>4 CLSI:S 2;R>4 EUCAST : S 0.12 CLSI:S 0.12;R>0.5 EUCAST : S 0.06 CLSI: NS C. guilliermondii EUCAST: EI CLSI: S 2;R>4 EUCAST: EI CLSI: S 2;R>4 EUCAST: EI CLSI: S 2;R>4 EUCAST: EI CLSI: NS EUCAST: EI CLSI: NS EUCAST: EI CLSI: NS NS= non stabilito; EI= evidenze insufficienti EUCAST, European Committee on Antimicrobial suceptibility Testing; CLSI, Clinical and Laboratory Standards Institute Per quanto riguarda le muffe e in particolare Aspergillus spp., la situazione relativa ai saggi di suscettibilità e alla disponibilità di breakpoints appare più complessa. Il CLSI ha sviluppato al riguardo un metodo di microdiluizione in brodo che costituisce il riferimento per la valutazione della suscettibilità delle muffe (CLSI M38A2 document). Il CLSI non ha prodotto breakpoints clinici ma i cosiddetti epidemiologic cutoff values (ECVs) che pur non essendo predittivi dell outcome clinico possono aiutare ad evidenziare la presenza di resistenza agli azoli dovute a mutazioni a carico di cyp51a, un meccanismo di resistenza dimostrato per alcune specie di Aspergillus. Al contrario EUCAST basandosi sulle distribuzioni dei valori di MIC, parametri di PK/PD, dati ottenuti su modelli animali e sull esperienza clinica ha indicato dei breakpoints per Aspergillus fumigatus nei confronti di itraconazolo, voriconazolo e posaconazolo. In tabella 23 sono sinteticamente riportati i breakpoints agli antifungini (AMFB e triazoli) proposti nei confronti di Aspergillus spp da parte dell EUCAST e gli ECVs proposti da parte del CLSI.
49 Tabella 23 Breakpoints nei confronti di Aspergillus spp. proposti da EUCAST e ECVs proposti da CLSI Antifungino Aspergillus flavus A.fumigatus A.nidulans A.niger A.terreus EUCAST MIC breakpoints (mg/l) S R> S R> S R> S R> S R> Amfotericina B EI EI 1 2 NS NS 1 2 Itraconazolo EI EI 1 2 Voriconazolo EI EI 1 2 EI EI EI EI EI EI Posaconazolo EI EI EI EI EI EI CLSI ECV (µg/ml) Itraconazolo Voriconazolo Posaconazolo Fonte dei dati : EspinelIngroff et al. J Clin Microbiol 2010; Arendrup et al. Drug Resist Updat EI= evidenze insufficienti ALTRE INFEZIONI FUNGINE Non vengono date indicazioni specifiche in questo documento riguardo alla terapia di infezioni fungine presenti esclusivamente in alcune aree endemiche (blastomicosi, coccidioidomicosi, paracoccidioidomicosi e penicilliosi marneffei) e di rarissimo riscontro in Italia. Per queste si rimanda, laddove esistano, alle linee guida (vedi allegato A) o alle indicazioni della letteratura. Lo stesso discorso vale per tutte quelle infezioni micotiche rare, per alcune delle quali l ESCMID ha recentemente pubblicato linee guida al riguardo. Si ricorda peraltro che tali linee guida per la assenza di studi clinici controllati sono basate per quanto riguarda le raccomandazioni terapeutiche quasi sempre sul parere degli esperti. PROFILASSI PRIMARIA ANTIFUNGINA L impiego della profilassi primaria antifungina trova indicazione pressoché esclusivamente nei pazienti con neoplasie ematologiche e/o sottoposti a trapianto allogenico di cellule staminali emopoietiche (di seguito Allo HSCT). In particolare sono considerati pazienti a rischio elevato di sviluppare infezioni fungine invasive i soggetti affetti da leucemia mieloide acuta durante la chemioterapia di induzione/reinduzione o con sindrome mieolodisplastica e i pazienti sottoposti ad AlloHSCT. Si tratta di tipologie di pazienti che usualmente non vengono ricoverati presso il nostro nosocomio e per tale motivo nelle precedenti linee guida questa problematica non era stata trattata. In considerazione del fatto che occasionalmente il Medico possa confrontarsi con pazienti
50 con tali problematiche anche presso le nostre divisioni si è deciso di introdurre una breve trattazione dell argomento basandosi sulle indicazioni tratte dalle più recenti linee guida e metaanalisi (Tacke et al. Ann Hematol 2014; Girmenia et al. Biol Blood Marrow Transplant 2014; Freifeld et al. Clin Infect Dis 2011; Slavin et al. Intern Med J 2008; Ziakas et al. Clin Ther 2014; Pagano et al. Clin Microbiol Infect 2014, Maertens et al. Bone Marrow Transplant 2011). I farmaci antifungini che presentano indicazione all utilizzo in profilassi primaria nel paziente ematologico sono i seguenti: fluconazolo, itraconazolo, voriconazolo, posaconazolo e micafungina. Il posaconazolo si è affermato come il farmaco di prima scelta in pressoché tutte le principali e più autorevoli linee guida per i pazienti con neutropenia grave indotta da chemioterapia e sottoposti ad AlloHSCT (tabella 24). Va tuttavia ricordato che il suo assorbimento erratico richiede l esecuzione della TDM per verificare la presenza di livelli terapeutici del farmaco. In uno studio retrospettivo condotto in Francia una breakthrough IFI venne identificata nel 3.2% dei pazienti sottoposti a profilassi primaria con posaconazolo e il singolo fattore di rischio significativamente associato allo sviluppo di IFI era la prima determinazione della concentrazione plasmatica inferiore a 0.3 mg/l (Lerolle et al. Clin Microbiol Infect 2014). Un altro aspetto importante che deve essere menzionato riguardo ai pazienti sottoposti a profilassi primaria con posazonazolo (o voriconazolo) è ridotta efficienza dell impiego dell antigene galattomannano come test di screening (Cornely Clin Infect Dis 2014; Duarte et al. Clin Infect Dis 2014). Tabella 24 Raccomandazioni all impiego di profilassi primaria antifungina nelle diverse linee guida in pazienti con leucemia mieloide acuta e sottoposti ad AlloHSCT Linea guida Posaconazolo Fluconazolo Itraconazolo Voriconazolo Micafungina Caspofungina LAMB AGIHO,2014 (AML/MDS) ALLOHSCT (preengrafment) (postengrafment) ECIL 34,2011 Leuk/induction AlloHSCT (neutropenia iniziale) AlloHSCT/GvHD ESCMID,2012 AntiCandida (AlloHSCTneutro) (AlloHSCT100 gg/no GvHD) (AlloHSCTGvHD) ESCMID,2014 AntiAspergillus AML/MDS AlloHSCTneutro AlloHSCTno neutronogvhd AlloHSCTGvHD e/o intensificazione AI BII AI (GvHD)/CI (no GvHD) AI No data AI AII CIII AI AI BII DIII AI CI BI CI (nogvhd)/di (GvHD) CI AI CI AI AI AI DIII CI CI CI CI BI BI BI BI CI DII DI DIII CII CII BI CI AI (prov) AI (prov) AI AI BI CI DIII CII BI CII CI Dati insufficienti AI CIII CII DIII CIII Dati insufficienti CII CII DIII BII* BI BII* Dati insufficienti BI CIII CII DIII
51 immunosoppressio ne LA con neutropenia prolungata e profonda GITMO,2014 AlloHSCTAlto rischio AlloHSCTrischio standard IDSA, 2011 AntiCandida LA (induzione) e AlloHSCT AntiAspergillus AML/MDS AII CIII CIII CIII CIII CIII CIII AI AI BI AI AI AI BI BI BI CIII BI CIII CIII* AI AI AI * Aerosol (12,5 mg 2 volte/settimana)+ fluconazolo: 50 mg a giorni alterni o 100 mg/settimana AGIHO= German Infectious Disease Working Party, ECIL=European Conference on Infections in Leukaemia, ESCMID=European Society of Clinical Microbiology and Infectious Diseases, GITMO= Gruppo Italiano Trapianto Midollo osseo AML= acute myeloid leukemia; MDS= myelodysplastic syndrome Appare degna di nota la segnalazione del documento relativo alla profilassi primaria elaborato dal GITMO (Gruppo Italiano Trapianto di Midollo Osseo) (Girmenia et al. Biol Blood Marrow Transplant 2014) come revisione delle precedenti raccomandazioni dello stesso gruppo (Girmenia et al. Clin Infect Dis 2009). In questo nuovo documento vengono individuati in maniera analitica i pazienti sottoposti a trapianto allogenico di cellule staminali emopoietiche ad alto rischio di sviluppare IFI e per i quali la profilassi con posaconazolo è fortemente raccomandata (tabella 25).
52 Tabella 25 Criteri per la definizione di alto rischio per la profilassi primaria in seguito ad AlloHSCT Fase precoce posttrapianto (giorno 040) Leucemia acuta attiva al momento del trapianto (AII) Trapianto da cordone ombelicale (AII) Graft versus host disease (GvHD) acuta di grado IIIIV dopo qualsiasi tipo di trapianto (AII) Trapianto da donatore mismatched (MMDR) o non correlato (UD) a 1 o più dei seguenti fattori di rischio aggiuntivi: GvHD acuta di grado II, dose di steroidi > 2 mg/kg/die per almeno 1 settimana, malattia da CMV, infezione ricorrente da CMV, neutropenia prolungata (neutrofili < 500/µL per più di 3 settimane), sovraccarico di ferro (BIII) Fase tardiva posttrapianto (giorno 41100) GvHD acuta di grado IIIIV dopo qualsiasi tipo di trapianto (AII) Trapianto da donatore mismatched (MMDR) o non correlato (UD) a 1 o più dei seguenti fattori di rischio aggiuntivi: GvHD acuta di grado II, dose di steroidi > 2 mg/kg/die per almeno 1 settimana, malattia da CMV,infezione ricorrente da CMV, neutropenia ricorrente (BIII) GvHD acuta steroide refrattaria/dipendente dopo qualsiasi tipo di trapianto (AIII) Fonte : Girmenia C et al. Biol Blood Marrow Transplant 2014 parzialmente modificata Fase molto tardiva posttrapianto (dopo > 100 giorni) GvHD acuta di grado IIIIV persistente o a esordio tardivo (AII) GvHD acuta steroide refrattaria/dipendente dopo qualsiasi tipo di trapianto (AII) GvHD acuta di grado II peristente o a esordio tardivo dopo MMRD o UD (BIII) GvHD cronica estesa quando preceduta da GvHD acuta (AII) In tabella 26 vengono infine riportati i dosaggi da impiegare per la profilassi primaria Tabella 26 Dosi raccomandate dei farmaci impiegabili per la profilassi primaria delle infezioni fungine invasive nei pazienti ematologici Farmaco Dose raccomandata Fluconazolo 400 mg/die per os Itraconazolo, sospensione orale 400 mg/die per os Micafungin, formulazione ev 50 mg/die ev Posaconazolo sospensione orale 200 mg ogni 8 ore per os Posaconazolo, compresse* 300 mg/die per os Voriconazolo, compresse 200 mg x 2/die per os * Non ancora disponibile in commercio
53 N.B. Indicazioni Terapeutiche e Dose dei Medicinali Nel presente documento sono riportate le indicazioni terapeutiche e le dosi raccomandate, che fanno riferimento a fonti bibliografiche accreditate. In alcuni casi è possibile che la dose raccomandata differisca da quanto autorizzato dalle Autorità Regolatorie e riportato nel Riassunto delle Caratteristiche del Prodotto e nel Foglietto Illustrativo. E quindi indispensabile che, qualora il medico prescrittore ritenga necessario il ricorso a dosaggi (come anche a indicazioni terapeutiche) non autorizzati, si attenga scrupolosamente alla procedura aziendale inerente la prescrizione di medicinali offlabel. A tal fine si riportano di seguito le INDICAZIONI TERAPEUTICHE REGISTRATE (ON LABEL) ANIDULAFUNGINA (Ecalta) Trattamento delle candidiasi invasive in pazienti adulti ECALTA non è stato studiato in pazienti con endocardite, osteomielite o meningite da Candida. L efficacia di ECALTA è stata valutata soltanto in un numero limitato di pazienti neutropenici AMFOTERICINA B LIPO (Ambisome) trattamento empirico di presunte infezioni fungine in pazienti con neutropenia febbrile. trattamento di severe micosi sistemiche e/o profonde, in pazienti che non hanno risposto o che hanno sviluppato nefrotossicità alla comune amfotericina, oppure in pazienti con controindicazioni renali. Le infezioni fungine trattate con successo con AmBisome comprendono: candidiasi disseminate, aspergillosi, mucormicosi, micetoma cronico e meningite criptococcica. AmBisome può anche essere efficace nelle seguenti infezioni fungine: blastomicosi del Nord America, coccidiomicosi, istoplasmosi, mucormicosi causata da specie dei generi Mucor, Rhizopus, Absidia, Eptomophtora e Basidiobolus e sporotricosi causata da Sporothrix schenckii. CASPOFUNGINA (Cancidas) Trattamento della candidiasi invasiva, in pazienti adulti o pediatrici. Trattamento della aspergillosi invasiva in pazienti adulti o pediatrici refrattari o intolleranti alla terapia con amfotericina B, formulazioni lipidiche di amfotericina B e/o itraconazolo. Vengono definiti refrattari alla terapia i pazienti con infezioni che progrediscono o non migliorano dopo un periodo minimo di 7 giorni di trattamento con dosi terapeutiche di terapia antifungina efficace. Terapia empirica di presunte infezioni fungine (come Candida o Aspergillus) in pazienti adulti o pediatrici neutropenici con febbre. MICAFUNGINA (Mycamine) Adulti, adolescenti 16 anni di età e anziani: Trattamento della candidosi invasiva. Trattamento della candidosi esofagea in pazienti per i quali sia appropriata una terapia endovenosa. Profilassi delle infezioni da Candida in pazienti sottoposti a trapianto allogenico di celule staminali ematopoietiche o in pazienti che si prevede possano manifestare neutropenia (conta assoluta dei neutrofili < 500 cellule/µl) per 10 o più giorni. Bambini (inclusi neonati) e adolescenti < 16 anni di età: Trattamento della candidosi invasiva. Profilassi dell infezione da Candida in pazienti sottoposti a trapianto allogenico di cellule staminali ematopoietiche o in pazienti che si prevede possano manifestare neutropenia (conta assoluta dei neutrofili < 500 cellule/µl) per 10 o più giorni. La decisione di utilizzare Mycamine deve tenere conto del rischio potenziale di sviluppare tumori epatici. Mycamine deve perciò essere usata solo se l utilizzo di altri antifungini non è appropriato.
54 POSACONAZOLO (Noxafil) Noxafil sospensione orale è indicato per l uso nel trattamento delle seguenti infezioni fungine negli adulti: Aspergillosi invasiva in pazienti con malattia refrattaria ad amfotericina B o ad itraconazolo o in pazienti intolleranti a questi medicinali; Fusariosi in pazienti con malattia refrattaria ad amfotericina B o in pazienti intolleranti ad amfotericina B; Cromoblastomicosi e micetoma in pazienti con malattia refrattaria a itraconazolo o in pazienti intolleranti ad itraconazolo; Coccidioidomicosi in pazienti con malattia refrattaria ad amfotericina B, itraconazolo o fluconazolo o in pazienti intolleranti a questi medicinali; Candidiasi orofaringea: come terapia di prima linea in pazienti con malattia grave o immunocompromessi, in cui ci si aspetta scarsa risposta ad una terapia topica. La refrattarietà è definita come progressione dell infezione o assenza di miglioramento dopo un trattamento minimo di 7 giorni con dosi terapeutiche di una terapia antifungina efficace. Noxafil sospensione orale è indicato anche nella profilassi di infezioni fungine invasive nei seguenti pazienti: Pazienti in chemioterapia per induzione della remissione di leucemia mieloblastica acuta (AML) o sindromi mielodisplastiche (MDS) per le quali si prevede una neutropenia prolungata e che sono ad alto rischio di sviluppare infezioni fungine invasive; Soggetti sottoposti a trapianto di cellule staminali emopoietiche (HSCT) in terapia immunosoppressiva ad alto dosaggio per malattia del trapianto contro l ospite e che sono ad alto rischio di sviluppare infezioni fungine invasive VORICONAZOLO (Vfend) Voriconazolo è un agente antimicotico triazolico ad ampio spettro ed è indicato negli adulti e nei bambini di età pari o superiore ai 2 anni, nei seguenti casi: Trattamento dell aspergillosi invasiva. Trattamento della candidemia in pazienti nonneutropenici. Trattamento di infezioni gravi e invasive da Candida resistenti al fluconazolo (inclusa la C. krusei). Trattamento di infezioni micotiche gravi causate da Scedosporium spp. e Fusarium spp. VFEND deve essere somministrato principalmente a pazienti con infezioni a carattere progressivo che possono mettere in pericolo la vita del paziente stesso. Profilassi di infezioni fungine invasive in pazienti ad alto rischio sottoposti a trapianto allogenico di cellule staminali ematopoietiche (HSCT, Hematopoietic Stem Cell Transplant). PROCEDURA OPERATIVA Presso l ospedale L. Sacco la prescrizione di farmaci antimicotici innovativi deve essere preceduta dalla verifica indicazione e compilazione della scheda di monitoraggio (allegata) da parte del medico specialista infettivologo. L'approvvigionamento non segue il flusso standard, tramite procedura informatica EncoGPI, ma avviene esclusivamente previa compilazione della scheda di monitoraggio. La scheda di monitoraggio, compilata dal medico specialista infettivologo, deve essere inviata all U.O. Farmacia via fax o via mail [email protected] Viene contestualmente istituito un tavolo tecnico tra Dipartimento di Malattie Infettive e Dipartimento Farmaceutico che si riunirà con cadenza periodica (semestrale) per analizzare le schede di monitoraggio elaborate ed aggiornare il presente documento.
55 Ospedale Luigi Sacco U.O. FARMACIA SCHEDA DI MONITORAGGIO FARMACI ANTIMICOTICI INNOVATIVI MFA.P72 Rev.1 del Pag. 1/1 L'approvvigionamento dei farmaci antimicotici innovativi non è effetuato tramite procedura informatica EncoGPI, ma avviene esclusivamente previa compilazione della presente scheda di monitoraggio: Inviare la presente scheda debitamente compilata all U.O. Farmacia (via fax o via [email protected].) Per la corretta compilazione, fare riferimento alla specifica Linea Guida Aziendale LFA.P26. In caso di compilazione incompleta, la richiesta non verrà evasa e sarà ritrasmessa all U.O. richiedente. La richiesta NON è cumulativa: deve essere compilata una richiesta per singolo paziente per una terapia di 57 giorni (quest ultima situazione nel caso in cui il 5 giorno cada di sabato o domenica). In caso di proseguimento di terapia, deve essere compilata un altra richiesta. Data U.O. PAZIENTE (NOME E COGNOME)../..../... DIAGNOSI (barrare la scelta e/o aggiungere informazioni) Aspergillosi invasiva Candidemia Certa C.albicans Probabile C.glabrata Possibile C.parapsilosis Polmonare C.tropicalis Cerebrale C.krusei Disseminata Altro:.. Altro Criptococcosi Meningite Malattia disseminata Localizzazione polmonare Altro Istoplasmosi Disseminata Polmonare diffusa Altro.... Numero Cartella Clinica/DH/Amb.. Esofagite da Candida resistenza clinica agli azoli resistenza in vitro agli azoli Mucormicosi Rinocerebrale Polmonare Cerebrale Disseminata FUO in paziente neutropenico Terapia empirica Motivazioni cliniche: Switch da precedente terapia con. Terapia preemptive FARMACO/I PRESCRITTO/I (selezionare) N.B. valutare in prima istanza le indicazioni terapeutiche on label ANIDULAFUNGINA (Ecalta) AMFOTERICINA B LIPO (Ambisome) CASPOFUNGINA (Cancidas) MICAFUNGINA (Mycamine) POSACONAZOLO (Noxafil) VORICONAZOLO (Vfend) POSOLOGIA /DIE... DURATA TERAPIA GIORNI. FIRMA /TIMBRO DEL MEDICO INFETTIVOLOGO FIRMA DEL FARMACISTA SPAZIO RISERVATO ALLA U.O. FARMACIA
56 Riferimenti bibliografici Agarwal R, Chakrabarti A, Shah A, et al. Allergic bronchopulmonary aspergillosis. Review of the literature and proposal of new diagnostic and classification criteria. Clin Exp Allergy 2013;43: Aitken SL, Beyda ND, Shah DN, et al. Clinical practice patterns in hospitalized patients at risk for invasive candidiasis:role of antifungal stewardship programs in an era of rapid diagnostics. Ann Pharmacother 2014;48: Alexander BD, Johnson MD, Pfeiffer CD, et al. Increasing echinocandin resistance in Candida glabrata:clinical failure correlates with presence of FKS mutations and elevated minimum inhibitory concentrations. Clin Infect Dis 2013;56: Alfandari S, Berthon C, Coiteux V. Antifungal stewardship: implementation in a French teaching hospital. Med Malad Infect 2014;44:1548. AnandaRajah MR, Slavin MA, Thursky KT. The case for antifungal stewardship. Curr Opin Infect Dis 2012;25: Andes DR, Safdar N, Baddley JW, et al. Impact of treatment strategy on outcome in patients with candidemia and other forms of invasive candidiasis: a patientlevel quantitative review of randomized trials. Clin Infect Dis 2012; 54: Antinori S. Molluscum or a mimic? Add Penicillium marneffei. Am J Med 2007;120:e1920. Antinori S. Histoplasma capsulatum: more widespread than previously thought. Am J Trop Med Hyg 2014;90:9823. Antinori S, Magni C, Nebuloni M, et al. Histoplasmosis among human immunodeficiency virusinfected people in Europe: report of 4 cases and review of the literature. Medicine 2006;85:2236. Arendrup M, CuencaEstrella M, Lass Florl C, Hope WW. Breakpoints for antifungal agents: an update from EUCAST focussing on echinocandins against Candida spp. and triazoles against Aspergillus spp. Drug Resist Updat 2013;16:8195 Ashbee HR, Barnes RA, Johnson EM, Richardson MD, Gorton R, Hope WW. Therapeutic drug monitoring (TDM) of antifungal agents:guidelines from the British Society for Medical Mycology. JAC 2014;69: Baddley JW, Forrest GN and the AST Infectious Diseases Community of Practice. Cryptococcosis in solid organ transplantation. Am J Transplant 2013; 13: Baddley JW, Stephens JM, Ji X, et al. Aspergillosis in intensive care unit (ICU) patients: epidemiology and economic aoutcomes. BMC Infect Dis 2013; 13:29 Bennett JE. Echinocandins for candidemia in adults without neutropenia. N Engl J Med 2006; 355: Blot SI, Taccone FS, van den Abeele AM, et al. A clinical algorithm to diagnose invasive pulmonary aspergillosis in critically ill patients. Am J Respir Crit Care Med 2012; 186:5664. Boulware DR, Meya DB, Muzoora C, et al. Timing of antiretroviral therapy after diagnosis of cryptococcal meningitis. N Engl J Med 2014;370: Caston JJ, Linares MJ, Gallego C, et al. Risk factors for pulmonary Aspergillus terreus infection in patients with positive culture for filamentous fungi. Chest 2007; 131:2306.
57 CendejasBueno E, CuencaEstrella M, GomezLopez A. Indicaciones clinicas de la monitorizacion de azoles de uso sistemico. Hacia la optimizacion del tratamiento de la infeccion fungica. Rev Esp Quimioter 2014;27:116. Cornerly OA, Bassetti M, Calandra T, et al. ESCMID guideline for the diagnosis and management of Candida disease in adult nonneutropenic patients. Clin Microbiol Infect 2012; 18(Suppl.7):1937. Cornerly OA, ArikanAkdagli S, Dannaoui E, et al. ESCMID and ECMM joint clinical guidelines for the diagnosis and management of mucormycosis Clin Microbiol Infect 2014; 20 (Suppl3):526. Cornerly OA. Galactomannan testing during moldactive prophylaxis. Clin Infect Dis 2014 (advance access august 27). Denning DW, Pleuvry A, Cole DC. Global burden of allergic bronchopulmonary aspergillosis with asthma and its complication chronic pulmonary aspergillosis in adults. Med Mycol 2013;51: De Pauw B, Walsh TJ, Donnelly P, et al. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of cancer/invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycoses study Group (EORTC/MSG) Consensus Group. Clin Infect Dis 2008; 46: Dimopoulos G, Antonopoulou A, Armaganidis A, Vincent JL. How to select an antifungal agent in critically ill patients. J Crit Care 2013; 28: Duarte RF, SanchezOrtega I, Cuesta I,et al. Serum galactomannanbased early detection of invasive aspergillosis in hematology patients receiving effective antimold prophylaxis. Clin Infect Dis 2014 (advanced access august 27) Eggimann P, Bille J, Marchetti O. Diagnosis of invasive candidiasis in the ICU. Ann Intensive Care 2011;1.37. Eggimann P, Marchetti O. Is (13)βDglucan the missing link from bedside assessment to preemptive therapy of invasive candidiasis? Crit Care 2011;15:1017. Gotzche PC, Johansen HK. Routine versus selective antifungal administration for control of fungal infections in patients with cancer. Cochrane Database of Systematic reviews 2014; 9: CD EORTC. Empiric antifungal therapy in febrile granulocytopenic patients. EORTC International Antimicrobial Therapy Cooperative Group. Am J Med 1989; 86:66872 EspinelIngroff D, Diekema DJ, Fothergill A, et al. Wildtype MIC distributions and epidemiological cutoff values for the triazoles and six Aspergillus spp for the CLSI broth microdilution method (M38A2 document). J Clin Microbiol 2010;48: EspinelIngroff A, Arendrup MC, Pfaller MA, et al. Interlaboratory variability of caspofungin MICs for Candida spp. using CLSI and EUCAST methods: should the clinical laboratory be testing this agent? Antimicrob Agents Chemother 2013;57: Falcone M, Barzaghi N, Carosi G, et al. Candida infective endocarditis. Report of 15 cases from a prospective multicenter study. Medicine 2009;88:1608. Freifeld AG, Bow EJ, Sepkowitz KA, et al. Clinical practice guideline for the use of antimicrobial agents in neutropenic patients with cancer: 2010 update by the Infectious Diseases Society of America. Clin Infect Dis 2011;52:e56e93. GarnachoMontero J, Olaechea P, AlvarezLerma F, et al. Epidemiology, diagnosis and treatment of fungal respiratory infections in the critically ill patient. Rev Esp Quimioter 2013; 26:
58 Girmenia C, Barosi G, Aversa F et al. Prophylaxis and treatment of invasive fungal diseases in allogenic stem cell transplantation: results of a Consensus process by Gruppo Italiano Trapianto di Midollo osseo (GITMO). Clin Infect Dis 2009; 49: Girmenia C, Barosi G, Piciocchi A,et al. Primary prophylaxis of invasive fungal diseases in allogenic stem cell transplantation: recise recommendations from a consensus process by Gruppo Italiano Trapianto Midollo osseo (GITMO). Biol Blood Marrow Transplant 2014;20: Guinea J, Torresnarbona M, Gijon P, et al. Pulmonary aspergillosis in patients with chronic obstructive pulmonary disease:incidence, risk factors, and outcome. Clin Microbiol Infect 2010; Guinea J, Bouza E. Current challenges in the microbiological diagnosis of invasive aspergillosis. Mycopathologia 2014, (ahead of print). Guinea J. Global trends in the distribution of Candida species causing candidemia. Clin Microbiol Infect 2014; 20 (Suppl.6):510 Guo YL, Chen YQ, Wang K, et al. Accuracy of BAL galactomannan in diagnosing invasive aspergillosis: a bivariate metaanalysis and systematic review. Chest 2010;138: Haddow LJ, Colebunders R, Meintjes, G et al. Cryptococcal immune reconstitution inflammatory syndrome in HIV1infected individuals.proposed clinical case definitions. Lancet Infect Dis 2010;10: Harris JR, Lockhart SR, Debess E, et al. Cryptococcus gattii in the United States: clinical aspects of infection with an emerging pathogen. Clin Infect Dis 2011; 53: Hamada Y, Tokimatsu I, Mikamo H, et al. Practice guidelines for therapeutic drug monitoring of voriconazole: a consensus review of the Japanese Society of Chemotherapy and the Japanese Society of Therapeutic Drug Monitoring. J Infect Chemother 2013; 19: Hanson KE, Pfeiffer CD, Lease ED, et al. βdglucan surveillance with preemptive anidulafungin for invasive candidiasis in Intensive care unit patients: a randomized pilot study. Plos One 2012,7:e Jarvis JN, Lawn SD, Vogt M, et al. Screening for cryptococcal antigenemia in patients accessing an antiretroviral treatment program in South Africa. Clin Infect Dis 2009,48: Jarvis JN, Govender N, Chiller T, et al. Cryptococcal antigen screening and preemptive therapy in patients initiating antiretroviral therapy in resourcelimited settings: a proposed algorithm for clinical implementation. J Int Assoc Physicians AIDS Care 2012;11:3749. Jorgensen KJ, Gotzche PC, Dalboge CS, Johansen HK. Voriconazole versus amphotericin B or fluconazole in cancer patients with neutropenia.cochrane Database of Systematic Reviews 2014; 2: CD Khasawneh F, Mohamad T, Moughrabieh MK, et al. isolation of aspergillus in critically ill patients: a potential marker of poor outcome. J Crit Care 2006;21:3227. Kontoyiannis DP, Lewis RE. How I treat mucormycosis. Blood 2011;118: Koulenti D, GarnachoMontero J, Blot S. Approach to invasive pulmonary aspergillosis in critically ill patients. Curr Opin Infect Dis 2014;27: Kuse ER, Chetchotisakd P, de Cunha CA, et al. Micafungin versus liposomal amphotericin B for candidaemia and invasive candidosis : a phase III randomised doubleblind trial. Lancet 2007;369: KwonChung KJ. Taxonomy of fungi causing Mucormycosis and Entomophthoramycosis (Zygomycosis) and nomenclature of the disease:molecular mycologic perspectives. Clin Infect Dis 2012; 54 (Suppl 1):S815.
59 Leon C, RuizSantana S, Saavedra P, et al. Usefulness of the Candida score for discriminating between Candida colonization and invasive candidiasis in nonneutropenic critically ill patients: a prospective multicenter study. Crit Care Med 2009;37: LopezMedrano F, San Juan R, Lizasoain M, et al. A noncompulsory stewardship programme for the management of antifungals in a universityaffiliated hospital. Clin Microbiol Infect 2013;19:5661. Maertens J, Marchetti O, Herbrecht R, et al. European guidelines for antifungal management in leukemia and hematopoietic stem cell transplant recipients: summary of the ECIL update. Bone Marrow Transplant 2011;46: Mckenney J, Smith RM, Chiller TM, et al. Prevalence and correlates of cryptococcal antigen positivity among AIDS patients United States Morbidity and Mortality Weekly Report (MMWR) 2014;63:5857. Milazzo L, Peri AM, Mazzali C, et al. Candidaemia observed at University hospital in Milan (Northern Italy) and review of published studies from 2010 to Mycopathologia 2014 ;178: Mondain V, Lieutier F, Hasseine L, et al. A 6year antifungal stewardship programme in a teaching hospital. Infection 2013;41:6218. MoraDuarte J, Betts R, Rotstein C, et al. Comparison of caspofungin and amphotericin B for invasive candidiasis. N Engl J Med 2002;347: Morell M, Fraser V, Kollef MH. Delaying the empiric treatment of Candida bloodstream infection until positive blood culture results are obtained: a potential risk factor for hospital mortality. Antimicrob Agents Chemother 2005;39: Mousset S, Buchheidt D, Heinz W, et al. Treatment of invasive fungal infections in cancer patientsupdated recommendations of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol 2014;93:1332. Muller M, Wandel S, Colebunders R, et al. Immune reconstitution inflammatory syndrome in patients starting antiretroviral therapy for HIV infection: a systematic review and metaanalysis. Lancet Infect Dis 2010;10: Mussini C, Pezzotti P, Mirò JM, et al. Discontinuation of maintenance therapy for cryptococcal meningitis in patients with AIDS treated with highly active antiretroviral therapy: an International observational study. Clin Infect Dis 2004;38: OstroskyZeichner L, Pappas PG, Shoham S, et al. Improvement of a clinical prediction rule for clinical trials on prophylaxis for invasive candidiasis in the intensive care unit. Mycoses 2011;54:4651. Pagano L, Caira M. The role of primary antifungal prophylaxis in patients with haematological malignancies. Clin Microbiol Infect 2014;20 (Suppl 6):1926. Pappas PG, Rotstein CM, Betts RF, et al. Micafungin versus caspofungin for treatment of candidemia and other forms of invasive candidiasis. Clin Infect Dis 2007;45: Pappas PG, Kaufmann CA, Andes D, et al. Clinical practice Guidelines for the management of candidiasis : 2009 update by the Infectious Diseases Society of America. Clin Infect Dis 2009; 48: Perfect JR, Dismukes WE, Dromer F, et al. Clinical practice guidelines for the management of cryptococcal disease: 2010 update by the Infectious Diseases Society of America. Clin Infect Dis 2010; 50: Petrikkos GL. Lipid formulations of amphotericin B as firstline treatment of zygomycosis. Clin Microbiol Infect 2009; 15 (Suppl 5):
60 Pfaller MA, Diekema DJ, Andes S, et al. Clinical breakpoints for the echinocandins and Candida revisited: integration of molecular, clinical,and microbiological data to arrive at speciesspecific interpretive criteria. Drug Resist Updat 2011;14: Pfaller MA, Diekema DJ, Jones RN, Castanheira M. use of anidulafungin as a surrogate marker to predict suceptibility and resi stance to caspofungin among 4,290 clinical isolates of Candida by using CLSI Methods interpretive criteria. J Clin Microbiol 2014, 52: Pittet D, Monod M, Suter PM, Frenk E, Auckenthaler R. Candida colonization and subsequent infections in critically ill surgical patients. Ann Surg 1994;220:7518. Pizzo PA, Robichau KJ, Gill FA, Witebsky FG. Empiric antibiotic and antifungal therapy for cancer patients with prolonged fever and granulocytopenia. Am J Med 1982;72: Posteraro B, De Pascale G, Tumbarello M, et al. Early diagnosis of candidemia in intensive care unit patients with sepsis: a prospective comparison of (13)βDglucan assay, candida score, and colonization index. Crit Care 2011;15:R249. Rajasingham R, Boulware DR. Reconsidering cryptococcal antigen screening in the US among persons with CD4< 100 cells/mcl. Clin Infect Dis 2012;55: Reboli AC, Rotstein C, Pappas PG,et al. Anidulafungin versus fluconazole for invasive candidiasis. N Engl J Med 2007; Reed EE, West JE, Keating EA, et al. Improving the management of candidemia through antimicrobial stewardship interventions. Diagn Microbiol Infect Dis 2014; 78: Ruhnke M, Rickerts V, Cornely OA, et al. Diagnosis and therapy of Candida infections: joint recommendations of the German Speaking Mycological Society and the PaulEhrlichSociety for Chemotherapy. Mycoses 2011;54: Ruhnke M. Antifungal stewardship in invasive Candida infections. Clin Microbiol Infect 2014; 20 (Suppl.6):1118. Slavin MA, Heath CH, Thursky KA, et al. Antifungal prophylaxis in adult stem cell transplantation and haematological malignancy. Intern Med J 2008;38: Skiada A, Lanternier F, Groll AH, et al. Diagnosis and treatment of mucormycosis in patients with haematological malignancies:guidelines from the 3 rd European Conference on Infections in Leukemia (ECIL3). Haematologica 2013; 98: Singh N. How I treat cryptococcosis in organ transplant recipients. Transplantation 2012;15:1721. Sobel JD, Revankar SG. Echinocandins first choice or firstline therapy for invasive candidiasis? N Engl J Med 2007; 356: Spellberg B, Edwards JJr., Ibrahim A. Novel perspectives on mucormycosis: pathophysiology, presentation, and management. Clin Microbiol Rev 2005;18: Tacke D, Buchheidt D, Karthaus M, et al. primary prophylaxis of invasive fungal infections in patients with haematologic malignancies update of the recommendations of the Infectious Diseases Working Party of the German Society for Hematology and Oncology. Ann Hematol 2014;93: Torres HA, Hachem RY, Chemaly RF, et al. Posaconazole : a broadspectrum triazole antifungal. Lancet Infect Dis 2005; 5: Tortorano AM, Peman J, Bernhardt H, et al. Epidemiology of candidaemia in Europe: results of 28month European Confederation of Medical Mycology (ECMM) hospitalbased surveillance study. Eur J Clin Microbiol Infect Dis 2004;23: Ullmann AJ, Akova M, Herbrecht R, et al. ESCMID guideline for the diagnosis and management of Candida diseases 2012: adults with haematological malignancies and after haematopoietic stem cell transplantation (HCT). Clin Microbiol Infect 2012;18 (Suppl.7):5367.
61 Valerio M, RodriguezGonzalez CG, Munoz P, et al. Evaluation of antifungal use in a tertiary care institution: antifungal stewardship urgently needed. J Antimicrob Chemother 2014 ahead of print. Vandewoude KH, Blot SI, Depuydt P, et al. Clinical relevance of Aspergillus isolation from respiratory tract samples in critically ill patients. Crit Care 2006;10:R31 Vasquez JA, Sobel JD. Anidulafungin : a novel echinocandin. Clin Infect Dis 2006 ; 43 : Vasquez J, Reboli A, Pappas PG, et al. Evaluation of an early stepdown strategy from intravenous anidulafungin to oral azole therapy for the treatment of candidemia and other forms of invasive candidiasis :results from an openlabel trial. BMC Infect Dis 2014;14:97. Walsh JT,Anaissie EJ, Denning DW, et al. Treatment of aspergillosis : clinical practice Guidelines of the Infectious Diseases Society of America. Clin Infect Dis 2008; 46: Wheat LJ, Freifeld AG, Kleiman MB, et al. Clinical practice guidelines for the management of patients with histoplasmosis : 2007 update by the Infectious Diseases Society of America. Clin Infect Dis 2007; 45: Ziakas PD, Kourbeti IS, Mylonakis E. Systemic antifungal prophylaxis after hematopoietic stem cell transplantation : a metaanalysis. Clin Ther 2014;36: Zou M, Tang L, Zhao S, et al. Systematic review and metaanalysis of detecting galactomannan in bronchoalveolare lavage fluid for diagnosis of invasive aspergillosis. Plos One 2012;7:e43347.
62 Allegato A Principali linee guida di terapia antimicotica suddivise per argomento Autori Titolo Rivista Commenti Aspergillosi Walsh TJ, Anaissie EJ, Denning DW, et al. Clin Infect Dis 2008, 46:32760 Ullmann AJ, Akova M, Barnes R, et al. Denning DW, Dimopoulos G, Lange C, et al. Candidosi Pappas PG, Kaufmann CA, Andes D, et al. Cornely OA, Bassetti M, Calandra T, et al. Ullmann AJ, Akova M, herbrecht R, et al. Lortholary O, Petrikkos G, Akova M, et al. Bow EJ, Evans G, Fuller J et al. Scudeller L, Viscoli C, menichetti F, et al. Colombo AL, Guimaraes T, Aranha Camargo LF, et al. Nucci M, ThompsonMoya L, GuzmanBlanco M, et al. Ruhnke M, Rickerts V, Cornely OA, et al. Criptococcosi Perfect JR, Dismukes WE, Dromer F, et al. Diagnosi IFI CuencaEstrella M, Verveij PE, Arendrup MC, et al. Ruhnke M, Bohme A, Bucheheidt D, et al. Treatment of Aspergillosis: clinical practice guidelines of the Infectious Diseases society of America ESCMID Aspergillosis guideline haematology and Oncology, haematopoietic Cell Transplantation 2014 ESCMID Aspergilllus guideline. Chronic pulmonary aspergillosis. Joint ESCMID and ERS guidelines Clinical practice guidelines for the management of Candidiasis: 2009 Update by the Infectious Diseases Society of America ESCMID guideline for the diagnosis and management of Candida diseases 2012: nonneutropenic adult patients ESCMID guideline for the diagnosis and management of Candida diseases 2012: adults with hematological malignancies and after haematopoietic stem cell transplantation (HCT) ESCMID guideline for the diagnosis and management of Candida diseases 2012: patients with HIV infection or AIDS Canadian clinical practice guidelines for invasive candidiasis in adults An Italian consensus for invasive candidiasis management (ITALIC) Brazilian guidelines for the management of candidiasis a joint meeting report of the three medical societies: Sociedade Brasileira de Infectologia, Sociedade Paulista de infectologia and Sociedade Brasileira de Medicina Tropical Recommendations for the management of candidemia in adults in Latin America Diagnosis and therapy of Candida infections: joint recommendations of the German Speaking Mycological Society and the PaulEhrlich Society for Chemotherapy Clinical practice guidelines for the management of cryptococcal disease: 2010 update by the Infectious Diseases Society of America ESCMID guideline for the diagnosis and management of Candida diseases 2012: diagnostic procedures Diagnosis of invasive fungal infections in hematology and oncologyguidelines from the Infectious Diseases Working Party in Haematology and Oncology of the German Society for Haematology and Oncology (AGIHO) ESCMID Online lecture Library ESCMID Online lecture Library Clin Infect Dis 2009; 48:50335 Clin Microbiol Infect 2012; 18 (Suppl.7):1937 Clin Microbiol Infect 2012;18(Suppl.7):5367 Clin Microbiol Infect 2012; 18(Suppl.7):6877 Can J Infect Dis Med Microbiol 2010; 21:e 122e150 Infection 2014;42: Braz J Infect Dis 2013; 17: Rev Iberoam Micol 2013;30:17988 Mycoses 2011, Clin Infect Dis 2010; 50: Clin Microbiol Infect 2012; 18 (Suppl.7):918 Le linee guida statunitensi. In corso l aggiornamento con pubblicazione prevista per la primavera 2015 Non ancora pubblicato; versione ridotta online Non ancora pubblicato; versione ridotta online Le linee guida statunitensi. In corso l aggiornamento con pubblicazione prevista per la primavera 2015 Le linee guida europee (ESCMID) per la terapia della malattia da Candida nei pazienti non neutropenici Le linee guida europee (ESCMID) per la terapia della malattia da Candida nei pazienti ematologici ( neutropenici) Le linee guida europee (ESCMID) per il trattamento delle infezioni da Candida nei pazienti con infezione da HIV Le linee guida canadesi che sotto molti punti di vista appaiono simili a quelle statunitensi Una Consensus di esperti italiani relativa al trattamento delle infezioni da Candida Le linee guida relative al trattamento delle infezioni da Candida elaborate da 3 società di malattie infettive e tropicali brasiliane Le raccomandazioni elaborate dal Latin America Invasive Mycosis Network Linne guida tedesche su tutti fli aspetti delle infezioni da Candida. Le uniche line guida specifiche su tutti gli aspetti della malattia criptococcica. Alcuni degli estensori sono europei Le linee guida europee relative alle procedure diagnostiche per le infezioni da Candida Ann Oncol 2012; Le linee guida tedesche (di 3 società) per la diagnosi delle IFI nei pazienti oncoematologici
63 Lagrou K, Buchheidt D, Richardson M, et al. Istoplasmosi Wheat LJ, Freifeld AG, Kleiman MB, et al. Mucormicosi Cornely OA, ArikanAkdagli S, Dannaoui E, et al. Skiada A, lanternier F, Groll AH, et al. Infezioni fungine rare Chowdhary A, Meis JF, Guarro J, et al. Arendrup MC, Boekhout T, Akova M, et al. Tortorano AM, Richardson M, Roilides E, et al. Chapman SW, Dismukes WE, Proia LA, et al. Galgiani JN, Ampel NM, Blair JE, et al. Kaufmann CA, Bustamante B, Chapman SW, Pappas PG. Diagnostic Group 2014 ESCMID Aspergillus guideline Clinical practice guidelines for the management of patients with histoplasmosis: 2007 update by the Infectious Diseases Society of America ESCMID and ECMM joint clinical guidelines for the diagnosis and management of mucormycosis 2013 Diagnosis and treatment of mucormycosis in patients with haematological malignancies: guidelines from the 3 rd European Conference on Infections in Leukaemia (ECIL 3) ESCMID and ECMM joint clinical guidelines for the diagnosis and management of systemic phaehyphomycosis :diseases caused by black fungi ESCMID and ECMM joint clinical guidelines for the diagnosis and management of rare invasive yeast infections ESMID and ECMM joint guidelines on diagnosis and management of hyalohyphomycosis: Fusarium spp., Scedosporium spp. and others Clinical practice guidelines for the management of blastomycosis: 2008 update by the Infectious Diseases ESCMID Online lecture Library Clin Infect Dis 2007;45:80725 Clin Microbiol Infect 2014;20 (Suppl.3):526 Haematologica 2013; Clin Microbiol Infect 2014; 20(Suppl. 3): 4775 Clin Microbiol Infect 2014; 20(Suppl.3):7698 Clin Microbiol Infect 2014; 20(Suppl.3):2746 Clin Infect Dis 2008;46: Versione maggio 2014, non ancora pubblicata Le line guida statunitensi (uniche ). Patologia emergente nei pazienti con infezione da HIV provenienti da aree endemiche Le linee guida della Società europea di microbiologia (ESCMID) e della Confederazione Europea di Micologia Medica (ECMM) per il trattamento della mucormicosi. Molti Autori presenti anche nelle linee guida ECIL Le linee guida ECIL (European Conference on Infections in Leukemia) sulla diagnosi e terapia della mucormicosi. Molti Autori presenti anche nelle linee guida ESCMID/ECMM Indicazioni sul trattamento delle micosi causate dalle seguenti specie: Alternaria, Acrophialophora, Aureobasidium, Bipolaris, Chaetomium, Cladophialophora, Curvularia, Exophiala, Exserohilum, Fonsecaea, Hortaea werneckii, Neoscytalidium dimidiatum, Ochroconis, Phaeoacremonium, Phoma, Pyrenochaeta, Rhinocladiella, Veronaea Indicazioni sul trattamento di specie rare di Candida, Cryptococcus (nonneoformans e nongattii), Malassezia, Rhodotorula, Saccharomyces, Sporobolomyces, Trichosporon Indicazioni su diagnosi e terapia di Fusariosi, scedosporiosi e infezioni da Acremonium, Paecilomyces e Scopulariopsis. Linee guida statunitensi relative alla blastomicosi (micosi endemica negli Stati Uniti e dei Grandi laghi del Canada) Society of America Coccidioidomycosis Clin Infect Dis 2005;41: Linee guida statunitensi relative alla coccidioidomicosi (micosi endemica in Arizona, California, Nuovo Messico, Texas). Aggiornamento in corso con pubblicazione prevista nella primavera 2015 Clinical practice guidelines for the management of sporotrichosis: 2007 update by the Infectious Diseases Society of America Monitoraggio terapeutico dei farmaci Ashbee HR, Barnes RA, Johnson EM, et al. Scodavolpe S, Quaranta S, Lacarelle B, Solas C. Therapeutic drug monitoring (TDM) of antifungal agents: guidelines from the British Society for Medical Mycology Triazole antifungal agents: practice guidelines of therapeutic drug monitoring and perspectives in treatment optimization Clin Infect Dis 2007;45: J Antimicrob Chemother 2014; 69: Ann Biol Clin 2014;72: Linee guida statunitensi relative alla sporotricosi. Diffusa in tutto il mondo ma di rara osservazione Documento della BSMM con indicazioni al monitoraggio degli azoli e della flucitosina con I target terapeutici Documento in francese del servizio di farmacocinetica dell Hopital de la Timone, Marsiglia sull impiego della TDM Hamada Y, Tokimatsu I, Practice guidelines for J Infect Chemother 2013;19:38192 Una Consensus giapponese
64 Mikamo H, et al therapeutic drug monitoring of voriconazole: a consensus review of the Japanese Society of Chemotherapy and the Japanese Society of Therapeutic Drug Monitoring Profilassi primaria delle IFI nei pazienti ematologici Tacke D, Buchheidt D, karthaus M, et al. Primary prophylaxis of invasive fungal infections in patients with haematologic malignancies update of the recommendations of the Infectious Diseases Working Party of the German Society for haematology and Oncology Girmenia C, Barosi G, Primary prophylaxis of invasive Piciocchi A, et al. fungal diseases in allogenic stem cell transplantation: recise recommendations from a Consensus process by Gruppo Italiano Trapianto Midollo Osseo (GITMO) Terapia delle IFI nei pazienti con neoplasie/ematologici Mousset S, Buchheidt D, Heinz W, et al. Maertens J, Marchetti O, Herbrecht R, et al. Prentice AG, Glasmacher A, Hobson RP, et al. Treatment of invasive fungal infections in cancer patientsupdated recommendations of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO) European guidelines for antifungal management in leukemia and hematopoietic stem cell transplant recipients: summary of the ECIL32009 update Guidelines on the management of invasive fungal infection during therapy for haematological malignancy. British Committee for Standards in Haematology Ann Hematol 2014;93: Biol Blood marrow Transplant 2014;20: Ann Hematol 2014;93:1332 Bone Marrow Transplant 2011; 46: sull impiego di TDM per il voriconazolo Le line guida tedesche sulla profilassi primaria antifungina nei pazienti ematologici Le raccomandazioni del GITMO per la profilassi primaria antifungina Le raccomandazioni tedesche per il trattamento delle infezioni fungine invasive nei pazienti affetti da neoplasie Le linee guida ECIL per il trattamento delle IFI nei pazienti con leucemia e trapianto di cellule staminali emopoietiche Le linee guida britanniche per il trattamento delle IFI nei pazienti con neoplasie ematologiche (reperibili all indirizzo web riportato) Allegato B Team multidisciplinare per la stewardship antimicotica Malattie Infettive ruolo Riferimento III Divisione Prof Spinello Antinori Responsabile Componente [email protected]; tel Dr Mario Corbellino Componente [email protected]; tel.2583 Dr Fabio Franzetti Componente [email protected]; tel.2949 Dr Agostino Riva Componente [email protected]; tel.2676 Dr Laura Milazzo Componente [email protected]; tel.3350 I Divisione Dr Massimo Coen Componente [email protected] ; tel 3504 Dr Marco Fasan Componente [email protected] ; tel 2908 Dr.ssa Giovanna Orlando Componente [email protected]; tel 2572 Dr.ssa Stefania Piconi Componente [email protected]; tel 3476/3497 Dr Agostino Zambelli Componente [email protected]; tel 3160 Farmacia Dr Massimo Medaglia ResponsabileComponente [email protected]; 2206 Dr Sechi Francesca Componente [email protected] ; 2757 Farmacologia clinica Dr Dario Cattaneo Responsabilecomponente [email protected]; tel Microbiologia Dr Romualdo Grande Responsabilecomponente [email protected]; tel 4036
65
66 Allegato C fattori di rischio per lo sviluppo di aspergillosi invasiva polmonare nei pazienti sottoposti a trapianto di organo solido Tipo di trapianto Precoce Tardiva (> 90 giorni posttrapianto) Trapianto di polmone Ischemia vie respiratorie Trapianto di singolo Infezioni batteriche polmone ricorrenti Protesi endobronchiale Infezione da CMV Insufficienza renale Pregressa colonizzazione delle vie aeree Rigetto cronico Insufficienza renale Terapia renale sostitutiva Trapianto di fegato Ritrapianto Insufficienza renale soprattutto se emodialisi posttrapianto Trapianto a seguito di insufficienza epatica fulminante Infezione da CMV Trapianto di cuore Isolamento di Aspergillus spp. da colture vie aeree Reintervento chirurgico Infezione da CMV Emodialisi posttrapianto Trapianto di rene Rigetto organo Emodialisi Dosi elevate e prolungate di steroidi Fonte: GarnachoMontero J et al. Rev Esp Quimioter 2013;26: > 6g di prednisone nel 3 mese posttrapianto Emodialisi posttrapianto Insufficienza renale posttrapianto Leucopenia posttrapianto (< 500/µL) Riammissione in ICU Insufficienza renale posttrapianto Concentrazioni di tacrolimus > 15 ng/ml o di ciclosporina > 500 ng/ml nel 3 mese posttrapianto 2 episodi di rigetto acuto
67 Allegato D Approccio pratico al paziente a rischio di candidosi invasiva in ICU Paziente a rischio di candidosi invasiva/candidemia Vedi tabella 1 Indice di colonizzazione Candida score Regole predittive di OZ N siti+/n siti sottoposti a scrrening (2 volte/settimana) > 0.5 o 0.4 (corretto) Chirurgica (ricovero in ICU) 1 pt Nutrizione parenterale totale 1 pt Sepsi grave 2 pt Colonizzazione Candida 1 pt > 2.5 pts In ICU > 4 giorni Sepsi+CVC+Ventilazione meccanica + 1 dei seguenti: NPT (giorni 13) Dialisi (giorni 13) Chirurgia maggiore (entro 7 giorni) Pancreatite (entro 7 giorni) Terapia immunosoppressiva (entro 7 giorni) o steroidi (entro 7 giorni) Iniziare terapia antifungina Pazienti trattati 1015% Candidiasi catturate 8590% Pazienti trattati 1520% Candidiasi catturate 7585% Pazienti trattati 1015% Candidiasi catturate 6075% Fonte: Eggimann P et al. Annals of Intensive Care 2011;1:37
68 Allegato E Criteri diagnostici proposti per la diagnosi putativa di aspergillosi polmonare invasiva nei pazienti ospedalizzati in ICU 1. Coltura positiva per Aspergillus spp. da materiale di provenienza respiratoria 2. Segni e sintomi clinici compatibili (almeno uno dei seguenti) Febbre refrattaria dopo almeno 3 giorni di terapia antibiotica appropriata Ricomparsa di febbre dopo un periodo di deferevescenza di almeno 48 ore mentre il paziente sta ricevendo ancora terapia antibiotica e senza altre cause apparenti Dolore di tipo pleuritico Sfregamento pleurico Dispnea Emottisi Peggioramento del quadro di insufficienza respiratoria nonostante appropriata terapia antibiotica e supporto ventilatorio 3. Alterazioni a carico dei polmoni dimostrate con RX torace o TC torace 4. 4a o 4b 4a Fattori di rischio relativi all ospite (una delle seguenti condizioni) Neutropenia (conta assoluta dei neutrofili inferiore a 500/µL) precedente o al momento del ricovero in ICU Patologia ematologica o neoplasia trattata con farmaci citotossici Terapia con corticosteroidi (dose giornaliera di prednisone o equivalente > 20 mg/die) Immunodeficienza congenita o acquisita 4b. Coltura semiquantitativa positiva per Aspergillus spp. da lavaggio broncoalveolare (+ o ++) senza crescita batterica associata a un esame citologico positivo che mostra ife dicotomiche La diagnosi richiede che tutti i criteri siano rispettati (i.e a o 4b) Adattata da : Vandewoude et al. Crit Care 2006; 10:R31; validata in Blot et al. Am J Respir Crit Care Med 2012;
Casi di IFI in pazienti sottoposti a HSCT allogenico con GVHD
 Casi di IFI in pazienti sottoposti a HSCT allogenico con GVHD Sindrome polmonare Sindrome sino-facciale Terapia pre-emptive Sepsi Sindrome al CNS Sindrome cutanea 58 CASO #1 Sepsi nel HSCT allogenico:
Casi di IFI in pazienti sottoposti a HSCT allogenico con GVHD Sindrome polmonare Sindrome sino-facciale Terapia pre-emptive Sepsi Sindrome al CNS Sindrome cutanea 58 CASO #1 Sepsi nel HSCT allogenico:
Le micosi sistemiche. Tiziana Quirino
 Le micosi sistemiche Tiziana Quirino Micosi sistemiche Candidosi Aspergillosi Ricovero in U.O. Medicina Donna di 68 anni Ricovero il 3 maggio 2013 per dolori addominali in carcinomatosi peritoneale
Le micosi sistemiche Tiziana Quirino Micosi sistemiche Candidosi Aspergillosi Ricovero in U.O. Medicina Donna di 68 anni Ricovero il 3 maggio 2013 per dolori addominali in carcinomatosi peritoneale
AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO. Il protocollo vaccinale per la malattia invasiva da Streptococcus pneumoniae
 AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Il protocollo vaccinale per la malattia invasiva da Streptococcus pneumoniae A cura del C.I.O. (C. Bonada, P.Pellegrino, G. Raineri) giugno 2015 Condizioni
AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Il protocollo vaccinale per la malattia invasiva da Streptococcus pneumoniae A cura del C.I.O. (C. Bonada, P.Pellegrino, G. Raineri) giugno 2015 Condizioni
ANIDULAFUNGINA ( )
 ANIDULAFUNGINA (16-12-2008) Specialità: Ecalta (Pfizer Italia srl) Forma farmaceutica: FL 30 ML 100MG - Prezzo: euro 594 ATC: J02AX06 Categoria terapeutica: Altri antimicotici per uso sistemico Fascia
ANIDULAFUNGINA (16-12-2008) Specialità: Ecalta (Pfizer Italia srl) Forma farmaceutica: FL 30 ML 100MG - Prezzo: euro 594 ATC: J02AX06 Categoria terapeutica: Altri antimicotici per uso sistemico Fascia
EVENTO FORMATIVO RES "CORE FOCUS alla radice del problema delle IFI INFORMAZIONI DI DETTAGLIO SUL PROGRAMMA FORMATIVO
 EVENTO FORMATIVO RES "CORE FOCUS alla radice del problema delle IFI Diagnosi e terapia delle infezioni micotiche invasive nel paziente oncoematologico: definizione di un protocollo diagnostico-terapeutico
EVENTO FORMATIVO RES "CORE FOCUS alla radice del problema delle IFI Diagnosi e terapia delle infezioni micotiche invasive nel paziente oncoematologico: definizione di un protocollo diagnostico-terapeutico
La candidiasi invasiva in geriatria: un problema emergente. Gli antimicotici nella politerapia dell anziano fragile
 INFEZIONI DA CANDIDA NEL PAZIENTE ANZIANO: CHI, COME E QUANDO TRATTARE? La candidiasi invasiva in geriatria: un problema emergente Candidiasi invasiva: dal sospetto alla diagnosi Approccio ragionato alla
INFEZIONI DA CANDIDA NEL PAZIENTE ANZIANO: CHI, COME E QUANDO TRATTARE? La candidiasi invasiva in geriatria: un problema emergente Candidiasi invasiva: dal sospetto alla diagnosi Approccio ragionato alla
Consumi di antifungini e orientamenti prescrittivi nella realtà locale
 Hospital Meeting Infezioni invasive da Candida: attuali aspetti epidemiologici e nuove opzioni terapeutiche Consumi di antifungini e orientamenti prescrittivi nella realtà locale Dott.ssa Rossella Carletti
Hospital Meeting Infezioni invasive da Candida: attuali aspetti epidemiologici e nuove opzioni terapeutiche Consumi di antifungini e orientamenti prescrittivi nella realtà locale Dott.ssa Rossella Carletti
Indicazioni su diagnosi e terapia delle infezioni fungine profonde (IFI)
 S.C. Malattie Infettive e Tropicali Direttore Dr Guido RAINERI Indirizzo: Via A. Carle, 5 Fraz.ne Confreria 12100 CUNEO Telefono +39 0171.616260 E-mail :[email protected] Fax +39 0171.616270
S.C. Malattie Infettive e Tropicali Direttore Dr Guido RAINERI Indirizzo: Via A. Carle, 5 Fraz.ne Confreria 12100 CUNEO Telefono +39 0171.616260 E-mail :[email protected] Fax +39 0171.616270
Update in Endocrinologia Clinica
 12 Congresso Nazionale AME Associazione Medici Endocrinologi Update in Endocrinologia Clinica 6th Joint Meeting with AACE Refreshment in Medicina Interna: Terapia antibiotica nel 2013 American Association
12 Congresso Nazionale AME Associazione Medici Endocrinologi Update in Endocrinologia Clinica 6th Joint Meeting with AACE Refreshment in Medicina Interna: Terapia antibiotica nel 2013 American Association
LINEE GUIDA DI TERAPIA ANTIMICOTICA SISTEMICA
 LINEE GUIDA DI TERAPIA ANTIMICOTICA SISTEMICA Dipartimento di Malattie Infettive Dipartimento Farmaceutico Elaborato da : Prof Spinello Antinori - U.O.C. Malattie Infettive III Approvato da Data invio
LINEE GUIDA DI TERAPIA ANTIMICOTICA SISTEMICA Dipartimento di Malattie Infettive Dipartimento Farmaceutico Elaborato da : Prof Spinello Antinori - U.O.C. Malattie Infettive III Approvato da Data invio
Dùtor, a mè gnù la prospera! Operetta (non proprio comica) in due atti
 Operetta (non proprio comica) in due atti ATTO PRIMO 1. il quesito ATTO SECONDO 5. il quesito ATTO PRIMO 4. la risposta Il caso clinico ATTO PRIMO 2. il PICO ATTO SECONDO 6. la risposta ATTO PRIMO 3. la
Operetta (non proprio comica) in due atti ATTO PRIMO 1. il quesito ATTO SECONDO 5. il quesito ATTO PRIMO 4. la risposta Il caso clinico ATTO PRIMO 2. il PICO ATTO SECONDO 6. la risposta ATTO PRIMO 3. la
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
Le infezioni in onco-ematologia. Dott.ssa Mariella Grasso S.C. Ematologia Cuneo
 Le infezioni in onco-ematologia Dott.ssa Mariella Grasso S.C. Ematologia Cuneo Fattori di rischio infettivo Patologia di base Chemioterapia Immunoterapia Auto e allo trapianto CVC Mucosite Neutropenia
Le infezioni in onco-ematologia Dott.ssa Mariella Grasso S.C. Ematologia Cuneo Fattori di rischio infettivo Patologia di base Chemioterapia Immunoterapia Auto e allo trapianto CVC Mucosite Neutropenia
Domenico Careddu, Milena Lo Giudice. Le infezioni delle vie urinarie
 Domenico Careddu, Milena Lo Giudice Le infezioni delle vie urinarie Banche dati utilizzate Valutazione AGREE Cosa fare nel sospetto di IVU? Nel sospetto clinico di IVU, è necessario raccogliere un campione
Domenico Careddu, Milena Lo Giudice Le infezioni delle vie urinarie Banche dati utilizzate Valutazione AGREE Cosa fare nel sospetto di IVU? Nel sospetto clinico di IVU, è necessario raccogliere un campione
Miceti di interesse medico
 ANTIMICOTICI Miceti di interesse medico Miceti lievitiformi o lieviti: Pityrosporum ovale, Candida albicans, Cryptococcus neoformans Miceti filamentosi o muffe: dermatofiti o cheratinofili (tinea corporis,
ANTIMICOTICI Miceti di interesse medico Miceti lievitiformi o lieviti: Pityrosporum ovale, Candida albicans, Cryptococcus neoformans Miceti filamentosi o muffe: dermatofiti o cheratinofili (tinea corporis,
LA NEUTROPENIA FEBBRILE
 LA NEUTROPENIA FEBBRILE Pazienti ematologici adulti a rischio infettivo Leucemie acute in terapia di induzione, consolidamento e salvataggio, sottoposte a trapianto di cellule staminali autologhe e allogeniche.
LA NEUTROPENIA FEBBRILE Pazienti ematologici adulti a rischio infettivo Leucemie acute in terapia di induzione, consolidamento e salvataggio, sottoposte a trapianto di cellule staminali autologhe e allogeniche.
IldocumentoGOLD completo(w ORKSHOPREPORTS)èconsultabilesulsitowww.goldcopd.it
 GUIDA RAPIDA PER LA GESTIONE AMBULATORIALE DELLA BPCO Basatasuprogettoglobaleperladiagnosi,gestionee prevenzionebpco (Aggiornamento2007) IldocumentoGOLD completo(w ORKSHOPREPORTS)èconsultabilesulsitowww.goldcopd.it
GUIDA RAPIDA PER LA GESTIONE AMBULATORIALE DELLA BPCO Basatasuprogettoglobaleperladiagnosi,gestionee prevenzionebpco (Aggiornamento2007) IldocumentoGOLD completo(w ORKSHOPREPORTS)èconsultabilesulsitowww.goldcopd.it
Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica
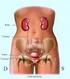 Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica I miei riferimenti per questa relazione: le linee-guida nazionali e internazionali Clinical Practice Guidelines
Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica I miei riferimenti per questa relazione: le linee-guida nazionali e internazionali Clinical Practice Guidelines
Esperienza di un programma di stewardship antimicrobica nel Policlinico S.Orsola Malpighi
 Esperienza di un programma di stewardship antimicrobica nel Policlinico S.Orsola Malpighi Marta Morotti Farmacia Clinica SiFaCT 1 Congresso Nazionale Milano, 13-14 settembre 2013 Agenda Contesto: il Policlinico
Esperienza di un programma di stewardship antimicrobica nel Policlinico S.Orsola Malpighi Marta Morotti Farmacia Clinica SiFaCT 1 Congresso Nazionale Milano, 13-14 settembre 2013 Agenda Contesto: il Policlinico
MICAFUNGIN ( )
 MICAFUNGIN (09-09-2009) Specialità: MYCAMINE (ASTELLAS PHARMA) Forma farmaceutica: 1 flaconcino per infusione endovenosa 50 mg/10 ml - Prezzo: euro 334.21 1 flaconcino per infusione endovenosa 100 mg/10
MICAFUNGIN (09-09-2009) Specialità: MYCAMINE (ASTELLAS PHARMA) Forma farmaceutica: 1 flaconcino per infusione endovenosa 50 mg/10 ml - Prezzo: euro 334.21 1 flaconcino per infusione endovenosa 100 mg/10
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
Infezioni ospedaliere (IO)
 Infezioni ospedaliere (IO) Infezioni che non erano clinicamente manifeste né in incubazione al momento del ricovero. Le infezioni ospedaliere possono manifestarsi anche dopo la dimissione o essere presenti
Infezioni ospedaliere (IO) Infezioni che non erano clinicamente manifeste né in incubazione al momento del ricovero. Le infezioni ospedaliere possono manifestarsi anche dopo la dimissione o essere presenti
Gli antimicotici nella politerapia dell anziano fragile
 Gli antimicotici nella politerapia dell anziano fragile Gaetano Serviddio Università degli Studi di Foggia MEDICINA INTERNA UNIVERSITARIA, Direttore: Prof. G. Vendemiale La dimensione del problema La peculiarità
Gli antimicotici nella politerapia dell anziano fragile Gaetano Serviddio Università degli Studi di Foggia MEDICINA INTERNA UNIVERSITARIA, Direttore: Prof. G. Vendemiale La dimensione del problema La peculiarità
Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una
 1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR POSACONAZOLO
 RICHIESTA DI INSERIMENTO IN PTR DI ATC J02AC04 (NOXAFIL ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data Novembre 2007 Per le seguenti motivazioni (sintesi): Nelle ultime
RICHIESTA DI INSERIMENTO IN PTR DI ATC J02AC04 (NOXAFIL ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data Novembre 2007 Per le seguenti motivazioni (sintesi): Nelle ultime
Salvatore Renna DEA Pediatrico UOC di PS Medico e Medicina d Urgenza IRCCS - Istituto G. Gaslini - Genova
 Salvatore Renna DEA Pediatrico UOC di PS Medico e Medicina d Urgenza IRCCS - Istituto G. Gaslini - Genova La patologia (adeno) faringo tonsillare, per l aspetto flogistico - infettivo, rappresenta uno
Salvatore Renna DEA Pediatrico UOC di PS Medico e Medicina d Urgenza IRCCS - Istituto G. Gaslini - Genova La patologia (adeno) faringo tonsillare, per l aspetto flogistico - infettivo, rappresenta uno
Candidemie in Medicina Interna Massimo Giusti
 Candidemie in Medicina Interna Massimo Giusti - Epidemiologia (1) - Sepsi in U.S.A. 1979-2000 Incremento del 200% negli ultimi 30 anni Candida spp in Europa tra i dieci patogeni più isolati 1 - The epidemiology
Candidemie in Medicina Interna Massimo Giusti - Epidemiologia (1) - Sepsi in U.S.A. 1979-2000 Incremento del 200% negli ultimi 30 anni Candida spp in Europa tra i dieci patogeni più isolati 1 - The epidemiology
L aggiornamento pubblicato nel marzo del 2007 è stato integrato con la pubblicazione della prima lista di farmaci essenziali ad uso pediatrico
 Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
Cos è un CVC( catetere venoso centrale)
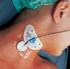 Cos è un CVC( catetere venoso centrale) A cura del Dott. Pierpaolo Casalini U.O. Rianimazione P.O. Faenza Cos è un CVC? E una porta aperta ( soluzione di continuo) fra il torrente venoso in prossimità
Cos è un CVC( catetere venoso centrale) A cura del Dott. Pierpaolo Casalini U.O. Rianimazione P.O. Faenza Cos è un CVC? E una porta aperta ( soluzione di continuo) fra il torrente venoso in prossimità
LE INFEZIONI FUNGINE
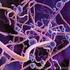 LE INFEZIONI FUNGINE Premessa. In seguito all incremento del numero di pazienti immunocompromessi, le infezioni micotiche sono progressivamente aumentate, rappresentando oggi un importante causa di morbilità
LE INFEZIONI FUNGINE Premessa. In seguito all incremento del numero di pazienti immunocompromessi, le infezioni micotiche sono progressivamente aumentate, rappresentando oggi un importante causa di morbilità
Torino, 19 ottobre 2011
 WORKSHOP Risultati del Programma Regionale di Screening Colorettale Aggiornamenti Protocollo Regionale Sono indicati: Test emocoagulativi? Profilassi antibiotica? Arrigo Arrigoni S.C.GASTROENTEROLOGIA
WORKSHOP Risultati del Programma Regionale di Screening Colorettale Aggiornamenti Protocollo Regionale Sono indicati: Test emocoagulativi? Profilassi antibiotica? Arrigo Arrigoni S.C.GASTROENTEROLOGIA
Documento PTR n. 222 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 222 relativo a: ECHINOCANDINE: Caspofungin, Micafungin e Anidulafungin
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 222 relativo a: ECHINOCANDINE: Caspofungin, Micafungin e Anidulafungin
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE.
 Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
L antimaicrobialstiuarscip (antimicrobialstewardship)
 L antimaicrobialstiuarscip (antimicrobialstewardship) Angelo Pan Area Rischio Infettivo E molto meglio somministrare l antibiotico giusto alla dose corretta ed al momento giusto, facendo guarire il paziente,
L antimaicrobialstiuarscip (antimicrobialstewardship) Angelo Pan Area Rischio Infettivo E molto meglio somministrare l antibiotico giusto alla dose corretta ed al momento giusto, facendo guarire il paziente,
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
Dott.. Giuseppe Di Mauro. (Caserta)
 Problematiche e prospettive dell antibioticoterapia in età pediatrica Dott.. Giuseppe Di Mauro (Caserta) Obiettivo Migliorare la prescrizione di farmaci in termini di efficacia e di efficienza tenendo
Problematiche e prospettive dell antibioticoterapia in età pediatrica Dott.. Giuseppe Di Mauro (Caserta) Obiettivo Migliorare la prescrizione di farmaci in termini di efficacia e di efficienza tenendo
1INFEZIONI DA CANDIDA
 1INFEZIONI DA CANDIDA Le infezioni da Candida sono frequenti nei pazienti in area critica in particolare nei pazienti traumatizzati, nei settici e nei post operatori, in quanto queste categorie sono per
1INFEZIONI DA CANDIDA Le infezioni da Candida sono frequenti nei pazienti in area critica in particolare nei pazienti traumatizzati, nei settici e nei post operatori, in quanto queste categorie sono per
PANCREATITE ACUTA DA FARMACI
 SCUOLA REGIONALE DI FORMAZIONE SPECIFICA IN MEDICINA GENERALE, CORSO 2010/2013. PATOLOGIA DEL PANCREAS PANCREATITE ACUTA DA FARMACI Elisabetta Ascari Fabio Bassi Medicina III Gastroenterologia Azienda
SCUOLA REGIONALE DI FORMAZIONE SPECIFICA IN MEDICINA GENERALE, CORSO 2010/2013. PATOLOGIA DEL PANCREAS PANCREATITE ACUTA DA FARMACI Elisabetta Ascari Fabio Bassi Medicina III Gastroenterologia Azienda
IL POST-ACUTO: LA RIABILITAZIONE RESPIRATORIA
 Dott. Michele Maiellari Specialista in Malattie dell Apparato Respiratorio Universita di Bari U.O. di Medicina e Chirurgia d Urgenza e Pronto Soccorso Resp.Dott.F. Serafino Ospedale San Giacomo Monopoli
Dott. Michele Maiellari Specialista in Malattie dell Apparato Respiratorio Universita di Bari U.O. di Medicina e Chirurgia d Urgenza e Pronto Soccorso Resp.Dott.F. Serafino Ospedale San Giacomo Monopoli
Polmoniti. Linee guida
 Linee guida Raccomandazioni sviluppate in modo sistematico per assistere medici e pazienti nelle decisioni sulla gestione appropriata di specifiche condizioni cliniche (Institute of Medicine1992) (IDSA
Linee guida Raccomandazioni sviluppate in modo sistematico per assistere medici e pazienti nelle decisioni sulla gestione appropriata di specifiche condizioni cliniche (Institute of Medicine1992) (IDSA
Dove si usano troppi antibiotici?
 Introduzione Resilienza dei microrganismi Primi fenomeni di resistenza descritti subito dopo la commercializzazione della penicillina Gli antibiotici rendono poco e l industria ha smesso di cercare La
Introduzione Resilienza dei microrganismi Primi fenomeni di resistenza descritti subito dopo la commercializzazione della penicillina Gli antibiotici rendono poco e l industria ha smesso di cercare La
MICOSI PROFONDE MICOSI PROFONDE CRITOTOCOCCOSI
 MICOSI PROFONDE Le micosi profonde sono infezioni che interessano solitamente il polmone, le quali possono eventualmente disseminare per via ematica con coinvolgimento degli organi interni e della cute
MICOSI PROFONDE Le micosi profonde sono infezioni che interessano solitamente il polmone, le quali possono eventualmente disseminare per via ematica con coinvolgimento degli organi interni e della cute
La prevenzione e la vaccinazione negli asplenici
 La prevenzione e la vaccinazione negli asplenici Pietro Ragni Struttura Governo Clinico ma Gratuità Offerta attiva Buona copertura vaccinale La vaccinazione delle persone a rischio aumentato dovrebbe
La prevenzione e la vaccinazione negli asplenici Pietro Ragni Struttura Governo Clinico ma Gratuità Offerta attiva Buona copertura vaccinale La vaccinazione delle persone a rischio aumentato dovrebbe
Microbiologia delle infezioni e sepsi correlate a catetere
 In collaborazione con Settore igiene ospedaliera e Centro studi EBN SEMINARIO Gestione dei cateteri venosi centrali 22 gennaio 2009 Policlinico Sant'Orsola-Malpighi Aula Murri Microbiologia delle infezioni
In collaborazione con Settore igiene ospedaliera e Centro studi EBN SEMINARIO Gestione dei cateteri venosi centrali 22 gennaio 2009 Policlinico Sant'Orsola-Malpighi Aula Murri Microbiologia delle infezioni
LE LINEE GUIDA ITALIANE SULLA GESTIONE DELLA TUBERCOLOSI IN ETÀ PEDIATRICA A. Villani
 LE LINEE GUIDA ITALIANE SULLA GESTIONE DELLA TUBERCOLOSI IN ETÀ PEDIATRICA A. Villani Le Linee Guida Italiane sulla gestione della Tubercolosi in età pediatrica Conduce: Susanna Esposito Partecipano: Luisa
LE LINEE GUIDA ITALIANE SULLA GESTIONE DELLA TUBERCOLOSI IN ETÀ PEDIATRICA A. Villani Le Linee Guida Italiane sulla gestione della Tubercolosi in età pediatrica Conduce: Susanna Esposito Partecipano: Luisa
L UTILITÀ E I LIMITI DEL VACCINO PNEUMOCOCCICO MULTIVALENTE IN ETÀ ADULTA E PEDIATRICA
 L UTILITÀ E I LIMITI DEL VACCINO PNEUMOCOCCICO MULTIVALENTE IN ETÀ ADULTA E PEDIATRICA ORDINE DEI MEDICI DI TORINO SALA RIVA ROCCI TORINO, 5 OTTOBRE 2006 CHE COSA DICE LA LETTERATURA? LA VACCINAZIONE
L UTILITÀ E I LIMITI DEL VACCINO PNEUMOCOCCICO MULTIVALENTE IN ETÀ ADULTA E PEDIATRICA ORDINE DEI MEDICI DI TORINO SALA RIVA ROCCI TORINO, 5 OTTOBRE 2006 CHE COSA DICE LA LETTERATURA? LA VACCINAZIONE
Casi di IFI in pazienti con AML
 Casi di IFI in pazienti con AML Sindrome polmonare Sindrome sino-facciale Sindrome al CNS Terapia pre-emptive Sepsi Sindrome epatosplenica (Candidosi disseminata cronica) Sindrome cutanea 38 CASO #1 Sindrome
Casi di IFI in pazienti con AML Sindrome polmonare Sindrome sino-facciale Sindrome al CNS Terapia pre-emptive Sepsi Sindrome epatosplenica (Candidosi disseminata cronica) Sindrome cutanea 38 CASO #1 Sindrome
CASO CLINICO. Tutto per un calcolo. R.Bassu, A. Alessandrì, M. Checchi, I. Lucchesi, L. Teghini, G. Panigada
 CASO CLINICO Tutto per un calcolo R.Bassu, A. Alessandrì, M. Checchi, I. Lucchesi, L. Teghini, G. Panigada - G.F. Uomo di 47 aa - In anamnesi: storia di poliposi nasale e nefrolitiasi per cui nel 2001
CASO CLINICO Tutto per un calcolo R.Bassu, A. Alessandrì, M. Checchi, I. Lucchesi, L. Teghini, G. Panigada - G.F. Uomo di 47 aa - In anamnesi: storia di poliposi nasale e nefrolitiasi per cui nel 2001
Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali. Meccanismo di azione e interazioni farmacologiche
 A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it [email protected]
A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it [email protected]
Profilo prescrittivo e risultati terapeutici della terapia antiretrovirale nel paziente HIV presso l Azienda Ospedaliero Universitaria di Ferrara
 Dipartimento Farmaceutico Interaziendale Profilo prescrittivo e risultati terapeutici della terapia antiretrovirale nel paziente HIV presso l Azienda Ospedaliero Universitaria di Ferrara Missere M.L.,
Dipartimento Farmaceutico Interaziendale Profilo prescrittivo e risultati terapeutici della terapia antiretrovirale nel paziente HIV presso l Azienda Ospedaliero Universitaria di Ferrara Missere M.L.,
CHEMIOPROFILASSI PRIMARIA
 CHEMIOPROFILASSI PRIMARIA Somministrazione di chemioterapici o antibiotici a persone recentemente esposte a un rischio di contagio con lo scopo di bloccare lo sviluppo del processo infettivo. CHEMIOPROFILASSI
CHEMIOPROFILASSI PRIMARIA Somministrazione di chemioterapici o antibiotici a persone recentemente esposte a un rischio di contagio con lo scopo di bloccare lo sviluppo del processo infettivo. CHEMIOPROFILASSI
PERCORSO DIAGNOSTICO TERAPEUTICO DELLA MALATTIA PEPTICA
 Rev.: 0 Pag. 1/5 AUTORIZZAZIONI REV. DATA REDATTO VERIFICATO APPROVATO 26/06/02 DR. Matergi, Dr. Biscontri, Igiene e Dr. Diversi, Dr. Lavagni, Organizzazione dei Dr. Magnanelli Servizi Sanitari Rev.: 0
Rev.: 0 Pag. 1/5 AUTORIZZAZIONI REV. DATA REDATTO VERIFICATO APPROVATO 26/06/02 DR. Matergi, Dr. Biscontri, Igiene e Dr. Diversi, Dr. Lavagni, Organizzazione dei Dr. Magnanelli Servizi Sanitari Rev.: 0
BPCO: l avvio di un Percorso Diagnostico Terapeutico Assistenziale (PDTA) nell Azienda USL di Ferrara
 BPCO: l avvio di un Percorso Diagnostico Terapeutico Assistenziale (PDTA) nell Azienda USL di Ferrara Carlotta Serenelli *, Sandro Bartalotta **, Mauro Manfredini*** *Dipartimento Cure Primarie Azienda
BPCO: l avvio di un Percorso Diagnostico Terapeutico Assistenziale (PDTA) nell Azienda USL di Ferrara Carlotta Serenelli *, Sandro Bartalotta **, Mauro Manfredini*** *Dipartimento Cure Primarie Azienda
Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche?
 ANDREA GIUSTINA Direttore Cattedra Endocrinologia Università degli Studi di Brescia Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche? Come da determinazione
ANDREA GIUSTINA Direttore Cattedra Endocrinologia Università degli Studi di Brescia Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche? Come da determinazione
PROFILASSI ANTITROMBOTICA IN CHIRURGIA GENERALE
 CHIRURGIA GENERALE MAGGIORE (tutti gli interventi di durata > 30 minuti o di chirurgia addominale) TIPO DI PATOLOGIA TIPO DI CHIRURGIA MIRE (tutti gli interventi di durata < 30 minuti, esclusa la chirurgia
CHIRURGIA GENERALE MAGGIORE (tutti gli interventi di durata > 30 minuti o di chirurgia addominale) TIPO DI PATOLOGIA TIPO DI CHIRURGIA MIRE (tutti gli interventi di durata < 30 minuti, esclusa la chirurgia
La BPCO e le comorbilità. Federico Sciarra
 La BPCO e le comorbilità Federico Sciarra La BPCO, essendo una malattia cronica con caratteristiche di infiammazione sistemica, facilmente coesiste con altre patologie sia acute che croniche, che influenzano
La BPCO e le comorbilità Federico Sciarra La BPCO, essendo una malattia cronica con caratteristiche di infiammazione sistemica, facilmente coesiste con altre patologie sia acute che croniche, che influenzano
Paziente con batteriemia da ceppo multi resistente, considerazioni su che fare
 Paziente con batteriemia da ceppo multi resistente, considerazioni su che fare Elio Castagnola Unità di Malattie Infettive Istituto Giannina Gaslini - Genova diagnosi LLA-B in altro centro, esegue chemioterapia
Paziente con batteriemia da ceppo multi resistente, considerazioni su che fare Elio Castagnola Unità di Malattie Infettive Istituto Giannina Gaslini - Genova diagnosi LLA-B in altro centro, esegue chemioterapia
SINDROME DA ANTICORPI ANTI-FOSFOLIPIDI
 SINDROME DA ANTICORPI ANTI-FOSFOLIPIDI Malattia caratterizzata da trombosi arteriose e/o venose ricorrenti, aborti ripetuti, trombocitopenia,, in associazione a titoli medio-alti di anticorpi anti-fosfolipidi
SINDROME DA ANTICORPI ANTI-FOSFOLIPIDI Malattia caratterizzata da trombosi arteriose e/o venose ricorrenti, aborti ripetuti, trombocitopenia,, in associazione a titoli medio-alti di anticorpi anti-fosfolipidi
UNIVERSITA' degli STUDI di PERUGIA. Corso di Laurea in Medicina e Chirurgia AA Farmaci
 UNIVERSITA' degli STUDI di PERUGIA Corso di Laurea in Medicina e Chirurgia AA 2013-2014 Farmaci antimicotici Infezioni fungine generalizzate Aumentata incidenza nelle ultime tre decadi in reparti a rischio
UNIVERSITA' degli STUDI di PERUGIA Corso di Laurea in Medicina e Chirurgia AA 2013-2014 Farmaci antimicotici Infezioni fungine generalizzate Aumentata incidenza nelle ultime tre decadi in reparti a rischio
SCREENING TUBERCOLOSI & D.O.T. TRA IMMIGRATI E FASCE DI POPOLAZIONI A RISCHIO: L ESPERIENZA DELL ULSS 20
 SCREENING TUBERCOLOSI & D.O.T. TRA IMMIGRATI E FASCE DI POPOLAZIONI A RISCHIO: L ESPERIENZA DELL ULSS 20 Dott.sa Emma Conti METODI DI SCREENING Test intradermico secondo Mantoux (TST) La Mantoux è positiva
SCREENING TUBERCOLOSI & D.O.T. TRA IMMIGRATI E FASCE DI POPOLAZIONI A RISCHIO: L ESPERIENZA DELL ULSS 20 Dott.sa Emma Conti METODI DI SCREENING Test intradermico secondo Mantoux (TST) La Mantoux è positiva
ENDOCARDITE INFETTIVA
 ENDOCARDITE INFETTIVA E NDOCARDITE INFETTIVA Infezione dell endocardio endocardio causata da microorganismi patogeni. Nella grandissima maggioranza dei casi l endocardio l interessato è l endocardio valvolare.
ENDOCARDITE INFETTIVA E NDOCARDITE INFETTIVA Infezione dell endocardio endocardio causata da microorganismi patogeni. Nella grandissima maggioranza dei casi l endocardio l interessato è l endocardio valvolare.
EVENTO FORMATIVO RESIDENZIALE:
 EVENTO FORMATIVO RESIDENZIALE: L attività di counseling: la gestione del paziente con BPCO Informazione di dettaglio sul programma formativo NR. DI ACCREDITAMENTO 2714-135166 Ed.1 DATA E LOCATION 11-10-2015
EVENTO FORMATIVO RESIDENZIALE: L attività di counseling: la gestione del paziente con BPCO Informazione di dettaglio sul programma formativo NR. DI ACCREDITAMENTO 2714-135166 Ed.1 DATA E LOCATION 11-10-2015
AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri)
 AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
I test per la trombofilia: quali no!
 I test per la trombofilia: quali no! Benedetto Morelli Laboratorio e Trombofilia congenita ed acquisita: quali test, a chi, quando, perché? Bari, 9 aprile 2016 ROAD MAP Importanza della appropriatezza
I test per la trombofilia: quali no! Benedetto Morelli Laboratorio e Trombofilia congenita ed acquisita: quali test, a chi, quando, perché? Bari, 9 aprile 2016 ROAD MAP Importanza della appropriatezza
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI MICAFUNGINA (MYCAMINE ) Presentata da Dott. E. Angelucci Direttore S.C. Ematologia P.O. Businco ASL 8 In data luglio 2010 Per le seguenti motivazioni (sintesi): Micafungina
RICHIESTA DI INSERIMENTO IN PTR DI MICAFUNGINA (MYCAMINE ) Presentata da Dott. E. Angelucci Direttore S.C. Ematologia P.O. Businco ASL 8 In data luglio 2010 Per le seguenti motivazioni (sintesi): Micafungina
UNIVERSITA DEGLI STUDI DI PALERMO FACOLTA DI MEDICINA E CHIRURGIA
 UNIVERSITA DEGLI STUDI DI PALERMO FACOLTA DI MEDICINA E CHIRURGIA CDL IN TECNICHE DI LABORATORIO BIOMEDICO (abilitante all esercizio della professione di Tecnico di Laboratorio Biomedico) Presidente: Prof.
UNIVERSITA DEGLI STUDI DI PALERMO FACOLTA DI MEDICINA E CHIRURGIA CDL IN TECNICHE DI LABORATORIO BIOMEDICO (abilitante all esercizio della professione di Tecnico di Laboratorio Biomedico) Presidente: Prof.
PROTOCOLLO Per il trattamento dell iperpiressia. nei pazienti sottoposti ad intervento di protesi d anca e di ginocchio PROTOCOLLO
 nei pazienti sottoposti ad intervento PRCIO 18 Data 18/08/2008 Pagina 1 di 8 PROTOCOLLO INDICE 1. SCHEDA RIASSUNTIVA 2 2. SCOPO 3 3. CAMPO DI APPLICAZIONE 3 4. DESCRIZIONE DELLE ATTIVITA 4 5. FASI OPERATIVE
nei pazienti sottoposti ad intervento PRCIO 18 Data 18/08/2008 Pagina 1 di 8 PROTOCOLLO INDICE 1. SCHEDA RIASSUNTIVA 2 2. SCOPO 3 3. CAMPO DI APPLICAZIONE 3 4. DESCRIZIONE DELLE ATTIVITA 4 5. FASI OPERATIVE
Epidemiologia della tubercolosi in Italia (anni )
 Epidemiologia della tubercolosi in Italia (anni 1995 2005) Prefazione Il sistema di notifica della tubercolosi, elemento indispensabile al programma di controllo della malattia stessa, ha tra gli obiettivi
Epidemiologia della tubercolosi in Italia (anni 1995 2005) Prefazione Il sistema di notifica della tubercolosi, elemento indispensabile al programma di controllo della malattia stessa, ha tra gli obiettivi
Convulsioni febbrili. Quale terapia preventiva? Quando approfondire?
 Convulsioni febbrili. Quale terapia preventiva? Quando approfondire? Dr Fabio M. Corsi UOC Neurologia e Neurofisiopatologia A.O. San Camillo Forlanini DEFINIZIONI Convulsione febbrile semplice (CFS) Una
Convulsioni febbrili. Quale terapia preventiva? Quando approfondire? Dr Fabio M. Corsi UOC Neurologia e Neurofisiopatologia A.O. San Camillo Forlanini DEFINIZIONI Convulsione febbrile semplice (CFS) Una
Modulo 4. Manifestazioni cliniche e possibili complicanze dell'asma allergico
 Modulo 4 Manifestazioni cliniche e possibili complicanze dell'asma allergico Classificazione di gravità prima dell inizio del trattamento STEP 4 Grave persistente STEP 3 Moderato persistente STEP 2 Lieve
Modulo 4 Manifestazioni cliniche e possibili complicanze dell'asma allergico Classificazione di gravità prima dell inizio del trattamento STEP 4 Grave persistente STEP 3 Moderato persistente STEP 2 Lieve
FONTE :
 FONTE : http://www.msd-italia.it/altre/manuale/sez01/0040059e.html MALATTIA DI WILSON Tossicosi da rame Il morbo di Wilson è una malattia progressiva e costantemente fatale del metabolismo del rame che
FONTE : http://www.msd-italia.it/altre/manuale/sez01/0040059e.html MALATTIA DI WILSON Tossicosi da rame Il morbo di Wilson è una malattia progressiva e costantemente fatale del metabolismo del rame che
MANIFESTAZIONI NEUROLOGICHE IN CORSO DI INFEZIONE DA HIV
 MANIFESTAZIONI NEUROLOGICHE IN CORSO DI INFEZIONE DA HIV L'HIV è stato isolato nel tessuto cerebrale e nel liquor, edèpresente nel SNC fin dai primi stadi dell'infezione virale generalizzata I disturbi
MANIFESTAZIONI NEUROLOGICHE IN CORSO DI INFEZIONE DA HIV L'HIV è stato isolato nel tessuto cerebrale e nel liquor, edèpresente nel SNC fin dai primi stadi dell'infezione virale generalizzata I disturbi
I medici non devono più prescrivere medicinali contenenti calcitonina in forma di spray nasale per il trattamento dell'osteoporosi.
 20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
LA PREVENZIONE DELLA BPCO
 Claudio M.Sanguinetti LA PREVENZIONE DELLA BPCO Consulente Pneumologo Casa di Cura Quisisana Già Direttore UOC Pneumologia- UTIR Az.Compl.Ospedaliero San Filippo Neri ROMA PREVENZIONE PRIMARIA DELLA BPCO
Claudio M.Sanguinetti LA PREVENZIONE DELLA BPCO Consulente Pneumologo Casa di Cura Quisisana Già Direttore UOC Pneumologia- UTIR Az.Compl.Ospedaliero San Filippo Neri ROMA PREVENZIONE PRIMARIA DELLA BPCO
Uso del Levamisolo e della Ciclofosfamide nella Sindrome Nefrosica Idiopatica in età Pediatrica
 Uso del Levamisolo e della Ciclofosfamide nella Sindrome Nefrosica Idiopatica in età Pediatrica Luciana Ghio Elena Groppali ROMA 4 Maggio 2013 IV Congresso ASNIT Onlus Incontro medici e famiglie Risposta
Uso del Levamisolo e della Ciclofosfamide nella Sindrome Nefrosica Idiopatica in età Pediatrica Luciana Ghio Elena Groppali ROMA 4 Maggio 2013 IV Congresso ASNIT Onlus Incontro medici e famiglie Risposta
RICERCA E SVILUPPO DI NUOVI FARMACI
 RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana. Massimo Landi Pediatria di gruppo - Torino
 Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana Massimo Landi Pediatria di gruppo - Torino Rapporto pediatria 2003 Campione Arno Dei 645 principi attivi i primi
Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana Massimo Landi Pediatria di gruppo - Torino Rapporto pediatria 2003 Campione Arno Dei 645 principi attivi i primi
Presentazione dei dati
 Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
PERCORSO DIAGNOSTICO Infezioni Fungine Invasive
 PERCORSO DIAGNOSTICO Infezioni Fungine Invasive Algoritmi diagnostici BAL Liquor Anticorpi anti- Aspergillus Galattomannano Mannano/anti-Mannano FISH, Array β-d- Glucano Esame colturale Spettrometria PCR
PERCORSO DIAGNOSTICO Infezioni Fungine Invasive Algoritmi diagnostici BAL Liquor Anticorpi anti- Aspergillus Galattomannano Mannano/anti-Mannano FISH, Array β-d- Glucano Esame colturale Spettrometria PCR
8 a Conferenza Nazionale GIMBE Evidence, Governance, Performance
 8 a Conferenza Nazionale GIMBE Evidence, Governance, Performance Bologna, 15 marzo 2013 Polmonite acquisita in comunità Misurare l appropriatezza professionale e organizzativa Carlo Barbetta Centro di
8 a Conferenza Nazionale GIMBE Evidence, Governance, Performance Bologna, 15 marzo 2013 Polmonite acquisita in comunità Misurare l appropriatezza professionale e organizzativa Carlo Barbetta Centro di
Commissione Regionale Farmaco (D.G.R. 1209/2002)
 Commissione Regionale Farmaco (D.G.R. 1209/2002) Documento relativo a: BUDESONIDE + FORMOTEROLO SALMETEROLO XINAFOATO + FLUTICASONE PROPIONATO usi appropriati delle associazioni di farmaci steroidei e
Commissione Regionale Farmaco (D.G.R. 1209/2002) Documento relativo a: BUDESONIDE + FORMOTEROLO SALMETEROLO XINAFOATO + FLUTICASONE PROPIONATO usi appropriati delle associazioni di farmaci steroidei e
RUOLO DEL MEDICO DI M.G. NELLA GESTIONE DELLE INTOLLERANZE ALIMENTARI. DOTT Pesola
 RUOLO DEL MEDICO DI M.G. NELLA GESTIONE DELLE INTOLLERANZE ALIMENTARI DOTT Pesola Ambito delle cure primarie Ospedale Specialistica Medicina di Famiglia Pazienti sintomatici esordio MALATTIA e MALATTIA
RUOLO DEL MEDICO DI M.G. NELLA GESTIONE DELLE INTOLLERANZE ALIMENTARI DOTT Pesola Ambito delle cure primarie Ospedale Specialistica Medicina di Famiglia Pazienti sintomatici esordio MALATTIA e MALATTIA
OGGETTO: Ricoveri ospedalieri per patologie respiratorie nella popolazione nata in Italia, residente a S. Polo e nel resto del comune di Brescia.
 OGGETTO: Ricoveri ospedalieri per patologie respiratorie nella popolazione nata in Italia, residente a S. Polo e nel resto del comune di Brescia. Introduzione I risultati ottenuti dall indagine precedente
OGGETTO: Ricoveri ospedalieri per patologie respiratorie nella popolazione nata in Italia, residente a S. Polo e nel resto del comune di Brescia. Introduzione I risultati ottenuti dall indagine precedente
Strategie per la diagnosi e la terapia delle Infezioni Fungine Invasive (IFI) in pazienti ad alto rischio
 Strategie per la diagnosi e la terapia delle Infezioni Fungine Invasive (IFI) in pazienti ad alto rischio 28 Obiettivi della presentazione Fornire una visione generale sui fattori di rischio, segni e sintomi,
Strategie per la diagnosi e la terapia delle Infezioni Fungine Invasive (IFI) in pazienti ad alto rischio 28 Obiettivi della presentazione Fornire una visione generale sui fattori di rischio, segni e sintomi,
La vaccinazione per l influenza stagionale
 La vaccinazione per l influenza stagionale Sigismondo Ferrante 1 12 settembre 2009 2 Roma, 23 luglio2009 1 Obiettivi della campagna vaccinale stagionale contro l influenza riduzione del rischio individuale
La vaccinazione per l influenza stagionale Sigismondo Ferrante 1 12 settembre 2009 2 Roma, 23 luglio2009 1 Obiettivi della campagna vaccinale stagionale contro l influenza riduzione del rischio individuale
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO
 EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
LE NECESSITA SANITARIE DEI PAZIENTI E IL RUOLO DEI CENTRI EMOSTASI E TROMBOSI
 LE NECESSITA SANITARIE DEI PAZIENTI E IL RUOLO DEI CENTRI EMOSTASI E TROMBOSI Sophie Testa Centro Emostasi e Trombosi Laboratorio Analisi Chimico- Cliniche e Microbiologia Istituti Ospitalieri, Cremona
LE NECESSITA SANITARIE DEI PAZIENTI E IL RUOLO DEI CENTRI EMOSTASI E TROMBOSI Sophie Testa Centro Emostasi e Trombosi Laboratorio Analisi Chimico- Cliniche e Microbiologia Istituti Ospitalieri, Cremona
4ª UNITA DIDATTICA Modello Nutrizionale metabolico
 4ª UNITA DIDATTICA Modello Nutrizionale metabolico Contenuti Modello Nutrizionale metabolico Sezione del modello: Equilibrio idro-elettrolitico e acido-base Assistenza alla persona con problemi relativi
4ª UNITA DIDATTICA Modello Nutrizionale metabolico Contenuti Modello Nutrizionale metabolico Sezione del modello: Equilibrio idro-elettrolitico e acido-base Assistenza alla persona con problemi relativi
Terapia medica e terapia chirurgica
 Terapia medica e terapia chirurgica Terapia della Rinite Allergica Educazione del Paziente Prevenzione Ambientale Lavaggio Nasale Trattamento Farmacologico Immunoterapia Specifica Trattamento Chirurgico
Terapia medica e terapia chirurgica Terapia della Rinite Allergica Educazione del Paziente Prevenzione Ambientale Lavaggio Nasale Trattamento Farmacologico Immunoterapia Specifica Trattamento Chirurgico
Percorso scompenso cardiaco secondo Chronic Care nella zona montana: a che punto siamo, quali sono i problemi e quali le prospettive di sviluppo.
 Percorso scompenso cardiaco secondo Chronic Care nella zona montana: a che punto siamo, quali sono i problemi e quali le prospettive di sviluppo. Scompenso cardiaco Lo scompenso cardiaco rappresenta una
Percorso scompenso cardiaco secondo Chronic Care nella zona montana: a che punto siamo, quali sono i problemi e quali le prospettive di sviluppo. Scompenso cardiaco Lo scompenso cardiaco rappresenta una
