ANALISI QUALITATIVA: SAGGI PRELIMINARI. Odore
|
|
|
- Maddalena Gigli
- 8 anni fa
- Просмотров:
Транскрипт
1 Esame organolettico: Stato fisico ANALISI QUALITATIVA: SAGGI PRELIMINARI Colore Odore
2 ANALISI QUALITATIVA: SAGGI PRELIMINARI Saggi per via secca: Si eseguono sulla sostanza secca, cioè senza portarla in soluzione. Non vanno mai trascurati poiché forniscono informazioni molto utili per lo svolgimento dell analisi e, in qualche caso, possono portare a risultati pressoché definitivi.
3 LA RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è una forma di energia che si propaga. Essa è la risultante di due campi, uno elettrico (E) e l altro magnetico (B) che vibrano in direzioni perpendicolari fra loro e perpendicolari alla direzione di propagazione dell onda stessa. E y B z x
4 LA RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica presenta una duplice natura: ondulatoria e corpuscolare. MODELLO ONDULATORIO Il carattere ondulatorio di una radiazione può essere descritto da alcuni parametri: y Lunghezza d onda ampiezza x Lunghezza d onda (λ): distanza fra due punti successivi in fase fra loro (per esempio fra due massimi o due minimi dell onda che si propaga). Frequenza (ν): numero di oscillazioni al secondo (numero di onde che in un secondo passano in un punto). Ampiezza (A) : massimo spostamento di un punto rispetto alla posizione di equilibrio. Velocità di propagazione (c): velocità delle onde elettromagnetiche (nel vuoto: velocità della luce = cm/sec). Questi parametri sono legati dalla relazione: c = ν. λ
5 LA RADIAZIONE ELETTROMAGNETICA MECCANICA ONDULATORIA La radiazione elettromagnetica può essere anche definita come un flusso di particelle, dette fotoni. I fotoni, quanti di energia, sono dei veri e propri corpuscoli in movimento. L energia di un fotone è proporzionale alla frequenza della radiazione ed è data dalla equazione di Einstein-Planck: E = hν Sapendo che c = ν λ, potremo scrivere: E = hν = h c λ dove h è la costante di Planck, che vale 6,63 x J. s. Le radiazioni a maggiore energia, dunque, sono quelle a più alta frequenza (e minore lunghezza d onda). N.B. Quando un onda elettromagnetica passa dal vuoto ad un altro mezzo, la sua velocità diminuisce e, in proporzione, diminuisce anche la lunghezza d onda (λ), mentre la frequenza (ν) rimane costante, per cui quest ultima risulta la grandezza più caratteristica di un onda elettromagnetica. Tuttavia, nell uso comune, le radiazioni vengono spesso indicate con λ: in tal caso si intende riferita al vuoto.
6 SPETTRO ELETTROMAGNETICO L insieme di tutte le radiazioni elettromagnetiche costituisce lo spettro elettromagnetico che copre tutto l intervallo compreso fra i raggi gamma (λ ~ 1 pm) e le onde lunghe (λ ~ 1 Km). Lunghezza d onda 1 pm 1 nm 1 µm 1 mm 1 m 1 Km Raggi gamma forti Raggi x deboli Ultravioletto infrarosso microonde Onde corte Onde radio Onde lunghe Lo spettro visibile nm λ ν E E = hν = h c λ
7 SPETTRO ELETTROMAGNETICO Raggi gamma Raggi X Ultravioletto Visibile Infrarosso Microonde Radio Lunghezza d onda in centimetri Circa le dimensioni di.. Nuclei Atomi Molecole Protozoi Punte di spillo Api Uomini Palazzi
8 SPETTRO VISIBILE violetto indaco azzurro verde giallo arancio rosso lunghezza d onda (nm)
9 SPETTRO VISIBILE λ (nm)
10 IL COLORE Una sostanza appare colorata quando assorbe una parte delle radiazioni e.m. che costituiscono la luce solare, cioè se assorbe radiazioni con λ comprese nella parte visibile dello spettro e.m. Il colore della sostanza sarà dato da quella porzione di radiazioni dello spettro visibile che non sono state assorbite e che pertanto vengono riflesse dalla sostanza. La radiazione che giunge all occhio contiene solo le lunghezze d onda che non sono state assorbite, cioè le radiazioni complementari. Il colore sarà dato dalle radiazioni complementari a quelle assorbite In questo caso l oggetto illuminato assorbe le radiazioni nella regione del blu verde, quindi verranno trasmesse prevalentemente le radiazioni nella regione del rosso e quindi l oggetto viene percepito come rosso.
11 Rosa dei colori o ruota dei colori I colori complementari sono disposti in settori opposti al vertice. Se un oggetto assorbe tutte le radiazioni visibili che riceve, appare nero. Se, invece, un oggetto non assorbe nel visibile, appare bianco.
12 Il colore delle sostanze L energia luminosa assorbita da una sostanza eccita gli elettroni della sostanza stessa, provocando il trasferimento di un elettrone ad un livello superiore dell atomo. L energia richiesta per i salti elettronici è diversa a seconda del tipo di atomo e del modo in cui esso è legato nelle molecole. L assorbimento di energia radiante è in stretta relazione alla struttura elettronica degli atomi che costituiscono la sostanza. Le radiazioni assorbite sono caratteristiche delle diverse sostanze (sostanze diverse assorbono radiazioni diverse e, conseguentemente appariranno di colori diversi) solfato di rame nitrato di cobalto cloruro di manganese cloruro di nichel
13 Colore dei metalli Quando un metallo viene colpito dalla luce, gli atomi del metallo possono interagire con i fotoni incidenti, i quali pertanto possono venire assorbiti oppure riflessi. Un fotone viene assorbito se la sua energia è sufficiente a promuovere un elettrone dal suo livello energetico fondamentale ad un livello superiore. Alcuni fotoni della zona visibile dello spettro, avendo un energia corrispondente alla differenza di energia tra un livello occupato (da un elettrone) e un livello vuoto più elevato, vengono facilmente assorbiti dal metallo. rame I fotoni riflessi daranno la colorazione del rame metallico. Cu, Ag, Au appartengono tutti al I sottogruppo B e pertanto hanno la stessa configurazione elettronica esterna. argento oro
14
15 Colore dei metalli Cu Ag Au 3d 10 4s 1 4d 10 5s 1 5d 10 6s 1 I metalli come rame, oro e argento possono perdere elettroni anche dal penultimo strato. Per azione dei fotoni non si ha perdita di tali elettroni ma si può avere il passaggio di questi da un livello più basso ad un livello più alto. Dei tre, solo l argento ha gli elettroni interni che vengono trattenuti abbastanza fortemente, quindi non assorbe fotoni nella zona visibile dello spettro, cioè riflette tutta la luce visibile e appare bianco argenteo. ENERGIA DI LEGAME (energia necessaria per rompere i legami interatomici dei metalli) ~ 80 Kcal/mole ~ 70 Kcal/mole ~ 90 Kcal/mole Conclusione: il colore dei metalli è in stretta relazione con la energia di legame. I metalli con minore energia di legame interatomico, cioè quelli che trattengono fortemente gli elettroni interni, cioè i metalli meno polarizzabili, non possono assorbire fotoni della zona visibile dello spettro: essi riflettono la luce bianca e quindi hanno un colore argenteo.
16 Colore e salto degli elettroni tra gli orbitali Le transizioni elettroniche (transizioni intraatomiche) sono importanti soprattutto nel caso dei metalli di transizione, che hanno gli orbitali d parzialmente riempiti, e i cui ioni (idratati) sono generalmente colorati. Colori degli ioni idratati dei metalli della I a serie di transizione Catione Numero di elettroni d Numero di elettroni d spaiati Colore K + Ca 2+ Sc Incolore Ti Rosa V Verde Cr Violetto Cr Azzurro Mn Rosa pallido Fe Violetto pallido Fe Verde Co 2+ Ni Rosa Verde Cu Azzurro Cu + Zn 2+ Ga Incolore Quindi gli ioni che hanno uno strato elettronico completo (K +, Ca 2+, Sc 3+, che hanno 8 elettroni esterni e Cu +, Zn 2+, Ga 3+, che invece ne hanno 18) sono incolori. Gli altri ioni aventi orbitali d parzialmente occupati, in soluzione acquosa sono variamente colorati, secondo il numero degli elettroni d. Il colore degli ioni può cambiare quando la distribuzione degli e - negli orbitali d viene perturbata dalla presenza di un legante diverso: es. Ni(H 2 O) 6 2+ è verde, Ni(NH 3 ) 4 2+ è blu, Ni(CN) 4 2- è bruno.
17
18 IL COLORE DEI COMPOSTI INORGANICI Composti nettamente ionici: dipende dal colore dei singoli ioni costituenti. Generalmente sono bianchi a parte qualche caso particolare (es. FeSO 4, CuSO 4 ). Composti covalenti polari: il colore non deriva da una semplice combinazione dei colori degli ioni costituenti Transizioni intraatomiche Assorbimento energia luminosa Es. AgI (giallo) Ag (na 47) + I (na 53) Trasferimenti di carica (scambi di elettroni tra i diversi atomi o tra i diversi orbitali di una molecola) Ag + : incolore (4d 10 ) I - : incolore (5s 2 5p 6 ) E Ag + I - Ag : I E corrisponde ad una radiazione di λ compresa nello spettro visibile Altri esempi: CdS (giallo), K 2 CrO 4 (giallo), KMnO 4 (violetto) AgI assorbe questa radiazione e quindi risulta colorato KFe III [Fe II (CN) 6 ] KFe II [Fe III (CN) 6 ] Esacianoferrato di potassio o blu di prussia
19 Il colore di alcuni composti Il colore dipende a volte anche dallo stato di associazione degli atomi: es lo iodio allo stato solido è grigio, allo stato di vapore è violetto, le sue soluzioni alcoliche sono rosso-brune, quelle in cloroformio sono viola Composto Colore Composto Colore Composto Colore AgCl AgBr AgI Al(OH) 3 Bi(OH) 3 Bi 2 S 3 CoS (NH 4 ) 2 Co(CNS) 4 Cr(OH) 3 PbCrO 4 Bianco Giallo Giallo Bianco Bianco Nero Nero Azzurro Verde Giallo CuS [Cu(NH 3 ) 4 ] 2+ Fe(OH) 2 Fe(OH) 3 Fe(CNS) 3 Fe(CN) 4 6 Hg 2 Cl 2 Hg(OH) 2 HgO HgS Nero Azzurro Verde Rosso bruno Rosso Blu Bianco Bianco Giallo Nero MnO 2 MnS MnO 4 MnO 4 2 Ni ++ -dimetilgliossima NiS PbI 2 PbCl 2 Sb 2 S 3 Sb 2 S 5 ZnS Bruno Rosa Viola Verde Rosso-fragola Nero Giallo Bianco Arancio Arancio Bianco
20 Il colore dei composti e l analisi qualitativa In analisi qualitativa le reazioni in cui si formano composti colorati sono molto utilizzate per riconoscere i vari ioni. Un composto colorato è generalmente più caratteristico e facilmente riconoscibile di un composto incolore. I metalli alcalini ed alcalino-terrosi non danno reazioni cromatiche perché i loro ioni non possono subire né cambiamenti di stato di ossidazione (non possono dare colorazioni per trasferimenti di carica) né possono presentare transizioni interne come fanno gli ioni dei metalli di transizione. I pochi composti colorati degli ioni alcalini o alcalino-terrosi devono il loro colore all anione.
21 ANALISI PER VIA SECCA ANALISI DI EMISSIONE (Saggi alla fiamma) REAZIONI ALLO STATO FUSO (Saggi alle perle e su crogiolo)
22 EMISSIONE Negli atomi e negli ioni, gli elettroni possono occupare solo determinati livelli energetici. Nello stato fondamentale gli elettroni occupano il livello a minore energia. E 2 Se si fornisce energia sufficiente (riscaldamento, eccitazione elettrica ) si può verificare la promozione degli elettroni a livelli energetici superiori. E 1 E 1 E 2 E 0 Lo stato eccitato non è stabile e dura per tempi brevissimi, perché atomi e molecole tendono a ritornare quasi istantaneamente nello stato di partenza, restituendo all ambiente l energia assorbita (rilassamento). Si parla di emissione quando tale energia viene emessa sotto forma di energia radiante avente lunghezze d onda (λ) caratteristiche. La relazione fra l energia assorbita (ΔE) per passare allo stato eccitato e la λ del fotone emesso in fase di rilassamento radiante è descritta dalla legge di Plank: E 2 E 1 E 0 h. c λ 1 h. c λ 2 Δ E = hν = h c λ
23 EMISSIONE DI UN ATOMO DI SODIO Se un atomo di sodio assorbe l energia (termica) E 1, l elettrone dell orbitale 3s (stato elettronico fondamentale) può saltare nell orbitale 4p. Analogamente, l assorbimento delle energie E 2 o E 3 porta alle transizioni 3s 3p e 3p 3d. Quasi immediatamente l elettrone ritorna nell orbitale di partenza e l atomo emette una radiazione elettromagnetica la cui lunghezza d onda dipende dall energia assorbita. Se l atomo assorbe un energia maggiore dell energia di ionizzazione (E i ), l elettrone 3s viene espulso e l atomo si ionizza. E (ev) 5 E i = p 3 d + E 1 λ 1 = 330 nm + E 3 λ 3 = 819 nm E 4p = E 3d = p E 3p = E 2 λ 2 = 589 nm 0 3 s E 3s = 0.00
24 Analisi di emissione L analisi di emissione si basa sullo studio delle radiazioni emesse dalle sostanze opportunamente eccitate. La misura delle λ delle radiazioni emesse consente di individuare gli atomi che hanno generato tali radiazioni (analisi qualitativa). Ogni elemento è caratterizzato da uno specifico sistema di elettroni, distribuiti in ben precisi livelli di energia: perciò l emissione (conseguente a eccitazione elettronica) consiste in un sistema di radiazioni caratteristico per ciascun elemento. Se si raccolgono le radiazioni emesse su pellicola fotografica, mediante uno spettrografo, si ottiene uno spettrogramma, cioè l immagine dello spettro di righe (di emissione) caratteristico di ciascun elemento. Ogni riga dello spettro corrisponde a un salto elettronico; di conseguenza, dalla lunghezza d onda di tutte le righe di uno spettro si può risalire all elemento che le ha emesse mediante il confronto con gli spettri degli elementi puri. La quantità di energia necessaria a produrre l eccitazione degli atomi è relativamente alta, ne deriva che somministrando energia alle sostanze nell intento di indurvi l emissione, si provoca inevitabilmente ed ancor prima la dissociazione in atomi (dissociazione omolitica). L analisi di emissione può essere rivolta esclusivamente alla ricerca e alla determinazione dei singoli tipi di atomi, mentre non è possibile l analisi delle molecole come tali.
25 Spettri di emissione Il diagramma che riporta in ascissa le λ e in ordinata le corrispondenti intensità si definisce spettro di emissione delle sostanze. Spettri continui. (Solidi o liquidi incandescenti) Sono costituiti da radiazioni più o meno intense di qualsiasi lunghezza d onda (entro un certo intervallo di lunghezza d onda). Non presentano alcun interesse analitico. Spettri discontinui (sostanze gassose o vaporizzate) Sono costituiti da radiazioni più o meno intense comprendenti solo determinate lunghezze d onda. Spettro a bande sostanze gassose allo stato di molecole Bande di emissione dell azoto molecolare Spettro a righe sostanze gassose allo stato di atomi o ioni Righe di emissione dell atomo di idrogeno
26 Spettri di emissione Gli spettri di emissione variano al variare delle condizioni di eccitazione. Fissate le condizioni di eccitazione, diventano caratteristici delle differenti sostanze (spettri a righe). I livelli di ogni elemento sono definiti e limitati n limitato di righe spettrali Il n di righe risulta maggiore o minore, secondo l energia di eccitazione. Le diverse righe hanno un intensità relativa caratteristica che dipende dalla probabilità che il «salto» elettronico tra i 2 livelli abbia luogo. Entro certi limiti, l intensità è indipendente dall eccitazione.
27 Analisi di emissione e ionizzazione La ionizzazione rappresenta un inconveniente poiché riduce il n di atomi disponibili per l analisi. Dipende dal potenziale di ionizzazione dell atomo. Se l energia di eccitazione è molto elevata può accadere che si abbia ionizzazione. I livelli energetici dello ione risultano modificati emissione di radiazioni con ν (λ) differenti Lo spettro dell atomo ionizzato è molto diverso da quello dell atomo da cui ha avuto origine, ma può avere analogia con quello dell atomo neutro con na inferiore di un unità
28 Analisi alla fiamma I saggi alla fiamma rappresentano un esempio rudimentale di analisi di emissione. Il metodo più semplice di eccitazione delle sostanze è il riscaldamento con la fiamma: l apporto di energia, in tal caso, è piuttosto limitato, per cui solo poche sostanze (metalli o ioni alcalini e alcalino-terrosi) danno i rispettivi spettri. Gli spettri ottenuti sono molto semplici perché costituiti da poche righe caratteristiche, che rientrano nella porzione visibili dello spettro, quindi facilmente riconoscibili. L esame dello spettro costituisce per alcuni elementi il saggio di riconoscimento più sensibile e specifico. Quando l eccitazione è eseguita alla fiamma e la radiazione emessa è monocromatica (sodio, potassio, litio ) è sufficiente l osservazione del colore che assume la fiamma stessa Il saggio alla fiamma permette di evidenziare la presenza di certi metalli in un campione ridotto in polvere sottile. Poiché gli effetti più evidenti si ottengono con i cloruri dei metalli, la sostanza deve essere umettata in acido cloridrico prima di essere portata alla fiamma. sodio bario potassio calcio litio stronzio rame
29 RIGHE DI EMISSIONE DI ALCUNI ELEMENTI Violetto Blu Verde Giallo Arancio Rosso Ca Li K Na Sr λ, nm
30 Lampada (becco, bruciatore) Bunsen
31 Lampada bunsen Nella fiamma del bunsen esistono diverse zone distinte per luminosità e temperatura; una zona centrale detta cono freddo, costituita da gas incombusto, una zona intermedia molto luminosa detta zona riducente, in cui avviene una combustione parziale, e una esterna molto calda e poco luminosa detta zona ossidante, in cui si completa la combustione. Zona ossidante superiore Zona riducente superiore Zona ossidante inferiore Zona riducente inferiore Cono freddo Nella zone ossidante e riducente si distinguono la parte inferiore a minore temperatura e superiore a maggiore temperatura.
32 Analisi alla fiamma COLORE ELEMENTO Giallo Na (persistente nasconde quella degli altri elementi) violetto rosso rosso arancio verde K (poco persistente, dietro al vetro al cobalto: rosso carminio) Li (immediata ma poco persistente), Sr (sprazzo iniziale arancio intenso, la colorazione rossa compare in ritardo ma molto persistente) Ca (a sprazzi) Cu (immediata ma poco persistente), Ba (compare in ritardo, persistente)
33 SPETTRO DI TRASMITTANZA DEL FILTRO OTTICO AL VETRO DI COBALTO E RIGHE DI EMISSIONE DI ALCUNI ELEMENTI I 0 I x Violetto Blu Verde Giallo Arancio Rosso I 0 = intensità radiazione incidente I x = intensità radiazione trasmessa Ca Li K Na , , T = I x I 0 0<T<1 % TRASMITTANZA I x = 0 T = 0 I x = I 0 T = λ, nm
34 Co, Ni, Fe, Cu, Mn e Cr PERLE AL BORACE Na 2 B 4 O H 2 O calore Na 2 B 4 O H 2 O Na 2 B 4 O 7. 10H 2 O Sodio tetraborato decaidrato Il borace ha la proprietà di trasformarsi, alla fiamma del bunsen, in una massa vetrosa, incolore e trasparente perla che allo stato fuso scioglie gli ossidi di certi metalli assumendo colorazioni caratteristiche. Il borace dapprima rigonfia perdendo l acqua di cristallizzazione ( effetto popcorn ) Na 2 B 4 O 7 calore 2 NaBO 2 + B 2 O 3 e poi, per forte e prolungato riscaldamento, fonde dando origine ad una perla vetrosa, incolore e trasparente di metaborato di sodio (NaBO 2 ) e anidride borica (B 2 O 3 ). MeCO 3 Es: CuCO 3 MeO + CO 2 CuO + CO 2 I sali di alcuni metalli subiscono decomposizione termica con formazione dei corrispondenti ossidi basici. MeO + B 2 O 3 Es: CuO + B 2 O 3 Me(BO 2 ) 2 Cu(BO 2 ) 2 L anidride borica reagendo con gli ossidi metallici produce i metaborati dei rispettivi cationi. Me(BO 2 ) 2 + 2NaBO 2 MeNa 2 (BO 2 ) 4 Es: Cu(BO 2 ) 2 + 2NaBO 2 CuNa 2 (BO 2 ) 4 I metaborati dei metalli reagendo con il metaborato sodico formano sali doppi con colorazione caratteristica.
35 PERLE AL BORACE COLORAZIONE DELLA PERLA Fiamma ossidante Fiamma riducente a caldo a freddo a caldo a freddo Cobalto blu blu blu blu Cromo giallo scura verde verde verde Ferro giallo bruna gialla verde verde Nichel violacea rosso bruna grigia grigia Rame verde azzurra incolore rosso opaco Manganese violetta viola incolore incolore N.B. Il diverso colore della perla a fiamma ossidante e a fiamma riducente è dovuto alla formazione di metaborati corrispondenti a diversi stati di ossidazione del metallo [es. Fe (III) e Fe (II)]
36 PERLE AL BORACE La colorazione impartita dal cobalto è la più intensa e specifica e maschera tutte le altre. I colori che si osservano per uno stesso metallo possono variare a seconda delle condizioni operative in cui è stato effettuato il saggio. Ad esempio, il rame in fiamma ossidante dà metaborato di rame (II), Cu(BO 2 ) 2, di colore verde-blu: CuO + B 2 O 3 Cu(BO 2 ) 2 Per contro, in fiamma riducente il rame può essere ridotto dalle particelle carboniose della fiamma a metaborato di rame (I), CuBO 2, incolore, o a rame elementare, Cu, rosso opaco: 2Cu(BO2)2 + 2NaBO2 + C 2CuBO2 + Na2B4O7 + CO(g) 2Cu(BO2)2 + 4NaBO2 + C 2Cu(s) + 2Na2B4O7 + CO(g) Anche il ferro si presenterà con colori diversi a seconda del suo stato di ossidazione (F 3+ e Fe 2+ )
37 Mn e Cr SAGGIO SU CROGIOLO (Na 2 CO 3 -KNO 3 in rapporto 3:1) In una capsula di porcellana si pone una piccola quantità della sostanza da analizzare con una miscela formata da 1 parte di KNO 3 e 3 parti di Na 2 CO 3 e si riscalda. KNO 3 KNO 2 + 1/2O 2 Il nitrato si decompone con liberazione di ossigeno MnCO 3 MnO + CO 2 Cr 2 (SO 4 ) 3 Cr 2 O 3 + 3SO 3 I sali di Mn e Cr si decompongono con formazione dei relativi ossidi MnO + O 2 2Cr 2 O 3 + 3O 2 MnO 3 4CrO 3 Gli ossidi di Mn e Cr vengono ossidati alle corrispondenti anidridi MnO 3 + Na 2 CO 3 Na 2 MnO 4 (verde) + CO 2 CrO 3 + Na 2 CO 3 Na 2 CrO 4 + CO 2 (giallo) Le anidridi reagiscono con il carbonato sodico per formare il manganato sodico (verde) e il cromato sodico (giallo)
38 Elemento Perle al borace Fiamma ossidante Na 2 B 4 O 7. 10H 2 O Sodio tetraborato decaidrato Cobalto Cromo Ferro Nichel Rame Manganese a caldo Azzurra Giallo-rossiccia Rosso-gialla Violacea Verde Violetto a freddo Azzurra Verde Gialla o incolore Rosso-bruna Verde-azzurra Violetto-rossa Saggio su crogiolo (Na 2 CO 3 -KNO 3 in rapporto 3:1) Cromo giallo Manganese verde
39 COLORE ELEMENTI OSSERVAZIONI GIALLO nm VIOLETTO violetto 404 nm rosso: nm Na K La colorazione compare anche alla base della fiamma ed è molto persistente: nasconde quella del K, Li, Ca, ecc Immediata alla base della fiamma: se è presente Na bisogna osservare la fiamma attraverso un vetrino al cobalto: la colorazione del Na è assorbita e rimane quella del K rosso porpora. ROSSO ARANCIO nm ROSSO VIVO 671 nm ROSSO SCARLATTO nm VERDE PALLIDO nm VERDE BOTTIGLIA Ca Li Sr Ba Cu Colorazione a sprazzi appena si porta alla fiamma. Mai persistente. Grigio-verde attraverso il vetrino al cobalto. Colorazione immediata e persistente alla base della fiamma. Può confondersi col K attraverso il vetrino al cobalto. Specifico in assenza di Sr. Sprazzo iniziale (arancio) e colorazione persistente più tardi. Specifico in assenza di Li. La colorazione compare in ritardo nella sola zona ossidante ed è molto persistente. (Differenza dal Cu). Immediata alla base della fiamma. Il CuCl 2 dà una fiamma azzurro-celeste e poi verde.
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO
 RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
Lo Spettro Elettromagnetico
 Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Spettroscopia. Spettroscopia
 Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Composti di coordinazione
 Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Spettroscopia. 05/06/14 SPET.doc 0
 Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
La Fisica Applicata ai Beni Culturali: l'effetto fotoelettrico per l'analisi non distruttiva di campioni di interesse storico-artistico
 La Fisica Applicata ai Beni Culturali: l'effetto fotoelettrico per l'analisi non distruttiva di campioni di interesse storico-artistico Giovanni BUCCOLIERI e-mail: [email protected] Università
La Fisica Applicata ai Beni Culturali: l'effetto fotoelettrico per l'analisi non distruttiva di campioni di interesse storico-artistico Giovanni BUCCOLIERI e-mail: [email protected] Università
catastrofe ultravioletta
 Fisica moderna Radiazione termica La radiazione termica è l insieme di onde elettromagnetiche che ogni corpo emette per effetto della sua temperatura Un corpo nero è un corpo che assorbe completamente
Fisica moderna Radiazione termica La radiazione termica è l insieme di onde elettromagnetiche che ogni corpo emette per effetto della sua temperatura Un corpo nero è un corpo che assorbe completamente
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
Appunti di Stechiometria per Chimica Numero d ossidazione
 Appunti di Stechiometria per Chimica Numero d ossidazione Si definisce numero d ossidazione la carica complessiva di un atomo (differenza tra protoni ed elettroni dell atomo), ottenuta assegnando, solo
Appunti di Stechiometria per Chimica Numero d ossidazione Si definisce numero d ossidazione la carica complessiva di un atomo (differenza tra protoni ed elettroni dell atomo), ottenuta assegnando, solo
ANALISI CHIMICA QUALITATIVA
 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ASSORBIMENTO UV-VIS. Atomo
 ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
Come vediamo. La luce: aspetti fisici. Cos è la luce? Concetti fondamentali:
 La luce in fisica La luce: aspetti fisici Cos è la luce? Concetti fondamentali: - velocità, ampiezza, lunghezza d onda - assorbimento - riflessione -rifrazione - diffrazione - indice di rifrazione - temperatura
La luce in fisica La luce: aspetti fisici Cos è la luce? Concetti fondamentali: - velocità, ampiezza, lunghezza d onda - assorbimento - riflessione -rifrazione - diffrazione - indice di rifrazione - temperatura
Fe(OH) 3. Mn(OH) 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI. Dr. Francesco Musiani
 REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
Reazioni di ossido-riduzione
 Reazioni di ossido-riduzione Secondo la teoria di Bronsted-Lowry le reazioni acido-base possono essere considerate processi di scambio protonico HCl + H 2 O Cl - + H 3 O + Cl H O H H Cl H O H H In questi
Reazioni di ossido-riduzione Secondo la teoria di Bronsted-Lowry le reazioni acido-base possono essere considerate processi di scambio protonico HCl + H 2 O Cl - + H 3 O + Cl H O H H Cl H O H H In questi
SPETTROSCOPIA UV-VIS LEZIONE 9
 SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
LASER. Light Amplification by Stimulated Emission of Radiation. Introduzione. Assorbimento, emissione spontanea, emissione stimolata
 LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
SPETTROSCOPIA ATOMICA
 SPETTROSCOPIA ATOMICA È la tecnica più usata per l analisi (specialmente quantitativa) degli elementi in tracce, in tutte le matrici. Il campione viene atomizzato e gli atomi presenti in esso vengono riconosciuti
SPETTROSCOPIA ATOMICA È la tecnica più usata per l analisi (specialmente quantitativa) degli elementi in tracce, in tutte le matrici. Il campione viene atomizzato e gli atomi presenti in esso vengono riconosciuti
STRUTTURA ATOMICA. Per lo studio della struttura dell atomo ci si avvale della Spettroscopia.
 STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO
 SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
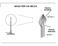 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
 ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
FISICA QUANTISTICA LIMITI AL MODELLO ATOMICO DI RUTHERFORD. e - Per spiegare la disposizione degli elettroni nell atomo (STRUTTURA ELETTRONICA)
 LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
ESERCIZI. 1. Completa le seguenti reazioni e, se necessario, bilanciale: b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore!
 ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
Spettroscopia di assorbimento UV-Vis
 Spettroscopia di assorbimento UV-Vis Metodi spettroscopici La spettroscopia studia i fenomeni alla base delle interazioni della radiazione con la materia Le tecniche spettroscopiche sono tutte quelle tecniche
Spettroscopia di assorbimento UV-Vis Metodi spettroscopici La spettroscopia studia i fenomeni alla base delle interazioni della radiazione con la materia Le tecniche spettroscopiche sono tutte quelle tecniche
FISICA delle APPARECCHIATURE per RADIOTERAPIA
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Trasmissione di calore per radiazione
 Trasmissione di calore per radiazione Sia la conduzione che la convezione, per poter avvenire, presuppongono l esistenza di un mezzo materiale. Esiste una terza modalità di trasmissione del calore: la
Trasmissione di calore per radiazione Sia la conduzione che la convezione, per poter avvenire, presuppongono l esistenza di un mezzo materiale. Esiste una terza modalità di trasmissione del calore: la
Fenomeni quantistici
 Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
PRINCIPALI CLASSI DI COMPOSTI INORGANICI
 PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI
 PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali 1 Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali 1 Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
Reazioni ed Equazioni Chimiche. Coefficienti stechiometrici :
 Reazioni ed Equazioni Chimiche Reazione chimica Trasformazione di una o più sostanze (REAGENTI) in una o più sostanze (PRODOTTI) Equazioni chimiche Traduzione scritta delle reazioni chimiche Per scrivere
Reazioni ed Equazioni Chimiche Reazione chimica Trasformazione di una o più sostanze (REAGENTI) in una o più sostanze (PRODOTTI) Equazioni chimiche Traduzione scritta delle reazioni chimiche Per scrivere
La spettrofotometria è una tecnica analitica, qualitativa e quantitativa e permette il riconoscimento e la quantizzazione di una sostanza in base al
 SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Le onde elettromagnetiche
 Campi elettrici variabili... Proprietà delle onde elettromagnetiche L intuizione di Maxwell (1831-1879) Faraday ed Henry misero in evidenza che un campo magnetico variabile genera un campo elettrico indotto.
Campi elettrici variabili... Proprietà delle onde elettromagnetiche L intuizione di Maxwell (1831-1879) Faraday ed Henry misero in evidenza che un campo magnetico variabile genera un campo elettrico indotto.
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA
 LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
Reazioni di ossido-riduzione
 Reazioni di ossido-riduzione Con reazioni di ossido riduzione si intende una vasta classe di reazioni che implicano un trasferimento elettronico più o meno evidente. Ad esempio il trasferimento elettronico
Reazioni di ossido-riduzione Con reazioni di ossido riduzione si intende una vasta classe di reazioni che implicano un trasferimento elettronico più o meno evidente. Ad esempio il trasferimento elettronico
ANALISI CHIMICA ANALISI QUANTITATIVA ANALISI QUALITATIVA ANALISI ORGANICA. Riconoscimento di sostanze organiche. ANALISI INORGANICA
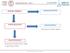 ANALISI CHIMICA ANALISI QUANTITATIVA ANALISI QUALITATIVA ANALISI ORGANICA Riconoscimento di sostanze organiche. ANALISI INORGANICA Riconoscimento di sostanze ioniche e solubili in acqua (cationi ed anioni).
ANALISI CHIMICA ANALISI QUANTITATIVA ANALISI QUALITATIVA ANALISI ORGANICA Riconoscimento di sostanze organiche. ANALISI INORGANICA Riconoscimento di sostanze ioniche e solubili in acqua (cationi ed anioni).
Problema 1 Mg + 2HCl H 2 + MgCl 2. di Mg 1 Mg 1 H 2 quindi 0,823 moli di H 2 di H 2
 REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
ELETTROLISI TRASFORMAZIONE DI ENERGIA ELETTRICA IN ENERGIA CHIMICA
 ELETTROLISI TRASFORMAZIONE DI ENERGIA ELETTRICA IN ENERGIA CHIMICA L elettrolisi è una reazione non spontanea ( G>0) di ossidoriduzione provocata dal passaggio di corrente tra due elettrodi immersi in
ELETTROLISI TRASFORMAZIONE DI ENERGIA ELETTRICA IN ENERGIA CHIMICA L elettrolisi è una reazione non spontanea ( G>0) di ossidoriduzione provocata dal passaggio di corrente tra due elettrodi immersi in
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Trasformazione di una o più sostanze (REAGENTI) in una o più sostanze (PRODOTTI)
 Reazioni ed Equazioni Chimiche Reazione chimica Trasformazione di una o più sostanze (REAGENTI) in una o più sostanze (PRODOTTI) Equazioni chimiche Traduzione scritta delle reazioni chimiche Per scrivere
Reazioni ed Equazioni Chimiche Reazione chimica Trasformazione di una o più sostanze (REAGENTI) in una o più sostanze (PRODOTTI) Equazioni chimiche Traduzione scritta delle reazioni chimiche Per scrivere
2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una
 Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Test di Matematica di base e Logica
 Università degli Studi di Perugia. Facoltà di Scienze MM.FF.NN. Test di Autovalutazione per l accesso al corso di laurea triennale in chimica 1 ottobre 2010 Test di Matematica di base e Logica 1) Un triangolo
Università degli Studi di Perugia. Facoltà di Scienze MM.FF.NN. Test di Autovalutazione per l accesso al corso di laurea triennale in chimica 1 ottobre 2010 Test di Matematica di base e Logica 1) Un triangolo
Esempi di calcolo del numero di ossidazione
 ESERCITAZIONE 3 1 Esempi di calcolo del numero di ossidazione 1) Calcolare il numero di ossidazione del Mn nel KMnO 4. K n.o. +1 O n.o. 2 La molecola è neutra per cui: n.o. Mn + n.o. K + 4 n.o. O = 0 Mn
ESERCITAZIONE 3 1 Esempi di calcolo del numero di ossidazione 1) Calcolare il numero di ossidazione del Mn nel KMnO 4. K n.o. +1 O n.o. 2 La molecola è neutra per cui: n.o. Mn + n.o. K + 4 n.o. O = 0 Mn
ANALISI CHIMICHE PER I BENI CULTURALI
 ANALISI CHIMICHE PER I BENI CULTURALI Nicola Ludwig ricevimento: in via Noto giovedì dopo lezione [email protected] Istituto di Fisica Generale Applicata, via Celoria 16 Programma Obbiettivo del corso
ANALISI CHIMICHE PER I BENI CULTURALI Nicola Ludwig ricevimento: in via Noto giovedì dopo lezione [email protected] Istituto di Fisica Generale Applicata, via Celoria 16 Programma Obbiettivo del corso
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
La reazione da bilanciare è quindi: Cu + HNO 3 CuNO 3 + NO. Le due semireazioni da bilanciare saranno: HNO 3 NO (1) Cu CuNO 3 (2)
 Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
I Colori sono gli Atti della Luce. (Goethe)
 I Colori sono gli Atti della Luce (Goethe) tutto cominciò con JSAC NEWTON 1600 e rotti DISTINZIONE TRA: MONDO FISICO dove tutto è oggettivo e misurabile MONDO DELLA PERCEZIONE dove tutto è soggettivo
I Colori sono gli Atti della Luce (Goethe) tutto cominciò con JSAC NEWTON 1600 e rotti DISTINZIONE TRA: MONDO FISICO dove tutto è oggettivo e misurabile MONDO DELLA PERCEZIONE dove tutto è soggettivo
Reazioni Redox. Riferimento Elemento libero, cioè singolo atomo, o combinato con se stesso (Na, O 2, Cl 2, O 3 ) Ossigeno -2.
 Reazioni Redox Ad ogni elemento di un dato composto si attribuisce un numero di ossidazione, N.O., corrispondente ad una carica elettrica fittizia, multiplo, positivo o negativo, della carica elettronica.
Reazioni Redox Ad ogni elemento di un dato composto si attribuisce un numero di ossidazione, N.O., corrispondente ad una carica elettrica fittizia, multiplo, positivo o negativo, della carica elettronica.
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
