UNIVERSITA DEGLI STUDI DI VERONA
|
|
|
- Leone Beretta
- 8 anni fa
- Visualizzazioni
Transcript
1 UNIVERSITA DEGLI STUDI DI VERONA FACOLTA DI SCIENZE MM FF NN CORSO DI LAUREA IN BIOTECNOLOGIE AGROINDUSTRIALI TESI DI LAUREA LE BASI STRUTTURALI DELLA FOTOSINTESI: DETERMINAZIONE DELL ORIENTAMENTO DEI CROMOFORI NELLA PROTEINA ANTENNA CP29 Relatore: Correlatore: Prof. ROBERTO BASSI Dott. MASSIMO CRIMI Laureando: ROBERTO SIMONETTO ANNO ACCADEMICO
2
3 Alla mia famiglia
4
5 RINGRAZIAMENTI Si desidera ringraziare per la preziosa collaborazione: il Prof. Roberto Bassi, presso il cui laboratorio ho svolto il lavoro presentato in questa tesi, il Dott. Massimo Crimi, e tutte le persone che hanno lavorato al mio fianco: Paolo, Daniela, MG, Aldo, Roberta, Dorianna, Gianluca e Gianfelice; il Dott. Jaques Breton per il suo prezioso contributo e per l ospitalità e la cordialità dimostratami; un ringraziamento particolare va a Claudio per la critica discussione sugli argomenti trattati in questo lavoro ed a Diana per l amicizia e la sua profonda dedizione al laboratorio. Infine il ringraziamento più grande va alla mia famiglia e ai miei amici che mi hanno consentito di lavorare liberamente in un ambiente sereno e che mi hanno sostenuto per tutti questi cinque anni, ringrazio pertanto: Germana, Luigi, Enrico, Carla, Renato, Claudio V, Salvatore, Claudio G, Roberta, Mara, Lorenza, Fabrizia e tutti gli altri amici, a cui devo moltissimo. Grazie Alessandra per il tuo amore.
6
7 ABBREVIAZIONI aa aminoacido BBY membrane tilacoidali arricchite in componenti del PSII BChl Batterioclorofilla CD dicroismo circolare Chl clorofilla DCCD dicicloesilcarbodiimide Deriphat-160 Lauril, b-d imminopropionidato DM dodecilmaltoside DMSO dimetilsolfossido DTT ditiotreitolo ELFE elettroforesi elettroendosmotica HPLC cromatografia liquida ad alta risoluzione IEF isoelettrofocalizzazione IPTG isopropil tiogalactoside LD dicroismo lineare LDS litiododecilsolfato LHCI complesso antenna maggiore del PSII LHCII complesso antenna maggiore del PSII NAT proteina nativa estratta dai tilacoidi NPQ smorzamento non fotochimico della fluorescenza OD densità ottica o assorbanza OGP octilglucopiranoside PAGE elettroforesi su gel di acrilammide PDB Protein Data Bank PS (I oppure II) fotosistema (primo o secondo) SDS sodiododecilsolfato Triton (X-100) polietilenglicole terzioctifeniletere VMT versore del momento associato alla transizione elettronica WT wild type,proteina ricostituita a partire dal gene originario, non mutato
8
9 SOMMARIO A. INTRODUZIONE...1 I. GENERALITA' FOTOSINTESI 3 I.1 INTRODUZIONE 3 I.2 I PIGMENTI FOTOSINTETICI 4 I.3 IL CLOROPLASTO 7 I.4 LA CATENA DI TRASPORTO ELETTRONICA : COMPONENTI ED ORGANIZZAZIONE FUNZIONALE 9 II. STRUTTURA ED ORGANIZZAZIONE FUNZIONALE DELLE MEMBRANE TILACOIDALI 12 II.1 FOTOSISTEMA I 12 II.2 FOTOSISTEMA II 14 III. SISTEMI LIGHT-HARVESTING IN NATURA 15 III.1 INTRODUZIONE 15 III.2 SISTEMI LIGHT-HARVESTING IN PROCARIOTI 16 III.3 IL SISTEMA ANTENNA DEL PSI (LHCI) 20 IV. IL SISTEMA ANTENNA DEL PSII (LHCII) 22 IV.1 COMPLESSO MAGGIORE LHCII 22 IV.2 OMOLOGIA ENTRO LA FAMIGLIA DI PROTEINE CAB 25 IV.3 ANTENNE MINORI 27 V. IL TRASFERIMENTO DELL'ENERGIA 30 V.1 INTRODUZIONE 30 V.2 ACCOPPIAMENTO FORTE. 33 V.3 ACCOPPIAMENTO DEBOLE 34 V.4 TRASFERIMENTO DI ENERGIA DI SCAMBIO 35 V.5 TRASFERIMENTI DI ENERGIA REVERSIBILI 36 V.6 MIGRAZIONE ED INTRAPPOLAMENTO 36 B. SCOPO DELLA TESI...39 I. PREMESSA 41 II. SCOPO DELLA TESI 43 III. PERCHE USARE CP29 AL POSTO DI LHCII 43 C. MATERIALI E METODI...45 I. BIOCHIMICA 47 I.1 ELETTROFORESI 47 I.2 CROMATOGRAFIA SU COLONNA A SCAMBIO ANIONICO 53 I.3 ESTRAZIONE DEI PIGMENTI CON ACETONE 80% 54 I.4 ESTRAZIONE DEI CAROTENOIDI TRAMITE SAPONIFICAZIONE A FREDDO 55 I.5 PURIFICAZIONE E ANALISI DEI PIGMENTI 56
10 I.6 ULTRACENTRIFUGAZIONE IN GRADIENTE 58 I.7 PROCEDURA DI RICOSTITUZIONE 59 II. SPETTROSCOPIA 60 II.1 ASSORBIMENTO 60 II.2 FLUORESCENZA 60 II.3 DICROISMO CIRCOLARE 61 II.4 STABILITA' DELLE PROTEINE MUTANTI 61 II.5 DICROISMO LINEARE 61 III. SOFTWARE 63 III.1 MAXSPROUT 63 III.2 SWISS-PDB VIEWER III.3 PROGRAMMA PER IL CALCOLO GEOMETRICO SULLE STRUTTURE PROTEICHE 63 III.4 PROGRAMMA PER LA NORMALIZZAZIONE DEGLI SPETTRI DIFFERENZIALI DI ABS E LD 64 D. RISULTATI...69 I. STABILITA' DELLE PROTEINE MUTANTI 71 I.1 MUTANTI 71 I.2 STABILITA' DEI COMPLESSI A 4 C E TEMPERATURA AMBIENTE 72 I.3 VALUTAZIONE DELLA STABILITA' DI OGNI PROTEINA MUTANTE 73 II. COSTRUZIONE DEL MODELLO 79 II.1 DATI DISPONIBILI 79 II.2 RICOSTRUZIONE RESIDUI LATERALI CON MAXSPROUT 79 II.3 MUTAZIONE RESIDUI SU SEQUENZA CP29 80 II.4 REINSERIMENTO ETEROATOMI NEL PDB 82 II.5 VERIFICA DELLA CORRETTA COORDINAZIONE DELLE CLOROFILLE 83 III. STRATEGIA IMPIEGATA 86 III.1 INFORMAZIONI NECESSARIE ALLA DETERMINAZIONE DEI VMT DI CHL ALL'INTERNO DI UNA STRUTTURA 86 III.2 LIMITI DELLA STRUTTURA ESISTENTE DI LHCII 87 III.3 INFORMAZIONI CHE E' IN GRADO DI FORNIRE IL DICROISMO LINEARE 88 III.4 STRATEGIA IMPIEGATA NEL CALCOLO 89 IV. DATI SPETTROSCOPICI DEI MUTANTI 90 IV.1 NORMALIZZAZIONE DEGLI SPETTRI DI ASSORBIMENTO 90 IV.2 NORMALIZZAZIONE DEGLI SPETTRI DI DICROISMO LINEARE 94 IV.3 NORMALIZZAZIONE TRA LD E ABS 94 V. CALCOLO DEGLI ANGOLI TRA I VMT E LA NORMALE ALLA MEMBRANA 96 V.1 RELAZIONE TRA ABS E LD 96 V.2 RIDUZIONE DELLE SOLUZIONI POSSIBILI SULLA BASE DELLA STRUTTURA PROTEICA 97 V.3 RISULTATI 98
11 VI. CALCOLO GEOMETRICO DEI POSSIBILI VMT 105 VI.1 DATI CRISTALLOGRAFICI 105 VI.2 RISULTATI 106 VI.3 NORMALE DEL PIANO DELLA MEMBRANA 109 VII. IDENTIFICAZIONE DEL FATTORE F N 112 VIII. MOMENTI DI TRANSIZIONE DELLE XANTOFILLE IN CP VIII.1 RELAZIONE FRA LE XANTOFILLE E LE MOLECOLE DI CLOROFILLA 115 IX. RIEPILOGO RISULTATI VMT 118 E. DISCUSSIONE I. ANALISI DEI DATI SPETTROSCOPICI 123 II. APPROCCIO CONGIUNTO AL PROBLEMA DELL'ORIENTAMENTO DEI VMT: MODELLO STRUTTURALE ED ANALISI LD 125 III. RISULTATI 126 IV. LIMITAZIONI 127 V. PROSPETTIVE 128 APPENDICE A Basi teoriche e tecnica del dicroismo lineare I. LUCE POLARIZZATA 131 I.1 ASSORBIMENTO DELLA LUCE DA PARTE DI MOLECOLE [30] 131 II. DICROISMO LINEARE 133 II.1 LD DI ASSORBIMENTO 134 III. ORIENTAMENTO DEL CAMPIONE 135 III.1 COMPRESSIONE GEL DI POLIACRILAMIDE 135
12 INDICE DELLE FIGURE Figura 1 Struttura delle clorofilla a, b e Batterioclorofilla...4 Figura 2 Struttura di alcuni carotenoidi primari...6 Figura 3 Il cloroplasto...7 Figura 4 Rappresentazione schematica dell'organizzazione dei tilacoidi...8 Figura 5 Organizzazione funzionale della membrana tilacoidale...9 Figura 6 Schema Z di Bendall e Hill Figura 7 Modello per l'organizzazione spaziale del PSI Figura 8 Modello per l'organizzazione del core del PSII Figura 9 Struttura del pirrolo lineare delle biline Figura 10 Rappresentazione dimero αβ di LH2 di R. acidophila Figura 11 Rappresentazione della struttura cristallografica di A. carterae Figura 12 Modello per l'organizzazione sovramolecolare del PSI Figura 13 Rappresentazione schematica della struttura di LHCII Figura 14 Rappresentazione struttura tridimensionale di LHCII Figura 15 Modello di arrangiamento delle antenne minori nel PSII Figura 16 Modello schematico di struttura per CP Figura 17 Modello schematico di struttura per CP Figura 18 Modello schematico della struttura di CP Figura 19 Rappresentazione schematica dei contributi al trasferimento dell'energia di eccitazione di Coulomb e di scambio Figura 20 CP29 come appare nel programma R3D Figura 21 Normalizzazione degli spettri differenziali di ABS e LD con la procedura Figura 22 Dati disponibili di LHCII: Cα, struttura dei tetrapirroli e delle xantofille Figura 23 Rappresentazione della struttura di LHCII dopo la ricostruzione dei residui laterali con MAXPROUT Figura 24 Rappresentazione di CP29 ottenuta dopo elaborazione della sequenza Figura 25 Modello di struttura di CP29 in cui sono stati reinseriti i riferimenti ai pigmenti Figura 26 Rappresentazione del modello strutturale completo di CP Figura 27 Posizione dei residui implicati nella coordinazione delle 8 Chl di CP Figura 28 Momento della transizione QY della Chl a secondo Fragata Figura 29 Possibili siti di aggancio della catena fitilica Figura 30 Disposizione dei fitoli nella truttura di LHII di R. acidophila Figura 31 Posizione della Chl A3 nella struttura proteica Figura 32 Programma per il calcolo dei versori geometrici a partire dalla struttura Figura 33 Sovrapposizione dei gruppi rappresentati da Lut1-Chl a2:lut2-chl a5: Figura 34 Complanarità fra piani degli anelli tetrapirrolici e l'asse delle xantofille Figura 35 Posizione dei punti di connessione dei fitoli agli anelli tetrapirrolici Figura 36 Geometria usata per il calcolo degli angoli di orientazione Figura 37 Schema per l'allineamento di membrane e di particelle cilindriche Figura 38 Rappresentazione dell'azione della compressione sul cilindro di gel Tabella 1 Nomenclatura genica delle proteine del fotosistema I e II Tabella 2 Composizione in pigmenti delle proteine del PSI... 20
13 Tabella 3 Allineamento delle sequenze dedotte dai cdna delle Lhcb...27 Tabella 4 Distanza critica di Förster R0, efficienza di fluorescenza in vivo φ D e tempo di vita di fluorescenza τ1 D...36 Tabella 5 Contenuto in pigmenti del CP29 wt e dei complessi mutati...73 Tabella 6 Riepilogo stabilità proteine ricostituite...79 Tabella 7 Allineamento di sequenza da Mais delle eliche di LHCII utilizzato nella costruzione del modello di CP Tabella 8 Riepilogo risultati della normalizzazione Tabella 9 Tavola riepilogativa dei risultati del calcolo dei possibili VMT dal modello strutturale di CP29 (a) Tabella 10 Tavola riepilogativa dei risultati del calcolo dei possibili VMT dal modello strutturale di CP29 (b) Tabella 11 Calcolo degli angoli fra i VMT possibili e la normale alla membrana; utilizzati la prima serie di VMT Tabella 12 Calcolo degli angoli fra i VMT possibili e la normale alla membrana; utilizzati la seconda serie di VMT Tabella 13 Risultati calcolo FN sulla prima serie di VMT Tabella 14 Risultati calcolo FN sulla seconda serie di VMT Tabella 15 Determinazione del fattore di normalizzazione Tabella 16 Ambiguità sul VMT della Chl A2 e della chl A Tabella 17 Versori delle due xantofille nella struttura di CP Tabella 18 Confronto fra VMT possibili delle Chl A2 e A5, e VMT delle xantofille Tabella 19 Riepilogo risultati VMT dei cromofori in CP Spettro 1 Assorbimento pigmenti fotosintetici...5 Spettro 2 Prova stabilità CP29 wt...74 Spettro 3 Prova stabilità proteina CP29 H216F...75 Spettro 4 Prova stabilità proteina CP29 Q230L...75 Spettro 5 Prova stabilità proteina CP29 E111V^R218L...76 Spettro 6 Prova stabilità proteina CP29 H114F...76 Spettro 7 Prova stabilità proteina CP29 E174V...77 Spettro 8 Prova stabilità proteina CP29 E166V...77 Spettro 9 Prova stabilità proteina CP29 H245L...78 Spettro 10 Riepilogo stabilità mutazioni...78 Spettro 11 Assorbimento del CP29 wild type...91 Spettro 12 Normalizzazione effettuata sui massimi di assorbimento dei campioni...92 Spettro 13 Normalizzazione effettuata per deconvoluzione in gaussiane degli spettri...93 Spettro 14 Analisi differenziale degli spettri dei mutanti, riferiti a quello del wt...94 Spettro 15 Deconvoluzione in gaussiane dello spettro differenziale di CP29wt e CP29E174V...94 Spettro 16 Risultato della normalizzazione degli spettri della proteina H216F...99 Spettro 17 Risultato della normalizzazione degli spettri della proteina E111V^R218L Spettro 18 Risultato della normalizzazione degli spettri della proteina H114F Spettro 19 Risultato della normalizzazione degli spettri della proteina E174V Spettro 20 Risultato della normalizzazione degli spettri della proteina H245L Spettro 21 Risultato della normalizzazione degli spettri della proteina E166V...104
14
15 A. Introduzione
16 Parte - A 2
17 Introduzione Pagina 3 I. GENERALITA FOTOSINTESI I.1 INTRODUZIONE L a fotosintesi è il processo con cui gli organismi viventi autotrofi convertono l energia originata all esterno della biosfera in una forma fruibile dalle altre forma di vita non autotrofe. Tale conversione consiste nell organicazione del carbonio a partire da composti inorganici elementari. I processi fotosintetici hanno luogo all interno del cloroplasto. Si possono distinguere due fasi di tali processi, conosciute come fase luminosa e fase oscura. La prima consiste nella cattura dell energia luminosa da parte dei complessi proteici situati nelle membrane tilacoidali e porta alla riduzione del NADP + a NADPH ed alla formazione di ATP a partire da ADP. Nella seconda fase (fase oscura), il potere riducente del NADPH e l energia accumulata nell ATP vengono utilizzate per la riduzione della CO 2 a carboidrato (ciclo di Calvin) [11] da parte di enzimi solubili presenti nello stroma. 3
18 Parte - A I.2 I PIGMENTI FOTOSINTETICI [29] I pigmenti sono sostanze che assorbono la radiazione luminosa visibile, apparendo così colorate. Si tratta di composti chimici che possiedono un esteso sistema di doppi legami coniugati, in cui la delocalizzazione degli orbitali rende la differenza di energia tra lo stato fondamentale e quello eccitato sufficientemente bassa da far rientrare la lunghezza d'onda della radiazione associata alla transizione, nell intervallo del visibile. L'energia luminosa proveniente dal sole, giunta sulla superficie terrestre, possiede uno spettro significativo nell'intervallo di lunghezze d'onda compreso tra i 300 ed i 1150 nm, con un massimo di intensità attorno ai 600 nm; esistono differenti pigmenti fotosintetici, ciascuno assorbe in diverse regioni dello spettro, in modo da coprire un intervallo da 350 a 800 nm. Si tratta di carotenoidi, clorofille (tetrapirroli ciclici) e biline (tetrapirroli lineari). Figura 1 Struttura delle clorofilla a, b e Batterioclorofilla La clorofilla a (Chl a) è di gran lunga il pigmento più comune nel regno vegetale: essa adempie sia la funzione di assorbimento e trasferimento dell'energia luminosa, sia quella di donatore primario di elettroni nei centri di reazione dei fotosistemi, nel processo di separazione di carica. 4
19 Introduzione Pagina 5 La clorofilla b (Chl b) è molto meno diffusa della Chl a: è presente nelle piante superiori, nelle alghe verdi, euglenofite e proclorofite, associata a complessi non strettamente connessi ai centri di reazione. Clorofilla a e b possiedono una struttura porfirinica, in cui un anello tetrapirrolico coordina al centro un atomo di magnesio. Sul tetrapirrolo oltre ai gruppi che definiscono il tipo di clorofilla, è presente un anello a 5 atomi di carbonio (anello V) ed una catena fitilica di 20 atomi di carbonio connessa al C 7 del pirrolo IV. Le due forme si differenziano per una sostituzione al terzo anello, che lega un metile nella Chl a ed un gruppo aldeide nella Chl b (fig 1). Spettro 1 Assorbimento pigmenti fotosintetici Lo spettro di assorbimento della Chl a mostra due picchi principali: il primo a 430 nm 1, nella regione di Soret, è associato ad una transizione elettronica dallo stato fondamentale al secondo stato eccitato; mentre il secondo a 662 nm 1 rappresenta la banda Q Y, dovuta alla transizione al primo stato eccitato di singoletto. 1 In dietiletere 5
20 Parte - A La Chl b possiede massimi di assorbimento differenti rispetto a quelli della Chl a; la banda nella regione di Soret si trova infatti a 455 nm mentre quella Q Y a 644 nm. L'altra classe di pigmenti presente nei processi fotosintetici è quella dei carotenoidi. Nei tessuti vegetali è possibile trovare diversi tipi di carotenoidi nei cloroplasti, ma anche nei fiori, frutti, ecc. Quelli coinvolti nei processi fotosintetici sono detti carotenoidi primari ed includono: β-carotene, violaxantina, neoxantina, luteina ed, in minori quantità, zeaxantina e anteraxantina. Il β-carotene fa parte del gruppo dei carotenoidi composti da 40 atomi di carbonio e privi di ossigeno (caroteni), mentre gli altri carotenoidi primari, pur mantenendo lo stesso numero di atomi di carbonio, contengono ossigeno sotto forma di gruppi idrossidi, epossidi, e sono detti xantofille. Figura 2 Struttura di alcuni carotenoidi primari Tutti i carotenoidi primari hanno spettri di assorbimento fra loro simili, e significativi nell'intervallo fra i 400 nm ed i 500 nm. In condizioni di eccessiva illuminazione la xantofilla violaxantina può essere deepoossidata via 6
21 Introduzione Pagina 7 anteraxantina (un intermedio che non si accumula) a zeaxantina. Questo meccanismo (ciclo delle xantofille) [21] sembra avere un ruolo fisiologico nella protezione del centro di reazione in condizioni di stress luminoso. I carotenoidi funzionano essenzialmente come pigmenti accessori nell'assorbimento fotosintetico della luce, ma sembra che la luteina abbia anche un importante ruolo nello stabilizzare la struttura in alcuni complessi antenna del PSII. Il β-carotene, inoltre, è presente nel centro di reazione dove ha la funzione di proteggere la Chl a dalla foto-ossidazione [5] neutralizzando i tripletti di clorofilla (quenching dei tripletti) e prevenendo quindi la formazione dell'ossigeno singoletto, specie altamente ossidante e tossica per le cellule. I.3 IL CLOROPLASTO [56] Il cloroplasto è un organello specializzato. Nelle piante superiori è delimitato dall envelope: una doppia membrana di rivestimento che circoscrive la matrice interna acquosa, lo stroma, e le membrane interne fotosintetiche, i tilacoidi. Figura 3 Il cloroplasto La principale funzione del rivestimento esterno è quella di controllare il movimento di metaboliti, lipidi e proteine da e per il cloroplasto. Inoltre 7
22 Parte - A svolge la funzione di sito per i processi di sintesi di lipidi e proteine, a livello della membrana interna, e di protezione, a livello di quella esterna. Tutte le funzioni di raccolta e trasduzione dell'energia luminosa del processo fotosintetico sono state localizzate nelle membrane tilacoidali. Entro ogni cloroplasto queste formano un intreccio tridimensionale fisicamente continuo e chiuso di una singola membrana, che ne delimita un unico spazio interno, il lume tilacoidale. La relazione spaziale che intercorre tra lumen e stroma è stata determinata inizialmente attraverso la ricostruzione tridimensionale della struttura tilacoidale da micrografie elettroniche di sezioni successive del cloroplasto stesso [46] e confermata successivamente da esperimenti di freeze-fracture. Le membrane tilacoidali sono distinte in due diversi tipi di domini: in un caso i tilacoidi si impilano l'uno sull'altro dando origine ai grana tilacoidali (appressed regions), nell altro si dispongono come lamelle singole per interconnettere diversi grana, dando luogo a strutture chiamate lamelle stromatiche (non appressed regions). Vengono infine definiti come margini le estremità delle vescicole granali, dove la membrana subisce una brusca curvatura. Lo stroma è definito quindi come il compartimento localizzato tra la membrana interna del cloroplasto e le membrane dei tilacoidi. I principali componenti dello stroma includono: copie multiple (circa 300) di DNA cloroplastico [14], ribosomi 70s, Figura 4 Rappresentazione schematica dell organizzazione dei tilacoidi nel mrnas e tutti gli altri elementi cloroplasto necessari per la sintesi proteica [34]; enzimi necessari per il ciclo di riduzione del carbonio, in particolare la 8
23 Introduzione Pagina 9 ribulosio bifosfato carbossilasi-ossigenasi [58]; gli enzimi coinvolti nella sintesi dei lipidi, terpenoidi, chinoni ed altri composi aromatici [55]. I.4 LA CATENA DI TRASPORTO ELETTRONICA : COMPONENTI ED ORGANIZZAZIONE FUNZIONALE [32, 43, 56] I tilacoidi contengono tutti gli elementi necessari per la cattura e la trasduzione dell'energia luminosa ad energia chimica: ATP e NADPH. Tali reazioni sono svolte da complessi proteici di membrana, associati a cofattori e proteine periferiche. Tre di questi complessi, fotosistema I (PSI/LHCI), fotosistema II (PSII/Antenne interne) e il complesso periferico lightharvesting II (LHCII), legano clorofille. Nel complesso dell ATP sintetasi, invece, non ritroviamo pigmenti. Figura 5 Organizzazione funzionale della membrana tilacoidale Il primo evento nella cattura dell energia consiste nell'assorbimento di un fotone da parte di una molecola Chl del complesso antenna LHCII. Dopo assorbimento, l'energia del fotone è conservata sotto forma di eccitone che 9
24 Parte - A migra per meccanismi di trasferimento energetico di risonanza fino alle clorofille del P680, coppia speciale del centro di reazione del fotosistema II. A questo livello avviene la separazione di carica ed inizia il processo di trasferimento elettronico. Il donatore primario, dimero di Chl a detto coppia speciale (special pair), nella forma eccitata, P680 *, trasferisce un elettrone ad una feofitina; la neutralità elettronica del P680 viene ripristinata estraendo un elettrone dall'acqua con concomitante evoluzione di ossigeno molecolare ogni 4 cicli fotosintetici. Gli elettroni, attraverso una serie di trasportatori (plastochinoni, complesso b6f e plastocianina) giungono al centro di reazione del fotosistema I (PSI), P700. Analogamente al PSII, l'energia luminosa raccolta dalle antenne del PSI permette un trasferimento di carica contro gradiente elettrochimico: il P700 * cede un elettrone alla ferrodoxina e da qui al NADP + che viene ridotto a NADPH. L'insieme di tali reazioni è rappresentato dallo schema a Z di Bendall e Hill. Figura 6 Schema Z di Bendall e Hill 10
25 Introduzione Pagina 11 La separazione di carica attraverso la membrana tilacoidale con accumulo di protoni nel lume, conseguenza del trasporto elettronico, fornisce l'energia per la fosforilazione dell'adp ad ATP catalizzata dall'atp sintetasi. L'energia collegata al trasporto di un elettrone dai +820 mv della coppia H 2 O/O 2 ai -320 mv della coppia NADPH+H + /NADP + (1.14 ev = 23.8 Kcal/mole), se si tiene conto che il rendimento della conversione è di circa il 40%, non può essere ottenuta da un singolo fotone nel visibile. Ciò spiega l'intervento dei due fotosistemi, con due distinte reazioni fotochimiche per la formazione di un riducente molto forte (P700 * ), per la riduzione del NADP+, ed un ossidante molto forte (P680 * ) per l'ossidazione dell'acqua. 11
26 Parte - A II. STRUTTURA ED ORGANIZZAZIONE FUNZIONALE DELLE MEMBRANE TILACOIDALI [56] Ciascuno dei cinque complessi principali delle membrane tilacoidali (fig. 5), è composto da proteine multiple e gruppi prostetici. Nella tabella 1 sono riportate le proteine, con la nomenclatura relativa ai geni codificanti, che compongono i due fotosistemi. Gene Prodotto genico Gene Prodotto genico psaa PSI-core Lhca1 LHCI-730 psab PSI-core Lhca2 LHCI-680 psba D1 Lhca3 LHCI-680 psbd D2 Lhca4 LHCI-730 psbb CP47 Lhcb1 LHCII tipo I psbc CP43 Lhcb2 LHCII tipo II psbe cyt b 559 Lhcb3 LHCII tipo III psbf cyt b 559 Lhcb4 CP29 psbo OEE1 Lhcb5 CP26 psbp OEE2 Lhcb6 CP24 psbq OEE3 Tabella 1 Nomenclatura genica delle proteine del fotosistema I e II I complessi del PSII, PSI, cyt b 6 f e dell ATP sintetasi sono formati da proteine codificate sia dal genoma del cloroplasto, che da quello nucleare; si ritiene che questa organizzazione permetta al nucleo di mantenere il controllo e la supervisione dell assemblaggio di tali complessi. II.1 FOTOSISTEMA I [13, 44] Il fotosistema I (PSI) è situato principalmente nelle regioni non impilate dei tilacoidi (lamelle stromatiche), e funziona come il riduttore finale nella catena di trasporto elettronica fotosintetica. Più precisamente il PSI è una plastocianina(pc)-ferrodoxina(fd) ossido-reduttasi. 12
27 Introduzione Pagina 13 Negli organismi fotosintetici eucarioti (alghe e piante), il complesso del PSI è composto da una antenna light-harvesting complex I (LHCI), ed un core (CCI). Questi sono composti a formare il PSI-200. Figura 7 Modello per l organizzazione spaziale del PSI-200 La funzione di LHCI è quella di antenna accessoria, e l energia che essa cattura viene passata al centro di reazione, P700, che si trova nel CCI. II.1.1 Core Complex I, il centro di reazione del PSI [6] Il CCI è il componente del PSI-200 in cui ha luogo la separazione di carica ed il processo di trasporto elettronico. Attualmente si stima che nel CCI siano presenti almeno 10 differenti polipeptidi, circa 100 molecole di Chl a, diverse molecole di β-carotene, due molecole di vitamina K 1 e 3 clusters ferro-zolfo ([4Fe-4S]). Questi formano un complesso pigmentato con una massa apparente in gel non denaturante di 250 kda. E costituito da due subunità, codificate dai geni plastidiali psaa e psab, disposte in modo da coordinare, all interfaccia tra le due, il P
28 Parte - A II.2 FOTOSISTEMA II [13] Il fotosistema II (PSII) è un complesso multi-subunità, formato almeno da 17 subunità, che comprendono anche piccole proteine di massa molecolare inferiore ai 10 kda [24]. Circa 10 subunità sono necessarie per la riduzione del plastochinone e per l evoluzione di ossigeno. II.2.1 Centro di reazione del PSII [13] Il centro di rezione è costituito da un complesso formato dalle subunità D1 (psba) e D2 (psbd), dalle subunità α e β del citocromo b559 (psbe e psbf), e dal prodotto genico di psbi. Una subunità estrinseca di 33 kda (psbo) stabilizza il cluster manganese che catalizza l evoluzione di ossigeno a partire da H 2 O. I pigmenti legati al core del PSII comprendono 4-6 molecolre di Chl a, 2 di feofitina e β-carotene. II.2.2 Antenne interne [6] Le antenne interne del PSII sono le proteine omologhe CP43 e CP47, codificate dai geni psbb e psbc. Tale definizione è giustificata dalla posizione ravvicinata di tali complessi rispetto al P680. In particolare dei due complessi pigmentati è CP47 quello che sembra associato più strettamente al centro di reazione. Si pensa che ciascuna delle due molecole omologhe leghi molecole di Chl a, del β-carotene ed, in basse quantità, della luteina. Benché i dati sul numero dei pigmenti delle antenne interne sia ancora piuttosto dibattuto, sembra certo che l orientamento del β-carotene in CP43 ed in Figura 8 Modello per l organizzazione del core del PSII CP47 sia profondamente diverso: nel primo [38] la molecola è parallela al piano della membrana, mentre nella seconda è perpendicolare allo stesso. 14
29 Introduzione Pagina 15 III. SISTEMI LIGHT-HARVESTING IN NATURA III.1 INTRODUZIONE [54] Come descritto nel paragrafo I.2 i pigmenti coinvolti nei processi fotosintetici sono carotenoidi, clorofille e biline. Questi pigmenti non sono liberi, ma associati a proteine localizzate nelle membrane fotosintetiche (tilacoidi), o a proteine solubili connesse con queste ultime. I sistemi antenna o LHC sono complessi pigmentoproteina che svolgono funzione di raccolta di energia luminosa e di Figura 9 Struttura del pirrolo trasferimento di tale lineare delle biline energia sotto forma di eccitone al centro di reazione, dove avviene la separazione di carica. Il trasferimento dell energia dal sistema antenna al centro di reazione avviene in meno di sec. e con una efficienza oltre al 90%. L elevata efficienza di tale sistema è garantita dal fatto che le molecole di Chl sono disposte alla giusta distanza e con un orientamento corretto entro la proteina che le coordina e fra le diverse proteine che formano il complesso. Le proteine dei complessi light-harvesting possono essere divise in quattro classi sulla base delle caratteristiche delle proteine stesse e del tipo di pigmento fondamentale impiegato: i) Sistemi di membrana leganti clorofille. Questo tipo di sistema si ritrova in piante, alghe verdi, Cryptophyceae, dinoflagellati, Euglenophyta ed alcuni procarioti ossigenici (prochloron); ii) iii) Sistemi solubili leganti clorofilla. Si ritrovano in batteri verdi fotosintetici (Chlorobium, ProsthecoChloris) e dinoflagellati; Sistemi di ficobiline e complessi antenna solubili. Si ritrovano in cianobatteri, alghe rosse e Cryptophyaceae; 15
30 Parte - A iv) Sistemi contenenti batterioclorofilla (BChl) e proteine integrali di membrana. Sono tipiche dei procarioti: Chlorobiaceae, Chloroflexaceae, Chromatiaceae e Rhodospirillaceae; In questi complessi, la componente proteica ha le seguenti funzioni: i) determina il legame specifico e l arrangiamento spaziale delle molecole dei pigmenti; la conformazione della tasca idrofobica, responsabile dell alloggiamento del pigmento, determina infatti l orientamento del pigmento entro la proteina vincolandolo questo ad assumere una posizione ben determinata. Inoltre la forma della tasca è importante nel discriminare fra le due diverse forme di clorofilla, e nel rendere, quindi, un particolare sito più o meno preferenziale per una di esse. ii) determina la configurazione e la conformazione dei pigmenti, e quindi ne modula le proprietà di assorbimento e di emissione, essenziali per le funzioni di cattura dell energia luminosa; i gruppi chimici delle catene laterali, che formano la tasca idrofobica in cui alloggia il pigmento, influenzano, oltre alla configurazione preferenziale del pigmento, anche gli orbitali molecolari di questo. In tal modo anche le proprietà spettroscopiche dei pigmenti vengono modulate, in modo differente a seconda del sito. iii) Media le interazioni con gli altri componenti proteici nell organizzazione sopramolecolare del sistema antenna, permettendo il trasferimento energetico. III.2 SISTEMI LIGHT-HARVESTING IN PROCARIOTI III.2.1 Generalità [60] La maggior parte dei sistemi LHC contengono insiemi organizzati di pigmenti diversi dalla clorofilla deputati all assorbimento dell energia luminosa. 16
31 Introduzione Pagina 17 Ad esempio gli organismi che vivono nell acqua, responsabili di circa la metà della fotosintesi sulla Terra, contengono pigmenti accessori particolari, in quanto la luce, al di fuori delle lunghezze d onda comprese tra 450 e 550 nm (luce blu e verde), viene assorbita quasi completamente durante il suo passaggio attraverso 10 metri d acqua. Nelle alghe rosse e nei cianobatteri, la Chl a viene quindi sostituita come pigmento antenna da una serie di tetrapirroli lineari, in particolare la ficoeritrobilina (rossa) e la ficocianina (blu). Gli stati eccitati più bassi di questi vari tipi di biline sono ad energia più bassa di quelli della clorofilla, facilitando quindi il trasferimento dell energia ai centri di reazione. In questi sistemi, le biline sono legate covalentemente alle ficobiliproteine che sono, a loro volta, organizzate in particelle ad elevata massa molecolare, chiamate ficobilisomi. Altri organismi procarioti possiedono invece un sistema light-harvesting basato su proteine integrali di membrana che legano in modo non-covalente, molecole di batterioclorofilla (BChl). Tali complessi pigmento-proteina, pur non essendo omologhi a quelli delle piante superiori (infatti non mostrano in alcun caso cross-reattività con anticorpi sviluppati contro i primi), rappresentano degli utili modelli. Recentemente sono state ottenute le strutture cristallografiche ad alta risoluzione di complessi LH da due ceppi di batteri rossi [42, 40] e dell LHC solubile presente nei dinoflagellati fotosintetici [33]. Queste strutture consentono di formulare ipotesi di trasferimenti energetici interni e quindi di funzionamento delle antenne stesse. III.2.2 Rhodospirillaceae [57] Dal punto di vista tassonomico, i batteri rossi (Rhodospirillaceae) sono un piccolo gruppo di eubatteri Gram-negativi comprendente solo 30 specie circa. Si tratta di organismi unicellulari che si riproducono per scissione binaria o, in alcune specie, per gemmazione. 17
32 Parte - A Nonostante le sue piccole dimensione questo gruppo di batteri dimostra al sua interno una certa diversità di ordine genetico, come è dimostrato dalla composizione in basi del DNA che varia dal 43 al 73 per cento (%GC). Tutti i batteri rossi sono, almeno potenzialmente, fotoautotrofi, capaci cioè di crescere in condizioni anaerobiche ed alla luce utilizzando CO 2 come fonte di carbonio e composti inorganici ridotti come donatori di elettroni. Si distinguono due sottogruppi di batteri rossi; la maggior parte dei batteri rossi sono anaerobi stretti con un metabolismo basato sull utilizzo di H 2 S come donatore di elettroni, questo sottogruppo viene identificato come batteri rossi sulfurei. Il secondo sottogruppo, i batteri rossi non sulfurei, sono invece sensibili all H 2 S ed utilizzano, come donatore di elettroni, l H 2 O. Di quest ultimo sottogruppo fanno parte i generi Rhodospirillum e Rhodopseudomonas di cui sono state determinate le strutture cristallografiche dei rispettivi complessi antenna LH2. III.2.3 Struttura cristallografica di LH2 di Rhodopseudomonas acidophila [42] I batteri rossi contengono due tipi di complessi antenna, entrambi costituiti da proteine di membrana intrinseche. Il primo tipo, LH1, è intimamente connesso con il centro di reazione a formare il cosiddetto core complex. Disposto più perifericamente, il secondo tipo LH2 è presente in proporzioni variabili. 18
33 Introduzione Pagina 19 Entrambi LH1 ed LH2 sono organizzati con il medesimo principio modulare: i pigmenti fotosintetici, BChl a ed i carotenoidi, sono legati non covalentemente a due apoproteine idrofobiche di basso peso molecolare, le subunità α e β (rispettivamente lunghe 53 e 41 aminoacidi). I complessi nativi sono costituiti da un arrangiamento di questi oligomeri a formare strutture ad anello di dimensioni variabili. La struttura Figura 10 Rappresentazione dimero αβ cristallografica di LH2 di Rhodopseudomonas acidophila è stata determinata ad una risoluzione di 2.5 Å e può essere descritta semplicemente: le eliche trans-membrana di 9 subunità α sono disposte lateralmente a formare un cilindro cavo del diametro di 18 Å mentre le 9 eliche delle subunità β sono arrangiate radialmente alle prime, e formano un cilindro esterno di 34 Å di diametro. Le subunità α sono inclinate di 2 rispetto all asse del cilindro, mentre le β di un angolo pari a 15. Nella struttura le molecole di BChl a si dispongono con due differenti orientamenti rispetto alla membrana. Alcune presentano il piano dell anello disposto internamente e parallelo alla normale della membrana con la molecola del fitolo rivolta verso l interno (chiamate B850); le altre sono disposte invece esternamente con il piano dell anello parallelo alla membrana stessa (chiamate B800). III.2.4 Struttura cristallografica di LHC di Amphidinium carterae La maggior parte dei dinoflagellati, come A. carterae, possiede un sistema antenna costituito prevalentemente da carotenoidi, che consente loro di catturare efficacemente la luce nell intervallo del blu-verde. Oltre a proteine LHC integrali di membrana, strutturalmente e funzionalmente simili a quelle delle piante superiori, i dinoflagellati hanno sviluppato un sistema antenna 19
34 Parte - A solubile con un elevato rapporto carotenoidi:clorofilla. tali complessi sono chiamati PCP (peridinin-chlorophyll-proteins), dal nome del carotenoide presente. La struttura cristallografica di una PCP è stata determinata ad una risoluzione di 2 Å [33]. Figura 11 Rappresentazione della struttura cristallografica di A. carterae e disposizione dei pigmenti (Chl in verde, carotenoidi in rosso) III.3 IL SISTEMA ANTENNA DEL PSI (LHCI) [54] L apparato LHCI si distingue in due complessi, associati al core in modo indipendente. Si distinguono in base ai rispettivi picchi di emissione della fluorescenza a bassa temperatura LHCI-730 ed LHCI-680. Questi complessi sono in realtà formati da più di due polipeptidi, e vengono codificati dai geni lhca1-4. Chl a Chl b β-carotene luteina Neoxant. Violaxant. PSI Core 100 / 14 / / / LHCI Lhca 1 ND ND ND + / + Lhca 2 ND ND ND + / ND Lhca 3 ND ND ND + / ND Lhca 4 ND ND ND + / ND Tabella 2 Composizione in pigmenti delle proteine del PSI 20
35 Introduzione Pagina 21 Dato che LHCI-730 è l unico componente ad emettere fluorescenza quando il trasporto elettronico nel centro di reazione del PSI viene bloccato a 77 K, l energia di eccitazione può passare da LHCI-680 a LHCI-730. Su tali basi, il modello proposto per l organizzazione del PSI prevede il trasferimento dell energia di eccitazione da LHCI-680 attraverso LHCI-730 al core del PSI [4]. Figura 12 Modello per l organizzazione sovramolecolare del PSI [4] Per quanto riguarda la loro composizione in pigmenti, evidenze indirette suggeriscono che ogni polipeptide LHCI leghi 8-10 molecole di Chl, per un totale di circa 120 molecole in tutto il sistema antenna, ed è confermata la presenza in LHCI di luteina e di violaxantina, mentre la neoxantina non è stata rilevata [6]. Sono stati riportati valori variabili del rapporto Chl a/b, da 1.4 a
36 Parte - A IV. IV.1 IL SISTEMA ANTENNA DEL PSII (LHCII) COMPLESSO MAGGIORE LHCII La comprensione di come clorofille e carotenoidi sono legati alle proteine, e cioè da interazioni non covalenti, coincide con la scoperta, più di 25 anni fa, del complesso LH del PSII, LHCII. Il termine LHCII identifica un complesso pigmenti-proteina in cui sono contenute circa la metà delle Chl ed un terzo delle proteine dei tilacoidi di piante superiori [54]. Figura 13 Rappresentazione schematica della struttura di LHCII Il così diffuso interesse per LHCII rispetto alle altre proteine implicate nella fotosintesi deriva quindi dalla sua abbondanza e dalla stabilità del complesso che consente di isolarlo facilmente ed in grandi quantità dalle membrane tilacoidali. LHCII non solo è interessante in sé, per le sue specifiche caratteristiche e funzioni, ma l omologia di sequenza con molte altre proteine in entrambi i fotosistemi delle piante superiori, rende tale complesso un 22
37 Introduzione Pagina 23 utilissimo modello generale per l organizzazione dei pigmenti e per il trasferimento energetico nei complessi antenna. IV.1.1 Funzioni I ruoli funzionali che vengono attribuiti al complesso LHCII sono essenzialmente tre. L attività principale è quella di catturare l energia luminosa e di trasferirla efficacemente in direzione del centro di reazione del PSII. In secondo luogo esso controllerebbe, al variare della luce esterna, l attività coordinata dei due fotosistemi regolando la quantità di luce assorbita da ciascuno di essi. A conferma di tale asserzione è stato verificato che, in presenza di luce assorbita preferenzialmente dal PSII, una sottopopolazione di LHCII migrerebbe, in seguito a fosforilazione, dai grana alle lamelle stromatiche, connettendosi al PSI e determinando così una ridistribuzione dell energia di eccitazione tra i due fotosistemi(transizioni di stato) [1]. Infine LHCII interviene nel processo di impilamento delle lamelle a formare i grana, probabilmente stabilizzandone la struttura attraverso ponti di Mg ++ tra le numerose cariche negative residenti nella parte stromatica N-terminale della proteina [3]. IV.1.2 Composizione in polipeptidi Il termine globale LHCII indica in realtà un insieme di complessi caratterizzati da una diversa composizione polipeptidica e funzione non ancora del tutto compresa. Non solo possono essere discriminate diverse apoproteine appartenenti a LHCII, ma è possibile risolvere anche un certo numero di sottopopolazioni di complessi pigmento-proteina. I polipeptidi di LHCII sono codificati da una famiglia multigenica nucleare. Sono stati descritti fino a 20 diversi geni, raggruppati in tre tipi principali detti lhcb1, lhcb2 e lhcb3. 23
38 Parte - A IV.1.3 Composizione in pigmenti Come già detto LHCII lega circa il 50 per cento della Chl totale presente nei tilacoidi. Le analisi del complesso purificato mostrano che esso contiene, oltre a Chl a e Chl b, le xantofille luteina, neoxantina e violaxantina, escludendo la presenza di β-carotene. La struttura cristallografica ottenuta da Kühlbrandt nel 1994 [36] ha confermato le precedenti analisi che indicavano il valore di molecole di Chl per proteina. Sulla base di questo dato e del rapporto Chl a/b di 1.4, in complessi altamente purificati, possono essere assegnate 7 Chl a e 5 Chl b ad ogni monomero di LHCII. IV.1.4 Struttura cristallografica L unità funzionale di LHCII è un trimero con simmetria C3. Ciascuna proteina del trimero possiede tre eliche trans-membrana, denominate B, C e A, connesse tramite loop idrofilici da entrambi i lati della membrana. Entrambe le eliche A e B formano un angolo di 32 con la normale alla membrana, mentre l elica C è pressochè parallela ad essa. Le eliche A e B, lunghe rispettivamente 43 e 51 Å ( 29 e 34 residui), formano una struttura ad X, stabilizzata dalla forte attrazione elettrostatica tra i residui carichi di due coppie ioniche (Arg70-Glu180, Arg185- Glu65). Due molecole di carotenoidi sono localizzate al centro del complesso, dove, Figura 14 Rappresentazione struttura tridimensionale di LHCII interagendo con l elica A e B, contribuirebbero in modo determinante al legame tra i due domini idrofobici. Dai dati di stechiometria si può ipotizzare che queste due molecole di carotenoidi siano due molecole di luteina, ma non ci sono prove sperimentali. 24
39 Introduzione Pagina 25 Su 12 molecole di Chl, solo 8 interagiscono direttamente con la catena aminoacidica, attraverso la coordinazione degli ioni magnesio da parte delle catene laterali aminoacidiche oppure tramite la catena carbonilica principale. I ligandi presunti sono istidina, glutamina, asparagina e la coppia ionica glutamato-arginina. Le rimanenti 4 molecole di Chl potrebbero rapportarsi indirettamente alla proteina tramite molecole di acqua. Le molecole di Chl risultano disposte su due diversi livelli rispetto allo spessore della membrana, con gli anelli porfirinici perpendicolari al piano della membrana stessa. L analisi cristallografica portata ad una risoluzione di 3.4 Å, permette la localizzazione dei cromofori, ma non ne consente la precisa discriminazione. A tale risoluzione, infatti, le differenze strutturali fra i diversi tipi di carotenoidi e molecole di Chl non possono essere evidenziate. Delle molecole di clorofilla è stata identificata la posizione degli atomi della struttura grezza dell anello tetrapirrolico, ma non è possibile a tale risoluzione evidenziare, oltre ai sostituenti dell anello, né l anello V, né la catena fitilica. Mancano quindi gli elementi necessari per orientare le molecole dei pigmenti al fine di identificarne la disposizione dei momenti di transizione. IV.2 OMOLOGIA ENTRO LA FAMIGLIA DI PROTEINE CAB Il primo polipeptide CAB è stato scoperto più di 25 anni fa e, per i primi 20 anni dopo questa scoperta, è perdurata una considerevole confusione circa il numero delle proteine CAB, la loro localizzazione e funzione. Negli ultimi anni, la possibilità di isolare e caratterizzare estensivamente i geni codificanti tali proteine, ha allargato enormemente il campo delle conoscenze. Le ricerche hanno evidenziato che ogni polipeptide CAB è codificato da un diverso gene nucleare e che esiste una elevata omologia di sequenza entro la famiglia. In particolare le regioni delle eliche trans-membrana esiste un alto livello di conservazione. Da allineamenti di sequenza delle proteine CAB, 25
40 Parte - A usando come modello LHCII, è possibile assegnare i ligandi per le clorofille conservate. ttttttt lut_ 1 Lhcb1 RKTAAKAKP-AASGSP WYGPDRVL-YLFPLSGEPPS----YLTGEFPFDYGWDTAGL Lhcb6 AAAAAKKSWIPAIKSDAEIVNPPW LDGSLPGDFGFDPLGLGK Lhcb5 LFSKKPAQKPKPSAVSSSSPDISDELAKWYGPDRRIYLPDGLLDRSVPEYLTGEVPGDYGYDPFGLGK Lhcb4 RFGFGLGGKAKPAPKKVAKTSTSSDRPLWFPGAVAPDYLDGSLV GDYGFDPFGLGKPVEYLQFELDSLDQNLAKNEAGGIIGTRFES 1 _lut_ 52 a4_a5 a1 b6 b5 b5_ Lhcb SADPETFAKNRELEVIHCRWAMLGALGCVFPELLARNGVKFG-EAVWFKAGSQIFSEGGLDYLGNPSLIHAQSILAIWACQVVLMGAVEGYRIA Lhcb DPAFLKWYREADVIHGRWAMAAVLGIFVGQAWSG PIWFEAGAPDTRIAPF SFGSLLGTQLLLMGWVESKRWD Lhcb KPEDFAKYQAYELIHARWAMLGAAGAVIPEACNKFGANCGPEAVWFKTGALLLDGNTLSYFGNSIPI---NLVVAVIAEVVLVGGAEYYRII Lhcb4 SEVKSTPLQPYSEVFGLQRFRECELIHGRWAMLATLGALSVEWLTGVT WQDAGKVELVDGS-SYLGQPLPF---SISTLIWIEVLVIGYIEFQRNA 88 lut lut 145 a1_a2_a4 a3 Lhcb1 GGPLGEVVDPLYPG GSFDPLGLAD DPEAFGELKVKELKNGRLAMLSMFGFFVQAIVTGKG Lhcb6 FFNPDSQAVEWATPWSRTAENFANFTGEQGYPGGKFFDPLALAGTSRDGVYIPDVDKLERLKLAEIKHAR-AMLAMLAFYFEAGQ-GKTRLGALGL Lhcb5 NLDLEDKL HPGGGPFDPLGLAS DPDQAAILKVKEIKNGRLAMFSMFAFFIQAYVTFEG Lhcb4 ELDPEKRL YPGGSYFDPLGLAA DPEKKERLQLAEIKHARLAMVAFLGFAVQAAATGKG b3_ Lhcb1 PLENLADHIADPVDNNAWAYATNFVPGK Lhcb6 Lhcb5 PVENLAKHLSDPFGNNLLTVISGAAERTPSL Lhcb4 PLNNWATHLSDPLHTTIFDTFGGSS 238 t Tabella 3 Allineamento delle sequenze dedotte dai cdna delle Lhcb 26
41 Introduzione Pagina 27 IV.3 ANTENNE MINORI Accanto ad LHCII, vi sono, nel sistema antenna del PSII, altri tre complessi pigmento-proteina. Tali complessi, isolati da alcuni anni [41, 16, 7], sono stati recentemente caratterizzati grazie alle tecniche di purificazione di IEF non denaturante [19]. Queste antenne minori sono chiamate CP29, CP26 e CP24 in base alla loro massa apparente in elettroforesi non denaturante. Le rispettive apoproteine sono codificate dai geni nucleari lhcb4, lhcb5 ed lhcb6. Le antenne minori, presenti in quantità uguale nel PSII, legano complessivamente solo il 15 per cento della Chl totale del fotosistema. In Figura 15 Modello di arrangiamento delle antenne questi complessi è localizzata la maggior parte minori nel PSII [38] della violaxantina contenuta nel PSII (più dell 80%). Dal momento che la violaxantina è l immediato precursore della zeaxantina, pigmento coinvolto nella dissipazione degli eccessi di energia di eccitazione (ciclo delle xantofille), le antenne minori potrebbero essere la sede principale del meccanismo di smorzamento non fotochimico (NPQ) che regola il flusso di energia verso il centro di reazione [9, 18, 2]. IV.3.1 CP24 Prodotto genico di lhcb6, CP24 è il complesso meno caratterizzato tra le antenne minori riguardo alla composizione in pigmenti. Le difficoltà probabilmente derivano dalla perdita di pigmenti durante la sua purificazione. Sono stati riportati valori divergenti del Figura 16 Modello schematico di struttura per CP24 27
42 Parte - A rapporto Chl a/b ( ) e della stechiometria Chl-proteina (5-13).Più recentemente è stato possibile determinare che CP24 lega 5 Chl a e 5 Chl b attraverso la ricostituzione in vitro di proteine ricombinanti [45]. A differenza delle altre antenne minori, CP24 non sembra legare neoxantina, pur presentando violaxantina e luteina [18, 50]. IV.3.2 CP26 Il complesso CP26 è il prodotto genico di lhcb5. Esistono due isoforme di tale pigmento-proteina, di 28 e 29 kda, entrambe riconosciute dall anticorpo ottenuto contro il prodotto genico di lhcb5. La composizione in pigmenti di Figura 17 Modello schematico di CP26 comprende violaxantina, struttura per CP26 luteina, neoxantina, Chl a e Chl b (rapporto Chl a/b pari a 2.2). Si ritiene che siano legate a questo complesso 9 molecole di Chl [18, 50]. 28
43 Introduzione Pagina 29 IV.3.3 CP29 Il gene nucleare lhcb4 codifica per la proteina a peso molecolare più elevato (31 kda) tra le antenne di LHCII, CP29. Figura 18 Modello schematico della struttura di CP29 basato sull omologia di sequenza e su dati biochimici (vedi oltre) La sua massa molecolare, maggiore degli altri LHC, è dovuta all inserzione di 42 aminoacidi all N-terminale. Il complesso lega 8 molecole di Chl, probabilmente 2 Chl a e 6 Chl b, visto che il rapporto Chl a/b è di L N-terminale, dominio esposto allo stroma, può essere fosforilato in condizioni di eccessiva illuminazione, e, tale fosforilazione, ne modifica la conformazione e le proprietà spettroscopiche [12]. 29
44 Parte - A V. IL TRASFERIMENTO DELL ENERGIA V.1 INTRODUZIONE Il processo chiave della fotosintesi e l assorbimento della luce solare da parte dei pigmenti antenna ed l efficiente trasferimento dell energia di eccitazione al centro di reazione fotochimica dove l energia viene intrappolata in forma di una stabile separazione di carica. La sequenza di reazioni coinvolte, che interessa sia processi fotochimici che fotofisici, avviene con una resa quantica di circa il 90%, quindi con alta efficienza ed a basso costo per tutti gli organismi fotosintetici. Il processo di trasferimento dell energia di eccitazione deve essere considerato un processo non radiativo che e dovuto ad interazioni colombiane tra la molecola originariamente eccitata, il donatore D, e quella alla quale l energia verrà trasferita, l accettore A. Se lo stato eccitato del donatore (D * ) fluoresce (k fd ) o forma uno stato di tripletto via intersystem crossing (k iscd ) o se torna allo stato fondamentale emettendo calore, secondo il meccanismo di conversione interna (k icd ) allora il tempo di vita del suo stato eccitato (τ 1D ) e la sua resa di fluorescenza (Φ D ) sono dati da: τ 1D = 1/k 1D = 1/(k fd +k iscd +k icd ) ; Φ D = k fd /k 1 D (1) dove k D 1 rappresenta la costante di decadimento totale dello stato eccitato D *. Se l energia viene trasferita in maniera irreversibile alla molecola A (costante di trasferimento k DA ) allora la fluorescenza e la resa di tripletto di D vengono smorzate: la fluorescenza di D va rapidamente a zero, mentre quella di A aumenta. La resa di fluorescenza e il tempo di vita dello stato eccitato di D, in presenza di A, saranno quindi: τ D = 1/(k 1D + k DA ); Φ D = k fd /(k 1D + k DA ) (2) 30
45 Introduzione Pagina 31 Il processo di trasferimento sarà completamente irreversibile solo se la differenza di energia tra D * ed A *, E DA, sarà sufficientemente grande rispetto al valore di energia termica. La velocità di trasferimento di energia da un donatore ad un accettore può essere calcolata utilizzando la teoria eccitonica [37, 25, 39]. In meccanica quantistica lo stato fondamentale di singoletto (S 0 ) ed il primo stato eccitato di singoletto (S 1 ) di D ed A, vengono descritti come funzioni d onda normalizzate, Ψ 0 A, Ψ 0 D, Ψ 1 A, Ψ 1 D, che sono le soluzioni stazionarie dell equazione di Schrödinger tempo-dipendente: H A Ψ 0 A = E 0 AΨ 0 A; H A Ψ 1 A = E 1 AΨ 1 A (3) dove H rappresenta l Hamiltoniano della molecola isolata A. L espressione tiene conto sia dell energia cinetica di nuclei ed elettroni, che delle forze coulombiane attrattive e repulsive tra vari nuclei ed elettroni. Quando A e D sono molecole interagenti, cioè c è interazione tra le nuvole elettroniche di A e D, l Hamiltoniano dell intero sistema viene espresso come: H DA = H D + H A + V DA (4) dove il termine V DA rappresenta l accoppiamento. Se una delle due molecole, ad es. D, viene eccitata, la probabilità di trovare l eccitazione in A, dopo un certo tempo, non e nulla. Il fatto che l eccitazione si possa trovare sia su D che su A viene descritto usando una combinazione lineare degli stati localmente eccitati Ψ 0 AΨ 1 D e Ψ 0 DΨ 1 A. Se si assume che la transizione coinvolga solo due elettroni le funzioni d onda dello stato iniziale (i, dove e eccitato D) e finale (f, dove e eccitato A) saranno: Ψ i = (1/ 2) [Ψ 1 D(1)Ψ 0 A(2) - Ψ 1 D(2)Ψ 0 A(1)] (5) Ψ f = (1/ 2) [Ψ 0 D(1)Ψ 1 A(2) - Ψ 0 D(2)Ψ 1 A(1)] (6) Il numero tra parentesi indica l elettrone coinvolto. 31
46 Parte - A La velocità del trasferimento di energia dallo stato iniziale allo stato finale, e governata dall elemento della matrice di interazione dato da: U DA = Ψ i V DA Ψ f = U C DA + U EX DA (7) Il termine U C e il contributo coulombiano: U C DA = Ψ 1 D(1)Ψ 0 A(2) V DA Ψ 0 D(1)Ψ 1 A(2) (8) dove U C DA rappresenta l interazione coulombiana tra le densità di carica di Ψ 1 D(1)Ψ 0 A(2) e Ψ 0 D(1)Ψ 1 A(2). L elettrone su D, inizialmente eccitato, ritorna allo stato fondamentale e simultaneamente l elettrone su A e promosso ad uno degli orbitali dello stato eccitato di A. (vedi fig. 19). Figura 19 Rappresentazione schematica dei contributi al trasferimento dell energia di eccitazione di Coulomb (in alto) e di scambio (in basso) Il termine U EX e il contributo di scambio: U EX DA = Ψ 1 D(1)Ψ 0 A(2) V DA Ψ 0 D(2)Ψ 1 A(1) (9) in questo caso il trasferimento dell eccitazione e descritto come uno scambio dell elettrone eccitato di D con quello non eccitato di A. Il risultato finale e ancora che D torna allo stato fondamentale mentre A viene eccitato. In 32
47 Introduzione Pagina 33 contrasto con il meccanismo di Coulomb, che può essere efficacie anche a grande distanza, il meccanismo di scambio e operativo solo nel caso in cui si abbia sovrapposizione delle funzioni d onda, ma può essere operativo anche nel caso in cui gli stati di D ed A, coinvolti nel trasferimento, siano otticamente proibiti, condizione nella quale il meccanismo di Coulomb non e valido. Nel caso in cui siano coinvolte transizioni otticamente permesse e la distanza tra D ed A non sia troppo piccola il termine coulombiano diventa dominante. In questo caso l iterazione D-A può essere approssimata ad un interazione dipolo-dipolo e l integrale di interazione (eq.8) può essere approssimato nel modo seguente: U C DA = 5.04 ( µ A * µ D / R 3 DA) (cos α - 3cos β 1 cos β 2 ) = 5.04 ( µ A * µ D / R 3 DA) * k dove U C è dato in cm -1 i dipoli di transizione in debyes e R DA, distanza tra i dipoli in nm. k è il fattore di orientazione dove α è l angolo tra i due dipoli e β 1 e β 2 sono gli angoli tra ogni dipolo ed il vettore R DA che li congiunge. Il valore del momento per la Chl a è di circa 5 debye. Vediamo ora di analizzare i due casi della possibile interazione tra la molecola di donatore D e quella di accettore A. V.2 ACCOPPIAMENTO FORTE. Per avere un accoppiamento forte è necessario che U C DA» E, dove E è una misura della larghezza di banda della transizione elettronica coinvolta (A A *, D D * ). Lo spettro combinato di D ed A è modificato e porta a due nuove bande di assorbimento, dovute alla combinazione delle transizioni in fase (+) e fuori fase (-) degli stati eccitati localmente. Le transizioni (+) e (-) sono separate da 2 U DA. La transizione ottica di ogni dimero eccitato può essere più o meno permessa a seconda della geometria di D ed A. Nel caso di accoppiamento forte il trasferimento dell eccitazione è un processo coerente 33
48 Parte - A cioè la relazione tra le fasi degli stati eccitati locali, Ψ 0 DΨ 1 A e Ψ 1 DΨ 0 A è fissa. L eccitazione oscilla avanti e indietro tra D ed A ed è solo istantaneamente localizzata (anche questa è una semplificazione). La frequenza dell oscillazione è 2cU C DA e, partendo con l eccitazione in D, la densità di eccitazione su A raggiungerà il suo valore massimo dopo: t = 1/ 4cU C DA che corrisponde ad una costante: k DA = 4cU C DA. Notiamo che k DA R -3 DA. Il tempo durante il quale l eccitazione può essere considerata coerente è molto piccolo ( s). Ciò è dovuto a tutti i processi che potranno alla perdita della relazione di fase tra gli stati eccitati (collisioni, interazioni con vibrazioni intramolecolari o con il lattice). Quindi, dopo un cortissimo periodo nel quale l eccitazione può venire considerata delocalizzata e ci si ritrova nel caso dell accoppiamento forte, l eccitazione diventa localizzata su D o su A ed il processo può essere descritto secondo la teoria di Förster. V.3 ACCOPPIAMENTO DEBOLE Nella teoria dell accoppiamento debole la velocità totale di trasferimento di energia da D ad A è data da: k DA = k fd (R 0 /R DA ) 6 D dove k f è la velocità di fluorescenza del donatore in assenza dell accettore, R 0 è la distanza (in nm) alla quale la costante di velocità per il trasferimento di energia ad A e per la fluorescenza sono uguali, ed è data da: R 0 = 8.8 x k 2 n -4 F D (ν) ε A (ν) ν -4 dν dove ε A (ν) è il coeff. di estinzione molare, ν il numero d onda, F D (ν) è lo spettro di emissione di D normalizzato ( F D (ν)dν = 1), n è l indice di rifrazione, e k, parametro di orientazione è dato da: k = (cos α - 3cos β 1 cos β 2 ) 34
49 Introduzione Pagina 35 Il parametro R 0 dipende fortemente dalla sovrapposizione dello spettro di fluorescenza del donatore e di assorbimento dell accettore e può essere misurato sperimentalmente in tabella 3 sono riportati i valori di R 0 e k f per lacune combinazioni donatore-accettore.il fattore R 06 dipende dal quadrato del fattore di orientazione k. Il valore massimo di k 2 è 4, il minimo 0. Per un orientazione casuale di D e A k 2 assume un valore di 2/3. Donatore Accettore R 0 (Å) φ D τ D 1 (ns) Chlb Chl a Chl a Chl a β-carotene Chl a 50 <10-5 >10-3 BChl a 875 BChl BChl a 800 BChl BChl a 800 BChl Tabella 4 Distanza critica di Förster R 0, efficienza di fluorescenza in vivo φ D e tempo di vita di fluorescenza τ 1 D per diverse coppie accettore-donatore coinvolti in processi fotosintetici V.4 TRASFERIMENTO DI ENERGIA DI SCAMBIO Come già visto il termine U EX DA contribuisce in maniera significativa al processo di trasferimento di energia solo quando il termine coulombiano è piccolo, cioè quando le transizioni coinvolte sono proibite e la distanza tra donatore ed accettore è piccola (R DA 0.5nm). Un esempio può essere quello del trasferimento dallo stato di tripletto della Chl alla molecola di carotenoide strettamente associata: Chl T + Car Chl + Car T Questo processo avviene n un tempo vicino ai 20 ns e benchè il processo sia lento, i lunghi tempi di vita degli stati di tripletto assicurano un alta efficienza. 35
50 Parte - A La costante di velocità totale per il trasferimento di energia mediante il meccanismo di scambio [22] è data da: k EX DA = (2π/ h-) 2 (U EX DA) 2 F D (ν) ε A (ν)dν U EX DA decresce esponenzialmente con R DA, è dipendente dall orientazione di D ed A, ma indipendente dalla forza di dipolo delle transizioni in D ed A. Per una distanza donatore-accettore maggiore di 4 Å Dexter stima una trasferimento di energia di scambio 100 volte meno efficiente del trasferimento di Forster, assumendo che entrambi siano permessi. Il trasferimento di energia di singoletto dai carotenoidi alle clorofille avviene molto probabilmente ancora secondo questo meccanismo, dato che la fluorescenza dei carotenoidi è estremamente bassa il che suggerisce una rapida conversione interna (k ic s) e indica che clorofille e carotenoidi siano molto vicini all interno della matrice proteica. V.5 TRASFERIMENTI DI ENERGIA REVERSIBILI Se la temperatura è sufficientemente alta o il E DA abbastanza piccolo il trasferimento all indietro dell energia di eccitazione, cioè da A a D, è possibile. Quando D ed A sono nello stato termicamente rilassato, prima che avvenga il trasferimento di energia, il rapporto tra la velocità di trasferimento da D ad A e quella tra A e D è data da: k DA /k AD = e - E / k T DA B dove k B è la costante di Boltzmann e T la temperatura assoluta. Il rapporto può essere calcolato anche dall integrale di sovrapposizione appropriato. V.6 MIGRAZIONE ED INTRAPPOLAMENTO Il trasferimento di energia in sistemi fotosintetici coinvolge un grande numero di trasferimenti di energia molto veloci tra singoli pigmenti e gruppi di 36
51 Introduzione Pagina 37 pigmenti fino a che l energia non raggiunge il centro di reazione. Il tempo di intrappolamento è definito come il tempo necessario per equilibrare lo stato di separazione di carica P + I - con lo stato eccitato antenna/p. Il tempo totale richiesto per intrappolare l eccitazione è dato da : τ trap = τ mig +τ RC per un lattice bidimensionale il tempo di migrazione è dato da: τ mig = ½ Nf p (N) τ hop dove N è il numero di pigmenti antenna per centro di reazione f p (N) è la caratteristica funzione-struttura per il lattice e τ hop è l hopping time. Il tempo di intrappolamento (τ RC )è dato da: τ RC = N {1/zW 1 + (W 2 /W 1 ) 1/k CS } in cui W 1 è la velocità del trasferimento di energia da uno dei pigmenti vicini a P a P stesso, W 2 è la velocità del trasferimento all indietro tra questi stessi pigmenti, z è il numero di pigmenti che si trovano vicini a P e k CS è la velocità di separazione di carica. Vediamo alcuni casi: W 1 W 2 > k CS. Questo caso è chiamato: trap-limited (limitato dalla trappola) -1 e τ RC = Nk CS. Il tempo si intrappolamento che si ottiene può essere interpretato nel seguente modo: poiché l energia di eccitazione è trasportata sul tutti i siti dei pigmenti antenna (compreso P) con una velocità più grande di quella dei processi che portano alla diseccitazione (compresa la separazione di carica), la probabilità di trovare l eccitazione si P è 1/N, assumendo che tutti i siti siano energeticamente equivalenti. Poiché in questo caso W 1 e W 2 sono entrambe più grandi di k RC ci si aspetta un significativo contributo dei pigmenti del centro di reazione alla fluorescenza del sistema. W 1 W 2 < k CS Questo caso è chiamato diffusion limited: Limitato dalla diffusione. Il tempo di intrappolamento è dato da: 37
52 Parte - A τ RC = N/zW 1 In questo caso il passo lento è la migrazione dell energia dai pigmenti antenna al centro di reazione, tutto ciò si riflette con una bassa fluorescenza di P e nella debole dipendenza del tempo di intrappolamento dalla velocità di separazione di carica. Le ragioni fisiche per questo lento trasferimento possono essere la grande distanza tra i pigmenti ed il centro di reazione o la presenza, come vedremo, di pigmenti antenna ad energia più bassa di quella di P. 38
53 B. Scopo della tesi
54 Parte - B 40
55 Scopo della tesi Pagina 41 I. PREMESSA L a comprensione accurata dei processi di trasferimento energetico all interno dei complessi antenna e dei centri di reazione, richiede conoscenze sulla distanza tra i cromofori coinvolti in tali processi, sull orientazione reciproca dei loro momenti di transizione e sulla distribuzione dei livelli energetici di assorbimento e di fluorescenza all interno del fotosistema. Recentemente, un gran numero di conoscenze sono state ottenute per il fotosistema II sull organizzazione topologica delle subunità che lo compongono [10], sulla composizione delle forme spettroscopiche [35, 62] e sulla struttura del complesso maggiore LHCII [36] determinata su cristalli bidimensionali ad una risoluzione di 3.4 Å. La struttura di LHCII ha permesso l identificazione dei siti di legame per le molecole di clorofilla e della distanza tra cromofori vicini che risulta essere compresa fra 8 e 15 Å. La risoluzione della struttura di LHCII, finora ottenuta, non consente di ottenere informazioni essenziali quali: a) determinazione dei livelli energetici delle transizioni dei singoli cromofori b) identificazione delle Chl a e Chl b c) identificazione dei momenti dipolari di transizione d) identificazione dei carotenoidi legati al complesso. e) determinazione dei livelli energetici delle transizioni dei singoli cromofori. La complessità delle caratteristiche ottiche di LHCII, nelle quali si sommano i contributi dei singoli cromofori (che vengono influenzati diversamente a seconda del sito di legame a cui appartengono), rende molto difficile risalire alle informazioni strutturali mancanti, utilizzando analisi spettroscopiche. Gli scarsi sviluppi recenti nella comprensione della eterogeneità spettroscopica è dovuta, in parte, alla mancanza di tecniche sperimentali che 41
56 Parte - B consentano di modificare selettivamente le transizioni ottiche e di isolare quindi i diversi contributi dei singoli cromofori. In questo contesto, è molto interessante l approccio che prevede l utilizzo di complessi pigmenti-proteina ricostituiti. Esperimenti di questo tipo utilizzavano, inizialmente, apoproteine ottenute da purificazione da cui i pigmenti venivano staccati attraverso trattamenti con detergenti [51]; recentemente, la tecnica di ricostituzione è stata applicata ad apoproteine da cdna codificante per un singolo prodotto genico Lhcb1, ottenute per sovraespressione in E. coli [47]. Nella maggior parte di questi casi, comunque, le proprietà ottiche dei complessi ricostituiti si allontanavano da quelle dei complessi nativi limitando la possibilità di utilizzare questi campioni per studi spettroscopici. Solo recentemente è stata ricostituito con successo il complesso antenna CP29, utilizzando l apoproteina Lhcb4 di mais sovraespressa in E. coli [28]. Il complesso ricostituito mostra caratteristiche di assorbimento, fluorescenza e di dicroismo circolare che ricalcano con estrema precisione quelle del complesso nativo; inoltre anche altre caratteristiche biochimiche peculiari, come il legame del DCCD [61], sono mantenute [49]. Il sistema del CP29 ricombinante può perciò essere impiegato per una serie di analisi sperimentali per ottenere i parametri lasciati indeterminati dopo il lavoro sulla struttura di LHCII di Kühlbrandt e collaboratori [36]. I punti significativi sono i seguenti: i) identificazione dei livelli energetici di ciascun cromoforo. ii) determinazione dell orientazione dei momenti delle transizioni elettroniche per ciascuna molecola di clorofilla. A tale scopo sono stati utilizzati 7 mutanti puntiformi degli 8 residui coinvolti nella coordinazione di molecole di clorofilla [53]; in un caso, infatti, la mutazione porta alla completa distruzione della struttura terziaria della proteina. 42
57 Scopo della tesi Pagina 43 II. SCOPO DELLA TESI In questo lavoro di tesi di laurea mi sono concentrato sul seguente problema: determinare l orientazione dei momenti delle transizioni Q Y delle singole molecole di clorofilla in CP29. A tale scopo è necessario caratterizzare matematicamente le componenti l, m ed n dei versori di ciascuna transizione, rispetto ad un sistema di coordinate relativo alla struttura proteica. Ho affrontato questo problema attraverso l analisi spettroscopica di dicroismo lineare della libreria di mutanti di CP29 sulla base di un modello strutturale per tale proteina che ho ottenuto per omologia con LHCII, l unica proteina della famiglia la cui struttura è stata risolta. III. PERCHE USARE CP29 AL POSTO DI LHCII Per risolvere il problema dell orientazione dei pigmenti devono essere soddisfatti due requisiti fondamentali: i) è necessario avere a disposizione un sistema sperimentale in cui i singoli cromofori possano essere modificati, e quindi analizzati, individualmente. ii) è necessario avere a disposizione un modello strutturale della proteina rispetto a cui determinare le coordinate delle componenti dei versori relativi alle transizioni che si vogliono determinare. Allo stato attuale un modello strutturale è disponibile solo per LHCII [36]. L utilizzo di LHCII come sistema sperimentale è comunque sconveniente per i seguenti motivi: a) LHCII è un trimero in cui le interazioni fra i cromofori appartenenti a diverse subunità, rispetto al monomero, sono molto forti e modificano significativamente le proprietà spettroscopiche del sistema trimerico rispetto a quello monomerico. b) LHCII lega 12 molecole di clorofilla per polipeptide e 3 xantofille, ma solo 8 siti di legame per le molecole di clorofilla e 2 per quelle di xantofilla sono stati identificati. Quindi 43
58 Parte - B almeno 4 molecole di clorofilla e 1 xantofilla, non possono essere modificate sperimentalmente (non si possono ottenere mutanti). c) LHCII purificato dalle piante risulta essere una proteina eterogenea rappresentata da una miscela di 18 prodotti genici. Per il requisito i) CP29 è un sistema indubbiamente migliore di LHCII per i seguenti motivi: a) è una proteina monomerica. b) lega 8 molecole di clorofilla e 2 molecole di xantofille. Nel caso di CP29 i siti di legame sono tutti noti, quindi è possibile modificare sperimentalmente ciascun cromoforo. c) CP29 è il prodotto di un singolo gene, ciò permette di controllare che il sistema impiegato sia identico alla proteina nativa. Per il requisito ii), cioè la necessità della struttura, abbiamo costruito un modello strutturale di CP29 per omologia con LHCII. 44
59 C. Materiali e Metodi
60 Parte - C 46
61 Materiali e Metodi Pagina 47 I. BIOCHIMICA I.1 ELETTROFORESI L e tecniche elettroforetiche consentono la separazione di peptidi in base a PM, carica e forma delle molecole stesse. Un sistema elettroforetico può essere denaturante, parzialmente denaturante o non denaturante nei confronti dei campioni caricati. Nell'elettroforesi denaturante (Tris-SO 4 SDS PAGE) i campioni sono trattati con agenti riducenti (b-mercaptoetanolo), con il detergente anionico Sodio Dodecil Solfato (SDS) e infine denaturati affinché le proteine perdano la struttura terziaria. L' SDS si lega nel rapporto costante di 1.4 g per grammo di proteina: ciò conferisce a ciascun polipeptide un uguale rapporto carica/massa per cui la discriminazione tra le molecole avviene solo in base alla loro capacità di passare attraverso il reticolo del gel, cioè in base al PM. Più le molecole sono grandi, maggiori sono gli ostacoli che incontrano e che rallentano quindi la migrazione. Anche l'urea, presente nel gel, contribuisce alla denaturazione delle proteine. Nei gel non denaturanti (gel verdi o Deriphat-page), i polipeptidi mantengono la propria struttura terziaria e quindi, nel caso di proteine vegetali leganti pigmenti, non si ha perdita degli stessi a queste coordinati. Il detergente nel tampone superiore (Deriphat) forma delle micelle con le proteine, solubilizzate nel blando detergente Dodecilmaltoside (DM) o Octilglucoside (OGP), trascinandole nel gel. Un gel verde modificato, con LDS nel tampone superiore, è parzialmente denaturante nei confronti di proteine leganti la clorofilla, solubilizzate in DM o in OGP: solo i complessi più stabili rimangono integri. Le due soluzioni del gel di separazione (running gel) e del gel di impaccamento (stacking gel) vengono preparate a partire da soluzioni stock dei vari componenti. La funzione dello stacking gel, localizzato al di sopra del 47
62 Parte - C resolving, è quella di focalizzare i polipeptidi in bande dallo spessore molto ridotto prima del loro ingresso nel gel di separazione. Le soluzioni di acrilamide vengono fatte polimerizzare tra due lastre di vetro di mm 160 x 180 o di dimensioni 10 x 8 mm, separate da spaziatori dello spessore desiderato ( mm). La corsa elettroforetica viene eseguita applicando una differenza di potenziale variabile a seconda del tipo di gel utilizzato e delle sue dimensioni, per un tempo sufficiente ad effettuare la migrazione del fronte della clorofilla fino al margine inferiore del gel. 48
63 Materiali e Metodi Pagina 49 I.1.1 Tris-H2SO4 SDS-PAGE [8] Bassi R. et al. (1985) Eur. J. Biochem. 146, pag Stacking gel : 5% (W/V) acrilamide 60/08 (60% acrilamide, 08% bis-acrilamide) M Tris-H2SO4 ph 8.9 Resolving gel : 14% (W/V) acrilamide 60/08 (60% acrilamide, 08% bis-acrilamide) M Tris-H2SO4 ph M urea La polimerizzazione avviene aggiungendo TEMED e Persolfato di ammonio (APS) alle concentrazioni finali rispettive di 0.05% e 0.02% per il running e di 0.125% e 0.05% per lo stacking gel. Resolving gel (14%) Stacking gel (5%) acrilamide 60/ ml 0.3 ml 3 M Tris H 2 SO 4 ph ml 0.5 ml urea 3.6 g saccarosio 1.8 g H 2 O 1.4 ml 3.2 ml TEMED 5 µl 5 µl 10% APS 20 µl 20 µl 10 ml 4 ml 49
64 Parte - C Tampone di corsa: inferiore (+) Tris 42.9 mm glicina 67.6 mm superiore (-) Tris 42.9 mm glicina 67.7 mm SDS 0.1% (W/V) EDTA 1 mm L'elettroforesi viene effettuata a temperatura ambiente per circa 14 ore, a 30 Volts costanti per gel di dimensioni 10 x 7 x 0.5 cm. I.1.2 Colorazione al Coomassie Il legame del colorante Coomassie ad alcuni aminoacidi permette di visualizzare le proteine separate elettroforeticamente. I gel vengono immersi nella soluzione di colorazione per circa 90 minuti e messi ad agitare. Soluzione di colorazione: 0.04% (w/v) Coomassie Brillant Blue R-250, 500 ml metanolo, 500 ml H 2 O, 100 ml acido acetico. Ne segue la decolorazione, che continua fino a quando le bande proteiche contrasteranno nettamente con il fondo del gel. Soluzione di decolorazione: 7.5% (v/v) acido acetico, 92.5% (v/v) H 2 O. I gel possono essere conservati in glicerolo 10% e soluzione decolorante all'interno di bustine di plastica sigillate oppure possono essere seccati sottovuoto in Gel-Dryer. 50
65 Materiali e Metodi Pagina 51 I.1.3 Isoelettrofocalizzazione non denaturante su gel [19] Dainese P. et al. (1990) Photochem. Photobiol. 51, pag L IEF è una tecnica elettroforetica che permette la separazione di composti proteici in un gradiente lineare di ph stabilizzato tra due elettrodi grazie alla presenza di particolari sostanze, gli anfoliti. Gli anfoliti presentano alta capacità tamponante al loro punto isoelettrico con valori di pi continui tra i due estremi dell intervallo di ph prescelto (nel nostro caso ph 4-6). Le proteine migrano fino a raggiungere l intervallo di pih corrispondente al loro pi (carica totale nulla) e si allineano in questa posizione. Gli esperimenti di IEF sono stati effettuati su strato sottile di gel granulare. Composizione del gel: glicina anfoliti dodecil-maltoside Ultrodex (LKB) come fase solida 1% (W/V) 2% (W/V) 0.06% (W/V) 5% (W/V) Gli anfoliti sono disponibili in stock al 40% (W/V). Il gel è stato disposto su un piatto alle estremità del quale sono state messe delle striscioline imbevute di soluzione al 1% di anfoliti. Con un applicatore è stato posto, in prossimità del catodo, il campione, prelevato da un gradiente di saccarosio, portato al 2% di anfoliti. Alle estremità del vassoio sono state sistemate delle striscie di carta da filtro, imbevute con le soluzioni degli elettrodi. Polo positivo: 1 M H3PO4 Polo negativo: 1 M NaOH 51
66 Parte - C Parametri di corsa: 4 C, potenza costante (8 W per 15 ore oppure 15 W per 7 ore, per un vassoio da 100 ml) Le bande verdi vengono raccolte ed eluite attraverso appositi filtri. Soluzione di eluizione: Hepes/KOH ph 7.5 DM 50 mm 0.06% (W/V) Il gradiente di ph viene determinato raccogliendo campioni di gel a varia distanza dall estremità del vassoio: si determina quindi una retta di regressione che permette di determinare i valori di pi delle bande verdi raccolte. 52
67 Materiali e Metodi Pagina 53 I.2 CROMATOGRAFIA SU COLONNA A SCAMBIO ANIONICO I pigmenti aspecifici che rimangono adesi al complesso ricostituito dopo la centrifugazione in gradiente di saccarosio possono essere eliminati pressoché completamente tramite cromatografia a scambio anionico a media pressione. Una colonna di tipo EMD-DEAE 650 Fractogel (10 x 150 mm) (Merck) viene equilibrata col Tampone A per circa un'ora ad un flusso di 1 ml/min. Quindi viene iniettato il campione concentrato in modo da non superare la capacità massima della colonna (max 1mg. di proteina). Un programma automatizzato prevede tre fasi o segmenti durante lo sviluppo della colonna: 1h: il campione entra in colonna insieme al Tampone A; la proteina, carica negativamente, si lega alla matrice; i pigmenti liberi non vengono trattenuti dalla colonna e quindi ne escono; 20': diminuisce gradualmente la concentrazione di Tampone A e proporzionalmente aumenta il Tampone B. A una concentrazione specifica di NaCl (500 mm per LHCII) il controione Cl - sostituisce la proteina nel legame con la matrice. Il complesso pigmentato viene quindi eluito in un volume di pochi ml. 40': il Tampone B fluisce in colonna; ciò completa l'eluizione e pulisce la colonna da ogni residuo proteico. Le frazioni in uscita, prima di essere inviate all'apposito raccoglitore, vengono analizzate da un rivelatore UV e l'andamento dell'assorbanza nel tempo è visualizzato graficamente. La cromatografia si svolge in stanza fredda, a 4 C, per evitare la degradazione dei pigmenti indotta dal calore. Tampone A: 50 mm Tris ph 7.4, % DM Tampone B: 500 mm NaCl, Tris 50 mm ph 7.4, % DM 53
68 Parte - C I.3 ESTRAZIONE DEI PIGMENTI CON ACETONE 80% [29] Goodwin T. W.(1981) Chem. and Biochem. of Plant Pigments, vol. 2 pag.3-4,18 Alle foglie di mais o spinacio, congelate in azoto liquido e rapidamente triturate con un pestello, viene aggiunto acetone 80% tamponato con MgCl 2. Dopo aver ben mescolato, il tutto viene lasciato in ghiaccio per 10', quindi centrifugato per 15' a X g e il pellet riestratto finché non sia quasi bianco. Alternativamente i pigmenti totali possono essere ricavati da preparati di tilacoidi o BBY, trattati anch'essi con acetone 80% tamponato. La stessa procedura a partire da foglie o da tilacoidi del mutante Chlorina f2 ci consente di ottenere clorofilla a e β-carotene senza contaminazioni da clorofilla b. All'estratto in acetone vengono aggiunti 0.8 volumi di NaCl 0.33 M e 0.25 volumi di dietiletere; la miscela viene agitata al vortex e successivamente lasciata riposare in ghiaccio in modo che si ottenga la separazione di fase. In alcuni casi per migliorare la separazione può essere utile centrifugare per alcuni minuti, eliminando così le emulsioni. I pigmenti, che si trovano nella fase superiore di dietiletere, vengono lavati per 2 volte con acqua, per eliminare i sali; quindi sono distribuiti in aliquote uguali in tubi eppendorf e fatti seccare sottovuoto nell'evaporatore rotante. Tutta la procedura è svolta avendo cura di non esporre i pigmenti alla luce, al calore o al contatto con l'ossigeno. I pigmenti liofilizzati sono conservati a -80 C in atmosfera di azoto. 54
69 Materiali e Metodi Pagina 55 I.4 ESTRAZIONE DEI CAROTENOIDI TRAMITE SAPONIFICAZIONE A FREDDO [15] Britton and Goodwin (1971) Meth. Enzym. 244 pag [29] Goodwin T.W.(1981) Chem. and Biochem. of Plant pigments, vol. 2 pag Alle foglie di mais o di spinacio, congelate in azoto liquido e rapidamente triturate con un pestello, viene aggiunto etanolo 96%. Dopo aver ben mescolato, si lascia in ghiaccio per qualche minuto; quindi si centrifuga a X g per 15'. Il sovranatante viene filtrato con filtro Nalgene 0.4 mm e successivamente lasciato incubare per ore con 0.1 volumi di KOH 80 % a 4 C. Quindi si aggiungono 2 volumi d' acqua e 1 volume di dietiletere, si mescola e si lasciano separare le due fasi.la fase superiore di dietiletere, in cui sono solubilizzati i carotenoidi, viene prelevata e lavata per 3-4 volte con acqua, per togliere i sali. Le separazioni di fase e i lavaggi sono seguiti da una breve centrifugazione, per eliminare le eventuali emulsioni. Infine l'estratto in dietiletere viene distribuito in aliquote uguali e liofilizzato sotto vuoto nell'evaporatore rotante. Durante tutta la procedura i pigmenti devono essere protetti dalla luce, dal calore e dal contatto con l'ossigeno per evitarne la degradazione. I carotenoidi sono conservati a -80 C in atmosfera di azoto. 55
70 Parte - C I.5 PURIFICAZIONE E ANALISI DEI PIGMENTI [27] Gilmore A. M., Yamamoto H. T. (1991) J. Chromatography 543, pag I.5.1 HPLC Le clorofille a e b pure e le singole specie di carotenoidi sono state ottenute per mezzo di comatografie preparative in HPLC seguendo il metodo di Gilmore e Yamamoto, usando una colonna C18 bondclone (7.3 x 300mm) in fase inversa. I pigmenti, raccolti all'uscita dalla colonna, sono stati seccati sottovuoto nell'evaporatore rotante e quindi conservati a -80 C in atmosfera di azoto. La composizione in pigmenti dei complessi ricostituiti è stata analizzata dopo estrazione con acetone 80% tramite RPHPLC seguendo anche in questo caso il metodo di Gilmore e Yamamoto. Tampone A: acetonitrile metanolo Tris-HCl 0.1M 86.8 % (72 parti) 9.6 % (8 parti) 3.6 % (3 parti) Tampone B: metanolo esano 80 % (4 parti) 20 % (1 parte) 56
71 Materiali e Metodi Pagina 57 I.5.2 Determinazione della concentrazione dei pigmenti [20] Davies T. H. (1965) Carotenoids, in Chem. and Biochem. of Plant Pigments (Goodwin T. J., ed.) (1981) Vol. 2, pag [52] Porra R. J. et al. (1989) Bioch. et Biophysica Acta 975, pag La concentrazione dei pigmenti è stata determinata spettroscopicamente seguendo le leggi di Porra et al. (1989) per le clorofille e usando i coefficienti specifici di estinzione di Davies per le xantofille pure. Formule di Porra: Chl a: x A663.6 nm-2.55 x A646.6 nm Chl b: x A646.6 nm x A663.6 nm Chl a + Chl b: x A646.6 nm x A663.6 nm Coefficienti di estinzione di Davies: E 1% 1 cm luteina (l=445 nm) = 2550 E 1% 1 cm violaxantina (l=443 nm) = 2550 E 1% 1 cm neoxantina (l=439 nm) = 2243 E 1% 1 cm b-carotene (l=453 nm) = 2620 Legge di Lamber-Beer: C [g/100 ml ] = (OD/ E 1% 1 cm ) x b b (cammino ottico) = 1 cm La concentrazione delle miscele di carotenoidi totali è stata stimata sulla base del coefficiente di estinzione percentuale medio di 2500 a 440 nm (Davies, 1965). 57
72 Parte - C I.6 ULTRACENTRIFUGAZIONE IN GRADIENTE [19] Dainese P. et al. (1990) Photochem. Photobiol. 51, pag I.6.1 Gradienti di saccarosio I gradienti di saccarosio 0.2 M-1.0 M vengono preparati con un formatore di gradienti. Questo apparecchio è costituito da due contenitori cilindrici collegati tra loro mediante un tubo fornito di una valvola. Nelle due camere sono contenute le soluzioni pesante (1 M saccarosio ) e leggera ( 0.2 M saccarosio ) le quali vengono mescolate in proporzioni tali che la miscela in uscita sia via via arricchita del componente più leggero. Nella soluzione sono presenti anche DM allo 0.06% (w/v) e 10 mm Hepes/KOH ph 7.5. I gradienti vengono centrifugati per ore a X g (rotore Beckman SW 41). I.6.2 Gradienti di glicerolo Anche i gradienti di glicerolo 15 % - 40 % sono stati ottenuti con un formatore di gradienti. Le due camere contengono le soluzioni pesante (40 % glicerolo w/v) e leggera (15 % glicerolo w/v ). Nelle soluzioni sono presenti anche DM allo 0.06 % e10 mm Hepes ph 7.5. I gradienti vengono centrifugati per ore a X g (rotore Beckman SW 60). 58
73 Materiali e Metodi Pagina 59 I.7 PROCEDURA DI RICOSTITUZIONE [51] Plumley F. G., Schmidt G. W. (1987) Proc. Natl. Acad. Sci. USA 84, pag [48] Paulsen H., Rümler U. and Rüdiger W. (1990) Planta 181, pag [17] Cammarata K. V., Schmidt G. W. (1991) Biochemistry vol. 31, n.10, pag [28] Giuffra et al.(1996) Eur.J.Biochem. 238: I pigmenti liofilizzati sono solubilizzati in etanolo, in modo che quest' ultimo non superi il 7% del volume finale della reazione; quindi vengono aggiunti sotto vortex al Tampone di Ricostituzione, che contiene già DTT 10 mm. Nel frattempo una quantità di proteina tale da ottenere un rapporto proteina/volume totale di 0.35 mg/ml viene denaturata, bollendo per 1'30'', prima di essere aggiunta alla miscela di ricostituzione. Infine i campioni vengono sonicati per 5'. Seguono tre cicli più o meno prolungati di graduale congelamento a -80 C e scongelamento a temperatura ambiente. Per sostituire il detergente, al termine dei cicli, si aggiunge ai campioni octilglucoside (OGP) 1% finale e, dopo 15' di incubazione in ghiaccio, KCl 150 mm finale. Si lascia la reazione in ghiaccio per 30' circa, quindi si precipitano i sali centrifugando per 15' a rpm in Minifuge. Si ottiene un pellet bianco con un sottile strato verde sopra e un surnatante limpido che verrà successivamente caricato su gradiente di saccarosio. Tampone di Ricostituzione (2%LDS, 12.5% saccarosio, 5 mm acido amminocaproico, 1 mm benzamidina, 100 mm Hepes KOH ph 8) 59
74 Parte - C II. II.1 SPETTROSCOPIA ASSORBIMENTO Gli spettri di assorbimento nel visibile da 350 nm a 800 nm della proteina nativa e dei complessi ricostituiti sono stati registrati a temperatura ambiente con uno spettrofotometro SLM-AMINCO DW-2000 con cuvette di quarzo di cammino ottico pari a 1 cm. La velocità di scansione dello strumento è di 100 nm/sec.; l ampiezza di banda è di 1 nm e l intervallo di rilevamento dei dati di 0.4 nm. Gli spettri di assorbimento dei campioni preparati per le misure di dicroismo lineare, sono stati acquisiti con lo stesso strumento usato per LD. E infatti possibile convertire l amplificatore di tale strumento in modo da consentire l acquisizione dello spettro di assorbimento nelle stesse condizioni utilizzate per gli spettri di LD, utilizzando quindi lo stesso campione e la stessa ottica II.2 FLUORESCENZA Gli spettri di emissione e di eccitazione di fluorescenza sono stati misurati a temperatura ambiente con un fluorimetro JASCO FP-777, con un ampiezza di banda di 5 nm e un intervallo di rilevamento dei dati di 0.5 nm. La velocità di scansione dello strumento è di 100 nm/sec. Gli spettri di emissione di fluorescenza sono stati registrati nell intervallo tra 600 e 800 nm, eccitando a 440 oppure a 475 nm. Gli spettri di eccitazione di fluorescenza, misurati eccitando nell intervallo tra 350 e 550 nm, sono stati rilevati con emissione a 680 nm. È stato usato un filtro giallo OG530 (SCHOTT) per eliminare le interferenze di secondo ordine. 60
75 Materiali e Metodi Pagina 61 II.3 DICROISMO CIRCOLARE Gli spettri di dicroismo circolare sono stati effettuati a 4 C con un dicrografo modello JASCO 600.Tutti gli spettri sono stati registrati in presenza di DM 0.06%. II.4 STABILITA DELLE PROTEINE MUTANTI La stabilità delle proteine mutanti è stata valutata attraverso la cinetica di degradazione nel tempo ad alta temperatura seguita con dicroismo circolare. I pigmenti liberi, o non ordinati, presentano segnale CD trascurabile; i pigmenti vicini ed orientati in modo fisso, invece, danno luogo ad un forte segnale CD di accoppiamento. E perciò possibile seguire la denaturazione di una proteina che coordina cromofori seguendo l estinzione del segnale di dicroismo circolare dei cromofori stessi. Il campione viene posto nello strumento con cella termostatata a 60 C, e si acquisisce uno spettro ogni 2 minuti della regione compresa fra nm: tale regione comprende il maggior picco negativo dello spettro CD di CP29. Il decadimento dell area di tale picco viene interpolato con una funzione di decadimento esponenziale singolo. Viene in tal modo determinato parametro τ: il tempo di un decadimento esponenziale, che può essere un buon indice della stabilità della proteina. II.5 DICROISMO LINEARE ( VEDI APPENDICE A) Gli spettri di dicroismo lineare a 300 e 100 K sono stati registrati, nel modo descritto da Haworth et al. [31], presso il Centro di Studi Nucleari Saclay, 61
76 Parte - C Parigi. Per orientare i campioni abbiamo impiegato la tecnica di compressione di gel di poliacrilamide. Con lo stesso strumento è stato possibile, inoltre, acquisire gli spettri di assorbimento dei campioni nelle stesse condizioni impiegate per gli spettri di LD. L intervallo di lunghezze d onda è compreso fra 380 nm e nm, con 2 nm di larghezza della banda passante e 0.2 nm di intervallo di scansione. 62
77 Materiali e Metodi Pagina 63 III. III.1 SOFTWARE MAXSPROUT Questo programma, disponibile come servizio telematico al sito dell EMBL, consente di ricostruire le catene laterali degli aminoacidi in una struttura proteica a partire dalle coordinate dei carboni α. III.2 SWISS-PDB VIEWER 2.6 Programma che consente di visualizzare, manipolare e modellare per omologia le strutture proteiche. Disponibile presso il sito internet III.3 PROGRAMMA PER IL CALCOLO GEOMETRICO SULLE STRUTTURE PROTEICHE La natura delle analisi svolte in questa tesi ha reso necessario lo sviluppo di un software che permettesse di ottenere rapidamente qualsiasi informazione di tipo geometrico a partire dalla struttura della proteina. Figura 20 CP29 come appare nel programma R3D 63
78 Parte - C La procedura creata consente la visualizzazione di file di coordinate in formato PDB (Protein Data Bank) con una avanzata capacità di selezione e manipolazione delle varie parti della struttura. Direttamente dall interfaccia grafica (completa di prospettiva, gestione dell intensità del colore in funzione della distanze, libera rotazione in 3D) è possibile ottenere le componenti di qualsiasi versore fra due atomi; alla creazione dei versori è possibile imporre dei vincoli per il piano di giacenza e per l angolo fra i due atomi di partenza. La procedura è scritta con Microsoft Visual Basic 5.0 per Windows 95, una versione compilata di tale programma è disponibile presso l autore di questa tesi. III.4 PROGRAMMA PER LA NORMALIZZAZIONE DEGLI SPETTRI DIFFERENZIALI DI ABS E LD Per normalizzare gli spettri di LD di ciascun mutante con quello del WT, non è possibile utilizzare lo stesso metodo usato per gli spettri di Assorbimento 64
79 Materiali e Metodi Pagina 65 (transizione totale). In questo caso infatti l ampiezza del contributo di ogni singolo cromoforo allo spettro dipende dall angolo del momento della transizione del cromoforo stesso con la normale al piano di orientamento dell esperimento. Inoltre il fatto che una componente possa essere sia positiva che negativa, complica la valutazione delle normalizzazioni effettuate. Per aggirare tali ostacoli ho ideato un programma che consente di normalizzare, anche se con un certo margine di errore, gli spettri di LD fra loro utilizzando le informazioni derivate dalle differenze tra lo spettro di assorbimento del WT e quello di ciascun mutante, dopo normalizzazione secondo la transizione totale. Sono partito dalla constatazione che lo spettro LD di un composto è uguale come forma allo spettro di Abs dello stesso, moltiplicato per una costante che tiene conto dell angolo fra il momento della transizione e la normale al piano di orientamento. Quindi, una volta normalizzato correttamente lo spettro LD di un mutante rispetto a quello del WT, la differenza fra questi darà uno spettro proporzionale punto per punto allo spettro differenza fra l Abs del WT e quello dello stesso mutante ottenuto dopo normalizzazione per la transizione totale. Sfruttando questa proprietà, l algoritmo procede per via iterativa all esplorazione di un intervallo di possibili fattori di normalizzazione. Per valutare la bontà di ciascun fattore provato, la procedura calcola per ognuno lo spettro differenza, lo normalizza a quello ottenuto per differenza fra i rispettivi spettri Abs e computa un parametro che tiene conto delle differenze esistenti fra i due spettri così ottenuti. Questo parametro che tiene conto delle differenze consiste nella sommatoria del valore assoluto della differenza punto per punto dei due spettri, normalizzata per l intensità del segnale di dicroismo lineare del WT. In tal modo è possibile identificare il fattore di normalizzazione che minimizza tali differenze e che quindi corrisponde al putativo fattore di normalizzazione cercato. 65
80 Parte - C Figura 21 Normalizzazione degli spettri differenziali di ABS e LD con la procedura sviluppata 66
81 Materiali e Metodi Pagina 67 Nella Fig. 21 sono mostrati due momenti del calcolo eseguito dalla procedura. Nel primo (A) è mostrata la situazione prima della normalizzazione: sono presenti lo spettro differenziale di assorbimento del mutante con il wt ( wtmutante, in rosso), lo spettro di LD del wt (in blu) e lo spettro di LD del mutante considerato (in verde). Le linee verticali rosse delimitano l intervallo in cui vuole svolgere l analisi. Nel secondo (B) è mostrata la situazione dopo normalizzazione. In rosso è presente ancora lo spettro differenziale di Abs del mutante con il wt (wtmutante) mentre in verde è rappresentato lo spettro differenziale di LD del mutante con il wt (wt-mutante), ottenuto dopo il calcolo del fattore di normalizzazione degli spettri mostrati nel riquadro precedente. La procedura cerca il fattore di normalizzazione che consente di ottenere questi due spettri differenziali simili il più possibile come forma. La procedura, scritta con Microsoft Visual Basic 5.0 per Windows 95, è in grado di leggere i file ASCII degli spettri necessari e calcola per via iterativa il fattore di normalizzazione, indicando direttamente le aree delle regioni degli spettri differenziali di dicroismo lineare e di assorbimento in cui è stata svolta l analisi. Una versione compilata di tale programma è disponibile presso l autore di questa tesi. 67
82 Parte - C 68
83 D. Risultati
84 Parte - D 70
85 Risultati Pagina 71 C ome introdotto nella sezione Scopo della tesi, abbiamo cercato di ottenere informazioni sulle proprietà spettroscopiche dei singoli cromofori legati alla proteina antenna esaminando proteine ricombinanti in cui fosse stato eliminato, volta per volta, un singolo cromoforo. Queste proteine ricombinanti sono state ottenute operando per ciascuna una mutazione puntiforme nella sequenza primaria a seguito della quale un residuo in grado di legare un cromoforo è stato sostituito con uno non legante. In questa prima parte del lavoro abbiamo valutato le caratteristiche delle proteine mutate per stabilire se fossero utilizzabili come strumento di investigazione per le caratteristiche della proteina nativa; a questo scopo abbiamo calcolato la loro stabilità I. STABILITA DELLE PROTEINE MUTANTI I.1 MUTANTI Le proteine ricombinanti di CP29 ricostruite derivano da mutazioni puntiformi in cui si è cercato di modificare, volta per volta, ciascun sito di coordinazione delle molecole di clorofilla. A questo scopo è stato necessario sostituire uno o più residui della sequenza originale con altri che da un lato non permettessero più la coordinazione del cromoforo, dall altro non modificassero eccessivamente la proteina per non influenzare il folding e la stabilità. 71
86 Parte - D Proteina Chl Differenze nello spettro Chl Totale Car. Totali Chl /Car Chl a/ Chl b n Chl a n Chl b OD max nel rosso CP29 WT 8 2 4,00 3, ,77 H245L B ,50 3,12 5,3 1,7 1,64 H216F A 2 678,5 6,2 (7*) 2 (2,3*) 3,10 2,53 4,45 (5*) 1,75 (2*) 1,03 H114F A 5 678, ,47 2, ,67 Q230L A , ,45 2,28 4,8 2,1 1,29 E111V^R218L A 4 677,5 7,7 (7*) 2 (1,8*) 3,85 2,50 5,5 (5*) 2,2 (2*) 1,66 499(+) E166V B 6 640, * 1,1* 6,12 4,80 5,76* 1,2* 0,80 E166Q B 6 3,27 2,56 0,80 E174V A 6 679, * 1,5* 4,75 2,52 5* 2* 1,40 R116L^E213V a 1? nr nr nr Nr nr nr nr nr Tabella 5 Contenuto in pigmenti del CP29 wt e dei complessi mutati. (*): in questi casi il contenuto in carotenoidi è stato influenzato dalla mutazione; per questo motivo consideriamo 7 molecole di Chl presenti nella proteina mutata I.2 STABILITA DEI COMPLESSI A 4 C E TEMPERATURA AMBIENTE L impiego dei mutanti nello studio dei VMT nell antenna minore CP29 ha imposto la necessità di valutare la stabilità di tali complessi ricombinanti. I complessi mutanti di CP29 sono sufficientemente stabili a temperatura ambiente ed a 4 C. Le proteine tenute al buio e ad una temperatura di 4 C mantengono inalterate le loro proprietà spettroscopiche di assorbimento e CD per oltre 24h; a temperatura ambiente questo valore si riduce ad 8h. Il tempo necessario per l analisi di ciascun mutante rientra, con un buon margine, entro questi valori, quindi le informazioni che otteniamo sono da considerare attendibili e non distorte da fenomeni di instabilità. 72
87 Risultati Pagina 73 I.3 VALUTAZIONE DELLA STABILITA DI OGNI PROTEINA MUTANTE Per valutare la stabilità relativa di ogni proteina mutante ricostituita, abbiamo seguito la cinetica di denaturazione a temperatura selettiva attraverso misure di dicroismo circolare (vedi C-II.4). Spettro 2 Prova stabilità CP29 wt 73
88 Parte - D Spettro 3 Prova stabilità proteina CP29 H216F Spettro 4 Prova stabilità proteina CP29 Q230L 74
89 Risultati Pagina 75 Spettro 5 Prova stabilità proteina CP29 E111V^R218L Spettro 6 Prova stabilità proteina CP29 H114F 75
90 Parte - D Spettro 7 Prova stabilità proteina CP29 E174V Spettro 8 Prova stabilità proteina CP29 E166V 76
91 Risultati Pagina 77 Spettro 9 Prova stabilità proteina CP29 H245L Spettro 10 Riepilogo stabilità mutazioni 77
92 Parte - D COMPLESSI DECADIMENTO ESPONENZIALE (min.) CP29wt 4.23 H216F 6.98 Q230L 1.70 E111V^R218L 3.35 H114F 0.51 E174V 1.34 E166V 0.89 H245L 2.01 Tabella 6 Riepilogo stabilità proteine ricostituite. Tempi di 1 decadimento esponenziale I risultati di queste analisi ci dicono che i valori della stabilità dei complessi mutanti ricostituiti sono dello stesso ordine di grandezza del valore della proteina nativa. Questo risultato giustifica un impiego di tali mutanti nella caratterizzazione, attraverso una analisi differenziale, delle proprietà dei singoli cromofori presenti in CP29. Inoltre, si può vedere che le singole mutazioni influiscono diversamente la stabilità del complesso e che in alcuni casi i residui leganti la clorofilla hanno anche una funzione di stabilizzare la struttura secondaria della proteina nei domini interessati. Queste valutazioni verranno discusse nella sezione Discussione. 78
93 Risultati Pagina 79 II. II.1 COSTRUZIONE DEL MODELLO DATI DISPONIBILI Le informazioni disponibili per la costruzione di un modello strutturale di CP29, sono le coordinate dei carboni α dei residui aminoacidici dei domini idrofobici della proteina. Inoltre sono state ottenute le coordinate per i 12 anelli tetrapirrolici e le 2 xantofille in LHCII [36]. L'esatta posizione delle catene laterali di ciascun residuo aminoacidico e quella dei loops che connettono le eliche non sono fattori indispensabili per l interpretazione dei dati di dicroismo lineare, comunque, la loro ricostruzione è importante per Figura 22 Dati disponibili da K. [36] di LHCII: Cα, struttura dei tetrapirroli e delle valutare la bontà del modello. In xantofille particolare, ci aspettiamo che i residui coinvolti nella coordinazione delle molecole di clorofilla, evidenziati da esperimenti di mutagenesi sito-specifica, abbiano una disposizione spaziale compatibile con tale funzione. Nel seguito viene descritto di seguito il modo con cui è stato ottenuto il modello ed una breve valutazione dei risultati. II.2 RICOSTRUZIONE RESIDUI LATERALI CON MAXSPROUT Per tale operazione abbiamo utilizzato il programma MAXSPROUT disponibile come servizio telematico presso il server dell'embl. Tale 79
94 Parte - D programma è in grado di ricostruire le catene laterali di una struttura dai Cα dei residui coinvolti. Figura 23 Rappresentazione della struttura di LHCII dopo la ricostruzione dei residui laterali con MAXPROUT E stato necessario eliminare dal file PDB della struttura di partenza, i riferimenti agli eteroatomi (di cui il programma MAXSPROUT non tiene conto per la computazione). Sono stati tolti quindi tutti i riferimenti alle molecole di clorofilla e di xantofilla presenti. Il risultato di questa operazione è una struttura completa (file PDB) dei residui delle eliche transmembrana di LHCII in cui i Cα sono mantenuti come posizione rispetto a quelli della struttura originaria. II.3 MUTAZIONE RESIDUI SU SEQUENZA CP29 Sulla struttura ottenuta dall elaborazione con MAXSPROUT è possibile modellare per omologia la sequenza di CP29. L allineamento delle sequenze delle regioni trans-membrana di CP29 e LHCII, necessario per la costruzione del modello, è stato ottenuto con CLUSTAL. L analisi ha rivelato un elevato grado di omologia soprattutto nelle regioni delle α-eliche che sono coinvolte nella coordinazione delle molecole dei cromofori. 80
95 Risultati Pagina 81 LHCII - helix B CP29 - PETFSKNRELEVIHSRWAMLGALGCVFPELLSR VFGLQRFRECELIHGRWAMLATLGALSVEWLTG.. ** *.**.*****..**. * *. 42% identity LHCII - helix C CP29 SILA-IWATQVVLMGAVEGYRI SISTLIW-IEVLVIGYIEFQRN **. **..*...*.* * 38% identity LHCII - helix A CP29 PEAFAELKVKELKNGRLAMFSMFGFFVQAI PEKKERLQLAEIKHARLAMVAFLGFAVQAA **. *.. *.*..****...** *** 47% identity LHCII - helix D CP29 PLENLADHLA PLNNWATHLS **.* *.**. 50% identity Tabella 7 Allineamento di sequenza da Mais delle quattro eliche note nella struttura di LHCII utilizzato nella costruzione del modello di CP29 Per la costruzione del modello è stata impiegata la funzione Mutation dell applicazione SWISS-PDB VIEWER, un programma di visualizzazione ed elaborazione dei file PDB (disponibile presso GENEVA BIOMEDICAL RESEARCH). Tale funzione consente di sostituire le catene laterali del residuo aminoacidico interessato senza modificare l'angolo phi e psi dello stesso all'interno della struttura e conservando il più Figura 24 Rappresentazione della possibile la disposizione della struttura di CP29 ottenuta dopo elaborazione della sequenza catena laterale. Il risultato di questa operazione è un modello strutturale completo della parte proteica di CP29. 81
96 Parte - D II.4 REINSERIMENTO ETEROATOMI NEL PDB Il passo successivo consiste nel completare la struttura: la componente proteica ottenuta va integrata con quella dei pigmenti. Dato che le posizioni dei Cα della struttura originaria non sono variate, è sufficiente reintrodurre i riferimenti dei cromofori direttamente nel file PDB utilizzando le stesse coordinate degli anelli tetrapirrolici e delle xantofille di LHCII. In CP29 sono presenti solo 8 delle 12 molecole di clorfilla presenti in LHCII. Una analisi della struttura re-integrata con tutti i pigmenti di LHCII mostra che gli 8 residui identificati come ligandi in CP29. Attraverso esperimenti di mutagenesi sito-specifica, sono in posizione ideale per la coordinazione della rispettiva Chl. Rimangono escluse 4 Chl che non hanno nessun residuo che le possa coordinare; queste sono state perciò eliminate dalla struttura. Figura 25 Modello di struttura di CP29 in cui sono stati reinseriti i riferimenti ai pigmenti. In rosso quelli che non trovano riscontro con gli esperimenti di mutagenesi sito-diretta e che sono stati perciò eliminati dalla struttura 82
97 Risultati Pagina 83 Figura 26 Rappresentazione del modello strutturale completo di CP29 Nel seguito si assume che le 8 molecole di Chl presenti in CP29 abbiano una posizione uguale alle corrispondenti molecole in LHCII. Questa assunzione non è completamente verificata in questa fase e si basa sull elevata omologia di sequenza tra le due proteine; verrà poi discussa alla luce dei dati sperimentali. II.5 VERIFICA DELLA CORRETTA COORDINAZIONE DELLE CLOROFILLE Il modello è stato verificato controllando la corretta coordinazione delle 8 clorofille presenti da parte dei residui conosciuti come responsabili. In ogni caso considerato esiste un riscontro corretto di tale coordinazione, che conferma la plausibilità del modello. Abbiamo scelto di non sottoporre la struttura ad altri raffinamenti con cilci MD o minimizzazioni energetica, sia per l'incompletezza del modello stesso 83
98 Parte - D che per la difficoltà nel lavorare con proteine contenenti un elevato numero di gruppi etero. La struttura rimane quindi solo un modello di massima in cui però le coordinate degli anelli tetrapirrolici conservati sono quelle ottenute sperimentalmente dai cristalli bidimensionali di LHCII; vista l'elevata omologia che esiste entro questa famiglia di proteine è ragionevolmente corretto impiegare tali informazioni strutturali per il calcolo dei VMT (versori dei momenti di transizione). 84
99 Risultati Pagina 85 Figura 27 Posizione dei residui implicati nella coordinazione delle 8 Chl di CP29 85
100 Parte - D III. STRATEGIA IMPIEGATA III.1 INFORMAZIONI NECESSARIE ALLA DETERMINAZIONE DEI VMT DI CHL ALL'INTERNO DI UNA STRUTTURA Le conoscenze attuali sull orientazione delle transizioni elettroniche delle Chl, rispetto ad un sistema di coordinate fisso con la molecola, vengono in larga parte da esperimenti di dicroismo lineare su soluzioni di Chl orientate in diversi sistemi. La principale transizione elettronica nella Chl ha il massimo di assorbimento a 670 nm, e viene chiamata Q Y. E stato mostrato che i momenti di tali transizioni giacciono sul piano dell anello tetrapirrolico; questi vengono convenzionalmente definiti da un angolo misurato in gradi in senso orario a partire dall'asse X dell anello tetrapirrolico. L'asse X è quello che passa per il carbonio C7 del pirrolo IV e per Figura 28 Momento della transizione Q Y della Chl a secondo Fragata [26] quello C3 del pirrolo II all'interno della struttura dell anello. Le orientazioni delle transizioni Q Y della Chl a e chlb sono state determinate sperimentalmente e si trovano, rispettivamente, a 20 e 29 dall asse Y [59] [26]. Esiste a questo proposito una ambiguità: non è stato specificato se questi valori sono ottenuti da rotazione in senso orario o antiorario dall asse Y della molecola. Si possono quindi ottenere i seguenti valori: 70 (Chl a) 61 (chlb) [26], oppure 110 (Chl a) e 119 (Chl b) [59]. Per determinare i VMT di più Chl all'interno di una stessa proteina, è necessario avere a disposizione la struttura risolta. Solo da questa, infatti, è 86
101 Risultati Pagina 87 possibile determinare, attraverso la risoluzione di sistemi di tipo geometrico, i versori di tali momenti relativi ad un sistema di coordinate fisso rispetto all'intera proteina e non più al singolo pigmento. III.2 LIMITI DELLA STRUTTURA ESISTENTE DI LHCII L'unica struttura attualmente disponibile per una antenna minore di piante superiori è quella di LHCII [36] ottenuta per microscopia elettronica su cristalli bidimensionali. Tale struttura è però incompleta ed a bassa risoluzione (3.4 Å). Non è stato possibile infatti, in tale esperimento, determinare la posizione in cui la catena del fitolo si connette al tetrapirrolo, né la posizione dell'anello V rispetto a quest ultimo in nessuna clorofilla. Ciascuna di queste due informazioni sarebbe di per se sufficiente per orientare l'anello tetrapirrolico e quindi identificare senza ambiguità l'asse X da cui calcolare i versori dei momenti di transizione (vedi fig. 25). L'assenza di tali elementi nella struttura di Kühlbrandt [36] rappresenta un serio ostacolo all'identificazione dei VMT. Senza tali riferimenti, infatti, i siti possibili di connessione fra la catena del fitolo e l'anello sono 8, a causa della doppia simmetria della struttura del tetrapirrolo (vedi fig. 26). Figura 29 Possibili siti di aggancio della catena fitilica. Inoltre, le combinazioni possibili dei versori crescono esponenzialmente con il numero di clorofille presenti all'interno della proteina: considerando le 12 clorofille di LHCII, le combinazioni possibili sono
102 Parte - D III.3 INFORMAZIONI CHE E' IN GRADO DI FORNIRE IL DICROISMO LINEARE La tecnica del dicroismo lineare su sistemi orientati è in grado di fornire un segnale che è direttamente proporzionale al quadrato del coseno dell'angolo esistente fra il versore del momento della transizione elettronica considerata e la normale al piano di orientamento nel sistema sperimentale. E' possibile fare del dicroismo lineare su complessi proteici orientati in membrane. Vi sono diversi problemi che impediscono di calcolare i VMT direttamente dal dicroismo lineare: i) in complessi proteici con più pigmenti, il segnale dicroico fornisce l'angolo fra il versore del momento della transizione elettronica del pigmento considerato e la normale al piano di orientamento ma non è in grado di dare alcuna informazione sull'angolo esistente fra VMT di pigmenti diversi. ii) sempre in caso di più pigmenti, si ha la sovrapposizione dei segnali dicroici di tutte le transizione considerate nella parte dello spettro interessata. iii) per l analisi è infine necessaria la normalizzazione dell ampiezza tra i diversi spettri LD ottenuti. Queste normalizzazioni non si possono ottenere per via sperimentale e costituiscono un serio limite nell ottenimento di informazioni utili da tale tecnica. Per ottenere il segnale isolato di una sola molecola di clorofilla all'interno di un aproteina come CP29 che ne coordina 8, vista l'impossibilità di ricostituire un mutante contenente un solo pigmento, abbiamo scelto di condurre le misure su una serie di mutanti puntiformi in cui manca volta per volta un solo cromoforo. Da queste misure si ottenengono le informazioni riguardanti il pigmento mancante attraverso un analisi differenziale fra lo spettro del WT e quello del mutante considerato dopo normalizzazione. 88
103 Risultati Pagina 89 III.4 STRATEGIA IMPIEGATA NEL CALCOLO Nella strategia che ho impiegato nel calcolo dei VMT, i dati che possono essere ricavati dal modello strutturale sono uniti a quelli sperimentali ottenuti dalle misure LD dei mutanti; in questo modo è possibile superare i limiti delle informazioni sui VMT che si possono ottenere da ciascuna di queste due fonti separatamente. Dal modello siamo in grado di calcolare tutti i possibili VMT di ciascun pigmento. Le caratteristiche spettroscopiche sono invece impiegate come vincoli per discriminare fra le diverse combinazioni possibili dei VMT. 89
104 Parte - D IV. DATI SPETTROSCOPICI DEI MUTANTI IV.1 NORMALIZZAZIONE DEGLI SPETTRI DI ASSORBIMENTO Per normalizzare lo spettro di assorbimento del CP29 WT rispetto a quello ottenuto da ciascun mutante, sono state valutate diverse strategie. In tutti i casi prendiamo in considerazione solo una regione dello spettro che va da 630 a 720 nm, in modo da eliminare il contributo delle transizioni secondarie delle clorofille (Q X, nm per Chl a e nm per Chl b), e la regione di Soret dello spettro in cui intervengono anche gli assorbimenti dei carotenoidi. Spettro 11 Assorbimento del CP29 wild type nell intervallo tra nm (riquadro) ed in quella utilizzata per l analisi nm. Uno dei metodi più comuni per normalizzare prevede l impiego come riferimento di uno dei due picchi principali nel rosso: 640 o 667 nm. A seconda che la mutazione riguardi una clorofilla a od una clorofilla b, si prende come riferimento il picco di cui è responsabile l altra forma 90
105 Risultati Pagina 91 considerando nullo l effetto della mutazione su tale zona dello spettro. Questo approccio non ha portato però a risultati accettabili (vedi spettro 12). Anche perché alcuni siti sono occupati in maniera eterogenea: sia Chl a che Chl b possono occupare il sito benchè con probabilità diverse [28, 45]. Spettro 12 Normalizzazione effettuata sui massimi di assorbimento dei campioni impiegati (spettro differenziale non soddisfacente) In un altro tentativo è stata utilizzata la deconvoluzione dello spettro in gaussiane per cercare le componenti dello spettro che rimangono invariate nel WT e nei mutanti, su cui poter normalizzare. Anche in questo caso non è possibile identificare forme con tali caratteristiche, e tutti i tentativi hanno portato a normalizzazioni non soddisfacenti (vedi spettro 13). 91
106 Parte - D Spettro 13 Normalizzazione effettuata su una componente (indicata da una freccia), ritenuta non variabile, della deconvoluzione in gaussiane degli spettri I risultati migliori si sono ottenuti normalizzando invece per l area della transizione complessiva. Questa può essere ottenuta considerando il numero esatto di Chl a e di Chl b nel campione e tenendo conto del fattore di correzione per il coefficiente di estinzione molare delle due forme. Il numero preciso di Chl a e Chl b nel campione può essere ottenuto attraverso analisi per HPLC dello stesso [28, 49] (vedi D-I.1). Per verificare la bontà della normalizzazione, si calcolano tutti gli spettri differenza fra WT e ciascun mutante. Gli spettri ottenuti sono in tutti i casi sempre positivi (ci sono due eccezioni ma solo nella regione terminale dello spettro dovute alla deriva della linea di base; vedi spettro 14) e si possono scomporre in poche gaussiane con base pari a zero (vedi spettro 15). 92
107 Risultati Pagina 93 Spettro 14 Analisi differenziale degli spettri dei mutanti, riferiti a quello del wt, dopo normalizzazione per la transizione totale Spettro 15 Deconvoluzione in gaussiane dello spettro differenziale di CP29wt e CP29E174V 93
108 Parte - D IV.2 NORMALIZZAZIONE DEGLI SPETTRI DI DICROISMO LINEARE Per la normalizzazione degli spettri di LD di ciascun mutante rispetto a quello del wt, non è possibile applicare lo stesso metodo usato per gli spettri di assorbimento. In questo caso, infatti, l ampiezza del contibuto di ogni componente allo spettro dipende dall angolo del momento della transizione elettronica del cromoforo stesso con la normale al piano di orientamento dell esperimento. Inoltre, il fatto che una componente possa essere sia positiva che negativa, complica la valutazione delle normalizzazioni effettuate. Per aggirare tali ostacoli è stato ideato un programma che consente di normalizzare, anche se con un certo margine di errore, gli spettri di LD fra di loro utilizzando informazioni derivate dalle differenze tra spettri di assorbimento del wt e quello di ciascun mutante dopo normalizzazione secondo la transizione totale (vedi C-III.4). Una verifica dei risultati di tale metodo di normalizzazione si ottiene calcolando la differenza degli spettri LD fra il WT e ciascun mutante e valutando gli spettri ottenuti per la loro possibilità di essere deconvoluti in poche gaussiane simmetriche tutte positive o negative. Tutti gli spettri differenza ottenuti risultano completamente positivi o completamente negativi (nella regione in cui è stata svolta la computazione del fattore di normalizzazione). IV.3 NORMALIZZAZIONE TRA LD E ABS Infine è necessario anche normalizzare gli spettri differenza di Abs con quelli differenza di LD. In realtà, visto che entro questi due gruppi gli spettri sono già normalizzati fra loro, è sufficiente trovare il fattore di normalizzazione per uno solo degli spettri di Abs con il rispettivo LD. Questo risulta però 94
109 Risultati Pagina 95 impossibile dal momento che l intensità dell intero spettro LD dipende dal grado di orientamento delle molecole nella preparazione misurata che varia da esperimento ad esperimento. Lasciamo quindi questo Fattore di Normalizzazione F N come una incognita dell intero sistema. 95
110 Parte - D V. CALCOLO DEGLI ANGOLI TRA I VMT E LA NORMALE ALLA MEMBRANA V.1 RELAZIONE TRA ABS E LD Per calcolare gli angoli esistenti tra i VMT e la normale alla membrana, è necessario conoscere la relazione che intercorre tra gli spettri di assorbimento di un campione, e quelli di dicroismo lineare dello stesso. La relazione tra l intensità del segnale di dicroismo lineare e quella del relativo assorbimento, nel caso di complessi proteici orientati in una membrana ideale, è data da [30]: LD A = 3 (1 3cos 2 ) 2 ϕ = A A Questa è l equazione utilizzata per membrane planari orientate contenenti dipoli di assorbimento con angoli ben definiti rispetto al piano della membrana stessa. Data l impossibilità di normalizzare gli spettri di assorbimento con quelli di dicroismo, è necessario aggiungere a tale relazione un fattore moltiplicativo che chiamiamo F N : LD A = 3 (1 3cos 2 ) 2 ϕ = A A F N Il segnale di dicroismo lineare e quello di assorbimento impiegato in tale calcolo è quello dell area sottoscritta dalla regione dello spettro coinvolta nella transizione, cioè quella utilizzata dalla procedura di normalizzazione. 96
111 Risultati Pagina 97 V.2 RIDUZIONE DELLE SOLUZIONI POSSIBILI SULLA BASE DELLA STRUTTURA PROTEICA Per semplificare i calcoli ed eliminare i problemi dovuti alla doppia simmetria dell anello tetrapirrolico (vedi D-III.2) è necessario ridurre i possibili siti di connessione della catena del fitolo con gli anelli delle clorofille (e quindi delle possibili orientazioni dei VMT). A questo scopo è utile indagare sul comportamento di tale catena in altri sistemi fotosintetici, come quello batterico (vedi A-III.2). LHII di sistemi fotosintetici batterici, sono stati cristallizzati ed è disponibile la loro struttura completa ad alta risoluzione [42, 40] in cui è possibile osservare la disposizione delle catene dei fitoli. In questi sistemi si ritrovano due diverse disposizioni di clorofille: alcune giacciono su un piano parallelo a quello della membrana; queste non trovano alcun riscontro nella struttura delle piante superiori. Altre Chl sono invece disposte più o meno lungo la normale alla membrana come nel caso delle Chl della struttura di LHCII di piante superiori. Le catene dei fitoli di tali clorofille sono invariabilmente connesse all anello nella parte della clorofilla che guarda verso l interno della membrana. Da qui le catene dei fitoli puntano dritte verso Figura 30 Disposizione dei fitoli nella truttura di LHII di R. acidophila il centro della membrana dove solitamente si piegano a 90 per proseguire parallelamente al piano di quest ultima. Questo comportamento è spiegabile in base all esistenza di un gradiente di idrofobicità nella membrana e che raggiunge il massimo al centro di essa. I siti possibili di connessione del fitolo all anello che puntano verso l esterno della membrana sono perciò estremamente sfavoriti, in quanto il la catena 97
112 Parte - D fitilica non avrebbe lo spazio sufficiente per ripiegarsi e rientrare nella membrana: si troverebbe quindi in una regione polare sfavorita. Su tali basi si possono non considerare come siti possibili di connessione quelli rivolti verso l esterno; in tutti i casi considerati sul modello di CP29 c è una netta distinzione fra siti esterni ed interni che ha consentito una agevole valutazione di quelli da scartare poiché nessuna Chl giace al centro del doppio strato lipidico Al fine del calcolo considereremo solo 4 possibili siti di connessione del fitolo all anello tetrapirrolico. V.3 RISULTATI V.3.1 Mutazione H216F Sito coordinante Chl A2 Spettro 16 Risultato della normalizzazione degli spettri differenziali di ABS e di LD della proteina H216F Intervallo nm Area ABS Area LD
113 Risultati Pagina 99 V.3.2 Mutazione E111V^R218L Sito coordinante Chl A4 Spettro 17 Risultato della normalizzazione degli spettri differenziali di ABS e di LD della proteina E111V^R218L Intervallo nm Area ABS Area LD
114 Parte - D V.3.3 Mutazione H114F Sito coordinante Chl A5 Spettro 18 Risultato della normalizzazione degli spettri differenziali di ABS e di LD della proteina H114F Intervallo nm Area ABS Area LD
115 Risultati Pagina 101 V.3.4 Mutazione E174V Sito coordinante Chl A6 Spettro 19 Risultato della normalizzazione degli spettri differenziali di ABS e di LD della proteina E174V Intervallo nm Area ABS Area LD In questo caso la normalizzazione non è stata effettuata nel picco principale in quanto in tale regione l algoritmo non trova nessuna soluzione. Nella regione del picco secondario è invece possibile trovare una soluzione valida che possiamo utilizzare in quanto è possibile assumere che sia la Chl a che la Chl b, che possono essere legate, conservino la medesima configurazione 101
116 Parte - D V.3.5 Mutazione H245L Sito coordinante Chl B3 Spettro 20 Risultato della normalizzazione degli spettri differenziali di ABS e di LD della proteina H245L Intervallo nm Area ABS Area LD Anche in questo caso l algoritmo non trova soluzioni per il picco principale. La regione utilizzata è quella compresa fra 630 e 640 nm, tale scelta è giustificata dal fatto che tale mutante coinvolge un sito legante una Chl b,che assorbe a questa lunghezza d onda (vedi tab. 5). 102
117 Risultati Pagina 103 V.3.6 Mutazione E166V Sito coordinante Chl B6 Spettro 21 Risultato della normalizzazione degli spettri differenziali di ABS e di LD della proteina E166V Intervallo nm Area ABS Area LD Nel caso della Chl B6, pur essendo preferenzialmente un sito per una Chl b, nella regione del picco principale è possibile trovare un ottima soluzione. L abbiamo considerata valida in quanto questo sito di legame ha una selettività non molto grande e può quindi legare anche Chl a. V.3.7 Mutante Q230L Chl A3 Tutti i tentativi di calcolo sugli spettri del mutante Q230L non hanno portato a risultati soddisfacenti. Sono stati eseguite misure spettroscopiche di assorbimento e di dicroismo lineare su più campioni provenienti da 103
118 Parte - D esperimenti di ricostituzione diversi. Gli spettri di LD di tali mutanti hanno dato un segnale basso e non riproducibile fra le diverse ricostituzioni. Anche se la stabilità di tale mutante non sembra tale da giustificare un tale comportamento (vedi D-I.3), si ritiene che l orientazione del cromoforo (data anche la posizione nella struttura proteica) non sia stabile, o, più verosimilmente che la mutazione induca una modificazione conformazionale che interferisce con l orientamento del campione durante le misure di LD. Figura 31 Posizione della Chl A3 (Mutante Q230L) nella struttura proteica Chl Abs LD A2 Mutante H216F 1,5 379 A4 Mutante E111V^R218L 1, A5 Mutante H114F 1, A6 Mutante E174V 0, B3 Mutante H245L 0,42 68 B6 Mutante E166V 1, Tabella 8 Riepilogo risultati della normalizzazione e dell analisi delle aree dei dati spettroscopici sperimentali 104
FOTOSINTESI: LA FASE LUMINOSA
 FOTOSINTESI: LA FASE LUMINOSA Un video : Clic Premessa (I) In questa lezione si esamina in dettaglio la serie di reazioni che trasformano l'energia solare in energia chimica fino alla sintesi di ATP e
FOTOSINTESI: LA FASE LUMINOSA Un video : Clic Premessa (I) In questa lezione si esamina in dettaglio la serie di reazioni che trasformano l'energia solare in energia chimica fino alla sintesi di ATP e
La fotosintesi: energia dal Sole
 La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
Figura 1. Rappresentazione della doppia elica di DNA e struttura delle differenti basi.
 Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
Classificazione dei Sensori. (raccolta di lucidi)
 Classificazione dei Sensori (raccolta di lucidi) 1 Le grandezze fisiche da rilevare nei processi industriali possono essere di varia natura; generalmente queste quantità sono difficili da trasmettere e
Classificazione dei Sensori (raccolta di lucidi) 1 Le grandezze fisiche da rilevare nei processi industriali possono essere di varia natura; generalmente queste quantità sono difficili da trasmettere e
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
4) PROTEINE FERRO ZOLFO. Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S.
 4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
Gli organismi viventi
 Gli organismi viventi Gli organismi viventi Quali caratteristiche contraddistinguono i viventi? È facile distinguere un organismo vivente da un oggetto non vivente? Gli organismi viventi Tutti gli organismi
Gli organismi viventi Gli organismi viventi Quali caratteristiche contraddistinguono i viventi? È facile distinguere un organismo vivente da un oggetto non vivente? Gli organismi viventi Tutti gli organismi
Il flusso dell informazione genetica. DNA -->RNA-->Proteine
 Il flusso dell informazione genetica DNA -->RNA-->Proteine Abbiamo visto i principali esperimenti che hanno dimostrato che il DNA è la molecola depositaria dell informazione genetica nella maggior parte
Il flusso dell informazione genetica DNA -->RNA-->Proteine Abbiamo visto i principali esperimenti che hanno dimostrato che il DNA è la molecola depositaria dell informazione genetica nella maggior parte
CHIMICA ORGANICA: IBRIDAZIONE & RISONANZA IBRIDIZZAZIONE. un atomo compie all atto di formazione di un composto al fine di formare un maggior
 CHIMICA ORGANICA: IBRIDAZIONE & RISONANZA IBRIDIZZAZIONE L ibridizzazione o ibridazione è una ricombinazione dei propri orbitali atomici che un atomo compie all atto di formazione di un composto al fine
CHIMICA ORGANICA: IBRIDAZIONE & RISONANZA IBRIDIZZAZIONE L ibridizzazione o ibridazione è una ricombinazione dei propri orbitali atomici che un atomo compie all atto di formazione di un composto al fine
Diversità tra i viventi
 Diversità tra i viventi PROPRIETÀ della VITA La CELLULA CLASSIFICAZIONE dei VIVENTI Presentazione sintetica Alunni OIRM Torino Tutti i viventi possiedono delle caratteristiche comuni Ciascun vivente nasce,
Diversità tra i viventi PROPRIETÀ della VITA La CELLULA CLASSIFICAZIONE dei VIVENTI Presentazione sintetica Alunni OIRM Torino Tutti i viventi possiedono delle caratteristiche comuni Ciascun vivente nasce,
Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose.
 Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose. 2.1 Spettro di emissione Lo spettro di emissione di
Capitolo 2 Caratteristiche delle sorgenti luminose In questo capitolo sono descritte alcune grandezze utili per caratterizzare le sorgenti luminose. 2.1 Spettro di emissione Lo spettro di emissione di
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
Determinazione della composizione elementare dello ione molecolare. Metodo dell abbondanza isotopica. Misure di massa esatta
 Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Relazioni statistiche: regressione e correlazione
 Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
UNIVERSITÀ DEGLI STUDI DI PADOVA Facoltà di Ingegneria sede di Vicenza A.A. 2007/08
 UNIVERSITÀ DEGLI STUDI DI PADOVA Facoltà di Ingegneria sede di Vicenza Corso di Disegno Tecnico Industriale per il Corso di Laurea triennale in Ingegneria Meccanica e in Ingegneria Meccatronica Tolleranze
UNIVERSITÀ DEGLI STUDI DI PADOVA Facoltà di Ingegneria sede di Vicenza Corso di Disegno Tecnico Industriale per il Corso di Laurea triennale in Ingegneria Meccanica e in Ingegneria Meccatronica Tolleranze
Polimeri semiconduttori negli OLED
 Polimeri semiconduttori negli OLED Nella figura viene mostrato uno schema di funzionamento di un Organic Light Emitting Diode (OLED). Il catodo e formato da un elettrodo di Alluminio (Magnesio o Calcio)
Polimeri semiconduttori negli OLED Nella figura viene mostrato uno schema di funzionamento di un Organic Light Emitting Diode (OLED). Il catodo e formato da un elettrodo di Alluminio (Magnesio o Calcio)
Genova 15 01 14 TIPOLOGIE DI LAMPADE
 Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
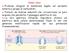 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Gruppo di Lavoro Scienze
 Gruppo di Lavoro Scienze Brainstorming a) acido ascorbico titolazioni b) acidità nei vari distretti dell apparato digerente c) zuccheri nelle bibite d) comportamento delle rocce e) meteorologia: guarda
Gruppo di Lavoro Scienze Brainstorming a) acido ascorbico titolazioni b) acidità nei vari distretti dell apparato digerente c) zuccheri nelle bibite d) comportamento delle rocce e) meteorologia: guarda
CONVENZIONE UNIVERSITÀ DI PERUGIA DELTATECH. Rapporto Attività di Ricerca. Prove ad impatto su laminati compositi con.
 CONVENZIONE UNIVERSITÀ DI PERUGIA DELTATECH Rapporto Attività di Ricerca Prove ad impatto su laminati compositi con Ball Drop Tester Prof. L. Torre Fase 1: Terni 18/6/214 METODI Sono stati effettuati test
CONVENZIONE UNIVERSITÀ DI PERUGIA DELTATECH Rapporto Attività di Ricerca Prove ad impatto su laminati compositi con Ball Drop Tester Prof. L. Torre Fase 1: Terni 18/6/214 METODI Sono stati effettuati test
SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA)
 SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA) ORGANIZZAZIONE TERZIARIA DEL DNA Il DNA cellulare contiene porzioni geniche e intergeniche, entrambe necessarie per le funzioni vitali della
SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA) ORGANIZZAZIONE TERZIARIA DEL DNA Il DNA cellulare contiene porzioni geniche e intergeniche, entrambe necessarie per le funzioni vitali della
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
Introduzione all analisi dei segnali digitali.
 Introduzione all analisi dei segnali digitali. Lezioni per il corso di Laboratorio di Fisica IV Isidoro Ferrante A.A. 2001/2002 1 Segnali analogici Si dice segnale la variazione di una qualsiasi grandezza
Introduzione all analisi dei segnali digitali. Lezioni per il corso di Laboratorio di Fisica IV Isidoro Ferrante A.A. 2001/2002 1 Segnali analogici Si dice segnale la variazione di una qualsiasi grandezza
Database. Si ringrazia Marco Bertini per le slides
 Database Si ringrazia Marco Bertini per le slides Obiettivo Concetti base dati e informazioni cos è un database terminologia Modelli organizzativi flat file database relazionali Principi e linee guida
Database Si ringrazia Marco Bertini per le slides Obiettivo Concetti base dati e informazioni cos è un database terminologia Modelli organizzativi flat file database relazionali Principi e linee guida
Tecniche di microscopia
 Tecniche di microscopia I microscopi permettono di vedere l estremamente piccolo I microscopi ottici utilizzano lenti di vetro in grado di deflettere e focalizzare i raggi luminosi per riprodurre le immagini
Tecniche di microscopia I microscopi permettono di vedere l estremamente piccolo I microscopi ottici utilizzano lenti di vetro in grado di deflettere e focalizzare i raggi luminosi per riprodurre le immagini
Scuola Media Piancavallo 2
 LA CELLULA Una caratteristica di quasi tutti gli esseri viventi è quella di possedere una struttura più o meno complessa in cui parti diverse, gli organi, sono adatte a svolgere funzioni specifiche. Il
LA CELLULA Una caratteristica di quasi tutti gli esseri viventi è quella di possedere una struttura più o meno complessa in cui parti diverse, gli organi, sono adatte a svolgere funzioni specifiche. Il
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Amplificatori Audio di Potenza
 Amplificatori Audio di Potenza Un amplificatore, semplificando al massimo, può essere visto come un oggetto in grado di aumentare il livello di un segnale. Ha quindi, generalmente, due porte: un ingresso
Amplificatori Audio di Potenza Un amplificatore, semplificando al massimo, può essere visto come un oggetto in grado di aumentare il livello di un segnale. Ha quindi, generalmente, due porte: un ingresso
IL FOTOVOLTAICO E L ARCHITETTURA
 IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
IL FOTOVOLTAICO E L ARCHITETTURA Prof. Paolo ZAZZINI Ing. Nicola SIMIONATO COME FUNZIONA UNA CELLA FOTOVOLTAICA EFFETTO FOTOVOLTAICO: Un flusso luminoso che incide su un materiale semiconduttore opportunamente
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
Indice generale. OOA Analisi Orientata agli Oggetti. Introduzione. Analisi
 Indice generale OOA Analisi Orientata agli Oggetti Introduzione Analisi Metodi d' analisi Analisi funzionale Analisi del flusso dei dati Analisi delle informazioni Analisi Orientata agli Oggetti (OOA)
Indice generale OOA Analisi Orientata agli Oggetti Introduzione Analisi Metodi d' analisi Analisi funzionale Analisi del flusso dei dati Analisi delle informazioni Analisi Orientata agli Oggetti (OOA)
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI
 TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
Ecolezione: La fotosintesi artificiale. A cura di : Roberto Meneghetti e Alex Mazzon classe 2 A IPAA Corazzin-ISISS Cerletti
 Ecolezione: La fotosintesi artificiale A cura di : Roberto Meneghetti e Alex Mazzon classe 2 A IPAA Corazzin-ISISS Cerletti Definizione La fotosintesi artificiale è un processo chimico che riproduce il
Ecolezione: La fotosintesi artificiale A cura di : Roberto Meneghetti e Alex Mazzon classe 2 A IPAA Corazzin-ISISS Cerletti Definizione La fotosintesi artificiale è un processo chimico che riproduce il
Strutturazione logica dei dati: i file
 Strutturazione logica dei dati: i file Informazioni più complesse possono essere composte a partire da informazioni elementari Esempio di una banca: supponiamo di voler mantenere all'interno di un computer
Strutturazione logica dei dati: i file Informazioni più complesse possono essere composte a partire da informazioni elementari Esempio di una banca: supponiamo di voler mantenere all'interno di un computer
Energia e Lavoro. In pratica, si determina la dipendenza dallo spazio invece che dal tempo
 Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
SymCAD/C.A.T.S. modulo Canali Schema
 SymCAD/C.A.T.S. modulo Canali Schema Il modulo Ventilazione Standard permette di effettuare la progettazione integrata (disegno e calcoli) in AutoCAD di reti di canali aria (mandata e ripresa). Il disegno
SymCAD/C.A.T.S. modulo Canali Schema Il modulo Ventilazione Standard permette di effettuare la progettazione integrata (disegno e calcoli) in AutoCAD di reti di canali aria (mandata e ripresa). Il disegno
REGOLAMENTO (UE) N. 1235/2011 DELLA COMMISSIONE
 30.11.2011 Gazzetta ufficiale dell Unione europea L 317/17 REGOLAMENTO (UE) N. 1235/2011 DELLA COMMISSIONE del 29 novembre 2011 recante modifica del regolamento (CE) n. 1222/2009 del Parlamento europeo
30.11.2011 Gazzetta ufficiale dell Unione europea L 317/17 REGOLAMENTO (UE) N. 1235/2011 DELLA COMMISSIONE del 29 novembre 2011 recante modifica del regolamento (CE) n. 1222/2009 del Parlamento europeo
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Il magnetismo nella materia
 Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
COMUNE DI RAVENNA GUIDA ALLA VALUTAZIONE DELLE POSIZIONI (FAMIGLIE, FATTORI, LIVELLI)
 COMUNE DI RAVENNA Il sistema di valutazione delle posizioni del personale dirigente GUIDA ALLA VALUTAZIONE DELLE POSIZIONI (FAMIGLIE, FATTORI, LIVELLI) Ravenna, Settembre 2004 SCHEMA DI SINTESI PER LA
COMUNE DI RAVENNA Il sistema di valutazione delle posizioni del personale dirigente GUIDA ALLA VALUTAZIONE DELLE POSIZIONI (FAMIGLIE, FATTORI, LIVELLI) Ravenna, Settembre 2004 SCHEMA DI SINTESI PER LA
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Strategie di purificazione di proteine
 Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Analisi sensitività. Strumenti per il supporto alle decisioni nel processo di Valutazione d azienda
 Analisi sensitività. Strumenti per il supporto alle decisioni nel processo di Valutazione d azienda Premessa Con l analisi di sensitività il perito valutatore elabora un range di valori invece di un dato
Analisi sensitività. Strumenti per il supporto alle decisioni nel processo di Valutazione d azienda Premessa Con l analisi di sensitività il perito valutatore elabora un range di valori invece di un dato
Excel. A cura di Luigi Labonia. e-mail: luigi.lab@libero.it
 Excel A cura di Luigi Labonia e-mail: luigi.lab@libero.it Introduzione Un foglio elettronico è un applicazione comunemente usata per bilanci, previsioni ed altri compiti tipici del campo amministrativo
Excel A cura di Luigi Labonia e-mail: luigi.lab@libero.it Introduzione Un foglio elettronico è un applicazione comunemente usata per bilanci, previsioni ed altri compiti tipici del campo amministrativo
LA CORRENTE ELETTRICA CONTINUA
 LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LE FUNZIONI A DUE VARIABILI
 Capitolo I LE FUNZIONI A DUE VARIABILI In questo primo capitolo introduciamo alcune definizioni di base delle funzioni reali a due variabili reali. Nel seguito R denoterà l insieme dei numeri reali mentre
Capitolo I LE FUNZIONI A DUE VARIABILI In questo primo capitolo introduciamo alcune definizioni di base delle funzioni reali a due variabili reali. Nel seguito R denoterà l insieme dei numeri reali mentre
Automazione Industriale (scheduling+mms) scheduling+mms. adacher@dia.uniroma3.it
 Automazione Industriale (scheduling+mms) scheduling+mms adacher@dia.uniroma3.it Introduzione Sistemi e Modelli Lo studio e l analisi di sistemi tramite una rappresentazione astratta o una sua formalizzazione
Automazione Industriale (scheduling+mms) scheduling+mms adacher@dia.uniroma3.it Introduzione Sistemi e Modelli Lo studio e l analisi di sistemi tramite una rappresentazione astratta o una sua formalizzazione
Il campionamento. La digitalizzazione. Teoria e pratica. La rappresentazione digitale delle immagini. La rappresentazione digitale delle immagini
 ACQUISIZIONE ED ELABORAZIONE DELLE IMMAGINI Teoria e pratica La digitalizzazione La digitalizzazione di oggetti legati a fenomeni di tipo analogico, avviene attraverso due parametri fondamentali: Il numero
ACQUISIZIONE ED ELABORAZIONE DELLE IMMAGINI Teoria e pratica La digitalizzazione La digitalizzazione di oggetti legati a fenomeni di tipo analogico, avviene attraverso due parametri fondamentali: Il numero
La cellula è l unità fondamentale di tutti gli organismi viventi ed è la più piccola struttura ad essere classificabile come vivente.
 CHE COS E LA CELLULA? La cellula è l unità fondamentale di tutti gli organismi viventi ed è la più piccola struttura ad essere classificabile come vivente. DA COSA SONO COSTITUITE LE CELLULE? Tutte le
CHE COS E LA CELLULA? La cellula è l unità fondamentale di tutti gli organismi viventi ed è la più piccola struttura ad essere classificabile come vivente. DA COSA SONO COSTITUITE LE CELLULE? Tutte le
SINTESI PROTEICA. Replicazione. Trascrizione. Traduzione
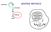 Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
VALORE DELLE MERCI SEQUESTRATE
 La contraffazione in cifre: NUOVA METODOLOGIA PER LA STIMA DEL VALORE DELLE MERCI SEQUESTRATE Roma, Giugno 2013 Giugno 2013-1 Il valore economico dei sequestri In questo Focus si approfondiscono alcune
La contraffazione in cifre: NUOVA METODOLOGIA PER LA STIMA DEL VALORE DELLE MERCI SEQUESTRATE Roma, Giugno 2013 Giugno 2013-1 Il valore economico dei sequestri In questo Focus si approfondiscono alcune
Nota interpretativa. La definizione delle imprese di dimensione minori ai fini dell applicazione dei principi di revisione internazionali
 Nota interpretativa La definizione delle imprese di dimensione minori ai fini dell applicazione dei principi di revisione internazionali Febbraio 2012 1 Mandato 2008-2012 Area di delega Consigliere Delegato
Nota interpretativa La definizione delle imprese di dimensione minori ai fini dell applicazione dei principi di revisione internazionali Febbraio 2012 1 Mandato 2008-2012 Area di delega Consigliere Delegato
«Macromolecole» Lipidi
 LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
CELLULE EUCARIOTICHE
 CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
Capitolo 25: Lo scambio nel mercato delle assicurazioni
 Capitolo 25: Lo scambio nel mercato delle assicurazioni 25.1: Introduzione In questo capitolo la teoria economica discussa nei capitoli 23 e 24 viene applicata all analisi dello scambio del rischio nel
Capitolo 25: Lo scambio nel mercato delle assicurazioni 25.1: Introduzione In questo capitolo la teoria economica discussa nei capitoli 23 e 24 viene applicata all analisi dello scambio del rischio nel
Controlli Automatici T. Trasformata di Laplace e Funzione di trasferimento. Parte 3 Aggiornamento: Settembre 2010. Prof. L.
 Parte 3 Aggiornamento: Settembre 2010 Parte 3, 1 Trasformata di Laplace e Funzione di trasferimento Prof. Lorenzo Marconi DEIS-Università di Bologna Tel. 051 2093788 Email: lmarconi@deis.unibo.it URL:
Parte 3 Aggiornamento: Settembre 2010 Parte 3, 1 Trasformata di Laplace e Funzione di trasferimento Prof. Lorenzo Marconi DEIS-Università di Bologna Tel. 051 2093788 Email: lmarconi@deis.unibo.it URL:
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI
 UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
Struttura e funzioni della cellula. Corso di Biofisica, Università di Cagliari 1
 Struttura e funzioni della cellula 1 Riferimenti Books and others Biological Physics (updated 1 st ed.), Philip Nelson, Chap. 2 Physical Biology of the Cell, Phillips et al., Chap. 2 Movies Exercise 2
Struttura e funzioni della cellula 1 Riferimenti Books and others Biological Physics (updated 1 st ed.), Philip Nelson, Chap. 2 Physical Biology of the Cell, Phillips et al., Chap. 2 Movies Exercise 2
USO DIAGNOSTICO E DI COMPLESSI METALLICI
 USO DIAGNOSTICO E DI COMPLESSI METALLICI Uso diagnostico di complessi di gadolinio La Risonanza Magnetica e un fenomeno che accade quando i nuclei di alcuni atomi immersi in un campo magnetico statico
USO DIAGNOSTICO E DI COMPLESSI METALLICI Uso diagnostico di complessi di gadolinio La Risonanza Magnetica e un fenomeno che accade quando i nuclei di alcuni atomi immersi in un campo magnetico statico
MANUALE MOODLE STUDENTI. Accesso al Materiale Didattico
 MANUALE MOODLE STUDENTI Accesso al Materiale Didattico 1 INDICE 1. INTRODUZIONE ALLA PIATTAFORMA MOODLE... 3 1.1. Corso Moodle... 4 2. ACCESSO ALLA PIATTAFORMA... 7 2.1. Accesso diretto alla piattaforma...
MANUALE MOODLE STUDENTI Accesso al Materiale Didattico 1 INDICE 1. INTRODUZIONE ALLA PIATTAFORMA MOODLE... 3 1.1. Corso Moodle... 4 2. ACCESSO ALLA PIATTAFORMA... 7 2.1. Accesso diretto alla piattaforma...
Sistemi Informativi e Sistemi ERP
 Sistemi Informativi e Sistemi Trasformare i dati in conoscenza per supportare le decisioni CAPODAGLIO E ASSOCIATI 1 I SISTEMI INFORMATIVI LI - E IMPRESA SISTEMA DI OPERAZIONI ECONOMICHE SVOLTE DA UN DATO
Sistemi Informativi e Sistemi Trasformare i dati in conoscenza per supportare le decisioni CAPODAGLIO E ASSOCIATI 1 I SISTEMI INFORMATIVI LI - E IMPRESA SISTEMA DI OPERAZIONI ECONOMICHE SVOLTE DA UN DATO
INTRODUZIONE: PERDITE IN FIBRA OTTICA
 INTRODUZIONE: PERDITE IN FIBRA OTTICA Il nucleo (o core ) di una fibra ottica è costituito da vetro ad elevatissima purezza, dal momento che la luce deve attraversare migliaia di metri di vetro del nucleo.
INTRODUZIONE: PERDITE IN FIBRA OTTICA Il nucleo (o core ) di una fibra ottica è costituito da vetro ad elevatissima purezza, dal momento che la luce deve attraversare migliaia di metri di vetro del nucleo.
Modello generale di trasduttore Come leggere la scheda tecnica di un trasduttore
 Modello generale di trasduttore Come leggere la scheda tecnica di un trasduttore Modello generale di trasduttore Informazioni sulle caratteristiche fisiche Sistema di misura Catena di misura Dati numerici
Modello generale di trasduttore Come leggere la scheda tecnica di un trasduttore Modello generale di trasduttore Informazioni sulle caratteristiche fisiche Sistema di misura Catena di misura Dati numerici
Forza. Forza. Esempi di forze. Caratteristiche della forza. Forze fondamentali CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA
 Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Il metabolismo dell RNA. Prof. Savino; dispense di Biologia Molecolare, Corso di Laurea in Biotecnologie
 Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Tesina di scienze. L Elettricità. Le forze elettriche
 Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Tesina di scienze L Elettricità Le forze elettriche In natura esistono due forme di elettricità: quella negativa e quella positiva. Queste due energie si attraggono fra loro, mentre gli stessi tipi di
Come visto precedentemente l equazione integro differenziale rappresentativa dell equilibrio elettrico di un circuito RLC è la seguente: 1 = (1)
 Transitori Analisi nel dominio del tempo Ricordiamo che si definisce transitorio il periodo di tempo che intercorre nel passaggio, di un sistema, da uno stato energetico ad un altro, non è comunque sempre
Transitori Analisi nel dominio del tempo Ricordiamo che si definisce transitorio il periodo di tempo che intercorre nel passaggio, di un sistema, da uno stato energetico ad un altro, non è comunque sempre
CORRENTE ELETTRICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V 2 isolati tra loro V 2 > V 1 V 2
 COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
Matematica e Statistica
 Matematica e Statistica Prova d esame (0/07/03) Università di Verona - Laurea in Biotecnologie - A.A. 0/3 Matematica e Statistica Prova di MATEMATICA (0/07/03) Università di Verona - Laurea in Biotecnologie
Matematica e Statistica Prova d esame (0/07/03) Università di Verona - Laurea in Biotecnologie - A.A. 0/3 Matematica e Statistica Prova di MATEMATICA (0/07/03) Università di Verona - Laurea in Biotecnologie
Guida Compilazione Piani di Studio on-line
 Guida Compilazione Piani di Studio on-line SIA (Sistemi Informativi d Ateneo) Visualizzazione e presentazione piani di studio ordinamento 509 e 270 Università della Calabria (Unità organizzativa complessa-
Guida Compilazione Piani di Studio on-line SIA (Sistemi Informativi d Ateneo) Visualizzazione e presentazione piani di studio ordinamento 509 e 270 Università della Calabria (Unità organizzativa complessa-
Per studio di funzione intendiamo un insieme di procedure che hanno lo scopo di analizzare le proprietà di una funzione f ( x) R R
 Studio di funzione Per studio di funzione intendiamo un insieme di procedure che hanno lo scopo di analizzare le proprietà di una funzione f ( x) R R : allo scopo di determinarne le caratteristiche principali.
Studio di funzione Per studio di funzione intendiamo un insieme di procedure che hanno lo scopo di analizzare le proprietà di una funzione f ( x) R R : allo scopo di determinarne le caratteristiche principali.
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Capitolo 4 Le spettroscopie. 1. Lo spettro elettromagnetico
 Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Termodinamica. Sistema termodinamico. Piano di Clapeyron. Sistema termodinamico. Esempio. Cosa è la termodinamica? TERMODINAMICA
 Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Luigi Piroddi piroddi@elet.polimi.it
 Automazione industriale dispense del corso 10. Reti di Petri: analisi strutturale Luigi Piroddi piroddi@elet.polimi.it Analisi strutturale Un alternativa all analisi esaustiva basata sul grafo di raggiungibilità,
Automazione industriale dispense del corso 10. Reti di Petri: analisi strutturale Luigi Piroddi piroddi@elet.polimi.it Analisi strutturale Un alternativa all analisi esaustiva basata sul grafo di raggiungibilità,
Probabilità condizionata: p(a/b) che avvenga A, una volta accaduto B. Evento prodotto: Evento in cui si verifica sia A che B ; p(a&b) = p(a) x p(b/a)
 Probabilità condizionata: p(a/b) che avvenga A, una volta accaduto B Eventi indipendenti: un evento non influenza l altro Eventi disgiunti: il verificarsi di un evento esclude l altro Evento prodotto:
Probabilità condizionata: p(a/b) che avvenga A, una volta accaduto B Eventi indipendenti: un evento non influenza l altro Eventi disgiunti: il verificarsi di un evento esclude l altro Evento prodotto:
TRAGUARDI PER LO SVILUPPO DELLE COMPETENZE AL TERMINE DELLA SCUOLA PRIMARIA
 SCUOLA PRIMARIA DI CORTE FRANCA MATEMATICA CLASSE QUINTA TRAGUARDI PER LO SVILUPPO DELLE COMPETENZE AL TERMINE DELLA SCUOLA PRIMARIA L ALUNNO SVILUPPA UN ATTEGGIAMENTO POSITIVO RISPETTO ALLA MATEMATICA,
SCUOLA PRIMARIA DI CORTE FRANCA MATEMATICA CLASSE QUINTA TRAGUARDI PER LO SVILUPPO DELLE COMPETENZE AL TERMINE DELLA SCUOLA PRIMARIA L ALUNNO SVILUPPA UN ATTEGGIAMENTO POSITIVO RISPETTO ALLA MATEMATICA,
Regione Piemonte Portale Rilevazioni Crediti EELL Manuale Utente
 Pag. 1 di 15 VERS V01 REDAZIONE VERIFICHE E APPROVAZIONI CONTROLLO APPROVAZIONE AUTORIZZAZIONE EMISSIONE NOME DATA NOME DATA NOME DATA A. Marchisio C. Pernumian 29/12/2014 M. Molino 27/02/2015 M. Molino
Pag. 1 di 15 VERS V01 REDAZIONE VERIFICHE E APPROVAZIONI CONTROLLO APPROVAZIONE AUTORIZZAZIONE EMISSIONE NOME DATA NOME DATA NOME DATA A. Marchisio C. Pernumian 29/12/2014 M. Molino 27/02/2015 M. Molino
Dal DNA alle proteine: La trascrizione e la traduzione
 Dal DNA alle proteine: La trascrizione e la traduzione DNA RNA Trascrizione RNA PROTEINE Traduzione Dove avvengono? GLI EUCARIOTI I PROCARIOTI Cambell, Reece Biologia ZANICHELLI Trascrizione Sintesi di
Dal DNA alle proteine: La trascrizione e la traduzione DNA RNA Trascrizione RNA PROTEINE Traduzione Dove avvengono? GLI EUCARIOTI I PROCARIOTI Cambell, Reece Biologia ZANICHELLI Trascrizione Sintesi di
Regione Toscana. ARPA Fonte Dati. Manuale Amministratore. L. Folchi (TAI) Redatto da
 ARPA Fonte Dati Regione Toscana Redatto da L. Folchi (TAI) Rivisto da Approvato da Versione 1.0 Data emissione 06/08/13 Stato DRAFT 1 Versione Data Descrizione 1,0 06/08/13 Versione Iniziale 2 Sommario
ARPA Fonte Dati Regione Toscana Redatto da L. Folchi (TAI) Rivisto da Approvato da Versione 1.0 Data emissione 06/08/13 Stato DRAFT 1 Versione Data Descrizione 1,0 06/08/13 Versione Iniziale 2 Sommario
PROGRESS: UN CODICE PER IL CALCOLO DELLE EMISSIONI DA VEICOLI STRADALI IN AMBITO URBANO
 VIII Incontro EXPERT PANEL EMISSIONI DA TRASPORTO STRADALE Roma, 5 novembre 2003 PROGRESS: UN CODICE PER IL CALCOLO DELLE EMISSIONI DA VEICOLI STRADALI IN AMBITO URBANO Massimo Capobianco, Giorgio Zamboni
VIII Incontro EXPERT PANEL EMISSIONI DA TRASPORTO STRADALE Roma, 5 novembre 2003 PROGRESS: UN CODICE PER IL CALCOLO DELLE EMISSIONI DA VEICOLI STRADALI IN AMBITO URBANO Massimo Capobianco, Giorgio Zamboni
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
Sistemi di tracciabilità per un attestato di identità molecolare. FEM 2 - Ambiente S.r.l. Spin-off dell Università degli Studi di Milano-Bicocca
 Sistemi di tracciabilità per un attestato di identità molecolare FEM 2 - Ambiente S.r.l. Spin-off dell Università degli Studi di Milano-Bicocca PROBLEMA L identificazione e il controllo della filiera delle
Sistemi di tracciabilità per un attestato di identità molecolare FEM 2 - Ambiente S.r.l. Spin-off dell Università degli Studi di Milano-Bicocca PROBLEMA L identificazione e il controllo della filiera delle
E ESSENZIALMENTE L UNICO MECCANISMO DI IMMISSIONE DI ENERGIA NEL MONDO VIVENTE CENNI STORICI < 1700 SI RITENEVA CHE LE PIANTE TRAESSERO NUTRIMENTO
 E ESSENZIALMENTE L UNICO MECCANISMO DI IMMISSIONE DI ENERGIA NEL MONDO VIVENTE CENNI STORICI < 1700 SI RITENEVA CHE LE PIANTE TRAESSERO NUTRIMENTO DALLA TERRA 1727 STEPHEN HALES SCOPRE CHE PARTE DEL NUTRIMENTO
E ESSENZIALMENTE L UNICO MECCANISMO DI IMMISSIONE DI ENERGIA NEL MONDO VIVENTE CENNI STORICI < 1700 SI RITENEVA CHE LE PIANTE TRAESSERO NUTRIMENTO DALLA TERRA 1727 STEPHEN HALES SCOPRE CHE PARTE DEL NUTRIMENTO
