UNIVERSITÀ DEGLI STUDI DI MESSINA FACOLTÀ DI SCIENZE MM.FF.NN. CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE
|
|
|
- Filomena Borrelli
- 8 anni fa
- Visualizzazioni
Transcript
1 UNIVERSITÀ DEGLI STUDI DI MESSINA FACOLTÀ DI SCIENZE MM.FF.NN. CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE Esercitazioni di fisica a cura di Valeria Conti Nibali A.A. 2008/09
2 Esercizio 1 Si consideri un blocco di sostanza omogenea (avente coefficiente di conducibilità termica k), di lunghezza L e di sezione S, interposto tra due superfici piane metalliche mantenute rispettivamente alle temperature T 1 e T 2. Considerando il sistema in uno stato stazionario, si calcoli: 1) Il flusso di calore (cal/sec) che passa fra le due superfici. 2) L'andamento della temperatura T(x) nello spazio fra le due superfici. Dati: L:0,5 m, S: 10cm 2, T 1 =0 C, T 2 =60 C, k:1, cal/sec cm K T ( ! T1 cal/sec, T ( x) " T1! x ) L Esercizio 2 In un recipiente di volume V=5 litri sono presenti 8 moli di un dato gas ed 8 moli di un altro a T=25 C. Entrambi i gas sono perfetti. Calcolare la pressione nel recipiente. Supponendo ora che i due gas si combinino tra di loro completamente tramite una reazione esoenergetica che fa aumentare la temperatura del sistema di 50 C, quale sarà la nuova pressione? (78,2 atm, 45,6 atm) Esercizio 3 Si consideri un sistema, costituito da due specie chimiche A e B, caratterizzato dai valori delle seguenti variabili intensive p=2 atm., T:27 C., # A =5 Kcal/mole e # B =8 Kcal/mole. Detto sistema compie una trasformazione nel corso della quale le variabili estensive cambiano del seguente ammontare: Variazione di volume: 100 cm 3 (in aumento) Variazione di entropia: 0,03 cal/ K (in diminuzione) Variazione del numero di moli della specie A: 3 milli moli (in diminuzione) Variazione del numero di moli della specie B: 6 milli moli (in aumento) Calcolare la variazione di energia totale del sistema sapendo di poter considerare molto piccole tali variazioni. 2
3 (19,16 cal = 80,17 Joule) Esercizio 4 Una mole di gas perfetto compie un ciclo di Carnot A-B-C-D tra le temperature T 1 = 700 C e T 2 = 20 C. II volume iniziale è V A = 30 I mentre V B = 60 l. Calcolare: 1. i volumi V C e V D; 2. il lavoro effettuato in un ciclo. (V C = 363,2 l; V D = 181,5 l; L=3916,8 J) Esercizio 5 Un oggetto avente la capacità termica di 100 Kcal/ K che si trova inizialmente alla temperatura di 500 K viene gettato in mare (temperatura 15 C). Calcolare: 1) La temperatura finale dell'oggetto; 2) La variazione di entropia dell'oggetto, quella del mare e quella complessiva 3) Supponendo che anziché essere gettato in mare l'oggetto venga usato come sorgente calda per far funzionare una macchina reversibile di Carnot che usa il mare come sorgente fredda, quanto lavoro si riuscirebbe ad ottenere in questo processo ideale? (15 C, - 55,2 Kcal/ K, 73,6 Kcal/ K, 18,4 Kcal/ K, 5313 Kcal/ K) Esercizio 6 Essendo il calore latente di fusione dell'acqua 80 cal/g qual è il lavoro massimo che si può ottenere da una macchina termica che usa una tonnellata di ghiaccio a 0 C come sorgente fredda e l'ambiente come sorgente calda (temp. 20 C) finchè tutto il ghiaccio non si sia fuso? (2, Joule) Esercizio 7 Una miscela di due gas monoatomici A e B (una mole per ciascuno) è contenuta in un recipiente adiabatico di 35 litri e si trova alla temperatura di 300 K. Ha 3
4 luogo una reazione chimica: A+ B = C dove C è un gas biatomico. Sapendo che la reazione è esoenergetica e libera 10 Kcal/mole si calcoli la pressione finale. (I gas vanno trattati come perfetti) (1, Pa) Esercizio 8 Si vuole portare a ebollizione e trasformare in vapore un Kg di un liquido il cui calore specifico vale 0,8cal/g/K ed il calore latente di evaporazione 300 cal/g. Il liquido si trova inizialmente alla temperatura di 30 C e bolle a 90 C. Si vuole sapere: 1) Quanto calore avrà assorbito il liquido in questo processo? 2) Qual è la sua variazione di entropia? Sapendo che per realizzare detto processo si dispone di due sorgenti termiche l'una alla temperatura di 100 K e I'altra alla temperatura di 300 K; 3) si illustri il procedimento che può essere seguito per ottenere il risultato voluto; 4) si calcoli la corrispondente variazione totale di entropia. (3, cal, 970,9 cal/ K) Esercizio 9 Un recipiente cilindrico chiuso mediante un pistone scorrevole contiene una mole di gas perfetto (monoatomico) in equilibrio alla pressione P A e volume V A = 5 litri. Agendo bruscamente sul pistone la pressione esterna viene triplicata ed il volume nelle nuove condizioni di equilibrio risulta essere V C =3 litri. Calcolare la variazione di entropia del gas. (0,75 cal/ K) Esercizio 10 Un calorimetro delle mescolanze contiene 100 g di acqua alla temperatura di 20 C. Un corpo di massa m=20g viene portato alla temperatura di 80 C e quindi 4
5 immerso nel calorimetro. La nuova temperatura raggiunta i di 25 C. Qual è il calore specifico del corpo? (0,45 cal.g -1 C -1 ) Esercizio 11 In un calorimetro sono contenuti 100 g di acqua a T=20 C. Altri 100 g di acqua vengono portati ad 80 C e versati nel calorimetro. La temperatura si porta a T=48 C. Calcolare l'equivalente in acqua del calorimetro 1 e correggere, in base a quanto trovato, il risultato dell'esercizio precedente. (14,28 g, 0,52 cal g -1 C -1 ) Esercizio 12 Un blocco di ghiaccio sta galleggiando in una vasca piena di acqua. Dire se, dopo che il blocco si è sciolto, il livello dell'acqua nella vasca è aumentato, diminuito o rimasto invariato e spiegare il perché. (Rimane invariato) Esercizio 13 Un corpo di massa m=20 g di capacità termica c=0.5 cal g -1 C-1 viene portato ad una temperatura di 80 C. Viene quindi immerso in un calorimetro a ghiaccio di Bunsen. Calcolare la massa di ghiaccio fusa. Dati: Calore latente del ghiaccio!=80 cal/g. (10 g) Esercizio 14 ln un recipiente isolante di capacità termica trascurabile c è un Kg di acqua allo stato liquido a 10 C. Si introduce una certa quantità di vapore a 100 C. Quando 1 L equivalente in acqua del calorimetro è quella massa fittizia # che occorre aggiungere, nei calcoli, al fluido calorimetrico per tenere conto della presenza di altre masse (termometro, agitatore, ) e delle inevitabili perdite, che sottraggono calore da quello che potrebbe essere usato per variare la temperatura del corpo in esame. 5
6 il sistema raggiunge il nuovo equilibrio l'acqua è a 40 C. Si trascuri la quantità di vapore nello stato finale ed il lavoro fatto nell'introduzione del vapore. Calcolare la massa del vapore introdotto. Dati: Calore latente di evaporazione q=540 cal/g (0,05 Kg) Esercizio 15 Un vaso isolato (calorimetro) contiene una massa M 1 =200 g di acqua ed una massa M 2 = 100 Kg di ghiaccio alla temperatura T 0 =0 C. In esso viene gettato un pezzo di ferro di massa m=150 g avente una temperatura T=600 C. Qual è la temperatura finale del sistema? Dati: Calore specifico del ferro, c=0,11 cal/g C Calore latente di fusione del ghiaccio,!=80 cal/g. (~5,7 C) Esercizio 16 Un recipiente cilindrico chiuso mediante un pistone scorrevole contiene una mole di gas, perfetto (monoatomico) in equilibrio alla pressione P A e volume V A =5 litri. Agendo bruscamente sul pistone la pressione esterna viene triplicata ed il volume, nelle nuove condizioni di equilibrio, risulta V C =3 litri. Calcolare la variazione di entropia del gas. (0,75 J/ K) Esercizio 17 Una mole di gas ideale (monoatomico) percorre un ciclo reversibile indicato in figura, dove: 1-2 è una trasformazione a volume costante; 2-3 una trasformazione adiabatica; 3-1 a una isobara costante. Si sa inoltre che v 3 =8v 1 ; determinare il rendimento del ciclo percorso dalla mole di gas. 6
7 (0,69) Esercizio 18 L'energia libera di un sistema è data, in funzione di temperatura e volume, dall'espressione A(T,V)=-RT logt 3/2 V Calcolare il valore del calore specifico a volume costante del sistema. (3R/2) Esercizio 19 Dato un sistema formato da 20 g di azoto (N 2 ) contenuti in un recipiente di volume V 0 alla pressione P 0 e temperatura T 0 =0 C, determinare il lavoro totale compiuto quando il sistema viene sottoposto ai seguenti processi quasi statici: 1) Un riscaldamento a volume costante V 0 che porta la temperatura a T 1 =To+50 C, e la pressione al valore P 1. 2) Un espansione isoterma (T=T 1 ) che porta il volume al valore V 2 =2V 0 e la pressione al valore P 2. 3) Una compressione isobarica (P=P 2 ) che porta il volume al valore originario V 0. (L 1 =0; L 2 =nrt 1 ln(2); L 3 =-P 2 V 0 ; L tot =370,3 Joule) 7
8 Esercizio 20 Si consideri l'aria come un miscuglio di azoto (N 2 ) ed ossigeno (O 2 ), da ritenersi entrambi come gas perfetti. Si abbia ora un recipiente di volume costante V, pieno d'aria a pressione p 0 e contenente anche una certa quantità di magnesio (il volume del quale può essere ritenuto trascurabile). Si pensi ora di far bruciare il magnesio (per esempio accendendolo elettricamente) che è in quantità tale da combinarsi con tutto l'ossigeno presente per dare ossido di magnesio (solido, il cui volume è trascurabile). Quando il sistema torna alla temperatura iniziale, si legge una nuova pressione p. Qual è la percentuale in peso di N 2 e di O 2 dell'aria? Dati: peso mol. azoto PM(N)=14 ; peso mol. Ossigeno PM(O)=16 p 0 =760 mmhg ; p=593 mmhg (24,4% in peso di O 2 e 75,6% in peso di N 2 ) Esercizio 21 Due oggetti aventi la capacità termica di 20 cal/ C e 30 cal/ C, si trovano inizialmente alla temperatura T 1 =80 C e T 2 =20 C, rispettivamente. Vengono quindi posti a contatto in un contenitore adiabatico per evitare scambi di calore con l'esterno. Si calcoli la temperatura finale e la variazione di entropia totale. (44 C; 2, ) Esercizio 22 Si consideri un sistema composto da due moli di un gas perfetto, contenuto in un volume di 1 litro, alla temperatura di 20 C. Determinare il lavoro fornito ed il calore assorbito durante un espansione isoterma reversibile, che fa aumentare il volume di 3 litri. Se il sistema viene invece fatto espandere adiabaticamente fino ad ottenere la stessa variazione di volume del caso precedente, quanto valgono in questo caso il calore assorbito ed il lavoro fornito? (Q = 1614 cal; L = 6754 Joule ; Q = 0; L Joule) 8
9 Esercizio 23 Un sistema omogeneo avente capacità termica di 1000 cal/ K si trova inizialmente alla temperatura uniforme di 20 C. In seguito ad una opportuna interazione con l'ambiente subisce una trasformazione (da considerare reversibile) al termine della quale metà del sistema si trova a 100 C e l'altra metà a -60 C. Calcolare la variazione di entropia subita dall'ambiente. (38,7 cal/ K) Esercizio 24 Un pendolo di massa 100 g e lunghezza l=50cm, immerso in un ambiente a temperatura T=20 C, viene abbandonato a se stesso a partire dalla posizione indicata in figura. Il pendolo, dopo aver oscillato per un certo tempo si ferma a causa degli attriti. Calcolare la variazione di entropia. ( cal/ K) Esercizio 25 Un generatore di tensione di 200 Volt con resistenza interna di 5 ohm è collegato ad un riscaldatore la cui resistenza è 300 ohm. Questo riscaldatore è collocato all'interno di un contenitore adiabatico a contatto termico con 3 grammi di ghiaccio alla temperatura iniziale di 0 C. Una delle pareti della camera adiabatica è costituita da un pistone che mantiene costante la pressione al valore di 1 atm. Se il circuito viene chiuso per il tempo di 10 s: 9
10 1) Quale sarà la potenza erogata dal generatore? 2) Quale sarà lo stato fisico finale del sistema? Se vogliamo che lo stato finale del sistema sia gassoso in un volume di 10 litri: 3) Quale deve essere il nuovo valore della resistenza del riscaldatore se si vogliono lasciare inalterati tutti gli altri parametri? (Trascurare la variazione della resistenza del riscaldatore a causa della variazione della temperatura e considerare il vapore d'acqua come un gas perfetto) Dati: Calore latente di fusione 80 cal/g Calore latente di evaporazione 540 cal/g (1307 Joule; stato liquido; 25,33 oppure 0,987) Esercizio 26 Un blocco di ghiaccio di massa M 1 viene lasciato cadere da un'altezza h in un recipiente adiabatico contenente una massa M 2 diacqua. Discutere il problema. Quale energia occorre fornire ad una tonnellata di H 2 O per farla salire da un pozzo profondo 10 metri ad un appartamento che si trova a 12 metri di altezza? (2.156/105 Joule) Esercizio 27 In un recipiente cilindrico viene versata H 2 O al ritmo di 5 l/minuto. Sul fondo del recipiente è praticato un foro del diametro di un centimetro. Quale altezza raggiungerà l'acqua del recipiente? (3,54 m) Esercizio 28 Un fusto di raggio R = 0,4 metri è pieno per un'altezza di 1,1 metri di acqua. Sul fondo è praticato un forellino circolare di raggio 1 mm. In quanto tempo si svuota il fusto? 10
11 (22 ore) Esercizio 29 In un tubo a U (diametro 1cm) vengono versati 38 cm 3 di H 2 O e successivamente 10 cm 3 di olio (densità = 0,85 g/cm 3 ). Quale sarà la differenza di altezza del fluido nei due rami? Esercizio 30 Un nebulizzatore trasforma 100 cm 3 di acqua in goccioline di 10 #m di raggio. Qual e' il valore minimo dell'energia che si deve trasferire all'acqua in questa trasformazione? Tensione superficiale acqua-aria "=72 dine/cm 2 (2,16 Joule) Esercizio 31 Un apparecchio elettrico presenta una resistenza R=15 # e deve essere alimentato a 110 Volt. Avendo a disposizione una ddp di 260 Volt, si calcoli quale resistenza deve essere posta in serie all'apparecchio affinché questo funzioni correttamente. (20,5 #) Esercizio 32 Si hanno a disposizione resistenze di 10 # capaci di sopportare una corrente massima di 1 A. Volendo usare una ddp di 200 V per alimentare una stufa da 1KW, quante resistenze occorreranno e come dovranno essere collegate? (5 rami in parallelo, ciascun ramo formato da 20 resistenze in serie) 11
12 Esercizio 33 Si ha a disposizione un certo numero di condensatori uguali, di capacità C=1#F ciascuno, che per ragioni di isolamento non possono essere caricati a più di 1000 Volt. Quanti condensatori occorrerebbe disporre in parallelo per riuscire ad immagazzinare una energia di 10 Joule? Quanti condensatori occorrerebbe disporre in serie per ottenere lo stesso risultato? E in questo caso di quale ddp si avrebbe bisogno? (20, 20,20000 Volt) Esercizio 34 Un generatore di tensione V=20 Volt è collegato a due resistenze in serie R 1 =200 # ed R 2 =500 #. Sia C un condensatore di capacità pari a 20 #F, posto in parallelo alla resistenza R 2. Calcolare la carica presente sulle armature di C quando il circuito è a regime. (285,7 #C) Esercizio 35 Un motore elettrico M assorbe una potenza di 300 W ed ha un rendimento del 70 %. Tale motore viene usato per mettere in moto un volano A costituito da un cilindro massiccio (raggio 10 cm, altezza 5 cm) fino a fargli raggiungere una velocità di rotazione di 50 giri al secondo. Il materiale di cui è fatto il volano ha una densità $=5 g/cm 3. Per quanto tempo avrà funzionato il motore? (9,21 s) 12
13 Esercizio 36 In un processo che avviene senza variazione di volume e ad energia libera costante, una massa sferica di 1 mg di acqua si frammenta in 4 masse sferiche uguali. Si calcoli la variazione di temperatura. Dati: tensione sup. acqua:10-2 unità cgs entropia dell'acqua S=0.6 cal/ K Esercizio 37 Calcolare la velocità media (in modulo) che possiedono gli atomi di elio in un gas alla temperatura di 300 K. (1368m /sec) Esercizio 38 Un cilindro (massa m=2 Kg, raggio R=2 cm) ruota con una velocità angolare uniforme compiendo un giro al secondo. Sapendo che in seguito ad un urto la metà dell'energia posseduta dal cilindro passa ai gradi di libertà traslazionali, si calcoli la velocità con cui si sposterà il cilindro. (6.28 cm/sec) Esercizio 39 Un grave viene lanciato con una velocità iniziale di 5 m/sec secondo una direzione che forma un angolo di 30 con l'orizzonte. Quanto in alto giunge il grave? E quanto lontano? (2,2 m, m) Esercizio 40 Un pallone aereostatico di 100 m 3 contiene aria calda (T=60 C), mentre l'ambiente è a 20 C. Quale peso è in grado di sollevare il pallone? 13
14 (si consideri l'aria come un gas perfetto, densità dell'aria a 20 C pari a 0,001 g/cm 3 ) Esercizio 41 Una cella contenente una soluzione elettrolitica viene fatta passare una corrente di 1 A per 10 minuti. Quanto ossigeno si libera? (carica elementare q=1, C) (0,05 g) Esercizio 42 Quattro pile (fem=1.5v, resistenza interna r=10 #) vengono collegate come indicato in figura. Quale sarà la fem totale e la resistenza totale? (3 Volt, 10 %) Esercizio 43 Si consideri il sistema indicato in figura. I recipienti contengono acqua (viscosità poise). Il tubo T è lungo 1 m ed ha un raggio di 0,1 mm. Inizialmente h 1 =2m ed h 2 =1m. 1) Si calcoli la portata iniziale. 2) Dopo un certo tempo si sarà raggiunta una situazione di equilibrio (h 1 =h 2 ). Calcolare la variazione complessiva di entropia. (Il raggio dei due recipienti cilindrici è R=0,2 m; la temperatura costante è T=20 C) 14
15 Esercizio 44 In un recipiente adiabatico sono contenuti 20 litri d'acqua a temperatura iniziale di 20 C. Nel recipiente è immersa una resistenza elettrica R=10 %, che viene alimentata da una tensione V=220 Volt. Dopo quanto tempo l'acqua inizierà a bollire? (~23 min) Esercizio 45 Un vaso cilindrico le cui pareti hanno spessore e peso trascurabili ha un raggio di 10 cm e un altezza di 50 cm. Nel vaso vi è una certa quantità di liquido ($=1,5 g/cm 3 ). Detto vaso galleggia in una vasca piena d'acqua essendo la sua parte emersa metà del totale. Quanto liquido contiene il vaso? (5,2 litri) Esercizio 46 Si consideri la situazione in figura. Il recipiente A contiene un gas (perfetto) mentre il tubo ad U contiene acqua che inizialmente ha lo stesso livello nei due rami. La temperatura iniziale d 300 K. Avendo successivamente constatato che si è creato un dislivello di 50 cm, calcolare la variazione di temperatura. 15
16 (14,6 K) Esercizio 47 Si consideri il circuito in figura. f è una pila di resistenza interna 2 % e fem 15 Volt; R 1 =20 %, R 2 =20 %. Calcolare la ddp fra i punti A e B. Di quanto varia tale ddp se la resistenza R 2 si interrompe? (11,54 volt, 13,64 volt) 16
a) L altezza del palazzo; b) Di quanti gradi salirà la temperatura della palla dopo l impatto.
 A_1)Una rana sta poggiata su una foglia di ninfea trasportata dalla corrente ad una velocità di 15 cm/s, ad un certo punto compie un balzo nella stessa direzione della corrente, con un angolo di 30 rispetto
A_1)Una rana sta poggiata su una foglia di ninfea trasportata dalla corrente ad una velocità di 15 cm/s, ad un certo punto compie un balzo nella stessa direzione della corrente, con un angolo di 30 rispetto
Esercizi di Fisica Generale
 Esercizi di Fisica Generale 2. Temodinamica prof. Domenico Galli, dott. Daniele Gregori, prof. Umberto Marconi dott. Alessandro Tronconi 27 marzo 2012 I compiti scritti di esame del prof. D. Galli propongono
Esercizi di Fisica Generale 2. Temodinamica prof. Domenico Galli, dott. Daniele Gregori, prof. Umberto Marconi dott. Alessandro Tronconi 27 marzo 2012 I compiti scritti di esame del prof. D. Galli propongono
LEZIONE 5-6 ENERGIA TERMICA, TRASPORTO DEL CALORE (CONDUZIONE, CONVEZIONE) ESERCITAZIONI 2
 LEZIONE 5-6 ENERGIA TERMICA, TRASPORTO DEL CALORE (CONDUZIONE, CONVEZIONE) ESERCITAZIONI 2 Esercizio 11 Una pentola contiene 2 kg di acqua ad una temperatura iniziale di 17 C. Si vuole portare l'acqua
LEZIONE 5-6 ENERGIA TERMICA, TRASPORTO DEL CALORE (CONDUZIONE, CONVEZIONE) ESERCITAZIONI 2 Esercizio 11 Una pentola contiene 2 kg di acqua ad una temperatura iniziale di 17 C. Si vuole portare l'acqua
1) Due grandezze fisiche si dicono omogenee se:
 1) Due grandezze fisiche si dicono omogenee se: A. Si possono moltiplicare tra loro B. Si possono dividere tra loro C. Ci possono sommare tra loro D. Sono divisibili per uno stesso numero 2) Un blocchetto
1) Due grandezze fisiche si dicono omogenee se: A. Si possono moltiplicare tra loro B. Si possono dividere tra loro C. Ci possono sommare tra loro D. Sono divisibili per uno stesso numero 2) Un blocchetto
Preparazione alle gare di II livello delle Olimpiadi della Fisica 2013
 Preparazione alle gare di II livello delle Olimpiadi della Fisica 01 Incontro su temi di termodinamica 14/1/01 Giuseppina Rinaudo - Dipartimento di Fisica dell Università di Torino Sommario dei quesiti
Preparazione alle gare di II livello delle Olimpiadi della Fisica 01 Incontro su temi di termodinamica 14/1/01 Giuseppina Rinaudo - Dipartimento di Fisica dell Università di Torino Sommario dei quesiti
Esercizi di Fisica Tecnica 2013-2014. Termodinamica
 Esercizi di Fisica Tecnica 2013-2014 Termodinamica TD1 In un sistema pistone-cilindro, 1 kg di gas ( = 1,29 ed R * = 190 J/(kg K)) si espande da 5 bar e 90 C ad 1 bar. Nell'ipotesi che la trasformazione
Esercizi di Fisica Tecnica 2013-2014 Termodinamica TD1 In un sistema pistone-cilindro, 1 kg di gas ( = 1,29 ed R * = 190 J/(kg K)) si espande da 5 bar e 90 C ad 1 bar. Nell'ipotesi che la trasformazione
Prova scritta di Fisica Generale I Corso di studio in Astronomia 22 giugno 2012
 Prova scritta di Fisica Generale I Corso di studio in Astronomia 22 giugno 2012 Problema 1 Due carrelli A e B, di massa m A = 104 kg e m B = 128 kg, collegati da una molla di costante elastica k = 3100
Prova scritta di Fisica Generale I Corso di studio in Astronomia 22 giugno 2012 Problema 1 Due carrelli A e B, di massa m A = 104 kg e m B = 128 kg, collegati da una molla di costante elastica k = 3100
MASSA VOLUMICA o DENSITA
 MASSA VOLUMICA o DENSITA Massa volumica di una sostanza: è la massa di sostanza, espressa in kg, che occupa un volume pari a 1 m 3 1 m 3 di aria ha la massa di 1,2 kg 1 m 3 di acqua ha la massa di 1000
MASSA VOLUMICA o DENSITA Massa volumica di una sostanza: è la massa di sostanza, espressa in kg, che occupa un volume pari a 1 m 3 1 m 3 di aria ha la massa di 1,2 kg 1 m 3 di acqua ha la massa di 1000
Termodinamica. Sistema termodinamico. Piano di Clapeyron. Sistema termodinamico. Esempio. Cosa è la termodinamica? TERMODINAMICA
 Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
CALORE. Compie lavoro. Il calore è energia. Temperatura e calore. L energia è la capacità di un corpo di compiere un lavoro
 Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ
 Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
QUESITI DI FISICA RISOLTI A LEZIONE TERMODINAMICA
 QUESITI DI FISICA RISOLTI A LEZIONE TERMODINAMICA Un recipiente contiene gas perfetto a 27 o C, che si espande raggiungendo il doppio del suo volume iniziale a pressione costante. La temperatura finale
QUESITI DI FISICA RISOLTI A LEZIONE TERMODINAMICA Un recipiente contiene gas perfetto a 27 o C, che si espande raggiungendo il doppio del suo volume iniziale a pressione costante. La temperatura finale
Correnti e circuiti a corrente continua. La corrente elettrica
 Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Esercizi e Problemi di Termodinamica.
 Esercizi e Problemi di Termodinamica. Dr. Yves Gaspar March 18, 2009 1 Problemi sulla termologia e sull equilibrio termico. Problema 1. Un pezzetto di ghiaccio di massa m e alla temperatura di = 250K viene
Esercizi e Problemi di Termodinamica. Dr. Yves Gaspar March 18, 2009 1 Problemi sulla termologia e sull equilibrio termico. Problema 1. Un pezzetto di ghiaccio di massa m e alla temperatura di = 250K viene
LA CORRENTE ELETTRICA CONTINUA
 LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
ESERCIZI SULLA DILATAZIONE TERMICA
 ESERCIZI SULLA DILATAZIONE TERMICA Esercizio n. 1 Di quanto varia la lunghezza di una sbarra di ferro che ha, a 0 C, una lunghezza di 20 m se fosse portata alla temperatura di 50 C? (coefficiente di dilatazione
ESERCIZI SULLA DILATAZIONE TERMICA Esercizio n. 1 Di quanto varia la lunghezza di una sbarra di ferro che ha, a 0 C, una lunghezza di 20 m se fosse portata alla temperatura di 50 C? (coefficiente di dilatazione
POMPA DI CALORE CICLO FRIGORIFERO A COMPRESSIONE DI VAPORE
 POMPA DI CALORE CONDENSATORE = + L T = + L C ORGANO DI ESPANSIONE LIQUIDO COMPRESSORE T COND. E D T 1 VAPORE T EVAP. A B T 2 Schema a blocchi di una macchina frigorifera EVAPORATORE Dal punto di vista
POMPA DI CALORE CONDENSATORE = + L T = + L C ORGANO DI ESPANSIONE LIQUIDO COMPRESSORE T COND. E D T 1 VAPORE T EVAP. A B T 2 Schema a blocchi di una macchina frigorifera EVAPORATORE Dal punto di vista
'RPDQGHFRQFHWWXDOL Alcuni interrogativi su fenomeni fisici e chimici
 ,OPDWHULDOHGLGDWWLFRFKHVHJXHqVWDWRVFHOWRWUDGRWWRHDGDWWDWRGDO*UXSSRGLFKLPLFD GHOO,7,60DMRUDQDGL*UXJOLDVFR7RULQR0DUFR)DODVFD$QJHOR&LPHQLV3DROD&RVFLD /RUHGDQD$QJHOHUL$QWRQHOOD0DUWLQL'DULR*D]]ROD*UD]LD5L]]R*LXVL'L'LR
,OPDWHULDOHGLGDWWLFRFKHVHJXHqVWDWRVFHOWRWUDGRWWRHDGDWWDWRGDO*UXSSRGLFKLPLFD GHOO,7,60DMRUDQDGL*UXJOLDVFR7RULQR0DUFR)DODVFD$QJHOR&LPHQLV3DROD&RVFLD /RUHGDQD$QJHOHUL$QWRQHOOD0DUWLQL'DULR*D]]ROD*UD]LD5L]]R*LXVL'L'LR
Esercitazione IX - Calorimetria
 Esercitazione IX - Calorimetria Esercizio 1 Un blocco di rame di massa m Cu = 5g si trova a una temperatura iniziale T i = 25 C. Al blocco viene fornito un calore Q = 120J. Determinare la temperatura finale
Esercitazione IX - Calorimetria Esercizio 1 Un blocco di rame di massa m Cu = 5g si trova a una temperatura iniziale T i = 25 C. Al blocco viene fornito un calore Q = 120J. Determinare la temperatura finale
Pressione. Esempio. Definizione di pressione. Legge di Stevino. Pressione nei fluidi EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI
 Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
Acqua azzurra, acqua chiara. Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao
 Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
COMPONENTI TERMODINAMICI APERTI
 CAPITOLO NONO COMPONENTI TERMODINAMICI APERTI Esempi applicativi Vengono di seguito esaminati alcuni componenti di macchine termiche che possono essere considerati come sistemi aperti A) Macchina termica
CAPITOLO NONO COMPONENTI TERMODINAMICI APERTI Esempi applicativi Vengono di seguito esaminati alcuni componenti di macchine termiche che possono essere considerati come sistemi aperti A) Macchina termica
3. Le Trasformazioni Termodinamiche
 3. Le Trasformazioni Termodinamiche Lo stato termodinamico di un gas (perfetto) è determinato dalle sue variabili di stato: ressione, olume, Temperatura, n moli ffinché esse siano determinate è necessario
3. Le Trasformazioni Termodinamiche Lo stato termodinamico di un gas (perfetto) è determinato dalle sue variabili di stato: ressione, olume, Temperatura, n moli ffinché esse siano determinate è necessario
LEGGE DI STEVINO. La pressione non dipende dalla superficie della base del recipiente
 LA PRESSIONE NEI LIQUIDI DOVUTA ALLA FORZA PESO In condizioni di equilibrio la superficie libera di un liquido pesante deve essere piana ed orizzontale. Liquido di densitàρ Ogni strato orizzontale di liquido
LA PRESSIONE NEI LIQUIDI DOVUTA ALLA FORZA PESO In condizioni di equilibrio la superficie libera di un liquido pesante deve essere piana ed orizzontale. Liquido di densitàρ Ogni strato orizzontale di liquido
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
LEGGE DI STEVIN (EQUAZIONE FONDAMENTALE DELLA STATICA DEI FLUIDI PESANTI INCOMPRIMIBILI) z + p / γ = costante
 IDRAULICA LEGGE DI STEVIN (EQUAZIONE FONDAMENTALE DELLA STATICA DEI FLUIDI PESANTI INCOMPRIMIBILI) z + p / γ = costante 2 LEGGE DI STEVIN Z = ALTEZZA GEODETICA ENERGIA POTENZIALE PER UNITA DI PESO p /
IDRAULICA LEGGE DI STEVIN (EQUAZIONE FONDAMENTALE DELLA STATICA DEI FLUIDI PESANTI INCOMPRIMIBILI) z + p / γ = costante 2 LEGGE DI STEVIN Z = ALTEZZA GEODETICA ENERGIA POTENZIALE PER UNITA DI PESO p /
Esperienza con la macchina. termica
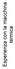 Esperienza con la macchina termica Macchina termica Il pistone in grafite scorre all interno del cilindro in pyrex in condizioni di quasi assenza di attrito. il sistema pistone-cilindro non garantisce
Esperienza con la macchina termica Macchina termica Il pistone in grafite scorre all interno del cilindro in pyrex in condizioni di quasi assenza di attrito. il sistema pistone-cilindro non garantisce
Il lavoro nelle macchine
 Il lavoro nelle macchine Corso di Impiego industriale dell energia Ing. Gabriele Comodi I sistemi termodinamici CHIUSO: se attraverso il contorno non c è flusso di materia in entrata ed in uscita APERTO:
Il lavoro nelle macchine Corso di Impiego industriale dell energia Ing. Gabriele Comodi I sistemi termodinamici CHIUSO: se attraverso il contorno non c è flusso di materia in entrata ed in uscita APERTO:
BILANCI DI ENERGIA. Capitolo 2 pag 70
 BILANCI DI ENERGIA Capitolo 2 pag 70 BILANCI DI ENERGIA Le energie in gioco sono di vario tipo: energia associata ai flussi entranti e uscenti (potenziale, cinetica, interna), Calore scambiato con l ambiente,
BILANCI DI ENERGIA Capitolo 2 pag 70 BILANCI DI ENERGIA Le energie in gioco sono di vario tipo: energia associata ai flussi entranti e uscenti (potenziale, cinetica, interna), Calore scambiato con l ambiente,
Lezione estd 29 pagina 1. Argomenti di questa lezione (esercitazione) Iniziare ad affrontare esercizi di termodinamica
 Lezione estd 29 pagina 1 Argomenti di questa lezione (esercitazione) Iniziare ad affrontare esercizi di termodinamica Lezione estd 29 pagina 2 Esercizio 3, 5 luglio 2005 Una macchina di Carnot produce
Lezione estd 29 pagina 1 Argomenti di questa lezione (esercitazione) Iniziare ad affrontare esercizi di termodinamica Lezione estd 29 pagina 2 Esercizio 3, 5 luglio 2005 Una macchina di Carnot produce
Corrente elettrica. Esempio LA CORRENTE ELETTRICA CONTINUA. Cos è la corrente elettrica? Definizione di intensità di corrente elettrica
 Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
Corrente elettrica LA CORRENTE ELETTRICA CONTINUA Cos è la corrente elettrica? La corrente elettrica è un flusso di elettroni che si spostano dentro un conduttore dal polo negativo verso il polo positivo
C V. gas monoatomici 3 R/2 5 R/2 gas biatomici 5 R/2 7 R/2 gas pluriatomici 6 R/2 8 R/2
 46 Tonzig La fisica del calore o 6 R/2 rispettivamente per i gas a molecola monoatomica, biatomica e pluriatomica. Per un gas perfetto, il calore molare a pressione costante si ottiene dal precedente aggiungendo
46 Tonzig La fisica del calore o 6 R/2 rispettivamente per i gas a molecola monoatomica, biatomica e pluriatomica. Per un gas perfetto, il calore molare a pressione costante si ottiene dal precedente aggiungendo
2B LSSA Prof. Gariboldi a.s.14/15 Ripassare tutti gli argomenti come da programma e svolgere i seguenti esercizi
 COMPITI DELLE VACANZE PER IL RECUPERO DEL DEBITO 2B LSSA Prof. Gariboldi a.s.14/15 Ripassare tutti gli argomenti come da programma e svolgere i seguenti esercizi Moti 1) Scrivi la legge oraria del moto
COMPITI DELLE VACANZE PER IL RECUPERO DEL DEBITO 2B LSSA Prof. Gariboldi a.s.14/15 Ripassare tutti gli argomenti come da programma e svolgere i seguenti esercizi Moti 1) Scrivi la legge oraria del moto
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Statica e dinamica dei fluidi. A. Palano
 Statica e dinamica dei fluidi A. Palano Fluidi perfetti Un fluido perfetto e incomprimibile e indilatabile e non possiede attrito interno. Forza di pressione come la somma di tutte le forze di interazione
Statica e dinamica dei fluidi A. Palano Fluidi perfetti Un fluido perfetto e incomprimibile e indilatabile e non possiede attrito interno. Forza di pressione come la somma di tutte le forze di interazione
Temperatura. V(t) = Vo (1+at) Strumento di misura: termometro
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
LA TERMOLOGIA. studia le variazioni di dimensione di un corpo a causa di una
 LA TERMOLOGIA La termologia è la parte della fisica che si occupa dello studio del calore e dei fenomeni legati alle variazioni di temperatura subite dai corpi. Essa si può distinguere in: Termometria
LA TERMOLOGIA La termologia è la parte della fisica che si occupa dello studio del calore e dei fenomeni legati alle variazioni di temperatura subite dai corpi. Essa si può distinguere in: Termometria
Temperatura e Calore
 Temperatura e Calore La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero
Temperatura e Calore La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero
Aprile (recupero) tra una variazione di velocità e l intervallo di tempo in cui ha luogo.
 Febbraio 1. Un aereo in volo orizzontale, alla velocità costante di 360 km/h, lascia cadere delle provviste per un accampamento da un altezza di 200 metri. Determina a quale distanza dall accampamento
Febbraio 1. Un aereo in volo orizzontale, alla velocità costante di 360 km/h, lascia cadere delle provviste per un accampamento da un altezza di 200 metri. Determina a quale distanza dall accampamento
È una grandezza fisica FONDAMENTALE, SCALARE UNITÀ DI MISURA NEL S.I. : K (KELVIN)
 È una grandezza fisica FONDAMENTALE, SCALARE UNITÀ DI MISURA NEL S.I. : K (KELVIN) È STRETTAMENTE LEGATA ALLA VELOCITÀ DI VIBRAZIONE DELLE MOLECOLE IN UN CORPO: SE LA TEMPERATURA DI UN CORPO AUMENTA LE
È una grandezza fisica FONDAMENTALE, SCALARE UNITÀ DI MISURA NEL S.I. : K (KELVIN) È STRETTAMENTE LEGATA ALLA VELOCITÀ DI VIBRAZIONE DELLE MOLECOLE IN UN CORPO: SE LA TEMPERATURA DI UN CORPO AUMENTA LE
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti.
 Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
LEGGI DEI GAS / CALORI SPECIFICI. Introduzione 1
 LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
Corso di Laurea in Farmacia Verifica in itinere 3 dicembre 2014 TURNO 1
 Corso di Laurea in Farmacia Verifica in itinere 3 dicembre 2014 TURNO 1 COMPITO A Un blocco di massa m 1 = 1, 5 kg si muove lungo una superficie orizzontale priva di attrito alla velocità v 1 = 8,2 m/s.
Corso di Laurea in Farmacia Verifica in itinere 3 dicembre 2014 TURNO 1 COMPITO A Un blocco di massa m 1 = 1, 5 kg si muove lungo una superficie orizzontale priva di attrito alla velocità v 1 = 8,2 m/s.
Stati di aggregazione della materia unità 2, modulo A del libro
 Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
13.1 (a) La quantità di calore dissipata dal resistore in un intervallo di tempo di 24 h è
 1 RISOLUZIONI cap.13 13.1 (a) La quantità di calore dissipata dal resistore in un intervallo di tempo di 24 h è (b) Il flusso termico è 13.2 (a) Il flusso termico sulla superficie del cocomero è (b) La
1 RISOLUZIONI cap.13 13.1 (a) La quantità di calore dissipata dal resistore in un intervallo di tempo di 24 h è (b) Il flusso termico è 13.2 (a) Il flusso termico sulla superficie del cocomero è (b) La
Macchine termiche. Alla fine di ogni ciclo il fluido ripassa per lo stesso stato.
 Macchine termiche In una macchina termica - ad esempio un motore - un fluido (il vapore delle vecchie locomotive, la miscela del motore a scoppio) esegue qualche tipo di ciclo termodinamico. Alla fine
Macchine termiche In una macchina termica - ad esempio un motore - un fluido (il vapore delle vecchie locomotive, la miscela del motore a scoppio) esegue qualche tipo di ciclo termodinamico. Alla fine
La teleferica dilatazione termica lineare
 La teleferica dilatazione termica lineare Una teleferica di montagna è costituita da un cavo di acciaio (λ = 1,2 10-5 K -1 ) di lunghezza 5,4 km. D'estate, la temperatura del cavo può passare dai 5 gradi
La teleferica dilatazione termica lineare Una teleferica di montagna è costituita da un cavo di acciaio (λ = 1,2 10-5 K -1 ) di lunghezza 5,4 km. D'estate, la temperatura del cavo può passare dai 5 gradi
Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1. Termodinamica
 Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Termodinamica 1) In un recipiente di volume V = 20 l sono contenute 0.5 moli di N 2 (PM=28) alla temperatura di 27 0 C.
Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Termodinamica 1) In un recipiente di volume V = 20 l sono contenute 0.5 moli di N 2 (PM=28) alla temperatura di 27 0 C.
Q t CORRENTI ELETTRICHE
 CORRENTI ELETTRICHE La corrente elettrica è un flusso di particelle cariche. L intensità di una corrente è definita come la quantità di carica netta che attraversa nell unità di tempo una superficie: I
CORRENTI ELETTRICHE La corrente elettrica è un flusso di particelle cariche. L intensità di una corrente è definita come la quantità di carica netta che attraversa nell unità di tempo una superficie: I
3) In una gara sui 100 m piani, percorsi in 10 s ad accelerazione costante, quale sarà (in km/h) la velocità finale
 Esercizi 1) Un sasso di massa 1 kg lasciato cadere dalla cima di un grattacielo giunge a terra dopo 4 s. Calcolare la velocità del sasso al momento dell impatto e l altezza dell edificio. 2) Un sasso di
Esercizi 1) Un sasso di massa 1 kg lasciato cadere dalla cima di un grattacielo giunge a terra dopo 4 s. Calcolare la velocità del sasso al momento dell impatto e l altezza dell edificio. 2) Un sasso di
Fisica II. 4 Esercitazioni
 Fisica Esercizi svolti Esercizio 4. n un materiale isolante si ricava una semisfera di raggio r m, sulla cui superficie si deposita uno strato conduttore, che viene riempita di un liquido con ρ 5 0 0 Ωm.
Fisica Esercizi svolti Esercizio 4. n un materiale isolante si ricava una semisfera di raggio r m, sulla cui superficie si deposita uno strato conduttore, che viene riempita di un liquido con ρ 5 0 0 Ωm.
F S V F? Soluzione. Durante la spinta, F S =ma (I legge di Newton) con m=40 Kg.
 Spingete per 4 secondi una slitta dove si trova seduta la vostra sorellina. Il peso di slitta+sorella è di 40 kg. La spinta che applicate F S è in modulo pari a 60 Newton. La slitta inizialmente è ferma,
Spingete per 4 secondi una slitta dove si trova seduta la vostra sorellina. Il peso di slitta+sorella è di 40 kg. La spinta che applicate F S è in modulo pari a 60 Newton. La slitta inizialmente è ferma,
Cos è una. pompa di calore?
 Cos è una pompa di calore? !? La pompa di calore aria/acqua La pompa di calore (PDC) aria-acqua è una macchina in grado di trasferire energia termica (calore) dall aria esterna all acqua dell impianto
Cos è una pompa di calore? !? La pompa di calore aria/acqua La pompa di calore (PDC) aria-acqua è una macchina in grado di trasferire energia termica (calore) dall aria esterna all acqua dell impianto
Una forza, per la fisica, compie un lavoro se provoca uno spostamento.
 Lavoro La forza è la causa del cambiamento di moto di un corpo (dinamica). Se la risultante di puù forze applicate ad un corpo è nulla il corpo è in equilibrio stabile (statica). Una forza può causare
Lavoro La forza è la causa del cambiamento di moto di un corpo (dinamica). Se la risultante di puù forze applicate ad un corpo è nulla il corpo è in equilibrio stabile (statica). Una forza può causare
Michele D'Amico (premiere) 6 May 2012
 Michele D'Amico (premiere) CORRENTE ELETTRICA 6 May 2012 Introduzione La corrente elettrica può essere definita come il movimento ordinato di cariche elettriche, dove per convenzione si stabilisce la direzione
Michele D'Amico (premiere) CORRENTE ELETTRICA 6 May 2012 Introduzione La corrente elettrica può essere definita come il movimento ordinato di cariche elettriche, dove per convenzione si stabilisce la direzione
PROBLEMA 1. Soluzione. Indicare quattro requisiti fondamentali che un fluido frigorigeno deve possedere: 1) 2) 3) 4)
 PROBLEMA 1 Indicare quattro requisiti fondamentali che un fluido frigorigeno deve possedere: 1) 2) 3) 4) Deve possedere un elevato calore latente, cioè, deve evaporare asportando molto calore dall ambiente
PROBLEMA 1 Indicare quattro requisiti fondamentali che un fluido frigorigeno deve possedere: 1) 2) 3) 4) Deve possedere un elevato calore latente, cioè, deve evaporare asportando molto calore dall ambiente
CHIMICA GENERALE MODULO
 Corso di Scienze Naturali CHIMICA GENERALE MODULO 6 Termodinamica Entalpia Entropia Energia libera - Spontaneità Relatore: Prof. Finelli Mario Scienza che studia i flussi energetici tra un sistema e l
Corso di Scienze Naturali CHIMICA GENERALE MODULO 6 Termodinamica Entalpia Entropia Energia libera - Spontaneità Relatore: Prof. Finelli Mario Scienza che studia i flussi energetici tra un sistema e l
CICLO FRIGORIFERO PER RAFFREDDAMENTO
 CICLO FRIGORIFERO PER RAFFREDDAMENTO REGIONE CALDA Liquido saturo o sottoraffreddato Q out 3 2 Vapore surriscaldato valvola di espansione condensatore compressore P c evaporatore 4 1 Miscela bifase liquidovapore
CICLO FRIGORIFERO PER RAFFREDDAMENTO REGIONE CALDA Liquido saturo o sottoraffreddato Q out 3 2 Vapore surriscaldato valvola di espansione condensatore compressore P c evaporatore 4 1 Miscela bifase liquidovapore
Temperatura e Calore
 Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
Termodinamica: legge zero e temperatura
 Termodinamica: legge zero e temperatura Affrontiamo ora lo studio della termodinamica che prende in esame l analisi dell energia termica dei sistemi e di come tale energia possa essere scambiata, assorbita
Termodinamica: legge zero e temperatura Affrontiamo ora lo studio della termodinamica che prende in esame l analisi dell energia termica dei sistemi e di come tale energia possa essere scambiata, assorbita
Seconda legge della termodinamica
 Seconda legge della termodinamica In natura tutti i processi devono soddisfare il principio di conservazione dell energia (e quindi anche la a legge della termodinamica) ma non tutti i processi che conservano
Seconda legge della termodinamica In natura tutti i processi devono soddisfare il principio di conservazione dell energia (e quindi anche la a legge della termodinamica) ma non tutti i processi che conservano
Prova intercorso di Fisica 2 dott. Esposito 27/11/2009
 Prova intercorso di Fisica 2 dott. Esposito 27/11/2009 Anno di corso: 1) Una carica puntiforme q=-8.5 10-6 C è posta a distanza R=12 cm da un piano uniformemente carico condensità di carica superficiale
Prova intercorso di Fisica 2 dott. Esposito 27/11/2009 Anno di corso: 1) Una carica puntiforme q=-8.5 10-6 C è posta a distanza R=12 cm da un piano uniformemente carico condensità di carica superficiale
Esercitazione X - Legge dei gas perfetti e trasformazioni
 Esercitazione X - Legge dei gas perfetti e trasformazioni termodinamiche Formulario Il primo principio della termodinamica afferma che la variazione dell energia interna di un sistema U è uguale alla somma
Esercitazione X - Legge dei gas perfetti e trasformazioni termodinamiche Formulario Il primo principio della termodinamica afferma che la variazione dell energia interna di un sistema U è uguale alla somma
ENERGIA INTERNA ENERGIA INTERNA SPECIFICA. e = E/m = cv T ENTALPIA. H = E + pv ENTALPIA SPECIFICA. h = H/m = cp T h = e + pv = e + p/d L-1
 L - SISTEMI APERTI ENERGIA INTERNA E = n Cv T E = m cv T (Cv molare = J/kmol C) (cv massico = J/kg C) ENERGIA INTERNA SPECIFICA e = E/m = cv T ENTALPIA H = E + pv H = n Cp T H = m cp T (Cp molare = J/kmol
L - SISTEMI APERTI ENERGIA INTERNA E = n Cv T E = m cv T (Cv molare = J/kmol C) (cv massico = J/kg C) ENERGIA INTERNA SPECIFICA e = E/m = cv T ENTALPIA H = E + pv H = n Cp T H = m cp T (Cp molare = J/kmol
Esempio Esame di Fisica Generale I C.d.L. ed.u. Informatica
 Esempio Esame di Fisica Generale I C.d.L. ed.u. Informatica Nome: N.M.: 1. 1d (giorno) contiene all incirca (a) 8640 s; (b) 9 10 4 s; (c) 86 10 2 s; (d) 1.44 10 3 s; (e) nessuno di questi valori. 2. Sono
Esempio Esame di Fisica Generale I C.d.L. ed.u. Informatica Nome: N.M.: 1. 1d (giorno) contiene all incirca (a) 8640 s; (b) 9 10 4 s; (c) 86 10 2 s; (d) 1.44 10 3 s; (e) nessuno di questi valori. 2. Sono
Fisica Generale 1 per Ing. Gestionale e Chimica (Prof. F. Forti) A.A. 2011/12 Appello del 29/01/2013.
 Fisica Generale per Ing. Gestionale e Chimica (Prof. F. Forti) A.A. 20/2 Appello del 29/0/203. Tempo a disposizione: 2h30. Scrivere solamente su fogli forniti Modalità di risposta: spiegare sempre il procedimento
Fisica Generale per Ing. Gestionale e Chimica (Prof. F. Forti) A.A. 20/2 Appello del 29/0/203. Tempo a disposizione: 2h30. Scrivere solamente su fogli forniti Modalità di risposta: spiegare sempre il procedimento
Motori e cicli termodinamici
 Motori e cicli termodinamici 1. Motore a scoppio 2. Motore diesel 3. Frigoriferi 4. Centrali elettriche XXII - 0 Trasformazioni Trasformazioni reversibili (quasistatiche: Ciascun passo della trasformazione
Motori e cicli termodinamici 1. Motore a scoppio 2. Motore diesel 3. Frigoriferi 4. Centrali elettriche XXII - 0 Trasformazioni Trasformazioni reversibili (quasistatiche: Ciascun passo della trasformazione
Ottava esercitazione di Fisica I Termodinamica 1 PROBLEMI RISOLTI
 Ottava esercitazione di Fisica I ermodamica PROBLEMI RISOLI. Il rapporto tra il lavoro compiuto ed il calore assorbito da una mole di gas monoatomico che si espande isobaricamente alla pressione di una
Ottava esercitazione di Fisica I ermodamica PROBLEMI RISOLI. Il rapporto tra il lavoro compiuto ed il calore assorbito da una mole di gas monoatomico che si espande isobaricamente alla pressione di una
CORRENTE ELETTRICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V 2 isolati tra loro V 2 > V 1 V 2
 COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
Prova Scritta Completa-Fisica 9 CFU Corso di Laurea in Tossicologia dell ambiente e degli alimenti Novembre 2013
 Prova Scritta Completa-Fisica 9 CFU Corso di Laurea in Tossicologia dell ambiente e degli alimenti Novembre 2013 Quesito 1 Due cubi A e B costruiti con lo stesso legno vengono trascinati sullo stesso pavimento.
Prova Scritta Completa-Fisica 9 CFU Corso di Laurea in Tossicologia dell ambiente e degli alimenti Novembre 2013 Quesito 1 Due cubi A e B costruiti con lo stesso legno vengono trascinati sullo stesso pavimento.
Applicazioni del secondo principio. ovvero. Macchine a vapore a combustione esterna: Macchine a vapore a combustione interna: Ciclo Otto, ciclo Diesel
 Termodinamica Applicazioni del secondo principio ovvero Macchine a vapore a combustione esterna: macchina di Newcomen e macchina di Watt Macchine a vapore a combustione interna: Ciclo Otto, ciclo Diesel
Termodinamica Applicazioni del secondo principio ovvero Macchine a vapore a combustione esterna: macchina di Newcomen e macchina di Watt Macchine a vapore a combustione interna: Ciclo Otto, ciclo Diesel
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
DINAMICA. 1. La macchina di Atwood è composta da due masse m
 DINAMICA. La macchina di Atwood è composta da due masse m e m sospese verticalmente su di una puleggia liscia e di massa trascurabile. i calcolino: a. l accelerazione del sistema; b. la tensione della
DINAMICA. La macchina di Atwood è composta da due masse m e m sospese verticalmente su di una puleggia liscia e di massa trascurabile. i calcolino: a. l accelerazione del sistema; b. la tensione della
Il Sistema Respiratorio. Fisica Medica
 Il Sistema Respiratorio La respirazione Trachea Bronchi Muscoli del diaframma I muscoli che controllano la respirazione fanno variare volume e pressione interna ai polmoni Fase Inspirazione Espirazione
Il Sistema Respiratorio La respirazione Trachea Bronchi Muscoli del diaframma I muscoli che controllano la respirazione fanno variare volume e pressione interna ai polmoni Fase Inspirazione Espirazione
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
Ripetizioni Cagliari di Manuele Atzeni - 3497702002 - info@ripetizionicagliari.it
 Calorimetria: soluzioni Problema di: Calorimetria - Q0001 Problema di: Calorimetria - Q0002 Scheda 8 Ripetizioni Cagliari di Manuele Atzeni - 3497702002 - info@ripetizionicagliari.it Testo [Q0001] Quanta
Calorimetria: soluzioni Problema di: Calorimetria - Q0001 Problema di: Calorimetria - Q0002 Scheda 8 Ripetizioni Cagliari di Manuele Atzeni - 3497702002 - info@ripetizionicagliari.it Testo [Q0001] Quanta
p atm 1. V B ; 2. T B ; 3. W A B 4. il calore specifico a volume costante c V
 1 Esercizio (tratto dal Problema 13.4 del Mazzoldi 2) Un gas ideale compie un espansione adiabatica contro la pressione atmosferica, dallo stato A di coordinate, T A, p A (tutte note, con p A > ) allo
1 Esercizio (tratto dal Problema 13.4 del Mazzoldi 2) Un gas ideale compie un espansione adiabatica contro la pressione atmosferica, dallo stato A di coordinate, T A, p A (tutte note, con p A > ) allo
Nome e Cognome. Nella copia da riconsegnare si scrivano solo il risultato numerico e la formula finale. Non riportare tutto il procedimento.
 Dipartimento di Scienze Agrarie, Alimentari e Agro-Ambientali: Corso di Fisica AA 13/14 Test di ammissione all'orale di Fisica. Appello del 16 Marzo 2015 Nome e Cognome Nella copia da riconsegnare si scrivano
Dipartimento di Scienze Agrarie, Alimentari e Agro-Ambientali: Corso di Fisica AA 13/14 Test di ammissione all'orale di Fisica. Appello del 16 Marzo 2015 Nome e Cognome Nella copia da riconsegnare si scrivano
Esercitazione 5 Dinamica del punto materiale
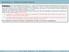 Problema 1 Un corpo puntiforme di massa m = 1.0 kg viene lanciato lungo la superficie di un cuneo avente un inclinazione θ = 40 rispetto all orizzontale e altezza h = 80 cm. Il corpo viene lanciato dal
Problema 1 Un corpo puntiforme di massa m = 1.0 kg viene lanciato lungo la superficie di un cuneo avente un inclinazione θ = 40 rispetto all orizzontale e altezza h = 80 cm. Il corpo viene lanciato dal
La fisica di Feynmann Termodinamica
 La fisica di Feynmann Termodinamica 3.1 TEORIA CINETICA Teoria cinetica dei gas Pressione Lavoro per comprimere un gas Compressione adiabatica Compressione della radiazione Temperatura Energia cinetica
La fisica di Feynmann Termodinamica 3.1 TEORIA CINETICA Teoria cinetica dei gas Pressione Lavoro per comprimere un gas Compressione adiabatica Compressione della radiazione Temperatura Energia cinetica
Proprieta meccaniche dei fluidi
 Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
Termologia. Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti
 Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Ripasso sulla temperatura, i gas perfetti e il calore
 Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
I.T.C.G.T T. Acerbo - Pescara LABORATORIO DI FISICA A. S. 2009/10
 I.T.C.G.T T. Acerbo - Pescara LABORATORIO DI FISICA A. S. 2009/10 Cognome: D Ovidio Nome: Stefania Classe: 2 B Geometri Data: 04/12/2009 Gruppo: F. Illiceto; V. Ivanochko; M.C. Scopino; M.Terenzi N. pagine:
I.T.C.G.T T. Acerbo - Pescara LABORATORIO DI FISICA A. S. 2009/10 Cognome: D Ovidio Nome: Stefania Classe: 2 B Geometri Data: 04/12/2009 Gruppo: F. Illiceto; V. Ivanochko; M.C. Scopino; M.Terenzi N. pagine:
IMPIANTI DI CLIMATIZZAZIONE
 IMPIANTI DI CLIMATIZZAZIONE parti 3 4 1 IMPIANTO TERMICO In generale si può pensare articolato nelle seguenti parti: Generatore uno o più apparati che forniscono energia termica ad un mezzo di trasporto
IMPIANTI DI CLIMATIZZAZIONE parti 3 4 1 IMPIANTO TERMICO In generale si può pensare articolato nelle seguenti parti: Generatore uno o più apparati che forniscono energia termica ad un mezzo di trasporto
2. La disequazione 9 (3x 2 + 2) > 16 (x - 3) è soddisfatta: A) sempre B) solo per x < 0 C) solo per x > 2/3 D) mai E) solo per x < 2/3
 MATEMATICA 1. Per quali valori di x è x 2 > 36? A) x > - 6 B) x < - 6, x > 6 C) - 6 < x < 6 D) x > 6 E) Nessuno 2. La disequazione 9 (3x 2 + 2) > 16 (x - 3) è soddisfatta: A) sempre B) solo per x < 0 C)
MATEMATICA 1. Per quali valori di x è x 2 > 36? A) x > - 6 B) x < - 6, x > 6 C) - 6 < x < 6 D) x > 6 E) Nessuno 2. La disequazione 9 (3x 2 + 2) > 16 (x - 3) è soddisfatta: A) sempre B) solo per x < 0 C)
CAFFE` Il segreto è nel fisico
 CAFFE` Il segreto è nel fisico Preparata la macchina del caffè, e messala sul fuoco: L acqua raggiunge rapidamente la temperatura di ebollizione (100 C). Lo spazio del serbatoio lasciato libero viene occupato
CAFFE` Il segreto è nel fisico Preparata la macchina del caffè, e messala sul fuoco: L acqua raggiunge rapidamente la temperatura di ebollizione (100 C). Lo spazio del serbatoio lasciato libero viene occupato
Le macchine termiche e il secondo principio della termodinamica
 Le macchine termiche e il secondo principio della termodinamica ) Definizione di macchina termica È sperimentalmente verificato che nel rispetto del primo principio della termodinamica (ovvero della conservazione
Le macchine termiche e il secondo principio della termodinamica ) Definizione di macchina termica È sperimentalmente verificato che nel rispetto del primo principio della termodinamica (ovvero della conservazione
Simulazione test di ingresso Ingegneria Industriale Viterbo. Quesiti di Logica, Chimica e Fisica. Logica
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di numeri? 9, 16, 25, 36,... A) 47 B) 49 C) 48 D) 45 L2 - Quale
Miglioramenti Energetici Solare Termico. Aslam Magenta - Ing. Mauro Mazzucchelli Anno Scolastico 2014-2015 81
 Miglioramenti Energetici Solare Termico Scolastico 2014-2015 81 Sostituzione Generatore di Calore Sostituzione adeguamento sistema di Distribuzione Sostituzione del sistema di emissione Installazione Solare
Miglioramenti Energetici Solare Termico Scolastico 2014-2015 81 Sostituzione Generatore di Calore Sostituzione adeguamento sistema di Distribuzione Sostituzione del sistema di emissione Installazione Solare
LEGGE GAS PERFETTI. Gas perfetto è governato dalla legge: PV=nRT=(N/NA) RT. kb=1.38*10-23 (J/K) cost Boltzmann
 LEGGE GAS PERFETTI Gas perfetto è governato dalla legge: PV=nRT=(N/NA) RT PV=NkBT dove kb=r/na kb=1.38*10-23 (J/K) cost Boltzmann TEORIA CINETICA DEI GAS Scopo: legame tra quantità macroscopiche e microscopiche
LEGGE GAS PERFETTI Gas perfetto è governato dalla legge: PV=nRT=(N/NA) RT PV=NkBT dove kb=r/na kb=1.38*10-23 (J/K) cost Boltzmann TEORIA CINETICA DEI GAS Scopo: legame tra quantità macroscopiche e microscopiche
Facoltà di Ingegneria. Fisica 1. AA.2007/08. Prova in itinere n.2. Cognome Nome Anno di corso
 Siena 28/03/2008 vers.1 Si consideri il ciclo reversibile ABCA che riguarda del gas perfetto monoatomico e che è costituito, nell ordine, dalla compressione adiabatica AB, dall isoterma BC e dall isocora
Siena 28/03/2008 vers.1 Si consideri il ciclo reversibile ABCA che riguarda del gas perfetto monoatomico e che è costituito, nell ordine, dalla compressione adiabatica AB, dall isoterma BC e dall isocora
Energia e Lavoro. In pratica, si determina la dipendenza dallo spazio invece che dal tempo
 Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
CORRENTE E TENSIONE ELETTRICA LA CORRENTE ELETTRICA
 CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
Forza. Forza. Esempi di forze. Caratteristiche della forza. Forze fondamentali CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA
 Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Capitolo 10 Il primo principio 113
 Capitolo 10 Il primo principio 113 QUESITI E PROBLEMI 1 Tenuto conto che, quando il volume di un gas reale subisce l incremento dv, il lavoro compiuto dalle forze intermolecolari di coesione è L = n 2
Capitolo 10 Il primo principio 113 QUESITI E PROBLEMI 1 Tenuto conto che, quando il volume di un gas reale subisce l incremento dv, il lavoro compiuto dalle forze intermolecolari di coesione è L = n 2
 ST1 Un serbatoio contenente azoto liquido saturo a pressione ambiente (temperatura di saturazione -196 C) ha forma sferica ed è realizzato con due gusci metallici concentrici di spessore trascurabile e
ST1 Un serbatoio contenente azoto liquido saturo a pressione ambiente (temperatura di saturazione -196 C) ha forma sferica ed è realizzato con due gusci metallici concentrici di spessore trascurabile e
Fresco con il sol e 60% de risparmio energetico. SOLARCOOL TECNOLOGIA Spiegazione termodinamica
 Fresco con il sol e 60% de risparmio energetico SOLARCOOL TECNOLOGIA Spiegazione termodinamica L efficienza del sistema Solar Cool è possibile grazie ad un effetto fisico del flusso di massa, che è un
Fresco con il sol e 60% de risparmio energetico SOLARCOOL TECNOLOGIA Spiegazione termodinamica L efficienza del sistema Solar Cool è possibile grazie ad un effetto fisico del flusso di massa, che è un
Gas, liquidi, solidi. Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni).
 Gas, liquidi, solidi Tutti i gas raffreddati liquefano Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni). Sostanza T L ( C) T E ( C) He - -269 H 2-263
Gas, liquidi, solidi Tutti i gas raffreddati liquefano Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni). Sostanza T L ( C) T E ( C) He - -269 H 2-263
Analogia tra il circuito elettrico e il circuito idraulico
 UNIVERSITÁ DEGLI STUDI DELL AQUILA Scuola di Specializzazione per la Formazione degli Insegnanti nella Scuola Secondaria Analogia tra il circuito elettrico e il circuito idraulico Prof. Umberto Buontempo
UNIVERSITÁ DEGLI STUDI DELL AQUILA Scuola di Specializzazione per la Formazione degli Insegnanti nella Scuola Secondaria Analogia tra il circuito elettrico e il circuito idraulico Prof. Umberto Buontempo
