LA STRUTTURA DELLE MOLECOLE. Meccanica Quantistica e Orbitali Atomici
|
|
|
- Michelina Masini
- 7 anni fa
- Visualizzazioni
Transcript
1 LA STRUTTURA DELLE MOLECOLE Meccanica Quantistica e Orbitali Atomici
2 LE MOLECOLE Le molecole sono i costituenti di tutta la materia e possono essere considerate degli oggetti costruiti con componenti chiamati atomi che a loro volta hanno una complessa struttura composta da un nucleo con neutroni e protoni circondato all esterno da elettroni Le molecole sono oggetti molto piccoli, non visibili direttamente, esse hanno comunque delle dimensioni (tra 0,1 e 100 nm), una massa (tra e g) e delle forme molto variabili dipendenti da come gli atomi della molecola si assemblano tra di loro. Si è scoperto che, per la loro piccolissima dimensione, esse hanno un comportamento particolare differente dagli oggetti macroscopici che siamo abituati a vedere. I componenti delle molecole, gli atomi, posseggono al loro interno particelle come i protoni e gli elettroni con una carica elettrica. Gli elettroni, con la loro carica elettrica giocano un ruolo fondamentale nel tenere uniti gli atomi che formano una molecola
3 MATERIA MOLECOLE ATOMI PROTONI, NEUTRONI, ELETTRONI
4 DIFFERENZA TRA OGGETTI MACROSCOPICI E OGGETTI DI DIMENSONI ATOMICHE v v s s s = v t elettrone v? Possiamo solo calcolare la probabilità che ha l elettrone di trovarsi nel punto s al tempo t
5 Pulci con sufficiente energia per uscire dal buco Pulci con insufficiente energia per uscire dal buco Elettroni con sufficiente energia per uscire dal buco EFFETTO ANTITUNNEL Elettroni con insufficiente energia per uscire dal buco EFFETTO TUNNEL
6 PROBABILITA ED EFFETTI TUNNEL E ANTITUNNEL L effetto tunnel si manifesta anche se tutti gli elettroni della buca hanno la stessa energia, insufficiente a saltarne fuori, tuttavia la probabilità che un elettrone salti fuori è tanto più bassa quanto più elevata è la differenza tra l energia che possiede l elettrone e quella necessaria per saltare fuori. Lo stesso vale per l effetto antitunnel la probabilità che un elettrone ha di non riuscire a saltare fuori è tanto più alta quanto minore è la differenza di energia tra quella che possiede l elettrone (sufficiente a uscire dalla buca) e l energia minima necessaria per uscire dalla buca.
7
8
9 LA PROBABILITA Testa o croce? Vi è il 50% di probabilità che esca testa e il 50% che esca croce Quale è la probabilità che esca il 3? Vi sono 6 facce e quindi la probabilità è di una su sei e quindi del 16,7 % In matematica la probabilità si esprime non solo come % ma anche con un numero compreso tra 0 e 1 dove 0 o 0% significa che l evento non accade mentre 1 o 100% si è sicuri che l evento accade.
10 LE FORZE ELETTRICHE Legge di Coulomb : F = k q 1 q 2 /r 2 se q 1 = q 2 allora q = r(f/k) ½ La forza F è la stessa che si esercita tra gli elettroni e i protoni del nucleo atomico POLARIZZAZIONE : + - e- e- +
11 ENERGIA NELLA MECCANICA CLASSICA Energia cinetica: K = ½ mv 2 Energia potenziale: V = mgh Energia totale : E = K + V = ½ mv 2 + mgh
12 ENERGIA NELLA MECCANICA QUANTISTICA Equazione di Schrödinger Operatore complesso chiamato Hamiltoniano. Gli operatori in matematica sono i simboli che servono a fare un operazione. Es: +, x,, log, ecc. Hψ = E ψ Energia della particella (esempio: elettrone) Funzione matematica detta funzione d onda Risolvere l equazione di Scrödinger significa trovare la giusta forma della funzione ψ che soddisfa l equazione (In matematica sono funzioni ad esempio: y = ax, y = c + bx 2, ecc.) La funzioneψci permette anche di calcolare la probabilità che una particella ha di trovarsi in un certo posto o avere una certa energia, ecc.
13 METAFORA DELL EQUAZIONE DI SCHROEDINGER L equazione di Schrödinger è composta da un operatore H (detto hamiltoniano) che agisce su una funzione ψ (detta funzione d onda) il cui risultato è la funzione stessa moltiplicata per una costante che risulta pari al valore dell energia E del sistema. Hψ = E ψ Possiamo avere un idea di come funziona l equazione immaginando un qualsiasi operatore matematico, ad esempio: moltiplica la funzione per 2 e quindi aggiungi 5, da cui avremo per analogia: {operatore f(x)} = Ef(x) Se per semplicità la funzione è uguale a una costante: f(x) = a, è facile ricavare E da: E = {operatore a}/a Si noti che in questo caso per ogni funzione (valore di a) che soddisfa l equazione esiste uno specifico valore di E. In effetti risolvere l equazione di Schrödinger significa trovare la forma di una serie di funzioni ψ ognuna delle quali corrisponde a un specifico valore di energia E (quantizzazione dell energia). La funzione ψ ci permette poi di determinare la probabilità di trovare ad esempio un elettrone in una certa posizione attorno al nucleo atomico in tutto lo spazio che circonda il nucleo, e questo vale però per una specifica funzione ψ associata a una particolare energia E dell elettrone. Se l energia dell elettrone cambia, cambia anche la funzione ψ e viceversa.
14 UTILIZZAZIONE DELL EQUAZIONE DI SCHROEDINGER L equazione di Schrödinger in chimica è utile per determinare l energia e la funzione ψ degli elettroni che ci permette di localizzarli in zone precise in cui vi è un alta probabilità di trovarli (orbitali). La sua soluzione ci fornisce quindi le possibili energie e i possibili orbitali corrispondenti in cui vi è un elevata probabilità di trovarli. Essa si applica quindi agli atomi costituiti da un nucleo e uno o più elettroni, ma anche alle molecole costituite da almeno due nuclei e almeno due o più elettroni (molecola biatomica) o da più di due nuclei e numerosi elettroni (molecole poliatomiche). In ogni caso l equazione ci fornisce i livelli di energia possibili per gli elettroni e i possibili corrispondenti orbitali che, nel caso degli atomi, contengono solo un nucleo mentre, per le molecole, contengono almeno due o più nuclei.
15 DIFFERENZE TRA MECCANICA QUANTISTICA E MECCANICA CLASSICA Mentre in meccanica classica è sempre possibile stabilire dove si trova una certa particella e che proprietà ha, in meccanica quantistica si può solo stabilire la probabilità che una particella si trovi in un certo posto o che abbia una certa energia, ecc. Le particelle possono avere inoltre proprietà, come quella di natura magnetica detta spin, che non si ritrovano nei corpi macroscopici In meccanica quantistica certe grandezze come l energia o lo spin possono avere solo valori precisi quantizzati e non qualsiasi valore come in meccanica classica
16 Immagine del cervello umano ottenuta per risonanza magnetica nucleare e basata sull esistenza di proprietà di spin nei nuclei atomici
17 L ATOMO DI IDROGENO L atomo di idrogeno è il più semplice degli atomi poiché è costituito semplicemente da un protone e da un elettrone. Se applichiamo al caso dell atomo di idrogeno l equazione di Schrödinger possiamo ottenere esattamente la sua funzione ψ che sarà in grado di indicarci i possibili valori di energia che può possedere l elettrone nel suo moto attorno al nucleo e la probabilità di trovare l elettrone nei vari punti dello spazio attorno al nucleo. I vari livelli di energia possibili per l elettrone sono indicati con i i numeri n uguale a 1, 2, 3, ecc. nella figura seguente che indica anche i possibili salti di livello di energia che può avere l elettrone se viene eccitato fornendogli energia
18 LIVELLI ENERGETICI DELL ELETTRONE NELL ATOMO DI IDROGENO
19 GLI ORBITALI ATOMICI Se noi prendiamo ora in considerazione la zona dello spazio in cui esiste, come indicato dall equazione di Schrödinger, un elevata probabilità di trovare un elettrone, ad esempio del 90%, possiamo definire una superficie nello spazio che racchiude questa zona che è chiamata orbitale atomico. Gli orbitali atomici hanno una forma differente a seconda del livello di energia preso in considerazione. La forma dell orbitale atomico viene indicata con le lettere s, p, d, f mentre il numero che precede la lettera il livello n di energia. Avremo così ad esempio l orbitale 1s per il livello di energia n =1 e 2s per il livello di energia n = 2. ecc. La forma dell orbitale s è una superficie sferica mentre gli altri orbitali hanno forme alquanto variabili come indicato nella figura seguente.
20 UN ALTRO MODO DI DEFINIRE GLI ORBITALI ATOMICI DELL ATOMO DI IDROGENO L atomo di idrogeno è composto da un nucleo costituito da un protone e da un elettrone. Risolvendo l equazione di Schrödinger per un tale sistema, si trova che esistono vari livelli di energia che può avere l elettrone e che sono indicati con la lettera n=1, n=2, n=3, ecc. Ad ogni livello di energia è associata una particolare funzione ψ 1, ψ 2, ψ 3, ecc. che ci permette di calcolare la probabilità di trovare l elettrone in un certo punto dello spazio attorno al nucleo. Se si prendono in considerazione per un certo livello n e la sua funzione ψ associata, tutti i punti dello spazio attorno al nucleo in cui la probabilità di trovare l elettrone è maggiore ad esempio del 90%, si formerà una figura di una certa forma che è chiamata orbitale. Nei punti distanti dal nucleo, che non sono però all interno di questa figura, avremo quindi una probabilità di trovare l elettrone inferiore al 10%. Nel caso del livello energetico più basso (n=1) la forma dell orbitale è una sfera con al centro il nucleo e l orbitale è indicato come 1s. Per il livello di energia più alto (n =2) l equazione di Schrödinger presenta ben 4 soluzioni di ψ da cui si possono dedurre 4 tipi di orbitali: uno, il 2s, è anch esso di forma sferica come l 1s ma più grande mentre gli altri tre hanno la forma di due lobi uniti in un punto corrispondente al nucleo e orientati rispettivamente verso i tre assi dello spazio x, y e z.
21
22 Orbitali s dell idrogeno: le zone ombreggiate indicano dove all interno dell orbitale si ha la maggiore probabilità di trovare l elettrone Questa immagine mostra come varia la funzione ψ per gli orbitali 1s, 2s, 3s dell atomo di idrogeno. Come si può vedere la probabilità di trovare un elettrone all interno di un orbitale s non è omogenea in tutto l orbitale ma è massima a certe distanze dal nucleo. Più gli orbitali s sono energetici più vi sono zone dove la probabilità è massima. Questa situazione assomiglia al caso delle corde vibranti e alle onde stazionarie che si formano (vedi caso della chitarra o del violino) da cui il nome dato alla funzione ψ di funzione d onda Valori della funzione ψ in funzione della distanza r tra il nucleo e l elettrone
23 LIVELLI ENERGETICI ED ORBITALI In conclusione l equazione di Schrödinger prevede che l elettrone che si muove attorno al nucleo possa avere vari livelli di energia e a che ogni livello energetico siano associati delle zone ad alta probabilità di trovare l elettrone (orbitali) che possono avere forme differenti. In particolare essa prevede ad esempio: Al livello di energia n=1 esiste solo l orbitale 1s Al livello di energia n=2 esiste l orbitale 2s e tre orbitali p di forma simile ma orientati nello spazio nei tre assi x, y, z (2p x, 2p y, 2p z ) Al livello di energia n = 3 esiste l orbitale 3s, i tre orbitali 3p e ben 5 orbitali 3d Al livello di energia n = 4 esistono, oltre all orbitale 4s, i tre orbitali 4p e i 5 orbitali 4d anche 7 orbitali 4f
24 VERIFICHE SPERIMENTALI I risultati ottenuti con l equazione di Schrödinger per l atomo di idrogeno sono confermati dalle misure fatte sull emissione di luce che avviene quando si eccitano gli elettroni degli atomi di idrogeno con l alta temperatura o con scariche elettriche. Infatti si è osservato che gli elettroni assorbono in questo caso l energia necessaria per saltare tra i vari livelli e poi ritornano verso i livelli più bassi di energia emettendo l energia ricevuta sotto forma di pacchetti o quanti di luce, chiamati fotoni, che possiedono quindi quantità di energia precise che possono essere intercettate e misurate in un apparecchiatura chiamata spettrometro. Questo strumento separa la luce che riceve a seconda dell energia dei vari fotoni facendo apparire sullo schermo varie righe. Interpretando il numero e le energie corrispondenti a queste righe è possibile ricostruire i vari tipi di salti fatti e quindi i livelli di energia che può possedere l atomo di idrogeno e che corrispondono molto bene a quelli calcolati con l equazione di Schrödinger. E dimostrato inoltre che l elettrone dell atomo di idrogeno che non è eccitato si trova nell orbitale 1s che è quello con il livello più basso di energia.
25 IL PRINCIPIO DI INDETERMINAZIONE DI HEISENBERG Orbitale p Se conosciamo con precisione l energia dell elettrone in un orbitale non conosciamo però con esattezza la sua posizione Orbitale s Nucleo dell atomo Se conosciamo con precisione la posizione dell elettrone non possiamo conoscere con precisione la sua energia Il fatto che non possiamo conoscere contemporaneamente con precisione la posizione e l energia di una particella, nel nostro caso un elettrone, è quanto stabilito dal cosiddetto PRINCIPIO DI INDETERMINAZIONE DI HEISENBERG
26 LO SPIN DELL ELETTRONE Come tutte le particelle anche l elettrone possiede uno spin, proprietà che non ha equivalenti per i corpi macroscopici. Lo spin dell elettrone come l energia è quantizzato ed esiste per due valori di segno opposto. Senza entrare in dettaglio su come si misura si possono indicare i due stati di spin con i segni: e Lo spin è in relazione con il magnetismo ma ciò non significa che l elettrone debba essere considerato come un piccolo ago di bussola. In effetti con una calamita è possibile invertire la direzione dell ago di una bussola ruotandola di 180 e ritornare nella posizione di partenza ruotando la calamita di 360. Nel caso dell elettrone è anche qui possibile con speciali campi magnetici invertire lo spin ma è necessario ruotarli di 360 e per riportarlo nella posizione iniziale occorre fare ben due giri completi (720 ).
27 GLI ATOMI POLIELETTRONICI Gli atomi polielettronici sono gli atomi che posseggono più di un elettrone e cioè praticamente tutti gli atomi ad esclusione dell idrogeno. Questi atomi sono molto più complicati ed è possibile trovare solo soluzioni approssimate dell equazione di Schrödinger i cui risultati si possono confrontare, come per l idrogeno, con quelli ottenuti allo spettroscopio. Le soluzioni approssimate dell equazione di Schrödinger e i risultati spettroscopici confermano sostanzialmente la struttura a livelli energetici e la forma degli orbitali simile a quella riscontrata per l atomo di idrogeno, anche se le energie dei livelli e la dimensione degli orbitali non è la stessa. Inoltre, la sequenza dei livelli energetici non è esattamente la stessa e, ad esempio, per gli atomi polielettronici gli orbitali p di un certo livello sono un po più energetici di quelli s dello stesso livello, e lo stesso avviene per gli orbitali d come rappresentato nella figura seguente.
28 LIVELLI DI ENERGIA E ORBITALI NEGLI ATOMI
29 DISPOSIZIONE DEGLI ELETTRONI La disposizione degli elettroni nei vari livelli ed orbitali degli atomi polielettronici segue essenzialmente due regole fondamentali dettate da: PRINCIPIO DI PAULI: questo principio stabilisce che gli elettroni occupano prima di tutto gli orbitali che sono meno energetici e che in un orbitale vi possono stare solo due elettroni con lo spin opposto REGOLA DI HUND : questa regola stabilisce che se vi sono più orbitali con la stessa energia gli elettroni si dispongono nel massimo numero possibile di questi orbitali. Se un orbitale contiene un solo elettrone, esso si dispone con lo spin orientato nella stessa direzione degli altri elettroni che si trovano soli in un orbitale della stessa energia
30 ESEMPI DI DISPOSIZIONE DEGLI ELETTRONI NEGLI ATOMI POLIELETTRONICI Energia relativa 2p C 1s 2 2s 2 2p 2 N 1s 2 2s 2 2p 3 O 1s 2 2s 2 2p 4 2s 1s
31 CONCLUSIONI SULLA STRUTTURA ELETTRONICA DEGLI ATOMI Gli elettroni nel loro movimento attorno al nucleo non obbediscono alle leggi della meccanica classica ma a quelle della meccanica quantistica Per gli elettroni noi possiamo conoscere solo i vari livelli di energia che possono assumere e il valore della probabilità di trovarli nello spazio attorno al nucleo I vari livelli energetici degli elettroni sono associati a corrispondenti zone di spazio attorno al nucleo di forma e dimensione diversa in cui esiste un elevata probabilità di trovare gli elettroni (orbitali atomici) Negli atomi polielettronici gli elettroni si sistemano negli orbitali obbedendo al Principio di esclusione di Pauli e alla Regola di Hund La struttura elettronica attorno al nucleo è determinata in meccanica quantistica dall equazione di Schrödinger i cui risultati sono in buon accordo con le misure spettroscopiche effettuate eccitando gli elettroni
LA STRUTTURA DELLE MOLECOLE. Mappa concettuale
 LA STRUTTURA DELLE OLECOLE appa concettuale INTRODUZIONE Questa mappa concettuale è stata preparata per un ciclo di lezioni sulla struttura delle molecole destinata a una 2 Liceo che ha già avuto lezioni
LA STRUTTURA DELLE OLECOLE appa concettuale INTRODUZIONE Questa mappa concettuale è stata preparata per un ciclo di lezioni sulla struttura delle molecole destinata a una 2 Liceo che ha già avuto lezioni
Struttura Elettronica degli Atomi Meccanica quantistica
 Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE
 LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
Modello atomico ad orbitali e numeri quantici
 Modello atomico ad orbitali e numeri quantici Il modello atomico di Bohr permette di scrivere correttamente la configurazione elettronica di un atomo ma ha dei limiti che sono stati superati con l introduzione
Modello atomico ad orbitali e numeri quantici Il modello atomico di Bohr permette di scrivere correttamente la configurazione elettronica di un atomo ma ha dei limiti che sono stati superati con l introduzione
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE
 LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
LA STRUTTURA DEGLI ATOMI GLI SPETTRI ATOMICI DI EMISSIONE LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LA RADIAZIONE ELETTROMAGNETICA LO SPETTRO ELETTROMAGNETICO LA QUANTIZZAZIONE DELL
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
La struttura dell atomo
 La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
La Teoria Atomica La struttura dell atomo 10-10 m 10-14 m Proprietà delle tre particelle subatomiche fondamentali Carica Massa Nome (simbolo) relativa assoluta (C) relativa (uma)* Assoluta (g) Posizione
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 3 STRUTTURA ATOMICA
 1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno:
 La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno: Vedi documento Atomo di Bohr.pdf sul materiale didattico per la derivazione di queste equazioni Livelli Energetici dell Atomo di Idrogeno
La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno: Vedi documento Atomo di Bohr.pdf sul materiale didattico per la derivazione di queste equazioni Livelli Energetici dell Atomo di Idrogeno
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
numeri quantici orbitale spin
 La funzione d onda ψ definisce i diversi stati in cui può trovarsi l elettrone nell atomo. Nella sua espressione matematica, essa contiene tre numeri interi, chiamati numeri quantici, indicati con le lettere
La funzione d onda ψ definisce i diversi stati in cui può trovarsi l elettrone nell atomo. Nella sua espressione matematica, essa contiene tre numeri interi, chiamati numeri quantici, indicati con le lettere
LA STRUTTURA DELLE MOLECOLE. Orbitali molecolari e legame chimico
 LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
Particelle Subatomiche
 GLI ATOMI Particelle Subatomiche ELEMENTI I diversi atomi sono caratterizzati da un diverso numero di protoni e neutroni; il numero di elettroni è sempre uguale al numero dei protoni (negli atomi neutri)
GLI ATOMI Particelle Subatomiche ELEMENTI I diversi atomi sono caratterizzati da un diverso numero di protoni e neutroni; il numero di elettroni è sempre uguale al numero dei protoni (negli atomi neutri)
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
ATOMO. Avogadro (1811) Volumi uguali di gas diversi contengono un ugual numero di MOLECOLE (N A =6,022*10 23 )
 ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
E. SCHRODINGER ( )
 E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA. (Plank Einstein)
 L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
Corso di CHIMICA LEZIONE 2
 Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica
 ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
ATOMI E PARTICELLE SUBATOMICHE
 ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
ATOMI E PARTICELLE SUBATOMICHE ELETTRICITÀ DELL ATOMO ESISTONO DUE TIPI DI CARICHE ELETTRICHE, DENOMINATE CONVENZIONALMENTE NEGATIVA E POSITIVA CARICHE DI SEGNO UGUALE SI RESPINGONO, MENTRE CARICHE DI
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Ma se dobbiamo trattare l elettrone come un onda occorre una funzione (che dobbiamo trovare) che ne descriva esaurientemente queste proprietà.
 Ma se dobbiamo trattare l elettrone come un onda occorre una funzione (che dobbiamo trovare) che ne descriva esaurientemente queste proprietà. Nell atomo l energia associata ad un elettrone (trascurando
Ma se dobbiamo trattare l elettrone come un onda occorre una funzione (che dobbiamo trovare) che ne descriva esaurientemente queste proprietà. Nell atomo l energia associata ad un elettrone (trascurando
COMPORTAMENTO DUALISTICO della MATERIA
 COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
L atomo di Bohr. Argomenti. Al tempo di Bohr. Spettri atomici 19/03/2010
 Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
Argomenti Spettri atomici Modelli atomici Effetto Zeeman Equazione di Schrödinger L atomo di Bohr Numeri quantici Atomi con più elettroni Al tempo di Bohr Lo spettroscopio è uno strumento utilizzato per
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
Comune ordine di riempimento degli orbitali di un atomo
 Comune ordine di riempimento degli orbitali di un atomo Le energie relative sono diverse per differenti elementi ma si possono notare le seguenti caratteristiche: (1) La maggior differenza di energia si
Comune ordine di riempimento degli orbitali di un atomo Le energie relative sono diverse per differenti elementi ma si possono notare le seguenti caratteristiche: (1) La maggior differenza di energia si
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
I numeri quantici. Numero quantico principale, n: numero intero Caratterizza l energia dell elettrone
 I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
Lezione n. 19. L equazione. di Schrodinger L atomo. di idrogeno Orbitali atomici. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
ATOMI MONOELETTRONICI
 ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
Generalità delle onde elettromagnetiche
 Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
the power of ten Prof.ssa Patrizia Gallucci
 https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
https://www.youtube.com/watch?v=5ckd0apswe8 the power of ten Prof.ssa Patrizia Gallucci ESPERIMENTO DI RUTHEFORD Dopo l esperimento Rutheford ipotizzò un atomo con un nucleo centrale,formato da neutroni
Atomo. Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale)
 Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Atomo Evoluzione del modello: Modello di Rutherford Modello di Bohr Modello quantomeccanico (attuale) 1 Modello di Rutherford: limiti Secondo il modello planetario di Rutherford gli elettroni orbitano
Modelli atomici Modello atomico di Rutheford Per t s d u i diare la t s rutt ttura t a omica Ruth th f or (
 Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Teoria Atomica Moderna. Chimica generale ed Inorganica: Chimica Generale. sorgenti di emissione di luce. E = hν. νλ = c. E = mc 2
 sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
CHIMICA: studio della struttura e delle trasformazioni della materia
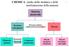 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
La struttura elettronica degli atomi
 1 In unità atomiche: a 0 me 0,59A unità di lunghezza e H 7, ev a H=Hartree unità di energia L energia dell atomo di idrogeno nello stato fondamentale espresso in unità atomiche è: 4 0 me 1 e 1 E H 13,
1 In unità atomiche: a 0 me 0,59A unità di lunghezza e H 7, ev a H=Hartree unità di energia L energia dell atomo di idrogeno nello stato fondamentale espresso in unità atomiche è: 4 0 me 1 e 1 E H 13,
Rappresentazione dell atomo. Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano.
 Rappresentazione dell atomo Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano. Informazioni importanti circa la dimensione dell atomo e la distribuzione della massa
Rappresentazione dell atomo Rutherford (1911) : modello planetario con il nucleo al centro e gli elettroni che ruotano. Informazioni importanti circa la dimensione dell atomo e la distribuzione della massa
RIASSUNTI DI CHIMICA
 Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 1 - LA STRUTTURA DELLA MATERIA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 1 - LA STRUTTURA DELLA MATERIA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
Quarta unità didattica. Disposizione degli elettroni nell atomo
 Quarta unità didattica Disposizione degli elettroni nell atomo Modello atomico di Bohr 1913 L' atomo di Borh consiste in un nucleo di carica positiva al quale ruotano intorno gli elettroni di carica negativa
Quarta unità didattica Disposizione degli elettroni nell atomo Modello atomico di Bohr 1913 L' atomo di Borh consiste in un nucleo di carica positiva al quale ruotano intorno gli elettroni di carica negativa
Gli argomenti trattati
 LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
ATOMO POLIELETTRONICO. Numero quantico di spin m s
 ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
FISICA delle APPARECCHIATURE per RADIOTERAPIA
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
LA STRUTTURA DELL ATOMO
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 3 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 3 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL
STRUTTURA ATOMICA. Per lo studio della struttura dell atomo ci si avvale della Spettroscopia.
 STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
I NUMERI QUANTICI. per l = orbitale: s p d f
 I NUMERI QUANTICI I numeri quantici sono quattro. I primi tre servono a indicare e a distinguere i diversi orbitali. Il quarto numero descrive una proprietà tipica dell elettrone. Esaminiamo in dettaglio
I NUMERI QUANTICI I numeri quantici sono quattro. I primi tre servono a indicare e a distinguere i diversi orbitali. Il quarto numero descrive una proprietà tipica dell elettrone. Esaminiamo in dettaglio
CALCOLO DELLA STRUTTURA MOLECOLARE: 1. LE SUPERFICI DI ENERGIA POTENZIALE E L APPROSSIMAZIONE DI BORN-OPPENHEIMER
 CALCOLO DELLA STRUTTURA MOLECOLARE: 1. LE SUPERFICI DI ENERGIA POTENZIALE E L APPROSSIMAZIONE DI BORN-OPPENHEIMER 1 COSA E UNA MOLECOLA Tutti gli atomi a piccola distanza si attraggono (forze di van der
CALCOLO DELLA STRUTTURA MOLECOLARE: 1. LE SUPERFICI DI ENERGIA POTENZIALE E L APPROSSIMAZIONE DI BORN-OPPENHEIMER 1 COSA E UNA MOLECOLA Tutti gli atomi a piccola distanza si attraggono (forze di van der
Numeri quantici. Numero quantico principale n: determina l'energia dell'elettrone e può assumere qualsiasi valore intero positivo.
 Numeri quantici Numero quantico principale n: determina l'energia dell'elettrone e può assumere qualsiasi valore intero positivo. n= 1, 2, 3,. Numero quantico del momento angolare : Determina la forma
Numeri quantici Numero quantico principale n: determina l'energia dell'elettrone e può assumere qualsiasi valore intero positivo. n= 1, 2, 3,. Numero quantico del momento angolare : Determina la forma
Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti).
 4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
- Dati sperimentali: interazione luce / materia spettri caratteristici
 - Thomson: evidenza sperimentale per elettrone misura e/m e - Millikan: misura la carica dell elettrone e ne ricava la massa e = 1,60 x 10-19 C - Rutherford: stima le dimensioni atomiche struttura vuota
- Thomson: evidenza sperimentale per elettrone misura e/m e - Millikan: misura la carica dell elettrone e ne ricava la massa e = 1,60 x 10-19 C - Rutherford: stima le dimensioni atomiche struttura vuota
La Struttura degli Atomi
 La Struttura degli Atomi!!!!! Perché gli atomi si combinano per formare composti? Perché differenti elementi presentano differenti proprietà? Perché possono essere gassosi, liquidi, solidi, metalli o non-metalli?
La Struttura degli Atomi!!!!! Perché gli atomi si combinano per formare composti? Perché differenti elementi presentano differenti proprietà? Perché possono essere gassosi, liquidi, solidi, metalli o non-metalli?
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Dispense CHIMICA GENERALE E ORGANICA (STAL) 2012/13 Prof. P. Carloni GLI ATOMI
 GLI ATOMI L'atomo e le particelle che lo compongono, il nucleo e gli elettroni, numero atomico e numero di massa, isotopi, la struttura dell'atomo, gli orbitali s, p e d, la configurazione fondamentale
GLI ATOMI L'atomo e le particelle che lo compongono, il nucleo e gli elettroni, numero atomico e numero di massa, isotopi, la struttura dell'atomo, gli orbitali s, p e d, la configurazione fondamentale
Radioattività. 1. Massa dei nuclei. 2. Decadimenti nucleari. 3. Legge del decadimento XVI - 0. A. Contin - Fisica Generale Avanzata
 Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107
 LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
CHIMICA E BIOCHIMICA
 CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
6) Modello atomico a ORBITALI
 6) Modello atomico a ORBITALI PREMESSA: LIMITI DEL MODELLO DI BOHR (pag. 94 par.3) Applicando il concetto di quantizzazione dell E all atomo, Bohr ipotizzò che un atomo potesse esistere solo in determinati
6) Modello atomico a ORBITALI PREMESSA: LIMITI DEL MODELLO DI BOHR (pag. 94 par.3) Applicando il concetto di quantizzazione dell E all atomo, Bohr ipotizzò che un atomo potesse esistere solo in determinati
Il modello di Bohr. Lezioni d'autore di Giorgio Benedetti
 Il modello di Bohr Lezioni d'autore di Giorgio Benedetti VIDEO Gli spettri di emissione Nel 1859 il fisico G.R. Kirchoff scoprì che ogni elemento chimico presenta uno spettro di emissione caratteristico,
Il modello di Bohr Lezioni d'autore di Giorgio Benedetti VIDEO Gli spettri di emissione Nel 1859 il fisico G.R. Kirchoff scoprì che ogni elemento chimico presenta uno spettro di emissione caratteristico,
(98,9x12) + (1,1x13) = 12,01 100
 5 GLI ISOTOPI Le proprietà di un elemento non dipendono dal numero di massa, ma dal numero atomico; infatti è sufficiente il numero dei protoni a caratterizzare un atomo, in quanto esso condiziona un uguale
5 GLI ISOTOPI Le proprietà di un elemento non dipendono dal numero di massa, ma dal numero atomico; infatti è sufficiente il numero dei protoni a caratterizzare un atomo, in quanto esso condiziona un uguale
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
CONFIGURAZIONE ELETTRONICA
 CONFIGURAZIONE ELETTRONICA MODELLO DELL ATOMO DI BHOR La configurazione elettronica è la disposizione degli elettroni intorno al nucleo dell atomo, nei suoi orbitali. Gli orbitali hanno differenti forme
CONFIGURAZIONE ELETTRONICA MODELLO DELL ATOMO DI BHOR La configurazione elettronica è la disposizione degli elettroni intorno al nucleo dell atomo, nei suoi orbitali. Gli orbitali hanno differenti forme
Metalli come gas di elettroni liberi
 Metalli come gas di elettroni liberi I metalli sono caratterizzati da elevata conducibilità elettrica e termica. La conducibilità elettrica in particolare (o il suo inverso, la resistività) è una delle
Metalli come gas di elettroni liberi I metalli sono caratterizzati da elevata conducibilità elettrica e termica. La conducibilità elettrica in particolare (o il suo inverso, la resistività) è una delle
Molecole. 04/09/13 3-MOL-0.doc 0
 Molecole 04/09/13 3-MOL-0.doc 0 Legame covalente H 2 + Il potenziale cui è soggetto l elettrone ha 2 minimi equivalenti 1) H + si avvicina a H 2) Se la barriera diventa abbastanza sottile la probabilità
Molecole 04/09/13 3-MOL-0.doc 0 Legame covalente H 2 + Il potenziale cui è soggetto l elettrone ha 2 minimi equivalenti 1) H + si avvicina a H 2) Se la barriera diventa abbastanza sottile la probabilità
CONFIGURAZIONE ELETTRONICA DEGLI ELEMENTI
 CONFIGURAZIONE ELETTRONICA DEGLI ELEMENTI SOSTANZE: ELEMENTI E COMPOSTI Si definisce sostanza la materia che ha sempre la stessa composizione. Ogni campione di una sostanza ha le stesse propietà chimiche
CONFIGURAZIONE ELETTRONICA DEGLI ELEMENTI SOSTANZE: ELEMENTI E COMPOSTI Si definisce sostanza la materia che ha sempre la stessa composizione. Ogni campione di una sostanza ha le stesse propietà chimiche
Interazione Radiazione materia (intro) Sistema a due livelli e coefficienti di Einstein. Assorbimento
 Interazione Radiazione materia (intro) Sistema a due livelli e coefficienti di Einstein Emissione Spontanea b Assorbimento b Emissione Stimolata b a a a -Energia del fotone (Emesso/Assorbito) uguale alla
Interazione Radiazione materia (intro) Sistema a due livelli e coefficienti di Einstein Emissione Spontanea b Assorbimento b Emissione Stimolata b a a a -Energia del fotone (Emesso/Assorbito) uguale alla
n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]
![n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm] n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]](/thumbs/92/108343390.jpg) Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Unità 2. La teoria quantistica
 Unità 2 La teoria quantistica L'effetto fotoelettrico Nel 1902 il fisico P. Lenard studiò l'effetto fotoelettrico. Esso è l'emissione di elettroni da parte di un metallo su cui incide un'onda elettromagnetica.
Unità 2 La teoria quantistica L'effetto fotoelettrico Nel 1902 il fisico P. Lenard studiò l'effetto fotoelettrico. Esso è l'emissione di elettroni da parte di un metallo su cui incide un'onda elettromagnetica.
Le molecole ed il legame chimico
 La meccanica quantistica è in grado di determinare esattamente i livelli energetici dell atomo di idrogeno e con tecniche matematiche più complesse è anche in grado di descrivere l atomo di elio trovando
La meccanica quantistica è in grado di determinare esattamente i livelli energetici dell atomo di idrogeno e con tecniche matematiche più complesse è anche in grado di descrivere l atomo di elio trovando
Introduzione al corso. Cenni storici ed evidenze sperimentali determinanti lo sviluppo della fisica atomica come la conosciamo ora...
 Introduzione al corso Cenni storici ed evidenze sperimentali determinanti lo sviluppo della fisica atomica come la conosciamo ora... Legge di Boyle (1662)-> La pressione di un gas cresce quando decresce
Introduzione al corso Cenni storici ed evidenze sperimentali determinanti lo sviluppo della fisica atomica come la conosciamo ora... Legge di Boyle (1662)-> La pressione di un gas cresce quando decresce
Enrico Silva - diritti riservati - Non è permessa, fra l altro, l inclusione anche parziale in altre opere senza il consenso scritto dell autore
 Particelle della presente identiche. opera. Principio di Pauli. 1 Particelle identiche: sommario Finora: proprietà di particella singola. Volendo ottenere il comportamento di più particelle, è necessario
Particelle della presente identiche. opera. Principio di Pauli. 1 Particelle identiche: sommario Finora: proprietà di particella singola. Volendo ottenere il comportamento di più particelle, è necessario
Testi Consigliati. I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli. Qualsiasi altro testo che tratti gli argomenti elencati nel programma
 Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
STRUTTURA DELL'ATOMO
 STRUTTURA DELL'ATOMO IDROGENO 1 H ELIO He 1 2 4 Modello planetario di Rutherford -protoni e neutroni costituiscono il nucleo in cui è concentrata tutta la massa - gli elettroni ruotano attorno al nucleo
STRUTTURA DELL'ATOMO IDROGENO 1 H ELIO He 1 2 4 Modello planetario di Rutherford -protoni e neutroni costituiscono il nucleo in cui è concentrata tutta la massa - gli elettroni ruotano attorno al nucleo
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
Cosa succede se ad un corpo applichiamo una forza?
 LE FORZE Cosa succede se ad un corpo applichiamo una forza? Se ad un corpo applichiamo una forza, essa può: 1. mettere in moto il corpo se è fermo 2. modificare il movimento del corpo se è già in moto
LE FORZE Cosa succede se ad un corpo applichiamo una forza? Se ad un corpo applichiamo una forza, essa può: 1. mettere in moto il corpo se è fermo 2. modificare il movimento del corpo se è già in moto
Configurazione elettronica e collegamento alla tavola periodica
 Configurazione elettronica e collegamento alla tavola periodica Modelli atomici a confronto Un elettrone che si trova in un certo livello possiede l energia associata a quel livello, in particolare al
Configurazione elettronica e collegamento alla tavola periodica Modelli atomici a confronto Un elettrone che si trova in un certo livello possiede l energia associata a quel livello, in particolare al
I 4 NUMERI QUANTICI. I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali.
 I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
1. Scrivere l equazione di Schrödinger unidimensionale per una particella di massa m con energia potenziale V (x) = mω2
 1 Teoria Una particella di massa m = 1 g e carica elettrica q = 1 c viene accelerata per un tratto pari a l = m da una differenza di potenziale pari av = 0 volt Determinare la lunghezza d onda di De Broglie
1 Teoria Una particella di massa m = 1 g e carica elettrica q = 1 c viene accelerata per un tratto pari a l = m da una differenza di potenziale pari av = 0 volt Determinare la lunghezza d onda di De Broglie
Seconda parte Teorie atomiche. Configurazione elettronica. Il legame chimico. Prof. Stefano Piotto Università di Salerno
 Seconda parte Teorie atomiche. Configurazione elettronica. Il legame chimico Prof. Stefano Piotto Università di Salerno Seconda parte 1. Teoria atomica 2. Esperimenti di Thompson e Millikan 3. Modello
Seconda parte Teorie atomiche. Configurazione elettronica. Il legame chimico Prof. Stefano Piotto Università di Salerno Seconda parte 1. Teoria atomica 2. Esperimenti di Thompson e Millikan 3. Modello
Comunicazioni Docente - Studenti
 Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
Teoria atomica. Dr. Lucia Tonucci Ingegneria delle Costruzioni
 Teoria atomica Dr. Lucia Tonucci l.tonucci@unich.it Ingegneria delle Costruzioni Cenni storici V Sec. a.c. Democrito: la materia è costituita da corpuscoli indivisibili, gli atomi (atomo = indivisibile)
Teoria atomica Dr. Lucia Tonucci l.tonucci@unich.it Ingegneria delle Costruzioni Cenni storici V Sec. a.c. Democrito: la materia è costituita da corpuscoli indivisibili, gli atomi (atomo = indivisibile)
in cui le sommatorie sono fatte sugli elettroni dell atomo. Le componenti z di L e S sono date dalle somme scalari N
 Termini atomici (o termini spettroscopici) e loro determinazione a partire dalla configurazione elettronica Le configurazioni elettroniche degli atomi sono ambigue nel senso che esiste un certo numero
Termini atomici (o termini spettroscopici) e loro determinazione a partire dalla configurazione elettronica Le configurazioni elettroniche degli atomi sono ambigue nel senso che esiste un certo numero
Università degli Studi dell Aquila Corso di Laurea in Scienze e Tecnologie Chimiche e dei Materiali Corso di Fisica della Materia Prof. L.
 Università degli Studi dell Aquila Corso di Laurea in Scienze e Tecnologie Chimiche e dei Materiali Corso di Fisica della Materia Prof. L. Lozzi Testi degli esercizi svolti in aula Corpo Nero 1. Il corpo
Università degli Studi dell Aquila Corso di Laurea in Scienze e Tecnologie Chimiche e dei Materiali Corso di Fisica della Materia Prof. L. Lozzi Testi degli esercizi svolti in aula Corpo Nero 1. Il corpo
Effetti relativistici e quantistici
 Effetti relativistici e quantistici Dott. Fabiano Nart Gruppo Divulgazione Scientifica Dolomiti E. Fermi www.gdsdolomiti.org info.gdsdolomiti@gmail.com Museo Scienze Naturali Bolzano, 24/05/2016 Dott.
Effetti relativistici e quantistici Dott. Fabiano Nart Gruppo Divulgazione Scientifica Dolomiti E. Fermi www.gdsdolomiti.org info.gdsdolomiti@gmail.com Museo Scienze Naturali Bolzano, 24/05/2016 Dott.
ESERCIZI W X Y Z. Numero di massa Neutroni nel nucleo Soluzione
 ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI
 LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
Modelli atomici. Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle.
 Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
Corso di CHIMICA LEZIONE 1
 Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi
 Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi Gli elementi sono ordinati secondo numero atomico Z ( numero dei protoni ) crescente Il numero
Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi Gli elementi sono ordinati secondo numero atomico Z ( numero dei protoni ) crescente Il numero
LA STRUTTURA DELLA MATERIA
 LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
Il principio di indeterminazione di Heisenberg
 Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton)
 Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
