Soluzione tamponata contenente perossido di idrogeno, detergente e sodio azide 0,015 mol/l.
|
|
|
- Aureliano Martinelli
- 4 anni fa
- Visualizzazioni
Transcript
1 PD-L1 IHC 22C3 pharmdx SK test per l'utilizzo con Autostainer Link 48 Uso previsto Per uso diagnostico in vitro. PD-L1 IHC 22C3 pharmdx è un saggio immunoistochimico qualitativo che utilizza Monoclonal Mouse Anti-PD-L1, Clone 22C3, destinato all'uso nella rilevazione della proteina PD-L1 in tessuto di cancro del polmone non a piccole cellule (NSCLC) fissato in formalina, incluso in paraffina (FFPE), con il sistema di visualizzazione EnVision FLEX su Autostainer Link 48. L'espressione della proteina PD-L1 viene determinata utilizzando il punteggio TPS (Tumor Proportion Score), che rappresenta la percentuale di cellule tumorali vitali che mostrano una colorazione di membrana parziale o totale a qualunque intensità. PD-L1 IHC 22C3 pharmdx è indicato come ausilio nell'identificazione di pazienti affetti da NSCLC idonei al trattamento con KEYTRUDA (pembrolizumab). Vedere l'etichetta del prodotto KEYTRUDA per i valori di cut-off dell'espressione che determinano la terapia in condizioni cliniche specifiche. Riepilogo e spiegazione Il legame dei ligandi di PD-1, PD-L1 e PD-L2, al recettore PD-1, localizzato sulle cellule T, inibisce la proliferazione delle cellule T e la produzione di citochine. In alcuni tumori si verifica una sovraregolazione dei ligandi di PD-1 e la relativa via di trasduzione del segnale può contribuire a inibire la sorveglianza immunitaria delle cellule T attive dei tumori. KEYTRUDA è un anticorpo monoclonale umanizzato che si lega al recettore PD-1 e ne blocca l'interazione con PD-L1 e PD-L2, rilasciando l'inibizione della risposta immunitaria mediata dalla via di trasduzione del segnale di PD-1, inclusa la risposta immunitaria anti-tumorale. In modelli tumorali murini singenici, il blocco dell'attività di PD-1 ha portato a una riduzione della crescita tumorale (1). Principio della procedura PD-L1 IHC 22C3 pharmdx include il protocollo e i reagenti ottimizzati necessari per l'esecuzione di una procedura di colorazione IHC di campioni FFPE con Autostainer Link 48. Una volta eseguita l'incubazione con l'anticorpo monoclonale primario anti-pd-l1 o con il reagente di controllo negativo Negative Control Reagent (NCR), i campioni vengono incubati con un anticorpo Linker specifico per la specie ospite dell'anticorpo primario, quindi vengono incubati con un reagente di visualizzazione pronto per l'uso che consiste di molecole di anticorpo secondario e molecole di perossidasi di rafano legate a uno scheletro di polimeri di destrano. La conversione enzimatica del cromogeno aggiunto successivamente causa la precipitazione di un prodotto di reazione visibile nel sito dell'antigene. Il colore della reazione cromogena viene modificato da un reagente di potenziamento del cromogeno. Il campione può quindi essere sottoposto a colorazione di contrasto e coperto con un vetrino coprioggetto. L'interpretazione dei risultati avviene per mezzo di un microscopio ottico. Materiali forniti Ogni kit contiene 19,5 ml di anticorpo primario contro PD-L1 (concentrazione proteica pari a circa 3 µg/ml) e include i reagenti necessari per effettuare 50 test in un massimo di 15 cicli di colorazione singoli. I materiali elencati di seguito sono sufficienti per 50 test (50 vetrini incubati con Primary Antibody contro PD-L1 e 50 vetrini incubati con corrispondente Negative Control Reagent; 100 vetrini in totale). Il numero dei test è basato sull'uso di 2 x 150 µl per vetrino di ciascun reagente ad eccezione di DAB+ e Target Retrieval Solution. Il kit fornisce materiale sufficiente per un massimo di 15 cicli di colorazione singoli. Quantità Descrizione 1 x 34,5 ml Peroxidase-Blocking Reagent PEROXIDASE-BLOCKING REAGENT Soluzione tamponata contenente perossido di idrogeno, detergente e sodio azide 0,015 mol/l. 1 x 19,5 ml Primary Antibody: Monoclonal Mouse Anti-PD-L1, Clone 22C3 MONOCLONAL MOUSE ANTI-PD-L1 CLONE 22C3 Anti-PD-L1 monoclonale murino (IgG 1 ) in soluzione tamponata, contenente proteina stabilizzante e sodio azide 0,015 mol/l. 1 x 15 ml Reagente di controllo negativo NEGATIVE CONTROL REAGENT Anticorpo monoclonale IgG murino di controllo in soluzione tamponata contenente proteina stabilizzante e sodio azide 0,015 mol/l. P03928IT_04/SK / p. 1/17
2 1 x 34,5 ml Mouse LINKER LINKER, ANTI-MOUSE Anticorpo secondario di coniglio diretto contro immunoglobuline murine in soluzione tamponata contenente proteina stabilizzante e sodio azide 0,015 mol/l. 1 x 34,5 ml Visualization Reagent-HRP VISUALIZATION REAGENT-HRP Destrano legato a molecole di perossidasi e molecole di anticorpi secondari di capra diretti contro immunoglobuline di coniglio e di topo in soluzione tamponata contenente proteina stabilizzante e un agente antimicrobico. 15 x 7,2 ml DAB+ Substrate Buffer DAB+ SUBSTRATE BUFFER Soluzione tamponata, contenente perossido di idrogeno e un agente antimicrobico. 1 x 5 ml DAB+ Chromogen DAB+ CHROMOGEN 3,3 -diaminobenzidina tetraidrocloruro in solvente organico. 1 x 34,5 ml DAB Enhancer DAB ENHANCER Solfato rameico in acqua. 6 x 30 ml EnVision FLEX Target Retrieval Solution, Low ph (50x) EnVision FLEX TARGET RETRIEVAL SOLUTION LOW ph (50X) Soluzione tamponata, ph 6,1, contenente detergente e un agente microbico. 15 vetrini PD-L1 IHC 22C3 pharmdx Control Slides CONTROL SLIDES Ciascun vetrino contiene sezioni di due linee cellulari in pellet fissate in formalina e incluse in paraffina: NCI-H226* moderatamente positive per l'espressione della proteina PD-L1 e MCF-7 negative per l'espressione della proteina PD-L1. PD-L1 IHC 22C3 pharmdx XXXXX MCF-7: negative per PD-L1 NCI-H226: positive per PD-L1 *Si ringraziano il Dr. AF Gazdar e il Dr. JD Minna dell'nih per il loro contributo nello sviluppo della linea NCI-H226 (numero ATCC: CRL-5826 ) (2). Nota: tutti i reagenti inclusi sono formulati in modo specifico per l'utilizzo con questo kit. Per eseguire il test secondo quanto specificato, non è consentito effettuare sostituzioni, ad eccezione di EnVision FLEX Target Retrieval Solution, Low ph (50x) (codice K8005). PD-L1 IHC 22C3 pharmdx è stato formulato appositamente per l'uso con Autostainer Link 48. Per ulteriori informazioni, fare riferimento ai manuali utente di Autostainer Link 48 e PT Link. Materiali necessari ma non forniti PT Link Pre-treatment Module (codice PT100/PT101/PT200) Autostainer Link 48 (codice AS480) EnVision FLEX Wash Buffer (20x) (codice K8007) Hematoxylin (codice K8008) Acqua distillata o deionizzata (acqua di grado reagente) Timer Tessuti positivi e negativi da utilizzare come controlli della procedura (vedere la sezione Controllo di qualità) Vetrini per microscopia: Dako FLEX IHC Microscope Slides (codice K8020) o vetrini caricati Fisherbrand Superfrost Plus Vetrini coprioggetto Mezzo di montaggio permanente e reagenti ausiliari richiesti per il montaggio dei vetrini coprioggetto Microscopio ottico (ingrandimento obiettivi 4x 40x) Precauzioni P03928IT_04/SK / p. 2/17
3 1. Per uso diagnostico in vitro. 2. Per uso professionale. 3. Questo prodotto contiene sodio azide (NaN3), una sostanza chimica altamente tossica in forma pura. Sebbene non sia classificato come prodotto a rischio, il composto NaN3 alle concentrazioni indicate può reagire con il rame e il piombo delle tubature formando azidi metalliche fortemente esplosive. Durante lo smaltimento del prodotto, far scorrere abbondante acqua nelle tubature per impedire la formazione di azidi metalliche (3). 4. I reagenti Primary Antibody, Negative Control Reagent, Linker e Visualization Reagent contengono materiale di origine animale. 5. I campioni, prima e dopo la fissazione, e tutti i materiali esposti ad essi devono essere manipolati come potenziali vettori di infezione e smaltiti con le opportune precauzioni (4). 6. Tempi, temperature o metodi di incubazione diversi da quelli specificati possono generare risultati erronei. 7. I reagenti sono stati diluiti nel modo ottimale. L'ulteriore diluizione potrebbe compromettere la colorazione dell'antigene. 8. I reagenti Visualization Reagent, DAB+ Chromogen liquido e la soluzione substrato-cromogeno DAB+ preparata possono subire alterazioni se esposti a livelli di luce eccessivi. Non conservare questi componenti del sistema né eseguire la colorazione in condizioni di luce intensa, come ad esempio la luce solare diretta. 9. Residui di paraffina possono produrre risultati falsi negativi. 10. L'uso di volumi dei reagenti diversi da quelli consigliati può comportare la perdita di immunoreattività di PD-L1 visibile. 11. I risultati di un piccolo studio hanno mostrato un intervallo dinamico simile di espressione di PD-L1 in coppie di campioni di NSCLC primario e metastatico. È possibile che vi siano delle differenze nell'espressione di PD-L1 nei tumori primari rispetto alle sedi metastatiche dello stesso paziente. 12. Sezioni di tessuto di grandi dimensioni possono richiedere 3x150 µl di reagente. 13. Come regola generale, ai minori di 18 anni non è consentito lavorare con questo prodotto. È necessario preparare con attenzione gli utenti sulle corrette procedure di lavoro, le proprietà rischiose del prodotto e le norme di sicurezza necessarie. Fare riferimento alla scheda di sicurezza (SDS) per ulteriori informazioni. 14. Indossare dispositivi di protezione individuale appropriati per evitare il contatto con gli occhi e la cute. 15. La soluzione non utilizzata deve essere smaltita in conformità alle normative locali e nazionali vigenti in materia. 16. Su richiesta è disponibile una scheda di sicurezza per utenti professionisti. Pericolo DAB+ Chromogen: 1-5% di tetracloruro di bifenil-3,3',4,4'-tetrailtetraammonio H350 Può provocare il cancro. H341 Sospettato di provocare alterazioni genetiche. P201 Procurarsi istruzioni specifiche prima dell uso. P202 Non manipolare prima di avere letto e compreso tutte le avvertenze. P280 Indossare guanti protettivi. Proteggere gli occhi/il viso. Indossare indumenti protettivi. P308 + P313 IN CASO di esposizione o di possibile esposizione: consultare un medico. P405 Conservare sotto chiave. P501 Smaltire il prodotto e il recipiente in conformità a tutte le normative locali, regionali, nazionali e internazionali. Avvertenza EnVision FLEX Target Retrieval Solution, Low ph (50x): 1-5% di acido citrico H319 Provoca grave irritazione agli occhi. H411 Tossico per gli organismi acquatici con effetti di lunga durata. P280 Proteggere gli occhi/il viso. P273 Non disperdere nell'ambiente. P264 Lavare accuratamente le mani dopo l'uso. P305 + P351 + P338 IN CASO DI CONTATTO CON GLI OCCHI: sciacquare accuratamente per parecchi minuti. Togliere le eventuali lenti a contatto se è agevole farlo. Continuare a sciacquare. P337 + P313 Se l'irritazione degli occhi persiste: consultare un medico. P501 Smaltire il prodotto e il recipiente in conformità a tutte le normative locali, regionali, nazionali e internazionali. Conservazione Conservare tutti i componenti di PD-L1 IHC 22C3 pharmdx, inclusi i vetrini di controllo Control Slides, al buio a 2-8 C quando non in uso su Autostainer Link 48. Non utilizzare il kit dopo la data di scadenza stampata sull'esterno della confezione. Qualora i reagenti venissero conservati diversamente da quanto specificato nel presente foglietto informativo, le condizioni dovranno essere convalidate dall'utente. Non è possibile indicare segni evidenti di instabilità del prodotto, pertanto, è necessario analizzare gli opportuni controlli positivi e negativi contemporaneamente ai campioni dei pazienti. Preparazione dei campioni I campioni devono essere manipolati in modo tale da preservare il tessuto per la colorazione IHC. Utilizzare per tutti i campioni i metodi standard di processazione dei tessuti. Sezioni incluse in paraffina Tessuti fissati in formalina e inclusi in paraffina sono idonei all'uso. L'uso di altri fissativi non è stato convalidato e può produrre risultati erronei. Si raccomanda un tempo di fissazione di ore in formalina neutra tamponata al 10%, tuttavia, uno studio con un numero limitato di campioni ha mostrato che un tempo di fissazione compreso tra 4 e 168 ore in NBF 10% non ha alterato in modo sistematico la rilevazione di PD-L1. Un tempo di fissazione 3 ore può determinare una variabilità nella rilevazione di PD-L1. I campioni devono essere suddivisi in blocchi dello spessore di 3 o 4 mm, fissati in formalina, deidratati e chiarificati in una serie di alcoli e xilene, quindi infiltrati con paraffina fusa. La temperatura della paraffina non deve superare i 60 C. I blocchi di tessuto FFPE preparati almeno 5 anni prima possono determinare una perdita di immunoreattività di PD-L1. P03928IT_04/SK / p. 3/17
4 I campioni tissutali devono essere tagliati in sezioni di 4-5 µm. Dopo il sezionamento, i tessuti devono essere montati su vetrini Dako FLEX IHC Microscope Slides (codice K8020) o Fisherbrand Superfrost Plus e quindi incubati in forno a 58 ± 2 C per 1 ora. Per preservare l'antigenicità, una volta montate sui vetrini, le sezioni tissutali devono essere conservate al buio a 2-8 C (preferibilmente) o a una temperatura ambiente massima di 25 C, quindi sottoposti a colorazione entro 6 mesi dal sezionamento. La temperatura di conservazione e di manipolazione dei vetrini in ogni fase posteriore alla preparazione non dovrà superare i 25 C per assicurare l'integrità e l'antigenicità dei tessuti. L'uso di PD-L1 IHC 22C3 pharmdx su tessuti decalcificati non è stato convalidato e non è consigliato. Preparazione dei reagenti Prima della colorazione, è necessario preparare i reagenti indicati di seguito: EnVision FLEX Target Retrieval Solution, Low ph (50x) Preparare una quantità sufficiente di Target Retrieval Solution, Low ph, 1x, diluendo la soluzione Target Retrieval Solution, Low ph, 50x 1:50 con acqua distillata o deionizzata (acqua di grado reagente). Il ph della soluzione Target Retrieval Solution 1x deve essere 6,1 ± 0,2. Un ph della Target Retrieval Solution 1x inferiore a 5,9 può determinare la produzione di risultati errati. Con una bottiglia da 30 ml di Target Retrieval Solution, Low ph (50x), diluita 1:50 si ottengono 1,5 l di reagente 1x, quantità sufficiente per il riempimento di una tanica di PT Link, che consente di trattare fino a 24 vetrini per utilizzo. Eliminare la soluzione Target Retrieval Solution 1x dopo tre utilizzi e dopo non più di 5 giorni dalla diluizione. Se necessario, sono disponibili quantità aggiuntive di EnVision FLEX Target Retrieval Solution, Low ph (50x), con codice K8005. EnVision FLEX Wash Buffer (20x) Preparare una quantità sufficiente di tampone di lavaggio diluendo Wash Buffer 20x 1:20 con acqua distillata o deionizzata (acqua di grado reagente) per le fasi di lavaggio. Conservare la soluzione 1x inutilizzata a 2-8ºC per un periodo massimo di un mese. Eliminare il tampone se appare torbido. Per ulteriori informazioni, fare riferimento al manuale utente del sistema Autostainer Link 48 in uso. EnVision FLEX Wash Buffer (20x) è disponibile con il codice K8007. Soluzione substrato-cromogeno DAB+ Questa soluzione deve essere accuratamente miscelata prima dell'uso. La formazione di precipitati nella soluzione non influisce sulla qualità della colorazione. Per preparare la soluzione substrato-cromogeno DAB+, aggiungere 1 goccia di DAB+ Chromogen liquido per ml di DAB+ Substrate Buffer e miscelare. La soluzione substrato-cromogeno è stabile per 5 giorni se conservata al buio a 2-8 C. Note importanti: Se si utilizza una bottiglia di DAB+ Substrate Buffer intera, aggiungere 9 gocce di DAB+ Chromogen. Sebbene sull'etichetta sia riportata la dicitura 7,2 ml, questa indica il volume utilizzabile e non tiene in considerazione il "volume morto" nella bottiglia. Il colore di DAB+ Chromogen liquido nella bottiglia può variare da trasparente a color lavanda-marrone. Ciò non influisce sulle prestazioni del prodotto. Diluire secondo le linee guida fornite in precedenza. L'aggiunta di un eccesso di DAB+ Chromogen liquido a DAB+ Substrate Buffer causa una riduzione del segnale positivo. Procedura di colorazione sul sistema Autostainer Link 48 Note sulla procedura Prima dell'uso, l'utente deve leggere attentamente le seguenti istruzioni e acquisire dimestichezza con tutti i componenti e lo strumento (vedere la sezione "Precauzioni"). Prima di procedere all'immunocolorazione, tutti i reagenti devono essere equilibrati a temperatura ambiente (20-25 C). Analogamente, tutte le fasi di incubazione devono essere eseguite a temperatura ambiente. Non consentire l'essiccazione delle sezioni tissutali durante la procedura di colorazione. Sezioni tissutali asciutte possono mostrare livelli di colorazione aspecifica superiori. Tutte le fasi e i tempi di incubazione richiesti per la colorazione sono preimpostati nel software Dako Link. Per ulteriori informazioni sulla programmazione dei protocolli e sul caricamento di vetrini e reagenti, fare riferimento ai manuali utente di Autostainer Link 48 e PT Link. Nota: i reagenti e le istruzioni forniti in questo sistema sono stati progettati per l'ottenimento di prestazioni ottimali quando utilizzati con i reagenti e i materiali consigliati. L'ulteriore diluizione dei reagenti o l'uso di tempi o temperature di incubazione diversi da quelli indicati possono produrre risultati erronei o discordanti. Protocollo di colorazione Selezionare il protocollo di colorazione PD-L1 IHC 22C3 pharmdx dalle opzioni del menu a discesa Dako Link. Tutte le fasi e i tempi di incubazione richiesti per la colorazione sono preimpostati nell'autostainer Link 48. Se i protocolli PD-L1 IHC 22C3 pharmdx appropriati non sono disponibili nel server in uso, contattare il rappresentante dell'assistenza tecnica locale per richiederli. Fase 1: Procedura di deparaffinazione, reidratazione e smascheramento antigenico (3-in-1) Per i dettagli, vedere la Guida Utente PT Link. Impostare PT Link (codice PT100/PT101/PT200) con il preriscaldamento e il raffreddamento a 65 C. Impostare il riscaldamento a 97 C per 20 minuti. Riempire le taniche di PT Link con 1,5 L di soluzione di lavoro Target Retrieval Solution, Low ph, 1x, per tanica, per coprire le sezioni di tessuto. Preriscaldare la soluzione Target Retrieval Solution a 65 C. P03928IT_04/SK / p. 4/17
5 Immergere i rack Autostainer contenenti sezioni tissutali FFPE montate nella soluzione Target Retrieval Solution, Low ph, (soluzione di lavoro 1x) preriscaldata, all'interno della tanica di PT Link. Incubare per 20 minuti a 97 C. Una volta completata l'incubazione per lo smascheramento antigenico e portata la temperatura a 65 C, rimuovere ciascun rack dei vetrini Autostainer dalla tanica di PT Link e collocarlo immediatamente in una vaschetta apposita (ad esempio, PT Link Rinse Station, codice PT109) contenente tampone di lavaggio (codice K8007) diluito e a temperatura ambiente. Incubare i vetrini immersi in Wash Buffer diluito e a temperatura ambiente per 5 minuti. Fase 2: Procedura di colorazione Dopo la procedura di deparaffinazione, reidratazione e smascheramento antigenico (3-in-1), i rack Autostainer con i vetrini vengono posizionati in Autostainer Link 48. Lo strumento eseguirà la procedura di colorazione applicando il reagente appropriato, monitorando il tempo di incubazione ed effettuando il lavaggio dei vetrini tra le applicazioni dei reagenti. I tempi di incubazione dei reagenti sono preimpostati nel software Dako Link. Fase 3: Colorazione di contrasto I vetrini devono essere sottoposti a colorazione di contrasto per 5 minuti con Hematoxylin (Link) (codice K8008). Il tempo di incubazione con Hematoxylin è preimpostato nel protocollo. Fase 4: Montaggio È richiesto un mezzo di montaggio permanente e non acquoso. Nota: potrebbe verificarsi una perdita di intensità della colorazione dei vetrini associata a diversi fattori che includono, a titolo esemplificativo ma non limitativo, la colorazione di contrasto, metodi e materiali di montaggio e le condizioni di conservazione. Per ridurre al minimo la perdita di intensità della colorazione, conservare i vetrini al buio a temperatura ambiente (20-25 C). Controllo di qualità I reagenti in PD-L1 IHC 22C3 pharmdx sono stati sottoposti a controllo di qualità tramite immunoistochimica utilizzando le procedure di smascheramento antigenico e colorazione descritte in precedenza. Eventuali variazioni apportate alle procedure consigliate per la fissazione, la processazione e l'inclusione dei tessuti nel laboratorio dell'utente possono produrre una significativa variabilità nei risultati. I controlli di qualità devono essere inclusi in ogni ciclo di colorazione. Tali controlli di qualità sono indicati nella tabella 1 e includono un campione tissutale del paziente con colorazione H&E, tessuti di controllo positivo e negativo forniti dal laboratorio e un vetrino Control Cell Line Slide fornito da Dako (5). Negli Stati Uniti, consultare le linee guida per il controllo della qualità dell'accreditation Program for Immunohistochemistry del College of American Pathologists (CAP); per ulteriori informazioni, fare riferimento anche al documento del CLSI Quality Assurance for Immunocytochemistry, Approved Guideline (5, 6, 7). Verifica del saggio Prima del primo utilizzo di un sistema di colorazione in una procedura diagnostica, l'utente deve verificare le prestazioni del saggio su una serie di tessuti forniti dal laboratorio con prestazioni IHC note e che rappresentino tessuti con positività e negatività note. Consultare le procedure di controllo di qualità descritte nella rispettiva sezione sopra riportata. Tali procedure di controllo della qualità devono essere ripetute per ogni nuovo lotto di anticorpo o ogniqualvolta venga apportata una modifica ai parametri del saggio. Opzioni per la risoluzione di potenziali problemi, relative cause e interventi correttivi consigliati sono descritti nella tabella 12. Interpretazione del punteggio - NSCLC Tutte le cellule tumorali vitali sull'intero vetrino devono essere valutate e incluse nell'assegnazione del punteggio per PD-L1. Sul vetrino colorato per PD-L1 devono essere presenti un minimo di 100 cellule vitali perché il campione si possa considerare valido per la valutazione di PD-L1. Per assegnare correttamente un punteggio ai campioni colorati con PD-L1 IHC 22C3 pharmdx, è essenziale che siano valutate le cellule corrette, che sia identificata la giusta localizzazione cellulare e che l'intensità della colorazione sia interpretata in modo appropriato. La valutazione dei vetrini deve essere eseguita da un patologo per mezzo di un microscopio ottico. Per la valutazione della colorazione immunoistochimica e del punteggio, è consigliato l'impiego di un obiettivo con ingrandimento di 10-40x. Deve essere inclusa nel punteggio ogni colorazione percepibile delle membrane di cellule tumorali. Attribuire un punteggio alla colorazione parziale o completa della membrana cellulare ( 1+) percepita come distinta dalla colorazione citoplasmatica. La colorazione citoplasmatica deve essere considerata aspecifica ed è esclusa dalla valutazione dell'intensità della colorazione. Le cellule normali e le cellule immunitarie associate al tumore, quali i linfociti o i macrofagi infiltranti, non devono essere inclusi nel punteggio per la determinazione della positività di PD-L1. I campioni di tumore colorati con NCR devono mostrare colorazione specifica 0 e una colorazione di fondo 1+. Il punteggio TPS (Tumor Proportion Score) rappresenta la percentuale di cellule tumorali vitali che mostrano una colorazione di membrana parziale o totale ( 1+). Il campione deve essere considerato con espressione di PD-L1 se per un punteggio TPS delle cellule tumorali vitali 1% mostra una colorazione della membrana, di qualunque intensità. Il campione deve essere considerato con espressione di PD-L1 elevata se per un punteggio TPS delle cellule tumorali vitali 50% mostra una colorazione della membrana, di qualunque intensità. Per ogni ciclo di colorazione, i vetrini devono essere esaminati nell'ordine indicato nella tabella 1 per determinare la validità del ciclo di colorazione e per consentire la valutazione della colorazione del tessuto del campione. Per ulteriori indicazioni, fare riferimento al documento PD-L1 IHC 22C3 pharmdx Interpretation Manual (Manuale per l'interpretazione di PD-L1 IHC 22C3 pharmdx). Ulteriori raccomandazioni per l'interpretazione della colorazione con PD-L1 IHC 22C3 pharmdx 1. Per verificare la colorazione della membrana cellulare, utilizzare un obiettivo con ingrandimento 10-40x. 2. Vari elementi che non costituiscono un target, come cellule immunitarie associate al tumore (ad es. macrofagi) e stroma, possono altresì colorarsi positivamente per PD-L1, tuttavia non devono essere inclusi nel punteggio. P03928IT_04/SK / p. 5/17
6 Tabella 1. Ordine consigliato per la valutazione dei vetrini Campioni Principio Requisiti 1. H&E (componente fornito dal laboratorio) Una colorazione con ematossilina ed eosina (H&E) del campione tissutale viene analizzata per prima per valutare l'istologia e il livello di preservazione del tessuto. La colorazione con PD-L1 IHC 22C3 pharmdx e quella H&E devono essere eseguite su sezioni seriali provenienti dallo stesso blocco in paraffina del campione. I campioni tissutali devono essere integri, con un buon livello di preservazione e devono confermare l'indicazione del tumore. 2. Vetrino Control Cell Line Slide (componente fornito da Dako) Il vetrino Control Cell Line Slide sottoposto a colorazione con l'anticorpo primario contro PD-L1 di PD-L1 IHC 22C3 pharmdx deve essere esaminato per confermare il corretto funzionamento di tutti i reagenti. Il vetrino Control Cell Line Slide contiene il pellet di una linea cellulare positiva per PD-L1 e il pellet di una linea cellulare negativa per PD-L1. Un vetrino Control Cell Line Slide deve essere sottoposto a colorazione con Primary Antibody contro PD-L1 in ogni ciclo di colorazione. Criteri di accettazione per NCI-H226 (linea cellulare di controllo positiva per PD-L1): Colorazione della membrana cellulare di una percentuale di cellule 70%, con un'intensità della colorazione media 2+. Colorazione aspecifica con intensità < 1+. Criteri di accettazione per MCF-7 (linea cellulare di controllo negativa per PD-L1): Nessuna colorazione specifica. Colorazione aspecifica con intensità < 1+. Tenere presente che nel pellet cellulare MCF-7 occasionalmente è possibile osservare la colorazione di alcune cellule. Si applicano i seguenti criteri di accettazione: la presenza di un totale di cellule con colorazione caratteristica della membrana plasmatica 10 o una colorazione citoplasmatica con intensità 1+ entro i bordi del pellet cellulare MCF-7 è considerata accettabile. 3. Vetrini con tessuto di controllo positivo (componente fornito dal laboratorio) 4. Vetrini con tessuto di controllo negativo (componente fornito dal laboratorio) Successivamente devono essere esaminati i vetrini con tessuto di controllo positivo sottoposti a colorazione sia con l'anticorpo primario anti-pd-l1 sia con Negative Control Reagent. Questi vetrini consentono di verificare che il metodo di fissazione e il processo di smascheramento antigenico siano efficaci. I controlli basati su tessuti positivi noti devono essere utilizzati solo per il monitoraggio della correttezza delle prestazioni dei tessuti sottoposti alla procedura e dei reagenti di test e NON come ausilio nella formulazione di una diagnosi specifica dei campioni del paziente. Successivamente devono essere esaminati i vetrini con tessuto di controllo negativo (con negatività per PD-L1 nota) sottoposti a colorazione sia con l'anticorpo primario anti-pd-l1 sia con Negative Control Reagent, per verificare la specificità della marcatura dell'antigene bersaglio con l'anticorpo primario. In alternativa, è possibile usare porzioni di tessuto di controllo positivo come tessuto di controllo negativo, tuttavia ciò deve essere verificato dall'utente. Se una delle linee cellulari di controllo non soddisfa tali criteri, tutti i risultati relativi ai campioni del paziente devono essere considerati non validi. I controlli devono essere campioni bioptici/chirurgici della stessa indicazione tumorale del campione del paziente, fissati, sottoposti a processazione e inclusi prima possibile con le stesse modalità adottate per i campioni del paziente. Per l'interpretazione dei risultati della colorazione, utilizzare campioni integri poiché cellule necrotiche o deteriorate spesso presentano colorazioni aspecifiche. I tessuti selezionati per l'uso come controlli positivi devono presentare una colorazione positiva da debole a moderata quando sottoposti a colorazione con PD-L1, per consentire la rilevazione di variazioni anche lievi nella sensibilità del saggio. Due vetrini con tessuto di controllo positivo devono essere inclusi in ogni ciclo di colorazione. Vetrino sottoposto a colorazione con PD-L1: si deve riscontrare la presenza di colorazione marrone della membrana plasmatica. La colorazione aspecifica deve essere 1+. Vetrini sottoposti a colorazione con Negative Control Reagent: nessuna colorazione della membrana. La colorazione aspecifica deve essere 1+. Se i controlli con tessuto di controllo positivo non presentano la colorazione positiva appropriata, i risultati relativi ai campioni di test devono essere considerati non validi. I controlli devono essere campioni bioptici/chirurgici della stessa indicazione tumorale del campione del paziente, fissati, sottoposti a processazione e inclusi prima possibile con le stesse modalità adottate per i campioni del paziente. Due vetrini con tessuto di controllo negativo devono essere inclusi in ogni ciclo di colorazione. Vetrino sottoposto a colorazione con PD-L1: nessuna colorazione della membrana nelle cellule tumorali. La colorazione aspecifica deve essere 1+. Vetrini sottoposti a colorazione con Negative Control Reagent: nessuna colorazione della membrana. La colorazione aspecifica deve essere 1+. Se si osserva una colorazione specifica della membrana cellulare nei vetrini con tessuto di controllo negativo, i risultati relativi ai campioni del paziente devono essere considerati non validi. P03928IT_04/SK / p. 6/17
7 5. Tessuto di controllo tonsillare (facoltativo) (componente fornito dal laboratorio) 6. Vetrino del tessuto del paziente sottoposto a colorazione con Negative Control Reagent 7. Vetrino del tessuto del paziente sottoposto a colorazione con l'anticorpo primario anti-pd- L1 Utilizzare tessuto tonsillare umano sottoposto a fissazione, processazione e inclusione in modo analogo ai campioni del paziente, come materiale di controllo aggiuntivo per verificare la sensibilità, la specificità e la colorazione aspecifica di fondo del saggio. Esaminare i campioni del paziente sottoposti a colorazione con il reagente Negative Control Reagent di PD-L1 IHC 22C3 pharmdx. Questo reagente viene utilizzato al posto dell'anticorpo primario e fornisce un ausilio nell'interpretazione della colorazione specifica nel sito dell'antigene. Infine, esaminare l'intero vetrino dei campioni del paziente sottoposto a colorazione con l'anticorpo primario anti-pd-l1 di PD-L1 IHC 22C3 pharmdx. Per informazioni specifiche sull'immunoreattività di PD-L1 IHC 22C3 pharmdx, fare riferimento alle sezioni Cenni introduttivi, Limiti e Caratteristiche di prestazione. Si dovrebbe rilevare una colorazione fortemente positiva in alcune porzioni dell'epitelio criptico e una colorazione da debole a moderata dei macrofagi follicolari nei centri germinativi. Si dovrebbe osservare una colorazione negativa nell'endotelio, nei fibroblasti e nell'epitelio superficiale. L'assenza della colorazione della membrana cellulare consente di verificare la marcatura specifica dell'antigene bersaglio con l'anticorpo primario. La colorazione aspecifica deve essere 1+. L'intensità della colorazione positiva deve essere valutata nel contesto della colorazione aspecifica di fondo osservata sul vetrino del paziente trattato con Negative Control Reagent nello stesso ciclo. Come per ogni test immunoistochimico, un risultato negativo indica che l'antigene non è stato rilevato ma non necessariamente che l'antigene era assente nelle cellule/tessuti analizzati. Tutte le cellule tumorali vitali sull'intero vetrino del paziente sottoposto alla colorazione di PD-L1 devono essere valutate e incluse nell'assegnazione del punteggio per PD-L1. Nel campione devono essere presenti un minimo di 100 cellule vitali perché questo si possa considerare valido per la valutazione di PD-L1. Limiti generali 1. L'immunoistochimica è una tecnica diagnostica multifase che richiede una formazione specifica per quanto riguarda la selezione dei reagenti appropriati, la scelta dei tessuti, la fissazione, la processazione e la preparazione dei vetrini per immunoistochimica nonché l'interpretazione dei risultati della colorazione. 2. La colorazione dei tessuti è correlata alle modalità di manipolazione e processazione del tessuto precedenti alla colorazione. Procedure errate di fissazione, congelamento, scongelamento, lavaggio, asciugatura, riscaldamento e sezionamento oppure la contaminazione con altri tessuti o liquidi possono produrre artefatti, intrappolare l'anticorpo o generare risultati falsi negativi. Risultati incoerenti possono essere dovuti anche a variazioni nei metodi di fissazione e di inclusione o da irregolarità intrinseche del tessuto. 3. Una colorazione di contrasto eccessiva o incompleta può compromettere la correttezza dell'interpretazione dei risultati. 4. L'interpretazione clinica di qualsiasi colorazione positiva o della sua assenza deve essere effettuata tenendo in considerazione la presentazione clinica, la morfologia e altri criteri istopatologici. L'interpretazione clinica di una colorazione o della sua assenza deve essere integrata da studi morfologici e da controlli adeguati, nonché da altri test diagnostici. La colorazione deve essere interpretata da un patologo qualificato con un'approfondita conoscenza degli anticorpi, dei reagenti e dei metodi impiegati. La colorazione deve essere eseguita in un laboratorio autorizzato certificato, sotto la supervisione di un patologo, il quale esaminerà i vetrini colorati e garantirà l'adeguatezza dei controlli positivi e negativi. 5. I tessuti delle persone infette dal virus dell'epatite B e contenenti l'antigene di superficie dell'epatite B (HBsAg) potrebbero evidenziare una colorazione aspecifica con perossidasi di rafano (7). 6. I reagenti possono provocare reazioni impreviste in tipi di tessuto che non sono mai stati analizzati prima. Non si può escludere completamente la possibilità di reazioni impreviste anche in tipi di tessuto già analizzati in precedenza, a causa della variabilità biologica dell'espressione antigenica nelle neoplasie o in altri tessuti patologici. Si invita a documentare le reazioni impreviste e a comunicarle all'assistenza tecnica Dako. 7. È possibile che vengano generati risultati falsi positivi a causa del legame non immunologico di proteine o prodotti di reazione con il substrato. Risultati falsi positivi possono essere causati anche dall'attività della pseudoperossidasi (eritrociti) e dall'attività della perossidasi endogena (citocromo C) (7). 8. I reagenti e le istruzioni forniti in questo sistema sono stati concepiti per l'ottenimento di prestazioni ottimali. L'ulteriore diluizione dei reagenti o l'uso di tempi o temperature di incubazione diversi da quelli indicati possono produrre risultati erronei o discordanti. Limitazioni specifiche del prodotto 1. Il deterioramento dell'antigene nel tessuto, nel tempo, può provocare risultati falsi-negativi. I campioni devono essere sottoposti a colorazione entro sei mesi dal montaggio dei tessuti sui vetrini, quando conservati al buio a 2-8 C (preferibilmente) o a una temperatura ambiente massima di 25 C. 2. Per garantire risultati ottimali e riproducibili, la proteina PD-L1 richiede un pretrattamento di smascheramento antigenico quando i tessuti sono fissati come di routine (in formalina tamponata neutra) e inclusi in paraffina. 3. Non sostituire i reagenti con reagenti con numeri di lotto diversi di questo prodotto o di kit di altri produttori. L'unica eccezione è rappresentata da EnVision FLEX Target Retrieval Solution, Low ph (50x) che, se necessario, è disponibile con il codice K Le linee cellulari di controllo sottoposte a colorazione devono essere utilizzate esclusivamente per la convalida del ciclo di colorazione e non devono essere utilizzate per l'assegnazione del punteggio alla reazione di colorazione nelle sezioni tissutali. 5. L'uso di PD-L1 IHC 22C3 pharmdx su tessuti trattati con fissativi diversi dalla formalina non è stato convalidato. 6. L'uso di PD-L1 IHC 22C3 pharmdx su agoaspirati non è stato convalidato. P03928IT_04/SK / p. 7/17
8 Valutazione delle prestazioni cliniche KEYNOTE-024: Controlled trial of NSCLC patients naïve to treatment (Studio controllato su pazienti affetti da NSCLC non trattati in precedenza) La sicurezza e l'efficacia di pembrolizumab sono state analizzate nello studio multicentrico controllato KEYNOTE-024 sul trattamento di pazienti affetti da NSCLC metastatico e non trattati in precedenza. I pazienti presentavano un'espressione di PD-L1 con punteggio TPS (Tumor Proportion Score) 50% in base a PD-L1 IHC 22C3 pharmdx (9). I pazienti sono stati randomizzati (1:1) in modo da ricevere una dose di 200 mg di pembrolizumab ogni 3 settimane (n=154) o chemioterapia contenente platino a scelta del ricercatore (n=151), quale pemetrexed+carboplatino, pemetrexed+cisplatino, gemcitabina+cisplatino, gemcitabina+carboplatino o paclitaxel+carboplatino. I pazienti affetti da tumore non squamoso potevano essere sottoposti a terapia di mantenimento con pemetrexed. I pazienti sono stati trattati con pembrolizumab fino a livelli di tossicità inaccettabili o alla progressione della malattia. Il trattamento poteva essere proseguito anche oltre la progressione della malattia se il paziente risultava clinicamente stabile e il ricercatore riteneva che ottenesse un beneficio clinico. Sono stati esclusi dallo studio i pazienti che presentavano aberrazioni genomiche tumorali di EGFR o ALK, malattie autoimmuni che richiedevano una terapia sistemica entro 2 anni dal trattamento, una condizione medica che richiedeva immunosoppressione o che avevano ricevuto più di 30 Gy di radiazioni al torace nelle 26 settimane precedenti. La valutazione dello stato del tumore è stata effettuata ogni 9 settimane. È stato possibile trasferire al trattamento con pembrolizumab i pazienti sottoposti a chemioterapia che manifestavano una progressione della malattia verificata in modo indipendente. I 305 pazienti inclusi nello studio KEYNOTE-024 presentavano le seguenti caratteristiche di riferimento: età mediana di 65 anni (il 54% aveva un'età di 65 anni o più), 61% maschi, 82% bianchi e 15% asiatici, con stato delle prestazioni ECOG 0 e 1 rispettivamente nel 35% e nel 65% dei casi. Le caratteristiche della malattia erano: tumore squamoso (18%) e non squamoso (82%), M1 (99%) e metastasi cerebrali (9%). La misura principale dell'efficacia era data dalla sopravvivenza libera da progressione (PFS, Progression-Free Survival), determinata tramite una revisione centrale indipendente in cieco (BICR, Blinded Independent Central Review) secondo la versione 1.1 dei criteri di valutazione della risposta nei tumori solidi (RECIST, Response Evaluation Criteria on Solid Tumors). La misura secondaria dell'efficacia era data dalla sopravvivenza totale (OS, Overall Survival) e dal tasso di risposta oggettiva (ORR, Objective Response Rate), valutati tramite BICR applicando i criteri RECIST 1.1. La tabella 2 riassume gli endpoint principali di efficacia nell'intera popolazione ITT (Intention to Treat). Tabella 2: risultati sull'efficacia ottenuti nello studio KEYNOTE-024 Endpoint KEYTRUDA 200 mg ogni 3 settimane n=154 Chemioterapia n=151 PFS* Numero (%) di pazienti con evento 73 (47%) 116 (77%) Rapporto di rischio 0,50 (0,37, 0,68) --- Valore P <0, Mediana in mesi 10,3 (6,7, N/D) 6,0 (4,2, 6,2) OS Numero (%) di pazienti con evento 44 (29%) 64 (42%) Rapporto di rischio 0,60 (0,41, 0,89) --- Valore P 0, Mediana in mesi Non raggiunta (N/D, N/D) Non raggiunta (9,4, N/D) Tasso di risposta oggettiva* ORR % 45% (37, 53) 28% (21, 36) % di risposta completa 4% 1% % di risposta parziale 41% 27% Durata della risposta Mediana in mesi (intervallo) Non raggiunta (1,9+, 14,5+) % con durata > 6 mesi 88% 59%# * Valutato mediante revisione centrale indipendente in cieco (BICR), utilizzando i criteri RECIST 1.1 Rapporto di rischio (confronto tra KEYTRUDA e chemioterapia) basato sul modello dei rischi proporzionali di Cox stratificato Basato sul test dei ranghi logaritmici stratificato In base ai pazienti con risposta completa o parziale confermata come miglior risposta complessiva In base alle stime di Kaplan-Meier; include 43 pazienti con risposta di 6 mesi o superiore # In base alle stime di Kaplan-Meier; include 16 pazienti con risposta di 6 mesi o superiore N/D = Non disponibile 6,3 (2,1+, 12,6+) P03928IT_04/SK / p. 8/17
9 Figura 1: curva di Kaplan-Meier per la sopravvivenza totale nello studio KEYNOTE Sopravvivenza Overall Survival totale (%) (%) Treatment Braccio di arm trattamento KEYTRUDA Chemotherapy Chemioterapia Numero a Time Tempo in in Months mesi rischio Number at Risk KEYTRUDA: Chemioterapia: Chemotherapy: KEYNOTE-010: Controlled trial of NSCLC patients previously treated with chemotherapy (Studio controllato su pazienti affetti da NSCLC e precedentemente trattati con chemioterapia) Il beneficio clinico di PD-L1 IHC 22C3 pharmdx è stato esaminato nello studio clinico multicentrico randomizzato in aperto KEYNOTE- 010, condotto per valutare la sicurezza e l'efficacia di KEYTRUDA in pazienti affetti da NSCLC in stadio avanzato e precedentemente sottoposti a chemioterapia contenente platino (10).(9). I pazienti presentavano un'espressione di PD-L1 con punteggio TPS 1% in base a una versione CTA (Clinical Trial Assay, saggio dello studio clinico) di PD-L1 IHC 22C3 pharmdx. I pazienti con mutazione attivante di EGFR o traslocazione di ALK presentavano anche una progressione della malattia in seguito alla somministrazione della terapia approvata per tali mutazioni, prima di ricevere il pembrolizumab. I pazienti sono stati randomizzati (1:1:1) in modo da ricevere una dose di 2 (n=344) o 10 mg/kg (n=346) di pembrolizumab ogni 3 settimane oppure una dose di 75 mg/m 2 di docetaxel ogni 3 settimane (n=343) fino alla progressione della malattia o a livelli di tossicità inaccettabili. Sono stati esclusi dallo studio i pazienti che presentavano malattie autoimmuni, una condizione medica che richiedeva immunosoppressione o che avevano ricevuto più di 30 Gy di radiazioni al torace nelle 26 settimane precedenti. La valutazione dello stato del tumore è stata effettuata ogni 9 settimane. La misura principale dell'efficacia era data dalla sopravvivenza totale (OS) e dalla sopravvivenza libera da progressione (PFS) valutate tramite BICR applicando i criteri RECIST 1.1. Sulla base del CTA, nello studio sono stati randomizzati in totale pazienti affetti da NSCLC. Per valutare l'utilità clinica di PD-L1 IHC 22C3 pharmdx, alcuni campioni archiviati da studi clinici sono stati analizzati retrospettivamente con questo saggio presso un laboratorio di riferimento negli Stati Uniti. Sono stati analizzati retrospettivamente i tessuti tumorali di 529 pazienti su utilizzando il saggio PD-L1 IHC 22C3 pharmdx. I campioni di 413 pazienti presentavano espressione di PD-L1 ( 1% delle cellule tumorali vitali mostrava colorazione della membrana a una qualunque intensità), mentre i campioni di 94 pazienti non mostravano alcuna espressione di PD-L1 (<1% delle cellule tumorali vitali mostrava colorazione della membrana a qualunque intensità). Tra questi 413 pazienti con espressione di PD-L1, i campioni provenienti da 163 pazienti presentavano un'espressione elevata di PD-L1 ( 50% delle cellule tumorali vitali mostrava colorazione della membrana a qualunque intensità). Il livello di concordanza raggiunto tra il CTA e PD-L1 IHC 22C3 pharmdx è mostrato nella tabella 3. Tabella 3: Concordanza tra CTA e PD-L1 IHC 22C3 pharmdx Tassi di concordanza PD-L1 Cut-off Concordanza percentuale negativa (intervallo di confidenza (IC) al 95%) CTA vs. PD-L1 IHC 22C3 pharmdx P03928IT_04/SK / p. 9/17 Percentuale di concordanza positiva (intervallo di confidenza (IC) al 95%) TPS 1% 94,5% [91,4%-96,6%] 80,0% [76,9%-82,8%] TPS 50% 98,3% [97,1%-99,0%] 73,2% [67,9%-77,9%] Tra i pazienti randomizzati con espressione di PD-L1 in base al saggio PD-L1 IHC 22C3 pharmdx, le caratteristiche demografiche e le altre caratteristiche di base erano ben bilanciate tra i bracci di trattamento. L'età mediana era di 63 anni (44% di 65 anni di età o più). La maggior parte dei pazienti era bianca (77%) e di sesso maschile (58%); lo stato delle prestazioni ECOG alla linea di base era 0 (29%) o 1 (71%). Il 78% dei pazienti era stato o era fumatore. Il 22% dei pazienti presentava istologia squamosa e il 69% non squamosa. Le caratteristiche basali e demografiche erano parimenti ben bilanciate nei bracci pembrolizumab e docetaxel nella popolazione generale dello studio clinico. I risultati sull'efficacia sono riassunti nelle tabelle 4 e 5. KEYTRUDA ha dimostrato di apportare benefici clinici di lunga durata nei pazienti affetti da NSCLC con espressione di PD-L1 (TPS 1%), che risultavano amplificati nei pazienti con espressione di PD-L1 elevata (TPS 50%), come determinato mediante PD-L1 IHC 22C3 pharmdx. L'entità del beneficio era paragonabile a quella osservata nella popolazione generale dello studio clinico. La tabella che segue riassume gli endpoint principali di efficacia nell'intera popolazione con espressione di PD-L1 (TPS 1%) e nel sottoinsieme con espressione di PD-L1 elevata (TPS 50%) per la popolazione generale dello studio clinico (TPS 1% mediante CTA) e nella popolazione con espressione di PD-L1 in base a PD-L1 IHC 22C3 pharmdx. La curva di Kaplan-Meier per la sopravvivenza totale (TPS 1%), determinata in base a PD-L1 IHC 22C3 pharmdx, è illustrata nella figura 2. I risultati sull'efficacia ottenuti per i bracci che utilizzavano 2 mg/kg e 10 mg/kg di KEYTRUDA sono simili.
10 Tabella 4: risposta a KEYTRUDA in pazienti affetti da NSCLC e trattati in precedenza - Popolazione generale dello studio clinico e pazienti positivi in base a PD-L1 IHC 22C3 pharmdx: PD-L1 TPS 1% KEYTRUDA KEYTRUDA Docetaxel Endpoint 2 mg/kg ogni 3 settimane 10 mg/kg ogni 3 settimane 75 mg/m 2 ogni 3 settimane Studio clinico PD-L1 IHC 22C3 pharmdx Studio clinico PD-L1 IHC 22C3 pharmdx Studio clinico PD-L1 IHC 22C3 pharmdx Numero di pazienti OS Decessi (%) 172 (50%) 59 (42%) 156 (45%) 59 (42%) 193 (56%) 67 (51%) Rapporto di rischio* 0,71 (0,58, 0,88) 0,54 (0,37, 0,78) 0,61 (0,49, 0,75) 0,57 (0,39, 0,82) Valore P <0,001 <0,001 <0,001 0, Mediana in mesi 10,4 (9,4, 11,9) 11,8 (9,6, N/D) 12,7 (10,0, 17,3) 12,0 (8,7, N/D) 8,5 (7,5, 9,8) 7,5 (6,3, 9,9) PFS Eventi (%) 266 (77%) 97 (63%) 255 (74%) 103 (73%) 257 (75%) 94 (72%) Rapporto di rischio* 0,88 (0,73, 1,04) 0,68 (0,50, 0,92) 0,79 (0,66, 0,94) 0,79 (0,59, 1,06) Valore P 0,068 0, ,005 0, Mediana in mesi Tasso di risposta complessiva ORR % 3,9 (3,1, 4,1) 18% (14, 23) 4,9 (4,1, 6,2) 24% (17, 32) 4,0 (2,6, 4,3) 18% (15, 23) 4,0 (2,2, 4,6) 20% (14, 28) 4,0 (3,1, 4,2) 9% (7, 13) 3,8 (2,2, 4,2) 5% (2, 11) * Rapporto di rischio (KEYTRUDA in confronto a docetaxel) basato sul modello dei rischi proporzionali di Cox stratificato Basato sul test dei ranghi logaritmici stratificato Valutato mediante revisione centrale indipendente in cieco (BICR), utilizzando i criteri RECIST 1.1 Tutte le risposte erano risposte parziali Tabella 5: risposta a KEYTRUDA in pazienti affetti da NSCLC e trattati in precedenza - Popolazione generale dello studio clinico e pazienti positivi in base a PD-L1 IHC 22C3 pharmdx: PD-L1 TPS 50% KEYTRUDA KEYTRUDA Docetaxel Endpoint 2 mg/kg ogni 3 settimane 10 mg/kg ogni 3 settimane 75 mg/m 2 ogni 3 settimane Studio clinico PD-L1 IHC 22C3 pharmdx Studio clinico PD-L1 IHC 22C3 pharmdx Studio clinico Numero di pazienti OS PD-L1 IHC 22C3 pharmdx Decessi (%) 58 (42%) 18 (32%) 60 (40%) 19 (32%) 86 (57%) 25 (53%) Rapporto di rischio* 0,54 (0,38, 0,77) 0,45 (0,24, 0,84) 0,50 (0,36, 0,70) 0,29 (0,15, 0,56) Valore P <0,001 0,00541 <0,001 <0, Mediana in mesi PFS 14,9 (10,4, N/D) Non raggiunta (9,3, N/D) 17,3 (11,8, N/D) Non raggiunta (8,3, N/D) 8,2 (6,4, 10,7) 7,2 (4,4, 8,3) Eventi (%) 89 (64%) 33 (59%) 97 (64%) 34 (57%) 118 (78%) 33 (70%) Rapporto di rischio* 0,58 (0,43, 0,77) 0,47 (0,28, 0,80) 0,59 (0,45, 0,78) 0,41 (0,24, 0,70) Valore P <0,001 0,00221 <0,001 <0, Mediana in mesi Tasso di risposta complessiva ORR % 5,2 (4,0, 6,5) 30% (23, 39) 5,9 (4,2, 9,0) 37% (25, 52) 5,2 (4,1, 8,1) 29% (22, 37) 4,8 (2,8, N/D) 28% (18, 41) 4,1 (3,6, 4,3) 8% (4, 13) 3,9 (2,0, 4,3) 4% (1, 15) * Rapporto di rischio (KEYTRUDA in confronto a docetaxel) basato sul modello dei rischi proporzionali di Cox stratificato Basato sul test dei ranghi logaritmici stratificato Valutato mediante revisione centrale indipendente in cieco (BICR), utilizzando i criteri RECIST 1.1 Tutte le risposte erano risposte parziali P03928IT_04/SK / p. 10/17
11 Figura 2: curva di Kaplan-Meier per la sopravvivenza totale per braccio di trattamento (TPS 1% in base a PD-L1 IHC 22C3 pharmdx, popolazione Intent To Treat) Sopravvivenza totale (%) Docetaxel 75 mg/m 2 Q3W MK mg/kg Q3W MK mg/kg Q3W n a rischio Docetaxel 75 mg/m 2 Q3W 131 Tempo in mesi MK mg/kg Q3W 140 MK mg/kg Q3W 142 Sono state condotte analisi aggiuntive di affidabilità per tenere in considerazione l'impatto potenziale di dati mancanti dovuti alla presenza di pazienti con espressione di PD-L1 (TPS 1%) in base a PD-L1 IHC 22C3 pharmdx, ma che risultavano privi di espressione di PD-L1 (TPS <1%) in base al CTA. I pazienti che presentano tali risultati fanno parte della popolazione destinataria/intent To Diagnose (ITD) di PD-L1 IHC 22C3 pharmdx, ma sono stati esclusi dallo studio clinico perché non presentavano espressione di PD- L1 in base allo screening CTA. Per tenere conto di questi dati mancanti, è stata condotta un'analisi di sensibilità al fine di determinare l'intervallo plausibile per il rapporto di rischio (HR) stimato in base a PD-L1 IHC 22C3 pharmdx nelle sottopopolazioni con TPS 1% e TPS 50% in un contesto ITD, per verificare la coerenza con l'hr osservato in base all'arruolamento con CTA. I risultati dell'analisi di sensibilità dell'hr hanno mostrato che le stime dell'hr sono affidabili anche tenendo conto di ipotetiche attenuazioni dell'effetto del trattamento in un contesto ITD. Valutazione delle prestazioni non cliniche Sensibilità/specificità analitica La sensibilità analitica di PD-L1 IHC 22C3 pharmdx è stata valutata su 127 casi unici di campioni FFPE di carcinoma polmonare non a piccole cellule (NSCLC) negli stadi da I a IV utilizzando un lotto di produzione industriale. La valutazione dell'espressione di PD-L1 ha evidenziato una colorazione in un intervallo dallo 0 al 100% di cellule tumorali positive e un'intensità di colorazione compresa tra 0 e 3. Tessuti normali: la tabella 6 fornisce un quadro dell'immunoreattività dell'anticorpo Monoclonal Mouse Anti-PD-L1, Clone 22C3 relativamente a tessuti normali selezionati. È stata osservata colorazione della membrana plasmatica sulle cellule immunitarie e di origine epiteliale. È stata osservata colorazione citoplasmatica in alcuni tipi di cellule ma non è stata registrata come colorazione positiva. Tutti i tessuti analizzati sono stati fissati in formalina e inclusi in paraffina e successivamente colorati con PD-L1 IHC 22C3 pharmdx, secondo le istruzioni riportate nel presente foglietto informativo. Non sono stati riscontrati risultati inattesi nei tipi di cellule e di tessuti analizzati. La colorazione osservata è risultata compatibile con la letteratura disponibile per l'espressione IHC di PD-L1 nei tessuti normali (11, 12). Tabella 6: Reattività dei tessuti normali a PD-L1 IHC 22C3 pharmdx Tipo di tessuto (q.tà testata) Colorazione positiva della membrana plasmatica: Elementi del tessuto Colorazione positiva citoplasmatica: Elementi del tessuto Cellule mesoteliali (2) 0/2 0/2 0/2 Cerebrum (3) 0/3 0/3 0/3 Cervelletto (3) 0/3 0/3 0/3 Cervice (3) 1/3 epitelio 0/3 0/3 Colon (3) 2/3 macrofagi 0/3 0/3 Cute (3) 0/3 0/3 0/3 Esofago (3) 0/3 0/3 0/3 Fegato (3) 1/3 macrofagi 0/3 0/3 1/3 epatociti Ghiandola salivare (3) 0/3 0/3 0/3 Intestino tenue (3) 0/3 0/3 0/3 Ipofisi (3) 1/3 ipofisi anteriore 1/3 ipofisi anteriore 0/3 1/3 ipofisi posteriore 1/3 ipofisi posteriore Mammella (3) 0/3 0/3 0/3 Midollo osseo (3) 3/3 megacariociti 3/3 megacariociti 0/3 Milza (3) 2/3 macrofagi 0/3 0/3 Muscolo, cardiaco (3) 0/3 0/3 0/3 Colorazione aspecifica P03928IT_04/SK / p. 11/17
PD-L1 IHC 22C3 pharmdx. SK test per l'utilizzo con Autostainer Link 48. Sommario
 PD-L1 IHC 22C3 pharmdx SK006 50 test per l'utilizzo con Autostainer Link 48 Sommario 1. Uso previsto... 2 2. Riepilogo e spiegazione... 2 2.1 NSCLC...2 2.2 Melanoma...2 3. Principio della procedura...
PD-L1 IHC 22C3 pharmdx SK006 50 test per l'utilizzo con Autostainer Link 48 Sommario 1. Uso previsto... 2 2. Riepilogo e spiegazione... 2 2.1 NSCLC...2 2.2 Melanoma...2 3. Principio della procedura...
PD-L1 IHC 28-8 pharmdx. SK test per l'utilizzo con Autostainer Link 48
 PD-L1 IHC 28-8 pharmdx SK005 50 test per l'utilizzo con Autostainer Link 48 Sommario 1. Uso previsto...2 2. Riepilogo e spiegazione...2 2.1 NSCLC non squamoso...2 2.2 Carcinoma a cellule squamose di testa
PD-L1 IHC 28-8 pharmdx SK005 50 test per l'utilizzo con Autostainer Link 48 Sommario 1. Uso previsto...2 2. Riepilogo e spiegazione...2 2.1 NSCLC non squamoso...2 2.2 Carcinoma a cellule squamose di testa
Soluzione tamponata contenente perossido di idrogeno, detergente e sodio azide 0,015 mol/l.
 PD-L1 IHC 22C3 pharmdx SK006 50 test per l'utilizzo con Autostainer Link 48 Uso previsto Per uso diagnostico in vitro. PD-L1 IHC 22C3 pharmdx è un saggio immunoistochimico qualitativo che utilizza Monoclonal
PD-L1 IHC 22C3 pharmdx SK006 50 test per l'utilizzo con Autostainer Link 48 Uso previsto Per uso diagnostico in vitro. PD-L1 IHC 22C3 pharmdx è un saggio immunoistochimico qualitativo che utilizza Monoclonal
EnVision FLEX Mini Kit, High ph (Dako Omnis)
 EnVision FLEX Mini Kit, High ph (Dako Omnis) Code GV823 2 a edizione Il kit contiene i reagenti sufficienti per 150 test. Per strumenti Dako Omnis. Reagenti facoltativi: Codice Nome prodotto Test GV804
EnVision FLEX Mini Kit, High ph (Dako Omnis) Code GV823 2 a edizione Il kit contiene i reagenti sufficienti per 150 test. Per strumenti Dako Omnis. Reagenti facoltativi: Codice Nome prodotto Test GV804
PD-L1 IHC 28-8 pharmdx. SK test per l'utilizzo con Autostainer Link 48. Uso previsto Per uso diagnostico in vitro.
 PD-L1 IHC 28-8 pharmdx SK005 50 test per l'utilizzo con Autostainer Link 48 Uso previsto Per uso diagnostico in vitro. PD-L1 IHC 28-8 pharmdx è un saggio immunoistochimico qualitativo che utilizza Monoclonal
PD-L1 IHC 28-8 pharmdx SK005 50 test per l'utilizzo con Autostainer Link 48 Uso previsto Per uso diagnostico in vitro. PD-L1 IHC 28-8 pharmdx è un saggio immunoistochimico qualitativo che utilizza Monoclonal
EnVision FLEX Mini Kit, High ph (Link)
 EnVision FLEX Mini Kit, High ph (Link) Codice K8023 2 a edizione Il kit contiene reagenti sufficienti per 125 190 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
EnVision FLEX Mini Kit, High ph (Link) Codice K8023 2 a edizione Il kit contiene reagenti sufficienti per 125 190 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus)
 EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus) Codice K8012 6 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus) Codice K8012 6 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
EnVision FLEX+, Mouse, High ph, (Link)
 EnVision FLEX+, Mouse, High ph, (Link) Codice K8002 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
EnVision FLEX+, Mouse, High ph, (Link) Codice K8002 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
TEICOPLANINA QMS Saggio immunologico
 0155948-0 Gen. 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
0155948-0 Gen. 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3
 DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
HercepTest for Automated Link Platforms
 HercepTest for Automated Link Platforms Codice SK001 22 edizione (129284-001) P04456IT_01_SK00121-2/2016.05 p. 1/41 Sommario Pagina Finalità d uso...3 Cenni introduttivi - Mammella...4 Principio della
HercepTest for Automated Link Platforms Codice SK001 22 edizione (129284-001) P04456IT_01_SK00121-2/2016.05 p. 1/41 Sommario Pagina Finalità d uso...3 Cenni introduttivi - Mammella...4 Principio della
TEICOPLANINA QMS Saggio immunologico
 0155941-0 Gen., 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
0155941-0 Gen., 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
Rassegna Stampa. Comunicato stampa. Intermedia s.r.l. per la comunicazione integrata
 Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
HercepTest Codice nr. K5204
 HercepTest Codice nr. K5204 21 a edizione Per colorazione immunocitochimica. Il kit contiene i reagenti sufficienti per 35 test (70 vetrini). (129258-001) P04454IT_01_K520421-2/2016.05 p.1/55 Sommario
HercepTest Codice nr. K5204 21 a edizione Per colorazione immunocitochimica. Il kit contiene i reagenti sufficienti per 35 test (70 vetrini). (129258-001) P04454IT_01_K520421-2/2016.05 p.1/55 Sommario
HercepTest per Dako Autostainer
 HercepTest per Dako Autostainer Codice nr. K5207 19 a edizione Per colorazione immunocitochimica. Il kit contiene i reagenti sufficienti per 50 test (100 vetrini). (128388-001) P04087IT_01_K520721-2/2015.05
HercepTest per Dako Autostainer Codice nr. K5207 19 a edizione Per colorazione immunocitochimica. Il kit contiene i reagenti sufficienti per 50 test (100 vetrini). (128388-001) P04087IT_01_K520721-2/2015.05
Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP
 Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP Pag. 1 di 5 USO PREVISTO: Per uso diagnostico in vitro. DISPONIBILITÀ: Codice catalogo Quantità
Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP Pag. 1 di 5 USO PREVISTO: Per uso diagnostico in vitro. DISPONIBILITÀ: Codice catalogo Quantità
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Caratteristiche prestazionali
 Caratteristiche prestazionali Kit RNeasy DSP FFPE, Versione 1 73604 Gestione della versione Il presente è il documento Caratteristiche prestazionali del kit RNeasy DSP FFPE, Versione 1, R1. Prima di eseguire
Caratteristiche prestazionali Kit RNeasy DSP FFPE, Versione 1 73604 Gestione della versione Il presente è il documento Caratteristiche prestazionali del kit RNeasy DSP FFPE, Versione 1, R1. Prima di eseguire
Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30. Codice M3652. Uso previsto
 Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30 Codice M3652 Uso previsto Per uso diagnostico in vitro. Monoclonal Rabbit Anti-Human Cytokeratin 8/18, Clone EP17/EP30, è destinato all'utilizzo
Monoclonal Rabbit Anti-Human Cytokeratin 8/18 Clone EP17/EP30 Codice M3652 Uso previsto Per uso diagnostico in vitro. Monoclonal Rabbit Anti-Human Cytokeratin 8/18, Clone EP17/EP30, è destinato all'utilizzo
Test ELISA (enzyme-linked immunosorbent assay)
 PLS-BIOTECNOLOGIE Dipartimento di Scienze ATTIVITA LABORATORIALE 2017-2018 Test ELISA (enzyme-linked immunosorbent assay) Determinazione della presenza/assenza di un Antigene INTRODUZIONE ELISA è l'acronimo
PLS-BIOTECNOLOGIE Dipartimento di Scienze ATTIVITA LABORATORIALE 2017-2018 Test ELISA (enzyme-linked immunosorbent assay) Determinazione della presenza/assenza di un Antigene INTRODUZIONE ELISA è l'acronimo
URISTIKFIT LEV1 REF KCQURST1
 URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
RIDA QUICK Verotoxin/O157 Combi Control NP2204
 RIDA QUICK Verotoxin/O157 Combi Control NP2204 R-Biopharm AG, An der neuen Bergstraße 17, 64297 Darmstadt, Germania Telefono: +49 (0) 61 51 81 02-0, Fax: +49 (0) 61 51 81 02-20 1. Campo di applicazione
RIDA QUICK Verotoxin/O157 Combi Control NP2204 R-Biopharm AG, An der neuen Bergstraße 17, 64297 Darmstadt, Germania Telefono: +49 (0) 61 51 81 02-0, Fax: +49 (0) 61 51 81 02-20 1. Campo di applicazione
Monoclonal Mouse Anti-Human PD-L1 Clone 22C3. Codice M3653. Uso previsto
 Monoclonal Mouse Anti-Human PD-L1 Clone 22C3 Codice M3653 Uso previsto Sinonimo dell'antigene Riepilogo e spiegazione Per uso diagnostico in vitro. Monoclonal Mouse Anti-Human PD-L1, Clone 22C3, è destinato
Monoclonal Mouse Anti-Human PD-L1 Clone 22C3 Codice M3653 Uso previsto Sinonimo dell'antigene Riepilogo e spiegazione Per uso diagnostico in vitro. Monoclonal Mouse Anti-Human PD-L1, Clone 22C3, è destinato
Laura Borghi Anatomia Patologica Azienda ULSS 18 Rovigo
 Laura Borghi Anatomia Patologica Azienda ULSS 18 Rovigo Anatomia Patologica Azienda ULSS 18 Rovigo MARKERS PROGNOSTICI p16 INK4a / Ki67 IN UNA POPOLAZIONE SELEZIONATA HPV DNA-HR POSITIVO: CORRELAZIONE
Laura Borghi Anatomia Patologica Azienda ULSS 18 Rovigo Anatomia Patologica Azienda ULSS 18 Rovigo MARKERS PROGNOSTICI p16 INK4a / Ki67 IN UNA POPOLAZIONE SELEZIONATA HPV DNA-HR POSITIVO: CORRELAZIONE
VIDAS HBs Ag - Cod
 SCHEDA DI SICUREZZA N 256 Versione D Data : 07.02.2002 Data di revisione : 05.07.2002 Cartucce 1 x 60 Coni 2 x 30 Standard 3 x 1 ml Controllo positivo 1 x 1,5 ml Controllo negativo 1 x 1,5 ml * Ag HBs
SCHEDA DI SICUREZZA N 256 Versione D Data : 07.02.2002 Data di revisione : 05.07.2002 Cartucce 1 x 60 Coni 2 x 30 Standard 3 x 1 ml Controllo positivo 1 x 1,5 ml Controllo negativo 1 x 1,5 ml * Ag HBs
IMMUNOISTOCHIMICA ASPETTI BIOCHIMICI
 Università degli Studi di Ferrara Facoltà di Scienze MM.FF.NN. Laurea Triennale in Scienze Biologiche IMMUNOISTOCHIMICA ASPETTI BIOCHIMICI Guastella Giuseppe email giuseppe.guastella@unife.it telefono
Università degli Studi di Ferrara Facoltà di Scienze MM.FF.NN. Laurea Triennale in Scienze Biologiche IMMUNOISTOCHIMICA ASPETTI BIOCHIMICI Guastella Giuseppe email giuseppe.guastella@unife.it telefono
ZytoLight CEN X/Y Dual Color Probe
 ZytoLight CEN X/Y Dual Color Probe Z-2016-200 Z-2016-50 20 (0.2 ml) 5 (0.05 ml) Per la rilevazione degli alfa-satelliti del cromosoma X e della regione del satellite III del cromosoma Y mediante ibridazione
ZytoLight CEN X/Y Dual Color Probe Z-2016-200 Z-2016-50 20 (0.2 ml) 5 (0.05 ml) Per la rilevazione degli alfa-satelliti del cromosoma X e della regione del satellite III del cromosoma Y mediante ibridazione
TECNICHE IMMUNOISTOCHIMICHE IN PATOLOGIA VETERINARIA: VANTAGGI E LIMITI. Pezzolato Marzia, DVM LAB Istopatologia - IZSTO
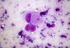 TECNICHE IMMUNOISTOCHIMICHE IN PATOLOGIA VETERINARIA: VANTAGGI E LIMITI Pezzolato Marzia, DVM LAB Istopatologia - IZSTO L immunoistochimica (IHC) serve per individuare un determinato antigene mediante
TECNICHE IMMUNOISTOCHIMICHE IN PATOLOGIA VETERINARIA: VANTAGGI E LIMITI Pezzolato Marzia, DVM LAB Istopatologia - IZSTO L immunoistochimica (IHC) serve per individuare un determinato antigene mediante
Anticorpo di topo monoclonale pronto all'uso, fornito in forma liquida in un tampone contenente la proteina stabilizzante e 0,015 mol/l NaN 3.
 FLEX Monoclonal Mouse Anti-Human Progesterone Receptor Ready-to-Use (Link) Codice IR068 Uso previsto Sinonimo dell'antigene Cenni introduttivi Reagente fornito Per uso diagnostico in vitro. FLEX Monoclonal
FLEX Monoclonal Mouse Anti-Human Progesterone Receptor Ready-to-Use (Link) Codice IR068 Uso previsto Sinonimo dell'antigene Cenni introduttivi Reagente fornito Per uso diagnostico in vitro. FLEX Monoclonal
Heat Shock Protein 27 (G3.1)
 Identificazione Prodotto N Catalogo Descrizione 46946 HSP27 0,1 M (G3.1) 46947 HSP27 1 M (G3.1) 46945 HSP27 RTU M (G3.1) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
Identificazione Prodotto N Catalogo Descrizione 46946 HSP27 0,1 M (G3.1) 46947 HSP27 1 M (G3.1) 46945 HSP27 RTU M (G3.1) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
VIDAS Anti HBs TOTAL - Cod
 SCHEDA DI SICUREZZA N 592 Versione C Data : 21.08.1995 Data di revisione :20.11.2000 NOME DEL PRODOTTO VIDAS Anti HBs TOTAL - Cod. 30 304 DESCRIZIONE DEL KIT Cartucce : 1 x 60 Coni : 2 x 30 Standard :
SCHEDA DI SICUREZZA N 592 Versione C Data : 21.08.1995 Data di revisione :20.11.2000 NOME DEL PRODOTTO VIDAS Anti HBs TOTAL - Cod. 30 304 DESCRIZIONE DEL KIT Cartucce : 1 x 60 Coni : 2 x 30 Standard :
Progensa PCA3 Urine Specimen Transport Kit
 Istruzioni per i medici Progensa PCA3 Urine Specimen Transport Kit Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
Istruzioni per i medici Progensa PCA3 Urine Specimen Transport Kit Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
SINOSSI DEL PROTOCOLLO
 Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
Anticorpo di topo monoclonale pronto all'uso, fornito in forma liquida in un tampone contenente la proteina stabilizzante e 0,015 mol/l NaN 3.
 FLEX Monoclonal Mouse Anti-Human Progesterone Receptor Ready-to-Use (Dako Autostainer/Autostainer Plus) Codice IS068 Uso previsto Per uso diagnostico in vitro. FLEX Monoclonal Mouse Anti-Human Progesterone
FLEX Monoclonal Mouse Anti-Human Progesterone Receptor Ready-to-Use (Dako Autostainer/Autostainer Plus) Codice IS068 Uso previsto Per uso diagnostico in vitro. FLEX Monoclonal Mouse Anti-Human Progesterone
ZytoDot SPEC HER2 Probe
 ZytoDot SPEC HER2 Probe C-3001-400 C-3001-100 40 (0.4 ml) 10 (0.1 ml) Per la rilevazione del gene umano HER2 mediante ibridazione in situ cromogenica (CISH).... Dispositivo per uso diagnostico in vitro
ZytoDot SPEC HER2 Probe C-3001-400 C-3001-100 40 (0.4 ml) 10 (0.1 ml) Per la rilevazione del gene umano HER2 mediante ibridazione in situ cromogenica (CISH).... Dispositivo per uso diagnostico in vitro
EGFR pharmdx. Codice K test per uso manuale Edizione 05/2015. Uso previsto Per uso diagnostico In Vitro.
 EGFR pharmdx Codice K1492 35 test per uso manuale Edizione 05/2015 Uso previsto Per uso diagnostico In Vitro. Il saggio EGFR pharmdx è un sistema di analisi qualitativa immunoistochimica (IHC) che consente
EGFR pharmdx Codice K1492 35 test per uso manuale Edizione 05/2015 Uso previsto Per uso diagnostico In Vitro. Il saggio EGFR pharmdx è un sistema di analisi qualitativa immunoistochimica (IHC) che consente
Università degli Studi dell Aquila Dipartimento MeSVA Sezione di Scienze Biologiche e Biotecnologiche. Laboratorio di Istologia
 Università degli Studi dell Aquila Dipartimento MeSVA Sezione di Scienze Biologiche e Biotecnologiche.. Laboratorio di Istologia Allestimento di un preparato istologico L'istologia è la disciplina scientifica
Università degli Studi dell Aquila Dipartimento MeSVA Sezione di Scienze Biologiche e Biotecnologiche.. Laboratorio di Istologia Allestimento di un preparato istologico L'istologia è la disciplina scientifica
Attività Scientifica AIOM Lazio
 Attività Scientifica AIOM Lazio 2016-2017 SURVEY FERTILITA E SESSUALITA IN ONCOLOGIA Società I taliana di Psico-Oncologia AIGO 237 Questionari 34% 66% Sesso 7% Femmine Maschi 16% 10% 67% Ospedale IRCCS
Attività Scientifica AIOM Lazio 2016-2017 SURVEY FERTILITA E SESSUALITA IN ONCOLOGIA Società I taliana di Psico-Oncologia AIGO 237 Questionari 34% 66% Sesso 7% Femmine Maschi 16% 10% 67% Ospedale IRCCS
QMS QUINIDINE. Immunoassay. Legenda dei simboli. Microgenics GmbH. D Passau. Tel: +49 (0) Fax: +49 (0)
 0155255-D October, 2014 QMS QUINIDINE Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
0155255-D October, 2014 QMS QUINIDINE Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
Protocollo ACC Lung. Dott.ssa G. Improta S.I.C. Anatomia Patologica IRCCS-CROB Rionero in Vulture (PZ)
 Protocollo ACC Lung Dott.ssa G. Improta S.I.C. Anatomia Patologica IRCCS-CROB Rionero in Vulture (PZ) ACC: Associazione di ricerca oncologica italiana no-profit ACC Genomics: Programma diagnostico-terapeutico
Protocollo ACC Lung Dott.ssa G. Improta S.I.C. Anatomia Patologica IRCCS-CROB Rionero in Vulture (PZ) ACC: Associazione di ricerca oncologica italiana no-profit ACC Genomics: Programma diagnostico-terapeutico
EMR Merck KGaA, Darmstadt, Germania. Fase clinica IIIb
 1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA
 Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA Tecniche Immunologiche La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono utilizzati
Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA Tecniche Immunologiche La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono utilizzati
Cytokeratin Cocktail (AE1 & AE3)
 Identificazione Prodotto N Catalogo Descrizione 44575 Cytokeratin Cocktail 0,1 M (AE1&AE3) 44576 Cytokeratin Cocktail 1 M (AE1&AE3) 44277 Cytokeratin Cocktail RTU M (AE1&AE3) Definizione Dei Simboli P
Identificazione Prodotto N Catalogo Descrizione 44575 Cytokeratin Cocktail 0,1 M (AE1&AE3) 44576 Cytokeratin Cocktail 1 M (AE1&AE3) 44277 Cytokeratin Cocktail RTU M (AE1&AE3) Definizione Dei Simboli P
VENTANA MMR IHC Panel Guida all interpretazione della colorazione del tessuto del colon-retto
 VENTANA MMR IHC Panel Guida all interpretazione della colorazione del tessuto del colon-retto VENTANA anti-mlh1 (M1) Mouse Monoclonal Primary Antibody VENTANA anti-pms2 (A16-4) Mouse Monoclonal Primary
VENTANA MMR IHC Panel Guida all interpretazione della colorazione del tessuto del colon-retto VENTANA anti-mlh1 (M1) Mouse Monoclonal Primary Antibody VENTANA anti-pms2 (A16-4) Mouse Monoclonal Primary
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus)
 EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Codice K8010 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Codice K8010 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
LE PRESCRIVO UNA APP DAL TACCUINO AL PERSONAL HEALTH RECORD
 LE PRESCRIVO UNA APP DAL TACCUINO AL PERSONAL HEALTH RECORD m-health e Medical APPs 10 domande sulla sicurezza del software medico Alla ricerca di risposte nel futuro Regolamento Europeo sui Dispositivi
LE PRESCRIVO UNA APP DAL TACCUINO AL PERSONAL HEALTH RECORD m-health e Medical APPs 10 domande sulla sicurezza del software medico Alla ricerca di risposte nel futuro Regolamento Europeo sui Dispositivi
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44674 Lambda Light Chain 0,1 M (Lamb14) 44675 Lambda Light Chain 1 M (Lamb14) 44326 Lambda Light Chain RTU M (Lamb14) Definizione Dei Simboli P C A E S DIL
Identificazione Prodotto N Catalogo Descrizione 44674 Lambda Light Chain 0,1 M (Lamb14) 44675 Lambda Light Chain 1 M (Lamb14) 44326 Lambda Light Chain RTU M (Lamb14) Definizione Dei Simboli P C A E S DIL
INGEZIM Gluten Quanti Test Guida all utilizzo
 INGEZIM Gluten Quanti Test Guida all utilizzo 1 - INTRODUZIONE Il kit è basato su un saggio immunoenzimatico ELISA di tipo sandwich come dettato dal Codex Alimentarius. Ogni pozzetto è rivestito sul fondo
INGEZIM Gluten Quanti Test Guida all utilizzo 1 - INTRODUZIONE Il kit è basato su un saggio immunoenzimatico ELISA di tipo sandwich come dettato dal Codex Alimentarius. Ogni pozzetto è rivestito sul fondo
A-1-Antichymotrypsin (Polyclonal)
 Identificazione Prodotto N Catalogo Descrizione 44421 Alpha-1-Antichymotrypsin 0,1 R (Poly) 44422 Alpha-1-Antichymotrypsin 1 R (Poly) 44197 Alpha-1-Antichymotrypsin RTU R (Poly) Definizione Dei Simboli
Identificazione Prodotto N Catalogo Descrizione 44421 Alpha-1-Antichymotrypsin 0,1 R (Poly) 44422 Alpha-1-Antichymotrypsin 1 R (Poly) 44197 Alpha-1-Antichymotrypsin RTU R (Poly) Definizione Dei Simboli
SCHEDA DI DATI DI SICUREZZA
 Data ultima revisione: 2007-03-30 1. IDENTIFICAZIONE DELLA SOSTANZA/ PREPARATO E DELLA SOCIETÀ/IMPRESA 1/5 2007-03-30 K3954 ARK (Animal Research Kit)/HRP K4004 EnVision + System/HRP, Mouse K4005 EnVision
Data ultima revisione: 2007-03-30 1. IDENTIFICAZIONE DELLA SOSTANZA/ PREPARATO E DELLA SOCIETÀ/IMPRESA 1/5 2007-03-30 K3954 ARK (Animal Research Kit)/HRP K4004 EnVision + System/HRP, Mouse K4005 EnVision
RIDASCREEN GIS. Test immunoenzimatico per la rilevazione del latte caprino nel latte ovino. Art. No.: R4802. Test in vitro Conservare a 2-8 C
 RIDASCREEN GIS Test immunoenzimatico per la rilevazione del latte caprino nel latte ovino Art. No.: R4802 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0
RIDASCREEN GIS Test immunoenzimatico per la rilevazione del latte caprino nel latte ovino Art. No.: R4802 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0
QMS TOBRAMYCIN. Immunoassay CALIBRATORI PER LA TOBRAMICINA Legenda dei simboli
 0155269-D-IT November, 2014 QMS TOBRAMYCIN Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
0155269-D-IT November, 2014 QMS TOBRAMYCIN Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44435 BCL2 0,1 R (E17) 44436 BCL2 1 R (E17) 44205 BCL2 RTU R (E17) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
Identificazione Prodotto N Catalogo Descrizione 44435 BCL2 0,1 R (E17) 44436 BCL2 1 R (E17) 44205 BCL2 RTU R (E17) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
RIDASCREEN CIS. Test immunoenzimatico per la rilevazione del latte vaccino nel latte ovino e caprino e nel formaggio ovino e caprino. Art. No.
 RIDASCREEN CIS Test immunoenzimatico per la rilevazione del latte vaccino nel latte ovino e caprino e nel formaggio ovino e caprino Art. No.: R4302 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt,
RIDASCREEN CIS Test immunoenzimatico per la rilevazione del latte vaccino nel latte ovino e caprino e nel formaggio ovino e caprino Art. No.: R4302 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt,
Cytokeratin 5 + Cytokeratin 14 (EP1601Y + LL002)
 Cytokeratin 5 + Cytokeratin 14 (EP1601Y Identificazione Prodotto N Catalogo Descrizione 45693 IMPATH CK5 + CK14 RTU M (EP1601Y & LL002) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero
Cytokeratin 5 + Cytokeratin 14 (EP1601Y Identificazione Prodotto N Catalogo Descrizione 45693 IMPATH CK5 + CK14 RTU M (EP1601Y & LL002) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero
I prodotti prediluiti sono diluiti in modo ottimale per l uso con un ampia varietà di kit di rivelazione offerti da altri produttori.
 Identificazione Prodotto N Catalogo Descrizione 44819 TSH 0,1 R (Poly) 44820 TSH 1 R (Poly) 44400 TSH RTU R (Poly) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
Identificazione Prodotto N Catalogo Descrizione 44819 TSH 0,1 R (Poly) 44820 TSH 1 R (Poly) 44400 TSH RTU R (Poly) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
diagnosi di GIST, né dovrebbe precludere il trattamento con Gleevec/Glivec.
 c-kit pharmdx Codice K1906 25 test per uso manuale Uso previsto Per uso diagnostico In Vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente di identificare
c-kit pharmdx Codice K1906 25 test per uso manuale Uso previsto Per uso diagnostico In Vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente di identificare
diagnosi di GIST, né dovrebbe precludere il trattamento con Gleevec/Glivec.
 c-kit pharmdx Codice K1907 35 test per il sistema Dako Autostainer Uso previsto Per uso diagnostico in vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente
c-kit pharmdx Codice K1907 35 test per il sistema Dako Autostainer Uso previsto Per uso diagnostico in vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente
ZytoLight SPEC BCR/ABL Dual Color Dual Fusion Probe
 ZytoLight SPEC BCR/ABL Dual Color Dual Fusion Probe Z-2111-200 20 (0.2 ml) Per la rilevazione della translocazione t(9;22)(q34;q11)mediante ibridazione in situ fluorescente (FISH).... Dispositivo per uso
ZytoLight SPEC BCR/ABL Dual Color Dual Fusion Probe Z-2111-200 20 (0.2 ml) Per la rilevazione della translocazione t(9;22)(q34;q11)mediante ibridazione in situ fluorescente (FISH).... Dispositivo per uso
Codice Studio: D7913L00138 Protocollo Versione No: 1 Data: 7 November 2011
 SINOSSI DEL PROTOCOLLO Studio di fase II in aperto, multicentrico, a singolo braccio per indagare l efficacia, la sicurezza e la tollerabilità di Gefitinib 250 mg (IRESSA ) come trattamento ri-sfida in
SINOSSI DEL PROTOCOLLO Studio di fase II in aperto, multicentrico, a singolo braccio per indagare l efficacia, la sicurezza e la tollerabilità di Gefitinib 250 mg (IRESSA ) come trattamento ri-sfida in
Striscia reattiva glicemia ematocrito emoglobina. N. modello: TD-4272 / GD40 DELTA
 Striscia reattiva glicemia ematocrito emoglobina AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori che eseguono
Striscia reattiva glicemia ematocrito emoglobina AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori che eseguono
Myelin Basic Protein (Polyclonal)
 Identificazione Prodotto N Catalogo Descrizione 45236 IMPATH Myelin Basic Protein RTU R (Poly) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero supernatante numero documento distribuito
Identificazione Prodotto N Catalogo Descrizione 45236 IMPATH Myelin Basic Protein RTU R (Poly) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero supernatante numero documento distribuito
Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE
 Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE Tecniche di laboratorio La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono
Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE Tecniche di laboratorio La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono
4F81BDSCHEDA TECNICA 4F81BD
 04011Pagina 1 di 5 pagine Codice prodotto: Nome prodotto: Consigliato per: Dimensioni disponibili: 120101 Gori Detergente concentrato rimuove alghe, muschio e strati verdi Tutti i legni per esterni 1 L
04011Pagina 1 di 5 pagine Codice prodotto: Nome prodotto: Consigliato per: Dimensioni disponibili: 120101 Gori Detergente concentrato rimuove alghe, muschio e strati verdi Tutti i legni per esterni 1 L
ERLOTINIB ( )
 ERLOTINIB (17-10-2006) Specialità: Tarceva (Roche) Forma Farmaceutica: 30 cpr Dosaggio: 100mg Prezzo: 2.596,41 30 cpr Dosaggio: 150mg Prezzo: 3.239,24 Prezzo al pubblico da banca dati Farmadati Marzo 2007
ERLOTINIB (17-10-2006) Specialità: Tarceva (Roche) Forma Farmaceutica: 30 cpr Dosaggio: 100mg Prezzo: 2.596,41 30 cpr Dosaggio: 150mg Prezzo: 3.239,24 Prezzo al pubblico da banca dati Farmadati Marzo 2007
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44586 EMA 0,1 M (E29) 44587 EMA 1 M (E29) 44282 EMA RTU M (E29) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
Identificazione Prodotto N Catalogo Descrizione 44586 EMA 0,1 M (E29) 44587 EMA 1 M (E29) 44282 EMA RTU M (E29) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI. Dott.ssa T. Tamburrano Dirigente Medico Oncologia A.O. Marche Nord
 IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI Fano 11-12 Novembre 2016 TUMORE DELLA PROSTATA-MALATTIA METASTATICA- LA TERAPIA DELLA MALATTIA ORMONOSENSIBILE Dott.ssa T. Tamburrano Dirigente
IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI Fano 11-12 Novembre 2016 TUMORE DELLA PROSTATA-MALATTIA METASTATICA- LA TERAPIA DELLA MALATTIA ORMONOSENSIBILE Dott.ssa T. Tamburrano Dirigente
PROGENSA PCA3 Urine Specimen Transport Kit
 PROGENSA PCA3 Urine Specimen Transport Kit Istruzioni per i medici Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
PROGENSA PCA3 Urine Specimen Transport Kit Istruzioni per i medici Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
IMPATH HER2 FISH. Identificazione del prodotto Cat. N. Descrizione ImPath HER2 FISH
 Identificazione del prodotto Cat. N. Descrizione 47862 ImPath HER2 FISH Uso previsto ImPath HER2 FISH (cat. n. 47862) è destinato all uso in combinazione con ImPath ISH Detection Kit (cat. n. 44996) per
Identificazione del prodotto Cat. N. Descrizione 47862 ImPath HER2 FISH Uso previsto ImPath HER2 FISH (cat. n. 47862) è destinato all uso in combinazione con ImPath ISH Detection Kit (cat. n. 44996) per
la dimostrazione dei linfomi di tipo B è possibile con studi di riarrangiamento genico clonale. Principi E Procedure
 Identificazione Prodotto N Catalogo Descrizione 44660 IgM 0,1 R (Poly) 44661 IgM 1 R (Poly) 44319 IgM RTU R (Poly) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
Identificazione Prodotto N Catalogo Descrizione 44660 IgM 0,1 R (Poly) 44661 IgM 1 R (Poly) 44319 IgM RTU R (Poly) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
WITNESS GIARDIA INTRODUZIONE
 WITNESS GIARDIA WITNESS GIARDIA INTRODUZIONE Giardia intestinalis (sin. G. duodenalis o G. lamblia) è un protozoo parassita dell apparato gastrointestinale di numerose specie di animali (ad es. cane e
WITNESS GIARDIA WITNESS GIARDIA INTRODUZIONE Giardia intestinalis (sin. G. duodenalis o G. lamblia) è un protozoo parassita dell apparato gastrointestinale di numerose specie di animali (ad es. cane e
IMPATH ALK D/C BREAK APART FISH
 Identificazione del prodotto Cat. N. Descrizione 47863 ImPath ALK D/C Break Apart FISH Uso previsto ImPath ALK D/C Break Apart FISH (cat. n. 47863) è destinato all uso in combinazione con ImPath ISH Detection
Identificazione del prodotto Cat. N. Descrizione 47863 ImPath ALK D/C Break Apart FISH Uso previsto ImPath ALK D/C Break Apart FISH (cat. n. 47863) è destinato all uso in combinazione con ImPath ISH Detection
Tumori stromali gastrointestinali (GIST)
 Tumori stromali gastrointestinali (GIST) GIST - epidemiologia Neoplasie mesenchimali che originano dalle cellule interstiziali di Cajal (cellule pacemaker) Sono i tumori connettivali più frequenti del
Tumori stromali gastrointestinali (GIST) GIST - epidemiologia Neoplasie mesenchimali che originano dalle cellule interstiziali di Cajal (cellule pacemaker) Sono i tumori connettivali più frequenti del
Anticorpo. Chimerico. Murino mab. Umanizzato. ..tinib 18/05/09. Totalmente umano
 Anticorpo Murino mab Chimerico ximab Umanizzato zumab Totalmente umano mumab..tinib Anticorpi monoclonali anti EGFR Vengono somministrati per via endovenosa ogni settimana o ogni 2 Sono specifiche per
Anticorpo Murino mab Chimerico ximab Umanizzato zumab Totalmente umano mumab..tinib Anticorpi monoclonali anti EGFR Vengono somministrati per via endovenosa ogni settimana o ogni 2 Sono specifiche per
PNA ISH Detection Kit Codice nr. K5201
 PNA ISH Detection Kit Codice nr. K5201 9 a edizione Per ibridazione in situ con l impiego di sonde di PNA coniugate con fluoresceina. Il kit contiene i reagenti sufficienti per almeno 40 test*. * Il numero
PNA ISH Detection Kit Codice nr. K5201 9 a edizione Per ibridazione in situ con l impiego di sonde di PNA coniugate con fluoresceina. Il kit contiene i reagenti sufficienti per almeno 40 test*. * Il numero
QUANTA Chek ANA Panel
 QUANTA Chek ANA Panel 708111 Finalità d uso Il Pannello ANA QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli anticorpi antinucleo IFA ed ELISA. Ciascun siero
QUANTA Chek ANA Panel 708111 Finalità d uso Il Pannello ANA QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli anticorpi antinucleo IFA ed ELISA. Ciascun siero
I prodotti prediluiti sono diluiti in modo ottimale per l uso con un ampia varietà di kit di rivelazione offerti da altri produttori.
 Identificazione Prodotto N Catalogo Descrizione 45264 IMPATH TSH RTU R (Poly) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero supernatante numero documento distribuito da Finalità D Uso
Identificazione Prodotto N Catalogo Descrizione 45264 IMPATH TSH RTU R (Poly) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero supernatante numero documento distribuito da Finalità D Uso
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44827 Tryptase 0,1 M (G3) 44828 Tryptase 1 M (G3) 44404 Tryptase RTU M (G3) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
Identificazione Prodotto N Catalogo Descrizione 44827 Tryptase 0,1 M (G3) 44828 Tryptase 1 M (G3) 44404 Tryptase RTU M (G3) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
Per la conservazione viene aggiunta sodio azide a una concentrazione finale inferiore allo 0,1 %.
 Scheda Tecnica 0123 Technical File No.: 38 Prodotto: Categoria di prodotto secondo la classificazione CE: Albumina Bovina 22% 30% Allegato III Autocertificazione del produttore Struttura della scheda tecnica
Scheda Tecnica 0123 Technical File No.: 38 Prodotto: Categoria di prodotto secondo la classificazione CE: Albumina Bovina 22% 30% Allegato III Autocertificazione del produttore Struttura della scheda tecnica
Ruolo dell anatomo-patologo. Carcinoma del seno: esame morfologico ed immunologico ER/PR ER/PR. Her-2 (C-erbB-2) Her-2
 Ruolo dell anatomo-patologo Carcinoma del seno: esame morfologico ed immunologico L. Mazzucchelli Istituto cantonale di patologia, Locarno Fondazione Oncologia Lago Maggiore, 5 ottobre 2006 Diagnosi preoperatoria
Ruolo dell anatomo-patologo Carcinoma del seno: esame morfologico ed immunologico L. Mazzucchelli Istituto cantonale di patologia, Locarno Fondazione Oncologia Lago Maggiore, 5 ottobre 2006 Diagnosi preoperatoria
Il Progetto di AIOM e SIAPEC-IAP Carmine Pinto
 Il Progetto di AIOM e SIAPEC-IAP Carmine Pinto Presidente Nazionale AIOM Terapie mirate su target molecolari nei primi cinque tumori per incidenza Melanoma Terapia dei tumori solidi personalizzata biomarker-dipendente
Il Progetto di AIOM e SIAPEC-IAP Carmine Pinto Presidente Nazionale AIOM Terapie mirate su target molecolari nei primi cinque tumori per incidenza Melanoma Terapia dei tumori solidi personalizzata biomarker-dipendente
Adenovirus (20/11 & 2/6)
 Identificazione Prodotto N Catalogo Descrizione 45606 Adenovirus 0,1 M (20/11 & 2/6) 45607 Adenovirus 1 M (20/11 & 2/6) 45631 Adenovirus RTU M (20/11 & 2/6) Definizione Dei Simboli P C A E S DIL DOC# DIS
Identificazione Prodotto N Catalogo Descrizione 45606 Adenovirus 0,1 M (20/11 & 2/6) 45607 Adenovirus 1 M (20/11 & 2/6) 45631 Adenovirus RTU M (20/11 & 2/6) Definizione Dei Simboli P C A E S DIL DOC# DIS
Dott. Francesco Fiorica
 Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
ALLflow Elution Technologies Egg Proteins Rapid Test
 ALLflow Elution Technologies Egg Proteins Rapid Test Lateral Flow kit Cat. # ETBEGG-1003 Kit per la rilevazione rapida delle proteine dell uovo in campioni alimentari ed ambientali Manuale d uso Leggere
ALLflow Elution Technologies Egg Proteins Rapid Test Lateral Flow kit Cat. # ETBEGG-1003 Kit per la rilevazione rapida delle proteine dell uovo in campioni alimentari ed ambientali Manuale d uso Leggere
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 45311 IMPATH HGAL RTU M (MRQ- 49) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero supernatante numero documento distribuito da Finalità
Identificazione Prodotto N Catalogo Descrizione 45311 IMPATH HGAL RTU M (MRQ- 49) Definizione Dei Simboli P A E S DOC# DIS pronto uso asciti siero supernatante numero documento distribuito da Finalità
ISTRUZIONI D USO IVD 0123 HLA CLASSE II REF 7029: HISTO TRAY DR 72 (10)
 ISTRUZIONI D USO IVD 0123 HISTO TRAY HLA CLASSE II PER USO DIAGNOSTICO IN VITRO REF 7029: HISTO TRAY DR 72 (10) 10 piastre Descrizione del prodotto La destinazione d uso dell HISTO TRAY è la tipizzazione
ISTRUZIONI D USO IVD 0123 HISTO TRAY HLA CLASSE II PER USO DIAGNOSTICO IN VITRO REF 7029: HISTO TRAY DR 72 (10) 10 piastre Descrizione del prodotto La destinazione d uso dell HISTO TRAY è la tipizzazione
AZIDE ETIL VIOLETTO - BRODO Cod
 SCHEDA DI CUREZZA N 467 Versione E Data : 24.02.1995 Data di revisione : 15.05.2003 NOME DEL PRODOTTO AZIDE ETIL VIOLETTO - BRODO Cod. 51 022 DESCRIZIONE DEL KIT Terreno disidratato : 500 g CENTRO ANTI-VELENI
SCHEDA DI CUREZZA N 467 Versione E Data : 24.02.1995 Data di revisione : 15.05.2003 NOME DEL PRODOTTO AZIDE ETIL VIOLETTO - BRODO Cod. 51 022 DESCRIZIONE DEL KIT Terreno disidratato : 500 g CENTRO ANTI-VELENI
Allegato III Autocertificazione del produttore
 Scheda Tecnica 0123 Technical File No.: 24 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-Lua, Anti-Lub coombsreactive Allegato III Autocertificazione del produttore Struttura della
Scheda Tecnica 0123 Technical File No.: 24 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-Lua, Anti-Lub coombsreactive Allegato III Autocertificazione del produttore Struttura della
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44527 CD79a 0,1 M (JCB117) 44528 CD79a 1 M (JCB117) 44253 CD79a RTU M (JCB117) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
Identificazione Prodotto N Catalogo Descrizione 44527 CD79a 0,1 M (JCB117) 44528 CD79a 1 M (JCB117) 44253 CD79a RTU M (JCB117) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
c-myc (EP121) Rabbit Monoclonal Antibody Identificazione Prodotto Definizione Dei Simboli Finalità D Uso Principi E Procedure Sommario E Spiegazione
 Identificazione Prodotto N Catalogo Descrizione 46928 c-myc 0,1 R (EP121) 46929 c-myc 1 R (EP121) 46927 c-myc RTU R (EP121) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
Identificazione Prodotto N Catalogo Descrizione 46928 c-myc 0,1 R (EP121) 46929 c-myc 1 R (EP121) 46927 c-myc RTU R (EP121) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI
 LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI 1 Che cosa sono le proteine? Indispensabili per il corretto funzionamento 2 Dove si trovano le proteine? Le proteine sono macromolecole ubiquitarie,
LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI 1 Che cosa sono le proteine? Indispensabili per il corretto funzionamento 2 Dove si trovano le proteine? Le proteine sono macromolecole ubiquitarie,
In caso di consultazione di un medico, tenere a disposizione il contenitore o l'etichetta del prodotto.
 http://www.msds-europe.com P101 In caso di consultazione di un medico, tenere a disposizione il contenitore o l'etichetta del prodotto. P102 Tenere fuori dalla portata dei bambini. P103 Leggere l'etichetta
http://www.msds-europe.com P101 In caso di consultazione di un medico, tenere a disposizione il contenitore o l'etichetta del prodotto. P102 Tenere fuori dalla portata dei bambini. P103 Leggere l'etichetta
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44458 CD10 0,1 M (56C6) 44459 CD10 1 M (56C6) 44217 CD10 RTU M (56C6) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
Identificazione Prodotto N Catalogo Descrizione 44458 CD10 0,1 M (56C6) 44459 CD10 1 M (56C6) 44217 CD10 RTU M (56C6) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
15 Anti-D policlonale / incompleto
 Scheda Tecnica 0123 Technical File No.: Prodotto: 15 Anti-D policlonale / incompleto Categoria di prodotto secondo la classificazione CE: Allegato II Lista A Struttura della scheda tecnica Descrizione
Scheda Tecnica 0123 Technical File No.: Prodotto: 15 Anti-D policlonale / incompleto Categoria di prodotto secondo la classificazione CE: Allegato II Lista A Struttura della scheda tecnica Descrizione
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44837 Vimentin 0,1 M (V9) 44838 Vimentin 1 M (V9) 44409 Vimentin RTU M (V9) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
Identificazione Prodotto N Catalogo Descrizione 44837 Vimentin 0,1 M (V9) 44838 Vimentin 1 M (V9) 44409 Vimentin RTU M (V9) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti
Principi E Procedure. Materiali E Metodi
 Identificazione Prodotto N Catalogo Descrizione 44761 PLAP 0,1 M (NB10) 44762 PLAP 1 M (NB10) 44371 PLAP RTU M (NB10) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
Identificazione Prodotto N Catalogo Descrizione 44761 PLAP 0,1 M (NB10) 44762 PLAP 1 M (NB10) 44371 PLAP RTU M (NB10) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile.
 Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile. Questi anticorpi sono delle molecole IgG che attaccano un solo
Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile. Questi anticorpi sono delle molecole IgG che attaccano un solo
EnVision G 2 Doublestain System, Rabbit/Mouse (DAB+/Permanent Red)
 EnVision G 2 Doublestain System, Rabbit/Mouse (DAB+/Permanent Red) Codice K5361 Seconda edizione Per l uso con anticorpi primari di coniglio e topo. Idoneo per 150 test. (114146-002) K5361/IT/SGA/13.10.06
EnVision G 2 Doublestain System, Rabbit/Mouse (DAB+/Permanent Red) Codice K5361 Seconda edizione Per l uso con anticorpi primari di coniglio e topo. Idoneo per 150 test. (114146-002) K5361/IT/SGA/13.10.06
