HercepTest per Dako Autostainer
|
|
|
- Alessio Lelli
- 5 anni fa
- Visualizzazioni
Transcript
1 HercepTest per Dako Autostainer Codice nr. K a edizione Per colorazione immunocitochimica. Il kit contiene i reagenti sufficienti per 50 test (100 vetrini). ( ) P04087IT_01_K / p. 1/55
2 Sommario Pagina Finalità d uso 4 Cenni introduttivi - Mammella 5 Dati di base 5 Caratteristiche 5 Principio della procedura - Mammella 5 Reagenti - Mammella 6 Materiali forniti 6 Materiali necessari ma non forniti 7 Conservazione - Mammella 7 Specimen preparation (Allestimento tessuto) - Mammella 8 Sezioni incluse in paraffina 8 Trattamento dei campioni prima della colorazione 8 Precauzioni - Mammella 9 ISTRUZIONI PER L USO - Mammella 10 A. Preparazione 10 A.1 Epitope Retrieval Solution 10 A.2 Tampone di lavaggio 10 A.3 Soluzione cromogeno-substrato (DAB) 10 A.4 Colorazione di contrasto 11 A.5 Mezzo di montaggio 11 B. Procedura di colorazione su Autostainer 11 B.1 Note sulla procedura 11 B.2 Protocollo di colorazione 12 Controllo di qualità - Mammella 13 Interpretazione della colorazione - Mammella 16 Limitazioni - Mammella 19 Limiti generali 19 Limiti specifici del prodotto 20 Caratteristiche prestazionali - Mammella 20 Dati di base 20 Studi comparativi 21 Studio comparativo con il CTA (Clinical Trial Assay) 21 Accuratezza 22 Riproducibilità 22 Immunoreattività 24 Risoluzione dei problemi - Mammella 25 Cenni introduttivi - Gastrico 28 Dati di base 28 Caratteristiche 28 Principio della procedura - Gastrico 28 Reagenti - Gastrico 29 Materiali forniti 29 Materiali necessari ma non forniti 30 Conservazione - Gastrico 31 Specimen preparation (Allestimento tessuto) - Gastrico 31 Sezioni incluse in paraffina 31 Trattamento dei campioni prima della colorazione 32 Precauzioni - Gastrico 32 ISTRUZIONI PER L USO - Gastrico 34 A. Preparazione 34 A.1 Epitope Retrieval Solution 34 A.2 Tampone di lavaggio 34 A.3 Soluzione cromogeno-substrato (DAB) 34 A.4 Colorazione di contrasto 34 A.5 Mezzo di montaggio 34 B. Procedura di colorazione su Autostainer 35 B.1 Note sulla procedura 35 B.2 Protocollo di colorazione 35 Controllo di qualità - Gastrico 37 Interpretazione della colorazione - Gastrico 39 Limitazioni - Gastrico 43 ( ) P04087IT_01_K / p. 2/55
3 Limiti generali 43 Limiti specifici del prodotto 44 Caratteristiche prestazionali - Gastrico 45 Dati di base 45 Riproducibilità 47 Immunoreattività 49 Risoluzione dei problemi - Gastrico 50 Bibliografia 53 Spiegazione dei simboli 55 ( ) P04087IT_01_K / p. 3/55
4 Finalità d uso Per uso diagnostico in vitro. Il test immunocitochimico semiquantitativo HercepTest consente di determinare l iperespressione della proteina HER2 nei tessuti affetti da tumore della mammella che sono stati sottoposti a trattamento di routine per la valutazione istologica e tessuto cancerogeno fissato in formalina e incluso in paraffina di pazienti con adenocarcinoma dello stomaco, compresa la giunzione gastroesofagea. Il test HercepTest è un valido strumento di supporto nella valutazione dei pazienti che devono essere dichiarati idonei al trattamento con Herceptin (trastuzumab) (vedere il foglietto illustrativo dell Herceptin ). NOTA solo per cancro mammario: tutti i pazienti ammessi agli studi clinici con Herceptin sono stati selezionati applicando un metodo di investigazione immunocitochimica ai fini della sperimentazione clinica (CTA, clinical trial assay). Nessuno dei pazienti ammessi agli studi clinici è stato selezionato con il test HercepTest. Il test HercepTest è stato comparato al CTA utilizzando una serie di campioni indipendenti. La conclusione è che produce risultati discretamente concordanti. L effettiva correlazione tra HercepTest e risultati clinici con Herceptin non è stata ancora stabilita. NOTA solo per cancro gastrico: tutti i pazienti nella fase III BO18255 dello studio ToGA sponsorizzato da Hoffmann-La Roche sono stati selezionati utilizzando l'herceptest (IHC) di Dako e il kit HER2 FISH pharmdx (FISH) di Dako. Lo studio ha dimostrato l utilità clinica di entrambi i test per la valutazione dello stato dell HER2 in pazienti con adenocarcinoma gastrico in stadio avanzato localmente non operabile, ricorrente e/o metastatico dello stomaco o della giunzione gastroesofagea. Per il presente kit, Codice nr. K5207, i volumi dei reagenti sono stati aggiustati specificatamente per l uso con lo strumento Autostainer. In questo documento, l'adenocarcinoma gastrico con giunzione gastroesofagea viene chiamato anche cancro gastrico. Per applicazione per cancro mammario, fare riferimento alle pagine Per applicazione per cancro gastrico, fare riferimento alle pagine Importante: si notino le differenze fra il tessuto di cancro alla mammella e il tessuto di cancro gastrico, specialmente all'interno delle sezioni di Interpretazione della colorazione. ( ) P04087IT_01_K / p. 4/55
5 Carcinoma mammario Cenni introduttivi - Mammella Dati di base Il gene umano HER2 (noto anche con le sigle ERBB2 o NEU) codifica una proteina che è generalmente denominata proteina HER2 o p185 HER2. La proteina HER2 è un recettore di transmembrana ad attività tirosin-chinasica con omologia per il recettore del fattore di crescita epidermico (EGFR o HER1) (1-8). La proteina HER2 è un componente normalmente espresso da numerosi tipi di cellule epiteliali (8). Una percentuale di pazienti con carcinoma mammario presenta una iperespressione della proteina HER2, come parte del processo di trasformazione maligna e di avanzamento del tumore (9). L iperespressione dell HER2 sulla superficie delle cellule di carcinoma mammario ha indicato la proteina come un possibile bersaglio nella terapia anticorpale. L Herceptin (trastuzumab) è un anticorpo monoclonale umanizzato 10 che presenta un elevata affinità di legame con la proteina HER2 e che, come si è dimostrato, è in grado di inibire la proliferazione delle cellule tumorali umane che iperesprimono la proteina HER2 sia in vitro sia in vivo (11-13). Caratteristiche Il test HercepTest è stato sviluppato allo scopo di fornire un alternativa al CTA investigativo utilizzato negli studi clinici con Herceptin. Le prestazioni del test HercepTest per quanto riguarda l iperespressione della proteina HER2 sono state valutate da uno studio indipendente, nel quale i risultati del test HercepTest sono stati comparati ai risultati del CTA su un totale di 548 campioni di tumore mammario, nessuno dei quali proveniente da pazienti coinvolte nella sperimentazione con Herceptin. I risultati dei due tipi di test eseguiti sugli stessi campioni hanno evidenziato una concordanza del 79%. In base ai dati sulla concordanza è inoltre possibile evidenziare l alta probabilità che una lettura 3+ con il test HercepTest corrisponda ad una lettura positiva con il CTA, ossia l ammissione alla sperimentazione (2+ o 3+). Non è stata invece stabilita una correlazione altrettanto chiara tra una lettura 2+ con il test HercepTest e i risultati del CTA. Nel 42% circa dei casi (53 su 126), le letture 2+ con il test HercepTest sono risultate negative con il CTA (0 1+), quindi i pazienti non sarebbero stati ammessi alla sperimentazione clinica con Herceptin. Il test HercepTest produce un risultato di negatività all iperespressione della proteina HER2 (intensità della colorazione 0 e 1+), un risultato di debole positività (intensità della colorazione 2+) e un risultato di forte positività (intensità della colorazione 3+). Il test HercepTest non è idoneo a fornire informazioni prognostiche al paziente e al medico e il suo impiego in questo senso non è stato approvato. Principio della procedura - Mammella HercepTest contiene i reagenti necessari per la completa esecuzione di una procedura di colorazione immunocitochimica a due fasi su campioni processati con i metodi convenzionali, inclusi in paraffina. Dopo l incubazione con l anticorpo primario di coniglio anti-proteina HER2 umana, il kit prevede l impiego di un Visualization Reagent pronto all uso, il quale sfrutta la tecnologia a base di destrano. Il reagente in questione è composto sia da molecole di immunoglobuline secondarie di capra anti-coniglio, sia da molecole di perossidasi di rafano, legate ad una comune catena principale di destrano. Questa tecnologia elimina la necessità di applicare in modo sequenziale un anticorpo di collegamento e un anticorpo coniugato con perossidasi. La reazione crociata del Visualization Reagent con le immunoglobuline umane e il siero fetale di vitello è stata rimossa mediante assorbimento in base solida. La conversione enzimatica del cromogeno aggiunto successivamente dà origine alla formazione di un prodotto di reazione visibile in corrispondenza dell antigene. A questo punto è possibile procedere alla colorazione di contrasto del campione e montare un vetrino coprioggetto. L interpretazione dei risultati avviene per mezzo di un microscopio ottico. Per convalidare le serie di colorazione vengono forniti vetrini di controllo contenenti tre linee cellulari di tumore della mammella umano, debitamente fissati in formalina e inclusi in paraffina, i quali esprimono tre gradi di ( ) P04087IT_01_K / p. 5/55
6 Carcinoma mammario intensità della colorazione: 0, 1+ e 3+. Vi è una correlazione tra l intensità della colorazione di queste linee cellulari e il numero di recettori presenti in ogni cellula. HercepTest, Codice nr. K5207, è indicato per la colorazione automatica con lo strumento Autostainer. Reagenti - Mammella Materiali forniti Il materiale elencato è sufficiente per effettuare 50 test (50 vetrini incubati con anticorpo primario anti-proteina HER2 e 50 vetrini incubati con il corrispondente reagente di controllo negativo). Il numero di test è calcolato in base all uso di 200 µl per sezione di tessuto (22 mm x 22 mm) di fiale n. 1, 2, 3 e 4 e della soluzione cromogeno-substrato (DAB). Il kit contiene materiale sufficiente per effettuare un massimo di 15 cicli di colorazione singoli. Fiala n. Quantità Descrizione 1 2 x 11 ml 2 1 x 12 ml 3 2 x 11 ml 4 1 x 12 ml 5 15 x 11 ml 6 3 x 3 ml 7 3 x 500 ml Reagente bloccante della perossidasi: Perossido di idrogeno 3% contenente sodio azide (NaN 3 ) 15 mmol/l. Anticorpo di coniglio anti-her2 umana: Anticorpo pronto all uso isolato per affinità. Viene fornito in Tris/HCl 0,05 mol/l; NaCl 0,1 mol/l; NaN 3 15 mmol/l; ph 7,2 e con proteina stabilizzante. Immunogeno: frammento sintetico C-terminale (parte intracitoplasmica) della proteina HER2 accoppiato a emocianina di patella. Specificità: proteina HER2. Metodo di purificazione: l anticorpo viene isolato per affinità utilizzando un peptide immobilizzato della proteina HER2. Reagente di visualizzazione: Polimero di destrano coniugato con perossidasi di rafano e immunoglobuline di capra anti-immunoglobuline di coniglio isolate per affinità. Viene fornito in tampone Tris/HCl contenente proteina stabilizzante e un agente antimicrobico. Reagente di controllo negativo: Frazione di immunoglobuline di siero di coniglio normale. Concentrazione della proteina equivalente alla concentrazione dell anticorpo anti-proteina HER2. Viene fornito in Tris/HCl 0,05 mol/l; NaCl 0,1 mol/l; NaN 3 15 mmol/l; ph 7,2 e con proteina stabilizzante. Substrato tamponato DAB: Soluzione tampone substrato, a ph 7,5, contenente perossido di idrogeno < 0,1%, stabilizzanti, enhancer e un agente antimicrobico. Cromogeno DAB: Soluzione cromogena contenente 3,3 -diaminobenzidina tetraidrocloruro (5%). Soluzione di smascheramento degli epitopi (Containing Detergent) (10x): Tampone citrato 0,1 mol/l con un detergente. ( ) P04087IT_01_K / p. 6/55
7 8 2 x 1 L 3 x 5 vetrini Carcinoma mammario Tampone di lavaggio (10x): tampone Tris/HCl contenente un detergente e un agente antimicrobico. Vetrini di controllo: Ogni vetrino contiene sezioni di tre linee cellulari di carcinoma mammario che sono state fissate in formalina e incluse in paraffina e che rappresentano livelli diversi di espressione della proteina HER2: MDA-231 (0), MDA-175 (1+) e SK-BR-3 (3+). I vetrini di controllo sono stati trattati termicamente per assicurare una maggiore aderenza delle sezioni al vetro. Se i vetrini vengono sottoposti ad ulteriori trattamenti termici per migliorare l aderenza delle sezioni al vetro, si corre il rischio di compromettere i risultati della colorazione. NOTA: tutti i reagenti, compresi la soluzione di smascheramento degli epitopi e il tampone di lavaggio, sono formulati specificatamente per l uso nell ambito di questo test. Per garantire la performance specificata del test, non effettuare alcuna sostituzione, fatta eccezione per il tampone di lavaggio, utilizzando eventualmente Dako Codice S3006. Materiali necessari ma non forniti Idrossido di ammonio, 15 mol/l, diluito a 37 mmol/l Colorante di contrasto: ematossilina, per esempio ematossilina di Mayer a base acquosa, Dako Codice S3301 (vedi ISTRUZIONI PER L USO, A.4) Vetrini coprioggetto Acqua distillata o deionizzata (acqua per lavaggio) Forno essiccante, in grado di mantenere una temperatura di 60 C o inferiore Etanolo, assoluto e al 95% Microscopio ottico (ingrandimento obiettivo 4 40x) Mezzo di montaggio, per esempio Dako Faramount, Codice S3025, oppure Glycergel, Codice C0563 Tessuti positivi e negativi da utilizzare come controlli di lavoro (vedere Controllo della qualità) Vetrini, SuperFrost Plus, polilisinati, oppure Dako Silanized Slides Codice S3003 (vedi Preparazione dei campioni) Vaschette o bagni per la colorazione Contaminuti (per intervalli di 2 40 minuti) Bagnomaria con coperchio (capace di mantenere la soluzione Epitope Retrieval Solution a C) Xilene, toluene o sostituti dello xilene K5207 è stato messo a punto per l uso con Autostainer Immunostaining System, Codice S3400. Fare riferimento alla Guida Autostainer per l utente per i componenti Autostainer necessari. Conservazione - Mammella Conservare a 2 8 C. Non utilizzare il kit dopo la data di scadenza stampata all esterno della confezione. Se i reagenti sono conservati in condizioni diverse da quelle specificate, l utente deve verificarne le condizioni (14a, 14b). Si fa presente che anche i vetrini di controllo devono essere conservati a 2 8 C. Non sono stati osservati segni evidenti che suggeriscano l instabilità di questo prodotto, pertanto è opportuno analizzare un controllo positivo e un controllo negativo insieme ai campioni dei pazienti. Se si dovesse osservare una colorazione inattesa non attribuibile a ( ) P04087IT_01_K / p. 7/55
8 Carcinoma mammario modifiche delle procedure di lavoro e si sospetta un problema relativo a HercepTest, contattare il Customer Support. Specimen preparation (Allestimento tessuto) - Mammella I campioni bioptici devono essere manipolati in modo da preservare il tessuto per la colorazione immunocitochimica. Adottare i metodi standard per il trattamento dei tessuti di tutti i campioni (15). Sezioni incluse in paraffina Sono idonei all uso tutti i tessuti conservati in formalina tamponata neutra o in fissativo di Bouin per i trattamenti di routine e l inclusione in paraffina. Ad esempio, i campioni bioptici devono essere bloccati in uno spessore di 3 o 4 mm e fissati per ore in formalina tamponata neutra. I tessuti vengono successivamente disidratati attraverso il passaggio in una serie di alcoli e in xilene e sottoposti ad infiltrazione di paraffina fusa ad una temperatura non superiore a 60 C. I tessuti che esprimono l HER2, quando ven gano sottoposti a fissazione e inclusione in modo corretto e siano conservati al fresco (15 25 C), preservano la loro morfologia a tempo indeterminato prima del taglio delle sezioni e del montaggio su vetrino (15, 16). Negli Stati Uniti, la norma 42 CFR (b) del Clinical Laboratory Improvement Act del 1988 prevede che i laboratori devono conservare i vetrini colorati per almeno dieci anni dalla data del saggio e devono altresì conservare blocchi di campioni per almeno due anni dalla data del saggio (16). I campioni di tessuto devono essere tagliati in sezioni di 4 5 µm, montati su vetrini e asciugati all aria a temperatura ambiente per un minimo di 12 ore (o fino all asciugatura) o a 37 C durante la notte o a 60 C per un ora. AVVISO: un calore eccessivo per più di un ora a 60 C può causare una diminuzione significativa o la perdita dell immunoreattività HER2 specifica associata alla membrana (17). Per preservare l antigenicità, le sezioni di tessuto già montate sui vetrini (SuperFrost Plus, Poly- L-lysine o vetrini silanizzati) dovranno essere sottoposte alla colorazione entro 4 6 settimane dal sezionamento se conservate a temperatura ambiente (20 25 C) (18). I vetrini da utilizzare per la valutazione della proteina HER2 e per la verifica della presenza di tumore devono essere preparati in contemporanea. Si consiglia di preparare almeno 5 vetrini: 1 per controllare la presenza tumorale, 2 per la valutazione della proteina HER2 (1 per l incubazione con la fiala n. 2 e 1 per l incubazione con la fiala n. 4) e 2 da conservare in caso di eventuali problemi. L uso di HercepTest TM su tessuti decalcificati non è stato validato e pertanto non viene raccomandato. Consultare la pubblicazione Dako intitolata Education Guide: Immunochemical Staining Methods (19) e i riferimenti bibliografici 15 e 16 per ulteriori informazioni sulla preparazione dei campioni. Trattamento dei campioni prima della colorazione Per conseguire un rendimento ottimale del test, è necessario utilizzare un metodo di recupero dell epitopo in tampone citrato 10 mmol/l. La soluzione idonea allo scopo è inclusa nel kit HercepTest. Questo metodo richiede il riscaldamento delle sezioni di tessuto montate su vetrini immerse in tampone citrato 10 mmol/l (20) a bagnomaria calibrato per mantenere la soluzione di smascheramento degli epitopi alla temperatura richiesta (95 99 C). I laboratori situati ad altitudini più elevate devono definire il metodo migliore per mantenere la temperatura richiesta del bagnomaria. Lo smascheramento dell epitopo deve essere eseguito a bagnomaria. Sono stati sperimentati altri metodi di riscaldamento, che tuttavia non hanno dato risultati riproducibili. Subito dopo lo smascheramento dell epitopo, iniziare la procedura di colorazione. Eventuali variazioni della procedura descritta potrebbero compromettere i risultati. ( ) P04087IT_01_K / p. 8/55
9 Precauzioni - Mammella 1. Per uso diagnostico in vitro. 2. Per uso professionale. Carcinoma mammario 3. Fiala 1, Peroxidase-Blocking Reagent, contiene 3% di perossido di idrogeno. Su richiesta è disponibile una scheda di sicurezza per utenti professionisti. 4. La fiala 6, il cromogeno DAB, contiene 5-<10% di 3,3 -diaminobenzidina tetracloridrato e riporta l etichetta: H350 H341 P201 P280 Pericolo P308 + P313 P405 P501 Può provocare il cancro. Sospettato di provocare alterazioni genetiche. Procurarsi istruzioni specifiche prima dell uso. Indossare guanti protettivi. Fare uso di un dispositivo di protezione degli occhi o del viso. Indossare indumenti protettivi. IN CASO di esposizione o di possibile esposizione: Richiedere assistenza medica. Conservare sotto chiave. Smaltire il prodotto e il recipiente in conformità a tutte le normative locali, regionali, nazionali e internazionali. Di norma, l utilizzo di questo prodotto non è consentito ai minori di 18 anni. Gli utenti devono essere accuratamente informati relativamente alla procedura di lavoro adeguata, alle proprietà pericolose del prodotto e alle istruzioni di sicurezza necessarie. Per ulteriori informazioni, fare riferimento alla scheda di sicurezza dei materiali (Safety Data Sheet, SDS) corrispondente. 5. La fiala 8, tampone di lavaggio, contiene 2-Amino-2-(hydroxymethyl)propane-1,3-diol hydrochloride e 0.1-<0.2% 5-bromo-5-nitro-1,3-diossano. Può indurre una reazione allergica. Wash Buffer (10x) è etichettato: Attenzione H319 P280 P264 P305 + P351 + P338 Provoca grave irritazione oculare. Proteggere gli occhi/il viso. Lavare accuratamente le mani dopo l'uso. IN CASO DI CONTATTO CON GLI OCCHI: sciacquare accuratamente per parecchi minuti. Togliere le eventuali lenti a contatto se è agevole farlo. Continuare a sciacquare. 6. Questo prodotto contiene sodio azide (NaN 3 ), una sostanza chimica fortemente tossica in forma pura. Sebbene non sia classificato come prodotto a rischio, la sodio azide alle concentrazioni indicate può reagire con il rame e il piombo delle tubature formando azidi metalliche fortemente esplosive. Per lo smaltimento del prodotto, è consigliabile sciacquare abbondantemente con acqua per evitare l accumulo di azidi metalliche nelle tubature (21, 22). 7. Le fiale 2, 3 e 4 contengono materiale di origine animale. Adottare le normali procedure previste per il trattamento dei prodotti di origine biologica. 8. I vetrini di controllo e i campioni, sia prima che dopo la fissazione, e tutti i materiali che entrano in contatto con essi devono essere trattati come materiali potenzialmente capaci di trasmettere un infezione, pertanto devono essere smaltiti assumendo tutte le precauzioni necessarie (23). Non pipettare mai i reagenti per bocca ed evitare che reagenti e campioni entrino in contatto con la pelle e le membrane mucose. In caso di contatto dei reagenti con zone sensibili, lavare la zona con abbondante acqua. ( ) P04087IT_01_K / p. 9/55
10 Carcinoma mammario 9. Ridurre al minimo la contaminazione microbica di reagenti per evitare una colorazione aspecifica. 10. Tempi, temperature e modalità di incubazione diversi da quelli specificati possono generare risultati erronei. Un asciugatura eccessiva per più di un ora a 60 C può causare una diminuzione significativa o la perdita dell immunoreattività HER2 specifica associata alla membrana (17). 11. I reagenti sono stati diluiti in modo ottimale. Ulteriori diluizioni potrebbero causare la perdita di colorazione antigenica. 12. Tutti i reagenti, compresi la soluzione di smascheramento degli epitopi e il tampone di lavaggio, sono formulati specificatamente per l uso nell ambito di questo test. Per garantire la performance indicata per il test, non effettuare alcuna sostituzione, fatta eccezione per il tampone di lavaggio, usando eventualmente Dako Codice S Il Visualization Reagent e il cromogeno DAB possono essere danneggiati dall esposizione a livelli di luce eccessivi. Non conservare i componenti del kit e non eseguire la colorazione in condizioni di luce intensa, ad esempio sotto la luce diretta del sole. 14. Indossare indumenti di protezione personale adeguati, per evitare il contatto con gli occhi e la pelle. Per ulteriori informazioni, fare riferimento alla scheda di sicurezza dei materiali (Material Safety Data Sheet, MSDS) corrispondente. 15. Residui di paraffina possono generare risultati falsi negativi. 16. L uso di volumi di reagente diversi da quelli raccomandati può comportare la perdita di immunoreattività HER2 visibile. Sezioni di tessuto maggiori di 22 mm x 22 mm richiedono l applicazione di 2-3x 200 µl di reagente in 2-3 aree di applicazione automatizzata. ISTRUZIONI PER L USO - Mammella Preparazione Per ragioni di praticità, prima di procedere alla colorazione è opportuno preparare i reagenti elencati di seguito: A.1 Epitope Retrieval Solution Diluire una quantità sufficiente della fiala 7 (Epitope Retrieval Solution x 10) 1:10 utilizzando acqua distillata o deionizzata per la procedura di colorazione pianificata. La soluzione diluita inutilizzata può essere conservata a 2 8 C per un mese. Elimina re la soluzione diluita se appare torbida. A.2 Tampone di lavaggio Diluire una quantità sufficiente di fiala 8 (tampone di lavaggio 10x) 1:10 con acqua distillata o deionizzata per le fasi di lavaggio. Il tampone diluito inutilizzato può essere conservato a 2 8 C per un mese. Eliminare la soluzione tampone se appare torbida. Lo strumento Autostainer è programmato per sciacquare le sezioni di tessuto dopo il trattamento con il reagente bloccante della perossidasi e con la soluzione substrato-cromogeno. Si fa presente che per queste fasi di lavaggio si può utilizzare acqua distillata (o deionizzata) o tampone di lavaggio. Tutte le altre fasi di lavaggio richiedono l utilizzo di tampone di lavaggio. A.3 Soluzione cromogeno-substrato (DAB) Preparare la soluzione cromogeno-substrato aggiungendo 11 gocce (25 30 µl per goccia) di cromogeno DAB dalla fiala 6 ad una fiala 5 contenente tampone substrato DAB (11 ml), quindi miscelare. La soluzione substrato-cromogeno (DAB) così preparata è stabile per circa 5 giorni se conservata a 2 8 C. La soluzione deve essere ag itata bene prima dell uso. La comparsa di qualsiasi precipitato all interno della soluzione non ne altera la qualità di colorazione. NOTA: il colore del cromogeno DAB nella fiala 6 può variare da trasparente a viola chiaromarrone. Questa caratteristica non altera il rendimento del prodotto. Diluire secondo le linee guida contenute nel presente foglietto illustrativo. L aggiunta in eccesso di DAB Chromogen al DAB Buffered Substrate può determinare un deterioramento del segnale positivo. ( ) P04087IT_01_K / p. 10/55
11 A.4 Colorazione di contrasto Carcinoma mammario Il prodotto finale della reazione di colorazione DAB è insolubile in alcol e in acqua. Utilizzare una controcolorazione con ematossilina e aggiustare l intensità di colorazione dell ematossilina ad un livello simile a quello riportato nel manuale di interpretazione dell'herceptest per il carcinoma mammario di Dako ( HercepTest Interpretation Manual Breast Cancer ). Per questa fase si può utilizzare ematossilina, a base alcolica o a base acquosa, per esempio ematossilina di Mayer Dako, Codice S3301. Successivamente alla controcolorazione con ematossilina, sciacquare in acqua distillata o deionizzata e quindi immergere i vetrini con i tessuti in un bagno acqua-ammoniaca 37 mmol/l (vedi sezione B.2, fase 3). La soluzione acquaammoniaca (37mmol/L) viene preparata mescolando 2,5 ml di idrossido di ammonio 15 mol/l (concentrato) con 1 L di acqua distillata o deionizzata. La soluzione ammoniacale 37 mmol/l inutilizzata può essere conservata in un flacone perfettamente sigillato a temperatura ambiente (20 25 C) per 12 mesi. A.5 Mezzo di montaggio Si consiglia di usare un mezzo di montaggio permanente e non acquoso. Tuttavia è accettabile anche un montaggio acquoso. Per il montaggio acquoso, si raccomanda l uso di Dako Faramount Aqueous Mounting Medium, pronto per l uso, Codice S3025, oppure Glycergel Mounting Medium, Codice C0563. Liquefare Glycergel riscaldando a circa 40 (±5) C prima dell uso. B. Procedura di colorazione su Autostainer B.1 Note sulla procedura Prima dell uso, si consiglia di leggere attentamente le istruzioni fornite di seguito e studiare le caratteristiche di tutti i componenti (vedere Precauzioni). Tutti i reagenti devono essere equilibrati a temperatura ambiente (20 25 C) prima dell immunocolorazione. Analogamente, tutte le fasi di incubazione devono svolgersi a temperatura ambiente. Non lasciare andare a secchezza le sezioni tissutali durante il caricamento su Autostainer e durante la procedura di colorazione. Le sezioni di tessuto secche possono presentare una maggiore colorazione aspecifica. Se la procedura di colorazione viene interrotta, è possibile conservare i vetrini in un bagno tampone dopo l incubazione dell anticorpo primario, per non più di un ora a temperatura ambiente (20 25 C), senza ripercussioni sui risult ati della colorazione. Sparaffinatura e reidratazione: prima della colorazione, i vetrini contenenti i tessuti devono essere deparaffinati per rimuovere il mezzo di inclusione e successivamente reidratati. Evitare la rimozione incompleta della paraffina. La presenza di eventuali residui del mezzo di inclusione può provocare un aumento della colorazione aspecifica. Questa operazione deve essere eseguita a temperatura ambiente (20 25 C). 1. Immergere i vetrini in un bagno di xilene e incubare per 5 (±1) minuti. Cambiare il bagno e ripetere il procedimento. 2. Picchiettare i vetrini per eliminare il liquido in eccesso e immergerli in etanolo assoluto per 3 (±1) minuti. Cambiare il bagno e ripetere il procedimento. 3. Eliminare l eccesso di liquido picchiettando i vetrini e immergerli in etanolo al 95% per 3 (±1) minuti. Cambiare il bagno e ripetere il procedimento. 4. Picchiettare per eliminare il liquido in eccesso e immergere i vetrini in acqua distillata o deionizzata per almeno 30 secondi. Iniziare la procedura di colorazione come descritto nella sezione B.2, fase 1, smascheramento degli epitopi. Soluzioni alcoliche e allo Xilene devono essere cambiate dopo 40 vetrini. Al posto dello xilene è possibile utilizzare i derivati di toluene o xilene, ad esempio Histoclear. NOTA: le istruzioni e i reagenti forniti in questo kit sono stati studiati per assicurare prestazioni ottimali. L ulteriore diluizione dei reagenti o una variazione delle temperature di incubazione ( ) P04087IT_01_K / p. 11/55
12 Carcinoma mammario potrebbero generare risultati erronei o discordanti. Le differenze che esistono tra i laboratori (per quanto riguarda il modo di trattare il tessuto o di eseguire le procedure tecniche) possono compromettere la validità dei risultati del test in quanto strumento di selezione dei pazienti idonei alla terapia con Herceptin. B.2 Protocollo di colorazione Eseguito a temperatura ambiente, C. Fase 1: Recupero dell epitopo Riempire le vaschette per la colorazione, p. es. vaschette di Coplin, con la soluzione di smascheramento degli epitopi diluita (vedi ISTRUZIONI PER L USO, sezione A.1). Immergere in un bagnomaria le vaschette contenenti la soluzione Epitope Retrieval Solution. Riscaldare bagnomaria e soluzione di smascheramento a C. Durante il riscaldamento, la soluzione Epitope Retrieval Solution assume un aspetto torbido. Coprire le vaschette con i rispettivi coperchi per stabilizzare la temperatura ed evitare l evaporazione. Immergere le sezioni deparaffinate a temperatura ambiente nelle vaschette con la soluzione Epitope Retrieval Solution precedentemente riscaldata. RIPORTARE LA TEMPERATURA DI BAGNOMARIA E SOLUZIONE DI SMASCHERAMENTO A C. Incubare per 40 (±1) minuti a C. Rimuovere tutta la vaschetta con i vetrini dal bagnomaria. Lasciare raffreddare i vetrini nella soluzione di smascheramento degli epitopi per 20 (±1) minuti a temperatura ambiente. Decantare la soluzione di smascheramento e risciacquare le sezioni con tampone di lavaggio diluito (vedi ISTRUZIONI PER L USO, sezione A.2). Per un risultato ottimale, immergere le sezioni in tampone di lavaggio per 5 20 minuti dopo lo smascheramento degli epitopi e prima della colorazione. NOTA: la soluzione Epitope Retrieval Solution è un prodotto monouso, idoneo a una sola applicazione. Non riutilizzare. Fase 2: Procedura Autostainer 1. Utilizzare la mappa generata da Autostainer sull autoprogramma HercepTest per conoscere i tempi del programma e i volumi dei reagenti (vedi il successivo punto 4 per informazioni sui volumi specifici). 2. Inserire le fiale per reagenti Autostainer nel raccoglitore portareagenti Autostainer conformemente alla mappa dei reagenti generata dal computer. 3. Caricare i vetrini sullo strumento Autostainer conformemente alla mappa dei vetrini generata dal computer. 4. Impostare il programma e iniziare il programma HercepTest. Qui di seguito viene riportata una descrizione dell esecuzione del programma: Risciacquare 200 µl di Peroxidase-Blocking Reagent - 5 minuti Risciacquare 200 µl di anticorpo primario anti-proteina HER2 (o reagente di controllo negativo) - 30 minuti Risciacquare 200 µl di Visualization Reagent - 30 minuti Risciacquare Risciacquare Cambiare ( ) P04087IT_01_K / p. 12/55
13 200 µl di soluzione cromogeno-substrato (DAB) - 10 minuti Carcinoma mammario Lavare i vetrini in acqua deionizzata dopo il passaggio con soluzione cromogeno-substrato NOTA: la versione 01 dell apparecchiatura Autostainer lava i vetrini nel tampone. Pertanto i vetrini devono essere lavati con acqua deionizzata dopo essere stati rimossi dall Autostainer. Fase 3: Colorazione di contrasto (le istruzioni si riferiscono all ematossilina) Estrarre i vetrini dall Autostainer e controcolorare in ematossilina come descritto qui di seguito. Immergere i vetrini in un bagno di ematossilina. Incubare per 2 5 minuti, a seconda dell intensità dell ematossilina utilizzata. Lavare delicatamente in un bagno di acqua distillata o deionizzata. Assicurarsi che tutta l ematossilina residua sia stata eliminata. Opzionalmente, è possibile immergere i vetrini 10 volte in un bagno di soluzione acquaammoniaca 37 mmol/l (vedi sezione A.4). Lavare delicatamente i vetrini in un bagno di acqua distillata o deionizzata per 2 5 minuti. NOTA: a seconda della durata dell incubazione o della potenza dell ematossilina impiegata, la colorazione di contrasto può produrre un blu più o meno scuro nel nucleo della cellula. Una colorazione di contrasto eccessiva o incompleta può compromettere l interpretazione dei risultati. Fase 4: Montaggio Si consiglia di usare un mezzo di montaggio permanente e non acquoso. Diversamente, è accettabile anche un mezzo di montaggio acquoso. I campioni possono essere montati e coperti con vetrini coprioggetto utilizzando un mezzo di montaggio a base acquosa come Dako Faramount, Codice S3025, oppure Glycergel, Codice C0563. NOTA: è possibile leggere i vetrini in qualunque momento. È tuttavia possibile che si verifichi un certo grado di scolorimento se i vetrini vengono coperti con un mezzo di montaggio acquoso e vengono esposti alla luce intensa per un periodo di una settimana. Per evitare che ciò accada, conservare i vetrini al buio a temperatura ambiente (20 25 C). Controllo di qualità - Mammella Se le procedure consigliate per la fissazione, il trattamento e l inclusione dei tessuti vengono modificate in laboratorio, è possibile che i risultati presentino una certa variabilità. n tal caso, oltre ad utilizzare i vetrini di controllo forniti da Dako, occorre effettuare tutta una serie di controlli interni con regolarità. Negli Stati Uniti, consultare le linee guida sul controllo di qualità del College of American Pathologists (CAP) Certification Program for Immunohistochemistry e vedere altresì il documento CLSI (precedentemente NCCLS) Quality Assurance for Immunocytochemistry, Approved Guideline (24) e il riferimento 25 per ulteriori informazioni. Tabella 1. L obiettivo del controllo di qualità quotidiano. Tessuto: fissato e trattato come il campione del paziente Controllo positivo: tessuti o cellule che contengono l antigene bersaglio da individuare (potrebbe essere presente nel tessuto del paziente). Il controllo ideale è un tessuto con una colorazione positiva debole, in quanto è più sensibile al deterioramento dell anticorpo o Anticorpo specifico e anticorpo secondario Controllo di tutte le fasi dell analisi. Convalida delle procedure e dei reagenti utilizzati per la colorazione HER2. Anticorpo non specifico* o tampone + anticorpo secondario come utilizzato con l anticorpo specifico Rilevamento della colorazione di fondo aspecifica. ( ) P04087IT_01_K / p. 13/55
14 Carcinoma mammario dell antigene. Controllo negativo: tessuto o cellule che si presume negativi (potrebbero trovarsi nel tessuto del paziente o nel tessuto di controllo positivo). Rilevamento di una reattività crociata indesiderata dell anticorpo rispetto alle cellule e/o ai componenti cellulari. Rilevamento della colorazione di fondo aspecifica. Tessuto del paziente Rilevamento della colorazione specifica. Rilevamento della colorazione di f ondo aspecifica. Vetrino di controllo fornito da Dako Controllo della sola procedura di colorazione. * Siero proveniente dalla stessa specie dell anticorpo specifico, ma non diretto contro lo stesso antigene bersaglio. Per individuare legami aspecifici con l anticorpo, ad es. legame della porzione Fc dell anticorpo ad opera del tessuto. ( ) P04087IT_01_K / p. 14/55
15 Carcinoma mammario Vetrino di controllo (fornito): tutti i vetrini di controllo forniti nel kit contengono tre linee cellulari umane pellettizzate, fissate in formalina e incluse in paraffina, con valori di intensità di colorazione pari a 0, 1+ e 3+. È necessario utilizzare un vetrino in ogni procedura di colorazione. Valutando le linee cellulari sul vetrino di controllo fornito da Dako è possibile verificare la validità della procedura di colorazione. Tessuto di controllo positivo: i controlli dovrebbero essere costituiti da campioni freschi di autopsia/biopsia/chirurgia che sono stati fissati, trattati e inclusi in paraffina nei tempi più brevi possibili, seguendo la medesima procedura utilizzata per i campioni dei pazienti da analizzare. I controlli positivi confermano se i tessuti sono stati preparati correttamente e se sono state adottate tecniche di colorazione corrette. È necessario includere un tessuto di controllo positivo per ogni set di condizioni di analisi previsto in ogni ciclo di colorazione. I controlli positivi devono produrre una colorazione positiva debole, così da evidenziare variazioni leggere nella sensibilità dell anticorpo primario. Se trattati diversamente dai campioni dei pazienti, i vetrini di controllo di questo kit o i campioni consentono di convalidare soltanto il rendimento del reagente, ma non di verificare la preparazione del tessuto. Come tessuto di controllo positivo ideale è possibile utilizzare un campione di carcinoma mammario umano invasivo (infiltrante) con iperespressione di proteina HER2 che abbia prodotto un risultato di positività 2+ in un test precedente. NOTA: i controlli positivi noti devono essere utilizzati esclusivamente per verificare il corretto rendimento dei tessuti trattati e dei reagenti per analisi, NON per formulare una diagnosi specifica dei campioni dei pazienti. Se i controlli positivi non producono una colorazione positiva, significa che i risultati ottenuti con i campioni dei pazienti analizzati non sono da ritenersi validi. Tessuto di controllo negativo: in ogni ciclo di colorazione è necessario utilizzare un tessuto di controllo negativo (negativo alla proteina HER2) che sia stato fissato, trattato e incluso in paraffina secondo la medesima procedura adottata per i campioni dei pazienti da analizzare. In questo modo è possibile verificare la specificità dell anticorpo primario e fornire un indicazione della colorazione di fondo specifica. Il colon, il fegato e la tiroide sono idonei ad essere impiegati come tessuti di controllo negativi. Molteplici tipi di cellule presenti nella maggior parte delle sezioni tissutali offrono siti interni di controllo negativo (è necessaria una verifica dell utente). I dotti mammari normali possono fungere da controlli negativi interni. Se si osserva una colorazione specifica nel tessuto di controllo negativo o nel sito di controllo interno, significa che i risultati ottenuti con i campioni dei pazienti analizzati non sono da ritenersi validi. Reagente di controllo negativo non specifico: al posto dell anticorpo primario, è possibile utilizzare il reagente di controllo negativo (fornito nel kit) su una sezione di ogni campione con lo scopo di valutare la colorazione aspecifica e favorire l interpretazione della colorazione specifica nel sito dell antigene. Il periodo di incubazione del reagente di controllo negativo deve corrispondere a quello dell anticorpo primario. Verifica del saggio: prima di utilizzare un anticorpo o un sistema di colorazione in una procedura diagnostica, l utente deve verificare la specificità dell anticorpo analizzandolo su una serie di tessuti archiviati con note caratteristiche di performance immunocitochimica, che rappresentano tessuti positivi o negativi noti. Fare riferimento alle procedure sul controllo della qualità descritte in questa sezione del foglietto illustrativo e ai requisiti descritti nelle istruzioni CAP Certification Program for Immunohistochemistry e/o CLSI (precedentemente NCCLS) Quality Assurance for Immunocytochemistry, Approved Guideline (24). Le procedure per il controllo della qualità vanno ripetute per ogni nuovo lotto di anticorpi o tutte le volte che viene apportata una modifica ai parametri del saggio. Per la verifica del saggio, sono adatti i carcinomi mammari con intensità di colorazione della proteina HER2 nota nella scala 0-3+ e i tessuti negativi, p.e. colon, fegato o tiroide. ( ) P04087IT_01_K / p. 15/55
16 Carcinoma mammario Interpretazione della colorazione - Mammella Ai fini della determinazione dell iperespressione di proteina HER2, si devono valutare solo il pattern e l intensità della colorazione della membrana, facendo riferimento alla scala dei valori illustrata nella Tabella 2. La valutazione dei vetrini deve essere effettuata da un patologo qualificato, con un microscopio ottico. Per la valutazione della colorazione immunocitochimica e l assegnazione di un punteggio, occorre utilizzare un obiettivo con ingrandimento 10x. Per confermare il punteggio è utile un obiettivo 20 40x. La colorazione citoplasmatica deve essere considerata non specifica e non deve essere inclusa nell accertamento dell intensità di colorazione della membrana (8). Per indicazioni nella differenziazione dei valori di colorazione 0, 1+, 2+ e 3+, fare riferimento alle figure rappresentative di intensità di colorazione riportate nel manuale di interpretazione dell'herceptest per il carcinoma mammario di Dako. Limitare la valutazione ai soli campioni provenienti da pazienti affette da carcinoma mammario invasivo. In caso di carcinoma in situ e carcinoma invasivo presenti nello stesso campione, assegnare un punteggio al solo componente invasivo. Tabella 2. Criteri di intensità di colorazione della membrana cellulare. Pattern di colorazione Colorazione assente o colorazione della membrana in meno del 10% delle cellule tumorali. Colorazione appena percettibile/debole della membrana in oltre il 10% delle cellule tumorali. Le cellule si colorano solo in una parte della membrana. Colorazione completa, da debole a moderata, della membrana in oltre il 10% delle cellule tumorali. Colorazione completa, forte, della membrana in oltre il 10% delle cellule tumorali. Punteggio (riferire al medico curante) Proteina HER2 Valutazione iperespressione (riferire al medico curante) Negativi Negativi Positiva debole Positiva forte Il test HercepTest produce un risultato di negatività all iperespressione della proteina HER2 (intensità della colorazione 0 e 1+), un risultato di debole positività (intensità della colorazione 2+) e un risultato di forte positività (intensità della colorazione 3+). Il test HercepTest non è idoneo a fornire informazioni prognostiche al paziente e al medico e il suo impiego in questo senso non è stato approvato. Ad ogni ciclo di colorazione, è importante esaminare i vetrini in una sequenza specifica (vedere Tabella 3), in modo da poter determinare la validità della sessione di analisi ed effettuare una valutazione semiquantitativa dell intensità della colorazione del tessuto campione. ( ) P04087IT_01_K / p. 16/55
17 Carcinoma mammario Tabella 3. Ordine di valutazione dei vetrini. Ordine di lettura dei vetrini Logica 1. Vetrino di controllo contenente le tre linee cellulari Un saggio valido è indicato dalla presenza di colorazione marrone 3+ della membrana cellulare (orletto) nella linea cellulare di controllo 3+ SK-BR-3, di orletto parziale marrone nella linea cellulare MDA-175 di controllo 1 + e da assenza di colorazione nella linea cellulare di controllo 0 MDA-231. Una colorazione della membrana discontinua e puntiforme è presente in un numero da piccolo a moderato di cellule nella linee cellulare di controllo 1 + debolmente positiva. In questa linea cellulare si può anche osservare una immunocolorazione puntiforme nella regione dei Golgi del citoplasma. Presenza di colorazione marrone nella linea cellulare di controllo 0 (Control Cell Line MDA-231), ovvero negatività alla proteina HER2. Indica che non c è stata colorazione aspecifica durante il test. I risultati del saggio possono essere non validi a causa di eccessiva colorazione. 2. Vetrino con il tessuto di controllo positivo Possibile presenza di colorazione marrone della membrana. La colorazione del citoplasma e dei tessuti negativi non deve essere superiore a Vetrino con il tessuto di controllo negativo L ASSENZA di colorazione specifica nel tessuto di controllo negativo conferma l assenza di reattività crociata con cellule/componenti cellulari. In caso di colorazione specifica di membrana nel vetrino del tessuto di controllo negativo, i risultati ottenuti con i campioni dei pazienti devono essere considerati non validi. 4. Vetrino con il tessuto del paziente, colorato con il reagente di controllo negativo 5. Vetrino con il tessuto del paziente, colorato con l anticorpo primario L assenza di colorazione di membrana specifica conferma la marcatura specifica dell antigene bersaglio da parte dell anticorpo primario. Una ulteriore colorazione marrone nel citoplasma del campione trattato con il reagente di controllo negativo, come per esempio nel tessuto connettivo, nei leucociti, negli eritrociti o nel tessuto necrotico, deve essere considerata come una colorazione di fondo non specifica e deve essere riportata nella sezione dei commenti del foglio dei dati. L iperespressione della proteina HER2 nel campione si manifesta come un orletto marrone localizzato sulla membrana cellulare delle cellule tumorali trattate con l anticorpo primario. 1. Vetrino di controllo (fornito): il primo vetrino di controllo da analizzare è quello sottoposto a colorazione con HercepTest, il quale consente di verificare il corretto funzionamento di tutti i reagenti. La presenza di un prodotto della reazione di colore marrone (3,3 -diaminobenzidina, DAB) in corrispondenza della membrana cellulare indica reattività positiva. Un test valido è confermato da: presenza di colorazione marrone (rimming) nella circonferenza della membrana cellulare per quanto riguarda la linea cellulare di controllo 3+ (Control Cell Line SK-BR-3); rimming parziale marrone per quanto riguarda la linea cellulare di controllo 1+ (Control Cell Line MDA-175); colorazione assente per quanto riguarda la linea cellulare di controllo 0 (Control Cell Line MDA-231). Se anche una sola delle linee cellulari di controllo fornite produce risultati che esulano dai criteri descritti, tutti i risultati ottenuti con i campioni dei pazienti sono da ritenersi non validi. 2. Tessuto di controllo positivo: il secondo vetrino da analizzare è quello con il tessuto di controllo positivo. Questo vetrino consente di verificare l efficacia del metodo di fissazione e del processo di recupero dell epitopo. Per l interpretazione dei risultati della colorazione, prendere in considerazione le cellule intatte, in quanto le cellule necrotiche o degradate assumono spesso una colorazione aspecifica (26). La colorazione del tessuto tumorale deve essere marrone e interessare la membrana cellulare. Il citoplasma e i tessuti negativi all interno del campione possono colorarsi di marrone, tuttavia l intensità di questa colorazione non deve superare il punteggio 1+. ( ) P04087IT_01_K / p. 17/55
18 Carcinoma mammario 3. Tessuto di controllo negativo: il vetrino del tessuto di controllo negativo deve essere analizzato dopo il tessuto di controllo positivo per verificare la specificità della marcatura dell antigene ricercato da parte dell anticorpo primario. L assenza di colorazione specifica nel tessuto di controllo negativo conferma l assenza di reattività crociata del kit con cellule/componenti cellulari. Se si osserva una colorazione specifica nel tessuto di controllo negativo, i risultati ottenuti con i campioni dei pazienti analizzati non sono da ritenersi validi. In alternativa, è possibile utilizzare alcune di queste porzioni negative nel tessuto di controllo positivo a mo di controlli negativi (è necessaria una verifica dell utente). Si fa presente che si può osservare una reazione debole (intensità di colorazione 0-1+) nella maggior parte del tessuto epiteliale normale. Possono essere impiegati come tessuti di controllo negativi il colon, il fegato e la tiroide. Se è presente, la colorazione aspecifica apparirà piuttosto diffusa. È possibile osservare anche la colorazione sporadica del tessuto connettivo nelle sezioni sottoposte ad eccessiva fissazione in formalina Tessuto del paziente: in ultimo esaminare i campioni dei pazienti sottoposti a colorazione con HercepTest. L intensità della colorazione positiva deve essere valutata tenendo conto di possibili colorazioni di fondo aspecifiche ad opera del reagente di controllo negativo. Come accade per tutti gli esami immunocitochimici, un risultato negativo significa che l antigene ricercato non è stato trovato, ma non significa che l antigene non è presente nelle cellule e nei tessuti analizzati. Per informazioni specifiche sulla immunoreattività del test HercepTest, vedere i paragrafi Cenni introduttivi, Limiti e Caratteristiche prestazionali. Altri suggerimenti per interpretare correttamente i risultati della colorazione con HercepTest La maggioranza dei carcinomi mammari sottoposti a test per individuare l iperespressione della proteina HER2 totalizza 0 oppure 3+ punti. Mentre nella stragrande maggioranza dei casi l interpretazione è chiara, in una piccola percentuale residua di casi i campioni ottengono punteggi 1+ e 2+ e sono più difficili da classificare. Per l interpretazione della colorazione con HercepTest in laboratorio, è possibile attenersi alle seguenti linee guida. Valutare sempre le linee cellulari di controllo per convalidare il rendimento del test. Valutare sia i vetrini di controllo positivi, sia i vetrini di controllo negativi. Si consiglia di colorare i campioni dei tessuti con ematossilina ed eosina (H&E), almeno per la prima valutazione. (La ragione è che il tumore potrebbe non essere evidente ad una prima osservazione del campione colorato con HercepTest. Il vetrino colorato con ematossilina - eosina serve al patologo per verificare la presenza del tumore.). HercepTest TM deve essere eseguito su una sezione appaiata (sezione seriale) proveniente dallo stesso blocco di paraffina del campione. Valutare la presenza di iperespressione della proteina HER2 nelle sezioni utilizzando prima un ingrandimento basso: La maggior parte dei casi positivi è già evidente con un ingrandimento basso. Per determinare la percentuale di cellule tumorali positive, scegliere le aree del campione meglio conservate e colorate. Di regola, il punteggio da attribuire ai casi dovrebbe risultare ovvio ad un ingrandimento basso. In caso di dubbio tra i punteggi 1+ e 2+ con un ingrandimento basso, in genere il punteggio è 1+. Per verificare la colorazione della membrana, usare un fattore di ingrandimento 20 40x. Se si è colorata la membrana nella maggioranza delle cellule tumorali, il punteggio è 2+ o 3+. Per confermare il valore, usare un ingrandimento 20 40x. ( ) P04087IT_01_K / p. 18/55
19 Carcinoma mammario Nella maggior parte dei casi con punteggio 3+, si colora almeno l 80% delle cellule tumorali e la colorazione della membrana è intensa. Se un campione è vicino al limite soglia per quanto riguarda la percentuale di cellule tumorali positive (10%), si consiglia di contare almeno 100 cellule tumorali e determinare la percentuale esatta di cellule che si sono colorate. Se la membrana cellulare si è colorata completamente con un intensità debolemoderata in più del 10% delle cellule tumorali, il punteggio da assegnare al campione è 2+. Contestualmente si osserva in genere la colorazione incompleta della membrana nella maggior parte delle restanti cellule tumorali. Se la colorazione della circonferenza della membrana è completa in meno del 10% delle cellule tumorali, il punteggio è 1+ (anche se nelle altre cellule tumorali si osserva una colorazione incompleta della membrana). Se la percentuale di cellule tumorali con una colorazione circonferenziale della membrana completa o incompleta è inferiore al 10%, il punteggio è 0. Limitazioni - Mammella Limiti generali 1. L immunocitochimica è una tecnica diagnostica multifase che richiede un addestramento specifico per quanto riguarda la scelta dei reagenti appropriati, la selezione, la fissazione e il trattamento dei tessuti, la preparazione del vetrino per l analisi immunocitochimica e l interpretazione dei risultati della colorazione. 2. La colorazione del tessuto dipende dal modo in cui il tessuto viene pretrattato. Una fissazione eseguita in maniera scorretta, il congelamento, lo scongelamento, il lavaggio, l essiccazione, il riscaldamento, il sezionamento o la contaminazione con altri tessuti o fluidi possono produrre artefatti, intrappolare l anticorpo o generare risultati falsi-negativi. Risultati incoerenti possono essere provocati anche da modifiche apportate ai metodi di fissazione e di inclusione o da irregolarità intrinseche del tessuto. 3. Una colorazione di contrasto eccessiva o incompleta può compromettere l interpretazione dei risultati. 4. L interpretazione clinica di qualsiasi colorazione positiva o assenza di colorazione non può prescindere dal contesto della presentazione clinica, della morfologia e di altri criteri istopatologici L interpretazione clinica di qualunque colorazione o della sua assenza deve essere completata da studi morfologici e da controlli adeguati nonché da altri test diagnostici. L interpretazione della colorazione è compito di un patologo qualificato, che deve avere una profonda conoscenza degli anticorpi, dei reagenti e dei metodi impiegati. La colorazione deve essere eseguita in un laboratorio autorizzato certificato, sotto la supervisione di un patologo, il quale esaminerà i vetrini colorati e garantirà la correttezza dei controlli positivi e negativi. 5. I tessuti delle persone infette dal virus dell epatite B e contenenti l antigene di superficie dell epatite B (HBsAg) possono essere interessati da una colorazione aspecifica con la perossidasi di rafano (27). 6. I reagenti potrebbero provocare reazioni impreviste in tipi di tessuto mai analizzati in passato. Inoltre non è escluso che possano verificarsi reazioni impreviste anche in tipi di tessuti già analizzati in passato, vista l elevata variabilità biologica dell espressione antigenica nelle neoplasie o in altri tessuti patologici (28). In caso di reazioni inattese documentate, contattare il Customer Support di Dako. 7. È possibile ottenere falsi positivi a causa del legame non immunologico di proteine o di prodotti di reazione del substrato. Falsi positivi possono essere causati anche ( ) P04087IT_01_K / p. 19/55
20 Carcinoma mammario dall attività della pseudoperossidasi (eritrociti) e dall attività della perossidasi endogena (citocromo C) (28). 8. La procedura di colorazione deve essere eseguita a temperatura ambiente (20 25 C). Limiti specifici del prodotto 1. L antigene presente nella linea cellulare di controllo 1+ (Control Cell Line MDA-175) è destinato a degradarsi nel tempo. Valutare i risultati del vetrino di controllo tenendo conto della data di scadenza del vetrino. La colorazione negativa delle cellule MDA-175 potrebbe indicare soltanto che il vetrino di controllo si è deteriorato. Conservare i vetrini di controllo a 2 8 C. 2. Il deterioramento dell antigene nel tessuto, nel tempo, può provocare risultati falsi-negativi. I campioni devono essere colorati entro 4 6 settimane dal montaggio dei tessuti sui vetrini, quando sono conservati a temperatura ambiente (20 25 C) (29). 3. Per ottenere risultati ottimali e riproducibili, la proteina HER2 richiede lo smascheramento termoindotto degli epitopi quando i tessuti sono fissati secondo i metodi convenzionali (formali tamponata neutra o fissativo di Bouin) e inclusi in paraffina. Questo pretrattamento deve essere completato all inizio dell intero processo di colorazione. Per ulteriori istruzioni, consultare la sezione Preparazione dei campioni, Trattamento dei tessuti prima della colorazione. 4. Per lo smascheramento termoindotto degli epitopi della proteina HER2, impiegare solamente un bagnomaria calibrato. Sono stati sperimentati altri metodi di riscaldamento, che tuttavia non hanno dato risultati riproducibili. 5. Non sostituire i reagenti del kit con reagenti che abbiano numeri di lotto diversi, né con reagenti di altri produttori. La sola eccezione riguarda il tampone di lavaggio, che può essere sostituito da DakoCytomation Wash Buffer, cod. n. S Dalla valutazione della colorazione del citoplasma si possono ottenere risultati falsi. Ai fini dell interpretazione della colorazione, tenere conto esclusivamente della colorazione della membrana cellulare. 7. I vetrini di controllo che si colorano servono esclusivamente per verificare la validità del ciclo di colorazione e non devono essere impiegati per assegnare un punteggio alla colorazione delle sezioni di tessuto. 8. Di tanto in tanto è possibile che si formino i cosiddetti hot spot, ovvero punti circoscritti con una colorazione focale intensa (3+). La presenza di questi hot spot potrebbe essere dovuta ad una procedura di fissazione e/o trattamento del tessuto non uniforme. In questi casi, si consiglia di procedere all immunocolorazione di un secondo blocco di tessuto appartenente allo stesso campione. 9. Non è stato approvato l uso del test HercepTest su campioni trattati con fissativi diversi dalla formalina tamponata neutra o dal fissativo di Bouin. 10. Il punteggio ottenuto dall epitelio mammario normale deve essere 0 o 1+. Se l epitelio normale ottiene un punteggio superiore a 1+, ripetere il test. Gli epiteli normali di tonsille ed esofago possono colorarsi con un intensità fino a 2+. Caratteristiche prestazionali - Mammella Dati di base Lo studio clinico (CTA) mirato ad individuare i pazienti idonei alla sperimentazione clinica con Herceptin era stato messo a punto per scopi di ricerca e non è più disponibile. Il test HercepTest è stato sviluppato allo scopo di fornire un metodo alternativo CTA di valore equiparabile. ( ) P04087IT_01_K / p. 20/55
21 Carcinoma mammario La sicurezza ed efficacia dell Herceptin erano state valutate in uno studio clinico controllato randomizzato e in un vasto studio open-labelled (vedere il foglietto illustrativo all interno della confezione dell Herceptin ). Tutti i pazienti ammessi alla sperimentazione con Herceptin presentavano valori elevati (iperespressione) di proteina HER2 secondo i test di immunocitochimica effettuati con il CTA in un laboratorio centrale. I pazienti erano candidati alla terapia con Herceptin se il tumore presentava livelli di iperespressione dell HER2 pari a 2+ o 3+ (in base alla scala 0-3+, dove 3+ rappresenta il livello più elevato). Un analisi dei sottogruppi di risultati ottenuti da questi studi suggerisce che i pazienti con tessuti fortemente positivi (3+) alla proteina HER2 possono trarre maggiore beneficio dalla cura con Herceptin rispetto ai pazienti con tessuti più debolmente positivi (2+). Potenzialmente il grado di iperespressione della proteina HER2 è un indicatore importante dell eventuale efficacia della terapia con Herceptin. Dal momento che nessuna delle pazienti sottoposte a sperimentazione con Herceptin sono state selezionate utilizzando il test HercepTest, non è nota la correlazione tra il grado di positività e le probabilità di successo clinico della terapia con Herceptin. Studi comparativi Gli studi eseguiti per caratterizzare il test HercepTest sono due. 1) Studio comparativo con il CTA. 2) Studio di accuratezza rispetto ad altri cinque test. Studio comparativo con il CTA (Clinical Trial Assay) Il test HercepTest è stato confrontato con il CTA utilizzato per identificare i pazienti idonei alla terapia con Herceptin. A questo scopo sono stati utilizzati 274 campioni di tessuti di tumore della mammella positivi alla proteina HER2 (2+ o 3+) e altrettanti campioni negativi alla proteina HER2. Nella Tabella 4 sono riportati i risultati in un grafico 2 x 2 dove i valori 0 e 1+ sono stati considerati negativi e i valori 2+ e 3+ sono stati considerati negativi. Tabella 4. Concordanza 2 x 2 di HercepTest con il saggio CTA (numero di campioni). CTA (Clinical Trial Assay) Positivo Negativi Totale HercepTest Positivo Negativi Totale Concordanza: intervallo di confidenza al 95% = 79% (76 82%). La concordanza binaria complessiva tra il test HercepTest e il CTA si è attestata sul 79% (431 casi su 548), con un intervallo di confidenza al 95% bilaterale del 76 82%. Ventuno risultati su cento (21%) sono stati discordanti tra questi due metodi. Per l iperespressione della proteina HER2, i risultati di HercepTest sono riportati in una scala 0 3+ ed interpretati come negativi (intensità di colorazione 0 e 1+), debolmente positivi (intensità di colorazione 2+) e fortemente positivi (intensità di colorazione 3+). Tabella 5. Concordanza 3 x 3 di HercepTest con il saggio CTA CTA (Clinical Trial Assay) Totale HercepTest Totale ( ) P04087IT_01_K / p. 21/55
22 Carcinoma mammario Questa rappresentazione 3 x 3 dello studio sulla concordanza evidenzia l alta probabilità che una lettura 3+ con il test HercepTest corrisponda ad una lettura positiva con il CTA, cioè risponda ai requisiti di idoneità alla sperimentazione con Herceptin (2+ o 3+). Non è stata invece stabilita una correlazione altrettanto chiara tra una lettura 2+ con il test HercepTest e i risultati del CTA. Nel 42% circa dei casi (53 su 126), le letture 2+ con il test HercepTest sono risultate negative con il CTA (0 1+), quindi i pazienti non sarebbero stati ammessi alla sperimentazione clinica con Herceptin. Accuratezza Il test HercepTest è stato provato su 2 vetrini per microscopia contenenti sezioni di tessuto incluse in paraffina provenienti da 168 tumori della mammella. In precedenza, questi tumori erano stati caratterizzati con cinque diverse tecniche per la determinazione dell amplificazione del gene HER2 e dell iperespressione della proteina HER2: Southern blot nel laboratorio interno; ibridazione in situ con sonde fluorescenti (FISH) per l amplificazione del DNA; analisi RNA mediante Northern blot; Western blot; immunocitochimica (ICC) su tessuti congelati (29). I risultati sono riassunti nella Tabella 6. Tabella 6. Comparazione tra HercepTest e risultati combinati (OE) provenienti da saggi di amplificazione genica e iperespressione della proteina HER2. Classificazione OE di riferimento + - Totale HercepTest Totale Corrispondenza dei risultati positivi: 43/69 = 62% Corrispondenza dei risultati negativi: 99/99 = 100% I risultati hanno evidenziato un livello di corrispondenza dell 85% (142 casi su 168) (intervallo di confidenza al 95% compreso tra 78% e 89%) tra intensità della colorazione da positività (2+ e 3+) e da negatività (0 e 1+) al test HercepTest. Nessuno dei campioni risultati negativi con i 5 diversi metodi è poi risultato positivo con il test HercepTest. Allo stesso tempo, sommando i risultati dei 5 diversi metodi si è registrato un numero maggiore di casi positivi. Riproducibilità Riproducibilità intra-ciclo: la riproducibilità nella serie è stata studiata in un laboratorio utilizzando 5 campioni con punteggi di intensità della colorazione ICC diversi. Ogni campione è stato elaborato in triplicato in modo mascherato e random. Il protocollo è stato applicato con un sistema di colorazione automatizzato. Tutti i campioni hanno generato risultati riproducibili al 100%. Riproducibilità inter-ciclo: la riproducibilità tra serie è stata studiata presso tre laboratori per un periodo di 4 giorni, utilizzando 5 campioni con punteggi di intensità della colorazione ICC diversi, selezionati in modo random e mascherati con una metodologia automatizzata. È stata osservata un ottima riproducibilità per i risultati positivi, al contrario dei risultati negativi (0 e 1+ contro 2+ e 3+), fatta eccezione per due campioni in un laboratorio, che hanno presentato una variazione da 1+ a 2+. La riproducibilità per i campioni con punteggi 2+ e 3+ è stata del 100%. Riproducibilità inter-laboratorio: la riproducibilità tra laboratori è stata studiata presso tre laboratori geograficamente distinti, con 40 campioni identici selezionati in modo random e mascherati, i quali esprimevano livelli di intensità della colorazione ICC diversi. I vetrini appena tagliati sono stati inviati a tutti i laboratori scelti per il test, affinché venissero sottoposti a colorazione automatizzata e valutati da un patologo. Il risultato è stato una corrispondenza tra i laboratori tra l 83% e il 90% per una determinazione dicotoma di positività/negatività, dove i valori 0 e 1+ erano negativi e i valori 2+ e 3+ erano positivi all iperespressione della proteina HER2. Rispetto ai risultati ottenuti presso il laboratorio di riferimento che aveva condotto i test per il CTA, è risultata una discrepanza del 12,5% (15 su 120) nei risultati comparativi per la ( ) P04087IT_01_K / p. 22/55
23 Carcinoma mammario determinazione tra negativi (0 o 1+) e positivi (2+ o 3+). Un ulteriore 10% (12 su 120) dei risultati ha evidenziato una discrepanza tra i punteggi 2+ e 3+. ( ) P04087IT_01_K / p. 23/55
24 Immunoreattività Carcinoma mammario La Tabella 7 fornisce un quadro dell immunoreattività all HercepTest relativamente alla serie di tessuti normali selezionati. Tutti i tessuti sono stati fissati in formalina e inclusi in paraffina e colorati con HercepTest seguendo le istruzioni riportate nell inserto della confezione. Tabella 7. Sommario della reattività a HercepTest dei tessuti normali Tipo di tessuto (n di campioni) Surrenale (3) Midollo osseo (3) Cervello/Cervelletto (3) Cervello/Cervelletto (3) Mammella (3) Collo dell utero (3) Colon (3) Esofago (3) Cuore (3) Rene (3) Fegato (3) Polmone (3) Cellule mesoteliali (3) Ovaio (3) Pancreas (3) Paratiroide (3) Nervo periferico (3) Pituitaria (3) Prostata (3) Ghiandola salivare (3) Muscolo scheletrico (3) Pelle (3) Intestino tenue (3) Milza (3) Stomaco (3) Testicolo (3) Timo (3) Tiroide (3) Tonsilla (3) Utero (3) Colorazione positiva dell elemento tissutale e pattern di colorazione Ghiandola mammaria (1/3 dei tessuti, intensità di colorazione 1+) Tubuli di midollo renale (3/3 dei tessuti, 1-2 in 5-50% di cellule, citoplasmatica) Ghiandola prostatica/dotti (3/3 dei tessuti, intensità di colorazione 1+, 50% delle cellule, citoplasmatica) Ghiandole sudoripare (1/3 dei tessuti, 1+, 30% delle cellule, citoplasmatica) Epitelio colonnare, superficie (1/3 dei tessuti, intensità di colorazione +2, 25% delle cellule) Epitelio (1/3 dei tessuti, intensità di colorazione +1, 25% delle cellule) Epitelio squamoso (1/3 dei tessuti, intensità di colorazione 1+, 80% delle cellule) In tutti i tessuti è stata riscontrata la colorazione della membrana, salvo diversa segnalazione. L intensità della colorazione di tutti e tre i campioni di ogni tipo di tessuto era la stessa, salvo diversa segnalazione. ( ) P04087IT_01_K / p. 24/55
25 Risoluzione dei problemi - Mammella Carcinoma mammario Fare riferimento alla sezione Eventuali problemi e risoluzione nel manuale Dako precedentemente citato (19) per gli interventi riparativi, oppure contattare il Customer Support Dako per riportare eventuali colorazioni inattese. Problema Probabile causa Intervento consigliato 1. colorazione dei vetrini 1a. Errore di programmazione. Reagenti non usati nell ordine adeguato 1a. Controllare la griglia di programmazione per verificare che il ciclo di colorazione sia stato programmato correttamente 1b. Le fiale dei reagenti non sono state caricate nelle posizioni corrette nei raccoglitori portareagenti 1c. La quantità di reagente nella fiala è insufficiente 1d. Azide sodica nella soluzione di lavaggio 1b. Controllare la Mappa dei reagenti per verificare il corretto posizionamento delle fiale dei reagenti 1c. Assicurarsi che il reagente sia caricato in quantità sufficiente nelle fiale prima dell avvio del ciclo. Fare riferimento alla Mappa dei reagenti per i volumi richiesti 1d. Utilizzare la preparazione fresca di tampone di lavaggio fornita nel kit 2. Colorazione debole dei vetrini 1e. Un riscaldamento eccessivo di sezioni di tessuto montate prima della deparaffinazione e del recupero dell antigene indotto dal calore può portare alla perdita di immunoreattività HER2 visibile. 2a. Smascheramento degli epitopi inadeguato 2b. Tempo di incubazione dei reagenti inadeguato 2c. È stato usato un metodo di fissazione inadeguato 2d. Un riscaldamento eccessivo di sezioni di tessuto montate prima della deparaffinazione e del recupero dell antigene indotto dal calore può provocare una diminuzione significativa dell immunoreattività HER2 visibile. 2e. Volume di reagente 1e. Far asciugare all aria le sezioni di tessuto a temperatura ambiente per un minimo di 12 ore o fino al completamento dell asciugatura. In alternativa, asciugare a 37 C durante la notte o asciugare a 60 C per un massimo di un ora. L asciugatura di sezioni di tessuto a temperature elevate deve essere eseguita solo in un forno calibrato con distribuzione uniforme del calore (17). 2a. Verificare che la soluzione Epitope Retrieval Solution raggiunga C per 40 minuti e che venga lasciata raffreddare per altri 20 minuti 2b. Rivedere le istruzioni sulla procedura di colorazione 2c. Assicurarsi che il tessuto del paziente non sia eccessivamente fissato o che non sia stato utilizzato un metodo di fissazione alternativo 2d. Far asciugare all aria le sezioni di tessuto a temperatura ambiente per un minimo di 12 ore o fino al completamento dell asciugatura. In alternativa, asciugare a 37 C durante la notte o asciugare a 60 C per un massimo di un ora. L asciugatura di sezioni di tessuto a temperature elevate deve essere eseguita solo in un forno calibrato con distribuzione uniforme del calore (17). ( ) P04087IT_01_K / p. 25/55
26 3. Eccessiva colorazione di sfondo dei vetrini insufficiente applicato 3a. La paraffina è stata rimossa solo parzialmente 3b. Additivi a base di amido utilizzati nel montaggio delle sezioni sui vetrini 3c. I vetrini non sono stati completamente lavati 3d. Le sezioni si sono seccate durante la procedura di colorazione 3e. Sezioni essiccate durante il caricamento su Autostainer 3f. È stato usato un metodo di fissazione inadeguato Carcinoma mammario 2e. Verificare le dimensioni della sezione di tessuto (22 mm x 22 mm) e il volume di reagente applicato. 3a. Usare soluzioni di chiarificazione nuove e seguire la procedura come indicato nella sezione B.1 3b. Evitare l uso di additivi amidacei per fare aderire le sezioni ai vetrini. Molti additivi sono immunoreattivi 3c. Prima di avviare il ciclo, verificare che il sistema Autostainer sia stato sottoposto a priming. Controllare che il tampone caricato sia sufficiente per l intero ciclo di analisi. Utilizzare soluzioni di tampone e di lavaggio fresche 3d. Controllare che sui vetrini sia stato applicato il volume di reagente corretto. Assicurarsi che durante il funzionamento il coperchio dello strumento Autostainer sia in posizione chiusa e che lo strumento non sia esposto a calore eccessivo o a correnti d aria 3e. Assicurarsi che le sezioni rimangano bagnate con tampone durante il caricamento e prima dell avvio del ciclo 3f. Controllare che sia stato utilizzato un fissativo approvato. Altri fissativi possono causare una eccessiva colorazione di fondo 4. Il tessuto si stacca dai vetrini 5. Colorazione specifica eccessivamente forte 3g. Legame aspecifico di reagenti al tessuto 3g. Controllare il metodo di fissazione del campione e la presenza di necrosi 4a. Uso di vetrini errati 4a. Utilizzare vetrini silanizzati, come per esempio Dako Silanized Slides, Codice S3003, SuperFrost Plus o vetrini polilisinati 5a. È stato usato un metodo di fissazione inadeguato 5b. Uso di una inadeguata fonte di calore per lo smascheramento degli epitopi, p.e. pentola a pressione, forno a microonde o autoclave 5a Assicurarsi che vengano utilizzati solamente fissativi e metodi di fissazione appropriati 5b. Assicurarsi che venga utilizzato solamente il trattamento a bagnomaria per la fase di smascheramento degli epitopi 5c. Tempi di incubazione reagente troppo lunghi 5d. È stata usata una soluzione di lavaggio inadeguata 5c. Rivedere le istruzioni sulla procedura di colorazione 5d. Usare solo il tampone di lavaggio consigliato per il kit ( ) P04087IT_01_K / p. 26/55
27 6. Debole colorazione della linea cellulare del vetrino di controllo La soluzione Epitope Retrieval Solution ha un aspetto torbido quando viene riscaldata 8. La soluzione Epitope Retrieval Solution ha un aspetto torbido durante la conservazione (prima di scaldarla) 6a. Protocollo inadatto per lo smascheramento degli epitopi 6b. Mancanza di reazione con la soluzione substratocromogeno (DAB) 6c. Degradazione del vetrino di controllo 7. Quando viene riscaldata, la soluzione assume un aspetto torbido 8. La soluzione è stata conservata in modo scorretto, oppure ne è stata superata la data di scadenza Carcinoma mammario 6a. Immergere i vetrini nella soluzione di smascheramento degli epitopi preriscaldata. Riportare la temperatura della soluzione di smascheramento a C e pretrattare per 40 minuti 6b. Assicurarsi che venga rispettato il tempo di incubazione di 10 minuti. Assicurarsi che venga aggiunta solamente una goccia di cromogeno DAB ad 1 ml di substrato tamponato DAB 6c. Controllare la data di scadenza del kit e le condizioni di conservazione del kit riportate all esterno della confezione 7. Ciò è normale e non influisce sulla colorazione. 8. Controllare la data di scadenza e le condizioni per la conservazione del kit stampate all esterno della confezione. Gettare via la soluzione di recupero dell'epitopo. NOTA: se il problema verificatosi non può essere attribuito ad alcuna delle cause riportate sopra, oppure se l azione correttiva suggerita non consente la risoluzione del problema, si prega di contattare il Customer Support Dako per ulteriore assistenza. Ulteriori informazioni sulle tecniche di colorazione e sulla preparazione dei campioni sono contenute in Handbook -Immunochemical Staining Methods (19) (disponibile presso Dako), Atlas of Immunohistology (30) e Immunoperoxidase Techniques, A Practical Approach to Tumor Diagnosis (31). ( ) P04087IT_01_K / p. 27/55
28 Carcinoma gastrico Cenni introduttivi - Gastrico Dati di base Il gene umano HER2 (noto anche con le sigle ERBB2 o NEU) codifica una proteina che è generalmente denominata proteina HER2 o p185 HER2. La proteina HER2 è un recettore di transmembrana ad attività tirosin-chinasica con omologia per il recettore del fattore di crescita epidermico (EGFR o HER1) (1-8). La proteina HER2 è un componente normalmente espresso da numerosi tipi di cellule epiteliali (8). L iperespressione della proteina HER2 e l amplificazione del gene HER2 nel cancro gastrico sono stati mostrati in molti studi (32). La positività all HER2 può essere rilevata in circa il 20% dei pazienti tramite IHC o FISH (32). Studi preclinici in vitro e in vivo hanno dimostrato che il trastuzumab (Herceptin ) è efficace in modelli di cancro gastrici differenti, portando così all'avvio di vari studi clinici (32-36). In uno studio di fase III BO18255, lo studio ToGA, i pazienti positivi all HER2 con adenocarcinoma in stadio avanzato localmente inoperabile, ricorrente e/o metastatico dello stomaco o della giunzione esofagea sono stati sottoposti in maniera randomizzata a terapia con 5 FU o capecitabina o cisplatina, da soli o in combinazione con il trastuzumab. È stato rilevato un aumento significativo nella sopravvivenza globale (OS) nei pazienti sottoposti al trattamento combinato di trastuzumab e chemioterapia (37, 38). Il trastuzumab è un anticorpo monoclonale umanizzato che presenta un elevata affinità di legame con la proteina HER2 e che, come si è dimostrato, è in grado di inibire la proliferazione delle cellule tumorali umane che iperesprimono la proteina HER2 sia in vitro, sia in vivo (33-36). Caratteristiche 3803 pazienti sono stati analizzati per verificare lo stato di HER2 per l inclusione nello studio ToGA. In questo studio, sia l iperespressione della proteina HER2 tramite IHC (HercepTest, Dako) sia l amplificazione del gene HER2 tramite FISH (HER2 FISH pharmdx, Dako) sono state misurate. Risultati di test validi sono stati ottenuti in 3665 campioni con test IHC o FISH e in 3280 campioni con entrambi i test. I risultati dello studio ToGA hanno mostrato che il 22,1% dei pazienti con cancro gastrico in stadio avanzato è risultato positivo all HER2, rilevato tramite IHC o FISH secondo la definizione dei criteri di selezione HER del ToGA (38). Rispetto all uso dell HercepTest nella valutazione dei pazienti che devono essere dichiarati idonei al trattamento con trastuzumab, vedere il foglietto illustrativo dell Herceptin. Principio della procedura - Gastrico HercepTest contiene i reagenti necessari per la completa esecuzione di una procedura di colorazione immunocitochimica a due fasi su campioni processati con i metodi convenzionali, inclusi in paraffina. Dopo l incubazione con l anticorpo primario di coniglio anti-proteina HER2 umana, il kit prevede l impiego di un Visualization Reagent pronto all uso, il quale sfrutta la tecnologia a base di destrano. Il reagente in questione è composto sia da molecole di immunoglobuline secondarie di capra anti-coniglio, sia da molecole di perossidasi di rafano, legate ad una comune catena principale di destrano. Questa tecnologia elimina la necessità di applicare in modo sequenziale un anticorpo di collegamento e un anticorpo coniugato con perossidasi. La reazione crociata del Visualization Reagent con le immunoglobuline umane e il siero fetale di vitello è stata rimossa mediante assorbimento in base solida. La conversione enzimatica del cromogeno aggiunto successivamente dà origine alla formazione di un prodotto di reazione visibile in corrispondenza dell antigene. A questo punto è possibile procedere alla colorazione di contrasto del campione e montare un vetrino coprioggetto. L interpretazione dei risultati avviene per mezzo di un microscopio ottico. Per convalidare le serie di colorazione vengono forniti vetrini di controllo contenenti tre linee cellulari di tumore della mammella ( ) P04087IT_01_K / p. 28/55
29 Carcinoma gastrico umano, debitamente fissati in formalina e inclusi in paraffina, i quali esprimono tre gradi di intensità della colorazione: 0, 1+ e 3+. Vi è una correlazione tra l intensità della colorazione di queste linee cellulari e il numero di recettori presenti in ogni cellula. HercepTest, Codice K5207, è indicato per la colorazione automatica con lo strumento Autostainer. Reagenti - Gastrico Materiali forniti Il materiale elencato è sufficiente per effettuare 50 test (50 vetrini incubati con anticorpo primario anti-proteina HER2 e 50 vetrini incubati con il corrispondente reagente di controllo negativo). Il numero di test è calcolato in base all uso di 200 µl per sezione di tessuto (22 mm x 22 mm) di fiale n. 1, 2, 3 e 4 e della soluzione cromogeno-substrato (DAB). Il kit contiene materiale sufficiente per effettuare un massimo di 15 cicli di colorazione singoli. Fiala n. Quantità Descrizione 1 2 x 11 ml 2 1 x 12 ml 3 2 x 11 ml 4 1 x 12 ml 5 15 x 11 ml 6 3 x 3 ml 7 3 x 500 ml Reagente bloccante della perossidasi: Perossido di idrogeno 3% contenente sodio azide (NaN 3 ) 15 mmol/l. Anticorpo di coniglio anti-her2 umana: Anticorpo pronto all uso isolato per affinità. Viene fornito in Tris/HCl 0,05 mol/l; NaCl 0,1 mol/l; NaN 3 15 mmol/l; ph 7,2 e con proteina stabilizzante. Immunogeno: frammento sintetico C-terminale (parte intracitoplasmica) della proteina HER2 accoppiato a emocianina di patella. Specificità: proteina HER2. Metodo di purificazione: l anticorpo viene isolato per affinità utilizzando un peptide immobilizzato della proteina HER2. Reagente di visualizzazione: Polimero di destrano coniugato con perossidasi di rafano e immunoglobuline di capra antiimmunoglobuline di coniglio isolate per affinità. Viene fornito in tampone Tris/HCl contenente proteina stabilizzante e un agente antimicrobico. Reagente di controllo negativo: Frazione di immunoglobuline di siero di coniglio normale. Concentrazione della proteina equivalente alla concentrazione dell anticorpo anti-proteina HER2. Viene fornito in Tris/HCl 0,05 mol/l; NaCl 0,1 mol/l; NaN 3 15 mmol/l; ph 7,2 e con proteina stabilizzante. Substrato tamponato DAB: Soluzione tampone substrato, a ph 7,5, contenente perossido di idrogeno < 0,1%, stabilizzanti, enhancer e un agente antimicrobico. Cromogeno DAB: Soluzione cromogena contenente 3,3 - diaminobenzidina tetraidrocloruro (5%). ( ) P04087IT_01_K / p. 29/55
30 8 2 x 1 L 3 x 5 vetrini Carcinoma gastrico Soluzione di smascheramento degli epitopi (Containing Detergent) (10x): Tampone citrato 0,1 mol/l con un detergente. Tampone di lavaggio (10x): tampone Tris/HCl contenente un detergente e un agente antimicrobico. Vetrini di controllo: Ogni vetrino contiene sezioni di tre linee cellulari di carcinoma mammario che sono state fissate in formalina e incluse in paraffina e che rappresentano livelli diversi di espressione della proteina HER2: MDA-231 (0), MDA-175 (1+) e SK-BR-3 (3+). I vetrini di controllo sono stati trattati termicamente per assicurare una maggiore aderenza delle sezioni al vetro. Se i vetrini vengono sottoposti ad ulteriori trattamenti termici per migliorare l aderenza delle sezioni al vetro, si corre il rischio di compromettere i risultati della colorazione. NOTA: tutti i reagenti, compresi la soluzione di smascheramento degli epitopi e il tampone di lavaggio, sono formulati specificatamente per l uso nell ambito di questo test. Per garantire la performance specificata del test, non effettuare alcuna sostituzione, fatta eccezione per il tampone di lavaggio, utilizzando eventualmente Dako Codice S3006. Materiali necessari ma non forniti Idrossido di ammonio, 15 mol/l, diluito a 37 mmol/l Colorante di contrasto: ematossilina, per esempio ematossilina di Mayer a base acquosa, Dako Codice S3301 (vedi ISTRUZIONI PER L USO, A.4) Vetrini coprioggetto Acqua distillata o deionizzata (acqua per lavaggio) Forno essiccante, in grado di mantenere una temperatura di 60 C o inferiore Etanolo, assoluto e al 95% Microscopio ottico (ingrandimento obiettivo 4 40x) Mezzo di montaggio, per esempio Dako Faramount, Codice S3025, oppure Glycergel, Codice C0563 Tessuti positivi e negativi da utilizzare come controlli di lavoro (vedere Controllo della qualità) Vetrini, SuperFrost Plus, polilisinati, oppure Dako Silanized Slides Codice S3003 (vedi Preparazione dei campioni) Vaschette o bagni per la colorazione Contaminuti (per intervalli di 2 40 minuti) Bagnomaria con coperchio (capace di mantenere la soluzione Epitope Retrieval Solution a C) Xilene, toluene o sostituti dello xilene K5207 è stato messo a punto per l uso con Autostainer Immunostaining System, Codice S3400. Fare riferimento alla Guida Autostainer per l utente per i componenti Autostainer necessari. ( ) P04087IT_01_K / p. 30/55
31 Conservazione - Gastrico Conservare a 2 8 C. Carcinoma gastrico Non utilizzare il kit dopo la data di scadenza stampata all esterno della confezione. Se i reagenti sono conservati in condizioni diverse da quelle specificate, l utente deve verificarne le condizioni (14a, 14b). Si fa presente che anche i vetrini di controllo devono essere conservati a 2 8 C. Non sono stati osservati segni evidenti che suggeriscano l instabilità di questo prodotto, pertanto è opportuno analizzare un controllo positivo e un controllo negativo insieme ai campioni dei pazienti. Se si dovesse osservare una colorazione inattesa non attribuibile a modifiche delle procedure di lavoro e si sospetta un problema relativo a HercepTest, contattare il Customer Support. Specimen preparation (Allestimento tessuto) - Gastrico I campioni di adenocarcinoma gastrico con giunzione gastroesofagea provenienti da biopsie, escissioni o resezioni devono essere manipolati correttamente in modo da preservare il tessuto per la colorazione immunocitochimica. Adottare i metodi standard per il trattamento dei tessuti di tutti i campioni (15). Quando si analizzano piccoli campioni provenienti da biopsia, accertare l'integrità della morfologia del tumore e la presenza di un numero sufficiente di cellule tumorali per la valutazione immunoistochimica (IHC). Se si esegue l'analisi HercepTest su un campione proveniente da biopsia, è necessario analizzare più (7-8) campioni bioptici da differenti regioni del tumore, al fine di garantire un'accurata determinazione dello stato dell'her2. Sezioni incluse in paraffina Sono idonei all uso i tessuti conservati in formalina tamponata neutra e inclusi in paraffina. Per esempio, i campioni devono essere bloccati in uno spessore di 3 o 4 mm e fissati per ore in formalina tamponata neutra. Nello studio ToGA, i campioni bioptici sono stati fissati per 6-8 ore (per riferimenti sullo studio, vedere (37)). I tessuti vengono successivamente disidratati attraverso il passaggio in una serie di alcoli e in xilene e sottoposti ad infiltrazione di paraffina fusa ad una temperatura non superiore a 60 C. I te ssuti che esprimono l HER2, quando vengano sottoposti a fissazione e inclusione in modo corretto e siano conservati al fresco (15 25 C), preservano la loro morfologia a tempo i ndeterminato prima del taglio delle sezioni e del montaggio su vetrino (15, 16). Negli Stati Uniti, la norma 42 CFR (b) del Clinical Laboratory Improvement Act del 1988 prevede che i laboratori devono conservare i vetrini colorati per almeno dieci anni dalla data del saggio e devono altresì conservare blocchi di campioni per almeno due anni dalla data del saggio (16). I campioni di tessuto devono essere tagliati in sezioni di 4 5 µm, montati su vetrini e asciugati all aria a temperatura ambiente per un minimo di 12 ore (o fino all asciugatura) o a 37 C durante la notte o a 60 C per un ora. AVVISO: un calore eccessivo per più di un ora a 60 C può causare una diminuzione significativa o la perdita dell immunoreattività HER2 specifica associata alla membrana (17). Per preservare l antigenicità, le sezioni di tessuto già montate sui vetrini (SuperFrost Plus, Poly- L-lysine o vetrini silanizzati) dovranno essere sottoposte alla colorazione entro 4 6 settimane dal sezionamento se conservate a temperatura ambiente (20 25 C) (18). I vetrini da utilizzare per la valutazione della proteina HER2 e per la verifica della presenza di tumore devono essere preparati in contemporanea. Si consiglia di preparare almeno 5 vetrini: 1 per controllare la presenza tumorale, 2 per la valutazione della proteina HER2 (1 per l incubazione con la fiala n. 2 e 1 per l incubazione con la fiala n. 4) e 2 da conservare in caso di eventuali problemi. L uso di HercepTest TM su tessuti decalcificati non è stato validato e pertanto non viene raccomandato. ( ) P04087IT_01_K / p. 31/55
32 Carcinoma gastrico Consultare la pubblicazione Dako intitolata Education Guide: Immunochemical Staining Methods (19) e i riferimenti bibliografici 15 e 16 per ulteriori informazioni sulla preparazione dei campioni. Trattamento dei campioni prima della colorazione Per conseguire un rendimento ottimale del test, è necessario utilizzare un metodo di recupero dell epitopo in tampone citrato 10 mmol/l. La soluzione idonea allo scopo è inclusa nel kit HercepTest. Questo metodo richiede il riscaldamento delle sezioni di tessuto montate su vetrini immerse in tampone citrato 10 mmol/l (20) a bagnomaria calibrato per mantenere la soluzione di smascheramento degli epitopi alla temperatura richiesta (95 99 C). I laboratori situati ad altitudini più elevate devono definire il metodo migliore per mantenere la temperatura richiesta del bagnomaria. Lo smascheramento dell epitopo deve essere eseguito a bagnomaria. Sono stati sperimentati altri metodi di riscaldamento, che tuttavia non hanno dato risultati riproducibili. Subito dopo lo smascheramento dell epitopo, iniziare la procedura di colorazione. Eventuali variazioni della procedura descritta potrebbero compromettere i risultati. Precauzioni - Gastrico 1. Per uso diagnostico in vitro. 2. Per uso professionale. 3. Fiala 1, Peroxidase-Blocking Reagent, contiene 3% di perossido di idrogeno. Su richiesta è disponibile una scheda di sicurezza per utenti professionisti. 4. La fiala 6, il cromogeno DAB, contiene DAB, contiene 5-<10% di 3,3 -diaminobenzidina tetracloridrato e riporta l etichetta: H350 H341 P201 P280 Pericolo P308 + P313 P405 P501 Può provocare il cancro. Sospettato di provocare alterazioni genetiche. Procurarsi istruzioni specifiche prima dell uso. Indossare guanti protettivi. Fare uso di un dispositivo di protezione degli occhi o del viso. Indossare indumenti protettivi. IN CASO di esposizione o di possibile esposizione: Richiedere assistenza medica. Conservare sotto chiave. Smaltire il prodotto e il recipiente in conformità a tutte le normative locali, regionali, nazionali e internazionali. Di norma, l utilizzo di questo prodotto non è consentito ai minori di 18 anni. Gli utenti devono essere accuratamente informati relativamente alla procedura di lavoro adeguata, alle proprietà pericolose del prodotto e alle istruzioni di sicurezza necessarie. Per ulteriori informazioni, fare riferimento alla scheda di sicurezza dei materiali (Safety Data Sheet, SDS) corrispondente Amino-2-(hydroxymethyl)propane-1,3-diol hydrochloride e 0.1-<0.2% 5-bromo-5-nitro- 1,3-diossano. Può indurre una reazione allergica. Wash Buffer (10x) è etichettato: Attenzione H319 P280 P264 P305 + P351 + P338 Provoca grave irritazione oculare. Proteggere gli occhi/il viso. Lavare accuratamente le mani dopo l'uso. IN CASO DI CONTATTO CON GLI OCCHI: sciacquare accuratamente per parecchi minuti. Togliere le eventuali lenti a contatto se è agevole farlo. Continuare a sciacquare. ( ) P04087IT_01_K / p. 32/55
33 Carcinoma gastrico 6. Questo prodotto contiene sodio azide (NaN 3 ), una sostanza chimica fortemente tossica in forma pura. Sebbene non sia classificato come prodotto a rischio, la sodio azide alle concentrazioni indicate può reagire con il rame e il piombo delle tubature formando azidi metalliche fortemente esplosive. Per lo smaltimento del prodotto, è consigliabile sciacquare abbondantemente con acqua per evitare l accumulo di azidi metalliche nelle tubature (21, 22). 7. Le fiale 2, 3 e 4 contengono materiale di origine animale. Adottare le normali procedure previste per il trattamento dei prodotti di origine biologica. 8. I vetrini di controllo e i campioni, sia prima che dopo la fissazione, e tutti i materiali che entrano in contatto con essi devono essere trattati come materiali potenzialmente capaci di trasmettere un infezione, pertanto devono essere smaltiti assumendo tutte le precauzioni necessarie (23). Non pipettare mai i reagenti per bocca ed evitare che reagenti e campioni entrino in contatto con la pelle e le membrane mucose. In caso di contatto dei reagenti con zone sensibili, lavare la zona con abbondante acqua. 9. Ridurre al minimo la contaminazione microbica di reagenti per evitare una colorazione aspecifica. 10. Tempi, temperature e modalità di incubazione diversi da quelli specificati possono generare risultati erronei. Un asciugatura eccessiva per più di un ora a 60 C può causare una diminuzione significativa o la perdita dell immunoreattività HER2 specifica associata alla membrana (17). 11. I reagenti sono stati diluiti in modo ottimale. Ulteriori diluizioni potrebbero causare la perdita di colorazione antigenica. 12. Tutti i reagenti, compresi la soluzione di smascheramento degli epitopi e il tampone di lavaggio, sono formulati specificatamente per l uso nell ambito di questo test. Per garantire la performance indicata per il test, non effettuare alcuna sostituzione, fatta eccezione per il tampone di lavaggio, usando eventualmente Dako Codice S Il Visualization Reagent e il cromogeno DAB possono essere danneggiati dall esposizione a livelli di luce eccessivi. Non conservare i componenti del kit e non eseguire la colorazione in condizioni di luce intensa, ad esempio sotto la luce diretta del sole. 14. Indossare indumenti di protezione personale adeguati, per evitare il contatto con gli occhi e la pelle. Per ulteriori informazioni, fare riferimento alla scheda di sicurezza dei materiali (Material Safety Data Sheet, MSDS) corrispondente. 15. Residui di paraffina possono generare risultati falsi negativi. 16. Per un'interpretazione precisa dei risultati dell'herceptest su campioni bioptici sottoposti a colorazione provenienti da adenocarcinomi gastrico con giunzione gastroesofagea, si consiglia un gruppo di almeno 5 cellule tumorali sottoposte a colorazione. Un cluster id almeno 5 cellule tumorali sottoposte a colorazione è composto di 5 cellule tumorali sottoposte a colorazione HER connesse. 17. Per ottenere un risultato affidabile, a causa della natura eterogenea dei campioni bioptici di cancro gastrico, è importante eseguire l'analisi IHC dell'her2 su campioni bioptici multipli (7-8) provenienti da regioni diverse del tumore. 18. L uso di volumi di reagente diversi da quelli raccomandati può comportare la perdita di immunoreattività HER2 visibile. Sezioni di tessuto maggiori di 22 mm x 22 mm richiedono l applicazione di 2-3x 200 µl di reagente in 2-3 aree di applicazione automatizzata. 19. Quando si osserva un livello elevato di eterogeneità nel campione, si consiglia di analizzare più blocchi di tessuto da resezioni di cancro gastrico (41). ( ) P04087IT_01_K / p. 33/55
34 Carcinoma gastrico ISTRUZIONI PER L USO - Gastrico A. Preparazione Per ragioni di praticità, prima di procedere alla colorazione è opportuno preparare i reagenti elencati di seguito: A.1 Epitope Retrieval Solution Diluire una quantità sufficiente della fiala 7 (Epitope Retrieval Solution x 10) 1:10 utilizzando acqua distillata o deionizzata per la procedura di colorazione pianificata. La soluzione diluita inutilizzata può essere conservata a 2 8 C per un mese. Eliminare la soluzione diluita se appare torbida. A.2 Tampone di lavaggio Diluire una quantità sufficiente di fiala 8 (tampone di lavaggio 10x) 1:10 con acqua distillata o deionizzata per le fasi di lavaggio. Il tampone diluito inutilizzato può essere conservato a 2 8 C per un mese. Eliminare la soluzione tampone se appare torbida. Lo strumento Autostainer è programmato per sciacquare le sezioni di tessuto dopo il trattamento con il reagente bloccante della perossidasi e con la soluzione substratocromogeno. Si fa presente che per queste fasi di lavaggio si può utilizzare acqua distillata (o deionizzata) o tampone di lavaggio. Tutte le altre fasi di lavaggio richiedono l utilizzo di tampone di lavaggio. A.3 Soluzione cromogeno-substrato (DAB) Preparare la soluzione cromogeno-substrato aggiungendo 11 gocce (25 30 µl per goccia) di cromogeno DAB dalla fiala 6 ad una fiala 5 contenente tampone substrato DAB (11 ml), quindi miscelare. La soluzione substrato-cromogeno (DAB) così preparata è stabile per circa 5 giorni se conservata a 2 8 C. La soluzione deve essere agita ta bene prima dell uso. La comparsa di qualsiasi precipitato all interno della soluzione non ne altera la qualità di colorazione. NOTA: il colore del cromogeno DAB nella fiala 6 può variare da trasparente a viola chiaromarrone. Questa caratteristica non altera il rendimento del prodotto. Diluire secondo le linee guida contenute nel presente foglietto illustrativo. L aggiunta in eccesso di DAB Chromogen al DAB Buffered Substrate può determinare un deterioramento del segnale positivo. A.4 Colorazione di contrasto Il prodotto finale della reazione di colorazione DAB è insolubile in alcol e in acqua. Utilizzare una controcolorazione con ematossilina e aggiustare l intensità di colorazione dell ematossilina ad un livello simile a quello riportato nel manuale di interpretazione dell'herceptest per il cancro gastrico di Dako ( HercepTest Interpretation Manual Gastric Cancer ). Per questa fase si può utilizzare ematossilina, a base alcolica o a base acquosa, per esempio ematossilina di Mayer Dako, Codice S3301. Successivamente alla controcolorazione con ematossilina, sciacquare in acqua distillata o deionizzata e quindi immergere i vetrini con i tessuti in un bagno acquaammoniaca 37 mmol/l (vedi sezione B.2, fase 3). La soluzione acqua-ammoniaca (37 mmol/l) viene preparata mescolando 2,5 ml di idrossido di ammonio 15 mol/l (concentrato) con 1 L di acqua distillata o deionizzata. La soluzione ammoniacale 37 mmol/l inutilizzata può essere conservata in un flacone perfettamente sigillato a temperatura ambiente (20 25 C) per 12 mesi. A.5 Mezzo di montaggio Si consiglia di usare un mezzo di montaggio permanente e non acquoso. Tuttavia è accettabile anche un montaggio acquoso. Per il montaggio acquoso, si raccomanda l uso di Dako Faramount Aqueous Mounting Medium, pronto per l uso, Codice S3025, oppure Glycergel Mounting Medium, Codice C0563. Liquefare Glycergel riscaldando a circa 40 (±5) C prima dell uso. ( ) P04087IT_01_K / p. 34/55
35 B. Procedura di colorazione su Autostainer Carcinoma gastrico B.1 Note sulla procedura Prima dell uso, si consiglia di leggere attentamente le istruzioni fornite di seguito e studiare le caratteristiche di tutti i componenti (vedere Precauzioni). Tutti i reagenti devono essere equilibrati a temperatura ambiente (20 25 C) prima dell immunocolorazione. Analogamente, tutte le fasi di incubazione devono svolgersi a temperatura ambiente. Non lasciare andare a secchezza le sezioni tissutali durante il caricamento su Autostainer e durante la procedura di colorazione. Le sezioni di tessuto secche possono presentare una maggiore colorazione aspecifica. Se la procedura di colorazione viene interrotta, è possibile conservare i vetrini in un bagno tampone dopo l incubazione dell anticorpo primario, per non più di un ora a temperatura ambiente (20 25 C), senza ripercussioni sui risult ati della colorazione. Sparaffinatura e reidratazione: prima della colorazione, i vetrini contenenti i tessuti devono essere deparaffinati per rimuovere il mezzo di inclusione e successivamente reidratati. Evitare la rimozione incompleta della paraffina. La presenza di eventuali residui del mezzo di inclusione può provocare un aumento della colorazione aspecifica. Questa operazione deve essere eseguita a temperatura ambiente (20 25 C). 1. Immergere i vetrini in un bagno di xilene e incubare per 5 (±1) minuti. Cambiare il bagno e ripetere il procedimento. 2. Picchiettare i vetrini per eliminare il liquido in eccesso e immergerli in etanolo assoluto per 3 (±1) minuti. Cambiare il bagno e ripetere il procedimento. 3. Eliminare l eccesso di liquido picchiettando i vetrini e immergerli in etanolo al 95% per 3 (±1) minuti. Cambiare il bagno e ripetere il procedimento. 4. Picchiettare per eliminare il liquido in eccesso e immergere i vetrini in acqua distillata o deionizzata per almeno 30 secondi. Iniziare la procedura di colorazione come descritto nella sezione B.2, fase 1, smascheramento degli epitopi. Soluzioni alcoliche e allo Xilene devono essere cambiate dopo 40 vetrini. Al posto dello xilene è possibile utilizzare i derivati di toluene o xilene, ad esempio Histoclear. NOTA: le istruzioni e i reagenti forniti in questo kit sono stati studiati per assicurare prestazioni ottimali. L ulteriore diluizione dei reagenti o una variazione delle temperature di incubazione potrebbero generare risultati erronei o discordanti. Le differenze che esistono tra i laboratori (per quanto riguarda il modo di trattare il tessuto o di eseguire le procedure tecniche) possono compromettere la validità dei risultati del test in quanto strumento di selezione dei pazienti idonei alla terapia con Herceptin. B.2 Protocollo di colorazione Eseguito a temperatura ambiente, C. Fase 1: Recupero dell epitopo Riempire le vaschette per la colorazione, p. es. vaschette di Coplin, con la soluzione di smascheramento degli epitopi diluita (vedi ISTRUZIONI PER L USO, sezione A.1). Immergere in un bagnomaria le vaschette contenenti la soluzione Epitope Retrieval Solution. Riscaldare bagnomaria e soluzione di smascheramento a C. Durante il riscaldamento, la soluzione Epitope Retrieval Solution assume un aspetto torbido. Coprire le vaschette con i rispettivi coperchi per stabilizzare la temperatura ed evitare l evaporazione. Immergere le sezioni deparaffinate a temperatura ambiente nelle vaschette con la soluzione Epitope Retrieval Solution precedentemente riscaldata. RIPORTARE LA TEMPERATURA DI BAGNOMARIA E SOLUZIONE DI SMASCHERAMENTO A C. Incubare per 40 (±1) minuti a C. ( ) P04087IT_01_K / p. 35/55
36 Carcinoma gastrico Rimuovere tutta la vaschetta con i vetrini dal bagnomaria. Lasciare raffreddare i vetrini nella soluzione di smascheramento degli epitopi per 20 (±1) minuti a temperatura ambiente. Decantare la soluzione di smascheramento e risciacquare le sezioni con tampone di lavaggio diluito (vedi ISTRUZIONI PER L USO, sezione A.2). Per un risultato ottimale, immergere le sezioni in tampone di lavaggio per 5 20 minuti dopo lo smascheramento degli epitopi e prima della colorazione. NOTA: la soluzione Epitope Retrieval Solution è un prodotto monouso, idoneo a una sola applicazione. Non riutilizzare. Fase 2: Procedura Autostainer 1. Utilizzare la mappa generata da Autostainer sull autoprogramma HercepTest per conoscere i tempi del programma e i volumi dei reagenti (vedi il successivo punto 4 per informazioni sui volumi specifici). 2. Inserire le fiale per reagenti Autostainer nel raccoglitore portareagenti Autostainer conformemente alla mappa dei reagenti generata dal computer. 3. Caricare i vetrini sullo strumento Autostainer conformemente alla mappa dei vetrini generata dal computer. 4. Impostare il programma e iniziare il programma HercepTest. Qui di seguito viene riportata una descrizione dell esecuzione del programma: Risciacquare 200 µl di Peroxidase-Blocking Reagent - 5 minuti Risciacquare 200 µl di anticorpo primario anti-proteina HER2 (o reagente di controllo negativo) 30 minuti Risciacquare 200 µl di Visualization Reagent - 30 minuti Risciacquare Risciacquare Cambiare 200 µl di soluzione cromogeno-substrato (DAB) - 10 minuti Lavare i vetrini in acqua deionizzata dopo il passaggio con soluzione cromogeno-substrato NOTA: la versione 01 dell apparecchiatura Autostainer lava i vetrini nel tampone. Pertanto i vetrini devono essere lavati con acqua deionizzata dopo essere stati rimossi dall Autostainer. Fase 3: Colorazione di contrasto (le istruzioni si riferiscono all ematossilina) Estrarre i vetrini dall Autostainer e controcolorare in ematossilina come descritto qui di seguito. Immergere i vetrini in un bagno di ematossilina. Incubare per 2 5 minuti, a seconda dell intensità dell ematossilina utilizzata. Lavare delicatamente in un bagno di acqua distillata o deionizzata. Assicurarsi che tutta l ematossilina residua sia stata eliminata. Opzionalmente, è possibile immergere i vetrini 10 volte in un bagno di soluzione acqua-ammoniaca 37 mmol/l (vedi sezione A.4). Lavare delicatamente i vetrini in un bagno di acqua distillata o deionizzata per 2 5 minuti. NOTA: a seconda della durata dell incubazione o della potenza dell ematossilina impiegata, la colorazione di contrasto può produrre un blu più o meno scuro nel nucleo ( ) P04087IT_01_K / p. 36/55
37 Carcinoma gastrico della cellula. Una colorazione di contrasto eccessiva o incompleta può compromettere l interpretazione dei risultati. Fase 4: Montaggio Si consiglia di usare un mezzo di montaggio permanente e non acquoso. Diversamente, è accettabile anche un mezzo di montaggio acquoso. I campioni possono essere montati e coperti con vetrini coprioggetto utilizzando un mezzo di montaggio a base acquosa come Dako Faramount, Codice S3025, oppure Glycergel, Codice C0563. NOTA: è possibile leggere i vetrini in qualunque momento. È tuttavia possibile che si verifichi un certo grado di scolorimento se i vetrini vengono coperti con un mezzo di montaggio acquoso e vengono esposti alla luce intensa per un periodo di una settimana. Per evitare che ciò accada, conservare i vetrini al buio a temperatura ambiente (20 25 C). Controllo di qualità - Gastrico Se le procedure consigliate per la fissazione, il trattamento e l inclusione dei tessuti vengono modificate in laboratorio, è possibile che i risultati presentino una certa variabilità. n tal caso, oltre ad utilizzare i vetrini di controllo forniti da Dako, occorre effettuare tutta una serie di controlli interni con regolarità. Negli Stati Uniti, consultare le linee guida sul controllo di qualità del College of American Pathologists (CAP) Certification Program for Immunohistochemistry e vedere altresì il documento CLSI (precedentemente NCCLS) Quality Assurance for Immunocytochemistry, Approved Guideline (24) e il riferimento 25 per ulteriori informazioni. ( ) P04087IT_01_K / p. 37/55
38 Carcinoma gastrico Tabella 8. L obiettivo del controllo di qualità quotidiano. Tessuto: fissato e trattato come il campione del paziente Controllo positivo: tessuti o cellule che contengono l antigene bersaglio da individuare (potrebbe essere presente nel tessuto del paziente). Il controllo ideale è un tessuto con una colorazione positiva debole, in quanto è più sensibile al deterioramento dell anticorpo o dell antigene. Anticorpo specifico e anticorpo secondario Controllo di tutte le fasi dell analisi. Convalida delle procedure e dei reagenti utilizzati per la colorazione HER2. Anticorpo non specifico* o tampone + anticorpo secondario come utilizzato con l anticorpo specifico Rilevamento della colorazione di fondo aspecifica. Controllo negativo: tessuto o cellule che si presume negativi (potrebbero trovarsi nel tessuto del paziente o nel tessuto di controllo positivo). Rilevamento di una reattività crociata indesiderata dell anticorpo rispetto alle cellule e/o ai componenti cellulari. Rilevamento della colorazione di fondo aspecifica. Tessuto del paziente Rilevamento della colorazione specifica. Rilevamento della colorazione di fondo aspecifica. Vetrino di controllo fornito da Dako Controllo della sola procedura di colorazione. * Siero proveniente dalla stessa specie dell anticorpo specifico, ma non diretto contro lo stesso antigene bersaglio. Per individuare legami aspecifici con l anticorpo, ad es. legame della porzione Fc dell anticorpo ad opera del tessuto. Vetrino di controllo (fornito): tutti i vetrini di controllo forniti nel kit contengono tre linee cellulari umane pellettizzate, fissate in formalina e incluse in paraffina, con valori di intensità di colorazione pari a 0, 1+ e 3+. È necessario utilizzare un vetrino in ogni procedura di colorazione. Valutando le linee cellulari sul vetrino di controllo fornito da Dako è possibile verificare la validità della procedura di colorazione. Tessuto di controllo positivo: i controlli dovrebbero essere costituiti da campioni freschi di autopsia/biopsia/chirurgia che sono stati fissati, trattati e inclusi in paraffina nei tempi più brevi possibili, seguendo la medesima procedura utilizzata per i campioni dei pazienti da analizzare. I controlli positivi confermano se i tessuti sono stati preparati correttamente e se sono state adottate tecniche di colorazione corrette. È necessario includere un tessuto di controllo positivo per ogni set di condizioni di analisi previsto in ogni ciclo di colorazione. I controlli positivi devono produrre una colorazione positiva debole, così da evidenziare variazioni leggere nella sensibilità dell anticorpo primario. Se trattati diversamente dai campioni dei pazienti, i vetrini di controllo di questo kit o i campioni consentono di convalidare soltanto il rendimento del reagente, ma non di verificare la preparazione del tessuto. Utilizzare come controllo positivo ideale un tessuto di adenocarcinoma gastrico con giunzione gastroesofagea in cui l'iperespressione di proteina HER2 abbia prodotto un risultato di positività 2+ in un test precedente. NOTA: i controlli positivi noti devono essere utilizzati esclusivamente per verificare il corretto rendimento dei tessuti trattati e dei reagenti per analisi, NON per formulare una diagnosi specifica dei campioni dei pazienti. Se i controlli positivi non producono una colorazione positiva, significa che i risultati ottenuti con i campioni dei pazienti analizzati non sono da ritenersi validi. ( ) P04087IT_01_K / p. 38/55
39 Carcinoma gastrico Tessuto di controllo negativo: in ogni ciclo di colorazione è necessario utilizzare un tessuto di controllo negativo (negativo alla proteina HER2) che sia stato fissato, trattato e incluso in paraffina secondo la medesima procedura adottata per i campioni dei pazienti da analizzare. In questo modo è possibile verificare la specificità dell anticorpo primario e fornire un indicazione della colorazione di fondo specifica. Il colon, il fegato e la tiroide sono idonei ad essere impiegati come tessuti di controllo negativi. Molteplici tipi di cellule presenti nella maggior parte delle sezioni tissutali offrono siti interni di controllo negativo (è necessaria una verifica dell utente). Se si osserva una colorazione specifica nel tessuto di controllo negativo, i risultati ottenuti con i campioni dei pazienti analizzati non sono da ritenersi validi e il test deve essere rieseguito. Reagente di controllo negativo non specifico: al posto dell anticorpo primario, è possibile utilizzare il reagente di controllo negativo (fornito nel kit) su una sezione di ogni campione con lo scopo di valutare la colorazione aspecifica e favorire l interpretazione della colorazione specifica nel sito dell antigene. Il periodo di incubazione del reagente di controllo negativo deve corrispondere a quello dell anticorpo primario. Verifica del saggio: prima di utilizzare un anticorpo o un sistema di colorazione in una procedura diagnostica, l utente deve verificare la specificità dell anticorpo analizzandolo su una serie di tessuti archiviati con note caratteristiche di performance immunocitochimica, che rappresentano tessuti positivi o negativi noti. Fare riferimento alle procedure sul controllo della qualità descritte in questa sezione del foglietto illustrativo e ai requisiti descritti nelle istruzioni CAP Certification Program for Immunohistochemistry e/o CLSI (precedentemente NCCLS) Quality Assurance for Immunocytochemistry, Approved Guideline (24). Le procedure per il controllo della qualità vanno ripetute per ogni nuovo lotto di anticorpi o tutte le volte che viene apportata una modifica ai parametri del saggio. Per la verifica del saggio, sono adatti i carcinomi gastrici con giunzione gastroesofagea con intensità di colorazione della proteina HER2 nota nella scala 0-3+ e i tessuti negativi, ad es. colon, fegato o tiroide. Interpretazione della colorazione - Gastrico Ai fini della determinazione dell espressione di proteina HER2, si devono valutare solo il pattern e l intensità della colorazione della membrana, facendo riferimento alla scala dei valori illustrata nella Tabella 9. La valutazione dei vetrini deve essere effettuata da un patologo qualificato, con un microscopio ottico. Per la valutazione della colorazione immunocitochimica e l assegnazione di un punteggio, occorre utilizzare un obiettivo con ingrandimento 10x. Per confermare il punteggio è utile un obiettivo 5 40x. La colorazione citoplasmatica deve essere considerata non specifica e non deve essere inclusa nell accertamento dell intensità di colorazione della membrana (8). Per indicazioni nella differenziazione dei valori di colorazione 0, 1+, 2+, and 3+, fare riferimento alle figure rappresentative di intensità di colorazione riportate nel manuale di interpretazione dell'herceptest per il cancro gastrico di Dako ( HercepTest Interpretation Manual Gastric Cancer ). Limitare la valutazione ai soli campioni provenienti da pazienti affetti da adenocarcinoma gastrico con giunzione gastroesofagea. In caso di metaplasia intestinale e adenocarcinoma gastrico presenti nello stesso campione, limitare la valutazione al solo componente dell'adenocarcinoma gastrico. Per l'interpretazione di campioni bioptici sottoposti a colorazione con HercepTest, si consiglia di utilizzare un gruppo di almeno 5 cellule tumorali sottoposte a colorazione. Un cluster id almeno 5 cellule tumorali sottoposte a colorazione è composto di 5 cellule tumorali sottoposte a colorazione HER connesse. ( ) P04087IT_01_K / p. 39/55
40 Carcinoma gastrico Tabella 9. Interpretazione e punteggio della colorazione immunoistochimica dell HER2 Punteggio Campione chirurgico Pattern di colorazione Campione bioptico Pattern di colorazione Valutazione dell iperespressione HER2 0 reattività o nessuna reattività membranosa in <10% delle cellule tumorali reattività o nessuna reattività membranosa in nessuna cellula tumorale (o <5 in cluster) Negativi 1+ Reattività membranosa scarsamente percettibile in 10% delle cellule tumorali; le cellule sono reattive sono in parte della membrana Cluster di cellule tumorali ( 5 cellule) con una reattività membranosa scarsamente percettibile indipendentemente dalle cellule tumorali sottoposte a colorazione Negativi 2+ Reattività membranosa basolaterale o laterale, completa, da debole a moderata in 10% delle cellule tumorali Cluster di cellule tumorali ( 5 cellule) con una reattività membranosa laterale o basolaterale completa, da debole a moderata, indipendentemente dalle cellule tumorali sottoposte a colorazione Equivoco 3+ Reattività membranosa basolaterale o laterale, completa, forte in 10% delle cellule tumorali Cluster di cellule tumorali ( 5 cellule) con una reattività membranosa laterale o basolaterale completa, forte, indipendentemente dalle cellule tumorali sottoposte a colorazione Positivo Linee guida basate su Hofmann et al. (40) Il test HercepTest produce un risultato di negatività all iperespressione della proteina HER2 (punteggio 0 e 1+), un risultato equivoco (punteggio 2+) e un risultato positivo (punteggio 3+). Il test HercepTest non è idoneo a fornire informazioni prognostiche al paziente e al medico e il suo impiego in questo senso non è stato approvato. Ad ogni ciclo di colorazione, è importante esaminare i vetrini in una sequenza specifica (vedere Tabella 10), in modo da poter determinare la validità della sessione di analisi ed effettuare una valutazione semiquantitativa dell intensità della colorazione del tessuto campione. ( ) P04087IT_01_K / p. 40/55
41 Carcinoma gastrico Tabella 10. Ordine di valutazione dei vetrini. Ordine di lettura dei vetrini Logica 1. Vetrino di controllo contenente le tre linee cellulari Un saggio valido è indicato dalla presenza di colorazione marrone 3+ della membrana cellulare (orletto) nella linea cellulare di controllo 3+ SK-BR-3, di orletto parziale marrone nella linea cellulare MDA-175 di controllo 1 + e da assenza di colorazione nella linea cellulare di controllo 0 MDA-231. Una colorazione della membrana discontinua e puntiforme è presente in un numero da piccolo a moderato di cellule nella linee cellulare di controllo 1 + debolmente positiva. In questa linea cellulare si può anche osservare una immunocolorazione puntiforme nella regione dei Golgi del citoplasma. Presenza di colorazione marrone nella linea cellulare di controllo 0 (Control Cell Line MDA-231), ovvero negatività alla proteina HER2. Indica che non c è stata colorazione aspecifica durante il test. I risultati del saggio possono essere non validi a causa di eccessiva colorazione. 2. Vetrino con il tessuto di controllo positivo Possibile presenza di colorazione marrone della membrana. La colorazione del citoplasma e dei tessuti negativi non deve essere superiore a Vetrino con il tessuto di controllo negativo L ASSENZA di colorazione specifica nel tessuto di controllo negativo conferma l assenza di reattività crociata con cellule/componenti cellulari. In caso di colorazione specifica di membrana nel vetrino del tessuto di controllo negativo, i risultati ottenuti con i campioni dei pazienti devono essere considerati non validi. 4. Vetrino con il tessuto del paziente, colorato con il reagente di controllo negativo 5. Vetrino con il tessuto del paziente, colorato con l anticorpo primario L assenza di colorazione di membrana specifica conferma la marcatura specifica dell antigene bersaglio da parte dell anticorpo primario. Una ulteriore colorazione marrone nel citoplasma del campione trattato con il reagente di controllo negativo, come per esempio nel tessuto connettivo, nei leucociti, negli eritrociti o nel tessuto necrotico, deve essere considerata come una colorazione di fondo non specifica e deve essere riportata nella sezione dei commenti del foglio dei dati. L iperespressione della proteina HER2 nel campione si manifesta come un orletto marrone localizzato sulla membrana cellulare delle cellule tumorali trattate con l anticorpo primario. 1. Vetrino di controllo (fornito): il primo vetrino di controllo da analizzare è quello sottoposto a colorazione con HercepTest, il quale consente di verificare il corretto funzionamento di tutti i reagenti. La presenza di un prodotto della reazione di colore marrone (3,3 -diaminobenzidina, DAB) in corrispondenza della membrana cellulare indica reattività positiva. Un test valido è confermato da: presenza di colorazione marrone (rimming) nella circonferenza della membrana cellulare per quanto riguarda la linea cellulare di controllo 3+ (Control Cell Line SK-BR-3); rimming parziale marrone per quanto riguarda la linea cellulare di controllo 1+ (Control Cell Line MDA-175); colorazione assente per quanto riguarda la linea cellulare di controllo 0 (Control Cell Line MDA-231). Se anche una sola delle linee cellulari di controllo fornite produce risultati che esulano dai criteri descritti, tutti i risultati ottenuti con i campioni dei pazienti sono da ritenersi non validi. 2. Tessuto di controllo positivo: il secondo vetrino da analizzare è quello con il tessuto di controllo positivo. Questo vetrino consente di verificare l efficacia del metodo di fissazione e del processo di recupero dell epitopo. Per l interpretazione dei risultati della colorazione, prendere in considerazione le cellule intatte, in quanto le cellule necrotiche o degradate assumono spesso una colorazione aspecifica (26). La colorazione del tessuto tumorale deve essere marrone e interessare la membrana cellulare. Il citoplasma e i tessuti negativi all interno del campione possono colorarsi di marrone, tuttavia l intensità di questa colorazione non deve superare il punteggio 1+. ( ) P04087IT_01_K / p. 41/55
42 Carcinoma gastrico 3. Tessuto di controllo negativo: il vetrino del tessuto di controllo negativo deve essere analizzato dopo il tessuto di controllo positivo per verificare la specificità della marcatura dell antigene ricercato da parte dell anticorpo primario. L assenza di colorazione specifica nel tessuto di controllo negativo conferma l assenza di reattività crociata del kit con cellule/componenti cellulari. Se si osserva una colorazione specifica nel tessuto di controllo negativo, i risultati ottenuti con i campioni dei pazienti analizzati non sono da ritenersi validi. In alternativa, è possibile utilizzare alcune di queste porzioni negative nel tessuto di controllo positivo a mo di controlli negativi (è necessaria una verifica dell utente). Si fa presente che si può osservare una reazione debole (intensità di colorazione 0-1+) nella maggior parte del tessuto epiteliale normale. Possono essere impiegati come tessuti di controllo negativi il colon, il fegato e la tiroide. Se è presente, la colorazione aspecifica apparirà piuttosto diffusa. È possibile osservare anche la colorazione sporadica del tessuto connettivo nelle sezioni sottoposte ad eccessiva fissazione in formalina Tessuto del paziente: in ultimo esaminare i campioni dei pazienti sottoposti a colorazione con HercepTest. L intensità della colorazione positiva deve essere valutata tenendo conto di possibili colorazioni di fondo aspecifiche ad opera del reagente di controllo negativo. Come accade per tutti gli esami immunocitochimici, un risultato negativo significa che l antigene ricercato non è stato trovato, ma non significa che l antigene non è presente nelle cellule e nei tessuti analizzati. Per informazioni specifiche sulla immunoreattività del test HercepTest, vedere i paragrafi Cenni introduttivi, Limiti e Caratteristiche prestazionali. Altri suggerimenti per interpretare correttamente i risultati della colorazione con HercepTest Gli adenocarcinomi gastrici con giunzione gastroesofagea sottoposti a test per individuare l'iperespressione della proteina HER2 vengono valutati su una scala da 0 a 3+. Mentre per i casi con punteggio 0 e 3+ l interpretazione è chiara, una piccola percentuale residua di campioni con punteggi 1+ e 2+ è più difficile da classificare. Per l interpretazione della colorazione con HercepTest in laboratorio, è possibile attenersi alle seguenti linee guida. Valutare sempre le linee cellulari di controllo per convalidare il rendimento del test. Valutare sia i vetrini di controllo positivi, sia i vetrini di controllo negativi. Si consiglia di colorare i campioni dei tessuti con ematossilina ed eosina (H&E), almeno per la prima valutazione. (La ragione è che il tumore potrebbe non essere evidente ad una prima osservazione del campione colorato con HercepTest. Il vetrino colorato con ematossilina - eosina serve al patologo per verificare la presenza del tumore.). HercepTest TM deve essere eseguito su una sezione appaiata (sezione seriale) proveniente dallo stesso blocco di paraffina del campione. Valutare la presenza di iperespressione della proteina HER2 nelle sezioni utilizzando prima un ingrandimento basso: la maggior parte dei casi positivi è già evidente con un ingrandimento basso. Per verificare la colorazione della membrana, utilizzare un obiettivo con un ingrandimento di 20 40x per i casi con punteggio 1+. Per verificare la colorazione della membrana, utilizzare un obiettivo con un ingrandimento di 10 20x per i casi con punteggio 2+. Campione chirurgico Per determinare la percentuale di cellule tumorali positive, scegliere le aree del campione meglio conservate e colorate. Se si è colorata la membrana laterale o basolaterale nella maggioranza delle cellule tumorali, il punteggio è 2+ o 3+. ( ) P04087IT_01_K / p. 42/55
43 Carcinoma gastrico Se la membrana laterale o basolaterale si è colorata completamente con un intensità forte in una percentuale pari o superiore al 10% delle cellule tumorali nei campioni chirurgici, il punteggio da assegnare al campione è 3+. Se la membrana laterale o basolaterale si è colorata completamente con un intensità da debole a moderata in una percentuale pari o superiore al 10% delle cellule tumorali nei campioni chirurgici, il punteggio da assegnare al campione è 2+. Se una percentuale pari o superiore al 10% delle cellule tumorali nei campioni chirurgici presenta una colorazione scarsamente percettibile solo parziale della membrana, il punteggio del campione Se la percentuale di cellule tumorali nei campioni chirurgici con una colorazione parziale, indipendentemente dal pattern di colorazione (ad es. completo, basolaterale o laterale o parte della membrana), inferiore al 10%, il punteggio è 0. Se non si evidenzia alcuna colorazione, il punteggio del campione chirurgico è 0. Campione bioptico Un cluster id almeno 5 cellule tumorali sottoposte a colorazione è composto di 5 cellule tumorali sottoposte a colorazione HER connesse. Se è presente un cluster di cellule tumorali di almeno 5 cellule tumorali sottoposte a colorazione con una colorazione membranosa laterale o basolaterale completa forte, il punteggio del campione bioptico è 3+, indipendentemente dalla percentuale di cellule tumorali sottoposte a colorazione. Se è presente un cluster di cellule tumorali di almeno 5 cellule tumorali sottoposte a colorazione con una colorazione membranosa laterale o basolaterale completa da debole a moderata, il punteggio del campione bioptico è 2+, indipendentemente dalla percentuale di cellule tumorali sottoposte a colorazione. Se è presente un cluster di cellule tumorali di almeno 5 cellule tumorali sottoposte a colorazione con una colorazione membranosa scarsamente percettibile e parziale della membrana, il punteggio del campione bioptico è 1+, indipendentemente dalla percentuale di cellule tumorali sottoposte a colorazione. Se non si evidenzia alcuna colorazione, il punteggio del campione bioptico è 0. Se si evidenzia una colorazione della membrana (indipendentemente dall'intensità della colorazione) in meno di 5 cellule tumorali del gruppo, il punteggio del campione bioptico è 0. Limitazioni - Gastrico Limiti generali 1. L immunocitochimica è una tecnica diagnostica multifase che richiede un addestramento specifico per quanto riguarda la scelta dei reagenti appropriati, la selezione, la fissazione e il trattamento dei tessuti, la preparazione del vetrino per l analisi immunocitochimica e l interpretazione dei risultati della colorazione. 2. La colorazione del tessuto dipende dal modo in cui il tessuto viene pretrattato. Una fissazione eseguita in maniera scorretta, il congelamento, lo scongelamento, il lavaggio, l essiccazione, il riscaldamento, il sezionamento o la contaminazione con altri tessuti o fluidi possono produrre artefatti, intrappolare l anticorpo o generare risultati falsi-negativi. Risultati incoerenti possono essere provocati anche da modifiche apportate ai metodi di fissazione e di inclusione o da irregolarità intrinseche del tessuto. ( ) P04087IT_01_K / p. 43/55
44 Carcinoma gastrico 3. Una colorazione di contrasto eccessiva o incompleta può compromettere l interpretazione dei risultati. 4. L interpretazione clinica di qualsiasi colorazione positiva o assenza di colorazione non può prescindere dal contesto della presentazione clinica, della morfologia e di altri criteri istopatologici L interpretazione clinica di qualunque colorazione o della sua assenza deve essere completata da studi morfologici e da controlli adeguati nonché da altri test diagnostici. L interpretazione della colorazione è compito di un patologo qualificato, che deve avere una profonda conoscenza degli anticorpi, dei reagenti e dei metodi impiegati. La colorazione deve essere eseguita in un laboratorio autorizzato certificato, sotto la supervisione di un patologo, il quale esaminerà i vetrini colorati e garantirà la correttezza dei controlli positivi e negativi. 5. I tessuti delle persone infette dal virus dell epatite B e contenenti l antigene di superficie dell epatite B (HBsAg) possono essere interessati da una colorazione aspecifica con la perossidasi di rafano (27). I reagenti potrebbero provocare reazioni impreviste in tipi di tessuto mai analizzati in passato. Inoltre non è escluso che possano verificarsi reazioni impreviste anche in tipi di tessuti già analizzati in passato, vista l elevata variabilità biologica dell espressione antigenica nelle neoplasie o in altri tessuti patologici (28). In caso di reazioni inattese documentate, contattare il Customer Support di Dako. 6. È possibile ottenere falsi positivi a causa del legame non immunologico di proteine o di prodotti di reazione del substrato. Falsi positivi possono essere causati anche dall attività della pseudoperossidasi (eritrociti) e dall attività della perossidasi endogena (citocromo C) (28). 7. La procedura di colorazione deve essere eseguita a temperatura ambiente (20 25 C). Limiti specifici del prodotto 1. L antigene presente nella linea cellulare di controllo 1+ (Control Cell Line MDA-175) è destinato a degradarsi nel tempo. Valutare i risultati del vetrino di controllo tenendo conto della data di scadenza del vetrino. La colorazione negativa delle cellule MDA-175 potrebbe indicare soltanto che il vetrino di controllo si è deteriorato. Conservare i vetrini di controllo a 2 8 C. 2. Il deterioramento dell antigene nel tessuto, nel tempo, può provocare risultati falsi-negativi. I campioni devono essere colorati entro 4-6 settimane dal montaggio dei tessuti sui vetrini, quando sono conservati a temperatura ambiente (20 25 C) (29). 3. Per garantire risultati ottimali e riproducibili, la proteina HER2 richiede il recupero dell epitopo termoindotto quando i tessuti sono fissati in formalina tamponata neutra e inclusi in paraffina secondo i metodi convenzionali. Questo pretrattamento deve essere completato all inizio dell intero processo di colorazione. Per ulteriori istruzioni, consultare la sezione Preparazione dei campioni, Trattamento dei tessuti prima della colorazione. 4. Per lo smascheramento termoindotto degli epitopi della proteina HER2, impiegare solamente un bagnomaria calibrato. Sono stati sperimentati altri metodi di riscaldamento, che tuttavia non hanno dato risultati riproducibili. 5. Non sostituire i reagenti del kit con reagenti che abbiano numeri di lotto diversi, né con reagenti di altri produttori. La sola eccezione riguarda il tampone di lavaggio, che può essere sostituito da DakoCytomation Wash Buffer, Codice S Dalla valutazione della colorazione del citoplasma si possono ottenere risultati falsi. Ai fini dell interpretazione della colorazione, tenere conto esclusivamente della colorazione della membrana cellulare. 7. I vetrini di controllo che si colorano servono esclusivamente per verificare la validità del ciclo di colorazione e non devono essere impiegati per assegnare un punteggio alla colorazione delle sezioni di tessuto. 8. Di tanto in tanto è possibile che si formino i cosiddetti hot spot, ovvero punti circoscritti con una colorazione focale intensa (3+). La presenza di questi hot spot potrebbe essere dovuta ad una procedura di fissazione e/o trattamento del tessuto non uniforme. In questi ( ) P04087IT_01_K / p. 44/55
45 Carcinoma gastrico casi, si consiglia di procedere all immunocolorazione di un secondo blocco di tessuto appartenente allo stesso campione. 9. Non è stato approvato l uso del test HercepTest su campioni trattati con fissativi diversi dalla formalina tamponata neutra. 10. Gli epiteli normali di tonsille ed esofago possono colorarsi con un intensità fino a Deve essere evitato l uso di campioni di cancro gastrico frantumati e l interpretazione della colorazione degli artefatti attorno a un bordo bioptico. Caratteristiche prestazionali - Gastrico Dati di base La sicurezza e l efficacia di trastuzumab (Herceptin ) è stata dimostrata in uno studio clinico (lo studio ToGA) (38, 39). Lo studio è stato pensato come uno studio di fase III multicentro, randomizzato in aperto in pazienti positivi all HER2 con adenocarcinoma gastrico in stadio avanzato localmente non operabile, ricorrente e/o metastatico dello stomaco o della giunzione gastroesofagea. Nello studio ToGA, la positività all HER2 è stata definita come positiva all IHC (3+) (HercepTest, Dako) e/o positiva tramite HER2 FISH (HER2/CEN17 2,0) (Kit HER2 FISH pharmdx, Dako). Dopo l inclusione nello studio, i pazienti sono stati sottoposti in maniera randomizzata a chemioterapia (5-FU o capecitabina e cisplatina) o chemioterapia più trastuzumab. L endpoint primario dello studio era la sopravvivenza complessiva (OS). Nello studio, sono stati randomizzati in totale 594 pazienti e 584 pazienti hanno assunto il farmaco di studio e sono stati inclusi nell intero insieme di analisi (FAS, full analyses set). Per l endpoint primario, la combinazione di chemioterapia più trastuzumab si è dimostrata statisticamente superiore rispetto alla sola chemioterapia. L OS mediana è aumentata da 11,1 a 13,8 mesi (p=0,0046), con un rapporto di pericolo di 0,74 (IC 95%: 0,60 0,91). Le curve di Kaplan-Meier per l OS sono mostrate in Figura 1. Probabilità di sopravvivenza 1,0 0,9 0,8 0,7 Test Log-rank P = 0,0046 0,6 0,5 0,4 0,3 0,2 0,1 0 11,1 13,8 Tempo (mesi) N. rimasti Fluoro/Cisp Tras/Fluoro/Cisp Gruppo di trattamento Fluoro/Cisp Tras/Fluoro/Cisp ( ) P04087IT_01_K / p. 45/55
46 Figura 1. Curva di Kaplan-Meier curve dell OS (n=584). Carcinoma gastrico Analisi di sottogruppi esplorativi pre-specificati per stato HER2 sono stati eseguiti quando sono stati disponibili i dati. Due nuovi sottogruppi HER2 sono stati definiti posthoc in base alla valutazione IHC: Gruppo 1 ( gruppo con espressione bassa dell HER2 ): Gruppo 2 ( gruppo con espressione elevata dell HER2 ): IHC 0/FISH+ e IHC 1+/FISH+ (n=131) IHC 2+/FISH+ e IHC 3+ compresi IHC 3+(FISH positivo o FISH negativo o FISH nessun risultato (n=446)) In occasione della ripetizione dell analisi primaria sull OS per il gruppo con espressione elevata dell HER2 (n=446), il beneficio in favore del trattamento combinato è risultato ancora maggiore. L OS mediana per il gruppo di pazienti sottoposti a chemioterapia più trastuzumab è aumentata a 16,0 mesi rispetto agli 11,8 mesi per i pazienti sottoposti solo a chemioterapia. Il rapporto di pericolo per questa analisi è sceso a 0,65 (95 % CI: 0,51 0,83). Le curve di Kaplan-Meier per l OS per il gruppo con espressione elevata dell HER2 sono mostrate in Figura 2. Probabilità di sopravvivenza 1,0 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0 11,8 16,0 Tempo (mesi) N. rimasti Fluoro/Cisp Tras/Fluoro/Cisp Gruppo di trattamento Fluoro/Cisp Tras/Fluoro/Cisp Figura 2. Curva di Kaplan-Meier per l OS per il gruppo con espressione elevata dell HER2 (n=446). Lo studio ToGA ha mostrato che la combinazione dei test IHC e FISH è predittiva dell effetto del trattamento combinato con chemioterapia e trastuzumab; tuttavia, l analisi esplorativa post-hoc sembra indicare che livelli elevati della proteina HER2 (IHC2+/FISH+ and IHC3+) offra benefici maggiori. Ciò può essere spiegato dal fatto che la proteina è il target per trastuzumab. Per ulteriori informazioni sullo studio ToGA, vedere il foglietto illustrativo dell Herceptin. ( ) P04087IT_01_K / p. 46/55
47 Riproducibilità Carcinoma gastrico Riproducibilità intra-ciclo: la riproducibilità nella serie è stata studiata in un laboratorio utilizzando 3 campioni con punteggi di intensità della colorazione IHC diversi. Ogni campione è stato elaborato in triplicato. Il protocollo è stato applicato con un sistema di colorazione automatizzato. Tutti i campioni hanno generato risultati riproducibili al 100%. La riproducibilità nella serie è stata studiata in un laboratorio utilizzando 11 campioni con punteggi di colorazione IHC diversi. Ogni campione è stato elaborato in triplicato. Questo protocollo è stato utilizzato con colorazione manuale. Tutti i campioni hanno generato risultati riproducibili al 100%. Riproducibilità tra serie e fra laboratori: le analisi HercepTest su 60 diversi campioni di cancro gastrico ottenuti da aree dello stomaco o da aree di giunzione gastroesofagea, risultati di resezioni chirurgiche e biopsie, sono state eseguite in cinque giorni non consecutivi, in tre siti di studio. I 60 campioni dello studio erano equamente distribuiti nelle tre categorie di stato dell'her2. Sei patologi hanno eseguito un totale di valutazioni dell'her2. La concordanza tra giorni (negativa, equivoca, positiva) ha assunto valori variabili tra l'83,1% e il 98,3%. In 47 dei 60 possibili confronti, la concordanza è stata del 90,0% o superiore. Nella Tabella 1 vengono mostrati alcuni esempi dei confronti tra un giorno e l'altro, con concordanze medie pari a 91,2%, 92,5% e 92,% per i tre siti. Le concordanze tra siti, nei confronti tra coppie di siti, sono state rispettivamente pari all'82,7%, al 75,0% e all'88,0% (vedere Tabella 12). Secondo quanto riportato nel testo di Fisher, non vi sono state differenze di risultati tra un sito e l'altro. Le concordanze tra osservatori riferite ai patologi di ciascun sito sono state pari all'88,0% nel Sito 1, all'83,6% nel Sito 2 e all'81,0% nel Sito 3 (Tabella 13). In conclusione, le analisi HercepTest sui campioni di cancro gastrico svolte in tre siti di studio hanno evidenziato un buon livello di concordanza tra le osservazioni, con riferimento ai giorni, ai siti e agli osservatori. Tabella 11. Concordanze complessive tra giorni in percentuale - 12 confronti su 60 Sito 1 Sito 2 Sito 3 Osservatore 1 Osservatore 2 Concordanza Concordanza CI95 LL 1 Concordanza CI95 LL 1 media Giorno 1 rispetto a giorno 2 85,0 74,4 93,3 84,9 Giorno 3 rispetto a giorno 4 93,3 84,9 93,3 84,9 Giorno 1 rispetto a giorno 2 95,0 87,3 83,1 72,0 Giorno 3 rispetto a giorno 4 96,7 89,7 95,0 87,3 Giorno 1 rispetto a giorno 2 90,0 80,5 91,7 82,7 Giorno 3 rispetto a giorno 4 96,7 89,7 91,7 82,7 1 CI95 LL: intervallo di confidenza del limite inferiore 95%. 91,2 92,5 92,5 Tabella 12. Concordanze complessive tra siti in percentuale Concordanza CI95 LL 1 Concordanza media Sito 1 rispetto a sito 2 Sito 1 rispetto a sito 3 Giorno 1 rispetto a giorno 1 83,3 72,4 Giorno 2 rispetto a giorno 2 85,0 74,4 Giorno 3 rispetto a giorno 3 85,0 74,4 Giorno 4 rispetto a giorno 4 81,7 70,5 Giorno 5 rispetto a giorno 5 78,3 66,7 Giorno 1 rispetto a giorno 1 80,0 68,6 Giorno 2 rispetto a giorno 2 73,3 61,2 Giorno 3 rispetto a giorno 3 78,3 66,7 Giorno 4 rispetto a giorno 4 68,3 55,9 Giorno 5 rispetto a giorno 5 75,0 63,0 82,7 75,0 ( ) P04087IT_01_K / p. 47/55
48 Carcinoma gastrico Sito 2 rispetto a sito 3 Giorno 1 rispetto a giorno 1 88,3 78,5 Giorno 2 rispetto a giorno 2 86,7 76,4 Giorno 3 rispetto a giorno 3 90,0 80,5 Giorno 4 rispetto a giorno 4 86,7 76,4 Giorno 5 rispetto a giorno 5 88,3 78,5 1 CI95 LL: intervallo di confidenza del limite inferiore 95%. 88,0 ( ) P04087IT_01_K / p. 48/55
49 Carcinoma gastrico Tabella 13. Concordanze tra osservatori in percentuale Concordanza CI 95 LL 1 Concordanza media Sito 1 Giorno 1 91,7 82,7 Giorno 2 91,7 82,7 Giorno 3 93,3 84,9 88,0 Sito 2 Sito 3 Giorno 4 83,3 72,4 Giorno 5 80,0 68,6 Giorno 1 86,4 76,0 Giorno 2 83,3 72,4 Giorno 3 83,3 72,4 Giorno 4 83,3 72,4 Giorno 5 81,7 70,5 Giorno 1 80,0 68,6 Giorno 2 78,3 66,7 Giorno 3 80,0 68,6 Giorno 4 78,3 66,7 Giorno 5 90,0 80,5 83,6 81,0 1 CI95 LL: intervallo di confidenza del limite inferiore 95%. Immunoreattività La Tabella 14 fornisce un quadro dell immunoreattività all HercepTest relativamente alla serie di tessuti normali selezionati. Tutti i tessuti sono stati fissati in formalina e inclusi in paraffina e colorati con HercepTest seguendo le istruzioni riportate nell inserto della confezione. Tabella 14. Sommario della reattività a HercepTest dei tessuti normali Tipo di tessuto (n di campioni) Surrenale (3) Midollo osseo (3) Cervello/Cervelletto (3) Cervello/Cervelletto (3) Mammella (3) Collo dell utero (3) Colon (3) Esofago (3) Cuore (3) Rene (3) Fegato (3) Polmone (3) Cellule mesoteliali (3) Ovaio (3) Pancreas (3) Paratiroide (3) Nervo periferico (3) Pituitaria (3) Prostata (3) Ghiandola salivare (3) Muscolo scheletrico (3) Pelle (3) Intestino tenue (3) Milza (3) Stomaco (3) Testicolo (3) Timo (3) Tiroide (3) Tonsilla (3) Utero (3) Colorazione positiva dell elemento tissutale e pattern di colorazione Ghiandola mammaria (1/3 dei tessuti, intensità di colorazione 1+) Tubuli di midollo renale (3/3 dei tessuti, 1-2 in 5-50% di cellule, citoplasmatica) Ghiandola prostatica/dotti (3/3 dei tessuti, intensità di colorazione 1+, 50% delle cellule, citoplasmatica) Ghiandole sudoripare (1/3 dei tessuti, 1+, 30% delle cellule, citoplasmatica) Epitelio colonnare, superficie (1/3 dei tessuti, intensità di colorazione +2, 25% delle cellule) Epitelio (1/3 dei tessuti, intensità di colorazione +1, 25% delle cellule) Epitelio squamoso (1/3 dei tessuti, intensità di colorazione 1+, 80% delle cellule) In tutti i tessuti è stata riscontrata la colorazione della membrana, salvo diversa segnalazione. L intensità della colorazione di tutti e tre i campioni di ogni tipo di tessuto era la stessa, salvo diversa segnalazione. ( ) P04087IT_01_K / p. 49/55
50 Risoluzione dei problemi - Gastrico Carcinoma gastrico Fare riferimento alla sezione Eventuali problemi e risoluzione nel manuale Dako precedentemente citato (19) per gli interventi riparativi, oppure contattare il Customer Support Dako per riportare eventuali colorazioni inattese. Problema Probabile causa Intervento consigliato 1. colorazione dei vetrini 1a. Errore di programmazione. Reagenti non usati nell ordine adeguato 1a. Controllare la griglia di programmazione per verificare che il ciclo di colorazione sia stato programmato correttamente 2. Colorazione debole dei vetrini 1b. Le fiale dei reagenti non sono state caricate nelle posizioni corrette nei raccoglitori portareagenti 1c. La quantità di reagente nella fiala è insufficiente 1d. Azide sodica nella soluzione di lavaggio 1e. Un riscaldamento eccessivo di sezioni di tessuto montate prima della deparaffinazione e del recupero dell antigene indotto dal calore può portare alla perdita di immunoreattività HER2 visibile. 2a. Smascheramento degli epitopi inadeguato 2b. Tempo di incubazione dei reagenti inadeguato 2c. È stato usato un metodo di fissazione inadeguato 2d. Un riscaldamento eccessivo di sezioni di tessuto montate prima della deparaffinazione e del recupero dell antigene indotto dal calore può provocare una diminuzione significativa dell immunoreattività HER2 visibile. 1b. Controllare la Mappa dei reagenti per verificare il corretto posizionamento delle fiale dei reagenti 1c. Assicurarsi che il reagente sia caricato in quantità sufficiente nelle fiale prima dell avvio del ciclo. Fare riferimento alla Mappa dei reagenti per i volumi richiesti 1d. Utilizzare la preparazione fresca di tampone di lavaggio fornita nel kit 1e. Far asciugare all aria le sezioni di tessuto a temperatura ambiente per un minimo di 12 ore o fino al completamento dell asciugatura. In alternativa, asciugare a 37 C durante la notte o asciugare a 60 C per un massimo di un ora. L asciugatura di sezioni di tessuto a temperature elevate deve essere eseguita solo in un forno calibrato con distribuzione uniforme del calore (17). 2a. Verificare che la soluzione Epitope Retrieval Solution raggiunga C per 40 minuti e che venga lasciata raffreddare per altri 20 minuti 2b. Rivedere le istruzioni sulla procedura di colorazione 2c. Assicurarsi che il tessuto del paziente non sia eccessivamente fissato o che non sia stato utilizzato un metodo di fissazione alternativo 2d. Far asciugare all aria le sezioni di tessuto a temperatura ambiente per un minimo di 12 ore o fino al completamento dell asciugatura. In alternativa, asciugare a 37 C durante la notte o asciugare a 60 C per un massimo di un ora. L asciugatura di sezioni di tessuto ( ) P04087IT_01_K / p. 50/55
51 3. Eccessiva colorazione di sfondo dei vetrini 2e. Volume di reagente applicato insufficiente. 3a. La paraffina è stata rimossa solo parzialmente 3b. Additivi a base di amido utilizzati nel montaggio delle sezioni sui vetrini 3c. I vetrini non sono stati completamente lavati 3d. Le sezioni si sono seccate durante la procedura di colorazione 3e. Sezioni essiccate durante il caricamento su Autostainer 3f. È stato usato un metodo di fissazione inadeguato Carcinoma gastrico a temperature elevate deve essere eseguita solo in un forno calibrato con distribuzione uniforme del calore (17). 2e. Verificare le dimensioni della sezione di tessuto (22 mm x 22 mm) e il volume di reagente applicato. 3a. Usare soluzioni di chiarificazione nuove e seguire la procedura come indicato nella sezione B.1 3b. Evitare l uso di additivi amidacei per fare aderire le sezioni ai vetrini. Molti additivi sono immunoreattivi 3c. Prima di avviare il ciclo, verificare che il sistema Autostainer sia stato sottoposto a priming. Controllare che il tampone caricato sia sufficiente per l intero ciclo di analisi. Utilizzare soluzioni di tampone e di lavaggio fresche 3d. Controllare che sui vetrini sia stato applicato il volume di reagente corretto. Assicurarsi che durante il funzionamento il coperchio dello strumento Autostainer sia in posizione chiusa e che lo strumento non sia esposto a calore eccessivo o a correnti d aria 3e. Assicurarsi che le sezioni rimangano bagnate con tampone durante il caricamento e prima dell avvio del ciclo 3f. Controllare che sia stato utilizzato un fissativo approvato. Altri fissativi possono causare una eccessiva colorazione di fondo 4. Il tessuto si stacca dai vetrini 5. Colorazione specifica eccessivamente forte 3g. Legame aspecifico di reagenti al tessuto 3g. Controllare il metodo di fissazione del campione e la presenza di necrosi 4a. Uso di vetrini errati 4a. Utilizzare vetrini silanizzati, come per esempio Dako Silanized Slides, Codice S3003, SuperFrost Plus o vetrini polilisinati 5a. È stato usato un metodo di fissazione inadeguato 5b. Uso di una inadeguata fonte di calore per lo smascheramento degli epitopi, p.e. pentola a pressione, forno a microonde o autoclave 5a. Assicurarsi che vengano utilizzati solamente fissativi e metodi di fissazione appropriati 5b. Assicurarsi che venga utilizzato solamente il trattamento a bagnomaria per la fase di smascheramento degli epitopi ( ) P04087IT_01_K / p. 51/55
52 Carcinoma gastrico 6. Debole colorazione della linea cellulare del vetrino di controllo La soluzione Epitope Retrieval Solution ha un aspetto torbido quando viene riscaldata 8. La soluzione Epitope Retrieval Solution ha un aspetto torbido durante la conservazione (prima di scaldarla) 5c. Tempi di incubazione reagente troppo lunghi 5d. È stata usata una soluzione di lavaggio inadeguata 6a. Protocollo inadatto per lo smascheramento degli epitopi 6b. Mancanza di reazione con la soluzione substrato-cromogeno (DAB) 6c. Degradazione del vetrino di controllo 7. Quando viene riscaldata, la soluzione assume un aspetto torbido 8. La soluzione è stata conservata in modo scorretto, oppure ne è stata superata la data di scadenza 5c. Rivedere le istruzioni sulla procedura di colorazione 5d. Usare solo il tampone di lavaggio consigliato per il kit 6a. Immergere i vetrini nella soluzione di smascheramento degli epitopi preriscaldata. Riportare la temperatura della soluzione di smascheramento a C e pretrattare per 40 minuti 6b. Assicurarsi che venga rispettato il tempo di incubazione di 10 minuti. Assicurarsi che venga aggiunta solamente una goccia di cromogeno DAB ad 1 ml di substrato tamponato DAB 6c. Controllare la data di scadenza del kit e le condizioni di conservazione del kit riportate all esterno della confezione 7. Ciò è normale e non influisce sulla colorazione. 8. Controllare la data di scadenza e le condizioni per la conservazione del kit stampate all esterno della confezione. Gettare via la soluzione di recupero dell'epitopo. NOTA: se il problema verificatosi non può essere attribuito ad alcuna delle cause riportate sopra, oppure se l azione correttiva suggerita non consente la risoluzione del problema, si prega di contattare il Customer Support Dako per ulteriore assistenza. Ulteriori informazioni sulle tecniche di colorazione e sulla preparazione dei campioni sono disponibili nel manuale Dako precedentemente citato (19) (disponibile presso Dako) in Atlas of Immunohistology (30) e in Immunoperoxidase Techniques. A Practical Approach to Tumor Diagnosis (31). ( ) P04087IT_01_K / p. 52/55
53 Bibliografia 1. Coussens L, Yang-Feng TL, Liao Y-C, Chen E, Gray A, McGrath J, et al. Tyrosine kinase receptor with extensive homology to EGF receptor shares chromosomal location with neu oncogene. Science 1985;230: King CR, Kraus MH, Aaronson SA. Amplification of a novel v-erbb-related gene in a human mammary carcinoma. Science 1985;229: Semba K, Kamata N, Toyoshima K, Yamamoto T. A v-erbb-related protooncogene, c-erbb-2, is distinct from the c-erbb-1/epidermal growth factor-receptor gene and is amplified in a human salivary gland adenocarcinoma. Proc Natl Acad Sci USA 1985;82: Yamamoto T, Ikawa S, Akiyama T, Semba K, Nomura N, Miyajima N, et al. Similarity of protein encoded by the human c-erb-b-2 gene to epidermal growth factor receptor. Nature 1986;319: Schechter AL, Hung M-C, Vaidyanathan L, Weinberg RA, Yang-Feng TL, Francke U, et al. The neu gene: an erbb-homologous gene distinct from and unlinked to the gene encoding the EGF receptor. Science 1985;229: Bargmann CI, Hung M-C, Weinberg RA. The neu oncogene encodes an epidermal growth factor receptor-related protein. Nature 1986;319: Natali PG, Nicotra MR, Bigotti A, Venturo I, Slamon DJ, Fendly BM, et al. Expression of the p185 encoded by HER2 oncogene in normal and transformed human tissues. Int J Cancer 1990;45: Press MF, Cordon-Cardo C, Slamon DJ. Expression of the HER-2/neu proto-oncogene in normal human adult and fetal tissues. Oncogene 1990;5: Lonardo F, Di Marco E, King CR, Pierce JH, Segatto O, Aaronson SA, et al. The normal erbb-2 product is an atypical receptor-like tyrosine kinase with constitutive activity in the absence of ligand. New Biologist 1990;2: Carter P, Presta L, Gorman CM, Ridgway JBB, Henner D, Wong WLT, et al. Humanization of an anti-p185 HER2 antibody for human cancer therapy. Proc Natl Acad Sci USA 1992;89: Hudziak RM, Lewis GD, Winget M, Fendly BM, Shepard HM, Ullrich A. p185 HER2 monoclonal antibody has antiproliferative effects in vitro and sensitizes human breast tumor cells to tumor necrosis factor. Mol Cell Biol 1989;9: Lewis GD, Figari I, Fendly B, Wong WL, Carter P, Gorman C, et al. Differential responses of human tumor cell lines to anti-p185 HER2 monoclonal antibodies. Cancer Immunol Immunother 1993;37: Baselga J, Norton L, Albanell J, Kim Y-M, Mendelsohn J. Recombinant humanized anti-her2 antibody (Herceptin ) enhances the antitumor activity of paclitaxel and doxorubicin against HER2/neu overexpressing human breast cancer xenografts. Cancer Res 1998;58: a. Medical Laboratories Particular requirements for quality and competence, ISO 15189:2003. b. Clinical Laboratory Improvement Amendments of 1988: Final Rule, 57CFR7163, February 28, Sheehan DC, Hrapchak BB. Theory and practice of histotechnology. St. Louis: The C. V. Mosby Company; Kiernan JA. Histological and histochemical methods: theory & practice. New York: Pergamon Press; Lundgaard Hansen B, Winther H, Moller K. Excessive section drying of breast cancer tissue prior to deparaffinisation and antigen retrieval causes a loss in HER2 immunoreactivity, Immunocytochemistry 2008;6, DakoCytomation California Inc., Data on file. 19. Key M. Education Guide: Immunohistochemical Staining Methods. Fifth Edition. Dako, Carpinteria, California; Leong AS-Y, Milios J, Leong FJ. Epitope retrieval with microwaves. A comparison of citrate buffer and EDTA with three commercial retrieval solutions. Appl Immunohistochem 1996;4: Procedures for decontamination of plumbing systems containing copper and/or lead azides, Department of Health, Education, and Welfare, National Institute for Occupational Safety and Health, Rockville, MD, Decontamination of laboratory sink drains to remove azide salts. Center for Disease Control Manual Guide: Safety Management, No. CDC-22, Atlanta, GA, April 30, Clinical and Laboratory Standards Institute (formerly NCCLS). Protection of Laboratory Workers From Occupationally Acquired Infections; Approved Guideline Third Edition. CLSI document M29-A3 [ISBN ]. Clinical and Laboratory Standards Institute, 940 West Valley Road, Suite 1400, Wayne, Pennsylvania USA, Clinical and Laboratory Standards Institute (formerly NCCLS). Quality assurance for immunocytochemistry; Approved guideline. CLSI document MM4-A ( ) CLSI, 940 West Valley Road, Suite 1400, Wayne, Pennsylvania USA; ( ) P04087IT_01_K / p. 53/55
54 25. Elias JM, Gown AM, Nakamura RM, Wilbur DC, Herman GE, Jaffe ES, et al. Special report: quality control in immunohistochemistry. Am J Clin Pathol 1989;92: Nadji M, Morales AR. Immunoperoxidase: Part I. The technique and its pitfalls. Lab Med 1983;14: Omata M, Liew C-T, Ashcavai M, Peters RL. Nonimmunologic binding of horseradish peroxidase to hepatitis B surface antigen: a possible source of error in immunohistochemistry. Am J Clin Path 1980;73: Herman GE, Elfont EA. The taming of immunohistochemistry: the new era of quality control. Biotech & Histochem 1991; 66: Press MF, Hung G, Godolphin W, Slamon DJ. Sensitivity of HER-2/neu antibodies in archival tissue samples: potential source of error in immunohistochemical studies of oncogene expression. Cancer Res 1994;54: Tubbs RR, Gephardt GN, Petras RE. Specimen processing and quality assurance. In: Atlas of immunohistology. Chicago: Amer Soc Clin Pathol Press; 1986: Nadji M, Morales AR. Immunoperoxidase techniques. A practical approach to tumor diagnosis. Chicago: Amer Soc Clin Pathol Press; Jørgensen JT. Targeted HER2 Treatment in Advanced Gastric Cancer. Oncology 2010;78: Tanner M, Hollmén M, Junttila TT, Kapanen AI, Tomola S, SoiniY et al. Amplification of HER-2 in gastric carcinoma: association with Topoisomerase II alpha gene amplification, intestinal type, poor prognosis and sensitivity to trastuzumab. Ann Oncol 2005;16: Matsui Y, Inomata M, Tojigamori M, Sonoda K, Shiraishi N, Kitano S. Suppression of tumor growth in human gastric cancer with HER2 overexpression by an anti-her2 antibody in a murine model. Int J Oncol 2005; 27: Fujimoto-Ouchi K, Sekiguchi F, Yasuno H, Moriya Y, Mor K, Tanaka Y. Antitumor activity of trastuzumab in combination with chemotherapy in human gastric cancer xenograft models. Cancer Chemother Pharmacol 2007; 59: Kim SY, Kim HP, Kim YJ, Oh DY, Im S-A, Lee D et al. Trastuzumab inhibits the growth of human gastric cancer cell lines with HER2 amplification synergistically with cisplatin. Int J Oncol 2008; 32: Bang YJ, Van Cutsem E, Feyereislova A, Chung HC, Shen L, Sawaki A et al. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-esophageal junction cancer (ToGA): a phase 3, open-label, randomized controlled trial. Lancet Bang Y, Chung J, Xu J, Lordick F, Sawaki A, Lipatov O et al. Pathological features of advanced Gastric Cancer (GC): Relationship to human epidermal growth factor receptor 2 (HER2) positivity in the global screening programme of the ToGA trial. J Clin Oncol 2009; 27:15s (suppl; abstr 4556). 39. Van Cutsem E, Kang YK, Chung HC, Shen L, Sawaki A, Lordick F, et al. Efficacy results from the ToGA trial: a phase III study of trastuzumab added to standard chemotherapy in first-line human epidermal growth factor receptor 2 (HER2)-positive advanced gastric cancer. (presentation ASCO 2009). 40. Hofmann M, Stoss O, Shi D, Büttner R, van de Vijver M, Kim W, et al. Assessment of a HER2 scoring system for gastric cancer: results from a validation study. Histopath 2008;52: Asioli S, Maletta F, Verdun di Cantogno L, Satolli MA, Schena M, Pecchioni C, et al. Approaching heterogeneity of human epidermal growth factor receptor 2 in surgical specimens of gastric cancer. Human Pathol 2012; 43;11: ( ) P04087IT_01_K / p. 54/55
55 Spiegazione dei simboli Numero di catalogo Limiti di temperatura Codice del lotto Pittogrammi di pericolo GHS (consultare la sezione relative alle precauzioni) Dispositivo medicodiagnostico in vitro Fragile, maneggiare con cura Utilizzare entro Pittogrammi di pericolo GHS (consultare la sezione relative alle precauzioni) Consultare le istruzioni per l uso Contenuto sufficiente per <n> saggi Fabbricante Prodotto da Dako Denmark A/S Produktionsvej 42 DK-2600 Glostrup Denmark Tel Fax Distribuito negli Stati Uniti da Dako North America, Inc Via Real Carpinteria, California 93013, USA Tel. 805/ Numero verde: 800/ Informazioni per gli ordini Tel. 800/ Fax 805/ Assistenza Tecnica: Tel. 800/ HercepTest ed Herceptin sono marchi di fabbrica di Genentech, Inc. e sono soggetti alle licenze detenute da Dako Denmark A/S e F. Hoffmann-La Roche Ltd. ( ) P04087IT_01_K / p. 55/55
HercepTest Codice nr. K5204
 HercepTest Codice nr. K5204 21 a edizione Per colorazione immunocitochimica. Il kit contiene i reagenti sufficienti per 35 test (70 vetrini). (129258-001) P04454IT_01_K520421-2/2016.05 p.1/55 Sommario
HercepTest Codice nr. K5204 21 a edizione Per colorazione immunocitochimica. Il kit contiene i reagenti sufficienti per 35 test (70 vetrini). (129258-001) P04454IT_01_K520421-2/2016.05 p.1/55 Sommario
HercepTest for Automated Link Platforms
 HercepTest for Automated Link Platforms Codice SK001 22 edizione (129284-001) P04456IT_01_SK00121-2/2016.05 p. 1/41 Sommario Pagina Finalità d uso...3 Cenni introduttivi - Mammella...4 Principio della
HercepTest for Automated Link Platforms Codice SK001 22 edizione (129284-001) P04456IT_01_SK00121-2/2016.05 p. 1/41 Sommario Pagina Finalità d uso...3 Cenni introduttivi - Mammella...4 Principio della
EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus)
 EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus) Codice K8012 6 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
EnVision FLEX+, Mouse, High ph, (Dako Autostainer/Autostainer Plus) Codice K8012 6 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
EnVision FLEX Mini Kit, High ph (Link)
 EnVision FLEX Mini Kit, High ph (Link) Codice K8023 2 a edizione Il kit contiene reagenti sufficienti per 125 190 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
EnVision FLEX Mini Kit, High ph (Link) Codice K8023 2 a edizione Il kit contiene reagenti sufficienti per 125 190 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
EnVision FLEX+, Mouse, High ph, (Link)
 EnVision FLEX+, Mouse, High ph, (Link) Codice K8002 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
EnVision FLEX+, Mouse, High ph, (Link) Codice K8002 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per strumenti Autostainer Link. Reagenti facoltativi Codice Nome prodotto Test K8004
TEICOPLANINA QMS Saggio immunologico
 0155948-0 Gen. 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
0155948-0 Gen. 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
EnVision FLEX Mini Kit, High ph (Dako Omnis)
 EnVision FLEX Mini Kit, High ph (Dako Omnis) Code GV823 2 a edizione Il kit contiene i reagenti sufficienti per 150 test. Per strumenti Dako Omnis. Reagenti facoltativi: Codice Nome prodotto Test GV804
EnVision FLEX Mini Kit, High ph (Dako Omnis) Code GV823 2 a edizione Il kit contiene i reagenti sufficienti per 150 test. Per strumenti Dako Omnis. Reagenti facoltativi: Codice Nome prodotto Test GV804
PNA ISH Detection Kit Codice nr. K5201
 PNA ISH Detection Kit Codice nr. K5201 9 a edizione Per ibridazione in situ con l impiego di sonde di PNA coniugate con fluoresceina. Il kit contiene i reagenti sufficienti per almeno 40 test*. * Il numero
PNA ISH Detection Kit Codice nr. K5201 9 a edizione Per ibridazione in situ con l impiego di sonde di PNA coniugate con fluoresceina. Il kit contiene i reagenti sufficienti per almeno 40 test*. * Il numero
URISTIKFIT LEV1 REF KCQURST1
 URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
TEICOPLANINA QMS Saggio immunologico
 0155941-0 Gen., 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
0155941-0 Gen., 2011 TEICOPLANINA QMS Saggio immunologico Prima dell'uso leggere attentamente il foglietto illustrativo del presente sistema quantitativo a microsfere (Quantitative Microsphere System -
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3
 DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
Laura Borghi Anatomia Patologica Azienda ULSS 18 Rovigo
 Laura Borghi Anatomia Patologica Azienda ULSS 18 Rovigo Anatomia Patologica Azienda ULSS 18 Rovigo MARKERS PROGNOSTICI p16 INK4a / Ki67 IN UNA POPOLAZIONE SELEZIONATA HPV DNA-HR POSITIVO: CORRELAZIONE
Laura Borghi Anatomia Patologica Azienda ULSS 18 Rovigo Anatomia Patologica Azienda ULSS 18 Rovigo MARKERS PROGNOSTICI p16 INK4a / Ki67 IN UNA POPOLAZIONE SELEZIONATA HPV DNA-HR POSITIVO: CORRELAZIONE
ALLwell Ingezim Gluten SemiQ (30.GSQ.K2)
 ALLwell Ingezim Gluten SemiQ (30.GSQ.K2) Test ELISA per rilevazione semi-quantitativa di glutine in campioni alimentari Cat. # LFD031 Manuale d uso ALLwell Ingezim Gluten SemiQ - Rev. 2 10/05/2019 1 1
ALLwell Ingezim Gluten SemiQ (30.GSQ.K2) Test ELISA per rilevazione semi-quantitativa di glutine in campioni alimentari Cat. # LFD031 Manuale d uso ALLwell Ingezim Gluten SemiQ - Rev. 2 10/05/2019 1 1
Caratteristiche prestazionali
 Caratteristiche prestazionali Kit RNeasy DSP FFPE, Versione 1 73604 Gestione della versione Il presente è il documento Caratteristiche prestazionali del kit RNeasy DSP FFPE, Versione 1, R1. Prima di eseguire
Caratteristiche prestazionali Kit RNeasy DSP FFPE, Versione 1 73604 Gestione della versione Il presente è il documento Caratteristiche prestazionali del kit RNeasy DSP FFPE, Versione 1, R1. Prima di eseguire
IMMUNOISTOCHIMICA ASPETTI BIOCHIMICI
 Università degli Studi di Ferrara Facoltà di Scienze MM.FF.NN. Laurea Triennale in Scienze Biologiche IMMUNOISTOCHIMICA ASPETTI BIOCHIMICI Guastella Giuseppe email giuseppe.guastella@unife.it telefono
Università degli Studi di Ferrara Facoltà di Scienze MM.FF.NN. Laurea Triennale in Scienze Biologiche IMMUNOISTOCHIMICA ASPETTI BIOCHIMICI Guastella Giuseppe email giuseppe.guastella@unife.it telefono
EGFR pharmdx. Codice K test per uso manuale Edizione 05/2015. Uso previsto Per uso diagnostico In Vitro.
 EGFR pharmdx Codice K1492 35 test per uso manuale Edizione 05/2015 Uso previsto Per uso diagnostico In Vitro. Il saggio EGFR pharmdx è un sistema di analisi qualitativa immunoistochimica (IHC) che consente
EGFR pharmdx Codice K1492 35 test per uso manuale Edizione 05/2015 Uso previsto Per uso diagnostico In Vitro. Il saggio EGFR pharmdx è un sistema di analisi qualitativa immunoistochimica (IHC) che consente
RIDASCREEN GIS. Test immunoenzimatico per la rilevazione del latte caprino nel latte ovino. Art. No.: R4802. Test in vitro Conservare a 2-8 C
 RIDASCREEN GIS Test immunoenzimatico per la rilevazione del latte caprino nel latte ovino Art. No.: R4802 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0
RIDASCREEN GIS Test immunoenzimatico per la rilevazione del latte caprino nel latte ovino Art. No.: R4802 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0
TECNICHE IMMUNOISTOCHIMICHE IN PATOLOGIA VETERINARIA: VANTAGGI E LIMITI. Pezzolato Marzia, DVM LAB Istopatologia - IZSTO
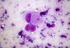 TECNICHE IMMUNOISTOCHIMICHE IN PATOLOGIA VETERINARIA: VANTAGGI E LIMITI Pezzolato Marzia, DVM LAB Istopatologia - IZSTO L immunoistochimica (IHC) serve per individuare un determinato antigene mediante
TECNICHE IMMUNOISTOCHIMICHE IN PATOLOGIA VETERINARIA: VANTAGGI E LIMITI Pezzolato Marzia, DVM LAB Istopatologia - IZSTO L immunoistochimica (IHC) serve per individuare un determinato antigene mediante
QMS QUINIDINE. Immunoassay. Legenda dei simboli. Microgenics GmbH. D Passau. Tel: +49 (0) Fax: +49 (0)
 0155255-D October, 2014 QMS QUINIDINE Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
0155255-D October, 2014 QMS QUINIDINE Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP
 Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP Pag. 1 di 5 USO PREVISTO: Per uso diagnostico in vitro. DISPONIBILITÀ: Codice catalogo Quantità
Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP Pag. 1 di 5 USO PREVISTO: Per uso diagnostico in vitro. DISPONIBILITÀ: Codice catalogo Quantità
VIDAS Anti HBs TOTAL - Cod
 SCHEDA DI SICUREZZA N 592 Versione C Data : 21.08.1995 Data di revisione :20.11.2000 NOME DEL PRODOTTO VIDAS Anti HBs TOTAL - Cod. 30 304 DESCRIZIONE DEL KIT Cartucce : 1 x 60 Coni : 2 x 30 Standard :
SCHEDA DI SICUREZZA N 592 Versione C Data : 21.08.1995 Data di revisione :20.11.2000 NOME DEL PRODOTTO VIDAS Anti HBs TOTAL - Cod. 30 304 DESCRIZIONE DEL KIT Cartucce : 1 x 60 Coni : 2 x 30 Standard :
QMS TOBRAMYCIN. Immunoassay CALIBRATORI PER LA TOBRAMICINA Legenda dei simboli
 0155269-D-IT November, 2014 QMS TOBRAMYCIN Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
0155269-D-IT November, 2014 QMS TOBRAMYCIN Immunoassay Prima dell uso, è necessario leggere con attenzione il presente foglio illustrativo relativo al sistema Quantitative Microsphere System (QMS). È necessario
Histology FISH Accessory Kit Codice K5799
 Histology FISH Accessory Kit Codice K5799 6 a edizione Per l ibridazione in situ con sonde fluorescenti (FISH) su sezioni di tessuto fissate in formalina e incluse in paraffina. Il kit contiene i reagenti
Histology FISH Accessory Kit Codice K5799 6 a edizione Per l ibridazione in situ con sonde fluorescenti (FISH) su sezioni di tessuto fissate in formalina e incluse in paraffina. Il kit contiene i reagenti
VIDAS HBs Ag - Cod
 SCHEDA DI SICUREZZA N 256 Versione D Data : 07.02.2002 Data di revisione : 05.07.2002 Cartucce 1 x 60 Coni 2 x 30 Standard 3 x 1 ml Controllo positivo 1 x 1,5 ml Controllo negativo 1 x 1,5 ml * Ag HBs
SCHEDA DI SICUREZZA N 256 Versione D Data : 07.02.2002 Data di revisione : 05.07.2002 Cartucce 1 x 60 Coni 2 x 30 Standard 3 x 1 ml Controllo positivo 1 x 1,5 ml Controllo negativo 1 x 1,5 ml * Ag HBs
RIDASCREEN CIS. Test immunoenzimatico per la rilevazione del latte vaccino nel latte ovino e caprino e nel formaggio ovino e caprino. Art. No.
 RIDASCREEN CIS Test immunoenzimatico per la rilevazione del latte vaccino nel latte ovino e caprino e nel formaggio ovino e caprino Art. No.: R4302 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt,
RIDASCREEN CIS Test immunoenzimatico per la rilevazione del latte vaccino nel latte ovino e caprino e nel formaggio ovino e caprino Art. No.: R4302 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt,
Università degli Studi dell Aquila Dipartimento MeSVA Sezione di Scienze Biologiche e Biotecnologiche. Laboratorio di Istologia
 Università degli Studi dell Aquila Dipartimento MeSVA Sezione di Scienze Biologiche e Biotecnologiche.. Laboratorio di Istologia Allestimento di un preparato istologico L'istologia è la disciplina scientifica
Università degli Studi dell Aquila Dipartimento MeSVA Sezione di Scienze Biologiche e Biotecnologiche.. Laboratorio di Istologia Allestimento di un preparato istologico L'istologia è la disciplina scientifica
HER2 IQFISH pharmdx Codice K5731 Terza edizione
 HER2 IQFISH pharmdx Codice K5731 Terza edizione HER2 IQFISH pharmdx è un saggio di ibridazione in situ in fluorescenza diretta (FISH) per la determinazione quantitativa dell amplificazione del gene HER2
HER2 IQFISH pharmdx Codice K5731 Terza edizione HER2 IQFISH pharmdx è un saggio di ibridazione in situ in fluorescenza diretta (FISH) per la determinazione quantitativa dell amplificazione del gene HER2
COLORAZIONE DELLE SEZIONI ISTOLOGICHE PER L OSSERVAZIONE OTTICA. COLORAZIONI TOPOGRAFICHE o ISTOMORFOLOGICHE COLORAZIONI IMMUNOISTOCHIMICHE
 COLORAZIONE DELLE SEZIONI ISTOLOGICHE PER L OSSERVAZIONE OTTICA Poiché la densità ottica delle diverse parti del campione biologico è pressoché identica, la colorazione interviene per aumentare il contrasto.
COLORAZIONE DELLE SEZIONI ISTOLOGICHE PER L OSSERVAZIONE OTTICA Poiché la densità ottica delle diverse parti del campione biologico è pressoché identica, la colorazione interviene per aumentare il contrasto.
IMMUFIT LEV1 REF KCQIMMU1
 IMMUFIT LEV1 REF KCQIMMU1 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Questo prodotto è inteso per l uso diagnostico in vitro come controllo di qualità dell accuratezza degli immunodosaggi sui sistemi
IMMUFIT LEV1 REF KCQIMMU1 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Questo prodotto è inteso per l uso diagnostico in vitro come controllo di qualità dell accuratezza degli immunodosaggi sui sistemi
test Circulating Tumor Cell Control Kit
 7900003 24 test Circulating Tumor Cell Control Kit 1 e631600016_it IMPIEGO PREVISTO Per uso diagnostico in vitro Il Kit CELLSEARCH Circulating Tumor Cell Control è stato formulato per essere utilizzato
7900003 24 test Circulating Tumor Cell Control Kit 1 e631600016_it IMPIEGO PREVISTO Per uso diagnostico in vitro Il Kit CELLSEARCH Circulating Tumor Cell Control è stato formulato per essere utilizzato
ZytoLight CEN X/Y Dual Color Probe
 ZytoLight CEN X/Y Dual Color Probe Z-2016-200 Z-2016-50 20 (0.2 ml) 5 (0.05 ml) Per la rilevazione degli alfa-satelliti del cromosoma X e della regione del satellite III del cromosoma Y mediante ibridazione
ZytoLight CEN X/Y Dual Color Probe Z-2016-200 Z-2016-50 20 (0.2 ml) 5 (0.05 ml) Per la rilevazione degli alfa-satelliti del cromosoma X e della regione del satellite III del cromosoma Y mediante ibridazione
LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI
 LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI 1 Che cosa sono le proteine? Indispensabili per il corretto funzionamento 2 Dove si trovano le proteine? Le proteine sono macromolecole ubiquitarie,
LOCALIZZAZIONE in situ DI PROTEINE IN CELLULE E TESSUTI 1 Che cosa sono le proteine? Indispensabili per il corretto funzionamento 2 Dove si trovano le proteine? Le proteine sono macromolecole ubiquitarie,
Test ELISA (enzyme-linked immunosorbent assay)
 PLS-BIOTECNOLOGIE Dipartimento di Scienze ATTIVITA LABORATORIALE 2017-2018 Test ELISA (enzyme-linked immunosorbent assay) Determinazione della presenza/assenza di un Antigene INTRODUZIONE ELISA è l'acronimo
PLS-BIOTECNOLOGIE Dipartimento di Scienze ATTIVITA LABORATORIALE 2017-2018 Test ELISA (enzyme-linked immunosorbent assay) Determinazione della presenza/assenza di un Antigene INTRODUZIONE ELISA è l'acronimo
RIDA QUICK Verotoxin/O157 Combi Control NP2204
 RIDA QUICK Verotoxin/O157 Combi Control NP2204 R-Biopharm AG, An der neuen Bergstraße 17, 64297 Darmstadt, Germania Telefono: +49 (0) 61 51 81 02-0, Fax: +49 (0) 61 51 81 02-20 1. Campo di applicazione
RIDA QUICK Verotoxin/O157 Combi Control NP2204 R-Biopharm AG, An der neuen Bergstraße 17, 64297 Darmstadt, Germania Telefono: +49 (0) 61 51 81 02-0, Fax: +49 (0) 61 51 81 02-20 1. Campo di applicazione
ZytoDot SPEC HER2 Probe
 ZytoDot SPEC HER2 Probe C-3001-400 C-3001-100 40 (0.4 ml) 10 (0.1 ml) Per la rilevazione del gene umano HER2 mediante ibridazione in situ cromogenica (CISH).... Dispositivo per uso diagnostico in vitro
ZytoDot SPEC HER2 Probe C-3001-400 C-3001-100 40 (0.4 ml) 10 (0.1 ml) Per la rilevazione del gene umano HER2 mediante ibridazione in situ cromogenica (CISH).... Dispositivo per uso diagnostico in vitro
QUANTA Chek ANA Panel
 QUANTA Chek ANA Panel 708111 Finalità d uso Il Pannello ANA QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli anticorpi antinucleo IFA ed ELISA. Ciascun siero
QUANTA Chek ANA Panel 708111 Finalità d uso Il Pannello ANA QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli anticorpi antinucleo IFA ed ELISA. Ciascun siero
Codice K4003: il prodotto seguente è sufficiente per 1100 sezioni di tessuto, sulla base di un utilizzo di 100 µl per sezione:
 Dako EnVision+ System- HRP Labelled Polymer Anti-Rabbit Codice K4002 15 ml Codice K4003 110 ml Uso previsto Per uso diagnostico in vitro. Queste istruzioni sono valide per il sistema Dako EnVision +, Peroxidase
Dako EnVision+ System- HRP Labelled Polymer Anti-Rabbit Codice K4002 15 ml Codice K4003 110 ml Uso previsto Per uso diagnostico in vitro. Queste istruzioni sono valide per il sistema Dako EnVision +, Peroxidase
Progensa PCA3 Urine Specimen Transport Kit
 Istruzioni per i medici Progensa PCA3 Urine Specimen Transport Kit Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
Istruzioni per i medici Progensa PCA3 Urine Specimen Transport Kit Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
diagnosi di GIST, né dovrebbe precludere il trattamento con Gleevec/Glivec.
 c-kit pharmdx Codice K1907 35 test per il sistema Dako Autostainer Uso previsto Per uso diagnostico in vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente
c-kit pharmdx Codice K1907 35 test per il sistema Dako Autostainer Uso previsto Per uso diagnostico in vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente
INGEZIM Gluten Quanti Test Guida all utilizzo
 INGEZIM Gluten Quanti Test Guida all utilizzo 1 - INTRODUZIONE Il kit è basato su un saggio immunoenzimatico ELISA di tipo sandwich come dettato dal Codex Alimentarius. Ogni pozzetto è rivestito sul fondo
INGEZIM Gluten Quanti Test Guida all utilizzo 1 - INTRODUZIONE Il kit è basato su un saggio immunoenzimatico ELISA di tipo sandwich come dettato dal Codex Alimentarius. Ogni pozzetto è rivestito sul fondo
ZytoLight SPEC BCR/ABL Dual Color Dual Fusion Probe
 ZytoLight SPEC BCR/ABL Dual Color Dual Fusion Probe Z-2111-200 20 (0.2 ml) Per la rilevazione della translocazione t(9;22)(q34;q11)mediante ibridazione in situ fluorescente (FISH).... Dispositivo per uso
ZytoLight SPEC BCR/ABL Dual Color Dual Fusion Probe Z-2111-200 20 (0.2 ml) Per la rilevazione della translocazione t(9;22)(q34;q11)mediante ibridazione in situ fluorescente (FISH).... Dispositivo per uso
Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA
 Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA Tecniche Immunologiche La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono utilizzati
Immunologia e Immunopatologia IMMUNOLOGIA DIAGNOSTICA Tecniche Immunologiche La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono utilizzati
PD-L1 IHC 28-8 pharmdx. SK test per l'utilizzo con Autostainer Link 48
 PD-L1 IHC 28-8 pharmdx SK005 50 test per l'utilizzo con Autostainer Link 48 Sommario 1. Uso previsto...2 2. Riepilogo e spiegazione...2 2.1 NSCLC non squamoso...2 2.2 Carcinoma a cellule squamose di testa
PD-L1 IHC 28-8 pharmdx SK005 50 test per l'utilizzo con Autostainer Link 48 Sommario 1. Uso previsto...2 2. Riepilogo e spiegazione...2 2.1 NSCLC non squamoso...2 2.2 Carcinoma a cellule squamose di testa
Le presenti istruzioni si applicano a Dako EnVision+, Peroxidase (Dako EnVision+, HRP).
 Dako EnVision+ System- HRP Labelled Polymer Anti-mouse Codice K4000 115 ml Codice K4001 110 ml Uso previsto Per uso diagnostico in vitro. Le presenti istruzioni si applicano a Dako EnVision+, Peroxidase
Dako EnVision+ System- HRP Labelled Polymer Anti-mouse Codice K4000 115 ml Codice K4001 110 ml Uso previsto Per uso diagnostico in vitro. Le presenti istruzioni si applicano a Dako EnVision+, Peroxidase
EnVision G 2 Doublestain System, Rabbit/Mouse (DAB+/Permanent Red)
 EnVision G 2 Doublestain System, Rabbit/Mouse (DAB+/Permanent Red) Codice K5361 Seconda edizione Per l uso con anticorpi primari di coniglio e topo. Idoneo per 150 test. (114146-002) K5361/IT/SGA/13.10.06
EnVision G 2 Doublestain System, Rabbit/Mouse (DAB+/Permanent Red) Codice K5361 Seconda edizione Per l uso con anticorpi primari di coniglio e topo. Idoneo per 150 test. (114146-002) K5361/IT/SGA/13.10.06
Allestimenti e diagnosi intra-day: tecniche a confronto. Mara Dal Santo Anatomia Patologica Ospedale S. Chiara - Trento
 Allestimenti e diagnosi intra-day: tecniche a confronto Mara Dal Santo Anatomia Patologica Ospedale S. Chiara - Trento 1 Nuove esigenze Domanda da parte dei Clinici Domanda da parte degli utenti Tempi
Allestimenti e diagnosi intra-day: tecniche a confronto Mara Dal Santo Anatomia Patologica Ospedale S. Chiara - Trento 1 Nuove esigenze Domanda da parte dei Clinici Domanda da parte degli utenti Tempi
Codice K4006 nel kit sono inclusi i seguenti materiali, sufficienti per 150 sezioni di tessuto, in base a un utilizzo di 100 µl per sezione:
 Dako EnVision+ System-HRP (DAB) For Use With Mouse Primary Antibodies Codice K4006 15 ml Codice K4007 110 ml Uso previsto Per uso diagnostico in vitro. Queste istruzioni sono valide per il sistema Dako
Dako EnVision+ System-HRP (DAB) For Use With Mouse Primary Antibodies Codice K4006 15 ml Codice K4007 110 ml Uso previsto Per uso diagnostico in vitro. Queste istruzioni sono valide per il sistema Dako
ZytoLight SPEC CMYC/CEN 8 Dual Color Probe
 ZytoLight SPEC CMYC/CEN 8 Dual Color Probe Z-2092-200 20 (0.2 ml) Per la rilevazione del gene umano CMYC e degli alfa-satelliti del cromosoma 8 mediante ibridazione in situ fluorescente (FISH).... Dispositivo
ZytoLight SPEC CMYC/CEN 8 Dual Color Probe Z-2092-200 20 (0.2 ml) Per la rilevazione del gene umano CMYC e degli alfa-satelliti del cromosoma 8 mediante ibridazione in situ fluorescente (FISH).... Dispositivo
Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE
 Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE Tecniche di laboratorio La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono
Immunologia e Immunologia Diagnostica TECNICHE IMMUNOLOGICHE Tecniche di laboratorio La maggior parte delle tecniche di laboratorio biomedico si basano sull utilizzo degli anticorpi. Gli anticorpi sono
Reagenti forniti Il Reticulin-No Counterstain Kit è composto da sette confezioni dispenser pronte all uso, ognuna delle quali contiene:
 Artisan Reticulin-No Counterstain Kit Codice AR182 Uso previsto Per uso diagnostico in vitro. Il Reticulin-No Counterstain Kit è destinato all uso in laboratorio per l identificazione, al microscopio ottico,
Artisan Reticulin-No Counterstain Kit Codice AR182 Uso previsto Per uso diagnostico in vitro. Il Reticulin-No Counterstain Kit è destinato all uso in laboratorio per l identificazione, al microscopio ottico,
diagnosi di GIST, né dovrebbe precludere il trattamento con Gleevec/Glivec.
 c-kit pharmdx Codice K1906 25 test per uso manuale Uso previsto Per uso diagnostico In Vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente di identificare
c-kit pharmdx Codice K1906 25 test per uso manuale Uso previsto Per uso diagnostico In Vitro. Il saggio c-kit pharmdx è un kit di analisi immunoistochimica (IHC) qualitativa che consente di identificare
Lo scopo delle tecniche di colorazione immunoistochimica (IHC) è quello di consentire la visualizzazione degli antigeni tissutali (cellulari).
 Dako LSAB 2 System-AP Codice K0674 110 ml Codice K0676 15 ml Uso previsto Per uso diagnostico in vitro. Queste istruzioni si riferiscono a Universal Dako LSAB 2 System, Alkaline Phosphatase (LSAB2 System,
Dako LSAB 2 System-AP Codice K0674 110 ml Codice K0676 15 ml Uso previsto Per uso diagnostico in vitro. Queste istruzioni si riferiscono a Universal Dako LSAB 2 System, Alkaline Phosphatase (LSAB2 System,
ISTRUZIONI D USO IVD 0123 HLA CLASSE II REF 7029: HISTO TRAY DR 72 (10)
 ISTRUZIONI D USO IVD 0123 HISTO TRAY HLA CLASSE II PER USO DIAGNOSTICO IN VITRO REF 7029: HISTO TRAY DR 72 (10) 10 piastre Descrizione del prodotto La destinazione d uso dell HISTO TRAY è la tipizzazione
ISTRUZIONI D USO IVD 0123 HISTO TRAY HLA CLASSE II PER USO DIAGNOSTICO IN VITRO REF 7029: HISTO TRAY DR 72 (10) 10 piastre Descrizione del prodotto La destinazione d uso dell HISTO TRAY è la tipizzazione
IMPATH HER2 FISH. Identificazione del prodotto Cat. N. Descrizione ImPath HER2 FISH
 Identificazione del prodotto Cat. N. Descrizione 47862 ImPath HER2 FISH Uso previsto ImPath HER2 FISH (cat. n. 47862) è destinato all uso in combinazione con ImPath ISH Detection Kit (cat. n. 44996) per
Identificazione del prodotto Cat. N. Descrizione 47862 ImPath HER2 FISH Uso previsto ImPath HER2 FISH (cat. n. 47862) è destinato all uso in combinazione con ImPath ISH Detection Kit (cat. n. 44996) per
Striscia reattiva per β-chetone ematico
 FOGLIETTO ILLUSTRATIVO Striscia reattiva per β-chetone ematico AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori
FOGLIETTO ILLUSTRATIVO Striscia reattiva per β-chetone ematico AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori
test Circulating Tumor Cell Control Kit
 7900003 24 test Circulating Tumor Cell Control Kit 1 IMPIEGO PREVISTO Per uso diagnostico in vitro Il Kit CELLSEARCH Circulating Tumor Cell Control è stato formulato per essere utilizzato come controllo
7900003 24 test Circulating Tumor Cell Control Kit 1 IMPIEGO PREVISTO Per uso diagnostico in vitro Il Kit CELLSEARCH Circulating Tumor Cell Control è stato formulato per essere utilizzato come controllo
Le istruzioni fornite si riferiscono a Dako EnVision+ Dual Link System-HRP (DAB+).
 Dako EnVision + Dual Link System-HRP (DAB+) Codice K4065 Uso previsto Per uso diagnostico In Vitro. Le istruzioni fornite si riferiscono a Dako EnVision+ Dual Link System-HRP (DAB+). Questo kit è destinato
Dako EnVision + Dual Link System-HRP (DAB+) Codice K4065 Uso previsto Per uso diagnostico In Vitro. Le istruzioni fornite si riferiscono a Dako EnVision+ Dual Link System-HRP (DAB+). Questo kit è destinato
SCHEDA DI SICUREZZA ART COLLECTION
 SCHEDA DI SICUREZZA ART COLLECTION 1 RELAXER GOCCE D'AMBRA (Cod. A254) 1. Identificazione del prodotto e del produttore e responsabile dell'immissione sul mercato Dati relativi al prodotto Nome commerciale
SCHEDA DI SICUREZZA ART COLLECTION 1 RELAXER GOCCE D'AMBRA (Cod. A254) 1. Identificazione del prodotto e del produttore e responsabile dell'immissione sul mercato Dati relativi al prodotto Nome commerciale
QUANTA Chek Celiac Panel 708113
 QUANTA Chek Celiac Panel 708113 Finalità d uso Il Pannello Celiac QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli autoanticorpi IFA ed ELISA. Ciascun siero
QUANTA Chek Celiac Panel 708113 Finalità d uso Il Pannello Celiac QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli autoanticorpi IFA ed ELISA. Ciascun siero
SCHEDA DI SICUREZZA ISTRUZIONE OPERATIVA SICUREZZA
 SCHEDA DI SICUREZZA ISTRUZIONE OPERATIVA SICUREZZA DATA DI EMISSIONE: SETTEMBRE 2004 1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETÀ 1.1 - ELEMENTI IDENTIFICATIVI DEL PREPARATO Nome del prodotto:
SCHEDA DI SICUREZZA ISTRUZIONE OPERATIVA SICUREZZA DATA DI EMISSIONE: SETTEMBRE 2004 1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETÀ 1.1 - ELEMENTI IDENTIFICATIVI DEL PREPARATO Nome del prodotto:
SAFE - Scuola di Scienze Agrarie, Forestali, Alimentari ed Ambientali. School of Agriculture, forest, Food and Environmental sciences.
 Protocollo SAFE Protocollo di estrazione DNA da colture di fermenti lattici (metodo del salting-out; Dr. Lara Aponte) Reagenti: Tampone STE (per lavaggio delle cellule) Tampone di lisi Tampone TE (per
Protocollo SAFE Protocollo di estrazione DNA da colture di fermenti lattici (metodo del salting-out; Dr. Lara Aponte) Reagenti: Tampone STE (per lavaggio delle cellule) Tampone di lisi Tampone TE (per
ISTRUZIONI PER L USO. Test per la diagnosi di infezione da dialisi peritoneale. Per l autodiagnosi. Leggere per intero MPV1 VERSION 03, MAY 2017
 ISTRUZIONI PER L USO Test per la diagnosi di infezione da dialisi peritoneale Per l autodiagnosi Leggere per intero VERSION 03, MAY 2017 MPV1 1 DESTINAZIONE D USO Il test PERiPLEX identifica due marcatori
ISTRUZIONI PER L USO Test per la diagnosi di infezione da dialisi peritoneale Per l autodiagnosi Leggere per intero VERSION 03, MAY 2017 MPV1 1 DESTINAZIONE D USO Il test PERiPLEX identifica due marcatori
Cytology FISH Accessory Kit Codice n. K 5499
 Cytology FISH Accessory Kit Codice n. K 5499 2 a edizione Per ibridazione in situ in fluorescenza (FISH, Fluorescence In Situ Hybridization) su campioni citologici. Il kit contiene reagenti sufficienti
Cytology FISH Accessory Kit Codice n. K 5499 2 a edizione Per ibridazione in situ in fluorescenza (FISH, Fluorescence In Situ Hybridization) su campioni citologici. Il kit contiene reagenti sufficienti
Tecnica di preparazione di vetrini istologici. By A. Pirola
 Tecnica di preparazione di vetrini istologici By A. Pirola Preparazione del materiale istologico Problema 1 I tessuti vanno incontro a fenomeni di degradazione Problema 2 La luce può attraversare solo
Tecnica di preparazione di vetrini istologici By A. Pirola Preparazione del materiale istologico Problema 1 I tessuti vanno incontro a fenomeni di degradazione Problema 2 La luce può attraversare solo
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus)
 EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Codice K8010 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
EnVision FLEX, High ph, (Dako Autostainer/Autostainer Plus) Codice K8010 5 a edizione Il kit contiene reagenti sufficienti per 400 600 test. Per Dako Autostainer/Autostainer Plus Reagenti facoltativi:
Heat Shock Protein 27 (G3.1)
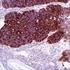 Identificazione Prodotto N Catalogo Descrizione 46946 HSP27 0,1 M (G3.1) 46947 HSP27 1 M (G3.1) 46945 HSP27 RTU M (G3.1) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
Identificazione Prodotto N Catalogo Descrizione 46946 HSP27 0,1 M (G3.1) 46947 HSP27 1 M (G3.1) 46945 HSP27 RTU M (G3.1) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero
Le seguenti istruzioni sono relative al sistema Dako EnVision+ System- HRP (AEC) (Dako EnVision+ System, HRP).
 Dako EnVision+ System-HRP (AEC) For Use with Mouse Primary Antibodies Codice n. K4004 115 ml Codice n. K4005 110 ml Uso previsto Per uso diagnostico in vitro. Le seguenti istruzioni sono relative al sistema
Dako EnVision+ System-HRP (AEC) For Use with Mouse Primary Antibodies Codice n. K4004 115 ml Codice n. K4005 110 ml Uso previsto Per uso diagnostico in vitro. Le seguenti istruzioni sono relative al sistema
Tessuto di controllo: sezione di arteria, appendice ed epidermide.
 Artisan Elastic Stain Kit Codice AR163 Uso previsto Per uso diagnostico in vitro. Il kit Elastic Stain Kit è destinato all'uso di laboratorio per l'identificazione con microscopia ottica di fibre ossitalane,
Artisan Elastic Stain Kit Codice AR163 Uso previsto Per uso diagnostico in vitro. Il kit Elastic Stain Kit è destinato all'uso di laboratorio per l'identificazione con microscopia ottica di fibre ossitalane,
WITNESS GIARDIA INTRODUZIONE
 WITNESS GIARDIA WITNESS GIARDIA INTRODUZIONE Giardia intestinalis (sin. G. duodenalis o G. lamblia) è un protozoo parassita dell apparato gastrointestinale di numerose specie di animali (ad es. cane e
WITNESS GIARDIA WITNESS GIARDIA INTRODUZIONE Giardia intestinalis (sin. G. duodenalis o G. lamblia) è un protozoo parassita dell apparato gastrointestinale di numerose specie di animali (ad es. cane e
SAFE - Scuola di Scienze Agrarie, Forestali, Alimentari ed Ambientali. School of Agriculture, forest, Food and Environmental sciences
 Protocollo SAFE Determinazione dell attività antiossidante Valutazione della resistenza allo stress ossidativo in presenza di perossido d idrogeno Soluzione di perossido d idrogeno 1,6 M. Esporre i campioni
Protocollo SAFE Determinazione dell attività antiossidante Valutazione della resistenza allo stress ossidativo in presenza di perossido d idrogeno Soluzione di perossido d idrogeno 1,6 M. Esporre i campioni
Streptavidina coniugata con perossidasi di rafano in PBS contenente una proteina stabilizzante e agenti antibatterici.
 Dako LSAB2 System-HRP Codice K0672 15 ml Codice K0673 15 ml Codice K0675 110 ml Uso previsto Per uso diagnostico In Vitro. Queste istruzioni si applicano al sistema universale Dako Labelled Streptavidin-Biotin2
Dako LSAB2 System-HRP Codice K0672 15 ml Codice K0673 15 ml Codice K0675 110 ml Uso previsto Per uso diagnostico In Vitro. Queste istruzioni si applicano al sistema universale Dako Labelled Streptavidin-Biotin2
RIDA QUICK CIS. Test immunocromatografico per la rilevazione del latte vaccino nel latte o nel formaggio di altre specie. Art. No.
 RIDA QUICK CIS Test immunocromatografico per la rilevazione del latte vaccino nel latte o nel formaggio di altre specie Art. No.: R4303 Test in vitro Conservare a 2-30 C R-Biopharm AG, Darmstadt, Germany
RIDA QUICK CIS Test immunocromatografico per la rilevazione del latte vaccino nel latte o nel formaggio di altre specie Art. No.: R4303 Test in vitro Conservare a 2-30 C R-Biopharm AG, Darmstadt, Germany
4F81BDSCHEDA TECNICA 4F81BD
 04011Pagina 1 di 5 pagine Codice prodotto: Nome prodotto: Consigliato per: Dimensioni disponibili: 120101 Gori Detergente concentrato rimuove alghe, muschio e strati verdi Tutti i legni per esterni 1 L
04011Pagina 1 di 5 pagine Codice prodotto: Nome prodotto: Consigliato per: Dimensioni disponibili: 120101 Gori Detergente concentrato rimuove alghe, muschio e strati verdi Tutti i legni per esterni 1 L
PROGENSA PCA3 Urine Specimen Transport Kit
 PROGENSA PCA3 Urine Specimen Transport Kit Istruzioni per i medici Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
PROGENSA PCA3 Urine Specimen Transport Kit Istruzioni per i medici Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
Artisan Grocott s Methenamine Silver Stain Kit * Codice AR176. Uso previsto Per uso diagnostico In Vitro.
 Artisan Grocott s Methenamine Silver Stain Kit * Codice AR176 Uso previsto Per uso diagnostico In Vitro. Il Grocott s Methenamine Silver (GMS) Stain Kit è destinato per l uso in laboratorio per identificare,
Artisan Grocott s Methenamine Silver Stain Kit * Codice AR176 Uso previsto Per uso diagnostico In Vitro. Il Grocott s Methenamine Silver (GMS) Stain Kit è destinato per l uso in laboratorio per identificare,
Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile.
 Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile. Questi anticorpi sono delle molecole IgG che attaccano un solo
Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile. Questi anticorpi sono delle molecole IgG che attaccano un solo
Artisan Reticulin-Nuclear Fast Red Stain Kit. Codice AR179. Uso previsto Per uso diagnostico in vitro.
 Artisan Reticulin-Nuclear Fast Red Stain Kit Codice AR179 Uso previsto Per uso diagnostico in vitro. Il Reticulin-Nuclear Fast Red Stain Kit è destinato all uso in laboratorio per l identificazione, al
Artisan Reticulin-Nuclear Fast Red Stain Kit Codice AR179 Uso previsto Per uso diagnostico in vitro. Il Reticulin-Nuclear Fast Red Stain Kit è destinato all uso in laboratorio per l identificazione, al
HER2 e carcinoma gastrico
 Modulo 1 HER2 e carcinoma gastrico Cosa è HER2 Con l'acronimo HER2 viene identificato uno dei recettori per i fattori epidermici di crescita, codificato dal cromosoma 17; HER2 appartiene alla famiglia
Modulo 1 HER2 e carcinoma gastrico Cosa è HER2 Con l'acronimo HER2 viene identificato uno dei recettori per i fattori epidermici di crescita, codificato dal cromosoma 17; HER2 appartiene alla famiglia
Foglio illustrativo: informazioni per l utilizzatore. NEOMERCUROCROMO soluzione cutanea. Eosina/ Cloroxilenolo/ Propilenglicole
 Foglio illustrativo: informazioni per l utilizzatore NEOMERCUROCROMO soluzione cutanea Eosina/ Cloroxilenolo/ Propilenglicole Legga attentamente questo foglio prima di usare questo medicinale perchè contiene
Foglio illustrativo: informazioni per l utilizzatore NEOMERCUROCROMO soluzione cutanea Eosina/ Cloroxilenolo/ Propilenglicole Legga attentamente questo foglio prima di usare questo medicinale perchè contiene
ADVANCE TM HRP. Codice K ml Codice K ml Codice K ml Prodotto pronto all'uso. Uso previsto. Per uso diagnostico In Vitro.
 ADVANCE TM HRP Codice K4067 500 ml Codice K4068 110 ml Codice K4069 11 ml Prodotto pronto all'uso Uso previsto Per uso diagnostico In Vitro. Questo sistema è destinato all'uso con anticorpi primari di
ADVANCE TM HRP Codice K4067 500 ml Codice K4068 110 ml Codice K4069 11 ml Prodotto pronto all'uso Uso previsto Per uso diagnostico In Vitro. Questo sistema è destinato all'uso con anticorpi primari di
Striscia reattiva glicemia ematocrito emoglobina. N. modello: TD-4272 / GD40 DELTA
 Striscia reattiva glicemia ematocrito emoglobina AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori che eseguono
Striscia reattiva glicemia ematocrito emoglobina AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori che eseguono
ESAME MORFOLOGICO DEL SANGUE
 ESAME MORFOLOGICO DEL SANGUE Obiettivo Con l esame morfologico del sangue si intende differenziare gli elementi figurati del sangue, tramite la colorazione di May Grunwald-Giemsa, per poterli riconoscere
ESAME MORFOLOGICO DEL SANGUE Obiettivo Con l esame morfologico del sangue si intende differenziare gli elementi figurati del sangue, tramite la colorazione di May Grunwald-Giemsa, per poterli riconoscere
ScanGel ScanSol ml ml
 ScanGel ScanSol 86448 100 ml 86449 500 ml MEZZO DI SOSPENSIONE DEI GLOBULI ROSSI IVD Tutti i prodotti fabbricati e commercializzati dalla società Bio-Rad sono sottoposti a un sistema di assicurazione qualità
ScanGel ScanSol 86448 100 ml 86449 500 ml MEZZO DI SOSPENSIONE DEI GLOBULI ROSSI IVD Tutti i prodotti fabbricati e commercializzati dalla società Bio-Rad sono sottoposti a un sistema di assicurazione qualità
I prodotti prediluiti sono diluiti in modo ottimale per l uso con un ampia varietà di kit di rivelazione offerti da altri produttori.
 Identificazione Prodotto N Catalogo Descrizione 44819 TSH 0,1 R (Poly) 44820 TSH 1 R (Poly) 44400 TSH RTU R (Poly) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
Identificazione Prodotto N Catalogo Descrizione 44819 TSH 0,1 R (Poly) 44820 TSH 1 R (Poly) 44400 TSH RTU R (Poly) Definizione Dei Simboli P C A E S DIL DOC# DIS pronto uso concentrato asciti siero supernatante
RIDA CHECK. Tamponi per la rilevazione dei residui proteici per il controllo delle procedure di lavaggio e dell igiene
 RIDA CHECK Tamponi per la rilevazione dei residui proteici per il controllo delle procedure di lavaggio e dell igiene Art. No.: R1091 (100 test) R1092 (40 test) R-Biopharm AG, Darmstadt, Germany Tel.:
RIDA CHECK Tamponi per la rilevazione dei residui proteici per il controllo delle procedure di lavaggio e dell igiene Art. No.: R1091 (100 test) R1092 (40 test) R-Biopharm AG, Darmstadt, Germany Tel.:
CLOSTRIDIUM DIFFICILE TOSSINE A e B
 MODALITA' DI RICHIESTA: Pazienti interni: tramite modulo interno prestampato. Pazienti esterni: tramite richiesta del medico curante. PREPARAZIONE DEL PAZIENTE ALL'ESAME: Nessuna. MODALITA' DI RACCOLTA
MODALITA' DI RICHIESTA: Pazienti interni: tramite modulo interno prestampato. Pazienti esterni: tramite richiesta del medico curante. PREPARAZIONE DEL PAZIENTE ALL'ESAME: Nessuna. MODALITA' DI RACCOLTA
Latte scremato (di bovino - origine Stati Uniti)
 ISTRUZIONI PER L USO Microrganismi EZ-Accu Shot USO PREVISTO I microrganismi EZ-Accu Shot sono preparati numerati liofilizzati di microrganismi da utilizzare in laboratori industriali per scopi di controllo
ISTRUZIONI PER L USO Microrganismi EZ-Accu Shot USO PREVISTO I microrganismi EZ-Accu Shot sono preparati numerati liofilizzati di microrganismi da utilizzare in laboratori industriali per scopi di controllo
HER2 IQFISH pharmdx (Dako Omnis)
 HER2 IQFISH pharmdx (Dako Omnis) Codice GM333 Seconda edizione HER2 IQFISH pharmdx (Dako Omnis) è un saggio di ibridazione in situ in fluorescenza (FISH) diretta, progettato per la determinazione quantitativa
HER2 IQFISH pharmdx (Dako Omnis) Codice GM333 Seconda edizione HER2 IQFISH pharmdx (Dako Omnis) è un saggio di ibridazione in situ in fluorescenza (FISH) diretta, progettato per la determinazione quantitativa
NORME DI SICUREZZA NEL LABORATORIO DIDATTICO
 NORME DI SICUREZZA NEL LABORATORIO DIDATTICO Pittogrammi di pericolo Vecchia normativa Nuova normativa Vecchia normativa Nuova normativa infiammabile effetti tossici acuti F F+ T T+ esplosivo effetti tossici
NORME DI SICUREZZA NEL LABORATORIO DIDATTICO Pittogrammi di pericolo Vecchia normativa Nuova normativa Vecchia normativa Nuova normativa infiammabile effetti tossici acuti F F+ T T+ esplosivo effetti tossici
ISTRUZIONI PER L USO. Microrganismi EZ-CFU USO PREVISTO COMPONENTI DELLA FORMULA
 ISTRUZIONI PER L USO Microrganismi EZ-CFU USO PREVISTO I microrganismi EZ-CFU sono preparati numerati liofilizzati di microrganismi da utilizzare in laboratori industriali per scopi di controllo di qualità.
ISTRUZIONI PER L USO Microrganismi EZ-CFU USO PREVISTO I microrganismi EZ-CFU sono preparati numerati liofilizzati di microrganismi da utilizzare in laboratori industriali per scopi di controllo di qualità.
Metodi colorimetrici. Metodi immunochimici
 WESTERN BLOTTING Metodi colorimetrici Metodi immunochimici SCOPO DEL WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING Colorazione (Blue Coomassie) Rilevazione con anticorpi SCOPO DEL WESTERN BLOTTING Tecnica
WESTERN BLOTTING Metodi colorimetrici Metodi immunochimici SCOPO DEL WESTERN BLOTTING SCOPO DEL WESTERN BLOTTING Colorazione (Blue Coomassie) Rilevazione con anticorpi SCOPO DEL WESTERN BLOTTING Tecnica
ALLflow Elution Technologies Egg Proteins Rapid Test
 ALLflow Elution Technologies Egg Proteins Rapid Test Lateral Flow kit Cat. # ETBEGG-1003 Kit per la rilevazione rapida delle proteine dell uovo in campioni alimentari ed ambientali Manuale d uso Leggere
ALLflow Elution Technologies Egg Proteins Rapid Test Lateral Flow kit Cat. # ETBEGG-1003 Kit per la rilevazione rapida delle proteine dell uovo in campioni alimentari ed ambientali Manuale d uso Leggere
GARA NAZIONALE DI CHIMICA VIII EDIZIONE PROVA PRATICA
 GARA NAZIONALE DI CHIMICA VIII EDIZIONE PROVA PRATICA Istruzioni Scrivere il proprio nome e cognome su questa pagina e sulla scheda delle risposte. Seguire le regole di sicurezza di laboratorio: se vengono
GARA NAZIONALE DI CHIMICA VIII EDIZIONE PROVA PRATICA Istruzioni Scrivere il proprio nome e cognome su questa pagina e sulla scheda delle risposte. Seguire le regole di sicurezza di laboratorio: se vengono
Leggete l etichetta! Tutto quello che c è da sapere per un utilizzo sicuro dei detersivi e dei prodotti di pulizia per la casa
 Leggete l etichetta! Tutto quello che c è da sapere per un utilizzo sicuro dei detersivi e dei prodotti di pulizia per la casa Presto vedrete sui prodotti per la pulizia domestica nuove etichette con le
Leggete l etichetta! Tutto quello che c è da sapere per un utilizzo sicuro dei detersivi e dei prodotti di pulizia per la casa Presto vedrete sui prodotti per la pulizia domestica nuove etichette con le
PLATELIA ASPERGILLUS IgG Negative and Positive Controls
 PLATELIA ASPERGILLUS IgG Negative and Positive Controls 48 62786 Sieri Umani per il Controllo di Qualità 881090-2012/06 sommario 1. USO PREVISTO...27 2. INDICAZIONI PER L USO...27 3. REAGENTI...27 4. AVVERTENZE
PLATELIA ASPERGILLUS IgG Negative and Positive Controls 48 62786 Sieri Umani per il Controllo di Qualità 881090-2012/06 sommario 1. USO PREVISTO...27 2. INDICAZIONI PER L USO...27 3. REAGENTI...27 4. AVVERTENZE
TOP2A IQFISH pharmdx. Codice K a edizione. Per uso diagnostico in vitro Il kit contiene i reagenti sufficienti per 20 test.
 101752-001 / 20-01-03 TOP2A IQFISH pharmdx Codice K5733 3a edizione Per uso diagnostico in vitro Il kit contiene i reagenti sufficienti per 20 test. P04092IT_02/K573311-2 p. 1/37 Sommario Pagina Finalità
101752-001 / 20-01-03 TOP2A IQFISH pharmdx Codice K5733 3a edizione Per uso diagnostico in vitro Il kit contiene i reagenti sufficienti per 20 test. P04092IT_02/K573311-2 p. 1/37 Sommario Pagina Finalità
SCHEDA DI SICUREZZA Soluzione Acquosa di Biossido di Titanio
 SCHEDA DI SICUREZZA Soluzione Acquosa di Biossido di Titanio HMIS RATING: 0,0,0 SEZIONE 1. Identificazione del prodotto INDIRIZZO PRODUTTORE nome prodotto nome chimico classe di rischio designazione della
SCHEDA DI SICUREZZA Soluzione Acquosa di Biossido di Titanio HMIS RATING: 0,0,0 SEZIONE 1. Identificazione del prodotto INDIRIZZO PRODUTTORE nome prodotto nome chimico classe di rischio designazione della
Û Pulizia e sterilizzazione COMPACT PIEZO LED
 Û Pulizia e sterilizzazione COMPACT PIEZO LED 06 Û PULIZIA E STERILIZZAZIONE 06 Û PULIZIA E STERILIZZAZIONE 06.1 Û PULIZIA E STERILIZZAZIONE DEL MANIPOLO PREPARAZIONE - Disconnettere il manipolo dal cordone
Û Pulizia e sterilizzazione COMPACT PIEZO LED 06 Û PULIZIA E STERILIZZAZIONE 06 Û PULIZIA E STERILIZZAZIONE 06.1 Û PULIZIA E STERILIZZAZIONE DEL MANIPOLO PREPARAZIONE - Disconnettere il manipolo dal cordone
I materiali utilizzati per questa seconda parte sono stati già descritti nel paragrafo 4.1.
 La seconda parte del progetto di dottorato ha riguardato l approfondimento della caratterizzazione chimico-fisica e meccanica di hydrogel di chitosano, in particolare per quanto riguarda l influenza della
La seconda parte del progetto di dottorato ha riguardato l approfondimento della caratterizzazione chimico-fisica e meccanica di hydrogel di chitosano, in particolare per quanto riguarda l influenza della
