Capitolo 13 Acidi Carbossilici e Derivati
|
|
|
- Maria Teresa Pappalardo
- 9 anni fa
- Просмотров:
Транскрипт
1 himica rganica Informazione Scientifica sul Farmaco apitolo 13 Acidi arbossilici e Derivati rganic hemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic hemistry, 3 rd Edition Paula Y. Bruice, Prentice Hall
2 Introduzione Il gruppo funzionale degli acidi carbossilici è costituito da un = con legato un H. R H Il gruppo carbossilico normalmente si scrive -H. Gli acidi carbossilici alifatici hanno un gruppo alchilico legato al - H. Gli acidi carbossilici aromatici hanno un gruppo arilico legato al - H. Gli acidi grassi sono acidi alifatici a lunga catena. 2
3 Importanza Acido acetico, presente nell aceto, usato nell industria come solvente, catalizzatore e reagente nelle sintesi. Acidi grassi presenti in grassi e oli. Acidi benzoici nei farmaci e nei conservanti. Acido adipico usato per fare il nylon 66. Acido ftalico usato per fare i poliesteri. H Acido stearico Un acido grasso H H 3 H 3 HH 2 HH H 3 H 3 Acido acetilsalicilico aspirina Ibuprofene moment, antalgyl, nurofen 3
4 Nomi comuni Molti acidi alifatici hanno nomi comuni. Le posizioni dei sostituenti lungo la catena sono indicati con le lettere greche. l H 3 H 2 H H Ph H 3 H 2 H 2 HH 2 H Acido α-clorobutirrico Acido β-fenilcaproico 4
5 Nomi IUPA La o degli alcani è sostituita con -oico e si premette acido. Il carbonio carbossilico è il #1. Il gruppo carbossilico ha la priorità rispetto a doppi e tripli legami, gruppi ossidrilici e carbonilici l H 3 H 2 H Acido 2-clorobutanoico H H Ph H H H Acido trans-3-fenil-2-propenoico (acido cinnamico) 1 H Acido 5-etil-6-idrossi-7-metil-3-oxo-7-nonenoico 5
6 Acidi carbossilici ciclici Quando un cicloalcano è legato direttamente ad un -H il nome è acido cicloalcancarbossilico. Se il H è legato al benzene l acido si chiama benzoico. H H H(H 3 ) 2 Acido 2-isopropilciclopentancarbossilico H Acido o-idrossibenzoico (acido salicilico) 6
7 Acidi bicarbossilici Gli acidi bicarbossilici hanno spesso nomi comuni (vanno memorizzati). Nomi IUPA: il gruppo 1 è quello più vicino al primo sostituente. Due gruppi carbossilici su un benzene: acidi ftalici. Br HH 2 HH 2 H 2 H Acido 3-bromoesandioico (acido β-bromoadipico) 7
8 Struttura del carbossile arbonio sp 2. Angoli di legame circa H eclissato con =, per avere la sovrapposizione degli orbitali π con il doppietto libero dell ossigeno. 8
9 Proprietà fisiche Punti di ebollizione più alti di quelli degli alcoli di pari peso molecolare a causa della formazione di dimeri. La solubilità in acqua diminuisce all aumentare del numero di carboni. Fino a 4 carboni gli acidi sono miscibili con l acqua. Più solubili degli alcoli. Solubili anche in solventi moderatamente polari come il cloroformio, si scioglie in forma di dimero. 9
10 Acidità Gli acidi carbossilici (Ka~10-5 ) sono più acidi dei fenoli (Ka~10-10 ) e degli alcoli (Ka~10-16 ) La maggiore acidità è dovuta alla stabilizzazione per risonanza della base coniugata 10
11 Effetto dei sostituenti sull acidità H H H H H N 2 N 2 H 3 N 2 p-methoxy benzoic acid m-nitro p-nitro o-nitro pk a = 4.46 pk a = 4.19 pk a = 3.47 pk a = 3.41 pk a =
12 Sali degli acidi carbossilici L idrossido di sodio rimuove un protone dagli acidi formando sali Se si aggiunge un acido più forte, come Hl, si riforma l acido (l acido forte sposta l acido debole). Aq. NaH RH R - Na + Aq. Hl Nome dell anione: sotituire -oico con -oato. Nome del catione l H 3 H 2 HH 2 - K + 3-cloropentanoato di potassio β-clorovalerato di potassio
13 Proprietà dei sali Di solito solidi ed inodori. I carbossilati di Na +, K +, Li +, e NH 4+ sono solubili in acqua. I saponi sono i sali degli acidi grassi (acidi a lunga catena, ). I Sali si possono preparare per reazione di un acido con NaH 3, si sviluppa 2. 13
14 Sintesi Review ssidazione degli alcoli primari e delle aldeidi con r VI (Na 2 r 2 7 /H 2 S 4 ). H 3 H 2 H 2 H H 3 H 2 H Na 2 r 2 7 H 2 S 4 Na 2 r 2 7 H 2 S 4 H 3 H 2 H H 3 H 2 H 14
15 Derivati degli acidi carbossilici Il gruppo legato al carbonio acilico determina la classe del composto: -H, acidi carbossilici arbonio acilico -l, cloruri acilici -R, esteri -NH 2, ammidi R H Possono essere interconvertiti con una certa facilità 15
16 Nomenclatura esteri Sono identificati come alchil carbossilati. Il gruppo alchilico deriva da un alcol, il carbossilato da un acido. H 3 H 3 HH 2 H 3 2-metilpropil etanoato HH 2 benzil metanoato Esteri ciclici Reazione tra un -H e un -H nella stessa molecola, lattone. Si premette la parola lattone al nome IUPA dell acido. H 3 lattone 4-idrossi-2-metilpentanoico H 3 16
17 Ammidi Formalmente deriva da un acido carbossilico e da ammoniaca o ammina. Non sono basiche perché il doppietto dell azoto _ è delocalizzato. H + H H N H N H H Ammide primaria: un solo legame -N (due N-H). Ammide secondaria: (N-sostituita) due legami -N (un N-H). Ammide terziaria: (N,N-disostituita) tre legami -N (nessun N-H) H 3 H 3 NH 2 Ammide 1 H 3 NH Ammide 2 H 3 Ammide 3 H 3 N H2H3 17
18 Nomenclatura ammidi Per le ammidi 1 sostituire -oico nel nome dell acido con -ammide. Per le 2 e 3, il gruppo alchilico legato all azoto è preceduto da N-. H 3 H 3 H N H 2 H 3 H 3 N-etil-N-metil-2-metilpropanammide Ammidi cicliche (lattami) Legame ammidico intramolecolare, lattami. α β γ N H 3 H γ-valerolattame 18
19 Alogenuri acilici Si preparano dall acido per reazione con Sl 2. H 3 H 2 H Sl 2 H 3 H 2 l Sono più reattivi degli acidi carbossilici. Nome: sostituire -oico dell acido con -oile e premettere il nome dell alogenuro l Br H 3 HH 2 Br cloruro di benzoile Benzoil cloruro bromuro di 3-bromobutanoile 3-bromobutanoil bromuro 19
20 Anidridi Formalmente si ottengono da due molecole di acido per perdita di una molecola di acqua. Più reattive degli acidi, meno degli alogenuri. R H H R R R Nomenclatura La parola acido sostituita con anidride. Gli acidi bicarbossilici formano anidridi cicliche di 5- o 6-termini. H 3 H 3 Anidride etanoica Anidride acetica Anidride 1,2-benzenedicarbossilica Anidride ftalica 20
21 Reattività: cloruri acilici Il carbonio carbossilico è elettrofilo, per cui reagisce con i nucleofili (vedi anche composti carbonilici) Il cloruro è un buon gruppo uscente, la reazione prosegue La reazione prende il nome di sostituzione nucleofila acilica È facilitata da buoni gruppi uscenti. Nu Nu δ - R δ - R δ+ H δ+ l R R Nu H l Nu R Nu δ - R δ+ l 21
22 Altri derivati cloruri acilici I cloruri acilici reagiscono con gli alcoli per formare esteri. Si tratta di una sostituzione nucleofila acilica. l H 3 + H 3 H + Hl I cloruri acilici reagiscono con ammoniaca e ammine per dare ammidi. l NHH 3 NaH + H 3 NH 2 + Nal + H 2 22
23 Esterificazione di Fischer Acido + alcol estere + acqua. atalizzata dagli acidi. Tutti i passaggi sono reversibili. E un equilibrio, per cui vanno scelte opportunamente le condizioni. H + H 3 H 2 H H + H 2 H 3 + HH 23
24 Interconversione I derivati più reattivi si convertono facilmente in quelli meno reattivi. 24
25 Idrolisi Tutti i derivati reagiscono con H 2 (con catalizzatore) per formare acidi carbossilici H 3 H 3 l + HH H 3 H + Hl H + H 3 + HH H 3 H + H 3 H H 3 H 2 NHH 3 + Hl H 3 H + H 3 NH 3 + l - 25
26 Saponificazione Idrolisi degli esteri Base-catalizzata. Saponificatione perché è il metodo di preparazione tradizionale dei saponi I saponi si preparano facendo bollire NaH con i grassi (trigliceridi) si formano i Sali sodici degli acidi grassi. Un esempio di sapone è il sodio stearato, Na +- (H 2 ) 16 H 3. R-H A triacylglycerol (a triglyceride) H 2 -R H 2 -R + 3NaH saponification H 2 H HH H 2 H 1,2,3-Propanetriol (Glycerol; Glycerin) + 3R - Na + Sodium soaps 26
27 ome funziona un sapone NaH 27
28 Riduzione ad alcoli 1 Si usano riducenti forti, LiAlH 4. Il Borano, BH 3 in THF, riduce gli acidi carbossilici ma non i chetoni. 28
29 Riduzione delle Ammidi LiAlH 4 riduce le ammidi 1 ad ammine 1. Le ammidi 2 sono ridotte ad ammine 2. Le ammide 3 sono ridotte ad ammine 3. H 3 NHH 3 H 3 H 2 NHH 3 1) LiAlH 4 2) H 2 29
30 ondensazione di laisen Gli idrogeni in α al gruppo estereo hanno pka circa 23 (i chetoni circa 19) Possono essere strappati con una base forte e formare uno ione enolato α H R base R R 30
31 ondensazione di laisen Lo ione enolato può attaccare una seconda molecola di estere dando un β-cheto estere H H - R - H R R R R R H 3 α H 2 H 3 + H 2 H H 2 H 3 1. H 3 H 2 Na 2. Hl H 3 H 2 + H 2 H 3 H 3 H 2 H 31
32 Polichetidi Una serie di condensazioni di laisen porta alla formazione di polichetidi, precursori ad esempio degli antibiotici macrolidici H 3 α H 2 H 3 + H 2 H H 2 H 3 1. H 3 H 2 Na 2. Hl H 3 H 2 H 2 H 3 H 3 H 2 H 3 H 3 H 2 H 2 H 2 H 3 n H 3 H 2 H 2 H 2 H 3 32
33 Fine del apitolo 13 33
Capitolo 8 Acidi Carbossilici e Derivati
 Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Composti Carbossilici. Acidi Carbossilici
 Composti Carbossilici Acidi Carbossilici ACIDI CARBSSILICI Gli acidi carbossilici sono caratterizzati dalla presenza del gruppo carbonilico legato ad un gruppo idrossilico R C Il gruppo carbossilico viene
Composti Carbossilici Acidi Carbossilici ACIDI CARBSSILICI Gli acidi carbossilici sono caratterizzati dalla presenza del gruppo carbonilico legato ad un gruppo idrossilico R C Il gruppo carbossilico viene
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
ACIDI CARBOSSILICI. ac. formico ac. acetico ac. benzoico
 ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
Acidi Carbossilici CH 3. Caratterizzati dalla presenza di un gruppo carbossilico. Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico)
 Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Acidi carbossilici e derivati
 Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Acidi carbossilici. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Acidi carbossilici e derivati Composti organici che contengono legami doppi C=O e legami singoli C-eteroatomo (oppure il gruppo CN)
 himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
I composti acilici sono tutti quei composti che contengono il gruppo:
 omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Acidi carbossilici: nomenclatura. alcano -> acido alcanoico
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Si trovano generalmente come dimeri ciclici a causa dei legami a idrogeno
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Composti Carbossilici. Derivati Carbossilici
 omposti arbossilici Derivati arbossilici Derivati degli Acidi I derivati degli acidi carbossilici hanno attaccato al gruppo carbonilico anziché l'idrossile (-) altri gruppi elettron attrattori come: -N
omposti arbossilici Derivati arbossilici Derivati degli Acidi I derivati degli acidi carbossilici hanno attaccato al gruppo carbonilico anziché l'idrossile (-) altri gruppi elettron attrattori come: -N
FENOLI: nomenclatura IUPAC
 FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Sostituzione nucleofila Addizione a gruppi carbonilici Addizione a doppi legami attivati
 himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
Capitolo 10 Composti Aromatici
 himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI
 REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Aldeidi e chetoni. Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni
 Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI
 REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
Ammine R N + H. ammina terziaria ammina secondaria ammina primaria sale di ammonio quaternario
 AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
Gli Acidi Carbossilici ed i loro Derivati
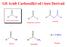 Gli Acidi arbossilici ed i loro Derivati Acido carbossilico X Alogenuro acilico Anidride ' ' N 2 N Estere Ammide Nitrile Nomenclatura degli Acidi arbossilici 3 3 2 3 2 1 Acido propanoico 3 2 2 5 4 3 2
Gli Acidi arbossilici ed i loro Derivati Acido carbossilico X Alogenuro acilico Anidride ' ' N 2 N Estere Ammide Nitrile Nomenclatura degli Acidi arbossilici 3 3 2 3 2 1 Acido propanoico 3 2 2 5 4 3 2
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1
 CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Esteri degli acidi carbossilici
 Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Acidi carbossilici
 Acidi carbossilici Nomi IUPAC Acido propanoico, Acido 4-Metilpentanoico, Acido 3-Etil-6-metilottandioico, Acido 3- Bromocicloesancarbossilico, Acido 1-Ciclopentencarbossilico, 4-Metilpentanonitrile
Acidi carbossilici Nomi IUPAC Acido propanoico, Acido 4-Metilpentanoico, Acido 3-Etil-6-metilottandioico, Acido 3- Bromocicloesancarbossilico, Acido 1-Ciclopentencarbossilico, 4-Metilpentanonitrile
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI
 IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
PROPRIETA FISICHE DEI COMPOSTI ORGANICI
 PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
Introduzione alla biochimica AO 11/14
 Introduzione alla biochimica AO 11/14 Il Gruppo Carbonilico 1. E uno dei gruppi funzionali più importanti 2. Sp2, legame polarizzato 1. Ossigeno elettronegativo: effetto induttivo 2. Effetto di risonanza
Introduzione alla biochimica AO 11/14 Il Gruppo Carbonilico 1. E uno dei gruppi funzionali più importanti 2. Sp2, legame polarizzato 1. Ossigeno elettronegativo: effetto induttivo 2. Effetto di risonanza
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
Capitolo 7 Composti organici alogenati
 himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
Reazioni degli epossidi
 12-04-2016 Reazioni degli epossidi Apertura dell anello acido-catalizzata, esempi Struttura intermedio: 3 forme limiti di risonanza H H a a O O b b H O CH 3 CH 3 CH 3 H H H H Struttura ibrido intermedio
12-04-2016 Reazioni degli epossidi Apertura dell anello acido-catalizzata, esempi Struttura intermedio: 3 forme limiti di risonanza H H a a O O b b H O CH 3 CH 3 CH 3 H H H H Struttura ibrido intermedio
Acido maleico anidride maleica acido ftalico andidride ftalica
 Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Aldeidi e Chetoni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
23 Le diverse classi di composti organici
 23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Unità Didattica 10. I composti carbonilici. Struttura, nomenclatura e reattività
 I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
H N H R N H R N R R N R H H H
 AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
Acido citrico. Nome IUPAC: Acido 3-carbossi-3-idrossi-1,5-pentandioico
 Acidi carbossilici Dove si trovano? 2 Acido citrico L'acido citrico è uno degli acidi più diffusi negli organismi vegetali ed è un prodotto metabolico di tutti quelli aerobici. Il succo di limone ne contiene
Acidi carbossilici Dove si trovano? 2 Acido citrico L'acido citrico è uno degli acidi più diffusi negli organismi vegetali ed è un prodotto metabolico di tutti quelli aerobici. Il succo di limone ne contiene
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri)
 CHIMICA ACIDO BASE DI COMPOSTI CARBONILICI Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri) Che altra reazione può avvenire al centro carbonilico
CHIMICA ACIDO BASE DI COMPOSTI CARBONILICI Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri) Che altra reazione può avvenire al centro carbonilico
N H CH 3 H 3 C. Ammine. Struttura. Classificazione. Nomenclatura. Reattività
 Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
Unità didattica 7 (segue) Reattività del benzene. Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili
 Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Alchini. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
DAI GRUPPI FUNZIONALI AI POLIMERI
 DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico
 Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Ammine N R N R R R-NH 2. Gruppo funzionale: NH 2. Gruppo amminico. Ammine terziarie. Ammine primarie. Ammine secondarie
 Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Aldeidi e chetoni. 1) Rottura α 2) Rottura i. Più pronunciate nei chetoni. 3) Rottura β con trasposizione di H in γ (McLafferty)
 Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
Assorbimenti di alcani (stretching. Corso Metodi Fisici in Chimica Organica Prof. Renzo LUISI Uniba. vietata la vendita
 Assorbimenti di alcani (stretching C-H) Corso Metodi Fisici in Chimica rganica Prof. Renzo LUISI Uniba. vietata la vendita Analisi di spettri: ALCANI (C-H) 4000 3500 3000 2500 2000 1500 1300 1000 700 500
Assorbimenti di alcani (stretching C-H) Corso Metodi Fisici in Chimica rganica Prof. Renzo LUISI Uniba. vietata la vendita Analisi di spettri: ALCANI (C-H) 4000 3500 3000 2500 2000 1500 1300 1000 700 500
CHIMICA. F 20 Classi di composti organici
 CHIMICA F 20 Classi di composti organici 1 I gruppi funzionali I composti di cui ci siamo interessati fin qui sono idrocarburi, cioè composti costituiti soltanto da carbonio e idrogeno. In molte molecole
CHIMICA F 20 Classi di composti organici 1 I gruppi funzionali I composti di cui ci siamo interessati fin qui sono idrocarburi, cioè composti costituiti soltanto da carbonio e idrogeno. In molte molecole
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI
 RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
