Scheda n. 14. Vania Bresolin Cinetica enzimatica. Costruzione di una curva di taratura standard glucosio + fruttosio
|
|
|
- Marcellina Bertoni
- 6 anni fa
- Visualizzazioni
Transcript
1 Scheda n. 14 Vania Bresolin Cinetica enzimatica Costruzione di una curva di taratura standard glucosio + fruttosio ITAS Santorre di Santarosa Istituto Tecnico, settore Tecnologico Indirizzo Chimica, Materiali e Biotecnologie Opzioni: Biotecnologie Sanitarie Biotecnologie Ambientali Laboratori di Chimica corso Peschiera, Torino tel sito web santorre@santorre.it Progetto: Libro elettronico di laboratorio docenti: Vania Bresolin Patrizia Sgalambro Gianni Saglietto anno scolastico
2 Gli obiettivi di questa esperienza sono: Obiettivi e principi teorici Acquisire abilità manuale nell utilizzo di pipette e micropipette. Misurare allo spettrofotometro le assorbanze di soluzioni a concentrazione nota di glucosio e fruttosio dopo reazione con un reagente che dà origine ad un cromoforo. Costruire una curva di taratura standard che metta in relazione i valori di assorbanza con le concentrazioni note di glucosio e fruttosio. Allo scopo di realizzare gli obiettivi, si preparano diverse soluzione a concentrazione nota dei due monosaccaridi e si fanno reagire le soluzioni a concentrazione nota di glucosio e fruttosio con una soluzione di 3,5-dinitrosalicilato di sodio, colorata di giallo. Il 3,5-dinitrosalicilato di sodio reagisce in modo quantitativo con gli zuccheri e viene da questi ridotto a 3-ammino, 5-nitrosalicilato di sodio rosso, che presenta un massimo di assorbimento della luce a 540 nm. Si costruisce quindi la curva di taratura standard misurando mediante lo spettrofotometro, l assorbanza di soluzioni di concentrazioni differenti di 3-ammino, 5-nitrosalicilato di sodio ottenute a partire da soluzioni a concentrazione nota di D-glucosio e D-fruttosio. Prima misurare allo spettrofotometro le assorbanze delle soluzioni di 3-ammino, 5-nitrosalicilato di sodio è necessario azzerare lo strumento. Questa operazione viene indicata come fare il bianco e richiede che tutte le sostanze coinvolte direttamente o indirettamente nella reazione (reagenti e loro solventi), tranne la specie da determinare, anche se colorate, vengano poste in maniera fittizia ad un valore zero di assorbanza. Lo scopo di questa operazione è quello di fare in modo che, a reazione avvenuta, sia possibile rilevare solo i cambiamenti rispetto alla situazione di partenza. In altre parole, la miscela di reazione utilizzata per determinare il bianco deve contenere tutti i reagenti escluso quello che subirà la reazione, quindi in questo caso tutte le sostanze tranne il glucosio e il fruttosio. La curva di taratura che prepareremo è ricavata da una soluzione che contiene, oltre a glucosio e fruttosio (due zuccheri riducenti), anche saccarosio (uno zucchero non riducente). Il saccarosio non subirà l ossidazione da parte del 3,5-dinitrosalicilato di sodio, ma la sua presenza nella miscela di reazione è importante come bianco. Nelle due esperienze successive, dove verrà studiata l influenza di alcuni parametri sull attività enzimatica, vedremo come questo disaccaride svolga un ruolo determinante dando origine a zuccheri riducenti, pur restando, in parte, inalterato nella miscela di reazione. La curva di taratura glucosio + fruttosio sarà utilizzata per determinare le concentrazioni incognite di glucosio + fruttosio che si verranno a formare dalla reazione dell enzima invertasi (o saccarasi) sul substrato saccarosio. Basterà infatti, dal punto della curva di taratura corrispondente al valore della assorbanza trovata, abbassare una retta sull ascissa per trovare la concentrazione di glucosio + fruttosio della soluzione in esame. La concentrazione di glucosio + fruttosio può anche essere determinata dall equazione della retta di taratura. 2
3 Attrezzatura e materiali Attrezzatura Spettrofotometro Vortex 2 Bunsen 2 Treppiede con reticella spargifiamma 2 Becher da 1 L con apposito portaprovette 4 posti Portaprovette 12 posti 8 Provette 16 x Tappi ad innesto per provette 16 x 160 Pinza di legno Provette 16 x160 e tappi ad innesto per provette Micropipetta da 0,1-1 ml con rispettivi puntali Micropipetta da 1-5 ml con rispettivi puntali Pipetta graduata da 10 ml Palla di Peleo Cuvette Materiali Soluzione 0,01 M di glucosio + fruttosio Soluzione 0,5 M di saccarosio Soluzione tampone acetato 0,05 M ph = 4,7 Soluzione 1% 3,5-dinitrosalicilato di sodio Acqua distillata 3
4 Procedimento L esperienza viene condotta in coppia. Un allievo introduce i reagenti nelle prime quattro provette, il secondo nelle altre quattro. Mettere l acqua nei 2 becher da litro con l apposito portaprovette a 4 posti e scaldare fino ad ebollizione. Intanto disporre 8 provette nel portaprovette a 12 posti e numerarle da 1 a 8 con il pennarello vetrografico. Disporre i reagenti nel seguente ordine: tampone acetato 0,05 M ph = 4,7 saccarosio 0,5 M glucosio + fruttosio 0,01 M acqua 3,5-dinitrosalicilato di sodio 1 %. Introdurre nelle 8 provette (p1-p8) i reagenti nei volumi qui di seguito riportati. Quando sarà necessario verrà anche indicata l operazione da compiere ad un certo momento della sequenza. Reagenti Volumi [ml] nelle provette p1 p2 p3 p4 p5 p6 p7 p8 tampone acetato 0,05 M ph = 4,7 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 saccarosio 0,5 M 1,0 1,0 1,0 1,0 1,0 1,0 1,0 1,0 glucosio + fruttosio 0,01 M / 0,2 0,4 0,6 0,8 1,0 1,2 1,4 acqua 1,5 1,3 1,1 0,9 0,7 0,5 0,3 0,1 3,5-dinitrosalicilato di sodio 1 % 2,0 2,0 2,0 2,0 2,0 2,0 2,0 2,0 Immergere le provette in acqua bollente (inizio reazione) per 5 minuti esatti. (La reazione tra glucosio / fruttosio e il 3,5-dinitrosalicilato di sodio avviene solo in queste condizioni). acqua 7,0 7,0 7,0 7,0 7,0 7,0 7,0 7,0 Chiudere le provette con i tappi ad innesto. Agitare le provette nel vortex per uniformare le soluzioni e raffreddare a temperatura ambiente. Azzerare lo spettrofotometro con il bianco (soluzione nella provetta 1) alla lunghezza d onda di 540nm. Leggere allo spettrofotometro le assorbanze delle soluzioni contenute nelle altre provette e annotare le misure nella sezione dati e calcoli. Costruire il grafico di taratura secondo quanto indicato nella sezione dati e calcoli. 4
5 Dati e calcoli Dati Concentrazione slz GLU+FRU : 0,01 M = 0,01 mol/l = 0,01 mmol/ml V FINALE reazione = 12 ml V slz GLU+FRU aggiunti nelle 8 provette (p1 p8) [ml] N provetta p1 p2 p3 p4 p5 p6 p7 p8 V slz GLU+FRU 0,0 0,2 0,4 0,6 0,8 1,0 1,2 1,4 Trascrivere i valori delle assorbanze misurate allo spettrofotometro alla lunghezza d onda di 540 nm. Dati registrati: Assorbanze misurate a 540 nm (A 540nm ) N provetta p1 p2 p3 p4 p5 p6 p7 p8 A 540 nm 0,000 Calcoli Primo parametro da determinare è la concentrazione di glucosio + fruttosio in µmol/ml (C GLU+FRU [µmol/ml]) presente nelle 8 provette. Impostazione dei calcoli C GLU+FRU [µmol/ml] C slz GLU+FRU [mmol/ml] x V GLU+FRU aggiunti [ml] x1000 [µmol/mmol] V FINALE reazione [ml] Le concentrazioni di glucosio + fruttosio nelle 8 provette sono le seguenti: Concentrazioni (C) di glucosio+ fruttosio [µmol/ml] nelle 8 provette (p1-p8) N provetta p1 p2 p3 p4 p5 p6 p7 p8 C GLU+FRU 0,000 Altro parametro da determinare è l equazione della retta di taratura e quindi il coefficiente angolare m di tale retta. Occorre pertanto costruire un grafico. 5
6 Si annotano dapprima in una tabella i valori di assorbanza letti a 540 nm, che verranno poi riportati in ordinate (asse y) e i valori calcolati delle concentrazioni di glucosio + fruttosio espressi in µmol/ml, che verranno poi riportati in ascisse (asse x). C GLU+FRU [µmol/ml]) Assorbanza a 540 nm (A 540nm ) Costruire il grafico utilizzando un apposito programma (Excel oppure Open Office). Riportati i valori sull asse delle x e delle y, si individuano otto punti di coordinate x;y. Tracciare una retta che interpoli i punti segnati sul grafico che parta dall origine degli assi, ossia dal punto (0;0), escludendo, se necessario, valori anomali. Nota La retta deve passare per l origine, ossia per il punto 0;0. Ricordarsi pertanto di impostare intercetta = 0;0. La retta deve avere equazione y = mx, poiché q = 0. Costruito il grafico, annotare nella tabella seguente i parametri della retta di taratura glucosio + fruttosio: Parametri della retta di taratura glucosio + fruttosio m q 0 Equazione della retta di taratura glucosio + fruttosio: 6
7 Approfondimento I dati misurati e i risultati ottenuti nel corso dell anno scolastico dagli alunni della classe quinta sezione M sono riassunti nelle seguenti tabelle: Dati registrati Alunni Assorbanze misurate a 540 nm (A 540nm ) nelle provette p1 p2 p3 p4 p5 p6 p7 p8 Gottardi - Pezua O. 0,000 0,098 0,198 0,318 0,479 0,592 0,766 0,871 Spagnolo - Divolo 0,000 0,140 0,263 0,385 0,496 0,615 0,720 0,874 Piepoli - Berrino 0,000 0,115 0,207 0,299 0,503 0,605 0,714 0,862 Guglielmo - Boni 0,000 0,121 0,237 0,362 0,526 0,624 0,721 0,832 Pezua A. Molaro 0,000 0,135 0,255 0,368 0,501 0,610 0,713 0,864 Bertinotti - Tota 0,000 0,092 0,194 0,336 0,423 0,577 0,667 0,810 Bochicchio - Savino 0,000 0,097 0,236 0,388 0,454 0,614 0,692 0,766 Assorbanze medie nelle otto provette (p1-p8) N provetta p1 p2 p3 p4 p5 p6 p7 p8 A 540nm media 0,000 0,114 0,227 0,351 0,483 0,605 0,713 0,840 7
8 Riportando sull asse delle ascisse (asse x) i valori delle concentrazioni di glucosio + fruttosio calcolate espresse in µmol/ml e sull asse delle ordinate (asse y) i valori medi delle assorbanze misurate alla lunghezza d onda di 540 nm, si ottiene il seguente grafico: A 540nm 0,900 0,800 0,700 0,600 0,500 0,400 0,300 0,200 0,100 Curva di taratura glucosio + fruttosio - media classe y = 0,7174x R² = 0,9994 0,000 0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 C glu + fru [µmol/ml] Parametri della retta di taratura GLU + FRU m q 0,72 0 Equazione retta di taratura: y = 0,72 x 8
9 Bibliografia Biochimica di base in laboratorio Giuliano Ricciotti Italo Bovolenta Editore, ISBN Carbohydrate Analysis: Can We Control the Ripening of Bananas? S. Todd Deal,* Catherine E. Farmer, and Paul F. Cerpovicz Journal of Chemical Education 2002, 79 (4), p 479 9
Scheda n.15. Vania Bresolin Cinetica enzimatica. Determinazione dell attività specifica di un enzima
 Scheda n.15 Vania Bresolin Cinetica enzimatica Determinazione dell attività specifica di un enzima ITAS Santorre di Santarosa Istituto Tecnico, settore Tecnologico Indirizzo Chimica, Materiali e Biotecnologie
Scheda n.15 Vania Bresolin Cinetica enzimatica Determinazione dell attività specifica di un enzima ITAS Santorre di Santarosa Istituto Tecnico, settore Tecnologico Indirizzo Chimica, Materiali e Biotecnologie
Scheda n. 13. Vania Bresolin Cinetica enzimatica. Scheda preparativa
 Scheda n. 13 Vania Bresolin inetica enzimatica Scheda preparativa ITAS Santorre di Santarosa Istituto Tecnico, settore Tecnologico Indirizzo himica, Materiali e Biotecnologie Opzioni: Biotecnologie Sanitarie
Scheda n. 13 Vania Bresolin inetica enzimatica Scheda preparativa ITAS Santorre di Santarosa Istituto Tecnico, settore Tecnologico Indirizzo himica, Materiali e Biotecnologie Opzioni: Biotecnologie Sanitarie
LABORATORIO DI SCIENZE NATURALI
 1 LABORATORIO DI SCIENZE NATURALI ESPERIENZA: L INVERTASI E L IDROLISI DEL SACCAROSIO Indice dei contenuti Obiettivo Introduzione o L enzima o Il substrato o L idea portante dell esperimento Lista dei
1 LABORATORIO DI SCIENZE NATURALI ESPERIENZA: L INVERTASI E L IDROLISI DEL SACCAROSIO Indice dei contenuti Obiettivo Introduzione o L enzima o Il substrato o L idea portante dell esperimento Lista dei
Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione
 1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione In banana durante il processo di maturazione avviene la trasformazione di amido in zuccheri riducenti
1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione In banana durante il processo di maturazione avviene la trasformazione di amido in zuccheri riducenti
Acido 3,5-dinitrosalicilico Glucosio Acido 3-amino-5-nitrosalicilico Acido gluconico (Incolore-giallo leggero)
 1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
RISOLUZIONE OIV/ENO 340/2010. DETERMINAZIONE DELL ATTIVITA β-glucanasi (β 1-3, β 1-6) DELLE PREPARAZIONI ENZIMATICHE
 RISOLUZIONE OIV/ENO 340/2010 DETERMINAZIONE DELL ATTIVITA β-glucanasi (β 1-3, β 1-6) DELLE PREPARAZIONI ENZIMATICHE L'ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo 2 iv dell Accordo del 3 aprile 2001
RISOLUZIONE OIV/ENO 340/2010 DETERMINAZIONE DELL ATTIVITA β-glucanasi (β 1-3, β 1-6) DELLE PREPARAZIONI ENZIMATICHE L'ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo 2 iv dell Accordo del 3 aprile 2001
Estrazione di acido salicilico con acetato di n-butile
 S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Estrazione di acido salicilico con acetato di n-butile L estrazione liquido-liquido
S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Estrazione di acido salicilico con acetato di n-butile L estrazione liquido-liquido
Laboratorio 29.1 CINETICA DI IDROLISI ALCALINA DELL ACETATO DI ETILE
 2 Analisi chimica strumentale Laboratorio 29.1 CINETICA DI IDROLISI ALCALINA DELL ACETATO DI ETILE SCOPO Determinazione della costante di velocità, dell energia di attivazione e del fattore di frequenza
2 Analisi chimica strumentale Laboratorio 29.1 CINETICA DI IDROLISI ALCALINA DELL ACETATO DI ETILE SCOPO Determinazione della costante di velocità, dell energia di attivazione e del fattore di frequenza
CINETICA ENZIMATICA: DETERMINAZIONE DELLA V M E DELLA K M DELL ENZIMA SACCARASI
 CINETICA ENZIMATICA: DETERMINAZIONE DELLA M E DELLA K M DELL ENZIMA SACCARASI PRINCIPI TEORICI Le reazioni che avvengono nelle cellule sono le stesse che avvengono in laboratorio, ciò che le differenzia
CINETICA ENZIMATICA: DETERMINAZIONE DELLA M E DELLA K M DELL ENZIMA SACCARASI PRINCIPI TEORICI Le reazioni che avvengono nelle cellule sono le stesse che avvengono in laboratorio, ciò che le differenzia
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
MA + H + MAH + Materiale: 500 cc di soluzione di NaOH 0.01 M 500 cc di soluzione di HCl 0.01 M fresca Metil-arancio (MA) Etanolo Acqua distillata
 Cambiamenti nell aspetto degli spettri di assorbimento elettronico del metilarancio in funzione del ph a seguito della reazione di protonazione del metilarancio. Scopo dell esperimento è osservare la variazione
Cambiamenti nell aspetto degli spettri di assorbimento elettronico del metilarancio in funzione del ph a seguito della reazione di protonazione del metilarancio. Scopo dell esperimento è osservare la variazione
Laboratorio 10.3 DETERMINAZIONE DEL FENOLO NELLE ACQUE
 2 Analisi chimica strumentale Laboratorio 10.3 DETERMINAZIONE DEL FENOLO NELLE ACQUE Determinazione spettrofotometrica U con il metodo delle aggiunte multiple Confronti tra l utilizzo dell altezza del
2 Analisi chimica strumentale Laboratorio 10.3 DETERMINAZIONE DEL FENOLO NELLE ACQUE Determinazione spettrofotometrica U con il metodo delle aggiunte multiple Confronti tra l utilizzo dell altezza del
DETERMINAZIONE della MASSA di ACIDO ACETICO PRESENTE in un 1 L di ACETO
 DETERMINAZIONE della MASSA di ACIDO ACETICO PRESENTE in un 1 L di ACETO OBIETTIVO: determinare i grammi di acido acetico presenti in 1 litro di aceto comune (concentrazione in g/l). Approccio al problema:
DETERMINAZIONE della MASSA di ACIDO ACETICO PRESENTE in un 1 L di ACETO OBIETTIVO: determinare i grammi di acido acetico presenti in 1 litro di aceto comune (concentrazione in g/l). Approccio al problema:
Esperienza n. 6 Costruzione per via potenziometrica della curva di titolazione acido debole base forte
 Esperienza n. 6 Costruzione per via potenziometrica della curva di titolazione acido debole base forte OBBIETTIVI Lo scopo di questa esperienza è quello di costruire la curva di titolazione acido debole-base
Esperienza n. 6 Costruzione per via potenziometrica della curva di titolazione acido debole base forte OBBIETTIVI Lo scopo di questa esperienza è quello di costruire la curva di titolazione acido debole-base
DETERMINAZIONE DEL CONTENUTO IN CAFFEINA
 DETERMINAZIONE DEL CONTENUTO IN CAFFEINA (PER VIA SPETTROFOTOMETRICA ATTRAVERSO LA COSTRUZIONE DELLA RETTA DI TARATURA). O CH 3 H 3 C 1 6 N N 7 5 2 8 O N N 3 4 9 CH 3 Caffeina (1,3,7-trimetil-3,7-diidro-1H-purin-2,6-dione)
DETERMINAZIONE DEL CONTENUTO IN CAFFEINA (PER VIA SPETTROFOTOMETRICA ATTRAVERSO LA COSTRUZIONE DELLA RETTA DI TARATURA). O CH 3 H 3 C 1 6 N N 7 5 2 8 O N N 3 4 9 CH 3 Caffeina (1,3,7-trimetil-3,7-diidro-1H-purin-2,6-dione)
DETERMINAZIONE CONTEMPORANEA DI CROMO E MANGANESE
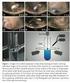 DETERMINAZIONE CONTEMPORANEA DI CROMO E MANGANESE Comparazione dei risultati ottenuti con il metodo dell additività delle assorbanze e il metodo di analisi per regressione lineare a diverse lunghezze d
DETERMINAZIONE CONTEMPORANEA DI CROMO E MANGANESE Comparazione dei risultati ottenuti con il metodo dell additività delle assorbanze e il metodo di analisi per regressione lineare a diverse lunghezze d
La legge. Il colorimetro. L esperienza. Realizzato da. August Beer ( ) Johann Heinrich Lambert ( )
 LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
ISTITUTO TECNICO AGRARIO Carlo Gallini
 Determinazione della densita di un solido PRINCIPIO La densità è ottenuta per calcolo dopo aver determinato massa e volume MATERIALI Cilindro di plastica da 100 ml REATTIVI Nessun reattivo 1. Determinazione
Determinazione della densita di un solido PRINCIPIO La densità è ottenuta per calcolo dopo aver determinato massa e volume MATERIALI Cilindro di plastica da 100 ml REATTIVI Nessun reattivo 1. Determinazione
RISOLUZIONE OIV-OENO
 RISOLUZIONE OIV-OENO 488-2013 REVISIONE DELLA MONOGRAFIA SULLA DETERMINAZIONE DELL ATTIVITÀ DELLA ß-GLUCANASI (ß-1,3; ß-1,6) NELLE PREPARAZIONI ENZIMATICHE (OIV-OENO 340-2010) L'ASSEMBLEA GENERALE, Visto
RISOLUZIONE OIV-OENO 488-2013 REVISIONE DELLA MONOGRAFIA SULLA DETERMINAZIONE DELL ATTIVITÀ DELLA ß-GLUCANASI (ß-1,3; ß-1,6) NELLE PREPARAZIONI ENZIMATICHE (OIV-OENO 340-2010) L'ASSEMBLEA GENERALE, Visto
Titolazione potenziometrica acido forte (HCl) base forte (NaOH)
 Titolazione potenziometrica acido forte (HCl) base forte (NaOH) Materiale occorrente: una pipetta a due tacche da 25 ml; una buretta Schellbach da 50 ml; un becher da 400 ml; un agitatore magnetico; un
Titolazione potenziometrica acido forte (HCl) base forte (NaOH) Materiale occorrente: una pipetta a due tacche da 25 ml; una buretta Schellbach da 50 ml; un becher da 400 ml; un agitatore magnetico; un
Intervallo di fiducia del coefficiente angolare e dell intercetta L intervallo di fiducia del coefficiente angolare (b 1 ) è dato da:
 Analisi chimica strumentale Intervallo di fiducia del coefficiente angolare e dell intercetta L intervallo di fiducia del coefficiente angolare (b 1 ) è dato da: (31.4) dove s y è la varianza dei valori
Analisi chimica strumentale Intervallo di fiducia del coefficiente angolare e dell intercetta L intervallo di fiducia del coefficiente angolare (b 1 ) è dato da: (31.4) dove s y è la varianza dei valori
Esperienza tipo B: Rimozione di inquinanti organici ed inorganici mediante assorbimento o adsorbimento
 Esperienza tipo B: Rimozione di inquinanti organici ed inorganici mediante assorbimento o adsorbimento 1. Preparare una soluzione di CuSO4 1.6x10-3 M pesando circa ma esatti 0.1 g di 2. Travasare 50 ml
Esperienza tipo B: Rimozione di inquinanti organici ed inorganici mediante assorbimento o adsorbimento 1. Preparare una soluzione di CuSO4 1.6x10-3 M pesando circa ma esatti 0.1 g di 2. Travasare 50 ml
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE
 SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE I Titolo dell esperienza N 4 DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO CON IL PRINCIPIO DI ARCHIMEDE
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE I Titolo dell esperienza N 4 DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO CON IL PRINCIPIO DI ARCHIMEDE
PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010
 PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010 1) PIANO CARTESIANO serve per indicare, identificare, chiamare... ogni PUNTO del piano (ente geometrico) con una coppia di valori numerici (detti COORDINATE).
PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010 1) PIANO CARTESIANO serve per indicare, identificare, chiamare... ogni PUNTO del piano (ente geometrico) con una coppia di valori numerici (detti COORDINATE).
Traduzione integrale ( non ufficiale) del metodo L35 LMBG Gennaio 1995 L (include l errata corrige del dicembre 2002)
 Traduzione integrale ( non ufficiale) del metodo L35 LMBG Gennaio 1995 L 00.00-6 (include l errata corrige del dicembre 2002) Ricerche su Alimenti ( L35LMBG ) Determinazione di Ammine Aromatiche Primarie
Traduzione integrale ( non ufficiale) del metodo L35 LMBG Gennaio 1995 L 00.00-6 (include l errata corrige del dicembre 2002) Ricerche su Alimenti ( L35LMBG ) Determinazione di Ammine Aromatiche Primarie
Materiale occorrente: una bilancia tecnica; due matracci da 250 ml; una pipetta tarata con propipetta.
 Materiale occorrente: una bilancia tecnica; due matracci da 250 ml; una pipetta tarata con propipetta. Reattivi: acido acetico; acetato di sodio; idrossido di ammonio e cloruro di ammonio; acqua distillata.
Materiale occorrente: una bilancia tecnica; due matracci da 250 ml; una pipetta tarata con propipetta. Reattivi: acido acetico; acetato di sodio; idrossido di ammonio e cloruro di ammonio; acqua distillata.
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Relazione giorno 4 Febbraio 2011
 Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Appendice cap. 29: applicazioni
 2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo
 UNIVERSITÀ DEGLI STUDI DI PAVIA CORSO DI LAUREA INTERFACOLTÀ IN BIOTECNOLOGIE Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo Relatore:
UNIVERSITÀ DEGLI STUDI DI PAVIA CORSO DI LAUREA INTERFACOLTÀ IN BIOTECNOLOGIE Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo Relatore:
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
XVII ZOLFO. Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE. Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI
 XVII ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI XVII - ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE 1. Principio Il campione viene
XVII ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI XVII - ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE 1. Principio Il campione viene
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE
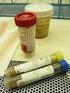 RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
RISOLUZIONE ENO 6/2007
 RISOLUZIONE ENO 6/2007 CODEX CINNAMIL ESTERASI L ASSEMBLEA GENERALE Visto l articolo 2, paragrafo 2 iv dell accordo del 3 aprile 2001 che istituisce la creazione dell Organizzazione Internazionale della
RISOLUZIONE ENO 6/2007 CODEX CINNAMIL ESTERASI L ASSEMBLEA GENERALE Visto l articolo 2, paragrafo 2 iv dell accordo del 3 aprile 2001 che istituisce la creazione dell Organizzazione Internazionale della
Progetto fumo. 2CT - ANNO SCOLASTICO 2015/16 Istituto tecnico industriale statale A.Volta
 Progetto fumo 2CT - ANNO SCOLASTICO 2015/16 Istituto tecnico industriale statale A.Volta 1 Processo di estrazione del monossido di carbonio Principi teorici Per comprendere questo procedimento, e i termini
Progetto fumo 2CT - ANNO SCOLASTICO 2015/16 Istituto tecnico industriale statale A.Volta 1 Processo di estrazione del monossido di carbonio Principi teorici Per comprendere questo procedimento, e i termini
cognome e nome turno banco data Indicare i CALCOLI per ESTESO Nei RIQUADRI TRATTEGGIATI riportare i dati con le CIFRE SIGNIFICATIVE appropriate
 PREPARAZIONE e STANDARDIZZAZIONE di una SOLUZIONE di ACIDO CLORIDRICO densità HCl (aq) conc. (g/ml) % peso prelievo HCl (aq) conc. (ml) mmoli HCl = volume matraccio (ml) titolo previsto HCl (aq) diluito
PREPARAZIONE e STANDARDIZZAZIONE di una SOLUZIONE di ACIDO CLORIDRICO densità HCl (aq) conc. (g/ml) % peso prelievo HCl (aq) conc. (ml) mmoli HCl = volume matraccio (ml) titolo previsto HCl (aq) diluito
GEOMETRIA ANALITICA 1 IL PIANO CARTESIANO
 GEOMETRI NLITIC 1 IL PINO CRTESINO Il piano cartesiano è costituito da due rette orientate e tra loro perpendicolari chiamate assi cartesiani, generalmente una orizzontale e l altra verticale, sulle quali
GEOMETRI NLITIC 1 IL PINO CRTESINO Il piano cartesiano è costituito da due rette orientate e tra loro perpendicolari chiamate assi cartesiani, generalmente una orizzontale e l altra verticale, sulle quali
Determinazione del contenuto di licopene
 Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
Se la base è 10, il risultato della potenza è una potenza di 10 con tanti zeri quante sono le unità dell esponente:
 Definizione di potenza Si definisce potenza ennesima di A, con n intero maggiore di 1, il prodotto di A per se stesso eseguito n volte A n =(AxAxAx A) n volte 2 5 = 2 2 2 2 2=32 Se la base è 10, il risultato
Definizione di potenza Si definisce potenza ennesima di A, con n intero maggiore di 1, il prodotto di A per se stesso eseguito n volte A n =(AxAxAx A) n volte 2 5 = 2 2 2 2 2=32 Se la base è 10, il risultato
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
Scale Logaritmiche. Matematica con Elementi di Statistica a.a. 2015/16
 Scale Logaritmiche Scala Logaritmica: sull asse prescelto (ad esempio, l asse x) si rappresenta il punto di ascissa = 0 0 nella direzione positiva si rappresentano, a distanze uguali fra di loro, i punti
Scale Logaritmiche Scala Logaritmica: sull asse prescelto (ad esempio, l asse x) si rappresenta il punto di ascissa = 0 0 nella direzione positiva si rappresentano, a distanze uguali fra di loro, i punti
DECIDE di completare il Codice enologico internazionale con la seguente monografia:
 RISOLUZIONE OIV/ENO 313/2009 CODEX EMICELLULASI L ASSEMBLEA GENERALE Visto l articolo 2, paragrafo 2 iv dell accordo del 3 aprile 2001 che istituisce la creazione dell Organizzazione internazionale della
RISOLUZIONE OIV/ENO 313/2009 CODEX EMICELLULASI L ASSEMBLEA GENERALE Visto l articolo 2, paragrafo 2 iv dell accordo del 3 aprile 2001 che istituisce la creazione dell Organizzazione internazionale della
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
RISOLUZIONE ENO 25/2004
 DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
Riconoscimento dei Glucidi (Glucosio):
 Riconoscimento dei Glucidi (Glucosio): Materiale occorrente: Soluzione di Glucosio Liquido di Feheling A (soluzione di solfato rameico pentaidrato (CuSO 4 5 H 2 O)) Liquido di Feheling B (soluzione di
Riconoscimento dei Glucidi (Glucosio): Materiale occorrente: Soluzione di Glucosio Liquido di Feheling A (soluzione di solfato rameico pentaidrato (CuSO 4 5 H 2 O)) Liquido di Feheling B (soluzione di
Una circonferenza e una parabola sono disegnate nel piano cartesiano. La circonferenza ha centro nel punto
 La parabola Esercizi Esercizio 368.395 Una circonferenza e una parabola sono disegnate nel piano cartesiano. La circonferenza ha centro nel punto 0 ;5 e raggio, e la parabola ha il suo vertice in 0 ;0.
La parabola Esercizi Esercizio 368.395 Una circonferenza e una parabola sono disegnate nel piano cartesiano. La circonferenza ha centro nel punto 0 ;5 e raggio, e la parabola ha il suo vertice in 0 ;0.
CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq) + H 2 O (l)
 2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
DETERMINAZIONE DELLA CAPACITÀ DI UN PREPARATO ENZIMATICO DI ROMPERE LE CATENE PECTICHE TRAMITE LA MISURAZIONE DELLA VISCOSITÀ
 RISOLUZIONE OIV/ENO 351/2009 DETERMINAZIONE DELLA CAPACITÀ DI UN PREPARATO ENZIMATICO DI ROMPERE LE CATENE PECTICHE TRAMITE LA MISURAZIONE DELLA VISCOSITÀ L'ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo
RISOLUZIONE OIV/ENO 351/2009 DETERMINAZIONE DELLA CAPACITÀ DI UN PREPARATO ENZIMATICO DI ROMPERE LE CATENE PECTICHE TRAMITE LA MISURAZIONE DELLA VISCOSITÀ L'ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO
 IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
CHIMICA GENERALE ED INORGANICA
 Corso di Laurea in Biotecnologie CHIMICA GENERALE ED INORGANICA Autori: Nivaldo J. Tro Chimica Un approccio molecolare EdiSES Per gli esercizi Autori : Rossi, Tesauro, Saviano, Randazzo Casa Editrice :
Corso di Laurea in Biotecnologie CHIMICA GENERALE ED INORGANICA Autori: Nivaldo J. Tro Chimica Un approccio molecolare EdiSES Per gli esercizi Autori : Rossi, Tesauro, Saviano, Randazzo Casa Editrice :
determinare le coordinate di P ricordando la relazione che permette di calcolare le coordinate del punto medio di un segmento si
 PROBLEMA Determinare il punto simmetrico di P( ;) rispetto alla retta x y =0 Soluzione Il simmetrico di P rispetto ad una retta r è il punto P che appartiene alla retta passante per P, perpendicolare ad
PROBLEMA Determinare il punto simmetrico di P( ;) rispetto alla retta x y =0 Soluzione Il simmetrico di P rispetto ad una retta r è il punto P che appartiene alla retta passante per P, perpendicolare ad
Esercitazione 1a: Determinazione fotometrica dell antimonio
 Esercitazione 1a: Determinazione fotometrica dell antimonio Principio del metodo L antimonio(iii), presente in soluzione come catione antimonile (SbO + ) complessato dal tartrato (C 4 H 4 O 6 2- ), reagisce
Esercitazione 1a: Determinazione fotometrica dell antimonio Principio del metodo L antimonio(iii), presente in soluzione come catione antimonile (SbO + ) complessato dal tartrato (C 4 H 4 O 6 2- ), reagisce
DOSAGGIO DELLA CARBOSSIMETILCELLULOSA (GOMMA DI CELLULOSA, CMC) NEI VINI BIANCHI
 RISOLUZIONE OIV/ENO 404/2010 DOSAGGIO DELLA CARBOSSIMETILCELLULOSA (GOMMA DI CELLULOSA, CMC) NEI VINI BIANCHI L ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce
RISOLUZIONE OIV/ENO 404/2010 DOSAGGIO DELLA CARBOSSIMETILCELLULOSA (GOMMA DI CELLULOSA, CMC) NEI VINI BIANCHI L ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce
Rappresentazione di Dati: Scala lineare Scala logaritmica. Grafici Lin Lin Grafici Lin Log Grafici Log Log
 Rappresentazione di Dati: Scala lineare Scala logaritmica Grafici Lin Lin Grafici Lin Log Grafici Log Log Grafici in scala lineare Grafici Lin Lin Nella rappresentazione di dati in un piano cartesiano
Rappresentazione di Dati: Scala lineare Scala logaritmica Grafici Lin Lin Grafici Lin Log Grafici Log Log Grafici in scala lineare Grafici Lin Lin Nella rappresentazione di dati in un piano cartesiano
2. Indicare l'affermazione che descrive più accuratamente il comportamento di un catalizzatore:
 1. "L'energia di attivazione, cioè l'energia necessaria a formare un composto ad alta energia potenziale, intermedio della reazione (il cosiddetto complesso attivato), è una grandezza caratteristica di
1. "L'energia di attivazione, cioè l'energia necessaria a formare un composto ad alta energia potenziale, intermedio della reazione (il cosiddetto complesso attivato), è una grandezza caratteristica di
Quaderno per il recupero del debito MATEMATICA ANNO SCOLASTICO 2016/2017 Prof.ssa Migliaccio Gabriella CLASSE III
 Quaderno per il recupero del debito MATEMATICA ANNO SCOLASTICO 016/017 Prof.ssa Migliaccio Gabriella CLASSE III Gli esercizi vanno svolti e consegnati, anche su un quaderno, il giorno dell esame per il
Quaderno per il recupero del debito MATEMATICA ANNO SCOLASTICO 016/017 Prof.ssa Migliaccio Gabriella CLASSE III Gli esercizi vanno svolti e consegnati, anche su un quaderno, il giorno dell esame per il
Dosaggio delle proteine
 Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
Statistica a lungo termine: calcolo dell onda di progetto
 Esercitazione Statistica a lungo termine: calcolo dell onda di progetto Sulla base delle misure ondametriche effettuate dalla boa di Ponza si calcoli, utilizzando la distribuzione di probabilità di Gumbel,
Esercitazione Statistica a lungo termine: calcolo dell onda di progetto Sulla base delle misure ondametriche effettuate dalla boa di Ponza si calcoli, utilizzando la distribuzione di probabilità di Gumbel,
FORMULARIO DI CHIMICA
 ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
Come allestire la vostra fermentazione
 Science in School Issue 24: Autumn 2012 1 Come allestire la vostra fermentazione Tradotto da Marianna Pizzetti Per svolgere tutte le attività proposte ogni gruppo di studenti avrà bisogno di circa 200
Science in School Issue 24: Autumn 2012 1 Come allestire la vostra fermentazione Tradotto da Marianna Pizzetti Per svolgere tutte le attività proposte ogni gruppo di studenti avrà bisogno di circa 200
4. In un becker ci sono 50 ml di NaOH 0,10 M. Quale soluzione, se aggiunta alla soluzione nel becker, non provoca variazioni del ph?
 1. Quale tra i seguenti acidi è il più debole? a. CH 3 COOH K a = 1,8*10 5 c. HF K a = 3,5*10 4 b. HCN K a = 4,9*10 10 d. HCNO K a = 1,6*10 4 2. Nell equilibrio: Fe 3+ ( aq ) + SCN ( aq ) Fe(SCN) 2+ (
1. Quale tra i seguenti acidi è il più debole? a. CH 3 COOH K a = 1,8*10 5 c. HF K a = 3,5*10 4 b. HCN K a = 4,9*10 10 d. HCNO K a = 1,6*10 4 2. Nell equilibrio: Fe 3+ ( aq ) + SCN ( aq ) Fe(SCN) 2+ (
IL PIANO CARTESIANO E LA RETTA
 IL PIANO CARTESIANO E LA RETTA ESERCIZI 1. Le coordinate di un punto su un piano 1 A Scrivi le coordinate dei punti indicati in figura. 1 B Scrivi le coordinate dei punti indicati in figura. Rappresenta
IL PIANO CARTESIANO E LA RETTA ESERCIZI 1. Le coordinate di un punto su un piano 1 A Scrivi le coordinate dei punti indicati in figura. 1 B Scrivi le coordinate dei punti indicati in figura. Rappresenta
Quadro riassuntivo di geometria analitica
 Quadro riassuntivo di geometria analitica IL PIANO CARTESIANO (detta ascissa o coordinata x) e y quella dall'asse x (detta ordinata o coordinata y). Le coordinate di un punto P sono: entrambe positive
Quadro riassuntivo di geometria analitica IL PIANO CARTESIANO (detta ascissa o coordinata x) e y quella dall'asse x (detta ordinata o coordinata y). Le coordinate di un punto P sono: entrambe positive
Sintesi dell acetanilide
 Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
KIT Le forme invisibili La cristallizzazione del lisozima
 KIT Le forme invisibili La cristallizzazione del lisozima MATERIALE NEL KIT - 3 provette da 1,5 ml contenenti la proteina del lisozima purificata (da conservare in freezer) - 6 piastre multiwell - una
KIT Le forme invisibili La cristallizzazione del lisozima MATERIALE NEL KIT - 3 provette da 1,5 ml contenenti la proteina del lisozima purificata (da conservare in freezer) - 6 piastre multiwell - una
Su proposta della Sottocommissione dei metodi d analisi e del gruppo d esperti "Specificazioni dei prodotti enologici",
 RISOLUZIONE ENO 8/2008 CODEX - CELLULASI L ASSEMBLEA GENERALE Visto l articolo 2, paragrafo 2 iv dell accordo del 3 aprile 2001 che istituisce la creazione dell Organizzazione Internazionale della vigna
RISOLUZIONE ENO 8/2008 CODEX - CELLULASI L ASSEMBLEA GENERALE Visto l articolo 2, paragrafo 2 iv dell accordo del 3 aprile 2001 che istituisce la creazione dell Organizzazione Internazionale della vigna
RELAZIONE FINALE DEL DOCENTE
 RELAZIONE FINALE DEL DOCENTE Materia: MATEMATICA Classe 3^AeT A. S. 2015/2016 Docente: Clara De Antoni In relazione alla programmazione curriculare sono stati conseguiti, in termini di livello medio, i
RELAZIONE FINALE DEL DOCENTE Materia: MATEMATICA Classe 3^AeT A. S. 2015/2016 Docente: Clara De Antoni In relazione alla programmazione curriculare sono stati conseguiti, in termini di livello medio, i
ESPONENZIALE ED EQUAZIONI DIFFERENZIALI
 ESPONENZIALE ED EQUAZIONI DIFFERENZIALI Prerequisiti: Obiettivi: Piano cartesiano funzione esponenziale e rappresentazione sul piano cartesiano concetto di limite definizione di derivata differenziale
ESPONENZIALE ED EQUAZIONI DIFFERENZIALI Prerequisiti: Obiettivi: Piano cartesiano funzione esponenziale e rappresentazione sul piano cartesiano concetto di limite definizione di derivata differenziale
Indici di maturazione per la maturità tecnologica dell uva
 Indici di maturazione per la maturità tecnologica dell uva Categories : Anno 2017, N. 264-15 ottobre 2017 di Gennaro Pisciotta Visto il carattere divulgativo e pratico dell articolo, che però non deve
Indici di maturazione per la maturità tecnologica dell uva Categories : Anno 2017, N. 264-15 ottobre 2017 di Gennaro Pisciotta Visto il carattere divulgativo e pratico dell articolo, che però non deve
LA RETTA. La retta è un insieme illimitato di punti che non ha inizio, né fine.
 LA RETTA La retta è un insieme illimitato di punti che non ha inizio, né fine. Proprietà: Per due punti del piano passa una ed una sola retta. Nel precedente modulo abbiamo visto che ad ogni punto del
LA RETTA La retta è un insieme illimitato di punti che non ha inizio, né fine. Proprietà: Per due punti del piano passa una ed una sola retta. Nel precedente modulo abbiamo visto che ad ogni punto del
Concorso Sperimenta anche tu Sperimentando 2017 RELAZIONE
 RELAZIONE Titolo Esperimento : L'ossigeno e i suoi strani effetti... Introduzione e Descrizione del fenomeno illustrato Nel cosmo, ma soprattutto nella nostra Terra c'è un enorme bisogno di ossigeno. Questo
RELAZIONE Titolo Esperimento : L'ossigeno e i suoi strani effetti... Introduzione e Descrizione del fenomeno illustrato Nel cosmo, ma soprattutto nella nostra Terra c'è un enorme bisogno di ossigeno. Questo
Trasformazioni Logaritmiche
 Trasformazioni Logaritmiche Una funzione y = f(x) può essere rappresentata in scala logaritmica ponendo Si noti che y = f(x) diventa ossia Quando mi conviene? X = log α x, Y = log α y. log α (x) = log
Trasformazioni Logaritmiche Una funzione y = f(x) può essere rappresentata in scala logaritmica ponendo Si noti che y = f(x) diventa ossia Quando mi conviene? X = log α x, Y = log α y. log α (x) = log
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: H 2 S (aq) + NO 3
 Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 (aq) + N 3 (aq) + + (aq) (s) + N (g) + 2 (l). Calcolare i grammi di (s) ed il volume di N (g) a 25 C ed 1
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 (aq) + N 3 (aq) + + (aq) (s) + N (g) + 2 (l). Calcolare i grammi di (s) ed il volume di N (g) a 25 C ed 1
VI - CORREZIONE DEI SUOLI A REAZIONE ANOMALA
 VI - CORREZIONE DEI SUOLI A REAZIONE ANOMALA Metodo VI.1 DETERMINAZIONE DEL FABBISOGNO IN CALCE Metodo VI.2 DETERMINAZIONE DEL FABBISOGNO IN GESSO VI - CORREZIONE DEI SUOLI A REAZIONE ANOMALA Metodo VI.1
VI - CORREZIONE DEI SUOLI A REAZIONE ANOMALA Metodo VI.1 DETERMINAZIONE DEL FABBISOGNO IN CALCE Metodo VI.2 DETERMINAZIONE DEL FABBISOGNO IN GESSO VI - CORREZIONE DEI SUOLI A REAZIONE ANOMALA Metodo VI.1
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN CORPO SOLIDO
 SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN CORPO SOLIDO I Titolo dell esperienza N 2 DETERMINAZIONE DEL VOLUME E DELLA DENSITÀ DI UN CORPO SOLIDO IRREGOLARE Autori Prof.sse Fabbri Fiamma,
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN CORPO SOLIDO I Titolo dell esperienza N 2 DETERMINAZIONE DEL VOLUME E DELLA DENSITÀ DI UN CORPO SOLIDO IRREGOLARE Autori Prof.sse Fabbri Fiamma,
Piano cartesiano e retta
 Piano cartesiano e retta Il punto, la retta e il piano sono concetti primitivi di cui non si da una definizione rigorosa, essi sono i tre enti geometrici fondamentali della geometria euclidea. Osservazione
Piano cartesiano e retta Il punto, la retta e il piano sono concetti primitivi di cui non si da una definizione rigorosa, essi sono i tre enti geometrici fondamentali della geometria euclidea. Osservazione
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
Misure di velocità con la guidovia a cuscino d aria (1)
 Misure di velocità con la guidovia a cuscino d aria (1) Obiettivo: Riprodurre un moto con velocità costante utilizzando la guidovia a cuscino d aria. Ricavare la tabella oraria e il grafico orario (grafico
Misure di velocità con la guidovia a cuscino d aria (1) Obiettivo: Riprodurre un moto con velocità costante utilizzando la guidovia a cuscino d aria. Ricavare la tabella oraria e il grafico orario (grafico
Spettroscopia molecolare: interazioni luce-materia
 Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
La reazione del ferro in una soluzione di solfato di rame
 La reazione del ferro in una soluzione di solfato di rame La presente reazione è in alternativa alla reazione di combustione del magnesio proposta nel percorso didattico di quarta media: La struttura della
La reazione del ferro in una soluzione di solfato di rame La presente reazione è in alternativa alla reazione di combustione del magnesio proposta nel percorso didattico di quarta media: La struttura della
PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA TRATTAMENTO DEL CAMPIONE
 PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA TRATTAMENTO DEL CAMPIONE ACIDO L-LATTICO su uova L acido L-lattico reagisce, per via enzimatica, con un derivato fenolico e induce la formazione di
PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA TRATTAMENTO DEL CAMPIONE ACIDO L-LATTICO su uova L acido L-lattico reagisce, per via enzimatica, con un derivato fenolico e induce la formazione di
Situazione patrimoniale: analisi per margini
 Laboratorio 2012 Scuola Duemila 1 Esercitazione svolta di laboratorio n. 1 Situazione patrimoniale: analisi per margini Roberto Bandinelli Riccardo Mazzoni Il caso Mauro Petri, responsabile del controllo
Laboratorio 2012 Scuola Duemila 1 Esercitazione svolta di laboratorio n. 1 Situazione patrimoniale: analisi per margini Roberto Bandinelli Riccardo Mazzoni Il caso Mauro Petri, responsabile del controllo
La media e la mediana sono indicatori di centralità, che indicano un centro dei dati.
 La media e la mediana sono indicatori di centralità, che indicano un centro dei dati. Un indicatore che sintetizza in un unico numero tutti i dati, nascondendo quindi la molteplicità dei dati. Per esempio,
La media e la mediana sono indicatori di centralità, che indicano un centro dei dati. Un indicatore che sintetizza in un unico numero tutti i dati, nascondendo quindi la molteplicità dei dati. Per esempio,
LABORATORIO DI FISICA 4 relazione: Saccarometria. De Mauro Giuseppe, Degradi Pablo, Restieri Andrea
 LABORATORIO DI FISICA 4 relazione: Saccarometria De Mauro Giuseppe, Degradi Pablo, Restieri Andrea Scopo dell'esperienza determinare il potere rotatorio specifico del saccarosio Materiale utilizzato e
LABORATORIO DI FISICA 4 relazione: Saccarometria De Mauro Giuseppe, Degradi Pablo, Restieri Andrea Scopo dell'esperienza determinare il potere rotatorio specifico del saccarosio Materiale utilizzato e
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione.
 Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Chimica Organica Relazione
 Titolo Sbarbada avide 4 /C I.S.I.I. Marconi -PC- Pagina 1 di 5 26/04/05 Chimica rganica Relazione Esperienza con gli zuccheri (glucosio, fruttosio e saccarosio) biettivo Prerequisiti Analizzare gli zuccheri
Titolo Sbarbada avide 4 /C I.S.I.I. Marconi -PC- Pagina 1 di 5 26/04/05 Chimica rganica Relazione Esperienza con gli zuccheri (glucosio, fruttosio e saccarosio) biettivo Prerequisiti Analizzare gli zuccheri
ALLwell Ingenasa Ingezim Gluten Quick
 ALLwell Ingenasa Ingezim Gluten Quick ELISA kit Cat. N. LFD030-Q TEST immunoenzimatico per la rivelazione quantitativa del glutine in campioni alimentari ed ambientali Manuale d uso Leggere attentamente
ALLwell Ingenasa Ingezim Gluten Quick ELISA kit Cat. N. LFD030-Q TEST immunoenzimatico per la rivelazione quantitativa del glutine in campioni alimentari ed ambientali Manuale d uso Leggere attentamente
 ACIDITA su burro, margarine, panna e grassi semilavorati PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA PREPARAZIONE DEL CAMPIONE CONDIZIONI DI REAZIONE (Edit) Gli acidi grassi del campione, in
ACIDITA su burro, margarine, panna e grassi semilavorati PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA PREPARAZIONE DEL CAMPIONE CONDIZIONI DI REAZIONE (Edit) Gli acidi grassi del campione, in
Sistemi di equazioni di secondo grado
 1 Sistemi di equazioni di secondo grado Risoluzione algebrica Riprendiamo alcune nozioni che abbiamo già trattato in seconda, parlando dei sistemi di equazioni di primo grado: Una soluzione di un'equazione
1 Sistemi di equazioni di secondo grado Risoluzione algebrica Riprendiamo alcune nozioni che abbiamo già trattato in seconda, parlando dei sistemi di equazioni di primo grado: Una soluzione di un'equazione
Equazione cartesiana della parabola con asse di simmetria parallelo all'asse delle ordinate Siano F(x F; y
 LEZIONI PARABOLA Definizione Si definisce parabola il luogo geometrico dei punti del piano equidistanti da un punto fisso,, detto fuoco, e da una retta fissa, d, detta direttrice. La definizione data mette
LEZIONI PARABOLA Definizione Si definisce parabola il luogo geometrico dei punti del piano equidistanti da un punto fisso,, detto fuoco, e da una retta fissa, d, detta direttrice. La definizione data mette
LICEO LINGUISTICO STATALE J. M. KEYNES
 LICEO LINGUISTICO STATALE J. M. KEYNES PROGRAMMA SVOLTO ANNO SCOLASTICO 206/207 DOCENTE DISCIPLINA CLASSE MARIA GRAZIA GOZZA MATEMATICA 3^ F LICEO LINGUISTICO Ripasso: Operazioni con le frazioni algebriche,
LICEO LINGUISTICO STATALE J. M. KEYNES PROGRAMMA SVOLTO ANNO SCOLASTICO 206/207 DOCENTE DISCIPLINA CLASSE MARIA GRAZIA GOZZA MATEMATICA 3^ F LICEO LINGUISTICO Ripasso: Operazioni con le frazioni algebriche,
Cuvette-test LCK 380 TOC Carbonio organico totale
 ATTENZIONE! La data dell edizione attuale è segnalata nella metodica opp. in lettura. Cuvette-test Principio Il carbonio totale () e il carbonio inorganico totale () vengono trasformati attraverso un'ossidazione
ATTENZIONE! La data dell edizione attuale è segnalata nella metodica opp. in lettura. Cuvette-test Principio Il carbonio totale () e il carbonio inorganico totale () vengono trasformati attraverso un'ossidazione
METODO DEI MINIMI QUADRATI
 Vogliamo determinare una funzione lineare che meglio approssima i nostri dati sperimentali e poter decidere sulla bontà di questa approssimazione. Sia f(x) = mx + q, la coppia di dati (x i, y i ) appartiene
Vogliamo determinare una funzione lineare che meglio approssima i nostri dati sperimentali e poter decidere sulla bontà di questa approssimazione. Sia f(x) = mx + q, la coppia di dati (x i, y i ) appartiene
LABORATORIO DI CHIMICA
 LABORATORIO DI CHIMICA Presentazione 3 a ESPERIENZA Titolazione Acido-Base ANALISI VOLUMETRICA Tipi di titolazioni Esistono diversi tipi di titolazione, classificati in funzione della reazione su cui si
LABORATORIO DI CHIMICA Presentazione 3 a ESPERIENZA Titolazione Acido-Base ANALISI VOLUMETRICA Tipi di titolazioni Esistono diversi tipi di titolazione, classificati in funzione della reazione su cui si
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Utilizzo di index() per determinare la colonna delle x
 Utilizzo di inde() per determinare la colonna delle In generale devo essere in grado di costruire un foglio dati con una colonna delle i cui estremi siano (a,b) bbiamo visto che le righe sono individuate
Utilizzo di inde() per determinare la colonna delle In generale devo essere in grado di costruire un foglio dati con una colonna delle i cui estremi siano (a,b) bbiamo visto che le righe sono individuate
SOLUZIONI derivate da: Acido debole/ sale (CH 3 COOH/CH 3 COONa) Base debole/ suo sale (NH 4 OH/NH 4 Cl)
 Soluzioni Tampone Si definiscono soluzioni tampone quelle soluzioni in grado di mantenere pressoché costante il proprio ph per aggiunta di una ragionevole quantità di acido o di base forte o per moderata
Soluzioni Tampone Si definiscono soluzioni tampone quelle soluzioni in grado di mantenere pressoché costante il proprio ph per aggiunta di una ragionevole quantità di acido o di base forte o per moderata
