EFFETTI DELLA NATURA DEI REAGENTI
|
|
|
- Rosa Pagani
- 6 anni fa
- Visualizzazioni
Transcript
1 La Chimica studia le trasformazioni della materia attraverso lo studio delle reazioni chimiche. Le reazioni più comuni, in generale, vengono suddivise in: reazioni di sintesi reazioni che portano alla formazione di un nuovo prodotto reazioni di precipitazione reazioni in cui si ha un cambiamento di fase attraverso la formazione di un solido insolubile reazioni acido base reazioni che prevedono il passaggio di protoni da un donatore ad un accettore reazioni di ossidazione reazione di una sostanza direttamente con l ossigeno reazioni di ossido-riduzione reazioni in cui si attua un trasferimento di elettroni da un reagente all altro 1
2 Tutte queste reazioni che possono avvenire in tempi estremamente diversi, che vanno dai pochi secondi (o frazioni di secondo) a milioni di anni come nel caso di alcune trasformazioni nucleari. La velocità con cui si realizza una reazione rappresenta la quantità di sostanza, normalmente espressa come grammomolecole o come concentrazione molare, che si trasforma nell unità di tempo. In genere una reazione avviene in più stadi, ognuno dei quali prende nome di atto elementare, la sequenza degli atti elementari che caratterizza una certa reazione prende nome di percorso di reazione 2
3 Il più lento degli atti elementari condiziona la velocità di tutto il processo. Se noi consideriamo una generica reazione: A prodotti di reazione La velocità di reazione potrebbe essere espressa come variazione della concentrazione della sostanza A nell intervallo di tempo considerato: V = c 2 c 1 = c t 2 t 1 t espressione in cui : c 2 = concentrazione di A al tempo t 2 c 1 = concentrazione di A al tempo t 1 t 2 = fine del periodo di osservazione t 1 = inizio del periodo di osservazione V rappresenta la velocità media nel periodo di osservazione 3
4 Se invece consideriamo un intervallo t molto piccolo, tendente a zero, potremo dire che il valore di v calcolato in queste condizioni rappresenterà la velocità istantanea della reazione stessa ad un certo tempo t. Considerando la estrema variabilità che si osserva nello studio della cinetica delle reazioni, dobbiamo dire che l intervallo di tempo t molto piccolo può assumere valore diverso nelle diverse reazioni, proprio in funzione dei differenti comportamenti In alcuni casi potrà essere il secondo, in altri casi dovrà essere l ora, in altri casi ancora il giorno o l anno La velocità di una reazione chimica è influenzata da diversi fattori, quali la concentrazione e la natura dei reagenti e dei prodotti, il solvente, la temperatura, la presenza di catalizzatori, la luce o altre radiazioni, ecc. 4
5 EFFETTI DELLA NATURA DEI REAGENTI In condizioni sperimentali equivalenti, la velocità di reazione è largamente influenzata dal tipo di contatto che si realizza tra i reagenti. In linea generale possiamo dire che una reazione in fase omogenea (es. due liquidi) è più rapida di una reazione in fase eterogenea (es. un liquido ed un solido) In questo caso la velocità è direttamente influenzata dalla superficie di contatto, vale a dire che un solido finemente suddiviso reagisce molto più rapidamente della stessa sostanza in un blocco unico. 5
6 EFFETTI DELLA CONCENTRAZIONE DEI REAGENTI Se consideriamo una generica reazione in fase omogenea: A + B prodotti è sperimentalmente dimostrabile, che la velocità aumenta all aumento della concentrazione dei reagenti. Questo fenomeno non sorprende poiché è ovvio che per far avvenire la reazione, le molecole di A e di B dovranno scontrarsi e la probabilità che questi urti avvengano è statisticamente proporzionale al numero di molecole in un certo spazio, ossia alla concentrazione dei reagenti. 6
7 L equazione che descrive la velocità in funzione della concentrazione dei reagenti è: nella quale: V = k [ A ] a [ B ] b k = costante di velocità (o velocità specifica di reazione) [ A ] = concentrazione molare del reagente A [ B ] = concentrazione molare del reagente B a e b = sono dei coefficienti sperimentali che rappresentano l ordine della reazione 7
8 REAZIONI DI PRIMO ORDINE Se consideriamo una reazione del tipo: A B + C la stechiometria della reazione ci dice che per la formazione di una molecola di B o di C, si consuma una molecola di A. La velocità della reazione, quindi, può essere definita dalla velocità di scomparsa di A o dalla velocità di formazione di B o di C, per cui potremo avere: V = - d[ A ] d[ B ] d[ C ] = = dt dt dt 8
9 il segno meno precede la concentrazione di A, poiché questa diminuisce nel tempo. Questo tipo di reazione, viene indicata come reazione di primo ordine poiché la velocità è proporzionale alla concentrazione di un solo reagente, elevato alla prima potenza. L equazione che descrive la velocità in funzione della concentrazione diviene: V = d[ A ] = k 1 [ A ] dt 9
10 REAZIONI DI SECONDO ORDINE Se consideriamo invece una reazione del tipo: A + B C oppure del tipo 2A C l equazione di velocità diviene: nel primo caso: V = k 2 [ A ] [ B ] nel secondo caso: V = k 2 [ A ] 2 in ambedue i casi si tratta di equazioni di velocità di reazioni di secondo ordine, in quanto la velocità è proporzionale al prodotto della concentrazione di due reagenti ognuno elevato alla prima potenza (primo caso) o al quadrato della concentrazione di un reagente (secondo caso). 10
11 REAZIONI DI ORDINE ZERO Questo tipo è rappresentato dalle reazioni che hanno velocità costante al variare della concentrazione dei reagenti, la equazione di velocità diviene: V = k 3 [ A ] 0 [ B ] 0 da cui V = k cinetica di questo tipo è possibile nel caso di una reazione che avvenga alla superficie di un solido, oppure nel caso di una reazione catalizzata o di una reazione enzimatica che sia giunta alla velocità di saturazione. 11
12 Si parla, in questo caso di reazioni di ordine zero, ossia di reazioni che non dipendono dalla concentrazione del reagente ma da un fattore esterno alla reazione stessa (superficie di contatto, catalizzatore, enzima,.) perché come appare dalla equazione prima riportata, il valore [ A ] 0 [ B ] 0 si comporta come una costante, da cui anche la velocità rimane costante, ma risente solo di fattori esterni 12
13 a) V= K b) V= K [A] b) V= K [A] [B] Vo Vo Vo [A] [A] [A] Andamento della velocità di reazione nei tre casi descritti: A = reazioni di ordine zero B = reazioni di primo ordine C = reazioni di secondo ordine 13
14 REAZIONI DI PSEUDO-PRIMO ORDINE In alcuni casi si parla di reazioni di pseudo-primo ordine, ossia di reazioni di secondo ordine ma che, apparentemente, si comportano come le reazioni di primo ordine Se prendiamo in considerazione una reazione del tipo: A + B C è chiaro che ci dovremmo aspettare un comportamento come quello descritto nelle pagine precedenti 14
15 Se ammettiamo che uno dei due reagenti (es. A) abbia una concentrazione molto maggiore di B, (intendendo 100, 500, 1000 volte maggiore) la velocità di una reazione di questo tipo sarà condizionata dalla presenza e dalla concentrazione di B, comportandosi A come una costante. In altre parole, se ammettiamo di avere 1000 molecole di A e una sola di B, la reazione potrà proseguire e formare C solo fino a che B è presente. Nel momento in cui si ha esaurimento di B la reazione cessa. Esempio classico di questo tipo sono le reazioni di idrolisi che avvengono in vivo, ossia quelle reazioni in cui uno dei reagenti è l acqua, che ha sempre concentrazioni molto maggiori di qualsiasi altro substrato. 15
16 EFFETTO DELLA TEMPERATURA L aumento di temperatura determina sempre un aumento della velocità di reazione, salvo rare eccezioni. In media un aumento di 10 gradi di temperatura determina il raddoppio della velocità di reazione. Questo effetto viene spiegato dalla teoria delle collisioni, secondo la quale per far avvenire una reazione è necessario che le particelle dei reagenti (atomi, molecole, ioni) si urtino tra di loro. La probabilità che una molecola di A urti una molecola di B dipende sia dal numero delle particelle presenti nell ambiente di reazione, sia dalla velocità media con cui si muovono, velocità media che a sua volta dipende dalla temperatura. 16
17 E altresì vero che non tutti gli urti che si realizzano tra le molecole dei reagenti sono efficaci, solamente una frazione di quelli che si realizzano possono provocare la rottura e/o la formazione di legami Questo significa che le particelle dei reagenti (siano atomi, molecole o altro) devono possedere una energia che sia pari o superiore ad un valore soglia che rappresenta la energia di attivazione Ea, che : dipende dal tipo di reazione considerata è una caratteristica della reazione stessa può assumere valori estremamente diversi a seconda della trasformazione. 17
18 Somministrando calore aumenta la temperatura del sistema di reazione aumenta la energia cinetica media delle singole particelle aumenta il numero di particelle che possiedono una energia uguale o superiore alla energia di attivazione, così che proporzionalmente aumenta il numero di urti efficaci Questo è facilmente dimostrabile, infatti se si riportano su grafico: in ascissa la energia cinetica media delle molecole in ordinata la frazione delle molecole che possiede E c E a a due temperature diverse, T e T+10, avremo: 18
19 La regione tratteggiata ci indica che per un aumento della T di 10 C, il numero di molecole che superano il valore soglia di E a è circa raddoppiato e questo spiega la constatazione empirica che per un generico aumento di 10 C di Temperatura, la velocità raddoppia 19
20 Arrhenius nel 1889 dette una spiegazione razionale di questo fenomeno tramite l equazione: k = A e -Ea/RT in cui K - rappresenta la costante di velocità di una reazione, A - è un fattore sperimentale, detto fattore di frequenza, proporzionale al numero degli urti e costante per un certo processo e - è la base dei logaritmi naturali R - è la costante universale dei gas T - è la temperatura assoluta E a - è la energia di attivazione In questa espressione aumentando il valore di T, diminuisce il valore dell esponente negativo della potenza e, di conseguenza, aumenta il valore di k 20
21 Ma K appare nelle equazioni di velocità V = k 1 [ A ] V = k 2 [ A ] [ B ] V = k 2 [ A ] 2 V = k reazione di primo ordine reazioni di secondo ordine reazione di ordine zero per cui aumentando il valore di K aumenta il valore di v 21
22 L equazione di Arrhenius: k = A e -Ea/RT viene usualmente modificata tenendo conto che nelle reazioni entra in gioco anche un fattore riguardante la geometria molecolare Infatti non tutte le molecole che possiedono energia cinetica superiore alla energia di attivazione, urtandosi, sono in grado di reagire, poiché per reagire devono incontrarsi secondo orientamenti favorevoli alla reazione stessa 22
23 L equazione di Arrhenius, pertanto, viene così modificata: k = P Z e -Ea/RT Z - rappresenta il numero di urti che avvengono nell unità di tempo e dipende dalla radice quadrata della temperatura P - è un coefficiente probabilistico che può assumere valori anche molto piccoli, fino a 10-8 per reazioni che coinvolgono molecole molto complesse 23
24 L equazione di Arrhenius permette anche di calcolare il valore di E a per una certa reazione, infatti k = A e -Ea/RT Può essere scritta in forma logartimica: E lnk = lna a RT che rappresenta l equazione di una retta, per cui mettendo in grafico i valori di lnk (ordinate) in funzione di 1/T si ottiene una retta con pendenza pari a -Ea/R e con intercetta sull asse delle ordinate pari a lna 24
25 lna Da cui è facile risalire al valore di Ea 25
26 Teoria del complesso attivato La teoria delle collisioni, in realtà è parte di un quadro di principio più vasto che va sotto il nome di Teoria del Complesso Attivato Questa teoria prevede che nel momento in cui due molecole si incontrano e interagiscono, avvenga tutta una serie di modificazioni, in particolare si modificano le lunghezze dei legami fino ad arrivare ad una configurazione che non è più quella dei reagenti, ma che rappresenta uno stato intermedio tra reagenti e prodotti, il Complesso Attivato o Stato di Transizione 26
27 L andamento di questo fenomeno è rappresentato dall andamento dell energia potenziale che passa dallo stato di - E 1 (reagenti) a - E 3 (stato attivato che corrisponde alla Energia di attivazione Ea) - E 2 (prodotti di reazione) E ovvio che se non si forma il complesso attivato la reazione non può procedere 27
28 Il complesso attivato si trova ad un livello energetico più elevato dei reagenti e dei prodotti e rappresenta una struttura altamente instabile, a causa della particolare distribuzione e geometria dei legami Questo fa sì che il complesso attivato esista per tempi estremamente brevi (in qualche caso si parla di nanosecondi) Questa esistenza così breve è la causa della impossibilità sperimentale di isolarlo e studiarlo 28
29 Meccanismi di reazione Abbiamo già detto che ogni reazione è caratterizzata da una serie di atti elementari che caratterizzano il percorso di reazione Uno dei parametri che condizionano il percorso di reazione è la molecolarità della reazione stessa, ossia il numero delle specie chimiche che intervengono nella formazione del complesso attivato In qualche caso la molecolarità corrisponde alla sommatoria dei coefficienti di reazione (ordine di reazione) ed allora si parla di reazione elementare 29
30 Questo significa che la reazione avviene attraverso la formazione di un unico complesso attivato Negli altri casi è possibile avere reazioni bimolecolari e trimolecolari, mentre una molecolarità superiore, teoricamente possibile, è altamente improbabile Questo perché le reazioni che coinvolgono più specie chimiche avvengono in più stadi, ognuno dei quali da origine ad uno specifico intermedio di reazione, con una sua specifica E a ed una specifica K c D altro canto se per far avvenire una reazione è necessario l urto di 2 specie chimiche, la probabilità di incontro sarà molto maggiore rispetto a quando entrano in gioco 3 specie chimiche e, ancora di più, nell ipotesi che siano 4 le specie necessarie. 30
31 Reazioni a catena radicaliche In molte reazioni a catena, l intermedio che si forma è un radicale, ossia una specie chimica transitoria nella quale si è determinata una carenza o un eccesso di elettroni, perturbando in questo modo il naturale assetto degli orbitali molecolari Questi disordini elettronici spingono naturalmente tali composti a reagire con altre molecole, sottraendo o cedendo elettroni che creano altri radicali che a loro volta propagano la reazione stessa 31
32 Un esempio di queste reazioni è quello che porta alla formazione dell HBr a partire dai suoi componenti molecolari. In realtà la reazione procede secondo questo schema: Br 2 2Br Br + H 2 HBr + H H + Br 2 HBr + Br E così via, teoricamente all infinito, in realtà dato l elevato numero di radicali in gioco si realizzano anche le reazioni: 2Br Br 2 Reazioni di arresto che formano 2H H specie non radicaliche 2 32
33 CATALISI I catalizzatori sono sostanze che aumentano la velocità di una reazione chimica senza venire a loro volta modificati per cui si ritrovano inalterati al termine della reazione stessa. Molti dubbi esistono ancora sul meccanismo con cui agiscono. Ma una delle teorie più accreditate propone che il catalizzatore si leghi in maniera labile ad uno o a tutti i reagenti, formando dei complessi estremamente instabili, ma che avrebbero il pregio di facilitare l orientamento delle molecole, la loro disposizione e, di conseguenza, il realizzarsi di urti efficaci. 33
34 In questo modo la reazione avverrebbe attraverso una serie di atti elementari diversi da quelli che si realizzano nella reazione non catalizzata, ossia la trasformazione chimica si realizzerebbe con un percorso di reazione diverso ma che ha una energia di attivazione minore, più facilmente raggiunta e superata dai reagenti. Percorso di una ipotetica reazione in assenza ed in presenza di un catalizzatore 34
35 L esempio classico è quello della reazione di scissione dell acqua ossigenata H 2 O 2 H 2 O + O questa reazione avviene spontaneamente ma può essere catalizzata. La energia di attivazione risulta essere: reazione non catalizzata: Ea = 18 Kcal/mole reazione in presenza di platino colloidale: Ea = 12 Kcal/mole reazione in presenza di catalasi: Ea = 2 Kcal/mole 35
36 Esistono anche i cosiddetti catalizzatori negativi o veleni che anziché velocizzare una reazione ne diminuiscono la velocità L attività di un catalizzatore (o attività catalitica) corrisponde alla velocità con cui la reazione chimica raggiunge l'equilibrio in presenza del catalizzatore stesso Viene espressa nel Sistema Internazionale in katal 1 katal rappresenta la quantità di catalizzatore che trasforma 1 mole di reagenti in 1 secondo L'attività catalitica può anche essere espressa in "unità" (in inglese "units", simbolo U), ed è calcolata in micromoli trasformate al minuto 36
37 Esistono diverse modalità di catalisi, per cui si parla di: CATALISI OMOGENEA quando i reagenti si trovano nella stessa fase del catalizzatore. il catalizzatore è disciolto nell ambiente di reazione, per cui la separazione del catalizzatore dai prodotti è più difficoltosa, e costosa, rispetto al caso della catalisi eterogenea Inoltre nel caso della catalisi omogenea il sito catalitico è completamente esposto all'azione dei reagenti, per cui si ha un attività catalitica maggiore ma una minore selettività 37
38 CATALISI ETEROGENEA quando il catalizzatore e il reagente esistono in due fasi differenti. Questo processo avviene in prossimità dell' interfase reagente-catalizzatore, che può essere di vari tipi, ad es. fluido-solido o liquido-liquido (es. 2 liquidi immiscibili) I sistemi catalitici eterogenei possono essere costituiti anche da un catalizzatore (propriamente detto) fissato ad un supporto solido. Il supporto ha la funzione di mantenere allo stato solido il catalizzatore che altrimenti si disperderebbe nel fluido, nel qual caso sarebbe necessario un processo più complesso per il recupero del catalizzatore stesso. 38
39 FOTOCATALISI si realizza tramite un catalizzatore che esplica la sua azione quando irradiato con luce di opportuna lunghezza d'onda I fotocatalizzatori classici sono rappresentati da composti metallici quali TiO 2,il più attivo e più utilizzato, ZnO, CeO 2, ZrO 2, SnO 2, CdS, ZnS ecc. Il fotocatalizzatore è un semiconduttore che assorbe un fotone di energia superiore al gap tra banda di valenza e banda di conduzione, modifica la struttura dei suoi orbitali molecolari medianti i cosiddetti fotoelettroni, che passano della banda di valenza a quella di conduzione Questi trasportatori di carica hanno vita breve, ritornano alla configurazione originaria o generano un flusso di corrente superficiale 39
40 AUTOCATALISI è il processo catalitico in cui il catalizzatore è costituito da uno degli stessi prodotti o intermedi di reazione in grado di agire sullo stadio lento della reazione chimica. Comuni esempi di autocatalisi sono rappresentati da: la peste dello stagno (una modificazione allotropica), la deplezione dello strato di ozono, il legame con l ossigeno da parte dell'emoglobina la reazione tra permanganato e acido ossalico (Mn 2+ è l'autocatalizzatore). 40
41 CATALISI ROTAZIONALE è il meccanismo catalitico usato nella sintesi di ATP ad opera della ATP sintasi, come proposto da Boyer nel Futai nel 1999 dimostrò sperimentalmente che la proteina compie una rotazione del cilindro mediante scatti di 120. L'energia liberata dal rientro dei protoni causa la rotazione delle subunità dell'atp sintasi. Tale ipotesi segue l'ipotesi chemiosmotica che Peter D. Mitchell propose nel 1961 secondo la quale era proprio l'energia liberata dal rientro degli ioni H + nel mitocondrio che determina la sintesi di ATP e utilizza l'ipotesi dell'accoppiamento conformazionale. 41
42 Il fenomeno della catalisi è ampiamente utilizzato in vivo, praticamente tutte le reazioni che avvengono nel nostro organismo sono reazioni catalizzate da particolari tipi di molecole, gli enzimi, che costituiscono dei catalizzatori biologici specifici, di natura proteica, prodotti dalle stesse cellule che li utilizzano. Gli enzimi ed il loro meccanismo di azione saranno trattati successivamente. 42
Cinetica Chimica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Cinetica Chimica Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Cinetica Chimica Termodinamica la reaction avrà luogo? Cinetica quanto sarà veloce la reazione?
Cinetica Chimica Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Cinetica Chimica Termodinamica la reaction avrà luogo? Cinetica quanto sarà veloce la reazione?
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile
 Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile Obiettivo dell'esperienza è la determinazione di parametri cinetici per la reazione di decomposizione
Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile Obiettivo dell'esperienza è la determinazione di parametri cinetici per la reazione di decomposizione
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
4) 8 g di idrogeno reagiscono esattamente con 64 g di ossigeno secondo la seguente reazione:
 Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
INDICAZIONI PER LA RICERCA DEGLI ASINTOTI VERTICALI
 2.13 ASINTOTI 44 Un "asintoto", per una funzione y = f( ), è una retta alla quale il grafico della funzione "si avvicina indefinitamente", "si avvicina di tanto quanto noi vogliamo", nel senso precisato
2.13 ASINTOTI 44 Un "asintoto", per una funzione y = f( ), è una retta alla quale il grafico della funzione "si avvicina indefinitamente", "si avvicina di tanto quanto noi vogliamo", nel senso precisato
CHIMICA ORGANICA. Gli alchini
 1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
Prontuario degli argomenti di Algebra
 Prontuario degli argomenti di Algebra NUMERI RELATIVI Un numero relativo è un numero preceduto da un segno + o - indicante la posizione rispetto ad un punto di riferimento a cui si associa il valore 0.
Prontuario degli argomenti di Algebra NUMERI RELATIVI Un numero relativo è un numero preceduto da un segno + o - indicante la posizione rispetto ad un punto di riferimento a cui si associa il valore 0.
Esercitazioni di statistica
 Esercitazioni di statistica Misure di associazione: Indipendenza assoluta e in media Stefania Spina Universitá di Napoli Federico II stefania.spina@unina.it 22 ottobre 2014 Stefania Spina Esercitazioni
Esercitazioni di statistica Misure di associazione: Indipendenza assoluta e in media Stefania Spina Universitá di Napoli Federico II stefania.spina@unina.it 22 ottobre 2014 Stefania Spina Esercitazioni
SISTEMI LINEARI MATRICI E SISTEMI 1
 MATRICI E SISTEMI SISTEMI LINEARI Sistemi lineari e forma matriciale (definizioni e risoluzione). Teorema di Rouché-Capelli. Sistemi lineari parametrici. Esercizio Risolvere il sistema omogeneo la cui
MATRICI E SISTEMI SISTEMI LINEARI Sistemi lineari e forma matriciale (definizioni e risoluzione). Teorema di Rouché-Capelli. Sistemi lineari parametrici. Esercizio Risolvere il sistema omogeneo la cui
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
La pompa sodio-potassio
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La pompa sodio-potassio 14/3/2006 Efficienza del cuore Dipende dall ordinata sequenza di eccitazione e di contrazione che procede
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La pompa sodio-potassio 14/3/2006 Efficienza del cuore Dipende dall ordinata sequenza di eccitazione e di contrazione che procede
Introduzione alle macchine a stati (non definitivo)
 Introduzione alle macchine a stati (non definitivo) - Introduzione Il modo migliore per affrontare un problema di automazione industriale (anche non particolarmente complesso) consiste nel dividerlo in
Introduzione alle macchine a stati (non definitivo) - Introduzione Il modo migliore per affrontare un problema di automazione industriale (anche non particolarmente complesso) consiste nel dividerlo in
SCUOLA PRIMARIA DI MAGGIATE Classe terza
 SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
Metodi per la risoluzione di sistemi lineari
 Metodi per la risoluzione di sistemi lineari Sistemi di equazioni lineari. Rango di matrici Come è noto (vedi [] sez.0.8), ad ogni matrice quadrata A è associato un numero reale det(a) detto determinante
Metodi per la risoluzione di sistemi lineari Sistemi di equazioni lineari. Rango di matrici Come è noto (vedi [] sez.0.8), ad ogni matrice quadrata A è associato un numero reale det(a) detto determinante
DISSOCIAZIONE DEGLI OSSIDI METALLICI NEI FORNI A VUOTO. Elio Gianotti - Trattamenti termici Ferioli & Gianotti S.p.A.
 DISSOCIAZIONE DEGLI OSSIDI METALLICI NEI FORNI A VUOTO Elio Gianotti - Trattamenti termici Ferioli & Gianotti S.p.A. Le basse pressioni unitamente alle temperature elevate che si possono raggiungere nei
DISSOCIAZIONE DEGLI OSSIDI METALLICI NEI FORNI A VUOTO Elio Gianotti - Trattamenti termici Ferioli & Gianotti S.p.A. Le basse pressioni unitamente alle temperature elevate che si possono raggiungere nei
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
La Terra nello spazio
 La Terra nello spazio L'Universo è sempre esistito? L'ipotesi più accreditata fino ad ora è quella del Big Bang. Circa 20 miliardi di anni fa, una massa di piccolo volume, in cui vi era racchiusa tutta
La Terra nello spazio L'Universo è sempre esistito? L'ipotesi più accreditata fino ad ora è quella del Big Bang. Circa 20 miliardi di anni fa, una massa di piccolo volume, in cui vi era racchiusa tutta
EQUAZIONI CON VALORE ASSOLUTO DISEQUAZIONI CON VALORE ASSOLUTO
 EQUAZIONI CON VALORE AOLUTO DIEQUAZIONI CON VALORE AOLUTO Prima di tutto: che cosa è il valore assoluto di un numero? Il valore assoluto è quella legge che ad un numero (positivo o negativo) associa sempre
EQUAZIONI CON VALORE AOLUTO DIEQUAZIONI CON VALORE AOLUTO Prima di tutto: che cosa è il valore assoluto di un numero? Il valore assoluto è quella legge che ad un numero (positivo o negativo) associa sempre
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
BILANCIO DEI VINCOLI ED ANALISI CINEMATICA
 BILANCIO DEI VINCOLI ED ANALISI CINEMATICA ESERCIZIO 1 Data la struttura piana rappresentata in Figura 1, sono richieste: - la classificazione della struttura in base alla condizione di vincolo; - la classificazione
BILANCIO DEI VINCOLI ED ANALISI CINEMATICA ESERCIZIO 1 Data la struttura piana rappresentata in Figura 1, sono richieste: - la classificazione della struttura in base alla condizione di vincolo; - la classificazione
Tracce di energia. viaggio dentro l atomo
 Tracce di energia viaggio dentro l atomo Di cosa è fatta la torre Eiffel? di 10.000 tonnellate di ferro ovvero 10.000.000.000 di grammi di ferro miliardi Ogni grammo di ferro, a sua volta, è composto da
Tracce di energia viaggio dentro l atomo Di cosa è fatta la torre Eiffel? di 10.000 tonnellate di ferro ovvero 10.000.000.000 di grammi di ferro miliardi Ogni grammo di ferro, a sua volta, è composto da
La reazione da bilanciare è quindi: Cu + HNO 3 CuNO 3 + NO. Le due semireazioni da bilanciare saranno: HNO 3 NO (1) Cu CuNO 3 (2)
 Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
Derivate delle funzioni di una variabile.
 Derivate delle funzioni di una variabile. Il concetto di derivata di una funzione di una variabile è uno dei più fecondi della matematica ed è quello su cui si basa il calcolo differenziale. I problemi
Derivate delle funzioni di una variabile. Il concetto di derivata di una funzione di una variabile è uno dei più fecondi della matematica ed è quello su cui si basa il calcolo differenziale. I problemi
Lezione 4. Sommario. L artimetica binaria: I numeri relativi e frazionari. I numeri relativi I numeri frazionari
 Lezione 4 L artimetica binaria: I numeri relativi e frazionari Sommario I numeri relativi I numeri frazionari I numeri in virgola fissa I numeri in virgola mobile 1 Cosa sono inumeri relativi? I numeri
Lezione 4 L artimetica binaria: I numeri relativi e frazionari Sommario I numeri relativi I numeri frazionari I numeri in virgola fissa I numeri in virgola mobile 1 Cosa sono inumeri relativi? I numeri
Radiazione solare. Energia elettrica
 Un modulo fotovoltaico è un dispositivo in grado di convertire energia solare direttamente in energia elettrica mediante effetto fotovoltaico ed è impiegato come generatore di corrente quasi puro in un
Un modulo fotovoltaico è un dispositivo in grado di convertire energia solare direttamente in energia elettrica mediante effetto fotovoltaico ed è impiegato come generatore di corrente quasi puro in un
FISICA Corso di laurea in Informatica e Informatica applicata
 FISICA Corso di laurea in Informatica e Informatica applicata I semestre AA 2004-2005 G. Carapella Generalita Programma di massima Testi di riferimento Halliday Resnick Walker CEA Resnick Halliday Krane
FISICA Corso di laurea in Informatica e Informatica applicata I semestre AA 2004-2005 G. Carapella Generalita Programma di massima Testi di riferimento Halliday Resnick Walker CEA Resnick Halliday Krane
EQUAZIONI DI PRIMO GRADO
 Cognome... Nome... Equazioni di primo grado EQUAZIONI DI PRIMO GRADO Un'equazione di primo grado e un'uguaglianza tra due espressioni algebriche di primo grado, vera solo per alcuni valori che si attribuiscono
Cognome... Nome... Equazioni di primo grado EQUAZIONI DI PRIMO GRADO Un'equazione di primo grado e un'uguaglianza tra due espressioni algebriche di primo grado, vera solo per alcuni valori che si attribuiscono
Esercizi e problemi tratti dal libro La chimica di Rippa Cap. 14 L'equilibrio chimico
 Esercizi e problemi tratti dal libro La chimica di Rippa Cap. 14 L'equilibrio chimico 43. A 723 K in un reattore dal volume di 5,000 L sono presenti all'equilibrio 3,356 mol di azoto, 4,070 mol di idrogeno
Esercizi e problemi tratti dal libro La chimica di Rippa Cap. 14 L'equilibrio chimico 43. A 723 K in un reattore dal volume di 5,000 L sono presenti all'equilibrio 3,356 mol di azoto, 4,070 mol di idrogeno
7 Disegni sperimentali ad un solo fattore. Giulio Vidotto Raffaele Cioffi
 7 Disegni sperimentali ad un solo fattore Giulio Vidotto Raffaele Cioffi Indice: 7.1 Veri esperimenti 7.2 Fattori livelli condizioni e trattamenti 7.3 Alcuni disegni sperimentali da evitare 7.4 Elementi
7 Disegni sperimentali ad un solo fattore Giulio Vidotto Raffaele Cioffi Indice: 7.1 Veri esperimenti 7.2 Fattori livelli condizioni e trattamenti 7.3 Alcuni disegni sperimentali da evitare 7.4 Elementi
Esercizi sulla conversione tra unità di misura
 Esercizi sulla conversione tra unità di misura Autore: Enrico Campanelli Prima stesura: Settembre 2013 Ultima revisione: Settembre 2013 Per segnalare errori o per osservazioni e suggerimenti di qualsiasi
Esercizi sulla conversione tra unità di misura Autore: Enrico Campanelli Prima stesura: Settembre 2013 Ultima revisione: Settembre 2013 Per segnalare errori o per osservazioni e suggerimenti di qualsiasi
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Insegnare relatività. nel XXI secolo
 Insegnare relatività nel XXI secolo E s p a n s i o n e d e l l ' U n i v e r s o e l e g g e d i H u b b l e La legge di Hubble Studiando distanze e moto delle galassie si trova che quelle più vicine
Insegnare relatività nel XXI secolo E s p a n s i o n e d e l l ' U n i v e r s o e l e g g e d i H u b b l e La legge di Hubble Studiando distanze e moto delle galassie si trova che quelle più vicine
SOTTOSPAZI E OPERAZIONI IN SPAZI DIVERSI DA R n
 SPAZI E SOTTOSPAZI 1 SOTTOSPAZI E OPERAZIONI IN SPAZI DIVERSI DA R n Spazi di matrici. Spazi di polinomi. Generatori, dipendenza e indipendenza lineare, basi e dimensione. Intersezione e somma di sottospazi,
SPAZI E SOTTOSPAZI 1 SOTTOSPAZI E OPERAZIONI IN SPAZI DIVERSI DA R n Spazi di matrici. Spazi di polinomi. Generatori, dipendenza e indipendenza lineare, basi e dimensione. Intersezione e somma di sottospazi,
I Bistabili. Maurizio Palesi. Maurizio Palesi 1
 I Bistabili Maurizio Palesi Maurizio Palesi 1 Sistemi digitali Si possono distinguere due classi di sistemi digitali Sistemi combinatori Il valore delle uscite al generico istante t* dipende solo dal valore
I Bistabili Maurizio Palesi Maurizio Palesi 1 Sistemi digitali Si possono distinguere due classi di sistemi digitali Sistemi combinatori Il valore delle uscite al generico istante t* dipende solo dal valore
La mobilità degli elementi chimici
 La mobilità degli elementi chimici Gli ioni contenuti nella parte sinistra del diagramma sono quelli che in soluzione si presentano sotto forma di cationi semplici. Gli ioni nella parte centrale del diagramma
La mobilità degli elementi chimici Gli ioni contenuti nella parte sinistra del diagramma sono quelli che in soluzione si presentano sotto forma di cationi semplici. Gli ioni nella parte centrale del diagramma
ARROTONDANDO FIGURE CON TRIANGOLI EQUILATERI
 ARROTONDANDO Cosa succede ad accostare figure identiche una all altra? Le figure ottenute che proprietà presentano? Posso trovare un qualche tipo di legge generale? Per rispondere a questa ed altre domande
ARROTONDANDO Cosa succede ad accostare figure identiche una all altra? Le figure ottenute che proprietà presentano? Posso trovare un qualche tipo di legge generale? Per rispondere a questa ed altre domande
Lezione del 24 Ottobre 2014
 MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
GAS IDEALI E MACCHINE TERMICHE. G. Pugliese 1
 GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
valore di a: verso l alto (ordinate crescenti) se a>0, verso il basso (ordinate decrescenti) se a<0;
 La parabola è una particolare conica definita come è una curva aperta, nel senso che non può essere contenuta in alcuna superficie finita del piano; è simmetrica rispetto ad una retta, detta ASSE della
La parabola è una particolare conica definita come è una curva aperta, nel senso che non può essere contenuta in alcuna superficie finita del piano; è simmetrica rispetto ad una retta, detta ASSE della
Esercizi sulle affinità - aprile 2009
 Esercizi sulle affinità - aprile 009 Ingegneria meccanica 008/009 Esercizio Sono assegnate nel piano le sei rette r : =, s : =, t : =, r : =, s : =, t : = determinare l affinità che trasforma ordinatamente
Esercizi sulle affinità - aprile 009 Ingegneria meccanica 008/009 Esercizio Sono assegnate nel piano le sei rette r : =, s : =, t : =, r : =, s : =, t : = determinare l affinità che trasforma ordinatamente
Leggi dei gas. PV = n RT SISTEMI DI PARTICELLE NON INTERAGENTI. perché le forze tra le molecole sono differenti. Gas perfetti o gas ideali
 Perché nelle stesse condizioni di temperatura e pressione sostanze differenti possono trovarsi in stati di aggregazione differenti? perché le forze tra le molecole sono differenti Da che cosa hanno origine
Perché nelle stesse condizioni di temperatura e pressione sostanze differenti possono trovarsi in stati di aggregazione differenti? perché le forze tra le molecole sono differenti Da che cosa hanno origine
3 H 2 (g) + N 2 (g) 2 NH 3 (g)
 L'equilibrio chimico Alcune reazioni chimiche, come quella tra idrogeno ed ossigeno, vanno avanti fino all'esaurimento del reagente in difetto stechiometrico. Tuttavia ce ne sono altre, come quella tra
L'equilibrio chimico Alcune reazioni chimiche, come quella tra idrogeno ed ossigeno, vanno avanti fino all'esaurimento del reagente in difetto stechiometrico. Tuttavia ce ne sono altre, come quella tra
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
OFFERTA DI LAVORO. p * C = M + w * L
 1 OFFERTA DI LAVORO Supponiamo che il consumatore abbia inizialmente un reddito monetario M, sia che lavori o no: potrebbe trattarsi di un reddito da investimenti, di donazioni familiari, o altro. Definiamo
1 OFFERTA DI LAVORO Supponiamo che il consumatore abbia inizialmente un reddito monetario M, sia che lavori o no: potrebbe trattarsi di un reddito da investimenti, di donazioni familiari, o altro. Definiamo
Il DNA, insieme a diverse proteine si organizza in una
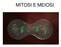 MITOSI E MEIOSI Il DNA, insieme a diverse proteine si organizza in una struttura che è detta CROMOSOMA. I cromosomi sono costituiti da cromatina, che consiste di fibre contenenti DNA e proteine. Quando
MITOSI E MEIOSI Il DNA, insieme a diverse proteine si organizza in una struttura che è detta CROMOSOMA. I cromosomi sono costituiti da cromatina, che consiste di fibre contenenti DNA e proteine. Quando
L unità di misura della dose nel S.I. è il Gray
 LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
Somma di numeri floating point. Algoritmi di moltiplicazione e divisione per numeri interi
 Somma di numeri floating point Algoritmi di moltiplicazione e divisione per numeri interi Standard IEEE754 " Standard IEEE754: Singola precisione (32 bit) si riescono a rappresentare numeri 2.0 10 2-38
Somma di numeri floating point Algoritmi di moltiplicazione e divisione per numeri interi Standard IEEE754 " Standard IEEE754: Singola precisione (32 bit) si riescono a rappresentare numeri 2.0 10 2-38
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico
 gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
Introduzione I contatori sono dispositivi fondamentali nell elettronica digitale e sono utilizzati per:
 INTRODUZIONE AI CONTATORI Introduzione I contatori sono dispositivi fondamentali nell elettronica digitale e sono utilizzati per: o Conteggio di eventi o Divisione di frequenza o Temporizzazioni Principi
INTRODUZIONE AI CONTATORI Introduzione I contatori sono dispositivi fondamentali nell elettronica digitale e sono utilizzati per: o Conteggio di eventi o Divisione di frequenza o Temporizzazioni Principi
STATISTICA DESCRITTIVA. Elementi di statistica medica GLI INDICI INDICI DI DISPERSIONE STATISTICA DESCRITTIVA
 STATISTICA DESCRITTIVA Elementi di statistica medica STATISTICA DESCRITTIVA È quella branca della statistica che ha il fine di descrivere un fenomeno. Deve quindi sintetizzare tramite pochi valori(indici
STATISTICA DESCRITTIVA Elementi di statistica medica STATISTICA DESCRITTIVA È quella branca della statistica che ha il fine di descrivere un fenomeno. Deve quindi sintetizzare tramite pochi valori(indici
Si dice parabola il luogo geometrico dei punti del piano, equidistanti da un punto fisso, detto fuoco, e da una retta fissa, detta direttrice.
 LA PARABOLA Definizione: Si dice parabola il luogo geometrico dei punti del piano, equidistanti da un punto fisso, detto fuoco, e da una retta fissa, detta direttrice. Dimostrazione della parabola con
LA PARABOLA Definizione: Si dice parabola il luogo geometrico dei punti del piano, equidistanti da un punto fisso, detto fuoco, e da una retta fissa, detta direttrice. Dimostrazione della parabola con
Quadro riassuntivo di geometria analitica
 Quadro riassuntivo di geometria analitica IL PIANO CARTESIANO (detta ascissa o coordinata x) e y quella dall'asse x (detta ordinata o coordinata y). Le coordinate di un punto P sono: entrambe positive
Quadro riassuntivo di geometria analitica IL PIANO CARTESIANO (detta ascissa o coordinata x) e y quella dall'asse x (detta ordinata o coordinata y). Le coordinate di un punto P sono: entrambe positive
CAPITOLO 2 CICLO BRAYTON TURBINE A GAS
 CAPITOLO 2 CICLO BRAYTON TURBINE A GAS 1 CICLO BRAYTON IL CICLO TERMODINAMICO BRAYTON E COMPOSTO DA QUATTRO TRASFORMAZIONI PRINCIPALI (COMPRESSIONE, RISCALDAMENTO, ESPANSIONE E RAFFREDDAMENTO), PIÙ ALTRE
CAPITOLO 2 CICLO BRAYTON TURBINE A GAS 1 CICLO BRAYTON IL CICLO TERMODINAMICO BRAYTON E COMPOSTO DA QUATTRO TRASFORMAZIONI PRINCIPALI (COMPRESSIONE, RISCALDAMENTO, ESPANSIONE E RAFFREDDAMENTO), PIÙ ALTRE
Le frazioni algebriche
 Le frazioni algebriche Le frazioni algebriche, a differenza delle frazioni numeriche, sono frazioni che prevedono al denominatore espressioni polinomiali. Le seguenti, ad esempio, sono frazioni algebriche
Le frazioni algebriche Le frazioni algebriche, a differenza delle frazioni numeriche, sono frazioni che prevedono al denominatore espressioni polinomiali. Le seguenti, ad esempio, sono frazioni algebriche
ITCS Erasmo da Rotterdam. Anno Scolastico 2014/2015. CLASSE 4^ M Costruzioni, ambiente e territorio
 ITCS Erasmo da Rotterdam Anno Scolastico 014/015 CLASSE 4^ M Costruzioni, ambiente e territorio INDICAZIONI PER IL LAVORO ESTIVO DI MATEMATICA e COMPLEMENTI di MATEMATICA GLI STUDENTI CON IL DEBITO FORMATIVO
ITCS Erasmo da Rotterdam Anno Scolastico 014/015 CLASSE 4^ M Costruzioni, ambiente e territorio INDICAZIONI PER IL LAVORO ESTIVO DI MATEMATICA e COMPLEMENTI di MATEMATICA GLI STUDENTI CON IL DEBITO FORMATIVO
Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici.
 LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
Il primo principio della termodinamica
 1 Il primo principio della termodinamica Il primo principio della termodinamica Nelle lezioni precedenti abbiamo visto che per far innalzare la temperatura di un sistema vi sono due possibilità: fornendo
1 Il primo principio della termodinamica Il primo principio della termodinamica Nelle lezioni precedenti abbiamo visto che per far innalzare la temperatura di un sistema vi sono due possibilità: fornendo
Esame di FONDAMENTI DI AUTOMATICA (9 crediti) SOLUZIONE
 Esame di FONDAMENTI DI AUTOMATICA (9 crediti) Prova scritta 16 luglio 2014 SOLUZIONE ESERCIZIO 1. Dato il sistema con: si determinino gli autovalori della forma minima. Per determinare la forma minima
Esame di FONDAMENTI DI AUTOMATICA (9 crediti) Prova scritta 16 luglio 2014 SOLUZIONE ESERCIZIO 1. Dato il sistema con: si determinino gli autovalori della forma minima. Per determinare la forma minima
ficobiline e carotenoidi. Ogni tipo di pigmento è in grado di assorbire una particolare lunghezza
 1.1.1 Fase luminosa e fotosistemi Sulle membrane si trovano molecole di pigmenti che formano due strutture molecolari dette fotosistema I e fotosistema II. Oltre alla clorofilla, vi sono anche pigmenti
1.1.1 Fase luminosa e fotosistemi Sulle membrane si trovano molecole di pigmenti che formano due strutture molecolari dette fotosistema I e fotosistema II. Oltre alla clorofilla, vi sono anche pigmenti
APPUNTI DI TECNOLOGIA. ENERGIA NUCLEARE Fissione nucleare Fusione nucleare Centrali nucleari Vantaggi - Svantaggi Produzione
 APPUNTI DI TECNOLOGIA ENERGIA NUCLEARE Fissione nucleare Fusione nucleare Centrali nucleari Vantaggi - Svantaggi Produzione 01 EN. NUCLEARE: MAPPA CONCETTUALE 01b EN. NUCLEARE: FISSIONE NUCLEARE La fissione
APPUNTI DI TECNOLOGIA ENERGIA NUCLEARE Fissione nucleare Fusione nucleare Centrali nucleari Vantaggi - Svantaggi Produzione 01 EN. NUCLEARE: MAPPA CONCETTUALE 01b EN. NUCLEARE: FISSIONE NUCLEARE La fissione
0.1 Esercizi calcolo combinatorio
 0.1 Esercizi calcolo combinatorio Esercizio 1. Sia T l insieme dei primi 100 numeri naturali. Calcolare: 1. Il numero di sottoinsiemi A di T che contengono esattamente 8 pari.. Il numero di coppie (A,
0.1 Esercizi calcolo combinatorio Esercizio 1. Sia T l insieme dei primi 100 numeri naturali. Calcolare: 1. Il numero di sottoinsiemi A di T che contengono esattamente 8 pari.. Il numero di coppie (A,
Il TU 81/2008 con le modifiche del D.lgs 39/2016
 Il TU 81/2008 con le modifiche del D.lgs 39/2016 Titolo IX Il D.lgs 39/2016 entrato in vigore il 29 marzo 2016, modifica così il Testo Unico Sicurezza Riferimento TU Testo ante modifiche Testo modificato
Il TU 81/2008 con le modifiche del D.lgs 39/2016 Titolo IX Il D.lgs 39/2016 entrato in vigore il 29 marzo 2016, modifica così il Testo Unico Sicurezza Riferimento TU Testo ante modifiche Testo modificato
L idrogeno. Cennii sull comportamento chiimiico dellll iidrogeno
 Appunti di Chimica Preparazione dell idrogeno L idrogeno...1 Cenni sul comportamento chimico dell idrogeno...1 Richiami sul legame ad idrogeno...2 Preparazione dell idrogeno...3 Il problema della riduzione
Appunti di Chimica Preparazione dell idrogeno L idrogeno...1 Cenni sul comportamento chimico dell idrogeno...1 Richiami sul legame ad idrogeno...2 Preparazione dell idrogeno...3 Il problema della riduzione
Problema 1 Mg + 2HCl H 2 + MgCl 2. di Mg 1 Mg 1 H 2 quindi 0,823 moli di H 2 di H 2
 REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
Sistemi Web per il turismo - lezione 3 -
 Sistemi Web per il turismo - lezione 3 - Software Si definisce software il complesso di comandi che fanno eseguire al computer delle operazioni. Il termine si contrappone ad hardware, che invece designa
Sistemi Web per il turismo - lezione 3 - Software Si definisce software il complesso di comandi che fanno eseguire al computer delle operazioni. Il termine si contrappone ad hardware, che invece designa
DESCRIZIONE CREAZIONE APP Si suddivide in 4 fasi di lavoro: 1. PIANIFICAZIONE; 2. PROGETTAZIONE; 3. SVILUPPO; 4. DISTRIBUZIONE.
 DESCRIZIONE CREAZIONE APP Si suddivide in 4 fasi di lavoro: 1. PIANIFICAZIONE; 2. PROGETTAZIONE; 3. SVILUPPO; 4. DISTRIBUZIONE. PIANIFICAZIONE La pianificazione è la prima fase. Questa è la più delicata
DESCRIZIONE CREAZIONE APP Si suddivide in 4 fasi di lavoro: 1. PIANIFICAZIONE; 2. PROGETTAZIONE; 3. SVILUPPO; 4. DISTRIBUZIONE. PIANIFICAZIONE La pianificazione è la prima fase. Questa è la più delicata
Normalizzazione. Definizione
 Normalizzazione Definizione Le forme normali 2 Una forma normale è una proprietà di una base di dati relazionale che ne garantisce la qualità, cioè l'assenza di determinati difetti Quando una relazione
Normalizzazione Definizione Le forme normali 2 Una forma normale è una proprietà di una base di dati relazionale che ne garantisce la qualità, cioè l'assenza di determinati difetti Quando una relazione
32 L influenza della politica monetaria e fiscale sulla domanda aggregata
 32 L influenza della politica monetaria e fiscale sulla domanda aggregata 1 La domanda aggregata è influenzata da molti fattori, inclusi i desideri di spesa delle famiglie e delle imprese Quando i desideri
32 L influenza della politica monetaria e fiscale sulla domanda aggregata 1 La domanda aggregata è influenzata da molti fattori, inclusi i desideri di spesa delle famiglie e delle imprese Quando i desideri
FISICA. isoterma T f. T c. Considera il ciclo di Stirling, in cui il fluido (=sistema) è considerato un gas ideale.
 Serie 10: ermodinamica X FISICA II liceo Esercizio 1 Ciclo di Carnot Considera il ciclo di Carnot, in cui il fluido (=sistema) è considerato un gas ideale. Si considerano inoltre delle trasformazioni reversibili.
Serie 10: ermodinamica X FISICA II liceo Esercizio 1 Ciclo di Carnot Considera il ciclo di Carnot, in cui il fluido (=sistema) è considerato un gas ideale. Si considerano inoltre delle trasformazioni reversibili.
Tensioni e corrente variabili
 Tensioni e corrente variabili Spesso, nella pratica, le tensioni e le correnti all interno di un circuito risultano variabili rispetto al tempo. Se questa variabilità porta informazione, si parla spesso
Tensioni e corrente variabili Spesso, nella pratica, le tensioni e le correnti all interno di un circuito risultano variabili rispetto al tempo. Se questa variabilità porta informazione, si parla spesso
Esercizi Le leggi di Lavoisier, Proust e Dalton
 Per riscaldamento, 123 g di clorato di potassio si decompongono, svolgendo ossigeno e lasciando un residuo di 75 g di cloruro di potassio. Calcola la massa dell ossigeno svolto. clorato di potassio ossigeno
Per riscaldamento, 123 g di clorato di potassio si decompongono, svolgendo ossigeno e lasciando un residuo di 75 g di cloruro di potassio. Calcola la massa dell ossigeno svolto. clorato di potassio ossigeno
Progetto del controllore
 Parte 10, 1 - Problema di progetto Parte 10, 2 Progetto del controllore Il caso dei sistemi LTI a tempo continuo Determinare in modo che il sistema soddisfi alcuni requisiti - Principali requisiti e diagrammi
Parte 10, 1 - Problema di progetto Parte 10, 2 Progetto del controllore Il caso dei sistemi LTI a tempo continuo Determinare in modo che il sistema soddisfi alcuni requisiti - Principali requisiti e diagrammi
LE OPERAZIONI STRAORDINARIE
 LE OPERAZIONI STRAORDINARIE 1. SONO OPERAZIONI DI FINANZA STRAORDINARIA, VOLTE A SODDISFARE I BISOGNI FISIOLOGICI DI CRESCITA, PATRIMONIALIZZAZIONE, INTERNAZIONALIZZAZIONE E RICAMBIO GENERAZIONALE DELLE
LE OPERAZIONI STRAORDINARIE 1. SONO OPERAZIONI DI FINANZA STRAORDINARIA, VOLTE A SODDISFARE I BISOGNI FISIOLOGICI DI CRESCITA, PATRIMONIALIZZAZIONE, INTERNAZIONALIZZAZIONE E RICAMBIO GENERAZIONALE DELLE
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
LED:SORGENTE LUMINOSA A BASSO CONSUMO VANTAGGI ED APPLICAZIONI. Saros Energia - Via gabelli, 17 Porcia (PN) - Tel. 0434-555156
 LED:SORGENTE LUMINOSA A BASSO CONSUMO VANTAGGI ED APPLICAZIONI Cos è un LED? I LED, anche chiamati diodi ad emissione di luce, sono molto più che semplici lampadine: sono sicuramente la nuova frontiera
LED:SORGENTE LUMINOSA A BASSO CONSUMO VANTAGGI ED APPLICAZIONI Cos è un LED? I LED, anche chiamati diodi ad emissione di luce, sono molto più che semplici lampadine: sono sicuramente la nuova frontiera
I differenti materiali differiscono per le caratteristiche meccaniche e fisiche.
 MATERIALI COMPOSITI I differenti materiali differiscono per le caratteristiche meccaniche e fisiche. I METALLI hanno forma cristallina e forti legami molecolari (legame metallico), che danno loro resistenza
MATERIALI COMPOSITI I differenti materiali differiscono per le caratteristiche meccaniche e fisiche. I METALLI hanno forma cristallina e forti legami molecolari (legame metallico), che danno loro resistenza
BOX 16. Lampade a confronto.
 Lampade a confronto. Un confronto tra lampade a risparmio energetico, comuni lampadine e tubi al neon. Le lampadine In una lampadina la corrente passa attraverso una sottile spirale di un metallo particolare
Lampade a confronto. Un confronto tra lampade a risparmio energetico, comuni lampadine e tubi al neon. Le lampadine In una lampadina la corrente passa attraverso una sottile spirale di un metallo particolare
Esercizi sulle equazioni logaritmiche
 Esercizi sulle equazioni logaritmiche Per definizione il logaritmo in base a di un numero positivo x, con a > 0 e a 1, è l esponente che occorre dare alla base a per ottenere il numero x. In simboli log
Esercizi sulle equazioni logaritmiche Per definizione il logaritmo in base a di un numero positivo x, con a > 0 e a 1, è l esponente che occorre dare alla base a per ottenere il numero x. In simboli log
L'energia media V di interazione fra uno ione avente carica q e un dipolo permanente ad una distanza r Ä
 Interazioni intermolecolari Interazioni ione-dipolo Interazioni dipolo-dipolo Interazione dipolo permanente-dipolo indotto Interazione dipolo istantaneo-dipolo indotto Forze di Van der Waals Legame idrogeno
Interazioni intermolecolari Interazioni ione-dipolo Interazioni dipolo-dipolo Interazione dipolo permanente-dipolo indotto Interazione dipolo istantaneo-dipolo indotto Forze di Van der Waals Legame idrogeno
Generatori di tensione
 Correnti alternate Generatori di tensione Sinora come generatore di forza elettromotrice abbiamo preso in considerazione soltanto la pila elettrica. Questo generatore ha la caratteristica di fornire sempre
Correnti alternate Generatori di tensione Sinora come generatore di forza elettromotrice abbiamo preso in considerazione soltanto la pila elettrica. Questo generatore ha la caratteristica di fornire sempre
10. Quale dei seguenti numeri
 Test d'ingresso di matematica per la secondaria di secondo grado (liceo classico) Il test si basa su alcuni test di ingresso (opportunamente modificati) assegnati al liceo classico e trovati in Rete Nome:
Test d'ingresso di matematica per la secondaria di secondo grado (liceo classico) Il test si basa su alcuni test di ingresso (opportunamente modificati) assegnati al liceo classico e trovati in Rete Nome:
Prova in itinere di Chimica Generale 8 Gennaio 2016 A
 Prova in itinere di Chimica Generale 8 Gennaio 2016 A COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno
Prova in itinere di Chimica Generale 8 Gennaio 2016 A COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno
Sistemi di equazioni lineari
 Sistemi di equazioni lineari A. Bertapelle 25 ottobre 212 Cos è un sistema lineare? Definizione Un sistema di m equazioni lineari (o brevemente sistema lineare) nelle n incognite x 1,..., x n, a coefficienti
Sistemi di equazioni lineari A. Bertapelle 25 ottobre 212 Cos è un sistema lineare? Definizione Un sistema di m equazioni lineari (o brevemente sistema lineare) nelle n incognite x 1,..., x n, a coefficienti
Occupazione e disoccupazione
 Lezione 20 1 Occupazione e disoccupazione L occupazione ha una fortissima importanza sociale, e pone molti problemi di rilevazione. In questa lezione vediamo come la definizione di occupazione fa emergere
Lezione 20 1 Occupazione e disoccupazione L occupazione ha una fortissima importanza sociale, e pone molti problemi di rilevazione. In questa lezione vediamo come la definizione di occupazione fa emergere
Psiche e complessità. 4. L approccio bottom-up ai problemi
 Psiche e complessità 4. L approccio bottom-up ai problemi Complessità della mente FENOMENI LINEARI (LOGICA, RAZIONALITA, CONTENUTI ESPLICITI) FENOMENI NON LINEARI (ASSOCIAZIONI ANALOGICHE, CONTENUTI IMPLICITI)
Psiche e complessità 4. L approccio bottom-up ai problemi Complessità della mente FENOMENI LINEARI (LOGICA, RAZIONALITA, CONTENUTI ESPLICITI) FENOMENI NON LINEARI (ASSOCIAZIONI ANALOGICHE, CONTENUTI IMPLICITI)
L equilibrio chimico
 L equilibrio chimico Vi sono molte reazioni chimiche che non procedono fino a completezza, cioè fino a che uno dei reagenti non si esaurisca, ad esempio la reazione di dimerizzazione del diossido di azoto:
L equilibrio chimico Vi sono molte reazioni chimiche che non procedono fino a completezza, cioè fino a che uno dei reagenti non si esaurisca, ad esempio la reazione di dimerizzazione del diossido di azoto:
BOLLETTINO dei controlli della produttività del latte 2015
 ASSOCIAZIONE ITALIANA ALLEVATORI ENTE MORALE D.P.R. N. 1051 DEL 27-10-1950 UFFICIO CENTRALE DEI CONTROLLI DELLA PRODUTTIVITÁ ANIMALE SOTTOPOSTO ALLA VIGILANZA DEL MINISTERO DELLE POLITICHE AGRICOLE E FORESTALI
ASSOCIAZIONE ITALIANA ALLEVATORI ENTE MORALE D.P.R. N. 1051 DEL 27-10-1950 UFFICIO CENTRALE DEI CONTROLLI DELLA PRODUTTIVITÁ ANIMALE SOTTOPOSTO ALLA VIGILANZA DEL MINISTERO DELLE POLITICHE AGRICOLE E FORESTALI
Procedura operativa per la gestione della funzione di formazione classi prime
 Procedura operativa per la gestione della funzione di formazione classi prime Questa funzione viene fornita allo scopo di effettuare la formazione delle classi prime nel rispetto dei parametri indicati
Procedura operativa per la gestione della funzione di formazione classi prime Questa funzione viene fornita allo scopo di effettuare la formazione delle classi prime nel rispetto dei parametri indicati
Soluzione dei sistemi lineari con metodo grafico classe 2H
 Soluzione dei sistemi lineari con metodo grafico classe H (con esempi di utilizzo del software open source multipiattaforma Geogebra e calcolatrice grafica Texas Instruments TI-89) Metodo grafico Il metodo
Soluzione dei sistemi lineari con metodo grafico classe H (con esempi di utilizzo del software open source multipiattaforma Geogebra e calcolatrice grafica Texas Instruments TI-89) Metodo grafico Il metodo
CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq) + H 2 O (l)
 2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
ESERCITAZIONE 3 : PERCENTUALI
 ESERCITAZIONE 3 : PERCENTUALI e-mail: tommei@dm.unipi.it web: www.dm.unipi.it/ tommei Ricevimento: Lunedi 14-17 Dipartimento di Matematica, piano terra, studio 114 22 Ottobre 2013 Esercizio 1 Nel 2006,
ESERCITAZIONE 3 : PERCENTUALI e-mail: tommei@dm.unipi.it web: www.dm.unipi.it/ tommei Ricevimento: Lunedi 14-17 Dipartimento di Matematica, piano terra, studio 114 22 Ottobre 2013 Esercizio 1 Nel 2006,
LEZIONE 4. Le soluzioni
 LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
ISTITUZIONI DI ECONOMIA AZIENDALE
 ISTITUZIONI DI ECONOMIA AZIENDALE IL REDDITO E IL CAPITALE DI IMPRESA 1 IL DIVENIRE ECONOMICO DI IMPRESA CAPITALE t (QUANTITA - FONDO) CAPITALE t+1 (QUANTITA - FONDO) REDDITO (QUANTITA -FLUSSO) 2 Pag.
ISTITUZIONI DI ECONOMIA AZIENDALE IL REDDITO E IL CAPITALE DI IMPRESA 1 IL DIVENIRE ECONOMICO DI IMPRESA CAPITALE t (QUANTITA - FONDO) CAPITALE t+1 (QUANTITA - FONDO) REDDITO (QUANTITA -FLUSSO) 2 Pag.
LA CIRCONFERENZA La circonferenza è il luogo geometrico dei punti equidistanti da un punto C, detto centro.
 Geometria Analitica Le coniche Queste curve si chiamano coniche perché sono ottenute tramite l'intersezione di una superficie conica con un piano. Si possono definire tutte come luoghi geometrici e, di
Geometria Analitica Le coniche Queste curve si chiamano coniche perché sono ottenute tramite l'intersezione di una superficie conica con un piano. Si possono definire tutte come luoghi geometrici e, di
SCOMPOSIZIONE IN FATTORI PRIMI:
 SCOMPOSIZIONE IN FATTORI PRIMI: 2 3 5 7 11 13 17 19 23 29 31 37 41 43 47 53 59 61 67 71 73 79 83 89 97 101 103 107 109 113 127 131 137 139 149 151 157 163 167 173 179 181 191 193 197 199 211 223 227 229
SCOMPOSIZIONE IN FATTORI PRIMI: 2 3 5 7 11 13 17 19 23 29 31 37 41 43 47 53 59 61 67 71 73 79 83 89 97 101 103 107 109 113 127 131 137 139 149 151 157 163 167 173 179 181 191 193 197 199 211 223 227 229
Problemi di scelta ESEMPI
 ESEMPI Risolvere i seguenti problemi 1. Una ditta deve effettuare delle spedizioni di un certo tipo di merce. Ha la possibilità di scegliere una o l altra delle due tariffe seguenti: a) 2.500 lire al quintale
ESEMPI Risolvere i seguenti problemi 1. Una ditta deve effettuare delle spedizioni di un certo tipo di merce. Ha la possibilità di scegliere una o l altra delle due tariffe seguenti: a) 2.500 lire al quintale
