Gruppi di studenti con i quali è stata svolta l'attività - ore per gruppo - prevista per tutti gli studenti (senza gruppi associati) - 30 ore
|
|
|
- Ugo Pasini
- 5 anni fa
- Visualizzazioni
Transcript
1 Attività didattica BIOCHIMICA [785ME] Dipartimento Universitario Clinico di Scienze mediche, chirurgiche e della salute Anno Accademico 2018/19 Registro lezioni del docente PASSAMONTI SABINA Periodo di svolgimento: Secondo Semestre Docente titolare del corso: GRASSI GABRIELE matr Altri docenti del corso: PASSAMONTI SABINA matr Riepilogo registro docente: PASSAMONTI SABINA matr Docente interno - Ricercatori Universitari Stato registro docente: Stampato Ore inserite: 30 ore Ore previste dall'offerta didattica: 20 ore Gruppi di studenti con i quali è stata svolta l'attività - ore per gruppo - prevista per tutti gli studenti (senza gruppi associati) - 30 ore Ore inserite per tipologia di attività 30 ore lezione : - prevista per tutti gli studenti (senza gruppi associati) - 30 ore Firma del docente: Firma del direttore: Data: Pagina 1 di 6
2 Dettaglio delle attività svolte: BIOCHIMICA [785ME] 04/03/ lezione - Lezione 1 Introduzione al corso di biochimica. Descrizione degli obiettivi di consocenza della biochimica strutturale e funzionale. L'acqua: caretteristiche molecolari; legame idrogeno. La solubilità in acqua di: sali, gas, molecole polari-apolari-anfipatiche. La solubilità di acqua e molecole polari nelle membrane. Osmosi. 05/03/ lezione - Lezione 2 Ionizzazione dell'acqua. ph. Acidi e basi. Amminoacidi. 06/03/ lezione - Lezione 3 Peptidi. Proteine. Stuttura primaria. Famiglie proteiche; domini proteici; sequenze tipo. Strutture secondarie: il legame peptidico; la catena alfa; il foglietto beta; il ripiegamento beta.strutture terziaria e quaternaria e forze che le stabilizzano. Proteine globulari e fibrose. 07/03/ lezione - Lezione 4 Collagene: livelli di struttura. Lisina e prolina: reazioni di idrossilazione e vitamina C. La mioglobina: livelli di struttura; il gruppo prostetico eme. I motivi strutturali delle proteine globulari: anse e barili. Le proteine intrinsecamente disordinate. La denaturazione delle proteine e gli agenti denaturanti. Gli stadi del ripiegamento (folding). La proteostasi e il suo controllo. I chaperoni. Gli enzimi che assistono il ripiegamento; il glutatione. I difetti del ripiegamento: l'amiloide. Le variazioni di energia libera negli stadi del ripiegamento. Pagina 2 di 6
3 08/03/ lezione - Lezione 5 Mioglobina ed emoglobina: trasportatori di ossigeno con diverse proprietà. Il problema del trasporto dell'ossigeno: i limiti di solubilità dell'ossigeno in acqua; il legame dell'ossigeno all'eme; le reazioni del ferro con l'ossigeno; il legame dell'eme alle catene proteiche della mioglobiane ed emoglobina. La caratterizzazione quantitativa del legame ossigeno-mioglobina. L'emoglobina: livelli di struttura proteica. Gli stati allosterici dell'emoglobina. Il legame dell'ossigeno all'emoglobina e suoi effetti allosterici. 12/03/ lezione - Lezione 6 La caratterizzazione quantitativa del legame ossigeno-emoglobina. L'equazione di Hill. I due modelli che spiegano l'allosteria. Il trasporto di protoni e anidride carbonica da parte dell'emeoglobina. L'effetto Bohr. Il 2,3-bisfosfoglicerato.Altri fattori che alterano il legame dell'ossigeno all'emoglobina: la temperatura; l'anemia; la carbossi-emoglobina.l'emoglobina fetale. L'emoglobina S. Gli enzimi. Le classi di enzimi e la nomenclatura. I nomi comuni degli enzimi. Le basi strutturali della catalisi e dell'adattamento indotto. L'equazione chimica delle reazioni enzimatiche (semplici). Equilibrio chimico ed energia libera.l'equazione della velocità di reazione enzimatica e significato della costante di reazione. 13/03/ lezione - Lezione 7 Enzimi: la formazione del complesso enzima-substrato. La cinetica enzimatica e l'equazione di Michaelis-Menten. Il significato della costante di Michaelis-Menten e della velocità massima di reazione. Le reazioni multisubstrato. Pagina 3 di 6
4 14/03/ lezione - Lezione 8 Enzimi: inibizione enzimatica (reversibile ed irreversibile). Inibizione competitiva, incompetitiva e mista. Il controllo dell'attività enzimatica (allosteria; modificazione post-traduzionale; proteolisi di precursori). La cinetica di reazione degli enzimi allosterici. La fosforilazione e defosforilazione degli enzimi, ed altri tipi di modificazione chimica. La proteolisi controllata di zimogeni. 15/03/ lezione - Lezione 9 I carboidrati. Triosi, tetrosi, pentosi, esosi. Isomeria degi monosaccaridi (struttrale; stereoisomeria; isomeria configurazionale e conformazionale). Derivati biologici degli esosi.disaccaridi. oligosaccaridi, polisaccaridi (omo- ed etero-polisaccaridi).glicogeno ed amido. Cellulaosa, chitina. Glicooamminoglicani. Glicoproteine e glicosfingolipidi. Legami O-glicosidici ed N-glicosidici. Nucleotidi: struttura delle basi puriniche e pirimidiniche; nomenclatura delle nucleobasi, nucleosidi e nucleotidi. Struttura dei polinucleotidi (legame fosfodiestere). Le coppie di nucleobasi nel DNA e RNA (legami idrogeno). Struttura dell'alfa-elica del DNA. Palindromi e sequenze ripetute ed effetti sulla struttura secondaria di DNA o RNA. Deamminazione e depurinazione. Dimeri di pirimidina e alchilazione delle basi. 18/03/ lezione - Lezione 10 Lipidi: acidi grassi saturi, insaturi e poli-insaturi. Esteri degli acidi grassi: triacilgliceroli, acido fosfatidico. Esteri dell'acido fosfatidico (fosfolipidi acidi, basici e neutri). Cardiolipine. Sfingolipidi. I glicisfingolipidi. Le fosfolipasi (A1, A2, C e D). Il turnover dei fosfolipisi nei lisosomi. Il colesteroli e suoi derivati (ormoni steroidei, sali biliari). La vitamina D. Le molecole segnale che derivano dai fosfolipidi. Gli eicosanoidi. Pagina 4 di 6
5 19/03/ lezione - Lezione 11 Le vitamine liposolubli: A, D, E, K. Membrane biologiche: composizione chimica e struttura. Le proteine di membrana estrinseche ed intrineche (monotopiche e politopiche). Le due classi strutturali (fascio di alfa-eliche e beta-barile). La struttura primaria delle proteine di membrana e l'indice idropatico. Le ancore lipidiche delle proteine estrinseche. Il riconoscimento proteina-membrana: dominio proteico PH e SH2. Traslocazione dei fosfolipidi di membrana (flippasi, floppasi e scramblasi). Le zattere di membrana. 20/03/ lezione - Lezione 12 Il trasporto di membrana. L'equilibrio chimico, elettrico ed osmotico del trasporto di membrana. I tipi di trasporto di membrana (passivo, facilitato e attivo).la catalisi del trasporto e le variazioni di energia libera. Trasportatori e canali. Il trasporto del glucosio negli eritrociti: l'equazione di velocità di trasporto e significato dei parametri.il trasportatore GLUT1: relazione struttura-funzione. I 12 trasportatori GLUT. I sistemi co-trasporto (simporto e antiporto). 21/03/ lezione - Lezione 13 Il trasporto di membrana. L'energia libera del trasporto di molecole neutre o cariche. Le variazioni di energia libera (trasporto endoergonico ed esoergonico). I trasportatori attivi primari: le cassi di ATPasi di trasporto. La pompa del calcio SERCA: ciclo catalitico e relazione struttura-funzione. La pompa sodio-potassio ATPasi: ciclo catalitico e relazione struttura-funzione. Le aquaporine: prototipo di canale. Pagina 5 di 6
6 25/03/ lezione - Lezione 14 Biosegnalazione: principi di trasduzione del segnale.i recettori accoppiati alle proteine G. Il ciclo di attivazione delle proteine G. Gli enzimi effettori. L'adenilato ciclasi: struttura e funzione. Il messaggero camp. Le proteine G attivatri e inibitrici. La proteina chinasi A: struttura e funzione. L'amplificazione del segnale. L'interruzione del segnale e del secondo messaggero. L'enzima effettore fosfolipasi C ed i secondi messaggeri da esso derivati (PIP3, DAG e calcio). La calmodulina. La fototrasduzione visiva. I recettori tirosina chinasi.il recettore dell'insulina. Le due vie di trasduzione intracellulare dell'insulina: attiviazione della trascrizione dei geni e attivazione degli enzimi della sintesi del glicogeno e dell'espressione di GLUT4. 27/03/ lezione - Lezione 15 Biosegnalazione: il messaggero cgmp. Le guanilati ciclasi (di membrana e citosoliche). Il monoossido d'azoto.il cross-talk delle vie di segnalazione. Le cellule eccitabili e i canali ionici. I diversi tipi di canali ionici. Ruono dei canali ionici nella trasmissione del segnale elettrico. Contrazione muscolare: le proteine del muscolo: actina, miosina, tropomiosina e troponina. Il sarcomerorilassato e contratto. La teoria dello scorrimento dell'actina sulla miosina: struttura e funzione del sarcomero, delle teste della miosina e loro catalisi dell'idrolisi dell'atp. Le vriazioni conformazionali che causano il colpo di potenza. Chiarimenti sulla modalità d'esame. Pagina 6 di 6
Informazioni sul corso a.a v.1. Insegnamento di Biochimica 090SM BIO/10 6 CFU 48 ore
 Informazioni sul corso a.a 2017-18 v.1 Insegnamento di Biochimica 090SM BIO/10 6 CFU 48 ore Informazioni sul corso Marco Scocchi Dip. Di Scienze della Vita - Prof. Associato Tel. 040-5588704 mscocchi@units.it
Informazioni sul corso a.a 2017-18 v.1 Insegnamento di Biochimica 090SM BIO/10 6 CFU 48 ore Informazioni sul corso Marco Scocchi Dip. Di Scienze della Vita - Prof. Associato Tel. 040-5588704 mscocchi@units.it
Informazioni sul corso a.a v.3. Insegnamento di Biochimica I 639SM BIO/10 6 CFU 48 ore
 Informazioni sul corso a.a 2018-19 v.3 Insegnamento di Biochimica I 639SM BIO/10 6 CFU 48 ore Informazioni sul corso Marco Scocchi Dip. Di Scienze della Vita - Prof. Associato Tel. 040-5588704 mscocchi@units.it
Informazioni sul corso a.a 2018-19 v.3 Insegnamento di Biochimica I 639SM BIO/10 6 CFU 48 ore Informazioni sul corso Marco Scocchi Dip. Di Scienze della Vita - Prof. Associato Tel. 040-5588704 mscocchi@units.it
Struttura esame Biochimica per Sc. Biologiche DM270 e DM509 da gennaio 2017
 Struttura esame Biochimica per Sc. Biologiche DM270 e DM509 da gennaio 2017 Prof. G. Gilardi : biomolecole, enzimi, vitamine Prof. S.J. Sadeghi : metabolismo ed esercitazioni Prof. G. Gilardi - Biological
Struttura esame Biochimica per Sc. Biologiche DM270 e DM509 da gennaio 2017 Prof. G. Gilardi : biomolecole, enzimi, vitamine Prof. S.J. Sadeghi : metabolismo ed esercitazioni Prof. G. Gilardi - Biological
CHIMICA BIOLOGICA. Università degli Studi della Campania Luigi Vanvitelli. Antimo Di Maro. Lezione 0. Corso di Laurea in Scienze Biologiche
 Università degli Studi della Campania Luigi Vanvitelli Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 0 Chimica Biologica o Biochimica
Università degli Studi della Campania Luigi Vanvitelli Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 0 Chimica Biologica o Biochimica
nm di spessore
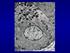 7.5-10 nm di spessore Modello a mosaico fluido Secondo il modello a mosaico fluido la membrana è discontinua, fluida e asimmetrica Nella struttura a mosaico gli strati lipidici formano una matrice fluida
7.5-10 nm di spessore Modello a mosaico fluido Secondo il modello a mosaico fluido la membrana è discontinua, fluida e asimmetrica Nella struttura a mosaico gli strati lipidici formano una matrice fluida
Le biomolecole si trovano negli organismi viventi
 Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
BIOMOLECOLE LE BASI DELLA BIOCHIMICA. Capitolo 1 Dal Carbonio agli OGM PLUS
 BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
Laurea di I Livello in SCIENZE E TECNOLOGIE AGRARIE L 25
 Laurea di I Livello in SCIENZE E TECNOLOGIE AGRARIE L 25 Corso Integrato Chimica Agraria (12 CFU) Moduli didattici Biochimica e Fisiologia Vegetale (6 CFU) Chimica del Suolo (6 CFU) Prof. Maria Rosaria
Laurea di I Livello in SCIENZE E TECNOLOGIE AGRARIE L 25 Corso Integrato Chimica Agraria (12 CFU) Moduli didattici Biochimica e Fisiologia Vegetale (6 CFU) Chimica del Suolo (6 CFU) Prof. Maria Rosaria
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Il carbonio è l elemento più abbondante nelle molecole biologiche
 Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Orientamento delle molecole di colesterolo in un doppio strato lipidico
 Orientamento delle molecole di colesterolo in un doppio strato lipidico Una cellula animale contiene fino al 50% in molarità di colesterolo rispetto al totale dei lipidi di membrana Il colesterolo ha l
Orientamento delle molecole di colesterolo in un doppio strato lipidico Una cellula animale contiene fino al 50% in molarità di colesterolo rispetto al totale dei lipidi di membrana Il colesterolo ha l
Jay Phelan, Maria Cristina Pignocchino. Scopriamo la biologia
 Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Fornire agli studenti adeguate informazioni sulle principali vie metaboliche e sui processi biochimici che si verificano nell organismo umano.
 DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2018/2019-2 anno BIOCHIMICA BIO/10-9 CFU - 2 semestre Docente titolare dell'insegnamento
DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2018/2019-2 anno BIOCHIMICA BIO/10-9 CFU - 2 semestre Docente titolare dell'insegnamento
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Proprietà di permeabilità della membrana
 Proprietà di permeabilità della membrana Il Trasporto attraverso le membrane La fase lipidica delle membrane le rende impermeabili alla maggior parte degli ioni e delle sostanze polari. Questi composti
Proprietà di permeabilità della membrana Il Trasporto attraverso le membrane La fase lipidica delle membrane le rende impermeabili alla maggior parte degli ioni e delle sostanze polari. Questi composti
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Lezione 3 Christian Skou ( )
 Lezione 3 Christian Skou (1918 - ) 1. I trasporti attivi (primari e secondari) 2. La Na/K ATPasi come modello di trasporto attivo primario 3. I trasportatori SGLT modello dei trasporti attivi secondari
Lezione 3 Christian Skou (1918 - ) 1. I trasporti attivi (primari e secondari) 2. La Na/K ATPasi come modello di trasporto attivo primario 3. I trasportatori SGLT modello dei trasporti attivi secondari
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Biochimica - canale 1
 DIPARTIMENTO DI SCIENZE BIOLOGICHE, GEOLOGICHE E AMBIENTALI Corso di laurea in Scienze biologiche Anno accademico 2017/2018-2 anno Biochimica - canale 1 BIO/10-9 CFU - 2 semestre Docente titolare dell'insegnamento
DIPARTIMENTO DI SCIENZE BIOLOGICHE, GEOLOGICHE E AMBIENTALI Corso di laurea in Scienze biologiche Anno accademico 2017/2018-2 anno Biochimica - canale 1 BIO/10-9 CFU - 2 semestre Docente titolare dell'insegnamento
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
INDICE PARTE I CHIMICA. Autori Introduzione
 INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Indice. La biochimica: introduzione 1 Il mondo vivente 4 I batteri 4 Gli archea 6 Gli eucarioti 6 I virus 7
 Iniziali indice (i-xiv) comm 22-02-2006 14:50 Pagina v Prefazione all edizione americana xi Prefazione all edizione italiana xiii CAPITOLO UNO La biochimica: introduzione 1 Il mondo vivente 4 I batteri
Iniziali indice (i-xiv) comm 22-02-2006 14:50 Pagina v Prefazione all edizione americana xi Prefazione all edizione italiana xiii CAPITOLO UNO La biochimica: introduzione 1 Il mondo vivente 4 I batteri
Università degli Studi di Enna Kore Facoltà di Scienze dell Uomo e della Società
 Anno Accademico 2016 2017 A.A. Settore Scientifico Disciplinare CFU Insegnamento Ore di aula Mutuazione 2016/17 BIO/10-Biochimica 6 Biochimica dell Attività Motoria 36 No Classe Corso di studi Tipologia
Anno Accademico 2016 2017 A.A. Settore Scientifico Disciplinare CFU Insegnamento Ore di aula Mutuazione 2016/17 BIO/10-Biochimica 6 Biochimica dell Attività Motoria 36 No Classe Corso di studi Tipologia
Le molecole della vita
 Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre
 Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Stampa Preventivo. A.S Pagina 1 di 8
 Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Biochimica Strutturale con Elementi di Enzimologia corso integrato di Struttura e Funzione delle Macromolecole Biologiche
 Biochimica Strutturale con Elementi di Enzimologia corso integrato di Struttura e Funzione delle Macromolecole Biologiche Codice Disciplina : BT019 Settore : BIO/10 N CFU: 6 Codice Corso integrato : BT067
Biochimica Strutturale con Elementi di Enzimologia corso integrato di Struttura e Funzione delle Macromolecole Biologiche Codice Disciplina : BT019 Settore : BIO/10 N CFU: 6 Codice Corso integrato : BT067
La massa è la quantità di materia di cui è fatta una qualsiasi cosa
 Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Corso di Laurea di I livello in Scienze Animali e Produzioni Alimentari Anno Accademico
 Corso di Laurea di I livello in Scienze Animali e Produzioni Alimentari Anno Accademico 07-8 Programma dell insegnamento di Biochimica delle Macromolecole dell esame integrato di Biochimica Generale Anno
Corso di Laurea di I livello in Scienze Animali e Produzioni Alimentari Anno Accademico 07-8 Programma dell insegnamento di Biochimica delle Macromolecole dell esame integrato di Biochimica Generale Anno
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, orradi, Desco, Ropa himica seconda edizione Bagatti, orradi, Desco, Ropa, himica seconda edizione apitolo 16. Molecole per la vita SEGUI LA MAPPA glicosidico distinguere tra peptidico Struttura
Bagatti, orradi, Desco, Ropa himica seconda edizione Bagatti, orradi, Desco, Ropa, himica seconda edizione apitolo 16. Molecole per la vita SEGUI LA MAPPA glicosidico distinguere tra peptidico Struttura
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Corso di Laurea in Scienze Animali Anno Accademico Programma dell insegnamento di BIOCHIMICA STRUTTURALE E METABOLICA
 Corso di Laurea in Scienze Animali Anno Accademico 018-19 Programma dell insegnamento di BIOCHIMICA STRUTTURALE E METABOLICA Anno di corso Semestre I II N CFU 6 Ore complessive 60 Programma di studio ed
Corso di Laurea in Scienze Animali Anno Accademico 018-19 Programma dell insegnamento di BIOCHIMICA STRUTTURALE E METABOLICA Anno di corso Semestre I II N CFU 6 Ore complessive 60 Programma di studio ed
Di cosa è fatta una cellula?
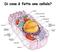 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Modulo 11 biosegnalazione
 Modulo 11 biosegnalazione La trasduzione del segnale Capacità di ricevere e rispondere a segnali esterni alla membrana è un processo fondamentale per la vita. Organismi pluricellulari si scambiano informazioni:
Modulo 11 biosegnalazione La trasduzione del segnale Capacità di ricevere e rispondere a segnali esterni alla membrana è un processo fondamentale per la vita. Organismi pluricellulari si scambiano informazioni:
Di cosa è fatta una cellula?
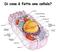 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Composizione della materia vivente. Composizione molecolare delle cellule: acqua, sali, aminoacidi, proteine, glicidi, lipidi e acidi nucleici.
 DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea in Scienze farmaceutiche applicate Anno accademico 2016/2017-2 anno - Curriculum Tossicologia dell'ambiente e degli Alimenti BIOCHIMICA BIO/10-8 CFU
DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea in Scienze farmaceutiche applicate Anno accademico 2016/2017-2 anno - Curriculum Tossicologia dell'ambiente e degli Alimenti BIOCHIMICA BIO/10-8 CFU
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
Trasporti attraverso. Proteine di trasporto
 Trasporti attraverso la membrana Proteine di trasporto Diffusione Facilitata Caratteristiche dei trasporti mediati I carriers sono dotati di specificità Sono soggetti a saturazione Possono essere bloccati
Trasporti attraverso la membrana Proteine di trasporto Diffusione Facilitata Caratteristiche dei trasporti mediati I carriers sono dotati di specificità Sono soggetti a saturazione Possono essere bloccati
Amminoacidi/peptidi/proteine. Chimica Organica II
 Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
Amminoacidi/peptidi/proteine Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II Amminoacidi Chimica Organica II II Amminoacidi: chiralità
Acqua e macromolecole
 Acqua e macromolecole La polarità della molecola dell acqua ha un enorme conseguenza, è responsabile della coesività della capacità di stabilizzare la temperatura delle proprietà di solvente dell
Acqua e macromolecole La polarità della molecola dell acqua ha un enorme conseguenza, è responsabile della coesività della capacità di stabilizzare la temperatura delle proprietà di solvente dell
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
Struttura della membrana plasmatica
 Struttura della membrana plasmatica Le membrane biologiche La struttura e la funzione delle cellule dipendono in modo critico dalle membrane che: separano l ambiente esterno della cellula da quello interno
Struttura della membrana plasmatica Le membrane biologiche La struttura e la funzione delle cellule dipendono in modo critico dalle membrane che: separano l ambiente esterno della cellula da quello interno
BIOCHIMICA - canale 4
 DIPARTIMENTO DI CHIRURGIA GENERALE E SPECIALITÀ MEDICO-CHIRURGICHE Corso di laurea magistrale in Medicina e chirurgia Anno accademico 2016/2017-1 anno BIOCHIMICA - canale 4 BIO/10-5 CFU - 2 semestre Docente
DIPARTIMENTO DI CHIRURGIA GENERALE E SPECIALITÀ MEDICO-CHIRURGICHE Corso di laurea magistrale in Medicina e chirurgia Anno accademico 2016/2017-1 anno BIOCHIMICA - canale 4 BIO/10-5 CFU - 2 semestre Docente
SCIENZE BIOMEDICHE OBIETTIVI FORMATIVI
 DIPARTIMENTO DI SCIENZE MEDICHE, CHIRURGICHE E TECNOLOGIE AVANZATE G.F. INGRASSIA Corso di laurea in Tecniche di laboratorio biomedico Anno accademico 2016/2017-1 anno SCIENZE BIOMEDICHE 6 CFU - 1 semestre
DIPARTIMENTO DI SCIENZE MEDICHE, CHIRURGICHE E TECNOLOGIE AVANZATE G.F. INGRASSIA Corso di laurea in Tecniche di laboratorio biomedico Anno accademico 2016/2017-1 anno SCIENZE BIOMEDICHE 6 CFU - 1 semestre
Le membrane biologiche
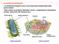 Le membrane biologiche Le membrane biologiche sono una componente fondamentale delle pareti cellulari Nelle cellule eucariotiche delimitano anche i compartimenti intracellulari (nucleo, mitocondri, ER,
Le membrane biologiche Le membrane biologiche sono una componente fondamentale delle pareti cellulari Nelle cellule eucariotiche delimitano anche i compartimenti intracellulari (nucleo, mitocondri, ER,
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
Esercitazione Esempi di domande del test intermedio
 Esercitazione Esempi di domande del test intermedio Materiale occorrente : Calcolatrice Penna Matita Righello Gomma Severamente vietato servirsi di libri, appunti, telefoni cellulari Quindi..!!!!! la legge
Esercitazione Esempi di domande del test intermedio Materiale occorrente : Calcolatrice Penna Matita Righello Gomma Severamente vietato servirsi di libri, appunti, telefoni cellulari Quindi..!!!!! la legge
Modulo 11 biosegnalazione
 Modulo 11 biosegnalazione La trasduzione del segnale Capacità di ricevere e rispondere a segnali esterni alla membrana è un processo fondamentale per la vita. Organismi pluricellulari si scambiano informazioni:
Modulo 11 biosegnalazione La trasduzione del segnale Capacità di ricevere e rispondere a segnali esterni alla membrana è un processo fondamentale per la vita. Organismi pluricellulari si scambiano informazioni:
LE MEMBRANE Le membrane sono composte da lipidi e proteine in composizioni che variano in base alla specie,al tipo cellulare e all organello.
 LE MEMBRANE Le membrane sono composte da lipidi e proteine in composizioni che variano in base alla specie,al tipo cellulare e all organello.il modello a mosaico fluido descrive la struttura comune a tutte
LE MEMBRANE Le membrane sono composte da lipidi e proteine in composizioni che variano in base alla specie,al tipo cellulare e all organello.il modello a mosaico fluido descrive la struttura comune a tutte
- lipidi strutturali, costituenti fondamentali delle membrane cellulari ed intracellulari (fosfolipidi, glicolipidi e colesterolo)
 I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
Nucleotidi 20/12/2013. Nucleotidi (1) Ribosio Vs. Desossirbosio
 I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
L insegnamento ha l obiettivo di far conseguire allo studente i seguenti risultati di apprendimento
 FACOLTÀ: Psicologia CORSO DI LAUREA: Scienze Biologiche INSEGNAMENTO: Biochimica CFU: 7 + 2 (Laboratorio) ANNO DI CORSO: Primo NOME DOCENTE: Paolo Scarpelli Indirizzo e-mail: paolo.scarpelli@uniecampus.it
FACOLTÀ: Psicologia CORSO DI LAUREA: Scienze Biologiche INSEGNAMENTO: Biochimica CFU: 7 + 2 (Laboratorio) ANNO DI CORSO: Primo NOME DOCENTE: Paolo Scarpelli Indirizzo e-mail: paolo.scarpelli@uniecampus.it
CHIMICA BIOLOGICA, LABORATORIO (gr.3) (prof.ssa P. Contursi) E METODOLOGIE BIOCHIMICHE (gr.3) (prof.ssa D. Limauro) Curriculum Molecolare
 CHIMICA BIOLOGICA, LABORATORIO (gr.3) (prof.ssa P. Contursi) E METODOLOGIE BIOCHIMICHE (gr.3) (prof.ssa D. Limauro) Corso di Studi in Biologia Generale ed Applicata Curriculum Molecolare CHIMICA BIOLOGICA,
CHIMICA BIOLOGICA, LABORATORIO (gr.3) (prof.ssa P. Contursi) E METODOLOGIE BIOCHIMICHE (gr.3) (prof.ssa D. Limauro) Corso di Studi in Biologia Generale ed Applicata Curriculum Molecolare CHIMICA BIOLOGICA,
Quando la sfingosina è legata ad 1 ac. grasso si forma il CERAMMIDE.
 SFINGOLIPIDI (costituenti delle membrane biologiche) Lo scheletro degli sfingolipidi è la SFINGOSINA (amminoalcol) con una lunga catena idrocarburica monoinsatura che parte dal C-3, gruppi OH legati in
SFINGOLIPIDI (costituenti delle membrane biologiche) Lo scheletro degli sfingolipidi è la SFINGOSINA (amminoalcol) con una lunga catena idrocarburica monoinsatura che parte dal C-3, gruppi OH legati in
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Concetti chiave Cascata ormonale Ormoni derivati da amminoacido Tirosina (catecolammine: adrenalina, noradrenalina, o.tiroidei) Ormoni peptidici e
 ORMONI Concetti chiave Cascata ormonale Ormoni derivati da amminoacido Tirosina (catecolammine: adrenalina, noradrenalina, o.tiroidei) Ormoni peptidici e proteici: -trasmettono il loro segnale legando
ORMONI Concetti chiave Cascata ormonale Ormoni derivati da amminoacido Tirosina (catecolammine: adrenalina, noradrenalina, o.tiroidei) Ormoni peptidici e proteici: -trasmettono il loro segnale legando
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Università degli Studi di Enna Kore Facoltà di Scienze dell Uomo e della Società
 Anno Accademico 2017 2018 A.A. Settore Scientifico Disciplinare CFU Insegnamento Ore di aula Mutuazione 2017/18 BIO/10-Biochimica 6 Biochimica dell Attività Motoria 36 No Classe Corso di studi Tipologia
Anno Accademico 2017 2018 A.A. Settore Scientifico Disciplinare CFU Insegnamento Ore di aula Mutuazione 2017/18 BIO/10-Biochimica 6 Biochimica dell Attività Motoria 36 No Classe Corso di studi Tipologia
Le funzioni delle membrane biologiche
 Modulo 9: Membrane Le funzioni delle membrane biologiche Membrane formano barriere fisiche. Separano il citosol dall ambiente esterno preservano l individualità della cellula mantenendola separata dall
Modulo 9: Membrane Le funzioni delle membrane biologiche Membrane formano barriere fisiche. Separano il citosol dall ambiente esterno preservano l individualità della cellula mantenendola separata dall
CPIA 1 FOGGIA punto di erogazione San Severo. Prof.ssa ANNA LUCIA L. CANCELLIERE
 CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA
 PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
Le proteine o protidi
 Le proteine o protidi A differenza di glucidi e lipidi (che di regola non contengono azoto), le proteine sono composti organici quaternari, che possiedono sempre atomi di azoto nella loro molecola (quasi
Le proteine o protidi A differenza di glucidi e lipidi (che di regola non contengono azoto), le proteine sono composti organici quaternari, che possiedono sempre atomi di azoto nella loro molecola (quasi
LIPIDI E MEMBRANE BIOLOGICHE
 Cap.8 LIPIDI E MEMBRANE BIOLOGICE Definizione (la parola deriva dal greco lípos, grasso): MOLECOLE INSOLUBILI IN ACQUA SOLUBILI NEI SOLVENTI ORGANICI NON POLARI Molecole con struttura chimica e funzioni
Cap.8 LIPIDI E MEMBRANE BIOLOGICE Definizione (la parola deriva dal greco lípos, grasso): MOLECOLE INSOLUBILI IN ACQUA SOLUBILI NEI SOLVENTI ORGANICI NON POLARI Molecole con struttura chimica e funzioni
Le membrane cellulari CORSO DI BIOLOGIA, PER OSTETRICIA
 Le membrane cellulari CORSO DI BIOLOGIA, PER OSTETRICIA LE MEMBRANE CELLULARI Sono costituite da Lipidi, Proteine e Carboidrati LE MEMBRANE CELLULARI Modello del mosaico fluido: il doppio strato lipidico
Le membrane cellulari CORSO DI BIOLOGIA, PER OSTETRICIA LE MEMBRANE CELLULARI Sono costituite da Lipidi, Proteine e Carboidrati LE MEMBRANE CELLULARI Modello del mosaico fluido: il doppio strato lipidico
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Liceo scientifico G.Castelnuovo Anno scolastico 2015/16 Programma svolto di Scienze Naturali Classe 2 L Docente D Agostino
 Liceo scientifico G.Castelnuovo Anno scolastico 2015/16 Programma svolto di Scienze Naturali Classe 2 L Docente D Agostino Chimica generale Concetto di materia Concetto di sostanza. Categorie di sostanze:pure
Liceo scientifico G.Castelnuovo Anno scolastico 2015/16 Programma svolto di Scienze Naturali Classe 2 L Docente D Agostino Chimica generale Concetto di materia Concetto di sostanza. Categorie di sostanze:pure
LE MEMBRANE CELLULARI
 LE MEMBRANE CELLULARI Sono strutture sovramolecolari che racchiudono e delimitano l ambiente intracellulare e negli eucarioti anche gli organuli citoplasmatici. Hanno funzione di Protezione. Sostegno.
LE MEMBRANE CELLULARI Sono strutture sovramolecolari che racchiudono e delimitano l ambiente intracellulare e negli eucarioti anche gli organuli citoplasmatici. Hanno funzione di Protezione. Sostegno.
