HerpeSelect 1 ELISA IgG (In Italiano)
|
|
|
- Orazio Durante
- 6 anni fa
- Visualizzazioni
Transcript
1 (In Italiano) HerpeSelect 1 ELISA IgG REF EL0910G Rev. K Enzyme-linked immunosorbent assay (ELISA) per il rilevamento di anticorpi umani di classe IgG anti HSV-1 Per Uso Diagnostico in vitro DESTINAZIONE D USO Il Focus Diagnostics HerpeSelect 1 ELISA IgG e un test indicato per l analisi qualitativa della presenza nel siero umano di anticorpi di classe IgG anti-hsv-1. Insieme con il Focus Diagnostics HerpeSelect 2 ELISA IgG, questo test e indicato per la diagnosi presuntiva di infezioni da HSV in adulti sessualmente attivi e in donne in stato di gravidanza. Il saggio può essere utilizzato in maniera manuale o insieme ad un sistema automatizzato, come indicato dall inserto nella confezione. L utilizzatore è responsabile delle caratteristiche d esecuzione, quando viene usato un sistema automatizzato. L uso di questo saggio non e stato testato per la popolazione pediatrica, per esami neonatali, per screening neonatale o per pazienti immunocompromessi. RIASSUNTO E SPIEGAZIONE DEL TEST L HSV e un patogeno diffuso in tutto il mondo e produce una grande varieta di malattie. L HSV infetta neonati, bambini e adulti; inoltre, dalla quarta decade d età, piu del 90% della popolazione adulta mostra la presenza di anticorpi anti-hsv. 1 La trasmissione dell HSV puo essere prodotta dal contatto con secrezioni infette di individui affetti, asintomatici o sintomatici. L herpes simplex e stato classificato in due sierotipi distinti: l HSV-1 e l HSV-2. L HSV-1 e generalmente associato ad infezioni alla lingua, alla bocca, alle labbra, alla faringe e agli occhi, mentre l HSV-2 e associato principalmente ad infezioni genitali e neonatali. Negli USA la maggioranza degli individui sessualmente attivi con ulcere genitali ha contratto l herpes genitale. 2 Le ulcere genitali sono state associate ad un aumento del rischio di infezioni da HIV. 2 L herpes genitale è solitamente causato dall HSV-2; in una minoranza di casi la prima infezione genitale (5 30 %) è dovuta all HSV-1. 2 Molti casi di herpes genitale sono trasmessi da persone che non sanno di essere infette o che non riconoscono sintomi lievi o atipici. I centri per il controllo e la prevenzione delle malattie (CDC) affermano che l informazione e un aspetto molto importante nella gestione di pazienti affetti da l herpes genitale. 2 Una delle conseguenze piu gravi dell herpes genitale e l herpes neonatale. 3 Senza terapia, il tasso di mortalita di bambini non curati che sviluppano l infezione supera il 70%, 3- e meta dei sopravvissuti riportano danni neurologici. Quasi tutte le infezioni neonatali da HSV-2 sono dovute al passaggio attraverso il canale del parto infetto. 2 La maggior parte delle madri (70%) che trasmette l HSV ai propri neonati e priva di sintomi al momento del parto. 5 Il rischio di trasmissione e piu elevato quando la madre e affetta da infezione genitale primaria o iniziale (>50%) 6, mentre il rischio e minore quando l infezione e ricorrente (<5%) 7-10 e quando la madre non sta ancora producendo anticorpi IgG anti-hsv. 8 I centri per il controllo e la prevenzione raccomandano che la prevenzione dell herpes neonatale deve essere favorita dalla prevenzione delle infezioni da HSV genitale durante la tarda gravidanza. Donne a rischio i cui partner sono affetti da HSV orale o genitale oppure non conoscono il loro stato infettivo, dovrebbero evitare contatti sessuali genitali e orali non protetti durante la tarda gravidanza. 2 Le madri sono a più alto rischio di contrarre un infezione genitale primaria o iniziale quando risultano sieronegative a uno o entrambi i tipi di HSV ed il loro partner e sieropositivo. 8 Le infezioni primarie da HSV-1 contratte attraverso il contatto diretto (principalmente non genitale) solitamente si sviluppano nella prima decade d età. Quando l infezione primaria e clinica, la classica presentazione della gengivostomatite erpetica e costituita da una seria infezione delle gengive, della bocca, della lingua, della faccia e/o della faringe.l infezione HSV-1,dovuta alla riattivazione del virus, e ricorrente nella forma herpes labialis (vesciche o febbri) o herpes oculare che si sviluppa in piu del 0% degli individui HSV-1 sieropositivi. 9 Una precedente infezione da HSV-1 orale non protegge dall infezione da HSV-2 genitale. 9 Le infezioni primarie da HSV-2, solitamente contratte con contatti sessuali, sono raramente presenti prima dell inizio dell attivita sessuale. Quando l infezione primaria da HSV-2 e clinica, si manifesta nella forma classica di herpes genitale, caratterizzata da lesioni distribuite in entrambi i genitali e accompagnata da febbre, linfadenopatia e disuria. Le infezioni da HSV-2 causano circa l 85% dei casi sintomatici di HSV genitale, le rimanenti infezioni sono da HSV-1. 3 Poichè e difficile che l HSV-1 produca infezioni genitali ricorrenti, il 99% dei casi di herpes genitale ricorrente e dovuto all HSV-2. 3 Dopo l infezione primaria da HSV-1, il virus colonizza i neuroni sensoriali e l infezione latente può riattivarsi causando infezioni sub-cliniche o cliniche. Poiche le infezioni ricorrenti possono essere sub-cliniche e asintomatiche, il virus silente e una significativa riserva per la trasmissione del virus 1 e, quindi, sono possibili inattese trasmissioni del virus difficili da prevenire. 3 L isolamento del virus, il test di direct fluorescent antibody (DFA), e la sierologia possono essere utilizzate per diagnosticare infezioni da HSV. Le colture positive e la DFA sono le metodiche piu sicure; inoltre, l isolamento del virus permette di classificare il virus stesso. Comunque, la DFA e le colture presentano diversi svantaggi, tra cui la durata del tempo della coltura, la collezione del campione, le difficolta di trasporto e la complessità delle procedure. 1-2 La maggior parte dei metodi sierologici per testare lo stato dell HSV usano lisati virali come antigeni. Inoltre, a causa della significativa cross-reattivita tra l HSV-1 e l HSV-2, i saggi che utilizzano lisati virali non sono in grado di distinguere tra le infezioni da HSV-1 e quelle da HSV-2. 3 Poiche molti adulti hanno avuto una precedente infezione da HSV-1, spesso senza sintomi primari o ricorrenti, e spesso impossibile determinare con sicurezza lo stato del siero per l HSV-2 se si usa un saggio basato sul lisato virale. 3 Recentemente, sono stati prodotti alcuni saggi sierologici HSV tipo-specifici basandosi sulla differenza significativa tra la proteina gg-1 dell HSV-1 e la proteina gg-2 dell HSV-2. 3 Il test ELISA della Focus Diagnostics utilizza come antigene proteine ricombinanti purificate tipospecifiche gg-1 immobilizzate su pozzetti di polistirene. PRINCIPIO DEL SAGGIO Nel saggio ELISA IgG Focus Diagnostics HerpeSelect 1, i pozzetti di polistirene sono rivestiti con l antigene ricombinante gg-1. I campioni di siero diluiti e i controlli sono incubati nei pozzetti per permettere all anticorpo specifico, presente nei campioni, di reagire con l antigene. I ligandi non specifici sono rimossi dai lavaggi; quindi viene aggiunto l anticorpo anti-igg umana coniugato con la perossidasi di rafano, che reagisce con le IgG specifiche. L eccesso di anticorpo coniugato e rimosso dai lavaggi. Si aggiunge il substrato dell enzima e il cromogeno e si lascia sviluppare il colore. Dopo avere aggiunto la reazione di stop, l intensità del colore viene quantificata con uno spettrofotometro leggendo la densità ottica (OD). Le letture della densità ottica dei diversi campioni vengono paragonate con i riferimenti delle letture dei cut-off per valutare i risultati.
2 Pag. 2 MATERIALE FORNITO Il Kit Focus Diagnostics HerpeSelect 1 ELISA IgG contiene materiale sufficiente per 96 determinazioni. Portare i reagenti a temperatura ambiente prima di utilizzarli. Una volta aperti, tutti i materiali vanno conservati tra i 2 e gli 8 C fino alla data di scadenza presente sull etichetta. 96 pozzetti rivestiti con l antigene Ag Antigen Wells, 96 wells REF EL strisce da 8 pozzetti di polistirene. Ogni pozzetto e rivestito con l antigene gg-1 ricombinante (peso molecolare di 3 5 kilodaltons). Ogni striscia puo essere divisa in pozzetti singoli per un uso efficiente. Prima di aprire i pacchetti sigillati con le strisce si consiglia di lasciarli riposare a temperatura ambiente, per evitare la formazione di condensa. IgG coniugate,16 ml CONJ IgG IgG Conjugate, 16 ml REF EL0916 Una vial di anticorpi di capra anti IgG umana (specifici per la catena pesante) purificati per affinita e coniugati con perossidasi di rafano. Contiene proteine, tampone e conservanti non azidici. IgG Controllo fortemente positivo, 0,3 ml CONTROL ++ IgG High Positive Control, 0.3 ml REF EL0905 Una vial di siero umano per ogni livello di controllo. Contiene conservante. Deve essere diluita prima dell uso (vedi il paragrafo sottostante: Campioni, Controlli e Calibrazioni preparatorie). IgG Controllo debolmente positivo, 0,3 ml CONTROL + IgG Low Positive Control, 0.3 ml REF EL0906 Una vial di siero umano per ogni livello di controllo. Contiene conservante. Deve essere diluita prima dell uso (vedi il paragrafo sottostante: Campioni, Controlli e Calibrazioni preparatorie). Controllo negativo, 0,3 ml CONTROL Negative Control, 0.3 ml REF EL090 Un vial di siero umano per ogni livello di controllo. Contiene 0,1% sodio azide come conservante. Deve essere diluita prima dell uso (vedi il paragrafo sottostante: Campioni, Controlli e Calibrazioni preparatorie). IgG Cut-Off Calibratore, 0,3 ml CONTROL CAL IgG Cut-Off Calibrator, 0.3 ml REF EL0903 Un vial di siero umano per ogni livello di controllo. Contiene 0,1% sodio azide come conservante. Deve essere diluita prima dell uso (vedi il paragrafo sottostante: Campioni, Controlli e Calibrazioni preparatorie). Diluente per i campioni, 100 ml DIL SPEC HerpeSelect ELISA Sample Diluent, 100 ml REF EL0928 Una vial di proteine, detergente, e PBS con conservanti non azidici. Stabile tra i 2 e gli 8 C fino alla data di scadenza presente sull etichetta. Lasciare a temperatura ambiente prima dell uso. 10x Tampone di lavaggio, 100 ml BUF WASH 10X Wash Buffer, 100 ml REF EL005 Una vial di PBS contenente detergente con conservanti non azidici. Diluire ad 1X prima dell uso. Per preparare una soluzione 1X di tampone di lavaggio, miscelare 100 ml di 10X tampone di lavaggio con 900 ml di acqua distillata (o deionizzata) e dissolvere tutti i cristalli. Si raccomanda l uso di acqua purificata della massima qualità. E stato osservato che alcuni tipi di acqua deionizzata contengono residui che possono interferire con il saggio. Agitare bene fino a quando la soluzione e ben miscelata e i cristalli sono dissolti. Substrato, 16 ml SUBS TMB Substrate Reagent, 16 ml REF EL0009 Una vial di tetrametilbenzidina (TMB) e perossido di idrogeno in tampone. Un colore blu scuro indica contaminazione con perossidasi; in questo caso usare una bottiglia nuova. Soluzione di stop, 16 ml SOLN STOP Stop Reagent, 16 ml REF El0105 Una vial di acido solforico 1 M. Nastro sigillante Due fogli di nastro sigillante. MATERIALI RICHIESTI MA NON FORNITI 1. acqua distillata o deionizzata. 2. spruzzette da 250 o da 500 ml o un apparecchio per il lavaggio automatico delle piastre. 3. cilindro graduato da 1 L. 12 x 75 mm provette di vetro di borosilicato o equivalenti. 5. pipette da 10 L a 100 L con puntali monouso (per saggi con piu di 8 pozzetti si consiglia l uso di una pipetta da 100 L con 8 canali). 6. pipetta da 1 ml o erogatore. 7. pipetta da 5 ml. 8. timer. 9. carta da banco o carta assorbente. 10. lavandino. 11. vortex o equivalente. 12. spettrofotometro per piastre ELISA, lungezza d onda = 50 nm. 13. processore ELISA automatizzato (facoltativo). VALIDITA E CONSERVAZIONE 1. I kit ed i reagenti sono validi fino alla fine del mese indicato sull etichetta se conservati tra i 2 e gli 8 C. 2. Non utilizzare il kit o i reagenti del kit dopo la data di scadenza. 3. Non esporre a luce intensa durante la conservazione e l incubazione.
3 Pag. 3. Portare i reagenti a temperatura ambiente prima dell uso. AVVERTENZE E PRECAUZIONI 1. Questo kit e destinato solo ad un uso diagnostico in vitro. 2 Tutti i derivati del sangue devono essere maneggiati come potenzialmente infetti. I materiali da cui questo prodotto (compresi i controlli) deriva sono stati testati per l antigene di superficie dell epatite B, per l antigene dell epatite C e per gli anticorpi dell HIV-1/2 (AIDS) con metodiche approvate dal FDA e sono risultati negativi. Comunque, poiche nessun test puo escludere al 100% che i prodotti derivati da sangue umano non trasmettano questi o altri agenti infettivi, tutti i controlli, i campioni di siero e gli oggetti che entrano in contatto con questi campioni devono essere considerati potenzialmente infetti e quindi decontaminati o eliminati secondo le disposizioni per i rifiuti contaminati. I Centers for Disease Control and Prevention e i National Institutes of Health raccomandano che la manipolazione degli agenti potenzialmente infetti venga eseguita al livello di biosicurezza 2. 12,18 3. I pozzetti con l antigene sono prodotti con antigeni gg-1 ricombinante. Dopo avere aggiunto i campioni dei pazienti o i controlli, le strisce devono essere considerate potenzialmente infette e trattate di conseguenza.. Sodio azide ad una concentrazione dello 0,1% e stato aggiunto ad alcuni reagenti come agente antibatterico. Per evitare la formazione di metalli azidici esplosivi nelle tubature di piombo e rame, questi reagenti (vedi il soprastante paragrafo Materiali Forniti) devono essere eliminati nelle fogne solo se diluiti con abbondante quantita di acqua. Dove possibile, si raccomanda l uso di scarichi privi di rame e di piombo. Occasionalmente si consiglia di decontaminare lo scarico con sodio idrossido (ATTENZIONE: caustico), lasciandolo agire per 10 minuti e facendo poi scorrere molta acqua. 5. Non sostituire o mescolare reagenti di kit differenti o di altri fornitori. 6. Seguire solo i protocolli descritti in questo inserto. Tempi di incubazione o temperature diverse da quelle specificate possono falsare i risultati. 7. Cross-contaminazioni di campioni di pazienti diversi possono anch esse falsare i risultati. Aggiungere i campioni e maneggiare le strisce attentamente, per evitare di mescolare i sieri di pozzetti adiacenti nella piastra. Versare attentamente. 8. La contaminazione batterica dei campioni di siero o dei reagenti puo falsare i risultati. Usare metodiche asettiche per evitare contaminazioni. 9. Effettuare il saggio a temperatura ambiente (20 25 C). 10. Usare le pipette nel modo corretto e nella stessa maniera durante tutta la procedura, per favorire la correttezza e la riproducibilita dei valori. 11. La soluzione di stop contiene acido solforico. Non mettere a contatto con la pelle o gli occhi. Se esposti al contatto, sciacquare con molta acqua. COLLEZIONE DEI CAMPIONI E PREPARAZIONE Il siero e il materiale usato per il saggio. Non e stata valutata la compatibilita del saggio con altri campioni. Sieri iperlipidici, inattivati con il calore, emolizzati o contaminati possono falsare i risultati, percio non devono essere utilizzati. Collezione dei campioni e maneggiamento Il sangue deve essere raccolto asetticamente da personale qualificato tramite venipunture. 12 Lasciare coagulare il campione a temperatura ambiente prima di centrifugarlo. Trasferire asetticamente il siero in un contenitore ben chiuso per la conservazione. Il siero separato non deve rimanere a 22 C per piu di 8 ore. Se non si intende portare a termine il saggio prima dello scadere delle 8 ore, refrigerare il campione a 2 8 C. Se il saggio non viene portato a termine prima delle 8 ore e se i campioni devono essere spediti, congelare a 20 C o a temperature inferiori. Scongelare e mescolare bene i campioni prima dell uso. Campioni, controlli e preparazione della calibrazione Diluire ogni campione, controllo e calibratore 1:101. Per esempio, segna le provette e versa 1 ml di diluente in ogni provetta. Aggiungi 10 L di campione, controllo o calibratore in ogni provetta contenente 1 ml di diluente, quindi mescola bene usando il vortex. PROCEDURA PER IL TEST 1. Portare tutti i reagenti a temperatura ambiente prima dell uso. Rimuovere il pacchetto con i pozzetti con l antigene dal posto freddo dove sono conservati. Per evitare la condensa, prima di aprire i pacchetti sigillati con le strisce di pozzetti si consiglia di lasciarli riposare a temperatura ambiente. Se la piastra non viene completamente utilizzata, rimettere le strisce nel pacchetto con dessicante e sigillare completamente. Conservare i pozzetti non utilizzati tra i 2 e gli 8 C (Nota bene: alla fine del saggio conservare il supporto per l utilizzo delle rimanenti strisce). 2. Ammollo FACOLTATIVO di 5 minuti. Se si tralascia l ammollo, andare al Passaggio 3. Riempire i pozzetti con il tampone di lavaggio 1X e tenere a bagno per 5 minuti. Travasare (o aspirare) i pozzetti dell antigene e lavare energicamente con acqua corrente per rimuovere il tampone di lavaggio 1X. Tamponare i pozzetti dell antigene vuoti, a faccia in giù, su salviette di carta pulita o su carta assorbente, per rimuovere ogni traccia del tampone di lavaggio 1X. 3. Pipettare 100 L del diluente nel pozzetto usato come bianco e 100 L di campione diluito, controllo o calibratore (vedi il capoverso soprastante Campioni, controlli e preparazione della calibrazione) nei pozzetti appropriati. (Nota bene: per saggi con piu di 8 pozzetti si consiglia di pipettare 250 L di ogni campione diluito in una micropiastra vuota nella posizione corrispondente a quella del pozzetto per l ELISA. Quindi i campioni possono essere facilmente trasferiti nei pozzetti con l antigene con una pipetta mulicanale da 100 L con 8 o 12 canali).. Sigillare i pozzetti con parafilm (o tenerli in una camera umidificata), e incubarli per 60 ± 1 minuti a temperatura ambiente (20 25 C). 5. Rimuovere il parafilm (o rimuovere i pozzetti dalla camera umida) e svuotare il contenuto dei pozzetti nel lavandino o in un contenitore per i rifiuti liquidi. 6. Riempire ogni pozzetto con un leggero spruzzo di soluzione di lavaggio con una spruzzetta, quindi svuotare il contenuto dei pozzetti nel lavandino o in un contenitore per i rifiuti. 7. Ripetere il lavaggio (passaggio 6) per altre 2 volte. 8. Battere vigorosamente sul bancone da lavoro i pozzetti per rimuovere la soluzione di lavaggio. Trasferire i pozzetti faccia in giù su carta da banco o carta assorbente per rimuovere i residui della soluzione di lavaggio. 9. Pipettare 100 L di coniugato in tutti i pozzetti usando una multipipetta da 100 l con 8 o 12 canali. 10. Sigillare i pozzetti con parafilm (o tenerli in una camera umidificata), e incubarli per 30 ± 1 minuti a temperatura ambiente (20 25 C). 11. Ripetere i lavaggi dal punto 5 al Pipettare 100 L di substrato in tutti i pozzetti, usando una pipetta multicanale da 100 L con 8 o 12 canali. Iniziare a misurare il tempo di incubazione partendo dall aggiunta del substrato al primo pozzetto. (Nota bene: non versare il substrato nello stesso modo usato per il coniugato). 13. Incubare per 10 ± 1 minuti a temperatura ambiente (20 25 C). 1. Bloccare la reazione aggiungendo a tutti i pozzetti 100 L di soluzione di stop utilizzando una pipetta multicanale da 100 L con 8 o 12 canali. Aggiungere la soluzione di stop nella stessa sequenza e con la stessa velocita usate nell aggiunta del substrato. Nei pozzetti positivi, il colore deve virare dal blu al giallo. 15. Asciugare con delicatezza i bordi esterni dei pozzetti con carta assorbente per rimuovere gocce che potrebbero interferire con la lettura allo spettrofotometro. Non sfregare con la carta assorbente perche potrebbe graffiare la superficie ottica del pozzetto. (Nota bene: le grosse bolle sulla superficie della soluzione possono influire sulle letture OD). 16. Misurare l assorbanza di ogni pozzetto entro un ora da quando la reazione e stata bloccata. Settare lo spettrofotometro per piastre ad una lunghezza d onda di 50 nm. Azzerare lo strumento con i pozzetti bianchi, o correggere tutte le OD manualmente sottraendo le letture dei bianchi.
4 Pag. CONTROLLO QUALITA Nel test di ogni piastra (o striscia o pozzetti della stessa piastra) includere il calibratore e i tre controlli. Se vengono usate diverse piastre nello stesso saggio, includere il calibratore e i tre controlli in ogni piastra. Si raccomanda che, fino a quando l utente non abbia familiarizzato con il kit, tutti i campioni, i controlli e i calibratori vengano analizzati in duplicati con il calibratore analizzato due volte per un totale di quattro pozzetti. Se vengono usati singoli pozzetti, i calibratori devono essere analizzati in triplice copia, includendo almeno un pozzetto bianco (contenente solamente diluente) al fine di calibrare lo strumento. I calibratori sono stati pensati per evidenziare nel modo migliore la differenza tra i sieri negativi e quelli positivi. Benche il valore dell assorbanza puo differire tra i singoli test e tra differenti laboratori, il valore medio dei pozzetti calibratori deve essere tra 0,100 e 0,700 unita OD. Tutte le repliche dei calibratori non devono differire dal valore medio per piu di 0,10 unita OD. Riportare i risultati relativi ai calibratori come valori indice. Per calcolare i valori indice, dividere i valori della densita ottica (OD) dei campioni per la media dei valori dell assorbanza dei calibratori. 1. Il valore indice del controllo altamente positivo deve essere maggiore di 3,5. 2. I valori indice del controllo debolmente positivo devono essere compresi tra 1,5 e 3,5. 3. I valori indice del controllo negativo devono essere inferiori a 0,8. Nel caso il calibratore o i controlli non siano conformi a questi parametri, i risultati del test del paziente devono essere considerati non validi e il test deve essere ripetuto. Lo scopo dei controlli negativi e positivi e valutare che i reagenti non siano malfuzionanti. Il controllo positivo non deve essere usato come un cut-off ma solo per assicurare la funzionalita dei reagenti. I calibratori e i controlli possono essere sintetizzati usando gli stessi lotti di materie prime. Controlli ulteriori possono essere effettuati secondo l indicazione o i requisiti locali, statali e/o di regolamenti federali o di organizzazioni accreditate. INTERPRETAZIONE DEI RISULTATI DEL TEST Riportare i risultati dei pazienti come Valori Indice relativi ai calibratori: per calcolare i Valori Indice, dividere i valori della densita ottica (OD) dei campioni per la media dei valori dell assorbanza dei calibratori. > 1.10 Positivo. Un valore indice >1,10 e presuntivo della presenza di anticorpi IgG anti HSV-1. < 0.90 Negativo. Un valore indice <0,90 indica che non sono stati trovati anticorpi IgG anti HSV e 1.10 Equivoco. Un valore indice 0,90 ma 1,10 e considerato un risultato equivoco. Questi campioni devono essere riesaminati. Se nella ripetizione del test il risultato rimane equivoco, un secondo prelievo deve essere fatto diverse settimane dopo per valutare un aumento del titolo degli anticorpi IgG. 1,15 In alternativa, il campione puo essere analizzato usando una metodica diversa come il western blot 1. Tutti i risultati di questo e di altre sierologie devono essere correlati ad un quadro clinico, a dati epidemiologici e ad altri dati a disposizione del medico curante per la valutazione del paziente. 2. La prevalenza dell infezione puo falsare la validita diagnostica del test. 3. Come riportato per altri test sierologci, risultati negativi non escludono la presenza della malattia herpes simplex. Il tempo necessario al siero per produrre anticorpi al seguito di un'infezione primaria varia negli individui, il campione può essere infettato prima della comparsa degli anticorpi rilevabili. 15 Sono noti casi di siero-reversione. 15,16 Quando appropriato, per esempio in casi di recente infezione da herpes simplex, il test deve essere ripetuto o eseguito con un saggio differente. 2,1 Se nel nuovo test, il risultato rimane negativo, il test deve allora essere ripetuto con un secondo campione dopo 12 settimane. 1,15. Si possono avere falsi negativi quando il virus infettante e gg deficiente, poiche non e riconosciuto se l antigene del saggio è glicosilato come le cellule di mammifero. Liljekvist ha dimostrato che circa lo 0,2% (5/200) degli HSV-2 isolati sono gg deficienti Come in altri test sierologici, si possono presentare falsi positivi. Si consiglia la ripetizione del test o l uso di un diverso tipo di test in alcune situazioni, come per esempio pazienti con una bassa possibilità di infezione da HSV. 2,1 6. Un singolo caso positvo indica che precedentemente e avvenuta una esposizione immunologica; il livello di risposta anticorpale o la classe degli anticorpi prodotti non puo essere usato per determinare l attivita dell infezione o lo stadio 7. L ampiezza del valore indice al di sopra del calibratore non indica la quantita totale di anticorpi presente. 8. La sierologia non distingue tra infezioni orali o genitali. Quando necessario, si raccomanda la cultura per individuare l'origine dell'infezione. Comunque, può accadere che le culture producano falsi negativi per l'hsv, specialmente in pazienti con infezioni ricorrenti o con lesioni in via di guarigione 2. LIMITI DI APPLICAZIONE 1. L uso di questo saggio non e stato previsto per persone non qualificate. 2. L uso di questo saggio non e stato progettato per escludere la presenza di malattie con sintomi simili, e.g., Candida albicans, specie Bacteriodi, G. vaginali e differenti specie di Mobiluncus. Si consiglia invece, l uso di colture o metodiche appropriate. 3. L uso di questo saggio non e` adatto per matrici differenti dal siero, per la determinazione visiva di risultati o per il monitoraggio della terapia HSV-1. VALORI ATTESI Un tecnico ha valutato il saggio con sieri mascherati, archiviati e non selezionati da 1) adulti sessualmente attivi con eta superiore ai 1 anni (n = 26) e 2) da donne gravide (n = 21). Il metodo di riferimento e il Western blot di una universita del nord ovest del Pacifico. La prevalenza osservata e i valori ipotetici previsti per le due popolazioni sono mostrati nelle tabelle sottostanti. I valori positivi previsti diminuiscono proporzionalmente con la prevalenza dell infezione HSV come mostrato nella tabella sottostante. Per i calcoli si considera che Focus Diagnostics HerpesSelect 1 ELISA IgG ha 1) un ipotetica sensibilita del 91,2% & un ipotetica specificita del 92,3% (adulti sessualmente attivi) e 2) un ipotetica sensibilta del 96,0% e un ipotetica specificita del 95,2% (donne gravide). Prevalenza osservata in adulti sessualmente attivi e donne gravide Popolazione HSV-1 Stato del siero Prevalenza osservata WB Focus ELISA Adulti sessualmente attivi* neg 2.9% (105/25) 1.2% (101/25) % (137/25) 56.7% (139/25) Donne gravide neg 25.7% (62/21) 22.% (5/21) % (178/21) 75.5% (182/21) * Esclusi 3 western blot atipici e 2 ELISA equivoche. Esclusi 1 western blot atipico e 1 ELISA equivoca.
5 Pag. 5 Valori della prevalenza Prevalenza Adulti sessualmente attivi Donne gravide PPV NPV PPV NPV 50% 92.2% 92.3% 95.2% 95.2% 0% 88.8% 9.7% 93.0% 96.7% 30% 83.5% 96.5% 89.6% 97.9% 25% 79.8% 97.3% 87.0% 98.3% 20% 7.8% 98.0% 83.3% 98.8% 15% 67.6% 98.5% 77.9% 99.1% 10% 56.8% 99.1% 69.0% 99.% 5% 38.% 99.6% 51.3% 99.7% Nota: Popolazioni di adulti sessualmente attivi e madri gravide in differenti aree geografiche possono produrre una differente distribuzione della frequenza. Ogni laboratorio dovrebbe stabilire la distribuzione di frequenza per la propria specifica popolazione di pazienti. CARATTERISTICHE DELLE PRESTAZIONI Cut-off Calibratore Cuando se diseñó el ensayo, el Límite fue validado usando cinco paneles de suero (n = 383) para inicialmente evaluar el rendimiento: 1) muestras de laboratorio clínico (n = 9); 2) muestras de laboratorio clínico que eran negativas por screening ELISAs (n = 37); 3) muestras de laboratorio clínico con reactividades en Western blot o inmunoblot insólitas (n = 32); ) Muestras del clínico español de ETS (n = 159); y 5) Muestras de la universidad Pacific Northwest (n = 61). El método de referencia fue el Western blot de VHS-1 de un laboratorio clínico licenciado. Excluyendo dos Western blots atípicos, el ELISA de IgG contra HSV-1 ELISA IgG de Focus y el Western blot concordaron en el 95.1% (116/122) de los positivos y en el 93.8% (23/259) de los negativos. De las dos muestras que resultaron atípicas por Western blot, una resultó ser negativa y la otra positiva por el ELISA. Sensibilita relativa e specificita relativa per le donne gravide Un tecnico esterno ha testato la sensibilita relativa e la precisione relativa del sistema con sieri di donne gravide (n = 21). In sequenza i sieri sono stati mandati al laboratorio, archiviati e mascherati. Il metodo di riferimento e l HSV-1 Western blot (WB) di una univerista del nord-ovest del Pacifico. Dei 178 WB positivi, per l ELISA 170 erano positivi, 7 negativi e 1 equivoco. Dei 62 WB negativi per l ELISA 59 erano negativi e 3 positivi. L unico atipico per WB era negativo per l ELISA. Sensibilita relativa e precisione relativa per donne gravide (n =21) Caratteristica % (EL/WB)* 95% CI Sensibilita relativa al Western blot 96.0% (170/177) % Precisione relativa al Western blot 95.2% (59/62) % * Escluso un Western blot atipico e un ELISA equivoco. questo saggio con la presenza o assenza Non puo essere fatta nessuna valutazione sull accuratezza dell altro saggio simile nella predizione Sensibilta relativa e precisione relativa per gli adulti sessualmente attivi Un tecnico esterno ha testato la sensibilita relativa e la precisione relativa del sistema con sieri di adulti sessualmente attivi con piu di 1 anni di eta (n = 26). I sieri sono stati mandati in successione al laboratorio, archiviati e mascherati. Il metodo di riferimento e l HSV-1 Western blot (WB) di una universita del nord-ovest del Pacifico. Dei 138 WB positivi, per l ELISA 125 erano positivi, 12 negativi e 1 equivoco. Dei 105 WB negativi per l ELISA 96 erano negativi, 8 positivi e uno equivoco. Dei 3 WB atipici, per l ELISA uno era negativo e due positivi. Sensibilta relativa e precisione relativa per gli adulti sessualmente attivi Caratteristica % (EL/WB)* 95% CI Sensibilita relativa al Western blot 91.2% (125/137) % Precisone relativa al Western blot 92.3% (96/10) % * Esclusi 3 Western blot atipici e 2 ELISA equivoci. questo saggio con la presenza o assenza Non puo essere fatta nessuna valutazione sull accuratezza dell altro saggio simile nella predizione Sensibilita relativa per colture positive Un tecnico esterno ha testato la sensibilita relativa e la precisione relativa del sistema con sieri di pazienti con colture positive ( n = 38 ). Il metodo di riferimento comprende la coltura (infezioni) e l HSV-1 Western blot (anticorpi) di una univerista del nord-ovest del Pacifico. Delle 38 colture positive: 1) il WB era negativo per 37 casi e positivo per uno e 2) l ELISA era positivo per 30 casi e negativo per 8. Dei 38 WB positivi, l ELISA era positivo in 30 casi e negativo per 7. Sensibilita relativa per le colture (n = 38) Caratteristica % (EL/WB o Colture) 95% CI Sensibilita relativa alla coltura 78.9% (30/38) % Precisione relativa al Western Blot 81.1% (30/37) % questo saggio con la presenza o assenza Non puo essere fatta nessuna valutazione sull accuratezza dell altro saggio simile nella predizione Confronti con le tabelle del CDC Le seguenti informazioni derivano da tabelle di sieri del CDC e testate dalla Focus Diagnostics. I risultati sono presentati come medie per esprimere ulteriori informazioni sulle prestazioni di questo saggio con un gruppo di sieri mascherati e caratterizzati. Questo non implica l approvazione da parte del CDC. Il gruppo consiste di campioni positivi nel 59% dei casi e negativi per nel 1% dei casi. Focus Diagnostics HerpeSelect 1 ELISA IgG ha mostrato di essere in accordo con il CDC nel 96% dei casi. Dei risultati ottenuti dalla Focus Diagnostics, c e una concordanza con il 93,1% dei casi positivi e del 100% con quelli negativi. Sensibilita relativa con una popolazione a bassa prevalenza Un tecnico esterno ha testato la sensibilita relativa e la precisione relativa del sistema con sieri di studenti di college che hanno dichiarato di non avere avuto rapporti sessuali (n = 81) e avendo una prevalenza di anticorpi anti HSV-1 del 26,9% (50/186). 13 Il metodo di riferimento e l HSV-1 Western blot di una univerista del nord-ovest del Pacifico. Dei 57 WB negativi, per l ELISA 55 erano negativi, 1 positivo e 1 equivoco. Dei 2 WB positivi, per l ELISA 18 erano positivi e 6 negativi.
6 Pag. 6 Sensibilita relativa con una popolazione a bassa prevalenza (n = 81) Caratteristica % (EL/WB)* 95% CI Sensibilita relativa al Western blot 98.2% (55/56) % Precisione relativa al Western blot 75.0% (18/2) % * Escluso un ELISA equivoco. questo saggio con la presenza o assenza Non puo essere fatta nessuna valutazione sull accuratezza dell altro saggio simile nella predizione Tipo specificita con western blot HSV-2 positivi Un tecnico esterno ha testato la sensibilita relativa e la precisione relativa del sistema con sieri della popolazione sopra descritta con HSV-2 positivi al Western blot e HSV-1 negativi al Western blot (n = 90): donne gravide, adulti sessualmente attivi, individui con bassa prevalenza e colture HSV-2 positive. Dei 90 HSV-2 positivi e HSV-1 negativi al WB, per l ELISA 82 erano negativi e 8 positivi. Tipo specificita con western blot HSV-2 positivi (n = 90) Caratteristica % (EL/WB) 95% CI Tipo-specificita relativa al WB 91.1% (82/90) % Tipo cross-reattivita relativa al WB 8.9% (8/90) % questo saggio con la presenza o assenza Non puo essere fatta nessuna valutazione sull accuratezza dell altro saggio simile nella predizione Cross-reattivita con virus tassonominamente simili Focus ha valutato la cross-reattivita usando sieri (n = 26) che erano 1) HSV siero-negativi secondo il test ELISA di un altra ditta autorizzata dalla FDA e 2) IFA IgG positivi per virus tassonominalmente simili: CMV, EBV VCA, HHV6 e VZV. Discrepanze tra i risultati dell ELISA della ditta autorizzata dalla FDA e quelli delle apparecchiature Focus sono stati analizzati con uno specifico Western blot da una grossa universita situata nel nord ovest degli Stati Uniti. Escludendo un risultato equivoco per l ELISA Focus il quale non e stato analizzato con il Wstern blot perche il volume era insufficiente, i risultati sono i seguenti: Cross-reattivita con virus tassonomicamente simili IFA IgG Pos % Focus EL Neg (n/n) 95% CI CMV 100% (12/12) % EBV VCA 100% (2/2) % HHV6 100% (2/2) % VZV 100% (23/23) % Totale 100% (83/83) % Riproducibilita intra-saggio ed inter-saggio Un tecnico interno ha valutato la riproducibilita intra-saggio e inter-saggio del test analizzando sette campioni in duplicato, due volte al giorno per 20 giorni, per un totale di 0 corse. Due serie di campioni erano duplicati mascherati Riproducibilita all interno dello stesso lotto Un tecnico interno ha valutato la riproducibilita all interno dello stesso lotto. Sono stati analizzati sette campioni in duplicato in parallelo con tre lotti differenti. Ognuno dei tre lotti aveva almeno un lotto differente per i pozzetti con l antigene. Riproducibilita tra laboratori diversi Un tecnico interno e due laboratori esterni hanno valutato la riproducibilita del saggio. Ognuno dei tre laboratori ha analizzato sette campioni in triplicato in tre giorni differenti. Riproducibilita Inter- & Intra-saggio Inter-lotto Inter-laboratorio Campione Indice medio Intra-saggio %CV Inter-saggio %CV Indice medio Indice %CV Indice medio Media del Lab %CVs %CV medie del Lab 11* % 50.% % % 70.9% 16* % 11.6% % % 63.1% 12** % 7.0% % % 7.0% 17** % 5.% % %.3% %.9% % % 5.7% % 6.5% % % 7.5% % 5.6% % % 6.6% * #11 & #16 sono duplicati mascherati. ** #12 & #17 sono duplicati mascherati. % Accordo tra i Metodi Manuale e Automatizzato Un investigatore interno ed uno esterno hanno analizzato la % di accordo tra il metodo automatizzato HerpeSelect ed il metodo manuale, durante il porcesso CLIA di validazione per un importante laboratorio situato nella California del Sud.L investigatore esterno ha selezionato in maniera sequenziale e testato poi manualmente 28 campioni. Ciascun campione proveniva da un individuo adulto ed è stato sottoposto al test per l HSV. 26 campioni provenivano dagli Stati Uniti e 2 campioni da paesi stranieri. Di questi 28 campioni, il metodo manuale ha identificato 108 negativi, 3 equivoci e 137 positivi. Dei 108 negativi al test manuale, il metodo automatizzato ne ha confermati il 98.1% (106/108). Dei 3 equivoci al test manuale, il 66.7% è stato confermato dal metodo automatizzato (2/3). Dei 137 postivi al metodo manuale, il metodo automatizzato ne ha confermati il 97.8% (13/137). In totale, i due metodi hanno dato risultati in accordo al 97.6% (22/28). Dei 5 campioni in disaccordo, 3 si sono risolti in favore del metodo automatizzato, mentre gli altri due non hanno avuto risoluzione.
7 Pag. 7 % Accordo tra i Metodi Manuale e Automatizzato Interpretazione* % Accordo 95% CI Negativo 98.1% (106/108) % Equivoco 66.7% (2/3) % Positivo 97.8% (13/137) % Totale 97.6% (22/28) % * Interpretazione tramite metodo manuale. Riproducibilità utilizzando uno strumento automatizzato Un investigatore interno ha valutato la riproducibilità inter- ed intra- saggio dll apparecchio, utilizzando uno strumento automatizzato. 10 campioni sono stati analizzati in triplicato, in 3 giorni diversi. Il metodo manuale e quello automatizzato sono risultati in accordo al 98.9% (87/90). Riproducibilità utilizzando uno strumento automatizzato Campione Indice Medio %CV Intra-saggio %CV Inter-saggio Stabilità dopo apertura dei reagenti Un investigatore interno ha valutato la stabilità dei reagenti, una volta aperti. Il kit era stato utilizzato nello studio di riproducibilità inter- ed intra-saggio (vd. sopra), richiuso, conservato a 2 8 C per almeno 30 giorni e quindi utilizzato ancora per ritestare i medesimi campioni. È stata valutata una percentuale di accordo dell indice pari al 96.7%, rispetto all analisi effettuata all apertura dei reagenti. BIBLIOGRAFIA 1. Aurelian, L. Herpes Simplex Viruses In Specter, S & G Lancz (eds.). Clinical Virology Manual. 2 nd Ed. Elsevier, New York. (1992). 2. Centers for Disease Control and Prevention. Sexually transmitted diseases treatment guidelines MMWR 2002:5 1 (No. RR-6). 3. Arvin, A, C Prober. Herpes Simplex Viruses In Murray, P, E Baron, M Pfaller, F Tenover, and R Yolkenet (eds.). Manual of Clinical Microbiology. 6th Ed. ASM, Washington, D.C. (1995).. Whitley, R. Herpes Simplex Viruses In Fields, B, D Knipe, P Howley, et al. (eds.). Fields Virology 3 rd Ed. Lippincott-Raven, Philadelphia. (1996). 5. Whitley, R, A Nahmias, A Visintine, C Fleming, C Alford. Natural history of herpes simplex virus infection of mother and newborn. Pediatrics 66:89-9 (1980). 6. Whitley, R. Herpes simplex, in J Klein & J Remington (ed.), Infectious diseases of the fetus and newborn infants, 3 rd ed., p Prober, C, W Sullender, L Yasukawa, D Au, A Yaeger, A Arvin. Low risk of herpes simplex virus infections in neonates exposed to the virus at the time of vaginal delivery to mothers with recurrent herpes simplex virus infections. N Engl J Med 3 16:20-2 (1987). 8. Brown, Z, S Sleke, J Zeh, J Kopelman, A Maslow, R Ashley, D Watts, S Berry, M Herd, L Correy. The acquisition of herpes simplex virus during pregnancy. N Engl J Med 337: (1997). 9. Prober CG, Corey L, Brown ZA et al The management of pregnancies complicated by genital infections with herpes simplex virus. Clin Infect Dis. 15: Brown ZA, Benedetti J, Ashley R et al Neonatal herpes simplex virus infection in relation to asymptomatic maternal infection at the time of labor. N Engl J Med. 32: Stewart, J. Herpes Simplex Virus In Rose, N, E demacario, J Fahey, H Friedman, G Penn (eds.). Manual of Clinical Laboratory Immunology. th Ed. ASM Press, Washington, D.C. (1992). 12. NCCLS H18-A2. Procedures for the Handling and Processing of Blood Specimens; Approved Guideline. 2 nd Ed. (1999). 13. Corey, L., A. Wald, New Developments in the Biology of Genital Herpes, in Clinical Management of Herpes Viruses, p Ashley RL. Performance and use of HSV type-specific serology test kits. Herpes 2002 Jul;9(2): Ashley-Morrow R, Krantz E, Wald A. Time Course of Seroconversion by HerpeSelect ELISA After Acquisition of Genital Herpes Simplex Virus Type 1 (HSV-1) or HSV-2. Sex Transm Dis Apr;30(): Cherpes TL, Ashley RL, Meyn LA, Hillier SL. Longitudinal reliability of focus glycoprotein G-based type-specific enzyme immunoassays for detection of herpes simplex virus types 1 and 2 in women. J Clin Microbiol 2003 Feb;1(2): Liljeqvist et al.typing of Clinical Herpes Simplex Virus Type 1 and Type 2 Isolates with Monoclonal Antibodies. J Clin Micro 37: (1999). 18. CDC-NIH Manual. (1999) Biosafety in Microbiological and Biomedical Laboratories. th ed. And National Committee for Clinical Laboratory Standards (NCCLS). Protection of Laboratory Workers from Instruments, Biohazards and Infectious Disease Transmitted by Blood, Body Fluids and Tissue (NCCLS M29-A). RAPPRESENTANTE AUTORIZZATO mdi Europa GmbH, Langenhagener Str. 71, Langenhagen-Hannover, La Germania INFORMAZIONI PER ORDINARE Telefono: (800) (U.S.A. only) (562) (International) Fax: (562) ASSISTENZA TECNICA Telefono: (800) (U.S.A. only) (562) (International) Fax: (562) PI.EL0910G-IT Rev. K Data scritta: 31 Marzo 2011 Visitate il nostro sito web a: Cypress, California USA
HerpeSelect 2 ELISA IgG (In Italiano)
 (In Italiano) HerpeSelect 2 ELISA IgG REF EL0920G Rev. K Enzyme-linked immunosorbent assay (ELISA) per il rilevamento di anticorpi umani di classe IgG anti HSV-2 Per uso diagnostico in vitro DESTINAZIONE
(In Italiano) HerpeSelect 2 ELISA IgG REF EL0920G Rev. K Enzyme-linked immunosorbent assay (ELISA) per il rilevamento di anticorpi umani di classe IgG anti HSV-2 Per uso diagnostico in vitro DESTINAZIONE
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3
 DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
Chlamydia MIF IgG. Caratteristiche prestazionali. Codice prodotto IF1250G Rev. J. Distribuzione esclusiva al di fuori degli Stati Uniti
 Codice prodotto IF1250G Rev. J Caratteristiche prestazionali Distribuzione esclusiva al di fuori degli Stati Uniti VALORI ATTESI Popolazione con polmonite acquisita comunità Due sperimentatori esterni
Codice prodotto IF1250G Rev. J Caratteristiche prestazionali Distribuzione esclusiva al di fuori degli Stati Uniti VALORI ATTESI Popolazione con polmonite acquisita comunità Due sperimentatori esterni
INGEZIM Gluten Quanti Test Guida all utilizzo
 INGEZIM Gluten Quanti Test Guida all utilizzo 1 - INTRODUZIONE Il kit è basato su un saggio immunoenzimatico ELISA di tipo sandwich come dettato dal Codex Alimentarius. Ogni pozzetto è rivestito sul fondo
INGEZIM Gluten Quanti Test Guida all utilizzo 1 - INTRODUZIONE Il kit è basato su un saggio immunoenzimatico ELISA di tipo sandwich come dettato dal Codex Alimentarius. Ogni pozzetto è rivestito sul fondo
HerpeSelect 1 e 2 Immunoblot IgG (In Italiano)
 HerpeSelect 1 e 2 Immunoblot IgG (In Italiano) REF IB0900G Rev. J Sistema di immunoblot per la ricerca e la differenzazione di anticorpi umani di classe IgG anti- HSV-1 e anti-hsv-2. Per uso diagnostico
HerpeSelect 1 e 2 Immunoblot IgG (In Italiano) REF IB0900G Rev. J Sistema di immunoblot per la ricerca e la differenzazione di anticorpi umani di classe IgG anti- HSV-1 e anti-hsv-2. Per uso diagnostico
URISTIKFIT LEV1 REF KCQURST1
 URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
Valutazione del test rapido Geenius HIV1/2 per la conferma degli anticorpi anti HIV1-2. Gianna Mazzarelli
 Valutazione del test rapido Geenius HIV1/2 per la conferma degli anticorpi anti HIV1-2 Gianna Mazzarelli 14/09/2015 Tempi di rilevazione di specifici markers di infezione HIV Test combinati Ag/Ab Ag ricombinanti
Valutazione del test rapido Geenius HIV1/2 per la conferma degli anticorpi anti HIV1-2 Gianna Mazzarelli 14/09/2015 Tempi di rilevazione di specifici markers di infezione HIV Test combinati Ag/Ab Ag ricombinanti
QUANTA Chek Celiac Panel 708113
 QUANTA Chek Celiac Panel 708113 Finalità d uso Il Pannello Celiac QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli autoanticorpi IFA ed ELISA. Ciascun siero
QUANTA Chek Celiac Panel 708113 Finalità d uso Il Pannello Celiac QUANTA Chek TM è utilizzato per il controllo della qualità delle procedure per la ricerca degli autoanticorpi IFA ed ELISA. Ciascun siero
ISTRUZIONI D USO IVD 0123 HLA CLASSE II REF 7029: HISTO TRAY DR 72 (10)
 ISTRUZIONI D USO IVD 0123 HISTO TRAY HLA CLASSE II PER USO DIAGNOSTICO IN VITRO REF 7029: HISTO TRAY DR 72 (10) 10 piastre Descrizione del prodotto La destinazione d uso dell HISTO TRAY è la tipizzazione
ISTRUZIONI D USO IVD 0123 HISTO TRAY HLA CLASSE II PER USO DIAGNOSTICO IN VITRO REF 7029: HISTO TRAY DR 72 (10) 10 piastre Descrizione del prodotto La destinazione d uso dell HISTO TRAY è la tipizzazione
PLATELIA ASPERGILLUS IgG Negative and Positive Controls
 PLATELIA ASPERGILLUS IgG Negative and Positive Controls 48 62786 Sieri Umani per il Controllo di Qualità 881090-2012/06 sommario 1. USO PREVISTO...27 2. INDICAZIONI PER L USO...27 3. REAGENTI...27 4. AVVERTENZE
PLATELIA ASPERGILLUS IgG Negative and Positive Controls 48 62786 Sieri Umani per il Controllo di Qualità 881090-2012/06 sommario 1. USO PREVISTO...27 2. INDICAZIONI PER L USO...27 3. REAGENTI...27 4. AVVERTENZE
WITNESS GIARDIA INTRODUZIONE
 WITNESS GIARDIA WITNESS GIARDIA INTRODUZIONE Giardia intestinalis (sin. G. duodenalis o G. lamblia) è un protozoo parassita dell apparato gastrointestinale di numerose specie di animali (ad es. cane e
WITNESS GIARDIA WITNESS GIARDIA INTRODUZIONE Giardia intestinalis (sin. G. duodenalis o G. lamblia) è un protozoo parassita dell apparato gastrointestinale di numerose specie di animali (ad es. cane e
EXTRA-GENE I Kit per l estrazione del DNA genomico 50 Estrazioni
 IT Istruzioni d uso EXTRA-GENE I Kit per l estrazione del DNA genomico 50 Estrazioni REF 7059 1. Descrizione del prodotto EXTRA-GENE è un kit per l estrazione veloce del DNA genomico senza l utilizzo di
IT Istruzioni d uso EXTRA-GENE I Kit per l estrazione del DNA genomico 50 Estrazioni REF 7059 1. Descrizione del prodotto EXTRA-GENE è un kit per l estrazione veloce del DNA genomico senza l utilizzo di
CLOSTRIDIUM DIFFICILE TOSSINE A e B
 MODALITA' DI RICHIESTA: Pazienti interni: tramite modulo interno prestampato. Pazienti esterni: tramite richiesta del medico curante. PREPARAZIONE DEL PAZIENTE ALL'ESAME: Nessuna. MODALITA' DI RACCOLTA
MODALITA' DI RICHIESTA: Pazienti interni: tramite modulo interno prestampato. Pazienti esterni: tramite richiesta del medico curante. PREPARAZIONE DEL PAZIENTE ALL'ESAME: Nessuna. MODALITA' DI RACCOLTA
Platelia Measles IgG. 1 piastra /12
 Platelia Measles IgG 1 piastra - 48 72686 METODO IMMUNOENZIMATICO PER LA DETERMINAZIONE QUALITATIVA DEGLI ANTICORPI IgG ANTI VIRUS DEL MORBILLO NEL SIERO UMANO 2014/12 SOMMARIO 1. UTILIZZAZIONE 2. INTRODUZIONE
Platelia Measles IgG 1 piastra - 48 72686 METODO IMMUNOENZIMATICO PER LA DETERMINAZIONE QUALITATIVA DEGLI ANTICORPI IgG ANTI VIRUS DEL MORBILLO NEL SIERO UMANO 2014/12 SOMMARIO 1. UTILIZZAZIONE 2. INTRODUZIONE
Dispositivo di prelievo Aptima Multitest Swab
 Uso previsto Il dispositivo di prelievo Aptima Multitest Swab è previsto per l uso con i test Aptima. Il dispositivo di prelievo Aptima Multitest Swab è previsto per l uso per la raccolta di campioni vaginali
Uso previsto Il dispositivo di prelievo Aptima Multitest Swab è previsto per l uso con i test Aptima. Il dispositivo di prelievo Aptima Multitest Swab è previsto per l uso per la raccolta di campioni vaginali
15 Anti-D policlonale / incompleto
 Scheda Tecnica 0123 Technical File No.: Prodotto: 15 Anti-D policlonale / incompleto Categoria di prodotto secondo la classificazione CE: Allegato II Lista A Struttura della scheda tecnica Descrizione
Scheda Tecnica 0123 Technical File No.: Prodotto: 15 Anti-D policlonale / incompleto Categoria di prodotto secondo la classificazione CE: Allegato II Lista A Struttura della scheda tecnica Descrizione
ALLwell Elution Technologies Bovine Casein Protein
 ALLwell Elution Technologies Bovine Casein Protein Elisa kit Cat. N. ETE-75CAS Kit per la rilevazione della caseina bovina in campioni alimentari Manuale d uso Leggere attentamente il manuale prima di
ALLwell Elution Technologies Bovine Casein Protein Elisa kit Cat. N. ETE-75CAS Kit per la rilevazione della caseina bovina in campioni alimentari Manuale d uso Leggere attentamente il manuale prima di
Allegato III Autocertificazione del produttore
 Scheda Tecnica 0123 Technical File No.: 24 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-Lua, Anti-Lub coombsreactive Allegato III Autocertificazione del produttore Struttura della
Scheda Tecnica 0123 Technical File No.: 24 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-Lua, Anti-Lub coombsreactive Allegato III Autocertificazione del produttore Struttura della
Simplexa BKV Quantitation Standards
 Simplexa BKV Quantitation Standards REF MOL2310 Rev. B I Simplexa BKV Quantitation Standards sono destinati alla definizione di una curva standard per il saggio Simplexa BKV sullo strumento 3M Integrated
Simplexa BKV Quantitation Standards REF MOL2310 Rev. B I Simplexa BKV Quantitation Standards sono destinati alla definizione di una curva standard per il saggio Simplexa BKV sullo strumento 3M Integrated
il rapporto sessuale è la via preminente di contagio sono guaribili (eccetto AIDS ed epatite C) se vengono riconosciute il più presto possibile
 LE MALATTIE SESSUALMENTE TRASMESSE il rapporto sessuale è la via preminente di contagio sono guaribili (eccetto AIDS ed epatite C) se vengono riconosciute il più presto possibile alcune possono essere
LE MALATTIE SESSUALMENTE TRASMESSE il rapporto sessuale è la via preminente di contagio sono guaribili (eccetto AIDS ed epatite C) se vengono riconosciute il più presto possibile alcune possono essere
Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile.
 Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile. Questi anticorpi sono delle molecole IgG che attaccano un solo
Molti anticorpi gruppo-ematici reagiscono con i corrispondenti antigeni sui globuli rossi in vitro senza determinare alcun effetto visibile. Questi anticorpi sono delle molecole IgG che attaccano un solo
CONFERMA DIAGNOSTICA IN CASO DI MORBILLO
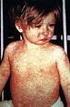 CONFERMA DIAGNOSTICA IN CASO DI MORBILLO Ai fini della segnalazione al Servizio di Igiene e Sanità Pubblica si intende per morbillo una forma morbosa caratterizzata da: febbre superiore a 38 C esantema
CONFERMA DIAGNOSTICA IN CASO DI MORBILLO Ai fini della segnalazione al Servizio di Igiene e Sanità Pubblica si intende per morbillo una forma morbosa caratterizzata da: febbre superiore a 38 C esantema
Per la conservazione viene aggiunta sodio azide a una concentrazione finale inferiore allo 0,1 %.
 Scheda Tecnica 0123 Technical File No.: 38 Prodotto: Categoria di prodotto secondo la classificazione CE: Albumina Bovina 22% 30% Allegato III Autocertificazione del produttore Struttura della scheda tecnica
Scheda Tecnica 0123 Technical File No.: 38 Prodotto: Categoria di prodotto secondo la classificazione CE: Albumina Bovina 22% 30% Allegato III Autocertificazione del produttore Struttura della scheda tecnica
ALLflow Elution Technologies Milk Proteins Rapid Test
 ALLflow Elution Technologies Milk Proteins Rapid Test Lateral Flow kit Cat. N. ETMILK-1004 Kit per la rilevazione rapida delle proteine del latte in campioni alimentari ed ambientali Manuale d uso Leggere
ALLflow Elution Technologies Milk Proteins Rapid Test Lateral Flow kit Cat. N. ETMILK-1004 Kit per la rilevazione rapida delle proteine del latte in campioni alimentari ed ambientali Manuale d uso Leggere
HBCon. ISTRUZIONI PER L USO VITROS Immunodiagnostic Products Kit di conferma dell HBsAg
 ISTRUZIONI PER L USO VITROS Immunodiagnostic Products Kit di conferma dell HBsAg HBCon 822 8595 Impiego Uso in vitro per la conferma della presenza dell antigene di superficie dell epatite B (HBsAg) in
ISTRUZIONI PER L USO VITROS Immunodiagnostic Products Kit di conferma dell HBsAg HBCon 822 8595 Impiego Uso in vitro per la conferma della presenza dell antigene di superficie dell epatite B (HBsAg) in
ISTRUZIONE OPERATIVA CAMPIONAMENTO ACQUA
 Pagina 1 di 5 ISTRUZIONE OPERATIVA REVISIONE NUMERO DATA REDATTA DA DIR VERIFICATA DA RAQ APPROVATA DA AMM PARAGRAFO REVISIONATO NUMERO MOTIVO 00 15-01-09 Prima emissione 01 22-04-13 4.1.2 01 22-04-13
Pagina 1 di 5 ISTRUZIONE OPERATIVA REVISIONE NUMERO DATA REDATTA DA DIR VERIFICATA DA RAQ APPROVATA DA AMM PARAGRAFO REVISIONATO NUMERO MOTIVO 00 15-01-09 Prima emissione 01 22-04-13 4.1.2 01 22-04-13
QUANTA Lite Jo-1 ELISA Per uso diagnostico In Vitro Complessità CLIA: elevata
 QUANTA Lite Jo-1 ELISA 708585 Per uso diagnostico In Vitro Complessità CLIA: elevata Finalità d uso QUANTA Lite Jo-1 è un test immunoenzimatico per la ricerca semi-quantitativa di anticorpi anti-jo-1 nel
QUANTA Lite Jo-1 ELISA 708585 Per uso diagnostico In Vitro Complessità CLIA: elevata Finalità d uso QUANTA Lite Jo-1 è un test immunoenzimatico per la ricerca semi-quantitativa di anticorpi anti-jo-1 nel
Un anticorpo è una proteina prodotta dai linfociti B in risposta all ingresso nell organismo di un antigene.
 Un antigene è una molecola (proteica o polisaccaridica), o una sua parte, che è in grado di stimolare una risposta specifica del sistema immunitario. Affinché una molecola funga da antigene è necessario
Un antigene è una molecola (proteica o polisaccaridica), o una sua parte, che è in grado di stimolare una risposta specifica del sistema immunitario. Affinché una molecola funga da antigene è necessario
Anti-Jka, Anti-Jkb coombs
 Scheda Tecnica 0123 Technical File No.: 3 Prodotto: Anti-Jka, Anti-Jkb coombs Categoria di prodotto secondo la classificazione CE: Allegato II Lista B Struttura della scheda tecnica Descrizione del prodotto:
Scheda Tecnica 0123 Technical File No.: 3 Prodotto: Anti-Jka, Anti-Jkb coombs Categoria di prodotto secondo la classificazione CE: Allegato II Lista B Struttura della scheda tecnica Descrizione del prodotto:
L INTEGRAZIONE CON IL LABORATORIO PER LA CORRETTA DIAGNOSI PRENATALE DI INFEZIONE
 L INTEGRAZIONE CON IL LABORATORIO PER LA CORRETTA DIAGNOSI PRENATALE DI INFEZIONE Licia Bordi Laboratorio di Virologia INMI Spallanzani Istituto Nazionale Malattie Infettive L. Spallanzani IRCCS 12/05/2017
L INTEGRAZIONE CON IL LABORATORIO PER LA CORRETTA DIAGNOSI PRENATALE DI INFEZIONE Licia Bordi Laboratorio di Virologia INMI Spallanzani Istituto Nazionale Malattie Infettive L. Spallanzani IRCCS 12/05/2017
Lavaggio degli eritrociti
 1 Lavaggio degli eritrociti Le attività emolitica ed emoagglutinante del virus Sendai richiedono una soluzione di eritrociti umani lavati in tampone PBS e diluiti al 2% (v/v). Reagenti Sangue umano fresco.
1 Lavaggio degli eritrociti Le attività emolitica ed emoagglutinante del virus Sendai richiedono una soluzione di eritrociti umani lavati in tampone PBS e diluiti al 2% (v/v). Reagenti Sangue umano fresco.
RIDASCREEN. Aflatoxin Total. Test immunoenzimatico per il dosaggio quantitativo di aflatossine. Art. No.: R4701. Test in vitro Conservare a 2-8 C
 RIDASCREEN Aflatoxin Total Test immunoenzimatico per il dosaggio quantitativo di aflatossine Art. No.: R4701 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0
RIDASCREEN Aflatoxin Total Test immunoenzimatico per il dosaggio quantitativo di aflatossine Art. No.: R4701 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0
BENZILPENICILLINA BENZATINICA PREPARAZIONE INIETTABILI. Benzilpenicillina Benzatinica polvere sterile per preparazioni iniettabili
 1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
Tecniche diagnostiche
 TEST DIAGNOSTICI Tecniche diagnostiche Infezione corrente Isolamento dell agente eziologico Identificazione del materiale genetico dell agente eziologico Segni clinici Alterazioni patognomoniche Alterazioni
TEST DIAGNOSTICI Tecniche diagnostiche Infezione corrente Isolamento dell agente eziologico Identificazione del materiale genetico dell agente eziologico Segni clinici Alterazioni patognomoniche Alterazioni
PLATELIA HSV 2 IgG 96 TEST 72821
 PLATELIA HSV 2 IgG 96 TEST 72821 DETERMINAZIONE QUALITATIVA DEGLI ANTICORPI IgG ANTI-HSV 2 NEL SIERO O NEL PLASMA UMANO MEDIANTE IMMUNODOSAGGIO ENZIMATICO 1. USO PREVISTO Platelia HSV 2 IgG è un immunodosaggio
PLATELIA HSV 2 IgG 96 TEST 72821 DETERMINAZIONE QUALITATIVA DEGLI ANTICORPI IgG ANTI-HSV 2 NEL SIERO O NEL PLASMA UMANO MEDIANTE IMMUNODOSAGGIO ENZIMATICO 1. USO PREVISTO Platelia HSV 2 IgG è un immunodosaggio
PROGENSA PCA3 Urine Specimen Transport Kit
 PROGENSA PCA3 Urine Specimen Transport Kit Istruzioni per i medici Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
PROGENSA PCA3 Urine Specimen Transport Kit Istruzioni per i medici Per l uso diagnostico in vitro. Solo per l esportazione dagli U.S.A. Istruzioni 1. Si consiglia di chiedere al paziente di bere una grande
AlereTM. HIV Combo TOCCARE QUI PER VEDERE IL PRODOTTO
 AlereTM HIV Combo TOCCARE QUI PER VEDERE IL PRODOTTO Cogli qualunque opportunità di fare il test. I casi di infezione acuta sono compresi fra il 5 e il 20% rispetto al totale dei casi di infezione da HIV
AlereTM HIV Combo TOCCARE QUI PER VEDERE IL PRODOTTO Cogli qualunque opportunità di fare il test. I casi di infezione acuta sono compresi fra il 5 e il 20% rispetto al totale dei casi di infezione da HIV
Arruolamento di coppie Criteri di inclusione per il partner sieropositivo
 Introduzione Molti studi riportano che i preservativi non vengono usati in modo costante all interno della coppia, anche quando un partner è sieropositivo e l altro è sieronegativo. Questo può essere dovuto
Introduzione Molti studi riportano che i preservativi non vengono usati in modo costante all interno della coppia, anche quando un partner è sieropositivo e l altro è sieronegativo. Questo può essere dovuto
Valutazione dei test diagnostici
 Valutazione dei test diagnostici Maria Miceli M. Miceli 2011 1 Diagnosi individuale (test di laboratorio) Esame collaterale nell ambito dell iter diagnostico condotto generalmente su animali sintomatici
Valutazione dei test diagnostici Maria Miceli M. Miceli 2011 1 Diagnosi individuale (test di laboratorio) Esame collaterale nell ambito dell iter diagnostico condotto generalmente su animali sintomatici
QUANTA Lite RNP ELISA Per uso diagnostico In Vitro Complessità CLIA: elevata
 QUANTA Lite RNP ELISA 708565 Per uso diagnostico In Vitro Complessità CLIA: elevata Finalità d uso QUANTA Lite RNP è un test immunoenzimatico per la ricerca semi-quantitativa di anticorpi anti-rnp nel
QUANTA Lite RNP ELISA 708565 Per uso diagnostico In Vitro Complessità CLIA: elevata Finalità d uso QUANTA Lite RNP è un test immunoenzimatico per la ricerca semi-quantitativa di anticorpi anti-rnp nel
Saggio immunoenzimatico per la misurazione dell attività totale del percorso classic del complement nel siero umano
 Saggio immunoenzimatico per la misurazione dell attività totale del percorso classic del complement nel siero umano Per uso diagnostico In Vitro SOMMARIO MicroVue CH50 Eq EIA Pagina 1 di 11 FINALITÀ D
Saggio immunoenzimatico per la misurazione dell attività totale del percorso classic del complement nel siero umano Per uso diagnostico In Vitro SOMMARIO MicroVue CH50 Eq EIA Pagina 1 di 11 FINALITÀ D
AVR: DIAGNOSI DI LABORATORIO
 Pievesestina di Cesena - 8 novembre 2013 Proposta di Gestione Integrata Clinico-Laboratoristica delle Infezioni Materno-Fetali nell'area Vasta Romagna AVR: DIAGNOSI DI LABORATORIO NELLE INFEZIONI DA TOXOPLASMA,
Pievesestina di Cesena - 8 novembre 2013 Proposta di Gestione Integrata Clinico-Laboratoristica delle Infezioni Materno-Fetali nell'area Vasta Romagna AVR: DIAGNOSI DI LABORATORIO NELLE INFEZIONI DA TOXOPLASMA,
Esperienza rapid test a Torino Il Laboratorio
 Bologna, 14 maggio 2012 HIV+ Late presenters: Il test rapido è una soluzione? Esperienza rapid test a Torino Il Laboratorio Evoluzione tecniche sierologiche per ricerca anticorpi anti-hiv Riduzione fase
Bologna, 14 maggio 2012 HIV+ Late presenters: Il test rapido è una soluzione? Esperienza rapid test a Torino Il Laboratorio Evoluzione tecniche sierologiche per ricerca anticorpi anti-hiv Riduzione fase
 ACIDITA su burro, margarine, panna e grassi semilavorati PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA PREPARAZIONE DEL CAMPIONE CONDIZIONI DI REAZIONE (Edit) Gli acidi grassi del campione, in
ACIDITA su burro, margarine, panna e grassi semilavorati PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA PREPARAZIONE DEL CAMPIONE CONDIZIONI DI REAZIONE (Edit) Gli acidi grassi del campione, in
WITNESS PARVO INTRODUZIONE
 WITNESS PARVO WITNESS PARVO INTRODUZIONE Il Parvovirus canino (CPV) appartiene ad un sottogruppo del parvovirus felino. È in stretto rapporto col virus della panleucopenia felina e col virus dell'enterite
WITNESS PARVO WITNESS PARVO INTRODUZIONE Il Parvovirus canino (CPV) appartiene ad un sottogruppo del parvovirus felino. È in stretto rapporto col virus della panleucopenia felina e col virus dell'enterite
Metodo di conferma in HPLC
 9 - TETRAIDROCANNABINOLO-COOH urinario in UV Cod. Z47010 Metodo di conferma in HPLC INTRODUZIONE Il 9 -THC-COOH è il metabolita urinario principale della Cannabis. La sua determinazione di screening nei
9 - TETRAIDROCANNABINOLO-COOH urinario in UV Cod. Z47010 Metodo di conferma in HPLC INTRODUZIONE Il 9 -THC-COOH è il metabolita urinario principale della Cannabis. La sua determinazione di screening nei
CH50 Eq SOMMARIO E SPIEGAZIONE PRINCIPIO DELLA PROCEDURA FINALITÀ D USO
 CH50 Eq Saggio immunoenzimatico per la misurazione dell attività totale del percorso classico del complemento nel siero umano MicroVue CH50 Eq EIA Sommario Preparato di il Campione ed il reagente Diluire
CH50 Eq Saggio immunoenzimatico per la misurazione dell attività totale del percorso classico del complemento nel siero umano MicroVue CH50 Eq EIA Sommario Preparato di il Campione ed il reagente Diluire
GARA NAZIONALE DI CHIMICA VIII EDIZIONE PROVA PRATICA
 GARA NAZIONALE DI CHIMICA VIII EDIZIONE PROVA PRATICA Istruzioni Scrivere il proprio nome e cognome su questa pagina e sulla scheda delle risposte. Seguire le regole di sicurezza di laboratorio: se vengono
GARA NAZIONALE DI CHIMICA VIII EDIZIONE PROVA PRATICA Istruzioni Scrivere il proprio nome e cognome su questa pagina e sulla scheda delle risposte. Seguire le regole di sicurezza di laboratorio: se vengono
bioelisa VEDI CAMBI RISALTATI
 VEDI CAMBI RISALTATI bioelisa RUBELLA IgM (Immunocapture) 3000-1231 96 tests Test ELISA per la determinazione degli anticorpi IgM anti-rosolia nel siero o nel plasma umano. Sommario La rosolia, o morbillo
VEDI CAMBI RISALTATI bioelisa RUBELLA IgM (Immunocapture) 3000-1231 96 tests Test ELISA per la determinazione degli anticorpi IgM anti-rosolia nel siero o nel plasma umano. Sommario La rosolia, o morbillo
Metodo di conferma in HPLC
 9 - TETRAIDROCANNABINOLO-COOH urinario in UV Cod. Z47010 Metodo di conferma in HPLC INTRODUZIONE Il 9 -THC-COOH è il metabolita urinario principale della Cannabis. La sua determinazione di screening nei
9 - TETRAIDROCANNABINOLO-COOH urinario in UV Cod. Z47010 Metodo di conferma in HPLC INTRODUZIONE Il 9 -THC-COOH è il metabolita urinario principale della Cannabis. La sua determinazione di screening nei
Scheda del protocollo QIAsymphony SP
 Scheda del protocollo QIAsymphony SP Protocollo DNA_Blood_400_V6_DSP Informazioni generali Per uso diagnostico in vitro. Questo protocollo è previsto per la purificazione del DNA genomico totale e mitocondriale
Scheda del protocollo QIAsymphony SP Protocollo DNA_Blood_400_V6_DSP Informazioni generali Per uso diagnostico in vitro. Questo protocollo è previsto per la purificazione del DNA genomico totale e mitocondriale
Per la conservazione viene aggiunta sodio azide a una concentrazione finale inferiore allo 0,1%.
 Scheda Tecnica 0123 Technical File No.: 21 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-S monoclonale (Sistema MNSs) Allegato III Autocertificazione del produttore Struttura della
Scheda Tecnica 0123 Technical File No.: 21 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-S monoclonale (Sistema MNSs) Allegato III Autocertificazione del produttore Struttura della
AMPICILLINA SODICA PREPARAZIONE INIETTABILE. Ampicillina sodica polvere sterile per preparazioni iniettabili
 1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
Sistema di sorveglianza nazionale della ROSOLIA IN GRAVIDANZA e della ROSOLIA CONGENITA
 Sistema di sorveglianza nazionale della ROSOLIA IN GRAVIDANZA e della ROSOLIA CONGENITA Il sistema di sorveglianza nazionale - dal 2005 D.M. del 14 ottobre 2004: a partire dal 1 gennaio 2005, l infezione
Sistema di sorveglianza nazionale della ROSOLIA IN GRAVIDANZA e della ROSOLIA CONGENITA Il sistema di sorveglianza nazionale - dal 2005 D.M. del 14 ottobre 2004: a partire dal 1 gennaio 2005, l infezione
Istruzioni per l uso di BVPro
 Numero di catalogo: MBVP15 per confezione da 5 e MBVP125 per confezione da 25 Istruzioni per l uso di BVPro BVPro Test diagnostico rapido per la determinazione di vaginosi batterica (VB). Per uso professionale.
Numero di catalogo: MBVP15 per confezione da 5 e MBVP125 per confezione da 25 Istruzioni per l uso di BVPro BVPro Test diagnostico rapido per la determinazione di vaginosi batterica (VB). Per uso professionale.
Modulo 15: Diagnosi microbiologica di influenza
 CdS Medicina e Chirurgia CI Medicina di Laboratorio MICROBIOLOGIA CLINICA AA 2015-2016 Modulo 15: Diagnosi microbiologica di influenza Giovanni DI BONAVENTURA, PhD Università «G. d Annunzio» di Chieti-Pescara
CdS Medicina e Chirurgia CI Medicina di Laboratorio MICROBIOLOGIA CLINICA AA 2015-2016 Modulo 15: Diagnosi microbiologica di influenza Giovanni DI BONAVENTURA, PhD Università «G. d Annunzio» di Chieti-Pescara
bioelisa VEDI CAMBI RISALTATI
 VEDI CAMBI RISALTATI bioelisa HIV-1+2 3.0 3000-1168 96 tests 3000-1169 480 tests Test ELISA per la determinazione degli anticorpi contro i virus dell immunodeficienza umana (HIV) tipo 1 (gruppo M-O) o
VEDI CAMBI RISALTATI bioelisa HIV-1+2 3.0 3000-1168 96 tests 3000-1169 480 tests Test ELISA per la determinazione degli anticorpi contro i virus dell immunodeficienza umana (HIV) tipo 1 (gruppo M-O) o
controllo delle malattie dei pesci
 Epidemiologia nel controllo delle malattie dei pesci Dr Ignacio de Blas Facoltà di Veterinaria Università di Zaragoza (Spagna) Erice, 24 ottobre 2008 Workshop Acquacoltura mediterranea: aspetti normativi
Epidemiologia nel controllo delle malattie dei pesci Dr Ignacio de Blas Facoltà di Veterinaria Università di Zaragoza (Spagna) Erice, 24 ottobre 2008 Workshop Acquacoltura mediterranea: aspetti normativi
VEDI CAMBI RISALTATI. Ac a-igm a-hav IgM HAV a-hav perossidasi
 VEDI CAMBI RISALTATI bioelisa HAV IgM 3000-1098 96 tests Test ELISA per la determinazione degli anticorpi IgM contro il virus dell'epatite A (HAV) nel siero o nel plasma umano. Sommario Il virus dell'epatite
VEDI CAMBI RISALTATI bioelisa HAV IgM 3000-1098 96 tests Test ELISA per la determinazione degli anticorpi IgM contro il virus dell'epatite A (HAV) nel siero o nel plasma umano. Sommario Il virus dell'epatite
SERVIZIO SANITARIO NAZIONALE REGIONE BASILICATA Asl 4 - Matera SERVIZIO ASSISTENZA
 SERVIZIO SANITARIO NAZIONALE REGIONE BASILICATA Asl 4 - Matera SERVIZIO ASSISTENZA Pagina 2/6 SOMMARIO 1. SCOPO/OBIETTIVO...3 2. CAMPO DI APPLICAZIONE...3 3. RIFERIMENTI NORMATIVI E DOCUMENTALI...3 4.
SERVIZIO SANITARIO NAZIONALE REGIONE BASILICATA Asl 4 - Matera SERVIZIO ASSISTENZA Pagina 2/6 SOMMARIO 1. SCOPO/OBIETTIVO...3 2. CAMPO DI APPLICAZIONE...3 3. RIFERIMENTI NORMATIVI E DOCUMENTALI...3 4.
PLATELIA CANDIDA Ab PLUS Negative and Positive Controls. Sieri Umani per il Controllo di Qualità
 PLATELIA CANDIDA Ab PLUS Negative and Positive Controls 48 62787 Sieri Umani per il Controllo di Qualità sommario 1. USO PREVISTO...27 2. INDICAZIONI PER L USO...27 3. REAGENTI...27 4. AVVERTENZE PER GLI
PLATELIA CANDIDA Ab PLUS Negative and Positive Controls 48 62787 Sieri Umani per il Controllo di Qualità sommario 1. USO PREVISTO...27 2. INDICAZIONI PER L USO...27 3. REAGENTI...27 4. AVVERTENZE PER GLI
Anti-Fya, Anti-Fyb coombs
 Scheda Tecnica 0123 Technical File No.: 2 Prodotto: Anti-Fya, Anti-Fyb coombs Categoria di prodotto secondo la classificazione CE: Allegato II Lista B Struttura della scheda tecnica Descrizione del prodotto:
Scheda Tecnica 0123 Technical File No.: 2 Prodotto: Anti-Fya, Anti-Fyb coombs Categoria di prodotto secondo la classificazione CE: Allegato II Lista B Struttura della scheda tecnica Descrizione del prodotto:
Biotecnologia Nella Tua Bocca
 Biotecnologia Nella Tua Bocca MATERIALI INCLUSI Il kit comprende materiale e reagenti per 30 studenti (sei gruppi di cinque studenti) Protein Dye Solution Pipetta grande Pipetta piccola Bottiglia Enzyme
Biotecnologia Nella Tua Bocca MATERIALI INCLUSI Il kit comprende materiale e reagenti per 30 studenti (sei gruppi di cinque studenti) Protein Dye Solution Pipetta grande Pipetta piccola Bottiglia Enzyme
RISOLUZIONE ENO 25/2004
 DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
LEVETIRACETAM PLASMATICO in UV - FAST Codice Z84010
 LEVETIRACETAM PLASMATICO in UV - FAST Codice Z84010 INTRODUZIONE Il trattamento del paziente epilettico richiede il contributo multidisciplinare di competenze mediche, farmacologiche, psicologiche e sociali.
LEVETIRACETAM PLASMATICO in UV - FAST Codice Z84010 INTRODUZIONE Il trattamento del paziente epilettico richiede il contributo multidisciplinare di competenze mediche, farmacologiche, psicologiche e sociali.
Kit per la determinazione immuno-turbidimetrica quantitativa delle sieroproteine umane su sistemi automatici.
 1 1. IMMUNOTURBIDIMETRIA METODI IMMUNO-TURBIDIMETRICI PER AUTOMAZIONE 2. LATTICI METODI IN AGGLUTINAZIONE AL LATTICE SU VETRINO 3. LATTICI PER AUTOMAZIONE METODI TURBIDIMETRICI AL LATTICE 2012 1 2 METODI
1 1. IMMUNOTURBIDIMETRIA METODI IMMUNO-TURBIDIMETRICI PER AUTOMAZIONE 2. LATTICI METODI IN AGGLUTINAZIONE AL LATTICE SU VETRINO 3. LATTICI PER AUTOMAZIONE METODI TURBIDIMETRICI AL LATTICE 2012 1 2 METODI
Dengue NS1 Antigen DxSelect (Italiano)
 Dengue NS1 Antigen DxSelect (Italiano) REF EL1510 Rev. C Saggio immuno-assorbente legato ad un enzima (ELISA) per la rilevazione dell'antigene NS1 nel siero umano Per utilizzo diagnostico in vitro USO
Dengue NS1 Antigen DxSelect (Italiano) REF EL1510 Rev. C Saggio immuno-assorbente legato ad un enzima (ELISA) per la rilevazione dell'antigene NS1 nel siero umano Per utilizzo diagnostico in vitro USO
Scheda del protocollo QIAsymphony SP
 Scheda del protocollo QIAsymphony SP Protocollo PC_AXpH_HC2_V1_DSP Uso previsto Per uso diagnostico in vitro. Questo protocollo è stato sviluppato per l uso con campioni cervicali conservati nella soluzione
Scheda del protocollo QIAsymphony SP Protocollo PC_AXpH_HC2_V1_DSP Uso previsto Per uso diagnostico in vitro. Questo protocollo è stato sviluppato per l uso con campioni cervicali conservati nella soluzione
Informazioni generali
 Un ausilio per la preparazione e l'isolamento di linfociti purificati direttamente dal sangue intero FOGLIO ILLUSTRATIVO Per uso diagnostico In Vitro PI-TT.610-IT-V5 Informazioni generali Uso previsto
Un ausilio per la preparazione e l'isolamento di linfociti purificati direttamente dal sangue intero FOGLIO ILLUSTRATIVO Per uso diagnostico In Vitro PI-TT.610-IT-V5 Informazioni generali Uso previsto
PLATELIA CMV IgM TEST
 PLATELIA CMV IgM 72811 96 TEST DETERMINAZIONE QUALITATIVA DEGLI ANTICORPI IgM ANTI-CYTOMEGALOVIRUS NEL SIERO O NEL PLASMA UMANO MEDIANTE DOSAGGIO IMMUNOENZIMATICO 1. USO PREVISTO Platelia CMV IgM è un
PLATELIA CMV IgM 72811 96 TEST DETERMINAZIONE QUALITATIVA DEGLI ANTICORPI IgM ANTI-CYTOMEGALOVIRUS NEL SIERO O NEL PLASMA UMANO MEDIANTE DOSAGGIO IMMUNOENZIMATICO 1. USO PREVISTO Platelia CMV IgM è un
2. Prima di eseguire il test, portare campioni e reagenti a temperatura ambiente.
 IVD NOME E SCOPO IMMUNOQUICK TETANUS è un test immunocromatografico rapido per la determinazione semiquantitativa, in siero o sangue umano intero, di anticorpi anti tossina tetanica. SOMMARIO E DESCRIZIONE
IVD NOME E SCOPO IMMUNOQUICK TETANUS è un test immunocromatografico rapido per la determinazione semiquantitativa, in siero o sangue umano intero, di anticorpi anti tossina tetanica. SOMMARIO E DESCRIZIONE
RIDASCREEN Histamin (enzymatic)
 RIDASCREEN Histamin (enzymatic) Test enzimatico per il dosaggio quantitativo di Istamina Art. No.: R1605 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germania Tel.: +49 (0) 61 51 81 02-0
RIDASCREEN Histamin (enzymatic) Test enzimatico per il dosaggio quantitativo di Istamina Art. No.: R1605 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germania Tel.: +49 (0) 61 51 81 02-0
ScanGel ABO Complete/RH/K Duo x 24 schede x 144 schede Schede ScanGel ABO Complete/RH1 Duo e ScanGel Monoclonal RH/K Phenotypes Duo
 ScanGel ABO Complete/RH/K Duo 86719 2 x 24 schede 86709 2 x 144 schede Schede ScanGel ABO Complete/RH1 Duo e ScanGel Monoclonal RH/K Phenotypes Duo GEL FORMULATI CON REAGENTI MONOCLONALI DI ORIGINE MURINA
ScanGel ABO Complete/RH/K Duo 86719 2 x 24 schede 86709 2 x 144 schede Schede ScanGel ABO Complete/RH1 Duo e ScanGel Monoclonal RH/K Phenotypes Duo GEL FORMULATI CON REAGENTI MONOCLONALI DI ORIGINE MURINA
BioOscientific Manuale Utente Leggere attentamente questo inserto prima di utilizzare il prodotto
 BioOscientific MaxSignal Aflatoxin M1 test kit Cat. N. BOS106005 Saggio ELISA per rilevazione di Aflatossina M1 Manuale Utente Leggere attentamente questo inserto prima di utilizzare il prodotto Via San
BioOscientific MaxSignal Aflatoxin M1 test kit Cat. N. BOS106005 Saggio ELISA per rilevazione di Aflatossina M1 Manuale Utente Leggere attentamente questo inserto prima di utilizzare il prodotto Via San
Striscia reattiva glicemia ematocrito emoglobina. N. modello: TD-4272 / GD40 DELTA
 Striscia reattiva glicemia ematocrito emoglobina AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori che eseguono
Striscia reattiva glicemia ematocrito emoglobina AVVERTENZE Per uso diagnostico in vitro (esclusivamente per uso esterno). Esclusivamente monouso. Il personale medico e gli altri operatori che eseguono
AdnaTest BreastCancerSelect
 AdnaTest BreastCancerSelect Arricchimento di cellule tumorali dal sangue di pazienti con tumore della mammella per l analisi dell espressione genica Per uso diagnostico in vitro Manuale T-1-508 Indice
AdnaTest BreastCancerSelect Arricchimento di cellule tumorali dal sangue di pazienti con tumore della mammella per l analisi dell espressione genica Per uso diagnostico in vitro Manuale T-1-508 Indice
CICLO VITALE DEL TOXOPLASMA
 CICLO VITALE DEL TOXOPLASMA STADI DEL CICLO VITALE DEL TOXOPLASMA Recenti Sviluppi nella Diagnosi dellatoxoplasmosi JOURNAL OF CLINICAL MICROBIOLOGY, Mar. 2004, p. 941 945 Vol. 42, No. 3 MINIREVIEW Recent
CICLO VITALE DEL TOXOPLASMA STADI DEL CICLO VITALE DEL TOXOPLASMA Recenti Sviluppi nella Diagnosi dellatoxoplasmosi JOURNAL OF CLINICAL MICROBIOLOGY, Mar. 2004, p. 941 945 Vol. 42, No. 3 MINIREVIEW Recent
SCHEDA E PROCEDURA APERTAPER LA FORNITURA IN SERVICE DI SISTEMI ANALITICI PER I LABORATORI
 SCHEDA E PROCEDURA APERTAPER LA FORNITURA IN SERVICE DI SISTEMI ANALITICI PER I LABORATORI OGGETTO DI VALUTAZIONE AL FINE DI STABILIRE IL PUNTEGGIO QUALITATIVO DEI PRODOTTI A GARA. Il punteggio qualitativo
SCHEDA E PROCEDURA APERTAPER LA FORNITURA IN SERVICE DI SISTEMI ANALITICI PER I LABORATORI OGGETTO DI VALUTAZIONE AL FINE DI STABILIRE IL PUNTEGGIO QUALITATIVO DEI PRODOTTI A GARA. Il punteggio qualitativo
LA PREVENZIONE DELL HPV IN PAZIENTI CON INFEZIONE DA HIV: SPERIMENTAZIONE CLINICA ALL OSPEDALE PEDIATRICO BAMBINO GESÙ.
 LA PREVENZIONE DELL HPV IN PAZIENTI CON INFEZIONE DA HIV: SPERIMENTAZIONE CLINICA ALL OSPEDALE PEDIATRICO BAMBINO GESÙ Luciana Nicolosi luciana.nicolosi@opbg.net Vaccinazioni a Rischio U.O.C. Pediatria
LA PREVENZIONE DELL HPV IN PAZIENTI CON INFEZIONE DA HIV: SPERIMENTAZIONE CLINICA ALL OSPEDALE PEDIATRICO BAMBINO GESÙ Luciana Nicolosi luciana.nicolosi@opbg.net Vaccinazioni a Rischio U.O.C. Pediatria
Rischio Biologico D.lgs. 81/08
 Rischio Biologico D.lgs. 81/08 TITOLO X - ESPOSIZIONE AD AGENTI BIOLOGICI CAPO I - DISPOSIZIONI GENERALI Articolo 266 - Campo di applicazione 1. Le norme del presente Titolo si applicano a tutte le attività
Rischio Biologico D.lgs. 81/08 TITOLO X - ESPOSIZIONE AD AGENTI BIOLOGICI CAPO I - DISPOSIZIONI GENERALI Articolo 266 - Campo di applicazione 1. Le norme del presente Titolo si applicano a tutte le attività
METADONE urinario in UV Cod. Z Metodo di conferma HPLC
 METADONE urinario in UV Cod. Z48010 Metodo di conferma HPLC INTRODUZIONE Il Metadone è una sostanza con una lunga storia di sostituto dell eroina. La sua determinazione di screening nei liquidi biologici
METADONE urinario in UV Cod. Z48010 Metodo di conferma HPLC INTRODUZIONE Il Metadone è una sostanza con una lunga storia di sostituto dell eroina. La sua determinazione di screening nei liquidi biologici
ZytoDot SPEC HER2 Probe
 ZytoDot SPEC HER2 Probe C-3001-400 C-3001-100 40 (0.4 ml) 10 (0.1 ml) Per la rilevazione del gene umano HER2 mediante ibridazione in situ cromogenica (CISH).... Dispositivo per uso diagnostico in vitro
ZytoDot SPEC HER2 Probe C-3001-400 C-3001-100 40 (0.4 ml) 10 (0.1 ml) Per la rilevazione del gene umano HER2 mediante ibridazione in situ cromogenica (CISH).... Dispositivo per uso diagnostico in vitro
RIDASCREEN. Nitrofuran (AHD) Test immunoenzimatico per l analisi quantitativa di AHD. Art. No.: R3713. Test in vitro Conservare a 2-8 C
 RIDASCREEN Nitrofuran (AHD) Test immunoenzimatico per l analisi quantitativa di AHD Art. No.: R3713 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 / Telefax:
RIDASCREEN Nitrofuran (AHD) Test immunoenzimatico per l analisi quantitativa di AHD Art. No.: R3713 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 / Telefax:
ISTRUZIONE OPERATIVA CAMPIONAMENTO ACQUA
 Pagina 1 di 6 ISTRUZIONE OPERATIVA REVISIONE NUMERO DATA REDATTA DA DIR (firma) VERIFICATA DA RAQ (firma) APPROVATA DA AMM (firma) PARAGRAFO REVISIONATO NUMERO MOTIVO 00 15-01-09 Prima emissione 01 22-04-13
Pagina 1 di 6 ISTRUZIONE OPERATIVA REVISIONE NUMERO DATA REDATTA DA DIR (firma) VERIFICATA DA RAQ (firma) APPROVATA DA AMM (firma) PARAGRAFO REVISIONATO NUMERO MOTIVO 00 15-01-09 Prima emissione 01 22-04-13
WITNESS RELAXIN GENERALITÀ
 WITNESS RELAXIN WITNESS RELAXIN GENERALITÀ Il kit WITNESS RELAXIN è utilizzato nella diagnosi di gravidanza della cagna e della gatta e permette la distinzione tra gravidanza vera e pseudogravidanza nella
WITNESS RELAXIN WITNESS RELAXIN GENERALITÀ Il kit WITNESS RELAXIN è utilizzato nella diagnosi di gravidanza della cagna e della gatta e permette la distinzione tra gravidanza vera e pseudogravidanza nella
QUANTA Lite TM RNA Pol III Per uso diagnostico In Vitro Complessità CLIA: elevata
 QUANTA Lite TM RNA Pol III 704555 Per uso diagnostico In Vitro Complessità CLIA: elevata Finalità d uso Il test QUANTA Lite TM RNA Pol III ELISA è un dosaggio di immunoassorbimento enzimatico semiquantitativo
QUANTA Lite TM RNA Pol III 704555 Per uso diagnostico In Vitro Complessità CLIA: elevata Finalità d uso Il test QUANTA Lite TM RNA Pol III ELISA è un dosaggio di immunoassorbimento enzimatico semiquantitativo
Esperienza 14: il test ELISA
 Esperienza 14: il test ELISA La tecnica di dosaggio immuno-assorbente legato a un enzima (in inglese Enzyme-Linked Immuno Assay) o ELISA è principalmente utilizzato in immunologia al fine di rilevare e/o
Esperienza 14: il test ELISA La tecnica di dosaggio immuno-assorbente legato a un enzima (in inglese Enzyme-Linked Immuno Assay) o ELISA è principalmente utilizzato in immunologia al fine di rilevare e/o
ahbs ISTRUZIONI PER L USO VITROS Immunodiagnostic Products Confezione dei reagenti Anti-HBs
 ISTRUZIONI PER L USO VITROS Immunodiagnostic Products Confezione dei reagenti Anti-HBs ahbs 178 7753 Impiego Per la misura quantitativa in vitro dell anticorpo anti-hbs (antigene di superficie dell epatite
ISTRUZIONI PER L USO VITROS Immunodiagnostic Products Confezione dei reagenti Anti-HBs ahbs 178 7753 Impiego Per la misura quantitativa in vitro dell anticorpo anti-hbs (antigene di superficie dell epatite
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE
 RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
LIFECODES Quik-ID Class II test
 ISTRUZIONI PER L USO LIFECODES Quik-ID Class II test REF C2ID IVD INDICE USO... 2 RIASSUNTO E SPIEGAZIONE... 2 PRINCIPIO... 2 REAGENTI... 2 AVVERTENZE... 3 PRECAUZIONI... 3 RACCOLTA CAMPIONI... 3 PROCEDURA...
ISTRUZIONI PER L USO LIFECODES Quik-ID Class II test REF C2ID IVD INDICE USO... 2 RIASSUNTO E SPIEGAZIONE... 2 PRINCIPIO... 2 REAGENTI... 2 AVVERTENZE... 3 PRECAUZIONI... 3 RACCOLTA CAMPIONI... 3 PROCEDURA...
IN THE LA SOLUZIONE RAPIDA PER I SINTOMI DELL HERPES GENITALE
 HERPES IN THE CITY? NOVITÀ LA SOLUZIONE RAPIDA PER I SINTOMI DELL HERPES GENITALE Riduce sin dai primi giorni di applicazione i sintomi dolorosi dell Herpes Riduce gli altri sintomi soggettivi dell Herpes
HERPES IN THE CITY? NOVITÀ LA SOLUZIONE RAPIDA PER I SINTOMI DELL HERPES GENITALE Riduce sin dai primi giorni di applicazione i sintomi dolorosi dell Herpes Riduce gli altri sintomi soggettivi dell Herpes
test Circulating Tumor Cell Control Kit
 7900003 24 test Circulating Tumor Cell Control Kit 1 IMPIEGO PREVISTO Per uso diagnostico in vitro Il Kit CELLSEARCH Circulating Tumor Cell Control è stato formulato per essere utilizzato come controllo
7900003 24 test Circulating Tumor Cell Control Kit 1 IMPIEGO PREVISTO Per uso diagnostico in vitro Il Kit CELLSEARCH Circulating Tumor Cell Control è stato formulato per essere utilizzato come controllo
METODICHE DI IMMUNOCHIMICA
 METODICHE DI IMMUNOCHIMICA IMMUNOCHIMICA permette la determinazione quantitativa di proteine in tessuti e omogenati INTERAZIONI ANTIGENE-ANTICORPO L immunochimica si basa sulle interazioni antigene-anticorpo
METODICHE DI IMMUNOCHIMICA IMMUNOCHIMICA permette la determinazione quantitativa di proteine in tessuti e omogenati INTERAZIONI ANTIGENE-ANTICORPO L immunochimica si basa sulle interazioni antigene-anticorpo
Esercitazione 2 Colorazione di Gram
 Esercitazione 2 Colorazione di Gram 1) Mettere 10 µl di coltura batterica sul vetrino; con il puntale della pipetta distribuire uniformemente la sospensione batterica. 2) FISSAZIONE: far asciugare all
Esercitazione 2 Colorazione di Gram 1) Mettere 10 µl di coltura batterica sul vetrino; con il puntale della pipetta distribuire uniformemente la sospensione batterica. 2) FISSAZIONE: far asciugare all
Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP
 Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP Pag. 1 di 5 USO PREVISTO: Per uso diagnostico in vitro. DISPONIBILITÀ: Codice catalogo Quantità
Sistema di rilevazione dei polimeri MultiVision: Polimeri Multivision anti-coniglio/ HRP + anti-topo/ AP Pag. 1 di 5 USO PREVISTO: Per uso diagnostico in vitro. DISPONIBILITÀ: Codice catalogo Quantità
VEDI CAMBI RISALTATI. 2. CONJ CONIUGATO: 1 x 160 µl di anticorpi IgG di capra anti-igg umane coniugati con fosfatasi alcalina. Contiene sodio azide.
 VEDI CAMBI RISALTATI bioblot HIV-1 plus 3000-1467 18 tests Test qualitativo immunoenzimatico per il rilevamento in-vitro degli anticorpi del virus di immunodeficienza umana tipo 1 (HIV-1) e tipo 2 (HIV-2)
VEDI CAMBI RISALTATI bioblot HIV-1 plus 3000-1467 18 tests Test qualitativo immunoenzimatico per il rilevamento in-vitro degli anticorpi del virus di immunodeficienza umana tipo 1 (HIV-1) e tipo 2 (HIV-2)
VALUTAZIONE DEL POTERE BATTERICIDA (SANIFICANTE 10)
 VALUTAZIONE DEL POTERE BATTERICIDA (SANIFICANTE 10) 1. SCOPO Testare le capacità battericida del SANIFICANTE 10, detergente igienizzante a base di sali quaternari di ammonio, nelle condizioni di sporco
VALUTAZIONE DEL POTERE BATTERICIDA (SANIFICANTE 10) 1. SCOPO Testare le capacità battericida del SANIFICANTE 10, detergente igienizzante a base di sali quaternari di ammonio, nelle condizioni di sporco
RIDASCREEN ß-Agonists
 RIDASCREEN ß-Agonists Saggio immunoenzimatico per l analisi quantitativa dei β-agonisti Art. No.: R1704 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 /
RIDASCREEN ß-Agonists Saggio immunoenzimatico per l analisi quantitativa dei β-agonisti Art. No.: R1704 Test in vitro Conservare a 2-8 C R-Biopharm AG, Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 /
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
BEIA MEASLES IgM Capture
 BEIA MEASLES IgM Capture 20939000 Edizione 20/04/2013 Solo per uso professionale 96 N 00DMM Pag. 1-16 BEIA Measles IgM Capture Ed. 20/04/2013 INTRODUZIONE Il kit BEIA Measles IgM Capture è un test immunoenzimatico
BEIA MEASLES IgM Capture 20939000 Edizione 20/04/2013 Solo per uso professionale 96 N 00DMM Pag. 1-16 BEIA Measles IgM Capture Ed. 20/04/2013 INTRODUZIONE Il kit BEIA Measles IgM Capture è un test immunoenzimatico
