TRASTUZUMAB ( )
|
|
|
- Maria Teresa Carletti
- 6 anni fa
- Visualizzazioni
Transcript
1 TRASTUZUMAB ( ) Specialità: Herceptin (Roche) Forma farmaceutica: 1fl ev 150 mg - Prezzo: euro ATC: L01XC03 Categoria terapeutica: altri antineoplastici: anticorpi monoclonali Fascia di rimborsabilità: H OSP-2 Indicazioni ministeriali: Indicazioni Ministeriali: Carcinoma mammario metastatico con iperespressione di HER2: a. in monoterapia per il trattamento di pazienti che hanno ricevuto almeno due regimi chemioterapici per la malattia metastatica. La chemioterapia precedentemente somministrata deve aver contenuto almeno una antraciclina e un taxano, tranne nel caso in cui il paziente non sia idoneo a tali trattamenti. I pazienti positivi al recettore ormonale devono inoltre non aver risposto alla terapia ormonale, tranne nel caso in cui il paziente non sia idoneo a tali trattamenti. b. In associazione al paclitaxel per il trattamento di pazienti che non sono stati sottoposti a chemioterapia per la malattia metastatica e per i quali non è indicato il trattamento con antracicline. c. In associazione al docetaxel per il trattamento di pazienti che non sono stati sottoposti a chemioterapia per la malattia metastatica. Carcinoma mammario in fase iniziale: Herceptin è indicato nel trattamento di pazienti con carcinoma mammario in fase iniziale HER-2-positivo dopo chirurgia, chemioterapia (neoadiuvante o adiuvante) e radioterapia (se applicabile). Herceptin deve essere utilizzato soltanto in pazienti affetti da tumore con iperespressione di HER2 o con amplificazione del gene HER2 o come determinato mediante un test accurato e convalidato. Decisioni PTORV Data riunione: Decisione: Allargamento indicazioni Nota Ufficiale: Nuova nota PTORV: Trattamento di pazienti con: Carcinoma mammario metastatico con iperespressione di HER2: a. In monoterapia per il trattamento di pazienti che hanno ricevuto almeno due regimi chemioterapici per la malattia metastatica. La chemioterapia precedentemente somministrata deve avere contenuto almeno 1 antraciclina e 1 taxano, tranne nel caso in cui il pz non sia idoneo a tali trattamenti. I pz positivi al recettore ormonale devono inoltre aver risposto alla terapia ormonale, tranne nel caso in cui il pz non sia idoneo a tali trattamenti. b. In associazione al paclitaxel per il trattamento di pazienti che non sono stati sottoposti a chemioterapia per la malattia metastatica e per il quali non è indicato il trattamento con antracicline. c. In associazione al docetaxel per il trattamento di pazienti che non sono stati sottoposti a chemioterapia per la malattia metastatica. Carcinoma mammario in fase iniziale HER2 positivo dopo chirurgia, chemioterapia (neoadiuvante o adiuvante) e radioterapia (se applicabile) nelle pazienti con sovraespressione del recettore HER 2 con compilazione scheda monitoraggio nazionale. Commenti: Gli studi pubblicati riportano solo dati a breve termine e rimangono pertanto incertezze sulla efficacia e sicurezza a lungo termine. Anche le linee guida del NICE riportano che il farmaco non dovrebbe essere utilizzato in pazienti con problemi di funzionalità cardiaca. Pertanto è opportuno solo l utilizzo in sequenza fermo restando che si deve essere in presenza di una sovrespressione del recettore HER 2 (cosa che avviene in circa il 10 15% delle pazienti).
2 Scheda di monitoraggio AIFA: Ai fini del monitoraggio delle prescrizioni, i centri utilizzatori dovranno compilare la scheda raccolta dati informatizzata, secondo le indicazioni pubblicate sul sito La scheda va compilata solo per l indicazione adiuvante. Analisi della letteratura Trastuzumab è un anticorpo monoclonale ricombinante umanizzato, con elevata affinità di legame per la proteina HER 2 ed in grado di inibirne gli effetti sulla trasformazione cellulare maligna a livello dei tessuti epiteliali, utilizzato per il trattamento di pazienti con carcinoma mammario metastatico con iperespressione di HER-2. Con Determinazione del 15 Dicembre 2005, l Agenzia Italiana del Farmaco ha inserito tale farmaco nell elenco dei medicinali erogabili a totale carico del Servizio Sanitario Nazionale, ai sensi dell articolo 1, comma 4, del decreto-legge 21 ottobre 1996, n. 536, convertito dalla legge 23 dicembre 1996, n. 648, per l indicazione terapeutica: trattamento adiuvante del carcinoma mammario operato HER-2 positivo [1]. Recentemente è stato, tuttavia, approvato l impiego di trastuzumab per il trattamento di pazienti con carcinoma mammario in fase iniziale HER-2-positivo dopo chirurgia, chemioterapia (neoadiuvante o adiuvante) e radioterapia (se applicabile) [2]. Tale farmaco deve essere utilizzato soltanto in pazienti affetti da tumore con iperespressione di HER-2 o con amplificazione del gene HER-2 determinato mediante un test accurato e convalidato. Ai fini del monitoraggio delle prescrizioni, i centri utilizzatori dovranno compilare la scheda raccolta dati informatizzata, secondo le indicazioni pubblicate sul sito scheda già prevista dalla precedente determinazione. L efficacia e la tollerabilità di trastuzumab nel carcinoma mammario in fase iniziale sono state valutate dall EMEA in 4 studi clinici, uno dei quali non è ancora stato pubblicato [3]. Uno studio randomizzato di fase III, multicentrico, in aperto, a gruppi paralleli (studio HERA - HERceptin Adjuvant) ha confrontato il trattamento con trastuzumab, somministrato in adiuvante per uno o due anni, e la sola osservazione, in pazienti con carcinoma mammario in fase iniziale HER-2-positivo dopo chirurgia, chemioterapia standard e radioterapia [4]. In questo studio, 5081 pazienti sono state assegnate in modo casuale all osservazione (n=1.693) o al trattamento con trastuzumab (8 mg/kg come dose di carico e poi 6 mg/kg ogni 3 settimane come dose di mantenimento) per 1 anno (n=1.694) o per 2 anni (n=1.694). Le pazienti avevano un adenocarcinoma operabile, primario, e invasivo della mammella, con linfonodi ascellari positivi o linfonodi ascellari negativi (tumore di dimensioni superiori a 1 cm), e avevano completato la terapia locoregionale (chirurgia con o senza radioterapia) e un minimo di 4 cicli di chemioterapia adiuvante e/o neoadiuvante. Le pazienti dovevano presentare una iperespressione HER-2 diagnosticata mediante un esame immuno-istochimico (IHC) di sezioni tumorali fissate e/o amplificazione del gene HER-2 riscontrata mediante ibridazione in situ tramite fluorescenza (FISH). Infine, sono state incluse nello studio pazienti che, una volta completate chemioterapia e radioterapia, presentavano una frazione d eiezione del ventricolo sinistro maggiore del 55%. Sono state, quindi, escluse pazienti con problemi cardiaci (documentata storia di insufficienza cardiaca congestizia, patologie coronariche con precedente infarto miocardico con onde Q, angina pectoris che richiedeva trattamento farmacologico, ipertensione-non controllata, patologie valvolari clinicamente significative e aritmie instabili). Come end point primario di efficacia è stata considerata la sopravvivenza libera da malattia, definita come il periodo intercorso tra la randomizzazione e l insorgenza di uno dei seguenti eventi: recidiva locale, regionale o distale del carcinoma, sviluppo di carcinoma mammario controlaterale, compreso il carcinoma duttale in situ o di patologie maligne non mammarie oppure morte senza documentazione di uno di questi eventi. Come end-point secondari sono stati considerati la sopravvivenza complessiva, la sopravvivenza libera da recidiva e la sopravvivenza libera da malattia a distanza, effettuando un confronto tra il gruppo trattato con trastuzumab per un anno e il gruppo di osservazione nonché tra il gruppo trattato con trastuzumab per 2 anni e il gruppo di osservazione. Infine, è stata valutata la tollerabilità di trastuzumab, prestando particolare attenzione all incidenza di disfunzioni cardiache nei pazienti trattati con trastuzumab e nei pazienti non trattati. L analisi ad interim, effettuata sulla popolazione intention to treat, ha confrontato il gruppo trattato con trastuzumab per un anno e il gruppo di osservazione ma, essendo lo studio ancora in corso, non è stato effettuato un confronto con il gruppo trattato per 2 anni. Nell analisi ad interim (follow up mediano di 1 anno) sono stati, quindi, osservati 347 eventi di cui 127 nel gruppo trattato con trastuzumab per un anno e 220 nel gruppo di osservazione. Relativamente all end-point primario, l hazard ratio nel gruppo trastuzumab rispetto al gruppo osservazione era di 0.54 (95% IC, , p<0.0001), rappresentando un beneficio assoluto in
3 termini di sopravvivenza libera da malattia a 2 anni pari a 8.4 punti percentuali a favore del braccio trattato con trastuzumab. Relativamente agli end-point secondari, nella analisi ad interim, tra il gruppo trattato con trastuzumab per un anno e il gruppo di osservazione non si sono riscontrate differenze statisticamente significative nella sopravvivenza complessiva. Sono state, invece, riscontrate differenze statisticamente significative tra i due bracci per quanto riguarda la sopravvivenza libera da recidiva e la sopravvivenza libera da malattia a distanza. Per quanto riguarda la tollerabilità, l incidenza di eventi avversi gravi e di eventi avversi di grado 3 o 4 secondo la classificazione NCI-CTC (National Cancer Institute - Common Toxicity Criteria) è stata maggiore nel gruppo trastuzumab rispetto al gruppo osservazione. Complessivamente, sono stati registrati 6 eventi fatali nel gruppo trastuzumab e 3 nel gruppo osservazione; 143 pazienti (8.5%) nel gruppo trastuzumab non hanno portato a termine il trattamento per diversi motivi. Una severa cardiotossicità si è sviluppata nel 0.5% delle donne trattate con trastuzumab. L incidenza di insufficienza cardiaca congestizia sintomatica è stata di 1.7 % nel gruppo trastuzumab e 0.06 % nel gruppo osservazione e nel 7.1% dei pazienti del gruppo trastuzumab è stata riscontrata una diminuzione del LVEF. I ricercatori dello studio HERA hanno, inoltre, valutato l effetto del farmaco sulla sopravvivenza generale dopo un periodo osservazionale mediano di 2 anni. L analisi è stata effettuata sulle 1703 donne trattate con trastuzumab per un anno e 1698 donne del gruppo di controllo, con un follow up mediano di 23,5 mesi (0-48 mesi): 58 pazienti (3.4%) trattate per 1 anno con trastuzumab e 97 pazienti (5.7%) del gruppo di controllo sono andate perse durante il periodo di follow-up, 172 pazienti hanno interrotto prematuramente la terapia con trastuzumab e 149 donne sono decedute (59 nel gruppo trastuzumab e 90 nel gruppo controllo). L hazard ratio non aggiustato per il rischio di morte con trastuzumab, rispetto alla sola osservazione, è stato 0.66 ( 95% IC, ; p = ). Nel gruppo trastuzumab sono stati riportati 218 eventi di sopravvivenza libera da malattia, vs i 321 nel gruppo controllo. L HR non aggiustato per il rischio di un evento con trastuzumab, rispetto alla sola osservazione, è stato 0.64 ( p < ). I risultati hanno, quindi, mostrato che il trattamento della durata di 1 anno con trastuzumab dopo chemioterapia adiuvante era associato ad un beneficio significativo sulla sopravvivenza generale [5] Due studi randomizzati di fase III (studio NSABP B-31 e studio NCCTG N9831) hanno valutato l efficacia e la tollerabilità del trattamento adiuvante con trastuzumab in pazienti con carcinoma mammario operato chirurgicamente HER-2 positivo [6]. Le pazienti incluse in tali studi presentavano un adenocarcinoma mammario con una iperespressione HER-2 diagnosticata mediante un esame immuno-istochimico (IHC) di sezioni tumorali fissate (score immunochimico 3+) e/o amplificazione del gene HER-2 riscontrata mediante ibridazione in situ tramite fluorescenza (FISH). Sono state escluse donne con evidenze cliniche o radiologiche di metastasi e pazienti con problemi cardiaci. Lo studio NSABP B-31 (National Surgical Adjuvant Breast and Bowel Project trial B-31) ha confrontato doxorubicina 60 mg/m² e ciclofosfamide 600 mg/m² somministrate ogni 21 giorni per 4 cicli seguita da paclitaxel 175 mg/m² ogni 3 settimane per 4 cicli (gruppo 1) con lo stesso regime chemioterapico associato, però, a trastuzumab settimanale (4 mg/kg come dose di carico e 2 mg/kg come dose di mantenimento) somministrato per 52 settimane a partire dalla prima dose di paclitaxel (gruppo 2). In questo studio sono stati arruolate 2043 pazienti affette da carcinoma mammario con linfonodi ascellari positivi, di cui 1024 assegnate al gruppo 1 e 1019 al gruppo 2. Lo studio NCCTG N9831 (North Central Cancer Treatment Group trial N9831) ha confrontato 3 regimi: doxorubicina 60 mg/m² e ciclofosfamide 600 mg/m² somministrate ogni 21 giorni per 4 cicli seguita da paclitaxel settimanale 80 mg/m² per 12 settimane (gruppo A), lo stesso regime chemioterapico seguito da trastuzumab (4 mg/kg come dose di carico la prima settimana e 2 mg/kg come dose di mantenimento settimanali per 51 settimane) somministrato una volta completata la terapia con paclitaxel (gruppo B), e lo stesso regime chemioterapico seguito da trastuzumab (4 mg/kg come dose di carico la prima settimana e 2 mg/kg come dose di mantenimento settimanali per 51 settimane) iniziato in concomitanza a paclitaxel (gruppo C). In questo studio sono stati arruolate 2766 pazienti ad alto rischio di recidiva, di cui 819 sono state assegnate al gruppo A e 814 al gruppo C. I gruppi di controllo dei due studi, come pure il gruppo 2 dello studio NSABP B-31 e il gruppo C dello studio NCCTG N9831, pur differendo nello schema di somministrazione di paclitaxel e per certi aspetti della terapia ormonale e della radioterapia praticata, erano complessivamente molto simili. È stata, pertanto, effettuata, una analisi combinata dei risultati, confrontando i gruppi 1 e A (controllo) con i gruppi 2 e C (gruppo trastuzumab), per valutare l effetto dell aggiunta di trastuzumab, iniziato in concomitanza a paclitaxel, alla chemioterapia. Il gruppo B dello studio NCCTG N9831, è stato escluso dalla analisi, in quanto il protocollo prevedeva la somministrazione di trastuzumab solo una volta completata la chemioterapia. Come end-point primario è stata considerata la sopravvivenza libera da malattia mentre come end-point secondari sono stati considerati la sopravvivenza complessiva, la sopravvivenza libera da recidiva e la sopravvivenza libera da malattia a distanza.
4 L analisi ad interim è stata condotta sulle pazienti per le quali era disponibile almeno una valutazione di follow-up (1.672 nel gruppo trastuzumab e nel controllo). In tale analisi (follow up mediano di 2.0 anni) sono stati osservati 394 eventi di cui 133 nel gruppo trastuzumab e 261 nel controllo. L hazard ratio per un primo evento nel gruppo trastuzumab rispetto al placebo era di 0.48 (95% IC, , p<0.0001). La terapia con trastuzumab è stata associata ad una riduzione del 33 % del rischio di morte (HR= 0.67; 95% IC, , p=0.015) e ad aumento della sopravvivenza libera da malattia a distanza (HR=0.47;95% IC, , p<0.0001). L uso di trastuzumab è associato a cardiotossicità [6,7]. L incidenza cumulativa di insufficienza cardiaca congestizia di grado III o IV secondo la New York Heart Association o morte per cause cardiache a 3 anni è risultata, nel gruppo trastuzumab, pari a 4.1 % (vs 0.8% nel controllo) nello studio B-31 e 2.9 % (vs 0% nel controllo) nel trial N9831. Uno studio clinico randomizzato di fase III (studio BCIRG Breast Cancer International Research Group) ha, infine, valutato il beneficio di 2 regimi terapeutici a base di trastuzumab in pazienti con carcinoma mammario HER-2 positivo [7,8]. In questo studio pazienti con tumore mammario HER2 positivo sono state randomizzate a ricevere doxorubicina 60 mg/m² + ciclofosfamide 600 mg/m² somministrate ogni 21 giorni per 4 cicli seguite da docetaxel 100 mg/m² ogni 3 settimane per 4 cicli (AC-T, n=1.073), oppure lo stesso regime chemioterapico + trastuzumab somministrato settimanalmente (ad un dosaggio non specificato nell abstract) durante la terapia con docetaxel e, quindi, ogni 3 settimane per un anno (AC-TH, n=1.074) oppure docetaxel 75 mg/m² + carboplatino AUC 6 somministrati ogni 3 settimane per 6 cicli + trastuzumab somministrato settimanalmente durante la chemioterapia e, quindi, ogni 3 settimane per un anno (TCH, n=1.075). Come end-point primario di efficacia è stata considerata la sopravvivenza libera da malattia. End-point secondari erano la sopravvivenza complessiva, sicurezza, compresa la cardiotossicità. Nell analisi ad interim (follow up mediano di 23 mesi) ogni braccio trattato con trastuzumab ha migliorato in maniera significativa la sopravvivenza libera da malattia rispetto al controllo. L hazard ratio per AC-TH vs AC-T e per TCH vs AC-T erano, rispettivamente, 0.49 (95% IC, , p<0.0001) e 0.61 (95% IC, , p=0.0002). Non sono state, invece, rilevate differenze tra i due gruppi trattati con trastuzumab. L incidenza di eventi cardiaci clinicamente significativi (morte, insufficienza cardiaca congestizia o ischemia cardiaca di grado 3 o 4, infarto e aritmie) è risultata di 0.95% nel braccio AC-T, 2.34% nel braccio AC-TH e 1.33% nel braccio TCH, con significatività statistica raggiunta solo per AC-TH vs AC-T (p=0.016). In un recente studio, condotto su 1010 pazienti per confrontare docetaxel e vinorelbina nel trattamento adiuvante del carcinoma mammario precoce, le 232 donne che presentavano tumori con sovraespressione di HER2/neu sono state ulteriormente randomizzate a ricevere o meno nove infusioni di trastuzumab con cadenza settimanale [10]. Come end-point primario è stata considerata la sopravvivenza libera da recidive. In questo studio, rispetto alla vinorelbina, il trattamento adiuvante con docetaxel ha mostrato di migliorare la sopravvivenza libera da recidive per le donne con carcinoma mammario precoce e un breve ciclo di trattamento con trastuzumab, somministrato in concomitanza con docetaxel o vinorelbina, è risultato efficace per le donne con un tumore mammario con sovraespressione di HER2/neu. Le linee guida del NICE raccomandano l utilizzo di trastuzumab per il trattamento delle donne con tumore mammario HER2-positivo in fase precoce, con l eccezione delle donne con problemi di funzionalità cardiaca [11]. In particolare, trastuzumab, somministrato ad intervalli di 3 settimane per 1 anno o fino a recidiva della malattia, viene raccomandato come opzione di trattamento per le donne con tumore mammario HER2- positivo in fase precoce dopo intervento chirurgico, chemioterapia (neoadiuvante o adiuvante ) e radioterapia (se applicabile); Prima di iniziare la terapia con trastuzumab, deve essere valutata la funzionalità cardiaca della paziente. Devono essere, infatti, escluse dal trattamento le pazienti con frazione di eiezione ventricolare sinistra LVEF 55%, o che presentano storia di insufficienza cardiaca congestizia documentata, aritmie ad alto rischio non-controllate, angina pectoris che richiede trattamento farmacologico, malattia vascolare clinicamente significativa, evidenza di infarto trasmurale all ECG, ipertensione scarsamente controllata. Durante il trattamento con trastuzumab le valutazioni della funzione cardiaca dovrebbero essere ripetute ogni 3 mesi e il farmaco dovrebbe essere sospeso qualora la LVEF scendesse al di sotto del 50%. La decisione di riprendere l assunzione di trastuzumab dovrebbe essere basata su ulteriori valutazioni della funzionalità cardiaca e del rapporto rischio-beneficio. L approvazione di trastuzumab per il trattamento di pazienti con carcinoma mammario in fase iniziale HER-2-positivo dopo chirurgia, chemioterapia e radioterapia ha, tuttavia, suscitato alcune perplessità nelle riviste scientifiche.
5 Un editoriale pubblicato sulla rivista The Lancet ha, infatti, criticato il giudizio estremamente positivo sull utilizzo di trastuzumab nelle fasi precoci del tumore alla mammella, espresso dalla rivista NEJM [12, 13]. Secondo il The Lancet gli studi clinici pubblicati sul NEJM hanno impiegato regimi posologici diversi, rendendo difficile i confronti e le conclusioni. L utilizzo della analisi congiunta degli studi NSABP B-31 e NCCTG N9831, inoltre, potrebbe far pensare che nessuno dei due trial, valutato singolarmente, avrebbe fornito un risultato positivo. I confronti sarebbero, poi, ostacolati dalla omissione di dati cruciali di sopravvivenza complessiva, di sopravvivenza libera da malattia e di cardiotossicità. In conclusione, le evidenze disponibili non sarebbero sufficienti per trarre conclusioni definitive. A questo editoriale sono seguite delle critiche [14, 15]. In particolare, è stata sottolineata la presenza dei dati di cardiotossicità in entrambi gli articoli, nonché l indicazione, nella appendice dell articolo di Romond (disponibile on line), dei dati di sopravvivenza libera da malattia relativi ai singoli studi NSABP B-31 e NCCTG N9831, i cui risultati sono sovrapponibili [16]. Sintesi: Trastuzumab è un anticorpo monoclonale ricombinante umanizzato, con elevata affinità di legame per la proteina HER 2 ed in grado di inibirne gli effetti sulla trasformazione cellulare maligna a livello dei tessuti epiteliali, recentemente approvato per il trattamento di pazienti con carcinoma mammario in fase iniziale HER-2-positivo dopo chirurgia, chemioterapia (neoadiuvante o adiuvante) e radioterapia (se applicabile). I dati clinici disponibili nella terapia del carcinoma mammario in fase iniziale sono relativi a 4 studi, uno dei quali non è ancora stato pubblicato. L obiettivo principale di questi studi era dimostrare l efficacia del trattamento, determinata dalla sopravvivenza libera da malattia. In questi studi la terapia adiuvante con trastuzumab ha dimostrato di apportare una riduzione significativa del rischio di recidiva: l HR della sopravvivenza libera da malattia era pari a 0.54 (95% IC, , p<0.0001) nello studio HERA e pari a 0.48 (95% IC, , p<0.0001) nell analisi congiunta degli studi NSABP B-31 e NCCTG N9831. In tale analisi è stata, inoltre, riscontrata una differenza statisticamente significativa nella sopravvivenza complessiva (HR= 0.67; 95% IC, , p=0.015), non riscontrata, peraltro, nello studio HERA. L efficacia e la sicurezza non sono state dimostrate nella patologia con linfonodi ascellari negativi di dimensioni 1 cm, generalmente considerati a basso rischio, e nelle pazienti con problemi cardiaci. Gli studi pubblicati riportano, inoltre, dati a breve termine, con una osservazione mediana di 2 anni nell analisi congiunta degli studi americani (il cui disegno non era in ogni caso completamente sovrapponibile) e di 1 solo anno nello studio HERA, mentre rimangono incertezze in merito alla efficacia e alla sicurezza e l efficacia a lungo termine. Inoltre, tali studi suggeriscono un incremento della tossicità cardiaca nelle pazienti trattate con trastuzumab; tale tossicità viene riportata come severa nello 0.5% delle pazienti nello studio HERA e tra il 2.9% e il 4.1% delle pazienti nella analisi congiunta degli studi NSABP B-31 e NCCTG N9831. I ricercatori dello studio HERA hanno, inoltre, valutato l effetto del farmaco sulla sopravvivenza generale dopo un follow up mediano di 2 anni. I risultati di tale analisi hanno mostrato che il trattamento della durata di 1 anno con trastuzumab dopo chemioterapia adiuvante era associato ad un beneficio significativo sulla sopravvivenza generale. Le linee guida del NICE raccomandano l impiego di trastuzumab per il trattamento delle donne con tumore mammario HER2-positivo in fase precoce, con l eccezione delle donne con problemi di funzionalità cardiaca. Bibliografia 1. Determinazione AIFA 15/12/2005. (accesso del 25/08/2006) 2. G.U. n.177 del 1 agosto Trastuzumab (Herceptin ). European Public Assessment Report - Scientific Discussion. (accesso del 25/08/2006) 4. Piccart-Gebhar MJ, et al. N Eng J Med. 2005;353: Smith I, et al. Lancet. 2007; 369: Romond EH, et al. N Eng J Med. 2005;353 (16): Tan - Chiu E, et al. J Clin Oncol 2005; 23: Slamon D, et al. Abstract Drugdex Micromedex vol Joensuu H, et al. N Eng J Med. 2006; 354: National Institute for Clinical Excellence. Breast Cancer (early) Trastuzumab (Herceptin ) Lancet 2005; 366: Hortobagyi GN. N Eng J Med. 2005; 353: Smith I. Lancet 2006; 367: Bryant J. Lancet 2006; 367: 728.
6 16.
7 Costi Principio attivo Trastuzumab Somministrazione ogni 3 settimane Trastuzumab Somministrazione settimanale Dosaggio da scheda tecnica 8 mg/kg la prima settimana seguito da 6 mg/kg ogni 3 settimane 4 mg/kg la prima settimana seguito da 2 mg/kg la settimana Costo all ospedale per 52 settimane di trattamento* (per una donna di 60 kg) ^ *Prezzo fornito dalla ditta (Marzo 2007) ^ nel caso si arrotondasse per difetto il numero di fiale somministrate ogni 21 gg il costo di un anno di trattamento sarebbe pari a Ultima revisione del testo: Marzo 2007
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
ERLOTINIB ( )
 ERLOTINIB (17-10-2006) Specialità: Tarceva (Roche) Forma Farmaceutica: 30 cpr Dosaggio: 100mg Prezzo: 2.596,41 30 cpr Dosaggio: 150mg Prezzo: 3.239,24 Prezzo al pubblico da banca dati Farmadati Marzo 2007
ERLOTINIB (17-10-2006) Specialità: Tarceva (Roche) Forma Farmaceutica: 30 cpr Dosaggio: 100mg Prezzo: 2.596,41 30 cpr Dosaggio: 150mg Prezzo: 3.239,24 Prezzo al pubblico da banca dati Farmadati Marzo 2007
Specialità: Mabthera (Roche SpA) Forma farmaceutica: 1fl ev 500mg - Prezzo: euro fl 10ml 100mg - Prezzo: euro
 RITUXIMAB Linfoma non-hodgkin: La terapia di mantenimento per pazienti con linfoma follicolare ricaduto/refrattario che rispondono a terapia di induzione con chemioterapia con o senza Rituximab. (09-01-2007)
RITUXIMAB Linfoma non-hodgkin: La terapia di mantenimento per pazienti con linfoma follicolare ricaduto/refrattario che rispondono a terapia di induzione con chemioterapia con o senza Rituximab. (09-01-2007)
MONOGRAFIA SINTESI. IBRANCE (palbociclib) Carcinoma Mammario. A cura della Commissione Terapeutica Oncologica
 MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
Sinossi Protocollo Sperimentale GOIM 21002
 1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
Trastuzumab. Il primo anticorpo monoclonale per il tumore della mammella HER 2 positivo
 Trastuzumab Il primo anticorpo monoclonale per il tumore della mammella HER 2 positivo Cos è trastuzumab? Trastuzumab è un anticorpo monoclonale studiato per individuare e bloccare le funzioni del recettore
Trastuzumab Il primo anticorpo monoclonale per il tumore della mammella HER 2 positivo Cos è trastuzumab? Trastuzumab è un anticorpo monoclonale studiato per individuare e bloccare le funzioni del recettore
Studio SENIORS Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza
 Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
LA TERAPIA DELLA MALATTIA METASTATICA
 IL TUMORE DELLA MAMMELLA: CONOSCERE PER DECIDERE LA TERAPIA DELLA MALATTIA METASTATICA Chiara Saggia SCDU Oncologia AOU Maggiore della Carità, Novara Torino, 8 marzo 2011 IL CARCINOMA MAMMARIO METASTATICO
IL TUMORE DELLA MAMMELLA: CONOSCERE PER DECIDERE LA TERAPIA DELLA MALATTIA METASTATICA Chiara Saggia SCDU Oncologia AOU Maggiore della Carità, Novara Torino, 8 marzo 2011 IL CARCINOMA MAMMARIO METASTATICO
DAL SAN ANTONIO BREAST CANCER SYMPOSIUM. Diversi studi dimostrano l'efficacia di varie combinazioni di medicinali, in aggiunta alla chemioterapia
 DAL SAN ANTONIO BREAST CANCER SYMPOSIUM Cocktail di farmaci per il tumore del seno DAL SAN ANTONIO BREAST CANCER SYMPOSIUM Diversi studi dimostrano l'efficacia di varie combinazioni di medicinali, in aggiunta
DAL SAN ANTONIO BREAST CANCER SYMPOSIUM Cocktail di farmaci per il tumore del seno DAL SAN ANTONIO BREAST CANCER SYMPOSIUM Diversi studi dimostrano l'efficacia di varie combinazioni di medicinali, in aggiunta
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE. Reggio Emilia 4 giugno 2008
 O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
EFFICACIA E TOLLERANZA DEL TRASTUZUMAB ADIUVANTE NEL TRATTAMENTO DEL CARCINOMA MAMMARIO IN FASE INIZIALE: ESPERIENZA DELL UNIVERSITÀ DI FIRENZE
 XXIII CONGRESSO NAZIONALE AIRO Taormina, 26-29 O/obre 2013 EFFICACIA E TOLLERANZA DEL TRASTUZUMAB ADIUVANTE NEL TRATTAMENTO DEL CARCINOMA MAMMARIO IN FASE INIZIALE: ESPERIENZA DELL UNIVERSITÀ DI FIRENZE
XXIII CONGRESSO NAZIONALE AIRO Taormina, 26-29 O/obre 2013 EFFICACIA E TOLLERANZA DEL TRASTUZUMAB ADIUVANTE NEL TRATTAMENTO DEL CARCINOMA MAMMARIO IN FASE INIZIALE: ESPERIENZA DELL UNIVERSITÀ DI FIRENZE
13.30 Introduzione al corso Dr.ssa Agnese Fabbri Dr.ssa Ida Paris
 Carcinoma mammario her 2 positivo in fase metastatica: la sequenza terapeutica dall algoritmo alla pratica clinica Hotel Ripa Roma, Roma 15 giugno 2018 Ble & Associates srl id. 5357 numero ecm 227755,
Carcinoma mammario her 2 positivo in fase metastatica: la sequenza terapeutica dall algoritmo alla pratica clinica Hotel Ripa Roma, Roma 15 giugno 2018 Ble & Associates srl id. 5357 numero ecm 227755,
CA GASTRICO E CASI CLINICI. Gli strumenti di governo clinico e la vigilanza da parte della farmacia febbraio 2012 Bologna
 3 corso regionale per farmacisti, tecnici e infermieri dell area oncologica. Schemi terapeutici in oncologia : prescrizione, allestimento e somministrazione CA GASTRICO E CASI CLINICI Gli strumenti di
3 corso regionale per farmacisti, tecnici e infermieri dell area oncologica. Schemi terapeutici in oncologia : prescrizione, allestimento e somministrazione CA GASTRICO E CASI CLINICI Gli strumenti di
DOCETAXEL ( )
 DOCETAXEL (20-12-2007) Specialità: Taxotere (Sanofi Aventis SpA) Forma Farmaceutica: Soluzione per infusione Dosaggio: 20mg/0.5ml Prezzo: 222.00 80mg/2ml Prezzo: 828.97 Prezzo da banca dati Farmadati Novembre
DOCETAXEL (20-12-2007) Specialità: Taxotere (Sanofi Aventis SpA) Forma Farmaceutica: Soluzione per infusione Dosaggio: 20mg/0.5ml Prezzo: 222.00 80mg/2ml Prezzo: 828.97 Prezzo da banca dati Farmadati Novembre
CASI EMBLEMATICI. Daniela Boggiani U.O.C. Oncologia Medica Azienda Ospedaliero-Universitaria di Parma. Martedì dell' Ordine Parma, 15 Maggio 2018
 CASI EMBLEMATICI Daniela Boggiani U.O.C. Oncologia Medica Azienda Ospedaliero-Universitaria di Parma Martedì dell' Ordine Parma, 15 Maggio 2018 Caso Clinico (1) Giugno 2017: donna di 36 anni con autoriscontro
CASI EMBLEMATICI Daniela Boggiani U.O.C. Oncologia Medica Azienda Ospedaliero-Universitaria di Parma Martedì dell' Ordine Parma, 15 Maggio 2018 Caso Clinico (1) Giugno 2017: donna di 36 anni con autoriscontro
Coordinatori Michela Cinquini, Simon Spazzapan. Presentatori Valentina Fanotto, Marta Pestrin, Alessia Levaggi
 2- QUESITO GRADE: Nelle pazienti con carcinoma mammario triplo negativo, candidate a chemioterapia neoadiuvante, è raccomandabile un regime contenente platino? Coordinatori Michela Cinquini, Simon Spazzapan
2- QUESITO GRADE: Nelle pazienti con carcinoma mammario triplo negativo, candidate a chemioterapia neoadiuvante, è raccomandabile un regime contenente platino? Coordinatori Michela Cinquini, Simon Spazzapan
LA TERAPIA ORMONALE NEL CA AVANZATO DELLA MAMMELLA. Istruzioni per la compilazione delle schede pazienti
 LA TERAPIA ORMONALE NEL CA AVANZATO DELLA MAMMELLA Istruzioni per la compilazione delle schede pazienti COME SI COLLABORA Lo studio ha l obiettivo di analizzare le terapie ormonali in pazienti con carcinoma
LA TERAPIA ORMONALE NEL CA AVANZATO DELLA MAMMELLA Istruzioni per la compilazione delle schede pazienti COME SI COLLABORA Lo studio ha l obiettivo di analizzare le terapie ormonali in pazienti con carcinoma
II SESSIONE: TERAPIA DELLA MALATTIA IN FASE PRECOCE LA RADIOTERAPIA COMPLEMENTARE ALESSANDRO GAVA RADIOTERAPIA ONCOLOGICA TREVISO
 II SESSIONE: TERAPIA DELLA MALATTIA IN FASE PRECOCE LA RADIOTERAPIA COMPLEMENTARE ALESSANDRO GAVA RADIOTERAPIA ONCOLOGICA TREVISO RUOLO RADIOTERAPIA INDICAZIONI ALLA RADIOTERAPIA RADIOTERAPIA DOPO CHIRURGIA
II SESSIONE: TERAPIA DELLA MALATTIA IN FASE PRECOCE LA RADIOTERAPIA COMPLEMENTARE ALESSANDRO GAVA RADIOTERAPIA ONCOLOGICA TREVISO RUOLO RADIOTERAPIA INDICAZIONI ALLA RADIOTERAPIA RADIOTERAPIA DOPO CHIRURGIA
Il trattamento oncologico
 Il trattamento oncologico 369.000 nuovi casi 177.000 (46%) circa 500 donne ogni giorni ricevono la diagnosi di cancro 25 Novembre 2017 Nel 2017, sono oltre 3 milioni e trecentomila (3.304.648) gli italiani
Il trattamento oncologico 369.000 nuovi casi 177.000 (46%) circa 500 donne ogni giorni ricevono la diagnosi di cancro 25 Novembre 2017 Nel 2017, sono oltre 3 milioni e trecentomila (3.304.648) gli italiani
IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI. Dott.ssa T. Tamburrano Dirigente Medico Oncologia A.O. Marche Nord
 IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI Fano 11-12 Novembre 2016 TUMORE DELLA PROSTATA-MALATTIA METASTATICA- LA TERAPIA DELLA MALATTIA ORMONOSENSIBILE Dott.ssa T. Tamburrano Dirigente
IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI Fano 11-12 Novembre 2016 TUMORE DELLA PROSTATA-MALATTIA METASTATICA- LA TERAPIA DELLA MALATTIA ORMONOSENSIBILE Dott.ssa T. Tamburrano Dirigente
Specialità: Herceptin (Roche spa) Forma farmaceutica:
 TRASTUZUMAB per l'indicazione: in associazione ad un inibitore dell aromatasi nel trattamento di pazienti in postmenopausa affetti da carcinoma mammario metastatico positivo per i recettori ormonali, non
TRASTUZUMAB per l'indicazione: in associazione ad un inibitore dell aromatasi nel trattamento di pazienti in postmenopausa affetti da carcinoma mammario metastatico positivo per i recettori ormonali, non
SINOSSI DEL PROTOCOLLO
 Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
Storia naturale del tumore della mammella. diagnosi. +/-trattamento/i. preclinica. nascita del tumore. diagnosi. exitus. clinica
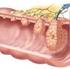 Storia naturale del tumore della mammella diagnosi preclinica +/-trattamento/i? nascita del tumore diagnosi clinica exitus Trattamento carcinoma della mammella chirurgia radioterapia terapia medica MASSIMO
Storia naturale del tumore della mammella diagnosi preclinica +/-trattamento/i? nascita del tumore diagnosi clinica exitus Trattamento carcinoma della mammella chirurgia radioterapia terapia medica MASSIMO
Sesto San Giovanni, 26 settembre 2015
 Sesto San Giovanni, 26 settembre 2015 TUMORI DELLA MAMMELLA: TERAPIA MEDICA Dr. Claudio Vergani U. O. di Oncologia P. O. Città di Sesto Sesto S. Giovanni - Milano TERAPIA MEDICA Adiuvante: - in fase postoperatoria
Sesto San Giovanni, 26 settembre 2015 TUMORI DELLA MAMMELLA: TERAPIA MEDICA Dr. Claudio Vergani U. O. di Oncologia P. O. Città di Sesto Sesto S. Giovanni - Milano TERAPIA MEDICA Adiuvante: - in fase postoperatoria
APREPITANT ( )
 APREPITANT (20-06-2006) Specialità: Emend (Merck Sharp & Dohme) Forma farmaceutica: 1 cps da 125mg + 2 cps da 80mg - Prezzo: 88,77 Prezzo d banca dati Farmadati Novembre 2006 ATC: A04AD12 Categoria terapeutica:
APREPITANT (20-06-2006) Specialità: Emend (Merck Sharp & Dohme) Forma farmaceutica: 1 cps da 125mg + 2 cps da 80mg - Prezzo: 88,77 Prezzo d banca dati Farmadati Novembre 2006 ATC: A04AD12 Categoria terapeutica:
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR ERLOTINIB
 RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
Alberto Bortolami. Coordinamento Rete Oncologica del Veneto - ROV
 Alberto Bortolami Coordinamento Rete Oncologica del Veneto - ROV Obiettivi Rete Oncologica del Veneto (DGR n. 2067 del 19 novembre 2013) Definire e condividere i Percorsi Diagnostici Terapeutici (PDTA)
Alberto Bortolami Coordinamento Rete Oncologica del Veneto - ROV Obiettivi Rete Oncologica del Veneto (DGR n. 2067 del 19 novembre 2013) Definire e condividere i Percorsi Diagnostici Terapeutici (PDTA)
SCLC - terapia di ii linea 53 II LINEA - RISULTATI E LIMITII
 SCLC - terapia di ii linea TRATTAMENTO STANDARD IN 53 II LINEA - RISULTATI E LIMITII SCLC - terapia di ii linea trattamento standard in ii linea - risultati e limiti Quasi la totalità dei pazienti affetti
SCLC - terapia di ii linea TRATTAMENTO STANDARD IN 53 II LINEA - RISULTATI E LIMITII SCLC - terapia di ii linea trattamento standard in ii linea - risultati e limiti Quasi la totalità dei pazienti affetti
Neoplasie della mammella - 2
 Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
SSD Cardiologia SCD Ematologia AORN Santobono Pausilipon Napoli
 SSD Cardiologia SCD Ematologia AORN Santobono Pausilipon Napoli Anthracycline-induced cardiomyopathy in paediatric patients: early echocardiographic detection and long term follow-up after early treatment
SSD Cardiologia SCD Ematologia AORN Santobono Pausilipon Napoli Anthracycline-induced cardiomyopathy in paediatric patients: early echocardiographic detection and long term follow-up after early treatment
STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO
 Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
Studio AMAROS SOMMARIO
 Studio AMAROS SOMMARIO Studio di fase III il cui principale obiettivo è dimostrare nelle pazienti con metastasi ai linfonodi ascellari, diagnosticate tramite biopsia con linfonodo sentinella, equivalente
Studio AMAROS SOMMARIO Studio di fase III il cui principale obiettivo è dimostrare nelle pazienti con metastasi ai linfonodi ascellari, diagnosticate tramite biopsia con linfonodo sentinella, equivalente
EMR Merck KGaA, Darmstadt, Germania. Fase clinica IIIb
 1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Perjeta 420 mg concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Perjeta 420 mg concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino
Bevacizumab e Cetuximab nel cancro colorettale metastastico in donne e uomini: Studio Multicentrico Retrospettivo in Toscana
 Bevacizumab e Cetuximab nel cancro colorettale metastastico in donne e uomini: Studio Multicentrico Retrospettivo in Toscana L. Bazzani, E. Terzuoli, S. Giorgi, G. Francini, L. Antonuzzo, F. Di Costanzo,
Bevacizumab e Cetuximab nel cancro colorettale metastastico in donne e uomini: Studio Multicentrico Retrospettivo in Toscana L. Bazzani, E. Terzuoli, S. Giorgi, G. Francini, L. Antonuzzo, F. Di Costanzo,
Oncology Division, Breats Unit Ospedale Perrino, Brindisi, Italy Phone: Fax: Versione n.
 A phase II study of metronomic oral chemotherapy with cyclophosphamide plus capecitabine combined with trastuzumab in advanced breast cancer (GOIM 2905) Oncology Division, Breats Unit Ospedale Perrino,
A phase II study of metronomic oral chemotherapy with cyclophosphamide plus capecitabine combined with trastuzumab in advanced breast cancer (GOIM 2905) Oncology Division, Breats Unit Ospedale Perrino,
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna
 PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO ADIUVANTE DEI TUMORI DELLA MAMMELLA RACCOMANDAZIONI sull impiego del trastuzumab in terapia adiuvante nelle pazienti
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO ADIUVANTE DEI TUMORI DELLA MAMMELLA RACCOMANDAZIONI sull impiego del trastuzumab in terapia adiuvante nelle pazienti
Metastasi cerebrali: Trattamento. Jennifer Foglietta Oncologia Medica - Perugia
 Metastasi cerebrali: Trattamento Jennifer Foglietta Oncologia Medica - Perugia Controllare i sintomi neurologici Trattamento delle metastasi cerebrali 1. Locale Radioterapia panencefalica (WBRT) Chirurgia
Metastasi cerebrali: Trattamento Jennifer Foglietta Oncologia Medica - Perugia Controllare i sintomi neurologici Trattamento delle metastasi cerebrali 1. Locale Radioterapia panencefalica (WBRT) Chirurgia
LA STRATEGIA TERAPEUTICA ADIUVANTE. Luciano Galletto
 I TUMORI DEL CORPO DELL UTERO: STRATEGIE TERAPEUTICHE IN EVOLUZIONE Torino, 26 Febbraio 2010 LA STRATEGIA TERAPEUTICA ADIUVANTE Luciano Galletto Proporzione dei tumori del corpo dell utero vs proporzione
I TUMORI DEL CORPO DELL UTERO: STRATEGIE TERAPEUTICHE IN EVOLUZIONE Torino, 26 Febbraio 2010 LA STRATEGIA TERAPEUTICA ADIUVANTE Luciano Galletto Proporzione dei tumori del corpo dell utero vs proporzione
SCHEDA FARMACO. Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Cabazitaxel (JEVTANA) SCHEDA FARMACO 60 mg - concentrato e solvente per soluzione per
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Cabazitaxel (JEVTANA) SCHEDA FARMACO 60 mg - concentrato e solvente per soluzione per
DIAGNOSI PRECOCE E TERAPIA DELLA CARDIOTOSSICITA DA FARMACI ANTITUMORALI
 DIAGNOSI PRECOCE E TERAPIA DELLA CARDIOTOSSICITA DA FARMACI ANTITUMORALI Dr. Carlo M Cipolla Divisione di Cardiologia Istituto Europeo di Oncologia - Milano ROMA, 25 GENNAIO 2013 1 Dimensioni del fenomeno
DIAGNOSI PRECOCE E TERAPIA DELLA CARDIOTOSSICITA DA FARMACI ANTITUMORALI Dr. Carlo M Cipolla Divisione di Cardiologia Istituto Europeo di Oncologia - Milano ROMA, 25 GENNAIO 2013 1 Dimensioni del fenomeno
IL RUOLO DEGLI ONCOLOGI NELL INNOVAZIONE E SOSTENIBILITA DEI TRATTAMENTI. Fausto Roila Oncologia Medica, Terni
 IL RUOLO DEGLI ONCOLOGI NELL INNOVAZIONE E SOSTENIBILITA DEI TRATTAMENTI Fausto Roila Oncologia Medica, Terni RUOLO DEGLI ONCOLOGI - Valutare criticamente l innovazione e distinguere: - reali novità terapeutiche
IL RUOLO DEGLI ONCOLOGI NELL INNOVAZIONE E SOSTENIBILITA DEI TRATTAMENTI Fausto Roila Oncologia Medica, Terni RUOLO DEGLI ONCOLOGI - Valutare criticamente l innovazione e distinguere: - reali novità terapeutiche
Interazione tra volume di trattamento e parametri clinici in brachiterapia della mammella ad alto rateo di dose (BRT-HDR)
 Interazione tra volume di trattamento e parametri clinici in brachiterapia della mammella ad alto rateo di dose (BRT-HDR) Dr.ssa Luigia Chirico S.C. Radioterapia Oncologica Direttore Dr. Ernesto Maranzano
Interazione tra volume di trattamento e parametri clinici in brachiterapia della mammella ad alto rateo di dose (BRT-HDR) Dr.ssa Luigia Chirico S.C. Radioterapia Oncologica Direttore Dr. Ernesto Maranzano
STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab. Sinossi del protocollo
 1 STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab Sinossi del protocollo Titolo Protocollo: Studio di fase II con doxorubicina liposomiale più ciclofosfamide in associazione a trastuzumab,
1 STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab Sinossi del protocollo Titolo Protocollo: Studio di fase II con doxorubicina liposomiale più ciclofosfamide in associazione a trastuzumab,
REPORT HTA REGIONALE. Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO
 REPORT HTA REGIONALE Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO fd Commenti: si tratta di un nuovo biosimilare di filgrastim, la cui efficacia è stata dimostrata da uno studio randomizzato
REPORT HTA REGIONALE Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO fd Commenti: si tratta di un nuovo biosimilare di filgrastim, la cui efficacia è stata dimostrata da uno studio randomizzato
ASSISTENZA AL PAZIENTE CON NEOPLASIA DELLA MAMMELLA
 ASSISTENZA AL PAZIENTE CON NEOPLASIA DELLA MAMMELLA Relatore: Biasotto Valentina 1 CRO Aviano SEDI DI MALATTIA La mammella è costituita da cute, tessuto adiposo, tessutto connettivo e tessuto ghiandolare.
ASSISTENZA AL PAZIENTE CON NEOPLASIA DELLA MAMMELLA Relatore: Biasotto Valentina 1 CRO Aviano SEDI DI MALATTIA La mammella è costituita da cute, tessuto adiposo, tessutto connettivo e tessuto ghiandolare.
Sinossi Protocollo LEGA Versione No. 1 Finale, 11 Novembre 2011
 1. SINOSSI 1.1. Identificativi del Protocollo Prodotto: Indicazione: Codice Protocollo: EudraCT No.: 2011-005537-39 Titolo dello Studio: 1.2. Razionale dello Studio Combinazioni chemioterapiche: Epirubicina
1. SINOSSI 1.1. Identificativi del Protocollo Prodotto: Indicazione: Codice Protocollo: EudraCT No.: 2011-005537-39 Titolo dello Studio: 1.2. Razionale dello Studio Combinazioni chemioterapiche: Epirubicina
Carcinoma mammario metastatico Herceptin è indicato per il trattamento di pazienti adulti con carcinoma mammario
 Inserimento, in accordo all articolo 12, comma 5 della Legge 189/2012, in apposita sezione (denominataclassec(nn))dedicataaifarmacinonancoravalutatiaifinidellarimborsabilitànelle more della presentazione
Inserimento, in accordo all articolo 12, comma 5 della Legge 189/2012, in apposita sezione (denominataclassec(nn))dedicataaifarmacinonancoravalutatiaifinidellarimborsabilitànelle more della presentazione
Criteri generali Semplici Riproducibili maniera omogenea Potenzialmente Realmente
 Criteri generali Semplici Riproducibili Rilevabili in maniera omogenea in tutte le regioni (e quindi confrontabili) Potenzialmente rilevabili Realmente rilevabili dai data base Le fasi del calcolo degli
Criteri generali Semplici Riproducibili Rilevabili in maniera omogenea in tutte le regioni (e quindi confrontabili) Potenzialmente rilevabili Realmente rilevabili dai data base Le fasi del calcolo degli
CARDIONCOLOGIA: dove siamo e dove andiamo. Il punto di vista del radioterapista: Maurizio Portaluri
 CARDIONCOLOGIA: dove siamo e dove andiamo Il punto di vista del radioterapista: Maurizio Portaluri Convegno II ZOOM JOURNAL CLUB 2012 - Roma, 25 gennaio 2013 Il danno cardiaco nella radioterapia del cancro
CARDIONCOLOGIA: dove siamo e dove andiamo Il punto di vista del radioterapista: Maurizio Portaluri Convegno II ZOOM JOURNAL CLUB 2012 - Roma, 25 gennaio 2013 Il danno cardiaco nella radioterapia del cancro
Rassegna Stampa. Comunicato stampa. Intermedia s.r.l. per la comunicazione integrata
 Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
SORAFENIB ( )
 SORAFENIB (28-02-2007) Specialità: Nexavar (Bayer SpA) Forma Farmaceutica: 112cpr riv Dosaggio: 200 mg Prezzo: 5.305,59 Prezzo da banca dati Farmadati Ottobre 2007 ATC: L01XE05 Categoria terapeutica: Farmaci
SORAFENIB (28-02-2007) Specialità: Nexavar (Bayer SpA) Forma Farmaceutica: 112cpr riv Dosaggio: 200 mg Prezzo: 5.305,59 Prezzo da banca dati Farmadati Ottobre 2007 ATC: L01XE05 Categoria terapeutica: Farmaci
Corso Formazione sul Carcinoma Mammario rivolto alle Associazioni Pazienti Trattamento Adiuvante e Neoadiuvante
 Corso Formazione sul Carcinoma Mammario rivolto alle Associazioni Pazienti Trattamento Adiuvante e Neoadiuvante Luisa Carbognin 1 University of Verona, Verona, Italy 2 Division of Gynecologic Oncology,
Corso Formazione sul Carcinoma Mammario rivolto alle Associazioni Pazienti Trattamento Adiuvante e Neoadiuvante Luisa Carbognin 1 University of Verona, Verona, Italy 2 Division of Gynecologic Oncology,
Radioterapia adiuvante dopo chirurgia conservativa: sempre a tutte le pazienti? Domenico Cante SC Radioterapia ASL TO4, Ospedale di Ivrea Direttore:
 Radioterapia adiuvante dopo chirurgia conservativa: sempre a tutte le pazienti? Domenico Cante SC Radioterapia ASL TO4, Ospedale di Ivrea Direttore: Maria Rosa La Porta -IPOFRAZIONAMENTO -RUOLO DEL BOOST
Radioterapia adiuvante dopo chirurgia conservativa: sempre a tutte le pazienti? Domenico Cante SC Radioterapia ASL TO4, Ospedale di Ivrea Direttore: Maria Rosa La Porta -IPOFRAZIONAMENTO -RUOLO DEL BOOST
Dipertimento di Urologia Università di Medicina e Chirurgia - Torino Ospedale S. Luigi Gonzaga - Orbassano (Torino), Italia
 Terapia combinata e chirurgia imaging-guidata nel trattamento del carcinoma prostatico Prof. F. Porpiglia Dipertimento di Urologia Università di Medicina e Chirurgia - Torino Ospedale S. Luigi Gonzaga
Terapia combinata e chirurgia imaging-guidata nel trattamento del carcinoma prostatico Prof. F. Porpiglia Dipertimento di Urologia Università di Medicina e Chirurgia - Torino Ospedale S. Luigi Gonzaga
Schema dello studio clinico di Fase 2b
 Sommario dei risultati dello studio clinico di Fase 2b di Ataluren presentato in occasione dell American Academy of Neurology Meeting il 16 Aprile 2010 Toronto, 16 Aprile 2010 - Un nuovo farmaco sperimentale
Sommario dei risultati dello studio clinico di Fase 2b di Ataluren presentato in occasione dell American Academy of Neurology Meeting il 16 Aprile 2010 Toronto, 16 Aprile 2010 - Un nuovo farmaco sperimentale
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs
 Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
IMRT POSTOPERATORIA ACCELERATA- IPOFRAZIONATA IN PAZIENTI ANZIANE (> 75 ANNI) AFFETTE DA CARCINOMA MAMMARIO: ANALISI SECONDARIA DI UN TRIAL DI FASE II
 IMRT POSTOPERATORIA ACCELERATA- IPOFRAZIONATA IN PAZIENTI ANZIANE (> 75 ANNI) AFFETTE DA CARCINOMA MAMMARIO: ANALISI SECONDARIA DI UN TRIAL DI FASE II M Massaccesi, C Digesù, S Cilla, G Macchia, F Deodato,
IMRT POSTOPERATORIA ACCELERATA- IPOFRAZIONATA IN PAZIENTI ANZIANE (> 75 ANNI) AFFETTE DA CARCINOMA MAMMARIO: ANALISI SECONDARIA DI UN TRIAL DI FASE II M Massaccesi, C Digesù, S Cilla, G Macchia, F Deodato,
Riduzione del colesterolo con simvastatina in pazienti ad alto rischio: risultati definitivi dello studio HPS
 Clinoscopio Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20.536 high-risk individuals: a randomised placebocontrolled trial. Lancet
Clinoscopio Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20.536 high-risk individuals: a randomised placebocontrolled trial. Lancet
IL NODO (tumorale) AL SENO: QUANDO LA TERAPIA FARMACOLOGICA?
 IL NODO (tumorale) AL SENO: QUANDO LA TERAPIA FARMACOLOGICA? Dr. Giorgio Bonciarelli Oncologia Medica Azienda ULSS17 Monselice, 8 Marzo 2014 ALCUNI NUMERI IN EUROPA In ITALIA, nel 2013, sono stati stimati
IL NODO (tumorale) AL SENO: QUANDO LA TERAPIA FARMACOLOGICA? Dr. Giorgio Bonciarelli Oncologia Medica Azienda ULSS17 Monselice, 8 Marzo 2014 ALCUNI NUMERI IN EUROPA In ITALIA, nel 2013, sono stati stimati
SCHEDA FARMACO. Principio attivo (nome commerciale) Ponatinib. (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Ponatinib SCHEDA FARMACO (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg Posologia: La dose
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Ponatinib SCHEDA FARMACO (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg Posologia: La dose
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
ONCOLOGIA MEDICA 1 A.O.U. San Giovanni Battista,TORINO
 ONCOLOGIA MEDICA 1 A.O.U. San Giovanni Battista,TORINO Il rapporto tra ormoni e carcinomi della mammella ormonodipendenti venne dimostrato per la prima volta nel 1896 da Beatson. L ovariectomia determinava
ONCOLOGIA MEDICA 1 A.O.U. San Giovanni Battista,TORINO Il rapporto tra ormoni e carcinomi della mammella ormonodipendenti venne dimostrato per la prima volta nel 1896 da Beatson. L ovariectomia determinava
MARGINI DI RESEZIONE: IMPATTO SULLA GESTIONE CHIRURGICA E RADIOTERAPICA. S.Giudici Struttura complessa di Radioterapia Ospedale di Sanremo
 MARGINI DI RESEZIONE: IMPATTO SULLA GESTIONE CHIRURGICA E RADIOTERAPICA S.Giudici Struttura complessa di Radioterapia Ospedale di Sanremo E rimarchevole il fatto che più di 25 anni dopo la dimostrazione
MARGINI DI RESEZIONE: IMPATTO SULLA GESTIONE CHIRURGICA E RADIOTERAPICA S.Giudici Struttura complessa di Radioterapia Ospedale di Sanremo E rimarchevole il fatto che più di 25 anni dopo la dimostrazione
PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/03/2017)
 POLMONE PROTOCOLLO TS-IRST PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/03/2017) Protocollo Descrizione protocollo Breve Sinossi Studio HighTySy randomizzato, di fase II, in aperto, disegnato per confrontare
POLMONE PROTOCOLLO TS-IRST PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 30/03/2017) Protocollo Descrizione protocollo Breve Sinossi Studio HighTySy randomizzato, di fase II, in aperto, disegnato per confrontare
Dati a confronto con placebo sull uso dei bifosfonati endovenosi Percentuale di pazienti con CS
 Complicanze scheletriche (CS) in pazienti con malattia neoplastica avanzata senza trattamento specifico Dati a confronto con placebo sull uso dei bifosfonati endovenosi Percentuale di pazienti con CS Media
Complicanze scheletriche (CS) in pazienti con malattia neoplastica avanzata senza trattamento specifico Dati a confronto con placebo sull uso dei bifosfonati endovenosi Percentuale di pazienti con CS Media
Federico Paolieri U.O. Oncologia Medica 2 Universitaria Azienda Ospedaliera-Universitaria Pisana
 Federico Paolieri U.O. Oncologia Medica 2 Universitaria Azienda Ospedaliera-Universitaria Pisana Once upon a time 1980s: Bepridil (calcio antagonista) riceve l approvazione per il trattamento dell angina
Federico Paolieri U.O. Oncologia Medica 2 Universitaria Azienda Ospedaliera-Universitaria Pisana Once upon a time 1980s: Bepridil (calcio antagonista) riceve l approvazione per il trattamento dell angina
Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti
 Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti Cuccaro F., Autelitano M., Bertù L., Randi G., Chiaffarino F., Ghilardi S., Leone R., Filipazzi L., Bonini
Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti Cuccaro F., Autelitano M., Bertù L., Randi G., Chiaffarino F., Ghilardi S., Leone R., Filipazzi L., Bonini
BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma mammario metastatico in combinazione con paclitaxel.
 BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma mammario metastatico in combinazione con paclitaxel. (09-09-2008) Specialità: Avastin(Roche spa) Forma farmaceutica:
BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma mammario metastatico in combinazione con paclitaxel. (09-09-2008) Specialità: Avastin(Roche spa) Forma farmaceutica:
MONOGRAFIA Sintesi. GAZYVARO (obinutuzumab) Linfoma follicolare II linea o successive
 MONOGRAFIA Sintesi GAZYVARO (obinutuzumab) Linfoma follicolare II linea o successive 1 A cura della Commissione Terapeutica Oncologica 2 1 SINTESI DELLA VALUTAZIONE «Gazyvaro» in associazione a bendamustina,
MONOGRAFIA Sintesi GAZYVARO (obinutuzumab) Linfoma follicolare II linea o successive 1 A cura della Commissione Terapeutica Oncologica 2 1 SINTESI DELLA VALUTAZIONE «Gazyvaro» in associazione a bendamustina,
RIASSUNTO DEL PROTOCOLLO
 RIASSUNTO DEL PROTOCOLLO Titolo: Studio a 2-corti di fase II, randomizzato a due dosi di BMS-275183 somministrato secondo una schedula settimanale continua in pazienti affetti da NSCLC già pretrattati.
RIASSUNTO DEL PROTOCOLLO Titolo: Studio a 2-corti di fase II, randomizzato a due dosi di BMS-275183 somministrato secondo una schedula settimanale continua in pazienti affetti da NSCLC già pretrattati.
Linfonodo sentinella. AJCC (6th edition 2002) Micrometastasi e ITC. Studi di Coorte. Assenza di metastasi linfonodali. pn0(i+)
 Dieci anni di linfonodo sentinella: un primo bilancio L. Mazzucchelli Istituto cantonale di patologia, Locarno Linfonodo sentinella Le metastasi linfonodali sono il fattore prognostico più importante per
Dieci anni di linfonodo sentinella: un primo bilancio L. Mazzucchelli Istituto cantonale di patologia, Locarno Linfonodo sentinella Le metastasi linfonodali sono il fattore prognostico più importante per
RITUXIMAB in associazione a metotressato è indicato per il trattamento dell artrite reumatoide attiva di grado severo in pazienti adulti.
 RITUXIMAB in associazione a metotressato è indicato per il trattamento dell artrite reumatoide attiva di grado severo in pazienti adulti. (28-02-2007) Specialità: Mabthera (Roche SpA) Forma farmaceutica:
RITUXIMAB in associazione a metotressato è indicato per il trattamento dell artrite reumatoide attiva di grado severo in pazienti adulti. (28-02-2007) Specialità: Mabthera (Roche SpA) Forma farmaceutica:
STUDIO GRUPPO ITALIANO PANCREAS GIP-2
 STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
SIEC. Napoli 16 aprile Follow-up ecocardiografico in soggetti trattati con chemioterapia: interrompere? Quando?
 SIEC Napoli 16 aprile 2011 Follow-up ecocardiografico in soggetti trattati con chemioterapia: interrompere? Quando? Patrizia Piotti & Carlo Materazzo UO Cardiologia Fondazione IRCCS - Istituto Nazionale
SIEC Napoli 16 aprile 2011 Follow-up ecocardiografico in soggetti trattati con chemioterapia: interrompere? Quando? Patrizia Piotti & Carlo Materazzo UO Cardiologia Fondazione IRCCS - Istituto Nazionale
EPIDEMIOLOGIA E MECCANISMI DEL DANNO CARDIACO
 INDICE EPIDEMIOLOGIA E MECCANISMI DEL DANNO CARDIACO EPIDEMIOLOGIA E MECCANISMI DELLA CARDIOTOSSICITÀ TERAPIA-CORRELATA G. Luca Frassineti Epidemiologia Lungo-sopravviventi Dose farmacologica e incidenza
INDICE EPIDEMIOLOGIA E MECCANISMI DEL DANNO CARDIACO EPIDEMIOLOGIA E MECCANISMI DELLA CARDIOTOSSICITÀ TERAPIA-CORRELATA G. Luca Frassineti Epidemiologia Lungo-sopravviventi Dose farmacologica e incidenza
L aggiornamento pubblicato nel marzo del 2007 è stato integrato con la pubblicazione della prima lista di farmaci essenziali ad uso pediatrico
 Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
CARCINOMA MAMMARIO - PRESENTAZIONE 2017
 CARCINOMA MAMMARIO - PRESENTAZIONE 2017 Abstract selezionati da: CONGRESSO ANNUALE DELL ASCO 2017 2-6 giugno 2017 Chicago, USA Sponsorizzato da Eli Lilly and Company. Eli Lilly and Company non ha influenzato
CARCINOMA MAMMARIO - PRESENTAZIONE 2017 Abstract selezionati da: CONGRESSO ANNUALE DELL ASCO 2017 2-6 giugno 2017 Chicago, USA Sponsorizzato da Eli Lilly and Company. Eli Lilly and Company non ha influenzato
Dott. Francesco Fiorica
 Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
TRASTUZUMAB EMTANSINE - KADCYLA
 giunta regionale Allegato B al Decreto n. 119 del 12 maggio 2015 pag. 1/9 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED TRASTUZUMAB EMTANSINE - KADCYLA Indicazione in esame: Trastuzumab
giunta regionale Allegato B al Decreto n. 119 del 12 maggio 2015 pag. 1/9 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED TRASTUZUMAB EMTANSINE - KADCYLA Indicazione in esame: Trastuzumab
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI SORAFENIB L01XE05 (Nexavar ) Presentata da Commissione Terapeutica Provinciale di Sassari In data gennaio 2009 Per le seguenti motivazioni: Sorafenib modifica lo standard
RICHIESTA DI INSERIMENTO IN PTR DI SORAFENIB L01XE05 (Nexavar ) Presentata da Commissione Terapeutica Provinciale di Sassari In data gennaio 2009 Per le seguenti motivazioni: Sorafenib modifica lo standard
TERAPIA MEDICA. Federica Grosso
 Federica Grosso # 230 nuovi casi/anno ~ 60 90 Provincia di Alessandria 33/100.000 anno CPO Piemonte Federica Grosso 2 INCIDENZA IN ITALIA 1.400 nuovi casi/anno UOMINI: 3,84/100.000 anno DONNE: 1,45/100.000
Federica Grosso # 230 nuovi casi/anno ~ 60 90 Provincia di Alessandria 33/100.000 anno CPO Piemonte Federica Grosso 2 INCIDENZA IN ITALIA 1.400 nuovi casi/anno UOMINI: 3,84/100.000 anno DONNE: 1,45/100.000
GISMa 2018 I nuovi numeri del GISMa, i nuovi percorsi, le nuove analisi
 GISMa 2018 I nuovi numeri del GISMa, i nuovi percorsi, le nuove analisi Valutare la qualità del percorso senologico su una scala regionale Antonio Giampiero Russo Unità di Epidemiologia Agenzia per la
GISMa 2018 I nuovi numeri del GISMa, i nuovi percorsi, le nuove analisi Valutare la qualità del percorso senologico su una scala regionale Antonio Giampiero Russo Unità di Epidemiologia Agenzia per la
SINOSSI. Studio di Fase II: Obiettivo primario Determinare l attività antitumorale della combinazione in termini di tempo alla progressione
 SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
Ca Duttale in Situ (DCIS)
 Ca Duttale in Situ (DCIS) unicentrico ampia exeresi margini negativi +/- radioterapia margini positivi nota 3 allargamento / mastectomia multicentrico mastectomia+ biopsia del linfonodo sentinella Nota
Ca Duttale in Situ (DCIS) unicentrico ampia exeresi margini negativi +/- radioterapia margini positivi nota 3 allargamento / mastectomia multicentrico mastectomia+ biopsia del linfonodo sentinella Nota
Linfonodo sentinella 10 anni dopo. L. Mazzucchelli Istituto cantonale di patologia, Locarno
 Linfonodo sentinella 10 anni dopo L. Mazzucchelli Istituto cantonale di patologia, Locarno Linfonodo sentinella Le metastasi linfonodali sono il fattore prognostico più importante per il carcinoma mammario
Linfonodo sentinella 10 anni dopo L. Mazzucchelli Istituto cantonale di patologia, Locarno Linfonodo sentinella Le metastasi linfonodali sono il fattore prognostico più importante per il carcinoma mammario
fd Decisioni CTR Data riunione: 17/04/2012 Decisione: Allargamento approvato, con compilazione della scheda di monitoraggio AIFA.
 REPORT HTA REGIONALE fd Decisioni CTR Data riunione: 17/04/2012 Decisione: Allargamento approvato, con compilazione della scheda di monitoraggio AIFA. CARATTERISTICHE DEL PRODOTTO PRINCIPIO ATTIVO: Lapatinib
REPORT HTA REGIONALE fd Decisioni CTR Data riunione: 17/04/2012 Decisione: Allargamento approvato, con compilazione della scheda di monitoraggio AIFA. CARATTERISTICHE DEL PRODOTTO PRINCIPIO ATTIVO: Lapatinib
Università del Piemonte Orientale. Corso di Laurea in Medicina e Chirurgia. Corso di Statistica Medica. I modelli di studio
 Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA
 Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Milano, 25 Marzo
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Milano, 25 Marzo
A cura di Marchese Rita
 A cura di Marchese Rita Abstract Obiettivo L ASTRO ha prodotto delle linee guida sulla radioterapia nel carcinoma squamoso dell orofaringe rilevanti anche per l ASCO che, dopo averle vagliate, ha optato
A cura di Marchese Rita Abstract Obiettivo L ASTRO ha prodotto delle linee guida sulla radioterapia nel carcinoma squamoso dell orofaringe rilevanti anche per l ASCO che, dopo averle vagliate, ha optato
Attività Scientifica AIOM Lazio
 Attività Scientifica AIOM Lazio 2016-2017 SURVEY FERTILITA E SESSUALITA IN ONCOLOGIA Società I taliana di Psico-Oncologia AIGO 237 Questionari 34% 66% Sesso 7% Femmine Maschi 16% 10% 67% Ospedale IRCCS
Attività Scientifica AIOM Lazio 2016-2017 SURVEY FERTILITA E SESSUALITA IN ONCOLOGIA Società I taliana di Psico-Oncologia AIGO 237 Questionari 34% 66% Sesso 7% Femmine Maschi 16% 10% 67% Ospedale IRCCS
BEVACIZUMAB - AVASTIN
 giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione
 Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
Mirko Di Martino. I trattamenti farmacologici nella prevenzione secondaria dell infarto miocardico acuto
 CONDIVISIONE DELLE LINEE GUIDA SUL TRATTAMENTO FARMACOLOGICO NELLA PREVENZIONE SECONDARIA DELL INFARTO MIOCARDICO ACUTO L aderenza alle linee guida per la prevenzione secondaria dell infarto miocardico
CONDIVISIONE DELLE LINEE GUIDA SUL TRATTAMENTO FARMACOLOGICO NELLA PREVENZIONE SECONDARIA DELL INFARTO MIOCARDICO ACUTO L aderenza alle linee guida per la prevenzione secondaria dell infarto miocardico
ALGORITMI E PERCORSI TERAPEUTICI CARCINOMA DELL OVAIO
 ALGORITMI E PERCORSI TERAPEUTICI CARCINOMA DELL OVAIO Aggiornamento: Luglio 2014 Carcinoma epiteliale dell ovaio TERAPIA Stadio clinico Standard Individualizzato Sperimentale IA IB G1 LIAB Omentectomia
ALGORITMI E PERCORSI TERAPEUTICI CARCINOMA DELL OVAIO Aggiornamento: Luglio 2014 Carcinoma epiteliale dell ovaio TERAPIA Stadio clinico Standard Individualizzato Sperimentale IA IB G1 LIAB Omentectomia
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Herceptin 150 mg polvere per concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Herceptin 150 mg polvere per concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 15/01/2018)
 POLMONE Studio EDEN PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 15/01/2018) Protocollo Descrizione protocollo Breve Sinossi Studio randomizzato di fase III, in aperto, di Nivolumab somministrato come terapia
POLMONE Studio EDEN PROTOCOLLI ATTIVI U.O. ONCOLOGIA IMOLA (al 15/01/2018) Protocollo Descrizione protocollo Breve Sinossi Studio randomizzato di fase III, in aperto, di Nivolumab somministrato come terapia
