ALDEIDI e CHETONI. Nu: sp 2. δ+ δ- C O C E + H acido ADDIZIONE NUCLEOFILA. Reazione caratteristica
|
|
|
- Michelina Nardi
- 4 anni fa
- Visualizzazioni
Transcript
1 ALDEIDI e ETNI Nu: sp 2 δ δ E acido eazione caratteristica ADDIZINE NULEFILA himica rganica e Laboratorio
2 Meccanismo: 1. Nu: Nu lento sp 2 (trigonale planare) sp 3 (tetraedrico) E Nu E generalmente E = 2. sp 2 (trigonale planare) himica rganica e Laboratorio :Nu lento Nu sp 3 (tetraedrico)
3 Sono reazioni di equilibrio isentono dell'effetto sterico isentono degli effetti elettronici dei sostituenti Sostituenti ad attrazione elettronica ENDN PIU' PSITIV il carbonilico FAVISN l'attacco del nucleofilo EATTIVITA' ESENTE ETNI < METILETNI < ALDEIDI < METANALE himica rganica e Laboratorio
4 a. NULEFILI ALL'SSIGEN 2 2 aldeide idrata 2 chetone idrato Meccanismo: : lento 2 himica rganica e Laboratorio
5 Meccanismo: : lento EMIAETALE esempi: La reazione può avvenire anche in modo intramolecolare: himica rganica e Laboratorio
6 Se la reazione con alcool si fa in ambiente AID ANID, prosegue: (*) ' 2 ' ' 2 (*) l (gas) AETALE " (*) l (gas) (*) ' 2 ' ' 2 " AETALE (ETALE) Meccanismo: ' ' come già descritto himica rganica e Laboratorio
7 '.. ' 2 ' '.. ' 3 3 ' ' ' ' on I chetoni (meno reattivi delle aldeidi) l equilibrio è spostato verso sinistra I chetoni danno chetali con equilibrio spostato verso destra solo se il nucleofilo è un diolo (1,2 o 1,3): la reazione è intramolecolare e si forma un anello stabile himica rganica e Laboratorio
8 Esempio di applicazione: come ottenere 2 da? 2 2 KMn 4 però, con KMn 4 : 2 KMn 4 himica rganica e Laboratorio
9 2 2 2 KMn , b. NULEFILI ALL ZLF S : S himica rganica e Laboratorio lento S S EMITIAETALE
10 esempi: S S S 3 S 2 3 Se la reazione con si fa in ambiente AID ANID, prosegue: S anidro S 2 3 TIAETALE S 2 3 on ditioli la reazione è intramolecolare quando si possono formare anelli stabili (5 e 6 termini).grado di.. S S himica rganica e Laboratorio S S S 2 S 2 2
11 2 S 2 S 2 2 S 2 S 2 2 S 2 2 S 2 S 2 2 S 2 TIAETALE (TIETALE) NaS 3 eazione di Bertagnini solo con aldeidi : S S reazione acidobase S Serve per purificare le aldeidi: l addotto precipita, si filtra, si torna ad aldeide himica rganica e Laboratorio
12 c. NULEFILI ALL AZT con i nucleofili all'azoto i prodotti di addizione perdono una molecola diacqua ammoniaca ed ammine primarie N 3, N 2 :N 3 N 2 N IMMINA (base di Schiff) 2.. 'N 2 N ' N ' 2 IMMINA (base di Schiff) Meccanismo: veloce himica rganica e Laboratorio
13 .. N 2 veloce 2 lento veloce N 2 veloce N N La velocità della reazione dipende dal p la velocità massima si ha a p 5 6 N 2 N 3 k 2.. N 5 6 p a p troppo acido manca il nucleofilo a p non abbastanza acido, la concentrazione di composto carbonilico protonato è troppo bassa himica rganica e Laboratorio
14 ammine secondarie 2 N 2 '.. 2 N ' 2 N 2 ' N 2 2 ENAMMINA Meccanismo: 2 veloce 2.. N lento N N veloce N 2 Esempi: 3 N 3 himica rganica e Laboratorio N 2, 2 N 3
15 3 ( 3 ) 2 N 2 N N 3 3 ammine terziarie 3 N 3 N 3 N NESSUNA EAZINE derivati dell'ammoniaca 2 NX X = 2.. N IDSSILAMMINA veloce himica rganica e Laboratorio 2.. N lento N
16 :N 2 2 N N SSIMA Esempio: N 2 N 2 N ossima della benzencarbaldeide N 3 2 N 3 2 N ossima del butanone himica rganica e Laboratorio
17 X = N N N 2 IDAZINA veloce.. 2 N N 2 lento N N 2 N 2 :N 2 2 N 2 N N N 2 IDAZNE Esempio: N N N N N N 2 idrazone del propanale himica rganica e Laboratorio
18 X = N 6 5 Nu.... N 2 N FENILIDAZINA veloce 2.. N N lento N N N :N 2 himica rganica e Laboratorio 2 N N N N FENILIDAZNE
19 Esempio: N N N N 2 fenilidrazone del fenil metil chetone N 2 N N N 2 fenilidrazone del butanale Nu N N N 2 2,4DINITFENILIDAZINA N 2 himica rganica e Laboratorio
20 N N N 2 N N N 2 N 2 N 2 2,4DINITFENILIDAZNE Esempio: 3 3 N 2 N N N 3 N N 2 N 2 N 2 2,4difenilfenilidrazone del del propanone himica rganica e Laboratorio
21 X = NN N N.. N 2 SEMIABAZIDE Nu 2.. N N.. N 2 2 N N N 2 SEMIABAZNE himica rganica e Laboratorio
22 d. NULEFILI AL ABNI N N N cianidrina N ' ' N cianidrina meccanismo: : N: lento :.. : : N: N: himica rganica e Laboratorio
23 Addizione di carbanioni (composti organometallici) MgX δ δ δ δ MgX MgX 2 ( ) Mg()X Esempi: MgBr MgBr MgI 3 MgI himica rganica e Laboratorio 3 2 MgI 3 MgI
24 Li δ esempio: δ 3 3 δ δ Li Li Li Li ( ) 2 Li() 3 3 FSFAN EAZINE DI WITTIG alogenoalcano trifenilfosfina base forte composto carbonilico ALENE himica rganica e Laboratorio
25 1. Sostituzione nucleofila 2 Br.. P S N 2 2 P Br sale di FSFNI (bromuro di alchiltrifenilfosfonio) 2. eazione acidobase base.. 2 P( 6 5 ) 3 P( 6 5 ) 3 P( 6 5 ) 3 FSFAN o ILIDE (yilide) Nu: BASE butillitio ( Li) oppure idruro di sodio (Na) IL FSF PU' ESPANDEE L'TTETT: stabilizza il carbanione 3. Addizione nucleofila.. P( 6 5 ) 3 ' " P( 6 5 ) 3 BETAINA " ' o FSFETAN himica rganica e Laboratorio
26 " ' P( 6 5 ) 3 fosfinossido "driving force (forza trainante) Il legame P è più forte del legame P Esempio: Br 3 1. :PPh 3 2. Na Na Br :PPh PPh PPh PPh PPh himica rganica e Laboratorio =PPh 3
27 Esempio: Br 3 1. :PPh Li PPh PPh NDENSAZINE ALDLIA % Na in 2 3 ALDL 2 himica rganica e Laboratorio
28 meccanismo: 1. reazione acidobase genera il nucleofilo α addizione nucleofila reazione acidobase la sua concentrazione non cambia himica rganica e Laboratorio
29 l'aldolo, sottoposto a riscaldamento, perde una molecola di acqua 3 2 Δ 2 3 doppio legame coniugato perché la condensazione aldolica possa avvenire, è necessario che l'aldeide abbia almeno un in α al carbonile per esempio: non reagiscono aldeidi con più dell'etanale, comunque danno il carbanione in α al carbonile 3 3 α 3 2 himica rganica e Laboratorio
30 3 δ 2 δ NDENSAZINE ALDLIA MISTA La reazione con due aldeidi, entrambe con in α, dà una miscela di prodotti himica rganica e Laboratorio
31 la condensazione aldolica mista (o incrociata) diventa utile quando una sola delle aldeidi ha un in α (precursore del nucleofilo). 3 2 nucleofilo himica rganica e Laboratorio
32 2 2 la coniugazione con l'anello benzenico facilita la disidratazione ATTENZINE! la condensazione aldolica in ambiente basico con i chetoni non avviene equilibrio spostato a sinistra i chetoni possono essere utilizzati come fonti di carbanioni in condensazioni miste con aldeidi senza in α EAZINE DI LAISENSMIDT nucleofilo himica rganica e Laboratorio
33 meccanismo: spontanea la coniugazione con l'anello benzenico facilita la disidratazione esempio: In questo caso, per avere disidratazione occorre SALDAE (meglio se in ambiente acido) Δ himica rganica e Laboratorio
34 EAZINE DI ANNIZZA Le aldeidi SENZA in α al carbonile possono reagire con Na, in condizioni più drastiche di quelle della condensazione aldolica (concentrazione più elevata di base, temperatura elevata) 2 Δ 3 eazione di disproporzione (un si ossida e un altro di riduce) meccanismo: 1. attacco nucleofilo al carbonilico δ δ annizzaro ( ) Questo EQUILIBI si ha anche nel caso della condensazione aldolica, ma in quel caso c è un altra strada (attraverso la base coniugata) che porta a himica prodotti rganica e quindi e Laboratorio questo equiibrio è come se non ci fosse.
35 2. trasferimento di idruro ( con gli elettroni di legame) δ /= δ 3. reazione acidobase 3 2 Danno la reazione di annizzaro tutte le aldeidi SENZA AIDI Di solito gli acidi sono in α al carbonile, ma NN NEESSAIAMENTE esempio: 2 ma:? acido! himica rganica e Laboratorio 3
36 ecc Nucleofilo condensazione aldolica himica rganica e Laboratorio 3
37 TAUTMEIA L'equilibrio tautomerico è catalizzato da acidi e da basi meccanismo in ambiente basico:.. 2 reazione acidobase ione enolato reazione acidobase enolo l'equilibrio è spostato verso la forma carbonilica % himica rganica e Laboratorio % % 0.10%
38 99.4% 0.06% l'equilibrio è spostato verso la forma enolica se ci sono fattori particolari che la stabilizzano % 80% stabilizzazione per legame idrogeno meccanismo in ambiente acido: 3 : 2 reazione acidobase reazione acidobase himica rganica e Laboratorio
39 Un chirale in α al carbonile in ambiente acido o basico racemizza * 3 3 * 3 * 3 (S) oppure (S) () IDUZINE 2, cat. idruro idruro = NaB 4, LiAl 4 (a) oppure (b) 2 (a) Zn(g), l lemmensen [] N 3 N 2 (b) N 2 N 2,, Δ WolffKischner himica rganica e Laboratorio
40 meccanismi: NaB 4 ADDIZINE NULEFILA Nu: = B 3 B N N 2 ADDIZINE NULEFILA Nu: = 2 NN N N 2 2 N N 2 Δ N N 2.. N 3 ADDIZINE NULEFILA Nu: = :N N 3 N Ni 2 N 2 idrogenazione catalitica himica rganica e Laboratorio
41 SSIDAZINE [] [] tutti gli ossidanti già visti con gli alcooli [] ' NESSUNA EAZINE Saggio di Tollens Ag(N 3 ) 2 Ag specchio d'argento gli αidrossichetoni possono dare un saggio positivo: Gottfried Tollens ' [2] ' Ag(N 3 ) 2 Ag himica rganica e Laboratorio
42 EAZINI IN ATENA LATEALE αalgenazine I chetoni vengono alogenati in α al carbonile. La reazione è promossa da basi oppure acidocatalizzata (Le aldeidi vengono ossidate dagli alogeni). promossa da basi: 3 3 Br 2 2 Br Br 2 Br 2 Br 2 la base si consuma 3 Br acidocatalizzata Br Br Br himica rganica e Laboratorio
43 Br 2 Br Br l'acido non si consuma La velocità dell'αalogenazione (sia in ambiente basico che in ambiente acido) NN dipende dalla concentrazione di alogeno. meccanismo della reazione promossa da basi: 3 3 lento Br Br 2 Br Br 3 himica rganica e Laboratorio
44 meccanismo della reazione acido catalizzata: lento 3 2 : Br Br Br Br 3 2 Br 3 2 Br himica rganica e Laboratorio
45 on i metilchetoni reazione dell'aloformio 3 con eccesso di alogeno e Na in acqua, 2 I I 2 3 iodoformio solido giallo meccanismo: I 2 I I I I I I Acidità maggiore di quella del metile I2 himica rganica e Laboratorio I2 I3 3 atomi di iodio (elettronegativi)
46 I3 I 3 :I 3 I 3 Si separa; giallo ATTENZINE!!! i possono essere falsi positivi I 2 ossidante anche composti diversi dai metilchetoni possono dare lo iodoformio (falsi positivi) se la molecola può essere ossidata dallo iodio a metilchetone 3 2 I 2 I 2 3 I 3 I 2 I I 3 himica rganica e Laboratorio
47 MPSTI ABNILI α,βinsatui 2 2 centro nucleofilo centro elettrofilo on reagenti elettrofili Addizione 1,2 e 1, Addizione 1,2 2 l l 2 Addizione 1,4 2 l l 2 2 himica rganica e Laboratorio
48 on reagenti nucleofili Addizione 1,2 e 1,4 2 3 N N 2 3 N 2 2 N 3 meccanismo: 1,4 2 N N N 3 2 N 2 N N N 3 1,2 2 3 N 2 3 N N 2 3 N N con nucleofili basi più forti è preferita l'addizione 1,2 (al =) himica rganica e Laboratorio
49 2 MgBr 3 3 MgI con nucleofili basi più deboli è preferita l'addizione 1,4 2 3 N N IDUZINE di composti carbonilici contenenti = 3 2 il prodotto dipende dal catalizzatore e dalle condizioni di reazione 2, Ni si riduce = NaB himica rganica e Laboratorio 2, Ni, Δ si riducono entrambi si riduce =
ALDEIDI e CHETONI. Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
 ALDEIDI e ETNI aratteristica strutturale di aldeidi e chetoni sp 2 legato a sp 2 = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con
ALDEIDI e ETNI aratteristica strutturale di aldeidi e chetoni sp 2 legato a sp 2 = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con
ALDEIDI e CHETONI. O sp 2 legato a C sp 2
 aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
Lezione: aldeidi e chetoni
 Lezione: aldeidi e chetoni Il gruppo funzionale carbonilico Nomenclatura Proprietà fisiche Principali reazioni eazioni con N eazioni con alcoli eazioni con tioli eazioni con ammine Tautomeria cheto-enolica
Lezione: aldeidi e chetoni Il gruppo funzionale carbonilico Nomenclatura Proprietà fisiche Principali reazioni eazioni con N eazioni con alcoli eazioni con tioli eazioni con ammine Tautomeria cheto-enolica
Aldeidi e Chetoni. Proprietà Chimico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami H Bassi pesi molecolari sono solubili in acqua
 Aldeidi e hetoni ' Gruppo carbonilico Aldeide hetone Proprietà himico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami Bassi pesi molecolari sono solubili in acqua Nomenclatura IUPA :
Aldeidi e hetoni ' Gruppo carbonilico Aldeide hetone Proprietà himico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami Bassi pesi molecolari sono solubili in acqua Nomenclatura IUPA :
Sostituzione nucleofila Addizione a gruppi carbonilici Addizione a doppi legami attivati
 himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
anidridi C R PREPARAZIONE DELLE ANIDRIDI + R C O - C Cl C R + P 2 O 5 C R C OH
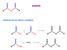 anidridi PEPAAZINE DELLE ANIDIDI l P 2 5 Nu = 2 Le anidridi sono più reattive di esteri ed ammidi: basta l acqua da sola : 2 2 2 2 EAZINI DELLE ANIDIDI: con acqua '.. ' ' ' ' EAZINI DELLE ANIDIDI: con
anidridi PEPAAZINE DELLE ANIDIDI l P 2 5 Nu = 2 Le anidridi sono più reattive di esteri ed ammidi: basta l acqua da sola : 2 2 2 2 EAZINI DELLE ANIDIDI: con acqua '.. ' ' ' ' EAZINI DELLE ANIDIDI: con
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Idrogeni in α a un carbonile
 Enoli e Enolati 1 Idrogeni in α a un carbonile Solo gli idrogeni α sono acidi Gli idrogeni β, γ e δ non sono acidi non possono essere rimossi da una base acido non acidi α β γ δ 2 Enoli Tutti i composti
Enoli e Enolati 1 Idrogeni in α a un carbonile Solo gli idrogeni α sono acidi Gli idrogeni β, γ e δ non sono acidi non possono essere rimossi da una base acido non acidi α β γ δ 2 Enoli Tutti i composti
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1
 CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
Esercitazione n. 15 - Reazioni e meccanismi di aldeidi e chetoni.
 Esercitazione n. 15 Reazioni e meccanismi di aldeidi e chetoni.. ompletare le equazioni chimiche per le reazioni del propanale con ciascuno dei seguenti reagenti: a) ab 4 (e poi ) a. ab 4 b. b) bromuro
Esercitazione n. 15 Reazioni e meccanismi di aldeidi e chetoni.. ompletare le equazioni chimiche per le reazioni del propanale con ciascuno dei seguenti reagenti: a) ab 4 (e poi ) a. ab 4 b. b) bromuro
Composti Carbonilici
 omposti arbonilici 1 Introduzione Due grandi classi di composti contengono il gruppo carbonilico: 1. omposti che hanno solo atomi di carbonio e di idrogeno legati al carbonile: aldeidi e chetoni. aldeidi
omposti arbonilici 1 Introduzione Due grandi classi di composti contengono il gruppo carbonilico: 1. omposti che hanno solo atomi di carbonio e di idrogeno legati al carbonile: aldeidi e chetoni. aldeidi
Composti carbonilici
 Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Esercitazione n Reazioni e meccanismi di aldeidi e chetoni.
 19. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene tra etanale e metanolo, in presenza di acidi. b) Spiegare come varia la reattività se con metanolo si fa reagire l'aldeide
19. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene tra etanale e metanolo, in presenza di acidi. b) Spiegare come varia la reattività se con metanolo si fa reagire l'aldeide
IDENTIFICAZIONE DEI COMPOSTI CARBONILICI C O
 IDENTIFIAZINE DEI MPSTI ABNILII Generalità Il gruppo carbonilico, caratteristico delle aldeidi e dei chetoni è polare, in quanto la nube elettronica del legame è attirata dall'atomo di ossigeno più elettronegativo.
IDENTIFIAZINE DEI MPSTI ABNILII Generalità Il gruppo carbonilico, caratteristico delle aldeidi e dei chetoni è polare, in quanto la nube elettronica del legame è attirata dall'atomo di ossigeno più elettronegativo.
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
Acidità degli Idrogeni α. IDROGENI α
 Acidità degli Idrogeni α ' α α IDGENI α 3 C C 2 + B B + 3 C C 2 3 C C 2 δ δ 3 C C 2 anione bidentato ANNE ENLAT NB: la stru+ura che più contribuisce all ibrido è quella con la carica nega:va sull ossigeno
Acidità degli Idrogeni α ' α α IDGENI α 3 C C 2 + B B + 3 C C 2 3 C C 2 δ δ 3 C C 2 anione bidentato ANNE ENLAT NB: la stru+ura che più contribuisce all ibrido è quella con la carica nega:va sull ossigeno
Composti carbonilici. Componente principale dell aceto. Principio attivo di molti farmaci. Resina per abbigliamento
 Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici: reazioni al carbonio in posizione a
 Composti carbonilici: reazioni al carbonio in posizione a Addizione nucleofila a composti carbonilici a,b-insaturi Nelle molecole contenenti carbonili coniugati con doppi legami sono presenti due siti
Composti carbonilici: reazioni al carbonio in posizione a Addizione nucleofila a composti carbonilici a,b-insaturi Nelle molecole contenenti carbonili coniugati con doppi legami sono presenti due siti
Unità Didattica 10. I composti carbonilici. Struttura, nomenclatura e reattività
 I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
14/11/2018. Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile.
 Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Composti carbonilici. Composti carbonilici. Componente principale dell aceto. Principio attivo di molti farmaci. Resina per abbigliamento
 Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
Composti carbonilici. Componente principale dell aceto. Principio attivo di molti farmaci. Resina per abbigliamento
 Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 L addizione coniugata In un sistema carbonilico α,β-insaturo dove avverà l attacco di un nucleofilo? Al carbonio carbonilico o al doppio legame? Il sistema ha due centri elettrofili: il carbonio carbonilico
L addizione coniugata In un sistema carbonilico α,β-insaturo dove avverà l attacco di un nucleofilo? Al carbonio carbonilico o al doppio legame? Il sistema ha due centri elettrofili: il carbonio carbonilico
ALDEIDI e CHETONI. O sp 2 legato a C sp 2. Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
 19/05/014 aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che
19/05/014 aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che
Reazioni degli Alogenuri Alchilici. Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici.
 Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
REATTIVITÀ DI R-XR M + R
 ... X.. M. M. M. M. M 2e- trasferiti dalla superficie metallica in 1 o 2 stadi EATTIVITÀ DI -X... X. -.. Ṙ.. - M + M + δ- δ+ -M nucleofilo -X elettrofilo 1) EAZIONE DI WUTZ -X + - Na + - + Na + X - 2)
... X.. M. M. M. M. M 2e- trasferiti dalla superficie metallica in 1 o 2 stadi EATTIVITÀ DI -X... X. -.. Ṙ.. - M + M + δ- δ+ -M nucleofilo -X elettrofilo 1) EAZIONE DI WUTZ -X + - Na + - + Na + X - 2)
ALCOOLI R-O-H C H. ... a. alcossido H C O - BASE H C O H + H C X. alcheni. a,d. ossidazione. aldeidi e chetoni. b b,c
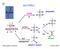 ALLI.. --.. BASE a - alcossido c d b.... a himica rganica e Laboratorio AID a,d ossidazione aldeidi e chetoni b b,c X alcheni ottura del legame SSTITUZINE NULEFILA Br Br 2 Br - 2 ELIMINAZINE 2 S 4 Δ 2
ALLI.. --.. BASE a - alcossido c d b.... a himica rganica e Laboratorio AID a,d ossidazione aldeidi e chetoni b b,c X alcheni ottura del legame SSTITUZINE NULEFILA Br Br 2 Br - 2 ELIMINAZINE 2 S 4 Δ 2
Composti Carbonilici. Aldeidi e Chetoni RCHO; RCRO
 omposti arbonilici Aldeidi e hetoni ; ALDEIDI e ETNI Sono caratterizzati dalla presenza del gruppo carbonilico che consiste in un atomo di carbonio legato con un doppio legame ad un atomo di ossigeno aldeide
omposti arbonilici Aldeidi e hetoni ; ALDEIDI e ETNI Sono caratterizzati dalla presenza del gruppo carbonilico che consiste in un atomo di carbonio legato con un doppio legame ad un atomo di ossigeno aldeide
Aldeidi e chetoni. Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni
 Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
AMMINE. con acidi RNH 2. con O come elettrofilo RNH 2 + H + + R NH 3 NESSUNA REAZIONE. atomo basico, atomo nucleofilo
 AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppo carbonilico. Aldeidi. Chetoni
 Gruppo carbonilico Aldeidi Chetoni Acetone Altri gruppi funzionali presentano il legame C=O In questi casi il C è legato ad un atomo elettronegativo: di conseguenza hanno una diversa reattività rispetto
Gruppo carbonilico Aldeidi Chetoni Acetone Altri gruppi funzionali presentano il legame C=O In questi casi il C è legato ad un atomo elettronegativo: di conseguenza hanno una diversa reattività rispetto
Esteri degli acidi carbossilici
 Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
La condensazione di Claisen
 La condensazione di Claisen Oltre alle aldeidi e chetoni anche gli esteri possono generare enolati e funzionare da elettrofili.. Quando un estere viene trattato con una base avviene una trasformazione
La condensazione di Claisen Oltre alle aldeidi e chetoni anche gli esteri possono generare enolati e funzionare da elettrofili.. Quando un estere viene trattato con una base avviene una trasformazione
ALDEIDI E CHETONI. Struttura e proprietà. Il gruppo carbonilico. Reattività dei composti carbonilici IL GRUPPO CARBONILICO C O R C
 Struttura e proprietà ALDEIDI E ETNI ALDEIDI E ETNI NTENGN IL GUPP ABNILI Molti altri composti presentano questo gruppo: Acili, acidi, esteri, ammidi, carboidrati, proteine Il gruppo carbonilico E il più
Struttura e proprietà ALDEIDI E ETNI ALDEIDI E ETNI NTENGN IL GUPP ABNILI Molti altri composti presentano questo gruppo: Acili, acidi, esteri, ammidi, carboidrati, proteine Il gruppo carbonilico E il più
Aldeidi e Chetoni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Alfa-alogenazionialogenazioni (sintesi aloformio)
 CHIMICA ACIDO-BASE DI COMPOSTI CARBONILICI Acidità: Acidità di acidi, ammidi, ammine. Effetti induttivi e di risonanza. Acidità CH Enoli/enolati Tautomeria cheto enolica (acido o base catalizzata) (isomerizzazioni
CHIMICA ACIDO-BASE DI COMPOSTI CARBONILICI Acidità: Acidità di acidi, ammidi, ammine. Effetti induttivi e di risonanza. Acidità CH Enoli/enolati Tautomeria cheto enolica (acido o base catalizzata) (isomerizzazioni
ALCHINI. legame π. Una frammentazione importante dà un valore m/z = 39, che corrisponde al carbocatione propargilico +. + R. +
 AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 9, che corrisponde al carbocatione propargilico.. 2 2 2 1-ottino 4-ottino
AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 9, che corrisponde al carbocatione propargilico.. 2 2 2 1-ottino 4-ottino
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
ALCHINI. Spettrometria di massa C CH 2 R. + CARATTERISTICA FUNZIONALE: legame π. Caratteristiche Spettrali
 AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 39, che corrisponde al carbocatione propargilico 2 +. +. + + 2 2 2
AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 39, che corrisponde al carbocatione propargilico 2 +. +. + + 2 2 2
Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri)
 CHIMICA ACIDO BASE DI COMPOSTI CARBONILICI Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri) Che altra reazione può avvenire al centro carbonilico
CHIMICA ACIDO BASE DI COMPOSTI CARBONILICI Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri) Che altra reazione può avvenire al centro carbonilico
Alcani. Idrogenazione degli alcheni. Riduzione degli areni H 2. /Pt H 3. Ni + 3 H C, 180 atm
 Sintesi Alcani Idrogenazione degli alcheni 2 /Pt 2 /Pt 3 3 iduzione degli areni Ni + 3 2 175, 180 atm Alcheni Deidroalogenazione degli alogenuri alchilici 3 α 3 X β 3 Disidratazione degli alcoli Idrogenazione
Sintesi Alcani Idrogenazione degli alcheni 2 /Pt 2 /Pt 3 3 iduzione degli areni Ni + 3 2 175, 180 atm Alcheni Deidroalogenazione degli alogenuri alchilici 3 α 3 X β 3 Disidratazione degli alcoli Idrogenazione
Composti carbonilici: 1) addizione nucleofila. 2) addizione nucleofila-eliminazione
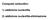 Composti carbonilici: 1) addizione nucleofila 2) addizione nucleofila-eliminazione È importante considerare se l atomo del gruppo legato alla funzione acilica è fortemente elettronegativo (caso degli acidi
Composti carbonilici: 1) addizione nucleofila 2) addizione nucleofila-eliminazione È importante considerare se l atomo del gruppo legato alla funzione acilica è fortemente elettronegativo (caso degli acidi
Si trovano generalmente come dimeri ciclici a causa dei legami a idrogeno
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura. alcano -> acido alcanoico
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
IDROCARBURI INSATURI: GLI ALCHENI HANNO ALMENO UN DOPPIO LEGAME NELLA STRUTTURA NOMENCLATURA: RADICE COME NEGLI IDROCARBURI, DESINENZA -ENE
 IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
Capitoli 18-20: reazione di addizione nucleofilo al gruppo carbonilico
 Capitoli 18-20: reazione di addizione nucleofilo al gruppo carbonilico Addizioni Nucleofile di Enolati a Composti Carbonilici L addizione di nucleofili come ossigeno, azoto, zolfo a composti carbonilici
Capitoli 18-20: reazione di addizione nucleofilo al gruppo carbonilico Addizioni Nucleofile di Enolati a Composti Carbonilici L addizione di nucleofili come ossigeno, azoto, zolfo a composti carbonilici
H H. R R δ+ R H. δ Cl
 Alogenuri alchilici: nomenclatura e reattività Nomenclatura: due possibilità a) Per gli alogenuri più semplici: residuo alchilico + nome dell alogeno (Es metilbromuro, etilbromuro). b) Per molecole più
Alogenuri alchilici: nomenclatura e reattività Nomenclatura: due possibilità a) Per gli alogenuri più semplici: residuo alchilico + nome dell alogeno (Es metilbromuro, etilbromuro). b) Per molecole più
L addizione coniugata
 L addizione coniugata In un sistema carbonilico α,β-insaturo dove avverà l attacco di un nucleofilo?? Al carbonio carbonilico o al doppio legame? Il sistema ha due centri elettrofili: : il carbonio carbonilico
L addizione coniugata In un sistema carbonilico α,β-insaturo dove avverà l attacco di un nucleofilo?? Al carbonio carbonilico o al doppio legame? Il sistema ha due centri elettrofili: : il carbonio carbonilico
Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, Nominativo.Matricola
 Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, 19-06-2017 Nominativo.Matricola Esercizio 1a. Il cis-2-pentene viene trattato con Br 2 in diclorometano. a) Descrivere
Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, 19-06-2017 Nominativo.Matricola Esercizio 1a. Il cis-2-pentene viene trattato con Br 2 in diclorometano. a) Descrivere
COMPOSTI AROMATICI POLICICLICI
 CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
Reazioni di aldeidi e chetoni
 Reazioni di aldeidi e chetoni www.pianetachimica.it Introduzione Il gruppo funzionale di aldeidi e chetoni è il carbonile ( terminale, nei chetoni si trova all interno della catena. pentanale aldeide ).
Reazioni di aldeidi e chetoni www.pianetachimica.it Introduzione Il gruppo funzionale di aldeidi e chetoni è il carbonile ( terminale, nei chetoni si trova all interno della catena. pentanale aldeide ).
Capitolo 12. Risposte alle Domande ed Esercizi a fine capitolo Le aldeidi e i chetoni più semplici sono facilmente idrosolubili poiché sono
 apitolo 12 Risposte alle Domande ed Esercizi a fine capitolo 12.1 Le aldeidi e i chetoni più semplici sono facilmente idrosolubili poiché sono in grado di formare legami a idrogeno intermolecolari con
apitolo 12 Risposte alle Domande ed Esercizi a fine capitolo 12.1 Le aldeidi e i chetoni più semplici sono facilmente idrosolubili poiché sono in grado di formare legami a idrogeno intermolecolari con
Mg-C. Δel = 1.3 C.I. = 34%
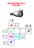 Mg-C Δel = 1.3 C.I. = 34% COMPOSTI ORGANOMETALLICI Sono composti che contengono un legame C-Metallo (R-M) dove R è un residuo organico e M un metallo monovalente (Na, Li) o bivalente (Mg). In genere il
Mg-C Δel = 1.3 C.I. = 34% COMPOSTI ORGANOMETALLICI Sono composti che contengono un legame C-Metallo (R-M) dove R è un residuo organico e M un metallo monovalente (Na, Li) o bivalente (Mg). In genere il
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI
 REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 MPSTI AMATII L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. aratteristiche Spettrali La maggior parte dei composti aromatici Spettrometria
MPSTI AMATII L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. aratteristiche Spettrali La maggior parte dei composti aromatici Spettrometria
S N. Reazioni di Sostituzione Nucleofila. Nucleofilo: Nu: + C X C + Nu + X - Sostituzione Nucleofila:
 Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
Composti carbonilici: Aldeidi Chetoni Acidi carbossilici Alogenuri acilici Esteri Ammidi Anidridi Nitrili
 Composti carbonilici: Aldeidi Chetoni Acidi carbossilici Alogenuri acilici Esteri Ammidi Anidridi Nitrili Struttura di composti carbonilici sp 2 sp 2 C = C H 3 C CH3 Il carbonile è un raggruppamento atomico
Composti carbonilici: Aldeidi Chetoni Acidi carbossilici Alogenuri acilici Esteri Ammidi Anidridi Nitrili Struttura di composti carbonilici sp 2 sp 2 C = C H 3 C CH3 Il carbonile è un raggruppamento atomico
AMMINE R'' H H C 2 H 5 C H C H C H NH 2 H H. azoto. alifatici o aliciclici. ammina primaria ammina secondaria ammina terziaria N CH 3
 AMMIE Si chiamano primarie le ammine che hanno un solo gruppo alchilico o aromatico legato all azoto azoto. Sono secondarie e terziarie le ammine al cui atomo di azoto sono legate, rispettivamente,, due
AMMIE Si chiamano primarie le ammine che hanno un solo gruppo alchilico o aromatico legato all azoto azoto. Sono secondarie e terziarie le ammine al cui atomo di azoto sono legate, rispettivamente,, due
+ + H 2 O NH 3 + H 3 2) NH 4 O + O + + CH 3 3) H 2 H H 3 O + CH 3. Esercitazione n Reazioni acido-base. ACIDO ACIDO ACIDO O + H H 2
 Esercitazione n. 10 Reazioni acidobase. 3. Nelle seguenti reazioni acidobase individuare l'acido e la base: 1) N : 3 2 N 4 2 2) N 4 2 N 3 3 3) 2 2 3 2 BASE 4) BASE AID AID AID BASE N N BASE AID 2 6) 5)
Esercitazione n. 10 Reazioni acidobase. 3. Nelle seguenti reazioni acidobase individuare l'acido e la base: 1) N : 3 2 N 4 2 2) N 4 2 N 3 3 3) 2 2 3 2 BASE 4) BASE AID AID AID BASE N N BASE AID 2 6) 5)
CHIMICA DEGLI IONI ENOLATO, ENOLI E COMPOSTI CARBONILICI COMPOSTI AROMATICI POLICONDENSATI. α,β LEZIONE 2
 CHIMICA DEGLI IONI ENOLATO, ENOLI E COMPOSTI CARBONILICI COMPOSTI AROMATICI POLICONDENSATI α,β -INSATURI LEZIONE 2 SINTESI DEL DIAZEPAM!???!!!! Mo te spiego ALCHILAZIONE DI ENOLATI Enolati: reattivi nucleofili
CHIMICA DEGLI IONI ENOLATO, ENOLI E COMPOSTI CARBONILICI COMPOSTI AROMATICI POLICONDENSATI α,β -INSATURI LEZIONE 2 SINTESI DEL DIAZEPAM!???!!!! Mo te spiego ALCHILAZIONE DI ENOLATI Enolati: reattivi nucleofili
ACIDI CARBOSSILCI e DERIVATI
 AIDI ABSSILI e DEIVATI aratteristica strutturale di acidi carbossilici e derivati aratteristiche Spettrali Spettrometria di massa Acidi carbossilici Lo ione molecolare di solito è spesso debole. La rottura
AIDI ABSSILI e DEIVATI aratteristica strutturale di acidi carbossilici e derivati aratteristiche Spettrali Spettrometria di massa Acidi carbossilici Lo ione molecolare di solito è spesso debole. La rottura
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Ammine. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Stabilità. 1. più sostituito = più stabile. 2. trans più stabile del cis; E più stabile del Z. II. Relazione struttura-reattività R C R R R
 Alcheni 1 II. Relazione struttura-reattività 1. più sostituito = più stabile Stabilità R R R R R > > R R, R 2 2 > R 2 > R R 2 2 2. trans più stabile del cis; E più stabile del Z repulsione trans-2-butene
Alcheni 1 II. Relazione struttura-reattività 1. più sostituito = più stabile Stabilità R R R R R > > R R, R 2 2 > R 2 > R R 2 2 2. trans più stabile del cis; E più stabile del Z repulsione trans-2-butene
miscela di reazione Si lava (estrae) con una base Si lava (estrae) con un acido Si lava (estrae) con acqua
 1. Si purificano (se necessario) reagenti e solventi.. Si mescolano i reagenti nelle opportune condizioni di reazione.. Si segue l andamento della reazione. 4. Si lavora la reazione. 5. Si analizza il
1. Si purificano (se necessario) reagenti e solventi.. Si mescolano i reagenti nelle opportune condizioni di reazione.. Si segue l andamento della reazione. 4. Si lavora la reazione. 5. Si analizza il
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico
 Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
REAZIONI DEGLI ALCHENI
 REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Addizioni Nucleofile di Enolati a Composti Carbonilici L addizione di nucleofili all ossigeno, azoto, zolfo a composti carbonilici è una reazione che avete già incontrato e studiato. Anche nucleofili al
Addizioni Nucleofile di Enolati a Composti Carbonilici L addizione di nucleofili all ossigeno, azoto, zolfo a composti carbonilici è una reazione che avete già incontrato e studiato. Anche nucleofili al
1. Per capire la chimica del gruppo carbonile bisogna ricordarsi che il legame C=O è polarizzato
 1. Per capire la chimica del gruppo carbonile bisogna ricordarsi che il legame C= è polarizzato elettrofili protoni, acidi di Lewis X Y X Y nucleofili Scrivere le formule di risonanza per acetaldeide,
1. Per capire la chimica del gruppo carbonile bisogna ricordarsi che il legame C= è polarizzato elettrofili protoni, acidi di Lewis X Y X Y nucleofili Scrivere le formule di risonanza per acetaldeide,
Reazioni degli alcoli
 Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Capitolo 7 Composti organici alogenati
 himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
himica Organica Informazione Scientifica sul Farmaco apitolo 7 omposti organici alogenati Organic hemistry, 5 th Edition L. G. Wade, Jr. Introduzione I composti organici alogenati sono importanti per vari
ALDEIDI E CHETONI. Nelle aldeidi il carbonile si trova in posizione terminale, nei chetoni si trova all interno della catena.
 ALDEIDI E ETI Indice: Struttura e reattività 1 Addizione di acqua 2 Addizione di alcoli 4 Addizione di acido cianidrico 6 Addizione di ammoniaca e derivati 7 Addizione di composti organometallici 9 Addizione
ALDEIDI E ETI Indice: Struttura e reattività 1 Addizione di acqua 2 Addizione di alcoli 4 Addizione di acido cianidrico 6 Addizione di ammoniaca e derivati 7 Addizione di composti organometallici 9 Addizione
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI
 IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
COMPOSTI TITANIOORGANICI
 MPSTI TITAIGAII aratteristiche generali legame -: non particolarmente debole termodinamicamente, ma labile cineticamente legame -: abbastanza forte "driving force" notevole se - si converte in - - (1.7Å)
MPSTI TITAIGAII aratteristiche generali legame -: non particolarmente debole termodinamicamente, ma labile cineticamente legame -: abbastanza forte "driving force" notevole se - si converte in - - (1.7Å)
Reazioni degli epossidi
 12-04-2016 Reazioni degli epossidi Apertura dell anello acido-catalizzata, esempi Struttura intermedio: 3 forme limiti di risonanza H H a a O O b b H O CH 3 CH 3 CH 3 H H H H Struttura ibrido intermedio
12-04-2016 Reazioni degli epossidi Apertura dell anello acido-catalizzata, esempi Struttura intermedio: 3 forme limiti di risonanza H H a a O O b b H O CH 3 CH 3 CH 3 H H H H Struttura ibrido intermedio
Domanda 4 Dal punto di vista della reattività, il doppio legame si comporta spesso da:
 Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
ALDEIDI E CHETONI. Nelle aldeidi il carbonile si trova in posizione terminale, nei chetoni si trova all interno della catena.
 ALDEIDI E ETI Indice: Struttura e reattività 1 Addizione di acqua 2 Addizione di alcoli 4 Addizione di acido cianidrico 6 Addizione di ammoniaca e derivati 7 Addizione di composti organometallici 9 Addizione
ALDEIDI E ETI Indice: Struttura e reattività 1 Addizione di acqua 2 Addizione di alcoli 4 Addizione di acido cianidrico 6 Addizione di ammoniaca e derivati 7 Addizione di composti organometallici 9 Addizione
Idrocarburi Saturi. Reazioni
 Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
FENOLI: nomenclatura IUPAC
 FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
ACIDI CARBOSSILICI. ac. formico ac. acetico ac. benzoico
 ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
ALCHENI: Reazioni del doppio legame
 ALCENI: REATTIVITÀ ALCENI: Reazioni del doppio legame Reazione di addizione Addizioni ioniche Addizioni con meccanismo concertato ADDIZIONI IONICE ADDIZIONE DI ACIDI ALOGENIDRICI ADDIZIONE DI ACQUA ROTTURA
ALCENI: REATTIVITÀ ALCENI: Reazioni del doppio legame Reazione di addizione Addizioni ioniche Addizioni con meccanismo concertato ADDIZIONI IONICE ADDIZIONE DI ACIDI ALOGENIDRICI ADDIZIONE DI ACQUA ROTTURA
Alchini. Suffisso: -ino. d. H 3 CCH 2 CC CH
 Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
ALCOLI. Tabella dei valori di pka compresi tra 10 e estere acetacetico. pka CH HC. acetilene COOEt 24.0.
 ALLI Indice: intesi degli alcossidi 2 intesi di Williamson degli eteri 2 intesi degli alogenuri alchilici 3 intesi degli esteri 6 Disidratazione degli alcoli ad eteri 7 Disidratazione degli alcoli ad alcheni
ALLI Indice: intesi degli alcossidi 2 intesi di Williamson degli eteri 2 intesi degli alogenuri alchilici 3 intesi degli esteri 6 Disidratazione degli alcoli ad eteri 7 Disidratazione degli alcoli ad alcheni
REGISTRO DELLE LEZIONI 2005/2006. Tipologia. Addì Tipologia. Addì Tipologia
 Presentazione del corso, libri di testo esami e propedeuticità La struttura elettronica dell'atomo, gli orbitali, tipi di legami, regola dell'ottetto Ibridizzazione strutture di Lewis, carica formale,
Presentazione del corso, libri di testo esami e propedeuticità La struttura elettronica dell'atomo, gli orbitali, tipi di legami, regola dell'ottetto Ibridizzazione strutture di Lewis, carica formale,
ALCOLI E FENOLI ALCOL FENOLO. Scaricato da Sunhope.it
 Indice Alcoli e fenoli: gruppo funzionale Alcoli: nomenclatura e classificazione Fenoli: nomenclatura Alcoli: principali reazioni Fenoli Eteri Epossidi Tioli Tioeteri ALLI E FENLI Alcoli e fenoli sono
Indice Alcoli e fenoli: gruppo funzionale Alcoli: nomenclatura e classificazione Fenoli: nomenclatura Alcoli: principali reazioni Fenoli Eteri Epossidi Tioli Tioeteri ALLI E FENLI Alcoli e fenoli sono
PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento
 PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
Una reazione chimica può avvenire in uno o più stadi; l insieme degli stadi costituisce il MECCANISMO DI REAZIONE.
 Una reazione chimica può avvenire in uno o più stadi; l insieme degli stadi costituisce il MECCANISMO DI REAZIONE. Ogni passaggio del meccanismo è costituito da reagenti e prodotti e deve essere bilanciato
Una reazione chimica può avvenire in uno o più stadi; l insieme degli stadi costituisce il MECCANISMO DI REAZIONE. Ogni passaggio del meccanismo è costituito da reagenti e prodotti e deve essere bilanciato
Reazioni degli Alcheni
 Prof Mauro Tonellato Itis Natta Padova Reazioni degli Alcheni Indice delle reazioni: 1) Addizione di acidi alogenidrici 2) Addizione di acqua ) Idrogenazione catalitica 4) Addizione radicalica di 5) Alogenazione
Prof Mauro Tonellato Itis Natta Padova Reazioni degli Alcheni Indice delle reazioni: 1) Addizione di acidi alogenidrici 2) Addizione di acqua ) Idrogenazione catalitica 4) Addizione radicalica di 5) Alogenazione
Configurazione elettronica degli elementi del gruppo 14 (Si, Ge, Sn, Pb) sp 3 d. sp 3 d 2
 MPSTI SILIIGANII onfigurazione elettronica degli elementi del gruppo 14 (, Ge, Sn, Pb) s p d M M 4 sp [MF 4 ] x sp d [ 2 MF ] x sp d [ M 2D] [ 2 MF 4 ] 2 xx xx x x sp d sp d 2 [F 4 ] [ 2 F 4 ] 2 A questo
MPSTI SILIIGANII onfigurazione elettronica degli elementi del gruppo 14 (, Ge, Sn, Pb) s p d M M 4 sp [MF 4 ] x sp d [ 2 MF ] x sp d [ M 2D] [ 2 MF 4 ] 2 xx xx x x sp d sp d 2 [F 4 ] [ 2 F 4 ] 2 A questo
