Estrazione solido-liquido
|
|
|
- Agnolo Valle
- 9 anni fa
- Просмотров:
Транскрипт
1 Estrazione solido-liquido L'estrazione solido-liquido, detta anche lisciviazione, è l'operazione mediante la quale un soluto disperso matrice solida inerte (cioè senza alcuna affinità per il soluto) viene estratto mediante solvente liquido, anch'esso inerte. Mentre esistono diverse possibilità per separare le soluzioni, l'estrazione solido-liquido è in pratica l'unica tecnica per separare un soluto in miscela intima in una matrice solida; nel caso di soluti liquidi, si può procedere con la pressatura, come con alcuni semi oleaginosi o con le olive, ma la resa d'estrazione non può essere elevatissima. Inoltre è necessario preparare l'alimentazione con opportuni trattamenti (essiccamento, macinazione, taglio, ecc.. a secondo dei casi). Impieghi dell'estrazione solido-1iquido L estrazione con acqua delle ceneri di vegetali per ottenere una soluzione alcalina, la liscivia, è un operazione nota fin dall'antichità. Il trattamento di un solido con un liquido, al fine di estrarne un componente solubile, ha sempre trovato una varietà di applicazioni spesso chiamate con termini diversi, oltre a lisciviazione, come percolazione, lavaggio, digestione, infusione, ecc. Tra le applicazioni dell'estrazione solido-liquido nell'industria alimentare, le più importanti sono: Oli vegetali: Zucchero (di barbabietola o di canna): Enocianina: Estratti aromatici: Infusi (thè, caffè, ecc.): solido: costituenti solidi dei semi oleaginosi soluto: olio solvente: solventi organici, soprattutto esano solido: costituenti solidi dei tessuti saccariferi soluto: saccarosio solvente: acqua solido: bucce d'uva soluto: antociani solvente: soluzione acquosa di S0 2 solido: parti solide di piante officinali (foglie, fiori, radici, frutti, ecc.) soluto: varie sostanze chimiche solvente: acqua o alcool etilico e miscele solido: parti solide di semi tostati, foglie soluto: varie sostanze solubili, aromatiche, sapide, ecc.. solvente: acqua (calda) Modello fenomenologico dell estrazione solido-liquido Quando un solvente viene aggiunto ad un solido che contiene un soluto avvengo in sequenza questi fenomeni: 1. diffusione del solvente dalla massa della soluzione alla superficie del solido attraverso lo strato limite; 2. il solvente penetra nel solido bagnandolo e riempiendo tutte le microporosità in esso contenute e finendo per costituire al suo interno una fase imbibente continua; 3. il soluto disperso nel solido si scioglie nel solvente creando così, all'interno del solido una soluzione relativamente concentrata in soluto;
2 4. La differenza di concentrazione del soluto a la soluzione relativamente concentrato,che è all'interno del solido, e quella diluita, che è all'esterno, genera una diffusione del soluto verso l'esterno; 5. diffusione del soluto attraverso lo strato limite nella massa della soluzione. La diffusione si arresta quando la concentrazione del soluto è la stessa nella soluzione che imbibisce il solido e in quella che bagna esternamente il solido. Dopo aver raggiunto tale condizione di equilibrio (che in teoria richiede un tempo infinito, ma in pratica tempi finiti e ragionevoli) si procede alla separazione meccanica della soluzione dai solidi inerti. Questa operazione può essere fatta con una semplice operazione di sgrondatura o per filtrazione o centrifugazione o spremitura. Se, in questa fase, fosse possibile separare tutta la soluzione dai solidi inerti, tutto il soluto risulterebbe estratto e l'operazione sarebbe così conclusa con una resa di estrazione del 100% Invece, per quanto sia efficace la separazione, ci sarà sempre una certa quantità di soluzione che rimane nel solidi (soluzione imbibente) e dunque la resa di estrazione (quantità di soluto estratto rispetto alla quantità di soluto presente inizialmente nei solidi) sarà inferiore al 100%. Si può intervenire allora con una seconda operazione consistente nell'aggiungere al solido imbibito una nuova quantità di solvente. Questa nuova aggiunta riproduce una nuova situazione di gradiente fra la soluzione più concentrata all'interno dei solidi e la soluzione più diluita all'esterno. Inizia allora una nuova fase di diffusione fino a che la concentrazione di soluto all'interno e all'esterno dei solidi è uguale. Ripetendo l'operazione di separazione meccanica un'ulteriore frazione di soluto viene estratta e il solido risulta imbibito di una soluzione più diluita della precedente. Questa sequenza di aggiunte di solvente-diffusione-separazione può essere ripetuta finché si considera soddisfacente la resa di estrazione e tollerabile la quantità di soluto che rimane nella soluzione imbibente dei solidi. Riassumendo dunque si può dire che l'estrazione solido-liquido comprende due fasi principali: una che è regolata dal fenomeno fisico della diffusione del soluto e che ha come obiettivo di pervenire all'equilibrio, cioè all'uguaglianza della concentrazione della soluzione imbibente e della soluzione libera, e una che è regolata dall'operazione meccanica di separazione della soluzione dai solidi e che ha come obiettivo di separare la maggior quantità possibile di soluzione dai solidi. Fattori che influenzano il processo diffusivo I fenomeni diffusivi rivestono particolare importanza nell'estrazione. La diffusione è descritta matematicamente dalla legge di Fick, che in questo caso possiamo scrivere come: C = dm dt C D = A i s (x s x) dove: C = è la portata istantanea di soluto che diffonde dal solido nella soluzione (kg/s); m C = è la massa di soluto C (kg); t = è il tempo (s); D = è il coefficiente di diffusione (kg/s m); s = è lo spessore dello strato limite (m); A = è l'area interfacciale (m 2 ); x s = è la concentrazione in frazione del soluto nella soluzione satura sulla superficie del solido; x = è la concentrazione in frazione del soluto nella massa della soluzione. I fattori che influenzano i termini che compaiono nell equazione influenzano anche il processo. Dimensioni delle particelle. Al diminuire delle dimensioni aumenta l'area interfacciale e si accorciano i percorsi diffusivi all'interno dei pori. Aumenta perciò la velocità della diffusione ma
3 aumentano anche le perdite di carico che il solvente deve affrontare per attraversare il letto di particelle, specie muovendosi in controcorrente. Per quanto possibile si riducono le dimensioni del solido in modo non uniforme, dandogli forme in cui almeno una dimensione sia molto piccola, si da assicurare un piccolo spessore almeno in una direzione, mentre nelle altre le dimensioni non piccole evitano un eccessivo impaccamento che potrebbe ostacolare il passaggio del liquido. Così le bietole si tagliano in fettucce, i semi in scaglie, ecc. Al diminuire delle dimensioni delle particelle, aumentano anche le difficoltà della separazione solido-liquido, specie se la differenza di densità è piccola. Temperatura. Aumentando la temperatura, aumenta il coefficiente di diffusione dato che diminuisce la viscosità. Aumenta abitualmente anche la solubilità delle sostanze da estrarre. Talvolta, come nell'estrazione del saccarosio, ciò è dovuto ad un effetto specifico del processo: in quel caso la denaturazione delle pareti cellulari. Un eccessivo aumento può provocare reazioni secondarie, perdita di selettività e possibili perdite di solvente per l'aumento della tensione di vapore. Pressione. Ha soprattutto influenza nell'estrazione con solventi in condizioni superentiche, detta anche estrazione gas-solido. Variando la pressione si riesce a modulare la solubilità del soluto, rendendone così agevole il suo recupero. Agitazione. Un agitazione della soluzione aumenta la turbolenza, fa diminuire lo spessore dello strato limite, mantiene più uniforme la concentrazione nella massa della soluzione e migliora lo sfruttamento dell'area interfacciale prevenendo la sedimentazione del solido. Però la presenza o meno di un vero e proprio sistema d'agitazione dipende dal tipo di apparecchiatura. Solvente. I criteri di scelta sono molteplici: Selettività. E la misura di quanto il soluto d'interesse si sciolga preferibilmente nell'estratto rispetto agli altri componenti, come eventuali altri soluti o il diluente stesso. Capacità del solvente. Indica la massima concentrazione che il soluto può raggiungere in quel solvente. Maggiore è la capacità, minore è la quantità di solvente richiesta. Tossicità, pericolosità e impatto ambientale. L uso di materiali pericolosi richiede il ricorso ad accorgimenti e apparecchiature particolari per ridurre il rischio entro limiti accettabili e le emissioni entro i limiti di legge. L uso di sostanze tossiche e ad elevato impatto ambientale fa perciò lievitare sia i costi dell'investimento sia i costi d'esercizio. La pericolosità è soprattutto da mettere in relazione con la più o meno facile infiammabilità che può richiedere per la costruzione degli impianti delle caratteristiche particolari alquanto costose. Sono anche da valutare le possibili tecniche di smaltimento dei reflui e la biodegradabilità. Tensione di vapore. Poiché l'estrazione richiede la susseguente separazione dell'estratto in soluto e solvente, l'efficacia e il costo di questa separazione può dipendere dalla tensione di vapore del solvente in relazione al metodo scelto. Cosi se si utilizza la distillazione per recuperare il solvente, sarebbe desiderabile una tensione di vapore elevata o bassa a seconda che si voglia ottenere il solvente come prodotto di testa o di coda. In ogni caso tanto più è elevata la tensione di vapore tanto maggiore può risultare l'impatto ambientale, in relazione alla tossicità del solvente, per la maggiore facilità di un suo rilascio nell'ambiente. Inoltre calore specifico e calore latente influiscono sui costi energetici dell'operazione. Stabilità termica. E in relazione alla necessità di operazioni a caldo per separare l'estratto. La stabilità termica influenza il consumo del solvente e la formazione di sottoprodotti, che debbono a loro volta essere separati e che possono presentare tossicità e impatto ambientale superiori a quelli del solvente. Anche l'inerzia chimica è un fattore da considerare, in quanto influisce sulla scelta dei materiali di costruzione delle apparecchiature. Viscosità. E bene che sia la più bassa possibile per favorire il trasporto di massa tra le due fasi, possibilmente inferiore a 10 mpa s. Costo. E importante soprattutto in relazione al consumo di solvente. Generalmente i criteri di scelta sono basati sul criterio generale che simile scioglie simile. Così gli oli vegetali, costituiti da trigliceridi degli acidi grassi, vengono abitualmente estratti con esano, mentre se si vogliono estrarre acidi grassi si ricorre, a solventi più polari.
4 Tempo. All'aumentare del tempo di contatto aumenta la quantità di soluto estratto ma diminuisce la forza spingente (x s - x). Operare con tempi di contatto brevi significa perciò operare con un'elevata forza spingente ma porta ad estratti più diluiti. BILANCI MATERIALI Nella esecuzione dei bilanci materiali dell'estrazione solido-liquido saranno definiti: Fd (abbreviazione dell' inglese feed ): la massa nei processi discontinui o la portata in massa nei processi continui del prodotto alimentato da estrarre; Sv la massa o la portata in massa del solvente ; Ex (abbreviazione del termine estratto ): la massa o la portata in massa della soluzione di soluto e solvente separata dai solidi; è detta anche miscella; Rt (abbreviazione del termine raffinato ): la massa o la portata in massa dei solidi residui, imbibiti di soluzione, dopo la separazione di Ex. Si indicheranno inoltre con: x: la frazione di massa del soluto in Rt o in Fd, y: la frazione di massa del soluto in Ex o in Sv. La massa cui si riferiscono x o y sarà indicata come indice, ad esempio x Fd è la massa di soluto in Fd e y Ex, è la frazione di massa del soluto nell'estratto Ex. Si definisce inoltre come: stadio di equilibrio: la fase dell'operazione o la parte di impianto nella quale raggiunge la uguaglianza della concentrazione fra la soluzione all'interno e la soluzione all'esterno dei solidi; rapporto di imbibizione: il rapporto fra la massa di soluzione imbibente e la massa di solidi (ad esempio se si dice che il rapporto di imbibizione è 0,5:1,0 vuol dire che ogni kg di solidi contiene 0,5 kg di soluzione imbibente); resa di estrazione: il rapporto percentuale fra la massa di soluto estratta (e separata in Ex) e la massa di soluto inizialmente presente nel prodotto, cioè Fd x Fd. Estrazione semplice Lo schema di un'estrazione semplice è rappresentato dalla figura: Operazione discontinua In un opportuno recipiente vengono miscelate una certa massa di Fd con una certa massa di Sv. Si lascia che il contatto fra la fase solida e la fase liquida sia abbastanza lungo da poter considerare che si è raggiunta l'uguaglianza della concentrazione in soluto fra la soluzione all'intero dei solidi e quella all'esterno (stadio di equilibrio). Infine con un adatto sistema di separazione meccanica, si separa l'estratto Ex dal raffinato Rt. Operazione continua Tutto come sopra, ma con i vari componenti in moto. I simboli Fd, Sv, Ex ed Rt indicano in questo caso delle portate in massa (kg/h). Valgono le seguenti relazioni: Fd + Sv = Ex + Rt Bilancio globale
5 Fd x Fd + Sv y Sv = Ex y Ex + Rt x Rt Bilancio relativo al soluto La conoscenza di tre portate su quattro e di tre composizioni su quattro consente calcolare la quarta incognita. Possono essere date, inoltre, la resa di estrazione o il rapporto di imbibizione in Rt. 1 Esempio 100 kg di un seme oleaginoso contenente il 22% di olio ( e il 79% di solidi inerti), vengono miscelati in uno stadio di equilibrio con 100 kg di esano. Se il rapporto di imbibizione del raffinato è di 0,5:1,0, calcolare la resa di estrazione, la massa e la composizione dei quattro componenti del sistema. Il calcolo di Rt può essere fatto facilmente conoscendo il rapporto di imbibizione. In Rt sono contenuti 78 kg di solidi (gli stessi contenuti in Fd) e dunque: 0,5 x 78 = 39 kg di soluzione imbibente In totale: Rt = = 117 kg Pertanto: Fd + Sv = Ex + Rt = Ex da cui: Ex = 83 kg. Passando ora al bilancio del soluto è facile calcolare y Ex, cioè la frazione di massa del soluto nell'estratto, poiché la soluzione che si forma all'equilibrio non è altro che la somma del solvente Sv più l'olio contenuto in Fd. 22 y Ex = = 0, Questa è anche la frazione di massa dei 39 kg di soluzione che imbibiscono Rt (la condizione di equilibrio è che la soluzione che costituisce Ex è identica alla soluzione che imbibisce Rt). Pertanto: Fd x Fd + Sv y Sv = Ex y Ex + Rt x Rt 100 0, ,00 = 83 0, x Rt Se ne deduce che: x Rt = 0,06 e che la resa percentuale di estrazione è: 14, = 67,9% 22 Estrazione multipla detta ad esaurimento o a correnti incrociate Consiste nel ripetere operazioni come la precedente aggiungendo ulteriori aliquote di solvente al raffinato e ripetendo l operazione di separazione.
6 2 Esempio Supponiamo di aggiungere di aggiungere al raffinato dell esempio precedente che chiameremo Rt 1 un ulteriore aliquota di 100 kg di solvente fresco e di ripetere l operazione. Lo schema del secondo stadio di estrazione è: Supponiamo inoltre che il rapporto di imbibizione anche dei 2 stadio sia di 0,5:l,0. Poiché i solidi non cambiano e si ritrovano integralmente in Rt 2, anche Rt 2 avrà una massa complessiva di 117 kg. Ne risulta che: Rt 1 + Sv = Rt 2 + Ex = Ex 2 da cui si ricava che: Ex 2 = 100 kg Con un ragionamento analogo a quello fatto per lo stadio precedente possiamo dire che y Ex2, sarà quello di una soluzione risultante da tutto l'olio e da tutto il solvente che entrano nel 2 stadio di equilibrio, cioè: olio = 7,06 kg (olio in Rt 1 ) solvente = 100 (solvente fresco) + 31,94 ( solvente in Rt 1 = (39 7,06) kg) = 131,94 kg y Ex 7,06 = 131,94 + 7,06 2 = 0,0508 il bilancio relativo all olio diventa: Rt 1 x Rt1 + Sv y Sv = Rt 2 x Rt2 + Ex 2 y Ex , ,00 = 117 x Rt ,0508
7 da cui si ricava che : x Rt2 = 0,0198 Riassumendo: Fd Sv Rt 1 Ex 1 Rt 2 Ex kg 100 kg 117 kg 83 kg 117 kg 100 kg x Fd y Sv x Rt1 y Ex1 x Rt2 y Ex2 0,22 0,00 0,06 0,18 0,0198 0,0508 Limiti dell estrazione ad esaurimento Con il secondo stadio di equilibrio siamo riusciti ad estrarre altri 5.08 kg di olio che, sommati ai kg estratti nello stadio precedente, fanno kg complessivi, cioè una resa del: 20, = 91% 22 E' evidente che se attuassimo un'ulteriore estrazione la resa aumenterebbe ulteriormente. E questo è un evidente vantaggio. Se però consideriamo gli estratti ci accorgiamo che la concentrazione dell'olio nel primo estratto è 0, 18 cioè del 18%, mentre la concentrazione di olio nel secondo estratto è cioè del 5.08%. In pratica gli estratti successivi devono essere riuniti per essere sottoposti all'evaporazione del solvente e al recupero dell'olio. Nel nostro caso avremo un unica soluzione contenente kg di olio in = 183 kg di soluzione. Ed una concentrazione finale di 20,02/183 = 0,109 cioè del 10,9%. Se proseguissimo con ulteriori stadi di estrazione otterremmo ulteriori incrementi di resa, ma soluzioni di Ex sempre più diluite e quindi spese sempre maggiori di evaporazione del solvente. E' dunque chiaro che l'aumento di resa si fa a costi progressivamente crescenti dell'evaporazione. E' possibile pensare ad una situazione in cui si realizzi la situazione ideale di ottenere rese elevate di estrazione e, allo stesso tempo concentrazioni elevate del soluto in Ex? Estrazione in controcorrente L'estrazione in controcorrente consiste nel condurre una serie di estrazioni successive (stadi di equilibrio) in cui ali estratti vengono in contatto con raffinati contenenti soluzioni sempre più concentrate di soluto fino a venire in contatto con Fd che contiene, evidentemente, la soluzione più concentrata possibile di soluto, cioè il soluto puro. In tal modo Ex si arricchisce progressivamente di soluto ed esce, infine, ad una concentrazione elevata. D'altro canto si fa in modo che i raffinati si miscelino con soluzioni (Ex) sempre più diluite in modo da impoverirsi progressivamente di soluto, Nell'ultimo stadio i raffinati incontrano, infine, il solvente puro e subiscono l'ultima fase di estrazione.
8 Dovendo numerare gli stadi dì equilibrio si assume la.convenzione di cominciare dallo stadio nel quale viene alimentato Fd. Lo schema di un estrattore in controcorrente è così rappresentato: Le coppie Rt 1 Ex 1, Rt 2 - Ex 2, Rt 3 - Ex 3, ecc rappresentano delle relazioni d'equilibrio, cioè flussi e masse che sono tra loro in equilibrio. Le coppie Rt 1, - Ex 2, Rt 2 - Ex 3, Rt 3 - Ex 4, ecc... rappresentano delle relazioni operative nel senso che sono i flussi e le masse che sono operativamente l'una in presenza dell'altra. Sono le differenze di concentrazione fra queste due correnti che determinano la diffusione del soluto. Le quattro correnti principali sono Fd, Ex 1, Rt n e Sv cioè le masse o i flussi che entrano ed escono dal sistema, Ex 1 è l'estratto finale e Rt n è il raffinato finale. Valgono, sia per le quattro correnti principali e cioè per l'estrattore nel suo complesso, sia per le correnti relative a ciascun stadio, le equazioni di bilancio materiale già viste per l'estrazione semplice. E cioè: - per l'estrattore nel suo complesso: Fd + Sv = Ex 1 + Rt n Fd x Fd + Sv y Sv = Ex 1 y Ex1 + Rt n x Rtn Bilancio globale Bilancio relativo al soluto - per uno stadio qualunque, ad esempio lo stadio n 3 Rt 2 + Ex 4 = Rt 3 + Ex 3 Rt 2 x Rt2 + Ex 4 y Ex4 = Rt 3 x Rt3 + Ex 3 y Ex3
9 3 Esempio Il problema che questi bilanci materiali permettono di risolvere è il calcolo del numero di stadi di equilibrio o numero di stadi teorici necessario per ottenere un dato esaurimento dei solidi (una data resa) ed un dato arricchimento degli estratti. Il risultato ottenibile con l'estrazione in controcorrente è davvero spettacolare. Facendo riferimento all'esempio 1 dell'estrazione semplice ci si può proporre, partendo dagli stessi 100 kg di Fd e dagli stessi 100 kg, di Sv, di ottenere una resa di estrazione del 95% invece del 67,9%. Il problema è soltanto di stabilire quanti stadi teorici ci vogliono. Effettuiamo questo calcolo seguendo una procedura valida per qualunque caso. l. Innanzitutto si effettua un bilancio per definire esattamente le quantità e la composizione delle quattro correnti principali. L'unico dato che dobbiamo conoscere, oltre quelli già forniti è il rapporto di imbibizione in Rt n. Per semplicità e comodità dell'esempio assumeremo che sia Rt n, che tutti gli altri Rt dell'estrattore abbiano lo stesso rapporto di imbibizione di 0,5:l,0. Fd + Sv = Ex 1 + Rt n E' evidente che essendo Rt n 117 kg, (78 kg di solidi + 39 kg di soluzione imbibente), Ex 1 sarà necessariamente 83 kg. Il dato di resa ci aiuta a definire la composizione di Rt n. In esso infatti ci devono essere non più del 5% dell'olio iniziale, cioè 22 x = 1,1 kg. E' dunque evidente che in Rt n sono contenuti 39,0 1,1 = 3 7,9 kg di solvente. La conoscenza di questi dati ci permette anche di conoscere completamente Ex 1. In esso sarà contenuto tutto l'olio che non è in Rt n cioè 22,0 1,1 = 20,9 kg e tutto il solvente che non è in Rt n cioè ,9 = 62,1 kg. Ex 1 è dunque complessivamente 20,9 + 62,1 = 83,0 kg ed ha una concentrazione di olio di 0,2518, cioè del 25.18%. E' possibile che l'estrattore in controcorrente ci dia un risultato così buono e cioè una resa di estrazione elevata e una concentrazione elevata di olio in Ex 1, con gli stessi ingredienti che ci hanno dato, nell'estrazione semplice, un risultato così modesto? E' certamente possibile, utilizzando un estrattore che abbia un numero adeguato di stadi teorici, Intanto riassumiamo in una tabella i risultati del bilancio di materia globale effettuato su tutto l'estrattore: Fd Sv Ex 1 Rt n Solidi, kg 78, ,0 Olio, kg 22, ,9 1,1 Solvente, kg ,0 62,1 37,9 Totale, kg 100,0 100,0 83,0 117,0 2. Si inizia il bilancio materiale stadio per stadio, cominciando dal primo:
10 Fd + Ex 2 = Rt 1 + Ex Ex 2 = da cui si ricava Ex 2 = 100 kg Fd x Fd + Ex 2 y Ex2 = Rt 1 x Rt1 + Ex 1 y Ex1 Il contenuto di olio in Fd è noto: Fd x Fd = 22 kg così pure in Ex 1 : Ex 1 y Ex1 = 20,9 kg. Il calcolo del contenuto in olio in Rt 1 è semplice poiché sappiamo che Rt 1 contiene 39 kg di una soluzione che ha la stessa concentrazione di olio in Ex 1 (relazione di equilibrio, cioè 20,9/83 = 0,2518. Per cui Rt 1 x Rt1 = 39 x 0,2518 = 9,82 kg. A questo punto possiamo subito dire che un solo stadio teorico non basta poiché contiene 9,82 kg di olio, molto più degli l,1 kg che dovrà contenere. Il bilancio dell'olio al 1 stadio diventa: 22 + Ex 2 y Ex2 = 9, ,9 da cui Ex 2 y Ex2 = 8,72 kg e quindi y Ex2 = 8,72/100 = 0, Si effettua il bilancio materiale sul secondo stadio: Rt 1 + Ex 3 = Rt 2 + Ex Ex 3 = da cui si ricava Ex 3 = 100 kg. Si può notare che, se il rapporto di imbibizione è costante anche i vari Rt sono sempre uguali (nel nostro caso 117 kg) e perciò anche gli Ex saranno necessariamente uguali (nel nostro caso 100 kg). Ripetendo gli stessi calcoli effettuati per lo stadio precedente avremo: Rt 1 x Rt1 + Ex 3 y Ex3 = Rt 2 x Rt2 + Ex 2 y Ex2 Ricordando che Rt 1 x Rt1 = 9,82 kg ; Ex 2 y Ex2 = 8,72 kg Poiché sappiamo che Rt 2 contiene 39 kg di una soluzione che ha la stessa concentrazione di olio in Ex 2 (relazione di equilibrio, cioè 8,72/100 = 0,0872. Per cui Rt 2 x Rt2 = 39 x 0,0872 = 3,401 kg (due stadi teorici non sono sufficienti!). Ex 3 y Ex3 = Rt 2 x Rt2 + Ex 2 y Ex2 - Rt 1 x Rt1 = 3, ,72 9,82 = 2,301 kg
11 Da cui : y Ex3 = 2,301/100 = 0, Si effettua il bilancio materiale sul secondo stadio: Ex 4 = 100 kg e Rt 3 = 117 kg. Rt 2 x Rt2 + Ex 4 y Ex4 = Rt 3 x Rt3 + Ex 3 y Ex3 Ricordando che Rt 2 x Rt2 = 3,14kg ; Ex 3 y Ex3 = 2,301 kg Poiché sappiamo che Rt 3 contiene 39 kg di una soluzione che ha la stessa concentrazione di olio in Ex 3 (relazione di equilibrio, cioè 2,301/100 = 0, Per cui Rt 3 x Rt3 = 39 x 0,02301 = 0,897kg. Dunque in Rt 3 ci sono meno di 1,1 kg di olio. Il che significa che per ottenere il risultato previsto dal bilancio globale ci vuole un estrattore con tre stadi teorici di estrazione. Stadi teorici ed efficienza degli estrattori La nozione di stadio è teorica da due punti di vista. Innanzitutto presuppone che si raggiunga la condizione di equilibrio fra soluzione imbibente e soluzione libera e ciò non è possibile, come si è detto, che in un tempo infinito. In secondo luogo lo stadio è teorico in quanto esso non esiste materialmente negli estrattori pratici. Questi sono generalmente continui e costituiti da impianti nei quali si realizza un flusso in controcorrente fra solidi da estrarre e soluzione estraente. Nulla in essi può essere rappresentato come uno stadio nel quale la miscela fra solidi e soluzione viene mantenuta finché non si raggiunga l'equilibrio. Che cos'è dunque, in pratica uno stadio teorico? E' una nozione, un concetto, che ci consente di valutare numericamente la difficoltà di un'operazione di estrazione e l'efficienza di un estrattore. Se, ad esempio, nelle condizioni indicate nell'esempio precedente si ottengono, con un dato estrattore, i risultati calcolati nel bilancio materiale globale, si può dire che l'estrattore ha un'efficienza equivalente a circa tre stadi teorici. Nozione importante poiché ci permette di prevedere le prestazioni dell'estrattore, in qualunque modo si modifichino le condizioni operative, le quantità e le concentrazioni. E' anche evidente che un estrattore avente un'efficienza equivalente ad un numero elevato di stadi teorici è in grado, a parità di condizioni, di ottenere prestazioni migliori e cioè un esaurimento spinto dei solidi, Rt n, e, contemporaneamente, un'elevata concentrazione di soluto in Ex 1.
12 Cosa significa a parità di condizioni? Significa essenzialmente a parità di rapporto di imbibizione poiché il rapporto di imbibizione è, con il numero di stadi teorici, l'altro fattore di efficienza di un estrattore. Come abbiamo avuto modo di notare, se fosse possibile avere un rapporto di imbibizione di zero (cioè una separazione totale della soluzione dai solidi), un solo stadio teorico sarebbe sufficiente per ottenere una resa del 100%, cioè l'estrazione di tutto il soluto. Il numero di stadi teorici che è necessario per ottenere una certa resa di estrazione è tanto più elevato quanto più elevato è il rapporto di imbibizione dei solidi. Pertanto non possiamo giudicare l'efficienza di un estrattore conoscendo soltanto il numero di stadi teorici. Non possiamo dire che un estrattore con un'efficienza equivalente a 5 stadi teorici è superiore ad un estrattore con 3 stadi teorici. Occorre anche conoscere i rispettivi rapporti di imbibizione e giudicare, con un calcolo come quello che abbiamo presentato nell'esempio precedente, quale dei due estrattori è in grado di realizzare la prestazione migliore (esaurimento più spinto di Rt n e arricchimento più spinto di Ex 1 ). Ancora sul rapporto di estrazione Negli esempi che abbiamo presentato finora abbiamo considerato che il rapporto di imbibizione fosse costante per tutti gli stadi di estrazione. Questa condizione non si verifica frequentemente nella pratica. Sia il particolare modo di funzionamento degli estrattori, sia la variazione delle caratteristiche fisiche (densità, viscosità) della soluzione imbibente determinano una variazione del rapporto di imbibizione nei vari punti dell'estrattore. Questa variazione non può che essere determinata sperimentalmente. Di essa si deve tener conto nei bilanci materiali per il calcolo dei numero di stadi teorici. In pratica si Procede come segue: Si definisce sperimentalmente la relazione fra rapporto di imbibizione e composizione della soluzione imbibente. Per fare ciò si prelevano campioni di raffinato in punti successivi dell'estrattore e se ne determina la composizione. Ad esempio, in un impianto di estrazione dell'olio: si prelevano campioni di Rt ; si determina, per evaporazione fino a peso costante, la percentuale in peso di solvente ; si determina, per estrazione al Soxhlet, la percentuale in peso di olio ; si determina, per differenza di peso, la percentuale in peso di solidi; si porta in grafico il rapporto di imbibizione o una misura equivalente (ad esempio la percentuale in peso della soluzione imbibente rispetto al peso totale di Rt) in funzione della concentrazione in olio della soluzione imbibente ; a questo grafico si fa riferimento nel calcolo degli stadi teorici rilevando ad ogni stadio quale è il rapporto di imbibizione che corrisponde alla composizione della soluzione imbibente. Rappresentazione del sistema di estrazione sul diagramma triangolare Tutti i calcoli e bilanci che abbiamo descritto nei paragrafi precedenti possono essere svolti con una procedura grafica. Un sistema di tre componenti è rappresentabile con un diagramma triangolare utilizzando il triangolo rettangolo. I tre componenti sono, nel nostro caso, l'olio -il solvente - i solidi. Nella figura è riportato un esempio di rappresentazione grafica su triangolo rettangolo di un problema di estrazione nel caso dell'olio. I vertici del triangolo rappresentano i tre componenti puri. I lati del triangolo rappresentano miscele binarie. Il cateto di base rappresenta miscele di olio e solidi: i semi oleaginosi da estrarre (Fd) sono rappresentabili da un punto su questo lato. E' indicata a titolo di esempio la composizione di Fd dell' esercizio III (22% di olio). L'ipotenusa rappresenta miscele di olio e solvente: tutti gli Ex saranno rappresentabili con punti dell'ipotenusa. E' indicata a titolo di esempio la composizione di Ex 1 dell'esercizio III (25.18%).
13 Infine l'altro cateto rappresenta miscele di solidi e solvente: queste miscele in pratica non esistono; si può dire soltanto che Rt n, sarà in una posizione molto vicina a questo lato, contenente i solidi, il solvente e pochissimo olio residuo. Tutti i punti interni al triangolo rappresentano miscele ternarie; pertanto cadono all'interno del triangolo rettangolo tutti gli Rt. La lettura della composizione di una miscela ternaria all'interno del triangolo è molto semplice. Si prenda ad esempio il punto A: esso rappresenta una miscela che contiene il 60% di olio e il 10% di solvente. Il contenuto in solidi è evidentemente dato dalla differenza a 100, cioè il 30%. Questa osservazione consente di introdurre il concetto di luogo dei raffinati come di una linea all'interno del triangolo sulla quale si situano le composizioni dei raffinati. Se, per esempio, ipotizziamo, come nell'esercizio III, che il rapporto di imbibizione dei raffinati sia 0,5:1,0 e che esso non vari al variare della composizione della soluzione: imbibente, allora il luogo dei raffinati è rappresentabile con un segmento parallelo all'ipotenusa, come quello riportato nella figura. In pratica si può dire che la soluzione imbibente rappresenta un terzo in peso, cioè il 33%, degli Rt. La retta tracciata nel diagramma triangolare ha la proprietà di rappresentare tutte le possibili condizioni in cui la soluzione imbibente rappresenta il 33% della miscela. Tutto quanto abbiamo detto mostra come possono essere indicate nel diagramma le composizioni. Vediamo ora come possono essere rappresentate quantità relative delle varie correnti. Il punto somma Se si miscelano due correnti di diversa composizione, la composizione della miscela risultante è sul segmento che congiunge le composizioni delle due correnti, in una posizione che dipende dalla proporzione delle due correnti nella miscela. Nel triangolo rettangolo abbiamo unito con un segmento il punto che rappresenta Fd con il vertice che rappresenta il solvente puro. Abbiamo inoltre indicato con la lettera M il punto intermedio del segmento. Esso rappresenta la composizione della miscela che si ottiene miscelando Fd e Sv in parti uguali, come ad esempio nell'estrazione semplice dell'esercizio I. Se le proporzioni della miscelazione fossero state diverse il punto M si sarebbe spostato di conseguenza, stante la seguente proporzione: lunghezza del segmento Fd-M quantità di Sv sta alla come sta alla lunghezza del segmento M-Sv quantità di Fd REGOLA DELLA LEVA
14 Questa proprietà del diagramma triangolare permette di risolvere agevolmente anche il problema di un'estrazione in controcorrente considerando che il bilancio globale si scrive: Fd + Sv = Rt n + Ex 1 Se nel sistema entrano 100 kg/h di Fd e 100 kg/h di Sv come nell'esercizio III, lo stesso punto M rappresenta la posizione della miscela fittizia che si otterrebbe miscelando Fd e Sv. Il punto M è detto punto somma e rappresenta condizione che nei bilanci materiali sono indicate come somma di due correnti. Possiamo pertanto dire che lo stesso M che rappresenta la somma Fd + Sv rappresenta anche la somma Rt n + Ex 1. Possiamo pertanto individuare Rt n sul luogo dei raffinati in base ai dati della tabella dell'esercizio III. Unendo Rt n al punto M e prolungando il segmento fino ad incontrare l'ipotenusa, si individua su questo il punto che rappresenta la composizione di Ex 1. Poiché la portata in massa Rt n + Ex 1 è di 200 kg/h anche il segmento da Rt n a Ex 1 rappresenta tale quantità. Si può dire inoltre che: lunghezza del segmento Rt n -M quantità di Ex 1 sta alla come sta alla lunghezza del segmento M-Ex 1 quantità di Rt n Ciò consente di valutare graficamente le quantità di Ex 1 e Rt n. 4 Esempio 2000 kg/h di semi al 20 % di olio vengono estratti con un solvente che contiene il 2 % di olio. Si vuole ottenere un residuo contenente oltre l'inerte il 4% di olio e il 20% di solvente ed un estratto privo d'inerte al 30 % di soluto. Si calcoli graficamente la portata di solvente necessario all'operazione e dell'estratto ottenuto. In figura sono rappresentate le correnti entranti ed uscenti dall'impianto. Riportiamo sul diagramma i punti rappresentativi delle correnti Fd, Sv, Ex, e Rt. Come si può vedere, alimentazione e solvente sono miscelati per dare il miscuglio eterogeneo M che si separa in un estratto ed un residuo. Per l'allineamento delle correnti, il punto M deve essere sia sulla congiungente i punti Fd ed Sv, sia sulla congiungente i punti Rt ed Ex, quindi non può essere che al punto d'intersezione dei due segmenti.
15 Dopo che si è localizzato M, applicando la regola della leva si può calcolare il rapporto Fd/Sv. Le lunghezze dei segmenti valgono: FdM = 76 mm SvM =123 mm Quindi si ha: da cui si ricava: Fd Sv SvM = FdM 123 mm = = 1, mm 2000 kg/h Sv = Fd = = 1236 kg/h 1,618 1,618 Sempre con la regola della leva, ricaviamo il rapporto Rt/Ex. I segmenti misurano: ExM = 73 mm RtM = 39,5 mm Per la regola della leva si ha: Rt ExM = Ex RtM Facendo un bilancio globale di materia si ha: Dividendo per Ex si ha: = 73 mm 39,5 mm = 1,848 Fd + Sv = M = Ex + Rt = 2000 kg/h kg/h = 3236 kg/h da cui si ottiene: M Ex = Ex Ex + Rt Ex = 1 + 1,848 = 2, kg/h Ex = M = = 1136 kg/h 2,848 2,848 Infine si può anche ricavare: Rt = M - Ex = 3236 kg/h kg/h = 2100 kg/h Qualche osservazione sul luogo dei raffinati Gli esempi che abbiamo fatto sono riferiti al caso ipotetico che il rapporto dì imbibizione sia costante. Soltanto in questo caso il luogo dei raffinati è un segmento parallelo al lato solvente - olio. Se il rapporto di imbibizione non è costante, come nella maggior parte dei casi, il luogo dei raffinati sarà una curva con uno specifico andamento che dovrà essere definito sperimentalmente. 5 Esempio In un estrattore in controcorrente di olio di semi si analizza una serie di campioni di Rt, prelevati in sequenza nell estrattore, ottenendo i seguenti risultati:
16 Campione N Solvente % Olio % Solidi % Concentrazione di olio nella soluzione imbibente Percentuale di soluzione imbibente in Rt , , , , , La figura rappresenta, nel diagramma triangolare, un luogo dei raffinati costruito con i dati della tabella dell'esempio V. Sono indicati i cinque dati sperimentali ed è tracciata la curva che li unisce. La costruzione del luogo dei raffinati può aver luogo in due modi, che indichiamo brevemente. Il primo, molto semplice e diretto, consiste nel porre i punti sperimentali sul diagramma, conoscendo la composizione percentuale di ciascun componente di Rt. Il secondo è invece basato sul rapporto di imbibizione ed è illustrato dal Segmento tracciato per il punto 5. Tale segmento congiunge il vertice che rappresenta i solidi con il punto sull'ipotenusa che rappresenta la composizione della soluzione imbibente (y Ex5 ). Su tale segmento la posizione del punto 5 potrebbe essere individuata in base al rapporto di massa fra solido e soluzione imbibente, sapendo che: lunghezza del segmento solidi-5 massa di soluzione imbibente in Rt sta alla come sta alla lunghezza del segmento 5-y Ex5 massa di solidi in Rt La stessa operazione, ripetuta per tutti i dati, consente di porre 5 punti sperimentali e di tracciare dunque il luogo dei raffinati. Altri casi pratici I sistemi reali si possono presentare con molte varianti rispetto allo schema base finora trattato. Per esempio, quando si studia l'estrazione di zucchero dalle barbabietole il punto Fd non si trova su un lato, ma all'interno del triangolo poiché le barbabietole contengono sia i solidi che il soluto (zucchero) e un po' di solvente (acqua). In altri casi invece del solvente puro si usa un estratto molto diluito che proviene da altre operazioni di recupero.
17 In altri casi il rapporto di imbibizione di Rt cambia bruscamente nell'ultimo stadio, dove i solidi vengono spremuti per recuperare il massimo di soluzione imbibente. CALCOLO GRAFICO DEL NUNIERO DI STADI TEORICI Il punto differenza Per risolvere graficamente, sul triangolo rettangolo, il problema del calcolo del numero di stadi teorici è necessario introdurre la nozione di punto differenza. Se ci riferiamo ai bilanci materiali dei vari stadi teorici possiamo scrivere, per un generico stadio m- esimo: Rt m-1 + Ex m+1 = Rt m + Ex m Che equivale alla seguente : Rt m-1 - Ex m = Rt m - Ex m+1 Quest'ultima espressione indica la relazione operativa fra un Rt generico e l'ex che gli sta di fronte. Indica in particolare che esiste una differenza costante in tutto l'estrattore fra le masse di Rt e le masse di Ex che gli sono operativamente di fronte. Questa relazione vale, ovviamente, anche per l inizio e per la fine del sistema, potendosi scrivere. Fd Ex 1 = Rt n - Sv = M che deriva dal bilancio globale dell'estrattore. Orbene: le proprietà dei diagramma triangolare sono tali per cui la differenza fra due correnti rappresentate nel diagramma è identificata da un punto che si trova sul prolungamento del segmento che unisce le due correnti. Nella figura è stato riprodotto il diagramma triangolare dell'esempio 3 con l'identificazione del punto M' come punto differenza comune alla retta che proviene dal segmento Rt n -Sv e a quella che proviene dal segmento Fd Ex 1.
18 Le rette che uniscono gli Ex e gli Rt che sono operativamente gli uni di fronte agli altri sono dette rette operative. Esse convergono tutte nel punto M. Le rette d'equilibrio Si intendono invece come rette d'equilibrio le rette che collegano tra loro Ex e Rt che sono tra loro. in equilibrio, come ad esempio Ex 1 e Rt 1 oppure Ex 2 e Rt 2 e così via. Tali rette d'equilibrio sono facilissime da definire poiché sono rette che hanno in comune il vertice del diagramma che corrisponde ai solidi inerti. Poiché infatti i solidi sono inerti e rimangono gli stessi qualunque sia la composizione della soluzione imbibente, una retta di equilibrio è quella che parte dal vertice dei solidi e raggiunge la composizione di Ex. Tale retta individua, al'incrocio con il luogo dei raffinati, il raffinato che è in equilibrio con l Ex in questione. La figura precedente riporta l'esempio della retta d'equilibrio che passa per Ex 1. Essa individua la composizione di Rt 1, che è in equilibrio con Ex 1. La valutazione grafica del numero degli stadi teorici si effettua allora continuando ad tracciare alternativamente rette operative e rette all'equilibrio finche Rt è uguale o inferiore a Rt n. Si capisce allora che la valutazione grafica del numero di stadi teorici è più semplice e rapida della soluzione matematica. Le rette che uniscono gli Ex e gli Rt che sono operativamente gli uni di fronte agli altri sono dette rette operative. Esse convergono tutte nel punto M. 6 Esempio 1000 kg/h di fegati di pesce contenenti il 26 % in massa di olio sono estratti con un solvente puro operando in più stadi in controcorrente. Si vuole ottenere un estratto al 40 % in massa di olio e un residuo con meno del 3 % di olio. Si vuole calcolare il numero di stadi ideali e la portata del solvente. I dati d'equilibrio sono riportati in tabella. CONCENTRAZIONE DEL SOLUTO NEL RESIDUO (x Rt ) CONCENTRAZIONE DEL SOLVENTE NEL RESIDUO (y Rt ) 0 0,291 0,025 0,228 0,057 0,229 0,096 0,224 0,142 0,213 0,199 0,199 0,267 0,178 0,238 0,162 Cominciamo con il tracciare sul diagramma triangolare il luogo dei raffinati con i dati della tabella, quindi localizziamo i punti rappresentativi dell'alimentazione (Fd), del solvente (Sv), del residuo (Rt n ) e dell'estratto (Ex 1 ) finali. Si congiungono quindi i punti Fd ed Sv e i punti Rt n ed Ex 1. Intersecandosi i due segmenti individuano il punto M, rappresentativo del miscuglio globale d'estrazione presente all'interno dell'apparecchiatura. Dalla misura dei segmenti FdM e SvM, applicando la regola della leva, possiamo calcolare il rapporto solvente/alimentazione e quindi la portata del solvente. Sv Fd FdM = SvM = 75 mm 131,5 mm = 0,57
19 da cui: Sv = 0,576 * Fd = 0,57 * 1000 kg/h = 570 kg/h Per calcolare il numero di stadi ideali è necessario localizzare il punto M (punto differenza). Esso si trova all intersezione delle rette operative ottenute dal prolungamento dei segmenti Ex 1 Fd e
20 SvRt n. Il numero di stadi ideali si calcola identificando sul diagramma i punti rappresentativi di tutte le correnti entranti ed uscenti da tutti gli stadi. Cominciando da E x1, si traccia un segmento che unisce tale punto al vertice solidi: ciò permette di localizzare, all'intersezione con il luogo dei raffinati Rt 1. Rt 1 è la composizione del raffinato del raffinato all uscita del primo stadio che si trova sulla retta di equilibrio con il vertice del diagramma corrisponde ai solidi inerti ed E x1. Congiungendo quindi M a Rt 1, e prolungando il segmento fino ad incontrare l'ipotenusa, si localizza Ex 2. Si ripete la procedura fino ad individuare un residuo con una concentrazione del soluto uguale o inferiore a quella voluta. I passi da ripetere sono: si individuano le correnti in equilibrio uscenti dallo stadio, nel nostro caso si congiunge Ex 2 al punto al vertice solidi e si individua Rt 2 all'intersezione il luogo dei raffinati; si individuano le correnti all'interstadio, nel nostro caso si traccia la congiungente tra M ed Rt 2 e la si prolunga fino all'ipotenusa, luogo degli estratti, e si localizza Ex 3 corrente all'interstadio con Rt 2. Come si può vedere dalla figura nel nostro caso sono sufficienti 3 stadi teorici per ottenere una concentrazione del soluto nel residuo inferiore a quella desiderata.
ESTRAZIONE CON SOLVENTE o ESTRAZIONE SOLIDO - LIQUIDO
 DEFINIZIONE E l operazione con cui un soluto disperso in una matrice solida inerte (cioè senza alcuna affinità per il soluto) viene estratto mediante un solvente liquido, anch esso inerte. Applicazioni
DEFINIZIONE E l operazione con cui un soluto disperso in una matrice solida inerte (cioè senza alcuna affinità per il soluto) viene estratto mediante un solvente liquido, anch esso inerte. Applicazioni
Estrazione Solido-Liquido
 Estrazione solido-liquido Separazione di uno o più componenti presenti in una fase solida per mezzo di una fase liquida o solvente. Obiettivi Eliminare dalla fase solida un componente indesiderato (lavaggio);
Estrazione solido-liquido Separazione di uno o più componenti presenti in una fase solida per mezzo di una fase liquida o solvente. Obiettivi Eliminare dalla fase solida un componente indesiderato (lavaggio);
Estrazione Solido-Liquido
 Estrazione a stadio singolo ESEMPIO 100kg di semi di soia contenenti il 18 % in peso di olio sono messi in un recipiente contenente due volte il peso iniziale della soia di esano. Il rapporto di imbibizione
Estrazione a stadio singolo ESEMPIO 100kg di semi di soia contenenti il 18 % in peso di olio sono messi in un recipiente contenente due volte il peso iniziale della soia di esano. Il rapporto di imbibizione
ESTRAZIONE SOLIDO/LIQUIDO - ESERCIZI
 ESTRAZIONE SOLIDO/LIQUIDO - ESERCIZI versione#b1 - Prof.A.Tonini www.andytonini.com ES. 1* ESTRAZIONE SOLIDO/LIQUIDO - MONOSTADIO discontinua 200 Kg di prodotto vegetale costituito da semi con 30% di olio
ESTRAZIONE SOLIDO/LIQUIDO - ESERCIZI versione#b1 - Prof.A.Tonini www.andytonini.com ES. 1* ESTRAZIONE SOLIDO/LIQUIDO - MONOSTADIO discontinua 200 Kg di prodotto vegetale costituito da semi con 30% di olio
SEPARAZIONE DI FASE SOLUZIONI NON IDEALI *
 SEPARAZIONE DI FASE SOLUZIONI NON IDEALI * La miscelazione di più componenti chimici allo stato liquido (a temperatura e pressione fissate) può dare origine ad un unica fase liquida, oppure a separazione
SEPARAZIONE DI FASE SOLUZIONI NON IDEALI * La miscelazione di più componenti chimici allo stato liquido (a temperatura e pressione fissate) può dare origine ad un unica fase liquida, oppure a separazione
ATTREZZATURE PER ESTRAZIONE CON SOLVENTE LIQUIDO/LIQUIDO,
 ISTITUTO TECNICO INDUSTRIALE «G. MARCONI» FORLI Tecnologie chimiche industriali CLASSE V ATTREZZATURE PER ESTRAZIONE CON SOLVENTE LIQUIDO/LIQUIDO, Prof. Roberto Riguzzi ESTRAZIONE LIQUIDO/LIQUIDO L estrattore
ISTITUTO TECNICO INDUSTRIALE «G. MARCONI» FORLI Tecnologie chimiche industriali CLASSE V ATTREZZATURE PER ESTRAZIONE CON SOLVENTE LIQUIDO/LIQUIDO, Prof. Roberto Riguzzi ESTRAZIONE LIQUIDO/LIQUIDO L estrattore
Bilancio di Materia per un processo multistadio
 SEZIONE 4.4 Bilancio di Materia per un processo multistadio Alimentazione 2 A C E Alimentazione 1 B UNITA 1 D UNITA 2 Prodotto 3 Prodotto 1 Prodotto 2 Alimentazione 3 Il confine A racchiude tutto il processo,
SEZIONE 4.4 Bilancio di Materia per un processo multistadio Alimentazione 2 A C E Alimentazione 1 B UNITA 1 D UNITA 2 Prodotto 3 Prodotto 1 Prodotto 2 Alimentazione 3 Il confine A racchiude tutto il processo,
ESTRAZIONE CON SOLVENTE
 ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
UNITÀ DIDATTICA 5 LA RETTA
 UNITÀ DIDATTICA 5 LA RETTA 5.1 - La retta Equazione generica della retta Dalle considerazioni emerse nel precedente capitolo abbiamo compreso come una funzione possa essere rappresentata da un insieme
UNITÀ DIDATTICA 5 LA RETTA 5.1 - La retta Equazione generica della retta Dalle considerazioni emerse nel precedente capitolo abbiamo compreso come una funzione possa essere rappresentata da un insieme
CAMPIONAMENTO fondamentale analisi campionamento omogenei stessa composizione variazione l abilità persona variabilità metodo analitico realtà
 CAMPIONAMENTO Un momento fondamentale di una analisi è rappresentato dal campionamento, generalmente si pensa che i campioni da analizzare siano omogenei e che abbiano in ogni punto la stessa composizione,
CAMPIONAMENTO Un momento fondamentale di una analisi è rappresentato dal campionamento, generalmente si pensa che i campioni da analizzare siano omogenei e che abbiano in ogni punto la stessa composizione,
LOGARITMI. Corso di laurea: BIOLOGIA Tutor: Floris Marta; Max Artizzu PRECORSI DI MATEMATICA. L uguaglianza: a x = b
 Corso di laurea: BIOLOGIA Tutor: Floris Marta; Max Artizzu PRECORSI DI MATEMATICA LOGARITMI L uguaglianza: a x = b nella quale a e b rappresentano due numeri reali noti ed x un incognita, è un equazione
Corso di laurea: BIOLOGIA Tutor: Floris Marta; Max Artizzu PRECORSI DI MATEMATICA LOGARITMI L uguaglianza: a x = b nella quale a e b rappresentano due numeri reali noti ed x un incognita, è un equazione
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
Piano cartesiano e retta
 Piano cartesiano e retta Il punto, la retta e il piano sono concetti primitivi di cui non si da una definizione rigorosa, essi sono i tre enti geometrici fondamentali della geometria euclidea. Osservazione
Piano cartesiano e retta Il punto, la retta e il piano sono concetti primitivi di cui non si da una definizione rigorosa, essi sono i tre enti geometrici fondamentali della geometria euclidea. Osservazione
con C A concentrazione del gas disciolto La PA è quindi funzione lineare della concentrazione. La pressione parziale è: P A = Y * Ptot.
 ASSORBIMENTO E una operazione unitaria la cui finalità è l eliminazione di un soluto volatile contenuto in una miscela gassosa. Il solvente liquido scende dall alto mentre la miscela gassosa entra dal
ASSORBIMENTO E una operazione unitaria la cui finalità è l eliminazione di un soluto volatile contenuto in una miscela gassosa. Il solvente liquido scende dall alto mentre la miscela gassosa entra dal
RAPPORTI E PROPORZIONI
 RAPPORTI E PROPORZIONI RAPPORTI E PROPORZIONI Definizione: Dicesi rapporto fra due numeri, preso in un certo ordine, il quoziente della divisione fra il primo di essi e il secondo. Il rapporto tra i numeri
RAPPORTI E PROPORZIONI RAPPORTI E PROPORZIONI Definizione: Dicesi rapporto fra due numeri, preso in un certo ordine, il quoziente della divisione fra il primo di essi e il secondo. Il rapporto tra i numeri
Il diagramma di stato presenta una concavità verso il basso. Distillando miscele che si trovano a sinistra dell azeotropo, cioè più diluite, la
 Il diagramma di stato presenta una concavità verso il basso. Distillando miscele che si trovano a sinistra dell azeotropo, cioè più diluite, la distillazione procede sino al valore massimo di concentrazione
Il diagramma di stato presenta una concavità verso il basso. Distillando miscele che si trovano a sinistra dell azeotropo, cioè più diluite, la distillazione procede sino al valore massimo di concentrazione
INSIEME N. L'insieme dei numeri naturali (N) è l'insieme dei numeri interi e positivi.
 INSIEME N L'insieme dei numeri naturali (N) è l'insieme dei numeri interi e positivi. N = {0;1;2;3... Su tale insieme sono definite le 4 operazioni di base: l'addizione (o somma), la sottrazione, la moltiplicazione
INSIEME N L'insieme dei numeri naturali (N) è l'insieme dei numeri interi e positivi. N = {0;1;2;3... Su tale insieme sono definite le 4 operazioni di base: l'addizione (o somma), la sottrazione, la moltiplicazione
Problemi sulla circonferenza verso l esame di stato
 Problemi sulla circonferenza verso l esame di stato * * * n. 0 pag. 06 a) Scrivi l equazione della circonferenza γ 1 di centro P ; ) e passante per il punto A0; 1). b) Scrivi l equazione della circonferenza
Problemi sulla circonferenza verso l esame di stato * * * n. 0 pag. 06 a) Scrivi l equazione della circonferenza γ 1 di centro P ; ) e passante per il punto A0; 1). b) Scrivi l equazione della circonferenza
RISOLUZIONE DI PROBLEMI DI FISICA
 RISOUZIONE DI PROBEMI DI FISICA Problema 1 Una massa puntiforme m = 2 kg è soggetta ad una forza centrale con associata energia potenziale radiale U( r) 6 A =, dove A = 2 J m 6. Il momento angolare della
RISOUZIONE DI PROBEMI DI FISICA Problema 1 Una massa puntiforme m = 2 kg è soggetta ad una forza centrale con associata energia potenziale radiale U( r) 6 A =, dove A = 2 J m 6. Il momento angolare della
Soluzione Per una miscela di due liquidi
 Soluzione soluto Si definisce soluto il componente che nel passaggio in soluzione perde il suo stato di aggregazione. Un sale che si scioglie in acqua, o un gas che si scioglie in un liquido Solvente Il
Soluzione soluto Si definisce soluto il componente che nel passaggio in soluzione perde il suo stato di aggregazione. Un sale che si scioglie in acqua, o un gas che si scioglie in un liquido Solvente Il
3 H 2 (g) + N 2 (g) 2 NH 3 (g)
 L'equilibrio chimico Alcune reazioni chimiche, come quella tra idrogeno ed ossigeno, vanno avanti fino all'esaurimento del reagente in difetto stechiometrico. Tuttavia ce ne sono altre, come quella tra
L'equilibrio chimico Alcune reazioni chimiche, come quella tra idrogeno ed ossigeno, vanno avanti fino all'esaurimento del reagente in difetto stechiometrico. Tuttavia ce ne sono altre, come quella tra
1. CALCOLO DELLA QUANTITÀ D'ARIA NECESSARIA ALLA COMBUSTIONE DI UN DATO COMBUSTIBILE
 1. ALL DELLA QUANTITÀ D'ARIA NEESSARIA ALLA MBUSTINE DI UN DAT MBUSTIBILE 1.1. Reazioni di combustione stechiometrica di un idrocarburo m omponente Simbolo Peso molecolare (M) arbonio (12) Idrogeno 2 (2)
1. ALL DELLA QUANTITÀ D'ARIA NEESSARIA ALLA MBUSTINE DI UN DAT MBUSTIBILE 1.1. Reazioni di combustione stechiometrica di un idrocarburo m omponente Simbolo Peso molecolare (M) arbonio (12) Idrogeno 2 (2)
Applicazione della TSVD allo studio di una colonna di distillazione
 UNIVERSITÀ DEGLI STUDI DI CAGLIARI SCUOLA DI DOTTORATO IN INGEGNERIA INDUSTRIALE Tesina di Metodi Iterativi per la Risoluzione di Sistemi Lineari e Non Lineari Applicazione della TSVD allo studio di una
UNIVERSITÀ DEGLI STUDI DI CAGLIARI SCUOLA DI DOTTORATO IN INGEGNERIA INDUSTRIALE Tesina di Metodi Iterativi per la Risoluzione di Sistemi Lineari e Non Lineari Applicazione della TSVD allo studio di una
Un sistema eterogeneo è in equilibrio quando in ogni sua parte è stato raggiunto l equilibrio:
 equilibri eterogenei Un sistema eterogeneo è in equilibrio quando in ogni sua parte è stato raggiunto l equilibrio: (a) termico (temperatura uguale dappertutto); (b) meccanico (pressione uniformemente
equilibri eterogenei Un sistema eterogeneo è in equilibrio quando in ogni sua parte è stato raggiunto l equilibrio: (a) termico (temperatura uguale dappertutto); (b) meccanico (pressione uniformemente
C I R C O N F E R E N Z A...
 C I R C O N F E R E N Z A... ESERCITAZIONI SVOLTE 3 Equazione della circonferenza di noto centro C e raggio r... 3 Equazione della circonferenza di centro C passante per un punto A... 3 Equazione della
C I R C O N F E R E N Z A... ESERCITAZIONI SVOLTE 3 Equazione della circonferenza di noto centro C e raggio r... 3 Equazione della circonferenza di centro C passante per un punto A... 3 Equazione della
Lezione 2. Leggi ponderali
 Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
DIMENSIONAMENTO Determinazione delle portate F, D, W a determinate condizioni di concentrazione z F, x D e x W Determinazione del numero teorico dei p
 2 ITIS Marconi Forlì Dicembre 204 Roberto Zannoni DIMENSIONAMENTO Determinazione delle portate F, D, W a determinate condizioni di concentrazione z F, x D e x W Determinazione del numero teorico dei piatti.
2 ITIS Marconi Forlì Dicembre 204 Roberto Zannoni DIMENSIONAMENTO Determinazione delle portate F, D, W a determinate condizioni di concentrazione z F, x D e x W Determinazione del numero teorico dei piatti.
I RADICALI QUADRATICI
 I RADICALI QUADRATICI 1. Radici quadrate Definizione di radice quadrata: Si dice radice quadrata di un numero reale positivo o nullo a, e si indica con a, il numero reale positivo o nullo (se esiste) che,
I RADICALI QUADRATICI 1. Radici quadrate Definizione di radice quadrata: Si dice radice quadrata di un numero reale positivo o nullo a, e si indica con a, il numero reale positivo o nullo (se esiste) che,
EVAPORAZIONE 2. Dati di progetto relativi ai vapori circolanti nell impianto:
 EVAPORAZIONE 2 1. Una soluzione acquosa deve essere concentrata dal 10% al 25% in massa mediante un sistema di evaporazione a doppio effetto in controcorrente. Sapendo che: a) la soluzione diluita entra
EVAPORAZIONE 2 1. Una soluzione acquosa deve essere concentrata dal 10% al 25% in massa mediante un sistema di evaporazione a doppio effetto in controcorrente. Sapendo che: a) la soluzione diluita entra
Illustrazione 1: Telaio. Piantanida Simone 1 G Scopo dell'esperienza: Misura di grandezze vettoriali
 Piantanida Simone 1 G Scopo dell'esperienza: Misura di grandezze vettoriali Materiale utilizzato: Telaio (carrucole,supporto,filo), pesi, goniometro o foglio con goniometro stampato, righello Premessa
Piantanida Simone 1 G Scopo dell'esperienza: Misura di grandezze vettoriali Materiale utilizzato: Telaio (carrucole,supporto,filo), pesi, goniometro o foglio con goniometro stampato, righello Premessa
numero complessivo di variabili = c f + 2
 Regola delle fasi Definiamo sostanza pura quella che ha composizione chimica costante Diremo fase di una sostanza pura una sua regione omogenea dal punto di vista fisico. Lo stato di un sistema è individuato
Regola delle fasi Definiamo sostanza pura quella che ha composizione chimica costante Diremo fase di una sostanza pura una sua regione omogenea dal punto di vista fisico. Lo stato di un sistema è individuato
Stabilire se il punto di coordinate (1,1) appartiene alla circonferenza centrata nell origine e di raggio 1.
 Definizione di circonferenza e cerchio. Equazione della circonferenza centrata in O e di raggio R. Esercizi. La circonferenza e il cerchio Definizioni: dato un punto C nel piano cartesiano e dato un numero
Definizione di circonferenza e cerchio. Equazione della circonferenza centrata in O e di raggio R. Esercizi. La circonferenza e il cerchio Definizioni: dato un punto C nel piano cartesiano e dato un numero
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia. Corso di Analisi Chimico-Tossicologica.
 Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
IMPIANTI E PROCESSI CHIMICI. Tema A 27 Settembre 2011 Estrazione con solvente configurazione multistadio controcorrente
 IMPIANTI E PROCESSI CHIMICI Tema A 27 Settembre 2011 Estrazione con solvente configurazione multistadio controcorrente Soluzione Utilizzando i dati di equilibrio è possibile ricavare il diagramma che lega
IMPIANTI E PROCESSI CHIMICI Tema A 27 Settembre 2011 Estrazione con solvente configurazione multistadio controcorrente Soluzione Utilizzando i dati di equilibrio è possibile ricavare il diagramma che lega
L insieme dei numeri Relativi (Z)
 L insieme dei numeri Relativi (Z) L esigenza dei numeri relativi Due precise situazioni ci spingono ad ampliare l'insieme de numeri naturali (N): una di carattere pratico, un'altra di carattere più teorico.
L insieme dei numeri Relativi (Z) L esigenza dei numeri relativi Due precise situazioni ci spingono ad ampliare l'insieme de numeri naturali (N): una di carattere pratico, un'altra di carattere più teorico.
Il riscaldamento può essere effettuato con un bagno ad acqua, ad olio, un mantello scaldante, tenendo in considerazione che deve essere effettuato
 DISTILLAZIONE La distillazione è una tecnica di purificazione che permette la separazione di liquidi o di solidi bassofondenti che fondono senza alterazione chimica. Si basa fondamentalmente sull equilibrio
DISTILLAZIONE La distillazione è una tecnica di purificazione che permette la separazione di liquidi o di solidi bassofondenti che fondono senza alterazione chimica. Si basa fondamentalmente sull equilibrio
SOTTOSPAZI E OPERAZIONI IN SPAZI DIVERSI DA R n
 SPAZI E SOTTOSPAZI 1 SOTTOSPAZI E OPERAZIONI IN SPAZI DIVERSI DA R n Spazi di matrici. Spazi di polinomi. Generatori, dipendenza e indipendenza lineare, basi e dimensione. Intersezione e somma di sottospazi,
SPAZI E SOTTOSPAZI 1 SOTTOSPAZI E OPERAZIONI IN SPAZI DIVERSI DA R n Spazi di matrici. Spazi di polinomi. Generatori, dipendenza e indipendenza lineare, basi e dimensione. Intersezione e somma di sottospazi,
Capitolo 5. Primo principio della Termodinamica nei sistemi aperti
 Capitolo 5. Primo principio della Termodinamica nei sistemi aperti 5.1. I sistemi aperti I sistemi aperti sono quei sistemi termodinamici nei quali, oltre allo scambio di lavoro e calore è possibile lo
Capitolo 5. Primo principio della Termodinamica nei sistemi aperti 5.1. I sistemi aperti I sistemi aperti sono quei sistemi termodinamici nei quali, oltre allo scambio di lavoro e calore è possibile lo
DAC Digital Analogic Converter
 DAC Digital Analogic Converter Osserviamo lo schema elettrico riportato qui a lato, rappresenta un convertitore Digitale-Analogico a n Bit. Si osservino le resistenze che di volta in volta sono divise
DAC Digital Analogic Converter Osserviamo lo schema elettrico riportato qui a lato, rappresenta un convertitore Digitale-Analogico a n Bit. Si osservino le resistenze che di volta in volta sono divise
Geometria analitica di base (seconda parte)
 SAPERE Al termine di questo capitolo, avrai appreso: il concetto di luogo geometrico la definizione di funzione quadratica l interpretazione geometrica di un particolare sistema di equazioni di secondo
SAPERE Al termine di questo capitolo, avrai appreso: il concetto di luogo geometrico la definizione di funzione quadratica l interpretazione geometrica di un particolare sistema di equazioni di secondo
2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO
 2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO E' noto che la combustione di un combustibile fossile produce anidride carbonica (CO 2 ), rinvenibile dunque nei prodotti della combustione. Nella
2. CALCOLO DELL'ANIDRIDE CARBONICA NEI GAS DI SCARICO E' noto che la combustione di un combustibile fossile produce anidride carbonica (CO 2 ), rinvenibile dunque nei prodotti della combustione. Nella
Collegamento generatori di tensione. Collegamento parallelo. Sia dato il sistema di figura 1: Fig. 1 -
 Collegamento generatori di tensione Collegamento parallelo Sia dato il sistema di figura : Fig. - vogliamo trovare il bipolo equivalente al parallelo dei tre generatori di tensione, il bipolo, cioè, che
Collegamento generatori di tensione Collegamento parallelo Sia dato il sistema di figura : Fig. - vogliamo trovare il bipolo equivalente al parallelo dei tre generatori di tensione, il bipolo, cioè, che
Navigazione Tattica. L intercettazione
 Navigazione Tattica I problemi di navigazione tattica si distinguono in: Intercettazione, che riguarda lo studio delle procedure atte a raggiungere nel minor tempo possibile un aeromobile o un qualsiasi
Navigazione Tattica I problemi di navigazione tattica si distinguono in: Intercettazione, che riguarda lo studio delle procedure atte a raggiungere nel minor tempo possibile un aeromobile o un qualsiasi
1 Prodotto cartesiano di due insiemi 1. 5 Soluzioni degli esercizi 6
 1 PRODOTTO CARTESIANO DI DUE INSIEMI 1 I-4 R 2 ed R 3 Piano e spazio cartesiani Indice 1 Prodotto cartesiano di due insiemi 1 2 Rappresentazione di R 2 sul piano cartesiano 2 3 Sottoinsiemi di R 2 e regioni
1 PRODOTTO CARTESIANO DI DUE INSIEMI 1 I-4 R 2 ed R 3 Piano e spazio cartesiani Indice 1 Prodotto cartesiano di due insiemi 1 2 Rappresentazione di R 2 sul piano cartesiano 2 3 Sottoinsiemi di R 2 e regioni
GASCROMATOGRAFIA INTRODUZIONE
 GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
Equazioni lineari con due o più incognite
 Equazioni lineari con due o più incognite Siano date le uguaglianze: k 0; x + y = 6; 3a + b c = 8. La prima ha un termine incognito rappresentato dal simbolo letterale k; la seconda ha due termini incogniti
Equazioni lineari con due o più incognite Siano date le uguaglianze: k 0; x + y = 6; 3a + b c = 8. La prima ha un termine incognito rappresentato dal simbolo letterale k; la seconda ha due termini incogniti
TERMODINAMICA. Studia le trasformazioni dei sistemi in relazione agli scambi di calore e lavoro. GENERALITÀ SUI SISTEMI TERMODINAMICI
 TERMODINAMICA Termodinamica: scienza che studia le proprietà e il comportamento dei sistemi, la loro evoluzione e interazione con l'ambiente esterno che li circonda. Studia le trasformazioni dei sistemi
TERMODINAMICA Termodinamica: scienza che studia le proprietà e il comportamento dei sistemi, la loro evoluzione e interazione con l'ambiente esterno che li circonda. Studia le trasformazioni dei sistemi
Unità Didattica N 9 : La parabola
 0 Matematica Liceo \ Unità Didattica N 9 La parabola Unità Didattica N 9 : La parabola ) La parabola ad asse verticale ) La parabola ad asse orizzontale 5) Intersezione di una parabola con una retta 6)
0 Matematica Liceo \ Unità Didattica N 9 La parabola Unità Didattica N 9 : La parabola ) La parabola ad asse verticale ) La parabola ad asse orizzontale 5) Intersezione di una parabola con una retta 6)
B6. Sistemi di primo grado
 B6. Sistemi di primo grado Nelle equazioni l obiettivo è determinare il valore dell incognita che verifica l equazione. Tale valore, se c è, è detto soluzione. In un sistema di equazioni l obiettivo è
B6. Sistemi di primo grado Nelle equazioni l obiettivo è determinare il valore dell incognita che verifica l equazione. Tale valore, se c è, è detto soluzione. In un sistema di equazioni l obiettivo è
Esercizi svolti. Geometria analitica: rette e piani
 Esercizi svolti. Sistemi di riferimento e vettori. Dati i vettori v = i + j k, u =i + j + k determinare:. il vettore v + u ;. gli angoli formati da v e u;. i vettore paralleli alle bisettrici di tali angoli;
Esercizi svolti. Sistemi di riferimento e vettori. Dati i vettori v = i + j k, u =i + j + k determinare:. il vettore v + u ;. gli angoli formati da v e u;. i vettore paralleli alle bisettrici di tali angoli;
( 1 ) AB:A B =BC:B C =CA:C A
 Goniometria II parte Funzioni goniometriche: seno, coseno tangente Ricordiamo che: Due triangoli si dicono simili se hanno gli angoli ordinatamente uguali e i lati omologhi (nel caso dei triangoli i lati
Goniometria II parte Funzioni goniometriche: seno, coseno tangente Ricordiamo che: Due triangoli si dicono simili se hanno gli angoli ordinatamente uguali e i lati omologhi (nel caso dei triangoli i lati
INSIEME Q. Le operazioni di addizione, moltiplicazione e sottrazione erano operazioni già chiuse su Z, e lo rimangono in Q. Alcune definizioni
 INSIEME Q L'insieme dei numeri razionali (Q) è un'estensione dell'insieme dei numeri interi Z. Ai numeri positivi e negativi interi si aggiungono, così, anche i numeri decimali. Tale estensione, però,
INSIEME Q L'insieme dei numeri razionali (Q) è un'estensione dell'insieme dei numeri interi Z. Ai numeri positivi e negativi interi si aggiungono, così, anche i numeri decimali. Tale estensione, però,
Amministrazione, finanza e marketing - Turismo Ministero dell Istruzione, dell Università e della Ricerca PROGRAMMAZIONE DISCIPLINARE PER U. di A.
 MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
Elementi di matematica - dott. I. GRASSI
 Gli assi cartesiani e la retta. Il concetto di derivata. È ormai d uso comune nei libri, in televisione, nei quotidiani descrivere fenomeni di varia natura per mezzo di rappresentazioni grafiche. Tali
Gli assi cartesiani e la retta. Il concetto di derivata. È ormai d uso comune nei libri, in televisione, nei quotidiani descrivere fenomeni di varia natura per mezzo di rappresentazioni grafiche. Tali
SCHEMA DELL ESTRAZIONE MISCELA ETEROGENEA
 SCHEMA DELL ESTRAZIONE MISCELA ETEROGENEA TIPOLOGIE DELLE ESTRAZIONI L ESTRAZIONE PUO ESSERE CONDOTTA: 1. A SINGOLO STADIO; 2. A STADI MULTIPLI IN CORRENTI INCROCIATE; 3. A STADI MULTIPLI IN CONTROCORRENTE.
SCHEMA DELL ESTRAZIONE MISCELA ETEROGENEA TIPOLOGIE DELLE ESTRAZIONI L ESTRAZIONE PUO ESSERE CONDOTTA: 1. A SINGOLO STADIO; 2. A STADI MULTIPLI IN CORRENTI INCROCIATE; 3. A STADI MULTIPLI IN CONTROCORRENTE.
La retta nel piano cartesiano
 La retta nel piano cartesiano Cominciamo con qualche esempio. I) Rette parallele agli assi cartesiani Consideriamo la retta r in figura: i punti della retta hanno sempre ordinata uguale a 3. P ( ;3) Q
La retta nel piano cartesiano Cominciamo con qualche esempio. I) Rette parallele agli assi cartesiani Consideriamo la retta r in figura: i punti della retta hanno sempre ordinata uguale a 3. P ( ;3) Q
Capitolo 2. Cenni di geometria analitica nel piano
 Capitolo Cenni di geometria analitica nel piano 1 Il piano cartesiano Il piano cartesiano è una rappresentazione grafica del prodotto cartesiano R = R R La rappresentazione grafica è possibile se si crea
Capitolo Cenni di geometria analitica nel piano 1 Il piano cartesiano Il piano cartesiano è una rappresentazione grafica del prodotto cartesiano R = R R La rappresentazione grafica è possibile se si crea
Sistema di due equazioni di primo grado in due incognite
 Sistema di due equazioni di primo grado in due incognite Problema Un trapezio rettangolo di area cm ha altezza di 8 cm. Sapendo che il triplo della base minore è inferiore di cm al doppio della base maggiore
Sistema di due equazioni di primo grado in due incognite Problema Un trapezio rettangolo di area cm ha altezza di 8 cm. Sapendo che il triplo della base minore è inferiore di cm al doppio della base maggiore
Algebra vettoriale. Capitolo 5. 5.1 Grandezze scalari. 5.2 Grandezze vettoriali
 Capitolo 5 5.1 Grandezze scalari Si definiscono scalari quelle grandezze fisiche che sono descritte in modo completo da un numero accompagnato dalla sua unità di misura. La temperatura dell aria in una
Capitolo 5 5.1 Grandezze scalari Si definiscono scalari quelle grandezze fisiche che sono descritte in modo completo da un numero accompagnato dalla sua unità di misura. La temperatura dell aria in una
FUNZIONE DI UTILITÀ CURVE DI INDIFFERENZA (Cap. 3)
 FUNZIONE DI UTILITÀ CURVE DI INDIFFERENZA (Cap. 3) Consideriamo un agente che deve scegliere un paniere di consumo fra quelli economicamente ammissibili, posto che i beni di consumo disponibili sono solo
FUNZIONE DI UTILITÀ CURVE DI INDIFFERENZA (Cap. 3) Consideriamo un agente che deve scegliere un paniere di consumo fra quelli economicamente ammissibili, posto che i beni di consumo disponibili sono solo
ESTRAZIONE SOLVENTI. tecnica di separazione e purificazione
 ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
Estrazione. Il processo di estrazione con solventi è impiegato per l isolamento di
 Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
CORSO DI CHIMICA. Esercitazione del 7 Giugno 2016
 CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
Risoluzione di problemi ingegneristici con Excel
 Risoluzione di problemi ingegneristici con Excel Problemi Ingegneristici Calcolare per via numerica le radici di un equazione Trovare l equazione che lega un set di dati ottenuti empiricamente (fitting
Risoluzione di problemi ingegneristici con Excel Problemi Ingegneristici Calcolare per via numerica le radici di un equazione Trovare l equazione che lega un set di dati ottenuti empiricamente (fitting
Equazioni Polinomiali II Parabola
 Equazioni Polinomiali II Parabola - 0 Equazioni Polinomiali del secondo grado (Polinomi II) Forma Canonica e considerazioni La forma canonica dell equazione polinomiale di grado secondo è la seguente:
Equazioni Polinomiali II Parabola - 0 Equazioni Polinomiali del secondo grado (Polinomi II) Forma Canonica e considerazioni La forma canonica dell equazione polinomiale di grado secondo è la seguente:
Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali.
 Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Rev. 02/13. Antonio Coviello. ITIS Fermi TV
 ASSORBIMENTO Rev. 02/13 Antonio Coviello ITIS Fermi TV SCHEMA COSTRUTTIVO TORRE DI ASSORBIMENTO CON RIEMPIMENTO ASS-ES01: Biossido di Zolfo / Aria / Acqua Una portata di 125 Kmoli/h di aria contenente
ASSORBIMENTO Rev. 02/13 Antonio Coviello ITIS Fermi TV SCHEMA COSTRUTTIVO TORRE DI ASSORBIMENTO CON RIEMPIMENTO ASS-ES01: Biossido di Zolfo / Aria / Acqua Una portata di 125 Kmoli/h di aria contenente
ax 1 + bx 2 + c = 0, r : 2x 1 3x 2 + 1 = 0.
 . Rette in R ; circonferenze. In questo paragrafo studiamo le rette e le circonferenze in R. Ci sono due modi per descrivere una retta in R : mediante una equazione cartesiana oppure mediante una equazione
. Rette in R ; circonferenze. In questo paragrafo studiamo le rette e le circonferenze in R. Ci sono due modi per descrivere una retta in R : mediante una equazione cartesiana oppure mediante una equazione
Y = ax 2 + bx + c LA PARABOLA
 LA PARABOLA La parabola è una figura curva che, come la retta, è associata ad un polinomio che ne definisce l'equazione. A differenza della retta, però, il polinomio non è di primo grado, ma è di secondo
LA PARABOLA La parabola è una figura curva che, come la retta, è associata ad un polinomio che ne definisce l'equazione. A differenza della retta, però, il polinomio non è di primo grado, ma è di secondo
4) 8 g di idrogeno reagiscono esattamente con 64 g di ossigeno secondo la seguente reazione:
 Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
ESERCIZI su ESTRAZIONE Liquido/Liquido caso immiscibilità diluente-solvente- versione#a2 Prof. A.Tonini
 ESERCIZI su ESTRAZIONE Liquido/Liquido caso immiscibilità diluente-solvente- versione#a2 www.andytonini.com [vedi documento di teoria su estrazione L/L immiscibilità totale] LEGENDA = A:SOLUTO; B:diluente=NON
ESERCIZI su ESTRAZIONE Liquido/Liquido caso immiscibilità diluente-solvente- versione#a2 www.andytonini.com [vedi documento di teoria su estrazione L/L immiscibilità totale] LEGENDA = A:SOLUTO; B:diluente=NON
LEZIONE 4. Le soluzioni
 LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
Estrazione solido-liquido
 Metodo grafico di calcolo - Gradi di libertà Il nuero di gradi di libertà dell operazione di estrazione solido-liquido può essere ricavato facilente dall analisi delle variabili in gioco e delle relazioni
Metodo grafico di calcolo - Gradi di libertà Il nuero di gradi di libertà dell operazione di estrazione solido-liquido può essere ricavato facilente dall analisi delle variabili in gioco e delle relazioni
La Retta Ogni funzione di primo grado rappresenta, graficamente, una retta. L equazione della retta può essere scritta in due modi
 La Retta Ogni funzione di primo grado rappresenta, graficamente, una retta. L equazione della retta può essere scritta in due modi Forma implicita Forma esplicita a x b y c 0 y m x q a c y x b b Esempio
La Retta Ogni funzione di primo grado rappresenta, graficamente, una retta. L equazione della retta può essere scritta in due modi Forma implicita Forma esplicita a x b y c 0 y m x q a c y x b b Esempio
SOLUZIONI. questa è l area della parte restante : è più grande o più piccola dell area del cerchio?
 IV a GARA MATEMATICA CITTÀ DI PADOVA 15 aprile 1989 SOLUZIONI 1.- Indichiamo con l il lato del triangolo rettangolo isoscele : Area del triangolo = Area del cerchio inscritto = che si ottiene dalla doppia
IV a GARA MATEMATICA CITTÀ DI PADOVA 15 aprile 1989 SOLUZIONI 1.- Indichiamo con l il lato del triangolo rettangolo isoscele : Area del triangolo = Area del cerchio inscritto = che si ottiene dalla doppia
PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010
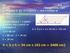 PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010 1) PIANO CARTESIANO serve per indicare, identificare, chiamare... ogni PUNTO del piano (ente geometrico) con una coppia di valori numerici (detti COORDINATE).
PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010 1) PIANO CARTESIANO serve per indicare, identificare, chiamare... ogni PUNTO del piano (ente geometrico) con una coppia di valori numerici (detti COORDINATE).
Le equazioni di I grado
 Le equazioni di I grado ITIS Feltrinelli anno scolastico 007-008 R. Folgieri 007-008 1 Le equazioni abbiamo una uguaglianza tra due quantità (espressioni algebriche, perché nei due termini ci possono essere
Le equazioni di I grado ITIS Feltrinelli anno scolastico 007-008 R. Folgieri 007-008 1 Le equazioni abbiamo una uguaglianza tra due quantità (espressioni algebriche, perché nei due termini ci possono essere
Sistemi di 1 grado in due incognite
 Sistemi di 1 grado in due incognite Problema In un cortile ci sono polli e conigli: in totale le teste sono 7 e zampe 18. Quanti polli e quanti conigli ci sono nel cortile? Soluzione Indichiamo con e con
Sistemi di 1 grado in due incognite Problema In un cortile ci sono polli e conigli: in totale le teste sono 7 e zampe 18. Quanti polli e quanti conigli ci sono nel cortile? Soluzione Indichiamo con e con
Anno 2. Circonferenza e retta: definizioni e proprietà
 Anno 2 Circonferenza e retta: definizioni e proprietà 1 Introduzione I Sumeri furono tra i primi popoli ad occuparsi di matematica, e in particolare di problemi relativi alla. La è una figura geometrica
Anno 2 Circonferenza e retta: definizioni e proprietà 1 Introduzione I Sumeri furono tra i primi popoli ad occuparsi di matematica, e in particolare di problemi relativi alla. La è una figura geometrica
COMPENDIO ESPONENZIALI LOGARITMI
 TORINO SETTEMBRE 2010 COMPENDIO DI ESPONENZIALI E LOGARITMI di Bart VEGLIA 1 ESPONENZIALi 1 Equazioni esponenziali Un espressione in cui l incognita compare all esponente di una o più potenze si chiama
TORINO SETTEMBRE 2010 COMPENDIO DI ESPONENZIALI E LOGARITMI di Bart VEGLIA 1 ESPONENZIALi 1 Equazioni esponenziali Un espressione in cui l incognita compare all esponente di una o più potenze si chiama
Lezione 6 Richiami di Geometria Analitica
 1 Piano cartesiano Lezione 6 Richiami di Geometria Analitica Consideriamo nel piano due rette perpendicolari che si intersecano in un punto O Consideriamo ciascuna di queste rette come retta orientata
1 Piano cartesiano Lezione 6 Richiami di Geometria Analitica Consideriamo nel piano due rette perpendicolari che si intersecano in un punto O Consideriamo ciascuna di queste rette come retta orientata
Elementi di teoria degli insiemi
 ppendice Elementi di teoria degli insiemi.1 Introduzione Comincia qui l esposizione di alcuni concetti primitivi, molto semplici da un punto di vista intuitivo, ma a volte difficili da definire con grande
ppendice Elementi di teoria degli insiemi.1 Introduzione Comincia qui l esposizione di alcuni concetti primitivi, molto semplici da un punto di vista intuitivo, ma a volte difficili da definire con grande
Esercizi svolti sulla parabola
 Liceo Classico Galilei Pisa - Classe a A - Prof. Francesco Daddi - 19 dicembre 011 Esercizi svolti sulla parabola Esercizio 1. Determinare l equazione della parabola avente fuoco in F(1, 1) e per direttrice
Liceo Classico Galilei Pisa - Classe a A - Prof. Francesco Daddi - 19 dicembre 011 Esercizi svolti sulla parabola Esercizio 1. Determinare l equazione della parabola avente fuoco in F(1, 1) e per direttrice
