Premesse. le reazioni di ossido-riduzione implicano il trasferimento di elettroni dalla specie ossidante alla specie riducente
|
|
|
- Ladislao Gattini
- 5 anni fa
- Visualizzazioni
Transcript
1 Premesse le reazini di ssid-riduzine implican il trasferiment di elettrni dalla specie ssidante alla specie riducente un fluss di elettrni genera unacrrente elettrica l'elettrchimica studia l'intercnversine tra energia chimica e energia elettrica
2 cella galvanica pila dispsitiv che trasfrma energia chimica in energia elettrica sfrutta unareazine redx spntanea cella elettrlitica dispsitiv che trasfrma energia elettrica in energia chimica vi avvengn reazini redx nn spntanee
3 Immergend una barretta di metall, es. Zinc, in acqua, alcuni ini del metall passan dal reticl metallic in sluzine, idratandsi, e lasciand gli elettrni nel metall. La sluzine di caricherà psitivamente e il metall negativamente, generand una differenza di ptenziale all interfaccia metallsluzine. Avverrà anche il passaggi invers: ini Zn + in sluzine si scarican sul metall trasfrmandsi in atmi. All interfase si avrà l equilibri dinamic: Zn (aq) + + e - Zn (s)
4
5 Pile Zn (s) + Cu (aq) + Zn (aq) + + Cu (s)
6 Pila Daniell elettrd elettrd and ( ) catd (+) semielement I semielement II reazini di ssidazine reazini di riduzine Zn (s) Zn (aq) + + e - Cu (aq) + + e - Cu (s) Zn (s) + Cu (aq) + Zn (aq) + + Cu (s)
7 Rappresentazine schematica di una pila Zn Zn + (aq) elettrd + sluzine semielement Cu Cu + (aq) elettrd + sluzine semielement (-) and Zn Zn + C 1 Cu + C Cu (+) catd semielement I semielement II
8 Ptenziale di cella gli elettrni migran dall'and al catd a causa della differenza di ptenziale che si genera tra i due elettrdi la frza in grad di spstare gli elettrni lung il circuit è chiamata ptenziale di cella () frza elettrmtrice (f.e.m.) si misura invlt = jule/culmb tramite un vltmetr
9 Ptenziale di cella Fluss di elettrni: and catd and ( ) catd (+) Differenza di ptenziale (d.d.p.) è detta frza elettrmtrice (f.e.m.) della pila f.e.m. = (+) - (-) = riduzine - ssidazine
10 il ptenziale di un elettrd si determina dalla misura della f.e.m. di pile ttenute accppiand l elettrd cn un di riferiment gli elettrdi devn trvarsi incndizinistandard: cncentrazine 1M delle specie iniche; pressine di 1 atm per sstanze gassse temperatura di 5 C l elettrd utilizzat cme riferiment è l elettrd nrmale ad idrgen Ptenziali d elettrd
11 lettrd nrmale a idrgen (elettrd nrmale standard) È il semielement utilizzat cme riferiment a cui si attribuisce il ptenziale di 0 V; utilizzat per la misura dei ptenziali degli altri semielementi H 3 O + (aq) + e - H (g) + H O H + (aq) + e - H (g) 0 V H / H (H + /H cppia redx) H (g), Pt H + P = 1 atm C = 1.0 M Cndizini standard ( nrmali): 5 C per sstanze gassse: P = 1.0 atm per sluzini: C = 1.0 M
12 Pile nrmali ( pile standard) Cu (aq) + + e - Cu (s) H (g) H + (aq) + e - catd (+) riduzine and ( ) ssidazine Cu (aq) + + H (g) Cu (s) + H + (aq) L elettrd ad idrgen fa da and (-) H (g), Pt H + P = 1 atm 1.0 M Cu + Cu (+) 1.0 M IMP. n e ceduti all and = n e acquisiti al catd (Faraday)
13 Misura dei ptenziali nrmali standard, (-) H (g), Pt H + P = 1 atm 1.0 M Cu + Cu (+) 1.0 M H (g) H + (aq) + e - Cu (aq) + + e - Cu (s) reazine di ssidazine reazine di riduzine Cu (aq) + + H (g) Cu (s) + H + (aq) reazine glbale f.e.m. Catd and Cu /Cu H / H Cu /Cu V Cu /Cu 0.34 V (Cu + /Cu cppia redx)
14 Pile nrmali ( pile standard) Zn (s) Zn (aq) + + e - and ( ) ssidazine H + (aq) + e - H (g) catd (+) riduzine Zn (s) + H + (aq)zn (aq) + + H (g) (-) Zn Zn M H + Pt, H (g) (+) 1.0 M P = 1 atm L elettrd ad idrgen fa da catd IMP. n e ceduti all and = n e acquisiti al catd (Faraday)
15 Misura dei ptenziali nrmali standard, (-) Zn Zn M H + Pt, H (g) (+) 1.0 M P = 1 atm H + (aq) + e - H (g) Zn (s) Zn (aq) + + e - Zn (s) + H + (aq)zn (aq) + + H (g) reazine di riduzine reazine di ssidazine reazine glbale f.e.m. Catd and H / H Zn / Zn 0 Zn / Zn 0.76 V Zn / Zn 0.76 V (Zn + /Zn cppia redx)
16 Ptenziali nrmali ( standard) di riduzine i ptenziali nrmali di riduzine,, si determinan misurand la f.e.m. di pile ttenute accppiand l elettrd nrmale ad idrgen cn semielementi (nrmali) cstituiti da elettrdi immersi in sluzini 1M dei prpri ini; per cnvenzine i ptenziali sn riprtati cme ptenziali nrmali di riduzine perché riferiti alla semireazine di riduzine dà una misura quantitativa della tendenza di una cppia redx a cmprtarsi cme ssidante riducente rispett alla cppia H + /H per una data semicppia (cppia redx): maggire è il valre di e maggire è la sua tendenza a ridursi, e viceversa.
17 Ptenziali nrmali di riduzine (serie elettrchimica degli elementi) Frza cme ssidante Frza cme riducente
18 Tipi di elettrdi gli elettrdi di Cu, Ag e Zn snelettrdi di1 a specie: metall immers in una sluzine cntenente i sui ini sn spess usati anche elettrdi inerti (elettrdi ad ssidriduzine): funzinan da semplici cnduttri di crrente nn intervengn nella reazine redx
19 lettrdi di 1 specie Zn (s) + Cu (aq) + Zn (aq) + + Cu (s) I) Zn Zn + + e Semireazine di ssidazine II) Cu + + e Cu Semireazine di riduzine (-) and Zn Zn + Cu + Cu (+) catd semielement I semielement II
20 lettrdi ad ssidriduzine si ssida Fe 3+ + Cr + Cr 3+ + Fe + si riduce I) Cr + Cr 3+ + e Semireazine di ssidazine II) Fe 3+ + e Fe + Semireazine di riduzine (-) and Pt Cr +, C1 Cr 3+, C Fe 3+, C1 Fe +, C Pt (+) catd semielement I semielement II
21 lettrdi a gas Zn Zn +, C 1 H 3 O +, C H, Pt (1 atm) semielement I lettrd di 1 specie semielement II lettrd a gas I) Zn Zn + + e Semireazine di ssidazine II) H + + e H Semireazine di riduzine
22 lettrdi di specie Ag AgCl (s) KCl 10 - M AgCl sale pc slubile Ks =1,5 x10-10 Ag / Ag Ag + + e V Ag (s) In sluzine abbiam: AgCl (s) Ag + + Cl - s s KCl K + + Cl Ks = [Ag + [Cl - s s Ks [ Ag [Cl Ks 0.01
23 Calclare la f.e.m. a 5 C della pila nrmale cstituita dai seguenti elettrdi. Scrivere le semireazini di riduzine ed ssidazine e la reazine glbale indicand il vers della reazine spntanea. Cu / Cu 0.34 V c Cu (aq) + + e - Cu (s) Zn / Zn 0.76 V a Zn (s) Zn (aq) + + e - f.e.m. = c a = (- 0.76) = V (-) and Zn Zn +, 1 M Cu +, 1 M Cu (+) catd La reazine spntanea è: Zn (s) + Cu (aq) + Zn (aq) + + Cu (s)
24 Data la seguente pila nrmale stabilire quale semielement funzina da catd e quale da and e calclare la f.e.m. a 5 C H / H 0.00 V a Cl / Cl V c f.e.m. c a Cl / Cl H / H V (-) and H, Pt (1 atm) H +, 1 M Cl -, 1 M Pt, Cl (1 atm) (+) catd Sarann spntanee le reazini nel vers: Cl + e Cl - H H + + e Cl + H Cl - + H + semireazine di riduzine semireazine di ssidazine reazine spntanea
25 Data la seguente pila nrmale stabilire quale semielement funzina da catd e quale da and e calclare la f.e.m. a 5 C. H / H 0.00 V a Ag / Ag 0.80 V c f.e.m. c a Ag / Ag H /H V (-) and H, Pt (1 atm) H + 1 M Ag + 1 M Ag (+) catd Sarann spntanee le reazini nel vers: Ag + + e Ag H H + + e (x ) semireazine di riduzine semireazine di ssidazine Ag + + H Ag + H + reazine spntanea
26 Data la seguente pila nrmale stabilire quale semielement funzina da catd e quale da and e calclare la f.e.m. a 5 C. (+) catd Cl, Pt (1 atm) Cl - 1 M Ag + 1 M Ag (-) and Cl / Cl V c Ag / Ag 0.80 V a Sarann spntanee le reazini nel vers: Ag Ag + + e Cl + e Cl - x semireazine di ssidazine semireazine di riduzine Ag + Cl Cl - + Ag + f.e.m. c a V
27 Stabilire se immergend una lamina di Cu in una sluzine di H SO 4 è spntanea la seguente reazine: Cu + H + Cu + + H H / H 0.00 V Cu / Cu 0.34 V Si sserverà la reazine inversa: Cu + + H Cu + H +
28 Quali metalli sn ssidati in ambiente acid? Au + 3 H + Au 3+ X + 3/ H La reazine nn è spntanea, si sserverà quella inversa
29 Disegnare l schema di una pila per la seguente reazine: MnO Cl H + Mn Cl + 4 H O Semireazine di x. (and): Cl / Cl 1.36 V 10 Cl - 5 Cl + 10 e - Semireazine di rid. (catd): MnO / Mn MnO H e - Mn H O 4,H 1.51 V (-) and Cl, Pt (atm) MnO - 4, C Cl -, C 1 Mn +, C 3 H +, C 4 Pt (+) catd lettrd a gas lettrd a ssidriduzine
30 quazine di Nernst Cme si calcla il ptenziale di un semielement che nn si trvi in cndizini standard? Il ptenziale di cella dipende dalla cncentrazine e dalla temperatura ed è descritt dall equazine: a Ox + n e b Rid ( Cu + + e - Cu (s) ) Ox/Rid RT nf ln a a a Ox b Rid = ptenziale standard di riduzine del semielement a 5 C T = temperatura assluta (K) F = cstante di Faraday (96500 C/ml, carica di 1mle di elettrni) a = attività (sstituita cn cncentrazini pressine) R = cstante mlare dei gas = 8.31 J/mle K n = n elettrni scambiati a, b = cefficienti stechimetrici
31 x/rid RT nf ln (a (a x rid ) ) a b x/rid n lg (a (a x rid ) ) a b x/rid n lg (a (a x rid ) ) a b Bisgna cnsiderare tutte le specie cinvlte nella semireazine.
32 Scrivere l equazine di Nernst per i seguenti elettrdi Cu Cu +, C 1 Cu (aq) + + e - Cu (s) Cu Cu /Cu lg Cu acu a /Cu lg [Cu 1 Pt Fe 3+, C 1 Fe +, C Fe (aq) e - Fe (aq) Fe Fe /Fe lg 3 Fe /Fe 1 a a Fe [Fe lg [Fe 3
33 Calclare la f.e.m. della pila: (-) and Zn Zn +, 0.1 M Cu +, 0.01 M (I) (II) Cu (+) catd Zn / Zn 0.76 V Cu / Cu 0.34 V [Zn I lg 0.76 ( 1) 0.79 V Zn / Zn [Cu II lg 0.34 ( 3) Cu /Cu V I = a II = c f.e.m. = c a = (- 0.79) = V
34 Scrivere l equazine di Nernst per: (-) and Cl, Pt (x atm) Cl -, C 1 MnO 4-, C Mn +, C 3 H +, C 4 Pt (+) catd Semireazine di x. (and): Cl - Cl + e - a Cl P lg [Cl Cl /Cl Semireazine di rid. (catd): MnO H e - Mn + + H O c MnO [MnO4 [H lg 5 [Mn 4,H / Mn 8
35 Scrivere l equazine di Nernst per l elettrd a idrgen: semireazine di riduzine H, Pt (1 atm) H 3 O +, C 1 H 3 O + + e - H + + e H H + H O H / H lg [H p H Sl se P di H = 1atm si può semplificare in: H / H lg[h
36 Pile a cncentrazine (+) catd Cu Cu +, C 1 Cu +, C Cu (-) and semielement I semielement II I lgc Cu /Cu 1 II lgc Cu /Cu se: C 1 > C I > II I = catd, II = and funzina da catd l elettrd a [ maggire f.e.m c a lgc1 Cu /Cu Cu /Cu lgc f.e.m. c a lg C C 1
37 Cme si calclail ptenziale di un elettrd di specie? Ag AgCl (s) KCl 10 - M AgCl sale pc slubile Ks =1,5 x10-10 Ag / Ag 0.80 V Ag + + e - Ag (s) Ag / Ag lg[ag
38 In sluzine abbiam: AgCl (s) Ag + + Cl - s s s KCl K + + Cl Ks = [Ag + [Cl - + s Ks [ Ag [Cl Ks 0.01 Ag Ag / Ag / Ag lg lg[ag Ks [0.01 Ag / Ag 0.67 V Ks lg [Cl
39 Calclare il Ks di AgCl sapend che la f.e.m. della seguente pila è 0,344 V a 5 C. (-) and Ag KCl, 10 - M AgCl (s) AgNO M Ag (+) catd elettrd di specie elettrd di 1 specie - è una pila a cncentrazine; - trvare le [ delle specie attive in sluzine. Al catd: [Ag + =0.01
40 All and: AgCl (s) Ag + Cl - s s s KCl K + + Cl s Ks [ Ag [Cl Ks 0.01 f.e.m c a lg Ks V [Ag lg [Ag C A lg 0.01 Ks 0.01 da cui: Ks = 1,5x10-10
41 nergia libera e f.e.m. in una cella galvanica avviene una reazine redx spntanea (DG < 0) che prduce lavr elettric In una pila in cui avviene un prcess reversibile a temperatura e pressine cstante si ha: DG = - W elettric Il lavr elettric ttenut da una pila in md reversibile crrispnde al massim lavr utile ttenibile, a T cstante
42 Relazine tra DG e f.e.m. DU = Q W in una pila: W = Wel + PDV DU = Q Wel PDV ricrdand che: DH = DU + PDV Q = DU + PDV + Wel = DH + Wel ciè: DH Q Wel ma in una trasf. rev. Qrev = TDS Wel = TDS DH = DG Wel = Wutile = DG = nf = f.e.m. = DG nf
43 Cstante di equilibri di una redx La f.e.m. di una pila indica la d.d.p. tra i due semielementi a circuit apert. Una pila funzine (erga crrente) fin a quand la reazine redx nn ha raggiunt l equilibri (f.e.m. = 0) Al passaggi di crrente il ptenziale del catd diminuisce e quell dell and aumenta fin a che la pila nn si scarica. Durante il funzinament della pila la [ delle specie varia fin a quand: c = a f.e.m. = 0 lg K n ( cat 0,059 an ) Se Cat >> An la cstante di equilibri è grande e la reazine è mlt spstata vers i prdtti
44 Relazine tra K, DG e f.e.m. lg K n ( cat 0,059 an ) n F( cat,303rt an ) ln K n F RT DG RT ( C A ) DG -nf (in cndizini standard)
45 Spntaneità delle redx Una redx è favrita termdinamicamente, ciè spntanea, se: ssidante > riducente m A + n B m A n- + n B m+ A + n e - A n- A si riduce (ssidante) DG x = -nf x B m+ + m e - B B si ssida (riducente) DG rid = -mf rid DG = mdg x - ndg rid = m (nf x ) - n (-mf rid ) = -n mf x + n mf rid = - n m F ( x - rid ) x rid > 0 x > rid
46 Data la seguente pila stabilire se la reazine è spntanea e calclare la Keq della redx a 5 C. (-) and Cu Cu Cu M / Cu 0.34 V Ag M Ag / Ag Ag 0.80 V (+) catd and [RID [Cu [OX [Cu + catd [RID [Ag [OX [Ag + Ag + + e Ag x Cu Cu + + e Ag + + Cu Cu + + Ag
47 La cstante di equilibri della reazine è: Kc [Cu [Ag Quand siam all equilibri f.e.m = 0 e c = a lg[ag Ag / Ag Cu / Cu lg[cu lg[ag lg[cu [Cu lg [Ag = lg Kc Kc = 3.47x10 15 [Cu [Ag 3.47x10 15 Reazine è spntanea e spstata vers i prdtti
48 Calcliam la f.e.m. all inizi: f.e.m. = lg[Ag + ( lg[Cu + ) = V c = V a = V Per invertire la plarità della pila si deve agire sulle [ delle specie attive in md chec<a. In quest cas si deve:[ag + e[cu +
49 Calcl della Keq dai valri di a Ox 1 + b Rid a Rid 1 + b Ox a b Ox 1 + b e Rid 1 Rid Ox + a e Keq [Ox [Rid b b [Rid [Ox 1 1 a a N.B. n = a b = n di e in gic nella reazine bilanciata. Per la stessa reazine in una pila (letta vers destra significa 1 = catd, = and), all equilibri si ha: f.e.m. = 0 e 1 = lg ba [Ox [Rid 1 1 a a ab [Ox lg [Rid b a [Ox [Rid lg lg K b a eq a b [Rid [Ox1 a b b b
50 ab [Ox lg [Rid b b [Rid [Ox 1 1 a a n lg Keq lg Keq (1 ) n 0,059 N.B. In generale una reazine è di fatt cmpleta se: V Infatti, cn n = 1 (è il minim) si ha Keq =
51 sercizi pile
52 La f.e.m. della seguente pila nrmale è di 0,680 V a 5 C, il vlume dei due cmpartimenti è 00 ml. Si fa funzinare la pila fin a che nn ha ergat Q. Calclare la nuva f.e.m. ed il ph nel I semielement, assumend invariat il vlume delle due sluzini. (+) catd Pt ClO - 3 Fe 3+ Pt H 3 O + Fe + Cl - (-) and semielement I semielement II Durante il funzinament della pila la [ delle specie attive varia: catd [RID [OX and [RID [OX
53 Le reazini sarann: catd: ClO e - + 6H + Cl - + 3H O and: Fe + Fe e - le nuve [ delle specie attive: eq = Q/F = / = 0.15 quindi al catd si cnsuman: 0.15 eq di ClO 3- pari a n = eq/6 = 0.05 mli 0.15 eq di H + = eq/1 =0.15 mli e si frman 0.15 eq Cl - pari a eq/6 = 0.05 mli
54 mentre all and si cnsuman: 0.15 eq di Fe + pari a n = eq/1 = 0.15 mli e si frman 0.15 eq Fe 3+ pari a eq/1 = 0.15 mli Le [ delle specie attive dp il funzinament della pila sn: [ClO 3- = 1 n/v = /0.00 = n/l [H + = /0.00 = 0.5 n/l [Cl - = /0.00 = 1.15 n/l [Fe + = /0.00 = 0.5 n/l [Fe 3+ = /0.00 = 1.75 n/l
55 All inizi: f.e.m. = c a =D V Dp: f.e.m. f.e.m. D lg 6 [ClO [Cl [H V [Fe [Fe 3 ph = -lg [H+ = -lg 0,5 = 0.60
56 s. Calclare il ptenziale dell elettrd Pt / Cr O 7 (0.01 M) ; H + (0.001 M) ; Cr 3+ (0.05 M) a 5 C, nt che = 1.33 V. Cr O H e Cr H O [CrO [H lg n ( N.B. n H O ) [Cr lg (0.01) (0.001) (0.05) V
57 s. Data la seguente reazine a 5 C MnO Sn H + Mn Sn H O a partire da cnc. 1 M di tutte le specie iniche, stabilire il vers della reazine, nt che e che Sn 4 / Sn 0.15 V MnO 4,H / Mn 1.51 Piché tutte le cncentrazini sn 1 M è sufficiente cnfrntare i ptenziali standard ( ). Da questi risulta che MnO 4 ha una maggire tendenza a ridursi rispett a Sn 4+. Quindi la reazine va a destra. Se si realizzasse la pila standard: (+) (-) Pt / MnO 4 ; Mn + ; H + // Sn + ; Sn 4+ / Pt catd and V
58 s. Calclare a 5 C la f.e.m. ed il vers della reazine spntanea nella pila frmata dagli elettrdi: Pt/Cr 3+; Cr + ( = 0.41 V) Cr 3+ + e Cr + Pt/Ti 3+ ;Ti + ( = 0.37 V) Ti 3+ + e Ti + a) quand tutti gli ini hann cncentrazine 1 M; b) quand Cr 3+ = 0.15 M, Cr + = M, Ti 3+ = M, Ti + = M. a) = per entrambi gli elettrdi. f.e.m. = c a = 0.37 ( 0.41) = V Ti 3+ + Cr + Ti + + Cr 3+
59 0.059 [Cr b) lg Cr /Cr 1 [Cr Ti 3+ = + 3 = /Ti [Ti lg [Ti 3 3 = c a = 0.38 ( 0.48) = 0.10 V Cr 3+ + Ti + Cr + + Ti V -0.48
60 s. A 5 C il ptenziale della semicella Pt / (H + N = 0.5 atm) / HNO (0.05 M) ; NaNO (0.1 M) vale 0.18 V. Nt che K a = calclare la frazine mlare di H nella miscela gasssa. H + + e [H H (g) lg 0.18 V P Per la sluzine tampne: H [H K a C C a s mli/l PH atm Legge di Daltn: P i = P tt X i XH
61 s. Un acid deble HA cntiene sl C (54.54 %), H (9.09 %) e O. La seguente pila: (1) Pt/H (1 atm)/naa (0.1 M)//NaCl/H (1 atm)/pt () ha f.e.m. = V a 5 C. Scigliend g di HA in 450 ml di acqua si ttiene ph =.70. Calclare la frmula mleclare di HA. 1) Frmula minima: per 100 g di HA abbiam n C n H n O 16.0 C H9.09 O = C H 4 O P.M. min = 44.0 u.m.a.
62 ) Per ph =.70 si ha [H + = mli/l Sluzine acid deble : [H K a C a K a g P.M. V quindi, se calcliam K a pssiam ricavare il P.M. [H lg [H ) Dalla pila : f.e.m. -1 dacui: [H [H piché [H + = 10 7 M [H + 1 = M tteniam:
63 4) [H + 1 è determinata dall idrlisi basica del sale NaA: - [OH quindi: 1 Kw K a C s s 1 Kw [H Kw C Ka [OH ( ) ) Sluzine acid deble : [H Ka Ca Ka P.M. K [H a 1 g V 88.0 u.m.a mli/l g P.M. V frmula minima = C H 4 O (44.0 u.m.a.) frmula mleclare = C 4 H 8 O
Premesse. le reazioni di ossido-riduzione implicano il trasferimento di elettroni dalla specie ossidante alla specie riducente
 Premesse le reazini di ssid-riduzine implican il trasferiment di elettrni dalla specie ssidante alla specie riducente un fluss di elettrni genera una crrente elettrica l'elettrchimica studia l'intercnversine
Premesse le reazini di ssid-riduzine implican il trasferiment di elettrni dalla specie ssidante alla specie riducente un fluss di elettrni genera una crrente elettrica l'elettrchimica studia l'intercnversine
Equilibri chimici omogenei ed eterogenei
 Equilibri chimici mgenei ed etergenei Fase: przine di un sistema che presenta stat fisic e cmpsizine chimica unifrmi Fase: una przine mgenea di un sistema, delimitata da una superficie di separazine fisicamente
Equilibri chimici mgenei ed etergenei Fase: przine di un sistema che presenta stat fisic e cmpsizine chimica unifrmi Fase: una przine mgenea di un sistema, delimitata da una superficie di separazine fisicamente
Gli atomi di zinco passano in soluzione come ioni Zn 2+ idrati: Zn Zn 2 +aq +2e- ; gli elettroni restano nel metallo e si crea un doppio strato
 Gli tmi di zinc pssn in sluzine cme ini idrti: q e- ; gli elettrni restn nel metll e si cre un dppi strt elettric fr l elettrd (cric negtivmente per l eccess di elettrni) e l sluzine (cric psitivmente
Gli tmi di zinc pssn in sluzine cme ini idrti: q e- ; gli elettrni restn nel metll e si cre un dppi strt elettric fr l elettrd (cric negtivmente per l eccess di elettrni) e l sluzine (cric psitivmente
Gli atomi di zinco passano in soluzione come ioni Zn 2+ idrati: Zn Zn 2 +aq +2e- ; gli elettroni restano nel metallo e si crea un doppio strato
 Gli tmi di zinc pssn in sluzine cme ini Zn idrti: Zn Zn q e- ; gli elettrni restn nel metll e si cre un dppi strt elettric fr l elettrd (cric negtivmente per l eccess di elettrni) e l sluzine (cric psitivmente
Gli tmi di zinc pssn in sluzine cme ini Zn idrti: Zn Zn q e- ; gli elettrni restn nel metll e si cre un dppi strt elettric fr l elettrd (cric negtivmente per l eccess di elettrni) e l sluzine (cric psitivmente
Elettrochimica. Studia la trasformazione dell energia chimica in energia elettrica e viceversa.
 lettrochimica Studia la trasformazione dell energia chimica in energia elettrica e viceversa. Ricordiamo che la corrente elettrica si origina grazie al movimento di cariche, elettroni, in un materiale
lettrochimica Studia la trasformazione dell energia chimica in energia elettrica e viceversa. Ricordiamo che la corrente elettrica si origina grazie al movimento di cariche, elettroni, in un materiale
Viscosità Energia superficiale. Liquidi puri (proprietà) Pressione di vapore. Temperatura di fusione. Temperatura di ebollizione.
 Liquidi puri (prprietà) Viscsità Energia superficiale ressine di vapre Temperatura di fusine Liquidi Temperatura di ebllizine sluzini (prprietà) Liquid + Liquid Liquid + Gas Liquid + Slid Meccanism di
Liquidi puri (prprietà) Viscsità Energia superficiale ressine di vapre Temperatura di fusine Liquidi Temperatura di ebllizine sluzini (prprietà) Liquid + Liquid Liquid + Gas Liquid + Slid Meccanism di
Reazioni di ossido-riduzione (redox) - Come stabilire il verso di una redox? -
 Reazioni di ossido-riduzione (redox) Reazioni in cui i reagenti si scambiano elettroni per formare i prodotti. Cu 2+ (aq) + Zn(s) Cu(s) + Zn 2+ (aq) Zn(s) Zn 2+ (aq) + 2 e - Cu 2+ (aq) + 2 e - Cu(s) ossidazione
Reazioni di ossido-riduzione (redox) Reazioni in cui i reagenti si scambiano elettroni per formare i prodotti. Cu 2+ (aq) + Zn(s) Cu(s) + Zn 2+ (aq) Zn(s) Zn 2+ (aq) + 2 e - Cu 2+ (aq) + 2 e - Cu(s) ossidazione
Laboratorio di Chimica Fisica
 Università degli studi di Padva Dipartiment di Scienze Chimiche Crs di Laurea Triennale in Chimica Industriale Labratri di Chimica Fisica (Ann Accademic 18-19) Pagina 1 di 7 1. Sistemi Elettrchimici I
Università degli studi di Padva Dipartiment di Scienze Chimiche Crs di Laurea Triennale in Chimica Industriale Labratri di Chimica Fisica (Ann Accademic 18-19) Pagina 1 di 7 1. Sistemi Elettrchimici I
SOLUBILITA EQUILIBRI ETEROGENEI
 SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
Termochimica. Sperimentalmente si verifica che il calore svolto o assorbito in una reazione dipende da:
 Termchimica La termchimica si ccupa del calre assciat alle reazini chimiche. Sperimentalmente si verifica che il calre svlt assrbit in una reazine dipende da: 1) Stat iniziale e finale del sistema quindi
Termchimica La termchimica si ccupa del calre assciat alle reazini chimiche. Sperimentalmente si verifica che il calre svlt assrbit in una reazine dipende da: 1) Stat iniziale e finale del sistema quindi
Laboratorio di Chimica Fisica
 Università degli studi di Padva Dipartiment di Scienze Chimiche Crs di Laurea Triennale in Chimica Industriale Labratri di Chimica Fisica (Ann Accademic 2016-2017) Pagina 1 di 27 1. Sistemi Elettrchimici
Università degli studi di Padva Dipartiment di Scienze Chimiche Crs di Laurea Triennale in Chimica Industriale Labratri di Chimica Fisica (Ann Accademic 2016-2017) Pagina 1 di 27 1. Sistemi Elettrchimici
1 Me Me (s) Me + (aq) + e -
 ELETTROCHIMICA 1 Me Me (s) Me + (aq) + e - Me + DOPPIO STRATO (+) (-) all interfaccia elettrodo-soluzione 2 Se inizialmente prevale la reazione 1, la lamina metallica si carica negativamente (eccesso di
ELETTROCHIMICA 1 Me Me (s) Me + (aq) + e - Me + DOPPIO STRATO (+) (-) all interfaccia elettrodo-soluzione 2 Se inizialmente prevale la reazione 1, la lamina metallica si carica negativamente (eccesso di
NUMERI DI OSSIDAZIONE
 NUMERI DI SSIDAZINE Il numero di ossidazione degli elementi allo stato libero è ZER La somma algebrica dei numeri di ossidazione di tutti gli atomi di una molecola neutra è ZER La somma algebrica dei numeri
NUMERI DI SSIDAZINE Il numero di ossidazione degli elementi allo stato libero è ZER La somma algebrica dei numeri di ossidazione di tutti gli atomi di una molecola neutra è ZER La somma algebrica dei numeri
2- (aq) + Zn (s) Zn 2+ (aq) + SO 4. Semi-reazione di ossidazione: in cui una specie chimica perde elettroni
 Reazioni con trasferimento di elettroni Modifica della struttura elettronica attraverso uno scambio di elettroni: Una ossidazione può avvenire soltanto se avviene contemporaneamente una riduzione (reazioni
Reazioni con trasferimento di elettroni Modifica della struttura elettronica attraverso uno scambio di elettroni: Una ossidazione può avvenire soltanto se avviene contemporaneamente una riduzione (reazioni
Studio delle trasformazioni dell energia chimica e dell energia elettrica
 ELETTROCHIMICA Studio delle trasformazioni dell energia chimica e dell energia elettrica Conduttori elettrolitici: soluzioni di acidi, di basi e di sali, nonché sali fusi. Ioni che partecipano alle reazioni
ELETTROCHIMICA Studio delle trasformazioni dell energia chimica e dell energia elettrica Conduttori elettrolitici: soluzioni di acidi, di basi e di sali, nonché sali fusi. Ioni che partecipano alle reazioni
L entropia e il II principio della termodinamica
 L entrpia e il II principi della termdinamica Una reazine chimica che prcede senza alcun intervent estern (sistema islat) viene definita spntanea e irreversibile. Analizziam la reazine, a 5 C e 1 atm tra
L entrpia e il II principi della termdinamica Una reazine chimica che prcede senza alcun intervent estern (sistema islat) viene definita spntanea e irreversibile. Analizziam la reazine, a 5 C e 1 atm tra
Reazioni di ossido-riduzione (redox) - Come stabilire il verso di una redox? -
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
-CALORIMETRIA -TERMOCHIMICA
 -CALORIMETRIA -TERMOCHIMICA Prim Principi della Termdinamica: E interna = q + w in un sistema islat E interna = 0 Scaldand un crp aumentiam la sua energia interna, ma anche cmpiend lavr sul sistema aumentiam
-CALORIMETRIA -TERMOCHIMICA Prim Principi della Termdinamica: E interna = q + w in un sistema islat E interna = 0 Scaldand un crp aumentiam la sua energia interna, ma anche cmpiend lavr sul sistema aumentiam
red 1 + ox 2 ox 1 + red 2
 Reazioni Redox Ossidanti e Riducenti Ossidante: molecola o ione capace di strappare elettroni ad un riducente Riducente: molecola o ione capace di fornire elettroni ad un ossidante Reazione redox: trasferimento
Reazioni Redox Ossidanti e Riducenti Ossidante: molecola o ione capace di strappare elettroni ad un riducente Riducente: molecola o ione capace di fornire elettroni ad un ossidante Reazione redox: trasferimento
Energia libera di Gibbs
 Entrpia = k ln w k è la cstante di Bltzmann 1.38 1-23 J -1 W è il numer di micrstati dierenti che cntribuiscn ad un stess macrstat Un prcess è spntane e irreversibile nella direzine in cui L'entrpia ttale
Entrpia = k ln w k è la cstante di Bltzmann 1.38 1-23 J -1 W è il numer di micrstati dierenti che cntribuiscn ad un stess macrstat Un prcess è spntane e irreversibile nella direzine in cui L'entrpia ttale
Esempio Zn (s) + CuSO 4(aq) î Cu (s) + ZnSO 4(aq)
 Pile Una reazione spontanea di ossidoriduzione (ΔE>0, ΔG
Pile Una reazione spontanea di ossidoriduzione (ΔE>0, ΔG
Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C. dove : R = costante dei gas T = 298,15 K F = Faraday
 A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 8: Elettrochimica: legge di Nernst e leggi di Faraday(4 h) Cella galvanica:
A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 8: Elettrochimica: legge di Nernst e leggi di Faraday(4 h) Cella galvanica:
Elettrochimica. Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s)
 217 1 Elettrochimica Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
217 1 Elettrochimica Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
Elettrochimica. Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s)
 2018 Elettrochimica 1 Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
2018 Elettrochimica 1 Cu 2+ (aq) + Zn(s) à Zn 2+ (aq) + Cu(s) 2 Le reazioni redox implicano specie che si ossidano e specie che si riducono. I due processi avvengono contemporaneamente. Terminologia OSSIDAZIONE
Elettrochimica. le trasformazioni redox spontanee (DG < 0) l energia elettrica in celle elettrolitiche per ottenere
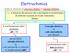 Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica. le trasformazioni redox spontanee (DG < 0) l energia elettrica in celle elettrolitiche per ottenere
 Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
Elettrochimica studia le relazioni tra processi chimici ed energia elettrica. i. e. si interessa dei processi che coinvolgono il trasferimento di elettroni (reazioni di ossido riduzione). Sfrutta: le trasformazioni
A + B C + D A + B (A B) C + D (A B) Cinetica Chimica
 Cinetia Chimia termdinamia : desrizine dei fenmeni energetii nsiderand sl stat iniziale e stat finale inetia himia : studi della velità e dei meanismi di reazine A + B C + D A e B devn urtarsi urt effiae
Cinetia Chimia termdinamia : desrizine dei fenmeni energetii nsiderand sl stat iniziale e stat finale inetia himia : studi della velità e dei meanismi di reazine A + B C + D A e B devn urtarsi urt effiae
Pile 1) Indicare gli schemi dei semielementi formati dalle seguenti semicoppie redox e scrivere la corrispondente equazione di Nernst:
 ile 1) Indicare gli schemi dei semielementi formati dalle seguenti semicoppie redox e scrivere la corrispondente equazione di Nernst: a) HO + + e - H (g) + HO b) Al + + e - Al(s) c) O(g) + 4 HO + + 4e
ile 1) Indicare gli schemi dei semielementi formati dalle seguenti semicoppie redox e scrivere la corrispondente equazione di Nernst: a) HO + + e - H (g) + HO b) Al + + e - Al(s) c) O(g) + 4 HO + + 4e
ELETTROCHIMICA: studia le relazioni tra energia chimica ed energia elettrica
 ELETTROCHIMICA: studia le relazioni tra energia chimica ed energia elettrica Pila Energia chimica? energia elettrica Si basa su reazioni redox con G < 0 Cella di elettrolisi Energia elettrica? energia
ELETTROCHIMICA: studia le relazioni tra energia chimica ed energia elettrica Pila Energia chimica? energia elettrica Si basa su reazioni redox con G < 0 Cella di elettrolisi Energia elettrica? energia
Capitolo 22 L elettrochimica
 Capitolo 22 L elettrochimica Hai capito? pag. 572 Le osservazioni sarebbero le stesse. 2 + Cu 2 Cu 2+ ; la soluzione assume un colore azzurro per la presenza di ioni Cu 2+ e si forma un deposito grigio
Capitolo 22 L elettrochimica Hai capito? pag. 572 Le osservazioni sarebbero le stesse. 2 + Cu 2 Cu 2+ ; la soluzione assume un colore azzurro per la presenza di ioni Cu 2+ e si forma un deposito grigio
Cellule galvaniche ed elettrolitiche
 Cellule galvaniche ed elettrolitiche Cella voltaica = galvanica fornisce E. elettrica (+) Cella elettrolitica richiede dall esterno corrente elettrica (-) La cella composta dai due semielementi Zn/Cu nei
Cellule galvaniche ed elettrolitiche Cella voltaica = galvanica fornisce E. elettrica (+) Cella elettrolitica richiede dall esterno corrente elettrica (-) La cella composta dai due semielementi Zn/Cu nei
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente.
 Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
ELETTROCHIMICA. Consideriamo la reazione che si ha quando si aggiunge dello zinco ad una soluzione acquosa di acido cloridrico:
 ELETTROCHIMICA Alcune fra le più importanti reazioni chimiche di ossidoriduzione prevedono una modifica dei numeri di ossidazione dei vari elementi che compongono reagenti e prodotti. Consideriamo la reazione
ELETTROCHIMICA Alcune fra le più importanti reazioni chimiche di ossidoriduzione prevedono una modifica dei numeri di ossidazione dei vari elementi che compongono reagenti e prodotti. Consideriamo la reazione
Soluzioni. B è spontanea nel senso opposto alla freccia. 12 Soluzione di HF in un contenitore di rame: C La soluzione rimane inalterata.
 Soluzioni capitolo 23 VERIFICA LE TUE CONOSCENZE LA PILA O CELLA GALVANICA 1 Una cella galvanica trasforma energia chimica in energia elettrica, utilizzando una redox spontanea. Una cella galvanica è formata
Soluzioni capitolo 23 VERIFICA LE TUE CONOSCENZE LA PILA O CELLA GALVANICA 1 Una cella galvanica trasforma energia chimica in energia elettrica, utilizzando una redox spontanea. Una cella galvanica è formata
L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche.
 Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente.
 Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
ESERCIZI Tabella dei potenziali
 ESERCIZI 1) Una pila chimica è un dispositivo in cui si ha trasformazione di: a. energia elettrica in energia chimica b. energia chimica in energia elettrica c. entalpia in energia elettrica d. entropia
ESERCIZI 1) Una pila chimica è un dispositivo in cui si ha trasformazione di: a. energia elettrica in energia chimica b. energia chimica in energia elettrica c. entalpia in energia elettrica d. entropia
Trasformazione di energia chimica in energia elettrica: generatori (pile, accumulatori, celle a combustibile)
 Elettrochimica Trasformazione di energia chimica in energia elettrica: generatori (pile, accumulatori, celle a combustibile) Trasformazione di energia elettrica in energia chimica: celle di elettrolisi
Elettrochimica Trasformazione di energia chimica in energia elettrica: generatori (pile, accumulatori, celle a combustibile) Trasformazione di energia elettrica in energia chimica: celle di elettrolisi
Reazioni di Ossido-Riduzione ed Elettrochimica
 Reazioni di Ossido-Riduzione ed Elettrochimica Reazione di trasferimento elettronico: + + Riducente: donatore di elettroni. Ossidante: accettore di elettroni. Uno o più elettronivengono trasferiti dalla
Reazioni di Ossido-Riduzione ed Elettrochimica Reazione di trasferimento elettronico: + + Riducente: donatore di elettroni. Ossidante: accettore di elettroni. Uno o più elettronivengono trasferiti dalla
ELETTROCHIMICA. Processi spontanei (ΔG < 0) possono essere utilizzati per produrre lavoro utile.
 ELETTROCHIMICA Processi spontanei (ΔG < 0) possono essere utilizzati per produrre lavoro utile. Processi spontanei: 1. Diluizione 2. Espansione di un gas 3. Precipitazione di specie poco solubili 4. Reazioni
ELETTROCHIMICA Processi spontanei (ΔG < 0) possono essere utilizzati per produrre lavoro utile. Processi spontanei: 1. Diluizione 2. Espansione di un gas 3. Precipitazione di specie poco solubili 4. Reazioni
ELETTROCHIMICA. Elettricità per fare avvenire reazioni chimiche (processi elettrolitici)
 ELETTROCHIMICA Reazioni chimiche per produrre elettricità Elettricità per fare avvenire reazioni chimiche (processi elettrolitici) Esperimento: Nel tempo la sbarretta di Zn si consuma e si deposita Cu
ELETTROCHIMICA Reazioni chimiche per produrre elettricità Elettricità per fare avvenire reazioni chimiche (processi elettrolitici) Esperimento: Nel tempo la sbarretta di Zn si consuma e si deposita Cu
Ognuno ha familiarità con il termine ossidazione relativo ad un metallo; ad esempio, la reazione Zn + ½ O 2 ZnO
 Cap.12 Reazioni di ossido-riduzione Secondo Bronsted-Lowry le reazioni acido/base comportano un trasferimento di protoni H +. Le reazioni di ossido-riduzione (redox) sono un altra importante classe di
Cap.12 Reazioni di ossido-riduzione Secondo Bronsted-Lowry le reazioni acido/base comportano un trasferimento di protoni H +. Le reazioni di ossido-riduzione (redox) sono un altra importante classe di
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 29-30 2010 Programma: a che punto siamo? Elettrochimica Elettrochimica è lo studio delle reazioni chimiche che producono
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 29-30 2010 Programma: a che punto siamo? Elettrochimica Elettrochimica è lo studio delle reazioni chimiche che producono
Lavoro ed energia di Gibbs. L Energia di Gibbs rappresenta il massimo lavoro non di espansione ottenbile da un processo (importante per le batterie):
 Lavoro ed energia di Gibbs L Energia di Gibbs rappresenta il massimo lavoro non di espansione ottenbile da un processo (importante per le batterie): Fornisce la direzione del processo DG Fornisce il massimo
Lavoro ed energia di Gibbs L Energia di Gibbs rappresenta il massimo lavoro non di espansione ottenbile da un processo (importante per le batterie): Fornisce la direzione del processo DG Fornisce il massimo
Termochimica. Sperimentalmente si verifica che il calore svolto o assorbito in una reazione dipende da:
 Termchimica La termchimica si ccupa del calre assciat alle reazini chimiche. Sperimentalmente si verifica che il calre svlt assrbit in una reazine dipende da: 1) Stat iniziale e finale del sistema quindi
Termchimica La termchimica si ccupa del calre assciat alle reazini chimiche. Sperimentalmente si verifica che il calre svlt assrbit in una reazine dipende da: 1) Stat iniziale e finale del sistema quindi
Definizioni. X aumenta il numero di ossidazione. Y diminuisce il numero di ossidazione. e - Trasferimento di elettroni
 Lezione 18 1. Elettrochimica e reazioni elettrochimiche: definizione e classificazione. 2. Sistemi elettrochimici. 3. La pila 4. Elettrodi: catodo e anodo. 5. Polarità dei sistemi e continuità del circuito
Lezione 18 1. Elettrochimica e reazioni elettrochimiche: definizione e classificazione. 2. Sistemi elettrochimici. 3. La pila 4. Elettrodi: catodo e anodo. 5. Polarità dei sistemi e continuità del circuito
Il riducente si ossida cedendo elettroni all agente ossidante
 L ossidante si riduce acquistando elettroni dall agente riducente Il riducente si ossida cedendo elettroni all agente ossidante La conduzione dell elettricità Quando una sostanza è sottoposta ad una differenza
L ossidante si riduce acquistando elettroni dall agente riducente Il riducente si ossida cedendo elettroni all agente ossidante La conduzione dell elettricità Quando una sostanza è sottoposta ad una differenza
Processi ossido-riduttivi chimici ed elettrochimici
 Processi ossido-riduttivi chimici ed elettrochimici Le reazioni ossidoriduttive comportano la variazione dello stato di ossidazione di almeno un elemento in seguito alla conversione dei reagenti nei prodotti
Processi ossido-riduttivi chimici ed elettrochimici Le reazioni ossidoriduttive comportano la variazione dello stato di ossidazione di almeno un elemento in seguito alla conversione dei reagenti nei prodotti
Appunti di Stechiometria per Chimica. Elettrochimica
 Appunti di Stechiometria per Chimica Elettrochimica Celle Elettrochimiche Le reazioni d ossidoriduzione possono essere sfruttate per formare delle celle galvaniche o pile che trasformano l energia chimica
Appunti di Stechiometria per Chimica Elettrochimica Celle Elettrochimiche Le reazioni d ossidoriduzione possono essere sfruttate per formare delle celle galvaniche o pile che trasformano l energia chimica
Stato solido forma propria incompressibile. reticolo cristallino nodi reticolari vibrazioni intorno ai nodi reticolari solidi covalenti.
 Stat slid frma prpria inmpressibile slidi ristallini slidi amrfi retil ristallin ndi retilari vibrazini intrn ai ndi retilari slidi valenti legami valenti alte T di fusine prprietà islanti (termihe ed
Stat slid frma prpria inmpressibile slidi ristallini slidi amrfi retil ristallin ndi retilari vibrazini intrn ai ndi retilari slidi valenti legami valenti alte T di fusine prprietà islanti (termihe ed
Elettrochimica. Studia la relazione fra variazione di energia libera e flussi di cariche in una reazione chimica.
 Elettrochimica Studia la relazione fra variazione di energia libera e flussi di cariche in una reazione chimica. Fornisce il modo per ricavare lavoro elettrico da una reazione spontanea = cella galvanica
Elettrochimica Studia la relazione fra variazione di energia libera e flussi di cariche in una reazione chimica. Fornisce il modo per ricavare lavoro elettrico da una reazione spontanea = cella galvanica
ESERCIZI POTENZIOMETRIA
 ESERCIZI POTENZIOMETRIA A. SPUNTI DI RIFLESSIONE 1. Quali sono i probabili fenomeni che permettono a un elettrodo al platino di assumere il potenziale di una soluzione contenente la coppia Fe 3+ /Fe 2+?
ESERCIZI POTENZIOMETRIA A. SPUNTI DI RIFLESSIONE 1. Quali sono i probabili fenomeni che permettono a un elettrodo al platino di assumere il potenziale di una soluzione contenente la coppia Fe 3+ /Fe 2+?
1. In n di ossidazione di un elemento libero è 0 2. La somma algebrica in qualsiasi composto è 0. In uno ione
 UMER DI SSIDAZIE Significato formale, viene stabilito in funzione della carica che un atomo ha apparentemente in un composto, ammettendo tutti i legami di natura ionica 1. In n di ossidazione di un elemento
UMER DI SSIDAZIE Significato formale, viene stabilito in funzione della carica che un atomo ha apparentemente in un composto, ammettendo tutti i legami di natura ionica 1. In n di ossidazione di un elemento
ESERCIZI SULLA f.e.m. DELLE PILE Kps, Keq E?G
 http://www. ESERCIZI SULLA f.e.m. DELLE PILE Kps, Keq E?G ESERCIZI SULLA f.e.m. DELLE PILE 1-Calcolare la fem della pila Zn/zn+2 0,01 Pb+2 0,06 M/Pb E zn= -0,76 V E Pb = -0,13 V pertanto Ezn = -0,76 +
http://www. ESERCIZI SULLA f.e.m. DELLE PILE Kps, Keq E?G ESERCIZI SULLA f.e.m. DELLE PILE 1-Calcolare la fem della pila Zn/zn+2 0,01 Pb+2 0,06 M/Pb E zn= -0,76 V E Pb = -0,13 V pertanto Ezn = -0,76 +
Le Reazioni redox. combustioni. corrosioni. fotosintesi. lo scambio di elettroni. metabolismo alimentare. preparazione dei metalli ...
 Le Reazioni redox Le Reazioni redox combustioni corrosioni fotosintesi metabolismo alimentare cosa hanno in comune? lo scambio di elettroni preparazione dei metalli... Ossidazione originariamente: reazione
Le Reazioni redox Le Reazioni redox combustioni corrosioni fotosintesi metabolismo alimentare cosa hanno in comune? lo scambio di elettroni preparazione dei metalli... Ossidazione originariamente: reazione
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI. Dr. Francesco Musiani
 REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
ELETTROCHIMICA. Zn(s) + Cu +2 Zn +2 + Cu. Ossidazione: perdita di elettroni Riduzione: acquisto di elettroni. +2e
 ELETTROCHIMICA Branca della chimica che studia le trasformazioni chimiche in cui sono coinvolti flussi di elettroni. Reazioni con trasferimento di elettroni (ossido riduzione) 2e Zn(s) + Cu +2 Zn +2 +
ELETTROCHIMICA Branca della chimica che studia le trasformazioni chimiche in cui sono coinvolti flussi di elettroni. Reazioni con trasferimento di elettroni (ossido riduzione) 2e Zn(s) + Cu +2 Zn +2 +
COME CALCOLARE I NUMERI DI OSSIDAZIONE
 COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
RADZ, / II PROVA IN ITINERE :00 - A
 POLITECNICO DI MILANO ING. ENG-AEE-MEC Corso di FONDAMENTI DI CHIMICA - sez. MOM RADZ, docente Cristian Gambarotti a.a. 2013/2014 - II PROVA IN ITINERE 14-02-2014 ore 13:00 - A 1 Quanta acqua (litri) è
POLITECNICO DI MILANO ING. ENG-AEE-MEC Corso di FONDAMENTI DI CHIMICA - sez. MOM RADZ, docente Cristian Gambarotti a.a. 2013/2014 - II PROVA IN ITINERE 14-02-2014 ore 13:00 - A 1 Quanta acqua (litri) è
ELETTROCHIMICA. Uso di reazioni chimiche per produrre corrente elettrica (Pile)
 ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
Corso di Economia Politica Esercitazione 1 21 febbraio 2014
 Crs i Ecnmia litica Esercitazine febbrai 04 Maalena Ragna (tutr) maalena.ragna@unib.it http://www.unib.it/sitweb/efault.aspx?un=maalena.ragna%40unib.it&view=link Esercizi Argmenti: mana, fferta, equilibri
Crs i Ecnmia litica Esercitazine febbrai 04 Maalena Ragna (tutr) maalena.ragna@unib.it http://www.unib.it/sitweb/efault.aspx?un=maalena.ragna%40unib.it&view=link Esercizi Argmenti: mana, fferta, equilibri
Agente ossidante è la specie chimica che acquistando elettroni passa ad uno stato di ossidazione inferiore: Es. Ce +4 + e - Ce +3
 OSSIDIMETRIA Titolazioni di ossidoriduzione. Principi: Ossidazione = perdita di elettroni Riduzione = acquisto di elettroni Reazione redox in generale Oss 1 + Rid 2 Rid 1 + Oss 2 Agente ossidante è la
OSSIDIMETRIA Titolazioni di ossidoriduzione. Principi: Ossidazione = perdita di elettroni Riduzione = acquisto di elettroni Reazione redox in generale Oss 1 + Rid 2 Rid 1 + Oss 2 Agente ossidante è la
Le Pile. Zn 2+ Ag + a=1 a=1
 Le Pile In questo capitolo sono illustrati alcuni problemi riguardanti pile con diversi tipi di elettrodi e nelle quali si realizzano processi di vario genere. Le pile sono utilizzate per ottenere informazioni
Le Pile In questo capitolo sono illustrati alcuni problemi riguardanti pile con diversi tipi di elettrodi e nelle quali si realizzano processi di vario genere. Le pile sono utilizzate per ottenere informazioni
Fase. P = 1 liquidi completamente miscibili 1 < P n liquidi parzialmente miscibili. P = n 1 < P n solidi parzialmente miscibili (soluzioni solide)
 1 Equilibri di fase 1. Definizine del cncett di Fase 2. Definizine del cncett di Numer di Cmpnenti Indipendenti 3. Definizine del cncett di Gradi di Libertà (Varianza) 4. Cndizini generali dell equilibri
1 Equilibri di fase 1. Definizine del cncett di Fase 2. Definizine del cncett di Numer di Cmpnenti Indipendenti 3. Definizine del cncett di Gradi di Libertà (Varianza) 4. Cndizini generali dell equilibri
Soluzioni di gas in acqua
 Sluzini di gas in acqua Cefficieni di assrbimen di gas in acqua. Le misure sn sae effeuae alla pressine di 1 am; i valri C a (T C) sn espresse in cc di gas discili in 1 cc di H 2 O alle emperaure indicae,
Sluzini di gas in acqua Cefficieni di assrbimen di gas in acqua. Le misure sn sae effeuae alla pressine di 1 am; i valri C a (T C) sn espresse in cc di gas discili in 1 cc di H 2 O alle emperaure indicae,
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23
 Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23 Esercizio PAG 541 ES 1 PAG 541 ES 2 PAG 541 ES 3 PAG 541 ES 4 PAG 541 ES 5 PAG 541 ES 6 PAG 541 ES 7 Al(s) Al 3+
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23 Esercizio PAG 541 ES 1 PAG 541 ES 2 PAG 541 ES 3 PAG 541 ES 4 PAG 541 ES 5 PAG 541 ES 6 PAG 541 ES 7 Al(s) Al 3+
elettroni in transito
 L ELETTROCHIMICA: elettroni in transito Studia l interconversione tra l energia elettrica (E el = q ΔE) e l energia chimica (E chim = ΔG reaz ). Qualsiasi reazione di ossido-riduzione spontanea (ΔG reaz
L ELETTROCHIMICA: elettroni in transito Studia l interconversione tra l energia elettrica (E el = q ΔE) e l energia chimica (E chim = ΔG reaz ). Qualsiasi reazione di ossido-riduzione spontanea (ΔG reaz
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 31-32 2009 Schema di una cella galvanica Zn (s) Zn 2+ (1 M) Cu 2+ (1 M) Cu (s) anodo Zn (s) Zn 2+ (aq) Cu 2+ (aq) Cu
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 31-32 2009 Schema di una cella galvanica Zn (s) Zn 2+ (1 M) Cu 2+ (1 M) Cu (s) anodo Zn (s) Zn 2+ (aq) Cu 2+ (aq) Cu
Schema di una cella galvanica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Schema di una cella galvanica Zn (s) Zn 2+ (1 M) Cu 2+ (1 M) Cu (s) anodo Zn (s) Zn 2+ (aq) Cu 2+ (aq) Cu (s) catodo Semicella
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Schema di una cella galvanica Zn (s) Zn 2+ (1 M) Cu 2+ (1 M) Cu (s) anodo Zn (s) Zn 2+ (aq) Cu 2+ (aq) Cu (s) catodo Semicella
COMBUSTIONE REAZIONE CHIMICA DI UNA SOSTANZA COMBUSTIBILE CON UNA SOSTANZA COMBURENTE CON SVILUPPO DI: CALORE FIAMMA FUMO GAS DI COMBUSTIONE
 COMBUSTIONE REAZIONE CHIMICA DI UNA SOSTANZA COMBUSTIBILE CON UNA SOSTANZA COMBURENTE CON SVILUPPO DI: CALORE FIAMMA FUMO GAS DI COMBUSTIONE CONDIZIONI NECESSARIE AFFINCHE SI VERIFICHI LA COMBUSTIONE SONO:
COMBUSTIONE REAZIONE CHIMICA DI UNA SOSTANZA COMBUSTIBILE CON UNA SOSTANZA COMBURENTE CON SVILUPPO DI: CALORE FIAMMA FUMO GAS DI COMBUSTIONE CONDIZIONI NECESSARIE AFFINCHE SI VERIFICHI LA COMBUSTIONE SONO:
Corsi di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica. FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti. Esercitazione del 11/01/2011
 Corsi di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti Esercitazione del 11/1/11 Si consideri la seguente semireazione di riduzione: O g ) 4H(
Corsi di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti Esercitazione del 11/1/11 Si consideri la seguente semireazione di riduzione: O g ) 4H(
Corso di Economia Politica Esercitazione 1 8 marzo 2013
 Crs i Ecnmia litica Esercitazine 1 8 marz 013 Maalena Ragna (tutr) maalena.ragna@unib.it http://cms.stat.unib.it/ragna/teaching.aspx Esercizi Argmenti: mana, fferta, equilibri i mercat, renita el cnsumatre
Crs i Ecnmia litica Esercitazine 1 8 marz 013 Maalena Ragna (tutr) maalena.ragna@unib.it http://cms.stat.unib.it/ragna/teaching.aspx Esercizi Argmenti: mana, fferta, equilibri i mercat, renita el cnsumatre
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 14. Le trasformazioni elettrochimiche SEGUI LA MAPPA Reazioni di ossidoriduzione
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 14. Le trasformazioni elettrochimiche SEGUI LA MAPPA Reazioni di ossidoriduzione
Equazioni. Prerequisiti. Definizioni e concetti generali. Incognita Lettera (di solito X) alla quale è possibile sostituire dei valori numerici
 Scmpsizini plinmiali Calcl del M.C.D. e del m.c.m. tra plinmi P), cn P) plinmi di grad qualsiasi Equazini Prerequisiti Definizini e cncetti generali Incgnita Lettera di slit ) alla quale è pssibile sstituire
Scmpsizini plinmiali Calcl del M.C.D. e del m.c.m. tra plinmi P), cn P) plinmi di grad qualsiasi Equazini Prerequisiti Definizini e cncetti generali Incgnita Lettera di slit ) alla quale è pssibile sstituire
Le celle elettrolitiche
 Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Le reazioni redox e l elettrochimica Capitolo 18
 Le reazioni redox e l elettrochimica Capitolo 18 I processi elettrochimici sono reazioni di ossido-riduzione in cui: l energia rilasciata da una reazione spontanea è convertita in elettricità oppure l
Le reazioni redox e l elettrochimica Capitolo 18 I processi elettrochimici sono reazioni di ossido-riduzione in cui: l energia rilasciata da una reazione spontanea è convertita in elettricità oppure l
Elettrochimica. 1. Celle elettrolitiche. 2. Celle galvaniche o pile
 Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
È un processo non spontaneo. DG elettrolisi > 0 a spese del lavoro elettrico necessario per. avere il passaggio di corrente attraverso la soluzione
 Elettrolisi: il complesso dei fenomeni che avvengono in una soluzione elettrolitica o in un elettrolita fuso al passaggio della corrente elettrica, di norma continua, e che realizzano la trasformazione
Elettrolisi: il complesso dei fenomeni che avvengono in una soluzione elettrolitica o in un elettrolita fuso al passaggio della corrente elettrica, di norma continua, e che realizzano la trasformazione
ELETTROCHIMICA 16/12/2015
 ELETTROCHIMICA Tratta delle trasformazioni tra energia chimica ed energia elettrica Alla base ci sono reazioni di ossidoriduzione, cioè con scambio di elettroni tra reagenti e prodotti della reazione Fe
ELETTROCHIMICA Tratta delle trasformazioni tra energia chimica ed energia elettrica Alla base ci sono reazioni di ossidoriduzione, cioè con scambio di elettroni tra reagenti e prodotti della reazione Fe
I TRASDUTTORI. Trasduttori Primari. Trasduttori Secondari
 I TRASDUTTORI Un trasduttre ( sensre) è un dispsitiv in grad di rilevare una grandezza fisica di tip qualsiasi (termic, lumins, magnetic, meccanic, chimic, eccetera) e di trasfrmarla in una grandezza di
I TRASDUTTORI Un trasduttre ( sensre) è un dispsitiv in grad di rilevare una grandezza fisica di tip qualsiasi (termic, lumins, magnetic, meccanic, chimic, eccetera) e di trasfrmarla in una grandezza di
INFLUENZA DELLO SPESSORE SULLA SENSIBILITA DEI SENSORI DI GAS A POLIMERO CONDUTTORE
 INFLUENZA DELLO SPESSORE SULLA SENSIBILITA DEI SENSORI DI GAS A POLIMERO ONDUTTORE L studi e la prgettazine di sensri di gas ha ricevut una grande spinta negli ultimi anni, sprattutt in ambiti quali la
INFLUENZA DELLO SPESSORE SULLA SENSIBILITA DEI SENSORI DI GAS A POLIMERO ONDUTTORE L studi e la prgettazine di sensri di gas ha ricevut una grande spinta negli ultimi anni, sprattutt in ambiti quali la
REAZIONI CHIMICHE : FORMALISMO
 Per reazione chimica si intende una trasformazione della materia in cui alcune sostanze (reagenti) si trasformano in altre (prodotti) attraverso un cambiamento delle interazioni fra gli atomi (legami)
Per reazione chimica si intende una trasformazione della materia in cui alcune sostanze (reagenti) si trasformano in altre (prodotti) attraverso un cambiamento delle interazioni fra gli atomi (legami)
Reazioni di ossido-riduzione
 Reazioni di ossido-riduzione Le reazioni di ossidoriduzioni o redox sono reazioni nelle quali si ha variazione del numero di ossidazione (n. o.) di ioni o atomi. La specie chimica che si ossida cede elettroni
Reazioni di ossido-riduzione Le reazioni di ossidoriduzioni o redox sono reazioni nelle quali si ha variazione del numero di ossidazione (n. o.) di ioni o atomi. La specie chimica che si ossida cede elettroni
Strumentazione biomedica
 Strumentazine bimedica Prgett e impieg dei sistemi di misura Capitl 4 Guid Avanzlini DEIS - Università di Blgna 10/10/2012 Sensri per Misure Bimediche Definizine: Un sensre è quella parte della catena
Strumentazine bimedica Prgett e impieg dei sistemi di misura Capitl 4 Guid Avanzlini DEIS - Università di Blgna 10/10/2012 Sensri per Misure Bimediche Definizine: Un sensre è quella parte della catena
luglio 2017 febbraio 2018 Problema 1 1. Bilanciare in forma molecolare la seguente equazione: Cr(OH)3 + NaIO3 + NaOH Na2CrO4 + NaI + H2O
 Problema 1 luglio 017 1. Bilanciare in forma molecolare la seguente equazione: Cr(OH)3 + NaIO3 + NaOH NaCrO4 + NaI + HO Calcolare quanti grammi di HO si possono ottenere, in base all equazione bilanciata,
Problema 1 luglio 017 1. Bilanciare in forma molecolare la seguente equazione: Cr(OH)3 + NaIO3 + NaOH NaCrO4 + NaI + HO Calcolare quanti grammi di HO si possono ottenere, in base all equazione bilanciata,
Numero di ossidazione
 Elettrochimica Elettrochimica Trasformazione di energia chimica in energia elettrica: generatori (pile, accumulatori) Trasformazione di energia elettrica in energia chimica (celle di elettrolisi, tecnologie
Elettrochimica Elettrochimica Trasformazione di energia chimica in energia elettrica: generatori (pile, accumulatori) Trasformazione di energia elettrica in energia chimica (celle di elettrolisi, tecnologie
Soluzione Es.1- In generale, le equazioni orarie del moto lungo l'asse orizzontale x e quello verticale y si possono scrivere come: (1a) (1b) (1c)
 Sluzine Es.1- In generale, le equazini rarie del mt lung l'asse rizzntale x e quell verticale si pssn scrivere cme: ( t) h + v (csα) t gt / h + v t / gt / (1a) v ( t) v csα gt v / gt (1b) x( t) v (sinα
Sluzine Es.1- In generale, le equazini rarie del mt lung l'asse rizzntale x e quell verticale si pssn scrivere cme: ( t) h + v (csα) t gt / h + v t / gt / (1a) v ( t) v csα gt v / gt (1b) x( t) v (sinα
Le reazioni di ossidoriduzione
 Le reazioni di ossidoriduzione Le reazioni di ossidoriduzioni o redox sono reazioni nelle quali si ha variazione del numero di ossidazione ( n. o. ) di ioni o atomi. La specie chimica che si ossida cede
Le reazioni di ossidoriduzione Le reazioni di ossidoriduzioni o redox sono reazioni nelle quali si ha variazione del numero di ossidazione ( n. o. ) di ioni o atomi. La specie chimica che si ossida cede
Elettrochimica. ChimicaGenerale_lezione22 1
 Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Elettrochimica L elettrochimica studia le variazioni chimiche prodotte dalla corrente elettrica e la produzione di elettricità ottenuta tramite reazioni chimiche. Le reazioni elettrochimiche implicano
Disequazioni in una incognita
 Disequazini in una incgnita. Cnsiderazini generali Dai principi di equivalenza delle disequazini segue che: a) quand si trasprta un termine da un membr all'altr si deve cambiarne il segn:. b) quand si
Disequazini in una incgnita. Cnsiderazini generali Dai principi di equivalenza delle disequazini segue che: a) quand si trasprta un termine da un membr all'altr si deve cambiarne il segn:. b) quand si
COMPITO A DI CHIMICA DEL 15-09-09
 COMPITO A DI CHIMICA DEL 15-09-09 1A) 3,447 g di anidride arsenica (As 2 O 5 ) solida e 6,278 g di zinco metallico vengono fatti reagire con un eccesso di acido solforico. Si calcoli il volume di arsina
COMPITO A DI CHIMICA DEL 15-09-09 1A) 3,447 g di anidride arsenica (As 2 O 5 ) solida e 6,278 g di zinco metallico vengono fatti reagire con un eccesso di acido solforico. Si calcoli il volume di arsina
SOLUZIONI COMPITO A DI CHIMICA DEL
 SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
Bioelettrodi. Elettrodi e pricipi di elettrochimica
 Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
Bioelettrodi Elettrodi e pricipi di elettrochimica Caratteristiche dei segnali biologici I segnali elettrici di origine biologica rappresentano variabili biomediche che necessitano di particolari strumentazioni
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A
 POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A Avvertenze: scrivere le soluzioni sull apposito foglio che va completato con tutti i
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A Avvertenze: scrivere le soluzioni sull apposito foglio che va completato con tutti i
Sommario della lezione 24. Equilibri di solubilità. Chimica Organica. Elettrochimica
 Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
Elettrochimica. Celle Galvaniche o Pile. Redox. Celle Galvaniche. Reazioni Redox. Celle Galvaniche. Celle Galvaniche
 Celle Galvaniche o Pile Elettrochimica La branca della chimica che si occupa dell'impiego delle reazioni chimiche per la produzione dell'elettricità e dell'impiego dell'elettricità per causare trasformazioni
Celle Galvaniche o Pile Elettrochimica La branca della chimica che si occupa dell'impiego delle reazioni chimiche per la produzione dell'elettricità e dell'impiego dell'elettricità per causare trasformazioni
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 18 Le ossido-riduzioni e l elettrochimica 1. Ossidazione e riduzione: che cosa sono e come si
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 18 Le ossido-riduzioni e l elettrochimica 1. Ossidazione e riduzione: che cosa sono e come si
Numeri di Ossidazione
 Numeri di ssidazione Si definiscono NUMERI o STATI di SSIDAZINE quei numeri che rappresentano lo squilibrio di carica a cui è soggetto un atomo in un composto bi o poliatomico rispetto al suo stato elementare
Numeri di ssidazione Si definiscono NUMERI o STATI di SSIDAZINE quei numeri che rappresentano lo squilibrio di carica a cui è soggetto un atomo in un composto bi o poliatomico rispetto al suo stato elementare
