Strategie per la purificazione delle proteine
|
|
|
- Emilia Gori
- 5 anni fa
- Visualizzazioni
Transcript
1 Strategie per la purificazione delle proteine
2 In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo % delle proteine totali Inoltre ci sono altri componenti: Acidi nucleici, carboidrati, lipidi, piccole molecole Le proteine possono essere trovate in diversi stati solubili, (insolubili -native o aggregate, inclusion bodies, integrate o associate alle membrane oppure in associazione con il DNA) ed in diverse localizzazioni (compartimenti subcellulari)
3 Principi per la purificazione delle proteine Definire gli obiettivi (scopi accademici o applicazioni industriali) Purezza, attività e quantità di prodotto finale richiesto (possibilità di produzione di proteine ricombinanti) Definire le proprietà della proteina di interesse ed eventualmente delle impurezze critiche (purezza elevata o estratto grezzo, se meno contaminanti più facile isolarla): ricorda che la purezza assoluta è un concetto astratto! Sviluppare saggi analitici È necessario identificare la proteina nel corso della purificazione (info su peso molecolare, pi, ) Rimuovere rapidamente i contaminanti capaci di danneggiare la proteina (proteasi)
4 Perchè purificare una proteina? Applicazioni industriali o farmacologiche Studi strutturali e/o funzionali Per produrre anticorpi Sequenza parziale La potenziale applicazione influenzerà l uso delle tecniche impiegate
5 Domande iniziali Quanta e quanto pura? (scelta del metodo per verificare la purezza) applicazione sorgente fattibilità Configurazione nativa? Studi struttura/funzione (si) microsequenza (no) anticorpi (forse) Metodi di identificazione? Saggi funzionali (ad esempio enzimatici) Saggi immunologici SDS-PAGE
6 Capacità: volume di miscela che può essere purificata Risoluzione: purezza della della proteina target Resa: % di proteina target che può essere recuperata (rispetto al quantitativo iniziale della stessa proteina) Velocità: è fondamentale soprattutto nei primi step (rimozione delle proteasi)
7 Principi generali per la purificazione delle proteine (rese elevate con minor numero di passaggi possibilecompromesso purezza-resa) Usare una tecnica diverse in ciascun passaggio Per avvantaggiarsi delle diverse proprietà della proteina (dimensione, carica, idrofobicità, eventuale specificità per ligandi) Minimizzare la manipolazione del campione ad ogni stadio Minimizzare l uso di additivi Minimizzare il numero di passaggi
8 Usare una tecnica diverse in ciascun passaggio Per avvantaggiarsi delle diverse proprietà della proteina (dimensione, carica, idrofobicità, eventuale specificità per ligandi) Minimizzare la manipolazione del campione ad ogni stadio Il materiale che si ottiene ad un passaggio deve essere nelle condizioni ph e forza ionica ideali per il passaggio successivo Minimizzare l uso di additivi Minimizzare il numero di passaggi Principi generali per la purificazione delle proteine
9 Principi generali per la purificazione delle proteine Usare una tecnica diverse in ciascun passaggio Per avvantaggiarsi delle diverse proprietà della proteina (dimensione, carica, idrofobicità, eventuale specificità per ligandi) Minimizzare la manipolazione del campione ad ogni stadio Minimizzare l uso di additivi (mantenimento dell attività biologica) Minimizzare il numero di passaggi
10 Principi generali per la purificazione delle proteine Usare una tecnica diverse in ciascun passaggio Per avvantaggiarsi delle diverse proprietà della proteina (dimensione, carica, idrofobicità, eventuale specificità per ligandi) Minimizzare la manipolazione del campione ad ogni stadio Minimizzare l uso di additivi Minimizzare il numero di passaggi (per non diminuire la resa) Ad ogni passaggio: analisi elettroforetiche
11 Es: purificazione di GGT1 Gamma glutamiltranspeptidasi 1 (enzima che taglia il legame g-glutamilico del glutatione extracellulare)
12 Ad esempio: La resa di una proteina ottenuta dopo 4 passaggi di purificazione, ciascuno caratterizzato da una perdita del 25% del prodotto, è pari al 32% 0.75 x 0.75 x 0.75 x 0.75 = (31.6%)
13 Sviluppare uno schema per la purificazione Condurre esperimenti su scala pilota per valutare l efficacia di varie tecniche di separazione Iniziare con tecniche rapide ad alta capacità (generalmente a bassa risoluzione), e proseguire con tecniche ad alta risoluzione e bassa capacità
14 La purificazione delle proteine è un processo complesso che generalmente richiede diversi passaggi Campione Tecnica separativa Frazionamento Saggi analitici Ripetere la separazione con una nuova tecnica, fino alla purificazione finale N o eliminare N o C è attività si Unire le frazioni Controllare la purezza Pura? Si Tecnica analitica
15 Prima di iniziare la purificazione è opportuno definire un saggio di identificazione della proteina a) Enzimatico. Poiché il controllo può essere ripetuto molte volte sarebbe utile disporre di un saggio semplice ed economico. Generalmente un attività enzimatica può essere controllata tramite cambiamenti in assorbanza che possono essere misurati con uno spettrofotometro. b) Immunologico. Attraverso l uso di anticorpi specifici c) Peso molecolare. Tramite SDS-PAGE d) Spettrofotometrico. Se la proteina possiede particolari cromofori
16 Capacità vs. Risoluzione Metodo capacità risoluzione tempo (e sforzo) Solubilità differenziale Scambio ionico Gel filtrazione Elettroforesi HPLC/FPLC Affinità dipende dai ligandi
17 Metodi di frazionamento preliminare a bassa risoluzione (I) Frazionamento con Sali (Salting out). il genere si usa solfato di ammonio. Fa precipitare le proteine senza denaturarle. L aggiunta di sale rimuove le molecole d acqua sulla superficie della proteina, permettendone l aggregazione e quindi la precipitazione. Le proteine molto idrofobiche precipitano a bassa concentrazione, quelle meno idrofobiche precipitano ad alta concentrazione di sale. Tutti i passaggi sono generalmente condotti a 4 C. Ogni data proteina precipita (effetto salting out) in un ristretto intervallo di solfato di ammonio.
18 La solubilità delle proteine è fortemente influenzata dalla forza ionica
19 Principio del salting out : 1. gli ioni di sale aggiunto competono con gli ioni presenti nella soluzione per le molecole di solvente, facilitando l aggregazione proteica; 2. Proteine diverse precipitano a diverse concentrazioni di sale. 100% 100% [(NH 4 ) 2 SO 4 ] solubilità 0% 0%
20
21 Metodi di frazionamento preliminare a bassa risoluzione (II) Precipitazione al calore. Il calore denatura le proteine che perdono la loro struttura terziaria, esponendo residui idrofobici sepolti nello stato nativo nel core proteico e causando la formazione di aggregati. Si stabilisce su un piccolo campione la temperatura a cui la proteina di interesse denatura. Si scalda la miscela ad una temperatura 5-10 C inferiore a quella critica per un tempo adeguato (15-30 minuti). Le proteine denaturate sono rimosse per centrifugazione.
22 Metodi di frazionamento preliminare a bassa risoluzione (III) Precipitazioni con solventi organici si basa sulla diversa solubilità delle diverse proteine in soluzioni acquose di solventi organici (soprattutto alcoli). Il processo è spesso condotto a 20 C per evitare la denaturazione. Precipitazione al punto isoelettrico. Le proteine possono essere cariche positivamente o negativamente e possono essere neutre per una eguaglianza di cariche; quando la carica netta è nulla le proteine si trovano nelle condizioni migliori per formare aggregati fra loro.
23 Metodi di frazionamento successivi:
24 Gel filtrazione
25 Cromatografia a scambio ionico
26 Cromatografia di affinità
27 Come identificare le frazioni che contengono proteine Frazioni # A A Peaks Le proteine totali vengono stimate registrando l assorbanza a 280 nm con uno spettrofotometro. I valori ottenuti possono essere utilizati per costruire un grafico che è chiamato profilo di eluizione. Fraction #
28 Il primo passaggio di purificazione cromatografica deve rimuovere la maggior parte dei contaminanti (scambio ionico/gel filtrazione?) I passaggi intermedi sfruttano proprietà differenti (le tecniche di assorbimento consentono di recuperare il campione in piccoli volumi) Il passaggio finale deve rimuovere gli ultimi contaminanti La proteina viene infine dializzata e concentrata
29 Metodi per la concentrazione precipitazione (NH 4 ) 2 SO 4 dialisi contro 50% glicerolo dialisi contro PEG ultrafiltrazione liofilizzazione cromatografia
30 Come valutare la procedura di purificazione quantità recupero (resa %) livello di purificazione
31 Attività specifica = unità totali di enzima quantita di proteine totali Livello di purificazione = attività spec. recuperata/mg attività spec. iniziale/mg Resa % = quantità di proteina purificata quantità di proteina nell estratto iniziale
32
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
Strategie per la purificazione delle proteine In una cellula ci possono essere molte proteine (ad esempio, ci sono circa 4300 geni in E. coli) Una singola proteina può rappresentare una frazione tra lo
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
Passaggi preliminari di purificazione
 Passaggi preliminari di purificazione Estratto iniziale Omogenato contiene materiale insolubile che generalmente viene eliminato per centrifugazione. Talvolta la soluzione mostra torbidità (dovuta alla
Passaggi preliminari di purificazione Estratto iniziale Omogenato contiene materiale insolubile che generalmente viene eliminato per centrifugazione. Talvolta la soluzione mostra torbidità (dovuta alla
MATERIALE DIDATTICO. A supporto sono rese disponibili le slides delle lezioni
 MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
MATERIALE DIDATTICO 1.Metodologie Biochimiche. Bonaccorsi, Contestabile, Di Salvo. Casa Editrice Ambrosiana. Ed.2012 2.Biochimica Applicata. Stoppini, Bellotti. EdiSES, 2012 3. Sono utilizzabili alcuni
PURIFICAZIONE DELLE PROTEINE
 PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
PURIFICAZIONE DELLE PROTEINE 1 proteina da 10.000-20.000 proteine diverse (in una cellula, tessuto) Il grado finale di purezza che si vuole raggiungere dipende dagli scopi. Cosa si intende per proteina
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea
 la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea Analisi delle sue proprietà fisiche e biologiche Come viene modulata la sua espressione
la purificazione può essere di tipo analitico o preparativo Purificare una proteina significa ottenerla in forma omogenea Analisi delle sue proprietà fisiche e biologiche Come viene modulata la sua espressione
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
Seminario di Cacciatore Rosalia
 Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
Strategie per la purificazione delle proteine Attenzione! C è differenza tra separazione per alcuni scopi analitici (Gel-electrophoresis, IEF, 2D-gels) e purificazione In una cellula ci possono essere
Modulo 3. Lavorare con le proteine
 Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Metodi di studio delle proteine (o altre macromolecole)
 Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
5- Estrazione ed analisi di DNA
 5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
5- Estrazione ed analisi di DNA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) La struttura del DNA La traduzione dell informazione
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
Dott. ssa Nadia D Ambrosi ----METODI BIOCHIMICI---- Ricevimento: Martedì (Dipartimento di Biologia, dente L)
 Dott. ssa Nadia D Ambrosi ----METODI BIOCHIMICI---- nadia.dambrosi@uniroma2.it Ricevimento: Martedì 14-16 (Dipartimento di Biologia, dente L) Organizzazione del corso: Lunedì h9-11 fino al 28/5 - didattica
Dott. ssa Nadia D Ambrosi ----METODI BIOCHIMICI---- nadia.dambrosi@uniroma2.it Ricevimento: Martedì 14-16 (Dipartimento di Biologia, dente L) Organizzazione del corso: Lunedì h9-11 fino al 28/5 - didattica
GENERALITA SULLA CROMATOGRAFIA
 GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
TIPI di CROMATOGRAFIA
 Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Strategie di purificazione di proteine
 Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
Strategie per la purificazione delle proteine
 Strategie per la purificazione delle proteine Attenzione! E opportuno distinguere tra metodi di separazione per specifici scopi analitici (basati su tecniche ad alta risoluzione, quali, ad esempio, IEF,,g
Strategie per la purificazione delle proteine Attenzione! E opportuno distinguere tra metodi di separazione per specifici scopi analitici (basati su tecniche ad alta risoluzione, quali, ad esempio, IEF,,g
CFU. Nome e cognome. Metodi Biochimici in Biotecnologie 19 luglio 2AA7- Test B
 Metodi Biochimici in Biotecnologie 19 luglio 2AA7- Test B Nome e cognome CFU 1B) (3 punti max) L'enzima YZ contiene un atomo di rame nel suo sito attivo. Lo spettro di assorbimento del visibile di questo
Metodi Biochimici in Biotecnologie 19 luglio 2AA7- Test B Nome e cognome CFU 1B) (3 punti max) L'enzima YZ contiene un atomo di rame nel suo sito attivo. Lo spettro di assorbimento del visibile di questo
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI
 METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008. Eloise Mastrangelo
 Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
differente ripartizione delle sostanze tra due fasi immiscibili
 Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
ELETTROFORESI DI PROTEINE
 ELETTROFORESI DI PROTEINE ELETTROFORESI DI PROTEINE Molto più complessa della separazione elettroforetica di DNA. forma delle proteine fortissime variazioni cariche delle proteine La > parte dei campioni
ELETTROFORESI DI PROTEINE ELETTROFORESI DI PROTEINE Molto più complessa della separazione elettroforetica di DNA. forma delle proteine fortissime variazioni cariche delle proteine La > parte dei campioni
2. LA PURIFICAZIONE DI PROTEINE:
 2. LA PURIFICAZIONE DI PROTEINE: LA CROMATOGRAFIA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU-16 ore) Marco Scocchi ( BIO/10-11) LA PURIFICAZIONE DI PROTEINE Purificare
2. LA PURIFICAZIONE DI PROTEINE: LA CROMATOGRAFIA Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU-16 ore) Marco Scocchi ( BIO/10-11) LA PURIFICAZIONE DI PROTEINE Purificare
Laboratorio di Biologia Molecolare
 UNIVERSITÀ DEGLI STUDI DELL AQUILA DIPARTIMENTO DI MEDICINA CLINICA, SANITÀ PUBBLICA, SCIENZE DELLA VITA E DELL AMBIENTE in collaborazione con Laboratorio di Biologia Molecolare Estrazione del DNA da tessuto
UNIVERSITÀ DEGLI STUDI DELL AQUILA DIPARTIMENTO DI MEDICINA CLINICA, SANITÀ PUBBLICA, SCIENZE DELLA VITA E DELL AMBIENTE in collaborazione con Laboratorio di Biologia Molecolare Estrazione del DNA da tessuto
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Preparazione del campione analitico
 Preparazione del campione analitico Workflow per l analisi farmaceutica Lotto Totalità del materiale Campionamento Il campione deve essere rappresentativo del lotto Conservazione Preparazione campione
Preparazione del campione analitico Workflow per l analisi farmaceutica Lotto Totalità del materiale Campionamento Il campione deve essere rappresentativo del lotto Conservazione Preparazione campione
cromatografia Esplorando le proteine
 Cromatografia Flavia Frabetti Tecnici di laboratorio 2010/2011 Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per
Cromatografia Flavia Frabetti Tecnici di laboratorio 2010/2011 Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per
Corso di Laurea magistrale in Medicina Veterinaria (LM42) Anno Accademico 2018/2019
 Corso di Laurea magistrale in Medicina Veterinaria (LM) Programma dell insegnamento di Biochimica Anno di corso I Bimestre III N CFU 6 Ore complessive 65 Anno Accademico 08/09 Obiettivi formativi specifici
Corso di Laurea magistrale in Medicina Veterinaria (LM) Programma dell insegnamento di Biochimica Anno di corso I Bimestre III N CFU 6 Ore complessive 65 Anno Accademico 08/09 Obiettivi formativi specifici
Primo Levi Il sistema periodico
 Primo Levi Il sistema periodico L anidride carbonica [...] questo gas che costituisce la materia prima della vita, la scorta permanente a cui tutto ciò che cresce attinge, e il destino ultimo di ogni carne,
Primo Levi Il sistema periodico L anidride carbonica [...] questo gas che costituisce la materia prima della vita, la scorta permanente a cui tutto ciò che cresce attinge, e il destino ultimo di ogni carne,
Dall omogenato... alla purificazione di proteine
 Dall omogenato... alla purificazione di proteine Per poter purificare una proteina bisogna disporre di: 1)Un metodo per poter seguire la proteina nei diversi passaggi di purificazione (saggio enzimatico,
Dall omogenato... alla purificazione di proteine Per poter purificare una proteina bisogna disporre di: 1)Un metodo per poter seguire la proteina nei diversi passaggi di purificazione (saggio enzimatico,
Estrazione di DNA. Laboratorio di Biologia Applicata
 Estrazione di DNA Laboratorio di Biologia Applicata Tecniche di estrazione Qualità del campione di partenza Numero di campioni Costo Tempo Semplicità e affidabilità Automazione Sicurezza Materiale biologico
Estrazione di DNA Laboratorio di Biologia Applicata Tecniche di estrazione Qualità del campione di partenza Numero di campioni Costo Tempo Semplicità e affidabilità Automazione Sicurezza Materiale biologico
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
cromatografia Elettroforesi
 Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Analisi quantitativa dell interazione proteina-proteina
 Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Composizione della sostanza azotata del latte vaccino (% rel)
 Composizione della sostanza azotata del latte vaccino (% rel) s1 29-35 Caseine s2 8-10 35-40 78 10-15 Materia Azotata Proteica ( ) lattoglobulina 4-8 8-9 94-95 Materia Azotata Totale (N*6,38) Proteine
Composizione della sostanza azotata del latte vaccino (% rel) s1 29-35 Caseine s2 8-10 35-40 78 10-15 Materia Azotata Proteica ( ) lattoglobulina 4-8 8-9 94-95 Materia Azotata Totale (N*6,38) Proteine
Applicazioni biotecnologiche degli enzimi: le lipasi
 Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Cosa determina l assorbanza di un cromoforo?
 Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Estrazione ed elettroforesi degli acidi nucleici
 Estrazione ed elettroforesi degli acidi nucleici Flavia Frabetti Estrazione acidi nucleici (DNA orna) Verifica tramite elettroforesi su gel di agarosio Amplificazione tramite PCR (da DNA) o RT-PCR (da
Estrazione ed elettroforesi degli acidi nucleici Flavia Frabetti Estrazione acidi nucleici (DNA orna) Verifica tramite elettroforesi su gel di agarosio Amplificazione tramite PCR (da DNA) o RT-PCR (da
fase stazionaria fase mobile
 Cromatografia Insieme di tecniche che hanno lo scopo di separare una miscela nei suoi componenti, per permetterne il riconoscimento qualitativo e quantitativo. Sono basate sulla distribuzione dei vari
Cromatografia Insieme di tecniche che hanno lo scopo di separare una miscela nei suoi componenti, per permetterne il riconoscimento qualitativo e quantitativo. Sono basate sulla distribuzione dei vari
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Lo studio delle varie conformazioni del DNA
 Lo studio delle varie conformazioni del DNA Separazione dei topoisomeri Molecole di DNA ccc di una uguale lunghezza e composizione in basi, ma diverso Lk, sono dette topoisomeri. I topoisomeri possono
Lo studio delle varie conformazioni del DNA Separazione dei topoisomeri Molecole di DNA ccc di una uguale lunghezza e composizione in basi, ma diverso Lk, sono dette topoisomeri. I topoisomeri possono
Acidi nucleici come materiale di studio. DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna
 Acidi nucleici come materiale di studio DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna Isolamento DNA da cellule eucariotiche Isolamento acidi nucleici 1. lisi cellulare 2. purificazione 2a.
Acidi nucleici come materiale di studio DNA endogeno DNA esogeno (transgeni) RNA strutturale mrna Isolamento DNA da cellule eucariotiche Isolamento acidi nucleici 1. lisi cellulare 2. purificazione 2a.
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Estrazione di proteine - Scelta della fonte biologica
 Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
Estrazione di proteine - Scelta della fonte biologica Proteine endogene Batteri Cellule eucariotiche Proteine ricombinanti Lieviti Tessuti Localizzazione della proteina PURIFICAZIONE DELLE PROTEINE 1 proteina
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
TECNICHE ELETTROFORETICHE. - Purificazione di molecole: elettroforesi preparativa. - Controllo della purezza di una molecola in un campione
 TECNICHE ELETTROFORETICHE Aree di applicazione: - Purificazione di molecole: elettroforesi preparativa - Controllo della purezza di una molecola in un campione - Determinazione quantitativa di una molecola
TECNICHE ELETTROFORETICHE Aree di applicazione: - Purificazione di molecole: elettroforesi preparativa - Controllo della purezza di una molecola in un campione - Determinazione quantitativa di una molecola
Applicazioni biotecnologiche degli enzimi: le lipasi
 Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE
 CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
CORSO DI LAUREA IN BIOLOGIA GENERALE ED APPLICATA ESERCITAZIONE DEL CORSO DI ANALISI DI MACROMOLECOLE Anno accademico 2016-2017 L esperimento consiste nella analisi di due estratti proteici frazionati
TECNOLOGIE BIOMOLECOLARI
 TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
Progetto Lars-Biotec
 Unità didattiche: prima fase: Progetto Lars-Biotec Laboratorio di Ricerca sperimentale nel settore delle Biotecnologie Bioinformatica: vengono scelti e analizzati geni appartenente al genoma umano conosciuti
Unità didattiche: prima fase: Progetto Lars-Biotec Laboratorio di Ricerca sperimentale nel settore delle Biotecnologie Bioinformatica: vengono scelti e analizzati geni appartenente al genoma umano conosciuti
Jay Phelan, Maria Cristina Pignocchino. Scopriamo la biologia
 Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
ESTRAZIONE PURIFICAZIONE. Modificazione chimica ANALISI STRUMENTALE
 Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
Tecniche di base di Biologia Molecolare
 Tecniche di base di Biologia Molecolare Isolamento e purificazione di DNA e RNA Manipolazione e quantificazione degli acidi nucleici Elettroforesi su gel Isolamento e purificazione di DNA e RNA Il primo
Tecniche di base di Biologia Molecolare Isolamento e purificazione di DNA e RNA Manipolazione e quantificazione degli acidi nucleici Elettroforesi su gel Isolamento e purificazione di DNA e RNA Il primo
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
Estrazione con solventi. Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti
 Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
2 ZEPPA G. BELVISO S.
 Appunti di Tecniche avanzate per il controllo degli alimenti Parte 2 ZEPPA G. BELVISO S. Università degli Studi di Torino Il termine cromatografia indica un insieme di tecniche che hanno lo scopo di separare
Appunti di Tecniche avanzate per il controllo degli alimenti Parte 2 ZEPPA G. BELVISO S. Università degli Studi di Torino Il termine cromatografia indica un insieme di tecniche che hanno lo scopo di separare
O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%.
 Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
V R V t. Proteine ad alto peso molecolare. Proteine a peso molecolare intermedio. Proteine a basso peso molecolare. Kd + piccolo.
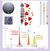 V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
La nutrizione minerale. Ovvero gli ioni inorganici necessari alla pianta e modalità di assorbimento e assimilazione
 La nutrizione minerale Ovvero gli ioni inorganici necessari alla pianta e modalità di assorbimento e assimilazione Assorbimento degli elementi minerali: riguarda il loro prelievo dal suolo da parte delle
La nutrizione minerale Ovvero gli ioni inorganici necessari alla pianta e modalità di assorbimento e assimilazione Assorbimento degli elementi minerali: riguarda il loro prelievo dal suolo da parte delle
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
L'attività di queste proteine, a sua volta è modulata dalla composizione dei fosfolipidi della membrana
 La funzione di ogni membrana biologica è determinata principalmente dall insieme di proteine integrali incorporate e dalle proteine periferiche collegate alla superficie della membrana L'attività di queste
La funzione di ogni membrana biologica è determinata principalmente dall insieme di proteine integrali incorporate e dalle proteine periferiche collegate alla superficie della membrana L'attività di queste
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Fondamenti di spettroscopia. Spettrofotometria UV/Vis (Tecnica analitica)
 Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
Genomica e Proteomica
 Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
Corso di Laurea triennale in Biotecnologie Piano farmaceutico
 Università degli Studi di Padova Dipartimento di Scienze del Farmaco Corso di Laurea triennale in Biotecnologie Piano farmaceutico 10 maggio 2018 AA 2018-2019 Patrizia Polverino de Laureto Impatto delle
Università degli Studi di Padova Dipartimento di Scienze del Farmaco Corso di Laurea triennale in Biotecnologie Piano farmaceutico 10 maggio 2018 AA 2018-2019 Patrizia Polverino de Laureto Impatto delle
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria contesto fisiologico livelli superiori funzione Elettrofores i
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria contesto fisiologico livelli superiori funzione Elettrofores i
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
metodi poco sensibili, laboriosi, costosi, e indaginosi
 dosaggi ormonali L ANALISI CHIMICA fasi di isolamento, purificazione e concentrazione elaborate non sufficientemente sensibile per il dosaggio di tutti gli ormoni nel sangue metodi poco sensibili, laboriosi,
dosaggi ormonali L ANALISI CHIMICA fasi di isolamento, purificazione e concentrazione elaborate non sufficientemente sensibile per il dosaggio di tutti gli ormoni nel sangue metodi poco sensibili, laboriosi,
Caratteristiche delle membrane biologiche
 Membrane Biologiche Caratteristiche delle membrane biologiche 1. Le membrane sono strutture a foglio che formano setti di separazione tra compartimenti con composizione diversa tra loro. 2. Sono costituite
Membrane Biologiche Caratteristiche delle membrane biologiche 1. Le membrane sono strutture a foglio che formano setti di separazione tra compartimenti con composizione diversa tra loro. 2. Sono costituite
concentrazione finale rispettivamente di 0.2 M e?%,a 55.c 60 minuti.
 SEPARAZIONE DELLE SUBUNITA' DELLA RIBULOSIO-1,5-DIFOSFATO CARBOSSILASI DA FOGLIE DI CARCIOFO. Cardinali A.,Miceli A.,Pacoda D. e Gallerani R. Centro di Biologia,Laboratorio di Chimica Biologica,Universita'
SEPARAZIONE DELLE SUBUNITA' DELLA RIBULOSIO-1,5-DIFOSFATO CARBOSSILASI DA FOGLIE DI CARCIOFO. Cardinali A.,Miceli A.,Pacoda D. e Gallerani R. Centro di Biologia,Laboratorio di Chimica Biologica,Universita'
BIOFISICA DELLE MEMBRANE
 BIOFISICA DELLE MEMBRANE Le funzioni biologiche di tutti gli organismi viventi si svolgono mediante scambio di sostanze ed informazioni attraverso membrane. Membrana = struttura che separa due mezzi diversi
BIOFISICA DELLE MEMBRANE Le funzioni biologiche di tutti gli organismi viventi si svolgono mediante scambio di sostanze ed informazioni attraverso membrane. Membrana = struttura che separa due mezzi diversi
Elettroforesi = migrazione in campo elettrico
 Elettroforesi = migrazione in campo elettrico Molte molecole di interesse biologico possiedono gruppi ionizzabili. In opportune condizioni di ph presentano una carica elettrica + o e quindi sono in grado
Elettroforesi = migrazione in campo elettrico Molte molecole di interesse biologico possiedono gruppi ionizzabili. In opportune condizioni di ph presentano una carica elettrica + o e quindi sono in grado
Estrazione. Il processo di estrazione con solventi è impiegato per l isolamento di
 Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
Saranno effettuate lezioni frontali. Sono previste esercitazioni teorico-pratiche e seminari di approfondimento.
 DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2018/2019-4 anno BIOCHIMICA APPLICATA BIO/10-8 CFU - 2 semestre Docente titolare dell'insegnamento
DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2018/2019-4 anno BIOCHIMICA APPLICATA BIO/10-8 CFU - 2 semestre Docente titolare dell'insegnamento
CARATTERIZZAZIONE DELLE INTERAZIONI
 CARATTERIZZAZIONE DELLE INTERAZIONI Costante di legame Concentrazione delle due specie Interazione Competizione con altre proteine Cofattori Compartimentazione cellulare Fattori che influenzano l interazione
CARATTERIZZAZIONE DELLE INTERAZIONI Costante di legame Concentrazione delle due specie Interazione Competizione con altre proteine Cofattori Compartimentazione cellulare Fattori che influenzano l interazione
0,8% riesce a separare un range di dimensioni da circa 500 bp a circa bp.
 L elettroforesi è una tecnica che utilizza un campo elettrico per separare e visualizzare frammenti di DNA in base al loro peso molecolare ed alla loro carica. Gli acidi nucleici, migrano sempre verso
L elettroforesi è una tecnica che utilizza un campo elettrico per separare e visualizzare frammenti di DNA in base al loro peso molecolare ed alla loro carica. Gli acidi nucleici, migrano sempre verso
Espressione eterologa, purificazione e saggio di attività della Fe-idrogenasi di Enterobacter cloacae
 Università degli studi di Padova - Facoltà di scienze MM.FF.NN. Laurea di primo livello in biologia molecolare Espressione eterologa, purificazione e saggio di attività della Fe-idrogenasi di Enterobacter
Università degli studi di Padova - Facoltà di scienze MM.FF.NN. Laurea di primo livello in biologia molecolare Espressione eterologa, purificazione e saggio di attività della Fe-idrogenasi di Enterobacter
Dicroismo circolare e chiralità. Una molecola si dice chirale se non è sovrapponibile alla sua immagine speculare.
 Dicroismo circolare Dicroismo circolare e chiralità Una molecola si dice chirale se non è sovrapponibile alla sua immagine speculare. Dicroismo circolare e chiralità Le molecole chirali assorbono in
Dicroismo circolare Dicroismo circolare e chiralità Una molecola si dice chirale se non è sovrapponibile alla sua immagine speculare. Dicroismo circolare e chiralità Le molecole chirali assorbono in
proteine enzimi RNA ribozimi substrati altamente specifici -asi
 I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
Sommario. Capitolo 1 La struttura della materia: miscugli e sostanze. Capitolo 2 Dalle sostanze all atomo
 Introduzione La Chimica e il metodo scientifico 1. La Chimica pag. 9 2. Il metodo scientifico pag. 10 3. Grandezze fondamentali e grandezze derivate pag. 11 3.1 Il Sistema Internazionale di unità di misura
Introduzione La Chimica e il metodo scientifico 1. La Chimica pag. 9 2. Il metodo scientifico pag. 10 3. Grandezze fondamentali e grandezze derivate pag. 11 3.1 Il Sistema Internazionale di unità di misura
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TRATTAMENTO DELL ACQUA DI LABORATORIO. sostanza più frequentemente adoperata in laboratorio.
 TRATTAMENTO DELL ACQUA DI LABORATORIO 15.10.17 sostanza più frequentemente adoperata in laboratorio. serve a molte cose solvente per preparare soluzioni, diluire, cristallizzare, lavare, raffreddare,..
TRATTAMENTO DELL ACQUA DI LABORATORIO 15.10.17 sostanza più frequentemente adoperata in laboratorio. serve a molte cose solvente per preparare soluzioni, diluire, cristallizzare, lavare, raffreddare,..
Never impure protein PURIFICAZIONE DI PROTEINE
 Never waste pure thoughts on an impure protein PURIFICAZIONE DI PROTEINE PURIFICARE Purificare significa ottenere solamente la nostra molecola di interesse. Purificare una proteina per: Determinarne la
Never waste pure thoughts on an impure protein PURIFICAZIONE DI PROTEINE PURIFICARE Purificare significa ottenere solamente la nostra molecola di interesse. Purificare una proteina per: Determinarne la
Chimica generale e inorganica Studia gli elementi e i composti inorganici
 Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
Corso di Laurea triennale in Biotecnologie Piano farmaceutico
 Università degli Studi di Padova Dipartimento di Scienze del Farmaco Corso di Laurea triennale in Biotecnologie Piano farmaceutico 7 aprile 2017 Edificio Botta AULA F, I PIANO AA 2017-2018 Patrizia Polverino
Università degli Studi di Padova Dipartimento di Scienze del Farmaco Corso di Laurea triennale in Biotecnologie Piano farmaceutico 7 aprile 2017 Edificio Botta AULA F, I PIANO AA 2017-2018 Patrizia Polverino
