Corso di Laurea in CHIMICA (L.T.) Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule
|
|
|
- Norberto Ceccarelli
- 4 anni fa
- Visualizzazioni
Transcript
1 orso di Laurea in IMIA (L.T.) IMIA RGAIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMII ED ARGMETI DA SERE PER L SVLGIMET DEGLI ESERIZI DI QUEST FGLI: Struttura elettronica. Forma tridimensionale delle molecole. arbonio tetraedrico. Angoli di legame e lunghezza di legame. Legame ionico e covalente. rbitali atomici e molecolari. rbitali atomici ibridati: sp, sp2, sp. Legami σ e π. Elettronegatività. Polarità dei legami covalenti non simmetrici. Momento dipolare di molecole. Legame idrogeno. Attrazioni intermolecolari e legami di Van der Waals. Struttura e proprietà fisiche. Modi di scrivere le formule: formule di Lewis, di Kekulé (o a legame di valenza), formule condensate, formule a linea di legame legami a cuneo e tratteggiati. Formula empirica e formula molecolare. Ione molecolare. arica formale. Risonanza. Radiazione elettromagnetica. Spettri uv-vis. Spettri IR. 1. Dare una definizione a parole (e con disegni, se necessario) dei seguenti termini: orbitale atomico s, legame covalente, orbitale ibrido sp, orbitale molecolare, legame σ, lunghezza di legame, carbonio tetraedrico, legame covalente polare, orbitale ibrido sp2, orbitale ibrido sp, legame π, legame idrogeno, legame delocalizzato, risonanza. 2. a) Individuare gli otto elettroni leganti associati all'atomo di carbonio in ciascuna delle seguenti strutture: ::.... :: :::::: ::::: :: b) elle strutture precedenti assegnare gli elettroni associati a ciascun atomo di e gli otto elettroni associati a ciascun atomo di ossigeno e di azoto.. Scrivere le strutture dei seguenti composti, usando un trattino per ogni coppia di elettroni costituenti un legame e due puntini per ogni coppia di elettroni non impegnata in legame: Br F acido solfidrico ( 2 S) acqua ammoniaca fosfina (P ) cloroformio (l ). 4. Scrivere le strutture di Lewis dei seguenti composti, tenendo conto che tutti gli atomi diversi da hanno l'ottetto completo:, S, F,, Br 4, S 4=, -, -, +,, (disposizione degli atomi ), + 2 (disposizione degli atomi ). 5. iascuna delle seguenti strutture contiene un doppio o un triplo legame. Scrivere le formule di Lewis e di Kekulé (a legame di valenza) corrispondenti:
2 , l 2, 2 l 4, 2 2, 2 4, 2 6. alcolare la carica formale su ciascun atomo (tranne l'atomo di idrogeno) nelle seguenti strutture, indicando la carica effettiva di ogni specie:.. Ṅ : : =: : :.. : : Ȯ : :.... :.. : : : : S l.. : S.. :.... : :.. : :.. : 7. Scrivere le formule a legame di valenza (di Kekulé) per ciascuna delle seguenti formule di Lewis: ::::: :::: :::.... :::: 8. Scrivere le coppie di elettroni di valenza non condivise (se ce n'è) in ciascuna delle seguenti formule:, (, ( +,, (, 2 = 2, 2 =, l, 2, 9. Scrivere le formule di Lewis per ciascuna delle seguenti strutture di Kekulé e condensate: 10. Scrivere le formule di Lewis e le corrispondenti formule di Kekulé (a legame di valenza) dei seguenti composti organici, scritti con le formule condensate: 2 2 l( 2 -, 2 +, 2., = 2, 2,,, -, 2 +, 2 =Br,,, (, ( ) Scrivere la formula strutturale completa, usando un trattino per ogni legame, per ciascuna delle seguenti formule condensate, facendo attenzione, perché i legami multipli non sono indicati: ( Br, ( (, ( ( ) 12. Scrivere la formula strutturale completa per ciascuno dei seguenti composti, facendo attenzione, perché ogni struttura contiene almeno un doppio od un triplo legame che non è mostrato (usare le regole di valenza per trovarli): 2 ==,, 2, 2, 2 1. Dire se le seguenti strutture rappresentano lo stesso composto o composti diversi (spiegare):
3 Br Br Br Br 14. Indicare l'ibridazione di ciascun atomo di carbonio nelle seguenti strutture: (, 2, 2, 2,, Br Br 15. Per ciascuna delle seguenti strutture dire se le coppie di atomi di carbonio indicate giacciono o no sullo stesso piano: Dire il valore degli angoli di legame indicati nelle seguenti strutture: Dire, in ciascuna delle seguenti coppie, se è più corto il legame (1) o (2): l 2 l L'angolo di legame -- nella anidride carbonica ( 2 ) è 180. Scrivere la struttura di Lewis e dire quale è l'ibridazione dell'atomo di carbonio. 19. Quanto è l'angolo di legame -- del metano [ 4 ]? Quanto vi aspettate sia l'angolo di legame -- e -- rispettivamente dell'acqua e dell'ammoniaca, confrontati con l'angolo - - del metano? Quanto vi aspettate sia l'angolo di legame l--l nel tetracloruro di carbonio [l 4 ]? E l'angolo di legame -- nello ione 4 +? 20. Quali sono gli orbitali atomici che contengono gli elettroni leganti del carbonio? Disegnare un atomo di carbonio con due orbitali p non ibridi: quali orbitali ibridi sono presenti su questo atomo di carbonio? 21. Quale elemento è il più elettronegativo in ciascuna delle seguenti serie? a),, b),, c),, Mg d), l, e),, F. 22. Tra i seguenti composti, quali hanno un legame ionico e quali solo legami covalenti? 2 a, I, Li, a,, 2 S, Mg()Br, l he cosa potete dire sul punto di fusione dei composti con un legame ionico rispetto a quelli con solo legami covalenti? 2. Indicare l'elemento più elettronegativo in ciascuna delle seguenti strutture e mostrare la direzione di polarizzazione dei suoi legami:,, F 2 (), ( 2 2 Quali segnali di stretching (stiramento) vi aspettate nello spettro IR per ciascuno di questi composti?
4 24. Indicare le estremità positive e negative del dipolo dei seguenti legami: -Mg -Br - - l - -B. 25. Sistemare i seguenti composti in ordine di polarità crescente: 2 2, 2, 2 2, 2 2 Br, 2 2 I, 2 2 l Quali segnali di stretching (stiramento) vi aspettate nello spettro IR per ciascuno di questi composti? 26. Sistemare i seguenti composti in ordine di carattere ionico crescente: 4, Br, Lil. 27. Quale è il composto più polare in ciascuna delle seguenti coppie? Spiegare. a) 2 e b) e 2 l c) e ( 28. a) Predire la direzione del dipolo (se c'è) nelle seguenti molecole: F, l 2, Il, 2 b) hi tra i seguenti composti ha momento dipolare e perché?: Br 4, 2 2, l, 4 +, BF a) Indicare la polarità dei legami in ciascuna delle seguenti strutture: (a) l l (b) (c) Vi aspettate che i composti (a) e (c) abbiano momento dipolare? Spiegare. b) Quali assorbimenti nell infrarosso vi aspettate? 0. Quale dei seguenti composti può formare legami idrogeno con altre molecole della stessa specie?: ( Scrivere le strutture di legame idrogeno (se c'è) che vi aspettate per i seguenti composti: F ( 2. Quale dei seguenti composti può formare legame idrogeno con se stesso? e con l'acqua?: 2 2 (. a) Mostrare tutti i tipi di legame idrogeno in una soluzione acquosa di (. Quale è il più forte? b) Indicare il legame idrogeno tra due molecole di metanolo ( ) e quello tra una molecola di metanolo ed una di acqua. 4. Se si prova a sciogliere in acqua: cloroformio [l ], metanolo [ ] e tetracloruro di carbonio [l 4 ], quale pensate si sciolga meglio? Perché? E' possibile sciogliere acqua in tetracloruro di carbonio? Perché? 5. Disporre i seguenti composti secondo l'ordine di solubilità crescente in acqua, dal meno solubile al più solubile. Spiegare. 2,, L'etere dietilico, 2 2, e l'1-butanolo, 2 2 2, sono ugualmente solubili in acqua, ma il punto di ebollizione dell'1-butanolo è di 8 più alto di quello dell'etere dietilico. he spiegazione si può dare a questa osservazione sperimentale?
5 7. Indicare, per ciascuna delle seguenti coppie di strutture, quale coppia costituisce strutture di risonanza: a) e b) e c) 2 2 =- d ) e e) e - = 2 = 2 -== + e + 2 = 8. alcolare l energia associata alle seguenti frequenze, lunghezze d onda o numeri d onda: a) ν = 2 x 10 8 z b) λ = 254 nm (2.54 x 10-9 m) c) λ = 1.0 cm d) ν = 2600 cm -1 e) ν = 4.1 x z f) ν = 2 x 10 8 m Una molecola è costituita da atomi di, e. L analisi elementare ha dato: % = 40, % = 1,. a) Determinare la formula empirica. b) Sapendo che lo spettro di massa presenta un valore m/z = 60, determinare la formula molecolare.
6 IMIA RGAIA I orso di laurea in IMIA Esercitazione n. 2 - omenclatura (I) TERMII ED ARGMETI PER L SVLGIMET DEGLI ESERIZI DI QUEST FGLI: Idrocarburi. Alcani. omenclatura sistematica IUPA. Isomeri strutturali. Gruppi alchilici. arbonio primario, secondario, terziario. icloalcani. : Alcheni ed alchini vinile, allile. Alcadieni. icloalcheni e cicloalcadieni. Idrocarburi aromatici e derivati fenile, fenilene, benzile. Idrocarburi biciclici. Idrocarburi spiro. Alogenuri alchilici ed arilici. itroderivati. Alcooli e fenoli. Dioli e polioli. Tioli. Eteri e solfuri. Ammine (primarie, secondarie, terziarie) ammine aromatiche. Sali di ammonio, ossonio, solfonio. Sali di diazonio. Solfossidi, solfoni, acidi solfonici. 1. Dire quale coppia tra le seguenti rappresenta due idrocarburi isomeri: a) 2 6 e 2 5 b) 5 12 e 5 10 c) 4 10 e 7 2. Quando si scrive una formula strutturale come quella sotto, gli atomi sono tutti sullo stesso piano? Spiegare.. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) e b) e l c) e l l l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano un idrocarburo lineare? a) b) c) d) e) f) g) h) 5. Indicare se ciascuna delle seguenti coppie di scheletri di atomi di carbonio rappresenta o no lo stesso composto: l l a) e b) l e l c) e l l
7 d) e e) e f) l e l g) e 6. Dare la formula molecolare di: etano, propano, butano e pentano. Scrivere la formula strutturale per ciascuna di queste molecole, mostrando tutti i legami - e - e scrivere le formule condensate corrispondenti. 7. Dare la formula molecolare di: esano, ottano e decano. Scrivere per ciascuno di questi composti le strutture condensate e quelle a linea di legame. 8. Scrivere le strutture dei cinque isomeri di formula molecolare Quanti gruppi metile ha ciascun isomero? Quali sono i nomi corrispondenti, secondo la nomenclatura IUPA? 9. Quali delle seguenti formule rappresenta correttamente il gruppo isobutile? Perché le altre non vanno bene? E' corretto chiamare metilbutano il composto di formula condensata (? E chianare metilpentano il composto di formula ( 2? 11. Scrivere per ciascuno dei seguenti nomi la formula (condensata e a linea di legame) corrispondente: 2,2-Dimetilpentano 4-etil-2-metilesano 2,4-dimetilesano -etil-4-metilpentano -etil-4-propilottano 2,-dimetil-4-propilottano 4-isopropileptano,-dimetilpentano, 4-etil-2,2-dimetildecano 2,4,7-trimetildecano 4-isopropil-2,-dimetilottano 2,2,6,6-tetrametil-4-terzbutilnonano 2-metiltridecano eicosano -metil-4-(1-metilpropil)ottano -metil-5-(2- metilpropil)nonano -etil-5-sec-butilnonano -metil-5-isobutilnonano. Metilcicloesano etilciclopentano 1-isopropil-1-metilciclobutano 1-metil-2-propilciclopentano 1,1-dimetilcicloesano. 12. Scrivere per ogni formula il nome corrispondente, secondo la nomenclatura IUPA: ( 2 5 )( ( 2 ( 2 5 ) ( 2 ) 4 ( 2 ( 2 ( ( 2 ( 2 5 ( 2 ( 2 ( 2 ( 2 ( )( 2 2 )( (
8 ( ( Per il composto di formula 2 2 ( )( 2 )( 2, quale tra i seguenti è il nome corretto? In che cosa sono sbagliati gli altri? (a) 5,6-dietil-4-metilottano (b),4-etil-5-metilottano (c,4-dietil-5-metilottano (d) 5-metil-,4-dietilottano. 14. Secondo la nomenclatura IUPA, i seguenti nomi sono sbagliati. Stabilire quale regola (o quali regole) è stata violata e dare il nome IUPA corretto. a) 1,1-dimetilbutano [per ( 2 2 ] b) isopentano [per ( ) 4 ] c) dimetilesano [per ( d) metilpentano e-isobutil-4-metilesano f-etileptano. 15. a) Quanti diversi tipi di idrogeno ci sono in ciascuno dei seguenti composti (ad esempio: nel propano ci sono due tipi di idrogeni, i 6 tutti equivalenti tra loro, legati ai primari ed i 2, equivalenti tra loro, legati al secondario): metilbutano 2-metilpentano -metilpentano esano 2,-dimetilbutano 2,2-dimetilbutano. b) Quanti diversi isomeri strutturali si possono formare per sostituzione di un atomo di idrogeno con un metile in ciascuno dei composti precedenti? (i saranno tanti isomeri strutturali quanti sono i tipi di non equivalenti. Per esempio dal propano si possono formare due soli isomeri strutturali, perché ci sono due tipi di ). Dare ad ogni composto il nome IUPA. 16. Scrivere le strutture per i cinque isomeri strutturali di formula molecolare In quali strutture sono presenti atomi di carbonio secondario? In quali sono presenti atomi di carbonio terziario? 17. Scrivere la struttura e dare il nome IUPA di un alcano o cicloalcano che abbia la seguente formula a) 5 12 con atomi di idrogeno primari e secondari b) 5 12 con solo atomi di idrogeno primari c) 5 12 con un atomo di idrogeno terziario d) 5 10 con solo atomi di idrogeno secondari. 18. Quanti dimetilciclobutani isomeri strutturali ci sono? Quanti dimetilciclopropani? 19. Scrivere la struttura dei nove possibili eptani ed assegnarne i nomi, secondo la nomenclatura sistematica (IUPA). 20. Scrivere per ciascuno dei seguenti nomi la formula (condensata e a linea di legame) corrispondente: Propene isobutene metilpropene 2,-dimetil-2-pentene -eptene -ottino, 1-ottino 2-metil-- ottino 2,2-dimetil--esino 2-undecene 4-tridecene -decino -ciclopentil-1-butino -terzbutil-2-esene 1,4-pentadiene 1,-pentadiene butadiene butenino 1-metilciclobutene -metilciclopentene cicloottene cicloesene,-dimetilcicloesene metilideneciclopentano metileneciclopentano 2-propenilcicloesano allilcicloesano 1-propenilcicloesano propiliden-
9 cicloesano ciclopentadiene 1,-cicloesadiene 1,4-cicloesadiene ciclopropilcicloesano - metilcicloesene 2-etil--metilcicloesene. Benzene toluene (=metilbenzene) m-xilene (=m-dimetilbenzene) 1,,5-trimetilbenzene bifenile trifenilmetano difenilmetano naftalene fenantrene 1-etil--metilbenzene 1- metilnaftalene α-metilnaftalene β-etilnaftalene 2-etilnaftalene 1,8-dimetilnaftalene 2,2'- dimetilbifenile. Biciclo[2.2.1]eptano biciclo[2.2.2]ottano 2-metilbiciclo[5.2.0]nonano biciclo[.2.2]-2-nonene -metilbiciclo[4.4.0]decano spiro-[.4]-ottano spiro[4.5]1,6-decadiene. 21. Scrivere per ogni formula il nome corrispondente, secondo la nomenclatura IUPA: ( = 2 2 = = 2 ( =( 2 2 ( )= 2 =( )= 2 2 ( )= 2 =( == === ( 2 2 ( 2 ) ( ( 22. iascuno dei seguenti composti è stato chiamato in modo improprio, secondo la nomenclatura IUPA. Indicare l'errore e dare il nome corretto. a-etil-2-pentene c-etil-2-ottene d,2- dimetil-4-pentene e) 1-etil-6-metilbenzene f-metil-4-propilbenzene g) 1-metil--metilbenzene h) 4-metil-4-etil-1-butene i) fenilmetano. 2. a) Quanti isomeri strutturali esistono di formula 5 10 con un doppio legame carboniocarbonio? b) Quanti isomeri strutturali con un triplo legame carbonio-carbonio hanno formula molecolare 5 8? c) Quanti alcadieni (attenzione: niente alleni!) hanno formula molecolare 5 8? Dare a tutti gli isomeri il nome, secondo la nomenclatura IUPA. 24. Quanti trimetilbenzeni ci sono? Scrivere le formule e dare i nomi IUPA. Quale di questi dà un solo monoetilderivato? Quale ne dà due? Quale tre? 25. Quale è il nome sistematico (IUPA) corretto per il composto di formula 2 =( 2 : vinilpentano, -vinilpentano, -etil-1-pentene?
10 TERMII ED ARGMETI PER L SVLGIMET DEGLI ESERIZI DI QUEST FGLI: omenclatura sistematica IUPA: Alogenuri alchilici ed arilici. itroderivati. Alcooli e fenoli. Dioli e polioli. Tioli. Eteri e solfuri. Ammine (primarie, secondarie, terziarie) ammine aromatiche. Sali di ammonio, ossonio, solfonio. Sali di diazonio. Solfossidi, solfoni, acidi solfonici. 26.Scrivere per ciascuno dei seguenti nomi la formula (condensata e a linea di legame) corrispondente: loruro di isobutile bromociclopentano 1,-dibromocicloesano 2-iodoeptano 1,1,1- tricloroetano 1,1,2-tricloroetano cloroformio tetracloruro di carbonio iodoformio cloruro di metilene diclorometano,,-tricloropropene 4-cloro-1-pentino bromuro di vinile 1,2- dibromoetene ioduro di allile bromuro di vinile cloruro di benzile 2-bromonaftalene p- clorometilbenzene, p-diclorobenzene bromuro di benzile. itroetano 2-nitrobutano 1-nitrobutano nitrobenzene o-metilnitrobenzene 9-nitroantracene. Metanolo etanolo 2-pentanolo alcool sec-butilico alcool terz-butilico cicloesanolo 1- metilcicloesanolo 2-metilcicloesanolo -cloro-5-etilcicloesanolo 2-propanolo alcool isopropilico alcool 2-feniletilico alcool benzilico benzenolo fenolo p-metilbenzenolo p- metilfenolo 4-metilbenzenolo -bromobenzenolo m-bromofenolo. Etantiolo 1-butantiolo 2-butantiolo benzentiolo tiofenolo. 2,-Butandiolo 1,2-propandiolo 1,-ciclopentandiolo 1,4-butanditiolo. Dietil etere isopropil metil etere etil propil solfuro anisolo (= fenil metil etere) metossibenzene propilossibenzene benzil etil etere -isopropilossiottano 4-metiltiononano ossaciclopropano 2- metilossaciclobutano. Etanammina 1-butanammina 2-butanammina cicloesanammina metilpropilammina - ammino-2-butanolo ciclopentilisopropilammina isopropildipropilammina benzenammina anilina 1-amminonaftalene 4-nitrobenzenammina p-nitroanilina 1,4-diamminobutano 1,2- diamminoetano etilendiammina,-dimetilanilina difenil ammina 1,4-diamminobenzene p- fenilendiammina 9-amminofenantrene 4-amminobifenile azacicloesano 1,4-diazacicloesano azaciclopentano. loruro di tetrabutilammonio idrossido di etilmetildipropilammonio bromuro di trietilossonio cloruro di cicloesiltrimetilammonio cloruro di etildimetilsolfonio bromuro di alliltrimetilammonio cloruro di trietilvinilammonio ioduro di dibenzilfenilsolfonio. loruro di benzendiazonio cloruro di p-clorobenzendiazonio. Dimetil solfossido etil metil solfossido dietil solfone benzil propil solfone acido metansolfonico acido benzensolfonico acido 1-butansolfonico acido 2-butansolfonico acido 1- metilpropan-solfonico acido p-toluensolfonico acido p-metilbenzensolfonico. 27. Scrivere per ogni formula il nome corrispondente, secondo la nomenclatura IUPA:
11 ( =Br l= 2 l 2 ( )Br ( F 2 I Br 4 l 2 2 Br( )= 2 l ( ( ( 2 2 S 2 2 ( ( )( ( 2 ( ) + ( + ( 2 ) Br - S + I - 2 ( ) ( 2 l - + ( 2 ( Br - S 2 ( ( 2 2 S l l Br 2 Br S S S 28. iascuno dei seguenti composti è stato chiamato in modo improprio, secondo la nomenclatura IUPA. Indicare l'errore e dare il nome corretto. a) 1-cloro-2-propene b) 1-cloro--etil-2-metil- 5-esene c) 4-bromo-4,5-dicloro-6-etileptene. 29. Scrivere tutti gli alcooli contenenti tre e quattro atomi di carbonio, specificando quali sono primari, quali secondari e quali terziari e dando a tutti il nome IUPA. 0. Scrivere le strutture dei seguenti alcooli, specificando per ognuno se è primario, secondario o terziario: etanolo alcool isopropilico ciclopentanolo alcool isobutilico dimetilpropanolo 1- metilcicloesanolo. 1. Scrivere le strutture di tre eteri isomeri di formula molecolare 4 10 e dare i nomi, secondo la nomenclatura IUPA. b) Qui di seguito sono riportati gli spettri 1 MR di due di questi eteri. Quali sono? Perché? ome vi aspettate sia lo spettro 1 del etere mancante?
12 2. Usando cinque atomi di carbonio ed il numero necessario di atomi di idrogeno e di altri elementi, scrivere le strutture dei seguenti composti: a) un alcool primario a catena aperta b) un alcool secondario a catena aperta c) un alcool terziario a catena aperta d) un alcool terziario ciclico e) un alcool secondario ciclico f) un composto ciclico che sia anche un alcool primario.. (a) Scrivere la struttura dell'etere isomero strutturale dei due propanoli. (b) Scrivere gli otto alcooli ed i sei eteri di formula molecolare i sono quattro diclorocicloesani isomeri strutturali, di formula 6 10 l 2. Scriverne la struttura ed assegnarne il nome, secondo la nomenclatura IUPA. 5. Scrivere le formule e dare i nomi agli isomeri strutturali dei seguenti composti: a) triclorobenzeni b) dibromonitrobenzeni c) diclorotolueni (= diclorometilbenzeni) d) monocloronaftaleni e) clorodinitrobenzeni f) metilbenzenoli g) dinitronaftaleni. 6. Quanti trimetilbenzeni ci sono? Quale di questi dà un solo mononitroderivato? Quale ne dà due? Quale tre? 7. Quale è il nome sistematico corretto per il composto di struttura 2 =( l: 1- cloro-2-metil-2-propene, clorometilpropene, -cloro-2-metilpropene? 8. I derivati fluorurati degli idrocarburi sono largamente usati nei sistemi frigoriferi e nelle bombolette spray aerosol. Sono correntemente conosciuti con nomi che sono marchi di fabbrica, come ad esempio Freon. elle bombolette aerosol si usa il diclorodifluorometano (scrivere la formula), che va sotto il nome di alocarbon-12. L'alocarbon-114 è il liquido frigorifero più usato nei frigoriferi domestici ed ha formula F 2 lf 2 l: che nome sistematico (IUPA) gli dareste? 9. Scrivere la formula del 2,2,2-trifluoroetil vinil etere, un anestetico per inalazione, noto come Fluoromar, che addormenta un paziente in 0-60 secondi e rende possibili risvegli accompagnati da una sensazione di nausea minore che con altri anestetici. 40. Il tritolo è tuttora il più importante degli esplosivi di uso militare. Fonde a 81, ma non esplode fino a 280. E' perciò possibile fonderlo e versarlo ancora liquido nei contenitori. Scriverne la struttura, sapendo che il suo nome è 2,4,6-trinitrotoluene.
13 IMIA RGAIA I orso di laurea in IMIA Esercitazione n. - omenclatura (II) TERMII ED ARGMETI PER L SVLGIMET DEGLI ESERIZI DI QUEST FGLI: omenclatura sistematica IUPA. Aldeidi e chetoni gruppo carbonile. Acidi carbossilici gruppo acile. Derivati degli acidi carbossilici: alogenuri acilici, ammidi (solfonammidi), esteri (solfonati), anidridi (immidi), nitrili. Derivati dell acido carbonico. omposti polifunzionali. 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o quando appropriato), specificandone la desinenza caratteristica (se c'è). Se quello indicato non fosse il gruppo funzionale principale, indicare il prefisso con cui si indica. a) b) c) d) Br e) f) ( g) h) i) j) k) l) m) ( ) 4 + n) o) S 2 + p) q) S l 2. iascuna delle seguenti strutture è polifunzionale. Indicare in ciascun caso il gruppo funzionale principale, specificandone la desinenza caratteristica. Indicare il prefisso con cui si indica in questo caso l'altro gruppo funzionale.
14 a) b) 2 c) d) e) f). Scrivere per ciascuno dei seguenti nomi la formula (condensata e a linea di legame) corrispondente: Pentanale aldeide -metilbutanoica -butenale ciclopentancarbaldeide benzencarbaldeide, aldeide benzoica benzaldeide o-idrossibenzaldeide 2-idrossibenzencarbaldeide acetone propanone dimetil chetone butanone isopropil sec-butil chetone 2,4-dimetil--esanone acetofenone fenil metil chetone feniletanone benzofenone (= difenil chetone) difeniletanone 2,4-pentandione cicloesanone 1,-cicloesandione ciclopropenone. 2-Idrossipentanale m-amminobenzaldeide -amminoesanale 4-allil-2-metossifenolo. 4. Scrivere per ogni formula il nome corrispondente, secondo la nomenclatura IUPA: 2 = ( 2 = Secondo la nomenclatura IUPA, i seguenti nomi sono sbagliati. Stabilire quale regola (o quali regole) è stata violata e dare il nome IUPA corretto. a) butanolo (b) idrossietano (c- mercaptopropano (d-idrossietilammina. 6. Dare i nomi IUPA ai sette composti carbonilici (aldeidi e chetoni) di formula Due aldeidi che si trovano in natura sono il tetradecanale, usato dal batterio luminescente Achrobacter fisceri nel processo di produzione della luce, ed il citronellale (nome sistematico:,7-dimetil-6-ottenale), che fa parte del sistema chimico di allarme delle formiche. Scrivere le formule di queste aldeidi. 8. a) Scrivere la struttura della vaniglina, il costituente odoroso principale dei baccelli di vaniglia, sapendo che il nome IUPA è 4-idrossi--metossibenzaldeide. 9. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale specificandone la desinenza caratteristica. Scrivere per ogni gruppo funzionale il prefisso da usare quando serve chuiamarlo come sostituente.
15 a) 2 b) l c) d) e) f) ( 10. iascuna delle seguenti strutture è polifunzionale. Indicare in ciascun caso il gruppo funzionale principale, specificandone la desinenza caratteristica. Indicare il prefisso con cui si indica in questo caso l'altro gruppo funzionale. Br a) b) c) d) g) e) f) 2 g) 11. Scrivere per ciascuno dei seguenti nomi la formula (condensata e a linea di legame) corrispondente: Acido acetico acido etanoico acido α-metilbutanoico acido -metilpentanoico acido benzencarbossilico acido benzoico acido ciclopentancarbossilico acido malonico (= ac. propandioico) acido ossalico (= ac. etandioico) acido p-toluico (= ac. p-metilbenzoico) acido -cloroeptanoico acido 2-butenoico acido esanoico acido -esenoico cloruro di butanoile bromuro di etanoile cloruro di benzoile bromuro di -cloropentanoile acetato di fenile ciclobutancarbossilato di metile benzoato di etile etanoato di benzile propenoato di isopropile ossalato (v. sopra ac. ossalico) dietilico malonato ( v. sopra ac. malonico) dietilico malonato acido di etile (più corretto: acido etossicarboniletanoico) p-nitrobenzoato di metile, pentanoato di isobutile 1,-diacetossicicloesano, 1,-diacetilcicloesano, acido -acetil-2- bromopentan-dioico anidride acetica anidride etanoica anidride metanoica anidride benzencarbossilica anidride benzoica, anidride pentanoica anidride fenilacetica anidride butandioica anidride 2-butenoica, anidride butendioica anidride 1,2-benzendicarbossilica anidride 1,2-naftalendicar-bossilica esanammide benzenammide benzammide m- bromobenzenammide -etilpentanam-mide 2-pentenammide acetonitrile etanonitrile benzenenitrile benzonitrile esanonitrile, p-ni-trobenzonitrile. iclopentansolfonato di metile -metilmetansolfonammide pentanimmide carbonato dietilico -cicloesilurea, -dicicloesilurea,-dicicloesilurea. Acido -formilpentanoico acido acetoacetico (= ac. -ossobutanoico) acido -idrossibutanoico acido o-metossibenzoico acido 2-amminopropanoico acido 2-ammino--(p-idrossifenil)propanoico acido -bromoformilpropanoico acido -bromocarbonilpropanoico acido - bromo--formilpropanoico acido -propilossicarbonilcicloesancarbossilico acido 4-butanoilossicarbonilcicloesancarbossilico acido 4-cianobenzencarbossilico. Acido -cloroformilpropanoico (= acido -clorocarbonilpropanoico) acido -formilbutanoico acido carbammoiletanoico, acido -etossicarbonilbenzoico. 12. Scrivere per ogni formula il nome corrispondente, secondo la nomenclatura IUPA:
16 ( 2 l ( 2 2 Br ( = Br l l S S Br S 1. Scrivere gli esteri isomeri di formula molecolare Scrivere le ammidi isomere di formula molecolare a) Dare il nome IUPA all'acido malico, 2 2 (, contenuto nelle mele. 16. onsiderando la struttura dell acido carbonico, provate a scrivere le formule dei seguenti composti: a) clorocarbonato di etile b) bromocarbonato di terz-butile.
17 26/02/201 Di seguito sono elencate alcune molecole biologicamente attive o di importanza industriale. Individuare il gruppo funzionale (o i gruppi funzionali) e, quando possibile, provate a darne il nome. a) b) omponente principale del feromone delle api è prodotto anche da una specie di orchidee ( Dendrobium sinense ), che se ne serve per ingannare i calabroni e farsi impollinare. Tyrosol Anestetico e sedativo intravenoso, è il farmaco che ha ucciso Michael Jackson. Propofolo c) Antiossidante. Si trova nell olio di oliva, contribuisce ad inibire l effetto del colesterolo. d) Antisettico e antifungo topico a base di mercurio. - a + S g Thimerosal e) Piriproxifene Insetticida, si usa contro le formiche si mette sul terreno sopra un esca: le formiche operaie lo portano nel formicaio, dove uccide tutte le formiche, regina compresa. f) 2 Pafurammidina E stata usata contro la tripanosomiasi Africana umana (malattia del sonno), ma nel 2008 è stata ritirata perché tossica per il fegato e provoca insufficienza renale. Attualmente è in sperimentazione clinica contro la polmonite pneumocistica, dove sembra efficace senza effetti collaterali. 1
18 26/02/201 g) 2 Spermina Spermidina 2 La spermina viene biosintetizzata dalla spermina, che a sua volta deriva dalla putre-scina. Anton van Leeuwenhoek, il pioniere della microscopia, ha descritto cristalli di spermina nel seme umano nel onostante il nome, entrambe le poliammine si trovano dappertutto negli organismi ed hanno numerose attività biologiche. h) + Sanguinarina Antimicrobico, è usato in dentifrici e colluttori, per prevenire le gengiviti protegge contro il cancro della pelle, aumentando la produzione di proteine che inducono la morte delle cellule malate. i) + 2- S 4 Efedrina 2 Broncodilatatore e stimolante, è stato bandito dalle limpiadi j) l - + S Blu di metilene E uno dei coloranti organici più vecchi: preparato nel 1876 e usato per tingere il cotone, dal 1880 è stato usato per colorare le cellule. E usato come fotosensibilizzatore (produzione di ossigeno singoletto) e come farmaco (contro la metemoglobinemia) k) Mescalina Alcaloide allucinogeno, isolato nel 1896 dal cactus peyote Lophophora williamsii, è usato dagli indiani d America da più di 000 anni nelle cerimonie religiose. 2
19 26/02/201 l) 2 Tamoxifen E stato per decenni il farmaco chiave per il trattamento del cancro alla mammella, efficace quando la malattia dipende dall estrogeno. m) Propanololo Beta-bloccante non selettivo, è usato soprattutto contro la pressione alta, l angina pectoris ed altri problemi cardiocircolatori. n) Guaiafensina espettorante (negli sciroppi come Robitussin ) o) Dopammina neurotrasmettitore, controlla il movimento, la sensibilità al dolore ed al piacere e la risposta emotiva un difetto di dopammina porta a tremore (morbo di Parkinson), un eccesso a schizofrenia p) p) odeina Alcaloide policiclico, si trova nel papavero da oppio è utilizzata nei medicinali contro la tosse e per trattare la diarrea. q) Guaiacolo espettorante, antisettico, anestetico locale
20 26/02/201 r) Kaempferolo Si trova nel pompelmo, nel tè, nei broccoli e nelle mele sembra diminuisca il rischio di cancro al pancreas ed ai polmoni s) urcumina pigmento giallo della curcuma, protegge lo stomaco dai cibi guasti. Inibisce la crescita di elicobacter pylori (implicato nella gastrite e nel cancro dello stomaco) t) Bupropion l antidepressivo coadiuvante per smettere di fumare u) Warfarina Anticoagulante. Identificato nel fieno marcio che provocava emorragia nel bestiame (anni 0), è stato poi usato come rodenticida (anni 40) e successivamente per prevenire trombosi ed embolia nell uomo (oumadin ) v) Acido Betulinico Si trova nella corteccia delle betulle è particolarmente utile contro il melanoma 4
21 26/02/201 w) Dolasetron (Anzement ) antiemetico (nelle chemioterapie) x) Lisinopril farmaco per trattare ipertensione e infarto e per prevenire le complicazioni renali e della retina causate dal diabete y) Theanina Si trova nelle foglie di tè e nel fungo Boletus badius. Sembra che aumenti la concentrazione mentale e viene aggiunto in bevande del tipo Gatorade. z) Platensimicina Antibiotico naturale, dal batterio Streptomyces platensis potenziale farmaco per il diabete aa) Acido Pantotenico E una vitamina B importante nella demolizione di grassi e carboidrati con produzione di energia ed è determinante nella produzione delle cellule rosse del sangue. 5
22 26/02/201 ab) Acido Jasmonic coronatina Uno degli ormoni che regolano la crescita delle piante, regola anche la risposta allo stress. Però alcuni patogeni delle piante producono un ormone che lo imita, la coronatina, che evita la risposta del sistema immunitario della pianta ac) Fenolftaleina Indicatore chimico, è usato nelle indagini forensi (con 2 2 diventa rosa in presenza di sangue). ad) rlistat Impedisce l assorbimento dei grassi nell intestino, ma ha anche effetti gastrointestinali collaterali. E sotto sperimentazione per accelerare l eliminazione della diossina da individui avvelenati. 6
Corso di Laurea in CHIMICA (L.T.) Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule
 orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
CHIMICA ORGANICA I con Elementi di Laboratorio. Corso di Laurea in CHIMICA, Chimica Applicata, Scienza dei Materiali (L.T.)
 IMIA ORGANIA I con Elementi di Laboratorio orso di Laurea in IMIA, himica Applicata, Scienza dei Materiali (L.T.) Esercitazione n. 2 Nomenclatura (I) TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERIZI
IMIA ORGANIA I con Elementi di Laboratorio orso di Laurea in IMIA, himica Applicata, Scienza dei Materiali (L.T.) Esercitazione n. 2 Nomenclatura (I) TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERIZI
1. Dire quale coppia tra le seguenti rappresenta due idrocarburi isomeri: a) C 2
 orso di laurea in IMIA (L.T.) Esercitazione n. 2 - Nomenclatura (I) IMIA RGANIA I con Elementi di Laboratorio TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Idrocarburi. Alcani. Nomenclatura
orso di laurea in IMIA (L.T.) Esercitazione n. 2 - Nomenclatura (I) IMIA RGANIA I con Elementi di Laboratorio TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Idrocarburi. Alcani. Nomenclatura
26. Scrivere per ciascuno dei seguenti nomi la formula (semicondensata e a linea di legame) corrispondente: Cl Cl (CH 3 CHCH 2 ) 2 CH CH.
 6. Scrivere per ciascuno dei seguenti nomi la formula (semicondensata e a linea di legame) corrispondente: cloruro di isobutile cloro metilpropano ( ) bromociclopentano, dibromocicloesano iodoeptano,,
6. Scrivere per ciascuno dei seguenti nomi la formula (semicondensata e a linea di legame) corrispondente: cloruro di isobutile cloro metilpropano ( ) bromociclopentano, dibromocicloesano iodoeptano,,
1. Dire quale coppia tra le seguenti rappresenta due idrocarburi isomeri: e C 5
 Esercitazione n. 2 Nomenclatura (I) 1. Dire quale coppia tra le seguenti rappresenta due idrocarburi isomeri: a) 2 6 O e 2 5 O; b) 5 12 e 5 10 ; c) 4 10 e 3 7 idrocarburi = composti con solo e 2 6 O 2
Esercitazione n. 2 Nomenclatura (I) 1. Dire quale coppia tra le seguenti rappresenta due idrocarburi isomeri: a) 2 6 O e 2 5 O; b) 5 12 e 5 10 ; c) 4 10 e 3 7 idrocarburi = composti con solo e 2 6 O 2
Esercitazione n. 3 - Nomenclatura (II)
 Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Corso di Laurea in CHIMICA (L.T.) Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule
 orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
3. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola:
 . Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
Esercitazione n. 3 - Nomenclatura (II)
 Esercitazione n. - Nomenclatura (II). iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo, 2 o quando appropriato), specificandone la desinenza
Esercitazione n. - Nomenclatura (II). iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo, 2 o quando appropriato), specificandone la desinenza
Esercitazione n. 3 - Nomenclatura (II)
 Esercitazione n. - omenclatura (II). iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo, o quando appropriato), specificandone la desinenza caratteristica
Esercitazione n. - omenclatura (II). iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo, o quando appropriato), specificandone la desinenza caratteristica
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1
 Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Verifiche dei Capitoli - Tomo C
 Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Ammine N R N R R R-NH 2. Gruppo funzionale: NH 2. Gruppo amminico. Ammine terziarie. Ammine primarie. Ammine secondarie
 Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 H 12 ; b. C 2 H 5 Cl; c. C 4 H 10 O.
 1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 12 ; b. C 2 5 Cl; c. C 4 10. 2. Scrivere la formula di struttura dei seguenti composti: a.
1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 12 ; b. C 2 5 Cl; c. C 4 10. 2. Scrivere la formula di struttura dei seguenti composti: a.
APPENDICE I. Proprietà critiche, fattori acentrici e costanti di Rackett di alcune sostanze. ω Z RA. Pc atm. Sostanza Formula Tc C.
 APPENDICE I Proprietà critiche, fattori acentrici e costanti di ackett di alcune sostanze Sostanza Formula Tc C Pc atm Vc cm 3 /mol ω Z A Normal paraffine Metano CH4-82.6 45.30 99 0.011 0.2892 Etano C2H6
APPENDICE I Proprietà critiche, fattori acentrici e costanti di ackett di alcune sostanze Sostanza Formula Tc C Pc atm Vc cm 3 /mol ω Z A Normal paraffine Metano CH4-82.6 45.30 99 0.011 0.2892 Etano C2H6
Capitolo A1 Chimica organica: un introduzione
 Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
CHIMICA ORGANICA I. Corso di laurea in CHIMICA (L.T.) Esercitazione n. 4 - Esercitazione sulle conformazioni di alcani e cicloesani.
 IMIA ORGANIA I orso di laurea in IMIA (L.T.) Esercitazione n. 4 - Esercitazione sulle conformazioni di alcani e cicloesani. TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERIZI DI QUESTO FOGLIO: Rotazione
IMIA ORGANIA I orso di laurea in IMIA (L.T.) Esercitazione n. 4 - Esercitazione sulle conformazioni di alcani e cicloesani. TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERIZI DI QUESTO FOGLIO: Rotazione
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
La chimica organica. La chimica organica è la chimica dei composti del carbonio.
 La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Idrocarburi Saturi. Alcani
 Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Esercitazione n Reazioni e meccanismi di acidi carbossilici e derivati.
 Esercitazione n. 16 Reazioni e meccanismi di acidi carbossilici e derivati. 1. Scrivere i prodotti (specificandone il nome) che si ottengono quando l'acido butanoico viene fatto reagire con ciascuno dei
Esercitazione n. 16 Reazioni e meccanismi di acidi carbossilici e derivati. 1. Scrivere i prodotti (specificandone il nome) che si ottengono quando l'acido butanoico viene fatto reagire con ciascuno dei
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Soluzioni degli esercizi di fine capitolo
 SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Chimica organica: i derivati degli idrocarburi Capitolo C3
 himica organica: i derivati degli idrocarburi apitolo 3 VERIFIA LE TUE NSENZE 1 A 2 B 3 4 D 5 A 6 D 7 8 A 9 B 10 A 11 D 12 B 13 14 15 B 16 B 17 A 18 D 19 20 B 21 D 22 23 B 24 B 25 A 26 D 27 B 28 29 A 30
himica organica: i derivati degli idrocarburi apitolo 3 VERIFIA LE TUE NSENZE 1 A 2 B 3 4 D 5 A 6 D 7 8 A 9 B 10 A 11 D 12 B 13 14 15 B 16 B 17 A 18 D 19 20 B 21 D 22 23 B 24 B 25 A 26 D 27 B 28 29 A 30
ALCANI metano. etano. pentano. butano. propano. Idrocarburo: molecola contenente solo carbonio ed idrogeno
 ALCANI Idrocarburo: molecola contenente solo carbonio ed idrogeno Idrocarburo saturo: molecola contenente solo legami semplici carbonio-carbonio Alcano: Idrocarburo saturo contenente solo catene aperte
ALCANI Idrocarburo: molecola contenente solo carbonio ed idrogeno Idrocarburo saturo: molecola contenente solo legami semplici carbonio-carbonio Alcano: Idrocarburo saturo contenente solo catene aperte
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
IDROCARBURI. Alcani Alcheni Alchini Areni. Tipo di legami carboniocarbonio. Solo legami semplici. Uno o più tripli legami. Uno o più doppi legami
 IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
CHIMICA ORGANICA I con Elementi di Laboratorio. Corso di Laurea in CHIMICA, Chimica Applicata, Scienza dei Materiali (L.T.)
 IMIA RGANIA I con Elementi di Laboratorio orso di Laurea in IMIA, himica Applicata, Scienza dei Materiali (L.T.) Esercitazione n. 5 - Esercitazione sulla stereoisomeria geometrica TERMINI ED ARGMENTI PER
IMIA RGANIA I con Elementi di Laboratorio orso di Laurea in IMIA, himica Applicata, Scienza dei Materiali (L.T.) Esercitazione n. 5 - Esercitazione sulla stereoisomeria geometrica TERMINI ED ARGMENTI PER
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Esercitazione n Reazioni sulle reazioni di alcheni.
 Esercitazione n. 1 - Reazioni sulle reazioni di alcheni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) -butene b) -butene acqua, in ambiente acido -bromobutano,
Esercitazione n. 1 - Reazioni sulle reazioni di alcheni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) -butene b) -butene acqua, in ambiente acido -bromobutano,
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Acidi Carbossilici CH 3. Caratterizzati dalla presenza di un gruppo carbossilico. Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico)
 Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Acidi carbossilici. IUPAC catena più lunga contenente il gruppo -COOH al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita con -oico
 Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Nomi e formule dei principali composti organici
 Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
CORSO DI CHIMICA ORGANICA. Testo consigliato: Chimica Organica H.Hart,D.J.Hart, L.E.Craine Zanichelli
 CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gruppo carbonilico. Il gruppo carbonilico è caratterizzato dalla presenza C=O ed i composti che lo contengono vengono definiti composti carbonilici.
 Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
1. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: CH 3 O, H +
 Esercitazione n. 14 - Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2-butene b) 2-butene acqua,
Esercitazione n. 14 - Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2-butene b) 2-butene acqua,
ACIDI CARBOSSILICI e derivati
 ACIDI CABSSILICI e derivati Il nome sistematico di un acido carbossilico alchilico si fa derivare dal nome dell idrocarburo con lo stesso numero di atomi di carbonio, sostituendo la o finale con la desinenza
ACIDI CABSSILICI e derivati Il nome sistematico di un acido carbossilico alchilico si fa derivare dal nome dell idrocarburo con lo stesso numero di atomi di carbonio, sostituendo la o finale con la desinenza
Nomi e formule dei principali composti organici
 Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Capitolo 23 Dal carbonio agli idrocarburi
 Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
Gli idrocarburi che hanno un doppio legame carbonio-carbonio (e quindi due C ibridati sp 2 ) si chiamano ALCHENI Formula generale: C n H 2n
 ALHENI Gli idrocarburi che hanno un doppio legame carbonio-carbonio (e quindi due ibridati sp ) si chiamano ALHENI Formula generale: n H n REGOLA Quando in un idrocarburo ci sono legami π, si parla di
ALHENI Gli idrocarburi che hanno un doppio legame carbonio-carbonio (e quindi due ibridati sp ) si chiamano ALHENI Formula generale: n H n REGOLA Quando in un idrocarburo ci sono legami π, si parla di
2) Scrivere il nome sistematico per i composti elencati di seguito:
 Chimica Organica Alcheni 1) Disegnare la struttura per le molecole elencate: a. 3,3- dimetilciclopentene c. etil vinil etere b. 6- bromo- 2,3- dimetil- 2- esene d. allil alcol 2) Scrivere il nome sistematico
Chimica Organica Alcheni 1) Disegnare la struttura per le molecole elencate: a. 3,3- dimetilciclopentene c. etil vinil etere b. 6- bromo- 2,3- dimetil- 2- esene d. allil alcol 2) Scrivere il nome sistematico
Chimica organica: gli idrocarburi Capitolo C2
 himica organica: gli idrocarburi apitolo 2 VERIFIA LE TUE SEZE 1 2 3 D 4 5 B 6 A 7 A 8 9 10 A 11 A 12 A 13 B 14 15 A 16 17 D 18 19 B 20 A 21 B 22 A 23 B 24 D 25 A 26 A 27 D 28 B 29 A 30 31 A 32 B 33 B
himica organica: gli idrocarburi apitolo 2 VERIFIA LE TUE SEZE 1 2 3 D 4 5 B 6 A 7 A 8 9 10 A 11 A 12 A 13 B 14 15 A 16 17 D 18 19 B 20 A 21 B 22 A 23 B 24 D 25 A 26 A 27 D 28 B 29 A 30 31 A 32 B 33 B
Prova scritta di CHIMICA III del 6 Maggio 2010
 Prova scritta di IMIA III del 6 Maggio 2010 1) Rappresentare e nominare i possibili isomeri dell idrocarburo 6 14, disponendoli in ordine crescente nel numero di ottano. 2) Descrivere i prodotti che si
Prova scritta di IMIA III del 6 Maggio 2010 1) Rappresentare e nominare i possibili isomeri dell idrocarburo 6 14, disponendoli in ordine crescente nel numero di ottano. 2) Descrivere i prodotti che si
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
Esercizi sulle Forze Intermolecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
Capitolo A1 Dal carbonio agli idrocarburi
 Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 6 7 8 C-1: sp 3 ; C-2: sp 2 ; C-3: sp
Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 6 7 8 C-1: sp 3 ; C-2: sp 2 ; C-3: sp
Chimica organica, biochimica e laboratorio
 Giuseppe Valitutti Gabriella Fornari Maria Teresa Gando Chimica organica, biochimica e laboratorio Soluzioni degli esercizi del testo Capitolo 1 1.1 Tutti gli ioni hanno l ottetto più esterno completo,
Giuseppe Valitutti Gabriella Fornari Maria Teresa Gando Chimica organica, biochimica e laboratorio Soluzioni degli esercizi del testo Capitolo 1 1.1 Tutti gli ioni hanno l ottetto più esterno completo,
PROPRIETA FISICHE DEI COMPOSTI ORGANICI
 PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
CHIMICA II (CHIMICA ORGANICA)
 CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
Domanda 4 Dal punto di vista della reattività, il doppio legame si comporta spesso da:
 Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
Esercitazione n Reazioni di alcooli, dioli, eteri, ammine, sali di ammonio.
 Esercitazione n. 1 - Reazioni di alcooli, dioli, eteri, ammine, sali di ammonio. 1. Scrivere il prodotto, specificandone il nome, della reazione con P di: R- P R- P S N 2 a) 1-propanolo b) 2-propanolo
Esercitazione n. 1 - Reazioni di alcooli, dioli, eteri, ammine, sali di ammonio. 1. Scrivere il prodotto, specificandone il nome, della reazione con P di: R- P R- P S N 2 a) 1-propanolo b) 2-propanolo
Esercitazione sulle conformazioni di alcani e cicloesani
 Esercitazione sulle conformazioni di alcani e cicloesani 1. Disegnare la molecola completa del butano, nella conformazione più favorevole per tutti i legami - (usare i legami a cuneo e tratteggiati). 2.
Esercitazione sulle conformazioni di alcani e cicloesani 1. Disegnare la molecola completa del butano, nella conformazione più favorevole per tutti i legami - (usare i legami a cuneo e tratteggiati). 2.
CHIMICA ORGANICA I. Corso di laurea in CHIMICA (L.T.)
 IMIA RGANIA I orso di laurea in IMIA (LT) Esercitazione n 10 - Reazioni degli alcani TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Reazioni degli alcani (alogenazione, pirolisi, ossidazione):
IMIA RGANIA I orso di laurea in IMIA (LT) Esercitazione n 10 - Reazioni degli alcani TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Reazioni degli alcani (alogenazione, pirolisi, ossidazione):
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
Esercizi sulle Forze Intermolecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
c. 3-cloro-2,4,5-trimetil-3-esene d. 2-cloro-5-metil-3-eptino 10.4 a. cis-3-esene e trans-3-esene, rispettivamente.
 Capitolo 10 Risposte alle Domande ed esercizi a fine Capitolo 10.1 a. d. 10.2 a. 2-pentino 4,5-dibromo-1-eptino 3-cloro-2,4,5-trimetil-3-esene d. 2-cloro-5-metil-3-eptino 10.3 a. cis- e trans- trans- e
Capitolo 10 Risposte alle Domande ed esercizi a fine Capitolo 10.1 a. d. 10.2 a. 2-pentino 4,5-dibromo-1-eptino 3-cloro-2,4,5-trimetil-3-esene d. 2-cloro-5-metil-3-eptino 10.3 a. cis- e trans- trans- e
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CHIMICA ORGANICA. Fabrizio Mancin
 IMIA ORGANIA Fabrizio Mancin Dipartimento di Scienze himiche Edificio himica Organica, II Piano, Stanza 5 tel. 049 8275666, e-mail: fabrizio.mancin@unipd.it, http://www.chimica.unipd.it/fabrizio.mancin
IMIA ORGANIA Fabrizio Mancin Dipartimento di Scienze himiche Edificio himica Organica, II Piano, Stanza 5 tel. 049 8275666, e-mail: fabrizio.mancin@unipd.it, http://www.chimica.unipd.it/fabrizio.mancin
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alogenuri Alchilici. Primari: CH 3 CH 2 X Secondari: (CH 3 ) 2 CHX Terziari: (CH 3 ) 3 CX.
 Alogenuri Alchilici Derivati degli idrocarburi in cui uno o più atomi di H sono stati sostituiti da alogeni. R-X (R sta per un qualunque residuo alchilico e X per un alogeno) Primari: CH 2 X Secondari:
Alogenuri Alchilici Derivati degli idrocarburi in cui uno o più atomi di H sono stati sostituiti da alogeni. R-X (R sta per un qualunque residuo alchilico e X per un alogeno) Primari: CH 2 X Secondari:
Soluzioni degli esercizi di fine capitolo
 Soluzioni degli esercizi di fine capitolo 1 Soluzioni degli esercizi per capitolo apitolo A1 VERIFIA LE TUE NSENZE 1 A 10 B 2 11 D 3 B 12 A 4 D 13 5 A 14 6 B 15 7 16 B 8 A 17 9 A VERIFIA LE TUE ABILITÀ
Soluzioni degli esercizi di fine capitolo 1 Soluzioni degli esercizi per capitolo apitolo A1 VERIFIA LE TUE NSENZE 1 A 10 B 2 11 D 3 B 12 A 4 D 13 5 A 14 6 B 15 7 16 B 8 A 17 9 A VERIFIA LE TUE ABILITÀ
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Diagramma di flusso degli idrocarburi
 Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
Esercitazione n Reazioni degli alcani
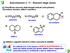 Esercitazione n 11 - Reazioni degli alcani 1 assificare ciascuno degli idrogeni indicati come primario, secondario, terziario, allilico o benzilico: a) ( ) C b) ( ) CH c) H primario d) e) terziario H H
Esercitazione n 11 - Reazioni degli alcani 1 assificare ciascuno degli idrogeni indicati come primario, secondario, terziario, allilico o benzilico: a) ( ) C b) ( ) CH c) H primario d) e) terziario H H
I composti acilici sono tutti quei composti che contengono il gruppo:
 omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Scienze dei Beni Culturali Compito A Chimica Fisica (Mod. A) A.A Compito in itinere '03
 AA 2003-04 2 ompito in itinere 12-12-'03 a) ciclo-1,3-epta-diene; 2,3-dicloro-3-terButil-toluene; c) metil-isopropil etere; d) benzoato di potassio; e) 4-bromo-3-etil-2-esanone F a) H 3 H 3 ; H 4 H Quale
AA 2003-04 2 ompito in itinere 12-12-'03 a) ciclo-1,3-epta-diene; 2,3-dicloro-3-terButil-toluene; c) metil-isopropil etere; d) benzoato di potassio; e) 4-bromo-3-etil-2-esanone F a) H 3 H 3 ; H 4 H Quale
Fondamenti di chimica organica Janice Gorzynski Smith Copyright 2009 The McGraw Hill Companies srl
 Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
23 Le diverse classi di composti organici
 23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI
 RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
Classificazione degli idrocarburi
 Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
BENZENE E DERIVATI. Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6. Arene: Idrocarburo aromatico
 BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
Sistema i seguenti carbocationi in ordine di stabilità crescente:
 Sistema i seguenti carbocationi in ordine di stabilità crescente: C 2 + + + Completa le seguenti reazioni: 3 C C C 2 + C 2 + + Disegna le formule di struttura per i carbocationi isomerici formati per reazione
Sistema i seguenti carbocationi in ordine di stabilità crescente: C 2 + + + Completa le seguenti reazioni: 3 C C C 2 + C 2 + + Disegna le formule di struttura per i carbocationi isomerici formati per reazione
Composti Carbossilici. Derivati Carbossilici
 omposti arbossilici Derivati arbossilici Derivati degli Acidi I derivati degli acidi carbossilici hanno attaccato al gruppo carbonilico anziché l'idrossile (-) altri gruppi elettron attrattori come: -N
omposti arbossilici Derivati arbossilici Derivati degli Acidi I derivati degli acidi carbossilici hanno attaccato al gruppo carbonilico anziché l'idrossile (-) altri gruppi elettron attrattori come: -N
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
Lezione 5. Alogenuri, alcoli, fenoli ed eteri
 Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Capitolo 19 Dal carbonio agli idrocarburi
 apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
Conformazione degli alcani
 onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
