COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
|
|
|
- Albana Sartori
- 4 anni fa
- Visualizzazioni
Transcript
1 MPSTI AMATII L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. aratteristiche Spettrali La maggior parte dei composti aromatici Spettrometria di massa presenta un picco dello ione molecolare molto intenso. Gli alchilbenzeni hanno una frammentazione molto facile con m/z 91. stato dimostrato che il carbocatione benzilico traspone a catione eptatrienilio... m/z 91 M (78) M m/z 91 (18)
2 UVvisibile Il benzene ha legami π coniugati Lo spettro di assorbimento elettronico è caratterizzato da due bande dette primarie e una banda detta secondaria o della struttura fine. λ = 184 nm (ε = ) λ = 0 nm (ε = 7 000) A struttura fine λ = 55 nm (ε = 0) È dovuta alle interazioni dei livelli elettronici con i modi vibrazionali nm I stretching = a sinistra di 000 cm 1 bending = (fuori dal piano) cm 1 stretching = spesso in coppia a 1600 e 1475 cm 1
3 1 M L anisotropia diamagnetica descherma il nucleo δ ppm 1 M L anisotropia diamagnetica descherma il nucleo δ 78 ppm
4 MPSTI AMATII I composti aromatici reagiscono MATD l aromaticità ADDIZI SSTITUZI possibili meccanismi? 1) meccanismo sincrono δ δ ) meccanismo in due stadi videnze sperimentali D La reazione è stata eseguita sul deuterobenzene D il legame D è piu forte del legame : D D D D k / k = 1 D significa che nello stadio lento non c'e rottura del legame 4
5 In alcuni casi si è riusciti ad isolare l'intermedio BF 4 SbF 6 MAISM I DU STADI MAISM DLLA SSTITUZI LTTFILA AMATIA primo stadio δ lento δ primo stato di transizione addotto sigma strutture di risonanza dell'intermedio secondo stadio veloce δ δ secondo stato di transizione nergia in funzione della coordinata di reazione: 1 ST ST 10.8 kcal/mole coordinata di reazione 5
6 Tutte le variazioni strutturali che abbassano l'energia dell'intermedio abbassano anche l'energia dello stato di transizione che porta all'addotto σ e quindi rendono più facile la reazione. SSTITUZII LTTFIL AMATI principali reazioni di Sostituzione lettrofila ITAZI S 4 SLFAZI S S 4 X S ALGAZI FeX X X (X = l) (X = ) l Fel l l Fe clorurazione bromurazione ALILAZI X All X Alchilazione di Friedelrafts AILAZI X All X Acilazione di Friedelrafts Queste reazioni permettono di introdurre nel benzene gruppi funzionali diversi, ma avvengono con lo STSS MAISM. ' perciò importante capire quale è il reagente elettrofilo e come si forma. 6
7 itrazione S 4 S 4 catione ITI S 4 S 4 S 4 S 4 Solfonazione S S S S S S Alogenazione l l Fel Fel 4 "l " l l Fel 4 l l Fel Fe Fe 4 " " Fe 4 Fe 7
8 Alchilazione (di Friedelrafts) δ δ δ δ l All... l... All All 4 All " Acilazione (di Friedelrafts) l δ δ All All 4 : All All 4 All l All All si deve usare in quantità stechiometrica perché dà complesso di Lewis con il prodotto Sostituzioni elettrofile aromatiche dei Benzeni SSTITUITI Tutte le posizioni del benzene sono equivalenti. Quando c'è un sostituente, le posizioni sono diverse: orto, meta e 1para se i prodotti si formassero solo su basi statistiche, si dovrebbe avere 40% di orto, 40% di meta e 0% di para a distribuzione dei prodotti osservata sperimentalmente non è MAI quella statistica questo significa che il sostituente presente sull'anello del benzene indirizza l'attacco dell'elettrofilo ITAMT per esempio: l l on è un effetto del sostituente sul substrato! 8
9 ITAMT Stadio lento: formazione dell addotto σ: più stabile è l'addotto sigma, minore è l'energia dello stato di transizione che porta all'addotto. 1. Si scrivono tutti i possibili addotti e le rispettive strutture di risonanza.. Si esamina se c'è una struttura con la carica positiva sul che lega il sostituente.. Si guarda se il sostituente stabilizza (o destabilizza) la carica positiva. benzene meta orto,para coordinata di reazione La reattività del benzene sostituito rispetto a quella del benzene dipende dall'energia di attivazione dello stadio lento e si vede dalla stabilità dell'addotto σ più stabile (del benzene sostituito) rispetto a quella dell'addottodel benzene. 9
10 l l l l l l l l l l orto,para l l meta benzene l l o coordinata di reazione 10
11 meta benzene orto,para o coordinata di reazione 11
12 orto,para meta benzene o coordinata di reazione 1
13 l l l l l l l l l l l l l meta orto,para benzene l l o l coordinata di reazione 1
14 è specie a difetto elettronico reagisce meglio con centri II di elettroni ATTIVITA Si deve considerare la densità elettronica delle PSIZII ATTIV (orientamento) sempio: mettere i seguenti composti in ordine decrescente di reattività, nei confronti di un reagente elettrofilo l 1. Si individua la posizione (o le posizioni) di attacco, cioè l'orientamento (sulla base della stabilità degli addotti σ).. Si considera l'effetto del sostituente SU QULLA PSIZI.. Maggiore è la densità elettronica, maggiore è la reattività (a parità di elettrofilo). Tutte le posizioni sono equivalenti. on ci sono sostituenti, la densità elettronica è quella di riferimento. rientamento in MTA. In questa posizione il gruppo esercita solo l'effetto induttivo. I attrazione elettronica Le posizioni reattive del nitrobenzene sono più povere di elettroni (e quindi M reattive) delle posizioni reattive del benzene rientamento in T PAA. In queste posizioni il gruppo esercita sia l'effetto induttivo che quello coniugativo. I, rilascio elettronico Le posizioni reattive del metossibenzene sono più ricche di elettroni (e quindi PIU reattive) delle posizioni reattive del benzene 14
15 rientamento in T PAA. In queste posizioni il gruppo esercita solo l'effetto induttivo. I rilascio elettronico Le posizioni reattive del metilibenzene sono più ricche di elettroni (e quindi PIU reattive) delle posizioni reattive del benzene l rientamento in T PAA. In queste posizioni il gruppo esercita sia l'effetto induttivo che quello coniugativo. I, attrazione elettronica Le posizioni reattive del clorobenzene sono più povere di elettroni (e quindi M reattive) delle posizioni reattive del benzene Il rilascio elettronico dovuto a risonanza è maggiore di quello induttivo (alchili) eattività: l > > > > Sostituzioni lettrofile sul AFTAL A differenza del benzene, le posizioni del naftalene non sono tutte equivalenti: ITAMT β β α α α α β β per conoscere l orientamento, basta confrontare gli addotti sigma nelle posizioni α e β L altro anello mantiene la completa aromaticità volte su nella risonanza dell addotto in α, solo 1 nella risonanza dell addotto in β e quindi è più stabile 15
16 Le sostituzioni elettrofile aromatiche sul naftalene avvengono in α S 4 Un caso a parte è la solfonazione, in cui l orientamento dipende dalla temperatura S T<100 o S 4 S S 4, Δ T>150 o S coordinata di reazione α β a T<100 : controllo cinetico, a T>150 : controllo termodinamico S S AZII LTTFILI DBLI Avvengono solo con aromatici MLT reattivi 1. eazione con i sali di benzendiazonio : X X 4idrossiazobenzene L elettrofilo (voluminoso) va in in orto solo se la posizione para è occupata eagiscono solo: benzenolo (=fenolo) e benzenammina (=anilina) (e analoghi del naftalene) 16
17 . eazione di carbossilazione (eazione di Kolbe) a Δ δ δ a solo con fenolo aspirina (acido acetilsalicilico) acido acetossibenzencarbossilico acido salicilico (acido idrossibenzencarbossilico). eazione di formilazione (reazione di eimertiemann) a a l K solo con fenolo l :l l :l lettrofilo :l l l l l l aldeide salicilica (idrossibenzencarbaldeide) 17
18 4. eazione di idrossimetilazione solo con fenolo ochinometano pchinometano PPAAZI ATTIVITA' DI SALI DI BZDIAZI [] (Fe, l) a, l, S 4 [] (F ), Δ l P l ul KI u u I AgBF 4 a, u BF 4 F Δ (solido) 18
19 US DI SALI DI BZDIAZI 1. Introduzione di gruppi che non si possono introdurre diversamente è nucleofilo da il benzene reagisce con gli elettrofili S 4 [] a l, 0 l. Introduzione di un secondo sostituente in una posizione diversa da quella possibile con una sostituzione elettrofila aromatica, sulla base dell'orientamento provocato dal primo sostituente esempi? PBLMI SLUZI difficile introdurre orienta un elettrofilo in meta sali di benzendiazonio ( ) All serve per ingombrare stericamente le posizioni orto ed avere solo la sostituzione in para e per diminuire la reattività altrimenti si avrebbero prodotti di polimetilazione, a l, 0 l u 19
20 PBLMA sia che orientano in orto, para SLUZI sali di diazonio (preparato come prima) Fe ( > I ) gruppo a rilascio elettronico più forte di, a S 4, 0 5 S 4 P? PBLMA orienta in orto, para Fe Fe Fe SLUZI SALI DI DIAZI 0
21 in queste condizioni reagiscono tutte le posizioni influenzate da a X, 0 5 gli atomi di sono nella posizione relativa voluta: basta togliere il gruppo X P ATTIVITA' DI ATA FAT I AGTI LTTFILI L'aumento del numero di anelli condensati diminuisce l'aromaticità Fenantrene ed antracene (meno aromatici di benzene e fenantrene) dannoa AZII DI ADDIZI FAT il legame 910 ha caratteristiche di un doppio legame poco delocalizzato (Fel ) 9bromofenantrene 9,10dibromo9,10diidrofenantrene ATTZI!! nel nome del prodotto di addizione va indicata la presenza dei due : 9,10dibromofenantrene indica che in 9 e 10 ci sono due atomi di AL PST DI DU 9,10dibromofenantrene 1
22 il fenantrene si comporta con X come un alchene l l 9cloro9,10diidrofenantrene L'addizione avviene al legame 910, perché in questo modo rimane intatta l'aromaticità degli altri due anelli benzenici ATA Si comporta anche come un diene coniugato, dando prodotti di addizione 1,4, oltre ai prodotti di sostituzione elettrofila aromatica (in posizione 9) (Fel ) 9bromoantracene 9,10dibromo9,10diidroantracene L antracene dà le caratteristiche reazioni dei dieni coniugati e perciò reagisce con elettrofili del tipo X e con i dienofili X 9X9,10diidroantracene X addotto di DielsAlder
23 eazioni in catena laterale I benzeni sostituiti possono reagire anche in catena laterale (cioè sul sostituente), se si usano condizioni opportune. l hν l l Fel l AZII DI SSIDAZI Monoalchilbenzeni Si ossidano a acido benzencarbossilico KMn 4, Δ KMn 4, Δ ( ) n KMn 4, Δ (n 1) Anello benzenico molto resistente all'ossidazione, V Il naftalene è un po più facile da ossidare, V
24 Un ossidazione meno drastica si può avere con r e gli aromatici con più anelli condensati r 1,4naftalenchinone (1,4naftochinone) r r 9,10fenantrenchinone 9,10antracenchinone benzendioli Si ossidano molto facilmente a chinoni Ag obenzochinone Ag pbenzochinone AZII DI IDUZI on La riduzione catalitica richiede pressioni e temperature elevate per la prima addizione (perdita dell aromaticità), mentre le addizioni successive sono più facili., P, Δ on a cat. (Pt, Pd, i, u, o h) iduzione di Birch a (o Li) meccanismo: a... carbanione anione radicale.. liquida, radicale. a 4
25 Se la reazione si effettua su un benzene sostituito ITAMT Si formano carbanioni stabilizzati da gruppi ad attrazione elettronica, destabilizzati da gruppi a rilascio elettronico Un carbonio che porta un gruppo ad attrazione elettronica viene ridotto a (o Li) liquida, intermedio stabilizzato Un carbonio che porta un gruppo a rilascio elettronico non viene ridotto a (o Li) liquida, intermedio destabilizzato a (o Li) liquida, intermedio destabilizzato Il benzene non reagisce con i nucleofili u Però.. la sintesi industriale del fenolo parte dal clorobenzene l K, Δ, P Kl..e allora???? SSTITUZI ULFILA AMATIA Perché i composti aromatici possano reagire con ULFILI, devono possedere i seguenti requisiti 1. BU GUPP UST. SSTITUT/I A FT ATTAZI LTTIA ( ) In questo caso si ha: Meccanismo di ADDIZILIMIAZI 5
26 La reazione avviene in due stadi, con formazione nello stadio lento di un intermedio (addotto σ negativo o complesso di Meisenheimer), stabilizzato per risonanza dal sostituente l l l X δ l δ X Δ =/ l X coordinata di reazione δ l δ X X l lento l l l videnze sperimentali: qualche complesso di Meisenheimer è stato isolato F il legame F è più forte di l, ma è più reattivo di l il legame con il gruppo uscente non si rompe nello stadio lento e F (più elettronegativo) favorisce l'attacco del nucleofilo, rendendo più positivo il a cui è legato Però.. la sintesi industriale del fenolo parte dal clorobenzene l K, Δ, P Kl..e allora???? Se manca il sostituente a forte attrazione elettronica, si può avere reazione con i nucleofili, purché vengano soddisfatti i seguenti requisiti: 1. BU GUPP UST. il nucleofilo è UA BAS FT K (solida) a in liquida In questo caso si ha: Meccanismo di LIMIAZIADDIZI 6
27 La base forte strappa un protone acido (in orto al gruppo uscente) e la base coniugata forma il benzino, che, essendo molto reattivo, addiziona l'acido coniugato della base l l.. l BZI l'addizione può avvenire in entrambi i modi videnze sperimentali: l * * * l * = 1 con un clorobenzene sostituito si hanno miscele di prodotti pmetilclorobenzene l l l.. l ometilclorobenzene l l 7
28 mmetilclorobenzene l l 8
29 aratteristica strutturale di aldeidi e chetoni ALDIDI e TI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni. Una scissione molto facile è la rottura α (αcleavage), che lascia un carbocatione acilio (stabilizzato per risonanza):... '. '.. ' ' M M P.M = 106 m/z 105 m/z 105 P.M = 10 M 1
30 UVvisibile due transizioni: π π* a λ = 190 nm (lontano UV) permessa dalla simmetria (ε> ) n π* a λ = 8090 nm proibita dalla simmetria (ε 150) La transizione n π* può non vedersi se la soluzione è diluita La coniugazione con doppi legami sposta I massimi di assorbimento verso lunghezze d onda maggiori (shift batocromico) π π* a λ = 1 nm (ε = M 1 cm 1 ) n π* a λ = 1 nm (ε = 40 M 1 cm 1 ) I ALDIDI stretching = stretching (del ) a circa 175 cm 1, spostato verso valori più bassi dalla coniugazione deboli bande a 750 e 850 cm 1. metilbutanale benzencarbaldeide
31 I stretching = TI a circa 1715 cm 1, spostato verso valori più bassi dalla coniugazione pentanone fenil metil chetone 1 M L effetto I dell ed il campo magnetico generato dagli elettroni π diminuiscono la densità elettronica attorno al nucleo del 1 : molto deschermato δ ppm (aldeidi) 0190 ppm (chetoni) metilbutanale pentanone
32 1 M ALDIDI L effetto I dell ed il campo magnetico generato dagli elettroni π diminuiscono la densità elettronica attorno al nucleo del 1 del : molto deschermato (9,510,5 δ) benzencarbaldeide metilbutanale 1 M TI L effetto I dell diminuisce la densità elettronica attorno al nucleo del 1 sul adiacente: deschermato da,0,5 ( ) fino a (, ) δ pentanone fenil metil chetone 4
33 ALDIDI e TI sp u: δ δ acido eazione caratteristica ADDIZI ULFILA Meccanismo: 1. u: u lento sp (trigonale planare) sp (tetraedrico) u generalmente =. sp (trigonale planare) :u lento u sp (tetraedrico) 5
34 Sono reazioni di equilibrio isentono dell'effetto sterico isentono degli effetti elettronici dei sostituenti Sostituenti ad attrazione elettronica D PIU' PSITIV il carbonilico FAVIS l'attacco del nucleofilo ATTIVITA' ST TI < MTILTI < ALDIDI < MTAAL a. ULFILI ALL'SSIG aldeide idrata chetone idrato Meccanismo: : lento 6
35 Meccanismo: : lento MIATAL esempi: La reazione può avvenire anche in modo intramolecolare: Se la reazione con alcool si fa in ambiente AID AID, prosegue: (*) ' ' ' (*) l (gas) ATAL (*) ' " ' ' " ATAL (TAL) (*) l (gas) Meccanismo: ' ' come già descritto 7
36 '.. ' ' '.. ' ' ' ' ' on I chetoni (meno reattivi delle aldeidi) l equilibrio è spostato verso sinistra I chetoni danno chetali con equilibrio spostato verso destra solo se il nucleofilo è un diolo (1, o 1,): la reazione è intramolecolare e si forma un anello stabile.. sempio di applicazione: come ottenere da? KMn 4 però, con KMn 4 : KMn 4 8
37 KMn 4, b. ULFILI ALL ZLF S : S lento S S MITIATAL esempi: S S S S anidro S Se la reazione con si fa in ambiente AID AID, prosegue: S S TIATAL on ditioli la reazione è intramolecolare quando si possono formare anelli stabili (5 e 6 termini).grado di.. S S S S S S 9
38 S S S S S S S S TIATAL (TITAL) as eazione di Bertagnini solo con aldeidi : S S reazione acidobase S Serve per purificare le aldeidi: l addotto precipita, si filtra, si torna ad aldeide c. ULFILI ALL AZT con i nucleofili all'azoto i prodotti di addizione perdono una molecola diacqua ammoniaca ed ammine primarie, : IMMIA (base di Schiff).. ' ' ' IMMIA (base di Schiff) Meccanismo: veloce 10
39 .. veloce lento veloce veloce La velocità della reazione dipende dal p la velocità massima si ha a p 5 6 k p a p troppo acido manca il nucleofilo a p non abbastanza acido, la concentrazione di composto carbonilico protonato è troppo bassa 11
40 ammine secondarie '.. ' ' AMMIA Meccanismo: veloce.. lento veloce sempi:, ( ) ammine terziarie SSUA AZI derivati dell'ammoniaca X =.. X IDSSILAMMIA veloce.. lento 1
41 : SSIMA sempio: ossima della benzencarbaldeide ossima del butanone X =.... IDAZIA veloce.. lento : IDAZ sempio: idrazone del propanale 1
42 X = 6 5 u.... FILIDAZIA veloce.. lento : FILIDAZ sempio:.... fenilidrazone del fenil metil chetone u.... fenilidrazone del butanale,4diitfilidazia 14
43 ....,4DIITFILIDAZ sempio:,4difenilfenilidrazone del del propanone X =.... SMIABAZID u.... SMIABAZ 15
44 meccanismo: d. ULFILI AL ABI : : ' cianidrina ' cianidrina lento :.. : : : : MgX Addizione di carbanioni (composti organometallici) δ δ MgX δ δ MgX ( ) Mg()X sempi: Mg Mg MgI MgI MgI MgI 16
45 Li esempio: δ δ δ δ Li Li Li Li ( ) Li() FSFA AZI DI WITTIG alogenoalcano trifenilfosfina base forte composto carbonilico AL 1. Sostituzione nucleofila.. P S P sale di FSFI (bromuro di alchiltrifenilfosfonio). eazione acidobase base.. P( 6 5 ) P( 6 5 ) P( 6 5 ) FSFA o ILID (yilide) u: BAS butillitio ( Li) oppure idruro di sodio (a) IL FSF PU' SPAD L'TTTT: stabilizza il carbanione. Addizione nucleofila.. P( 6 5 ) ' " P( 6 5 ) BTAIA " ' o FSFTA 17
46 " ' P( 6 5 ) fosfinossido "driving force (forza trainante) Il legame P è più forte del legame P sempio: 1. :PPh. a a.. :PPh PPh PPh PPh.. PPh =PPh sempio: 1. :PPh. 4 9 Li.. PPh PPh DSAZI ALDLIA 10% a in ALDL 18
47 meccanismo: 1. reazione acidobase genera il nucleofilo α. addizione nucleofila. reazione acidobase la sua concentrazione non cambia l'aldolo, sottoposto a riscaldamento, perde una molecola di acqua Δ doppio legame coniugato perché la condensazione aldolica possa avvenire, è necessario che l'aldeide abbia almeno un in α al carbonile per esempio: non reagiscono aldeidi con più dell'etanale, comunque danno il carbanione in α al carbonile α 19
48 δ δ DSAZI ALDLIA MISTA La reazione con due aldeidi, entrambe con in α, dà una miscela di prodotti la condensazione aldolica mista (o incrociata) diventa utile quando una sola delle aldeidi ha un in α (precursore del nucleofilo). nucleofilo 0
49 la coniugazione con l'anello benzenico facilita la disidratazione ATTZI! la condensazione aldolica in ambiente basico con i chetoni non avviene equilibrio spostato a sinistra i chetoni possono essere utilizzati come fonti di carbanioni in condensazioni miste con aldeidi senza in α AZI DI LAISSMIDT nucleofilo meccanismo: spontanea la coniugazione con l'anello benzenico facilita la disidratazione esempio: In questo caso, per avere disidratazione occorre SALDA (meglio se in ambiente acido) Δ 1
50 AZI DI AIZZA Le aldeidi SZA in α al carbonile possono reagire con a, in condizioni più drastiche di quelle della condensazione aldolica (concentrazione più elevata di base, temperatura elevata) Δ eazione di disproporzione (un si ossida e un altro di riduce) meccanismo: 1. attacco nucleofilo al carbonilico δ δ annizzaro ( ) Questo QUILIBI si ha anche nel caso della condensazione aldolica, ma in quel caso c è un altra strada (attraverso la base coniugata) che porta a prodotti e quindi questo equiibrio è come se non ci fosse.. trasferimento di idruro ( con gli elettroni di legame) δ δ. reazione acidobase Danno la reazione di annizzaro tutte le aldeidi SZA AIDI Di solito gli acidi sono in α al carbonile, ma SSAIAMT esempio: ma:? acido!
51 ecc. ucleofilo condensazione aldolica
52 TAUTMIA L'equilibrio tautomerico è catalizzato da acidi e da basi meccanismo in ambiente basico:.. reazione acidobase ione enolato reazione acidobase enolo l'equilibrio è spostato verso la forma carbonilica 99.99% 0.01% 99.90% 0.10% 99.4% 0.06% l'equilibrio è spostato verso la forma enolica se ci sono fattori particolari che la stabilizzano 0% 80% meccanismo in ambiente acido:..... stabilizzazione per legame idrogeno : reazione acidobase reazione acidobase 4
53 Un chirale in α al carbonile in ambiente acido o basico racemizza * * * oppure (S) (S) () icapitolando: Tutti gli equilibri SIST elettrofilo = u = B MA QUAD UQUILIBI SPSTAT VS I PDTTI, GLI ALTI TA IDIT: M S I FSS acidi IDUZI, cat. idruro idruro = ab 4, LiAl 4 (a) oppure (b) [] (a) Zn(g), l (b),, Δ lemmensen WolffKischner 5
54 meccanismi: ab 4 ADDIZI ULFILA u: = B B.. ADDIZI ULFILA u: =.. Δ.. ADDIZI ULFILA u: = :.. i idrogenazione catalitica SSIDAZI [] [] [] SSUA AZI ' tutti gli ossidanti già visti con gli alcooli Saggio di Tollens Ag( ) Ag specchio d'argento gli αidrossichetoni possono dare un saggio positivo: Gottfried Tollens ' [] Ag( ) Ag ' 6
55 AZII I ATA LATAL αalgazi I chetoni vengono alogenati in α al carbonile. La reazione è promossa da basi oppure acidocatalizzata (Le aldeidi vengono ossidate dagli alogeni). promossa da basi: la base si consuma acidocatalizzata l'acido non si consuma La velocità dell'αalogenazione (sia in ambiente basico che in ambiente acido) dipende dalla concentrazione di alogeno. meccanismo della reazione promossa da basi: lento 7
56 meccanismo della reazione acido catalizzata: lento : on i metilchetoni reazione dell'aloformio con eccesso di alogeno e a in acqua, I I iodoformio solido giallo meccanismo: I I I I I I I Acidità maggiore di quella del metile I I I atomi di iodio (elettronegativi) 8
57 I I :I I Si separa; giallo ATTZI!!! i possono essere falsi positivi I ossidante anche composti diversi dai metilchetoni possono dare lo iodoformio (falsi positivi) se la molecola può essere ossidata dallo iodio a metilchetone I I I I I I MPSTI ABILI α,βisatui centro nucleofilo centro elettrofilo on reagenti elettrofili Addizione 1, e 1,4 Addizione 1, l l Addizione 1,4 l l 9
58 on reagenti nucleofili Addizione 1, e 1,4 meccanismo: 1,4 1, con nucleofili basi più forti è preferita l'addizione 1, (al =) Mg MgI con nucleofili basi più deboli è preferita l'addizione 1,4 IDUZI di composti carbonilici contenenti = il prodotto dipende dal catalizzatore e dalle condizioni di reazione, i si riduce = 5, i, Δ si riducono entrambi 1. ab 4. si riduce = 0
59 AIDI ABSSILI e DIVATI aratteristica strutturale di acidi carbossilici e derivati Y aratteristiche Spettrali Spettrometria di massa Acidi carbossilici Lo ione molecolare di solito è spesso debole. La rottura α (αcleavage), lascia il carbocatione acilio (stabilizzato per risonanza):.. Può essere perso il gruppo.. m/z 45 Anche con gli altri gruppi funzionali è favorita la scissione dello ione molecolare che porta al carbocatione acilio Le ammidi non sostituite sull hanno un picco caratteristico a m/z 44.. m/z 44 acido butanoico, PM 88 acetato di etile, PM 88 M M 1
60 propanammide, PM 7 m/z 44 cloruro di butanoile, PM 106 M M l anidride benzencarbossilica, PM 6 UVvisibile Analogo a quello di aldeidi e chetoni I AIDI ABSSILII stretching stretching = stretching banda molto larga a 400 cm 1, spesso sovrapposta alle bande a circa cm 1, spostato verso valori più bassi dalla coniugazione tra 10 e 110 cm 1 acido butanoico
61 I STI stretching = stretching a circa 175 cm 1, spostato verso valori più bassi dalla coniugazione con. La coniugazione con sposta l assorbimento verso valori più alti. due o più bande tra 100 e 1000 cm 1 acetato di etile I AMMIDI stretching = a circa cm 1. stretching cm 1 ( hanno due bande) propanammide
62 I stretching = LUI AILII a circa 1800 cm 1, spostato verso valori più bassi dalla coniugazione. cloruro di butanoile cloruro di benzoile I AIDIDI stretching = sempre due bande tra 180 a 1800 cm 1 e tra 1775 e 1740, spostato verso valori più bassi dalla coniugazione con. stretching tra 100 e 900 cm 1 anidride propanoica 4
63 I stretching ITILI a circa 50 cm 1, spostato verso valori più bassi dalla coniugazione con. propanonitrile benzenecarbonitrile 1 M L effetto I dell ed il campo magnetico generato dagli elettroni π diminuiscono la densità elettronica attorno al nucleo del 1 : molto deschermato δ X ppm acetato di etile acido butanoico anidride propanoica propanammide 5
64 1 M L effetto I dell diminuisce la densità elettronica attorno al nucleo del 1 sul adiacente: deschermato da,0,5 ( ) fino a (, ) δ (negli acidi arbossilici) fortemente deschermato: 1015 δ; protone mobile, scambia con D (nelle ammidi) deschermato e molto allargato: 67 δ; protone mobile, scambia con D acido butanoico acido benzencarbossilico acetato di etile propanammide metiletanammide anidride benzoica 6
65 AIDI ABSSILI e DIVATI sp δ δ acido aratteristiche: acido u: Acidità del legame Il del carbossile subisce attacco da parte dei nucleofili I protoni in α al carbossile sono relativamente acidi e possono essere sostituiti sp gruppo uscente Y δ δ aratteristiche: sull' del carbonile (o sull' del nitrile) si ha protonazione I protoni in α al carbonile sono relativamente acidi e possono essere strappati con basi forti Qualche reazione caratteristica delle ammidi avviene sull' acido u: eazione caratteristica SSTITUZI ULFILA sp δ δ (la sostituzione nucleofila può avvenire con meccanismo base o acidocatalizzato) acido u: 7
66 Meccanismo: u: u lento Y Y sp sp (trigonale planare) (tetraedrico) u sp (trigonale planare) SSTITUZI ULFILA AL ABI AILI Principali nucleofili: :u =,,,,, S, u: =,, < < < < ' S' l reattività crescente Questo ordine di reattività è il risultto di più fattori Basicità del gruppo uscente meno basico: miglior gruppo uscente Basicità: < < () < l capacità come gruppo uscente isonanza l S' l S' ' ' 8
67 il contributo della struttura di risonanza a separazione di carica diminuisce la bontà del gruppo uscente ed è tanto maggiore quanto migliore è la sovrapposizione degli orbitali (cioè con gli elementi della stessa riga). ffetto induttivo Maggiore è l effetto ad attrazione elettronica, più positivo è il carbonilico ATTIVITA ST l ' più facile è l attacco del nucleofilo oppure ATTIVITA ST l " " ' ATTIVITA ST l ' 9
68 1. AZI u = a) Alogenuri acilici l : lento l l Sostituenti ad attrazione elettronica su FAILITA l'attacco del nucleofilo b) steri Gli esteri sono meno reattivi degli alogenuri acilici: l acqua da sola non reagisce), oppure, In ambiente basico u = lento : ' ' ' reazione acidobase ' L'ultimo passaggio rende IVSIBIL l'intero processo Sostituenti ad attrazione elettronica su FAILITA l'attacco del nucleofilo In ambiente acido u = ' ' ' lento ' : ' ' ' Processo VSIBIL Questo significa che in ambiente acido si può idrolizzare un estere ad acido carbossilico L'idrolisi acida degli esteri è praticamente insensibile agli effetti elettronici dei sostituenti; è invece sensibile agli effetti sterici ATTZI Questa insensibilità agli effetti elettronici (induttivo e coniugativo) dei sostituenti è una caratteristica SL dell IDLISI AIDA degli STI è il risultato di effetti opposti, praticamente uguali 10
69 Lo stadio lento è l attacco del nucleofilo sull estere protonato: dipende quindi dalla sua concentrazione, che, a sua volta, dipende dalla basicità dell estere K = [()' ] [ '][ ] [()'] = K [ '][ ] v = k[()' ] = kk [ '][ ] La reattività dipende dalla costante di velocità dello stadio lento (k) dalla costante di equilibrio acidobase preliminare (K) k K l'attacco del nucleofilo è favorito dai sostituenti ad attrazione elettronica la protonazione di una base è sfavorita dai sostituenti ad attrazione elettronica Solo nel caso dell'idrolisi acida degli esteri gli effetti hanno valori molto simili, cioè la sensibilità della protonazione e dell'attacco nucleofilo all'effetto dei sostituenti è praticamente la stessa. ssendo di segno opposto, gli effetti si annullano. c) Ammidi Le ammidi sono ancora meno reattive: l acqua da sola non reagisce), oppure, In ambiente basico u = : lento i sono solo ATTIVI gruppi uscenti, e, ma è più AID di : reazione acidobase L'ultimo passaggio rende IVSIBIL l'intero processo Sostituenti ad attrazione elettronica su FAILITA l'attacco del nucleofilo 11
70 In ambiente acido u = lento : 4 L'ultimo passaggio rende IVSIBIL l'intero processo Sostituenti ad attrazione elettronica su FAILITA l'attacco del nucleofilo d) Anidridi u = Le anidridi sono più reattive di esteri ed ammidi: basta l acqua da sola : e) itrili L'ultimo passaggio rende IVSIBIL l'intero processo Sostituenti ad attrazione elettronica su FAILITA l'attacco del nucleofilo I nitrili sono poco reattivi (meno delle ammidi): l acqua da sola non reagisce), oppure, 1
71 In ambiente acido u = : lento : tautomeria PSGU con l'idrolisi acida delle ammidi : 4 L'ultimo passaggio rende IVSIBIL l'intero processo Sostituenti ad attrazione elettronica su FAILITA l'attacco del nucleofilo. AZI ALLI a) Acidi carbossilici In ambiente acido u = lento : ' ' ' ' ' ' La reazione intramolecolare è facile, se si formano anelli stabili (5 e 6 termini) : γ Δ γlattone 1
72 : δ Δ δlattone se l' è più vicino al carbossile, ci sono altri percorsi di reazione, più facili della chiusura di un anello teso β Δ βeliminazione α Δ lattide se l' è più lontano dal carbossile, il prodotto dipende dalle condizioni di reazione in soluzione molto diluita: in soluzione concentrata: Δ Δ n ( ) n n b) Alogenuri acilici.. ' l lento l ' l ' opportuno effettuare la reazione in presenza di una base (per l) 14
73 es.: l l c) Anidridi.. ' ' ' ' ' d) steri TASSTIFIAZI In ambiente basico u = ' :" lento " ' " ' In ambiente acido u = ' " ' ' lento : " ' " ' " " " ' " 15
74 e) Ammidi ssendo meno reattive, richiedono condizioni di reazione troppo energiche per essere utili. AZI AMMIAA D AMMI a) Acidi carbossilici con : 4 reazione acidobase Scaldando il carbossilato di ammonio solido: 4 (solido) Meccanismo: : 4 Δ con ammine primarie (solido) Δ Meccanismo: 16
75 con ammine secondarie : (solido) Δ Meccanismo: : Se si ha un amminoacido con il gruppo amminico in γ o δ al carbossile, la reazione è intramolecolare (si formano anelli a 5 o a 6 termini) γ Δ γlattame Δ δ δlattame se l è più vicino al carbossile, ci sono altri percorsi di reazione, più facili della chiusura di un anello teso β Δ βeliminazione 17
76 b) Alogenuri acilici Meccanismo: l : lento l l l l : 4 l ' ' l ' l '" '" l ' " c) Anidridi : 4 18
77 ' ' " ' '" ' ''' ' ''' Le anidridi cicliche danno immidi.. 4 anidride ftalica Δ ftalimmide base debole, acido.. :B B d) steri lento : ' ' ' ' Gli esteri sono meno reattivi di alogenuri acilici e anidridi e perciòbisogna scaldare ' Δ " " ' ' " ''' Δ ' " ''' 19
78 4. AZI AIDI ABSSILII ABSSILATI on questi nucleofili possono reagire solo I derivati acilici più reattivi a) Alogenuri acilici l l l l es: l l l neutralizzato con una base man mano che si forma l b) Acidi carbossilici (SL con acidi bicarbossilici in grado di formare anelli stabili) Δ. AZI TILI a) Alogenuri acilici ' S l l ' S l es: S l S l S' 0
79 6. AZI MPSTI GAMTALLII con reattivi di Grignard e litioorganici a) steri MgX δ δ ' " MgX ' " ' "MgX da qui prosegue la reazione dei chetoni MgX δ δ, ' MgX ' ' i chetoni sono più reattivi degli esteri e perciò si arriva all'alcool terziario es.: Mg, Mg ' " δ Li δ Li ' " ' "Li da qui prosegue la reazione dei chetoni δ Li δ, ' Li ' b) loruri acilici MgX δ δ ' l MgX ' l ' ' MgXl con accorgimenti sperimentali, è possibile fermare la reazione alla formazione del chetone, altrimenti, si arriva ad alcool terziario δ MgX δ, ' MgX ' ' 1
80 ' l Li δ Li δ ' l ' Lil ' Li δ δ, Li ' ' con cadmioorganici e cuprati organici Per fermare la reazione a chetone si devono usare: composti organometallici meno reattivi solo con i cloruri acilici MgX dl d Mgl MgX ( =, alchile primario, fenile) esempio: Mg dl d d l l ' l δ δ uli ' l ' es.: l ( ) uli l ( ) uli 78 (feromone delle formiche) 9%
81 IDUZII a) on idruro LiAl 4 LiAl 4 l ' LiAl 4 LiAl 4 LiAl 4 Meccanismo: Al (Li ) (Li ) Al Y = l, ', Al : Y Y : Y Y = Y :
82 : : : Diminuendo la reattività dell'idruro è possibile fermare ad aldeide la riduzione dei LUI AILII [( Li ) ] Al l es.: l [( Li ) ] Al b) on idrogeno e catalizzatore, Pt on catalizzatore disattivato è possibile fermare ad aldeide la riduzione degli ALGUI AILII Pd, BaS 4 l Pd, chinolina es.: l Pd 4
83 AZII SPIFI DLL SIGL LASSI DI GUPPI FUZIALI 1. Acidi carbossilici (a) trasformazione del gruppo in buon gruppo uscente cattivo gruppo uscente Per trasformarlo in buon gruppo uscente si possono utilizzare i reagenti che trasformano in l on agenti alogenanti l Sl l S l Pl 5 l Pl l Pl P() esempi: l S l l l S Pl 5 l l Pl Pl l P() Meccanismo con Sl : l S l S l l S l l S S l on diazometano:.. : : : reazione acidobase u sp ottimo gruppo uscente 5
84 on diazometano si formano esteri metilici on dicicloesilcarbodiimmide, D u.. ' ' Addizione nucleofila buon gruppo uscente ' ' reazione acidobase dicicloesilurea La D permette di ottenere ammidi dagli acidi carbossilici in condizioni molto blande b) reazione in posizione α P, oppure P αalogenazione eazione VZ (ellvolhardzelinski) Meccanismo:.. P gli alogenuri acilici enolizzano più facilmente degli acidi carbossilici Il = addiziona 6
85 Quando si lavora la reazione (aggiunta di acqua), il bromuro acilico è più reattivo di quello alchilico. ppure si possono aggiungere nucleofili,. steri on alcossido (condensazione di laisen) a L alcossido DV essere identico al gruppo dell estere Meccanismo: (a ) a reazione acidobase u (equilibrio spostato a sinistra) (equilibrio spostato a sinistra) : 7
86 più acidi di quelli dell estere di partenza (equilibrio spostato a destra) (a ) ' possibile la condensazione incrociata, quando un solo estere ha in α: 1. a. qualsiasi carbanione è in grado di dare condensazione a ( ) (a ) ( ) ( ). Ammidi on anidride fosforica, P 5 on con a (Trasposizione di ofmann) 4 a a a (oppure a, ) meccanismo bromoammide 8
87 nitrene.... isocianato DABSSILAZI a) da carbossilati di metalli pesanti (reazione di unsdiecker) Ag Ag g g ) Pb( ) 4 Pb 4 ) 4 Ag (o I ) Δ ( I) 9
88 meccanismo: acil ipobromito inizio : : :... : radicale carbossilato : :.. propagazione b) da βchetoacidi Δ Δ # in ambiente basico: 0
89 b) da acidi βdicarbossilici Δ # la decarbossilazione è favorita da sostituenti ad attrazione elettronica SITSI "ATATIA" Sfrutta l'acidità degli in mezzo a due e la facile decarbossilazione dei βchetoacidi : ecc. a " " " (a ) c'è ancora un acido (meno di prima ) ( ) K : (K ) " sostituzione nucleofila 1 X al saturo, 1 " idrolisi " basica 1 X sostituzione nucleofila al saturo, " idrolisi " basica neutralizzazione (acidobase) " Δ decarbossilazione 1.. Δ " 1 " 1
90 Scegliendo opportunamente il reagente X, si possono ottenere chetoni con un altro gruppo funzionale X = αalogenoesteri : β β 1. a,. α γ Δ γchetoacido X = αalogenochetoni : 1. a,. Δ α β γdichetone X = alogenuri acilici on si può usare come base a in, perché l'alogenuro acilico è molto reattivo (e reagisce con l etossido ed anche con l'etanolo)
91 a : l 1. a, Δ. βdichetone on una base molto forte (ammide di sodio o di potassio) si possono strappare due protoni. Il dianione può essere fatto reagire con un equivalente di alogenuro alchilico K : K : 4 l X.. per la neutralizzazione conviene usare l'acido coniugato del solvente il βchetoestere con catena allungata può essere utilizzato in tutte le reazioni viste in precedenza SITSI "MALIA" Sfrutta l'acidità del metilene tra due funzioni esteree e la facile decarbossilazione degli acidi βdicarbossilici : propandioato dietilico (malonato dietilico) "estere malonico" : X 1., Δ X. acido acetico αsostituito
92 ( ) K : ' X 1., '.. Δ, ' acido acetico α,αdisostituito La reazione si può effettuare con tutti gli alogeno derivati utilizzati con il ossobutanoato di etile (estere acetoacetico) alogenuri alchilici, alogenuri acilici, αalogenochetoni, αalogenoesteri altri esempi (che si possono usare anche nella sintesi acetoacetica: X = α,ωdialogenoalcani a a : ( ) K : ' X 1., '.. Δ, ' acido acetico α,αdisostituito La reazione si può effettuare con tutti gli alogeno derivati utilizzati con il ossobutanoato di etile (estere acetoacetico) alogenuri alchilici, alogenuri acilici, αalogenochetoni, αalogenoesteri altri esempi (che si possono usare anche nella sintesi acetoacetica: X = α,ωdialogenoalcani a a : 4
93 a) in eccesso di estere : ( ) : n ( ) n 1), Δ ( ) ( ) n n ) acido bicarbossilico b) in quantità equimolari : ( ) n ( ) n : ( ) n ( ) 1) n, Δ ( ) ( n ) n ) n =,,4,5 acidi cicloalcancarbossilici 5
ACIDI CARBOSSILCI e DERIVATI
 AIDI ABSSILI e DEIVATI aratteristica strutturale di acidi carbossilici e derivati aratteristiche Spettrali Spettrometria di massa Acidi carbossilici Lo ione molecolare di solito è spesso debole. La rottura
AIDI ABSSILI e DEIVATI aratteristica strutturale di acidi carbossilici e derivati aratteristiche Spettrali Spettrometria di massa Acidi carbossilici Lo ione molecolare di solito è spesso debole. La rottura
COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 MPSTI ARMATII L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. aratteristiche Spettrali La maggior parte dei composti aromatici Spettrometria
MPSTI ARMATII L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. aratteristiche Spettrali La maggior parte dei composti aromatici Spettrometria
ALDEIDI e CHETONI. O sp 2 legato a C sp 2
 aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
ALDEIDI e CHETONI. Nu: sp 2. δ+ δ- C O C E + H acido ADDIZIONE NUCLEOFILA. Reazione caratteristica
 ALDEIDI e ETNI Nu: sp 2 δ δ E acido eazione caratteristica ADDIZINE NULEFILA himica rganica e Laboratorio Meccanismo: 1. Nu: Nu lento sp 2 (trigonale planare) sp 3 (tetraedrico) E Nu E generalmente E =
ALDEIDI e ETNI Nu: sp 2 δ δ E acido eazione caratteristica ADDIZINE NULEFILA himica rganica e Laboratorio Meccanismo: 1. Nu: Nu lento sp 2 (trigonale planare) sp 3 (tetraedrico) E Nu E generalmente E =
ALDEIDI e CHETONI. Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
 ALDEIDI e ETNI aratteristica strutturale di aldeidi e chetoni sp 2 legato a sp 2 = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con
ALDEIDI e ETNI aratteristica strutturale di aldeidi e chetoni sp 2 legato a sp 2 = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che con
COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
COMPOSTI AROMATICI. L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. UVvisibile Il benzene ha legami π coniugati Lo spettro di assorbimento
CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. UVvisibile Il benzene ha legami π coniugati Lo spettro di assorbimento
anidridi C R PREPARAZIONE DELLE ANIDRIDI + R C O - C Cl C R + P 2 O 5 C R C OH
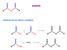 anidridi PEPAAZINE DELLE ANIDIDI l P 2 5 Nu = 2 Le anidridi sono più reattive di esteri ed ammidi: basta l acqua da sola : 2 2 2 2 EAZINI DELLE ANIDIDI: con acqua '.. ' ' ' ' EAZINI DELLE ANIDIDI: con
anidridi PEPAAZINE DELLE ANIDIDI l P 2 5 Nu = 2 Le anidridi sono più reattive di esteri ed ammidi: basta l acqua da sola : 2 2 2 2 EAZINI DELLE ANIDIDI: con acqua '.. ' ' ' ' EAZINI DELLE ANIDIDI: con
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1
 CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
Aromaticità. Addizione elettrofila alcheni
 Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Unità didattica 7 (segue) Reattività del benzene. Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili
 Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Idrogeni in α a un carbonile
 Enoli e Enolati 1 Idrogeni in α a un carbonile Solo gli idrogeni α sono acidi Gli idrogeni β, γ e δ non sono acidi non possono essere rimossi da una base acido non acidi α β γ δ 2 Enoli Tutti i composti
Enoli e Enolati 1 Idrogeni in α a un carbonile Solo gli idrogeni α sono acidi Gli idrogeni β, γ e δ non sono acidi non possono essere rimossi da una base acido non acidi α β γ δ 2 Enoli Tutti i composti
M: M +. + e. La risoluzione di un buon spettrometro di massa è 1 amu (atomic mass number) su10 4 amu.
 PIIPI DLLA SPTTMTIA DI MASSA A differenza delle altre tecniche analitiche (I, UVvis, M) in cui il campione rimane intatto dopo l analisi, la spettrometria di massa, che forma ed utilizza ioni invece di
PIIPI DLLA SPTTMTIA DI MASSA A differenza delle altre tecniche analitiche (I, UVvis, M) in cui il campione rimane intatto dopo l analisi, la spettrometria di massa, che forma ed utilizza ioni invece di
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
ALCHINI. legame π. Una frammentazione importante dà un valore m/z = 39, che corrisponde al carbocatione propargilico +. + R. +
 AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 9, che corrisponde al carbocatione propargilico.. 2 2 2 1-ottino 4-ottino
AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 9, che corrisponde al carbocatione propargilico.. 2 2 2 1-ottino 4-ottino
ALCHINI. Spettrometria di massa C CH 2 R. + CARATTERISTICA FUNZIONALE: legame π. Caratteristiche Spettrali
 AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 39, che corrisponde al carbocatione propargilico 2 +. +. + + 2 2 2
AATTEISTIA FUNZINALE: ALINI legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 39, che corrisponde al carbocatione propargilico 2 +. +. + + 2 2 2
Sostituzione nucleofila Addizione a gruppi carbonilici Addizione a doppi legami attivati
 himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
Alcani. Idrogenazione degli alcheni. Riduzione degli areni H 2. /Pt H 3. Ni + 3 H C, 180 atm
 Sintesi Alcani Idrogenazione degli alcheni 2 /Pt 2 /Pt 3 3 iduzione degli areni Ni + 3 2 175, 180 atm Alcheni Deidroalogenazione degli alogenuri alchilici 3 α 3 X β 3 Disidratazione degli alcoli Idrogenazione
Sintesi Alcani Idrogenazione degli alcheni 2 /Pt 2 /Pt 3 3 iduzione degli areni Ni + 3 2 175, 180 atm Alcheni Deidroalogenazione degli alogenuri alchilici 3 α 3 X β 3 Disidratazione degli alcoli Idrogenazione
Lezione: aldeidi e chetoni
 Lezione: aldeidi e chetoni Il gruppo funzionale carbonilico Nomenclatura Proprietà fisiche Principali reazioni eazioni con N eazioni con alcoli eazioni con tioli eazioni con ammine Tautomeria cheto-enolica
Lezione: aldeidi e chetoni Il gruppo funzionale carbonilico Nomenclatura Proprietà fisiche Principali reazioni eazioni con N eazioni con alcoli eazioni con tioli eazioni con ammine Tautomeria cheto-enolica
Benzene e Composti Aromatici
 Benzene e Composti Aromatici Contenuti della lezione: Il benzene e i requisiti per l aromaticità Nomenclatura di benzeni mono- e di-sostituiti Composti aromatici diversi dal benzene: IPA e eteroaromatici
Benzene e Composti Aromatici Contenuti della lezione: Il benzene e i requisiti per l aromaticità Nomenclatura di benzeni mono- e di-sostituiti Composti aromatici diversi dal benzene: IPA e eteroaromatici
REGISTRO DELLE LEZIONI 2005/2006. Tipologia. Addì Tipologia. Addì Tipologia
 Presentazione del corso, libri di testo esami e propedeuticità La struttura elettronica dell'atomo, gli orbitali, tipi di legami, regola dell'ottetto Ibridizzazione strutture di Lewis, carica formale,
Presentazione del corso, libri di testo esami e propedeuticità La struttura elettronica dell'atomo, gli orbitali, tipi di legami, regola dell'ottetto Ibridizzazione strutture di Lewis, carica formale,
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Composti carbonilici: reazioni al carbonio in posizione a
 Composti carbonilici: reazioni al carbonio in posizione a Addizione nucleofila a composti carbonilici a,b-insaturi Nelle molecole contenenti carbonili coniugati con doppi legami sono presenti due siti
Composti carbonilici: reazioni al carbonio in posizione a Addizione nucleofila a composti carbonilici a,b-insaturi Nelle molecole contenenti carbonili coniugati con doppi legami sono presenti due siti
Composti carbonilici
 Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Aldeidi e Chetoni. Proprietà Chimico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami H Bassi pesi molecolari sono solubili in acqua
 Aldeidi e hetoni ' Gruppo carbonilico Aldeide hetone Proprietà himico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami Bassi pesi molecolari sono solubili in acqua Nomenclatura IUPA :
Aldeidi e hetoni ' Gruppo carbonilico Aldeide hetone Proprietà himico Fisiche Sostanze Polari L ossigeno carbonilico forma forti legami Bassi pesi molecolari sono solubili in acqua Nomenclatura IUPA :
Esercitazione n Reazioni e meccanismi dei composti aromatici.
 sercitazione n. 1 Reazioni e meccanismi dei composti aromatici.. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del catalizzatore. Fe Fe Fe Fe. Il pdimetilbenzene
sercitazione n. 1 Reazioni e meccanismi dei composti aromatici.. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del catalizzatore. Fe Fe Fe Fe. Il pdimetilbenzene
Esercitazione n Reazioni e meccanismi di aldeidi e chetoni.
 19. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene tra etanale e metanolo, in presenza di acidi. b) Spiegare come varia la reattività se con metanolo si fa reagire l'aldeide
19. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene tra etanale e metanolo, in presenza di acidi. b) Spiegare come varia la reattività se con metanolo si fa reagire l'aldeide
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
COMPOSTI AROMATICI POLICICLICI
 CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
COMPOSTI AROMATICI. Formula C 6 H 6
 COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
miscela di reazione Si lava (estrae) con una base Si lava (estrae) con un acido Si lava (estrae) con acqua
 1. Si purificano (se necessario) reagenti e solventi.. Si mescolano i reagenti nelle opportune condizioni di reazione.. Si segue l andamento della reazione. 4. Si lavora la reazione. 5. Si analizza il
1. Si purificano (se necessario) reagenti e solventi.. Si mescolano i reagenti nelle opportune condizioni di reazione.. Si segue l andamento della reazione. 4. Si lavora la reazione. 5. Si analizza il
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Complementi di Chimica Organica. Composti Aromatici: Benzene C 6 H 6 (1825) (1865) Friedrich August Kekulé
 Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
La condensazione di Claisen
 La condensazione di Claisen Oltre alle aldeidi e chetoni anche gli esteri possono generare enolati e funzionare da elettrofili.. Quando un estere viene trattato con una base avviene una trasformazione
La condensazione di Claisen Oltre alle aldeidi e chetoni anche gli esteri possono generare enolati e funzionare da elettrofili.. Quando un estere viene trattato con una base avviene una trasformazione
Reazioni degli Alogenuri Alchilici. Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici.
 Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 L addizione coniugata In un sistema carbonilico α,β-insaturo dove avverà l attacco di un nucleofilo? Al carbonio carbonilico o al doppio legame? Il sistema ha due centri elettrofili: il carbonio carbonilico
L addizione coniugata In un sistema carbonilico α,β-insaturo dove avverà l attacco di un nucleofilo? Al carbonio carbonilico o al doppio legame? Il sistema ha due centri elettrofili: il carbonio carbonilico
Unità Didattica 10. I composti carbonilici. Struttura, nomenclatura e reattività
 I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
Idrocarburi AROMATICI
 Idrocarburi AROMATICI Composti aromatici Gli idrocarburi aromatici costituiscono una particolare classe di composti che contengono 2n 1 doppi legami coniugati in una struttura ciclica, strutturalmente
Idrocarburi AROMATICI Composti aromatici Gli idrocarburi aromatici costituiscono una particolare classe di composti che contengono 2n 1 doppi legami coniugati in una struttura ciclica, strutturalmente
Acidi carbossilici e derivati
 Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Composti carbonilici. Componente principale dell aceto. Principio attivo di molti farmaci. Resina per abbigliamento
 Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Stabilità del benzene (entalpie di idrogenazione) Energia di risonanza
 La chimica del benzene e dei suoi derivati I derivati del benzene vengono chiamati composti aromatici poiché inizialmente vennero isolati dal catrame nel 1800 ed erano caratterizzati da un odore aromatico.
La chimica del benzene e dei suoi derivati I derivati del benzene vengono chiamati composti aromatici poiché inizialmente vennero isolati dal catrame nel 1800 ed erano caratterizzati da un odore aromatico.
p p s sp sp sp s p p 1
 p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
Domanda 4 Dal punto di vista della reattività, il doppio legame si comporta spesso da:
 Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
Assorbimenti di alcani (stretching. Corso Metodi Fisici in Chimica Organica Prof. Renzo LUISI Uniba. vietata la vendita
 Assorbimenti di alcani (stretching C-H) Corso Metodi Fisici in Chimica rganica Prof. Renzo LUISI Uniba. vietata la vendita Analisi di spettri: ALCANI (C-H) 4000 3500 3000 2500 2000 1500 1300 1000 700 500
Assorbimenti di alcani (stretching C-H) Corso Metodi Fisici in Chimica rganica Prof. Renzo LUISI Uniba. vietata la vendita Analisi di spettri: ALCANI (C-H) 4000 3500 3000 2500 2000 1500 1300 1000 700 500
Esteri degli acidi carbossilici
 Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio.
 La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio. Proteine, zuccheri, lipidi, DNA.. farmaci arta, fibre, plastica s2p2 Z=6 2p 1s 2
La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio. Proteine, zuccheri, lipidi, DNA.. farmaci arta, fibre, plastica s2p2 Z=6 2p 1s 2
AMMINE R'' H H C 2 H 5 C H C H C H NH 2 H H. azoto. alifatici o aliciclici. ammina primaria ammina secondaria ammina terziaria N CH 3
 AMMIE Si chiamano primarie le ammine che hanno un solo gruppo alchilico o aromatico legato all azoto azoto. Sono secondarie e terziarie le ammine al cui atomo di azoto sono legate, rispettivamente,, due
AMMIE Si chiamano primarie le ammine che hanno un solo gruppo alchilico o aromatico legato all azoto azoto. Sono secondarie e terziarie le ammine al cui atomo di azoto sono legate, rispettivamente,, due
Alfa-alogenazionialogenazioni (sintesi aloformio)
 CHIMICA ACIDO-BASE DI COMPOSTI CARBONILICI Acidità: Acidità di acidi, ammidi, ammine. Effetti induttivi e di risonanza. Acidità CH Enoli/enolati Tautomeria cheto enolica (acido o base catalizzata) (isomerizzazioni
CHIMICA ACIDO-BASE DI COMPOSTI CARBONILICI Acidità: Acidità di acidi, ammidi, ammine. Effetti induttivi e di risonanza. Acidità CH Enoli/enolati Tautomeria cheto enolica (acido o base catalizzata) (isomerizzazioni
Aldeidi e chetoni. 1) Rottura α 2) Rottura i. Più pronunciate nei chetoni. 3) Rottura β con trasposizione di H in γ (McLafferty)
 Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
ACIDI CARBOSSILICI. ac. formico ac. acetico ac. benzoico
 ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
14/11/2018. Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile.
 Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
PIANO DELLE UDA Quarto Anno
 ITIS ENRICO MEDI PIANO DI STUDIO DELLA DISCIPLINA Chimica organica e biochimica (indirizzo biotecnologie ambientali) PIANO DELLE UDA Quarto Anno UDA COMPETENZE UDA ABILITÀ UDA CONOSCENZE UDA UDA N. 1 Titolo:
ITIS ENRICO MEDI PIANO DI STUDIO DELLA DISCIPLINA Chimica organica e biochimica (indirizzo biotecnologie ambientali) PIANO DELLE UDA Quarto Anno UDA COMPETENZE UDA ABILITÀ UDA CONOSCENZE UDA UDA N. 1 Titolo:
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile
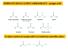 DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento
 PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
BENZENE E DERIVATI. Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6. Arene: Idrocarburo aromatico
 BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI
 REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
Composti carbonilici. Composti carbonilici. Componente principale dell aceto. Principio attivo di molti farmaci. Resina per abbigliamento
 Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
Composti carbonilici. Componente principale dell aceto. Principio attivo di molti farmaci. Resina per abbigliamento
 Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci Resina per abbigliamento
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
ALCHENI ALCHINI, ALCADIENI, CICLOALCHENI, CICLOALCADIENI ADDIZIONE
 ALNI ALINI, ALADINI, ILALNI, ILALADINI ARATTRISTIA FUNZINAL: legame π Più debole del legame σ, è il punto debole degli alcheni. la rottura del legame π porta a due valenze libere sui due atomi di, che
ALNI ALINI, ALADINI, ILALNI, ILALADINI ARATTRISTIA FUNZINAL: legame π Più debole del legame σ, è il punto debole degli alcheni. la rottura del legame π porta a due valenze libere sui due atomi di, che
AMMINE. con acidi RNH 2. con O come elettrofilo RNH 2 + H + + R NH 3 NESSUNA REAZIONE. atomo basico, atomo nucleofilo
 AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri)
 CHIMICA ACIDO BASE DI COMPOSTI CARBONILICI Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri) Che altra reazione può avvenire al centro carbonilico
CHIMICA ACIDO BASE DI COMPOSTI CARBONILICI Produzione di enolati: deprotonazione al carbonio in alfa a un gruppo carbonilico (aldeidi, chetoni, esteri) Che altra reazione può avvenire al centro carbonilico
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab.
 I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
REATTIVITA DEI BENZENI SOSTITUITI
 REATTIVITA DEI BENZENI SOSTITUITI 1) Sostituzione radicalica di idrogeni benzilici Reazioni dei sostituenti presenti sull anello benzenico Reazioni dei sostituenti presenti sull anello benzenico 2) Reazioni
REATTIVITA DEI BENZENI SOSTITUITI 1) Sostituzione radicalica di idrogeni benzilici Reazioni dei sostituenti presenti sull anello benzenico Reazioni dei sostituenti presenti sull anello benzenico 2) Reazioni
Derivati degli acidi carbossilici
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Derivati degli acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Derivati degli acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze
I composti acilici sono tutti quei composti che contengono il gruppo:
 omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
REAZIONI DEGLI ALCHENI
 REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
Idrocarburi Saturi. Reazioni
 Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Stabilità. 1. più sostituito = più stabile. 2. trans più stabile del cis; E più stabile del Z. II. Relazione struttura-reattività R C R R R
 Alcheni 1 II. Relazione struttura-reattività 1. più sostituito = più stabile Stabilità R R R R R > > R R, R 2 2 > R 2 > R R 2 2 2. trans più stabile del cis; E più stabile del Z repulsione trans-2-butene
Alcheni 1 II. Relazione struttura-reattività 1. più sostituito = più stabile Stabilità R R R R R > > R R, R 2 2 > R 2 > R R 2 2 2. trans più stabile del cis; E più stabile del Z repulsione trans-2-butene
Reazioni di radicali. Reazioni di propagazione Reazioni di terminazione
 Reazioni di radicali Reazioni di propagazione Reazioni di terminazione Reazioni di propagazione Processi di trasferimento di radicali coinvolgono un radicale ed una molecola di substrato e portano alla
Reazioni di radicali Reazioni di propagazione Reazioni di terminazione Reazioni di propagazione Processi di trasferimento di radicali coinvolgono un radicale ed una molecola di substrato e portano alla
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Reattività degli alogenuri alchilici: Reazioni di sostituzione nucleofila alifatica Reazioni di eliminazione
 Reattività degli alogenuri alchilici: Reazioni di sostituzione nucleofila alifatica Reazioni di eliminazione Queste reazioni hanno rilevanza prevalentemente per la sintesi organica Nucleofilo OH - Alogenuri
Reattività degli alogenuri alchilici: Reazioni di sostituzione nucleofila alifatica Reazioni di eliminazione Queste reazioni hanno rilevanza prevalentemente per la sintesi organica Nucleofilo OH - Alogenuri
ALDEIDI e CHETONI. O sp 2 legato a C sp 2. Lo ione molecolare di solito è osservabile, sia con le aldeidi che con i chetoni.
 19/05/014 aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che
19/05/014 aratteristica strutturale di aldeidi e chetoni ALDEIDI e ETI sp legato a sp = aratteristiche Spettrali Spettrometria di massa Lo ione molecolare di solito è osservabile, sia con le aldeidi che
Composti AROMATICI. Il Puzzle del Benzene. + Br 2 dà reazione di sostituzione elettrofila C 6. Br + H 2 H 12
 Composti AMATICI Dallo studio degli olii essenziali viene scoperta una nuova classe di composti con un elevato rapporto C /, chiamati AMATICI per il piacevole odore. Il Puzzle del Benzene C 6 6 relativamente
Composti AMATICI Dallo studio degli olii essenziali viene scoperta una nuova classe di composti con un elevato rapporto C /, chiamati AMATICI per il piacevole odore. Il Puzzle del Benzene C 6 6 relativamente
+ + H 2 O NH 3 + H 3 2) NH 4 O + O + + CH 3 3) H 2 H H 3 O + CH 3. Esercitazione n Reazioni acido-base. ACIDO ACIDO ACIDO O + H H 2
 Esercitazione n. 10 Reazioni acidobase. 3. Nelle seguenti reazioni acidobase individuare l'acido e la base: 1) N : 3 2 N 4 2 2) N 4 2 N 3 3 3) 2 2 3 2 BASE 4) BASE AID AID AID BASE N N BASE AID 2 6) 5)
Esercitazione n. 10 Reazioni acidobase. 3. Nelle seguenti reazioni acidobase individuare l'acido e la base: 1) N : 3 2 N 4 2 2) N 4 2 N 3 3 3) 2 2 3 2 BASE 4) BASE AID AID AID BASE N N BASE AID 2 6) 5)
Classi di composti: derivati carbonilici
 Classi di composti: derivati carbonilici Bande di controllo/conferma zona di stiramento del carbonile 59 Tabella sinottica della posizione della banda di stiramento del carbonile e della posizione delle
Classi di composti: derivati carbonilici Bande di controllo/conferma zona di stiramento del carbonile 59 Tabella sinottica della posizione della banda di stiramento del carbonile e della posizione delle
Classi di composti: derivati carbonilici
 Classi di composti: derivati carbonilici Bande di controllo/conferma zona di stiramento del carbonile 62 Tabella sinottica della posizione della banda di stiramento del carbonile e della posizione delle
Classi di composti: derivati carbonilici Bande di controllo/conferma zona di stiramento del carbonile 62 Tabella sinottica della posizione della banda di stiramento del carbonile e della posizione delle
Unità didattica 6. Cosa è una sostutizione? Reazioni di Sostituzione degli Alogenuri Alchilici
 Cosa è una sostutizione? Unità didattica 6 Reazioni di Sostituzione degli Alogenuri Alchilici Capitolo 7 e 8 di Brown e Poon L atomo o il gruppo che è sostituito o eliminato in queste reazioni è detto
Cosa è una sostutizione? Unità didattica 6 Reazioni di Sostituzione degli Alogenuri Alchilici Capitolo 7 e 8 di Brown e Poon L atomo o il gruppo che è sostituito o eliminato in queste reazioni è detto
R-X ALOGENURI ALCHILICI. F Cl Br I. Nomenclatura. In genere si indicano con. + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo
 ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
CLASSIFICAZIONE DEI TIPI DI REATTIVITA'
 riepilogo delle reazioni organiche LASSIFIAZIN DI TIPI DI ATTIVITA' UNA AZIN IMIA MPTA LA TTUA / LA FMAZIN DI LGAMI La scissione di un legame covalente può avvenire in due modi diversi: 1. LA PPIA DI LTTNI
riepilogo delle reazioni organiche LASSIFIAZIN DI TIPI DI ATTIVITA' UNA AZIN IMIA MPTA LA TTUA / LA FMAZIN DI LGAMI La scissione di un legame covalente può avvenire in due modi diversi: 1. LA PPIA DI LTTNI
Ammine. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
PROGRAMMA SVOLTO ANNO SCOLASTICO 2018/2019
 Nome docenti Materia insegnata Classe Testi adottati Dispense e materiali forniti dal docente Stefano BOTTIGLIENGO, Giuseppe SURANO CHIMICA ORGANICA E BIOCHIMICA 4EI (Istituto: Tecnico - Settore: Tecnologico
Nome docenti Materia insegnata Classe Testi adottati Dispense e materiali forniti dal docente Stefano BOTTIGLIENGO, Giuseppe SURANO CHIMICA ORGANICA E BIOCHIMICA 4EI (Istituto: Tecnico - Settore: Tecnologico
Acidi carbossilici: nomenclatura. alcano -> acido alcanoico
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Si trovano generalmente come dimeri ciclici a causa dei legami a idrogeno
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di:
 Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
