ELEMENTI DI CHIMICA ORGANICA
|
|
|
- Eva Paoli
- 7 anni fa
- Visualizzazioni
Transcript
1 ELEMENTI DI IMIA RGANIA La himica rganica è la chimica dei composti del carbonio, fatta eccezione per alcuni composti quali il monossido di carbonio (), il biossido di carbonio ( 2 ), i carbonati ( 3 - ) etc. Nei composti organici gli atomi di carbonio sono legati sia tra di loro che con atomi di altri elementi quali idrogeno, ossigeno, azoto, zolfo, alogeni. In tutti i composti organici gli atomi di carbonio sono sempre tetravalenti e possono presentare ibridazione tetraedrica (sp 3 ), trigonale (sp 2 ) o digonale (sp). I composti del carbonio si possono dividere in classi di composti organici. Gli Idrocarburi Gli idrocarburi sono composti organici formati soltanto da due elementi: il carbonio e l idrogeno ed in base alla loro struttura si dividono in due classi: gli idrocarburi alifatici e gli idrocarburi aromatici. A loro volta gli idrocarburi alifatici si dividono in alcani, alcheni, alchini (idrocarburi a catena aperta) e in idrocarburi cicloalifatici (idrocarburi a catena chiusa). Le fonti di approvvigionamento degli idrocarburi sono il petrolio e il gas naturale: dal petrolio di estraggono principalmente alcani, cicloalcani e idrocarburi aromatici mentre dal gas naturale si estrae principalmente il metano. Alcani aratteristiche generali: negli alcani ogni atomo di carbonio ha ibridazione tetraedrica (sp 3 ) e forma 4 legami con atomi di carbonio o idrogeno mediante legami σ, derivanti dalla sovrapposizione di un orbitale di tipo sp 3 del con un orbitale di tipo sp 3 di un atomo di oppure dalla sovrapposizione di un orbitale di tipo sp 3 del con un orbitale di tipo s del. Gli alcani hanno scarsa reattività, essendo costituiti da legami molto forti, infatti l energia di legame - è di 360 KJ/mol; per questo sono noti anche con il nome di paraffine. Vengono inoltre chiamati idrocarburi saturi poiché formano solo legami semplici. Formula generale: n 2n+2 ; costituiscono una serie omologa poiché differiscono per il termine 2. Riportiamo gli omologhi della famiglia degli alcani fino ad n =8: si osserva che ciascun membro differisce dal successivo per il termine Nomenclatura IUPA: ad eccezione dei primi quattro membri della famiglia che si chiamano metano, etano, propano e butano, il nome degli omologhi superiori deriva da: prefisso greco che indica il numero di atomi di + desinenza -ano Nome degli alcani Formula metano 4 etano 2 6 propano 3 8 butano
2 pentano 5 12 esano 6 14 eptano 7 16 ottano 8 18 Isomeri Strutturali: quando il numero di numero di atomi di è uguale o superiore a 4 si possono avere isomeri strutturali (hanno uguale formula bruta ma diversa formula molecolare) e quindi si usano dei prefissi per distinguerli: n = normale iso = uguale sec = secondario ter = terziario Ad esempio: formula generale: 4 10 isomeri strutturali: 2 2 formula generale: 5 12 isomeri strutturali: n-butano isobutano n-pentano isopentano neopentano Gli isomeri struttuali presentano temperature di fusione ed ebollizione che aumentano all aumentare del peso molecolare. Essi presentano, inoltre, proprietà chimico-fisiche diverse; ad esempio, all aumentare della ramificazione le temperature di ebollizione diminuiscono per la diminuzione delle forze intermolecolari di London e per la diminuzione della polarizzabilità. Qualora nella catena dell alcano siano presenti dei gruppi sostituenti, chiamati gruppi o radicali alchilici (gruppi di atomi che compongono solo parte della molecola) è opportuno indicarne il nome e la posizione all interno della catena. Gruppo o radicale alchilico: un gruppo funzionale corrispondente ad un alcano privo di un atomo di idrogeno; la formula generale è n 2n+1. Mantengono il nome dell alcano + desinenza ile Nome dei radicali alchilici Formula metile - etile propile butile pentile esile Quando il numero di numero di atomi di è uguale o superiore a 3 si possono avere isomeri strutturali (uguale formula bruta ma diversa formula molecolare) che andranno distinti utilizzando dei prefissi: Ad esempio: formula generale: isomeri strutturali: 2 2 n-propile isopropile 2
3 formula generale: isomeri strutturali: n-butile sec-butile 2 isobutile ter-butile Regole IUPA per la denominazione degli alcani che presentino in catena dei gruppi alchilici o altri sostituenti: 1) si sceglie come struttura base la ATENA LINEARE PIU LUNGA, dando la denominazione dell alcano; 2) se la struttura è ramificata, si indica la PSIZINE E IL NUMER dei gruppi alchilici che formano la ramificazione 3) la NUMERAZINE della catena deve iniziare dall estremità più vicina al sostituente; metil-pentano 4) se lo stesso gruppo compare più di una volta in catena si usano i prefissi di- (2 volte), tri- (3 volte), tetra- (4 volte) ; 2 2,2,4-trimetil-pentano 5) se sono presenti gruppi alchilici diversi si indicano in RDINE di GRANDEZZA RESENTE Fonti: gli alcani si estraggono dal petrolio. 2 2-metil-3-etileptano Preparazione: possono essere sintetizzati da una miscela di idrogeno molecolare ( 2 ) e monossido di carbonio () anche nota con il nome di gas di sintesi. La reazione avviene in presenza di catalizzatori (ad esempio Nichel o Ferro) e ad alta temperatura ( ). Reazione di sintesi del metano: (g) (g) 4 (g) + 2 (g) Proprietà: gli alcani sono molecole apolari (quindi lipofile) poiché si sciolgono in solventi apolari (ad esempio il benzene o il tetracloruro di carbonio) e sono poco solubili o insolubili in solventi polari (idrofili) quali l acqua e il metanolo. Reattività: - danno reazioni di combustione con 2, violente ed esotermiche; - danno reazioni di sostituzione con alogeni, formando ad esempio il freon, F x l 4-x. 3
4 Alcheni aratteristiche generali: negli alcheni vi sono almeno 2 atomi di con ibridazione trigonale (sp 2 ) che formano un doppio legame = costituito da un legame forte di tipo σ e da un legame più debole di tipo π. L energia di dissociazione del legame = è di 611 KJ/mol. Gli alcheni vengono anche chiamati olefine e sono idrocarburi insaturi per la presenza del doppio legame tra due atomi di carbonio. Formula generale: n 2n (n 2); costituiscono una serie omologa poiché differiscono per il termine 2. Nomenclatura IUPA: il nome degli alcheni deriva da quello degli alcani con l uso però della desinenza ene. Può capitare che il nome sia preceduto da un numero che indichi la posizione del doppio legame (che deve sempre avere il numero più piccolo). Nome degli alcheni Formula etene 2 4 propene butene butene = 2 2 = 2 2 = 2 = etene propene 1-butene 2-butene (etilene) (propilene) Radicali alchilici: formula generale n 2n-1 ; mantengono il nome dell alchene + desinenza ile. Il più importante è il vinile, 2 =. Dieni o diolefine: se sono presenti due doppi legami si tratta di dieni: 2 == 1,2-butadiene Se i due doppi legami sono separati da un legame singolo si tratta di dieni coniugati: 2 = = 2 1,3-butadiene In questo caso gli elettroni π sono delocalizzati tra tutti gli atomi di carbonio che costituiscono i doppi legami coniugati. Isomeri Geometrici: poiché la rotazione tra due atomi di carbonio impegnati in un doppio legame è impedita dalla presenza del legame π che imporrebbe la rottura del legame π in questione, si hanno isomeri geometrici (stessa formula molecolare, diversa struttura, diversa disposizione spaziale). Es. Isomeri geometrici del 2-butene: 3 cis-2-butene trans-2-butene Nell isomero cis i due atomi o gruppi uguali (ad es. i due atomi di ) sono dalla stessa parte del doppio legame, mentre nell isomero trans i due gruppi uguali sono da parti opposte. 4
5 Fonti: gli alcheni si ottengono dal cracking del petrolio, tramite reazione di deidrogenazione (reazione di eliminazione di due atomi di idrogeno): calore es: 2 2 = propano propene Proprietà: gli alcheni hanno proprietà fisiche simili agli alcani, sono molecole apolari quindi solubili in solventi apolari (ad es. benzene, l 4 ) e insolubili in solventi polari (ad es. acqua e metanolo). Le temperature di ebollizione aumentano all aumentare del numero di atomi di carbonio. La presenza di ramificazioni fa diminuire le temperature di ebollizione per la diminuzione delle forze intermolecolari di London e la diminuzione della polarizzabilità Reattività: - danno reazioni di addizione con rottura dei legami π e formazione di nuovi legami; calore es: 2 = etilene etano - danno reazioni di polimerizzazione con rottura del doppio legame e addizione di più molecole di alchene. Ad esempio dall etilene si può ottenere il polietilene formato dall unità strutturale ( 2 2 ) n. Alchini aratteristiche generali: negli alchini vi sono almeno 2 atomi di con ibridazione digonale (sp) che formano un triplo legame costituito da un legame forte di tipo σ e da due legami più deboli di tipo π. L energia di dissociazione del legame = è di 830 KJ/mol. Gli alchini sono idrocarburi insaturi per la presenza del triplo legame tra due atomi di carbonio. Formula generale: n 2n-2 (n 2); costituiscono una serie omologa poiché differiscono per il termine 2. Nomenclatura IUPA: il nome degli alchini deriva da quello degli alcani con l uso però della desinenza ino. Può capitare che il nome sia preceduto da un numero che indichi la posizione del triplo legame (che deve sempre avere il numero più piccolo). Nome degli alcheni Formula Etino 2 2 Propino 3 4 etino propino 4-metil-2-pentino (acetilene) (metilacetilene) Radicali alchilici: formula generale n 2n-3 ; mantengono il nome dell alchino + desinenza ile. Il più importante è l etinile,. Proprietà: gli alchini hanno proprietà fisiche simili ad alcani ed alcheni, sono molecole apolari quindi solubili in solventi apolari (ad es. benzene) e insolubili in solventi polari (ad es. acqua e metanolo). Le temperature di ebollizione aumentano all aumentare del numero di atomi di carbonio. La presenza di ramificazioni fa diminuire le temperature di ebollizione per la diminuzione delle forze intermolecolari di London e la diminuzione della polarizzabilità Reattività: hanno reattività simile agli alcheni essendo anch essi idrocarburi insaturi. 5
6 Idrocarburi icloalifatici aratteristiche generali: si tratta di composti organici in cui gli atomi di carbonio sono disposti in modo da formare degli anelli, si tratta infatti di composto ciclici. Gli idrocarburi alifatici si possono classificare come cicloalcani, cicloalcheni e cicloalchini (più rari). Nomenclatura IUPA: il nome degli idrocarburi alifatici deriva da quello degli idrocarburi corrispondenti a catena aperta ciclopropano ciclobutano cicloesano ciclopentene Proprietà: gli idrocarburi alifatici hanno proprietà chimiche e fisiche simili a quelle dei corrispondenti idrocarburi a catena aperta. Gli idrocarburi ciclo alifatici con anelli di 3/4 atomi di carbonio hanno una reattività chimica elevata (superiore a quella degli omologhi a catena aperta) perché hanno un contenuto energetico maggiore a causa della tensione d anello. Fonti: i cicloalcani (anche noti con il nome di nafteni) si ottengono per distillazione del petrolio. Idrocarburi Aromatici aratteristiche generali: si tratta di composti organici caratterizzati dalla presenza di un anello ciclico planare stabilizzato da un sistema di elettroni π. Tutti gli atomi di carbonio che formano l anello hanno ibridazione trigonale (sp 2 ) per questo di tratta di idrocarburi insaturi. apostipite di questa classe di composti è il benzene, la cui formula molecolare è 6 6 e viene rappresentato in questi modi: Tutti e dodici gli atomi del benzene (6 di e di ) giacciono sullo stesso piano. Tutte le distanze di legame carbonio-carbonio sono uguali poiché la molecola del benzene può essere descritta come un ibrido di risonanza di due strutture, caratterizzate dalla delocalizzazione degli elettroni π tra tutti gli atomi di carbonio: Le due strutture di risonanza (formule di Kekulé) sono energeticamente equivalenti e a destra viene rappresentata la media delle due strutture. Per sostituzione di uno o più atomi di con uno o più gruppi sostituenti, si ottengono diverse tipologie di derivati. 6
7 Derivati monosostituiti: un solo atomo di idrogeno è stato sostituito da un altro atomo o gruppo sostituente. Nomenclatura: prefisso che indica il nome del sostituente + benzene (tra parentesi i nomi comuni). N 2 metilbenzene idrossibenzene amminobenzene carbossibenzene (toluene) (fenolo) (anilina) (acido benzoico) l N 2 2 vinilbenzene clorobenzene nitrobenzene (stirene) Derivati disostituiti: per sostituzione di due atomi di idrogeno con due gruppi uguali o diversi si possono ottenere fino a 3 derivati che sono isomeri. Nomenclatura: si usano i prefissi per indicare la posizione dei sostituenti nell anello. orto (o-) i due sostituenti sono in posizione adiacente meta (m-) i due sostituenti sono separati da un atomo di carbonio para (p-) i due sostituenti sono contrapposti o-xilene m-xilene p-xilene Derivati trisostituiti: vengono sostituiti 3 atomi di con altrettanti atomi o gruppi sostituenti. Nomenclatura: prefisso che indica la posizione del sostituente + benzene. Br Br 2 N N 2 Br 1,2,4-tribromobenzene 2,6-dinitrotoluene Radicale arilico: formula generale 6 5 il cui nome è gruppo fenile. omposti aromatici ad anelli condensati: naftalene antracene Fonti: il benzene e gli alchilbenzeni si ottengono dalla distillazione del petrolio. 7
8 Proprietà: gli idrocarburi aromatici sono molecole apolari quindi solubili in solventi apolari (ad es. benzene) e insolubili in solventi polari (ad es. acqua e metanolo). Reattività: hanno reattività diversa dagli altri idrocarburi insaturi (alcheni e achini) poiché non danno reazioni di rottura dei doppi legami ma solo reazioni di sostituzione. Gruppi funzionali Atomi o gruppi di atomi che introdotti in una catena idrocarburica o in un anello idrocarburico ne determinano il comportamento chimico. Ad. Esempio il doppio legame negli alcheni e il triplo legame negli alchini. lassi di composti organici contenenti eteroatomi: azoto, ossigeno, alogeni. lassi di composti Gruppo funzionale Formula generale Alogenuri -X (l, F, Br, I) R-X Alcoli - R- Eteri -- R--R Aldeidi hetoni Acidi arbossilici Esteri Anidridi R-- R--R' R-- R---R' R----R' Ammine -N 2 R-N 2 Ammidi --N 2 R--N 2 Alogenuri Formula generale: R-X alogenuri alchilici alogenuri arilici (R = alchile) (R = arile) Nomenclatura per gli alogenuri alchilici IUPA: si considerano derivati dagli idrocarburi Tradizionale: si considerano come acidi alogenidrici (tra parentesi i nomi secondo la nomenclatura tradizionale) 8
9 Br 2 =l l 2 F 2 l 4 bromometano cloroetene diclorodifluorometano tetraclorometano (bromuro di metile) (cloruro di vinile) (tetracloruro di carbonio) 2 l 2 l 3 diclorometano triclorometano (cloruro di metilene) (cloroformio) Nomenclatura per gli alogenuri arilici prefisso che indica il nome del sostituente + nome benzene. Ad esempio 6 5 l, il clorobenzene. Formula generale: R- Alcoli Nomenclatura: R = alchile IUPA: nome idrocarburo + desinenza olo; la posizione del gruppo ossidrile viene indicata da un numero (il più piccolo possibile). Tradizionale: vengono chiamati alcoli (tra parentesi i nomi secondo la nomenclatura tradizionale ) metanolo etanolo 1-propanolo 2-propanolo (alcool metilico) (alcool etilico) (alcool n-propilico) (alcool isopropilico) Nomenclatura: R = arile vengono chiamati fenoli il cui capostipite è il fenolo di formula generale 6 5. La presenza del gruppo aromatico modifica le caratteristiche chimico-fisiche, sono infatti acidi deboli. Proprietà: sono diverse da quelle degli idrocarburi per la presenza del gruppo che è molto polare e favorisce la solubilità in acqua per la formazione di forze intermolecolari, i legami a idrogeno. Gli alcoli inferiori (metanolo, etanolo, propanolo) sono completamente solubili in acqua; per gli alcoli superiori la solubilità diminuisce all aumentare del numero di atomi di carbonio. atene di 6 atomi di sono completamente insolubili in acqua. Le temperature di ebollizione sono superiori a quelle degli idrocarburi a causa del legami a idrogeno relativamente forti che si formano tra molecole di alcoli, mentre negli idrocarburi sono presenti solo deboli interazioni di Van der Walls. Il legame è polare δ δ+ e gli alcoli sono debolmente acidi. Alcoli poliossidrilati: contengono più di un gruppo ossidrilico e sono solubili in acqua. Si dividono in dioli: contengono 2 gruppi ossidrilici e vengono anche chiamati glicoli trioli: contengono 3 gruppi ossidrilici e vengono anche chiamati glicerine 2 2 1,2-etandiolo (glicole etilenico) 2 2 1,2,3-propantriolo (glicerina o glicerolo) 9
10 Eteri Formula generale: R--R (R, R possono essere gruppi alchilici o arilici). Nomenclatura: IUPA: nome del gruppo R (chiamato gruppo alcossi) precede il nome della catena idrocarburica R. Tradizionale: il nome dei due gruppi R ed R precedono la parola etere (tra parentesi i nomi secondo la nomenclatura tradizionale) etossietano metossietano (etere dietilico o etere etilico) (etil metil etere) (etere difenilico) Proprietà: Gli eteri sono parzialmente solubili in acqua per la formazione di legami a idrogeno tra l atomo di ossigeno dell etere e l atomo di idrogeno dell acqua. Gli eteri sono composti polari poiché l angolo -Ô- è inferiore a 180. Aldeidi e hetoni aratteristiche generali: sono caratterizzati dalla presenza del gruppo carbonilico = in cui il carbonio ha ibridazione trigonale (sp 2 ). Il doppio legame -= è formato da un legame forte di tipo σ e da un legame più debole di tipo π. Gli angoli di legame sono di 120. Il legame -= è polare a causa della diversa elettronegatività tra carbonio e ossigeno, l atomo di è leggermente positivo mentre l atomo di è leggermente negativo: δ+ δ Aldeidi Formula generale: R--, la struttura può essere così rappresentata: R Nomenclatura: IUPA: nome idrocarburo + desinenza -ale. Tradizionale: mantengono il nome di aldeidi (tra parentesi i nomi secondo la nomenclatura tradizionale) metanale etanale (formaldeide) (acetaldeide) (benzaldeide) Usi: la formaldeide viene utilizzata nell industria per la preparazione di alcuni polimeri. Preparazione: si ottengono dall ossidazione degli alcoli. Formula generale: R--R' hetoni, la struttura può essere così rappresentata: R' Nomenclatura: IUPA: nome idrocarburo + desinenza -one. Eventualmente la posizione del gruppo carbonile è indicata da un numero, il più piccolo possibile. R 10
11 Tradizionale: mantengono il nome di chetoni (tra parentesi i nomi secondo la nomenclatura tradizionale) propanone (dimetilchetone o acetone) 2 2-butanone (metil etil chetone) Usi: vengono utilizzati come solventi. Preparazione: si ottengono dall ossidazione degli alcoli. Acidi arbossilici Formula generale: R--, dove R può essere un gruppo alchilico (acidi alifatici) o arilico (acidi aromatici); la struttura può essere così rappresentata: R Nomenclatura: IUPA: denominazione acido + nome idrocarburo con desinenza oico (tra parentesi i nomi secondo la nomenclatura tradizionale). 2 acido metanoico acido etanoico acido propanoico acido benzoico (acido formico) (acido acetico) (acido propionico) Preparazione: si ottengono dall ossidazione degli alcoli. Proprietà: la presenza del gruppo che è molto polare conferisce solubilità in acqua per la formazione di legami a idrogeno, sia molecole di acido che con altre molecole come l acqua. Gli acidi carbossilici con catene fino a 4 atomi di sono completamente solubili in acqua; la solubilità diminuisce all aumentare del numero di atomi di carbonio. Gli acidi monocarbossilici sono acidi deboli. Reattività: è essenzialmente legata alla presenza del gruppo per cui possono avere reazioni acido-base (con perdita di uno ione + ) o reazioni di sostituzione del gruppo ossidrile con un altro gruppo (ad. esempio N 2 per formare le ammidi). Reazioni acido-base: o o in acqua si ionizzano producendo lo ione carbossilato, R - R- + 2 R lo ione carbossilato è stabilizzato per delocalizzazione della carica negativa tra i due atomi di ossigeno: R - R - strutture di risonanza R ibrido di risonanza trattati con basi formano dei sali il cui nome si ottiene dal nome dell acido con l uso della desinenza ato: + Na - Na acetato di sodio 11
12 Esteri Formula generale: R--R', la struttura può essere così rappresentata: R Nomenclatura: R' IUPA: si utilizza il nome dell acido con desinenza ato cui segue il nome del gruppo R. 2 5 acetato di metile benzoato di etile Anidridi di acidi carbossilici Formula generale: (R) 2 Preparazione: si ottengono per perdita di acqua da due molecole di acido carbossilico anidride acetica Ammine Si dividono in tre classi a seconda del numero di atomi di idrogeno che sono stati sostituiti da un gruppo R nella molecola di ammoniaca, N 3. Primarie: RN 2 Secondarie: R 2 N Terziarie: R 3 N Si dividono inoltre in ammine alifatiche se R = gruppo alchilico ammine aromatiche se R = gruppo arilico Nomenclatura: si specificano i nomi dei gruppi R + suffisso ammina N 2 N N N metilammina dimetilammina trimetilammina difenilammina Proprietà: sono composti polari e possono formare legami a idrogeno sia tra loro (ad eccezione delle terziarie) che con altre molecole come l acqua. Le ammine con catene fino a 6 atomi di sono completamente solubili in acqua. Reattività: reagiscono con acidi e danno sali solubili in acqua. 12
13 Ammidi Formula generale: RN 2, la struttura può essere così rappresentata: R N 2 Nomenclatura: IUPA: si utilizza il nome dell acido con la desinenza ammide. N 2 N 2 acetammide benzammide Ammidi N-sostituite: quando l atomo di azoto è legato a gruppi sostituenti R e non ad atomi di. R N R' R N R' R'' ad esempio: N N,N-dimetilformammide 13
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
Riassunto delle lezioni precedenti..
 Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
La chimica organica. La chimica organica è la chimica dei composti del carbonio.
 La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
ALIFATICI AROMATICI (Areni) POLIENI BENZENE e derivati CICLOALCHENI CICLOALCANI ALCHINI
 CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Idrocarburi Saturi. Alcani
 Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1
 Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
2. Gli Idrocarburi IDROCARBURI. solo C e H. alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp 2 ) Alifatici
 2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
Nomi e formule dei principali composti organici
 Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Nomi e formule dei principali composti organici
 Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
CHIMICA ORGANICA. Gli idrocarburi aromatici
 1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
IDROCARBURI. Alcani Alcheni Alchini Areni. Tipo di legami carboniocarbonio. Solo legami semplici. Uno o più tripli legami. Uno o più doppi legami
 IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
Ammine N R N R R R-NH 2. Gruppo funzionale: NH 2. Gruppo amminico. Ammine terziarie. Ammine primarie. Ammine secondarie
 Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
DAI GRUPPI FUNZIONALI AI POLIMERI
 DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
CORSO PROPRIETA DEI MATERIALI PER L OTTICA CENNI DI CHIMICA ORGANICA
 CORSO PROPRIETA DEI MATERIALI PER L OTTICA CENNI DI CHIMICA ORGANICA INTRODUZIONE LA CHIMICA ORGANICA E LO STUDIO DELLA CHIMICA DEI COMPOSTI DEL CARBONIO. QUASI TUTTI GLI ELEMENTI DELLA TAVOLA PERIODICA
CORSO PROPRIETA DEI MATERIALI PER L OTTICA CENNI DI CHIMICA ORGANICA INTRODUZIONE LA CHIMICA ORGANICA E LO STUDIO DELLA CHIMICA DEI COMPOSTI DEL CARBONIO. QUASI TUTTI GLI ELEMENTI DELLA TAVOLA PERIODICA
CHIMICA ORGANICA. PON C1 di SCIENZE. Esperto prof. C. Formica
 CHIMICA ORGANICA PON C1 di SCIENZE Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it,
CHIMICA ORGANICA PON C1 di SCIENZE Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it,
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
CHIMICA ORGANICA. Gli alchini
 1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
PROPRIETA FISICHE DEI COMPOSTI ORGANICI
 PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
Classificazione degli idrocarburi
 Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA delle MACROMOLECOLE BIOLOGICHE
 Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
Gli idrocarburi e il petrolio
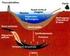 Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
Gli Alcheni. Ibridazione sp 2. I legami chimici degli alcheni
 Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
Chimica Organica. Breve storia della chimica organica
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
23 Le diverse classi di composti organici
 23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
GLI ALCANI. Michele Kodrič
 GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA
 Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Idrocarburi alifatici
 Idrocarburi alifatici Gli idrocarburi Gli idrocarburi sono composti organici costituiti esclusivamente da atomi di carbonio e idrogeno. In base alla loro struttura si suddividono in due grandi gruppi:
Idrocarburi alifatici Gli idrocarburi Gli idrocarburi sono composti organici costituiti esclusivamente da atomi di carbonio e idrogeno. In base alla loro struttura si suddividono in due grandi gruppi:
Verifiche dei Capitoli - Tomo C
 Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Approccio alla CHIMICA ORGANICA. Chimica organica: gli idrocarburi I gruppi funzionali. Paolo Pistarà, Principi di chimica moderna - Tomo A ATLAS
 Approccio alla IMIA ORGANIA himica organica: gli idrocarburi I gruppi funzionali IMIA ORGANIA: GLI IDROARBURI ompetenze Distinguere gli idrocarburi in base al legame covalente (singolo, doppio, triplo)
Approccio alla IMIA ORGANIA himica organica: gli idrocarburi I gruppi funzionali IMIA ORGANIA: GLI IDROARBURI ompetenze Distinguere gli idrocarburi in base al legame covalente (singolo, doppio, triplo)
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Capitolo 23 Dal carbonio agli idrocarburi
 Capitolo 23 Dal carbonio agli idrocarburi 1. I composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani 3. L isomeria 4. La nomenclatura degli idrocarburi saturi 5. Proprietà fisiche e chimiche
Capitolo 23 Dal carbonio agli idrocarburi 1. I composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani 3. L isomeria 4. La nomenclatura degli idrocarburi saturi 5. Proprietà fisiche e chimiche
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società CdL in Scienze delle attività motorie e sportive
 Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Chimica Organica. In passato, i composti chimici erano suddivisi in due grandi gruppi,
 Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
IDROCARBURI ALIFATICI
 CHIMICA ORGANICA (Lezioni in classe prof. Adriano Muschiato) Nel 1828 il chimico tedesco Friedrich Wöhler per la prima volta riesce a sintetizzare da reagenti inorganici l UREA: Nel sud della Germania
CHIMICA ORGANICA (Lezioni in classe prof. Adriano Muschiato) Nel 1828 il chimico tedesco Friedrich Wöhler per la prima volta riesce a sintetizzare da reagenti inorganici l UREA: Nel sud della Germania
Gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
ALCANI metano. etano. pentano. butano. propano. Idrocarburo: molecola contenente solo carbonio ed idrogeno
 ALCANI Idrocarburo: molecola contenente solo carbonio ed idrogeno Idrocarburo saturo: molecola contenente solo legami semplici carbonio-carbonio Alcano: Idrocarburo saturo contenente solo catene aperte
ALCANI Idrocarburo: molecola contenente solo carbonio ed idrogeno Idrocarburo saturo: molecola contenente solo legami semplici carbonio-carbonio Alcano: Idrocarburo saturo contenente solo catene aperte
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a
 Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Capitolo 19 Dal carbonio agli idrocarburi
 apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
Acidi carbossilici e derivati Composti organici che contengono legami doppi C=O e legami singoli C-eteroatomo (oppure il gruppo CN)
 himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
Capitolo A1 Chimica organica: un introduzione
 Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Nomenclatura. Gli idrocarburi alifatici
 Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Idrocarburi aromatici. Idrocarburi. Idrocarburi
 Lezioni di himica Generale Elementi chimica organica Prof. Roberto Sebastiano Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami
Lezioni di himica Generale Elementi chimica organica Prof. Roberto Sebastiano Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami
Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere CdL in Scienze delle attività motorie e sportive
 Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
CHIMICA ORGANICA Gli alcani e i cicloalcani
 1 C1-ALCANI E CICLOALCANI CHIMICA ORGANICA Gli alcani e i cicloalcani ALCANI Formula generale C n H 2n+2 Desinenza -ano Gli alcani Gli alcani, detti anche paraffine, appartengono alla classe degli idrocarburi
1 C1-ALCANI E CICLOALCANI CHIMICA ORGANICA Gli alcani e i cicloalcani ALCANI Formula generale C n H 2n+2 Desinenza -ano Gli alcani Gli alcani, detti anche paraffine, appartengono alla classe degli idrocarburi
Pillole di... Chimica organica
 ISIS Calabrese-Levi as 2009/2010 Pillole di... Chimica organica dispensa elaborata dalla prof.ssa Silvia Recchia sulla base del testo Chimica interattiva di Passannanti e Sbriziolo, Ed. Tramontana Trenz
ISIS Calabrese-Levi as 2009/2010 Pillole di... Chimica organica dispensa elaborata dalla prof.ssa Silvia Recchia sulla base del testo Chimica interattiva di Passannanti e Sbriziolo, Ed. Tramontana Trenz
Alcheni e alchini. idrocarburi. Insaturi C-C doppi/tripli. alcani. Saturi C-C semplici cicloalcani. aromatici
 Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Lezione 5. Alogenuri, alcoli, fenoli ed eteri
 Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
L acqua e il legame idrogeno
 Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI
 RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 Chimica rganica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica rganica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Alcani e Cicloalcani
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
CHIMICA ORGANICA CHIMICA ORGANICA 14.A PRE-REQUISITI 14.B PRE-TEST 14.C OBIETTIVI 14.4 I POLIMERI 14.1 INTRODUZIONE: I COMPOSTI ORGANICI DEL CARBONIO
 CIMICA RGANICA 14.A PRE-REQUISITI 14.B PRE-TEST 14.C BIETTIVI 14.1 INTRDUZINE: I CMPSTI RGANICI DEL CARBNI 14.1.1 RAPPRESENTAZINE DELLE MLECLE 14.1.2 ISMERIA 14.2 IDRCARBURI 14.3.2 ETERI 14.3.3 CMPSTI
CIMICA RGANICA 14.A PRE-REQUISITI 14.B PRE-TEST 14.C BIETTIVI 14.1 INTRDUZINE: I CMPSTI RGANICI DEL CARBNI 14.1.1 RAPPRESENTAZINE DELLE MLECLE 14.1.2 ISMERIA 14.2 IDRCARBURI 14.3.2 ETERI 14.3.3 CMPSTI
Pillole di... Chimica organica
 sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
14/11/2018. Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile.
 Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Appunti di CHIMICA ORGANICA. A cura del prof. Luvisi Lorenzo
 Appunti di CHIMICA ORGANICA 2 Introduzione La chimica organica è quella parte della chimica che studia i composti del carbonio. Questo nome si deve al fatto che a questo gruppo di composti appartengono
Appunti di CHIMICA ORGANICA 2 Introduzione La chimica organica è quella parte della chimica che studia i composti del carbonio. Questo nome si deve al fatto che a questo gruppo di composti appartengono
Acidi carbossilici. IUPAC catena più lunga contenente il gruppo -COOH al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita con -oico
 Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Acidi Carbossilici CH 3. Caratterizzati dalla presenza di un gruppo carbossilico. Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico)
 Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Capitolo 23 Dal carbonio agli idrocarburi
 Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
LA CHIMICA ORGANICA IBRIDAZIONE
 LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H
 Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
Isomeria ottica. Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi.
 Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Idrocarburi. Idrocarburi
 Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami singoli. Idrocarburi aromatici Idrocarburi insaturi, almeno un legame multiplo
Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami singoli. Idrocarburi aromatici Idrocarburi insaturi, almeno un legame multiplo
ESERCIZI SPETTROMETRIA DI MASSA
 ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
Acidi carbossilici e derivati
 Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
