BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
|
|
|
- Eugenia Forti
- 6 anni fa
- Visualizzazioni
Transcript
1 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI Prof. Augusto Parente Lezione 15
2 ENZIMI (3 Maggio)
3 NOMENCLATURA E CLASSIFICAZIONE Sito web: Classe funzionale Numero di enzimi % (numero attuale che non include gli enzimi trasferiti altrove o cancellati) ( ) 1. Ossidoreduttasi Transferasi Idrolasi Liasi Isomerasi Ligasi Totale 5933 Fonte: IUBMB EXPLORENZ- The Enzyme Database International Union of Biochemistry and Molecular Biology
4 NOMENCLATURA E CLASSIFICAZIONE Prima del 1961, i ricercatori assegnavano personalmente il nome agli enzimi. Questa situazione causava confusione. Fu quindi creata una Commissione sugli Enzimi (EC) e nel 1961 fu pubblicato il primo libro sulla nomenclatura e classificazione degli enzimi. Il sistema di classificazione proposto serve anche come base per assegnare loro un numero EC (Enzyme Code; enzyme Commission), formato da QUATTRO NUMERI separati da un punto, che hanno i seguenti significati: Il primo numero indica la classe di appartenenza. Le classi di appartenenza, come detto, sono 6 ( ), in base al tipo di reazione catalizzata; Il 2 numero indica una sotto classe che ha lo scopo di specificare in maggior dettaglio la reazione catalizzata. Esso può avere un significato diverso da classe a classe. Indica ad esempio il gruppo chimico coinvolto, il tipo di legame, etc. Il 3 numero indica una sotto sotto-classe e può indicare ad esempio l'eventuale coenzima, etc. Il 4 numero indica semplicemente il numero progressivo (la posizione) dell'enzima nella sotto sotto-classe.
5 Classi di appartenenza 1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi
6 ESEMPIO Il nome di un enzima termina generalmente in asi; Il nome deriva generalmente da quello del substrato (es., lattosio lattasi) acido lattico (lattico deidrogenasi) o da quello della reazione catalizzata (idrolisi idrolasi); Questa regola non vale in tutti in casi (es., la papaina, una proteasi, deriva dalla papaia da cui si estrae). EC "Enzyme Commission/Code " Enzima lattico deidrogenasi (Nome comune) Nome sistematico L-lattato: NAD ossidoreduttasi Reazione: L-lattato + NAD + = piruvato + NADH + H +
7 CLASSIFICAZIONE ENZIMI EC 1. Ossidorreduttasi - Tutti gli enzimi che catalizzano reazioni di ossido-riduzione appartengono a questa classe. - Il substrato ossidato è considerato un donatore di H o elettroni - Il nome comune è deidrogenasi, laddove possibile. - Si può usare, in alternativa, il nome dell accettore seguito da riduttasi (es. NAD + riduttasi) - Il termine ossidasi viene utilizzato solo SE l accettore è O 2. - In certi casi la classificazione è difficile, a causa della mancanza di specificità verso l accettore. AH 2 BH 2
8 EC 1.1 [+] Acting on the CH-OH group of donors (NAD + ) Sottoclassi Alcool deidrogenasi EC 1.2 [+] Acting on the aldehyde or oxo group of donors (NAD + ) 3-P-gliceraldeide EC 1.3 [+] Acting on the CH-CH group of donors (FAD) Sucinico deidrogenasi EC 1.4 [+] Acting on the CH-NH 2 group of donors EC 1.5 [+] Acting on the CH-NH group of donors EC 1.6 [+] Acting on NADH or NADPH EC 1.7 [+] Acting on other nitrogenous compounds as donors EC 1.8 [+] Acting on a sulfur group of donors EC 1.9 [+] Acting on a heme group of donors EC 1.10 [+] Acting on diphenols and related substances as donors EC 1.11 [+] Acting on a peroxide as acceptor EC 1.12 [+] Acting on hydrogen as donor EC 1.13 [+] Acting on single donors with incorporation of molecular oxygen (oxygenases) EC 1.14 [+] Acting on paired donors, with incorporation or reduction of molecular oxygen EC 1.15 [+] Acting on superoxide as acceptor EC 1.16 [+] Oxidizing metal ions EC 1.17 [+] Acting on CH or CH 2 groups EC 1.18 [+] Acting on iron-sulfur proteins as donors EC 1.19 [+] Acting on reduced flavodoxin as donor EC 1.20 [+] Acting on phosphorus or arsenic in donors EC 1.21 [+] Acting on X-H and Y-H to form an X-Y bond EC 1.22 [+] Acting on halogen in donors EC 1.23 [+] Reducing C-O-C group as acceptor EC 1.97 [+] Other oxidoreductases EC 1.98 [+] Enzymes using H 2 as reductant (deleted subclass) EC 1.99 [+] Other enzymes using O 2 as oxidant (deleted subclass)
9 Esempio EC EC. 1 (classe). 1 (HCOH). 1 (NAD + dipendente). 1 (prima posizione nell elenco) Nome: Alcool deidrogenasi Sinonimo: aldeide reduttasi Reazione: Un alcool + NAD + aldeide o chetone + NADH + H + Cofattori: Zinco o ferro
10 CLASSIFICAZIONE ENZIMI * glicogeno fosforilasi * B A (chinasi)
11 Esempio EC Nome: Esochinasi Sinonimo: esochinasi tipo I, esochinasi tipo II, esochinasi tipo III esochinasi tipo IV (glucochinasi) Reazione: ATP Mg 2+ + D-esoso ADP + D-esoso 6-fosfato D-glucosio, D-mannosio, D-fruttosio, sorbitolo e glucosammina possono fungere da accettori. Anche ITP e datp possono fungere da donatori Cofattori: nessuno, ma è richiesto Mg 2+ Mg 2+
12 CLASSIFICAZIONE ENZIMI *
13 Esempio EC Nome: Glucosio-6-fosfatasi Reazione: D-glucosio-6-fosfato + H 2 O D-glucosio + fosfato (reazione terminale della gluconeogenesi) Cofattori: nessuno. Enzima ampiamente distribuito nei tessuti animali
14 CLASSIFICAZIONE ENZIMI
15 Esempio EC Nome: Fosfopiruvato idratasi Sinonimo: enolasi Reazione: 2-fosfo-D-glicerato fosfoenolpiruvato + H 2 O Cofattori: Mg Isocitrato succinato + gliossilato
16 CLASSIFICAZIONE ENZIMI
17 Esempio EC Nome: Triosofosfato isomerasi Reazione: diidrossiaceton fosfato D- gliceraldeide 3- fosfato Cofattori: nessuno
18 CLASSIFICAZIONE ENZIMI
19 Esempio EC Nome: piruvato carbossilasi Reazione: ATP+ piruvato + HCO 3 - ADP + fosfato + ossalacetato Cofattori: Biotina, manganese o zinco P i +
20 Classe 1. OSSIDOREDUTTASI Nome sistematico: donatore: accettore ossidoreduttasi (es. L-lattato NAD ossidoreduttasi) 2. TRANSFERASI Nome sistematico: donatore: gruppo accettore transferasi (es. L-aspartato: 2-chetoglutarato amminotransferasi) 3. IDROLASI Nome sistematico: substrato idrolasi (es. succinil-coa idrolasi) Reazione catalizzata Reazioni di ossidoriduzione Nome comune: deidrogenasi o reduttasi Ossidasi (1.x.3): solo quando O 2 accettore e - (generalmente si forma H 2 O 2 ) Perossidasi (1.11.1): quando l accettore è H 2 O 2 Ossigenasi (1.13): solo quando O 2 introdotto nel substrato Trasferimento di gruppi funzionali Nomenclatura corrente 2.6: Transamminasi (ma meglio, amminotransferasi) da a 2.7.4: Chinasi (fosfotransferasi) Idrolisi: Rottura di un legame con intervento H 2 O Nome comune: substrato + suffiso asi 3.1: Idrolisi esteri (esterasi) Fosfatasi (idrolisi monoesteri fosforici) 3.2: Glicosilasi (es. amilasi) 3.4: Peptidasi (idrolisi legame peptidico) 3.6: Idrolisi legame anidridico anidridi acido fosforico (es. pirofosfatasi, ATPasi)
21 Classe 4. LIASI Nome sistematico: substrato: gruppo-liasi (es. citrato ossalacetato-liasi= citrato sintasi) 5. ISOMERASI Nome sistematico: in generale isomerasi, tranne quando si ha inversione di centri asimmetrici. In tal caso: racemasi, se un solo centro asimmetrico; epimerasi, se più di uno. Reazione catalizzata Rottura non idrolitica di un legame C-C, C-O, C-N o altro oppure addizione ad un doppio legame Schema comune di reazione: un substrato = due prodotti (o viceversa). Uno dei prodotti contiene un doppio legame (neoformato o preesistente) Nomenclatura comune: 4.1: Rottura legame C-C decarbossilasi (o carbossilasi) aldolasi 4.2: Rottura legame C-O Idro-liasi (eliminazione di acqua o addizione a doppio legame: deidratasi o idratasi. Tuttora consentiti i nomi: fumarasi, aconitasi, enolasi). Nel caso in cui la reazione di condensazione sia più importante, si può usare il termine sintasi, ma mai sintetasi (vedi citrato sintasi). Equilibrio fra isomeri Nome comune simile al sistematico, ma semplificato. 5.1: Racemasi e Epimerasi 5.2: cis-trans isomerasi 5.3: Ossidoreduttasi intramolecolari (es. triosofosfato isomerasi, spostamento doppi legami C-C e tautomerasi) 5.4: Transferasi intramolecolari Fosfomutasi (precedentemente classificate in 2.7.5: es. fosfoglucomutasi, fosfoglicerato mutasi)
22 6. LIGASI Classe Nome sistematico: X : Y ligasi (prodotto idrolisi) X e Y = nome molecole da unire; eventualmente, fra parentesi, il prodotto dell'idrolisi del nucleotide. [es. succinato - CoA ligasi (GDP)] Reazione catalizzata Fomazione di un legame accoppiata con idrolisi ATP o altro nucleotide Nome comune: Ligasi In alcuni casi si usa Sintasi o Carbossilasi. In questa classe, e solo in questa, è consentito l'uso di sintetasi in alternativa a sintasi. 6.4: Carbossilasi (enzimi con biotina come coenzima) es. piruvato carbossilasi, acil-coa carbossilasi
23 Cofattore, gruppo prostetico, coenzima Per il funzionamento di alcuni enzimi, è necessario che la loro parte proteica sia integrata da altre molecole essenziali per il processo catalitico (importanza delle vitamine). - Cofattore: in genere uno ione metallico (Fe 2+, Fe 3+, Mn 2+, Mg 2+, Cu 2+, Zn 2+ ) o altra molecola inorganica legata alla parte proteica dell enzima sia direttamente che attraverso un altro elemento non proteico - Gruppo prostetico: molecola organica (diversa da amminoacidi) stabilmente legata alla parte proteica (FAD). Il legame è in genere covalente con alcune eccezioni (emoglobina/mioglobina). - Coenzima: molecola organica non stabilmente legata alla parte proteica (NAD+, ecc.) In questi casi la parte proteica dell enzima viene chiamata apoenzima, mentre l enzima con il cofattore/gruppo prostetico/ coenzima viene chiamato oloenzima
24 I meccanismi catalitici - Catalisi acido-basica - Catalisi covalente - Catalisi da ioni metallici - Catalisi elettrostatica - Dimostrazione della catalisi acido-basica Esempio di catalisi acida generale
25 Gli enzimi possono avere un meccanismo catalitico che può essere ricondotto alla catalisi acida generale o basica generale.
26 CATALISI COVALENTE Nel corso della catalisi si forma un intermedio covalente tra Enzima e Substrato. Alla fine della catalisi si ha il Prodotto e l Enzima libero pronto a catalizzare un nuovo evento catalitico. A seconda del gruppo chimico della catena laterale dell AMMINOACIDO (AA) catalitico si instaurano diversi tipi di legami covalenti. Catena laterale dell AA del sito catalitico Ser (-OH) Cys (-SH) O O Reazione Enz-OH + O C R OH + Enz O C R * Enz-SH + O C R OH + Enz S C R O O Legame E-S Estere Tioestere His (-NH-) ENZ + O + O C R OH + ENZ + O + C R Acilimidazolo
27 Lys (-NH 2 ) R 1 R 1 Base di Schiff Enz NH 2 + O C H 2 O + Enz N C R 2 R 2 Asp Glu ( COOH ) O Enz C OH + O O O C R 1 H + ENZ C O C R 2 Anidridico R 2 R 1 *La freccia indica i siti dell attacco nucleofilico
CLASSIFICAZIONE ENZIMI
 CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
(2 x) (2 x) (2 x) Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi. Gliceraldeide 3-fosfato deidrogenasi
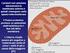 Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico
 Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale
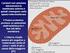 Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Attenzione: Lunedì 15 la lezione sarà dalle 14 alle 16 (al posto di L. Migliore)
 Attenzione: Lunedì 15 la lezione sarà dalle 14 alle 16 (al posto di L. Migliore) La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato
Attenzione: Lunedì 15 la lezione sarà dalle 14 alle 16 (al posto di L. Migliore) La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
6 H 2. con G=-686 kcal/mole di H 12 O 6 O + 6 CO O 2. glucosio La respirazione avviene in tre stadi principali; ognuno di questi
 La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
Principali vie di utilizzo del Glucosio
 Principali vie di utilizzo del Glucosio DESTINO DEL PIRUVATO Il piruvato, può seguire due vie. La via fermentativa La via della respirazione cellulare In presenza di ossigeno, il piruvato, viene ossidato
Principali vie di utilizzo del Glucosio DESTINO DEL PIRUVATO Il piruvato, può seguire due vie. La via fermentativa La via della respirazione cellulare In presenza di ossigeno, il piruvato, viene ossidato
Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la
 Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico 2014-15
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2014-15 Lezione 16 Degradazione dei lipidi
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2014-15 Lezione 16 Degradazione dei lipidi
GLI ENZIMI. Gli enzimi sono (quasi sempre) molecole proteiche che catalizzano tutte le reazioni chimiche che avvengono negli organismi viventi.
 GLI ENZIMI Gli enzimi sono (quasi sempre) molecole proteiche che catalizzano tutte le reazioni chimiche che avvengono negli organismi viventi. - Sono catalizzatori biologici non vengono alterati dalla
GLI ENZIMI Gli enzimi sono (quasi sempre) molecole proteiche che catalizzano tutte le reazioni chimiche che avvengono negli organismi viventi. - Sono catalizzatori biologici non vengono alterati dalla
Energia di attivazione
 1 ENZIMI Caratteristiche fondamentali della catalisi enzimatica e del meccanismo di azione degli enzimi Componenti strutturali e funzionali degli enzimi Nomenclatura e classificazione internazionale degli
1 ENZIMI Caratteristiche fondamentali della catalisi enzimatica e del meccanismo di azione degli enzimi Componenti strutturali e funzionali degli enzimi Nomenclatura e classificazione internazionale degli
Metabolismo glucidico
 Metabolismo glucidico Digestione degli zuccheri a-amilasi salivare e pancreatica maltotrioso destrina maltosio glucosio lattosio amido saccarosio maltosio maltotrioso destrine lattasi maltasi oligosaccaridasi
Metabolismo glucidico Digestione degli zuccheri a-amilasi salivare e pancreatica maltotrioso destrina maltosio glucosio lattosio amido saccarosio maltosio maltotrioso destrine lattasi maltasi oligosaccaridasi
Prof. Maria Nicola GADALETA DISPENSA N. 23
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
La quantità di glu presente nei liquidi extracellulari è di circa 20g, 80kcal.
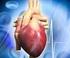 I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa
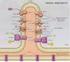 Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
scaricato da www.sunhope.it
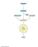 CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Gluconeogenesi. Le reazioni irreversibili della glicolisi sono aggirate attraverso l azione di enzimi differenti. Fegato e reni
 Gluconeogenesi Il glucosio può essere sintetizzato a partire da precursori più semplici, i precursori possono essere vari a seconda della specie vivente, nei mammiferi sono: piruvato, lattato, amminoacidi,
Gluconeogenesi Il glucosio può essere sintetizzato a partire da precursori più semplici, i precursori possono essere vari a seconda della specie vivente, nei mammiferi sono: piruvato, lattato, amminoacidi,
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Lezione 7. Il metabolismo terminale e la produzione di ATP
 Lezione 7 Il metabolismo terminale e la produzione di ATP 1 Il metabolismo terminale Catabolismo Lipidi Amminoacidi Carboidrati convergono sul metabolismo terminale, e producono una stessa molecola: l
Lezione 7 Il metabolismo terminale e la produzione di ATP 1 Il metabolismo terminale Catabolismo Lipidi Amminoacidi Carboidrati convergono sul metabolismo terminale, e producono una stessa molecola: l
DESTINI DEL PIRUVATO
 DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
Gluconeogenesi. Glicemia. Digiuno prolungato. prolungato,, la glicemia. digiuno, anche. scarse. subisce. Nel. sangue ed il cervello. Digiuno.
 Gluconeogenesi Glicemia [Glu] blood Insulina Fed Fast early Glucagone 1-2 hrs Digiuno late fast Glycogen Glicogeno esaurito gone 6-12 hrs Digiuno prolungato (giorni) Meal Un pasto Nel digiuno, anche prolungato,,
Gluconeogenesi Glicemia [Glu] blood Insulina Fed Fast early Glucagone 1-2 hrs Digiuno late fast Glycogen Glicogeno esaurito gone 6-12 hrs Digiuno prolungato (giorni) Meal Un pasto Nel digiuno, anche prolungato,,
Il ciclo di Krebs e la fosforilazione ossidativa
 Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Lezione 5. Il metabolismo dei carboidrati
 Lezione 5 Il metabolismo dei carboidrati 1 La produzione di energia: catabolismo dei nutrienti La degradazione enzimatica delle sostanze nutritive principali (carboidrati, lipidi e proteine) procede attraverso
Lezione 5 Il metabolismo dei carboidrati 1 La produzione di energia: catabolismo dei nutrienti La degradazione enzimatica delle sostanze nutritive principali (carboidrati, lipidi e proteine) procede attraverso
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Idratazione (introduciamo un gruppo OH sul Cβ) per mezzo della enoil-coa idratasi
 β-ossidazione di un Ac. Grasso Saturo con n PARI di atomi di carbonio Deidrogenazione FAD-dipendente del legame Cα- Cβ per mezzo della Acil-CoA deidrogenasi che è legata alla membrana mitocondriale interna)
β-ossidazione di un Ac. Grasso Saturo con n PARI di atomi di carbonio Deidrogenazione FAD-dipendente del legame Cα- Cβ per mezzo della Acil-CoA deidrogenasi che è legata alla membrana mitocondriale interna)
scaricato da 1
 scaricato da www.sunhope.it 1 La decarbossilazione ossidativa del piruvato rappresenta il legame tra glicolisi e ciclo di Krebs Questa reazione, come tutto il ciclo di Krebs, avviene nella matrice mitocondriale
scaricato da www.sunhope.it 1 La decarbossilazione ossidativa del piruvato rappresenta il legame tra glicolisi e ciclo di Krebs Questa reazione, come tutto il ciclo di Krebs, avviene nella matrice mitocondriale
Lezione 7. Il metabolismo terminale e la produzione di ATP
 Lezione 7 Il metabolismo terminale e la produzione di ATP 1 Il metabolismo terminale Catabolismo Lipidi Amminoacidi Carboidrati convergono sul metabolismo terminale, e producono una stessa molecola: l
Lezione 7 Il metabolismo terminale e la produzione di ATP 1 Il metabolismo terminale Catabolismo Lipidi Amminoacidi Carboidrati convergono sul metabolismo terminale, e producono una stessa molecola: l
METABOLISMO DEL Glucosio
 METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
Corso di Biochimica. Destino catabolico del piruvato. Prof. Paolo Cirri. Dipartimento Scienze Biomediche Sperimentali e Cliniche Università di Firenze
 Corso di Biochimica Prof. Paolo Cirri Dipartimento Scienze Biomediche Sperimentali e Cliniche Università di Firenze Orario ricevimento: martedì 14,30-16,30 Diapositive lezioni: http://bioserver2.sbsc.unifi.it/
Corso di Biochimica Prof. Paolo Cirri Dipartimento Scienze Biomediche Sperimentali e Cliniche Università di Firenze Orario ricevimento: martedì 14,30-16,30 Diapositive lezioni: http://bioserver2.sbsc.unifi.it/
IL METABOLISMO ENERGETICO BIOCHIMICA. GLICOLISI, FERMENTAZIONE E RESPIRAZIONE CELLULARE GSCATULLO
 IL METABOLISMO ENERGETICO BIOCHIMICA. GLICOLISI, FERMENTAZIONE E RESPIRAZIONE CELLULARE GSCATULLO ( Introduzione Metabolismo energetico Funzione Il metabolismo energetico è un attività coordinata cui partecipano
IL METABOLISMO ENERGETICO BIOCHIMICA. GLICOLISI, FERMENTAZIONE E RESPIRAZIONE CELLULARE GSCATULLO ( Introduzione Metabolismo energetico Funzione Il metabolismo energetico è un attività coordinata cui partecipano
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI
 METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
Ciclo dell acido citrico
 Ciclo dell acido citrico Il metabolismo ossidativo dei carburanti metabolici I gruppi acetili derivati da carboidrati, amminoacidi e acidi grassi entrano nel ciclo dell acido citrico dove vengono ossidati
Ciclo dell acido citrico Il metabolismo ossidativo dei carburanti metabolici I gruppi acetili derivati da carboidrati, amminoacidi e acidi grassi entrano nel ciclo dell acido citrico dove vengono ossidati
Regolazione della Glicolisi
 Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
energia di attivazione complesso attivato
 GLI ENZIMI: i catalizzatori delle reazioni nei sistemi biologici Diagrammi dello stato di L'energia di attivazione è l energia necessaria al sistema per iniziare un particolare processo L'energia di attivazione
GLI ENZIMI: i catalizzatori delle reazioni nei sistemi biologici Diagrammi dello stato di L'energia di attivazione è l energia necessaria al sistema per iniziare un particolare processo L'energia di attivazione
LE PIANTE E LA FOTOSINTESI
 PON di Scienze a.s. 013/14 Esperto prof. C. Formica LE PIANTE E LA FOTOSINTESI Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it,
PON di Scienze a.s. 013/14 Esperto prof. C. Formica LE PIANTE E LA FOTOSINTESI Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it,
Struttura e meccanismo d azione degli enzimi
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Struttura e meccanismo d azione degli enzimi Catalisi chimica Catalisi chimica: teoria dello stato di transizione - descrizione microscopica del
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Struttura e meccanismo d azione degli enzimi Catalisi chimica Catalisi chimica: teoria dello stato di transizione - descrizione microscopica del
Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali:
 Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali: proteine strutturali (collagene, cheratine); proteine catalitiche (enzimi); proteine di trasporto
Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali: proteine strutturali (collagene, cheratine); proteine catalitiche (enzimi); proteine di trasporto
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2015-16 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2015-16 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
RESPIRAZIONE CELLULARE (METABOLISMO DEL GLUCOSIO)
 RESPIRAZIONE CELLULARE (METABOLISMO DEL GLUCOSIO) LA GLICOLISI: dopo il ciclo di Calvin, che avviene nelle cellule autotrofe delle piante, il glucosio prodotto va a demolirsi per produrre energia nelle
RESPIRAZIONE CELLULARE (METABOLISMO DEL GLUCOSIO) LA GLICOLISI: dopo il ciclo di Calvin, che avviene nelle cellule autotrofe delle piante, il glucosio prodotto va a demolirsi per produrre energia nelle
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
L ATTIVITA DELLA CELLULA
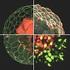 L ATTIVITA DELLA CELLULA nutrizione crescita eliminare i rifiuti mantenimento delle strutture movimento riproduzione comunicazione per svolgere tutte queste attività, le cellule hanno bisogno di ENERGIA
L ATTIVITA DELLA CELLULA nutrizione crescita eliminare i rifiuti mantenimento delle strutture movimento riproduzione comunicazione per svolgere tutte queste attività, le cellule hanno bisogno di ENERGIA
Catabolismo = degradazione di composti per recuperare i loro. Anabolismo = Le vie anaboliche e cataboliche sono in relazione fra loro
 Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
-uno o più IONI INORGANICI
 Coenzimi e vitamine Alcuni enzimi, per svolgere la loro funzione, hanno bisogno di componenti chimici addizionali, i COFATTORI APOENZIMA + COFATTORE = OLOENZIMA = enzima cataliticamente attivo Il cofattore
Coenzimi e vitamine Alcuni enzimi, per svolgere la loro funzione, hanno bisogno di componenti chimici addizionali, i COFATTORI APOENZIMA + COFATTORE = OLOENZIMA = enzima cataliticamente attivo Il cofattore
Attenzione : lunedì 29 aprile NON ci sarà lezione
 Attenzione : lunedì 29 aprile NON ci sarà lezione Metabolismo dei lipidi a) Ossidazione degli acidi grassi Triacilgliceroli (90% del totale) Gruppi metilenici o metilici Richiedono molto O 2 per essere
Attenzione : lunedì 29 aprile NON ci sarà lezione Metabolismo dei lipidi a) Ossidazione degli acidi grassi Triacilgliceroli (90% del totale) Gruppi metilenici o metilici Richiedono molto O 2 per essere
Respirazione cellulare Metabolismo dei glucidi
 Respirazione cellulare Metabolismo dei glucidi Metabolismo E l insieme delle reazioni chimiche che avvengono in una cellula o, più in generale, in qualsiasi organismo. Le sostanze coinvolte in tali reazioni
Respirazione cellulare Metabolismo dei glucidi Metabolismo E l insieme delle reazioni chimiche che avvengono in una cellula o, più in generale, in qualsiasi organismo. Le sostanze coinvolte in tali reazioni
COENZIMI. Molti enzimi richiedono l associazione con particolari cofattori per poter esplicare la loro attività catalitica.
 COENZIMI Molti enzimi richiedono l associazione con particolari cofattori per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
COENZIMI Molti enzimi richiedono l associazione con particolari cofattori per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono
 Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA) TEORIA DELLE
Ciclo dell Acido Citrico
 Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano -la glicolisi non è l unica via catabolica in grado di produrre energia Anzi, le
Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano -la glicolisi non è l unica via catabolica in grado di produrre energia Anzi, le
Il ciclo dell acido citrico
 Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Metabolismo dei carboidrati
 rof. Giorgio artor Metabolismo dei carboidrati Copyright 2001-2015 by Giorgio artor. All rights reserved. Versione 1.9.3 apr 2015 Indice Glicogeno Metabolismo del Glicogeno C 2 C 2 3 -- 3 C Gluconeogensi
rof. Giorgio artor Metabolismo dei carboidrati Copyright 2001-2015 by Giorgio artor. All rights reserved. Versione 1.9.3 apr 2015 Indice Glicogeno Metabolismo del Glicogeno C 2 C 2 3 -- 3 C Gluconeogensi
Catabolismo = degradazione di composti per recuperare i loro. Anabolismo = Le vie anaboliche e cataboliche sono in relazione fra loro
 Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
Il METABOLISMO comprende la totalità dei processi attraverso i quali gli esseri viventi ricavano e utilizzano energia secondo i limiti imposti dalle leggi della termodinamica : Catabolismo = degradazione
GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE. L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO
 GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO 75% DI TALE GLUCOSIO E NEL CERVELLO I FLUIDI CORPOREI CONTENGONO SOLO 20 g DI
GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO 75% DI TALE GLUCOSIO E NEL CERVELLO I FLUIDI CORPOREI CONTENGONO SOLO 20 g DI
METABOLISMO DEI LIPIDI
 METABOLISMO DEI LIPIDI STRUTTURA DEI TRIACILGLICEROLI -Molecole non polari (grassi neutri) -insolubili in H 2 O O= R-C-O - + R -OH O= R-C-O-R + H 2 O Acidi grassi: acidi carbossilici con catena idrocarburica
METABOLISMO DEI LIPIDI STRUTTURA DEI TRIACILGLICEROLI -Molecole non polari (grassi neutri) -insolubili in H 2 O O= R-C-O - + R -OH O= R-C-O-R + H 2 O Acidi grassi: acidi carbossilici con catena idrocarburica
Regolazione ormonale del metabolismo energetico. Lezione del 11 marzo 2014
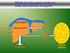 Regolazione ormonale del metabolismo energetico Lezione del 11 marzo 2014 Effetti fisiologici e metabolici dell adrenalina: preparazione all azione EFFETTO IMMEDIATO EFFETTO COMPLESSIVO Effetto fisiologico
Regolazione ormonale del metabolismo energetico Lezione del 11 marzo 2014 Effetti fisiologici e metabolici dell adrenalina: preparazione all azione EFFETTO IMMEDIATO EFFETTO COMPLESSIVO Effetto fisiologico
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 27 Panoramica del ciclo dell acido citrico e sintesi di acetil-coa Concetti chiave: Il ciclo dell acido citrico èun processo
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 27 Panoramica del ciclo dell acido citrico e sintesi di acetil-coa Concetti chiave: Il ciclo dell acido citrico èun processo
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
brown adipose tissue 2
 1 brown adipose tissue 2 Effects of adrenalin and glucagone on adipocytes: 3 lipolisi: adrenalina glucagone ADIPCITA insulina R G AC PDE ATP camp AMP PKA (inattiva) PKA (attiva) ATP ADP TAG lipasi (inattiva)
1 brown adipose tissue 2 Effects of adrenalin and glucagone on adipocytes: 3 lipolisi: adrenalina glucagone ADIPCITA insulina R G AC PDE ATP camp AMP PKA (inattiva) PKA (attiva) ATP ADP TAG lipasi (inattiva)
Anatomia biochimica di un mitocondrio
 Anatomia biochimica di un mitocondrio Le involuzioni(creste)aumentano considerevolmente l area della superficie della membrana interna. La membrana interna di un singolo mitocondrio può avere anche più
Anatomia biochimica di un mitocondrio Le involuzioni(creste)aumentano considerevolmente l area della superficie della membrana interna. La membrana interna di un singolo mitocondrio può avere anche più
METABOLISMO DEI COMPOSTI AZOTATI
 METABOLISMO DEI COMPOSTI AZOTATI CATABOLISMO DEI COMPOSTI AZOTATI Tutti gli organismi possono convertire l NH 3 in composti organici azotati, sono invece molti di meno gli organismi che possono sintetizzare
METABOLISMO DEI COMPOSTI AZOTATI CATABOLISMO DEI COMPOSTI AZOTATI Tutti gli organismi possono convertire l NH 3 in composti organici azotati, sono invece molti di meno gli organismi che possono sintetizzare
Digestione e assorbimento dei lipidi. β-ossidazione degli acidi grassi
 Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi
 Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
GLUCOSIO GLUCOSIO-6-FOSFATO ISOMERASI FRUTTOSIO-6-FOSFATO ATP FRUTTOSIO-1,6-DIFOSFATO ALDOLASI ISOMERASI
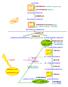 GLUCOSIO ESOCHINASI (costitutivo) inibizione feed-back GLUCOCHINASI (induttivo) GLUCOSIO-6-FOSFATO ISOMERASI - 2 FRUTTOSIO-6-FOSFATO FOSFOFRUTTOCINASI allosterico reg +: e Fr-2,6-dP reg -:, citrato FRUTTOSIO-1,6-DIFOSFATO
GLUCOSIO ESOCHINASI (costitutivo) inibizione feed-back GLUCOCHINASI (induttivo) GLUCOSIO-6-FOSFATO ISOMERASI - 2 FRUTTOSIO-6-FOSFATO FOSFOFRUTTOCINASI allosterico reg +: e Fr-2,6-dP reg -:, citrato FRUTTOSIO-1,6-DIFOSFATO
IL METABOLISMO ENERGETICO
 IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
2 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA
 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
USO DEGLI ENZIMI PER PRODURRE AMMINOACIDI E PEPTIDI
 USO DEGLI ENZIMI PER PRODURRE AMMINOACIDI E PEPTIDI Biocatalisi sintesi biocatalitica Forma L Asimmetrica Per risoluzione con enzimi idrolitici Forma L e D Aggiunta di ammoniaca al doppio legame di un
USO DEGLI ENZIMI PER PRODURRE AMMINOACIDI E PEPTIDI Biocatalisi sintesi biocatalitica Forma L Asimmetrica Per risoluzione con enzimi idrolitici Forma L e D Aggiunta di ammoniaca al doppio legame di un
Chimica Biologica A.A. 2010-2011. Bioenergetica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano e Metabolismo - nel metabolismo, reazioni in sé non spontanee (endoergoniche) possono
Chimica Biologica A.A. 2010-2011 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano e Metabolismo - nel metabolismo, reazioni in sé non spontanee (endoergoniche) possono
Gli enzimi. L azione degli enzimi è caratterizzata da alcune proprietà fondamentali:
 Gli enzimi Nel metabolismo energetico le cellule producono notevoli quantità di CO 2 che deve essere eliminata con l apparato respiratorio. Il trasferimento della CO 2 dalle cellule al sangue e da esso
Gli enzimi Nel metabolismo energetico le cellule producono notevoli quantità di CO 2 che deve essere eliminata con l apparato respiratorio. Il trasferimento della CO 2 dalle cellule al sangue e da esso
Trasporto degli elettroni e fosforilazione ossidativa
 Trasporto degli elettroni e fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobici Tutte le tappe enzimatiche della degradazione
Trasporto degli elettroni e fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobici Tutte le tappe enzimatiche della degradazione
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 17
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
FOSFORILAZIONE OSSIDATIVA
 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
Il metabolismo cellulare
 Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti:
 Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
LA RESPIRAZIONE CELLURARE
 LA RESPIRAZIONE CELLURARE La respirazione cellulare è il meccanismo attraverso cui la cellula, in presenza di ossigeno, è in grado di ricavare energia.la sede di questo processo è il mitocondrio. I mitocondri
LA RESPIRAZIONE CELLURARE La respirazione cellulare è il meccanismo attraverso cui la cellula, in presenza di ossigeno, è in grado di ricavare energia.la sede di questo processo è il mitocondrio. I mitocondri
Metabolismo Cellulare
 Scuola di Ingegneria Industriale e dell Informazione Course 096125 (095857) Elementi di Chimica Verde e Sostenibile A.A. 2015/2016 Metabolismo Cellulare Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/
Scuola di Ingegneria Industriale e dell Informazione Course 096125 (095857) Elementi di Chimica Verde e Sostenibile A.A. 2015/2016 Metabolismo Cellulare Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/
I più comuni polisaccaridi sono: AMIDO CELLULOSA GLICOGENO DESTRINA
 GLICOGENO POLISACCARIDI La maggior parte dei carboidrati che si ritrovano in natura sono polimeri ad alto peso molecolare chiamati polisaccaridi L u n i t à m o n o s a c c a r i d i c a p i ù frequente
GLICOGENO POLISACCARIDI La maggior parte dei carboidrati che si ritrovano in natura sono polimeri ad alto peso molecolare chiamati polisaccaridi L u n i t à m o n o s a c c a r i d i c a p i ù frequente
Introduzione al metabolismo
 Introduzione al metabolismo 1 2 Funzioni del metabolismo 1- Ottenere energia chimica 2- Convertire le molecole 3-Polimerizzare i precursori monomerici 4- Sintetizzare e degradare le biomolecole Il metabolismo
Introduzione al metabolismo 1 2 Funzioni del metabolismo 1- Ottenere energia chimica 2- Convertire le molecole 3-Polimerizzare i precursori monomerici 4- Sintetizzare e degradare le biomolecole Il metabolismo
Il metabolismo microbico
 Corso di Microbiologia Generale. A.A. 2015-2016 Il metabolismo microbico Dott.ssa Annalisa Serio Il metabolismo Insieme di reazioni chimiche che avvengono all interno di un organismo vivente: Le reazioni
Corso di Microbiologia Generale. A.A. 2015-2016 Il metabolismo microbico Dott.ssa Annalisa Serio Il metabolismo Insieme di reazioni chimiche che avvengono all interno di un organismo vivente: Le reazioni
Cofattori e vitamine
 Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Fegato e metabolismo lipidico
 Fegato e metabolismo lipidico LIPIDI : Acidi grassi liberi o esterificati ad Acil gliceroli ( mono, di, tri) Fosfolipidi e colesterolo FONTI : Grassi della dieta Depositati sotto forma di goccioline (tessuto
Fegato e metabolismo lipidico LIPIDI : Acidi grassi liberi o esterificati ad Acil gliceroli ( mono, di, tri) Fosfolipidi e colesterolo FONTI : Grassi della dieta Depositati sotto forma di goccioline (tessuto
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
Appunti di biologia IL CICLO DI KREBS. Giancarlo Dessì Licenza Creative Commons BY-NC-SA
 Appunti di biologia IL IL DI KREBS Giancarlo Dessì http://www.giand.it Licenza reative ommons BY-N-SA BY: Attribuzione - N: Non commerciale - SA: ondividi allo stesso modo IL DI KREBS detto anche IL DELL'AID
Appunti di biologia IL IL DI KREBS Giancarlo Dessì http://www.giand.it Licenza reative ommons BY-N-SA BY: Attribuzione - N: Non commerciale - SA: ondividi allo stesso modo IL DI KREBS detto anche IL DELL'AID
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Fosforilazione ossidativa
 Fosforilazione ossidativa H 2 2H + + 2e - NADH+H + NAD + + 2H + +2e - FADH 2 FAD + 2H + + 2e - ½O 2 + 2H + + 2e - H 2 O + Calore ½ O 2 + 2H + + 2e - H 2 O + ATP 1 La fosforilazione ossidativa avviene nella
Fosforilazione ossidativa H 2 2H + + 2e - NADH+H + NAD + + 2H + +2e - FADH 2 FAD + 2H + + 2e - ½O 2 + 2H + + 2e - H 2 O + Calore ½ O 2 + 2H + + 2e - H 2 O + ATP 1 La fosforilazione ossidativa avviene nella
