Esercitazione n Reazioni e meccanismi dei composti aromatici.
|
|
|
- Vincenzo Carella
- 5 anni fa
- Visualizzazioni
Transcript
1 Esercitazione n. 15 Reazioni e meccanismi dei composti aromatici. 1. Dare la definizione ed un esempio per ciascuno dei seguenti termini: a) complesso σ Intermedio (cationico) nella sostituzione elettrofila aromatica b) solfonazione c) nitrazione d) gruppo orto,para orientante corrispondenti e) alchilazione di FriedelCrafts f) gruppo meta orientante Sost. Elettrofila aromatica (E =S 3 ) che introduce il gruppo acido solfonico (S 3 ) Sost. Elettrofila aromatica (E = 2 ) che introduce il gruppo nitro ( 2 ) Sostituente presente sull anello benzenico che indirizza l attacco dell elettrofilo in ortopara, stabilizzando gli addotti Sost. Elettrofila aromatica (E =R ) che introduce un gruppo alchile (R di RX) Sostituente presente sull anello benzenico che indirizza l attacco dell elettrofilo in meta, destabilizzando gli addotti orto e para 2. Scrivere quale è e come si forma l'elettrofilo nelle seguenti reazioni aromatiche: a) nitrazione; b) clorurazione; c) solfonazione; d) acilazione con cloruro di acetile; e) alchilazione con cloruro di isobutile. v. lezione
2 3. Completare le seguenti reazioni del benzene. Scrivere in ogni caso il meccanismo. a) bromuro di terzbutile Al 3 C Al 3 C meccanismo: C Al C C 3 3 Al 4 C C Al 4 Al 3 C
3 b) 1clorobutano Al 3 C Al 2 C 2 C 2 C 2 C 2 C 2 3 C C 2 meccanismo:... Al 3 Al C 2 C 2 C 2 C 2 C 2 C 2 4 trasposizione C C... Al 2 4 Al C 4 2 C 2 C 2 C 2 C 2 C 2 C 2 C 2 C 2 Al 3 C 2 C C C 2 C 2 Al 4 Al 3 C C 2
4 c) bromo un chiodo (di ferro...non di acciaio!) 2 Fe Fe 3 Fe 3 2 meccanismo: 2 Fe 3 Fe 4 Fe 4 Fe 3 d) acido solforico fumante 2 S 4 S 3 S S
5 e) cloruro di benzoile Al 3 C Al 3 C meccanismo: C C Al 3 Al 4 C Al C 4 C Al 3
6 f) acido nitrico acido solforico 2 S meccanismo: 3 2 S 4 2 S catione ITRI 2 2 S 4 3 S = S S = 4 2 2
7 g) 1cloro2,2dimetilpropano Al 3 C 2 C Al 3 C C 2 C 2 C C3 meccanismo: Al 3 C 2 C C 3 Al4 C 2 C C 2 C C 2 C C C 2 C 3 C C 2 Al4 Al 3 C C 2
8 4. Completare le seguenti reazioni dell'isopropilbenzene: a) 2 alla luce; b) 2 Fe 3 ; c) S 3 in acido solforico; d) cloruro di acetile Al 3 ; e) cloruro di propile Al 3. 3 C C 3 C C C 3 C 2, hν S 3, 2 S 4 orto 2, Fe 3 C, S 3 3 C C 3 C C Al 3 C 2 Al 3 C 2 3 C C orto 3 C C 3 C C 3 C C C 2 2 C C 3 C C C C 2 C 2 C
9 5. Completare le seguenti reazioni, catalizzate da Al 3. Dimostrare in ciascun caso l'orientamento, servendosi degli addotti σ. a) clorocicloesano benzene a) Al 3 tutte le posizioni sono equivalenti b) cloruro di metile fenil metil etere Al C3 3 C3 3 C C3.. C3 C3.. C3 C3 3 C C 3
10 B. ei compiti (o negli esami scritti) l orientamento DEVE essere dimostrato come mostrato qui di seguito! Al 3 δ C δ Al3 E = C 3 stabile C 3 stabile
11 c) 3cloro2,2dimetilbutano isopropilbenzene C C Al 3 Al4 C C C3 C C C3 = E C 3 C stabile C 3 C E 3 C C 3 3 C C C E 3 C E 3 C C E 3 C C 3 C C C C C C stabile
12 d) 2cloropropano nitrobenzene Al 3 C C C C C = E Al4 2 C instabile C C 3 C C C 3 C C C 3 3 instabile C
13 6. Completare le seguenti reazioni di sostituzione elettrofila aromatica: a),dimetilanilina cloruro di acetile e cloruro di alluminio C 3 C C C 3 C 3 3 CC3 Al 3 b) clorobenzene bromo e bromuro ferrico 2 Fe 3 C c) propanoato di fenile e acido nitrico acido solforico C C 2 C C 2 2 S 4 2
14 d) isopropilbenzene acido solforico ed anidride solforica S 3 S 3 2 S 4 S 3 e) nitrobenzene acido nitrico ed acido solforico S 4 2 f) bifenile anidride acetica e cloruro di alluminio C ( C) 2 Al 3 C 2 C
15 7. Completare le seguenti reazioni, specificando i nomi dei composti organici che si formano: a) metilbenzene cloruro di isobutile Al 3 Al3 oisobutilmetilbenzene poco C 2 3 C C trasposizione 3 C C oterzbutilmetilbenzene pterzbutilmetilbenzene pisobutilmetilbenzene b) benzene 1cloro2butene e cloruro di alluminio C 2 C C C 2 C C Al 3 1fenil2butene C C C 2 3fenil1butene C 2 C C Al 3 Al4 C 2 C C C 2 C C
16 c) benzene cloruro di butanoile e cloruro di alluminio C 2 C 2 C Al 3 C 1fenil1butanone d) benzene anidride acetica cloruro di alluminio C 3 C C Al 3 C 2 Al 3 C ( C 2 )Al 3 feniletanone acetofenone fenil metil chetone
17 8. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) isopropilbenzene permanganato di potassio (KMn4), a caldo 3 C C C 2 KMn 4, Δ C 2 2 C 2 acido benzencarbossilico b) vinilbenzene acido cloridrico c) metilbenzene cloro, alla luce ultravioletta C C 2 C C C 3 3 C 2 2, hν 1cloro1feniletano cloruro di benzile d) etilbenzene cloro e cloruro ferrico C 2 C 2 2 Fe 3 ocloroetilbenzene C 2 pcloroetilbenzene
18 e) etilbenzene bromo, a caldo C 2 C 2 Δ 1bromo1feniletano f) vinilbenzene permanganato di potassio, a caldo C C 2 C 2 KMn 4, Δ C 2 C 2 acido benzencarbossilico g) metilbenzene 1cloropropano e cloruro di alluminio C 2 C 2 Al 3 C 2 C 2 C C 3 3 C C3 C 2 C 2 C ometilpropilbenzene C C3 3 oisopropilmetilbenzene pmetilpropilbenzene pisopropilmetilbenzene
19 h) vinilbenzene 2 (un equivalente) e Pt C C 2 2 Pt C 2 etilbenzene i) vinilbenzene e bromo C C 2 2 C C 2 1,2dibromo1fenilbenzene j) 1,4diidrossi2metossibenzene ossido di argento Ag 2 2metossi1,4benzochinone
20 k) benzene sodio in ammoniaca ed etanolo a in 3 C 2 1,4cicloesadiene l) vinilbenzene 2 (in eccesso) e Pt C C 2 C 2 2 (eccesso) Pt etilcicloesano 9. Scrivere l'equazione chimica delle seguenti reazioni: a) benzene ossigeno e pentossido di vanadio (V 2 5 ), ad elevata temperatura 2 V 2 5 Δ
21 b) antracene anidride cromica (Cr 3 ) ed acido solforico Cr 3 2 S 4 c) pbenzendiolo ossido di argento (Ag 2 ) Ag 2 d) propilbenzene permanganato di potassio, a caldo. C 2 C 2 C 2 C 2 KMn 4 2 C 2
22 10. Scrivere i prodotti delle seguenti reazioni del cloruro di p metilbenzendiazonio con: a) KI KI I b) CuC CuC C c) K K d) 2, a caldo 2 Δ e) Cu Cu f) a 2, Cu a 2, Cu 2
23 11. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del catalizzatore. 2 Fe 3 Fe 4 Fe 4 Fe Il pdimetilbenzene si nitra molto più facilmente del benzene. Spiegare. 2 C 3 C 3 tutte le posizioni sono identiche; l'addotto σ è stabilizzato dalla presenza del metile in orto 2
24 13. Scrivere il meccanismo della bromurazione aromatica di: Dimostrare l'orientamento, servendosi degli addotti σ. a) anilina (= benzenammina) 2 Fe 3 Fe Fe 4 Fe Fe 4 Fe 3
25 C 2 b) etossibenzene Fe 4 C 2 C 2 C 2 C 2 C 2 Fe 3 C 2 C 2 C 2 C 2 C 2 C 2 C 2 C 2 C 2 C 2 C 2 C 3 Fe 4 Fe 3
26 14. Spiegare perché il metilbenzene è ortopara orientante, mentre il triclorometilbenzene è meta orientante. E E E stabili C 3 C 3 C 3 C 3 E instabili E E
27 15. Scrivere le reazioni di bromurazione, solfonazione e nitrazione dei seguenti composti, scrivendo in ciascun caso il prodotto (o i prodotti) di reazione ed indicando se la reazione avviene più velocemente o più lentamente della corrispondente reazione del benzene: omurazione: 2 Fe 3 Fe4 E Solfonazione: S 3 E itrazione: E 2 2 S a) metossibenzene stabile stabile
28 C 3 S S S 3 S 3 S stabile S 3 S 3 S 3 S 3 S 3 S 3 S 3 S 3 stabile S 3 rientamento: orto para
29 stabile S stabile 2 2 Reattività: R,I, con R > I rilascio elettronico più reattivo di benzene B. L esercizio andrebbe svolto per tutti i composti come è stato svolto con il metossibenzene
30 b) difluorometilbenzene c) etilbenzene CF 2 rientamento: meta attrazione (I) meno reattivo C 2 rientamento: orto para rilascio (I) più reattivo d) clorobenzene e) nitrobenzene rientamento: orto para attrazione (I > R) meno reattivo 2 rientamento: meta attrazione (I) meno reattivo f) acido benzensolfonico g) benzoato di etile S 3 rientamento: meta C C C 2 3 attrazione (I) rientamento: meta meno reattivo attrazione (I) meno reattivo h) difenil etere rientamento: orto para rilascio (R > I) più reattivo
31 i) bifenile rientamento: orto para rilascio (R > I) più reattivo C 3 j) terzbutilbenzene k) fluorobenzene F C rientamento: orto para rilascio (I) più reattivo rientamento: orto para attrazione (I > R) meno reattivo l) metilbenzene rientamento: orto para rilascio (I) più reattivo C m) acetato di fenile rientamento: orto para rilascio (R > I) più reattivo
32 n) acetilbenzene (= acetofenone, oppure fenil metil chetone oppure 1feniletanone) C rientamento: meta attrazione (I) meno reattivo o) benzammide C 2 rientamento: meta attrazione (I) meno reattivo p) benzonitrile C rientamento: meta attrazione (I) meno reattivo q) iodobenzene I rientamento: orto para attrazione (I > R) meno reattivo
33 25. a) Scrivere l'equazione chimica della reazione che avviene trattando il metilbenzene con cloruro di propanoile e cloruro di alluminio, giustificando l'orientamento. Spiegare l'ordine di reattività che si osserva se, nelle condizioni di (a) si fanno reagire: mdimetilbenzene, metilbenzene, fluorobenzene, benzene. C 2 C Al 3 CC2 orientamento: CC 2 CC 2 REATTIVITA' > > > F I di due I I > R
34 27. Il fenolo viene trattato con una soluzione acquosa di bromo; a) scrivere l equazione chimica della reazione, giustificandone l orientamento; b) commentare le condizioni in cui la reazione avviene, confrontandole con quelle necessarie perché la reazione avvenga con il benzene. 2 2 orientamento: è gruppo a FRTE rilascio elettronico (R > I): arricchidce di elettroni l anello aromatico, tanto che basta la polarizzazione provocata dall acqua per far avvenire la sostituzione elettrofila aromatica: non serve l acido di Lewis come con il benzene.
35 32. a) Scrivere la reazione dell'anilina con il cloruro di p clorobenzendiazonio e spiegare perché questo elettrofilo non reagisce con l'acetanilide (= feniletanammide) Sale di diazonio: E debole reagisce solo con substrati MLT ricchi di elettroni C C C è un donatore peggiore di 2 : I maggiore (un atomo elettronegativo in più), R minore
36 b) L'anilina reagisce più velocemente con il cloruro di benzendiazonio o con il cloruro di 2,4dinitrobenzendiazonio? 2 2 elettrofilo più forte di Un elettrofilo è una specie PVERA di elettroni: i gruppi 2 (I, R) aumentano la carica positiva 33. L'acido salicilico (= acido oidrossibenzoico) e l'aldeide salicilica (= o idrossibenzencarbaldeide) si preparano dal fenolo. Scrivere le reazioni corrispondenti e spiegare perché gli stessi reagenti non danno reazione con il benzene. C elettrofili deboli C 2 Δ, P C 3 C
37 34. a) Scrivere l'equazione chimica ed il meccanismo della nitrazione aromatica del naftalene, giustificandone l'orientamento. equazione: S 4 meccanismo: 3 2 S S addotto in β meno stabile: orientamento in α
38 b) Scrivere l'equazione chimica ed il meccanismo della solfonazione a bassa temperatura del naftalene. Spiegare perché a temperature più elevate si ottiene un isomero diverso. equazione: S 3 S 3 meccanismo: 2 S 4 a bassa temperatura S 3 S 3 S 3 S 3 S 3 a bassa temperatura a temperatura elevata controllo cinetico controllo termodinamico S 3 (voluminoso) in β è più stabile S 3 S 3
39 35. A differenza di benzene e naftalene, il fenantrene addiziona una molecola di bromo. Scrivere la reazione e spiegare perché avviene, servendosi delle strutture di risonanza del fenantrene. 2 9,10dibromo9,10diidrofenantrene
40 37. Completare le seguenti reazioni di sostituzione nucleofila aromatica, specificando se avvengono con meccanismo di addizioneeliminazione o di eliminazioneaddizione (via benzino); spiegare il perché della scelta. a) pnitrobromobenzene K 2 K 2 2 b) mcloronitrobenzene K 2 K 2 2 addizioneeliminazione presenza di eliminazioneaddizione 2 non è in posizione tale da ospitare la carica negativa c) pdiclorobenzene K (in eccesso) K eliminazioneaddizione non c'è un sostituente in grado di stabilizzare l'addotto anionico
41 K (eccesso) eliminazioneaddizione non c'è un sostituente in grado di stabilizzare l'addotto anionico d) 2,4,6trinitroclorobenzene K 2 2 K 2 2 addizioneeliminazione 2 2 Tutti e tre i gruppo 2 sono in grado di stabilizzare la carica negativa dell'anione ecc.
42 e) 4nitroclorobenzene K 2 K 2 addizioneeliminazione 2 in grado di stabilizzare la carica negativa dell'anione f) mclorometilbenzene K K 2 eliminazioneaddizione non c'è un sostituente in grado di stabilizzare l'addotto anionico
43 g) pclorometilbenzene K K eliminazioneaddizione non c'è un sostituente in grado di stabilizzare l'addotto anionico 38. Scrivere equazione chimica e meccanismo delle seguenti reazioni: a) 2,4dinitroclorobenzene sodioammide a b) 1,2dicloro3,5dinitrobenzene metossido di sodio (un equivalente) in metanolo a addizioneeliminazione
44 c) 1,2dicloro3,5dinitrobenzene metossido di sodio (due equivalenti) in metanolo; a a C d) 4clorometilbenzene K ad elevata temperatura K Δ eliminazioneaddizione e) 3bromometilbenzene dietilammide di litio [= ( C 2 ) 2 Li ] in dietilammina. (C 2 ) 2 ( C 2 ) 2 Li (C 2 ) 2 R 2 R 2 R 2 R 2 (C 2 ) 2
45 40. Il 2,4,6trinitroclorobenzene reagisce con a in acqua. a) Scrivere equazione chimica e meccanismo della reazione. b) Il nome corrente del prodotto è "acido picrico", pur trattandosi di un fenolo. Come mai? 2 2 a è molto acido, per la presenza dei tre gruppi nitro (I, R) 45. Il defoliante Agent range, usato nella guerra del Vietnam (e che è ritenuto responsabile della malattia e della morte di molti reduci, anche a distanza di anni), contiene l'acido (2,4,5triclorofenossi)etanoico, indicato come 2,4,5T. Questo acido si prepara per reazione parziale dell'1,2,4,5tetraclorobenzene con a, seguita da reazione con cloroacetato di sodio. C 2 C 2 2,4,5T a) Scrivere la reazione di sintesi del 2,4,5T.
46 a C 2 C C 2 C 2 C 2 C 2 2,4,5T b) Una delle impurezze contenute nell' Agent range (probabilmente il principale componente tossico) era la 2,3,7,8tetraclorodibenzodiossina, 2,3,7,8TCDD, spesso chiamata, impropriamente, diossina. Indicare come 2,3,7,8TCDD si forma nel corso della sintesi di 2,4,5T. la 2,3,7,8tetraclorodibenzodiossina viene dalla sostituzione nucleofila tra due molecole di fenossido 2,3,7,8TCDD
47 c) Come si può eliminare la contaminazione da TCDD sia dopo il primo passaggio che alla fine della sintesi? c) 2,3,7,8TCDD non è solubile in acqua L estrazione con una soluzione acquosa moderatamente basica (bicarbonato) purifica il 2,4,5T
Esercitazione n Reazioni e meccanismi dei composti aromatici.
 sercitazione n. 1 Reazioni e meccanismi dei composti aromatici.. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del catalizzatore. Fe Fe Fe Fe. Il pdimetilbenzene
sercitazione n. 1 Reazioni e meccanismi dei composti aromatici.. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del catalizzatore. Fe Fe Fe Fe. Il pdimetilbenzene
CHIMICA ORGANICA I. 3. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del catalizzatore.
 CHIMICA RGANICA I Corso di laurea in CHIMICA (LT) Esercitazione n. 14 - Reazioni e meccanismi dei composti aromatici. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI QUEST FGLI: Reazione di sostituzione
CHIMICA RGANICA I Corso di laurea in CHIMICA (LT) Esercitazione n. 14 - Reazioni e meccanismi dei composti aromatici. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI QUEST FGLI: Reazione di sostituzione
1. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: CH 3
 Esercitazione n. 14 Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2butene b) 2butene acqua, in ambiente
Esercitazione n. 14 Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2butene b) 2butene acqua, in ambiente
Esercitazione - Reazioni sulle reazioni di alcheni. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: CH 3
 Esercitazione - Reazioni sulle reazioni di alcheni. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2-butene b) 2-butene acqua, in ambiente acido 2-bromobutano
Esercitazione - Reazioni sulle reazioni di alcheni. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2-butene b) 2-butene acqua, in ambiente acido 2-bromobutano
Esercitazione n Reazioni sulle reazioni di alcheni, alchini e dieni.
 Esercitazione n. 1 Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) butene b) butene acqua, in ambiente
Esercitazione n. 1 Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) butene b) butene acqua, in ambiente
CHIMICA ORGANICA I. Corso di laurea in CHIMICA, CHIMICA APPLICATA, SCIENZA DEI MATERIALI
 CHIMICA RGANICA I Corso di laurea in CHIMICA, CHIMICA APPLICATA, SCIENZA DEI MATERIALI Esercitazione n. 14 - Reazioni di alcheni, alchini e dieni. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI
CHIMICA RGANICA I Corso di laurea in CHIMICA, CHIMICA APPLICATA, SCIENZA DEI MATERIALI Esercitazione n. 14 - Reazioni di alcheni, alchini e dieni. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI
BENZENE E DERIVATI. Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6. Arene: Idrocarburo aromatico
 BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 H 12 ; b. C 2 H 5 Cl; c. C 4 H 10 O.
 1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 12 ; b. C 2 5 Cl; c. C 4 10. 2. Scrivere la formula di struttura dei seguenti composti: a.
1. Scrivere la formula di struttura di tutti i possibili isomeri aventi le seguenti formule molecolari: a. C 5 12 ; b. C 2 5 Cl; c. C 4 10. 2. Scrivere la formula di struttura dei seguenti composti: a.
Aromaticità. Addizione elettrofila alcheni
 Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
COMPOSTI AROMATICI. L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. UVvisibile Il benzene ha legami π coniugati Lo spettro di assorbimento
CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. UVvisibile Il benzene ha legami π coniugati Lo spettro di assorbimento
Benzene e Composti Aromatici
 Benzene e Composti Aromatici Contenuti della lezione: Il benzene e i requisiti per l aromaticità Nomenclatura di benzeni mono- e di-sostituiti Composti aromatici diversi dal benzene: IPA e eteroaromatici
Benzene e Composti Aromatici Contenuti della lezione: Il benzene e i requisiti per l aromaticità Nomenclatura di benzeni mono- e di-sostituiti Composti aromatici diversi dal benzene: IPA e eteroaromatici
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
CHIMICA ORGANICA. Gli idrocarburi aromatici
 1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
Stabilità del benzene (entalpie di idrogenazione) Energia di risonanza
 La chimica del benzene e dei suoi derivati I derivati del benzene vengono chiamati composti aromatici poiché inizialmente vennero isolati dal catrame nel 1800 ed erano caratterizzati da un odore aromatico.
La chimica del benzene e dei suoi derivati I derivati del benzene vengono chiamati composti aromatici poiché inizialmente vennero isolati dal catrame nel 1800 ed erano caratterizzati da un odore aromatico.
COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 MPSTI ARMATII L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. aratteristiche Spettrali La maggior parte dei composti aromatici Spettrometria
MPSTI ARMATII L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. aratteristiche Spettrali La maggior parte dei composti aromatici Spettrometria
Unità didattica 7 (segue) Reattività del benzene. Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili
 Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Complementi di Chimica Organica. Composti Aromatici: Benzene C 6 H 6 (1825) (1865) Friedrich August Kekulé
 Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
REATTIVITA DEI BENZENI SOSTITUITI
 REATTIVITA DEI BENZENI SOSTITUITI 1) Sostituzione radicalica di idrogeni benzilici Reazioni dei sostituenti presenti sull anello benzenico Reazioni dei sostituenti presenti sull anello benzenico 2) Reazioni
REATTIVITA DEI BENZENI SOSTITUITI 1) Sostituzione radicalica di idrogeni benzilici Reazioni dei sostituenti presenti sull anello benzenico Reazioni dei sostituenti presenti sull anello benzenico 2) Reazioni
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
COMPOSTI AROMATICI POLICICLICI
 CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
Esercitazione n Reazioni e meccanismi di acidi carbossilici e derivati.
 Esercitazione n. 16 Reazioni e meccanismi di acidi carbossilici e derivati. 1. Scrivere i prodotti (specificandone il nome) che si ottengono quando l'acido butanoico viene fatto reagire con ciascuno dei
Esercitazione n. 16 Reazioni e meccanismi di acidi carbossilici e derivati. 1. Scrivere i prodotti (specificandone il nome) che si ottengono quando l'acido butanoico viene fatto reagire con ciascuno dei
COMPOSTI AROMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti.
 CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
CMPSTI ARMATICI L aromaticità è l aspetto strutturale determinante per le caratteristiche spettrali e di reattività di questi composti. Caratteristiche Spettrali Spettrometria di massa La maggior parte
CICLOALCHENI. legame π C. Una frammentazione importante dà un valore m/z = 41, che corrisponde al carbocatione allilico +. + R CH + CH 2 CH CH 2
 ALI ILALI ARATTRISTIA FUZIAL: legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 41, che corrisponde al carbocatione allilico. R. R UVvisibile Un
ALI ILALI ARATTRISTIA FUZIAL: legame π aratteristiche Spettrali Spettrometria di massa Una frammentazione importante dà un valore m/z = 41, che corrisponde al carbocatione allilico. R. R UVvisibile Un
COMPOSTI AROMATICI. Formula C 6 H 6
 COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
Esercitazione n Reazioni degli alcani
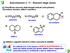 Esercitazione n 11 - Reazioni degli alcani 1 assificare ciascuno degli idrogeni indicati come primario, secondario, terziario, allilico o benzilico: a) ( ) C b) ( ) CH c) H primario d) e) terziario H H
Esercitazione n 11 - Reazioni degli alcani 1 assificare ciascuno degli idrogeni indicati come primario, secondario, terziario, allilico o benzilico: a) ( ) C b) ( ) CH c) H primario d) e) terziario H H
CHIMICA ORGANICA II. Corso di laurea in CHIMICA (LT)
 IMIA RGAIA II orso di laurea in IMIA (LT) Esercitazione n. 4 - Formazione di legami - (I) 1. Scrivere i prodotti delle seguenti reazioni indicare il nuovo legame carbonio-carbonio formato ed identificare
IMIA RGAIA II orso di laurea in IMIA (LT) Esercitazione n. 4 - Formazione di legami - (I) 1. Scrivere i prodotti delle seguenti reazioni indicare il nuovo legame carbonio-carbonio formato ed identificare
CHIMICA ORGANICA I. Corso di laurea in CHIMICA (LT) Esercitazione n Reazioni e meccanismi dei composti aromatici.
 CHIMICA RGAICA I Corso di laurea in CHIMICA (LT) Esercitazione n. 14 - Reazioni e meccanismi dei composti aromatici. TERMII ED ARGMETI PER L SVLGIMET DEGLI ESERCIZI DI QUEST FGLI: Reazione di sostituzione
CHIMICA RGAICA I Corso di laurea in CHIMICA (LT) Esercitazione n. 14 - Reazioni e meccanismi dei composti aromatici. TERMII ED ARGMETI PER L SVLGIMET DEGLI ESERCIZI DI QUEST FGLI: Reazione di sostituzione
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile
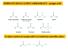 DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
CHIMICA ORGANICA I. Corso di laurea in CHIMICA, CHIMICA APPLICATA, SCIENZA DEI MATERIALI
 CHIMICA RGANICA I Corso di laurea in CHIMICA, CHIMICA APPLICATA, SCIENZA DEI MATERIALI Esercitazione n. 11 - Reazioni degli alogenuri alchilici. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI QUEST
CHIMICA RGANICA I Corso di laurea in CHIMICA, CHIMICA APPLICATA, SCIENZA DEI MATERIALI Esercitazione n. 11 - Reazioni degli alogenuri alchilici. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI QUEST
Idrocarburi AROMATICI
 Idrocarburi AROMATICI Composti aromatici Gli idrocarburi aromatici costituiscono una particolare classe di composti che contengono 2n 1 doppi legami coniugati in una struttura ciclica, strutturalmente
Idrocarburi AROMATICI Composti aromatici Gli idrocarburi aromatici costituiscono una particolare classe di composti che contengono 2n 1 doppi legami coniugati in una struttura ciclica, strutturalmente
Composti aromatici. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Composti aromatici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Composti aromatici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
30 Aprile 2008 Nome:
 30 Aprile 2008 Nome: SECND ESAME PARZIALE DI CHIMICA RGANICA per tossicologia ambientale. A.A. 2007/2008 Risolvi i seguenti esercizi nel tempo massimo di 1 ora, senza l'ausilio di libri di testo o appunti.
30 Aprile 2008 Nome: SECND ESAME PARZIALE DI CHIMICA RGANICA per tossicologia ambientale. A.A. 2007/2008 Risolvi i seguenti esercizi nel tempo massimo di 1 ora, senza l'ausilio di libri di testo o appunti.
BENZENE E COMPOSTI AROMATICI
 BENZENE E COMPOSTI AROMATICI Il capostipite dei composti aromatici è il benzene: H H H H H Il benzene è formato da 6 atomi di C, ibridizzati sp 2, di conseguenza ha una struttura planare. Ogni atomo di
BENZENE E COMPOSTI AROMATICI Il capostipite dei composti aromatici è il benzene: H H H H H Il benzene è formato da 6 atomi di C, ibridizzati sp 2, di conseguenza ha una struttura planare. Ogni atomo di
Anno accademico
 Scuola Normale Superiore Ammissione al 4 anno della Classe di Scienze Compito di Chimica rganica per l ammissione al Corso di laurea specialistica in Chimica, Chimica Industriale, Scienze Geologiche, Gestione
Scuola Normale Superiore Ammissione al 4 anno della Classe di Scienze Compito di Chimica rganica per l ammissione al Corso di laurea specialistica in Chimica, Chimica Industriale, Scienze Geologiche, Gestione
Esteri degli acidi carbossilici
 Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
CHIMICA ORGANICA I. Corso di laurea in CHIMICA (LT)
 CHIMICA RGANICA I Corso di laurea in CHIMICA (LT) Esercitazione n. 13 - Reazioni di alcheni, alchini e dieni. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI QUEST FGLI: Reazioni degli alcheni. Addizioni
CHIMICA RGANICA I Corso di laurea in CHIMICA (LT) Esercitazione n. 13 - Reazioni di alcheni, alchini e dieni. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERCIZI DI QUEST FGLI: Reazioni degli alcheni. Addizioni
PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento
 PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
Guida alla soluzione dei problemi da Chimica organica di Brown, Iverson, Anslyn, Foote
 B. L. Iverson S. Iverson Guida alla soluzione dei problemi da Chimica organica di Brown, Iverson, Anslyn, Foote IV edizione Titolo originale: Brown, Iverson, Anslyn, Foote Student Study Guide and Solutions
B. L. Iverson S. Iverson Guida alla soluzione dei problemi da Chimica organica di Brown, Iverson, Anslyn, Foote IV edizione Titolo originale: Brown, Iverson, Anslyn, Foote Student Study Guide and Solutions
Esercitazione n Reazioni e meccanismi di aldeidi e chetoni.
 19. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene tra etanale e metanolo, in presenza di acidi. b) Spiegare come varia la reattività se con metanolo si fa reagire l'aldeide
19. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene tra etanale e metanolo, in presenza di acidi. b) Spiegare come varia la reattività se con metanolo si fa reagire l'aldeide
1. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: CH 3 O, H +
 Esercitazione n. 14 - Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2-butene b) 2-butene acqua,
Esercitazione n. 14 - Reazioni sulle reazioni di alcheni, alchini e dieni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) 2-butene b) 2-butene acqua,
Sostituzione elttrofila aromatica. Avviene su tutti i substrati aromatici. Solo su substrati non disattivati. Soloo derivati attivati
 Sostituzione elttrofila aromatica Avviene su tutti i substrati aromatici Solo su substrati non disattivati. Soloo derivati attivati Le sostituzioni nucleofile possono esseree descritta da un unico meccanismo
Sostituzione elttrofila aromatica Avviene su tutti i substrati aromatici Solo su substrati non disattivati. Soloo derivati attivati Le sostituzioni nucleofile possono esseree descritta da un unico meccanismo
Il termine arene viene impiegato per descrivere gli idrocarburi aromatici, in analogia con gli alcheni. prodotto di sostituzione.
 I Il termine aromatico venne riferito inizialmente all odore caratteristico di questa categoria di idrocarburi. Successivamente, tale nome è stato usato per indicare che questi composti sono altamente
I Il termine aromatico venne riferito inizialmente all odore caratteristico di questa categoria di idrocarburi. Successivamente, tale nome è stato usato per indicare che questi composti sono altamente
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Delocalizzazione elettronica
 Il benzene Il benzene è un idrocarburo la cui formula bruta, nota sin dal 1825, è C 6 H 6. La formula molecolare evidenzia un elevato grado di insaturazione, tuttavia il benzene non mostra l elevata reattività
Il benzene Il benzene è un idrocarburo la cui formula bruta, nota sin dal 1825, è C 6 H 6. La formula molecolare evidenzia un elevato grado di insaturazione, tuttavia il benzene non mostra l elevata reattività
Composti aromatici. Il capofamiglia... il benzene. Scoperta del benzene
 Scoperta del benzene Composti aromatici Prof.ssa Silvia ecchia Il capofamiglia... il benzene Una molecola può essere definita aromatica se contiene almeno un anello aromatico, cioè un anello composto da
Scoperta del benzene Composti aromatici Prof.ssa Silvia ecchia Il capofamiglia... il benzene Una molecola può essere definita aromatica se contiene almeno un anello aromatico, cioè un anello composto da
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
14/11/2018. Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile.
 Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Benzene e areni. Struttura e aromaticità. N.B. La doppia freccia indica che le due strutture sono in equilibrio
 Benzene e areni Il benzene, C6H6, è il capostipite di una ampia classe di idrocarburi, eccezionalmente stabili, detti aromatici. Il nome è dovuto al caratteristico odore di questa sostanza che è stata
Benzene e areni Il benzene, C6H6, è il capostipite di una ampia classe di idrocarburi, eccezionalmente stabili, detti aromatici. Il nome è dovuto al caratteristico odore di questa sostanza che è stata
REAZIONI DEI COMPOSTI AROMATICI
 Mauro Tonellato REAZII DEI MPSTI ARMATII Indice 2 - Alogenazione 3 - itrazione 4 - Solfonazione 5 - Alchilazione di riedel rafts 6 - Acilazione di riedel rafts 7 - Sostituenti attivanti e disattivanti
Mauro Tonellato REAZII DEI MPSTI ARMATII Indice 2 - Alogenazione 3 - itrazione 4 - Solfonazione 5 - Alchilazione di riedel rafts 6 - Acilazione di riedel rafts 7 - Sostituenti attivanti e disattivanti
Esercitazione n Reazioni degli alogenuri alchilici.
 Esercitazione n. 1 - Reazioni degli alogenuri alchilici. 1. Dare definizione ed un esempio per ciascuno dei seguenti termini: Non sottovalutate questo tipo di esercizio: è importante saper esporre in modo
Esercitazione n. 1 - Reazioni degli alogenuri alchilici. 1. Dare definizione ed un esempio per ciascuno dei seguenti termini: Non sottovalutate questo tipo di esercizio: è importante saper esporre in modo
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1
 CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
Esercitazione n Reazioni acido-base. 3. Nelle seguenti reazioni acido-base individuare l'acido e la base: H NH
 Esercitazione n 10 Reazioni acidobase Nelle seguenti reazioni acidobase individuare l'acido e la base: 1) N : 2 N 4 2 2) N 4 2 N ) 2 2 2 BASE 4) BASE AID AID AID BASE N N BASE AID 2 6) 5) 2 AID BASE N
Esercitazione n 10 Reazioni acidobase Nelle seguenti reazioni acidobase individuare l'acido e la base: 1) N : 2 N 4 2 2) N 4 2 N ) 2 2 2 BASE 4) BASE AID AID AID BASE N N BASE AID 2 6) 5) 2 AID BASE N
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab.
 I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
REAZIONI DEGLI ALCHENI
 REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
La condensazione di Claisen
 La condensazione di Claisen Oltre alle aldeidi e chetoni anche gli esteri possono generare enolati e funzionare da elettrofili.. Quando un estere viene trattato con una base avviene una trasformazione
La condensazione di Claisen Oltre alle aldeidi e chetoni anche gli esteri possono generare enolati e funzionare da elettrofili.. Quando un estere viene trattato con una base avviene una trasformazione
Ammine. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, Nominativo.Matricola
 Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, 19-06-2017 Nominativo.Matricola Esercizio 1a. Il cis-2-pentene viene trattato con Br 2 in diclorometano. a) Descrivere
Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, 19-06-2017 Nominativo.Matricola Esercizio 1a. Il cis-2-pentene viene trattato con Br 2 in diclorometano. a) Descrivere
Composti AROMATICI. Il Puzzle del Benzene. + Br 2 dà reazione di sostituzione elettrofila C 6. Br + H 2 H 12
 Composti AMATICI Dallo studio degli olii essenziali viene scoperta una nuova classe di composti con un elevato rapporto C /, chiamati AMATICI per il piacevole odore. Il Puzzle del Benzene C 6 6 relativamente
Composti AMATICI Dallo studio degli olii essenziali viene scoperta una nuova classe di composti con un elevato rapporto C /, chiamati AMATICI per il piacevole odore. Il Puzzle del Benzene C 6 6 relativamente
Idrocarburi aromatici
 Idrocarburi aromatici Gli idrocarburi aromatici, o areni, sono composti organici costituiti da almeno un anello di atomi di carbonio uniti da legami ad elettroni delocalizzati. Il termine «aromatico» era
Idrocarburi aromatici Gli idrocarburi aromatici, o areni, sono composti organici costituiti da almeno un anello di atomi di carbonio uniti da legami ad elettroni delocalizzati. Il termine «aromatico» era
Esercitazione n Reazioni sulle reazioni di alcheni.
 Esercitazione n. 1 - Reazioni sulle reazioni di alcheni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) -butene b) -butene acqua, in ambiente acido -bromobutano,
Esercitazione n. 1 - Reazioni sulle reazioni di alcheni. 1. ompletare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a) -butene b) -butene acqua, in ambiente acido -bromobutano,
Idrocarburi Saturi. Reazioni
 Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Composti carbonilici
 Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1
 REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
AMMINE. con acidi RNH 2. con O come elettrofilo RNH 2 + H + + R NH 3 NESSUNA REAZIONE. atomo basico, atomo nucleofilo
 AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Esercitazione n Reazioni di alcooli, dioli, eteri, ammine, sali di ammonio.
 Esercitazione n. 1 - Reazioni di alcooli, dioli, eteri, ammine, sali di ammonio. 1. Scrivere il prodotto, specificandone il nome, della reazione con P di: R- P R- P S N 2 a) 1-propanolo b) 2-propanolo
Esercitazione n. 1 - Reazioni di alcooli, dioli, eteri, ammine, sali di ammonio. 1. Scrivere il prodotto, specificandone il nome, della reazione con P di: R- P R- P S N 2 a) 1-propanolo b) 2-propanolo
the polycyclic system is oriented so that (a) the greatest number of rings are in a horizontal row and (b) a maximum number of rings are above and to
 β α α β β α α β the polycyclic system is oriented so that (a) the greatest number of rings are in a horizontal row and (b) a maximum number of rings are above and to the right of the horizontal row (upper
β α α β β α α β the polycyclic system is oriented so that (a) the greatest number of rings are in a horizontal row and (b) a maximum number of rings are above and to the right of the horizontal row (upper
Voto. Prova scritta di Chimica Organica del 28/1/2011 Compito A CHO COGNOME: Nome:
 Prova scritta di Chimica rganica del 28/1/2011 Compito A _ riportata? CH (2) Scrivere il prodotto di di-ossidrilazione e di addizione di bromo del seguente composto (quale è il suo nome IUPAC?). Si indichino
Prova scritta di Chimica rganica del 28/1/2011 Compito A _ riportata? CH (2) Scrivere il prodotto di di-ossidrilazione e di addizione di bromo del seguente composto (quale è il suo nome IUPAC?). Si indichino
Alcoli ed eteri Composti organici che contengono legami singoli C-O
 Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Ammine R N + H. ammina terziaria ammina secondaria ammina primaria sale di ammonio quaternario
 AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
ACIDI CARBOSSILICI e derivati
 ACIDI CABSSILICI e derivati Il nome sistematico di un acido carbossilico alchilico si fa derivare dal nome dell idrocarburo con lo stesso numero di atomi di carbonio, sostituendo la o finale con la desinenza
ACIDI CABSSILICI e derivati Il nome sistematico di un acido carbossilico alchilico si fa derivare dal nome dell idrocarburo con lo stesso numero di atomi di carbonio, sostituendo la o finale con la desinenza
Le due formule limite equivalenti del cicloesatriene. I legami sono tutti uguali, perché le due formule sono equivalenti.
 Idrocarburi aromatici. Si è già visto come la coniugazione fra più sistemi di elettroni π porti ad una stabilizzazione della molecola, oltre che al cambiamento delle proprietà chimiche (addizione 1,2 e
Idrocarburi aromatici. Si è già visto come la coniugazione fra più sistemi di elettroni π porti ad una stabilizzazione della molecola, oltre che al cambiamento delle proprietà chimiche (addizione 1,2 e
Verifiche dei Capitoli - Tomo C
 Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Esercitazione n. 3 - Nomenclatura (II)
 Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
MECCANISMI DELLE REAZIONI ORGANICHE
 MEASM DELLE REAZ RGAE orso di Laurea Magistrale in himica Esercitazione #3. inetica delle reazioni 1. onsiderando una reazione di stechiometria: A B D, che è di primo ordine in ciascuno dei due reagenti,
MEASM DELLE REAZ RGAE orso di Laurea Magistrale in himica Esercitazione #3. inetica delle reazioni 1. onsiderando una reazione di stechiometria: A B D, che è di primo ordine in ciascuno dei due reagenti,
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di:
 Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
Sistema i seguenti carbocationi in ordine di stabilità crescente:
 Sistema i seguenti carbocationi in ordine di stabilità crescente: C 2 + + + Completa le seguenti reazioni: 3 C C C 2 + C 2 + + Disegna le formule di struttura per i carbocationi isomerici formati per reazione
Sistema i seguenti carbocationi in ordine di stabilità crescente: C 2 + + + Completa le seguenti reazioni: 3 C C C 2 + C 2 + + Disegna le formule di struttura per i carbocationi isomerici formati per reazione
Capitolo 6 Composti Aromatici
 himica Organica Scienze della Terra, dell Ambiente e del Territorio apitolo 6 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. Scoperta del Benzene I composti aromatici sono tra i primi
himica Organica Scienze della Terra, dell Ambiente e del Territorio apitolo 6 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. Scoperta del Benzene I composti aromatici sono tra i primi
Reazioni degli alcoli
 Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
ISTRUZIONE OPERATIVA N. 04 INCOMPATIBILITA. Revisione 00 - Gennaio A cura di: Servizio Ambiente e Progettazione per la Sicurezza
 ISTRUZIONE OPERATIVA N. 04 Revisione 00 - Gennaio 2015 A cura di: Servizio Ambiente e Progettazione per la Sicurezza ISTRUZIONE OPERATIVA N.04. Scopo e campo di applicazione Il rifiuto, prima di essere
ISTRUZIONE OPERATIVA N. 04 Revisione 00 - Gennaio 2015 A cura di: Servizio Ambiente e Progettazione per la Sicurezza ISTRUZIONE OPERATIVA N.04. Scopo e campo di applicazione Il rifiuto, prima di essere
Ammissione al dottorato in Scienze Chimiche 2014 COPIA UFFICIALE DEL TESTO DELLA PROVA SCRITTA
 Ammissione al dottorato in Scienze Chimiche 2014 COPIA UFFICIALE DEL TESTO DELLA PROVA SCRITTA CHIMICA FISICA: compito C 1) Dare la definizione di Quantità intensiva e di Quantità estensiva di un sistema
Ammissione al dottorato in Scienze Chimiche 2014 COPIA UFFICIALE DEL TESTO DELLA PROVA SCRITTA CHIMICA FISICA: compito C 1) Dare la definizione di Quantità intensiva e di Quantità estensiva di un sistema
Capitolo 10 Composti Aromatici
 himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
1. Per capire la chimica del gruppo carbonile bisogna ricordarsi che il legame C=O è polarizzato
 1. Per capire la chimica del gruppo carbonile bisogna ricordarsi che il legame C= è polarizzato elettrofili protoni, acidi di Lewis X Y X Y nucleofili Scrivere le formule di risonanza per acetaldeide,
1. Per capire la chimica del gruppo carbonile bisogna ricordarsi che il legame C= è polarizzato elettrofili protoni, acidi di Lewis X Y X Y nucleofili Scrivere le formule di risonanza per acetaldeide,
26. Scrivere per ciascuno dei seguenti nomi la formula (semicondensata e a linea di legame) corrispondente: Cl Cl (CH 3 CHCH 2 ) 2 CH CH.
 6. Scrivere per ciascuno dei seguenti nomi la formula (semicondensata e a linea di legame) corrispondente: cloruro di isobutile cloro metilpropano ( ) bromociclopentano, dibromocicloesano iodoeptano,,
6. Scrivere per ciascuno dei seguenti nomi la formula (semicondensata e a linea di legame) corrispondente: cloruro di isobutile cloro metilpropano ( ) bromociclopentano, dibromocicloesano iodoeptano,,
+ NO 2 + 3H 2 O = Ce +3 + NO 3 + 2H 3 O +, b) 0.478 g
 1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
Composti carbonilici. Componente principale dell aceto. Principio attivo di molti farmaci. Resina per abbigliamento
 Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Composti carbonilici Composti carbonilici Acido acetico Si trovano nella maggior parte delle molecole biologiche, farmaceutiche e di sintesi Componente principale dell aceto Principio attivo di molti farmaci
Reazioni di radicali. Reazioni di propagazione Reazioni di terminazione
 Reazioni di radicali Reazioni di propagazione Reazioni di terminazione Reazioni di propagazione Processi di trasferimento di radicali coinvolgono un radicale ed una molecola di substrato e portano alla
Reazioni di radicali Reazioni di propagazione Reazioni di terminazione Reazioni di propagazione Processi di trasferimento di radicali coinvolgono un radicale ed una molecola di substrato e portano alla
