Chimica Inorganica Biologica Il diossigeno O 2
|
|
|
- Oliviero Chiari
- 5 anni fa
- Visualizzazioni
Transcript
1 Il diossigeno O 2 Tossicità di O 2 La comparsa di O 2 sulla terra ha rappresentato una catastrofe ecologica in quanto organismi anaerobici dovettero trasformarsi in aerobici. Fe II (solubile) Fe III (insolubile); Cu I (insolubile) Cu II (solubile); S II (insolubile) SO 4 2 (solubile); Se II (insolubile) SeO 3 2 (solubile); MoS x (insolubile) MoO 4 2 (solubile); CH 4 CO 2 ; H 2 H 2 O; NH 3 NO 3, NO 2, NO.
2 Il diossigeno O 2 Tossicità di O 2 Per sopravvivere alla reattività dell'ossigeno e dei suoi derivati gli organismi dovettero sviluppare una moltitudine di antiossidanti biologici ed un processo opposto alla fotosintesi, la respirazione. I batteri anaerobici attuali derivano dai primitivi organismi anaerobici mentre gli attuali organismi aerobici si sono sviluppati adattando il loro metabolismo al potere ossidante del diossigeno. Il diossigeno è essenziale per la vita degli organismi aerobici, le cellule umane usano O 2 come accettore finale di elettroni nella respirazione: O 2 + 4H + + 4e 2H 2 O
3 Cenni storici Chimica Inorganica Biologica Il diossigeno O 2 o La tossicità del diossigeno fu riconosciuta da Rebecca Gerschman (1954). o Irwin Fridowich imputò invece la tossicità allo ione superossido (1968) o Attualmente il candidato principale è il radicale idrossile. L azione lesiva di queste specie reattive riguarda i lipidi, il DNA e le proteine. Il DNA presente all'interno della cellula è vulnerabile all'attacco ossidativo alla base e allo zucchero; L'ossidazione del DNA può portare a mutazioni. Le proteine possono subire un danno ossidativo alle catene laterali amminoacidiche in particolar modo i residui cisteinici e metioninici. Nella cellula sono comunque presenti le difese opportune.
4 Perossidazione lipidica Chimica Inorganica Biologica I lipidi sono componenti essenziali delle membrane ed il danno ossidativo osservato è dovuto ad autossidazione radicalica. Variazioni irreversibili della catena fosfolipidica o Lipidi o Proteine o DNA
5 Il diossigeno O 2 L'adattamento della vita alla presenza del diossigeno ha potuto realizzarsi, in assenza di catalizzatori, grazie alla lentezza della velocità di reazione del diossigeno. L utilizzazione del diossigeno comporta la possibilità di formazione di specie reattive quali: diossigeno singoletto, superosso, perosso ed ossidrile. Quest ultimo, uno dei più potenti radicali conosciuti, è prodotto dalla riduzione monoelettronica dell acqua ossigenata da Fe 3+ e Cu 2+
6 Sistemi di difesa dell organismo contro i danni ossidativi Le reazioni ossidative avvengono in compartimenti cellulari chiusi: mitocondri e cloroplasti Esistenza di specie molecolari capaci di catturare i derivati tossici dell ossigeno Sistemi che sequestrano ioni metallici con attività redox Tocoferolo (E) membrane cellulari Fe 2+ + H 2 O 2 Fe 3+ + OH - + OH. citosol acido ascorbico (C) Enzimi detossificanti glutatione
7 Cellula Chimica Inorganica Biologica Il diossigeno O 2
8 Enzimi detossificanti Citocromo P-450 Catalasi Perossidasi Superossidismutasi
9 Citocromo P-450 Sono emoproteine il cui sito attivo è molto simile a quello della emoglobina/mioglobina. Appartengono alla famiglia degli enzimi mono-ossigenasi perché catalizzano l inserzione di un atomo di ossigeno in una grande varietà di substrati C C OH Idrossilazione di composti alifatici H OH Idrossilazione di composti aromatici O Epossidazione di alcheni N N +_ O - Ossidazione di ammine a N-ossidi S S O Ossidazione di solfuri a solfossidi
10 Citocromo P-450
11 Citocromo P-450
12 Citocromo P-450 Gli enzimi citocromo P450 costituiscono una superfamiglia (CYP) che conta più di 7700 macromolecole. Il nome deriva dalla lunghezza d onda del picco di assorbimento Fegato Corteccia Surrenale Catalizza reazioni di ossidazione con scarsa selettività dei substrati Metabolismo di sostanze endogene (acidi grassi, steroidi) attraverso reazioni stereospecifiche Sono stati difficili da caratterizzare perché sono legati alle membrane del mitocondrio e del reticolo endoplasmatico e sono poco solubili in acqua. Si è isolato quello presente nel batterio Pseudomonas putida P-450 cam
13 Citocromo P-450 Questi enzimi consistono di una singola catena polipeptidica ( aa). Il gruppo eme b (Fe-protoporfirina IX) è privo di legami covalenti fra l anello porfirinico e la proteina. L atomo è un Fe III BS legato solo ad un atomo di S di una cisteina (RS - ). L altra posizione assiale è probabilmente occupata da una molecola di H 2 O in prossimità di una cavità Il potenziale redox, a ph 7 è 330 mv.
14 Citocromo P-450 Meccanismo Interesse biologico/fisiologico Interesse chimico/sintetico Si è ipotizzato che il meccanismo avvenga attraverso la reazione controllata di O 2 e substrato nella sfera di coordinazione dello ione metallico (reazione templata) Orientazione spaziale (stereospecificità) Attivazione elettronica
15 Citocromo P-450 Fe Fe Cys Met Cys: donatore σ donatore π Met: donatore σ accettore π Campo Debole Alto Spin Campo Forte Basso Spin
16 Interazione con il substrato genera Fe(III) pentacoordinato ad alto spin. La variazione di spin cambia il potenziale redox a +170 mv L aumento di potenziale favorisce la riduzione (via FADH 2 ): si ottiene Fe(II) pentacoordinato ad alto spin, del tutto simile alla specie che coordina O 2 in emoglobina Fe(III) esacoordinato a basso spin: potenziale redox a -330 mv Rimane nel ciclo catalitico la specie estremamente reattiva [Fe IV PO] + che ossida il substrato RH: [Fe IV PO] + +RH Fe III (P) + + ROH La cattura di un H + forma un Fe(III) idroperossido, il quale per rottura eterolitica del legame O-O si trasforma in OH - che viene eliminato come H 2 O per acquisto di un protone. XOH XOOH Se all enzima si aggiunge un peracido XOOH (che funge da donatore di O) il ciclo è cortocircuitato (effetto shunt); ne consegue che l atomo di ossigeno proviene dal perossido -O-OH. La seconda riduzione forma il complesso perossidico O 2 si coordina per dare addotto Fe(II)O 2 o Fe(III)-superossido
17 Perossidasi Classe di emoproteine che catalizza l ossidazione di molecole organiche da parte di H 2 O 2 che viene ridotta ad acqua H 2 O 2 + AH 2 2H 2 O + A Il centro metallico è un Fe(III) alto spin coordinato ad un imidazolo di una istidina. Nella sesta posizione coordina l H 2 O 2 : gli aa presenti da questo lato guidano la coordinazione e promuovono la reazione Mn-perossidasi V-perossidasi Mfree-perossidasi Questi enzimi consentono l eliminazione di H 2 O 2 La riduzione completa avviene solo per 80% di O 2
18 Perossidasi Acidi grassi Ammine Fenoli Xenobiotici Tossine Perossidasi R-CH 2 -COOH + 2H 2 O 2 3 H 2 O + R-CHO + CO 2 ossidazione R-COOH α-ossidazione controllata degli acidi grassi durante la crescita vegetale con formazione di anidride carbonica e di un omologo inferiore Tireoperossidasi Citocromo c perossidasi (CCP) Mieloperossidasi Lignina perossidasi
19 Perossidasi Chimica Inorganica Biologica L enzima più studiato nel gruppo delle perossidasi è HRP (Horseradish Peroxidase)
20 Perossidasi Chimica Inorganica Biologica H 2 O 2 coordina sul Fe(III) e istidina distale media il trasferimento di un H + in modo che entrambi gli idrogeni siano legati sull ossigeno non coordinato al ferro Arg polarizza il legame perossidico favorendo la rottura eterolitica di detto legame Si libera una molecola di acqua e si forma un intermedio Fe(IV)=O con il metallo in uno stato di ossidazione elevato. L anello porfirinco è un radicale catione Composto I è ridotto al Fe(III) di partenza a seguito di due trasferimenti elettronici. Gli elettroni provengono dal substrato che si ossida
21 Catalasi H 2 O 2 + H 2 O 2 2H 2 O + O 2 È stata determinata la struttura della catalasi presente nel fegato di vitello. È una perossidasi speciale perché il suo substrato è una seconda molecola di H 2 O 2. Catalizza la reazione di disproprozione di H 2 O 2 Il Ferro (III) alto spin è coordinato assialmente dal gruppo fenolato dell aminoacido tirosina e da una molecola di acqua che viene spostata dall H 2 O 2.
22 Fe(III)porf + H 2 O 2 Fe(III)porf(OOH) + H + Fe(III)porf(OOH) Fe(IV)porf +. =O + OH - Fe(IV)porf +. =O + H 2 O 2 O 2 + Fe(III)porf + H 2 O Stesso meccanismo visto per le perossidasi e si forma Composto I con ferro ad alta valenza Usando H 2 O 2 marcata si è stabilito che rottura legame O-O non avviene. Si tratta di una riduzione bielettronica del composto I da parte di H 2 O 2, con l ossigeno coordinato al ferro che viene rilasciato in una molecola di acqua
23 Perossidasi e citocromo P-450 R-H O Fe(IV)-Por +. S-Cys His + Arg O Fe(IV)-Por +. His Compound I Come è possibile che la stessa specie ipervalente dia due reazioni molto diverse: trasferimento di atomo di ossigeno nel cyt P-450 trasferimento elettronico in perossidasi e catalasi Le cavità in cui si dispone il substrato sono diverse: nel cytp450 RH è molto vicino al ferrile. Nella perossidasi alcuni aminoacidi bloccano di fatto l avvicinamento del substrato al ferrile, rendendo possibile solo il trasferimento dell elettrone. Come si effettua la rottura eterolitica del legame perossidico nei due sistemi enzimatici? Nella perossidasi la polarizzazione del legame è raggiunta grazie all azione degli aminoacidi. Nel citocromo P-450 tali aminoacidi non ci sono perché il complesso si trova in una tasca idrofobica. Probabilmente il legante assiale cisteina, per la sua natura basica, favorisce la rottura eterolitica.
24 SUPEROSSIDO DISMUTASI (SOD) Famiglia di metallo proteine che catalizza la disproporzione dello ione superossido attraverso un meccanismo che consiste di due passaggi consecutivi: 1) M n+ + O 2 - M (n-1)+ + O 2 2H + 2) M (n-1)+ + O 2 - M n+ (O 2 2- ) M n+ + H 2 O 2 Nello step 1) lo ione superossido riduce lo ione metallico ossidandosi ad ossigeno molecolare Nello step 2) lo ione superossido riossida lo ione metallico riducendosi a perossido La reazione complessiva è: 2O H + SOD O 2 + H 2 O 2
25 Cu-Zn (SOD) Chimica Inorganica Biologica Si trova nei mitocondri delle cellule eucariote consiste di due subunità identiche tenute insieme da interazioni idrofobiche il rame e lo zinco si trovano sul fondo di uno stretto canale fatto ad imbuto. Le dimensioni di questo canale consentono il passaggio solo a molecole molto piccole (H 2 O) e a piccoli ioni all imboccatura del canale sulla superficie esterna della proteina ci sono due aa lisina, che essendo carichi positivamente, attraggono lo ione superossido. lungo le pareti del canale vi è un aa arginina anch esso positivo che ha la funzione di convogliare l anione superossido verso il sito catalitico una modifica chimica delle lisine e della arginina comporta una forte diminuzione dell attività della SOD Struttura della forma ossidata della CuZn-SOD da eritrociti bovini
26 Cu-Zn (SOD) Chimica Inorganica Biologica Cu 2+ è coordinato a 4 imidazoli istidinici e a una molecola di H 2 O. La geometria è piramidale a base quadrata con acqua nella posizione apicale His118 H 2 O Cu His 46 His44 His 61 Zn His 69 His 78 Asp 81 Zn 2+ è coordinato a 3 imidazoli istidinici e al carbossilato di un aspartato A ponte tra i due centri metallici
27 Cu-Zn (SOD) Chimica Inorganica Biologica His118 H 2 O Cu His44 His 69 Zn Cu 2+ è il sito di interazione dello ione superossido. Quindi il Cu 2+ è il sito su cui avviene la disproporzione: His 46 Cu 2+ + O 2 - Cu + + O 2 His 61 His 78 Asp 81 Rimozione dello Zn 2+ non altera l attività della SOD ma rende più instabile la proteina che si denatura a temperatura più bassa della SOD nativa Cu + + O 2 - Cu 2+ (O 2 2- ) Cu 2+ + H 2 O 2 Attività della SOD è inibita in presenza di specie anioniche piccole come CN -, F -, N 3 - che competono con lo ione superossido nel sito catalitico. Zn 2+ ha ruolo strutturale
Chimica Inorganica Biologica Stabilità e ph
 Stabilità e ph Quando un gruppo OH o NH è coordinato ad un metallo la sua tendenza ad acquistare o perdere un protone è modificata: Coordinazione Amminoacidi Capacità coordinante di residui amminoacidici
Stabilità e ph Quando un gruppo OH o NH è coordinato ad un metallo la sua tendenza ad acquistare o perdere un protone è modificata: Coordinazione Amminoacidi Capacità coordinante di residui amminoacidici
I Mitocondri Centrale elettrica cellulare
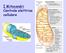 I Mitocondri Centrale elettrica cellulare Potenziale redox standard Fe 2+ D Fe 3+ + e - Fe 2+ + Cu 2+ D Fe 3+ + Cu + Cu 2+ + e - D Cu + Ε = E + RT nf ln [accettore elettroni] [donatore elettroni] n = n
I Mitocondri Centrale elettrica cellulare Potenziale redox standard Fe 2+ D Fe 3+ + e - Fe 2+ + Cu 2+ D Fe 3+ + Cu + Cu 2+ + e - D Cu + Ε = E + RT nf ln [accettore elettroni] [donatore elettroni] n = n
: : H-Cl + H-N: H-N-H + : Cl : H
 Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
L OSSIGENO COME SUBSTRATO DI ALTRE REAZIONI METABOLICHE
 L OSSIGENO COME SUBSTRATO DI ALTRE REAZIONI METABOLICHE Nella maggior parte delle cellule più del 90% dell ossigeno molecolare viene utilizzato per la fosforilazione ossidativa Il rimanente viene utilizzato
L OSSIGENO COME SUBSTRATO DI ALTRE REAZIONI METABOLICHE Nella maggior parte delle cellule più del 90% dell ossigeno molecolare viene utilizzato per la fosforilazione ossidativa Il rimanente viene utilizzato
Equilibrio Redox PARADOSSO DELL OSSIGENO: indispensabile per vita aerobia genera specie reattive dell ossigeno (ROS)
 Equilibrio Redox PARADOSSO DELL OSSIGENO: indispensabile per vita aerobia genera specie reattive dell ossigeno (ROS) Altera tutte le molecole biologiche (DNA, RNA, proteine, lipidi.) 1 Radicali endogeni
Equilibrio Redox PARADOSSO DELL OSSIGENO: indispensabile per vita aerobia genera specie reattive dell ossigeno (ROS) Altera tutte le molecole biologiche (DNA, RNA, proteine, lipidi.) 1 Radicali endogeni
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO)
 CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - -Ossidazione acidi grassi - Vie ossidative aa -Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte queste
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - -Ossidazione acidi grassi - Vie ossidative aa -Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte queste
C6H12O6 + 6O2 6CO2 + 6H2O + 36/38 molecole di ATP
 respirazione cellulare Reazioni di ossidazione progressiva dei substrati di natura organica ( tra cui il glucosio rappresenta il principale combustibile ) per produrre ATP che fornirà l energia per le
respirazione cellulare Reazioni di ossidazione progressiva dei substrati di natura organica ( tra cui il glucosio rappresenta il principale combustibile ) per produrre ATP che fornirà l energia per le
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Università degli Studi di Napoli Federico II
 Università degli Studi di Napoli Federico II FACOLTÀ DI SCIENZE MATEMATICHE, FISICHE E NATURALI CORSO DI LAUREA IN BIOLOGIA DELLE PRODUZIONI MARINE TESI SPERIMENTALE IN CITOLOGIA E ISTOLOGIA Stress ossidativo
Università degli Studi di Napoli Federico II FACOLTÀ DI SCIENZE MATEMATICHE, FISICHE E NATURALI CORSO DI LAUREA IN BIOLOGIA DELLE PRODUZIONI MARINE TESI SPERIMENTALE IN CITOLOGIA E ISTOLOGIA Stress ossidativo
Fosforilazione ossidativa
 Fosforilazione ossidativa FOSFORILAZIONE OSSIDATIVA La fosforilazione ossidativa è la via finale del metabolismo energetico, in cui gli elettroni (NADH e FADH 2 ) provenienti dalle molecole energetiche
Fosforilazione ossidativa FOSFORILAZIONE OSSIDATIVA La fosforilazione ossidativa è la via finale del metabolismo energetico, in cui gli elettroni (NADH e FADH 2 ) provenienti dalle molecole energetiche
Il laboratorio di Biochimica si svolgerà nei seguenti giorni;
 Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
 www.fisiokinesiterapia.biz I RADICALI LIBERI sono atomi o molecole che possiedono un elettrone spaiato nell orbita più esterna. SONO INSTABILI SONO MOLTO REATTIVI TENDONO AD AVVIARE REAZIONI A CATENA Come
www.fisiokinesiterapia.biz I RADICALI LIBERI sono atomi o molecole che possiedono un elettrone spaiato nell orbita più esterna. SONO INSTABILI SONO MOLTO REATTIVI TENDONO AD AVVIARE REAZIONI A CATENA Come
Chimica Inorganica Biologica Emeritrina
 Emeritrina La presenza biologica delle emeritrine è molto rara ed è ristretta a quattro phyla di invertebrati: Policheti, Sipunculidi, Priapulidi e Brachiopodi. Proteina binucleare di ferro meglio caratterizzata
Emeritrina La presenza biologica delle emeritrine è molto rara ed è ristretta a quattro phyla di invertebrati: Policheti, Sipunculidi, Priapulidi e Brachiopodi. Proteina binucleare di ferro meglio caratterizzata
La degradazione ossidativa di zuccheri, ac. grassi, e amminoacidi. livello del substrato) Equivalenti riducenti di NADH e FADH 2
 La degradazione ossidativa di zuccheri, ac. grassi, e amminoacidi produce energia: ATP (fosforilazioni a livello del substrato) Equivalenti riducenti di NADH e FADH 2 Dalla loro ri-ossidazione si può ottenere
La degradazione ossidativa di zuccheri, ac. grassi, e amminoacidi produce energia: ATP (fosforilazioni a livello del substrato) Equivalenti riducenti di NADH e FADH 2 Dalla loro ri-ossidazione si può ottenere
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
CATALISI COVALENTE. H 2 O Enz-R-OH + P. Enz-R-O S Enz-R-O-S
 CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
Programma del Corso di Chimica Generale II (6CFU) Corso di Laurea Specialistica in Farmacia
 Programma del Corso di Chimica Generale II (6CFU) Corso di Laurea Specialistica in Farmacia Prof. F. Punzo Obiettivo del corso: Trattare gli aspetti fondamentali della Chimica Generale ed Inorganica con
Programma del Corso di Chimica Generale II (6CFU) Corso di Laurea Specialistica in Farmacia Prof. F. Punzo Obiettivo del corso: Trattare gli aspetti fondamentali della Chimica Generale ed Inorganica con
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Gli enzimi. Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici
 Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
ADP + HPO 3, NAD +, NADP +, FAD ATP, NADH, NADPH, FADH 2 ENERGIA CHIMICA
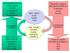 MACROMOLECOLE CELLULARI Proteine Polisaccaridi Lipidi Acidi nucleici ADP + HPO 3 2-, NAD +, NADP +, FAD Metaboliti complessi RICCHI DI ENERGIA Carboidrati Lipidi Proteine ANABOLISMO (biosintesi) MOLECOLE
MACROMOLECOLE CELLULARI Proteine Polisaccaridi Lipidi Acidi nucleici ADP + HPO 3 2-, NAD +, NADP +, FAD Metaboliti complessi RICCHI DI ENERGIA Carboidrati Lipidi Proteine ANABOLISMO (biosintesi) MOLECOLE
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Equilibrio Redox PARADOSSO DELL OSSIGENO: indispensabile per vita aerobia genera specie reattive dell ossigeno (ROS)
 Equilibrio Redox PARADOSSO DELL OSSIGENO: indispensabile per vita aerobia genera specie reattive dell ossigeno (ROS) Altera tutte le molecole biologiche (DNA, RNA, proteine, lipidi.) 1 Radicali endogeni
Equilibrio Redox PARADOSSO DELL OSSIGENO: indispensabile per vita aerobia genera specie reattive dell ossigeno (ROS) Altera tutte le molecole biologiche (DNA, RNA, proteine, lipidi.) 1 Radicali endogeni
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Mioglobina Emoglobina
 Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
AMINOACIDI Struttura. Funzione. Classificazione. Proprietà
 AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
CH 3 + CH 3 CH 3 - CH 3. 2 Radicali METILE ETANO
 Nella terminologia chimica vengono denominati radicali liberi atomi o molecole che presentino uno o più elettroni spaiati nell ambito dell orbitale più esterno. In base alla disposizione degli elettroni
Nella terminologia chimica vengono denominati radicali liberi atomi o molecole che presentino uno o più elettroni spaiati nell ambito dell orbitale più esterno. In base alla disposizione degli elettroni
Cr Mn Fe Co Ni Cu Zn. Chimica Inorganica Biologica Vita ed Energia
 Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
IL GRUPPO EME. PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici.
 IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
Malattie a carattere. Familiare (causa genetica, più casi nella stessa famiglia)
 I meccanismi biochimici che sottintendono alle malattie neurodegenerative sono (sorprendentemente) pochi, inter-connessi e (sorprendentemente) comuni alle diverse malattie Malattie a carattere Familiare
I meccanismi biochimici che sottintendono alle malattie neurodegenerative sono (sorprendentemente) pochi, inter-connessi e (sorprendentemente) comuni alle diverse malattie Malattie a carattere Familiare
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa
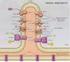 Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
I RADICALI NEI SISTEMI BIOLOGICI
 I RADICALI NEI SISTEMI BIOLOGICI L OSSIGENO E I SUOI DERIVATI Nei sistemi biologici, uno dei principali intermedi per la formazione di radicali liberi è l ossigeno. L ossigeno pur essendo assolutamente
I RADICALI NEI SISTEMI BIOLOGICI L OSSIGENO E I SUOI DERIVATI Nei sistemi biologici, uno dei principali intermedi per la formazione di radicali liberi è l ossigeno. L ossigeno pur essendo assolutamente
Complessi con gruppi M-O 2
 Complessi con gruppi M-O 2 complessi in cui sono presenti formalmente, come leganti, le specie ridotte dell ossigeno molecolare O 2 (12e - ), ossia: O 2 - (13e - ) legante ione superossido ; O 2 2- (14e
Complessi con gruppi M-O 2 complessi in cui sono presenti formalmente, come leganti, le specie ridotte dell ossigeno molecolare O 2 (12e - ), ossia: O 2 - (13e - ) legante ione superossido ; O 2 2- (14e
FOSFORILAZIONE OSSIDATIVA
 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
CO 2 + H 2 O H 2 CO 3 HCO 3 + H +
 26 Trasporto ed immagazzinamento di O 2 : Emoglobina e Mioglobina L utilizzo controllato di O 2 da parte di un organismo richiede innanzitutto il suo uptake reversibile dall atmosfera e il suo trasporto
26 Trasporto ed immagazzinamento di O 2 : Emoglobina e Mioglobina L utilizzo controllato di O 2 da parte di un organismo richiede innanzitutto il suo uptake reversibile dall atmosfera e il suo trasporto
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
Verso l esame: allenarsi con le prove esperte La chimica della carta
 Verso l esame: allenarsi con le prove esperte La chimica della carta Quesito 1 RISPOSTE ATTESE DOMANDA 1!Di che tipo sono i legami cerchiati? a. Legami a idrogeno. b. Legami ionici. c. Legami 1-4-ß-glucosidici.
Verso l esame: allenarsi con le prove esperte La chimica della carta Quesito 1 RISPOSTE ATTESE DOMANDA 1!Di che tipo sono i legami cerchiati? a. Legami a idrogeno. b. Legami ionici. c. Legami 1-4-ß-glucosidici.
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Tipi di trasportatori di elettroni nella catena respiratoria
 Tipi di trasportatori di elettroni nella catena respiratoria 1. Flavoproteine 2. Proteine Ferro Zolfo 3. Citocromi 4. Citocromi contenenti Rame 5. Chinone: Coenzima Q All eccezione del coenzima Q, tutti
Tipi di trasportatori di elettroni nella catena respiratoria 1. Flavoproteine 2. Proteine Ferro Zolfo 3. Citocromi 4. Citocromi contenenti Rame 5. Chinone: Coenzima Q All eccezione del coenzima Q, tutti
Metabolismo batterico
 Metabolismo batterico La somma di tutte le reazioni chimiche che avvengono nella cellula.questa è resa possibile dal flusso dell energia e dalla partecipazione di enzimi. Funzione principale della cellula
Metabolismo batterico La somma di tutte le reazioni chimiche che avvengono nella cellula.questa è resa possibile dal flusso dell energia e dalla partecipazione di enzimi. Funzione principale della cellula
Coenzimi. Ioni essenziali. Molti coenzimi hanno come precursori le vitamine.
 COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
FADH ADP + Pi ATP...29 AG ' = -30,5 kj/mol...29 Resa di ATP per l ossidazione completa del glucosio...31
 FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
Reazione di Maillard
 Reazione di Maillard 1 a fase: reazione di condensazione Base di Schiff (instabile) aldosilamina o chetosilamina Scala di reattività: pentosi>esosi (aldosi)>esosi (chetosi) funzione aminica lontana dal
Reazione di Maillard 1 a fase: reazione di condensazione Base di Schiff (instabile) aldosilamina o chetosilamina Scala di reattività: pentosi>esosi (aldosi)>esosi (chetosi) funzione aminica lontana dal
FOSFORILAZIONE OSSIDATIVA
 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
Biologia. La cellula al lavoro
 Biologia La cellula al lavoro Capitolo 5 La cellula al lavoro 1. Il metabolismo cellulare: come le cellule ricavano energia 2. La glicolisi è la prima fase della demolizione del glucosio 3. La respirazione
Biologia La cellula al lavoro Capitolo 5 La cellula al lavoro 1. Il metabolismo cellulare: come le cellule ricavano energia 2. La glicolisi è la prima fase della demolizione del glucosio 3. La respirazione
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
L energia negli esseri viventi: fotosintesi e respirazione viste dal punto di vista chimico
 Dipartimento di Scienze Chimiche e Geologiche L energia negli esseri viventi: fotosintesi e respirazione viste dal punto di vista chimico Gianantonio Battistuzzi La fotosintesi e la respirazione aerobica
Dipartimento di Scienze Chimiche e Geologiche L energia negli esseri viventi: fotosintesi e respirazione viste dal punto di vista chimico Gianantonio Battistuzzi La fotosintesi e la respirazione aerobica
Membri dell universo microbico
 Membri dell universo microbico Cellule procariote: mancanza di un nucleo ben delimitato all interno della cellula Cellule eucariote: presenza di un compartimento nucleare ben definito, maggiore complessità
Membri dell universo microbico Cellule procariote: mancanza di un nucleo ben delimitato all interno della cellula Cellule eucariote: presenza di un compartimento nucleare ben definito, maggiore complessità
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA
 I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
trasferimento degli elettroni dal donatore di elettroni di una
 Una reazione di ossidoriduzione può essere realizzata per via chimica o per via elettrochimica Gli ioni Cu + si ossidano a Cu 2+ mentre gli ioni Fe 3+ si riducono a Fe 2+. Nel primo caso la reazione di
Una reazione di ossidoriduzione può essere realizzata per via chimica o per via elettrochimica Gli ioni Cu + si ossidano a Cu 2+ mentre gli ioni Fe 3+ si riducono a Fe 2+. Nel primo caso la reazione di
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP. Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico
 Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
NADH FADH 2 (trasportatori ridotti di elettroni) Catena respiratoria (trasferimento degli
 NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
Metabolismo fermentativo
 Metabolismo fermentativo Anaerobio (non richiede ossigeno) Energeticamente poco efficiente (se confrontata alla respirazione) La catena di trasferimento degli elettroni è molto limitata: donatori ed accettori
Metabolismo fermentativo Anaerobio (non richiede ossigeno) Energeticamente poco efficiente (se confrontata alla respirazione) La catena di trasferimento degli elettroni è molto limitata: donatori ed accettori
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
L ossidazione è un processo estremamente importante per il metabolismo dell animale.
 STRESS OSSIDATIVO I LIPIDI, COSÌ COME DEL RESTO ALTRE MACROMOLECOLE QUALI PROTEINE, CARBOIDRATI E ACIDI NUCLEICI, POSSONO ANDARE INCONTRO A REAZIONI DI OSSIDAZIONE L ossidazione è un processo estremamente
STRESS OSSIDATIVO I LIPIDI, COSÌ COME DEL RESTO ALTRE MACROMOLECOLE QUALI PROTEINE, CARBOIDRATI E ACIDI NUCLEICI, POSSONO ANDARE INCONTRO A REAZIONI DI OSSIDAZIONE L ossidazione è un processo estremamente
IL METABOLISMO Somma delle reazioni che convertono sostanze nutrienti in fonti di ENERGIA o PRODOTTI COMPLESSI.
 IL METABOLISMO Somma delle reazioni che convertono sostanze nutrienti in fonti di ENERGIA o PRODOTTI COMPLESSI. reazioni enzimatiche organizzate in vie discrete H recettore procedono attraverso diversi
IL METABOLISMO Somma delle reazioni che convertono sostanze nutrienti in fonti di ENERGIA o PRODOTTI COMPLESSI. reazioni enzimatiche organizzate in vie discrete H recettore procedono attraverso diversi
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
ossidanti, come le specie reattive dell ossigeno (ROS), o più comunemente radicali liberi, e
 INTRODUZIONE Stress ossidativo Numerosi processi fisiologici e patologici possono aumentare la produzione di sostanze ossidanti, come le specie reattive dell ossigeno (ROS), o più comunemente radicali
INTRODUZIONE Stress ossidativo Numerosi processi fisiologici e patologici possono aumentare la produzione di sostanze ossidanti, come le specie reattive dell ossigeno (ROS), o più comunemente radicali
Aerobiosi C A T A B O L I S M O. Lez 4A. Schema generale del metabolismo dei glucidi
 Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
Xenobiotico. Lipofilo. BIOTRASFORMAZIONI DI FASE I: Ossidazione Riduzione Idrolisi Polare BIOTRASFORMAZIONI DI FASE II: Coniugazioni
 Xenobiotico Molto lipofilo ACCUMULO NEI GRASSI Lipofilo Polare Idrofilo BIOTRASFORMAZIONI DI FASE I: Ossidazione Riduzione Idrolisi Polare BIOTRASFORMAZIONI DI FASE II: Coniugazioni Idrofilo MOBILIZZAZIONE
Xenobiotico Molto lipofilo ACCUMULO NEI GRASSI Lipofilo Polare Idrofilo BIOTRASFORMAZIONI DI FASE I: Ossidazione Riduzione Idrolisi Polare BIOTRASFORMAZIONI DI FASE II: Coniugazioni Idrofilo MOBILIZZAZIONE
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
2) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici.
 LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
Metabolismo degli xenobiotici
 Prof. Giorgio Sartor degli xenobiotici Copyright 00100 by Giorgio Sartor. All rights reserved. Versione 3. oct 00 degli xenobiotici Scopo Convertire sostanze lipofile in idrofile Facilitare l escrezione
Prof. Giorgio Sartor degli xenobiotici Copyright 00100 by Giorgio Sartor. All rights reserved. Versione 3. oct 00 degli xenobiotici Scopo Convertire sostanze lipofile in idrofile Facilitare l escrezione
Esercitazione Esempi di domande del test intermedio
 Esercitazione Esempi di domande del test intermedio Materiale occorrente : Calcolatrice Penna Matita Righello Gomma Severamente vietato servirsi di libri, appunti, telefoni cellulari Quindi..!!!!! la legge
Esercitazione Esempi di domande del test intermedio Materiale occorrente : Calcolatrice Penna Matita Righello Gomma Severamente vietato servirsi di libri, appunti, telefoni cellulari Quindi..!!!!! la legge
CHEMISTRY DAY Istituto Superiore E.FERMI 12 Dicembre 2011
 CHEMISTRY DAY Istituto Superiore E.FERMI 12 Dicembre 2011 RUOLO BIOLOGICO dei METALLI di TRANSIZIONE Gianantonio Battistuzzi Università di Modena e Reggio Emilia Supradyn 1 compressa effervescente Multicentrum
CHEMISTRY DAY Istituto Superiore E.FERMI 12 Dicembre 2011 RUOLO BIOLOGICO dei METALLI di TRANSIZIONE Gianantonio Battistuzzi Università di Modena e Reggio Emilia Supradyn 1 compressa effervescente Multicentrum
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
LA VIA DEI PENTOSO FOSFATI
 LA VIA DEI PENTOSO FOSFATI Processo metabolico citosolico Sfrutta il glucosio per produrre ribosio 5-fosfato e equivalenti riducenti in forma di NADPH è la via con cui i pentosi introdotti con la dieta
LA VIA DEI PENTOSO FOSFATI Processo metabolico citosolico Sfrutta il glucosio per produrre ribosio 5-fosfato e equivalenti riducenti in forma di NADPH è la via con cui i pentosi introdotti con la dieta
Liceo Classico Pitagora Programma Biologia e Chimica 2016/2017 II F
 Liceo Classico Pitagora Programma Biologia e Chimica 2016/2017 II F 1)Struttura e funzioni della cellula -le caratteristiche degli esseri viventi -la teoria cellulare -la struttura delle cellula -gerarchia
Liceo Classico Pitagora Programma Biologia e Chimica 2016/2017 II F 1)Struttura e funzioni della cellula -le caratteristiche degli esseri viventi -la teoria cellulare -la struttura delle cellula -gerarchia
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Appunti di Stechiometria per Chimica Numero d ossidazione
 Appunti di Stechiometria per Chimica Numero d ossidazione Si definisce numero d ossidazione la carica complessiva di un atomo (differenza tra protoni ed elettroni dell atomo), ottenuta assegnando, solo
Appunti di Stechiometria per Chimica Numero d ossidazione Si definisce numero d ossidazione la carica complessiva di un atomo (differenza tra protoni ed elettroni dell atomo), ottenuta assegnando, solo
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
RESPIRAZIONE CELLULARE (METABOLISMO DEL GLUCOSIO)
 RESPIRAZIONE CELLULARE (METABOLISMO DEL GLUCOSIO) LA GLICOLISI: dopo il ciclo di Calvin, che avviene nelle cellule autotrofe delle piante, il glucosio prodotto va a demolirsi per produrre energia nelle
RESPIRAZIONE CELLULARE (METABOLISMO DEL GLUCOSIO) LA GLICOLISI: dopo il ciclo di Calvin, che avviene nelle cellule autotrofe delle piante, il glucosio prodotto va a demolirsi per produrre energia nelle
Argomenti di tesi disponibili presso il Gruppo di Chimica Bioinorganica e Bioelettrochimica
 Argomenti di tesi disponibili presso il Gruppo di Chimica Bioinorganica e Bioelettrochimica Gruppo di Chimica Bioinorganica e Bioelettrochimica G. Battistuzzi M. Borsari L. Paltrinieri A. Ranieri C. A.
Argomenti di tesi disponibili presso il Gruppo di Chimica Bioinorganica e Bioelettrochimica Gruppo di Chimica Bioinorganica e Bioelettrochimica G. Battistuzzi M. Borsari L. Paltrinieri A. Ranieri C. A.
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Gerard Tortora, Brian Derrickson. Conosciamo
 1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine:
 La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
Aminoacidi. Struttura generale Sono 20 e formano le
 Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
ANTIOSSIDANTI Grassi IV LEZIONE
 ANTIOSSIDANTI Grassi IV LEZIONE ANTIOSSIDANTE Sostanza che, pur presente in concentrazione ridotta rispetto al substrato ossidabile, può prevenire o ritardare l ossidazione iniziata da un fattore proossidante.
ANTIOSSIDANTI Grassi IV LEZIONE ANTIOSSIDANTE Sostanza che, pur presente in concentrazione ridotta rispetto al substrato ossidabile, può prevenire o ritardare l ossidazione iniziata da un fattore proossidante.
1. L importanza delle reazioni di ossido-riduzione 2. Il numero di ossidazione 3. Ossidazione e riduzione: cosa sono e come si riconoscono 4.
 Unità 20 Le reazioni di ossido-riduzione 1. L importanza delle reazioni di ossido-riduzione 2. Il numero di ossidazione 3. Ossidazione e riduzione: cosa sono e come si riconoscono 4. Reazioni redox molto
Unità 20 Le reazioni di ossido-riduzione 1. L importanza delle reazioni di ossido-riduzione 2. Il numero di ossidazione 3. Ossidazione e riduzione: cosa sono e come si riconoscono 4. Reazioni redox molto
 http://digilander.libero.it/glampis64 I composti organici di interesse biologico sono: Carboidrati Proteine Lipidi Acidi nucleici Le macromolecole sono composti di grandi dimensioni, unione di piccole
http://digilander.libero.it/glampis64 I composti organici di interesse biologico sono: Carboidrati Proteine Lipidi Acidi nucleici Le macromolecole sono composti di grandi dimensioni, unione di piccole
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a:
 I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
Respirazione cellullare
 Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
Fotosintesi: processo di traduzione dell energia luminosa in energia chimica. Pianta + Luce
 Fotosintesi: processo di traduzione dell energia luminosa in energia chimica Pianta + Luce CO + + H O (CH O) O 2 2 2 2 La fotosintesi non è un processo peculiare delle piante Luce, solfobatteri anaerobi
Fotosintesi: processo di traduzione dell energia luminosa in energia chimica Pianta + Luce CO + + H O (CH O) O 2 2 2 2 La fotosintesi non è un processo peculiare delle piante Luce, solfobatteri anaerobi
- natura riduttiva - richiede energia
 - natura ossidativa - produce energia - natura riduttiva - richiede energia 1 L O 2 è poco solubile in acqua (10 ml/l a 20 C): se esso fosse semplicemente disciolto, potrebbe diffondere efficacemente solo
- natura ossidativa - produce energia - natura riduttiva - richiede energia 1 L O 2 è poco solubile in acqua (10 ml/l a 20 C): se esso fosse semplicemente disciolto, potrebbe diffondere efficacemente solo
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
