Assorbimento. Ci sono altri fenomeni che possono accadere dopo l assorbimento di un fotone
|
|
|
- Aureliano Berardi
- 6 anni fa
- Visualizzazioni
Transcript
1 Fluorescenza
2 Assorbimento Rilassamento al più basso livello vibrazionale del primo stato eccitato (S1) (conversione interna o rilassamento vibrazionale) (picosecondo) La molecola rimane nello stato eccitato di singoletto (S1) in un periodo dell ordine dei nanosecondi (il più lungo periodo di tempo nei meccanismi di fluorescenza) per poi passare allo stato fondamentale emettendo un fotone (fluorescenza) Ci sono altri fenomeni che possono accadere dopo l assorbimento di un fotone
3 Stato di singoletto e stato di tripletto Stato di singoletto : Tutti gli spin elettronici nella molecola sono accoppiati Stato di tripletto: Un set di spin elettronico è disaccopiato
4 Fenomeni dopo l assorbimento di un fotone L energia dello stato eccitato può essere dissipata non radiativamente sottoforma di calore Il fluoroforo eccitato può collidere con un altra molecola per trasferire energia in un secondo tipo di processo non radiativo (quenching) L energia dello stato eccitato può essere dissipata non radiativamente se lo stato eccitato decade nel più basso stato di tripletto (intersystem crossing) Questo processo è piuttosto raro, poiché gli elettroni devono effettuare una conversione di spin per avere elettroni spaiati.
5
6 Range dei tempi per processi di fluorescenza Transition Processo Costante di rate S(0) => S(1) or S(n) S(n) => S(1) S(1) => S(1) Assorbimento (Eccitazione) Conversione interna Rilassamento vibrazionale Scala dei tempi (Secondi) Istantaneo k(ic) to k(vr) to S(1) => S(0) Fluorescenza k(f) or G 10-9 to 10-7 S(1) => T(1) S(1) => S(0) Intersystem Crossing Quenching Rilassamento non radiativo k(pt) to 10-8 k(nr), k(q) 10-7 to 10-5 T(1) => S(0) Fosforescenza k(p) 10-3 to 100 T(1) => S(0) Quenching Rilassamento non radiativo k(nr), k(qt) 10-3 to 100
7 Resa quantica di fluorescenza La resa quantica di fluorescenza è definita come il rapporto tra numero di fotoni emessi in fluorescenza (n g ) e numero di molecole eccitate nel campione (n e ), cioè numero di fotoni assorbiti. q n g n e k F k F k NR k F costantedi velocita k NR somma delle di decadiment o radiativo (emissione di luce di fluorescenza) costantidi velocità di tuttii decadiment i non radiativi
8 Tempo di vita di fluorescenza Il tempo medio di permanenza in S1 viene detto tempo di vita (t) e cioè: t q k F t t R 1 k NR se t R 1 k F tempodi vita radiativo Il tempo di vita radiativo dipende solo dalle funzioni d onda (probabilità) molecolari di S 0 e S 1 e può essere stimato dagli spettri di assorbimento e fluorescenza.
9 Quenching Il fluoroforo eccitato può collidere con un altra molecola per trasferire energia in un secondo tipo di processo non radiativo (quenching) M * M h M * Q M Q kt g fluorescenza quenching Le rese quantiche di fluorescenza sono: k k q F q F 0 k k k k k [ Q] F NR F NR Q [Q] concentrazione dei quencher
10 t t t ] [ 1 ] [ ] [ 0 Q k Q Q NR F Q NR F NR F NR k F k Q k k k q q Q k k k F k q k k F k q Equazione di Stern-Volmer t 0 t 0 q q vitadim *in presenzadiq tempo di vitadim *in assenzadiq tempodi 0 t t
11 Trasferimenti di energia tra stati eccitati Il tipo più semplice di trasferimento energetico è il trasferimento radiativo: I fotoni emessi dalla molecola donore sono riassorbiti dalla molecola accettore. Non c è nessuna interazione diretta tra la molecola donore ed accettore. L assorbimento da parte delle molecole accettrici dipende dalla concentrazione delle stesse ed è inversamente proporzionale alla distanza tra donore ed accettore.
12 Trasferimenti di energia tra stati eccitati Un altro tipo di trasferimento energetico avviene attraverso l accoppiamento elettronico delle molecole In questo caso la transizione non è radiativa ma avviene per deattivazione dello stato energetico eccitato e implica un riduzione della vita media della fluorescenza. Anche in questo caso il grado di eccitazione dipende dalla distanza tra le molecole ma anche dalla sovrapposizione spettrale e dalla orientazione dei dipoli di transizione del donore e dell accettore.
13 Trasferimenti di energia tra stati eccitati A seconda della distanza e della intensità di accoppiamento tra le molecole possiamo distinguere due tipi di meccanismi per il trasferimento tramite accoppiamento elettronico: 1. Trasferimento energetico per risonanza di Förster (FRET) per deboli accoppiamenti 2. Trasferimento energetico di Dexter per accoppiamenti forti e moderati Il FRET è il risultato di interazioni dipolo:dipolo (interazioni coulombiane) Nel Dexter invece si ha uno scambio elettronico vero e proprio e quindi la distanza tra accettore e donore deve essere all intorno in cui le forze di Van der Waals sono valide (5 Angstroem)
14 1 1 Chl 1 Car * Chl 1 1 Chl Chl 1 1 Car Chl * 1 Chl * Singoletto Singoletto (Förster) 3 Chl 1 * Car 1 Chl 3 Car * Tripletto Tripletto (Dexter)
15 Le quattro regole della Fluorescenza 1. Principio di Franck-Condon: i nuclei sono stazionari durante le transizioni elettroniche, quindi le eccitazioni sono relative a livelli vibrazionali eccitati dello stato elettronico eccitato 2. L emissione si ha dal livello più basso dello stato vibrazionale dello stato di singoletto eccitato più basso perché il rilassamento dai livelli vibrazionali eccitati è molto più veloce dell emissione. 3. Shift di Stokes : l emissione ha sempre un energia più bassa dell assorbimento a causa del rilassamento nucleare nello stato eccitato 4. Regola dell immagine riflessa: gli spettri di emissione sono immagini riflesse della banda di assorbimento più bassa.
16 Le transizioni di eccitazione (linee rosse) dallo stato fondamentale allo stato eccitato sono talmente veloci (femtosecondi) che la distanza internucleare associata agli orbitali di legame non ha abbastanza tempo per cambiare, quindi le transizioni sono rappresentate da linee verticali.
17 Le transizioni più favorevoli sono quelle in cui le probabilità delle energie rotazionali e vibrazionali dello stato fondamentale e dello stato eccitato si sovrappongono massimamente. In ogni caso si verificano altri tipi di transizioni che quindi rendono lo spettro continuo
18 Regola dell immagine riflessa
19 Spettroscopia di Fluorescenza Statica: spettro di eccitazione, spettro di emissione, resa quantica, polarizzazione Dinamica: tempi di vita degli stati eccitati, tempi di correlazione rotazionale (decadimento temporale dell anisotropia)
20 Spettro di emissione Variazione della intensità di fluorescenza letta ad una l em in funzione della l ecc Per molecole isolate in soluzione ed a bassa concentrazione lo spettro di eccitazione è indipendente dalla lunghezza d onda emessa ed è molto simile allo spettro di assorbimento (rapido rilassamento vibrazionale e conversione interna) Per molecole in cui subentrano altri meccanismi come quenching, trasferimento di energia, reazioni fotochimiche lo spettro è invece dipendente da l em. ed è molto diverso dallo spettro di assorbimento.
21 Batocromismo Spostamento verso il rosso dello spettro di fluorescenza in ambienti polari (con lieve diminuzione della resa quantica) Sonde fluorescenti sono state studiate appositamente per caratterizzare la polarita dei loro siti. Per esempio: L 8-anilino 1-naftalene sulfonato (ANS) presenta una fluorescenza attorno ai 450nm nell eme della apomioglobina e ha una fluorescenza attorno ai 515 nm in acqua.
22 Effetto del solvente Differenze nelle energie tra lo stato fondamentale e lo stato eccitato nel fluoroforo danno luogo a momenti di dipolo che riorientano le molecole del solvente stesso attorno al fluoroforo. Il decadimento vibrazionale avviene nel fluoroforo molto piu velocemente che nel solvente (dove si deve riorientare il dipolo)
23 Proteina azzurrina (contiene un solo triptofano) ANS in eme dell apomioglobina
24 Photobleaching A differenza del quenching, il photo bleaching accade quando un fluoroforo perde permanentemente la capacità di fluorescere a causa di danneggiamenti chimici indotti dai fotoni e modificazioni di legami covalenti. Da una transizione di un singoletto eccitato ad un tripletto eccitato, essendo quest ultimo uno stato con una vita media alta, la molecola rimane in uno stato di maggiore energia per un tempo sufficiente a reagire con l ambiente. Chiaramente il photobleaching è dipendente dalla struttura molecolare e dall ambiente locale.
25
26 Spettroscopia risolta in tempo I parametri che si misurano nella spettroscopia di fluorescenza statica (intensità, spettri, polarizzazione) rappresentano la media delle caratteristiche di emissione di tutti i tipi di fluorofori presenti nel campione. Se quindi diversi fluorofori hanno degli spettri che si sovrappongono anche parzialmente si vede una media del segnale e vengono perse delle informazioni importanti su transizioni energetiche. Se però le transizioni vengono risolte nel tempo e cioè si differenziano le varie transizioni a tempi diversi si riescono a risolvere i diversi spettri.
27 Tempo di vita di fluorescenza Il tempo di vita di fluorescenza corrisponde al tempo in cui la molecola rimane nello stato eccitato prima che ritorni allo stato fondamentale. Per un decadimento del primo ordine il numero di molecole che perdono un quanto di energia nel tempo dt è proporzionale al numero di molecole N nello stato eccitato, cioé : dn( t) N( t) k dt k costantedi proporzionalità integrando : ln N( t) ln N(0) ln N( t) N N(0) N(0) e kt dn(t) N(t) t 0 N( t) N(0) kdt kt
28 Tempo di vita di fluorescenza Il decadimento della intensità di fluorescenza in funzione del tempo in una popolazione uniforme di molecole eccitate con un impulso laser è descritto da una funzione esponenziale: I( t) I 0 e t t Da questa equazione si può dire che t è il tempo in cui l intensità di fluorescenza decade a 1/e della fluorescenza iniziale e cioè a circa il 37%
29
30 Anisotropia di fluorescenza L emissione di fluorescenza è polarizzata se i fluorofori sono eccitati con luce polarizzata piana. Il livello di emissione polarizzata è dipendente dalla anisotropia del campione, campioni con un certo grado di anisotropia hanno anche un certo livello di emissione polarizzata. Infatti l interazione avviene tra il campo elettrico e la transizione di dipolo creato dallo stato elettronico dagli orbitali molecolari del fluoroforo. I fluorofori assorbono preferibilmente i fotoni che hanno un vettore del campo elettrico parallelo al momento di dipolo della transizione di assorbimento.
31 Anisotropia di fluorescenza La probabilità di assorbimento è proporzionale al quadrato del coseno dell angolo tra il dipolo ed il vettore del campo elettrico della radiazione incidente.
32 Anisotropia di fluorescenza Quindi c è una specifica fotoselezione della sotto-popolazione dei fluorofori eccitati, risultante negli stati eccitati dei fluorofori orientati verso uno specifico asse. La radiazione di fluorescenza da questa sottopopolazione sarà anch essa parzialmente polarizzata. A I I II II I 2I I(II) emissione di fluorescenzamisurata sul piano parallelo al piano di eccitazione I( ) emissione di fluorescenzamisurata sul piano perpendicolare al piano di eccitazione
33 Polarizzazione di fluorescenza L emissione è polarizzata se la rotazione molecolare è lenta relativamente al tempo di vita di fluorescenza
34 Strumentazione per la polarizzazione di fluorescenza
35 Cuvetta Sorgente Monocromatore di eccitazione Polarizzatore Polarizzatore Amplificatore Rivelatore Monocromatore di emissione Computer
36
37 Misure di polarizzazione Le misure di polarizzazione sono eseguite inserendo due polarizzatori uno nel percorso ottico di eccitazione ed uno in quello di emissione. Si misurano le intensità di fluorescenza con il polarizzatore di emissione orientato parallelamente I e perpendicolarmente al II I polarizzatore di eccitazione, e viene valutato il grado di polarizzazione, P.
38 Polarizzazione di un sistema rigido In una soluzione in cui le molecole siano orientate casualmente ma immobilizzate, il valore di P è detto polarizzazione intrinseca P0. Il valore corrispondente per r è l anisotropia intrinseca, r0. P I I II II I I Grado di polarizzazione r I I II II I 2I Anisotropia R
39 Polarizzazione di un sistema rigido In una soluzione in cui le molecole siano orientate casualmente ma immobilizzate, il valore di P è detto polarizzazione intrinseca P 0. Il valore corrispondente per r è l anisotropia intrinseca, r 0.
40 Campione con orientazione casuale In un campione con orientazione casuale, la dipendenza dell intensità assorbita da cos 2 q comporta l eccitazione di un rilevante numero di molecole che non hanno dipoli di transizione orientati esattamente secondo il piano di polarizzazione. Quando queste molecole non allineate emettono, avranno componenti di luce polarizzata sia parallela che perpendicolare. Se si considera la media su tutti i possibili valori di q, tenendo conto della dipendenza da q del numero di molecole in un campione disordinato, risulta che il massimo valore possibile per P 0 è 0.5.
41 Campione con orientazione casuale e ordinata Questo è quello che si osserva in una soluzione rigida, disordinata, in cui i momenti di dipolo di transizione per l assorbimento e l emissione del fluoroforo sono paralleli. Questa è la situazione normale quando l eccitazione porta al primo singoletto eccitato, da cui si ha anche l emissione. La polarizzazione intrinseca sarebbe 1 se il campione fosse ordinato e immobile, con tutti i momenti di assorbimento, e di emissione, paralleli alla direzione di polarizzazione della radiazione eccitatrice.
42 Il valore misurato del grado di polarizzazione (o dell anisotropia) dipende, oltre che dal grado di ordine del campione, e dalla sua maggiore o minore mobilità, dall orientazione del momento di dipolo di transizione per l emissione rispetto a quello di assorbimento
43 Campione con orientazione Quando i dipoli di assorbimento ed emissione non sono paralleli,p0 è minore di 0.5, anche in una soluzione rigida, e al limite opposto (dipoli perpendicolari), P0 = Precisamente, la dipendenza dall angolo è: P 0 2 3cos 1 2 cos 3 Analogamente, anche l anisotropia intrinseca varia da un max di r0 = 2/5 = 0.4 (dipoli di assorbimento e di emissione paralleli) ad un minimo di r0 = 1/5 = -0.2 (dipoli perpendicolari).
44 Anisotropia osservata per la fluorescenza del colorante rodamina al variare della lunghezza d onda di eccitazione. Si possono osservare 5 transizioni a 5 diversi stati di singoletto eccitato.
45 La transizione ad S1 (470 nm) comporta un anisotropia di circa +0.4, come atteso dal momento che dipoli di assorbimento (S0-> S1) e di emissione (S1->S0) sono paralleli. Le transizioni ad energia maggiore (S0->S5, 300 nm e S0-> S4, 350 nm) portano ad un anisotropia di 0.16, indicando che i dipoli di assorbimento e di emissione sono circa perpendicolari. Dai valori di anisotropia che si osservano per eccitazione agli altri 2 singoletti (S3, 390 nm e S2, 420 nm) si possono ricavare gli angoli tra i corrispondenti dipoli: ~ 47 (r0 ~+0.08) e ~ 66 (r0 ~ -0.1), rispettivamente.
46 Depolarizzazione della Fluorescenza L effetto della fotoselezione viene perso se, nel tempo tra l assorbimento e l emissione, le molecole ruotano (si tratta di rotazione caotica, tumbling ). Si avrà depolarizzazione (P ed r tendono a zero) tanto maggiore quanto più veloci sono i moti di tumbling molecolare rispetto al tempo di vita di fluorescenza.
47 Relazione di Perrin La relazione tra r e r0, in stato stazionario (illuminazione costante), (relazione di Perrin), nell ipotesi che il moto rotazionale delle molecole sia isotropo (le molecole abbiano una forma approssimativamente sferica) è 1 1 (1 0 r t f è il tempo di vita della fluorescenza t r, tempo di correlazione rotazionale r r è una misura del tempo impiegato dalle molecole, nel loro moto disordinato e impedito dalla presenza delle altre molecole e del solvente (moto Browniano, o diffusivo, rotazionale), a compiere mediamente una rotazione di 1 radiante t r t t f )
48 Andamento lineare dell inverso dell anisotropia di fluorescenza del gruppo antraniloil legato covalentemente a Ser195 della chimotripsina, a 20 C. La variazione del tempo di correlazione è stata ottenuta variando la viscosità della soluzione mediante aggiunte di glicerina. Il moto rotazionale si riferisce qui al moto di tutto il complesso,ed è relativamente lento proprio perché il fluoroforo è legato alla proteina. L eccitazione con luce linearmente polarizzata fornisce quindi un mezzo per studiare la dinamica della struttura proteica.
49
50
51
52 Protezione dalla fotodistruzione dei carotenoidi L energia assorbita dai carotenoidi è trasferita alla clorofilla via transizioni singoletto-singoletto La funzione più importante è comunque quella di protezione dalla fotodistruzione: L effetto è originato dalla generazione di stati di tripletto della clorofilla per intersystem crossing sulla clorofilla stessa.
53
54
55 Spettrofotometro di Joliot
56 LUCE necessaria al processo fotosintetico è capace di incrementare la produzione di specie tossiche Ossidazione di lipidi, proteine e pigmenti Le piante superiori hanno evoluto diversi meccanismi che garantiscono la dissipazione dell energia di eccitazione in eccesso: ruolo dei carotenoidi scavenging di 1 O2 * (xantofille) legati alle proteine Lhc quenching di 3 Chl *
57 Calore t 1/2 = 2 µs Luminescence t 1/2 = 2 µs Absorption (fs) Fluorescence (µs) Phosphorescence (µs) Formazione dei Tripletti dei Carotenoidi Quenching di T Chl* e Scavenging dell S O 2 * Numero d onda, cm S 1 Intersystem crossing T Chl* T car* S O 2 -* Lunghezza d onda, nm Tcar* decay Chl S 0 S 0 Car T O 2
58 Spettroscopia differenziale pulsata risolta in tempo Spettrofotometro di Joliot Laser Nd:YAG Minilite Sfera di integrazione Cella di colorante filtro 650 nm M filtri diff Convertitore A/D M-R R Laser Nd:YAG Surelite 355 nm OPO R Fibra ottica OPO : oscillatore parametrico ottico M : misura, R : riferimento, diff : amplificatore differenziale
59
60 Absorption (arb. counts) Cinetiche nm Time (ms)
61 Absorption (arb. counts) Spettro differenziale CP26 WT P.I oxygen A B C D E F G H I J K L M N O P Q R S T UV WX a YZAABACADAEAFAG AH AI AK AJ b c d e f g h i j k l m n o p q r s t u v w x y za abac ad ae af ag ah ai ak aj Wavelength (A ) 7.5 ns 20 ns 45 ns 70 ns 82.5 ns 95 ns 120 ns 145 ns 170 ns 195 ns 295 ns 395 ns 495 ns 995 ns µs 1.95 µs µs A µs a 9.95 µs 14,95 µs 19,95 µs 29,95 µs
5 - SPETTROSCOPIA UV - VISIBILE EMISSIONE
 5 - SPETTROSCOPIA UV - VISIBILE EMISSIONE La maggior parte delle molecole, nello stato elettronico fondamentale, si trova in uno stato di singoletto, S 0, (tutti gli elettroni con spin appaiati, 2 elettroni
5 - SPETTROSCOPIA UV - VISIBILE EMISSIONE La maggior parte delle molecole, nello stato elettronico fondamentale, si trova in uno stato di singoletto, S 0, (tutti gli elettroni con spin appaiati, 2 elettroni
SPETTROSCOPIA UV-VIS LEZIONE 9
 SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
Corso di Laboratorio di Biofotonica
 SAPIENZA Università di Roma Laurea magistrale in Ingegneria delle Nanotecnologie A.A. 2015-2016 Corso di Laboratorio di Biofotonica Prof. Francesco Michelotti SAPIENZA Università di Roma Facoltà di Ingegneria
SAPIENZA Università di Roma Laurea magistrale in Ingegneria delle Nanotecnologie A.A. 2015-2016 Corso di Laboratorio di Biofotonica Prof. Francesco Michelotti SAPIENZA Università di Roma Facoltà di Ingegneria
Prof. R. Velotta Dr. R. Esposito
 Prof. R. Velotta Dr. R. Esposito La fluorescenza La spettroscopia di fluorescenza è un potente strumento per lo studio delle strutture e delle dinamiche molecolari, in fisica, chimica e biologia. Sebbene
Prof. R. Velotta Dr. R. Esposito La fluorescenza La spettroscopia di fluorescenza è un potente strumento per lo studio delle strutture e delle dinamiche molecolari, in fisica, chimica e biologia. Sebbene
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
LA FLUORESCENZA DELLA CLOROFILLA
 SPERIMENTA ANCHE TU ed. 2010 LICEO SCIENTIFICO L. DA VINCI TREVISO LA FLUORESCENZA DELLA CLOROFILLA Docente coordinatore: Sonia Mazzaro Assistente tecnico: Ornella Lorenzon Alunni classe 4C: Alessandro
SPERIMENTA ANCHE TU ed. 2010 LICEO SCIENTIFICO L. DA VINCI TREVISO LA FLUORESCENZA DELLA CLOROFILLA Docente coordinatore: Sonia Mazzaro Assistente tecnico: Ornella Lorenzon Alunni classe 4C: Alessandro
Spettroscopia. 05/06/14 SPET.doc 0
 Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Esperimenti FT-NMR a impulsi
 Vettore magnetizzazione netta M 0 per un nucleo immerso in un campo magnetico B 0, per indurre la transizione l impulso RF è applicato lungo la direzione dell asse x. Il campo magnetico alternante applicato
Vettore magnetizzazione netta M 0 per un nucleo immerso in un campo magnetico B 0, per indurre la transizione l impulso RF è applicato lungo la direzione dell asse x. Il campo magnetico alternante applicato
Metodi spettroscopici
 Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
Processi radiativi. Assorbimento Emissione spontanea Emissione stimolata. Gli stati eccitati sono instabili (il sistema non è in equilibrio)
 Processi radiativi conservazion e dell energia transizioni I I Assorbimento Emissione spontanea Emissione stimolata Lo stato ad energia più bassa è detto fondamentale, gli altri sono detti stati eccitati
Processi radiativi conservazion e dell energia transizioni I I Assorbimento Emissione spontanea Emissione stimolata Lo stato ad energia più bassa è detto fondamentale, gli altri sono detti stati eccitati
Altro metodo di indagine che utilizza la spettroscopia. Spettrofluorimetria
 Altro metodo di indagine che utilizza la spettroscopia Spettrofluorimetria La luminescenza Luminescenza: emissione di luce da atomi, molecole o cristalli eccitati elettronicamente. Eccitazione luminosa:
Altro metodo di indagine che utilizza la spettroscopia Spettrofluorimetria La luminescenza Luminescenza: emissione di luce da atomi, molecole o cristalli eccitati elettronicamente. Eccitazione luminosa:
CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica
 Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Maurizio D Auria. Fotochimica applicata alla sintesi organica
 A03 09 Maurizio D Auria Fotochimica applicata alla sintesi organica Copyright MMIV ARACNE editrice S.r.l. www.aracne editrice.it info@aracne editrice.it via Raffaele Garofalo, 133 A/B 00173 Roma redazione:
A03 09 Maurizio D Auria Fotochimica applicata alla sintesi organica Copyright MMIV ARACNE editrice S.r.l. www.aracne editrice.it info@aracne editrice.it via Raffaele Garofalo, 133 A/B 00173 Roma redazione:
LA FOTOSINTESI: conversione di energia luminosa in energia chimica
 LA FOTOSINTESI: conversione di energia luminosa in energia chimica Fonte principale di carboidrati Via principale di fissazione del carbonio Fonte di ossigeno dell atmosfera La FOTOSINTESI consiste di
LA FOTOSINTESI: conversione di energia luminosa in energia chimica Fonte principale di carboidrati Via principale di fissazione del carbonio Fonte di ossigeno dell atmosfera La FOTOSINTESI consiste di
Light Amplification by Stimulated Emission of Radiation
 Laser? Light Amplification by Stimulated Emission of Radiation Produce un fascio coerente di radiazione ottica da una stimolazione elettronica, ionica, o transizione molecolare a più alti livelli energetici
Laser? Light Amplification by Stimulated Emission of Radiation Produce un fascio coerente di radiazione ottica da una stimolazione elettronica, ionica, o transizione molecolare a più alti livelli energetici
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Scintillatori. Stage Residenziale 2012
 Scintillatori Stage Residenziale 2012 Rivelatori a Scintillazione Passaggio di radiazione attraverso materiale scintillante eccitazione di atomi e molecole del materiale emissione di luce raccolta e trasmessa
Scintillatori Stage Residenziale 2012 Rivelatori a Scintillazione Passaggio di radiazione attraverso materiale scintillante eccitazione di atomi e molecole del materiale emissione di luce raccolta e trasmessa
Spettroscopie di luminescenza
 Spettroscopie di luminescenza La luminescenza è il fenomeno per cui una specie eccitata ad un livello elettronico ad energia più elevata emette radiazione per tornare allo stato fondamentale: X eccitazione
Spettroscopie di luminescenza La luminescenza è il fenomeno per cui una specie eccitata ad un livello elettronico ad energia più elevata emette radiazione per tornare allo stato fondamentale: X eccitazione
Metodi spettroscopici per le Biotecnologie
 AA 2013-2014 Metodi spettroscopici per le Biotecnologie Spettroscopia di emissione UV-VIS Dott. Alfonso Zoleo Spe$roscopia di Emissione Cosa succede ad una molecola portata in uno stato ele$ronico eccitato?
AA 2013-2014 Metodi spettroscopici per le Biotecnologie Spettroscopia di emissione UV-VIS Dott. Alfonso Zoleo Spe$roscopia di Emissione Cosa succede ad una molecola portata in uno stato ele$ronico eccitato?
Lezione n. 20. Visibile. La spettroscopia UV/Visibile. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 20 Principi generali delle spettroscopie ottiche La spettroscopia UV/Visibile Visibile Antonino Polimeno 1 Spettroscopie ottiche (1) - Le tecniche di misura
Chimica Fisica Biotecnologie sanitarie Lezione n. 20 Principi generali delle spettroscopie ottiche La spettroscopia UV/Visibile Visibile Antonino Polimeno 1 Spettroscopie ottiche (1) - Le tecniche di misura
fenomeno X nm Å UV - visibile legami chimici infrarosso
 Spettroscopia IR radiazione f (Hz) energia (ev) fenomeno λ / dim. tipica X 10 18 10 20 10 3 10 5 livelli interni atomici nm Å UV - visibile 10 14 10 16 0.1 10 legami chimici 300 800 nm infrarosso 10 11
Spettroscopia IR radiazione f (Hz) energia (ev) fenomeno λ / dim. tipica X 10 18 10 20 10 3 10 5 livelli interni atomici nm Å UV - visibile 10 14 10 16 0.1 10 legami chimici 300 800 nm infrarosso 10 11
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
Risonanza Magnetica Nucleare
 Risonanza Magnetica Nucleare Il fenomeno della risonanza magnetica nucleare è legato ad una proprietà p di alcuni nuclei quale lo spin. Lo spin è una proprietà fondamentale come la carica e la massa. Protoni,
Risonanza Magnetica Nucleare Il fenomeno della risonanza magnetica nucleare è legato ad una proprietà p di alcuni nuclei quale lo spin. Lo spin è una proprietà fondamentale come la carica e la massa. Protoni,
Risonanza Magnetica Nucleare NMR
 Risonanza Magnetica Nucleare NMR Numeri quantici di spin di alcuni nuclei Gli isotopi più abbondanti di C e O non hanno spin Element 1 H 2 H 12 C 13 C 14 N 16 O 17 O 19 F N.ro quantico di Spin 1/2 1 0
Risonanza Magnetica Nucleare NMR Numeri quantici di spin di alcuni nuclei Gli isotopi più abbondanti di C e O non hanno spin Element 1 H 2 H 12 C 13 C 14 N 16 O 17 O 19 F N.ro quantico di Spin 1/2 1 0
Risonanza magnetica nucleare
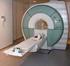 Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
Luce e Vita (Luce è Vita) LUCE: FONTE ENERGETICA E PORTATRICE DI INFORMAZIONI
 Luce e Vita (Luce è Vita) LUCE: FONTE ENERGETICA E PORTATRICE DI INFORMAZIONI Luce : Fonte di Energia Fotosintesi Sviluppo e mantenimento della vita sulla Terra 6CO 2 + 6H 2 O + 60 fotoni ----> C 6 H 12
Luce e Vita (Luce è Vita) LUCE: FONTE ENERGETICA E PORTATRICE DI INFORMAZIONI Luce : Fonte di Energia Fotosintesi Sviluppo e mantenimento della vita sulla Terra 6CO 2 + 6H 2 O + 60 fotoni ----> C 6 H 12
Analisi quantitativa dell interazione proteina-proteina
 Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Effetto Zeeman anomalo
 Effetto Zeeman anomalo Direzione del campo B esempio: : j=3/2 Direzione del campo B j=1+1/2 = 3/2 s m j =+3/2 m j =+1/2 l m j =-1/2 m j =-3/2 La separazione tra i livelli é diversa l e µ l antiparalleli
Effetto Zeeman anomalo Direzione del campo B esempio: : j=3/2 Direzione del campo B j=1+1/2 = 3/2 s m j =+3/2 m j =+1/2 l m j =-1/2 m j =-3/2 La separazione tra i livelli é diversa l e µ l antiparalleli
LA PRODUZIONE DEI RAGGI X
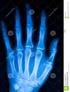 UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
La fluorescenza. Figura 1. una lampada a gas, un laser, ecc. viene assorbito dal fluoroforo in un tempo estremamente breve, dell'ordine 15
 La fluorescenza Tutte le forme di emissione di luce da parte di materiali sono chiamate luminescenza. Affinché il fenomeno avvenga, è necessario che una sorgente esterna fornisca al sistema una quantità
La fluorescenza Tutte le forme di emissione di luce da parte di materiali sono chiamate luminescenza. Affinché il fenomeno avvenga, è necessario che una sorgente esterna fornisca al sistema una quantità
ATOMO POLIELETTRONICO. Numero quantico di spin m s
 ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
Metodi spettroscopici per le Biotecnologie
 AA 203-204 Metodi spettroscopici per le Biotecnologie Spettroscopia di emissione UV-VIS (2) Dott. Alfonso Zoleo I percorsi possibili dallo stato eccitato In ragione della maggiore o minore probabilità
AA 203-204 Metodi spettroscopici per le Biotecnologie Spettroscopia di emissione UV-VIS (2) Dott. Alfonso Zoleo I percorsi possibili dallo stato eccitato In ragione della maggiore o minore probabilità
SPETTROFOTOMETRIA. Tutti sinonimi
 SPETTROFOTOMETRIA SPETTROSCOPIA SPETTROMETRIA SPF FORS (Fiber Optics Reflectance Spectroscopy) RS (Reflectance Spectroscopy ma anche Raman Spectroscopy!!! ) Tutti sinonimi Analisi scientifiche per i Beni
SPETTROFOTOMETRIA SPETTROSCOPIA SPETTROMETRIA SPF FORS (Fiber Optics Reflectance Spectroscopy) RS (Reflectance Spectroscopy ma anche Raman Spectroscopy!!! ) Tutti sinonimi Analisi scientifiche per i Beni
Dipartimento di Scienze Chimiche. Processi di decadimento degli stati elettronici eccitati: Descrizione generale dei processi di decadimento
 Processi di decadimento degli stati elettronici eccitati: Descrizione generale dei processi di decadimento Emissione di Fluorescenza Intersystem Crossing e Fosforescenza Internal Conversion. 1 Diagramma
Processi di decadimento degli stati elettronici eccitati: Descrizione generale dei processi di decadimento Emissione di Fluorescenza Intersystem Crossing e Fosforescenza Internal Conversion. 1 Diagramma
Spettroscopia in assorbimento overtone dell anidride carbonica con l uso di laser a diodo
 Spettroscopia in assorbimento overtone dell anidride carbonica con l uso di laser a diodo A. Lucchesini, S. Gozzini Istituto per i Processi Chimico Fisici del Consiglio Nazionale delle Ricerche - Pisa
Spettroscopia in assorbimento overtone dell anidride carbonica con l uso di laser a diodo A. Lucchesini, S. Gozzini Istituto per i Processi Chimico Fisici del Consiglio Nazionale delle Ricerche - Pisa
Atomi a più elettroni
 Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
1. PRINCIPI GENERALI IL METODO A IMPULSI
 1. PRINCIPI GENERALI IL METODO A IMPULSI LA RADIAZIONE EM CAMPO ELETTRICO OSCILLANTE CAMPO MAGNETICO OSCILLANTE Radiofrequenze n = 40-1000 MHz (In pratica: 300 1000 MHz) Lo Spin Nucleare I I = 0, 1/2,
1. PRINCIPI GENERALI IL METODO A IMPULSI LA RADIAZIONE EM CAMPO ELETTRICO OSCILLANTE CAMPO MAGNETICO OSCILLANTE Radiofrequenze n = 40-1000 MHz (In pratica: 300 1000 MHz) Lo Spin Nucleare I I = 0, 1/2,
Risonanza Magnetico Nucleare
 Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Risonanza Magnetico Nucleare 21/3/2005 RMN ovvero NMR Spettroscopia RMN permette di - acquisire immagini 2D e 3D di parti del corpo umano ottima risoluzione
Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Risonanza Magnetico Nucleare 21/3/2005 RMN ovvero NMR Spettroscopia RMN permette di - acquisire immagini 2D e 3D di parti del corpo umano ottima risoluzione
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO
 SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
La radioattività. La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche.
 La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
Applicazioni della Spettroscopia UV-vis all analisi delle proteine
 Applicazioni della Spettroscopia UV-vis all analisi delle proteine La radiazione elettromagnetica Con il termine radiazione s intende normalmente ogni forma di energia che si propaga mediante onde o particelle
Applicazioni della Spettroscopia UV-vis all analisi delle proteine La radiazione elettromagnetica Con il termine radiazione s intende normalmente ogni forma di energia che si propaga mediante onde o particelle
Chimica Fisica 2. Vibrazioni di molecole poliatomiche
 Chimica Fisica 2 chimica industriale 2 anno A.A. 2009-0 Vibrazioni di molecole poliatomiche Antonio Toffoletti Spettroscopia vibrazionale Molecole Bi-atomiche Approssimazione armonica E v = (v + ½)ħω ω
Chimica Fisica 2 chimica industriale 2 anno A.A. 2009-0 Vibrazioni di molecole poliatomiche Antonio Toffoletti Spettroscopia vibrazionale Molecole Bi-atomiche Approssimazione armonica E v = (v + ½)ħω ω
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Elettricità e Fisica Moderna
 Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Elettricità e Fisica Moderna 1) Una candela emette una potenza di circa 1 W ad una lunghezza d onda media di 5500 Å a)
Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Elettricità e Fisica Moderna 1) Una candela emette una potenza di circa 1 W ad una lunghezza d onda media di 5500 Å a)
ASSORBIMENTO UV-VIS. Atomo
 ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
Spettroscopia di Fluorescenza
 Spettroscopia di Fluorescenza assorbimento decadimento decadimento radiativo non radiativo stato eccitato h h calore stato fondamentale Spettroscopia di Fluorescenza assorbimento decadimento decadimento
Spettroscopia di Fluorescenza assorbimento decadimento decadimento radiativo non radiativo stato eccitato h h calore stato fondamentale Spettroscopia di Fluorescenza assorbimento decadimento decadimento
SPETTROFOTOMETRIA UV/VIS
 SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
Capitolo 10: Spettroscopia. Spettroscopia: interazione tra molecole e radiazione elettromagnetica
 Capitolo 10: Spettroscopia Spettroscopia: interazione tra molecole e radiazione elettromagnetica H O H 1 Dalla descrizione secondo Maxwell (1864) dei fenomeni elettromagnetici: radiazione elettromagnetica
Capitolo 10: Spettroscopia Spettroscopia: interazione tra molecole e radiazione elettromagnetica H O H 1 Dalla descrizione secondo Maxwell (1864) dei fenomeni elettromagnetici: radiazione elettromagnetica
Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame.
 Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame. Non necessariamente i due elettroni che concorrono alla formazione del legame devono provenire da entrambi gli atomi
Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame. Non necessariamente i due elettroni che concorrono alla formazione del legame devono provenire da entrambi gli atomi
Spettroscopia. Spettroscopia
 Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
Spettroscopia Spettroscopia IR Spettroscopia NMR Spettrometria di massa 1 Spettroscopia E un insieme di tecniche che permettono di ottenere informazioni sulla struttura di una molecola attraverso l interazione
1. Microscopio in campo chiaro 2. Microscopio in campo oscuro 3. Microscopio in contrasto di fase 4. Microscopio ad interferenza 5.
 Principali tipi di microscopi 1. Microscopio in campo chiaro 2. Microscopio in campo oscuro 3. Microscopio in contrasto di fase 4. Microscopio ad interferenza 5. Microscopio a contrasto di fase interferenziale
Principali tipi di microscopi 1. Microscopio in campo chiaro 2. Microscopio in campo oscuro 3. Microscopio in contrasto di fase 4. Microscopio ad interferenza 5. Microscopio a contrasto di fase interferenziale
L ONDA ELETTROMAGNETICA UNITA DI MISURA E DEFINIZIONI. ν ν. λ =
 IR: Teoria L ONDA ELETTROMAGNETICA Campo elettrico Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
IR: Teoria L ONDA ELETTROMAGNETICA Campo elettrico Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
TECNICHE RADIOCHIMICHE
 TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
ARGOMENTO: Cenni di Fisica del Nucleo
 UNIVERSITA DEGLI STUDI DI GENOVA C.L. TECNICHE DIAGNOSTICHE RADIOLOGICHE CORSO INTEGRATO: MISURE ELETTRICHE ED ELETTRONICHE MATERIA: FISICA APPLICATA 2 (2 anno 1 sem) ARGOMENTO: Cenni di Fisica del Nucleo
UNIVERSITA DEGLI STUDI DI GENOVA C.L. TECNICHE DIAGNOSTICHE RADIOLOGICHE CORSO INTEGRATO: MISURE ELETTRICHE ED ELETTRONICHE MATERIA: FISICA APPLICATA 2 (2 anno 1 sem) ARGOMENTO: Cenni di Fisica del Nucleo
ATOMI MONOELETTRONICI
 ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
Generalità delle onde elettromagnetiche
 Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
LASER. Light Amplification by Stimulated Emission of Radiation. Introduzione. Assorbimento, emissione spontanea, emissione stimolata
 LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
Capitolo 4 Le spettroscopie. 1. Lo spettro elettromagnetico
 Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Capitolo 4 Le spettroscopie 1. Lo spettro elettromagnetico 2) Tipi di spettroscopia Emissione: transizione da livello superiore a livello inferiore Assorbimento: contrario 2.1 Spettroscopie rotazionali,
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Interazione luce- atomo
 Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Corso di Laboratorio di Biofotonica
 SAIENZA Università di Roma Laurea magistrale in Ingegneria delle Nanotecnologie A.A. 2015-2016 Corso di Laboratorio di Biofotonica rof. Francesco Michelotti SAIENZA Università di Roma Facoltà di Ingegneria
SAIENZA Università di Roma Laurea magistrale in Ingegneria delle Nanotecnologie A.A. 2015-2016 Corso di Laboratorio di Biofotonica rof. Francesco Michelotti SAIENZA Università di Roma Facoltà di Ingegneria
Violazione della Parità
 Violazione della Parità Raffaele Pontrandolfi Corso di Astrosica e Particelle Elementari Motivazione Per spiegare l asimmetria nell universo tra particelle e antiparticelle bisogna trovare dei processi
Violazione della Parità Raffaele Pontrandolfi Corso di Astrosica e Particelle Elementari Motivazione Per spiegare l asimmetria nell universo tra particelle e antiparticelle bisogna trovare dei processi
SPETTROMETRIA GAMMA SPETTROMETRIA GAMMA
 La spettrometria gamma è un metodo di analisi che consente la determinazione qualitativa e quantitativa dei radionuclidi gamma-emettitori presenti in un campione di interesse. Il successo di questo metodo
La spettrometria gamma è un metodo di analisi che consente la determinazione qualitativa e quantitativa dei radionuclidi gamma-emettitori presenti in un campione di interesse. Il successo di questo metodo
Baldin Boris Liceo della Comunicazione "Maria Ausiliatrice" di Padova (PD) Trevisanello Enrico Istituto "P. Scalcerle" di Padova (PD) Finozzi
 Baldin Boris Liceo della Comunicazione "Maria Ausiliatrice" di Padova (PD) Trevisanello Enrico Istituto "P. Scalcerle" di Padova (PD) Finozzi Francesco ITIS "De Pretto" di Schio (VI) Scopo: Verificare
Baldin Boris Liceo della Comunicazione "Maria Ausiliatrice" di Padova (PD) Trevisanello Enrico Istituto "P. Scalcerle" di Padova (PD) Finozzi Francesco ITIS "De Pretto" di Schio (VI) Scopo: Verificare
CORSO DI LAUREA IN OTTICA E OPTOMETRIA
 CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
Il microscopio elettronico a scansione
 Il microscopio elettronico a scansione Nel SEM (ed in genere nella microscopia elettronica) viene sfruttata l interazione di un fascio di e - con il campione per ricavare informazioni sul campione stesso
Il microscopio elettronico a scansione Nel SEM (ed in genere nella microscopia elettronica) viene sfruttata l interazione di un fascio di e - con il campione per ricavare informazioni sul campione stesso
CARATTERIZZAZIONE RILASSOMETRICA DI VINI ED ACETI
 Università degli Studi di Torino Facoltà di Scienze M.F.N Corso di Laurea Magistrale in Chimica Clinica, Forense e dello Sport TESI DI LAUREA CARATTERIZZAZIONE RILASSOMETRICA DI VINI ED ACETI Candidato:
Università degli Studi di Torino Facoltà di Scienze M.F.N Corso di Laurea Magistrale in Chimica Clinica, Forense e dello Sport TESI DI LAUREA CARATTERIZZAZIONE RILASSOMETRICA DI VINI ED ACETI Candidato:
Corso di Chimica Generale CL Biotecnologie
 Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.)
 RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.) e una tecnica non invasiva impiega radiazioni a bassa frequenza (non ionizzanti!) ν 10-100 MHz (radiofrequenze) sfrutta la
RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.) e una tecnica non invasiva impiega radiazioni a bassa frequenza (non ionizzanti!) ν 10-100 MHz (radiofrequenze) sfrutta la
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
Beta decay. max e ) -5 Legge di Sargent
 Beta decay Nuclei emettono elettroni con una distribuzione continua di energia Il valore massimo dell energia energia cinetica dell elettrone elettrone e circa uguale alla differenza di massa tra i nuclei
Beta decay Nuclei emettono elettroni con una distribuzione continua di energia Il valore massimo dell energia energia cinetica dell elettrone elettrone e circa uguale alla differenza di massa tra i nuclei
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
DEFINIZIONI (D.Lgs. 81/08)
 Radiazioni Ottiche Artificiali -ROA- Cosa sono Anna Maria Vandelli Dipartimento di Sanità Pubblica AUSL Modena SPSAL Sassuolo Fonte ISPESL 1 DEFINIZIONI (D.Lgs. 81/08) si intendono per radiazioni ottiche:
Radiazioni Ottiche Artificiali -ROA- Cosa sono Anna Maria Vandelli Dipartimento di Sanità Pubblica AUSL Modena SPSAL Sassuolo Fonte ISPESL 1 DEFINIZIONI (D.Lgs. 81/08) si intendono per radiazioni ottiche:
Profili di trasmissione dei filtri interferenziali del telescopio PSPT
 I.N.A.F Osservatorio Astronomico di Roma Profili di trasmissione dei filtri interferenziali del telescopio PSPT Mauro Centrone Fabrizio Giorgi Nota tecnica - 2003 1 Introduzione I filtri interferenziali
I.N.A.F Osservatorio Astronomico di Roma Profili di trasmissione dei filtri interferenziali del telescopio PSPT Mauro Centrone Fabrizio Giorgi Nota tecnica - 2003 1 Introduzione I filtri interferenziali
ESPERIMENTO DI YOUNG DOPPIA FENDITURA
 ESPERIMENTO DI YOUNG DOPPIA FENDITURA Larghezza fenditure a > d (L = distanza fenditure - schermo; d = distanza tra le fenditure) Evidenza della natura ondulatoria della luce Luce monocromatica
ESPERIMENTO DI YOUNG DOPPIA FENDITURA Larghezza fenditure a > d (L = distanza fenditure - schermo; d = distanza tra le fenditure) Evidenza della natura ondulatoria della luce Luce monocromatica
INTERFERENZA - DIFFRAZIONE
 INTERFERENZA - F. Due onde luminose in aria, di lunghezza d onda = 600 nm, sono inizialmente in fase. Si muovono poi attraverso degli strati di plastica trasparente di lunghezza L = 4 m, ma indice di rifrazione
INTERFERENZA - F. Due onde luminose in aria, di lunghezza d onda = 600 nm, sono inizialmente in fase. Si muovono poi attraverso degli strati di plastica trasparente di lunghezza L = 4 m, ma indice di rifrazione
Il semiconduttore è irradiato con fotoni a λ=620 nm, che vengono assorbiti in un processo a due particelle (elettroni e fotoni).
 Fotogenerazione -1 Si consideri un semiconduttore con banda di valenza (BV) e banda di conduzione (BC) date da E v =-A k 2 E c =E g +B k 2 Con A =10-19 ev m 2, B=5, Eg=1 ev. Il semiconduttore è irradiato
Fotogenerazione -1 Si consideri un semiconduttore con banda di valenza (BV) e banda di conduzione (BC) date da E v =-A k 2 E c =E g +B k 2 Con A =10-19 ev m 2, B=5, Eg=1 ev. Il semiconduttore è irradiato
Spettroscopia: introduzione.
 Spettroscopia: introduzione. Le tecniche spettroscopiche di indagine strutturale utilizzano l'interazione di una radiazione elettromagnetica con le molecole del campione in esame per ricavare informazioni
Spettroscopia: introduzione. Le tecniche spettroscopiche di indagine strutturale utilizzano l'interazione di una radiazione elettromagnetica con le molecole del campione in esame per ricavare informazioni
Display devices. Dispositivi attivi: Emettono radiazione propria e questa radiazione è quella che è usata dal dispositivo stesso
 Display devices Dispositivi attivi: Emettono radiazione propria e questa radiazione è quella che è usata dal dispositivo stesso Dispositivi passivi: Modulano l intensità di luce incidente Luminescenza
Display devices Dispositivi attivi: Emettono radiazione propria e questa radiazione è quella che è usata dal dispositivo stesso Dispositivi passivi: Modulano l intensità di luce incidente Luminescenza
Cenni di Spettroscopia
 Cenni di Spettroscopia Gli elettroni di una molecola possono avere energie diverse, possono, cioè, essere più o meno legati ai nuclei degli atomi che costituiscono la molecola. l numero di energie possibili
Cenni di Spettroscopia Gli elettroni di una molecola possono avere energie diverse, possono, cioè, essere più o meno legati ai nuclei degli atomi che costituiscono la molecola. l numero di energie possibili
Introduzione ai fenomeni di polarizzazione. Lezioni d'autore di Claudio Cigognetti
 Introduzione ai fenomeni di polarizzazione Lezioni d'autore di Claudio Cigognetti VIDEO POLARIZZAZIONE IN UN IPAD, RICAPITOLANDO Impiegando occhiali aventi lenti polaroid e un display a cristalli liquidi
Introduzione ai fenomeni di polarizzazione Lezioni d'autore di Claudio Cigognetti VIDEO POLARIZZAZIONE IN UN IPAD, RICAPITOLANDO Impiegando occhiali aventi lenti polaroid e un display a cristalli liquidi
Lezione n. 28. EPR Esempi ed applicazioni in campo biochimico e medico. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 28 EPR Esempi ed applicazioni in campo biochimico e medico 02/03/2008 Antonino Polimeno 1 Risonanza paramagnetica elettronica (1) - La Risonanza
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 28 EPR Esempi ed applicazioni in campo biochimico e medico 02/03/2008 Antonino Polimeno 1 Risonanza paramagnetica elettronica (1) - La Risonanza
Spettroscopia overtone dell'anidride carbonica e dell'etilene tramite laser a diodo
 Spettroscopia overtone dell'anidride carbonica e dell'etilene tramite laser a diodo Lucchesini A., Gozzini S. Istituto per i Processi Chimico-Fisici del Consiglio Nazionale delle Ricerche Area della Ricerca
Spettroscopia overtone dell'anidride carbonica e dell'etilene tramite laser a diodo Lucchesini A., Gozzini S. Istituto per i Processi Chimico-Fisici del Consiglio Nazionale delle Ricerche Area della Ricerca
Molecole. 04/09/13 3-MOL-0.doc 0
 Molecole 04/09/13 3-MOL-0.doc 0 Legame covalente H 2 + Il potenziale cui è soggetto l elettrone ha 2 minimi equivalenti 1) H + si avvicina a H 2) Se la barriera diventa abbastanza sottile la probabilità
Molecole 04/09/13 3-MOL-0.doc 0 Legame covalente H 2 + Il potenziale cui è soggetto l elettrone ha 2 minimi equivalenti 1) H + si avvicina a H 2) Se la barriera diventa abbastanza sottile la probabilità
Identificazione di un composto organico:
 Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
Il principio di indeterminazione di Heisenberg
 Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
Il principio di indeterminazione di Heisenberg Il prodotto degli errori nella determinazione contemporanea della quantità di moto (q = mv) e della posizione di un corpo in movimento è almeno uguale a h
Prova Scritta di Elettricità e Magnetismo e di Elettromagnetismo A. A Febbraio 2008 (Proff. F.Lacava, C.Mariani, F.Ricci, D.
 Prova Scritta di Elettricità e Magnetismo e di Elettromagnetismo A. A. 2006-07 - 1 Febbraio 2008 (Proff. F.Lacava, C.Mariani, F.Ricci, D.Trevese) Modalità: - Prova scritta di Elettricità e Magnetismo:
Prova Scritta di Elettricità e Magnetismo e di Elettromagnetismo A. A. 2006-07 - 1 Febbraio 2008 (Proff. F.Lacava, C.Mariani, F.Ricci, D.Trevese) Modalità: - Prova scritta di Elettricità e Magnetismo:
Elementi di Fisica 2CFU
 Elementi di Fisica 2CFU III parte - Elettromagnetismo Andrea Susa MAGNETISMO 1 Magnete Alcune sostanze naturali, come ad esempio la magnetite, hanno la proprietà di attirare pezzetti di ferro, e per questo
Elementi di Fisica 2CFU III parte - Elettromagnetismo Andrea Susa MAGNETISMO 1 Magnete Alcune sostanze naturali, come ad esempio la magnetite, hanno la proprietà di attirare pezzetti di ferro, e per questo
La Polarizzazione della luce
 La Polarizzazione della luce Applet Java sulle OEM Le Onde Elettromagnetiche Sono onde trasversali costituite dalle vibrazioni del vuoto quantistico. Hanno velocità c=3.0 10 8 m/s. In ogni istante E è
La Polarizzazione della luce Applet Java sulle OEM Le Onde Elettromagnetiche Sono onde trasversali costituite dalle vibrazioni del vuoto quantistico. Hanno velocità c=3.0 10 8 m/s. In ogni istante E è
MOLECOLE. 2 - i legami chimici. Prof. Vittoria Patti
 MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
Radioattività. 1. Massa dei nuclei. 2. Decadimenti nucleari. 3. Legge del decadimento XVI - 0. A. Contin - Fisica Generale Avanzata
 Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
Misura del coefficiente di assorbimento di vari materiali in funzione dell'energia del fascio dei fotoni incidenti
 materiali in funzione dell'energia del fascio dei fotoni Esperto Qualificato LNF - INFN Interazioni delle particelle indirettamente ionizzanti con la materia Le particelle indirettamente ionizzanti, principalmente
materiali in funzione dell'energia del fascio dei fotoni Esperto Qualificato LNF - INFN Interazioni delle particelle indirettamente ionizzanti con la materia Le particelle indirettamente ionizzanti, principalmente
I PARAMETRI MICROCLIMATICI PER AMBIENTI INTERNI
 I PARAMETRI MICROCLIMATICI PER AMBIENTI INTERNI I PARAMETRI MICROCLIMATICI Temperatura Umidità Illuminazione TEMPERATURA TEMPERATURA La temperatura è la proprietà che caratterizza lo stato termico di un
I PARAMETRI MICROCLIMATICI PER AMBIENTI INTERNI I PARAMETRI MICROCLIMATICI Temperatura Umidità Illuminazione TEMPERATURA TEMPERATURA La temperatura è la proprietà che caratterizza lo stato termico di un
LO SPETTRO ELETTROMAGNETICO
 LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
Fluorescenza in stato stazionario
 4 luorescenza in ato azionario Conizioni fotoazionarie M+hν k M* k r * [ * = nr)[ M M+hν M ] k[ M] ( kr + k t k nr M * k [ M] = ( k + k )[ M ] I I * [ M ] [ M] k r = [ M * r ( k ] k τ = Φ r r nr k + k
4 luorescenza in ato azionario Conizioni fotoazionarie M+hν k M* k r * [ * = nr)[ M M+hν M ] k[ M] ( kr + k t k nr M * k [ M] = ( k + k )[ M ] I I * [ M ] [ M] k r = [ M * r ( k ] k τ = Φ r r nr k + k
