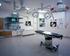
SERVIZIO PER CONVALIDA LABORATORIO PMA. CIG , IMPORTO BIENNALE POSTO A BASE D ASTA ,00 DI CUI 250,00 non suscettibili di ribasso
|
|
|
- Carmela Bonfanti
- 5 anni fa
- Visualizzazioni
Transcript
1 CAPITOLATO PRESTAZIONALE LOTTO 1 SERVIZIO PER CONVALIDA LABORATORIO PMA CIG , IMPORTO BIENNALE POSTO A BASE D ASTA ,00 DI CUI 250,00 non suscettibili di ribasso PREMESSA Trattasi di un servizio di convalida dei processi di allestimento in asepsi occorrente al Laboratorio di Procreazione Medicalmente Assistita (PMA) - Centro di Sterilità di Coppia, la Crioconservazione dei gameti e l Andrologia, UOC Ostetricia a Ginecologia - in ottemperanza alla normativa vigente della Banca dei tessuti Legge 191/2007 e DL 16/2010 che fa riferimento all EU Guidelines to Good Manufacturing Practice (GMP) Annex 1 per i requisiti minimi richiesti per la lavorazione delle cellule umane. Oggetto: Servizio per effettuare verifica concentrazione particellare e contaminazione microbiologica dell aria e delle superfici per Ambiente di Classe D e per le Cappe Biologiche di classe A del Laboratori di PMA per un importo max pari a circa 6000 per un anno (IVA esclusa). Documenti tecnici di riferimento, Norme ISO e Riferimenti internazionali - Decreto legislative 6 novembre 2007 n.191 (GURI n.261 del 9 novembre 2007) - Decreto legislative 25 gennaio 2010 n.16 (GURI n.40 del 18 febbraio 2010) - EU Guidelines to Good Manufacturing Practice (GMP) Annex 1 (update 2008) - UNI ISO e 2 in tema di Camere bianche ed ambienti associati controllati. - UNI ISO in tema di camere bianche ed ambienti associati controllati "Controllo della - biocontaminazione; - Manuale per le Banche dei Tessuti (I edizione settembre 2009) TIPOLOGIA DEL SERVIZIO La qualità e la sicurezza di tutte le fasi del processo di procreazione medicalmente assistita (PMA) che vanno dall accettazione del campione, raccolta/prelievo dei gameti, manipolazione, crioconservazione, stoccaggio e distribuzione delle cellule riproduttive dipendendo da un monitoraggio costante delle procedure. Durante queste fasi del processo esiste il rischio potenziale che si verifichino degli eventi dannosi per la salute delle cellule, gameti o embrioni con danni immediati al paziente. La fisiologia delle queste cellule riproduttive è molto delicata e risentono in modo determinante di varie condizioni ambientali (T, ph,% CO 2 ) e richiedono condizioni particolari di sterilità. Soltanto una attenzione meticolosa a tutti questi dettagli può ottimizzare le condizioni di crescita degli embrioni umani e la possibilità di avere una gravidanza di ogni paziente. In base al D.Lgs 16/2010 (All. V), che fa riferimento al EU Guidelines to GoodManufacturingPractice(GMP)Annex1(update 2008) un Centro di PMA deve possedere, dei requisitiminimi, per quanto riguardalaqualità dell aria. Una classificazione della qualità dell aria deve essere fatta inizialmente, dopo l installazione e la pulizia degli ambienti e poi monitorata periodicamente, mediante: - la conta delle particelle aerodisperse - la conta delle contaminazioni microbiologiche. La normativa richiede per la qualità dell aria una misurazione di numero di particelle e di colonie
2 microbiche (aria e superfice) in at rest equivalente al grado D secondo le linee Guida del Good Manufacturing Practice (GMP) Annex 1 (update 2008) di cui allegato 1; un controllo particellare dell aria e microbiologico di superfice in operation gradoa solo all interno delle cappe a flusso laminare. Limiti descrittinelle EU Guidelines to GMP Annex 1 (update 2008) parametri di riferimento cui è obbligatorio attenersi Limiti di concentrazione massima (particelle/m 3 ) per particelle maggiori o uguali alle dimensioni descritte in tabella. At rest In operation Grade 0.5 µm 5.0 µm 0.5 µm 5.0 µm A B C D Notdefined Notdefined Poiché talvolta i certificati rilasciati dalle ditte che effettuano i controlli della qualità dell aria riportano valori riferiti alla norma ISO, secondo la classificazione ISO il grado A della classificazione GMP equivale circa alla classe ISO 5, mentre il grado D della classificazione GMP equivale circa, nello stato atrest, alla classe ISO 8. Parametri strutturali del Laboratorio di PMA Grade Filtraggio aria Pressione positiva 99.97% (HEPA) % (ULPA) 5 Pa Ricambi d aria/ora 10 Temperatura 20 C - 24 C Umidità 40% - 60% Recommended limits for microbial contamination Air sample cfu/m 3 Settle plates (diameter 90 mm) Cfu/4 hours Contact plates (diameters 55 mm) Cfu/plate Glove print 5 fingers Cfu/glove A <1 <1 <1 <1 B C D
3 Strumenti per la conta delle particelle aerodisperse Lo strumento per la conta particellare utilizzato per le rilevazioni deve essere corredato di un certificato di taratura rilasciato da una struttura autorizzata e accreditata, copia del quale deve essere rilasciato insieme ai risultati del controllo. Numero di rilevazioni Il numero minimo di punti di campionamento è ricavato dalla tabella in funzione della superficie della camera bianca espressa in metri quadrati. (vedi norme ISO punto A4.1): N L = A dove N L è il numero minimo di rilevazioni A è l area del laboratorio espressa in metri quadrati Al fine di una significatività statistica, la campionatura dovrebbe essere effettuata tre volte per ogni singolo punto. Volume di aria da campionare Per il grado A, la rilevazione per ogni punto deve essere effettuata su almeno 1m 3 di aria, mentre per il grado D il volume dei campioni prelevati in corrispondenza di ciascun punto deve essere pari ad almeno 2 litri, con un tempo di campionamento minimo di 1 min per ogni punto (ISO :2016 parte 1, punto A4.4). Posizionamento dello strumento per la conta delle particelle (vedi ISO :2015 punto A4.2) ELENCO PROCEDURE RICHIESTE obbligatoriamente Devono essere obbligatoriamente previsti: 1) Verifica della classe di concentrazione particellare dell aria: Laboratorio di Embriologia zona pre filtro ( atrest grado D GMP): - Eseguita in stato di occupazione atrest mediante prelievo di campioni d aria e conteggio delle particelle con contatore particellare; - Il numero dei campionamenti saranno determinati in base alla radice quadrata delle superfici e dell ambiente. - Frequenza della verifica semestrale (per un totale di circa 2 verifiche l anno) 2) Verifica della classe di concentrazione particellare dell aria e visualizzazione flusso di aria smoke test Due cappe a flusso laminare in operation grado A GMP - Eseguita in stato di occupazione in operation mediante prelievo di campioni d aria e conteggio
4 delle particelle con contatore particellare; - Frequenza della verifica semestrale (per un totale di circa 2 campionamenti l anno) 3) Verifica della classe di contaminazione microbiologica dell aria Laboratorio di Embriologia, Seminologia, zona pre-filtro ( atrest grado D GMP) Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell aria con campionatore. - Frequenza dei campionamenti ognisei mesi con un numero minimo di 6 campionamenti per tipologia di controllo (per un totale di circa 24campionamenti l anno). Due cappe a flusso laminare in operation e atrest grado A GMP - Eseguita in stato di occupazione in operation CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell aria passivo. - Frequenza dei campionamenti ogni sei mesi con un numero minimo di3 campionamenti per tipologia di controllo (per un totale di circa 24 campionamenti l anno) 4) Verifica della classe di contaminazione microbiologica delle superfici Laboratorio di Embriologia e Seminologia( atrest grado D GMP): - Eseguita in stato di occupazione atrest per CBT (Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico delle superfici. - Frequenza dei campionamenti ogni sei mesi con un numero minimo di 9campionamenti per tipologia di controllo (per un totale di circa 36 campionamenti l anno) Due cappe a flusso laminare ( in operation e atrestgrado A GMP) - Eseguita in stato di occupazione in operation per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) sulle superfici. - Frequenza dei campionamenti ogni sei mesi con un numero minimo di 3 campionamenti per tipologia di controllo (per un totale di circa 24 campionamenti l anno) Treincubatori CO 2 ( at rest grado D GMP): - Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) sulle superfici - Frequenza dei campionamenti ogni sei mesi con un numero minimo di 1 campionamento per tipologia di controllo (per un totale di circa 12 campionamenti l anno) Deve essere prevista la possibilità di effettuare dei controlli particellari/microbiologici immediati senza attendere le scadenze previstein caso di eventi particolari quali contaminazionio installazione di nuove apparecchiature. Si richiede la misura della pressione differenziale tra i laboratori e la zona filtro, tra l ambulatorio chirurgico e le zone attigue. I laboratori destinati alla PMA sono il laboratorio di embriologia (circa 18m2) di seminologia (circa 18m2) ed il deposito criogenico. Si precisa che il depositi criogenico non deve essere covalidato. Le procedure dovranno essere comprensive di materiali di consumo (terreni di coltura conformi alla
5 Farmacopea Italiana e Europea, flaconi sterili e apirogeni per la dispensazione dei campioni finali) e attività di supporto (istruzioni sulla sequenza operativa, modalità di consegna e conservazione dei campioni, incubazione, analisi e lettura dei campioni, documentazione e certificazione), precisando che nulla verrà fornito da questa ASL. Tutti i controlli devono essere eseguiti secondo i requisiti previsti dalla normativa vigente con rilascio finale dei report comprovanti i risultati ottenuti e le metodiche impiegate. Nello specifico dovrà essere rilasciata la seguente documentazione a seguito di ogni controllo effettuato : - Tabella della concentrazione particellare - Rapporto prove microbiologiche (laboratorio accreditato) - Rapporto analisi sterilità (laboratorio accreditato) - Elenco caratteristiche strumentazioni di prova - Certificati di taratura di strumenti - Considerazioni, commenti e suggerimenti tecnici. Lo strumento per la conta particellare utilizzato per le rilevazioni deve essere corredato di un certificato di taratura rilasciato da una struttura autorizzata e accreditata, copia del quale deve essere rilasciato insieme ai risultati del controllo. Il predetto certificato deve essere consegnato ai Responsabili dei Laboratori sopra descritti in occasione di ogni verifica, a pena di risoluzione del contratto. La consegna del rapporto deve avvenire entro 30 giorni dalla data dell intervento.
6 LOTTO 2 SERVIZIO PER CONVALIDA PER EMATOLOGIA CON TRAPIANTO CIG , IMPORTO BIENNALE POSTO A BASE D ASTA ,00 DI CUI 200,00 non suscettibili di ribasso Premessa Trattasi di un servizio di convalida dei processi di allestimento in asepsi occorrente al Laboratorio di Crioconservazione cellule staminali ematopoietiche e Reparto Trapianti-UOC Ematologia con trapianto in ottemperanza alla normativa vigente della Banca dei tessuti Legge 191/2007e DL 16/2010 che fa riferimento all EU Guidelines to Good Manufacturing Practice (GMP) Annex 1 per i requisiti minimi richiesti per la lavorazione delle cellule umane. Oggetto: servizio per effettuare verifica concentrazione particellare e contaminazione microbiologica dell aria e delle superfici per Ambiente di Classe C e D e per le Cappe Biologiche di classe A del Laboratorio di Manipolazione Cellulare e Criopreservazione di cellule staminali ematopoietiche e Reparto trapianti per un importo pari a circa per un anno (IVA esclusa) Documenti tecnici di riferimento, Norme ISO e Riferimenti internazionali - Decreto legislative 6 novembre 2007 n.191 (GURI n.261 del 9 novembre 2007) - Decreto legislative 25 gennaio 2010 n.16 (GURI n.40 del 18 febbraio 2010) - EU Guidelines to Good Manufacturing Practice (GMP) Annex 1 (update 2008) - UNI ISO e 2 in tema di Camere bianche ed ambienti associati controllati. - UNI ISO in tema di camere bianche ed ambienti associati controllati "Controllo della biocontaminazione; TIPOLOGIA DEL SERVIZIO La qualità e la sicurezza di tutte le fasi del processo di manipolazione minima di cellule staminali ematopoietiche pretrapianto dipendendo da un monitoraggio costante delle procedure. Durante queste fasi del processo esiste il rischio potenziale che si verifichino degli eventi dannosi per la salute delle cellule, con danni immediati al paziente. In base al D.Lgs 16/2010 (All. V), che fa riferimento al EU Guidelines to GoodManufacturingPractice(GMP)Annex1(update 2008) un Laboratorio di Manipolazione Cellulare e Criopreservazione di cellule staminali ematopoietiche deve possedere, dei requisiti minimi, per quanto riguarda la qualità dell aria. Una classificazione della qualità dell aria deve essere fatta inizialmente, dopo l installazione e la pulizia degli ambienti e poi monitorata periodicamente, mediante: - la conta delle particelle aerodisperse
7 - la conta delle contaminazioni microbiologiche. La direttiva richiede per la qualità dell aria una misurazione di numero di particelle e di colonie microbiche (aria e superfice) in operation equivalente al grado C, secondo le linee Guida del Good Manufacturing Practice (GMP)Annex 1 (update 2008), per l area di manipolazione; un controllo particellare dell aria e microbiologico in atrest equivalente al grado D, secondo le linee Guida del Good Manufacturing Practice (GMP)Annex 1 (update 2008), per l area di stoccaggio e un controllo particellare dell aria e microbiologico di superfice in operation gradoa solo all interno delle cappe a flusso laminare. Ogni attività richiesta nel presente atto deve essere svolta dalla Ditta aggiudicatrice a pena di risoluzione del contratto. Limiti descrittinelle EU Guidelines to GMP Annex 1 (update 2008) parametri di riferimento cui è obbligatorio attenersi Maximum permitted number of particles per m 3 equal to or greater than the tabulated size At rest In operation Grade 0.5 µm 5.0 µm 0.5 µm 5.0 µm A B C D Notdefined Notdefined Poiché talvolta i certificati rilasciati dalle ditte che effettuano i controlli della qualità dell aria riportano valori riferiti alla norma ISO, secondo la classificazione ISO il grado A della classificazione GMP equivale circa alla classe ISO5 in condizioni atrest che operation, il grado C della classificazione GMP equivale circa alla classe ISO7in condizioni atrest e all ISO8 in condizioni di operation, mentre il grado D equivalecirca alla classe ISO8 in condizioni atrest. Filtraggio aria Parametri strutturali del laboratorio Pressione positiva 99.97% (HEPA) % (ULPA) 5 Pa Ricambi d aria/ora 10 Temperatura 20 C - 24 C Umidità 40% - 60% Recommended limits for microbial contamination Grade Air sample cfu/m 3 Settle plates (diameter 90 mm) Cfu/4 hours Contact plates (diameters 55 mm) Cfu/plate Glove print 5 fingers Cfu/glove A <1 <1 <1 <1
8 B C D Strumenti per la conta particellare Lo strumento per la conta particellare utilizzato per le rilevazioni deve essere corredato di un certificato di taratura rilasciato da una struttura autorizzata e accreditata, copia del quale deve essere rilasciato insieme ai risultati del controllo. Il predetto certificato deve essere consegnato al Responsabile del Laboratorio di Manipolazione Cellulare e Criopreservazionein occasione di ogni verifica, a pena di risoluzione del contratto. Numero di rilevazioni Il numero delle rilevazioni deve essere di almeno due punti; per ambienti con una superficie superiore ai 4 m 2 il numero dei punti da campionare deve essere calcolato secondo la seguente formula (vedi norme ISO ): N L = A dove N L è il numero minimo di rilevazioni A è l area del laboratorio espressa in metri quadrati Al fine di una significatività statistica, la campionatura dovrebbe essere effettuata tre volte per ogni singolo punto. Volume di aria da campionare Per il grado A, la rilevazione per ogni punto deve essere effettuata su almeno 1m 3 di aria, mentre per il grado C il volume dei campioni prelevati in corrispondenza di ciascun punto deve essere pari ad almeno 2 litri, con un tempo di campionamento minimo di 1 min per ogni punto (ISO B 4.2.2). ELENCO DELLE PROCEDURE RICHIESTE PER IL LABORATORIO DI MANIPOLAZIONE CELLULARE E CRIOPRESERVAZIONE Verifiche ambientali da effettuare: 1) controllo particellare e microbiologico dell aria dei seguenti ambienti - Laboratorio di Manipolazione cellulare-stanza n 4- modalità atrest e operational-5 piastre per CBT(Carica Batterica Totale) e 5-piastre per CMT (carica Micetica Totale)(per un totale di 20 campionamenti l anno) - Zona filtro-stanza n 3- modalità atrest -2 piastre per CBT(Carica Batterica Totale) e 2-piastre per CMT (carica Micetica Totale)(per un totale di 8 campionamenti l anno) - Area di accettazione-stanza n 2- modalità atrest -2 piastre per CBT(Carica Batterica Totale) e 2- piastre per CMT (carica Micetica Totale)(per un totale di 8 campionamenti l anno) - Area di stoccaggio-stanza n 1-modalità atrest -5 piastre per CBT(Carica Batterica Totale) e 5- piastre per CMT (carica Micetica Totale)(per un totale di 20 campionamenti l anno) Verifiche microbiologiche di superficie:
9 2) controllo microbiologico della strumentazione: - Centrifuga-2 piastre per CBT(Carica Batterica Totale) e 2-piastre per CMT (carica Micetica Totale)(per un totale di 8 campionamenti l anno) - Bilancia-1 piastra per CBT(Carica Batterica Totale) e 1-piastre per CMT (carica Micetica Totale)(per un totale di 4 campionamenti l anno) - congelatore a discesa programmata-1 piastraper CBT(Carica Batterica Totale) e 1-piastre per CMT (carica Micetica Totale)(per un totale di 4 campionamenti l anno) - bagnetto termostatato-1 piastraper CBT(Carica Batterica Totale) e 1-piastre per CMT (carica Micetica Totale)(per un totale di 4 campionamenti l anno) Verifica di una cappa a flusso laminare biohazard - controllo microbiologico e particellare dell aria - il controllo microbiologico deve essere fatto valutando 4 punti per CBT (Carica Batterica Totale) e 4-punti per CMT (carica Micetica Totale)(per un totale di 16 campionamenti l anno) Deve essere prevista la possibilità di effettuare dei controlli particellari/microbiologici immediati senza attendere le scadenze previste in caso di eventi particolari quali contaminazioni o installazione di nuove apparecchiature. Si richiede la misura della pressione differenziale tra la zona di accettazione, zona filtro e laboratorio di manipolazione cellulare. Il laboratorio è 50m 2 di superficie suddiviso in tre aree una di stoccaggio (ambiente classe D), una di accettazione, una zona filtro (classe D) e una di manipolazione cellulare (ambiente classe C). I controlli devono avvenire con scadenza semestrale così come stabilito dagli standard JACIE. ELENCO DELLE PROCEDURE RICHIESTE PER REPARTO TRAPIANTI L area trapianti è composta da 4 stanze con bagno attiguo e tutta l area è di circa 50m 2 Verifiche ambientali da effettuare: 1) controllo particellare e microbiologico dell aria nelle 4 stanze-modalità atrest -Verifica portata d aria, unidirezionalità, ricambi orari -Verifica livello pressurizzazione -Verifica microclima: temperatura e umidità 2) Verifiche microbiologiche di superficie - controlli microbiologici pareti e superfici di tutti gli ambienti-3 piastreper CBT(Carica Batterica Totale) e 3-piastre per CMT (carica Micetica Totale)(per un totale di 12 campionamenti l anno). - controllo microbiologico del tavolo e della struttura del letto-5 piastre per CBT(Carica Batterica Totale) e 5-piastre per CMT (carica Micetica Totale)(per un totale di 20 campionamenti l anno). - controllo microbiologico bagno-5 piastre per CBT(Carica Batterica Totale) e 5-piastre per CMT (carica Micetica Totale)(per un totale di 20 campionamenti l anno).
10 Si richiede inoltre misurazione dei parametri ambientali quali, temperatura, pressione e umidità. I controlli devono avvenire con scadenza semestrale così come stabilito dagli standard JACIE. Le procedure dovranno essere comprensive di materiali di consumo (terreni di coltura conformi alla Farmacopea Italiana e Europea, flaconi sterili e apirogeni per la dispensazione dei campioni finali) e attività di supporto (istruzioni sulla sequenza operativa, modalità di consegna e conservazione dei campioni, incubazione, analisi e lettura dei campioni, documentazione e certificazione), precisando che nulla verrà fornito da questa ASL. Tutti i controlli devono essere eseguiti secondo i requisiti previsti dalla normativa vigente con rilascio finale dei report comprovanti i risultati ottenuti e le metodiche impiegate. Nello specifico dovrà essere rilasciata la seguente documentazione: - Tabella della concentrazione particellare - Rapporto prove microbiologiche (laboratorio accreditato) - Rapporto analisi sterilità (laboratorio accreditato) - Elenco caratteristiche strumentazioni di prova - Certificati di taratura di strumenti - Considerazioni, commenti e suggerimenti tecnici. Lo strumento per la conta particellare utilizzato per le rilevazioni deve essere corredato di un certificato di taratura rilasciato da una struttura autorizzata e accreditata, copia del quale deve essere rilasciato insieme ai risultati del controllo. Il predetto certificato deve essere consegnato ai Responsabili dei Laboratori sopra descritti in occasione di ogni verifica, a pena di risoluzione del contratto. La consegna del rapporto deve avvenire entro 30 giorni dalla data dell intervento. LOTTO 3 SERVIZIO DI CONVALIDA PER IMMUNOEMATOLOGIA E MEDICINA TRASFUSIONALE CIG IMPORTO BIENNALE POSTO A BASE D ASTA ,00 DI CUI 350,00 non suscettibili di ribasso Oggetto: servizio per effettuare verifica concentrazione particellare e contaminazione microbiologica dell aria e
11 delle superfici per Ambiente di Classe A e D e per le Cappe Biologiche di classe A del Laboratorio di Manipolazione Cellulare e Criopreservazione di cellule staminali ematopoietiche e Reparto trapianti per un importo pari a circa per un anno (IVA esclusa) Documenti tecnici di riferimento, Norme ISO e Riferimenti internazionali Accordo Conferenza Stato-Regioni n. 242 ESR del , recepito con D.G.R. n. 139 del 2012, D.C.A. n di Accreditamento Istituzionale del SIMT di Latina all esercizio delle attività trasfusionali, Decreto Ministeriale n. 69 del Disposizioni relative ai Requisiti di qualità e sicurezza del sangue e degli emocomponenti, Decreto Legislativo n. 16 del 2010 European Union Guidelines to GoodManifacturingPractice, All. V, Rif. Annex 1 del Certificazione ISO edz ottenuta nel 2012, Direttiva UE n del 2016 GoodPracticeGuidelines in Medicina Trasfusionale TIPOLOGIA DEL SERVIZIO La qualità e la sicurezza di tutte le fasi di raccolta, produzione e conservazione degli emocomponenti dipendono da un monitoraggio costante delle procedure. Il controllo particellare e microbiologico consente di monitorare attentamente eventuali contaminazioni nel corso delle varie fasi del processo. In base al D.Lgs 16/2010 (All. V), che fa riferimento al EU Guidelines to Good Manufacturing Practice (GMP) Annex 1(update 2008) il SIMT deve possedere, dei requisiti minimi, per quanto riguarda la qualità dell aria. Una classificazione della qualità dell aria deve essere fatta inizialmente, dopo l installazione e la pulizia degli ambienti e poi monitorata periodicamente, mediante: - la conta delle particelle aerodisperse - la conta delle contaminazioni microbiologiche. La direttiva richiede per la qualità dell aria una misurazione di numero di particelle e di colonie microbiche (aria e superfice) in atrest equivalente al grado D secondo le linee Guida del Good Manufacturing Practice (GMP) Annex 1 (update 2008) di cui allegato 1; un controllo particellare dell aria e microbiologico di superfice in operation gradoa solo all interno delle cappe a flusso laminare. Limiti descritti nelle EU Guidelines to GMP Annex 1 (update 2008) cui bisogna obbligatoriamente attenersi Limiti di concentrazione massima (particelle/m 3 ) per particelle maggiori o uguali alle dimensioni descritte in tabella. At rest In operation Grade 0.5 µm 5.0 µm 0.5 µm A B C D Notdefined Poiché talvolta i certificati rilasciati dalle ditte che effettuano i controlli della qualità dell aria riportano valori riferiti alla norma ISO, secondo la classificazione ISO il grado A della classificazione GMP equivale circa alla classe ISO 5, mentre il grado D della classificazione GMP equivale circa, nello stato atrest, alla classe ISO 8. Parametri strutturali del SIMT
12 Filtraggio aria Pressione positiva 99.97% (HEPA) % (ULPA) 5 Pa Ricambi d aria/ora 10 Temperatura 20 C - 24 C Umidità 40% - 60% Recommended limits for microbial contamination Grade Air sample cfu/m 3 Settle plates (diameter 90 mm) Cfu/4 hours Contact plates (diameters 55 mm) Cfu/plate A <1 <1 <1 B C D Strumenti per la conta delle particelle aerodisperse Lo strumento per la conta particellare utilizzato per le rilevazioni deve essere corredato di un certificato di taratura rilasciato da una struttura autorizzata e accreditata, copia del quale deve essere rilasciato insieme ai risultati del controllo. Numero di rilevazioni Il numero minimo di punti di campionamento è ricavato dalla tabella in funzione della superficie della camera bianca espressa in metri quadrati. (vedi norme ISO punto A4.1): N L = A dove N L è il numero minimo di rilevazioni A è l area del laboratorio espressa in metri quadrati Al fine di una significatività statistica, la campionatura dovrebbe essere effettuata tre volte per ogni singolo punto. Volume di aria da campionare Per il grado A, la rilevazione per ogni punto deve essere effettuata su almeno 1m 3 di aria, mentre per il grado D il volume dei campioni prelevati in corrispondenza di ciascun punto deve essere pari ad almeno 2 litri, con un tempo di campionamento minimo di 1 min per ogni punto (ISO :2016 parte 1, punto A4.4). Posizionamento dello strumento per la conta delle particelle (vedi ISO :2015 punto A4.2) ELENCO PROCEDURE RICHIESTE Devono essere obbligatoriamente previsti: 1) Verifica della classe di concentrazione particellare dell aria : - Area raccolta sangue intero ed emocomponenti ( atrest grado D GMP): Eseguita in stato di occupazione atrest mediante prelievo di campioni d aria e conteggio delle particelle con contatore particellare; Il numero dei campionamenti saranno determinati in base alla radice quadrata delle superfici e dell ambiente. Frequenza della verifica semestrale(per un totale di circa 2 verifiche l anno)
13 - Area lavorazione emocomponenti ( atrest grado D GMP): Eseguita in stato di occupazione atrest mediante prelievo di campioni d aria e conteggio delle particelle con contatore particellare; Il numero dei campionamenti saranno determinati in base alla radice quadrata delle superfici e dell ambiente. Frequenza della verifica semestrale (per un totale di circa 2 verifiche l anno) - Area conservazione emocomponenti( atrest grado D GMP): Eseguita in stato di occupazione atrest mediante prelievo di campioni d aria e conteggio delle particelle con contatore particellare; Il numero dei campionamenti saranno determinati in base alla radice quadrata delle superfici e dell ambiente. Frequenza della verifica semestrale (per un totale di circa 2 verifiche l anno) - - Area raccolta cellule staminali ( atrest grado D GMP): Eseguita in stato di occupazione atrest mediante prelievo di campioni d aria e conteggio delle particelle con contatore particellare; Il numero dei campionamenti saranno determinati in base alla radice quadrata delle superfici e dell ambiente. Frequenza della verifica semestrale (per un totale di circa 2 verifiche l anno) - Laboratorio di immunoematologia ( atrest grado D GMP): Eseguita in stato di occupazione atrest mediante prelievo di campioni d aria e conteggio delle particelle con contatore particellare; Il numero dei campionamenti saranno determinati in base alla radice quadrata delle superfici e dell ambiente. Frequenza della verifica semestrale (per un totale di circa 2 verifiche l anno) Una cappa a flusso laminare (in stato occupazionale At rest e in operation grado A GMP (e visualizzazione flusso di aria smoke test2). Frequenza della verifica semestrale (per un totale di circa 1 campionamento l anno) 2) Verifica della classe di contaminazione microbiologica dell'aria( atrest grado D GMP): - Area raccolta sangue intero ed emocomponenti ( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell'aria con campionatore Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 1 campionamento per tipologia di controllo (per un totale di 2 campionamenti l'anno). - Area lavorazione emocomponenti( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell'aria con campionatore Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 2 campionamenti per tipologia di controllo (per un totale di 8 campionamenti l'anno) - Area conservazione emocomponenti( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell'aria con campionatore
14 Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 1 campionamento per tipologia di controllo. (per un totale di 4 campionamenti l'anno). - Area raccolta cellule staminali ( atrest grado D GMP) Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell'aria con campionatore Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 1 campionamento per tipologia di controllo (per un totale di 4 campionamenti l'anno). Una cappa a flusso laminare ( in operation grado A GMP) Eseguita in stato di occupazione in operation CBT (Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell aria con campionatore. Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 1 campionamento per tipologia di controllo (per un totale di circa 4 campionamenti l anno). - Laboratorio di immunoematologia ( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico dell'aria con campionatore Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 1 campionamento per tipologia di controllo ( per un totale di 4 campionamenti l'anno) 3) Verifica della classe di contaminazione microbiologica delle superfici ( atrest grado D GMP): - Area raccolta sangue intero ed emocomponenti ( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico delle superfici Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 4 campionamenti per tipologia di controllo per un totale di 16 campionamenti l'anno.) - Area lavorazione emocomponenti( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico delle superfici Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 5 campionamenti per tipologia di controllo (per un totale di 20 campionamenti l'anno). - Area conservazione emocomponenti( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico delle superfici Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 4 campionamenti per tipologia di controllo(per un totale di 16 campionamenti l'anno). - Area raccolta cellule staminali ( atrest grado D GMP) Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) mediante campionamento microbiologico delle superfici Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 3 campionamenti per tipologia di controllo (per un totale di 12 campionamenti l'anno). - Due centrifughe (cestelli e superfici interne)( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica
15 Micetica Totale) sulle superfici Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 2 campionamenti per tipologia di controllo (per un totale di circa 8 campionamenti l anno). Una cappa a flusso laminare ( in operation grado A GMP) Eseguita in stato di occupazione in operation per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) sulle superfici. Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 4campionamenti per tipologia di controllo (per un totale di circa 16 campionamenti l anno) Laboratorio di immunoematologia ( atrest grado D GMP): Eseguita in stato di occupazione atrest per CBT(Carica Batterica Totale) che per CMT (carica Micetica Totale) sulle superfici, Frequenza dei campionamenti ogni 6 mesi con un numero minimo di 2 campionamenti per tipologia di controllo (per un totale di circa 8 campionamenti l anno). Le procedure dovranno essere comprensive di materiali di consumo (terreni di coltura conformi alla Farmacopea Italiana e Europea, flaconi sterili e apirogeni per la dispensazione dei campioni finali) e attività di supporto (istruzioni sulla sequenza operativa, modalità di consegna e conservazione dei campioni, incubazione, analisi e lettura dei campioni, documentazione e certificazione), precisando che nulla verrà fornito da questa ASL. Tutti i controlli devono essere eseguiti secondo i requisiti previsti dalla normativa vigente con rilascio finale dei report comprovanti i risultati ottenuti e le metodiche impiegate. Nello specifico dovrà essere rilasciata la seguente documentazione: - Tabella della concentrazione particellare - Rapporto prove microbiologiche (laboratorio accreditato) - Rapporto analisi sterilità (laboratorio accreditato) - Elenco caratteristiche strumentazioni di prova - Certificati di taratura di strumenti - Considerazioni, commenti e suggerimenti tecnici. Lo strumento per la conta particellare utilizzato per le rilevazioni deve essere corredato di un certificato di taratura rilasciato da una struttura autorizzata e accreditata, copia del quale deve essere rilasciato insieme ai risultati del controllo. Il predetto certificato deve essere consegnato ai Responsabili dei Laboratori sopra descritti in occasione di ogni verifica, a pena di risoluzione del contratto. La consegna del rapporto deve avvenire entro 30 giorni dalla data dell intervento.
16 LOTTO 4 SERVIZIO DI CONVALIDA PER LABORATORIO UNITÀ FARMACI ANTITUMORALI (UFA) CIG e IMPORTO BIENNALE POSTO A BASE D ASTA ,00 DI CUI 950,00 non suscettibili di ribasso Trattasi di un servizio di convalida dei processi di allestimento in asepsi occorrente al Laboratorio Unità Farmaci Antitumorali (UFA) UOC Assistenza Farmaceutica 1 in ottemperanza alla normativa vigente in ambito di controlli ambientali e microbiologi (Farmacopea Ufficiale XII ed) e di sicurezza sui luoghi di lavoro (D.lgs. 9 aprile 2008, n. 81, Testo unico sulla salute e sicurezza sul lavoro). Oggetto: - Servizio per effettuare verifica concentrazione particellare e contaminazione microbiologica CBT e CMT dell aria e delle superfici per Ambiente di Classe B e per le Cappe del Laboratorio Unità Farmaci Antitumorali (UFA), e analisi di sterilità sui prodotti allestiti finiti. - Campionamento, analisi e relazione tecnica per ricerca analitica contaminanti prima e dopo la preparazione sulle superfici della camera bianca. per un importo pari a per un anno (IVA esclusa). Documenti tecnici di riferimento, Norme ISO e Riferimenti internazionali 1 USP 797 (draft2016) 2 USP 800 (draft2016) 3 EU-GMP (Good Manufacturing Practice ) 2008 Vol 4. Annex 1 (in attesa del nuovo draft) 4 ISOPP Standard of Practice Safe handling of Cytotoxics2006 (in revisione) 5 PIC/S guidelinespe (2014) 6 QUAPOS5 (2015) -ESOP 7 ICH HarmonisedTripartite Guideline Quality Risk Management Q9 NIOSH Alert: Preventing Occupational Exposures to Antineoplasticand Other Hazardous Drugs in Health Care Settings UNI EN ISO Classificazione del livello di pulizia dell aria (2015) 9 ISO Specifiche dei test e procedure di sorveglianza per rispettare i requisiti di ISO Procedure di esecuzione dei test
17 11 ISO Dispositivi separati (cappe, glovebox, isolatori, miniambienti ) 12 ISO Classificazioni di contaminazioni molecolari aereotrasportate TIPOLOGIA DEL SERVIZIO La qualità, la sicurezza e l efficacia delle terapie antitumorali e delle preparazioni da somministrare per via intravitreale, preparati obbligatoriamente sterili, dipendono dall accurata organizzazione e controllo costante e documentato di tutte le fasi del ciclo lavorativo. Esse sono garantite dalla corretta applicazione delle NBP, da ambienti idonei e dedicati, dall uso di attrezzature appropriate, da personale qualificato e addestrato, dalle procedure di pulizia e di disinfezione, dai monitoraggi ambientali. Per questo occorre attenersi rigorosamente a procedure e metodi di preparazione accuratamente definiti e convalidati a garanzia della qualità del prodotto allestito e della sicurezza degli operatori. La convalida dei processi di allestimento in asepsi consiste nelle seguenti attività: 1) verifica di performance dei locali e delle apparecchiature (cappe a flusso laminare verticale); 2) convalida dei processi di allestimento in asepsi. 1) Verifica di performance dei locali e delle apparecchiature (cappe a flusso laminare verticale): Scopo dell'attività è verificare: - la qualità microbiologica dell aria (a conferma finale della buona funzionalità degli impianti a seguito di interventi di qualifica/convalida e/o manutenzione); - la qualità microbiologica delle superfici prima dello svolgimento di attività produttive (indice della efficacia e della corretta applicazione delle procedure di pulizia e sanitizzazione in vigore). 2) Convalida dei processi di allestimento in asepsi Oltre ai controlli ambientali, dovrà esser fatta in contemporanea la convalida del processo in asepsi per l allestimento di farmaci citotossici e preparati intravitreali, utilizzando, come individuato dalle GMP- Annex 1, il test del media fill. I saggi di convalida dovranno simulare il più possibile il protocollo di preparazione asettica ed includere tutte le fasi critiche del processo di allestimento. A questo scopo la Ditta aggiudicataria eseguirà un controllo di biocontaminazione su un preparato allestito. 3) Campionamento e analisi per ricerca analitica contaminanti prima e dopo la preparazione Si richiede il campionamento e l analisi per la ricerca analitica prima e dopo la preparazione di: cappa per 3 punti, frigorifero, tavolo servitore, secchio rifiuti, maniglia porta d accesso alla camera bianca e, solo dopo la preparazione, citofono e sedia preparatore. ELENCO PROCEDURE RICHIESTE per l espletamento delle attività suindicate: Devono essere obbligatoriamente previsti eseguiti a pena di risoluzione del contratto: 1) Verifica della classe di concentrazione particellare dell aria : del locale in cui si eseguono gli allestimenti di farmaci antitumorali (Classe B GMP) e delle due Cappe a flusso laminare verticale (Classe A GMP)
18 eseguita semestralmente in stato di occupazione at rest mediante prelievo di campioni d aria e conteggio delle particelle con contatore particellare (n. 2 verifiche annuali per l ambiente e 2 verifiche annuali per ciascuna Cappa per un totale di 6 verifiche/anno; il numero dei punti da campionare relativamente al locale di allestimento sarà calcolato secondo la formula riportata nelle norme ISO ) 2) Verifica della classe di contaminazione microbiologica dell aria dell ambiente di Classe B GMP eseguita in stato di occupazione at rest sia per CBT (Carica Batterica Totale) che per CMT (Carica Micetica Totale) mediante campionamento biologico dell aria con campionatore; frequenza campionamenti ogni 90 giorni con numero minimo di cinque prelievi per tipologia di controllo (per un totale di 40 campionamenti l anno); 3) Verifica della classe di contaminazione microbiologica dell aria delle 2 Cappe a flusso laminare verticale (Classe A GMP) eseguita in stato di occupazione in operation sia per CBT (Carica Batterica Totale) che per CMT (Carica Micetica Totale) mediante campionamento biologico dell aria con campionatore; frequenza campionamenti ogni 90 giorni con numero minimo di tre prelievi per tipologia di controllo (per un totale di 48 campionamenti l anno); 4) Verifica della classe di contaminazione microbiologica delle superfici dell ambiente di Classe B GMP in stato di occupazione at rest sia per CBT (Carica Batterica Totale) che per CMT (Carica Micetica Totale); frequenza campionamenti ogni 90 giorni con numero minimo di cinque prelievi per tipologia di controllo nell ambiente di Classe B (per un totale di 40 campionamenti l anno); 5) Verifica della classe di contaminazione microbiologica delle superfici delle 2 Cappe a flusso laminare verticale (Classe A GMP) eseguita in stato di occupazione in operation sia per CBT (Carica Batterica Totale) che per CMT (Carica Micetica Totale); frequenza campionamenti ogni 90 giorni con un numero minimo di tre prelievi per tipologia di controllo per ciascuna Cappa (per un totale di 48 campionamenti l anno); 6) Analisi sterilità su prodotti allestiti finiti (soluzione all interno di sacca, di siringa e di elastomero); frequenza campionamenti ogni 90 giorni; dovrà essere monitorata la tecnica di allestimento di tutti e 5 i tecnici di laboratorio e infermieri preparatori assegnati all UFA, con minimo n. 3 campionamenti ad operatore di preparazioni con forme farmaceutiche diverse (per un totale di 15 campionamenti ogni 90 giorni); qualora una preparazione dovesse risultare non sterile deve essere prevista la possibilità di ripetere l analisi sulla preparazione allestita da quell operatore entro 15 giorni dalla consegna del relativo rapporto. 7) Campionamento e analisi per la ricerca analitica prima e dopo la preparazione di superfici: i principi attivi traccianti identificati dalla Linea Guida del 1999 sono i composti di coordinazione del platino, il 5-Fluorouracile e la Ciclofosfamide; tuttavia, se giustificato, è possibile modificare i traccianti in base alla capacità delle metodiche analitiche disponibili di rilevare l analita, l aggiornamento scientifico e il cambiamento dei principi attivi manipolati e la quantità manipolate dall UFA del tracciante proposto.
19 I punti da analizzare saranno: cappe per 3 punti, frigorifero, tavolo servitore, secchio rifiuti, maniglia porta d accesso alla camera bianca e, solo dopo la preparazione, citofono e sedia preparatore per un totale di 22 punti di analisi da ripetere annualmente con l elaborazione e consegna di una relazione tecnica. I metodi di campionatura e misurazione devono essere conformi alle indicazioni dell allegato XLI del D.lgv 81/2008 nel rispetto delle norme dell Annex 1 dell EU GMP, della ISO /2 e delle norme vigenti. Deve essere prevista la possibilità di effettuare un controllo analitico immediato qualora venissero a cambiare in modo sostanziale le condizioni di allestimento o si verificasse un incidente con contaminazione del locale di allestimento. Le procedure dovranno essere comprensive di materiali di consumo (terreni di coltura conformi alla Farmacopea Italiana e Europea, flaconi sterili e apirogeni per la dispensazione dei campioni finali) e attività di supporto, precisando che nulla verrà fornito da questa ASL. Tutti i controlli devono essere eseguiti secondo i requisiti previsti dalla normativa vigente con rilascio finale dei report comprovanti i risultati ottenuti e le metodiche impiegate. Nello specifico dovrà essere rilasciata la seguente documentazione: - Tabella della concentrazione particellare - Rapporto prove microbiologiche (laboratorio accreditato) - Rapporto analisi sterilità (laboratorio accreditato) - Elenco caratteristiche strumentazioni di prova - Certificati di taratura di strumenti - Considerazioni, commenti e suggerimenti tecnici. Lo strumento per la conta particellare utilizzato per le rilevazioni deve essere corredato di un certificato di taratura rilasciato da una struttura autorizzata e accreditata, copia del quale deve essere rilasciato insieme ai risultati del controllo. Il predetto certificato deve essere consegnato ai Responsabili dei Laboratori sopra descritti in occasione di ogni verifica, a pena di risoluzione del contratto. La consegna del rapporto deve avvenire entro 30 giorni dalla data dell intervento.
20 LOTTO 5 SERVIZIO DI CONVALIDA PER UOC MEDICINA NUCLEARE CIG B7A IMPORTO BIENNALE POSTO A BASE D ASTA ,00 DI CUI 700,00 non suscettibili di ribasso Le norme di buona preparazione dei Radiofarmaci, secondo le Linee Guida del Ministero della Salute, prevedono la convalida delle operazioni in asepsi mediante apposite procedure che utilizzano idonei terreni di coltura in sostituzione del prodotto, con frequenza semestrale (o maggiore, in rapporto all attività del laboratorio). Tale convalida deve essere effettuata da parte degli operatori addetti alla preparazione asettica, nello stesso modo e condizioni, nelle stesse postazioni di lavoro. Tutte le unità ripartite devono essere sottoposte al saggio di sterilità. La convalida deve dimostrare l assenza di unità contaminate. L introduzione di tali procedure in Medicina Nucleare è prevista da manuali di qualità redatti per la preparazione di radiofarmaci a base di kit e di Radiofarmaci con cellule analoghe marcate. La qualità microbiologica del Radiofarmaco è garantita dalla stretta osservanza delle suddette procedure, da ambienti dedicati, classificati e controllati, e da personale qualificato e certificato attraverso l esecuzione periodica di kit Media Fill. Per ognuno degli operatori addetti alle operazioni di preparazione è necessaria la procedura di convalidati mediante l esecuzione di Media Fill test. Ogni nuovo operatore deve eseguire almeno tre Media Fill run per poter essere convalidato ed inserito nel processo. Ogni operatore deve essere riconvalidato almeno annualmente mediante un Media Fill run. Analogamente è prevista dalle Norme sui Radiofarmaci (cap. 11) la qualificazione e il controllo degli ambienti e della strumentazione in uso dal punto di vista del rischio microbiologico. ELENCO PROCEDURE RICHIESTE Dovranno essere previsti obbligatoriamente: - Controlli microbiologici e particellari di n.2 celle isolatori di preparazione (cappe sterili per frazionamento di radiofarmaci) (semestrali): Comprensiva di risk assessment, scrittura ed esecuzione dei protocolli di IQ (Installation Qualification), OQ (Operative Qualification) e PQ (Performance Qualification), campionamenti particellari, campionamenti microbiologici e attività di supporto (incubazione, analisi e lettura dei campioni, documentazione e certificazione.
21 - Controlli microbiologici e particelllari di n. 1 ambiente classificato D (annuali). Procedura in qualifica in classe D (grado farmaceutico secondo GMP-EU) del locale in cui si eseguono marcature con cellule autologhe, comprensiva di risk assessment, scrittura ed esecuzione dei protocolli di IQ (Installation Qualification), OQ (Operative Qualification) e PQ Performance Qualification, campionamenti particellari, campionamenti microbiologici e attività di supporto (incubazione, analisi e lettura dei campioni, documentazione e certificazione. - Controllo Media Fill Radiofarmaci (semestrale) Il controllo Media Fill, semestrale dovrà riguardare le marcature dei Radiofarmaci le procedure dovranno essere comprensive di materiali di consumo (terreni di coltura conformi alla Farmacopea italiana e Europea, flaconi sterili e apirogeni per la dispensazione dei campioni finali), attività di supporto (istruzioni sulla sequenza operativa, modalità di consegna e conservazione dei campioni, incubazione, analisi e lettura dei campioni, documentazione e certificazione. - Controllo Media Fill marcature cellulare (semestrale). Il controllo Media Fill, semestrale dovrà riguardare le marcature cellulari. Il numero degli operatori da sottoporre ai controlli Media Fill verrà comunicato tempestivamente. Il controllo per le marcature cellulari potrà essere richiesto qualora venga riattivata la metodica durante la durata del contratto. Anche in quest ultimo caso si provvederà tempestivamente a fornire il numero degli operatori coinvolti. - Controllo ventilazione del locale classificato. Per tale controllo devono essere compresi i materiali di consumo (piastre, campionatori ecc) e attività di supporto (Istruzioni sulla sequenza operativa, modalità di consegna e conservazione dei campioni incubazioni, analisi e lettura dei campioni, documentazione e certificazione). Tutti i controlli devono essere eseguiti secondo i requisiti previsti dalla normativa con rilascio finale dei report comprovanti i risultati ottenuti. ELENCO PROCEDURE RICHIESTE Le procedure verranno eseguite secondo quanto indicato in riferimento ai locali e alle strumentazioni sopra specificate
Quesito n. 1. UOC Interaziendale ASL Latina/ASL Frosinone PROVVEDITORATO
 UOC Interaziendale ASL Latina/ASL Frosinone PROVVEDITORATO Tel: 0773/6556470 Fax: 0773/6553361 e-mail: v.poerio@ausl.latina.it pec:protocolloaoo01@pec.ausl.latina.it Latina, lì GARA EUROPEA A PROCEDURA
UOC Interaziendale ASL Latina/ASL Frosinone PROVVEDITORATO Tel: 0773/6556470 Fax: 0773/6553361 e-mail: v.poerio@ausl.latina.it pec:protocolloaoo01@pec.ausl.latina.it Latina, lì GARA EUROPEA A PROCEDURA
CONVALIDA DELLE CAPPE A FLUSSO LAMINARE
 Sessione 6 La Convalida degli ambienti nell eye-banking Moderatori: G. Mantegna P. Santoro CONVALIDA DELLE CAPPE A FLUSSO LAMINARE Maria Teresa Vicentini Dirigente Biologo c/o UOSD Banca degli Occhi dell
Sessione 6 La Convalida degli ambienti nell eye-banking Moderatori: G. Mantegna P. Santoro CONVALIDA DELLE CAPPE A FLUSSO LAMINARE Maria Teresa Vicentini Dirigente Biologo c/o UOSD Banca degli Occhi dell
Relatore: Carolina Bertipaglia Farmacia Clinica Policlinico S.Orsola-Malpighi PharmacOn, Firenze Ottobre 2017
 TEST MEDIA FILL: CONVALIDA MICROBIOLOGICA DEL PROCESSO DI ALLESTIMENTO CHEMIOTERAPICI PRESSO IL CENTRO COMPOUNDING DELLA FARMACIA DEL POLICLINICO S. ORSOLA-MALPIGHI DI BOLOGNA Referente del progetto: Dr.ssa
TEST MEDIA FILL: CONVALIDA MICROBIOLOGICA DEL PROCESSO DI ALLESTIMENTO CHEMIOTERAPICI PRESSO IL CENTRO COMPOUNDING DELLA FARMACIA DEL POLICLINICO S. ORSOLA-MALPIGHI DI BOLOGNA Referente del progetto: Dr.ssa
Requisiti ambientali e controlli di qualità ambientale
 Cap 1 Requisiti ambientali e controlli di qualità ambientale Aldo Volpes Centro Andros s.r.l. Unità di Medicina della Riproduzione, Palermo 1 I requisiti minimi, per quanto riguarda la qualità dell aria,
Cap 1 Requisiti ambientali e controlli di qualità ambientale Aldo Volpes Centro Andros s.r.l. Unità di Medicina della Riproduzione, Palermo 1 I requisiti minimi, per quanto riguarda la qualità dell aria,
primaria importanza, specie quando ci si trova ad affrontare realtà a stretto contatto con la vita.
 } IL bisogno di ricerca e garanzia di sicurezza rivestono oggi un ruolo di primaria importanza, specie quando ci si trova ad affrontare realtà a stretto contatto con la vita. } Gli obbiettivi della Technodal,
} IL bisogno di ricerca e garanzia di sicurezza rivestono oggi un ruolo di primaria importanza, specie quando ci si trova ad affrontare realtà a stretto contatto con la vita. } Gli obbiettivi della Technodal,
La prevenzione della contaminazione nell industria farmaceutica
 La prevenzione della contaminazione nell industria farmaceutica Dott. Valeriano Ciociola Quality Assurance & Regulatory Specialist EU GMP: CAPITOLO 3 PREMISES AND EQUIPMENT Il Capitolo 3 dà informazioni
La prevenzione della contaminazione nell industria farmaceutica Dott. Valeriano Ciociola Quality Assurance & Regulatory Specialist EU GMP: CAPITOLO 3 PREMISES AND EQUIPMENT Il Capitolo 3 dà informazioni
Sistema di monitoraggio particellare e microbiologico in continuo : esperienza applicativa in un laboratorio di tessuti oculari
 VI Corso Genova, 21 aprile 2012 Sistema di monitoraggio particellare e microbiologico in continuo : esperienza applicativa in un laboratorio di tessuti oculari Fondazione Banca degli Occhi del Veneto ONLUS
VI Corso Genova, 21 aprile 2012 Sistema di monitoraggio particellare e microbiologico in continuo : esperienza applicativa in un laboratorio di tessuti oculari Fondazione Banca degli Occhi del Veneto ONLUS
Servizio Sanitario Nazionale Regione Piemonte
 Azienda Ospedaliera Ordine Mauriziano di Torino Deliberazione n. 293 del 06/05/2014 Oggetto: PRESIDIO OSPEDALIERO UMBERTO I DI TORINO. AFFIDAMENTO DEL SERVIZIO DI CONVALIDA DEI PROCESSI DI ALLESTIMENTO
Azienda Ospedaliera Ordine Mauriziano di Torino Deliberazione n. 293 del 06/05/2014 Oggetto: PRESIDIO OSPEDALIERO UMBERTO I DI TORINO. AFFIDAMENTO DEL SERVIZIO DI CONVALIDA DEI PROCESSI DI ALLESTIMENTO
Controllo qualità emocomponenti
 L utilizzo degli emocomponenti ad uso non trasfusionale alla luce della recente normativa nazionale e regionale Bologna 18/09/2017 Controllo qualità emocomponenti 1 Dr.ssa Veronica Roverini (TSLB) Controlli
L utilizzo degli emocomponenti ad uso non trasfusionale alla luce della recente normativa nazionale e regionale Bologna 18/09/2017 Controllo qualità emocomponenti 1 Dr.ssa Veronica Roverini (TSLB) Controlli
GMP per RADIOFARMACI e AGENTI DIAGNOSTICI
 GMP per RADIOFARMACI e AGENTI DIAGNOSTICI PERCHÉ LE GMP? Perché sono un vincolo legislativo per i radiofarmaci e gli agenti diagnostici prodotti in regime galenico. Le normative vigenti, per utilizzo in
GMP per RADIOFARMACI e AGENTI DIAGNOSTICI PERCHÉ LE GMP? Perché sono un vincolo legislativo per i radiofarmaci e gli agenti diagnostici prodotti in regime galenico. Le normative vigenti, per utilizzo in
Presentazione dei nuovi Standard Tecnici di Galenica Sterile Oncologica
 Presentazione dei nuovi Standard Tecnici di Galenica Sterile Oncologica Coord. Scientifica: Emanuela Omodeo Salè GDL: Costantino Jemos; Alicia Tavella; Valentina Di Iorio; Silvia Adami; Marialuisa Giordano;
Presentazione dei nuovi Standard Tecnici di Galenica Sterile Oncologica Coord. Scientifica: Emanuela Omodeo Salè GDL: Costantino Jemos; Alicia Tavella; Valentina Di Iorio; Silvia Adami; Marialuisa Giordano;
Cosa si intende per validazione o qualifica?
 Cosa si intende per validazione o qualifica? Validazione (o qualifica nel caso di apparecchiature o di ambienti) significa la produzione di prove documentate, in grado di garantire con un elevato livello
Cosa si intende per validazione o qualifica? Validazione (o qualifica nel caso di apparecchiature o di ambienti) significa la produzione di prove documentate, in grado di garantire con un elevato livello
27 aprile 2010 Azienda Ospedaliera S. Gerardo - Monza
 Impianti di ventilazione e condizionamento a contaminazione controllata (VCCC) per il blocco operatorio Progettazione installazione, messa in marcia, qualifica, gestione e manutenzione 27 aprile 2010 Azienda
Impianti di ventilazione e condizionamento a contaminazione controllata (VCCC) per il blocco operatorio Progettazione installazione, messa in marcia, qualifica, gestione e manutenzione 27 aprile 2010 Azienda
QUALITA E SICUREZZA NELLE BIOBANCHE DI CELLULE E TESSUTI UMANI PER USO CLINICO
 UNIVERSITA DELL AQUILA Corso di perfezionamento DIPARTIMENTO DI MEDICINA CLINICA, SANITA PUBBLICA, SCIENZE DELLA VITA E DELL AMBIENTE QUALITA E SICUREZZA NELLE BIOBANCHE DI CELLULE E TESSUTI UMANI PER
UNIVERSITA DELL AQUILA Corso di perfezionamento DIPARTIMENTO DI MEDICINA CLINICA, SANITA PUBBLICA, SCIENZE DELLA VITA E DELL AMBIENTE QUALITA E SICUREZZA NELLE BIOBANCHE DI CELLULE E TESSUTI UMANI PER
...Fare meglio se possibile ed è sempre possibile... Mirco Pellacani (Amministratore)
 COMPANY PROFILE Aspiriamo a diventare una società leader in tutti i segmenti di mercato in cui operiamo e a costruire una reputazione senza confronti, grazie agli effetti positivi del nostro lavoro. La
COMPANY PROFILE Aspiriamo a diventare una società leader in tutti i segmenti di mercato in cui operiamo e a costruire una reputazione senza confronti, grazie agli effetti positivi del nostro lavoro. La
CONVALIDA DEL PROCESSO IN CONDIZIONI DI ASEPSI
 pag. 1 di 10 Redatto da : Supervisore del processo/convalida : dr.ssa Gabriella Ferraro dr.ssa Gabriella Ferraro Farmacista Responsabile della Convalida: dr.ssa Gabriella Ferraro Visionato da : dr.ssa
pag. 1 di 10 Redatto da : Supervisore del processo/convalida : dr.ssa Gabriella Ferraro dr.ssa Gabriella Ferraro Farmacista Responsabile della Convalida: dr.ssa Gabriella Ferraro Visionato da : dr.ssa
STOCCAGGIO E CONSERVAZIONE
 Pagina 1 di 5 STOCCAGGIO E CONSERVAZIONE Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Martino Responsabile UFA Dott.ssa Maria Teresa Verifica Perricone Direttore U.O.C. Farmacia Dr. Emanuele
Pagina 1 di 5 STOCCAGGIO E CONSERVAZIONE Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Martino Responsabile UFA Dott.ssa Maria Teresa Verifica Perricone Direttore U.O.C. Farmacia Dr. Emanuele
ALLEGATOA alla Dgr n. 12 del 11 gennaio 2011 pag. 1 /9
 ALLEGATOA alla Dgr n. 12 del 11 gennaio 2011 pag. 1 /9 ABBREVIAZIONI Azienda Sanitaria: AS Banche di Sangue Cordonale: BSC Sangue Cordonale: SC Punti Nascita: PN Unità di sangue cordonale: USC Donazioni
ALLEGATOA alla Dgr n. 12 del 11 gennaio 2011 pag. 1 /9 ABBREVIAZIONI Azienda Sanitaria: AS Banche di Sangue Cordonale: BSC Sangue Cordonale: SC Punti Nascita: PN Unità di sangue cordonale: USC Donazioni
CONVALIDA DI PROCESSO E QUALIFICA DI APPARECCHIATURE E STRUMENTI
 CONVALIDA DI PROCESSO E QUALIFICA DI APPARECCHIATURE E STRUMENTI Alessandra Bassi Servizio di Immunoematologia e Medicina Trasfusionale Servizio di Immunoematologia e Medicina Trasfusionale Area Metropolitana
CONVALIDA DI PROCESSO E QUALIFICA DI APPARECCHIATURE E STRUMENTI Alessandra Bassi Servizio di Immunoematologia e Medicina Trasfusionale Servizio di Immunoematologia e Medicina Trasfusionale Area Metropolitana
Principi Attivi ad Alta Attività materie prime che hanno dosaggi molto bassi in genere inferiori a 10 mg
 1 Principi Attivi ad Alta Attività materie prime che hanno dosaggi molto bassi in genere inferiori a 10 mg La loro preparazione, lavorazione e utilizzo implica la soluzione di problemi di contaminazione
1 Principi Attivi ad Alta Attività materie prime che hanno dosaggi molto bassi in genere inferiori a 10 mg La loro preparazione, lavorazione e utilizzo implica la soluzione di problemi di contaminazione
QUALIFICA E CONVALIDA DI AMBIENTI E ATTREZZATURE AMBIENTI E LABORATORI PMA - FPR AUSL DELLA ROMAGNA CAPITOLATO TECNICO
 QUALIFICA E CONVALIDA DI AMBIENTI E ATTREZZATURE AMBIENTI E LABORATORI PMA - FPR AUSL DELLA ROMAGNA CAPITOLATO TECNICO OGGETTO DELL APPALTO L Appalto ha per oggetto il servizio di qualifica e convalida
QUALIFICA E CONVALIDA DI AMBIENTI E ATTREZZATURE AMBIENTI E LABORATORI PMA - FPR AUSL DELLA ROMAGNA CAPITOLATO TECNICO OGGETTO DELL APPALTO L Appalto ha per oggetto il servizio di qualifica e convalida
30 settembre 5 ottobre Servizio di Immunoematologia e Medicina Trasfusionale Vigevano
 30 settembre 5 ottobre 2015 Servizio di Immunoematologia e Medicina Trasfusionale Vigevano REQUISITI STRUTTURALI Area Accettazione Ambulatorio REQUISITI STRUTTURALI Sala prelievo Area Ristoro
30 settembre 5 ottobre 2015 Servizio di Immunoematologia e Medicina Trasfusionale Vigevano REQUISITI STRUTTURALI Area Accettazione Ambulatorio REQUISITI STRUTTURALI Sala prelievo Area Ristoro
MONITORAGGIO DEL SERVIZIO: CONTROLLO DI PROCESSO O CONTROLLO DI RISULTATO
 MONITORAGGIO DEL SERVIZIO: CONTROLLO DI PROCESSO O CONTROLLO DI RISULTATO Gianfranco Finzi Nazzareno Manoni Direzione Medica Ospedaliera Azienda Ospedaliero-Universitaria di Bologna Policlinico Sant Orsola-Malpighi
MONITORAGGIO DEL SERVIZIO: CONTROLLO DI PROCESSO O CONTROLLO DI RISULTATO Gianfranco Finzi Nazzareno Manoni Direzione Medica Ospedaliera Azienda Ospedaliero-Universitaria di Bologna Policlinico Sant Orsola-Malpighi
Fabbricazione Industriale dei Medicinali
 Universita degli Studi di Milano Corso di Laurea in Chimica e Tecnologia Farmaceutiche Fabbricazione Industriale dei Medicinali slides Dott. Vittorino Ravelli Prof. Andrea Gazzaniga ORGANIZZAZIONE AZIENDALE
Universita degli Studi di Milano Corso di Laurea in Chimica e Tecnologia Farmaceutiche Fabbricazione Industriale dei Medicinali slides Dott. Vittorino Ravelli Prof. Andrea Gazzaniga ORGANIZZAZIONE AZIENDALE
PROCEDURE OPERATIVE CONTROLLO STERILITA FARMACI ANTIBLASTICI
 Pagina 1 di 7 Scopo e campo di applicazione Diagramma di flusso Descrizione attività Procedura analitica Emissione rapporto di prova ed archiviazione Riferimenti LISTA DI DISTRIBUZIONE Operazione Nome-COGNOME
Pagina 1 di 7 Scopo e campo di applicazione Diagramma di flusso Descrizione attività Procedura analitica Emissione rapporto di prova ed archiviazione Riferimenti LISTA DI DISTRIBUZIONE Operazione Nome-COGNOME
PIANO DI CONVALIDA SIMT-IO 059 PROCESSO DI CONSERVAZIONE DEGLI EMOCOMPONENTI A QUALUNQUE USO SIANO DESTINATI
 Prima Stesura Redattori: Gasbarri, Rizzo Data: 08/0/04 PIANO DI CONVALIDA SIMT-IO 059 PROCESSO DI CONSERVAZIONE DEGLI EMOCOMPONENTI A QUALUNQUE USO SIANO DESTINATI Indice DESCRIZIONE ATTIVITÀ... RESPONSABILITA...
Prima Stesura Redattori: Gasbarri, Rizzo Data: 08/0/04 PIANO DI CONVALIDA SIMT-IO 059 PROCESSO DI CONSERVAZIONE DEGLI EMOCOMPONENTI A QUALUNQUE USO SIANO DESTINATI Indice DESCRIZIONE ATTIVITÀ... RESPONSABILITA...
AZIENDA OSPEDALIERA UNIVERSITARIA SENESE
 Allegato N. 2 alla Determinazione n 18 del 09.01.2014 AZIENDA OSPEDALIERA UNIVERSITARIA SENESE AVVISO INTERNO PER L INDIVIDUAZIONE DI N. 1 DIRIGENTE BIOLOGO DA ASSEGNARE ALLA U.O.S.A CENTRO TRAPIANTI E
Allegato N. 2 alla Determinazione n 18 del 09.01.2014 AZIENDA OSPEDALIERA UNIVERSITARIA SENESE AVVISO INTERNO PER L INDIVIDUAZIONE DI N. 1 DIRIGENTE BIOLOGO DA ASSEGNARE ALLA U.O.S.A CENTRO TRAPIANTI E
L UNITA FARMACI ANTIBLASTICI NELLA ASL3 GENOVESE Dott.ssa Cristina Bianchi Farmacista Ospedaliera Ornella Gallone Coordinatrice Infermieristica CONVEG
 L UNITA FARMACI ANTIBLASTICI NELLA ASL3 GENOVESE Dott.ssa Cristina Bianchi Farmacista Ospedaliera Ornella Gallone Coordinatrice Infermieristica CONVEGNO REGIONALE C.I.D.: L EVOLZIONE DEL SISTEMA E DELLE
L UNITA FARMACI ANTIBLASTICI NELLA ASL3 GENOVESE Dott.ssa Cristina Bianchi Farmacista Ospedaliera Ornella Gallone Coordinatrice Infermieristica CONVEGNO REGIONALE C.I.D.: L EVOLZIONE DEL SISTEMA E DELLE
CAPITOLATO TECNICO CIG N C19
 Via Paderno, 21-24068 SERIATE (BG) Tel. 035/3063771 Telefax 035/3063708 C.F. e P.IVA n 02585160167 E-mail: gare.provveditorato@bolognini.bg.it Internet: www.bolognini.bg.it CAPITOLATO TECNICO PROCEDURA
Via Paderno, 21-24068 SERIATE (BG) Tel. 035/3063771 Telefax 035/3063708 C.F. e P.IVA n 02585160167 E-mail: gare.provveditorato@bolognini.bg.it Internet: www.bolognini.bg.it CAPITOLATO TECNICO PROCEDURA
Informazione Formazione e Addestramento del Personale
 Società Italiana Banche degli Occhi Torino, 10 ottobre 2009 IV Corso di Formazione Informazione Formazione e Addestramento del Personale Fondazione Banca degli Occhi del Veneto Normativa di riferimento
Società Italiana Banche degli Occhi Torino, 10 ottobre 2009 IV Corso di Formazione Informazione Formazione e Addestramento del Personale Fondazione Banca degli Occhi del Veneto Normativa di riferimento
CAPITOLATO TECNICO PER LA FORNITURA CHIAVI IN MANO DI ATTREZZATURE PER MANIPOLAZIONE RADIOFARMACI. Caratteristiche Tecniche
 SERVIZIO SANITARIO NAZIONALE REGIONE SICILIANA AZIENDA SANITARIA PROVINCIALE AGRIGENTO DISTRETTO AG 1 OSPEDALE SAN GIOVANNI DI DIO Contrada Consolida - 92100 AGRIGENTO Codice Fiscale e Partita IVA 02570930848
SERVIZIO SANITARIO NAZIONALE REGIONE SICILIANA AZIENDA SANITARIA PROVINCIALE AGRIGENTO DISTRETTO AG 1 OSPEDALE SAN GIOVANNI DI DIO Contrada Consolida - 92100 AGRIGENTO Codice Fiscale e Partita IVA 02570930848
GMP PER MEDICINALI DA TERAPIE AVANZATE
 GMP PER MEDICINALI DA TERAPIE AVANZATE LE TERAPIE AVANZATE I medicinali per Terapie Avanzate si basano su processi produttivi centrati su varie biomolecole prodotte mediante trasferimento di geni e/o cellule
GMP PER MEDICINALI DA TERAPIE AVANZATE LE TERAPIE AVANZATE I medicinali per Terapie Avanzate si basano su processi produttivi centrati su varie biomolecole prodotte mediante trasferimento di geni e/o cellule
CONVALIDA DELLA STRUMENTAZIONE. Rosanna Carroccia Banca Cornee Emilia Romagna SIBO 26 Maggio 2018
 CONVALIDA DELLA STRUMENTAZIONE Rosanna Carroccia Banca Cornee Emilia Romagna SIBO 26 Maggio 2018 NORMATIVA E LG CNT DIRETTIVA 2006/86/CE Tutte le attrezzature e i dispositivi tecnici critici devono essere
CONVALIDA DELLA STRUMENTAZIONE Rosanna Carroccia Banca Cornee Emilia Romagna SIBO 26 Maggio 2018 NORMATIVA E LG CNT DIRETTIVA 2006/86/CE Tutte le attrezzature e i dispositivi tecnici critici devono essere
Il Farmaco Gas Medicinale: le Responsabilità del Farmacista Ospedaliero
 Il Farmaco Gas Medicinale: le Responsabilità del Farmacista Ospedaliero Ing Vittorio Nistrio Gruppo di Lavoro 9G - Farmacopea Europea Cagliari, 7 ottobre 2010 1 Ruolo e Responsabilità del Farmacista ospedaliero
Il Farmaco Gas Medicinale: le Responsabilità del Farmacista Ospedaliero Ing Vittorio Nistrio Gruppo di Lavoro 9G - Farmacopea Europea Cagliari, 7 ottobre 2010 1 Ruolo e Responsabilità del Farmacista ospedaliero
Giornata di formazione reciproca presso Banca di Lucca: considerazioni finali. Dr. Claudio Giannarini
 V Corso SIBO Palazzo Ducale Lucca 6 novembre 2010 Giornata di formazione reciproca presso Banca di Lucca: considerazioni finali Dr. Claudio Giannarini L idea iniziale è nata per avere crediti ECM sulle
V Corso SIBO Palazzo Ducale Lucca 6 novembre 2010 Giornata di formazione reciproca presso Banca di Lucca: considerazioni finali Dr. Claudio Giannarini L idea iniziale è nata per avere crediti ECM sulle
Disposizioni relative ai requisiti di qualità e sicurezza del sangue e degli emocomponenti.
 Supplemento ordinario alla Gazzetta Ufficiale n. 300 del 28 dicembre 2015 - Serie generale Spediz. abb. post. 45% - art. - 1, art. comma 2, comma 1 20/b Legge 27-02-2004, 23-12-1996, n. n. 46-662 Filiale
Supplemento ordinario alla Gazzetta Ufficiale n. 300 del 28 dicembre 2015 - Serie generale Spediz. abb. post. 45% - art. - 1, art. comma 2, comma 1 20/b Legge 27-02-2004, 23-12-1996, n. n. 46-662 Filiale
PROPOSTA CONVENZIONE TRA LA GUACCI SERVICE E FEDERFARMA SALERNO
 PROPOSTA CONVENZIONE TRA LA GUACCI SERVICE E FEDERFARMA SALERNO Spett.le FEDERFARMA SALERNO c.a. PRESIDENTE LEONARDO ACCARINO Nola, 22/05/2012 Protocollo convenzione n. 02 GIUGNO 2012 Validità biennio
PROPOSTA CONVENZIONE TRA LA GUACCI SERVICE E FEDERFARMA SALERNO Spett.le FEDERFARMA SALERNO c.a. PRESIDENTE LEONARDO ACCARINO Nola, 22/05/2012 Protocollo convenzione n. 02 GIUGNO 2012 Validità biennio
CONTROLLO MICROBIOLOGICO AMBIENTALE NELLE SALE OPERATORIE
 Ident.Doc.PRO.8.2.3 Rev. 01 del 10.01.11 Pag 1 di 11 CONTROLLO MICROBIOLOGICO AMBIENTALE NELLE SALE OPERATORIE Procedura REV. DATA REV. DATA REV. DATA 8.2.3 00 10.01.09 01 10.01.11 RGQ DG DG FUNZ. FIRMA
Ident.Doc.PRO.8.2.3 Rev. 01 del 10.01.11 Pag 1 di 11 CONTROLLO MICROBIOLOGICO AMBIENTALE NELLE SALE OPERATORIE Procedura REV. DATA REV. DATA REV. DATA 8.2.3 00 10.01.09 01 10.01.11 RGQ DG DG FUNZ. FIRMA
Azienda sanitaria Provinciale Enna PROCESSO DI GESTIONE DELLA TERAPIA ANTITUMORALE IN UFA ONCOLOGIA EMATOLOGIA APPROVIGIONAMENTO
 Pagina 1 di 5 APPROVIGIONAMENTO Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Martino Responsabile UFA Dott. Giuseppe Scollo Farmacista Borsista Dott.ssa Maria Teresa Verifica Perricone
Pagina 1 di 5 APPROVIGIONAMENTO Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Martino Responsabile UFA Dott. Giuseppe Scollo Farmacista Borsista Dott.ssa Maria Teresa Verifica Perricone
La raccolta del sangue ed emocomponenti alla luce dei requisiti minimi per le Strutture trasfusionali e le Unità di raccolta
 La raccolta del sangue ed emocomponenti alla luce dei requisiti minimi per le Strutture trasfusionali e le Unità di raccolta Realtà e prospettive nelle Regioni centro-meridionali S. Giovanni Rotondo, 7
La raccolta del sangue ed emocomponenti alla luce dei requisiti minimi per le Strutture trasfusionali e le Unità di raccolta Realtà e prospettive nelle Regioni centro-meridionali S. Giovanni Rotondo, 7
XI Corso Nazionale Società Italiana Banche degli Occhi
 XI Corso Nazionale Società Italiana Banche degli Occhi 01 Aprile 2017 - Sede congressuale Circolo Sersanti Imola Validazione dei liquidi Home Made Dr. Claudio Giannarini Centro Conservazione Cornee Piero
XI Corso Nazionale Società Italiana Banche degli Occhi 01 Aprile 2017 - Sede congressuale Circolo Sersanti Imola Validazione dei liquidi Home Made Dr. Claudio Giannarini Centro Conservazione Cornee Piero
REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI PER L ESECUZIONE DI PROCEDURE DI AFERESI TERAPEUTICA
 Allegato B/1) REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI PER L ESECUZIONE DI PROCEDURE DI AFERESI TERAPEUTICA PER IL DIPARTIMENTO INTERAZIENDALE DI MEDICINA TRASFUSIONALE DELLA
Allegato B/1) REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI PER L ESECUZIONE DI PROCEDURE DI AFERESI TERAPEUTICA PER IL DIPARTIMENTO INTERAZIENDALE DI MEDICINA TRASFUSIONALE DELLA
PROCEDURA GP GP 00. DATA REDAZIONE FIRMA Nome e Cognome. DATA VERIFICA FIRMA Nome e Cognome. DATA APPROVAZIONE FIRMA Nome e Cognome
 Pagina 1 di 10 Documento Codice documento GP 00 DATA REDAZIONE FIRMA Nome e Cognome DATA VERIFICA FIRMA Nome e Cognome DATA APPROVAZIONE FIRMA Nome e Cognome Pagina 2 di 10 1. Generalità... 3 1.1 Scopo
Pagina 1 di 10 Documento Codice documento GP 00 DATA REDAZIONE FIRMA Nome e Cognome DATA VERIFICA FIRMA Nome e Cognome DATA APPROVAZIONE FIRMA Nome e Cognome Pagina 2 di 10 1. Generalità... 3 1.1 Scopo
Preparazione di una sacca-paziente a partire da flaconi (polveri liofilizzate)
 Istruzione Operativa Preparazione di una sacca-paziente a partire da flaconi (polveri liofilizzate) I_ PGS-DSA-7-01_04 ed. 0 rev. 00 17 giugno 2014 originale X copia controllata informatica copia controllata
Istruzione Operativa Preparazione di una sacca-paziente a partire da flaconi (polveri liofilizzate) I_ PGS-DSA-7-01_04 ed. 0 rev. 00 17 giugno 2014 originale X copia controllata informatica copia controllata
SCHEMA 0 STORIA. Schema certificativo CP DOCUMENTI ESTERNI DI RIFERIMENTO
 SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei profilati cavi di acciai non legati e a grano fine per impieghi strutturali di cui alle norme UNI
SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei profilati cavi di acciai non legati e a grano fine per impieghi strutturali di cui alle norme UNI
1. Introduzione. Negli ultimi anni il mondo scientifico ha riposto particolare attenzione verso la
 1. Introduzione Negli ultimi anni il mondo scientifico ha riposto particolare attenzione verso la ricerca e lo sviluppo di una nuova categoria di farmaci biologici, basati su materiale genetico, cellule
1. Introduzione Negli ultimi anni il mondo scientifico ha riposto particolare attenzione verso la ricerca e lo sviluppo di una nuova categoria di farmaci biologici, basati su materiale genetico, cellule
Preparazione di una pompa infusionale da flaconi (liquido concentrato per infusione)
 Istruzione Operativa Preparazione di una pompa infusionale da flaconi (liquido concentrato per infusione) I_ PGS-DSA-7-01_08 ed. 0 rev. 00 17 giugno 2014 originale X informatica cartacea copia non controllata
Istruzione Operativa Preparazione di una pompa infusionale da flaconi (liquido concentrato per infusione) I_ PGS-DSA-7-01_08 ed. 0 rev. 00 17 giugno 2014 originale X informatica cartacea copia non controllata
Corso di Laurea Magistrale in Chimica e Tecnologia Farmaceutiche E25
 Sezione di Tecnologia e Legislazione Farmaceutiche Maria Edvige Sangalli Corso di Laurea Magistrale in Chimica e Tecnologia Farmaceutiche E25 Fabbricazione Industriale dei Medicinali 4 CFU Prof. Andrea
Sezione di Tecnologia e Legislazione Farmaceutiche Maria Edvige Sangalli Corso di Laurea Magistrale in Chimica e Tecnologia Farmaceutiche E25 Fabbricazione Industriale dei Medicinali 4 CFU Prof. Andrea
Gestione dei Farmaci Off-Label
 Pagina 1 di 6 Gestione dei Farmaci Off-Label Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Verifica Approvazione Martino Responsabile UFA Dott.ssa Maria Teresa Perricone Direttore U.O.C.
Pagina 1 di 6 Gestione dei Farmaci Off-Label Nome/Funzione Data Firma Dott.ssa Giuseppa Cinzia Di Redazione Verifica Approvazione Martino Responsabile UFA Dott.ssa Maria Teresa Perricone Direttore U.O.C.
L Ospedale nel Terzo Millennio 17/18/19 maggio 2006 Fondazione Ferrero
 ASL 18 ALBA-BRA CONVEGNO INTERNAZIONALE L Ospedale nel Terzo Millennio 17/18/19 maggio 2006 Fondazione Ferrero LE NORME SUI BLOCCHI OPERATORI Dott. Ing. Cesare Taddia - Progettisti Associati Tecnarc S.r.l.
ASL 18 ALBA-BRA CONVEGNO INTERNAZIONALE L Ospedale nel Terzo Millennio 17/18/19 maggio 2006 Fondazione Ferrero LE NORME SUI BLOCCHI OPERATORI Dott. Ing. Cesare Taddia - Progettisti Associati Tecnarc S.r.l.
Corso di Laurea Magistrale in Chimica e Tecnologia Farmaceutiche E25. Fabbricazione Industriale dei Medicinali 4 CFU
 Corso di Laurea Magistrale in Chimica e Tecnologia Farmaceutiche E25 Qualifica, taratura e manutenzione Persona Qualificata imo- Prof. Andrea Gazzaniga QUALIFICA e CONVALIDA 2 QUALIFICA e CONVALIDA ASPETTI
Corso di Laurea Magistrale in Chimica e Tecnologia Farmaceutiche E25 Qualifica, taratura e manutenzione Persona Qualificata imo- Prof. Andrea Gazzaniga QUALIFICA e CONVALIDA 2 QUALIFICA e CONVALIDA ASPETTI
Organizzazione di un Centro di PMA in base alle norme vigenti. SC di Ostetricia e Ginecologia Arcispedale S. Maria Nuova Reggio Emilia
 Organizzazione di un Centro di PMA in base alle norme vigenti MT Villani SC di Ostetricia e Ginecologia Arcispedale S. Maria Nuova Reggio Emilia Indice Riferimenti giuridici europei e italiani Documento
Organizzazione di un Centro di PMA in base alle norme vigenti MT Villani SC di Ostetricia e Ginecologia Arcispedale S. Maria Nuova Reggio Emilia Indice Riferimenti giuridici europei e italiani Documento
Produzione emocomponenti e tracciabilità
 Produzione emocomponenti e tracciabilità Dr.ssa Annarita Cenacchi SIMT IOR AMBO Bologna, 18 settembre 2017, Sala Vasari IOR L utilizzo degli emocomponenti ad uso non trasfusionale alla luce della recente
Produzione emocomponenti e tracciabilità Dr.ssa Annarita Cenacchi SIMT IOR AMBO Bologna, 18 settembre 2017, Sala Vasari IOR L utilizzo degli emocomponenti ad uso non trasfusionale alla luce della recente
Genova 14/17 febbraio 2012 Valutazione di idoneità igienico sanitaria degli impianti aeraulici
 Genova 14/17 febbraio 2012 Valutazione di idoneità igienico sanitaria degli impianti aeraulici IRCCS A.O.U. SAN MARTINO IST di Genova: gli impianti aeraulici nelle aree ospedaliere: monitoraggio, manutenzione
Genova 14/17 febbraio 2012 Valutazione di idoneità igienico sanitaria degli impianti aeraulici IRCCS A.O.U. SAN MARTINO IST di Genova: gli impianti aeraulici nelle aree ospedaliere: monitoraggio, manutenzione
Oggetto della fornitura: Sistema composto da prodotti per la processazione in strato sottile e dotazione in service della relativa strumentazione.
 Oggetto della fornitura: Sistema composto da prodotti per la processazione in strato sottile e dotazione in service della relativa strumentazione. Caratteristiche della fornitura Sistema ad alta efficienza,
Oggetto della fornitura: Sistema composto da prodotti per la processazione in strato sottile e dotazione in service della relativa strumentazione. Caratteristiche della fornitura Sistema ad alta efficienza,
Le norme di accreditamento e l'applicazione, stato dell'arte e prospettive di miglioramento ed implementazione
 Dr.ssa Ivana Menichini Le norme di accreditamento e l'applicazione, stato dell'arte e prospettive di miglioramento ed implementazione REQUISITI Il quadro normativo europeo del sistema sangue: sangue ed
Dr.ssa Ivana Menichini Le norme di accreditamento e l'applicazione, stato dell'arte e prospettive di miglioramento ed implementazione REQUISITI Il quadro normativo europeo del sistema sangue: sangue ed
VERIFICA IN CAMPO Sistemi di Monitoraggio in Continuo delle Emissioni (AMS/SME) IAR - LINEARITÀ - TARATURA POLVERIMETRO - QAL2 - AST NOTA INFORMATIVA
 VERIFICA IN CAMPO Sistemi di Monitoraggio in Continuo delle Emissioni (AMS/SME) IAR - LINEARITÀ - TARATURA POLVERIMETRO - QAL2 - AST NOTA INFORMATIVA Assicurazione Qualità Sistemi di Monitoraggio in Continuo
VERIFICA IN CAMPO Sistemi di Monitoraggio in Continuo delle Emissioni (AMS/SME) IAR - LINEARITÀ - TARATURA POLVERIMETRO - QAL2 - AST NOTA INFORMATIVA Assicurazione Qualità Sistemi di Monitoraggio in Continuo
SCHEMA. Mandato CEN M/120 Prodotti metallici per impieghi strutturali e loro accessori.
 SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE di prodotti in acciai da bonifica da costruzione cui alla norma UNI EN 10343:2009 0 STORIA Edizione 0
SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE di prodotti in acciai da bonifica da costruzione cui alla norma UNI EN 10343:2009 0 STORIA Edizione 0
La Certificazione degli Ambienti della Centrale di Sterilizzazione
 La Certificazione degli Ambienti della Centrale di Sterilizzazione V Sessione Integrazione di Sistema Venerdì 23 Ottobre 2015 Dott. Roberto Ricci Cosa si intende per Convalida Quali sono gli ambienti della
La Certificazione degli Ambienti della Centrale di Sterilizzazione V Sessione Integrazione di Sistema Venerdì 23 Ottobre 2015 Dott. Roberto Ricci Cosa si intende per Convalida Quali sono gli ambienti della
2. QUALI SONO I RIFERIMENTI SULLA BASE DEI QUALI POSSIAMO CERTIFICARE CHE UN AMBIENTE RISPETTA DETERMINATI REQUISITI
 1. IN COSA CONSISTE LA VALIDAZIONE AMBIENTALE 2. QUALI SONO I RIFERIMENTI SULLA BASE DEI QUALI POSSIAMO CERTIFICARE CHE UN AMBIENTE RISPETTA DETERMINATI REQUISITI 3. QUALI SONO LE FASI SU CUI SI SVILUPPA
1. IN COSA CONSISTE LA VALIDAZIONE AMBIENTALE 2. QUALI SONO I RIFERIMENTI SULLA BASE DEI QUALI POSSIAMO CERTIFICARE CHE UN AMBIENTE RISPETTA DETERMINATI REQUISITI 3. QUALI SONO LE FASI SU CUI SI SVILUPPA
CONFERENZA DEI PRESIDENTI DELLE REGIONI E DELLE PROVINCE AUTONOME (ROMA 11 NOVEMBRE 2004)
 CONFERENZA DEI PRESIDENTI DELLE REGIONI E DELLE PROVINCE AUTONOME (ROMA 11 NOVEMBRE 2004) REQUISITI STRUTTURALI, STRUMENTALI E DI PERSONALE PER L AUTORIZZAZIONE DELLE STRUTTURE CHE EROGANO PRESTAZIONI
CONFERENZA DEI PRESIDENTI DELLE REGIONI E DELLE PROVINCE AUTONOME (ROMA 11 NOVEMBRE 2004) REQUISITI STRUTTURALI, STRUMENTALI E DI PERSONALE PER L AUTORIZZAZIONE DELLE STRUTTURE CHE EROGANO PRESTAZIONI
SCHEMA. Schema per la certificazione del controllo della produzione in. fabbrica ai fini della marcatura CE dei prodotti in acciaio
 SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei prodotti in acciaio inossidabile da costruzione cui alle norme UNI EN 10088-4:2009 e UNI EN 10088-5:2009
SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei prodotti in acciaio inossidabile da costruzione cui alle norme UNI EN 10088-4:2009 e UNI EN 10088-5:2009
Dr. Roberto Ricci Igiene Ospedaliera Ospedali Riuniti di Ancona
 LA CENTRALE DI STERILIZZAZIONE E IL LUOGO DOVE AVVIENE IL RICONDIZIONAMENTO DEI DM RIUTILIZZABILI. I DM UTILIZZATI NELLA PRATICA MEDICA O CHIRURGICA VENGONO INVIATI ALLA CENTRALE DI STERILIZZAZIONE AFFINCHE
LA CENTRALE DI STERILIZZAZIONE E IL LUOGO DOVE AVVIENE IL RICONDIZIONAMENTO DEI DM RIUTILIZZABILI. I DM UTILIZZATI NELLA PRATICA MEDICA O CHIRURGICA VENGONO INVIATI ALLA CENTRALE DI STERILIZZAZIONE AFFINCHE
1 DESCRIZIONE ATTIVITÀ RISULTATI ATTESI PER IL PROCESSO MATRICE DELLE RESPONSABILITA DELLE BIBLIOGRAFIA...
 1 SIMT- IO 067 B REV 1 Processo di confezionamento Prima Stesura Data: Revisione 1 Data Redattori : 20-11-2014 18-12-2015 PIANO DI CONVALIDA SIMT-IO 067 B REV 1 PROCESSO DI CONFEZIONAMENTO E TRASPORTO
1 SIMT- IO 067 B REV 1 Processo di confezionamento Prima Stesura Data: Revisione 1 Data Redattori : 20-11-2014 18-12-2015 PIANO DI CONVALIDA SIMT-IO 067 B REV 1 PROCESSO DI CONFEZIONAMENTO E TRASPORTO
RELAZIONE TECNICO - ILLUSTRATIVA Servizio di manutenzione globale della strumentazione analitica di alta tecnologia
 REGIONE AUTÒNOMA DE SARDIGNA REGIONE AUTONOMA DELLA SARDEGNA AGENTZIA REGIONALE PRO S AMPARU DE S AMBIENTE DE SARDIGNA AGENZIA REGIONALE PER LA PROTEZIONE DELL AMBIENTE DELLA SARDEGNA Direzione Tecnico-Scientifica
REGIONE AUTÒNOMA DE SARDIGNA REGIONE AUTONOMA DELLA SARDEGNA AGENTZIA REGIONALE PRO S AMPARU DE S AMBIENTE DE SARDIGNA AGENZIA REGIONALE PER LA PROTEZIONE DELL AMBIENTE DELLA SARDEGNA Direzione Tecnico-Scientifica
LINEE GUIDA Test di Sterilità delle preparazioni radiofarmaceutiche
 LINEE GUIDA Test di Sterilità delle preparazioni radiofarmaceutiche Data di emissione : 26/03/2019 Rev. n.1 Pag. 1/7 Indice 1. Introduzione... 2 2. Scopo e Campo di applicazione... 2 3. Responsabilità
LINEE GUIDA Test di Sterilità delle preparazioni radiofarmaceutiche Data di emissione : 26/03/2019 Rev. n.1 Pag. 1/7 Indice 1. Introduzione... 2 2. Scopo e Campo di applicazione... 2 3. Responsabilità
CONOSCERE IL RISCHIO
 CONOSCERE IL RISCHIO Agenti biologici Riferimenti normativi e legislativi Riferimenti legislativi 1. L 5 Marzo 1963, n. 292. Vaccinazione antitetanica obbligatoria 2. Dpr 7 Settembre 1965, n. 1301. Regolamento
CONOSCERE IL RISCHIO Agenti biologici Riferimenti normativi e legislativi Riferimenti legislativi 1. L 5 Marzo 1963, n. 292. Vaccinazione antitetanica obbligatoria 2. Dpr 7 Settembre 1965, n. 1301. Regolamento
Qualifica, Taratura, Manutenzione 17 ottobre 2018
 17 ottobre 2018 Persona Qualificata imo- Omeopatica QUALIFICA 2 QUALIFICA ASPETTI TEORICI 3 Le current Good Manufacturing Practices cgmp Le norme di buona fabbricazione o cgmp (current Good Manufacturing
17 ottobre 2018 Persona Qualificata imo- Omeopatica QUALIFICA 2 QUALIFICA ASPETTI TEORICI 3 Le current Good Manufacturing Practices cgmp Le norme di buona fabbricazione o cgmp (current Good Manufacturing
attrezzature conformi e idonee Garantire D. Lgs 81 / art. 71 e s.m.i.:
 Sicuri con Metodo Il datore di lavoro mette a disposizione dei lavoratori attrezzature conformi e idonee ai fini della salute e sicurezza adeguate al lavoro da svolgere. Esse devono essere utilizzate conformemente
Sicuri con Metodo Il datore di lavoro mette a disposizione dei lavoratori attrezzature conformi e idonee ai fini della salute e sicurezza adeguate al lavoro da svolgere. Esse devono essere utilizzate conformemente
Presentazione società Servizi offerti
 Presentazione società Servizi offerti Via XXV Luglio, 59 Presentazione società Safe nasce come laboratorio chimico biologico attrezzato per controlli merceologici e ambientali e studio di consulenza. La
Presentazione società Servizi offerti Via XXV Luglio, 59 Presentazione società Safe nasce come laboratorio chimico biologico attrezzato per controlli merceologici e ambientali e studio di consulenza. La
SCHEMA 0 STORIA. Schema certificativo CP DOCUMENTI ESTERNI DI RIFERIMENTO
 SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei prodotti laminati a caldo di acciai per impieghi strutturali di cui alla norma UNI EN 10025-1, edizione
SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei prodotti laminati a caldo di acciai per impieghi strutturali di cui alla norma UNI EN 10025-1, edizione
PO-TR-004 ACCETTAZIONE RICHIESTA TRASFUSIONALE ASSEGNAZIONE E CONSEGNA EMOCOMPONENTI
 Unità emittente SGQ Unità destinataria DIR TAL IMM Udr CQB SGQ BSCS SGA LAB UO CAR CR X X X X X X X X X X REDATTO Dott. P. A. Accardo 28/10/2013 REVISIONATO Dott.ssa M. Ferraro 06/11/2013 APPROVATO Dott.
Unità emittente SGQ Unità destinataria DIR TAL IMM Udr CQB SGQ BSCS SGA LAB UO CAR CR X X X X X X X X X X REDATTO Dott. P. A. Accardo 28/10/2013 REVISIONATO Dott.ssa M. Ferraro 06/11/2013 APPROVATO Dott.
SCHEMA per la certificazione dei tubi di rame senza saldatura per condizionamento e refrigerazione cui alla norma UNI EN :2010
 SCHEMA per la certificazione dei tubi di rame senza saldatura per condizionamento e refrigerazione cui alla norma UNI EN 12735-1:2010 Il presente documento è stato approvato dalla Commissione Prodotti
SCHEMA per la certificazione dei tubi di rame senza saldatura per condizionamento e refrigerazione cui alla norma UNI EN 12735-1:2010 Il presente documento è stato approvato dalla Commissione Prodotti
Provincia Autonoma di Trento
 PAT/RFS506-11/08/2017-0442252 - Allegato Utente 7 (A07) Azienda Provinciale per i Servizi Sanitari Provincia Autonoma di Trento Allegato n. 2f GARA A PROCEDURA APERTA FORNITURA, SUDDIVISA IN 6 LOTTI, DI
PAT/RFS506-11/08/2017-0442252 - Allegato Utente 7 (A07) Azienda Provinciale per i Servizi Sanitari Provincia Autonoma di Trento Allegato n. 2f GARA A PROCEDURA APERTA FORNITURA, SUDDIVISA IN 6 LOTTI, DI
Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria
 Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi per l esercizio di attività di CENTRO DI PROCREAZIONE
Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi per l esercizio di attività di CENTRO DI PROCREAZIONE
GESTIONE FARMACI E MATERIALE SANITARIO
 Ogni struttura sanitaria complessa deve disporre di spazi/locali per la ricezione, l immagazzinamento e la distribuzione dei farmaci, dei presidi medico-chirurgici e sanitari, del materiale di medicazione
Ogni struttura sanitaria complessa deve disporre di spazi/locali per la ricezione, l immagazzinamento e la distribuzione dei farmaci, dei presidi medico-chirurgici e sanitari, del materiale di medicazione
MASTER INTERFACOLTA DI II LIVELLO A.A
 MASTER INTERFACOLTA DI II LIVELLO A.A. 200-20 GESTIONE DELLA QUALITÀ E SICUREZZA NEI PROCESSI DI MANIPOLAZIONE E CONSERVAZIONE DI CELLULE E TESSUTI UMANI STATUTO Art. Attivazione del Master L Università
MASTER INTERFACOLTA DI II LIVELLO A.A. 200-20 GESTIONE DELLA QUALITÀ E SICUREZZA NEI PROCESSI DI MANIPOLAZIONE E CONSERVAZIONE DI CELLULE E TESSUTI UMANI STATUTO Art. Attivazione del Master L Università
U.O.PROVVEDITORATO ECONOMATO E VENDITE UFFICIO GARE E CONTRATTI PER ACQUISTO DI BENI E SERVIZI DETERMINAZIONE DIRIGENZIALE N.
 U.O.PROVVEDITORATO ECONOMATO E VENDITE UFFICIO GARE E CONTRATTI PER ACQUISTO DI BENI E SERVIZI DETERMINAZIONE DIRIGENZIALE N. 239/2017 - I.P. 496/2017 Tit./Fasc./Anno 5.3.1.0.0.0/100/2016 Oggetto: ACQUISIZIONE
U.O.PROVVEDITORATO ECONOMATO E VENDITE UFFICIO GARE E CONTRATTI PER ACQUISTO DI BENI E SERVIZI DETERMINAZIONE DIRIGENZIALE N. 239/2017 - I.P. 496/2017 Tit./Fasc./Anno 5.3.1.0.0.0/100/2016 Oggetto: ACQUISIZIONE
ACCREDITAMENTO LABORATORI DI ANALISI UNI CEI EN ISO/IEC 17025:2005. Dr.ssa Eletta Cavedoni Cosmolab srl Tortona
 ACCREDITAMENTO LABORATORI DI ANALISI UNI CEI EN ISO/IEC 17025:2005 Dr.ssa Eletta Cavedoni Cosmolab srl Tortona UNI CEI EN ISO/IEC 17025:2005 Titolo: Requisiti generali per la competenza dei laboratori
ACCREDITAMENTO LABORATORI DI ANALISI UNI CEI EN ISO/IEC 17025:2005 Dr.ssa Eletta Cavedoni Cosmolab srl Tortona UNI CEI EN ISO/IEC 17025:2005 Titolo: Requisiti generali per la competenza dei laboratori
CAMPIONAMENTO/RITIRO PG 507. Descrizione Modifica
 PG 507 Allegati e moduli gestiti con questo documento Mod. 507-a Verbale di Ritiro IO_Campionamento Stato di Revisione N Revisione Data Descrizione Modifica 0 01/06/16 Prima Emissione documento 1 20/09/16
PG 507 Allegati e moduli gestiti con questo documento Mod. 507-a Verbale di Ritiro IO_Campionamento Stato di Revisione N Revisione Data Descrizione Modifica 0 01/06/16 Prima Emissione documento 1 20/09/16
Allegato A. Lotto n. 1
 Allegato A Lotto n. 1 Fornitura di materiali di riferimento certificati per la taratura degli spettrofotometri nella regione del visibile e dell ultravioletto aventi le seguenti specifiche di ima: a) N.
Allegato A Lotto n. 1 Fornitura di materiali di riferimento certificati per la taratura degli spettrofotometri nella regione del visibile e dell ultravioletto aventi le seguenti specifiche di ima: a) N.
eventuale crioconservazione dei gameti maschili. REQUISITI MINIMI STRUTTURALI: I locali e gli spazi devono essere correlati alla tipologia ed al volum
 FASCICOLI Conferenza dei Presidenti delle Regioni e delle Province autonome ROMA, 11 NOVEMBRE 2004 Le Regioni e le Province autonome di Trento e di Bolzano VISTA la legge 19 febbraio 2004 n. 40 Norme in
FASCICOLI Conferenza dei Presidenti delle Regioni e delle Province autonome ROMA, 11 NOVEMBRE 2004 Le Regioni e le Province autonome di Trento e di Bolzano VISTA la legge 19 febbraio 2004 n. 40 Norme in
REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Farmacia Ospedaliera e Territoriale Dott.ssa E. Giordani
 REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Farmacia Ospedaliera e Territoriale Dott.ssa E. Giordani CHECK LIST AUTOCONTROLLO MAGAZZINO FARMACIA Allegato n. 2 Procedura Audit Armadio
REGIONE LAZIO AZIENDA UNITÀ SANITARIA LOCALE RIETI Direttore UOC Farmacia Ospedaliera e Territoriale Dott.ssa E. Giordani CHECK LIST AUTOCONTROLLO MAGAZZINO FARMACIA Allegato n. 2 Procedura Audit Armadio
IO-GA-002/5 Archiviazione e conservazione registrazioni di qualità e dei dati previsti dalle normative
 e dei Unità emittente Unità destinataria Unità interessata* SGQ DIR SGQ SGA BSCS LAB CRIO CR X X X X X X X REDATTO Dott.ssa A. Vaccaro 12/09/2012 REVISIONATO Dott.ssa N.M.Ardizzone 24/07/2015 APPROVATO
e dei Unità emittente Unità destinataria Unità interessata* SGQ DIR SGQ SGA BSCS LAB CRIO CR X X X X X X X REDATTO Dott.ssa A. Vaccaro 12/09/2012 REVISIONATO Dott.ssa N.M.Ardizzone 24/07/2015 APPROVATO
I FARMACISTI e le terapie biologiche: Aspetti tecnici e sostenibilità di budget I dispositivi medici Parte I
 I FARMACISTI e le terapie biologiche: Aspetti tecnici e sostenibilità di budget I dispositivi medici Parte I Dott.ssa Cristina AMATO Farmacista ASLTO4 Referente UFA- Laboratorio Galenica - Ospedale Ivrea
I FARMACISTI e le terapie biologiche: Aspetti tecnici e sostenibilità di budget I dispositivi medici Parte I Dott.ssa Cristina AMATO Farmacista ASLTO4 Referente UFA- Laboratorio Galenica - Ospedale Ivrea
La gestione operativa degli impianti gas medicali nelle strutture ospedaliere secondo le norme UNI e UNI 11100/2011
 La gestione operativa degli impianti gas medicali nelle strutture ospedaliere secondo le norme UNI 7396-1 e UNI 11100/2011 Ing. Orazio Scuderi Azienda Ospedaliera Ospedale Niguarda Cà Granda - Milano POLITECNICO
La gestione operativa degli impianti gas medicali nelle strutture ospedaliere secondo le norme UNI 7396-1 e UNI 11100/2011 Ing. Orazio Scuderi Azienda Ospedaliera Ospedale Niguarda Cà Granda - Milano POLITECNICO
Registrazione Partecipanti Introduzione al Corso 10.00 13.00 L azienda farmaceutica: organizzazione e funzioni G. Breghi
 05.02.16 9.00 9.30 9.30 10.00 Università degli Studi di Siena Dipartimento di Biotecnologie, Chimica e Farmacia Master di II Livello in Tecnologie Farmaceutiche Industriali A.A. 2015-2016 Unità Didattica
05.02.16 9.00 9.30 9.30 10.00 Università degli Studi di Siena Dipartimento di Biotecnologie, Chimica e Farmacia Master di II Livello in Tecnologie Farmaceutiche Industriali A.A. 2015-2016 Unità Didattica
AZIENDA OSPEDALIERO-UNIVERSITARIA OSPEDALI RIUNITI UMBERTO I G. M. LANCISI G. SALESI - ANCONA (CIG X3D0BFB523 ) RIF. 642 CF INDICE
 ALLEGATO 2 AZIENDA OSPEDALIERO-UNIVERSITARIA OSPEDALI RIUNITI UMBERTO I G. M. LANCISI G. SALESI - ANCONA Procedura negoziata per la fornitura in service di un sistema per colorazione automatica per GRAM
ALLEGATO 2 AZIENDA OSPEDALIERO-UNIVERSITARIA OSPEDALI RIUNITI UMBERTO I G. M. LANCISI G. SALESI - ANCONA Procedura negoziata per la fornitura in service di un sistema per colorazione automatica per GRAM
75^ Assemblea Generale AVIS. Corso di formazione. Bergamo, 21 maggio 2011
 75^ Assemblea Generale AVIS Corso di formazione Il percorso di accreditamento alla luce dei requisiti strutturali, tecnologici ed organizzativi minimi per le unità di raccolta del sangue e degli emocomponenti
75^ Assemblea Generale AVIS Corso di formazione Il percorso di accreditamento alla luce dei requisiti strutturali, tecnologici ed organizzativi minimi per le unità di raccolta del sangue e degli emocomponenti
ACCREDIA L Ente Italiano di Accreditamento
 ACCREDIA L Ente Italiano di Accreditamento 2 interconfronto internazionale radon in campo per sistemi di misura passivi: ambienti lavorativi e abitativi Accreditamento dei laboratori di prova per misure
ACCREDIA L Ente Italiano di Accreditamento 2 interconfronto internazionale radon in campo per sistemi di misura passivi: ambienti lavorativi e abitativi Accreditamento dei laboratori di prova per misure
GESTIONE DEI GAS MEDICINALI E DEI GAS DISPOSITIVI MEDICI IN OSPEDALE: APPROCCIO MULTIDISCIPLINARE TORINO, 13 OTTOBRE 2016
 GESTIONE DEI GAS MEDICINALI E DEI GAS DISPOSITIVI MEDICI IN OSPEDALE: APPROCCIO MULTIDISCIPLINARE TORINO, 13 OTTOBRE 2016 Autoproduzione gas medicinali: aria medicinale e ossigeno 93% L. Ferrari - L. Messa
GESTIONE DEI GAS MEDICINALI E DEI GAS DISPOSITIVI MEDICI IN OSPEDALE: APPROCCIO MULTIDISCIPLINARE TORINO, 13 OTTOBRE 2016 Autoproduzione gas medicinali: aria medicinale e ossigeno 93% L. Ferrari - L. Messa
REQUISITI SPECIFICI MINIMI UNITA FARMACI ANTITUMORALI - U.F.A.
 Allegato n. 2 alla Delib.G.R. n. 47/15 del 29.9.2015 REQUISITI SPECIFICI MINIMI UNITA FARMACI ANTITUMORALI - U.F.A. Scheda La preparazione dei farmaci antineoplastici per somministrazione parenterale,
Allegato n. 2 alla Delib.G.R. n. 47/15 del 29.9.2015 REQUISITI SPECIFICI MINIMI UNITA FARMACI ANTITUMORALI - U.F.A. Scheda La preparazione dei farmaci antineoplastici per somministrazione parenterale,
Progettazione e revisione degli ambienti
 XII Corso Nazionale SIBO Pavia 26 Maggio 2018 Progettazione e revisione degli ambienti Dr. Claudio Giannarini Centro Conservazione Cornee Piero Perelli - Lucca Clean Room (o Camera Bianca) Camera in cui
XII Corso Nazionale SIBO Pavia 26 Maggio 2018 Progettazione e revisione degli ambienti Dr. Claudio Giannarini Centro Conservazione Cornee Piero Perelli - Lucca Clean Room (o Camera Bianca) Camera in cui
Gli Schemi di External Quality Assessment Normativa e Introduzione
 A.O. Ospedale S.Anna Como - Giovedì 16 Aprile 2015 Formazione e Sicurezza nella Diagnostica Immunoematologica Gli Schemi di External Quality Assessment Normativa e Introduzione Bruno Brando Direttore dei
A.O. Ospedale S.Anna Como - Giovedì 16 Aprile 2015 Formazione e Sicurezza nella Diagnostica Immunoematologica Gli Schemi di External Quality Assessment Normativa e Introduzione Bruno Brando Direttore dei
1. Medicinali di terapia cellulare somatica e medicinali di ingegneria tissutale
 Allegato 1 1. Medicinali di terapia cellulare somatica e medicinali di ingegneria tissutale La sostanza attiva del medicinale è rappresentata da cellule e/o tessuti prodotti dall ingegneria cellulare o
Allegato 1 1. Medicinali di terapia cellulare somatica e medicinali di ingegneria tissutale La sostanza attiva del medicinale è rappresentata da cellule e/o tessuti prodotti dall ingegneria cellulare o
A. Utilizzo di radio-farmaci a scopo diagnostico e in vitro
 E una disciplina la cui specificità risiede nell impiego regolamentato di radionuclidi artificiali in forma non sigillata per attività sia di tipo diagnostico che terapeutico. E strutturata in due settori
E una disciplina la cui specificità risiede nell impiego regolamentato di radionuclidi artificiali in forma non sigillata per attività sia di tipo diagnostico che terapeutico. E strutturata in due settori
COME STERILIZZARE COSA STERILIZZARE
 SAN MARINO 4 Congresso Infermieri di Camera Operatoria COME STERILIZZARE COSA STERILIZZARE Graziano Sarti Impariamo a distinguere:? 2 Siamo operatori sanitari o altro? Ora va meglio! QUI C E UN PROCESSO
SAN MARINO 4 Congresso Infermieri di Camera Operatoria COME STERILIZZARE COSA STERILIZZARE Graziano Sarti Impariamo a distinguere:? 2 Siamo operatori sanitari o altro? Ora va meglio! QUI C E UN PROCESSO
CONTROLLO DI QUALITA DELL ARIA IN CLEAN ROOM
 Numero 23 giugno 2013 CONTROLLO DI QUALITA DELL ARIA IN CLEAN ROOM Il controllo della qualità dell aria in ambienti critici, in particolare in ambito farmaceutico e clinico, prevede l utilizzo di attrezzature
Numero 23 giugno 2013 CONTROLLO DI QUALITA DELL ARIA IN CLEAN ROOM Il controllo della qualità dell aria in ambienti critici, in particolare in ambito farmaceutico e clinico, prevede l utilizzo di attrezzature
