Allegato II. Conclusioni scientifiche e motivazioni del rifiuto presentati dall'ema
|
|
|
- Ottaviano Fabriciano Gianni
- 8 anni fa
- Visualizzazioni
Transcript
1 Allegato II Conclusioni scientifiche e motivazioni del rifiuto presentati dall'ema 29
2 Conclusioni scientifiche Riassunto generale della valutazione scientifica di Norditropin SimpleXx, Norditropin NordiFlex, Norditropin FlexPro e denominazioni associate (vedere allegato I) Norditropin contiene somatropina, un ormone della crescita umano prodotto con la tecnologia del DNA ricombinante, che ha ottenuto l'autorizzazione all'immissione in commercio nell'unione europea attraverso la procedura di mutuo riconoscimento (MRP). Norditropin è stato approvato in conformità all'articolo 8, paragrafo 3 della direttiva 2001/83/CE. Il 14 maggio 2010, il MAH ha inoltrato tramite MRP una variazione di tipo II relativa a Norditropin SimpleXx, Norditropin NordiFlex, Norditropin FlexPro e denominazioni associate (DK/H/0001/ e /II/078), per richiederne un'estensione delle indicazioni. Visto che gli Stati membri e di riferimento non sono stati in grado di raggiungere un accordo relativo alla variazione, il 20 aprile 2011 la Danimarca ha presentato un deferimento ai sensi dell'articolo 13 del regolamento CE n. 1234/2008 della Commissione. È stato richiesto al CHMP di esprimere un parere relativo alla necessità o meno di modificare le autorizzazioni all'immissione in commercio in modo tale da includere l'indicazione: "Miglioramento della crescita e della composizione corporea in bambini affetti da sindrome di Prader-Willi (PWS) confermato da idoneo test genetico". La procedura di deferimento è iniziata il 19 maggio La PWS è una malattia genetica. L'incidenza della PWS è compresa tra circa 1:10000 e 1:29000 nati vivi. La diagnosi si basa su un test genetico e su criteri clinici. Tra le caratteristiche della sindrome ci sono: bassa statura, ritardo mentale, problemi comportamentali, disfunzioni ormonali, debolezza muscolare e iperfagia, così come ipoattività. Le ultime due caratteristiche possono provocare obesità infantile. Anche lo sviluppo puberale è ritardato e, spesso, è incompleto. Molti dei soggetti di sesso femminile sono anche affetti da amenorrea. I bambini affetti da PWS spesso presentano un concomitante deficit dell'ormone della crescita (GHD) (dal 40 al 100%, a seconda del test di provocazione utilizzato). In Europa sono stati approvati due prodotti a base di GH ricombinante per il trattamento della PWS nei bambini. I dati dello studio presentati con la richiesta di autorizzazione di Novo Nordisk per supportare le indicazioni proposte non sono stati considerati sufficienti (studio retrospettivo, non controllato, in aperto) e di buona qualità (ampio intervallo di dosi utilizzato, misurazioni di altezza incomplete) dagli Stati membri in oggetto. Inoltre, è stato giudicato inappropriato il riferimento, fatto dal MAH, ai dati relativi ad altri prodotti GH per ottenere la stessa indicazione in quanto Norditropin non è stato autorizzato come prodotto medicinale biosimilare. Per dimostrare l'efficacia e la sicurezza relative alle indicazioni di applicazione, la documentazione della richiesta di autorizzazione è stata messa a punto sulla base dello studio GHLiquid Si tratta di uno studio multinazionale, multicentrico, in aperto, osservazionale, retrospettivo condotto su bambini affetti da PWS trattati per la bassa statura con Norditropin al di fuori delle indicazioni approvate. L'obiettivo primario dello studio era quello di valutare le variazioni della deviazione standard dell'altezza (HSDS) dopo 1 anno di trattamento con Norditropin, nei bambini affetti da PWS (riferite alla popolazione PWS). Gli obiettivi secondari erano quelli di valutare nella stessa popolazione la variazione di HSDS, dall'inizio del trattamento fino all'ultima osservazione durante il trattamento con Norditropin (riferita alla popolazione PWS), la variazione in composizione corporea (massa magra e massa grassa), la velocità di crescita in altezza (HV) e la sua variazione. La sicurezza è stata valutata mediante le reazioni negative, l'hba1c, l'igf-i, il quadro ematologico, il TSH, il T3 e il T4 totale, il T3 ed il T4 libero. 30
3 Efficacia Nello studio GHLiquid-1961 sono stati arruolati in Europa quarantuno (41) bambini affetti da PWS geneticamente documentata (19 bambine e 22 bambini). I bambini non erano mai stati trattati con GH al momento della prima dose di Norditropin. Nessuna restrizione relativa al livello di bassa statura è stata applicata e i bambini dello studio dovevano essere in fase prepuberale all'inizio del trattamento. L'età media al momento dell'inclusione nello studio era di 3,8 anni (minimo 0,4 anni; massimo 12,2 anni). Tutti i bambini erano caucasici. In questo studio il dosaggio di Norditropin somministrato è stato scelto a discrezione del medico e aggiustato di volta in volta durante il periodo di trattamento (il dosaggio medio era 0.03 mg/kg/giorno). Standardizzato sulla popolazione PWS, si ottiene un aumento medio stimato di HSDS di 0,9 in bambini di bassa statura affetti da PWS dopo un 1 anno di trattamento con Norditropin. L'aumento stimato di HSDS era di 1,3 all'ultima osservazione (approssimativamente 6 anni). La HSDS è migliorata da una media basale di 0,3 a 1,1 all'ultima osservazione. Standardizzato sulla popolazione normale, si ottiene un aumento medio stimato di HSDS di 0,7 in bambini di bassa statura affetti da PWS dopo un 1 anno di trattamento con Norditropin. L'aumento stimato di HSDS era di 1,1 all'ultima osservazione. La HSDS è migliorata da una media basale di - 1,8 a -1,2 dopo 1 anno ed a -0,7 all'ultima osservazione (approssimativamente 6 anni). I bambini con HSDS superiore a -2 erano 19 (46%) alla visita basale, 27 (66%) dopo 1 anno di trattamento e 35 (85%) all'ultima osservazione. Per cui 35 dei 41 bambini (85%) affetti da PWS avevano un'altezza entro l'intervallo di riferimento per i bambini di statura nella norma dopo il trattamento con Norditropin. La media di HSDS per questo sottogruppo era -0,6 dopo 1 anno e - 0,4 all'ultima osservazione. La composizione corporea è migliorata, con un aumento medio stimato della massa corporea del 9,9% e una corrispondente riduzione della massa grassa del 9,9% dopo 1 anno di trattamento con Norditropin. La massa magra è aumentata del 9,1% dalla visita basale fino all'ultima osservazione. La percentuale di massa magra reale era il 61,8% alla visita basale, 71,9% dopo 1 anno e 72,9% all'ultima osservazione. La percentuale di massa grassa reale era il 38,2% alla visita basale, 28,1% dopo 1 anno e 27,1% all'ultima osservazione. Considerando i dati sopra menzionati, il CHMP ha concluso che lo studio GHLiquid-1961 fornito, sul quale si fonda la base per la richiesta di autorizzazione all'estensione dell'indicazione di Norditropin ai bambini affetti da PWS, era non controllato, in aperto e retrospettivo e non conforme agli standard metodologici per la dimostrazione cardine. Oltre la sopramenzionata lacuna generale il CHMP ha evidenziato altri aspetti dello studio GHLiquid che destano perplessità come la validità e la qualità dei risultati dello studio e che sono elencati di seguito. Nella documentazione relativa alla richiesta di autorizzazione alla variazione, il dosaggio raccomandato da Novo Nordisk per il trattamento della bassa statura e dell'alterata composizione corporea nei bambini affetti da PWS era compreso tra 0,025 e 0,035 mg/kg/giorno. Tuttavia, considerando le richieste provenienti da alcuni Stati membri interessati (CSM) nel corso del deferimento al CMDh, il MAH ha concordato che dose raccomandata per la PWS può essere 0,035 mg/kg/giorno, la stessa degli altri due prodotti GH approvati per la stessa indicazione. Il CHMP ha concluso che il razionale per il dosaggio proposto (cioè 0,035 mg/kg/giorno) è ancora poco chiaro. Il dosaggio raccomandato non è lo stesso di quello esaminato nello studio GHLiquid che era scelto a discrezione del medico ed era in media 0.03 mg/kg/giorno. Inoltre, non è stato considerato opportuno accettare lo stesso dosaggio raccomandato degli altri prodotti GH, in quanto Norditropin non ha dimostrato un'efficacia comparabile e quei due prodotti hanno differenti raccomandazioni di dosaggio per altre indicazioni, cioè la sindrome di Turner e l'insufficienza renale cronica. Un'altra perplessità è rappresentata dal dubbio che tutti i pazienti, in base alla formulazione dei criteri di inclusione, siano stati inclusi nello studio dai rispettivi centri. I criteri di inclusione erano bambini in età prepuberale con diagnosi genetica di PWS, trattati con Norditropin per almeno 1 anno nel centro. Potevano essere inclusi anche i bambini che avevano ricevuto solo una dose di Norditropin. Non è stata fornita alcuna informazione aggiuntiva dal MAH sugli altri bambini affetti 31
4 da PWS per i quali non è stato ottenuto il consenso informato. Il CHMP ha concluso che, dato il disegno retrospettivo dello studio, non sia da escludere un bias di selezione. Anche la qualità dei dati è stata considerata discutibile a causa della mancanza, nel 10% dei pazienti, di alcune informazioni basilari, come l'altezza alla visita basale. L'altezza alla visita basale era disponibile solo per 37 pazienti. IGF-1 SDS alla visita basale era disponibile solo per 28 pazienti. I dati sulla modifica della velocità di crescita in altezza non sono stati considerati validi, in quanto i dati pre-clinici sulle misurazioni dell'altezza erano incompleti. Inoltre, parte dell'indicazione di Norditropin nel trattamento della PWS è rappresentato non solo dal miglioramento della crescita ma anche dal miglioramento della composizione corporea. Di conseguenza il controllo della composizione corporea avrebbe dovuto rappresentare un obiettivo chiave. Eppure, la raccolta dei dati sulla composizione corporea è stata eseguita in maniera differente nei tre centri. Un centro non ha raccolto alcun dato sulla composizione corporea e gli altri due centri hanno raccolto i dati solo su 11 bambini. I dati raccolti in 11 bambini su 41 sono risultati troppo scarsi per trarre conclusioni su questo obiettivo. Anche la velocità di crescita in altezza avrebbe potuto rappresentare un obiettivo interessante, eppure non è disponibile alcun dato. Non è stato fornito alcun dato neanche sull'altezza finale da adulti. In generale, i dati retrospettivi raccolti sono insufficienti e di scarsa qualità. Sicurezza Sono state riportate 128 reazioni negative in 31 bambini (75,6%) affetti da PWS durante l'esposizione a Norditropin (esposizione media 4,1 anni, intervallo da 0,3 a 9,5 anni). La maggior parte di queste reazioni sono state di gravità leggera/moderata. Le reazioni negative più frequenti sono state infezioni del tratto respiratorio che sono comuni nei bambini piccoli (14,6% dei bambini), e la scoliosi che è comune nella PWS (19,5% dei bambini). Trentatre (33,26%) reazioni negative in 17 (41,5%) bambini sono state valutate come probabilmente/possibilmente associate al trattamento con Norditropin. Le più frequenti di queste reazioni negative probabilmente/possibilmente associate al trattamento sono stati la scoliosi (in 8 bambini, 19,5%) e l'apnea notturna (in 3 bambini, 7,3%). Non è stato riportato alcun decesso. Il profilo di sicurezza dei prodotti contenenti somatropina è ben conosciuto. L'apnea notturna e la morte improvvisa sono stati riportati nella pratica clinica dopo l'inizio della terapia in pazienti affetti dalla sindrome di Prader-Willi che presentavano uno o più dei seguenti fattori di rischio: obesità grave, storia clinica di ostruzione delle vie aeree superiori o apnea notturna, o infezione respiratoria ad eziologia non identificata. I dati retrospettivi presentati non hanno prodotto nuove perplessità relative alla sicurezza. Profilo rischio-beneficio In relazione all'efficacia sulla base dei dati disponibili il CHMP ha concluso che la dimostrazione di efficacia di Norditropin nella PWS è basata su dati limitati e inaffidabili di evidente scarsa qualità. Solo 33 bambini sono stati inclusi nell'analisi di efficacia primaria e, a causa del progetto dello studio, non può essere escluso un bias di selezione. Inoltre, la qualità dei dati è stata considerata discutibile, come per la mancanza, nel 10% dei soggetti, di dati relativi all'altezza alla visita basale. L'efficacia di Norditropin sugli obiettivi chiave secondari come la composizione corporea e la velocità di crescita in altezza, non sono noti. Non sono disponibili dati sui pesi finali di adulti. Inoltre, nello studio retrospettivo è stato utilizzato un ampio intervallo di dosi (dosaggio medio da 0,03 mg/kg/giorno - fino a 0,06 mg/kg/giorno). Il CHMP ha concluso che il razionale relativo alla dose proposta (cioè 0,035 mg/kg/giorno) è poco chiaro. In merito alla sicurezza, i dati retrospettivi presentati non hanno prodotto nuove perplessità. In conclusione, i dati forniti dal MAH, in particolare per supportare l'efficacia, sono insufficienti per sostenere l'estensione di indicazione nella PWS. Inoltre, non è considerato accettabile fare riferimento a dati prospettici ottenuti con altro prodotto GH per ottenere la stessa indicazione con lo stesso regime di dosaggio, in considerazione delle basi legali per l'autorizzazione all'immissione in commercio di Norditropin, cioè l'articolo 8, paragrafo 3 della direttiva 2001/83/CE. 32
5 Motivazioni del rifiuto Considerando che: Il comitato ha considerato la notifica di deferimento presentata dalla Danimarca in conformità all'articolo 13 del regolamento (CE) n. 1234/2008 della Commissione. Il comitato ha revisionato tutti i dati disponibili presentati dal titolare dell'autorizzazione all'immissione in commercio, a supporto della sicurezza e dell'efficacia di Norditropin SimpleXx, Norditropin NordiFlex, Norditropin FlexPro e denominazioni associate nell'indicazione di applicazione "Miglioramento della crescita e della composizione corporea in bambini affetti da sindrome di Prader-Willi (PWS) confermato da idoneo test genetico". È opinione del Comitato che i dati forniti dal MAH, in particolare per supportare l'efficacia, siano limitati in quanto derivati da uno studio non comparativo, osservazionale e retrospettivo. Inoltre, i dati sono considerati inaffidabili e pertanto il rapporto rischi-benefici di Norditropin SimpleXx, di Norditropin NordiFlex, di Norditropin FlexPro e denominazioni associate nelle indicazioni di applicazione non è positivo. È altresì opinione del comitato che i dettagli presentati a supporto della richiesta di autorizzazione ad estendere le indicazioni di Norditropin SimpleXx, Norditropin NordiFlex, Norditropin FlexPro e denominazioni associate non siano conformi ai requisiti di un prodotto autorizzato in base all'articolo 8, paragrafo 3, della direttiva 2001/83/CE. il CHMP ha raccomandato il rifiuto della variazione delle autorizzazioni all'immissione in commercio per Norditropin SimpleXx, Norditropin NordiFlex, Norditropin FlexPro e per le denominazioni associate (vedere allegato I). 33
farmaceutica Clavulanic acid 10 mg Dosaggio standard di 10 mg di amoxicillina/2,5 mg di acido clavulanico/kg di peso corporeo Repubblica Ceca
 Allegato I Elenco dei nomi, della forma farmaceutica, del dosaggio del medicinale veterinario, della specie animale, della via di somministrazione, del richiedente/titolare dell autorizzazione all immissione
Allegato I Elenco dei nomi, della forma farmaceutica, del dosaggio del medicinale veterinario, della specie animale, della via di somministrazione, del richiedente/titolare dell autorizzazione all immissione
Nozioni generali. Principali forme di trattamento
 tano essere di vitale importanza per il benessere psicofisico del paziente, pertanto vale sempre la pena impegnarsi, anche quando la sindrome non venga diagnosticata subito dopo la nascita. Principali
tano essere di vitale importanza per il benessere psicofisico del paziente, pertanto vale sempre la pena impegnarsi, anche quando la sindrome non venga diagnosticata subito dopo la nascita. Principali
Allegato I. Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio
 Allegato I Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio Conclusioni scientifiche Vista la relazione di valutazione del comitato di valutazione
Allegato I Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio Conclusioni scientifiche Vista la relazione di valutazione del comitato di valutazione
SMID a.a. 2004/2005 Corso di Metodi Statistici in Biomedicina Tassi di incidenza 9/2/2005
 SMID a.a. 2004/2005 Corso di Metodi Statistici in Biomedicina Tassi di incidenza 9/2/2005 Ricerca epidemiologica Gli epidemiologi sono interessati a conoscere l incidenza delle malattie per prevedere i
SMID a.a. 2004/2005 Corso di Metodi Statistici in Biomedicina Tassi di incidenza 9/2/2005 Ricerca epidemiologica Gli epidemiologi sono interessati a conoscere l incidenza delle malattie per prevedere i
AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune)
 AIFA - Sirolimus (Rapamune) 08/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune) Nota Informativa Importante (08 Febbraio 2010) file:///c /documenti/sir653.htm [08/02/2010 10.47.36]
AIFA - Sirolimus (Rapamune) 08/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune) Nota Informativa Importante (08 Febbraio 2010) file:///c /documenti/sir653.htm [08/02/2010 10.47.36]
Trials clinici. Disegni di studio
 Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Conclusioni scientifiche
 Allegato II Conclusioni scientifiche e motivi della revoca o variazione dei termini delle autorizzazioni all immissione in commercio e spiegazione dettagliata delle differenze rispetto alla raccomandazione
Allegato II Conclusioni scientifiche e motivi della revoca o variazione dei termini delle autorizzazioni all immissione in commercio e spiegazione dettagliata delle differenze rispetto alla raccomandazione
AIFA Agenzia Italiana del Farmaco Valproato
 AIFA - Valproato 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Valproato Rivalutazione CHMP file:///c /documenti/val9510.htm [18/12/2009 12.44.38] Domande e risposte sulla rivalutazione dei
AIFA - Valproato 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Valproato Rivalutazione CHMP file:///c /documenti/val9510.htm [18/12/2009 12.44.38] Domande e risposte sulla rivalutazione dei
l'insieme di tutti i casi esistenti in un determinato momento ed in una
 Le misure di frequenza delle malattie possono descrivere: l'insieme di tutti i casi esistenti in un determinato momento ed in una determinata popolazione il verificarsi di nuovi casi A questo scopo si
Le misure di frequenza delle malattie possono descrivere: l'insieme di tutti i casi esistenti in un determinato momento ed in una determinata popolazione il verificarsi di nuovi casi A questo scopo si
STUDI SU MATERIALE GENETICO
 Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
della manutenzione, includa i requisiti relativi ai sottosistemi strutturali all interno del loro contesto operativo.
 L 320/8 Gazzetta ufficiale dell Unione europea IT 17.11.2012 REGOLAMENTO (UE) N. 1078/2012 DELLA COMMISSIONE del 16 novembre 2012 relativo a un metodo di sicurezza comune per il monitoraggio che devono
L 320/8 Gazzetta ufficiale dell Unione europea IT 17.11.2012 REGOLAMENTO (UE) N. 1078/2012 DELLA COMMISSIONE del 16 novembre 2012 relativo a un metodo di sicurezza comune per il monitoraggio che devono
Potenza dello studio e dimensione campionaria. Laurea in Medicina e Chirurgia - Statistica medica 1
 Potenza dello studio e dimensione campionaria Laurea in Medicina e Chirurgia - Statistica medica 1 Introduzione Nella pianificazione di uno studio clinico randomizzato è fondamentale determinare in modo
Potenza dello studio e dimensione campionaria Laurea in Medicina e Chirurgia - Statistica medica 1 Introduzione Nella pianificazione di uno studio clinico randomizzato è fondamentale determinare in modo
Calcolo delle probabilità
 Calcolo delle probabilità Laboratorio di Bioinformatica Corso A aa 2005-2006 Statistica Dai risultati di un esperimento si determinano alcune caratteristiche della popolazione Calcolo delle probabilità
Calcolo delle probabilità Laboratorio di Bioinformatica Corso A aa 2005-2006 Statistica Dai risultati di un esperimento si determinano alcune caratteristiche della popolazione Calcolo delle probabilità
Effetti sull opinione di pazienti riguardo all utilizzo di un computer in uno studio medico nell assistenza ordinaria
 Effetti sull opinione di pazienti riguardo all utilizzo di un computer in uno studio medico nell assistenza ordinaria Christopher N. Sciamanna, Scott P. Novak, Bess H. Marcus. International Journal of
Effetti sull opinione di pazienti riguardo all utilizzo di un computer in uno studio medico nell assistenza ordinaria Christopher N. Sciamanna, Scott P. Novak, Bess H. Marcus. International Journal of
Criteri di selezione del collettivo e definizioni
 Appendice A Criteri di selezione del collettivo e definizioni Introduzione L indagine sull integrazione sociale delle persone con disabilità è stata realizzata nell ambito del progetto Sistema di Informazione
Appendice A Criteri di selezione del collettivo e definizioni Introduzione L indagine sull integrazione sociale delle persone con disabilità è stata realizzata nell ambito del progetto Sistema di Informazione
CARTA INTESTATA DEL CENTRO CLINICO
 CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
Servizio Laboratorio di Prevenzione. INDAGINE DI CUSTOMER SATISFACTION su prestazioni di Laboratorio
 Servizio Laboratorio di Prevenzione INDAGINE DI CUSTOMER SATISFACTION su prestazioni di Laboratorio anno 2014 Pag. 1 di 6 Indice 1 Introduzione... 2 2 Percorso attuato... 2 3 Analisi dei dati... 3 4 Valutazione
Servizio Laboratorio di Prevenzione INDAGINE DI CUSTOMER SATISFACTION su prestazioni di Laboratorio anno 2014 Pag. 1 di 6 Indice 1 Introduzione... 2 2 Percorso attuato... 2 3 Analisi dei dati... 3 4 Valutazione
Risultati dell indagine sul benessere dei dipendenti 2014
 Risultati dell indagine sul benessere dei dipendenti 2014 (art. 14 comma 5 - d.lgs 150/2009) sintesi dati Generali, per Area e tipologia di dipendente Le Amministrazioni pubbliche, nella prospettiva di
Risultati dell indagine sul benessere dei dipendenti 2014 (art. 14 comma 5 - d.lgs 150/2009) sintesi dati Generali, per Area e tipologia di dipendente Le Amministrazioni pubbliche, nella prospettiva di
03/12/2008 10.30 REGIONE LOMBARDIA -> Page 006 of 10
 03/12/2008 10.30 REGIONE LOMBARDIA -> Page 006 of 10 EMENCHMP/590563/2008 EMEA/H/A-5.3 Parere del Comitato per i Prodotti Medicinali ad Uso Umano, ai sensi dell'articolo 5(39) del regolamento (CE) n. 726/2004,
03/12/2008 10.30 REGIONE LOMBARDIA -> Page 006 of 10 EMENCHMP/590563/2008 EMEA/H/A-5.3 Parere del Comitato per i Prodotti Medicinali ad Uso Umano, ai sensi dell'articolo 5(39) del regolamento (CE) n. 726/2004,
MANUALE DELLA QUALITÀ SIF CAPITOLO 08 (ED. 01) MISURAZIONI, ANALISI E MIGLIORAMENTO
 INDICE 8.1 Generalità 8.2 Monitoraggi e Misurazione 8.2.1 Soddisfazione del cliente 8.2.2 Verifiche Ispettive Interne 8.2.3 Monitoraggio e misurazione dei processi 8.2.4 Monitoraggio e misurazione dei
INDICE 8.1 Generalità 8.2 Monitoraggi e Misurazione 8.2.1 Soddisfazione del cliente 8.2.2 Verifiche Ispettive Interne 8.2.3 Monitoraggio e misurazione dei processi 8.2.4 Monitoraggio e misurazione dei
Legga le informazioni che seguono e poi risponda alla domanda:
 La scoperta del gene responsabile della fibrosi cistica ha permesso la messa a punto di un test genetico per identificare il portatore sano del gene della malattia. Si è aperto quindi un importante dibattito
La scoperta del gene responsabile della fibrosi cistica ha permesso la messa a punto di un test genetico per identificare il portatore sano del gene della malattia. Si è aperto quindi un importante dibattito
Ministero della Salute Agenzia Italiana del Farmaco
 Ministero della Salute Agenzia Italiana del Farmaco Linee guida per la classificazione e conduzione degli studi osservazionali sui farmaci IL DIRETTORE GENERALE VISTO il Decreto del Ministero della Salute
Ministero della Salute Agenzia Italiana del Farmaco Linee guida per la classificazione e conduzione degli studi osservazionali sui farmaci IL DIRETTORE GENERALE VISTO il Decreto del Ministero della Salute
Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia
 EIOPA-BoS-14/176 IT Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia EIOPA Westhafen Tower, Westhafenplatz 1-60327 Frankfurt Germany - Tel. + 49 69-951119-20; Fax. +
EIOPA-BoS-14/176 IT Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia EIOPA Westhafen Tower, Westhafenplatz 1-60327 Frankfurt Germany - Tel. + 49 69-951119-20; Fax. +
Allegato 11 Modello di Rapporto annuale di controllo
 Allegato 11 Modello di Rapporto annuale di controllo Modello di Rapporto annuale di controllo a norma dell articolo 62 par. 1, lettera d) punto i) del Regolamento (CE) n. 1083/2006 e dell articolo 18 paragrafo
Allegato 11 Modello di Rapporto annuale di controllo Modello di Rapporto annuale di controllo a norma dell articolo 62 par. 1, lettera d) punto i) del Regolamento (CE) n. 1083/2006 e dell articolo 18 paragrafo
Richiedente Nome di fantasia Dosaggio Forma farmaceutica Via di somministrazione. 40 mg tablet uso orale. 40 mg tablet uso orale
 Allegato I Elenco dei nomi, delle forme farmaceutiche, dei dosaggi di prodotti medicinali, delle vie di somministrazione, dei titolari dell autorizzazione all immissione in commercio negli Stati membri
Allegato I Elenco dei nomi, delle forme farmaceutiche, dei dosaggi di prodotti medicinali, delle vie di somministrazione, dei titolari dell autorizzazione all immissione in commercio negli Stati membri
Bambini e ragazzi affetti da tumore
 Bambini e ragazzi affetti da tumore Firenze, 29 maggio 2014 Gianfranco Manneschi U.O. Epidemiologia clinica e descrittiva ISPO Istituto per lo Studio e la Prevenzione Oncologica introduzione La patologia
Bambini e ragazzi affetti da tumore Firenze, 29 maggio 2014 Gianfranco Manneschi U.O. Epidemiologia clinica e descrittiva ISPO Istituto per lo Studio e la Prevenzione Oncologica introduzione La patologia
Esiste un legame. tra il sonno e la mia salute dentale? Nuovo sistema di diagnosi e trattamento per l'apnea del sonno e la roncopatia
 Esiste un legame tra il sonno e la mia salute dentale? Nuovo sistema di diagnosi e trattamento per l'apnea del sonno e la roncopatia I disturbi del sonno Il sonno è talmente importante che gli esseri umani
Esiste un legame tra il sonno e la mia salute dentale? Nuovo sistema di diagnosi e trattamento per l'apnea del sonno e la roncopatia I disturbi del sonno Il sonno è talmente importante che gli esseri umani
LA SINDROME DI DOWN LA STORIA
 LA SINDROME DI DOWN LA STORIA La sindrome di Down, che è detta anche trisomia 21 o mongoloidismo, è una malattia causata dalla presenza di una terza copia del cromosoma 21; è la più comune anomalia cromosomica
LA SINDROME DI DOWN LA STORIA La sindrome di Down, che è detta anche trisomia 21 o mongoloidismo, è una malattia causata dalla presenza di una terza copia del cromosoma 21; è la più comune anomalia cromosomica
MINISTERO DEL LAVORO, DELLA SALUTE E DELLE POLITICHE SOCIALI
 MINISTERO DEL LAVORO, DELLA SALUTE E DELLE POLITICHE SOCIALI DECRETO 14 luglio 2009 Requisiti minimi per le polizze assicurative a tutela dei soggetti partecipanti alle sperimentazioni cliniche dei medicinali.
MINISTERO DEL LAVORO, DELLA SALUTE E DELLE POLITICHE SOCIALI DECRETO 14 luglio 2009 Requisiti minimi per le polizze assicurative a tutela dei soggetti partecipanti alle sperimentazioni cliniche dei medicinali.
REGOLAMENTO DI ESECUZIONE (UE) N. 489/2012 DELLA COMMISSIONE
 9.6.2012 Gazzetta ufficiale dell Unione europea L 150/71 REGOLAMENTO DI ESECUZIONE (UE) N. 489/2012 DELLA COMMISSIONE dell 8 giugno 2012 recante norme d esecuzione ai fini dell applicazione dell articolo
9.6.2012 Gazzetta ufficiale dell Unione europea L 150/71 REGOLAMENTO DI ESECUZIONE (UE) N. 489/2012 DELLA COMMISSIONE dell 8 giugno 2012 recante norme d esecuzione ai fini dell applicazione dell articolo
I problemi endocrinologici in età evolutiva
 III CONVEGNO REGIONALE SINDROME DI PRADER WILLI I problemi endocrinologici in età evolutiva Lorenzo Iughetti Dipartimento Materno-Infantile Università di Modena e Reggio Emilia Rappresentazione schematica
III CONVEGNO REGIONALE SINDROME DI PRADER WILLI I problemi endocrinologici in età evolutiva Lorenzo Iughetti Dipartimento Materno-Infantile Università di Modena e Reggio Emilia Rappresentazione schematica
Valutazione dell IG di Frollini tradizionali e preparati con farina con l aggiunta del % di Freno SIGI.
 Valutazione dell IG di Frollini tradizionali e preparati con farina con l aggiunta del % di Freno SIGI. Premessa L'indice glicemico (IG) di un alimento, definito come l'area sotto la curva (AUC) della
Valutazione dell IG di Frollini tradizionali e preparati con farina con l aggiunta del % di Freno SIGI. Premessa L'indice glicemico (IG) di un alimento, definito come l'area sotto la curva (AUC) della
INN Nome di fantasia Dosaggi Forma CAUSTINERF ARSENICAL. CAUSTINERF ARSENICAL, pâte pour usage dentaire. YRANICID ARSENICAL, pâte pour usage dentaire
 Allegato I Elenco dei nomi, delle forme farmaceutiche, dei dosaggi dei medicinali, delle vie di somministrazione, dei titolari dell'autorizzazione all'immissione in commercio negli Stati membri 1 Stato
Allegato I Elenco dei nomi, delle forme farmaceutiche, dei dosaggi dei medicinali, delle vie di somministrazione, dei titolari dell'autorizzazione all'immissione in commercio negli Stati membri 1 Stato
Nome di fantasia. Asprimax 850 mg/g. 100%, soluzione in polvere per amministrazione orale 80% WSP
 ALLEGATO I NOME, FORMA FARMACEUTICA, CONCENTRAZIONE DEL MEDICINALE, SPECIE ANIMALI, VIE DI SOMMINISTRAZIONE E TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO / RICHIEDENTE 1/9 Stato membro / Numero
ALLEGATO I NOME, FORMA FARMACEUTICA, CONCENTRAZIONE DEL MEDICINALE, SPECIE ANIMALI, VIE DI SOMMINISTRAZIONE E TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO / RICHIEDENTE 1/9 Stato membro / Numero
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
PROCEDURA DI COORDINAMENTO TRA GESTORI DI RETE AI SENSI DEGLI ARTICOLI 34 E 35 DELL ALLEGATO A ALLA DELIBERA ARG/ELT 99/08 (TICA)
 PROCEDURA DI COORDINAMENTO TRA GESTORI DI RETE AI SENSI DEGLI ARTICOLI 34 E 35 DELL ALLEGATO A ALLA DELIBERA ARG/ELT 99/08 (TICA) Il presente documento descrive le modalità di coordinamento tra gestori
PROCEDURA DI COORDINAMENTO TRA GESTORI DI RETE AI SENSI DEGLI ARTICOLI 34 E 35 DELL ALLEGATO A ALLA DELIBERA ARG/ELT 99/08 (TICA) Il presente documento descrive le modalità di coordinamento tra gestori
COMUNE DI PERUGIA AREA DEL PERSONALE DEL COMPARTO DELLE POSIZIONI ORGANIZZATIVE E DELLE ALTE PROFESSIONALITA
 COMUNE DI PERUGIA AREA DEL PERSONALE DEL COMPARTO DELLE POSIZIONI ORGANIZZATIVE E DELLE ALTE PROFESSIONALITA METODOLOGIA DI VALUTAZIONE DELLA PERFORMANCE Approvato con atto G.C. n. 492 del 07.12.2011 1
COMUNE DI PERUGIA AREA DEL PERSONALE DEL COMPARTO DELLE POSIZIONI ORGANIZZATIVE E DELLE ALTE PROFESSIONALITA METODOLOGIA DI VALUTAZIONE DELLA PERFORMANCE Approvato con atto G.C. n. 492 del 07.12.2011 1
Documento approvato dal Consiglio Direttivo dell ANVUR nella seduta del 15/5/2013
 Documento approvato dal Consiglio Direttivo dell ANVUR nella seduta del 15/5/2013-1. Premessa Con la pubblicazione nella Gazzetta Ufficiale n. 104 del 06/05/2013 del DM 45/2013 Regolamento recante modalità
Documento approvato dal Consiglio Direttivo dell ANVUR nella seduta del 15/5/2013-1. Premessa Con la pubblicazione nella Gazzetta Ufficiale n. 104 del 06/05/2013 del DM 45/2013 Regolamento recante modalità
Autorità Nazionale Anticorruzione e per la valutazione e la trasparenza delle amministrazioni pubbliche
 Autorità Nazionale Anticorruzione e per la valutazione e la trasparenza delle amministrazioni pubbliche Metodologia dell attività di vigilanza e controllo dell Autorità in relazione agli obblighi di pubblicazione
Autorità Nazionale Anticorruzione e per la valutazione e la trasparenza delle amministrazioni pubbliche Metodologia dell attività di vigilanza e controllo dell Autorità in relazione agli obblighi di pubblicazione
ANALISI. Questionario per il personale ASI. Data Sezione del documento / Motivo della revisione Revisione 14.01.2011 Prima emissione documento A
 Pagina: 1 di 13 Data Sezione del documento / Motivo della revisione Revisione 14.01.2011 Prima emissione documento A Pagina: 2 di 13 QUESTIONARIO PER IL PERSONALE In seno all analisi SWOT, al fine di valutare
Pagina: 1 di 13 Data Sezione del documento / Motivo della revisione Revisione 14.01.2011 Prima emissione documento A Pagina: 2 di 13 QUESTIONARIO PER IL PERSONALE In seno all analisi SWOT, al fine di valutare
Principi generali. Vercelli 9-10 dicembre 2005. G. Bartolozzi - Firenze. Il Pediatra di famiglia e gli esami di laboratorio ASL Vercelli
 Il Pediatra di famiglia e gli esami di laboratorio ASL Vercelli Principi generali Carlo Federico Gauss Matematico tedesco 1777-1855 G. Bartolozzi - Firenze Vercelli 9-10 dicembre 2005 Oggi il nostro lavoro
Il Pediatra di famiglia e gli esami di laboratorio ASL Vercelli Principi generali Carlo Federico Gauss Matematico tedesco 1777-1855 G. Bartolozzi - Firenze Vercelli 9-10 dicembre 2005 Oggi il nostro lavoro
Articolo 1. Oggetto e ambito di applicazione
 L 107/76 25.4.2015 DECISIONE (UE) 2015/656 DELLA BANCA CENTRALE EUROPEA del 4 febbraio 2015 sulle condizioni in presenza delle quali è consentito agli enti creditizi di includere nel capitale primario
L 107/76 25.4.2015 DECISIONE (UE) 2015/656 DELLA BANCA CENTRALE EUROPEA del 4 febbraio 2015 sulle condizioni in presenza delle quali è consentito agli enti creditizi di includere nel capitale primario
Roma 22 settembre 2004
 RISOLUZIONE N. 123/E Roma 22 settembre 2004 Direzione Centrale Normativa e Contenzioso Oggetto: Istanza di interpello. Fondazione XY - Onlus - Attività di ricerca scientifica di particolare interesse sociale.
RISOLUZIONE N. 123/E Roma 22 settembre 2004 Direzione Centrale Normativa e Contenzioso Oggetto: Istanza di interpello. Fondazione XY - Onlus - Attività di ricerca scientifica di particolare interesse sociale.
QUESTIONARIO SODDISFAZIONE FAMIGLIA. Nome del bambino: Sesso: F M
 QUESTIONARIO SODDISFAZIONE FAMIGLIA Ministero della Salute - Centro Nazionale per la Prevenzione delle Malattie (CCM) Progetti applicativi al programma CCM 2009 Presa in carico precoce nel primo anno di
QUESTIONARIO SODDISFAZIONE FAMIGLIA Ministero della Salute - Centro Nazionale per la Prevenzione delle Malattie (CCM) Progetti applicativi al programma CCM 2009 Presa in carico precoce nel primo anno di
Servizio di Mineralometria Ossea Computerizzata (MOC) e Composizione Corporea
 Servizio di Mineralometria Ossea Computerizzata (MOC) e Composizione Corporea Associazione Italiana per l Educazione Demografica Sezione di Roma L osteoporosi È una condizione dello scheletro caratterizzata
Servizio di Mineralometria Ossea Computerizzata (MOC) e Composizione Corporea Associazione Italiana per l Educazione Demografica Sezione di Roma L osteoporosi È una condizione dello scheletro caratterizzata
ANALISI DELLE FREQUENZE: IL TEST CHI 2
 ANALISI DELLE FREQUENZE: IL TEST CHI 2 Quando si hanno scale nominali o ordinali, non è possibile calcolare il t, poiché non abbiamo medie, ma solo frequenze. In questi casi, per verificare se un evento
ANALISI DELLE FREQUENZE: IL TEST CHI 2 Quando si hanno scale nominali o ordinali, non è possibile calcolare il t, poiché non abbiamo medie, ma solo frequenze. In questi casi, per verificare se un evento
Allegato III. Modifiche agli specifici paragrafi del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Modifiche agli specifici paragrafi del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Queste modifiche agli specifici paragrafi del Riassunto delle Caratteristiche
Allegato III Modifiche agli specifici paragrafi del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Queste modifiche agli specifici paragrafi del Riassunto delle Caratteristiche
FARMACISTI, DONNE E FARMACI EQUIVALENTI
 FARMACISTI, DONNE E FARMACI EQUIVALENTI L atteggiamento delle donne verso il generico visto attraverso gli occhi del farmacista Sintesi dei risultati di ricerca per Conferenza Stampa Milano, 16 ottobre
FARMACISTI, DONNE E FARMACI EQUIVALENTI L atteggiamento delle donne verso il generico visto attraverso gli occhi del farmacista Sintesi dei risultati di ricerca per Conferenza Stampa Milano, 16 ottobre
Infezione da HIV e AIDS in Piemonte
 Infezione da HIV e AIDS in Piemonte anno 212 a cura di Chiara Pasqualini, Vittorio Demicheli si ringraziano i medici referenti del Sistema di Sorveglianza HIV/AIDS del Piemonte: O. Bargiacchi, S. Bonora,
Infezione da HIV e AIDS in Piemonte anno 212 a cura di Chiara Pasqualini, Vittorio Demicheli si ringraziano i medici referenti del Sistema di Sorveglianza HIV/AIDS del Piemonte: O. Bargiacchi, S. Bonora,
LA PANDEMIA SILENTE DEL DIABETE: UN EMERGENZA SANITARIA, SOCIALE ED ECONOMICA
 LA PANDEMIA SILENTE DEL DIABETE: UN EMERGENZA SANITARIA, SOCIALE ED ECONOMICA Antonio Nicolucci Direttore Dipartimento di Farmacologia Clinica e Epidemiologia, Consorzio Mario Negri Sud Coordinatore Data
LA PANDEMIA SILENTE DEL DIABETE: UN EMERGENZA SANITARIA, SOCIALE ED ECONOMICA Antonio Nicolucci Direttore Dipartimento di Farmacologia Clinica e Epidemiologia, Consorzio Mario Negri Sud Coordinatore Data
Corso: Statistica e Metodologia Epidemiologica 1
 Università degli Studi di Padova Scuola di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia - A.A. 2014-15 Corso: Statistica e Metodologia Epidemiologica 1 Docenti: prof.ssa Anna Chiara Frigo
Università degli Studi di Padova Scuola di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia - A.A. 2014-15 Corso: Statistica e Metodologia Epidemiologica 1 Docenti: prof.ssa Anna Chiara Frigo
COMUNE DI SOLBIATE ARNO
 SISTEMA DI MISURAZIONE E VALUTAZIONE DEL PERSONALE DIPENDENTE Approvato con deliberazione della Giunta Comunale n. 98 del 14.11.2013 1 GLI ELEMENTI DEL SISTEMA DI VALUTAZIONE Oggetto della valutazione:obiettivi
SISTEMA DI MISURAZIONE E VALUTAZIONE DEL PERSONALE DIPENDENTE Approvato con deliberazione della Giunta Comunale n. 98 del 14.11.2013 1 GLI ELEMENTI DEL SISTEMA DI VALUTAZIONE Oggetto della valutazione:obiettivi
Monitoraggio sulla conversione dei prezzi al consumo dalla Lira all Euro
 ISTAT 17 gennaio 2002 Monitoraggio sulla conversione dei prezzi al consumo dalla Lira all Euro Nell ambito dell iniziativa di monitoraggio, avviata dall Istat per analizzare le modalità di conversione
ISTAT 17 gennaio 2002 Monitoraggio sulla conversione dei prezzi al consumo dalla Lira all Euro Nell ambito dell iniziativa di monitoraggio, avviata dall Istat per analizzare le modalità di conversione
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI
 UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
CAPITOLO 20 AGGIORNAMENTO DEL CODICE DI STOCCAGGIO
 CAPITOLO 20 AGGIORNAMENTO DEL CODICE DI STOCCAGGIO 20.1 PREMESSA... 255 20.2 COMITATO DI CONSULTAZIONE... 255 20.3 SOGGETTI TITOLATI A PRESENTARE RICHIESTE DI MODIFICA... 255 20.4 REQUISITI DI RICEVIBILITA
CAPITOLO 20 AGGIORNAMENTO DEL CODICE DI STOCCAGGIO 20.1 PREMESSA... 255 20.2 COMITATO DI CONSULTAZIONE... 255 20.3 SOGGETTI TITOLATI A PRESENTARE RICHIESTE DI MODIFICA... 255 20.4 REQUISITI DI RICEVIBILITA
Metodi statistici per le ricerche di mercato
 Metodi statistici per le ricerche di mercato Prof.ssa Isabella Mingo A.A. 2014-2015 Facoltà di Scienze Politiche, Sociologia, Comunicazione Corso di laurea Magistrale in «Organizzazione e marketing per
Metodi statistici per le ricerche di mercato Prof.ssa Isabella Mingo A.A. 2014-2015 Facoltà di Scienze Politiche, Sociologia, Comunicazione Corso di laurea Magistrale in «Organizzazione e marketing per
Linee guida per la rilevazione sistematica della customer satisfaction tramite emoticons
 Allegato 1 Linee guida per la rilevazione sistematica della customer satisfaction tramite emoticons 1. Premessa La rilevazione della customer satisfaction è utilizzata da molte amministrazioni per misurare
Allegato 1 Linee guida per la rilevazione sistematica della customer satisfaction tramite emoticons 1. Premessa La rilevazione della customer satisfaction è utilizzata da molte amministrazioni per misurare
Project Cycle Management La programmazione della fase di progettazione esecutiva. La condivisione dell idea progettuale.
 Project Cycle Management La programmazione della fase di progettazione esecutiva. La condivisione dell idea progettuale. Il presente materiale didattico costituisce parte integrante del percorso formativo
Project Cycle Management La programmazione della fase di progettazione esecutiva. La condivisione dell idea progettuale. Il presente materiale didattico costituisce parte integrante del percorso formativo
Manca qualcosa: cosa c èc. di sbagliato nell usare l età alla diagnosi/decesso o la latenza nei casi. Farina OJC 15 maggio 2013
 Manca qualcosa: cosa c èc di sbagliato nell usare l età alla diagnosi/decesso o la latenza nei casi Consonni, Epidemiol Prev,, 2013 Farina OJC 15 maggio 2013 Introduzione Negli ultimi decenni l epidemiologia
Manca qualcosa: cosa c èc di sbagliato nell usare l età alla diagnosi/decesso o la latenza nei casi Consonni, Epidemiol Prev,, 2013 Farina OJC 15 maggio 2013 Introduzione Negli ultimi decenni l epidemiologia
Studio di ricerca clinica sul dolore da endometriosi. Il dolore che Lei sente è reale... anche se gli altri non possono vederlo.
 Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
DIABETE E AUTOCONTROLLO
 DIABETE E AUTOCONTROLLO Sì, gestire il diabete è possibile. Il monitoraggio della glicemia fa parte della terapia generale del diabete. Grazie all autocontrollo, potete misurare il livello di glicemia
DIABETE E AUTOCONTROLLO Sì, gestire il diabete è possibile. Il monitoraggio della glicemia fa parte della terapia generale del diabete. Grazie all autocontrollo, potete misurare il livello di glicemia
Corso di. Dott.ssa Donatella Cocca
 Corso di Statistica medica e applicata Dott.ssa Donatella Cocca 1 a Lezione Cos'è la statistica? Come in tutta la ricerca scientifica sperimentale, anche nelle scienze mediche e biologiche è indispensabile
Corso di Statistica medica e applicata Dott.ssa Donatella Cocca 1 a Lezione Cos'è la statistica? Come in tutta la ricerca scientifica sperimentale, anche nelle scienze mediche e biologiche è indispensabile
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza
 Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
Seconda Parte Specifica di scuola - Statistica sanitaria e Biometria - 31/07/2015
 Domande relative alla specializzazione in: Statistica sanitaria e Biometria Domanda #1 (codice domanda: n.641) : In epidemiologia, una variabile di confondimento è una variabile: A: associata sia alla
Domande relative alla specializzazione in: Statistica sanitaria e Biometria Domanda #1 (codice domanda: n.641) : In epidemiologia, una variabile di confondimento è una variabile: A: associata sia alla
Questionario per indagine nazionale conoscitiva data di avvio: marzo 2015
 IL DOVERE E IL DIRITTO DI DARE VOCE E CURA AL DOLORE DELLA PERSONA NON IN GRADO DI RIFERIRLO Questionario per indagine nazionale conoscitiva data di avvio: marzo 2015 Il dolore è il più soggettivo tra
IL DOVERE E IL DIRITTO DI DARE VOCE E CURA AL DOLORE DELLA PERSONA NON IN GRADO DI RIFERIRLO Questionario per indagine nazionale conoscitiva data di avvio: marzo 2015 Il dolore è il più soggettivo tra
Il RUOLO DEL MEDICO DI MEDICINA GENERALE NELLA IDENTIFICAZIONE DELLE PERSONE CON SOSPETTA DEMENZA. T. Mandarino (MMG ASL RMA )
 Il RUOLO DEL MEDICO DI MEDICINA GENERALE NELLA IDENTIFICAZIONE DELLE PERSONE CON SOSPETTA DEMENZA T. Mandarino (MMG ASL RMA ) La Malattia di Alzheimer La malattia di Alzheimer è la forma più frequente
Il RUOLO DEL MEDICO DI MEDICINA GENERALE NELLA IDENTIFICAZIONE DELLE PERSONE CON SOSPETTA DEMENZA T. Mandarino (MMG ASL RMA ) La Malattia di Alzheimer La malattia di Alzheimer è la forma più frequente
LA VALIDITÀ DEGLI STUDI E IL CONTROLLO DEL CONFONDIMENTO
 LA VALIDITÀ DEGLI STUDI E IL CONTROLLO DEL CONFONDIMENTO Accuratezza degli studi Miettinen, nel 1985, afferma che : la accuratezza di uno studio epidemiologico consiste nel grado di - assenza di errori
LA VALIDITÀ DEGLI STUDI E IL CONTROLLO DEL CONFONDIMENTO Accuratezza degli studi Miettinen, nel 1985, afferma che : la accuratezza di uno studio epidemiologico consiste nel grado di - assenza di errori
Nota interpretativa. La definizione delle imprese di dimensione minori ai fini dell applicazione dei principi di revisione internazionali
 Nota interpretativa La definizione delle imprese di dimensione minori ai fini dell applicazione dei principi di revisione internazionali Febbraio 2012 1 Mandato 2008-2012 Area di delega Consigliere Delegato
Nota interpretativa La definizione delle imprese di dimensione minori ai fini dell applicazione dei principi di revisione internazionali Febbraio 2012 1 Mandato 2008-2012 Area di delega Consigliere Delegato
RELAZIONE DEL COLLEGIO DEI REVISORI AL CONSIGLIO DI AMMINISTRAZIONE
 RELAZIONE DEL COLLEGIO DEI REVISORI AL CONSIGLIO DI AMMINISTRAZIONE Ai Signori Consiglieri della Fondazione Patrizio Paoletti Nel corso dell esercizio chiuso il 31 dicembre 2014 la nostra attività è stata
RELAZIONE DEL COLLEGIO DEI REVISORI AL CONSIGLIO DI AMMINISTRAZIONE Ai Signori Consiglieri della Fondazione Patrizio Paoletti Nel corso dell esercizio chiuso il 31 dicembre 2014 la nostra attività è stata
PROGETTO INDAGINE DI OPINIONE SUL PROCESSO DI FUSIONE DEI COMUNI NEL PRIMIERO
 PROGETTO INDAGINE DI OPINIONE SUL PROCESSO DI FUSIONE DEI COMUNI NEL PRIMIERO L indagine si è svolta nel periodo dal 26 agosto al 16 settembre 2014 con l obiettivo di conoscere l opinione dei residenti
PROGETTO INDAGINE DI OPINIONE SUL PROCESSO DI FUSIONE DEI COMUNI NEL PRIMIERO L indagine si è svolta nel periodo dal 26 agosto al 16 settembre 2014 con l obiettivo di conoscere l opinione dei residenti
STATISTICA IX lezione
 Anno Accademico 013-014 STATISTICA IX lezione 1 Il problema della verifica di un ipotesi statistica In termini generali, si studia la distribuzione T(X) di un opportuna grandezza X legata ai parametri
Anno Accademico 013-014 STATISTICA IX lezione 1 Il problema della verifica di un ipotesi statistica In termini generali, si studia la distribuzione T(X) di un opportuna grandezza X legata ai parametri
Il riduttore di focale utilizzato è il riduttore-correttore Celestron f/ 6.3.
 LE FOCALI DEL C8 Di Giovanni Falcicchia Settembre 2010 Premessa (a cura del Telescope Doctor). Il Celestron C8 è uno Schmidt-Cassegrain, ovvero un telescopio composto da uno specchio primario concavo sferico
LE FOCALI DEL C8 Di Giovanni Falcicchia Settembre 2010 Premessa (a cura del Telescope Doctor). Il Celestron C8 è uno Schmidt-Cassegrain, ovvero un telescopio composto da uno specchio primario concavo sferico
Circolare N.24 del 07 Febbraio 2013. Sicurezza sul lavoro. Obblighi e scadenze
 Circolare N.24 del 07 Febbraio 2013 Sicurezza sul lavoro. Obblighi e scadenze Sicurezza sul lavoro: obblighi e scadenze Gentile cliente, con la presente desideriamo informarla che, il D.Lgs n. 81/2008
Circolare N.24 del 07 Febbraio 2013 Sicurezza sul lavoro. Obblighi e scadenze Sicurezza sul lavoro: obblighi e scadenze Gentile cliente, con la presente desideriamo informarla che, il D.Lgs n. 81/2008
LE CARTE DI CONTROLLO (4)
 LE CARTE DI CONTROLLO (4) Tipo di carta di controllo Frazione difettosa Carta p Numero di difettosi Carta np Dimensione campione Variabile, solitamente >= 50 costante, solitamente >= 50 Linea centrale
LE CARTE DI CONTROLLO (4) Tipo di carta di controllo Frazione difettosa Carta p Numero di difettosi Carta np Dimensione campione Variabile, solitamente >= 50 costante, solitamente >= 50 Linea centrale
Allegato 1 Conclusioni scientifiche e motivazioni per la variazione dei termini dell autorizzazione all immissione in commercio
 Allegato 1 Conclusioni scientifiche e motivazioni per la variazione dei termini dell autorizzazione all immissione in commercio Conclusioni scientifiche Tenendo conto della valutazione del Comitato per
Allegato 1 Conclusioni scientifiche e motivazioni per la variazione dei termini dell autorizzazione all immissione in commercio Conclusioni scientifiche Tenendo conto della valutazione del Comitato per
A cura di Giorgio Mezzasalma
 GUIDA METODOLOGICA PER IL MONITORAGGIO E VALUTAZIONE DEL PIANO DI COMUNICAZIONE E INFORMAZIONE FSE P.O.R. 2007-2013 E DEI RELATIVI PIANI OPERATIVI DI COMUNICAZIONE ANNUALI A cura di Giorgio Mezzasalma
GUIDA METODOLOGICA PER IL MONITORAGGIO E VALUTAZIONE DEL PIANO DI COMUNICAZIONE E INFORMAZIONE FSE P.O.R. 2007-2013 E DEI RELATIVI PIANI OPERATIVI DI COMUNICAZIONE ANNUALI A cura di Giorgio Mezzasalma
SINTESI GENERALE DELLA VALUTAZIONE SCIENTIFICA DEI MEDICINALI CONTENENTI ACIDO VALPROICO/VALPROATO (cfr. allegato I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEI RIASSUNTI DELLE CARATTERISTICHE DEL PRODOTTO E DEI FOGLIETTI ILLUSTRATIVI PRESENTATI DALL AGENZIA EUROPEA PER I MEDICINALI 108 CONCLUSIONI
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEI RIASSUNTI DELLE CARATTERISTICHE DEL PRODOTTO E DEI FOGLIETTI ILLUSTRATIVI PRESENTATI DALL AGENZIA EUROPEA PER I MEDICINALI 108 CONCLUSIONI
Inflazione. L indice dei prezzi al consumo ci consente quindi di introdurre anche il concetto di inflazione:
 Il potere di acquisto cambia nel tempo. Un euro oggi ha un potere di acquisto diverso da quello che aveva 5 anni fa e diverso da quello che avrà fra 20 anni. Come possiamo misurare queste variazioni? L
Il potere di acquisto cambia nel tempo. Un euro oggi ha un potere di acquisto diverso da quello che aveva 5 anni fa e diverso da quello che avrà fra 20 anni. Come possiamo misurare queste variazioni? L
Siamo così arrivati all aritmetica modulare, ma anche a individuare alcuni aspetti di come funziona l aritmetica del calcolatore come vedremo.
 DALLE PESATE ALL ARITMETICA FINITA IN BASE 2 Si è trovato, partendo da un problema concreto, che con la base 2, utilizzando alcune potenze della base, operando con solo addizioni, posso ottenere tutti
DALLE PESATE ALL ARITMETICA FINITA IN BASE 2 Si è trovato, partendo da un problema concreto, che con la base 2, utilizzando alcune potenze della base, operando con solo addizioni, posso ottenere tutti
PraenaTest. Esame non invasivo delle trisomie nel feto. Qualità dall Europa ORA NUOVO. Brochure informativa per gestanti
 ORA NUOVO PraenaTest express Esito in 1 settimana PraenaTest Qualità dall Europa Esame non invasivo delle trisomie nel feto Brochure informativa per gestanti Care gestanti, Tutti i futuri genitori si chiedono
ORA NUOVO PraenaTest express Esito in 1 settimana PraenaTest Qualità dall Europa Esame non invasivo delle trisomie nel feto Brochure informativa per gestanti Care gestanti, Tutti i futuri genitori si chiedono
REGOLAMENTO DELEGATO (UE) N. /.. DELLA COMMISSIONE. del 17.7.2014
 COMMISSIONE EUROPEA Bruxelles, 17.7.2014 C(2014) 4581 final REGOLAMENTO DELEGATO (UE) N. /.. DELLA COMMISSIONE del 17.7.2014 relativo alle condizioni per la classificazione, senza prove, dei profili e
COMMISSIONE EUROPEA Bruxelles, 17.7.2014 C(2014) 4581 final REGOLAMENTO DELEGATO (UE) N. /.. DELLA COMMISSIONE del 17.7.2014 relativo alle condizioni per la classificazione, senza prove, dei profili e
ATI. Umbria 3. RELAZIONE INCIDENZA AMMORTAMENTI ED ONERI FINANZIARI SU REVISIONE PIANO D AMBITO TRIENNIO 2011/2013 V.U.S. Spa
 Regione dell Umbria Provincia di Perugia ATI Umbria 3 RELAZIONE INCIDENZA AMMORTAMENTI ED ONERI FINANZIARI SU REVISIONE PIANO D AMBITO TRIENNIO 2011/2013 V.U.S. Spa INTRODUZIONE Lo scopo del presente documento
Regione dell Umbria Provincia di Perugia ATI Umbria 3 RELAZIONE INCIDENZA AMMORTAMENTI ED ONERI FINANZIARI SU REVISIONE PIANO D AMBITO TRIENNIO 2011/2013 V.U.S. Spa INTRODUZIONE Lo scopo del presente documento
Indagine di previsione per il I trimestre 2016 per le imprese della provincia di Cuneo
 Nota congiunturale Indagine di previsione per il I trimestre 2016 per le imprese della provincia di Cuneo L indagine congiunturale di previsione per il primo trimestre 2016 di Confindustria Cuneo evidenzia
Nota congiunturale Indagine di previsione per il I trimestre 2016 per le imprese della provincia di Cuneo L indagine congiunturale di previsione per il primo trimestre 2016 di Confindustria Cuneo evidenzia
COMUNE DI VILLESSE PROVINCIA DI GORIZIA REGOLAMENTO PER LA VALUTAZIONE DELLE POSIZIONI ORGANIZZATIVE
 COMUNE DI VILLESSE PROVINCIA DI GORIZIA REGOLAMENTO PER LA VALUTAZIONE DELLE POSIZIONI ORGANIZZATIVE Approvato con deliberazione giuntale n. 116 del 29/09/2005, dichiarata immediatamente esecutiva ai sensi
COMUNE DI VILLESSE PROVINCIA DI GORIZIA REGOLAMENTO PER LA VALUTAZIONE DELLE POSIZIONI ORGANIZZATIVE Approvato con deliberazione giuntale n. 116 del 29/09/2005, dichiarata immediatamente esecutiva ai sensi
F 81 Disturbi evolutivi specifici delle abilità scolastiche
 GESUNDHEITSBEZIRK MERAN COMPRENSORIO SANITARIO DI MERANO Krankenhaus Meran Ospedale di Merano Fachambulanz für psychosoziale Gesundheit Ambulatorio Specialistico F 81 Disturbi evolutivi specifici delle
GESUNDHEITSBEZIRK MERAN COMPRENSORIO SANITARIO DI MERANO Krankenhaus Meran Ospedale di Merano Fachambulanz für psychosoziale Gesundheit Ambulatorio Specialistico F 81 Disturbi evolutivi specifici delle
LA REVISIONE LEGALE DEI CONTI La comprensione
 LA REVISIONE LEGALE DEI CONTI La comprensione dell impresa e del suo contesto e la valutazione dei rischi di errori significativi Ottobre 2013 Indice 1. La comprensione dell impresa e del suo contesto
LA REVISIONE LEGALE DEI CONTI La comprensione dell impresa e del suo contesto e la valutazione dei rischi di errori significativi Ottobre 2013 Indice 1. La comprensione dell impresa e del suo contesto
STUDIO LEGALE ASSOCIATO KANAYAMA Norme base della retribuzione degli avvocati (versione abbreviata)
 STUDIO LEGALE ASSOCIATO KANAYAMA Norme base della retribuzione degli avvocati (versione abbreviata) ART. 1 TIPOLOGIE DI RETRIBUZIONE DEGLI AVVOCATI, ECC. 1) Le tipologie di retribuzione degli avvocati
STUDIO LEGALE ASSOCIATO KANAYAMA Norme base della retribuzione degli avvocati (versione abbreviata) ART. 1 TIPOLOGIE DI RETRIBUZIONE DEGLI AVVOCATI, ECC. 1) Le tipologie di retribuzione degli avvocati
(Atti per i quali la pubblicazione non è una condizione di applicabilità) COMMISSIONE
 L 86/6 Gazzetta ufficiale dell Unione europea 5.4.2005 II (Atti per i quali la pubblicazione non è una condizione di applicabilità) COMMISSIONE DECISIONE DELLA COMMISSIONE del 22 marzo 2005 che stabilisce
L 86/6 Gazzetta ufficiale dell Unione europea 5.4.2005 II (Atti per i quali la pubblicazione non è una condizione di applicabilità) COMMISSIONE DECISIONE DELLA COMMISSIONE del 22 marzo 2005 che stabilisce
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Marzo 2009 Nuove modalità di prescrizione per i medicinali contenenti isotretinoina ad
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Marzo 2009 Nuove modalità di prescrizione per i medicinali contenenti isotretinoina ad
I quattro ordini di scuola a confronto Elisabetta Malaguti
 I quattro ordini di scuola a confronto Elisabetta Malaguti Esperienze censite, destinate ad uno o più ordini di scuola. Le esperienze censite nella regione sono 2246. Nella figura che segue è, però, riportato
I quattro ordini di scuola a confronto Elisabetta Malaguti Esperienze censite, destinate ad uno o più ordini di scuola. Le esperienze censite nella regione sono 2246. Nella figura che segue è, però, riportato
PASQUALE FREGA Assobiotec
 ITALIAN ORPHAN DRUGS DAY Venerdì 13 febbraio 2015 Sala conferenze Digital for Business - Sesto San Giovanni (MI) PASQUALE FREGA Assobiotec www.digitalforacademy.com Italian Orphan Drug Day Malattie Rare
ITALIAN ORPHAN DRUGS DAY Venerdì 13 febbraio 2015 Sala conferenze Digital for Business - Sesto San Giovanni (MI) PASQUALE FREGA Assobiotec www.digitalforacademy.com Italian Orphan Drug Day Malattie Rare
Diagnosi precoce delle neoplasie del collo dell utero
 Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
NPTT- NON-INVASIVE PRENATAL TESTING
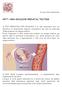 Dr.ssa Chiara Boschetto NPTT- NON-INVASIVE PRENATAL TESTING Il TEST PRENATALE NON INVASIVO è un test molecolare nato con l obiettivo di determinare l assetto cromosomico del feto da materiale fetale presente
Dr.ssa Chiara Boschetto NPTT- NON-INVASIVE PRENATAL TESTING Il TEST PRENATALE NON INVASIVO è un test molecolare nato con l obiettivo di determinare l assetto cromosomico del feto da materiale fetale presente
Progetto Comes, sostegno all handicap
 TITOLO Progetto Comes, sostegno all handicap TEMPI ANNO SCOLASTICO 2010/2011 Destinatari Minori disabili (fascia d età 3/14 anni) frequentanti la scuola dell obbligo, affetti da patologie varie: ipoacusia,
TITOLO Progetto Comes, sostegno all handicap TEMPI ANNO SCOLASTICO 2010/2011 Destinatari Minori disabili (fascia d età 3/14 anni) frequentanti la scuola dell obbligo, affetti da patologie varie: ipoacusia,
un controllo di accettazione tipo A ogni 300 mc massimo di getto
 Laboratorio autorizzato dal ministero delle infrastrutture ad effettuare prove sui materiali da costruzione per strutture metalliche ed opere in cemento armato con D.M. n. 39073 del 23/3/1995 e successivi
Laboratorio autorizzato dal ministero delle infrastrutture ad effettuare prove sui materiali da costruzione per strutture metalliche ed opere in cemento armato con D.M. n. 39073 del 23/3/1995 e successivi
BS OHSAS 18001: 2007. Occupational. Health. Safety. Assesments. Series
 BS OHSAS 18001: 2007 Occupational Health Safety Assesments Series Prefazione La Norma è stata sviluppata per essere compatibile con le Norme: ISO 9001:2000 (Qualità) ISO 14001:2004 (Ambiente) Dr.ssa Carlotta
BS OHSAS 18001: 2007 Occupational Health Safety Assesments Series Prefazione La Norma è stata sviluppata per essere compatibile con le Norme: ISO 9001:2000 (Qualità) ISO 14001:2004 (Ambiente) Dr.ssa Carlotta
Rapporto dal Questionari Insegnanti
 Rapporto dal Questionari Insegnanti SCUOLA CHIC81400N N. Docenti che hanno compilato il questionario: 60 Anno Scolastico 2014/15 Le Aree Indagate Il Questionario Insegnanti ha l obiettivo di rilevare la
Rapporto dal Questionari Insegnanti SCUOLA CHIC81400N N. Docenti che hanno compilato il questionario: 60 Anno Scolastico 2014/15 Le Aree Indagate Il Questionario Insegnanti ha l obiettivo di rilevare la
Il ragionamento diagnostico TEST DIAGNOSTICO. Dott.ssa Marta Di Nicola. L accertamento della condizione patologica viene eseguito TEST DIAGNOSTICO
 Il ragionamento diagnostico http://www.biostatistica biostatistica.unich unich.itit 2 L accertamento della condizione patologica viene eseguito All'inizio del decorso clinico, per una prima diagnosi In
Il ragionamento diagnostico http://www.biostatistica biostatistica.unich unich.itit 2 L accertamento della condizione patologica viene eseguito All'inizio del decorso clinico, per una prima diagnosi In
ALLEGATO CONCLUSIONI SCIENTIFICHE E MOTIVI DEL RIFIUTO PRESENTATI DALL EMEA
 ALLEGATO CONCLUSIONI SCIENTIFICHE E MOTIVI DEL RIFIUTO PRESENTATI DALL EMEA 1 CONCLUSIONI SCIENTIFICHE Il richiedente BioMimetic Therapeutics Ltd. ha presentato all Agenzia europea per i medicinali (EMEA)
ALLEGATO CONCLUSIONI SCIENTIFICHE E MOTIVI DEL RIFIUTO PRESENTATI DALL EMEA 1 CONCLUSIONI SCIENTIFICHE Il richiedente BioMimetic Therapeutics Ltd. ha presentato all Agenzia europea per i medicinali (EMEA)
LA CORRELAZIONE LINEARE
 LA CORRELAZIONE LINEARE La correlazione indica la tendenza che hanno due variabili (X e Y) a variare insieme, ovvero, a covariare. Ad esempio, si può supporre che vi sia una relazione tra l insoddisfazione
LA CORRELAZIONE LINEARE La correlazione indica la tendenza che hanno due variabili (X e Y) a variare insieme, ovvero, a covariare. Ad esempio, si può supporre che vi sia una relazione tra l insoddisfazione
