Nomenclatura e nomi comuni Struttura e proprietà Fonti Reazioni Derivati degli acidi carbossilici
|
|
|
- Evangelista Piccolo
- 7 anni fa
- Visualizzazioni
Transcript
1 Nomenclatura e nomi comuni Struttura e proprietà Fonti Reazioni Derivati degli acidi carbossilici
2 Sono dei composti che hanno come gruppo funzionale il carbossile costituito da un carbonile e un gruppo OH legato al carbonio del carbonile. Il gruppo carbossile può essere scritto in uno dei seguenti modi C O OH R C O OH COOH CO 2 H I tre atomi del gruppo carbossilico (ossigeno, carbonio, ossigeno) hanno ibridazione sp 2 e questo permette ai loro elettroni p di essere delocalizzati in tutto il sistema. COOH O HCOOH Le formiche rosse producono acido formico Acido linoleico CH 3 (CH 2 ) 3 COOH Le radici dell eliotropo Contengono acido valerico COOH Acido benzoico CH 3 (CH 2 ) n COOH Me OH Acido acetico Le capre producono gli acidi capronico n= 4, caprilico n= 6 e caprinico n= 8
3 Trovare la catena più lunga di atomi di C, contenente il gruppo COOH. Sostituire la e finale del nome dell alcano con oico, facendo precedere la parola da acido. Assegnare un nome e numero ai sostituenti. Il carbonio 1 è quello del carbossile Acidi Alifatici Acidi Aromatici Acido o-idrossi benzoico Acido salicilico acido 2-(acetilossi)benzoico Acido acetil salicilico
4 Per gli acidi Bicarbossilici: la parola acido acido + il suffisso dioico Acidi bicarbossilici Alifatici Acido salicilico Acidi bicarbossilici Aromatici Alimenti naturalmente ricchi di acido salicilico sono le albicocche (3 mg/100g), il ribes rosso e nero (5 mg/100g), la cicoria (1 mg/100g),le arance (2,4 mg/100g), l'ananas (2 mg/100g) e i lamponi (5 mg/100g).
5 HO OH COOH COOH O O HOOC COOH CH 3 Ac. etandioico Ac. Butandioico Ac. Ciclopentanoico (Ac. Ossalico) (Ac. Succinico) Ac. 3-metilbenzencarbossilico Br O H 3 C COOH O COOH H 2 C COOH H 3 C Br COOH Ac. 2-bromopropanoico Ac. 3-oxopropanoico Ac. Propenoico Ac. 3-bromo-4-oxopentanoico
6 HO OH O Il rabarbaro è fonte di acido ossalico O HO Ac. trans-3-clorociclopentancarbossilico Acido ciclopentancarbossilico COOH COOH HOOC COOH L acido succinico è presente nel vino invecchiato deriva dalla fermentazione alcolica HOOC C H CH COOH Ac. fumarico (Ac. trans-2-butendioico) HOOC CH 3 C H C H COOH Ac. maleico (Ac. cis-2-butendioico)
7 Acidi carbossilici a catena alifatica
8 Acidi bicarbossilici a catena alifatica
9 I primi termini della serie sono liquidi incolori con odori pungenti o sgradevoli. Per esempio l odore del nostro corpo è formato da una miscela di acidi carbossilici a lunga catena. Ciascuno di noi ha la propria miscela ed è per questo che i cani riescono a individuare una persona dopo averne annusato gli indumenti Composti polari e, come gli alcoli, formano legami idrogeno con se stessi o con altre molecole. Di conseguenza: punti di ebollizione più elevati, degli alcoli di pari peso molecolare. [es. l'acido acetico e l'alcol propilico hanno lo stesso peso formula (60) e bollono rispettivamente a 118 C e 97 C]. Ciò è dovuto al fatto che si possono formare forti legami idrogeno che portano alla formazione di dimeri. Come dimeri sono solubili anche nei solventi relativamente non polari.
10
11 Acidi carbossilici Proprietà chimiche del gruppo carbossilico Possono essere dedotte dal profilo di distribuzione della carica elettronica accumulo di carica negativa O relativamente basico Carbonio non particolarmente elettrofilo Il carbonile degli acidi carbossilici è meno reattivo con i nucleofili rispetto al carbonile di aldeidi e chetoni per via della risonanza: accumulo di carica positiva H relativamente acido Acido carbossilico aldeide Strutture risonanti della funzione carbossilica Reazione sfavorita Nu: Rezione favorita Strutture risonanti della funzione carbonilica
12 Acidi carbossilici Proprietà chimiche del gruppo carbossilico La maggiore acidità del gruppo OH del carbossile rispetto a quello alcolico è dovuta al fatto che l idrogeno che viene strappato in un acido permette la delocalizzazione della carica negativa che si forma e non viene bloccata sull ossigeno (come in un alcol), ma è distribuita sui due ossigeni per risonanza. carbossilato (carica negativa delocalizzata sui due ossigeni) Infatti i due legami con C O, che hanno lunghezza diversa (1.23 Å il legame doppio e 1.36 Å il singolo), diventano di uguale lunghezza (1.27 Å) nell anione carbossilato. + Alcossido (carica negativa ferma) Distribuzione della carica elettronica nell anione carbossilato
13 Gli acidi carbossilici si dissociano in acqua dando luogo ad un anione carbossilato ed uno ione idronio:
14 Acidi carbossilici Proprietà chimiche
15 Acidi carbossilici Effetto induttivo della risonanza Fra acidi carbossilici le acidità possono variare a seconda degli altri gruppi presenti nella molecola. - Es. tra l'acido acetico e gli acidi mono-, di- e tricloroacetico, l'acidità aumenta di volte, ciò è dovuto all'effetto induttivo dei gruppi vicini al carbossile. Il legame Cl C diventa polare con il (C + ) ed il (Cl - ), rispetto a quanto avveniva con CH 3 COOH non sostituito. Maggiore è il numero di atomi di Cl, tanto maggiore è la delocalizzazione della carica e maggiore la forza dell'acido.
16 Acidi carbossilici Effetto induttivo dei sostituenti L effetto trasmette la carica lungo i legami, polarizzando gli elettroni di legame in direzione degli atomi più elettronegativi. Se il Cl (o un altro atomo molto elettronegativo) è posizionato su un carbonio più lontano dal carbossile, l effetto induttivo è molto minore e si riduce ulteriormente con l aumentare della distanza dal gruppo carbossilato. Quindi l acido 2-clorobutanoico è molto più acido del 3-clorobutanoico.
17 Acidi carbossilici Reazioni degli acidi carbossilici La maggior parte delle reazioni degli acidi carbossilici produce derivati ottenuti tramite un attacco nucleofilo sull'atomo di carbonio carbonilico. Tutti si ottengono sostituendo il gruppo -OH di un acido carbossilico con i gruppi OR (-SR), -Cl, -NH 2, RCOO- Gruppo Derivato N.B.Tutti i derivati degli acidi carbossilici possono essere OR (-SR) Esteri (Tioesteri) riconvertiti per idrolisi nell acido -Cl Cloruri acilici carbossilico -NH 2 Ammidi RCOO- Anidridi Alfa-alogenazione L introduzione di un alogeno in posizione alfa rispetto al carbonile di un acido carbossilico simile a quella vista per aldeidi e chetoni è più difficile (gli acidi carbossilici presentano una forma enolica in percentuale inferiore a quanto avviene per aldeidi e chetoni), vengono -brominati utilizzando tricloruro di fosforo come catalizzatore reazione di Hell-Volhard-Zelinsky
18 Derivati degli Acidi carbossilici Composti nei quali l'ossidrile carbossilico è stato sostituito da altri gruppi. Esteri e ammidi sono molto diffusi in natura e per idrolisi danno corrispondenti O O acidi carbossilici. R C OR' R C NH 2 Estere Ammide
19 1.Riduzione Acidi carbossilici Reazioni Trattando gli acidi carbossilici con un riducente come l idruro di litio e alluminio (Li AlH 4 ) in etere etilico anidro o l idruro di sodio e boro (NaBH 4 ) in soluzione acquosa si ottiene il relativo alcol primario RCOOH(l) + 4 [H] Acido carbossilico RCH 2 OH(l) + H 2 O(l) Alcol 2.Reazione con cloruro di fosforo (V) Quando un acido carbossilico reagisce col pentacloruro di fosforo, il gruppo OH dell acido viene sostituito da un atomo di cloro formando il cloruro acilico, con formula generale RCOCl. RCOOH + PCl 5 Acido carbossilico RCOCl + HCl Cloruro acilico acido cloridrico I cloruri acilici sono più reattivi dei corrispondenti acidi carbossilici e nell industria sono preferiti per la maggiore velocità delle loro reazioni. Per reazione con l ammoniaca danno le ammidi primarie: RCOCl + NH 3 Cloruro acilico ammoniaca RCONH 2 + HCl Ammide acido Cloridrico
20 3.Esterificazione: reazione di sostituzione nucleofila acilica tra alcoli e acidi carbossilici che, eseguita a caldo e in ambiente acido per acido solforico, porta alla formazione degli esteri, i più importanti derivati degli acidi carbossilici. Poiché la reazione è reversibile, bisogna allontanare l estere via via che si forma. Acidi carbossilici Reazioni Reazione di esterificazione Reazione di idrolisi Nella reazione di idrolisi la molecola di acqua attacca il carbonio del carbonile agendo da nucleofilo. La reazione deve essere catalizzata da acidi per la scarsa nucleofilicità della molecola dell acqua che rende la reazione molto lenta. L acetato di isoamile ha un forte odore di banana e viene utilizzato per aromatizzare gli alimenti. Prodotto in natura dalla pianta di banane, viene sintetizzata a partire da acido acetico e 3-metil-1-butanolo (alcol isoamilico). Viene inoltre rilasciato dai pungiglioni delle api come feromone per attirare altre api. etanoato di 3-metil-1-butile Industrialmente gli esteri si preparano per reazione dei cloruri acilici con gli alcoli (o i fenoli), dato che questa reazione è completa. Quasi tutti gli aromi utilizzati nell industria alimentare non sono esteri naturali ma di sintesi.
21 Acidi carbossilici Salificazione Gli acidi carbossilici reagiscono anche con le basi forti per formare dei sali. Esempi per la nomenclatura
22 Acidi carbossilici Salificazione Proprietà dei Sali Di solito sono solidi e non hanno odore. I sali carbossilati di Na +, K +, Li + e NH 4+ sono solubili in acqua. I saponi sono i sali di sodio solubili di acidi grassi a lunga catena. Coda non polare Testa polare controione H 2 O
23 Acidi carbossilici Saponificazione La saponificazione è una reazione acido base o meglio l'idrolisi basica (di solito si impiega soda caustica,naoh) di un trigliceride, che può essere un estere o acido grasso, per produrre il corrispettivo sale sodico (carbossilato di sodio). E il processo attraverso il quale vengono prodotti i saponi a partire da grassi e idrossidi di metalli alcalini. Assieme al sapone, i tradizionali processi di saponificazione producono glicerolo. Tutte le sostanze che per idrolisi basica possono produrre dei saponi sono dette saponificabili. Al sapone si possono poi aggiungere additivi per conferirgli caratteristiche particolari (ad esempio sabbia e pomice per renderlo abrasivo), coloranti e profumi per migliorarne l aspetto e la gradevolezza. Estere di un trigliceride Sale alcalino (sapone) gliceriolo A seconda del tipo di base utilizzata nella loro preparazione, i saponi acquistano proprietà differenti. L'idrossido di sodio (NaOH) genera saponi solidi, l idrossido di potassio (KOH), dà luogo a saponi liquidi.
24 Applicazioni dei saponi La conoscenza della saponificazione è attinente a molti campi delle tecnologie e della vita di ogni giorno. Saponi liquidi e solidi A seconda del tipo di base utilizzata nella loro preparazione, i saponi acquistano proprietà differenti. L'idrossido di sodio (NaOH) genera saponi solidi, mentre se si impiega idrossido di potassio (KOH), si formano saponi liquidi. Grasso al litio I derivati del 12-idrossistearato e del litio e molti altri acidi carbossilici sono importanti costituenti di grassi lubrificanti. Nello specifico, i carbossilati di litio fungono da addensanti. Anche i saponi complessi sono piuttosto comuni, essendo combinazioni di saponi metallici, come saponi di litio e calcio.
25 Estintori Gli incendi di grassi di cottura e olii bruciano a temperature maggiori di quelli causati da liquidi infiammabili, rendendo inefficace un normale estintore di classe B. I liquidi infiammabili hanno un flash point inferiore a 50 C. L'olio alimentare è un liquido combustibile, perché ha un punto di infiammabilità superiore ai 50 gradi. Incendi del genere dovrebbero essere spenti con un estintore chimico. I dispositivi di questo tipo sono progettati per estinguere i grassi e gli oli di cottura attraverso la saponificazione. L'agente estinguente converte rapidamente la sostanza che sta bruciando in un sapone non-combustible. Questo processo è endotermico, cioè assorbe l'energia termica dall'ambiente circostante inibendo ulteriormente il fuoco. STORIA DEL SAPONE
26 Palmitato di sodio Meccanismo di azione dei saponi Utilizzato come detergente, il sapone ha funzione di tensioattivo. La molecola di sapone è costituita da una parte idrocarburica (coda) idrofoba, ma solubile in sostanze organiche poco polari e da un estremità ionica (testa) che è invece idrofila. Il potere pulente della miscela acqua-sapone è attribuito all'azione delle micelle, piccole sferette rivestite all'esterno di gruppi polari idrofilici (la testa della molecola) e contenente all'interno una tasca idrofobica costituita dalle code idrofobiche che disciolgono le sostanze grasse. Aggiungendo un sapone all acqua contenente lo sporco (in genere di natura grassa), la coda si scioglie nelle particelle di sporco, mentre la testa crea dei legami deboli con le molecole dell acqua. Agitando l acqua, lo sporco viene completamente circondato dal detergente, cioè solubilizzato e rimosso. Meccanismo di azione di un sapone
27 Possono essere preparati in diversi modi, alcuni dei quali sono: 1. Ossidazione di alcoli primari e di aldeidi 2. Ossidazione di catene laterali alchiliche di anelli aromatici 3. Idrolisi dei nitrili
28 1. Ossidazione di alcoli primari e di aldeidi
29 Ossidazione di catene laterali alchiliche di anelli aromatici Gli anelli aromatici sono molto resistenti all ossidazione anche in presenza di forti agenti ossidanti quali il permanganato di potassio o il dicromato di sodio (si ricordi che con il termine di ossidazione si intende l aggiunta di ossigeno, la diminuzione di idrogeno o la perdita di elettroni). Se però un anello aromatico presenta un sostituente alchilico come il gruppo metilico, etilico, ecc. tali composti possono essere facilmente ossidati:
30 Ossidazione di catene laterali alchiliche di anelli aromatici
31 Se non sono presenti legami C H di tipo benzilico, si ossida l anello aromatico, anche se sono necessarie condizioni più drastiche. (CH 3 ) 3 CCOOH
32 Industrialmente si utilizzano ossidanti diversi dal permanganato di potassio. L acido tereftalico, per esempio, uno dei prodotti di partenza per preparare il Dacron (polietilentereftalato-pet) Si produce per ossidazione all aria in presenza di Sali di Co (III) come catalizzatori Il dacron è una fibra che rimane inalterata all umidità
33 L acido ftalico, usato per preparare resine,coloranti e plastificanti, si ottiene nelle stesse condizioni di reazione, per ossidazione dell orto-xilene O 2,Co(III) CH 3 CO2H acido 1,2-benzendicarbossilico Braccialetti provenienti dalla cina e sequestrati perché contenenti acido ftalico, aggiunto per migliorarne la flessibilità
34 Idrolisi dei nitrili Il triplo legame carbonio-azoto dei cianuri organici può essere idrolizzato a carbossile, sia in ambiente acido che basico. In ambiente acido l azoto del cianuro si ritrova alla fine sotto forma di ione Ammonio. In ambiente basico si forma invece il sale dell acido carbossilico e ammoniaca. Per avere l acido libero, bisogna neutralizzare in uno stadio successivo.
35 Acidi carbossilici: derivati I derivati degli acidi carbossilici si ottengono per reazioni di sostituzione nucleofila acilica del gruppo carbossilico. Cloruri acilici Anidridi Esteri Ammidi
36 Nomenclatura dei derivati degli acidi carbossilici 1) Gli esteri RCOOR prendono il nome dall acido, cambiando il suffisso da -ico ad -ato, seguito dal nome del radicale alchilico R presente nel gruppo OR 2) I cloruri acilici con struttura: RCOCl prendono il nome dall acido, cambiando il suffisso -ico in ile. O 3) Le ammidi con struttura C RCONH R NH 2 2 prendono il nome dall acido, cambiando il suffisso -oico in ammide.
37 4) Le anidridi con struttura generale prendono il nome dai gruppi acilici che le formano con suffisso -oico RCOOCOR Anidride etanoica 5) I nitrili, con struttura generale R-C N, usano la desinenza onitrile e la radice della catena carboniosa più lunga contenente il gruppo ciano. In alternativa vengono anche nominati come cianuri alchilici. CH 3 CN Etanonitrile (Acetonitrile) (Cianuro di metile) Etanonitrile (Cianuro di metile) CH 3 CH 2 CN propanonitrile (Cianuro di etile) N.B. I nitrili possono essere classificati come derivati degli acidi carbossilici perché possono essere convertiti in acidi carbossilici tramite idrolisi.
ACIDI CARBOSSILICI. ac. formico ac. acetico ac. benzoico
 ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Nomenclatura e nomi comuni Struttura e proprietà Fonti Reazioni Derivati degli acidi carbossilici
 Acidi carbossilici e derivati Nomenclatura e nomi comuni Struttura e proprietà Fonti Reazioni Derivati degli acidi carbossilici Acidi carbossilici Acidi carbossilici Composti carbonilici Gli acidi carbossilici
Acidi carbossilici e derivati Nomenclatura e nomi comuni Struttura e proprietà Fonti Reazioni Derivati degli acidi carbossilici Acidi carbossilici Acidi carbossilici Composti carbonilici Gli acidi carbossilici
Acido citrico. Nome IUPAC: Acido 3-carbossi-3-idrossi-1,5-pentandioico
 Acidi carbossilici Dove si trovano? 2 Acido citrico L'acido citrico è uno degli acidi più diffusi negli organismi vegetali ed è un prodotto metabolico di tutti quelli aerobici. Il succo di limone ne contiene
Acidi carbossilici Dove si trovano? 2 Acido citrico L'acido citrico è uno degli acidi più diffusi negli organismi vegetali ed è un prodotto metabolico di tutti quelli aerobici. Il succo di limone ne contiene
Acidi carbossilici e derivati
 Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi Carbossilici CH 3. Caratterizzati dalla presenza di un gruppo carbossilico. Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico)
 Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Acidi Carbossilici Caratterizzati dalla presenza di un gruppo carbossilico CH 3 H Acido etanoico (Acido Acetico) Acido metanoico (Acido Formico) Struttura del gruppo carbossilico δ- CH 3 δ+ Il legame è
Capitolo 8 Acidi Carbossilici e Derivati
 Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Acidi carbossilici. IUPAC catena più lunga contenente il gruppo -COOH al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita con -oico
 Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Acidi carbossilici. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Composti Carbossilici. Acidi Carbossilici
 Composti Carbossilici Acidi Carbossilici ACIDI CARBSSILICI Gli acidi carbossilici sono caratterizzati dalla presenza del gruppo carbonilico legato ad un gruppo idrossilico R C Il gruppo carbossilico viene
Composti Carbossilici Acidi Carbossilici ACIDI CARBSSILICI Gli acidi carbossilici sono caratterizzati dalla presenza del gruppo carbonilico legato ad un gruppo idrossilico R C Il gruppo carbossilico viene
14/11/2018. Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile.
 Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Gruppo carbonilico. Il gruppo carbonilico è caratterizzato dalla presenza C=O ed i composti che lo contengono vengono definiti composti carbonilici.
 Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile
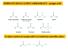 DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Acidi carbossilici e derivati Composti organici che contengono legami doppi C=O e legami singoli C-eteroatomo (oppure il gruppo CN)
 himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
chiamato i questo modo a causa della presenza del gruppo carbonilico e del gruppo idrossilico. C sp 2 ibrido di risonanza del gruppo carbossilico
 ACIDI CARBOSSILICI ACIDI CARBOSSILICI Gli acidi carbossilici isono caratterizzati idll dalla presenza dl del gruppo carbossilico, chiamato i questo modo a causa della presenza del gruppo carbonilico e
ACIDI CARBOSSILICI ACIDI CARBOSSILICI Gli acidi carbossilici isono caratterizzati idll dalla presenza dl del gruppo carbossilico, chiamato i questo modo a causa della presenza del gruppo carbonilico e
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Acidi carbossilici: nomenclatura. alcano -> acido alcanoico
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Si trovano generalmente come dimeri ciclici a causa dei legami a idrogeno
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Isomeria ottica. Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi.
 Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Introduzione alla biochimica AO 11/14
 Introduzione alla biochimica AO 11/14 Il Gruppo Carbonilico 1. E uno dei gruppi funzionali più importanti 2. Sp2, legame polarizzato 1. Ossigeno elettronegativo: effetto induttivo 2. Effetto di risonanza
Introduzione alla biochimica AO 11/14 Il Gruppo Carbonilico 1. E uno dei gruppi funzionali più importanti 2. Sp2, legame polarizzato 1. Ossigeno elettronegativo: effetto induttivo 2. Effetto di risonanza
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Derivati degli acidi carbossilici
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Derivati degli acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Derivati degli acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze
Composti carbonilici: Aldeidi Chetoni Acidi carbossilici Alogenuri acilici Esteri Ammidi Anidridi Nitrili
 Composti carbonilici: Aldeidi Chetoni Acidi carbossilici Alogenuri acilici Esteri Ammidi Anidridi Nitrili Struttura di composti carbonilici sp 2 sp 2 C = C H 3 C CH3 Il carbonile è un raggruppamento atomico
Composti carbonilici: Aldeidi Chetoni Acidi carbossilici Alogenuri acilici Esteri Ammidi Anidridi Nitrili Struttura di composti carbonilici sp 2 sp 2 C = C H 3 C CH3 Il carbonile è un raggruppamento atomico
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI
 I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI
 IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
IDENTIFICAZIONE DEGLI ACIDI CARBOSSILICI Acidi carbossilici Stato fisico alifatici il primo termine degli ac. carbossilici alifatici è l'acido formico, che avendo un p.e. di 100,5 C, è liquido a temperatura
Capitolo 24 Le famiglie dei composti organici
 Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
FENOLI: nomenclatura IUPAC
 FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
Ammine R N + H. ammina terziaria ammina secondaria ammina primaria sale di ammonio quaternario
 AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
ACIDI CARBOSSILICI e derivati
 ACIDI CABSSILICI e derivati Il nome sistematico di un acido carbossilico alchilico si fa derivare dal nome dell idrocarburo con lo stesso numero di atomi di carbonio, sostituendo la o finale con la desinenza
ACIDI CABSSILICI e derivati Il nome sistematico di un acido carbossilico alchilico si fa derivare dal nome dell idrocarburo con lo stesso numero di atomi di carbonio, sostituendo la o finale con la desinenza
Introduzione alla Chimica Organica V Ed.
 William H. Brown - Thomas Poon Introduzione alla Chimica Organica V Ed. Capitolo 2 2.1 Cosa sono gli acidi e le basi secondo Arrhenius? Un Acido di Arrhenius è una sostanze che sciolta in acqua produce
William H. Brown - Thomas Poon Introduzione alla Chimica Organica V Ed. Capitolo 2 2.1 Cosa sono gli acidi e le basi secondo Arrhenius? Un Acido di Arrhenius è una sostanze che sciolta in acqua produce
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Aldeidi e Chetoni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
CHIMICA ORGANICA. Gli idrocarburi aromatici
 1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
CLASSIFICAZIONE E NOMENCLATURA DEI COMPOSTI CHIMICI
 CLASSIFICAZIONE E NOMENCLATURA DEI COMPOSTI CHIMICI Valenza e numero di ossidazione La capacità di combinazione di un elemento è chiamata valenza, e corrisponde al numero di legami che un atomo di quell
CLASSIFICAZIONE E NOMENCLATURA DEI COMPOSTI CHIMICI Valenza e numero di ossidazione La capacità di combinazione di un elemento è chiamata valenza, e corrisponde al numero di legami che un atomo di quell
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1
 CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
CHIMICA DEGLI IONI ENOLATO ED ENOLI LEZIONE 1 ACIDITÀ Ragionare sulla base coniugata: quanto più la base coniugata è stabilizzata (è debole) tanto più l'acido sarà forte. ASPETTI CHE DETERMINANO LA STABILITA
Aldeidi e chetoni. 1) Rottura α 2) Rottura i. Più pronunciate nei chetoni. 3) Rottura β con trasposizione di H in γ (McLafferty)
 Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
R = GRUPPO FUNZIONALE Atomo o raggruppamento atomico
 GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Nomenclatura chimica
 Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
Alcoli ed eteri Composti organici che contengono legami singoli C-O
 Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli e Tioli. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Nomenclatura chimica
 Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
Capitolo 13 Acidi Carbossilici e Derivati
 himica rganica Informazione Scientifica sul Farmaco apitolo 13 Acidi arbossilici e Derivati rganic hemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic hemistry, 3 rd Edition Paula Y. Bruice, Prentice
himica rganica Informazione Scientifica sul Farmaco apitolo 13 Acidi arbossilici e Derivati rganic hemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic hemistry, 3 rd Edition Paula Y. Bruice, Prentice
23 Le diverse classi di composti organici
 23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
Domanda 4 Dal punto di vista della reattività, il doppio legame si comporta spesso da:
 Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
p p s sp sp sp s p p 1
 p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
CHIMICA ORGANICA. Gli alchini
 1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
GRUPPI FUNZIONALI GLI ALCOLI
 GRUPPI FUNZIONALI In chimica organica è detto gruppo funzionale una parte della struttura di una molecola caratterizzata da specifici elementi (atomi) e da una struttura ben definita e precisa, che conferisce
GRUPPI FUNZIONALI In chimica organica è detto gruppo funzionale una parte della struttura di una molecola caratterizzata da specifici elementi (atomi) e da una struttura ben definita e precisa, che conferisce
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Esteri degli acidi carbossilici
 Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
CHIMICA. F 20 Classi di composti organici
 CHIMICA F 20 Classi di composti organici 1 I gruppi funzionali I composti di cui ci siamo interessati fin qui sono idrocarburi, cioè composti costituiti soltanto da carbonio e idrogeno. In molte molecole
CHIMICA F 20 Classi di composti organici 1 I gruppi funzionali I composti di cui ci siamo interessati fin qui sono idrocarburi, cioè composti costituiti soltanto da carbonio e idrogeno. In molte molecole
Reazioni degli Alogenuri Alchilici. Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici.
 Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
Reazioni degli Alogenuri Alchilici Reazioni di sostituzione nucleofila alifatica degli alogenuri alchilici. Un nucleofilo ( reagente amante del nucleo) è un qualsiasi reagente che dona una coppia non condivisa
Ammine. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, Nominativo.Matricola
 Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, 19-06-2017 Nominativo.Matricola Esercizio 1a. Il cis-2-pentene viene trattato con Br 2 in diclorometano. a) Descrivere
Corso di Laurea Triennale in Biotecnologie, AA 2016/17, Esame di Chimica Organica, 19-06-2017 Nominativo.Matricola Esercizio 1a. Il cis-2-pentene viene trattato con Br 2 in diclorometano. a) Descrivere
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI
 RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
RIEPILOGO DEI PRINCIPALI COMPOSTI ORGANICI Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione. Idrocarburi:
REAZIONI CHIMICHE. Idrogeno + ossigeno acqua
 REAZIONI CHIMICHE Reagenti Prodotti L unità che si conserva è l atomo, durante una reazione cambia solo la disposizione relative degli atomi. Si rompono i legami chimici tra le molecole dei reagenti e
REAZIONI CHIMICHE Reagenti Prodotti L unità che si conserva è l atomo, durante una reazione cambia solo la disposizione relative degli atomi. Si rompono i legami chimici tra le molecole dei reagenti e
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di:
 Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcoli
 Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
Composti Carbossilici. Derivati Carbossilici
 omposti arbossilici Derivati arbossilici Derivati degli Acidi I derivati degli acidi carbossilici hanno attaccato al gruppo carbonilico anziché l'idrossile (-) altri gruppi elettron attrattori come: -N
omposti arbossilici Derivati arbossilici Derivati degli Acidi I derivati degli acidi carbossilici hanno attaccato al gruppo carbonilico anziché l'idrossile (-) altri gruppi elettron attrattori come: -N
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico
 Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
Gli alcoli vengono classificati come primari, secondari e terziari in base alla natura del carbonio che lega il gruppo ossidrilico Legami idrogeno. Il legame carbonio-ossigeno è un legame polare, con una
L acqua e il legame idrogeno
 Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
I composti del carbonio
 Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Acido maleico anidride maleica acido ftalico andidride ftalica
 Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
I composti acilici sono tutti quei composti che contengono il gruppo:
 omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
omposti acilici I composti acilici sono tutti quei composti che contengono il gruppo: X in cui, contrariamente a quello che si ha nei composti carbonilici, X è un atomo o gruppo più elettronegativo di.
REATTIVITÀ DI R-XR M + R
 ... X.. M. M. M. M. M 2e- trasferiti dalla superficie metallica in 1 o 2 stadi EATTIVITÀ DI -X... X. -.. Ṙ.. - M + M + δ- δ+ -M nucleofilo -X elettrofilo 1) EAZIONE DI WUTZ -X + - Na + - + Na + X - 2)
... X.. M. M. M. M. M 2e- trasferiti dalla superficie metallica in 1 o 2 stadi EATTIVITÀ DI -X... X. -.. Ṙ.. - M + M + δ- δ+ -M nucleofilo -X elettrofilo 1) EAZIONE DI WUTZ -X + - Na + - + Na + X - 2)
Nomenclatura delle sostanze chimiche
 Nomenclatura delle sostanze chimiche SOSTANZE CHIMICHE!1 ELEMENTI Metalli Non metalli COMPOSTI Ossidi Anidridi Idrossidi Acidi Sali Idruri - ossiacidi - idracidi METALLI!2 Duttili Malleabili Buoni conduttori
Nomenclatura delle sostanze chimiche SOSTANZE CHIMICHE!1 ELEMENTI Metalli Non metalli COMPOSTI Ossidi Anidridi Idrossidi Acidi Sali Idruri - ossiacidi - idracidi METALLI!2 Duttili Malleabili Buoni conduttori
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
DAI GRUPPI FUNZIONALI AI POLIMERI
 DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
3. Le Reazioni Chimiche
 . Le Reazioni Chimiche Equazioni Chimiche e Reazioni Chimiche il simbolismo delle reazioni chimiche il bilanciamento delle equazioni chimiche Reazioni di Precipitazione le soluzioni acquose le reazioni
. Le Reazioni Chimiche Equazioni Chimiche e Reazioni Chimiche il simbolismo delle reazioni chimiche il bilanciamento delle equazioni chimiche Reazioni di Precipitazione le soluzioni acquose le reazioni
H N H R N H R N R R N R H H H
 AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
ACIDI E BASI ORGANICI: pka e ph
 Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 12 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 12 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI
 REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
