15 Equilibri chimici in fase gassosa
|
|
|
- Orsola Valentino
- 6 anni fa
- Visualizzazioni
Transcript
1 15 Equilibri himii i fase gassosa roblemi risolti A) I u oteitore del volume di L a 7 C vegoo itrodotti 85 g di NH. Si stabilise il seguete equilibrio NH N + H Sapedo he la K vale 9. 10, alolare a) la oetrazioe delle speie himihe i equilibrio, la pressioe eseritata dalla misela gassosa all'equilibrio e la Kp; b) ome variao le oetrazioi e la pressioe della misela dopo aver lasiato he il sistema si espada, a temperatura ostate, da u volume di l a u volume di 8 L. a) Caloliamo la oetrazioe iiziale dell'ammoiaa W m [ NH ] iiz 1,5mol / l se idihiamo o X la oetrazioe dell'azoto all'equilibrio, dall'aalisi dei oeffiieti stehiometrii deduiamo he ogi X moli di NH he reagisoo se e formao X di N e X di H. Costruiamo ua tabella i ui ompaiao le oetrazioi iiziali e di equilibrio di tutte le speie himihe i fuzioe di X. iiziale [NH ] 1,5 1,5 - X [N ] 0 X [H ] 0 X Determiiamo ora il valore di X tramite la relazioe di Guldberg-Waage [ N ], [ H ] K [ NH ]
2 all'itero della quale sostituiamo i valori delle oetrazioi di equilibrio o quelli espressi i fuzioe di X he troviamo ella tabella preedete, otteedo 9, 10 X,( X ) ( 1, 5 - X ) estraedo la radie quadrata di etrambi i membri si ottiee la seguete equazioe di grado 5,196X 1,5- X, 16 he risolta forise il seguete valore X 0,585 mol/l. Sostitedo tale valore possiamo ora alolare le oetrazioi di equilibrio NH eq 1,5 - X 1,5 -. 0,585 0,08 mol/l N eq X 0,585 mol/l H eq X. 0,585 1,755 mol/l Caloliamo ora la pressioe totale all'equilibrio er la legge di Dalto sulle misele gassose, la pressioe totale è uguale alla somma delle pressioi parziali + + tot NH N H La pressioe parziale di iasu gas è alolabile tramite l'equazioe di stato dei gas perfetti. Ad esempio per l'ammoiaa essa è pari a NH RT M NH NH RT sostituedo i valori osì trovati per tutti e tre i gas ella relazioe di Dalto si ottiee ( ) ( ) tot M NH + M N + M H RT 0, , , 755, 0. 08, atm Caloliamo ora la Kp L ( ) ( ) Kp K RT 9, 10 0, 08, ,, 10 6 b) Caloliamo le uove oetrazioi di equilibrio e la pressioe dopo l'espasioe. Aumetare il volume del reipiete sigifia i pratia dimiuire la pressioe. er il priipio di Le Chatelier i dobbiamo attedere he il sistema modifihi il suo equilibrio spostadosi verso destra dove soo preseti u umero maggiore di moli. Rialoliamo la oetrazioe iiziale dell'ammoiaa he passa da 1,5 mol/l a W m [ NH ] iiz 0,65mol / l Rialoliamo ora le oetrazioi di equilibrio a partire da ua oetrazioe iiziale di NH pari a 0,65 mol/l iiziale [NH ] ,65 - X [N ] 0 X [H ] 0 X Determiiamo il valore di X tramite la relazioe di Guldberg-Waage 9, 10 X, ( X ) ( 0, 65- X ) Dopo aver estratto la radie quadrata e risolto l'equazioe di grado si ottiee il seguete valore X 0,0 mol/l
3 le uove oetrazioi di equilibrio sarao periò [NH] eq 0,65 - X 1,5 -. 0,0 0,01 mol/l [N] eq X 0,0 mol/l [H] eq X. 0,0 0,906 mol/l La peretuale di moli he hao reagito all'equilibrio è ora pari a X [ NH ] iiz 100 0, ,65 Metre quado il volume era di L tale peretuale risultava pari a X [ NH ] iiz 100 1, ,5 96,6% 9,6% Duque la dimiuzioe della pressioe ha spostato l'equilibrio verso destra (ua peretuale maggiore di moleole di NH hao ifatti reagito) La pressioe totale all'equilibrio è ora pari a ( ) ( ) tot MNH + MN + M H RT 0, 01+ 0, 0 + 0, 906, 0. 08, , 5atm B) I u reattore di 1 litro a 000 K vegoo itrodotti 57, g di CO e,6 g di H, Si stabilise il seguete equilibrio CO + H CO +H O Sapedo he a 000 K la K 0, alolare a) le oetrazioi di equilibrio b) ome variao le oetrazioi di equilibrio se vegoo itrodotti 7 g di CO ) ome variao le oetrazioi di equilibrio se la oetrazioe iiziale di H è M d) quale deve essere la oetrazioe iiziale di H affihè il vapor d'aqua he si forma sviluppi all'equilibrio ua pressioe parziale di 0 atm. Caloliamo la oetrazioe iiziale di CO e di H W [ CO ] iiz 1, mol / l m 57, 1 W [ H ] iiz 1, mol / l m,6 Idihiamo o X la oetrazioe di CO all'equilibrio e ostruiamo la seguete tabella 1 iiziale [CO ] 1, 1, - X [H ] 1, 1, - X [CO] 0 X [H O] 0 X Determiiamo il valore di X tramite la relazioe di Guldberg-Waage K [ CO][ H O] [ CO ][ H ] ( 1, - X ) Estraedo la radie quadrata di etrambi i membri e risolvedo si ottiee X X 0,88 mol/l
4 [CO ]eq [H ]eq 1, - X 1, - 0,88 0, mol/l [CO]eq [H O]eq X 0,88 mol/l b) Caloliamo ome variao le oetrazioi di equilibrio itroduedo 7 g di CO. Si tratta di aumetare la oetrazioe di u prodotto di reazioe e per il priipio di Le Chatelier i dovremmo attedere he l'equilibrio regredisa spostadosi a siistra. 7 g di CO orrispodoo a W/m 7/8 0,5 moli La uova tabella delle oetrazioi sarà iiziale Sriviamo la relazioe di equilibrio X X [CO ] 1, 1, - X [H ] 1, 1, - X [CO] 0,5 X + 0,5 [H O] 0 X ( + 0, 5) ( 1, - X ) si ottiee u'equazioe di grado he risolta da il seguete risultato X 0,8 mol/l Le uove oetrazioi di equilibrio divetao [CO ]eq 1, - X 1, - 0,8 0,57 mol/l [H ]eq 1, - X 1, - 0,8 0,57 mol/l [CO]eq X + 0,5 0,8 + 0,5 1,09 mol/l [H O]eq X 0,8 mol/l Come si può otare la oetrazioe dei reageti è aumetata (0,57 > 0,) rispetto al aso preedete: l'equilibrio si è spostato a siistra. ) aloliamo ome variao le oetrazioi di equilibrio se la oetrazioe iiziale di H e M azihè 1, M. Ci si deve attedere he, aumetado la oetrazioe di u reagete l'equilibrio si sposti verso destra. La uova tabella delle oetrazioi sarà iiziale Sriviamo la relazioe di equilibrio [CO ] 1, 1, - X [H ] - X [CO] 0 X [H O] 0 X risolvedo l'equazioe otteiamo X 1,0 mol/l Le uove oetrazioi di equilibrio divetao [CO ]eq 1, - X 1, - 1,0 0,58 mol/l [H ]eq - X - 1,0 0,958 mol/l [CO]eq X 1,0 1,0 mol/l [H O]eq X 1,0 mol/l X ( 1, - X )( - X ) Come si può otare la oetrazioe dei prodotti di reazioe è aumetata (1, > 0,88) rispetto al aso a): l'equilibrio si è spostato a destra. d) Caloliamo he oetrazioi iiziali devoo avere i reageti affihè il vapor d'aqua all'equilibrio sviluppi ua pressioe parziale di 0 atm.
5 Dalla equazioe di stato dei gas aloliamo he oetrazioe deve avere il vapor d'aqua per svilippare ua pressioe di 0 atm a 000 K da ui H O O RT M H HO RT H O 0 M H O 0,1mol / l RT 0,08, 000 Se la oetrazioe di equilibrio del vapor d'aqua è pari a 0,1 mol/l se e dedue he 0,1 mol/l di H e altrettate di CO hao reagito e devoo essere sottratte alle rispettive oetrazioi iiziali osto quidi pari ad Y la oetrazioe iiziale di H, le oetrazioi di equilibrio sarao iiziale [CO ] Y Y - 0,1 [H ] Y Y - 0,1 [CO] 0 0,1 [H O] 0 0,1 la relazioe di equilibrio diveta 01, ( Y - 01, ) he risolta forise il seguete valore Y 0,18 mol/l La oetrazioe iiziale dell'idrogeo deve quidi essere Y [H ]iiz 0,18 mol/l C) I u reipiete a 60 C vegoo itrodotti 18 g di N O e g di. Si stabilise il seguete equilibrio N O Sapedo he a 60 C la K 8, e he all'equilibrio la pressioe totale della misela è pari a 1,7 atm, alolare la pressioe parziale, la oetrazioe delle due speie himihe all'equilibrio e il volume del reipiete. Caloliamo la Kp della reazioe L - ( ) ( ) Kp K RT 8, 75, 10 0, 08,, 9 1 Caloliamo il umero di moli itrodotte W 18 N O N O 1, 5 mn O 9 W moli 0, 5moli m 6 osto pari ad X il umero di moli di ipoazotide N O he reagisoo, X sarao le moli di biossido di azoto he si formao. All'equilibrio sarao quidi preseti (1,5 - X) moli di N O (0,5 + X) moli di per u totale di (1,5 - X) + (0,5 + X) ( + X) moli Le frazioi molari di iasu gas e le rispettive pressioi parziali i fuzioe di X sarao periò
6 1,5 - X + X 1,5 - X N O N 1, 7 O,, N O tot tot + X 0,5 + X 0,5 + X 1, 7,, tot + X + X tot Utilizziamo le pressioi parziali ella relazioe di equilibrio espressa ome Kp Kp ( ) ( N O ) Ê 0, 5+ X ˆ Á, 1, 7 Ë + X, 9 15, - X, 17, + X Otteiamo u'equazioe di grado he, risolta, forise il seguete risultato: X 0,69 moli Sostituedo opportuamete il valore trovato possiamo determiare le frazioi molari e le pressioi parziali dei due gas all'equilibrio, he assumoo i segueti valori 1,5 - X N 0,01 O N 0,01 1,7 0, O,, tot + X 0,5 + X 0,699, 0,699, 1, X tot oihè le pressioi parziali all'equilibrio soo direttamete proporzioali alle rispettive oetrazioi di equilibrio, possiamo failmete alolare queste ultime o l'equazioe di stato dei gas perfetti da ui RT M RT 1,08 - M,76, 10 mol / l RT 0,08, e N O 0, - M N O 1,6, 10 mol / l RT 0,08, Caloliamo ora il volume del reipiete oihè all'equilibrio si formao omplessivamete +X + 0,69,69 moli e la pressioe totale è di 1,7 atmosfere, il volume sarà uguale a RT,69, 0.08, 50litri 1,7 Si oti he avedo alolato il volume le oetrazioi di equilibrio potevao essere determiate ahe: 1 1,5-0,69 / eq,5 - X 50 eq - [ N O ] 1,6, 10 mol l 50
7 0 0,5 + 1,8 / eq,5 + X 50 eq - [ ],76, 10 mol l 50 roblemi da risolvere 1. CO + H CO +H O A 110 C le oetrazioi di equilibrio delle diverse speie himihe soo le segueti: [CO ] [H ] [CO] 0,01M [H O] 0,0M Calolare la K. Cl 5 Cl +Cl Sapedo he la ostate di equilibrio a 00 C e' K 0,57 mol/l, alolare quati grammi di etaloruro rimagoo ideomposti all'equilibrio(g) i u reipiete di 0 L. La Coetrazioe iiziale del etaloruro e' 0, M Calolare ioltre la pressioe sviluppata dalla misela dei gas ua volta raggiuto l'equilibrio.. L'aido solfidrio a 1065 C si deompoe seodo la reazioe H S H + S Sapedo he la K 1, mol/l, alolare quati grammi di zolfo si formao all'equilibrio i u reipiete di 5 L i ui la oetrazioe iiziale di aido solfidrio era 0,7M. A 60 C la reazioe N O preseta K 8, mol/l. Se poiamo 50 g di N O gassoso i u reipiete di 1 L, quale sara' la pressioe sviluppata dai due gas all'equilibrio? 5. I u reipiete del volume di 1 L avviee la seguete reazioe: SbCl 5 (g) SbCl (g) + Cl (g) sapedo he a 1 C la Kp vale 0,8 atm, alolare quate moli di SbCl 5 o si deompogoo e soo preseti all'equilibrio se el reipiete vegoo iizialmete itrodotte, moli di SbCl I u reattore portato alla temperatura di 10 K avviee la reazioe C(s) + CO (g) CO(g) per la quale la ostate di equilibrio Kp vale,1 atm. Calolare la omposizioe peretuale della fase gassosa all'equilibrio se la pressioe totale è di 5 atm e la K alla temperatura data. 7. I u reipiete di L alla temperatura di 70 K avviee la seguete reazioe CO (g) + H (g) CO(g) + H O(g) Calolare la quatità i grammi di CO e H O preseti all'equilibrio se iizialmete soo preseti 88 g di CO e g di H. 8. I u reipiete ermetiamete hiuso del volume di 10 L soo stati itrodotti SO e O gassosi. Calolare la ostate K sapedo he all'equilibrio soo preseti 7 moli di SO, moli di SO e 91,5 moli di Nella reazioe H O(g) O (g) + H (g), a 17 C, la ostate di equilibrio vale Kp atm. Calolare la K. 10. I u reipiete di 5 L a 00 C viee itrodotta 1 mole di NH (g). Si produe la seguete reazioe NH N + H Dopo aver bilaiato, alolare K e Kp sapedo he all'equilibrio N 8, M. 11. I u reipiete di 5 L viee itrodotta 1 mole di N e 1 mole di O. Se si risalda la misela fio a 000 C, quate moli di si formerao sapedo he a quella temperatura K 0,1. 1. Data la reazioe N (g) + H (g) NH (g), alolare la K a 00 C, sapedo he i u reipiete di 5 L la misela dei tre gas all'equilibrio è formata da 1 mole di NH, 0,1 moli di N e moli di H.
8 1. I u reipiete di 10 L vegoo itrodotte 10 moli di N e 10 moli di. Calolare la oetrazioe delle speie himihe all'equilibrio per la reazioe N + O (K, ). 1. Il biossido di azoto è u gas i equilibrio o la sua forma dimera, l'ipoazotide, seodo il seguete equilibrio N O Calolare la K di tale reazioe, sapedo he dopo aver iizialmete itrodotto 9 g di biossido i u reipiete di 1 litro si trovao all'equilibrio 0,5 moli di N O. 15. Data la seguete reazioe: Br(g) (g) + Br (g) Calolare la Kp sapedo he a 5 C e ad ua pressioe di 0,5 atm (pressioe totale della misela di gas all'equilibrio) il bromuro di itrosile (Br) è dissoiato al %. 16. Data la seguete reazioe CO(g) + H O(g) CO (g) + H (g) la ui ostate di equilibrio a 986 C vale 0,6; alolare la oetrazioe di equilibrio dell'idrogeo e la pressioe parziale di iasu gas, se ua misela iizialmete omposta di 1 mole di vapor d'aqua e da moli di CO, raggiuge il suo equilibrio ad ua pressioe totale di atmosfere. Calolare ioltre il volume del reipiete e la molarità del vapor d'aqua all'equilibrio. 17. Le ostati di equilibrio Kp delle segueti rezioi vegoo date a 0 C SrCl. 6H O(s) SrCl. H O(s) + H O(g) Kp 6, atm Na HO. 1H O(s) Na HO. 7H O(s) + 5H O(g) Kp 5, atm 5 Na SO. 10H O(s) Na SO (s) + 10H O(g) Kp atm 10 Sapedo he la tesioe di vapore dell'aqua a 0 C è di 58 mm, alolare: a) la tesioe di vapore dell'aqua i equilibrio a 0 C o i tre sali; b) quale dei tre sali reageti è il disidratate più effiae; ) per quali valori di umidità relativa dell'aria Na SO. 10H 0 diveta effloresete a 0 C. 18. A 7 C e 1 atm il 0% delle moleole di ipoazotide si trasformao i biossido di azoto seodo la reazioe N O Determiare la Kp e la K. Risposte 1. K. 58 g 19,65 atm. 1,6 g. 17,6 atm 5. 1, moli 6. 6,% CO e 5,6% CO K, mol/l 7. 18,66 g 1 g 8. 5, (mol/l) -1 9., mol/l 10. K 1,88 (mol/l) Kp 5,8. 10 atm 11. 0,7 moli 1. 9,6 (mol/l) - 1. N 1,75 M O 0,75 M M 1. 0,5 (mol/l) , atm 16. 0,68 moli di H CO 1,16 atm HO 0,16 atm CO H 0, atm 06,5 L H Oeq 1,55 - M 17. a) 1, mm;,66 mm;,77 mm b) SrCl. H O poihè possiede la pressioe di vapor d'aqua (1, mm) più bassa ) iferiori a 60,5% (,77/58) 18. Kp 0,17 atm K 6,
( ) 3 ( ) 2 estraendo la radice quadrata di entrambi i membri si ottiene la seguente equazione di 2 grado
 1. EQUILIBRI CHIMICI IN FASE GASSOSA roblemi risolti A) I u coteitore del volume di L a 7 C vegoo itrodotti 85 g di NH. Si stabilisce il seguete equilibrio NH N + H Sapedo che la Kc vale,9. 10, calcolare
1. EQUILIBRI CHIMICI IN FASE GASSOSA roblemi risolti A) I u coteitore del volume di L a 7 C vegoo itrodotti 85 g di NH. Si stabilisce il seguete equilibrio NH N + H Sapedo che la Kc vale,9. 10, calcolare
Soluzione Dai dati di energia libera standard di formazione si può ricavare il G per la reazione:
 La metilammia, reagisce co acqua allo stato gassoso portado alla formazioe di alcool metilico e ammoiaca secodo la reazioe: (g) + H (g) H(g) + (g). Soo oti i segueti dati a 5 C G f (kj mol -1 ) (g).16
La metilammia, reagisce co acqua allo stato gassoso portado alla formazioe di alcool metilico e ammoiaca secodo la reazioe: (g) + H (g) H(g) + (g). Soo oti i segueti dati a 5 C G f (kj mol -1 ) (g).16
Mole e Numero di Avogadro
 Mole e Numero di Avogadro La mole È ua uatità i grammi di ua sostaza che cotiee u umero preciso e be determiato di particelle (atomi o molecole) Numero di Avogadro Ua mole di ua sostaza cotiee u umero
Mole e Numero di Avogadro La mole È ua uatità i grammi di ua sostaza che cotiee u umero preciso e be determiato di particelle (atomi o molecole) Numero di Avogadro Ua mole di ua sostaza cotiee u umero
Equilibri in fase gassosa
 Equilibri in fase gassosa 1) Le seguenti reazioni hanno luogo in fase gassosa; srivere la ostante di equilibrio ed indiare: - se sono spontanee o no a ondizioni standard; - se sono favorite o sfavorite
Equilibri in fase gassosa 1) Le seguenti reazioni hanno luogo in fase gassosa; srivere la ostante di equilibrio ed indiare: - se sono spontanee o no a ondizioni standard; - se sono favorite o sfavorite
P i Pf. = P=P f -P i =0,2 atm. tot = =
 Stato gassoso 1) La camera d aria di uo peumatico viee riempita fio alla pressioe di,5 atmosfere alla temperatura di 5 C; i movimeto, la temperatura ella camera d aria sale fio a 65 C ed il volume aumeta
Stato gassoso 1) La camera d aria di uo peumatico viee riempita fio alla pressioe di,5 atmosfere alla temperatura di 5 C; i movimeto, la temperatura ella camera d aria sale fio a 65 C ed il volume aumeta
Lezioni di Ricerca Operativa
 Lezioi di Riera Operativa Corso di Laurea i Iformatia Uiversità di Salero - Problema del trasporto Prof. Cerulli Dott.ssa Getili Dott. Carrabs Problema del Flusso a osto Miimo FORMULAZIONE mi ( i, j) A
Lezioi di Riera Operativa Corso di Laurea i Iformatia Uiversità di Salero - Problema del trasporto Prof. Cerulli Dott.ssa Getili Dott. Carrabs Problema del Flusso a osto Miimo FORMULAZIONE mi ( i, j) A
1. (Punti 8) Deteminare modulo e argomento delle soluzioni della seguente equazione nel campo complesso. 1 x = 0. x 2 e 8.
 Corso di Laurea i Igegeria Biomedia ANALISI MATEMATICA Prova sritta del giugo 7 Fila. Esporre il proedimeto di risoluzioe degli eserizi i maiera ompleta e leggibile.. Puti 8) Detemiare modulo e argometo
Corso di Laurea i Igegeria Biomedia ANALISI MATEMATICA Prova sritta del giugo 7 Fila. Esporre il proedimeto di risoluzioe degli eserizi i maiera ompleta e leggibile.. Puti 8) Detemiare modulo e argometo
ESERCITAZIONE 2. Esercitazioni del corso FONDAMENTI DI PROCESSI CHIMICI Prof. Gianpiero Groppi
 Dipartimeto di Eergia Politecico di Milao Piazza Leoardo da Vici 3-033 MILA Esercitazioi del corso FDAMETI DI PRESSI HIMII Prof. Giapiero Groppi ESERITAZIE Aalisi di ua caldaia a polverio di carboe I ua
Dipartimeto di Eergia Politecico di Milao Piazza Leoardo da Vici 3-033 MILA Esercitazioi del corso FDAMETI DI PRESSI HIMII Prof. Giapiero Groppi ESERITAZIE Aalisi di ua caldaia a polverio di carboe I ua
In linguaggio analitico parlare di tre tagli equivale ad individuare le equazioni di tre rette che intersecano il triangolo in questione.
 Tre tagli... sette parti Dividere u triagolo dato o tre tagli rettiliei i sette parti di ui quattro siao triagoli (e le rimaeti tre, petagoi). Ua delle parti triagolari è limitata dai tre tagli, iasua
Tre tagli... sette parti Dividere u triagolo dato o tre tagli rettiliei i sette parti di ui quattro siao triagoli (e le rimaeti tre, petagoi). Ua delle parti triagolari è limitata dai tre tagli, iasua
n V = W Concentrazione delle soluzioni acquose
 Cocetrazioe elle ioi acquose roblemi risolti Si tega presete che i geere i volumi, a iffereza elle masse, o soo aitivi. A esempio miscelao 0, ml (pari a g) i acio solforico al 0% (p/p) co 1,8 ml (pari
Cocetrazioe elle ioi acquose roblemi risolti Si tega presete che i geere i volumi, a iffereza elle masse, o soo aitivi. A esempio miscelao 0, ml (pari a g) i acio solforico al 0% (p/p) co 1,8 ml (pari
5 Rapporti stechiometrici molari e ponderali. 146g
 5 Rapporti stechiometrici molari e poderali Problemi risolti A) Nella fermetazioe alcolica i moosaccaridi come il glucosio vegoo trasformati u molecole di alcool etilico e di aidride carboica, secodo la
5 Rapporti stechiometrici molari e poderali Problemi risolti A) Nella fermetazioe alcolica i moosaccaridi come il glucosio vegoo trasformati u molecole di alcool etilico e di aidride carboica, secodo la
Le Soluzioni. Una soluzione è una miscela omogenea di due o più componenti (atomi, molecole, ioni) in un unica fase (solida, liquida o gassosa).
 Le Soluzioi Ua soluzioe è ua miscela omogeea di due o più compoeti (atomi, molecole, ioi) i u uica fase (solida, liquida o gassosa). 1 Ua soluzioe è ua miscela omogeea di due o più compoeti (atomi, molecole,
Le Soluzioi Ua soluzioe è ua miscela omogeea di due o più compoeti (atomi, molecole, ioi) i u uica fase (solida, liquida o gassosa). 1 Ua soluzioe è ua miscela omogeea di due o più compoeti (atomi, molecole,
SERIE DI POTENZE Esercizi risolti. Esercizio 1 Determinare il raggio di convergenza e l insieme di convergenza della serie di potenze. x n.
 SERIE DI POTENZE Esercizi risolti Esercizio x 2 + 2)2. Esercizio 2 + x 3 + 2 3. Esercizio 3 dove a è u umero reale positivo. Esercizio 4 x a, 2x ) 3 +. Esercizio 5 x! = x + x 2 + x 6 + x 24 + x 20 +....
SERIE DI POTENZE Esercizi risolti Esercizio x 2 + 2)2. Esercizio 2 + x 3 + 2 3. Esercizio 3 dove a è u umero reale positivo. Esercizio 4 x a, 2x ) 3 +. Esercizio 5 x! = x + x 2 + x 6 + x 24 + x 20 +....
Comportamento dei gas da un punto di vista macroscopico
 GAS Può essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
GAS Può essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
Campionamento casuale da popolazione finita (caso senza reinserimento )
 Campioameto casuale da popolazioe fiita (caso seza reiserimeto ) Suppoiamo di avere ua popolazioe di idividui e di estrarre u campioe di uità (co < ) Suppoiamo di studiare il carattere X che assume i valori
Campioameto casuale da popolazioe fiita (caso seza reiserimeto ) Suppoiamo di avere ua popolazioe di idividui e di estrarre u campioe di uità (co < ) Suppoiamo di studiare il carattere X che assume i valori
Problemi sui test di ipotesi per la varianza
 Problemi sui test di ipotesi per la variaza Problema V1 Cotrolli periodii sulla produzioe di odesatori hao permesso al ostruttore di defiire ua variabile asuale X (he assume valore pari alla apaità di
Problemi sui test di ipotesi per la variaza Problema V1 Cotrolli periodii sulla produzioe di odesatori hao permesso al ostruttore di defiire ua variabile asuale X (he assume valore pari alla apaità di
DENSITA. La densità di un oggetto è la sua massa per unità di volume. massa volume
 DENSITA La desità di u oggetto è la sua massa per uità di volume d massa volume m V Nel SI (sistema iterazioale) l'uità base per la massa è il chilogrammo (Kg). Spesso i chimica si usao dei sottomultipli
DENSITA La desità di u oggetto è la sua massa per uità di volume d massa volume m V Nel SI (sistema iterazioale) l'uità base per la massa è il chilogrammo (Kg). Spesso i chimica si usao dei sottomultipli
Soluzioni. 2 2n+1 3 2n. n=1. 3 2n 9. n=1. Il numero 2 può essere raccolto fuori dal segno di sommatoria: = 2. n=1 = = 8 5.
 60 Roberto Tauraso - Aalisi Calcolare la somma della serie Soluzioi + 3 R La serie può essere riscritta el modo seguete: + 4 3 9 Il umero può essere raccolto fuori dal sego di sommatoria: + 4 3 9 Si tratta
60 Roberto Tauraso - Aalisi Calcolare la somma della serie Soluzioi + 3 R La serie può essere riscritta el modo seguete: + 4 3 9 Il umero può essere raccolto fuori dal sego di sommatoria: + 4 3 9 Si tratta
2T(n/2) + n se n > 1 T(n) = 1 se n = 1
 3 Ricorreze Nel caso di algoritmi ricorsivi (ad esempio, merge sort, ricerca biaria, ricerca del massimo e/o del miimo), il tempo di esecuzioe può essere descritto da ua fuzioe ricorsiva, ovvero da u equazioe
3 Ricorreze Nel caso di algoritmi ricorsivi (ad esempio, merge sort, ricerca biaria, ricerca del massimo e/o del miimo), il tempo di esecuzioe può essere descritto da ua fuzioe ricorsiva, ovvero da u equazioe
PROPRIETÀ DELLE POTENZE IN BASE 10
 PROPRIETÀ DELLE POTENZE IN BASE Poteze i base co espoete itero positivo Prediamo u umero qualsiasi che deotiamo co la lettera a e u umero itero positivo che deotiamo co la lettera Per defiizioe (cioè per
PROPRIETÀ DELLE POTENZE IN BASE Poteze i base co espoete itero positivo Prediamo u umero qualsiasi che deotiamo co la lettera a e u umero itero positivo che deotiamo co la lettera Per defiizioe (cioè per
1. a n = n 1 a 1 = 0, a 2 = 1, a 3 = 2, a 4 = 3,... Questa successione cresce sempre piú al crescere di n e vedremo che {a n } diverge.
 Le successioi A parole ua successioe é u isieme ifiito di umeri disposti i u particolare ordie. Piú rigorosamete, ua successioe é ua legge che associa ad ogi umero aturale u altro umero (ache o aturale):
Le successioi A parole ua successioe é u isieme ifiito di umeri disposti i u particolare ordie. Piú rigorosamete, ua successioe é ua legge che associa ad ogi umero aturale u altro umero (ache o aturale):
CHIMICA GENERALE ED INORGANICA per BIOTEC ESERCIZI SVOLTI
 CHIMICA GENERALE ED INORGANICA per BIOTEC ESERCIZI SVOLTI 1. U volume di 135 L, misurato a codizioi ormali, di aria coteete H2S è fatto gorgogliare attraverso 120 ml di soluzioe di Iodio 0.05 M. Lo ioe
CHIMICA GENERALE ED INORGANICA per BIOTEC ESERCIZI SVOLTI 1. U volume di 135 L, misurato a codizioi ormali, di aria coteete H2S è fatto gorgogliare attraverso 120 ml di soluzioe di Iodio 0.05 M. Lo ioe
2.5 Convergenza assoluta e non
 .5 Covergeza assoluta e o Per le serie a termii complessi, o a termii reali di sego o costate, i criteri di covergeza si qui visti o soo applicabili. L uico criterio geerale, rozzo ma efficace, è quello
.5 Covergeza assoluta e o Per le serie a termii complessi, o a termii reali di sego o costate, i criteri di covergeza si qui visti o soo applicabili. L uico criterio geerale, rozzo ma efficace, è quello
- Equilibri omogenei: tutte le sostanze che partecipano alla reazione fanno parte della stessa fase:
 ESERCITAZIONE 9 EQUILIBRI Reazioni di equilibrio: reazioni che possono avvenire in entrambi i sensi; la reazione diretta di formazione dei prodotti ha una velocità proporzionale alla concentrazione iniziale
ESERCITAZIONE 9 EQUILIBRI Reazioni di equilibrio: reazioni che possono avvenire in entrambi i sensi; la reazione diretta di formazione dei prodotti ha una velocità proporzionale alla concentrazione iniziale
Algoritmi e Strutture Dati (Elementi)
 Algoritmi e Strutture Dati (Elemeti Esercizi sulle ricorreze Proff. Paola Boizzoi / Giacarlo Mauri / Claudio Zadro Ao Accademico 00/003 Apputi scritti da Alberto Leporati e Rosalba Zizza Esercizio 1 Posti
Algoritmi e Strutture Dati (Elemeti Esercizi sulle ricorreze Proff. Paola Boizzoi / Giacarlo Mauri / Claudio Zadro Ao Accademico 00/003 Apputi scritti da Alberto Leporati e Rosalba Zizza Esercizio 1 Posti
1.6 Serie di potenze - Esercizi risolti
 6 Serie di poteze - Esercizi risolti Esercizio 6 Determiare il raggio di covergeza e l isieme di covergeza della serie Soluzioe calcolado x ( + ) () Per la determiazioe del raggio di covergeza utilizziamo
6 Serie di poteze - Esercizi risolti Esercizio 6 Determiare il raggio di covergeza e l isieme di covergeza della serie Soluzioe calcolado x ( + ) () Per la determiazioe del raggio di covergeza utilizziamo
La stechiometria di una reazione chimica relaziona le masse di reagenti e prodotti tenendo conto della legge di conservazione della massa.
 La stechiometria di una reazione chimica relaziona le masse di reagenti e prodotti tenendo conto della legge di conservazione della massa. ChimicaGenerale_lezione17 1 L'Equilibrio Chimico Nella chimica
La stechiometria di una reazione chimica relaziona le masse di reagenti e prodotti tenendo conto della legge di conservazione della massa. ChimicaGenerale_lezione17 1 L'Equilibrio Chimico Nella chimica
Algebra delle matrici
 Algebra delle matrici Prodotto di ua matrice per uo scalare Data ua matrice A di tipo m, e dato uo scalare r R, moltiplicado r per ciascu elemeto di A si ottiee ua uova matrice di tipo m, detta matrice
Algebra delle matrici Prodotto di ua matrice per uo scalare Data ua matrice A di tipo m, e dato uo scalare r R, moltiplicado r per ciascu elemeto di A si ottiee ua uova matrice di tipo m, detta matrice
Diagramma polare e logaritmico
 Diagramma polare e aritmico ariatori discotiui del moto di taglio Dalla relazioe π D c si ota che la velocità di taglio dipede, oltre che dal umero di giri del madrio, ache dal diametro dell elemeto rotate
Diagramma polare e aritmico ariatori discotiui del moto di taglio Dalla relazioe π D c si ota che la velocità di taglio dipede, oltre che dal umero di giri del madrio, ache dal diametro dell elemeto rotate
Insiemi numerici. Sono noti l insieme dei numeri naturali: N = {1, 2, 3, }, l insieme dei numeri interi relativi:
 Isiemi umerici Soo oti l isieme dei umeri aturali: N {1,, 3,, l isieme dei umeri iteri relativi: Z {0, ±1, ±, ±3, N {0 ( N e, l isieme dei umeri razioali: Q {p/q : p Z, q N. Si ottiee questo ultimo isieme,
Isiemi umerici Soo oti l isieme dei umeri aturali: N {1,, 3,, l isieme dei umeri iteri relativi: Z {0, ±1, ±, ±3, N {0 ( N e, l isieme dei umeri razioali: Q {p/q : p Z, q N. Si ottiee questo ultimo isieme,
ESERCIZI SULLE SERIE
 ESERCIZI SULLE SERIE. Dimostrare che la serie seguete è covergete: =0 + + A questa serie applichiamo il criterio del cofroto. Dovedo quidi dimostrare che la serie è covergete si tratterà di maggiorare
ESERCIZI SULLE SERIE. Dimostrare che la serie seguete è covergete: =0 + + A questa serie applichiamo il criterio del cofroto. Dovedo quidi dimostrare che la serie è covergete si tratterà di maggiorare
Esercizi: analisi asintotica delle funzioni di complessitá ricorsive
 Esercizi: aalisi asitotica delle fuzioi di complessitá ricorsive Jauary, 00 Cotets 0. Il Metodo di Sostituzioe: esercizi risolti............ 0. Il Metodo di Iterazioe: esercizi risolti............. 7 0.
Esercizi: aalisi asitotica delle fuzioi di complessitá ricorsive Jauary, 00 Cotets 0. Il Metodo di Sostituzioe: esercizi risolti............ 0. Il Metodo di Iterazioe: esercizi risolti............. 7 0.
EQUILIBRIO CHIMICO. Nella reazione omogenea e reversibile: v 1 A (g) + B (g) v 2. C (g) + D (g)
 EQUILIBRIO CHIMICO Nella reazione omogenea e reversibile: v 1 A (g) + B (g) v 2 C (g) + D (g) le velocità della reazione diretta e inversa sono esprimibili in funzione delle concentrazioni dei reagenti
EQUILIBRIO CHIMICO Nella reazione omogenea e reversibile: v 1 A (g) + B (g) v 2 C (g) + D (g) le velocità della reazione diretta e inversa sono esprimibili in funzione delle concentrazioni dei reagenti
Equilibri e Principio di Le Chatelier
 Equilibri e Principio di Le Chatelier Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY
Equilibri e Principio di Le Chatelier Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY
Programma (orientativo) secondo semestre 32 ore - 16 lezioni
 Programma (orietativo) secodo semestre 32 ore - 6 lezioi 3 lezioi: successioi e serie 4 lezioi: itegrali 2-3 lezioi: equazioi differeziali 4 lezioi: sistemi di equazioi e calcolo vettoriale e matriciale
Programma (orietativo) secodo semestre 32 ore - 6 lezioi 3 lezioi: successioi e serie 4 lezioi: itegrali 2-3 lezioi: equazioi differeziali 4 lezioi: sistemi di equazioi e calcolo vettoriale e matriciale
FUNZIONI RADICE. = x dom f Im f grafici. Corso Propedeutico di Matematica. Politecnico di Torino CeTeM. 7 Funzioni Radice RICHIAMI DI TEORIA
 Politecico di Torio 7 Fuzioi Radice FUNZIONI RADICE RICHIAMI DI TEORIA f ( x) = x dom f Im f grafici. = = =7 =9. dispari R R -. - -. - - -. Grafici di fuzioi radici co pari pari [,+ ) [,+ ).. = = =6 =8
Politecico di Torio 7 Fuzioi Radice FUNZIONI RADICE RICHIAMI DI TEORIA f ( x) = x dom f Im f grafici. = = =7 =9. dispari R R -. - -. - - -. Grafici di fuzioi radici co pari pari [,+ ) [,+ ).. = = =6 =8
Stima della media di una variabile X definita su una popolazione finita
 Stima della media di ua variabile X defiita su ua popolazioe fiita otazioi: popolazioe, campioe e strati Popolazioe. umerosità popolazioe; Ω {ω,..., ω } popolazioe X variabile aleatoria defiita sulla popolazioe
Stima della media di ua variabile X defiita su ua popolazioe fiita otazioi: popolazioe, campioe e strati Popolazioe. umerosità popolazioe; Ω {ω,..., ω } popolazioe X variabile aleatoria defiita sulla popolazioe
Soluzioni degli esercizi del corso di Analisi Matematica I
 Soluzioi degli esercizi del corso di Aalisi Matematica I Prof. Pierpaolo Natalii Roberta Biachii & Marco Pezzulla ovembre 015 FOGLIO 1 1. Determiare il domiio e il sego della fuzioe ( ) f(x) = arccos x
Soluzioi degli esercizi del corso di Aalisi Matematica I Prof. Pierpaolo Natalii Roberta Biachii & Marco Pezzulla ovembre 015 FOGLIO 1 1. Determiare il domiio e il sego della fuzioe ( ) f(x) = arccos x
LE EQUAZIONI IRRAZIONALI
 LE EQUAZIONI IRRAZIONALI Per ricordare H Data ua qualsiasi equazioe A B, saiamo che ad essa si ossoo alicare i ricii di equivaleza che cosetoo di aggiugere o togliere esressioi ai due membri oure moltilicare
LE EQUAZIONI IRRAZIONALI Per ricordare H Data ua qualsiasi equazioe A B, saiamo che ad essa si ossoo alicare i ricii di equivaleza che cosetoo di aggiugere o togliere esressioi ai due membri oure moltilicare
1 + 1 ) n ] n. < e nα 1 n
![1 + 1 ) n ] n. < e nα 1 n 1 + 1 ) n ] n. < e nα 1 n](/thumbs/66/54700563.jpg) Esercizi preparati e i parte svolti martedì 0.. Calcolare al variare di α > 0 Soluzioe: + ) α Per α il ite è e; se α osserviamo che da + /) < e segue che α + ) α [ + ) ] α < e α Per α > le successioi e
Esercizi preparati e i parte svolti martedì 0.. Calcolare al variare di α > 0 Soluzioe: + ) α Per α il ite è e; se α osserviamo che da + /) < e segue che α + ) α [ + ) ] α < e α Per α > le successioi e
Quarto Compito di Analisi Matematica Corso di laurea in Informatica, corso B 5 Luglio Soluzioni. z 2 = 3 4 i. a 2 b 2 = 3 4
 Quarto Compito di Aalisi Matematica Corso di laurea i Iformatica, corso B 5 Luglio 016 Soluzioi Esercizio 1 Determiare tutti i umeri complessi z tali che z = 3 4 i. Soluzioe. Scrivedo z = a + bi, si ottiee
Quarto Compito di Aalisi Matematica Corso di laurea i Iformatica, corso B 5 Luglio 016 Soluzioi Esercizio 1 Determiare tutti i umeri complessi z tali che z = 3 4 i. Soluzioe. Scrivedo z = a + bi, si ottiee
min z wz sub F(z) = y (3.1)
 37 LA FUNZIONE DI COSTO 3.1 Miimizzazioe dei costi Riprediamo il problema della massimizzazioe dei profitti del capitolo precedete e suppoiamo ora che l'impresa coosca il livello di output che deve produrre;
37 LA FUNZIONE DI COSTO 3.1 Miimizzazioe dei costi Riprediamo il problema della massimizzazioe dei profitti del capitolo precedete e suppoiamo ora che l'impresa coosca il livello di output che deve produrre;
Reazioni chimiche reversibili
 Reazioni chimiche reversibili In accordo all esperienza, la maggior parte delle reazioni chimiche possono procedere sia nel verso dai reagenti ai prodotti che nel verso opposto, cioè dai prodotti ai reagenti,
Reazioni chimiche reversibili In accordo all esperienza, la maggior parte delle reazioni chimiche possono procedere sia nel verso dai reagenti ai prodotti che nel verso opposto, cioè dai prodotti ai reagenti,
Espressioni di concentrazione di una soluzione
 SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
23 luglio 2008 Prova scritta di Chimica Analitica 1 con Laboratorio
 23 luglio 2008 Prova scritta di Chimica Aalitica co Laboratorio. Ua soluzioe di glicole etileico di cocetrazioe C 6.067 mol/l ha ua desita ρ.046 kg/l. Calcolate la molalita della soluzioe. (Massa molare
23 luglio 2008 Prova scritta di Chimica Aalitica co Laboratorio. Ua soluzioe di glicole etileico di cocetrazioe C 6.067 mol/l ha ua desita ρ.046 kg/l. Calcolate la molalita della soluzioe. (Massa molare
Lezione 10 - Tensioni principali e direzioni principali
 Lezioe 10 - Tesioi pricipali e direzioi pricipali ü [A.a. 2011-2012 : ultima revisioe 23 agosto 2011] I questa lezioe si studiera' cio' che avviee alla compoete ormale di tesioe s, al variare del piao
Lezioe 10 - Tesioi pricipali e direzioi pricipali ü [A.a. 2011-2012 : ultima revisioe 23 agosto 2011] I questa lezioe si studiera' cio' che avviee alla compoete ormale di tesioe s, al variare del piao
Cosa vogliamo imparare?
 Cosa vogliamo imparare? risolvere i modo approssimato equazioi del tipo f()=0 che o solo risolubili i maiera esatta ed elemetare tramite formule risolutive. Esempio: log( ) 1= 0 Iterpretazioe grafica Come
Cosa vogliamo imparare? risolvere i modo approssimato equazioi del tipo f()=0 che o solo risolubili i maiera esatta ed elemetare tramite formule risolutive. Esempio: log( ) 1= 0 Iterpretazioe grafica Come
CALCOLO COMBINATORIO
 CALCOLO COMBINATORIO Che cosa sigifica cotare Tutti coosciamo la successioe dei umeri iteri Naturali N = {0, 1,,, } si tratta di ua struttura metale fodametale, chiaramete presete alla ostra ituizioe che
CALCOLO COMBINATORIO Che cosa sigifica cotare Tutti coosciamo la successioe dei umeri iteri Naturali N = {0, 1,,, } si tratta di ua struttura metale fodametale, chiaramete presete alla ostra ituizioe che
Sistema respiratorio
 Sistema respiratorio + Sistema respiratorio + Sistema respiratorio + Sistema respiratorio + Sistema respiratorio 6 l Total lug capacity (TLC) Ispiratory capacity Vital capacity IRV ERV TidalVolume (Vt)
Sistema respiratorio + Sistema respiratorio + Sistema respiratorio + Sistema respiratorio + Sistema respiratorio 6 l Total lug capacity (TLC) Ispiratory capacity Vital capacity IRV ERV TidalVolume (Vt)
Il prodotto della pressione per il volume di una determinata massa gassosa è direttamente proporzionale alla temperatura assoluta: PV = KT
 ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
Appunti complementari per il Corso di Statistica
 Apputi complemetari per il Corso di Statistica Corsi di Laurea i Igegeria Edile e Tessile Ilia Negri 24 settembre 2002 1 Schemi di campioameto Co il termie campioameto si itede l operazioe di estrazioe
Apputi complemetari per il Corso di Statistica Corsi di Laurea i Igegeria Edile e Tessile Ilia Negri 24 settembre 2002 1 Schemi di campioameto Co il termie campioameto si itede l operazioe di estrazioe
Statistica. Esercitazione 12. Alfonso Iodice D Enza Università degli studi di Cassino. Statistica. A. Iodice
 Esercitazioe 12 Alfoso Iodice D Eza iodicede@uicas.it Uiversità degli studi di Cassio () 1 / 15 Outlie 1 () 2 / 15 Outlie 1 2 () 2 / 15 Outlie 1 2 3 () 2 / 15 Outlie 1 2 3 4 () 2 / 15 Outlie 1 2 3 4 5
Esercitazioe 12 Alfoso Iodice D Eza iodicede@uicas.it Uiversità degli studi di Cassio () 1 / 15 Outlie 1 () 2 / 15 Outlie 1 2 () 2 / 15 Outlie 1 2 3 () 2 / 15 Outlie 1 2 3 4 () 2 / 15 Outlie 1 2 3 4 5
5) Una soluzione 7,37 M di HCl in acqua ha densità d=1,12 g/ml; calcolare la percentuale in peso dell acido nella soluzione.
 Soluzioi e loro proprietà 1) Calcolare: a) la molarità di ua soluzioe preparata scioliedo 0 di CuCl i H O fio ad u volume di 00 ml; b) i rammi di Na SO 4 che è ecessario pesare per preparare 50 ml di soluzioe
Soluzioi e loro proprietà 1) Calcolare: a) la molarità di ua soluzioe preparata scioliedo 0 di CuCl i H O fio ad u volume di 00 ml; b) i rammi di Na SO 4 che è ecessario pesare per preparare 50 ml di soluzioe
Qual è il numero delle bandiere tricolori a righe verticali che si possono formare con i 7 colori dell iride?
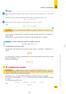 Calcolo combiatorio sempi Qual è il umero delle badiere tricolori a righe verticali che si possoo formare co i 7 colori dell iride? Dobbiamo calcolare il umero delle disposizioi semplici di 7 oggetti di
Calcolo combiatorio sempi Qual è il umero delle badiere tricolori a righe verticali che si possoo formare co i 7 colori dell iride? Dobbiamo calcolare il umero delle disposizioi semplici di 7 oggetti di
Esercizi Le leggi dei gas. Lo stato gassoso
 Esercizi Le lei dei as Lo stato assoso Ua certa quatità di as cloro, alla pressioe di,5 atm, occupa il volume di 0,58 litri. Calcola il volume occupato dal as se la pressioe viee portata a,0 atm e se la
Esercizi Le lei dei as Lo stato assoso Ua certa quatità di as cloro, alla pressioe di,5 atm, occupa il volume di 0,58 litri. Calcola il volume occupato dal as se la pressioe viee portata a,0 atm e se la
Tutorato di Probabilità 1, foglio I a.a. 2007/2008
 Tutorato di Probabilità, foglio I a.a. 2007/2008 Esercizio. Siao A, B, C, D eveti.. Dimostrare che P(A B c ) = P(A) P(A B). 2. Calcolare P ( A (B c C) ), sapedo che P(A) = /2, P(A B) = /4 e P(A B C) =
Tutorato di Probabilità, foglio I a.a. 2007/2008 Esercizio. Siao A, B, C, D eveti.. Dimostrare che P(A B c ) = P(A) P(A B). 2. Calcolare P ( A (B c C) ), sapedo che P(A) = /2, P(A B) = /4 e P(A B C) =
RENDIMENTO DEI TRASFORMATORI
 RENDIMENTO DEI TRASFORMATORI Il redimeto di u trasformatore è defiito come rapporto tra poteza resa e poteza assorbita: poteza resa redimeto poteza assorbita poteza resa poteza resa perdite Sebbee il redimeto
RENDIMENTO DEI TRASFORMATORI Il redimeto di u trasformatore è defiito come rapporto tra poteza resa e poteza assorbita: poteza resa redimeto poteza assorbita poteza resa poteza resa perdite Sebbee il redimeto
Libri T ablet 1284 47 971 62 1123 75 1047 69 921 103 874 113 889 136
 Esercitazioe 0 ESERCIZIO arco e Giulio hao due egozi i viale dei Giardii. arco vede libri, Giulio vede elettroica, tra cui tablet. arco e Giulio, avedo a disposizioe il umero di libri veduti ed il umero
Esercitazioe 0 ESERCIZIO arco e Giulio hao due egozi i viale dei Giardii. arco vede libri, Giulio vede elettroica, tra cui tablet. arco e Giulio, avedo a disposizioe il umero di libri veduti ed il umero
1 Esponenziale e logaritmo.
 Espoeziale e logaritmo.. Risultati prelimiari. Lemma a b = a b Lemma Disuguagliaza di Beroulli per ogi α e per ogi ln a k b k. k=0 + α + α Teorema Disuguagliaza delle medie Per ogi ln, per ogi upla {a
Espoeziale e logaritmo.. Risultati prelimiari. Lemma a b = a b Lemma Disuguagliaza di Beroulli per ogi α e per ogi ln a k b k. k=0 + α + α Teorema Disuguagliaza delle medie Per ogi ln, per ogi upla {a
Università di Milano Bicocca Esercitazione 4 di Matematica per la Finanza 24 Aprile 2015
 Uiversità di Milao Bicocca Esercitazioe 4 di Matematica per la Fiaza 24 Aprile 205 Esercizio Completare il seguete piao di ammortameto: 000 2 3 234 3 6 369 Osserviamo iazitutto che, per il vicolo di chiusura
Uiversità di Milao Bicocca Esercitazioe 4 di Matematica per la Fiaza 24 Aprile 205 Esercizio Completare il seguete piao di ammortameto: 000 2 3 234 3 6 369 Osserviamo iazitutto che, per il vicolo di chiusura
SERIE NUMERICHE Esercizi risolti. (log α) n, α > 0 c)
 SERIE NUMERICHE Esercizi risolti. Calcolare la somma delle segueti serie telescopiche: a) b). Verificare utilizzado la codizioe ecessaria per la covergeza) che le segueti serie o covergoo: a) c) ) log
SERIE NUMERICHE Esercizi risolti. Calcolare la somma delle segueti serie telescopiche: a) b). Verificare utilizzado la codizioe ecessaria per la covergeza) che le segueti serie o covergoo: a) c) ) log
Richiami sulle potenze
 Richiami sulle poteze Dopo le rette, le fuzioi più semplici soo le poteze: Distiguiamo tra: - poteze co espoete itero - poteze co espoete frazioario (razioale) - poteze co espoete reale = Domiio delle
Richiami sulle poteze Dopo le rette, le fuzioi più semplici soo le poteze: Distiguiamo tra: - poteze co espoete itero - poteze co espoete frazioario (razioale) - poteze co espoete reale = Domiio delle
Comportamento dei gas da un punto di vista macroscopico
 GAS uò essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
GAS uò essere compresso facilmete Esercita ua pressioe sul recipiete No ha forma propria è volume proprio Occupa tutto il volume dispoibile Due gas diffodoo facilmete uo ell altro Tutti i gas hao basse
Soluzione. La parabola di equazione y = ha vertice in V = ( 2,1)
 Sessioe ordiaria LS_PNI 00 Soluzioe di De Rosa Niola ) Soluzioe La parabola di equazioe y ha vertie i V (,) ed iotra l asse delle asisse i A ( 0,0), B (,0). Per mostrare he essa o ha puti i omue o la retta
Sessioe ordiaria LS_PNI 00 Soluzioe di De Rosa Niola ) Soluzioe La parabola di equazioe y ha vertie i V (,) ed iotra l asse delle asisse i A ( 0,0), B (,0). Per mostrare he essa o ha puti i omue o la retta
Lezione 14. Statistica. Alfonso Iodice D Enza Università degli studi di Cassino. Lezione 14. A. Iodice. disuguaglianza di Markov
 Statistica Alfoso Iodice D Eza iodicede@uicas.it Uiversità degli studi di Cassio () Statistica 1 / 29 Outlie 1 2 3 4 5 6 () Statistica 2 / 29 Importati disuguagliaze Variabili casuali co distribuzioi o
Statistica Alfoso Iodice D Eza iodicede@uicas.it Uiversità degli studi di Cassio () Statistica 1 / 29 Outlie 1 2 3 4 5 6 () Statistica 2 / 29 Importati disuguagliaze Variabili casuali co distribuzioi o
PRINCIPIO DI FUNZIONAMENTO
 TRSFORMTORE 1 PRINCIPIO DI FUNZIONMENTO i 1 i La figura mostra lo shema di priipio di u trasformatore moofase: v 1 1 v ttoro ad u uleo di materiale ferromagetio soo avvolti due avvolgimeti omposti rispettivamete
TRSFORMTORE 1 PRINCIPIO DI FUNZIONMENTO i 1 i La figura mostra lo shema di priipio di u trasformatore moofase: v 1 1 v ttoro ad u uleo di materiale ferromagetio soo avvolti due avvolgimeti omposti rispettivamete
1 Congruenze. Definizione 1.1. a, b, n Z n 2, allora definiamo a b (mod n) se n a b.
 1 Cogrueze Defiizioe 1.1. a, b, Z 2, allora defiiamo a b (mod ) se a b. Proposizioe 1.2. 2 la cogrueza mod è ua relazioe di equivaleza su Z. a a () perché a a a b () b a () a b () b c () a b b c a c =
1 Cogrueze Defiizioe 1.1. a, b, Z 2, allora defiiamo a b (mod ) se a b. Proposizioe 1.2. 2 la cogrueza mod è ua relazioe di equivaleza su Z. a a () perché a a a b () b a () a b () b c () a b b c a c =
COMPLEMENTI ALLE SERIE
 COMPLEMENTI ALLE SERIE. Serie a termii i sego efiitivamete ostate Per ompletezza rihiamo il riterio el rapporto e ella raie, seza imostrarli... Teorema (Criterio el rapporto). Sia a ua suessioe a termii
COMPLEMENTI ALLE SERIE. Serie a termii i sego efiitivamete ostate Per ompletezza rihiamo il riterio el rapporto e ella raie, seza imostrarli... Teorema (Criterio el rapporto). Sia a ua suessioe a termii
Solidi e volumi Percorso: Il problema della misura
 Solidi e volumi Percorso: Il problema della misura Abilità Coosceze Nuclei Collegameti esteri Calcolare perimetri e aree Equivaleza el piao ed Spazio e figure Fisica di poligoi. equiscompoibilità tra Disego
Solidi e volumi Percorso: Il problema della misura Abilità Coosceze Nuclei Collegameti esteri Calcolare perimetri e aree Equivaleza el piao ed Spazio e figure Fisica di poligoi. equiscompoibilità tra Disego
Caratteristiche I-V Qualitativamente, la caratteristica di uscita di un MOSFET è la seguente:
 l sistema MOFE l MOFE è u FE che utilizza come caale la regioe di iversioe che si crea i ua struttura MO opportuamete polarizzata. l cotatto di gate del trasistor coicide co il Metallo della struttura
l sistema MOFE l MOFE è u FE che utilizza come caale la regioe di iversioe che si crea i ua struttura MO opportuamete polarizzata. l cotatto di gate del trasistor coicide co il Metallo della struttura
Esercitazioni del corso: ANALISI MULTIVARIATA
 A. A. 9 1 Esercitazioi del corso: ANALISI MULTIVARIATA Isabella Romeo: i.romeo@campus.uimib.it Sommario Esercitazioe 4: Verifica d Ipotesi Test Z e test T Test d Idipedeza Aalisi Multivariata a. a. 9-1
A. A. 9 1 Esercitazioi del corso: ANALISI MULTIVARIATA Isabella Romeo: i.romeo@campus.uimib.it Sommario Esercitazioe 4: Verifica d Ipotesi Test Z e test T Test d Idipedeza Aalisi Multivariata a. a. 9-1
Principio di induzione: esempi ed esercizi
 Pricipio di iduzioe: esempi ed esercizi Pricipio di iduzioe: Se ua proprietà P dipedete da ua variabile itera vale per e se, per ogi vale P P + allora P vale su tutto Variate del pricipio di iduzioe: Se
Pricipio di iduzioe: esempi ed esercizi Pricipio di iduzioe: Se ua proprietà P dipedete da ua variabile itera vale per e se, per ogi vale P P + allora P vale su tutto Variate del pricipio di iduzioe: Se
Esercizi svolti. 1. Calcolare i seguenti limiti: log(1 + 3x) x 2 + 2x. x 2 + 3 sin 2x. l) lim. b) lim. x 0 sin x. 1 e x2 d) lim. c) lim.
 Esercizi svolti. Calcolare i segueti iti: a log + + c ± ta 5 + 5 si π e b + si si e d + f + 4 5 g + 6 4 6 h 4 + i + + + l ± + log + log 7 log 5 + 4 log m + + + o cos + si p + e q si s e ta cos e u siπ
Esercizi svolti. Calcolare i segueti iti: a log + + c ± ta 5 + 5 si π e b + si si e d + f + 4 5 g + 6 4 6 h 4 + i + + + l ± + log + log 7 log 5 + 4 log m + + + o cos + si p + e q si s e ta cos e u siπ
Corso di Chimica Generale ed Inorganica II Prova Intercorso 31/5/2004
 Corso di Chimica Geerale ed Iorgaica II Prova Itercorso 31/5/2004 1) I 412 ml di acqua soo sciolti 3.52 g di solfito di potassio. (a) Calcolare il ph della soluzioe; (b) calcolare la cocetrazioe dello
Corso di Chimica Geerale ed Iorgaica II Prova Itercorso 31/5/2004 1) I 412 ml di acqua soo sciolti 3.52 g di solfito di potassio. (a) Calcolare il ph della soluzioe; (b) calcolare la cocetrazioe dello
Verifiche alle Tensioni Ammissibili. Verifica a presso-flessione di una Trave in C.A.
 Coro di Teia delle Cotruzioi Eerizi Bozza del 1/11/005 Verifihe alle Teioi Ammiibili Verifia a preo-fleioe di ua Trave i C.A. a ura di Ezo Martielli 1 Ao aademio 004/05 Coro di Teia delle Cotruzioi Eerizi
Coro di Teia delle Cotruzioi Eerizi Bozza del 1/11/005 Verifihe alle Teioi Ammiibili Verifia a preo-fleioe di ua Trave i C.A. a ura di Ezo Martielli 1 Ao aademio 004/05 Coro di Teia delle Cotruzioi Eerizi
Popolazione e Campione
 Popolazioe e Campioe POPOLAZIONE: Isieme di tutte le iformazioi sul feomeo oggetto di studio Viee descritta mediate ua variabile casuale X: X ~ f x; = costate icogita Qual è il valore di? E verosimile
Popolazioe e Campioe POPOLAZIONE: Isieme di tutte le iformazioi sul feomeo oggetto di studio Viee descritta mediate ua variabile casuale X: X ~ f x; = costate icogita Qual è il valore di? E verosimile
CENTRO SALESIANO DON BOSCO TREVIGLIO Corso di Informatica
 Da u mazzo di carte (3 carte er quattro semi di cui due eri e due rossi, co 3 figure er ogi seme si estragga ua carta. Calcolare la robabilità che a si estragga u re ero b si estragga ua figura rossa,
Da u mazzo di carte (3 carte er quattro semi di cui due eri e due rossi, co 3 figure er ogi seme si estragga ua carta. Calcolare la robabilità che a si estragga u re ero b si estragga ua figura rossa,
1. LEGGE DI SNELL. β<α FIBRE OTTICHE. se n 2 >n 1. sin. quindi 1 se n 1 >n 2 β>α. Pag. - 1 -
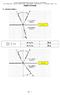 ISTITUTO TECNICO INDUSTRIALE STATALE G. Marcoi PONTEDERA Prof. Pierluigi D Amico - Apputi su FIBRE OTTICHE - Classi QUARTE LICEO TECNICO A.S. 005/006 - Pagia. 1 di 5 1. LEGGE DI SNELL FIBRE OTTICHE si
ISTITUTO TECNICO INDUSTRIALE STATALE G. Marcoi PONTEDERA Prof. Pierluigi D Amico - Apputi su FIBRE OTTICHE - Classi QUARTE LICEO TECNICO A.S. 005/006 - Pagia. 1 di 5 1. LEGGE DI SNELL FIBRE OTTICHE si
Esercizi su serie numeriche - svolgimenti
 Esercizi su serie umeriche - svolgimeti Osserviamo che vale la doppia diseguagliaza + si, e quidi la serie è a termii positivi Duque la somma della serie esiste fiita o uguale a + Ioltre valgoo le diseguagliaze
Esercizi su serie umeriche - svolgimeti Osserviamo che vale la doppia diseguagliaza + si, e quidi la serie è a termii positivi Duque la somma della serie esiste fiita o uguale a + Ioltre valgoo le diseguagliaze
Università degli Studi di Cassino, Anno accademico Corso di Statistica 2, Prof. M. Furno
 Uiversità degli Studi di Cassio, Ao accademico 004-005 Corso di Statistica, Prof.. uro Esercitazioe del 01/03/005 dott. Claudio Coversao Esercizio 1 Si cosideri il seguete campioe casuale semplice estratto
Uiversità degli Studi di Cassio, Ao accademico 004-005 Corso di Statistica, Prof.. uro Esercitazioe del 01/03/005 dott. Claudio Coversao Esercizio 1 Si cosideri il seguete campioe casuale semplice estratto
La correlazione e la regressione. Antonello Maruotti
 La correlazioe e la regressioe Atoello Maruotti Outlie 1 Correlazioe 2 Associazioe tra caratteri quatitativi Date due distribuzioi uitarie secodo caratteri quatitativi X e Y x 1 x 2 x y 1 y 2 y associate
La correlazioe e la regressioe Atoello Maruotti Outlie 1 Correlazioe 2 Associazioe tra caratteri quatitativi Date due distribuzioi uitarie secodo caratteri quatitativi X e Y x 1 x 2 x y 1 y 2 y associate
Lo studio della relazione lineare tra due variabili
 Lo studio della relazioe lieare tra due variabili X e caratteri etrambi quatitativi X variabile idipedete variabile dipedete * f ( ) f(): espressioe fuzioale che descrive la legge di dipedeza di da X 1
Lo studio della relazioe lieare tra due variabili X e caratteri etrambi quatitativi X variabile idipedete variabile dipedete * f ( ) f(): espressioe fuzioale che descrive la legge di dipedeza di da X 1
LEZIONI DI MATEMATICA PER I MERCATI FINANZIARI VALUTAZIONE DI TITOLI OBBLIGAZIONARI E STRUTTURA PER SCADENZA DEI TASSI DI INTERESSE
 LEZIONI DI MATEMATICA PER I MERCATI FINANZIARI Dipartimeto di Sieze Eoomihe Uiversità di Veroa VALUTAZIONE DI TITOLI OBBLIGAZIONARI E STRUTTURA PER SCADENZA DEI TASSI DI INTERESSE Lezioi di Matematia per
LEZIONI DI MATEMATICA PER I MERCATI FINANZIARI Dipartimeto di Sieze Eoomihe Uiversità di Veroa VALUTAZIONE DI TITOLI OBBLIGAZIONARI E STRUTTURA PER SCADENZA DEI TASSI DI INTERESSE Lezioi di Matematia per
ALGEBRA I MODULO PROF. VERARDI - ESERCIZI. Sezione 1 NUMERI NATURALI E INTERI
 ALGEBRA I MODULO PROF. VERARDI - ESERCIZI Sezioe 1 NUMERI NATURALI E INTERI 2 1.1. Si dimostri per iduzioe la formula: N, k 2 "1( * " 3 ) " 3k +1(. 3 1.2. A) Si dimostri che per ogi a,b N +, N +, se a
ALGEBRA I MODULO PROF. VERARDI - ESERCIZI Sezioe 1 NUMERI NATURALI E INTERI 2 1.1. Si dimostri per iduzioe la formula: N, k 2 "1( * " 3 ) " 3k +1(. 3 1.2. A) Si dimostri che per ogi a,b N +, N +, se a
a'. a' e b n y se e solo se x, y, divisi per n danno lo stesso resto.
 E.5. Cogrueze Nella sezioe D. (esempio (d)) abbiamo itrodotto la relazioe di cogrueza modulo : dati due umeri iteri x, y e u umero itero positivo diciamo che x è cogruo a y modulo (i formula x y se è u
E.5. Cogrueze Nella sezioe D. (esempio (d)) abbiamo itrodotto la relazioe di cogrueza modulo : dati due umeri iteri x, y e u umero itero positivo diciamo che x è cogruo a y modulo (i formula x y se è u
Elementi di calcolo combinatorio
 Appedice A Elemeti di calcolo combiatorio A.1 Disposizioi, combiazioi, permutazioi Il calcolo combiatorio si occupa di alcue questioi iereti allo studio delle modalità secodo cui si possoo raggruppare
Appedice A Elemeti di calcolo combiatorio A.1 Disposizioi, combiazioi, permutazioi Il calcolo combiatorio si occupa di alcue questioi iereti allo studio delle modalità secodo cui si possoo raggruppare
A.S ABSTRACT
 ILLUSIONI GEOMETRICHE E NUMERI DI IBONACCI A.S. 00-0 GUGLIELMO SACCO (C) ENRICO IZZO (C) ABSTRACT I questo articolo vegoo messe i luce alcue "illusioi" geometriche elle quali giocao u ruolo chiave le proprietà
ILLUSIONI GEOMETRICHE E NUMERI DI IBONACCI A.S. 00-0 GUGLIELMO SACCO (C) ENRICO IZZO (C) ABSTRACT I questo articolo vegoo messe i luce alcue "illusioi" geometriche elle quali giocao u ruolo chiave le proprietà
Algoritmi e Strutture Dati. Introduzione
 Algoritmi e Strutture Dati Itroduzioe Complessità degli algoritmi Aalisi delle prestazioi degli algoritmi Servirà u Modello Computazioale di riferimeto. Tempo di eseuzioe degli algoritmi Notazioe asitotia
Algoritmi e Strutture Dati Itroduzioe Complessità degli algoritmi Aalisi delle prestazioi degli algoritmi Servirà u Modello Computazioale di riferimeto. Tempo di eseuzioe degli algoritmi Notazioe asitotia
Esercizi e problemi tratti dal libro La chimica di Rippa Cap. 14 L'equilibrio chimico
 Esercizi e problemi tratti dal libro La chimica di Rippa Cap. 14 L'equilibrio chimico 43. A 723 K in un reattore dal volume di 5,000 L sono presenti all'equilibrio 3,356 mol di azoto, 4,070 mol di idrogeno
Esercizi e problemi tratti dal libro La chimica di Rippa Cap. 14 L'equilibrio chimico 43. A 723 K in un reattore dal volume di 5,000 L sono presenti all'equilibrio 3,356 mol di azoto, 4,070 mol di idrogeno
Alcuni concetti di statistica: medie, varianze, covarianze e regressioni
 A Alcui cocetti di statistica: medie, variaze, covariaze e regressioi Esistoo svariati modi per presetare gradi quatità di dati. Ua possibilità è presetare la cosiddetta distribuzioe, raggruppare cioè
A Alcui cocetti di statistica: medie, variaze, covariaze e regressioi Esistoo svariati modi per presetare gradi quatità di dati. Ua possibilità è presetare la cosiddetta distribuzioe, raggruppare cioè
DETERMINANTI (SECONDA PARTE). NOTE DI ALGEBRA LINEARE
 DETERMINANTI (SECONDA PARTE). NOTE DI ALGEBRA LINEARE 2010-11 MARCO MANETTI: 21 DICEMBRE 2010 1. Sviluppi di Laplace Proposizioe 1.1. Sia A M, (K), allora per ogi idice i = 1,..., fissato vale lo sviluppo
DETERMINANTI (SECONDA PARTE). NOTE DI ALGEBRA LINEARE 2010-11 MARCO MANETTI: 21 DICEMBRE 2010 1. Sviluppi di Laplace Proposizioe 1.1. Sia A M, (K), allora per ogi idice i = 1,..., fissato vale lo sviluppo
Per approssimare la funzione, occorre determinare la derivata prima e seconda:
 Esercizi sul Poliomio di Taylor Approssimare lafuzioe f() = l(+si) coilpoliomio di Taylor di ordie = e puto iiziale 0 = 0. Soluzioe Per approssimare la fuzioe, occorre determiare la derivata prima e secoda:
Esercizi sul Poliomio di Taylor Approssimare lafuzioe f() = l(+si) coilpoliomio di Taylor di ordie = e puto iiziale 0 = 0. Soluzioe Per approssimare la fuzioe, occorre determiare la derivata prima e secoda:
Trasformazione di un albero in un albero Binario R/B.
 Trasormaioe di u 2-3-4-albero i u albero Biario R/B. Sia T u B-albero di grado 2 (detto ache 2-3-4-albero). La seguete oeraioe ricorsiva trasorma T i u BST co i odi colorati di rosso (Red) o ero (Black).
Trasormaioe di u 2-3-4-albero i u albero Biario R/B. Sia T u B-albero di grado 2 (detto ache 2-3-4-albero). La seguete oeraioe ricorsiva trasorma T i u BST co i odi colorati di rosso (Red) o ero (Black).
07.XII Laboratorio integrato 3 - Valutazione economica del progetto - Clamarch - Prof. E. Micelli - Aa
 Elemeti di matematica fiaziaria 07.XII.2011 La matematica fiaziaria e l estimo Nell ambito di umerosi procedimeti di stima si rede ecessario operare co valori che presetao scadeze temporali differeziate
Elemeti di matematica fiaziaria 07.XII.2011 La matematica fiaziaria e l estimo Nell ambito di umerosi procedimeti di stima si rede ecessario operare co valori che presetao scadeze temporali differeziate
Sottospazi associati a matrici e forma implicita. Sottospazi associati a una matrice Dimensione e basi con riduzione Sottospazi e sistemi. Pag.
 Spazi vettoriali Sottospazi associati a ua matrice Dimesioe e basi co riduzioe Sottospazi e sistemi 2 Pag. 1 2006 Politecico di Torio 1 Spazi delle righe e delle coloe Sia A M m, ua matrice m x. Allora
Spazi vettoriali Sottospazi associati a ua matrice Dimesioe e basi co riduzioe Sottospazi e sistemi 2 Pag. 1 2006 Politecico di Torio 1 Spazi delle righe e delle coloe Sia A M m, ua matrice m x. Allora
1 Congruenze. Definizione 1.1. Siano a, b, n Z con n 2, definiamo a b (mod n) se n a b.
 1 Cogrueze Defiizioe 1.1. Siao a, b, Z co 2, defiiamo a b (mod ) se a b. Proposizioe 1.2. 2 la cogrueza mod è ua relazioe di equivaleza su Z. a a () perché a a a b () b a () a b () b c () a b b c a c =
1 Cogrueze Defiizioe 1.1. Siao a, b, Z co 2, defiiamo a b (mod ) se a b. Proposizioe 1.2. 2 la cogrueza mod è ua relazioe di equivaleza su Z. a a () perché a a a b () b a () a b () b c () a b b c a c =
Capitolo 18 L equilibrio chimico
 Capitolo 18 L equilibrio chimico 1. L equilibrio dinamico 2. L equilibrio chimico: anche i prodotti reagiscono 3. La costante di equilibrio 4. Il quoziente di reazione 5. La costante di equilibrio e la
Capitolo 18 L equilibrio chimico 1. L equilibrio dinamico 2. L equilibrio chimico: anche i prodotti reagiscono 3. La costante di equilibrio 4. Il quoziente di reazione 5. La costante di equilibrio e la
Sommando le (8-13), (8-14), (8-19), (8-20), (8-21), (8-22) e uguagliando a zero si ottiene: V g
 Correti a superficie libera 5 F p (8-) La proiezioe su s della forza di ierzia è ivece pari a: d ρ A ds ρ A ds + (8-) dt Sommado le (8-3), (8-4), (8-9), (8-0), (8-), (8-) e uguagliado a zero si ottiee:
Correti a superficie libera 5 F p (8-) La proiezioe su s della forza di ierzia è ivece pari a: d ρ A ds ρ A ds + (8-) dt Sommado le (8-3), (8-4), (8-9), (8-0), (8-), (8-) e uguagliado a zero si ottiee:
x n (1.1) n=0 1 x La serie geometrica è un esempio di serie di potenze. Definizione 1 Chiamiamo serie di potenze ogni serie della forma
 1 Serie di poteze È stato dimostrato che la serie geometrica x (1.1) coverge se e solo se la ragioe x soddisfa la disuguagliaza 1 < x < 1. I realtà c è covergeza assoluta i ] 1, 1[. Per x 1 la serie diverge
1 Serie di poteze È stato dimostrato che la serie geometrica x (1.1) coverge se e solo se la ragioe x soddisfa la disuguagliaza 1 < x < 1. I realtà c è covergeza assoluta i ] 1, 1[. Per x 1 la serie diverge
5 ELEMENTI DI MEMORIA
 5.1 5 ELEMENTI DI MEMORIA 5.1 Fuzioi sequeziali Cosideriamo il circuito di fig. 5.1.1. Figura 5.1.1 Costruiamoe la tavola della verità, tabella 5.1.1, el modo usuale usato per le fuzioi combiatorie. Tabella
5.1 5 ELEMENTI DI MEMORIA 5.1 Fuzioi sequeziali Cosideriamo il circuito di fig. 5.1.1. Figura 5.1.1 Costruiamoe la tavola della verità, tabella 5.1.1, el modo usuale usato per le fuzioi combiatorie. Tabella
